Bệnh tim mạch
Thuốc điều trị bệnh động mạch vành: Phân nhóm, tác dụng
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
Nguồn: Sách Thuốc tim mạch trong thực hành lâm sàng (PGS.TS.BS. Phạm Mạnh Hùng – Ths. BSNT. Phạm Trần Linh)
Tác giả
Nguyễn Quốc Thái
Nguyễn Mạnh Quân
Vũ Quang Ngọc
Nguyễn Đức Nhương
Bùi Nguyên Tùng
Lê Ngọc Thạch
Phùng Đình Thọ
Nhà thuốc Ngọc Anh xin giới thiệu đến bạn đọc về Thuốc điều trị bệnh động mạch vành qua bài viết sau đây.
PHẦN I: HỘI CHỨNG ĐỘNG MẠCH VÀNH MẠN
ĐỊNH NGHĨA VÀ THUẬT NGỮ
Hội chứng động mạch vành mạn (Chronic coronary syndrome) là thuật ngữ mới được đưa ra tại Hội Nghị Tim Mạch châu u (ESC) 2019, thay cho tên gọi trước đây là đau thắt ngực ổn định, bệnh ĐMV ổn định, bệnh cơ tim thiếu máu cục bộ mạn tính hoặc suy vành.
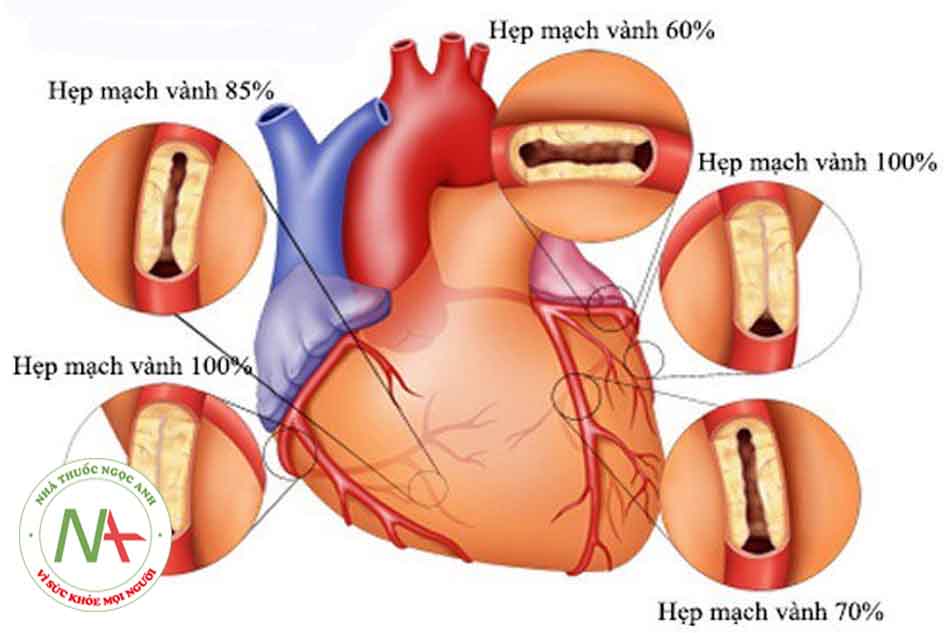
Hội chứng động mạch vành mạn là bệnh lý liên quan đến sự ổn định tương đối của mảng xơ vữa động mạch vành, khi không có sự nứt vỡ đột ngột hoặc sau giai đoạn cấp hoặc sau khi đã được can thiệp/phẫu thuật. Khi mảng xơ vữa tiến triển dần gây hẹp lòng ĐMV một cách đáng kể (thường là hẹp trên 70% đường kính lòng mạch) thì có thể gây ra triệu chứng, điển hình nhất là đau thắt ngực/khó thở khi bệnh nhân gắng sức và đỡ khi nghỉ.
Trong quá trình phát triển của mảng xơ vữa, một số trường hợp có thể xuất hiện những biến cố cấp tính do sự nứt vỡ mảng xơ vữa, dẫn tới hình thành huyết khối gây hẹp hoặc tắc lòng mạch một cách nhanh chóng được gọi là hội chứng động mạch vành cấp (HCMVC).
Do quá trình diễn tiến động của bệnh lý mạch vành và cơ chế sinh lý bệnh không chỉ là tổn thương mạch vành thượng tâm mạc mà có cả cơ chế tổn thương hệ vi tuần hoàn vành, co thắt mạch… Do vậy, hiện nay thuật ngữ “Hội chứng động mạch vành mạn” được chính thức công bố, viết tắt là HCMVM.
CÁC BỆNH CẢNH LÂM SÀNG CỦA HCMVM
Theo ESC 2019, hội chứng ĐMV mạn có 6 bệnh cảnh lâm sàng:
- Bệnh nhân nghi ngờ có bệnh ĐMV với triệu chứng đau thắt ngực ổn định và/hoặc khó thở.
- Bệnh nhân mới khởi phát triệu chứng suy tim/giảm chức năng thất trái và nghi ngờ có bệnh lý bệnh ĐMV.
- Bệnh nhân có tiền sử hội chứng động mạch vành cấp hoặc được tái thông ĐMV trong vòng 1 năm, có hoặc không có triệu chứng.
- Bệnh nhân sau hội chứng động mạch vành cấp hoặc được tái thông ĐMV trên 1 năm.
- Bệnh nhân đau thắt ngực nghi ngờ do bệnh lý vi mạch hoặc co thắt ĐMV.
- Bệnh nhân không triệu chứng, khám sàng lọc phát hiện ra bệnh động mạch vành.
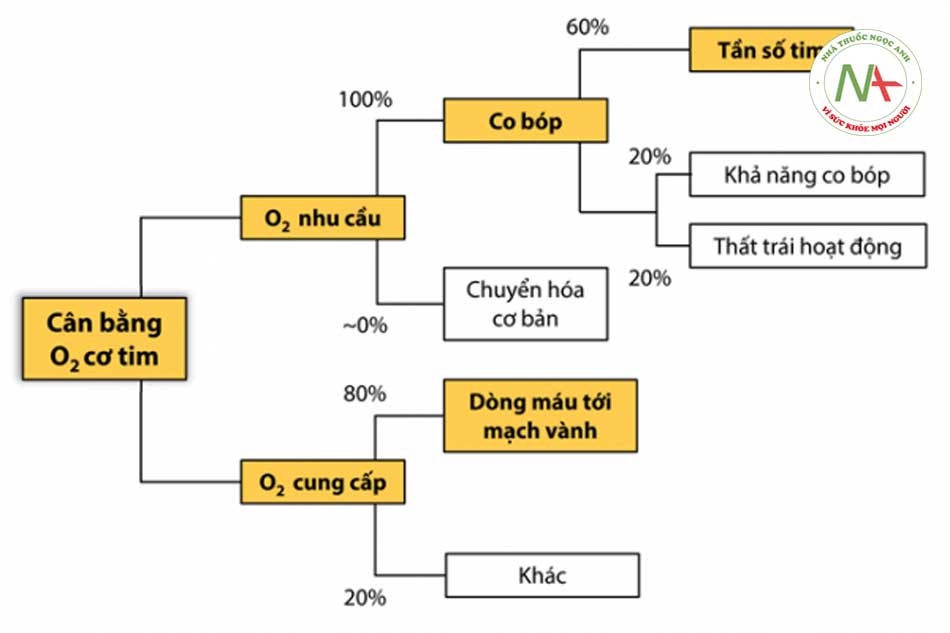
SINH LÝ BỆNH
Do có sự mất cân bằng giữa khả năng cung cấp oxy cho cơ tim (80% liên quan đến dòng chảy trong mạch vành) và nhu cầu tiêu thụ (60% liên quan đến nhịp tim).
MỤC TIÊU ĐIỀU TRỊ
Mục tiêu điều trị
Hai mục tiêu điều trị chính ở bệnh nhân hội chứng ĐMV mạn là giảm triệu chứng đau thắt ngực, thiếu máu cục bộ cơ tim do gắng sức và phòng ngừa biến cố tim mạch.
- Giảm triệu chứng do thiếu máu cục bộ cơ tim: Có nhiều loại thuốc để điều trị triệu chứng đau thắt ngực nhanh chóng cũng như lâu dài, lựa chọn và phối hợp thuốc là khác nhau giữa các cá nhân.
- Phòng ngừa biến cố tim mạch: Tập trung chủ yếu vào giảm tỷ lệ biến cố cấp (hội chứng mạch vành cấp) và xuất hiện rối loạn chức năng tâm thất, thông qua các thuốc, can thiệp và thay đổi lối sống.
- Điều trị tối ưu có thể được định nghĩa là kiểm soát được các triệu chứng và phòng ngừa các biến cố tim mạch liên quan đến HCMVM với sự tuân thủ điều trị tối đa và biến cố tối thiểu. Tuy nhiên, định nghĩa toàn cầu về điều trị tối ưu ở bệnh nhân HCMVM đến nay vẫn chưa có và việc lựa chọn thuốc ban đầu phụ thuộc vào khả năng dung nạp, đặc điểm, các bệnh đồng mắc của từng bệnh nhân, tương tác giữa các thuốc điều trị, sự lựa chọn của bệnh nhân sau khi được giải thích các tác dụng phụ cũng như sự sẵn có của thuốc. Thuốc khởi trị thường bao gồm một hoặc hai thuốc chống đau thắt ngực cộng với các thuốc phòng ngừa thứ phát các biến cố tim mạch.
Thay đổi lối sống
Theo khuyến cáo chung trong bệnh lý động mạch vành.
- Bỏ thuốc lá.
- Chế độ ăn lành mạnh.
- Hạn chế rượu.
- Kiểm soát cân nặng.
- Tập luyện thể dục thường xuyên.
- Điều trị các rối loạn tâm lý nếu có.
- Tránh môi trường ô nhiễm.
- Tiêm phòng cúm hằng năm.
ĐIỀU TRỊ NỘI KHOA: THUỐC ĐIỀU TRỊ CƠN ĐAU THẮT NGỰC
Thuốc chẹn beta giao cảm
Chẹn beta giao cảm là thuốc khởi đầu trong điều trị giảm đau ngực ở hầu hết bệnh nhân.
– Cơ chế của thuốc:
- Giảm tiêu thụ oxy cơ tim do giảm nhịp tim, giảm co bóp cơ tim và giảm hậu gánh.
- Giảm tái cấu trúc cơ tim do giảm sức căng thành thất trái.
- Kéo dài thời kỳ tâm trương, tăng tưới máu động mạch vành, làm tăng cung cấp oxy cơ tim.
– Lợi ích của việc điều trị chẹn beta giao cảm lâu dài : chưa chứng minh được làm giảm tỷ lệ tử vong và các biến cố tim mạch chính ở các bệnh nhân có bệnh lý động mạch vành được can thiệp qua da mà không có nhồi máu cơ tim và suy tim trước đó. Tuy nhiên, trên nhóm bệnh nhân được CABG chẹn beta được chứng minh làm giảm tỷ lệ tử vong và các biến cố tim mạch. Sử dụng chẹn beta sau một năm ở nhóm bệnh nhân sau NMCT chưa chứng minh hiệu quả rõ ràng.
– Thuốc được chỉ định bắt buộc cho các bệnh nhân có rối loạn chức năng tâm thu thất trái (EF ≤ 40%) hoặc tiền sử nhồi máu cơ tim, trừ khi có chống chỉ định. Các thuốc đã được chứng minh làm giảm nguy cơ tử vong: metoprolol succinate, carvedilol, bisoprolol, nebivolol.
- Liều lượng: liều tối đa có thể dụng nạp để đạt tần số tim 55 -60 nhịp/phút.( metoprolol succinate 200 mg, carvedilol 50 mg, bisoprolol 10 mg).
- Chống chỉ định: đợt cấp bệnh phổi mạn tính, nhịp chậm, suy tim sung huyết. Thận trọng khi dùng phối hợp các thuốc làm giảm nhịp tim khác.
Chẹn kênh canxi
- Gồm hai nhóm dihydropyridine (amlodipine, felodipine, lacidipine, nifedipine) và nondihydropyridine (diltiazem và verapamil).
- Cả hai nhóm đều có vai trò trong cải thiện cung cấp oxy cơ tim do giảm sức cản mạch vành, tăng dòng chảy động mạch hệ thống. Làm giảm nhu cầu oxy cơ tim bằng cách giảm co bóp cơ tim, giảm sức cản mạch hệ thống và giảm huyết áp. Các thuốc chẹn kênh canxi được chứng minh làm giảm tỷ lệ nhập viện do đau ngực và giảm tỷ lệ can thiệp động mạch vành.Tuy nhiên, chưa được chứng minh làm giảm đáng kể tỷ lệ tử vong và các biến cố tim mạch trên bệnh nhân hội chứng động mạch vành mạn.
Nhóm nitrate
– Giãn hệ động mạch vành và hệ tĩnh mạch, giảm triệu chứng đau thắt ngực dựa trên cơ chế giải phóng nitric oxide (NO) và giảm tiền gánh.
– Các nitrate tác dụng ngắn: Nitroglycerine xịt/ngậm dưới lưỡi (liều 0,3 – 0,6 mg mỗi 5 phút, cho đến tối đa 1,2 mg trong 15 phút), tác dụng tức thời dùng trong cơn đau ngực cấp hoặc dự phòng đau thắt ngực sau các hoạt động gắng sức, cảm xúc mạnh hay thời tiết lạnh…
– Các nitrate tác dụng dài: Được cân nhắc như là liệu pháp thay thế để giảm đau ngực khi có chống chỉ định với thuốc chẹn beta và chẹn kênh canxi non-dihydropyrine, không kiểm soát được triệu chứng đau ngực. Thuốc sẽ mất hiệu quả nếu sử dụng thường xuyên trong thời gian dài mà không có khoảng nghỉ hoặc giảm liều nitrate trong khoảng 10 – 14h.
- Liều lượng nitrate tác dụng dài: Liều tối đa có thể dung nạp giúp giảm triệu chứng đau ngực. Dạng mononitrate có sinh khả dụng cao hơn so với dinitrate. Các tác dụng phụ hay gặp: tụt huyết áp, đau đầu.
- Lưu ý: Nitrate đường uống tác dụng kéo dài không phải là thuốc đầu tay điều trị triệu chứng đau ngực. Thuốc được phối hợp thêm với chẹn beta hoặc chẹn kênh canxi trong trường hợp bệnh nhân hội chứng động mạch vành mạn còn triệu chứng (Hình 17.2).
– Chống chỉ định: Bệnh cơ tim phì đại có gây hẹp đường ra thất trái, hẹp van động mạch chủ nặng và dùng phối hợp với nhóm ức chế phosphodiesterase (ví dụ: sildenafil…)
Ivabradine
Có vai trò trong kiểm soát tần số tim và triệu chứng đau thắt ngực. Các nghiên cứu cho thấy ivabradine không thua kém atenolol và amlodipine trong điều trị giảm triệu chứng đau ngực. Nghiên cứu BEAUTIFUL (n=10917) và SIGNIFY (n=19102) chưa cho thấy hiệu quả giảm biến cố tim mạch, nhồi máu cơ tim và suy tim của ivabradine.
Thuốc có thể sử dụng kết hợp cùng hoặc thay thế thuốc chẹn beta giao cảm khi không dung nạp với thuốc chẹn beta. Nghiên cứu CONTROL-2 cho thấy việc phối hợp ivabradine với chẹn beta giao cảm giúp cải thiện triệu chứng thiếu máu cơ tim hơn là tăng liều chẹn beta giao cảm.
Trimetazidine
Là thuốc điều chỉnh chuyển hóa năng lượng cơ tim, giảm nhu cầu oxy cơ tim, giúp cải thiện tình trạng đau ngực, vì vậy ít ảnh hưởng đến huyết động. Trimetazidine (35 mg x 2 lần/24h) điều trị phối hợp với chẹn beta (metoprolol, atenolol) chứng minh làm giảm thiếu máu cơ tim so với dùng chẹn beta giao cảm đơn độc. Khuyến cáo ESC 2019 về điều trị Hội chứng mạch vành mạn tính đã nâng mức khuyến cáo của trimetazidine lên Iia, khẳng định hiệu quả, độ an toàn của trimetazidine.
- Các nghiên cứu lâm sàng đã cho thấy hiệu quả và an toàn của trimetazidine trong điều trị trên các bệnh nhân có hội chứng động mạch vành mạn tính, khi điều trị đơn độc hoặc phối hợp điều trị với các thuốc chống đau thắt ngực khác, giúp giảm triệu chứng đau ngực và tăng khả năng gắng sức (Nghiên cứu TRIMPOL-II, Nghiên cứu VASCO).
- Nghiên cứu thế giới thực ODA thực hiện trên 3066 bệnh nhân đau thắt ngực tại Nga đã chứng minh TMZ 80mg 1 lần/ngày, kết hợp với các biện pháp điều trị chống đau ngực khác, làm giảm số cơn đau ngực và số lần sử dụng nitrate tác dụng ngắn, cải thiện khả năng gắng sức và tăng mức độ tuân thủ điều trị trên cả hai nhóm bệnh nhân được khởi trị hoặc chuyển đổi từ liều TMZ MR 35mg 2 lần/ngày hoặc TMZ 20mg 3 lần/ngày.
- Phân tích gộp trên 13 nghiên cứu khác (n = 1628 bệnh nhân) cho thấy thuốc làm giảm tần suất, mức độ xuất hiện cơn đau ngực, khả năng gắng sức so với các thuốc giảm đau khác ở bệnh nhân đau ngực không rõ nguyên nhân, chụp động mạch vành bình thường. Thuốc không được chỉ định ở bệnh nhân Parkinson hoặc có rối loạn vận động( run cơ, co cứng cơ…).
Nicorandil
Là một dẫn xuất nitrate của nicotinamide được sử dụng để phòng ngừa và điều trị đau thắt ngực lâu dài. Nghiên cứu IONA (n = 5.126) chưa cho thấy hiệu quả giảm tử vong do bệnh tim thiếu máu, nhồi máu cơ tim không tử vong. Thuốc được chỉ định liệu pháp thứ phát trong điều trị đau ngực do bệnh lý động mạch vành mạn tính, có thể phối hợp với chẹn beta giao cảm.
Ranolazine
Ức chế lựa chọn kênh natri muộn giảm triệu chứng đau ngực. Trong một phân tích dưới nhóm ở các bệnh nhân đau ngực mạn tính (n = 3.565) thuốc giúp làm giảm tần suất xuất hiện, mức độ đau ngực và tối ưu hoá điều trị đau ngực ở các bệnh nhân đã điều trị với các thuốc khác. Trên nhóm bệnh nhân đái tháo đường và có bệnh lý động mạch vành đã điều trị 1 hoặc 2 thuốc giảm đau ngực thông thường, ranolazine cho thấy giúp làm giảm mức độ đau ngực và sử dụng nitroglycerine dạng xịt. Nghiên cứu RIVER-PCI (n = 2.651) ranolazine không làm giảm tỷ lệ can thiệp động mạch vành. Thuốc được chỉ định như liệu pháp thứ phát ở bệnh nhân CCS còn đau ngực sau khi đã điều trị bằng chẹn beta giao cảm, chẹn kênh canxi và hoặc nitrate tác dụng kéo dài. Thuốc có thể gây tác dụng phụ: buồn nôn, nôn, táo bón và làm QTc dài.
Chiến lược điều trị chống thiếu máu cục bộ ở bệnh nhân hội chứng động mạch vành mạn
Chiến lược tiếp cận từng bước điều trị thuốc chống đau thắt ngực trong hội chứng động mạch vành mạn được đề xuất dưới đây phụ thuộc vào một số đặc điểm ban đầu của bệnh nhân (Hình 17.2). Đáp ứng không hoàn toàn hoặc dung nạp kém ở mỗi bước cần chuyển sang bước tiếp theo. Chiến lược nên được điều chỉnh theo đặc điểm và sự phù hợp với từng bệnh nhân (cá thể hoá điều trị).
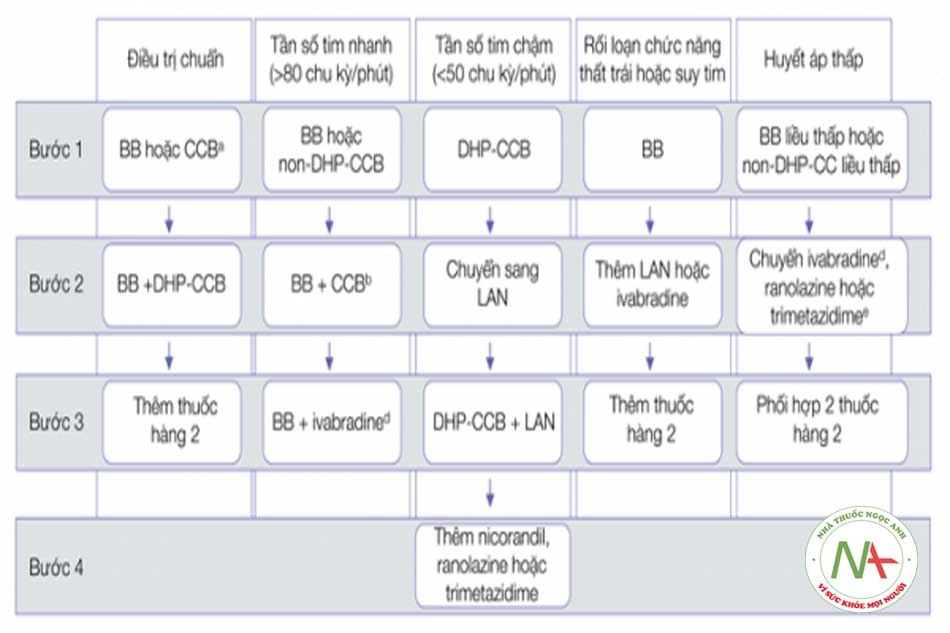
Chú thích: BB: Chẹn beta giao cảm, CCB: Chẹn kênh canxi (bất kỳ nhóm nào), DHP-CCB: Chẹn kênh canxi nhóm dihydropyridine, non-DHP-CCB: Chẹn kênh canxi nhóm non-dihydropyridine LAN: Nitrate tác dụng kéo dài. a: kết hợp BB với DHP-CCB nên được cân nhắc là bước 1, kết hợp BB hoặc CCB với một thuốc hàng hai có thể được cân nhắc là bước 1; b: sự kết hợp BB và non-DHP-CCB nên khởi đầu với liều thấp ở mỗi thuốc và theo dõi chặt chẽ đáp ứng đặc biệt là tần số tim và huyết áp; c: BB liều thấp hoặc non-DHP-CCB liều thấp nên được dùng dưới sự theo dõi chặt chẽ đáp ứng đặc biệt là tần số tim và huyết áp; d: Ivabradine không nên kết hợp cùng non-DHP-CCB; e: cân nhắc phối hợp thêm thuốc được chọn ở bước 2 với thuốc đã được dùng thử ở bước 1 nếu huyết áp vẫn duy trì không đổi.
ĐIỀU TRỊ NỘI KHOA: CÁC THUỐC PHÒNG NGỪA BIẾN CỐ TIM MẠCH
Thuốc kháng kết tập tiểu cầu
Aspirin vẫn là nền tảng trong điều trị phòng ngừa biến cố huyết khối động mạch. Thuốc hoạt động thông qua ức chế không hồi phục cyclooxygenase (COX-1).
- Aspirin 75 – 100 mg/24h được chỉ định: Những bệnh nhân tiền sử NMCT hoặc tái thông ĐMV; hoặc xem xét ở bệnh nhân không có tiền sử NMCT hoặc tái thông ĐMV nhưng có bằng chứng hình ảnh rõ ràng của bệnh ĐMV.
- Clopidogrel 75 mg/24h ở bệnh nhân hội chứng ĐMV mạn trong tình huống nói trên để thay cho aspirin khi bệnh nhân có chống chỉ định với aspirin. Nghiên cứu CAPRIE (so sánh clopidogrel với aspirin ở bệnh nhân có nguy cơ thiếu máu do xơ vữa) cho thấy clopidogrel không thua kém so với aspirin trong phòng ngừa các biến cố tim mạch ở bệnh nhân tiền sử NMCT, đột quỵ não hoặc có bệnh động mạch ngoại biên (PAD). Thậm chí trong nhóm bệnh động mạch chi dưới clopidogrel còn cho thấy hiệu quả vượt trội hơn. Thuốc tác động qua CYP2C19 nên có thể tương tác với các thuốc ức chế enzym này (omeprazol), do đó cần thận trọng khi phối hợp thuốc.
- Prasugrel: Hiệu quả chống kết tập tiểu cao, nhanh hơn, mạnh hơn và cũng ít tương tác với gen CYP2C19 hơn so với clopidogrel. Tuy nhiên, nguy cơ chảy máu ( cả tử vong và không tử vong) cao hơn clopidogrel đặc biệt trên các bệnh nhân > 75 tuổi, cân nặng < 60 kg và tiền sử nhồi máu não. Thuốc được chỉ định cho nhóm bệnh nhân có hội chứng động mạch vành cấp cần can thiệp động mạch vành qua da.
- Ticagrelor: Hiệu quả kháng kết tập tiểu cầu nhanh hơn và mạnh hơn so với clopidogrel. Ticagrelor liều 90 mg và 60 mg hai lần/24h giúp làm giảm tỷ lệ biến cố gồm NMCT, đột quỵ và tử vong do tim mạch ở thời điểm 3 năm trên các bệnh nhân có tiền sử NMCT trước đó. Tuy nhiên, thuốc cũng làm tăng tỷ lệ chảy máu. Hiện tại bằng chứng về lợi ích của việc sử dụng ticagrelor trên bệnh nhân có hội chứng động mạch vành mạn tính còn hạn chế. Nghiên cứu THEMIS mới được công bố gần đây (2019) được thực hiện trên 19.271 bệnh nhân có bệnh mạch vành mạn và đái tháo đường. Trên nền điều trị aspirin hằng ngày (75 – 100 mg), sử dụng thêm ticagrelor liều 60 mg hai lần mỗi ngày cho thấy hiệu quả vượt trội trên tiêu chí chính làm giảm tỷ lệ biến cố tử vong tim mạch, nhồi máu cơ tim hay đột quỵ. Đặc biệt, ticagrelor hiệu quả tốt hơn với phân nhóm bệnh nhân có tiền sử can thiệp mạch vành qua da.
- Kháng kết tập tiểu cầu kép: Chỉ định dùng 6 tháng cho bệnh nhân HCMVM được PCI. Có thể chỉ định ngắn hơn 1-3 tháng nếu nguy cơ chảy máu đe doạ tính mạng cao và nguy cơ huyết khối thấp. Nghiên cứu DAPT cho thấy với việc sử dụng kéo dài trên 12 tháng sau PCI với clopidogrel và prasugrel giúp làm giảm biến cố về thiếu máu và huyết khối trong stent nhưng chưa cho thấy lợi ích cải thiện tử vong chung và làm tăng nguy cơ chảy máu. Nghiên cứu PEGASUS-TIMI 54 cho thấy sử dụng ticagrelor kéo dài cho bệnh nhân ổn định sau 1 năm NMCT giúp làm giảm biến cố liên quan thiếu máu. Đặc biệt liều 60 mg x 2 lần/24h giúp làm giảm rõ ràng trên nhóm bệnh nhân nguy cơ NMCT cao: đái tháo đường, bệnh động mạch chi dưới và tổn thương nhiều nhánh động mạch vành.
- Dùng aspirin kết hợp với thuốc chống huyết khối thứ 2 (kháng kết tập tiểu cầu hoặc thuốc chống đông khác) trong phòng ngừa thứ phát nên cân nhắc ở bệnh nhân nguy cơ tắc mạch cao và nguy cơ chảy máu thấp:
- Nguy cơ tắc mạch cao: Bệnh nhiều thân ĐMV kèm theo ít nhất một trong các yếu tố sau: Đái tháo đường cần điều trị bằng thuốc, NMCT tái phát, bệnh động mạch ngoại biên hoặc bệnh thận mạn với MLCT từ 15 – 59 mL/phút/1,73m2.
- Nguy cơ chảy máu cao: Tiền sử chảy máu nội sọ/đột quỵ thiếu máu não; xuất huyết tiêu hóa gần đây hoặc thiếu máu do suy gan, suy thận; bệnh lý tăng nguy cơ chảy máu, tuổi cao.
Thuốc chống đông đường uống
- Bệnh nhân nhịp xoang: Các báo cáo gần đây cho thấy có thể kết hợp các thuốc chống đông đường uống liều thấp với kháng KTTC nhằm phòng ngừa các huyết khối trong stent.
- Rivaroxaban 2,5 mg so với giả dược giúp làm giảm biến cố NMCT, đột quỵ, tử vong do tim mạch ở bệnh nhân sau ACS và được điều trị phối hợp aspirin và clopidogrel.
- Nghiên cứu COMPASS khi so sánh việc sử dụng aspirin đơn độc và rivaroxaban 5 mg đơn độc ở bệnh nhân CCS hoặc PAD cho thấy rivaroxaban giúp làm giảm các biến cố liên quan đến thiếu máu đặc biệt trên nhóm đái tháo đường, bệnh động mạch chi dưới, bệnh thận mạn mức độ trung bình và còn sử dụng thuốc lá.
- Nghiên cứu GEMINI-ACS cho thấy việc sử dụng rivaroxaban 2,5 mg x 2 lần/24h so với dùng aspirin ở bệnh nhân được dùng kháng P2Y12 và ổn định sau can thiệp động mạch vành có độ an toàn như nhau. Tuy nhiên, vẫn cần các nghiên cứu lớn hơn và độ an toàn thực sự trên nhóm bệnh nhân được tiến hành can thiệp động mạch vành mà không dùng aspirin thì vẫn chưa rõ ràng.
- Bệnh nhân rung nhĩ: Có chỉ định dùng kéo dài thuốc chống đông đường uống (DOAC hoặc VKA với khoảng thời gian đạt liều điều trị đạt trên 70% (time-in-therapeutic range > 70%) nếu CHA2DS2-VASc ≥ 3 điểm ở nữ, ≥ 2 điểm ở nam. Liệu pháp chống đông đường uống ở bệnh nhân rung nhĩ và HCMVM giúp làm giảm tỷ lệ đột quỵ và biến cố liên quan đến thiếu máu. Nó cho thấy hiệu quả vượt trội hơn so với aspirin đơn độc hoặc kháng kết tập tiểu cầu kép trong phòng ngừa đột quỵ. Trong đó DOAC được khuyến cáo thích hợp hơn kháng vitamin K đường uống. Chống đông đường uống dùng đơn độc cho bệnh nhân rung nhĩ sau can thiệp động mạch vành 6 – 12 tháng. Tuy nhiên nhóm bệnh nhân nguy cơ thiếu máu cao có thể cân nhắc dùng phối hợp chống đông đường uống với aspirin hoặc clopidogrel.
Bảng 17.1. Các thuốc được dùng phối hợp với aspirin trong dự phòng biến cố ở bệnh nhân có nguy cơ tắc mạch trung bình/cao và không có nguy cơ xuất huyết
| Thuốc | Liều | Chỉ định | Thận trọng |
| Clopidogrel | 75 mg, 1 lần/24h | Sau NMCT dung nạp tốt với liệu pháp kháng kết tập tiểu cầu kép trên 12 tháng | |
| Prasugrel | 10 mg 1 lần/24h hoặc 5 mg 1 lần/24h nếu < 60 kg hoặc > 75 tuổi | Sau can thiệp do NMCT dung nạp tốt với liệu pháp kháng kết tập tiểu cầu kép trên 12 tháng | Trên 75 tuổi |
| Rivaroxaban | 2,5 mg x 2 lần/24h | Sau NMCT >1 năm hoặc bệnh nhiều thân mạch vành | MLCT 15 – 29 mL/phút/1,73m2 |
| Ticagrelor | 60 mg x 2 lần/24h | Bệnh nhân sau NMCT dung nạp tốt với liệu pháp kháng kết tập tiểu cầu kép trên 12 tháng |
Chú thích: NMCT: Nhồi máu cơ tim, MLCT: Mức lọc cầu thận
Thuốc điều trị hạ lipid máu
- Statin được chỉ định cho tất cả bệnh nhân hội chứng ĐMV mạn với mục tiêu giảm LDL-C ≥ 50% so với mức nền (khi bệnh nhân chưa được điều trị bằng bất kỳ thuốc hạ lipid máu nào) và đích LDL-C < 1,4 mmol/L (< 55 mg/dL). Mức đích LDL-C <1,0 mmol/L được cân nhắc ở những bệnh nhân có biến cố mạch máu vẫn xuất hiện trong vòng 2 năm khi đã điều trị tối ưu.
- Nếu mục tiêu không đạt được với liều tối đa dung nạp được của statin, khuyến cáo phối hợp thêm ezetimibe. Việc thêm này giúp làm giảm biến cố tim mạch ở bệnh nhân sau ACS, tuy nhiên chưa chứng minh hiệu quả trong việc giảm tỷ lệ tử vong. Nếu vẫn không đạt được mục tiêu điều trị thì khuyến cáo phối hợp thêm với thuốc ức chế PCSK9.
- Với những bệnh nhân được tiến hành PCI, việc sử dụng statin cường độ cao (atorvastatin 40 – 80mg, rosuvastatin 20mg) giúp làm giảm các biến cố xung quanh thủ thuật.
- Khởi đầu với statin càng sớm càng tốt, trước khi tiến hành PCI giúp giảm đáng kể hsCRP, giảm có ý nghĩa thống kê biến cố tim mạch sau PCI.
Thuốc ức chế hệ Renin – Angiotensin – Aldosterone
- Thuốc ức chế men chuyển nên được sử dụng ở tất cả bệnh nhân hội chứng ĐMV mạn có tăng huyết áp, đái tháo đường, phân suất tống máu thất trái (EF) ≤ 40%, bệnh thận mạn, trừ khi có chống chỉ định.
- Một phân tích tổng hợp từ 24 nghiên cứu (n = 61.961) cho thấy ở bệnh nhân hội chứng động mạch vành mạn mà không có suy tim việc sử dụng ức chế hệ thống renin – angiotensin (RAS) chưa chứng minh được hiệu quả rõ ràng giúp làm giảm tỷ lệ tử vong và các biến cố tim mạch.
- Thuốc ƯCMC nên cân nhắc ở bệnh nhân hội chứng ĐMV mạn có nguy cơ rất cao xảy ra biến cố tim mạch. Thuốc ƯCTT được khuyến cáo ở bệnh nhân hội chứng ĐMV mạn khi không dung nạp với ức chế men chuyển.
- Việc sử dụng thuốc phối hợp giữa valsartan và sacubitril (ức chế neprilysin) trong một viên thay thế cho ƯCMC ở những bệnh nhân suy tim EF ≤ 35% vẫn còn triệu chứng sau điều trị với ƯCMC, chẹn beta và kháng aldosterone được khuyến cáo giúp làm giảm tỷ lệ nhập viện do suy tim và cải thiện tỷ lệ tử vong (nghiên cứu PIONEER và PARADIGM- HF).
- Kháng aldosterone (spironolactone và eplerenone) được chỉ định ở các bệnh nhân suy tim EF ≤ 35% sau nhồi máu cơ tim đã được điều trị với ƯCMC và chẹn beta. Thận trọng ở bệnh nhân có suy thận (eGFR < 45 mL/ phút/1,73 m2) và kali máu > 5,0 mmol/L.
Các thuốc khác
Nếu bệnh nhân có nguy cơ xuất huyết tiêu hóa cao, thuốc ức chế bơm proton được khuyến cáo sử dụng đồng thời với liệu pháp chống ngưng tập tiểu cầu hoặc chống đông.
Những điều trị không giảm nguy cơ tử vong/nhồi máu cơ tim
- Liệu pháp hormone bằng estrogen.
- Vitamin C, vitamin E, beta-carotene.
- Điều trị tăng homocystein với folate hoặc vitamin B6, B12.
- Liệu pháp chống oxy hóa.
- Điều trị với tỏi, coenzyme Q10, Selenium hoặc Crom.
PHẦN II. NHỒI MÁU CƠ TIM CẤP CÓ ST CHÊNH LÊN
Bước đầu tiên trong việc xử trí bệnh nhân bị nhồi máu cơ tim cấp có ST chênh lên (STEMI) là chẩn đoán kịp thời, vì tái tưới máu cơ tim chỉ đạt được hiệu quả cao với các trường hợp được chẩn đoán sớm. Một khi bệnh nhân đã được chẩn đoán xác định, vấn đề điều trị tiếp theo cần đạt được các mục tiêu sau đây:
- Giảm đau do thiếu máu cơ tim.
- Đánh giá tình trạng huyết động và điều chỉnh các bất thường đang có.
- Bắt đầu điều trị tái tưới máu bằng can thiệp mạch vành qua da (PCI) tiên phát hoặc tiêu sợi huyết.
- Sử dụng thuốc chống đông để ngăn ngừa tình trạng tăng đông hoặc huyết khối stent cấp tính.
- Thuốc chẹn beta giao cảm để ngăn ngừa thiếu máu cục bộ tái phát và rối loạn nhịp thất đe dọa tính mạng.
Tiếp theo là sử dụng các loại thuốc giúp cải thiện tiên lượng lâu dài bao gồm:
- Thuốc kháng tiểu cầu để giảm nguy cơ huyết khối động mạch vành tái phát hoặc trong trường hợp được PCI – tránh huyết khối stent động mạch vành.
- Thuốc ƯCMC hoặc ƯCTT để giảm nguy cơ tái cấu trúc cơ tim.
- Thuốc statin.
- Thuốc chống đông nếu có sự hiện diện của huyết khối thất trái hoặc rung nhĩ để ngăn ngừa thuyên tắc.
Trong khuôn khổ cuốn sách này chúng tôi chỉ trình bày về các thuốc điều trị nội khoa tương ứng với từng mục tiêu điều trị. Vấn đề chẩn đoán, can thiệp tái thông động mạch vành độc giả có thể tham khảo ở cuốn “Lâm sàng tim mạch học”.
GIẢM ĐAU DO THIẾU MÁU CƠ TIM
Nitrate
- Nitroglycerin truyền tĩnh mạch (liều từ 10 – 100 µg/phút, chỉnh liều theo đáp ứng của bệnh nhân) có thể có tác dụng ở những bệnh nhân vẫn còn đau ngực sau khi dùng nitroglycerin xịt dưới lưỡi hoặc ở các bệnh nhân tăng huyết áp, suy tim.
- Tuy nhiên, khi sử dụng phải hết thận trọng nếu bệnh nhân có khả năng bị hạ huyết áp hoặc có thể dẫn đến mất bù huyết động nghiêm trọng, như nhồi máu thất phải hoặc hẹp van động mạch chủ kèm theo. Ngoài ra, còn chống chỉ định ở những bệnh nhân đã sử dụng chất ức chế phosphodiesterase để điều trị rối loạn cương dương (hoặc tăng áp ĐMP) trong vòng 24h.
Morphine
- Liều dùng: tiêm tĩnh mạch ( hoặc tiêm bắp) ban đầu từ 2 – 4 mg, tăng thêm 2 – 8 mg được lặp lại sau khoảng thời gian từ 5 đến 15 phút nếu bệnh nhân còn đau.
- Nghiên cứu CRUSADE với 57.039 bệnh nhân mắc hội chứng động mạch vành cấp không có ST chênh lên cho thấy những bệnh nhân được điều trị bằng morphine (29,8%) có nguy cơ tử vong cao hơn so với những người không sử dụng (OR 1,48; CI 95% 1,33-1,64). Do đó nên tránh dùng morphine nếu có thể và chỉ cho khi bệnh nhân đau dữ dội không đáp ứng với liệu pháp khác.
- Mặc dù cơ chế morphine liên quan đến tăng tỷ lệ tử vong vẫn chưa được hiểu rõ nhưng có ít nhất hai nghiên cứu đã cho thấy morphine có khả năng ảnh hưởng đến tác dụng kháng tiểu cầu của thuốc chẹn thụ thể P2Y12:
- Trong thử nghiệm IMPRESSION, 70 bệnh nhân NMCT được điều trị bằng ticagrelor được dùng ngẫu nhiên morphine tiêm tĩnh mạch (5 mg) hoặc giả dược. Kết quả cho thấy morphine làm giảm nồng độ ticagrelor trong huyết tương, vì vậy làm giảm tác dụng kháng tiểu cầu.
- Trong một nghiên cứu khác trên 24 đối tượng khỏe mạnh được dùng liều nạp 600 mg clopidogrel và 5 mg morphine hoặc giả dược tiêm tĩnh mạch, morphine đã làm chậm đáng kể sự tái hấp thu clopidogrel và giảm diện tích dưới đường cong của chất chuyển hóa hoạt động của clopidogrel xuống 52% . Hoạt độ ức chế tiểu cầu, được đo bằng nhiều xét nghiệm, ít hơn rõ rệt ở những người sử dụng morphine.
TÁI TƯỚI MÁU CƠ TIM BẰNG THUỐC TIÊU SỢI HUYẾT
Tái thông mạch vành bằng phương pháp tiêu sợi huyết đem lại hiệu quả cho 50 – 70% các bệnh nhân NMCT cấp có ST chênh lên trong vòng 4 – 6h đầu từ khi xuất hiện triệu chứng đau ngực; giúp làm giảm tỷ lệ tử vong, rối loạn chức năng thất trái, suy tim sau nhồi máu, sốc tim và rối loạn nhịp tim. Phương pháp này nên được tiến hành càng sớm càng tốt, thậm chí ngay trên xe cấp cứu đến bệnh viện (nếu có thể).
Trong vòng 2 – 24h sau khi tiêu sợi huyết thành công, người bệnh vẫn cần được chụp lại động mạch vành, đánh giá lại tổn thương thủ phạm và đặt stent giải quyết tình trạng hẹp mạch vành nếu cần thiết.
Chỉ định tiêu sợi huyết
- Đau thắt ngực điển hình kèm theo hình ảnh đoạn ST chênh lên trên điện tâm đồ (ít nhất 2 chuyển đạo liên tiếp với đoạn ST chênh lên ≥ 2,5 mm ở nam < 40 tuổi, ≥ 2,0 mm ở nam ≥ 40 tuổi hoặc ≥ 0,5 mm ở nữ trong chuyển đạo V2-V3 và/ hoặc ≥ 1 mm ở các chuyển đạo khác) trong vòng 12h từ khi khởi phát triệu chứng.
- Đau thắt ngực với block nhánh trái mới xuất hiện.
- Nếu điện tâm đồ không rõ ràng lúc nhập viện, phải làm lại sau 15-30 phút để theo dõi sự tiến triển.
- Tiêu sợi huyết không được chỉ định nếu hình ảnh điện tâm đồ bình thường, hoặc chỉ có ST chênh xuống (cần loại trừ nhồi máu cơ tim thành sau), hoặc ST chênh lên mà không có triệu chứng đau ngực trước đấy.
Chống chỉ định của tiêu sợi huyết
a. Chống chỉ định tuyệt đối
- Chảy máu đang tiến triển.
- Nghi ngờ tách thành động mạch chủ.
- Mới chấn thương đầu hoặc có khối u trong sọ.
- Tiền sử đột quỵ xuất huyết não.
- Tiền sử đột quỵ thiếu máu não trong vòng 3 tháng.
- Tiền sử dị ứng với thuốc tiêu sợi huyết.
- Chấn thương hoặc phẫu thuật trong vòng 2 tuần trước mà nguy cơ chảy máu cao.
b. Chống chỉ định tương đối
- Tiền sử chấn thương hoặc phẫu thuật trên 2 tuần.
- Tăng huyết áp nặng không kiểm soát (> 180/110 mmHg).
- Đột quỵ không xuất huyết não trên 1 năm.
- Rối loạn đông máu hoặc đang sử dụng thuốc chống đông (PT-INR > 2).
- Suy gan và thận nặng.
- Đã có cấp cứu ngừng tuần hoàn (> 10 phút).
- Tiền sử sử dụng streptokinase (đối với trường hợp dùng streptokinase làm thuốc tiêu sợi huyết).
- Mang thai hoặc sau sinh 1 tuần.
- Chọc dịch não tuỷ trong vòng 1 tháng trước.
- Chọc mạch ở vị trí không ép được (ví dụ tĩnh mạch dưới đòn).
Thời gian tiêu sợi huyết
Trong vòng 12h đầu: nên tiến hành sớm (đặc biệt trong 4h đầu) nếu các bệnh nhân không thể đến được các trung tâm có can thiệp ĐMV qua da trong vòng 2h kể từ khi được chẩn đoán NMCT cấp có ST chênh lên.
Chọn thuốc tiêu sợi huyết
- Phụ thuộc một phần vào chiến lược tiêu sợi huyết của bệnh viện.
- So với các thuốc khác, streptokinase gặp nhiều hơn phản ứng dị ứng và tụt huyết áp.
- Thuốc rt-PA có khả năng tái thông mạch vành thành công cao hơn và tỷ lệ sống sau 30 ngày cao hơn so với streptokinase nhưng tăng nguy cơ xuất huyết. Các dẫn xuất mới hơn của rt-PA tuy có tỷ lệ tái thông mạch vành trong vòng 90 phút với dòng chảy TIMI-3 cao hơn nhưng tỷ lệ tử vong sau 30 ngày tương tự rt-PA.
- Các dẫn xuất rt-PA nên xem xét cho các bệnh nhân sau:
- Nhồi máu cơ tim rộng thành trước, đặc biệt trong 4h đầu.
- Đã sử dụng streptokinase trước đây hoặc mới nhiễm khuẩn streptococcal.
- Huyết áp thấp (huyết áp tâm thu < 100 mmHg).
- Nguy cơ đột quỵ thấp (tuổi < 55, huyết áp tâm thu < 144 mmHg).
- Tái nhồi máu trong viện khi mà can thiệp mạch vành không sẵn sàng.
Bệnh nhân được hưởng lợi nhiều nhất từ tiêu sợi huyết
- Nhồi máu cơ tim thành trước.
- Đoạn ST chênh lên cao.
- Suy thất trái, block nhánh trái, tụt huyết áp.
- Huyết áp tâm thu < 100 mmHg.
- Đến viện trong vòng 1h từ khi đau ngực.
Biến chứng của tiêu sợi huyết
a. Chảy máu: tỷ lệ gặp khoảng 10%, hầu hết là chảy máu nhẹ, tại vị trí chọc mạch, chỉ cần băng ép tại chỗ là đủ. Tuy nhiên, đôi khi vẫn cần truyền máu. Nếu chảy máu nặng, có thể đảo ngược tác dụng của streptokinase với acid tranexamic (10 mg/kg truyền tĩnh mạch chậm).
b. Tụt huyết áp trong khi truyền streptokinase khá thường gặp. Xử trí:
- Để bệnh nhân nằm đầu bằng.
- Tạm ngừng hoặc truyền chậm tới khi huyết động ổn định.
- Test truyền dịch với 100 – 500 mL dịch đẳng trương có thể có ích đặc biệt với nhồi máu cơ tim thất phải. Trong trường hợp này, tụt huyết áp không phải là phản ứng dị ứng.
c. Phản ứng dị ứng
- Chủ yếu gặp với thuốc streptokinase, bao gồm: sốt, nổi ban, buồn nôn, đau đầu.
- Xử trí: Hydrocortisone 100 mg tiêm tĩnh mạch và chlorpheniramine 10 mg tĩnh mạch.
d. Xuất huyết nội sọ gặp ở 0,3% bệnh điều trị với streptokinase và 0,6% ở bệnh nhân điều trị với rt-PA.
e. Rối loạn nhịp sau tái tưới máu: hầu hết là tạm thời, tự hết, do tái tưới máu.
f. Tắc mạch hệ thống do ly giải huyết khối từ nhĩ trái, thất trái hoặc phình động mạch chủ.
Liều và đường dùng các thuốc tiêu sợi huyết
a. Streptokinase (SK):
- Liều 1,5 triệu đơn vị pha trong 100 mL nước muối sinh lý truyền trong 1h.
- Không dùng thường quy heparin sau khi truyền streptokinase, do tăng nguy cơ chảy máu mà không giảm nguy cơ tử vong.
b. rt-PA hay alteplase:
- Hiệu quả tiêu sợi huyết cao nhất khi dùng rt-PA liều cao từ đầu hoặc tăng tốc độ truyền (như nghiên cứu GUSTO).
- Liều dùng: 15 mg bolus tĩnh mạch, sau đó truyền tĩnh mạch 0,75 mg/kg trong 30 phút (không quá 50 mg), tiếp theo truyền 0,5 mg/kg trong 60 phút (không quá 35 mg).
- Cần tiếp tục truyền heparin sau khi dừng truyền alteplase.
c. Reteplase: Dùng 2 liều, mỗi liều 10 đơn vị, bolus trong vòng 10 phút. Mỗi liều cách nhau 30 phút.
d. Tenecteplase: chỉnh liều theo cân nặng
- < 60 kg: 30 mg
- ≥ 60 tới <70 kg: 35 mg
- ≥ 70 tới <80 kg: 40 mg
- ≥ 80 tới <90 kg: 45 mg
- ≥ 90 kg: 50 mg
- Khuyến cáo giảm nửa liều ở bệnh nhân >= 75 tuổi
e. APSAC (anistreplase): Tiêm tĩnh mạch 30 mg trong 2 – 5 phút.
Chú ý: Tất cả các bệnh nhân sau tiêu sợi huyết đều phải được vận chuyển tới trung tâm có thể can thiệp ĐMV qua da từ 2 – 24h sau tiêu sợi huyết. Chụp ĐMV cấp cứu với các trường hợp tiêu sợi huyết thất bại hoặc sốc tim, rối loạn huyết động.
THUỐC CHỐNG ĐÔNG
- NMCT cấp là hậu quả của hiện tượng nứt vỡ mảng xơ vữa ĐMV, dẫn đến hình thành huyết khối cấp gây ngừng trệ hoặc làm giảm lưu lượng tưới máu đoạn xa. Quá trình tạo nên cục máu đông bao gồm cả sự hình thành cục máu và tiêu sợi huyết nội tại. Vì vậy, mục tiêu của liệu pháp chống huyết khối (sự kết hợp giữa điều trị chống đông máu và kháng tiểu cầu) là ngăn ngừa sự tiến triển của cục máu đông và giúp tái cấu trúc trong trường hợp cục máu đông đã được điều trị tiêu sợi huyết (cơ chế tự thân hoặc bằng thuốc tiêu sợi huyết) hoặc PCI.
- Trên thực hành lâm sàng điều trị NMCT cấp có ST chênh lên chúng ta sẽ đối mặt với một trong ba bệnh cảnh:
- Bệnh nhân được tái thông ĐMV bằng PCI.
- Bệnh nhân được tái thông bằng tiêu sợi huyết.
- Bệnh nhân chỉ còn chỉ định điều trị nội khoa đơn thuần hoặc đã từ chối 2 phương án trên.
- Sử dụng thuốc chống đông trong 3 bệnh cảnh trên có sự khác biệt, cụ thể sẽ được trình bày sau đây.
Phân loại (xem thêm ở chương 9 – Các thuốc chống đông):
Có ba loại thuốc chống đông được sử dụng trong điều trị NMCT cấp có ST chênh lên:
a. Các loại heparin:
- Bao gồm heparin không phân đoạn (UFH) và heparin trọng lượng phân tử thấp (LMWH).
- Heparin không phân đoạn có một số hạn chế khi sử dụng ở bệnh nhân NMCT cấp. Trong đó hạn chế lớn nhất là phức hợp heparin-antithrombin không thể bất hoạt được thrombin liên kết trong một cục máu đông. Các thrombin này quay trở lại hoạt động như một yếu tố kích đông quan trọng tại vị trí của cục huyết khối trong mạch vành, đặc biệt nếu các cục đông này đã bị giáng hóa bởi các tác nhân tiêu sợi huyết
b. Thuốc ức chế trực tiếp thrombin
- Gồm các chất như hirudin, bivalirudin, lepirudin liên kết và làm bất hoạt một hoặc nhiều vị trí hoạt động trên phân tử thrombin. Trên thực hành lâm sàng hiện chỉ sử dụng bivalirudin.
c. Thuốc ức chế chọn lọc yếu tố Xa
- Fondaparinux: sản phẩm từ heparin pentasaccharide tổng hợp
Bệnh nhân được can thiệp ĐMV qua da thì đầu
- Thuốc chống đông phải được sử dụng càng sớm càng tốt một khi bệnh nhân được chỉ định can thiệp ĐMV qua da thì đầu. Các loại heparin, bivalirudin được khuyến cáo sử dụng ưu tiên trong trường hợp này, ngược lại với fondaparinux do thuốc này có nguy cơ gây huyết khối trong ống thông ( nghiên cứu OASIS -6). Nếu bệnh nhân sử dụng fondaparinux trước can thiệp, cần sử dụng heparin không phân đoạn hoặc bivalirudin trong quá trình can thiệp.
a. So sánh heparin không phân đoạn với bivalirudin
- Bắt đầu từ nghiên cứu HORIZONS AMI 2008 so sánh heparin KPĐ trực tiếp với bivalirudin, các nghiên cứu tiếp theo bao gồm EUROMAX 2013, HEAT – PPCI 2014, BRIGHT 2015, MATRIX 2015 và nghiên cứu quan trọng nhất VALIDATE – SWEDEHEART 2017 cho chúng ta thấy được tính hiệu quả, các biến chứng trong sử dụng hai thuốc này. Kết quả từ nghiên cứu VALIDATE – SWEDEHEART với 6006 bệnh nhân bị HCMVC cho thấy heparin KPĐ và bivalirudin không có sự khác biệt về kết cục chính (MACE) (12,8% so với 12,3%; HR 0,96; CI 95% 0,83 – 1,1), tỷ lệ huyết khối cấp trong stent cũng tương đương giữa hai nhóm. Kết quả này khác với một nghiên cứu registry cũng trong năm 2017 với 67.368 bệnh nhân bị NMCT cấp có ST chênh lên được PCI qua đường động mạch quay. Mặc dù tỷ lệ biến cố MACE giữa hai nhóm cũng không có sự khác biệt nhưng tỷ lệ huyết khối cấp trong stent cao hơn có ý nghĩa ở nhóm sử dụng bivalirudin.
- Với sự ra đời của các thuốc kháng kết tập tiểu cầu mới (ticagrelor, cangrelor, prasugrel) và sự phát triển của PCI qua đường động mạch quay. Hiện nay các khuyến cáo điều trị ưu tiên sử dụng heparin KPĐ so với bivalirudin nếu như bệnh nhân được dùng ticagrelor hoặc prasugrel trước can thiệp, PCI qua đường mạch quay, đồng thời không có dự tính phải sử dụng thuốc kháng GP IIb/IIIa.
- Có thể sử dụng bivalirudin trong các trường hợp sau:
- Bệnh nhân chỉ sử dụng clopidogrel.
- Bệnh nhân có nguy cơ chảy máu cao bao gồm phụ nữ, suy thận, can thiệp qua đường động mạch đùi.
b. Heparin không phân đoạn (UFH) so với heparin trọng lượng phân tử thấp:
- Nghiên cứu ATOLL là nghiên cứu đầu tiên so sánh heparin KPĐ và heparin TLPTT trên bệnh nhân NMCT cấp có ST chênh lên với 910 bệnh nhân được sử dụng ngẫu nhiên heparin KPĐ và heparin TLPTT tiêm tĩnh mạch, lưu ý rằng tất cả bệnh nhân chỉ sử dụng clopidogrel và có tới 80% bệnh nhân được dùng kháng GP IIb/IIIa. Kết quả cho thấy tỷ lệ biến cố MACE trong 30 ngày không có sự khác biệt (28% so với 34%, RR 0,83; CI 95% 0,68 – 1,01), tần suất chảy máu cũng tương tự giữa hai nhóm.
- Kết quả từ hai nghiên cứu cộng gộp (có bao gồm nghiên cứu ATOLL) cho thấy heparin TLPTT làm giảm tỷ lệ tử vong và chảy máu so với heparin KPĐ, tuy nhiên hai nghiên cứu này còn nhiều hạn chế.
- Với các bệnh nhân có chỉ định PCI, khuyến cáo ưu tiên sử dụng heparin KPĐ, tuy nhiên có thể sử dụng heparin TLPTT tiêm tĩnh mạch để thay thế heparin KPĐ ở các bệnh nhân này.
c. Liều dùng
Heparin không phân đoạn:
- Tiêm tĩnh mạch bolus 70 – 100 UI/kg ( tới 10.000 UI) nếu không dùng kèm kháng GP IIb/IIIa ( để đạt được ACT > 250 giây).
- Nếu dùng kèm kháng GP IIb/IIIa : 50 – 70 UI/kg ( tới 7000 UI) để đạt được ACT > 200 giây.
Heparin trọng lượng phân tử thấp:
- Bệnh nhân chuẩn bị được PCI: Tiêm dưới da trong thời gian nằm viện cho đến khi PCI được tiến hành. Liều thường dùng là 1 mg/kg tiêm dưới da mỗi 12h, mỗi 24h ở bệnh nhân có suy thận với MLCT < 30 mL/phút. Tiếp đó khi PCI tùy theo thời gian từ liều enoxaparine cuối cùng:
- > 12h: dùng heparin KPĐ
- < 8h: không cần dùng thêm enoxaparine
- từ 8 đến 12h: tiêm tĩnh mạch thêm 0,3 mg/kg enoxaparine.
- Trong lúc PCI: Nếu bệnh nhân được PCI qua đường động mạch quay, tiêm TM 0,5 mg/kg enoxaparine (nếu thủ thuật kéo dài > 2h, tiêm bổ sung 0,25 mg/kg)
Bivalirudin:
- Bolus 0,75 mg/kg , sau đó duy trì 1,75 mg/kg/h. Bivalirudin vẫn được sử dụng kể cả bệnh nhân đã được dùng heparin KPĐ hoặc heparin TLPTT trước đó.
d. Thời gian sử dụng:
Câu hỏi đến nay còn chưa có câu trả lời chính xác là tiếp tục sử dụng thuốc chống đông sau thủ thuật có giúp cải thiện kết cục lâm sàng hay không?
- Bivalirudin: có ý kiến cho rằng nên dừng sau khi kết thúc thủ thuật, tuy nhiên có ý kiến (từ nghiên cứu EUROMAX, MATRIX, BRIGHT) nên tiếp tục sử dụng liều 1,75 mg/kg/h kéo dài.
- Heparin : dừng ngay sau thủ thuật.
- Trên thực hành nên cân nhắc các yếu tố để quyết định thời gian sử dụng thuốc:
- Tính phức tạp của thủ thuật (can thiệp thân chung, stent dài, chỗ chia đôi).
- Nguy cơ thuyên tắc huyết khối (suy chức năng thất trái nặng, huyết khối buồng tim) hoặc bệnh nhân đã có tiền sử sử dụng thuốc chống đông vì chỉ định khác ( van cơ học, rung nhĩ, tiền sử thuyên tắc huyết khối tĩnh mạch, động mạch phổi).
Bệnh nhân được sử dụng thuốc tiêu sợi huyết
- Tất cả bệnh nhân sử dụng thuốc tiêu sợi huyết đều phải được dùng thuốc chống đông. Heparin KPĐ và heparin TLPTT đều có thể sử dụng được trong trường hợp này. Mặc dù có nhiều nghiên cứu cho thấy hiệu quả và an toàn của heparin TLPTT trên các bệnh nhân này (nghiên cứu ASSENT 3, ASSENT -3 PLUS, ExTRACT – TIMI 25), nhưng trên thực tế các bác sĩ vẫn ưu tiên sử dụng heparin KPĐ trước và sau lúc tiêu sợi huyết do thời gian bán hủy ngắn, chỉnh liều theo ACT nhanh (rất phù hợp nếu bệnh nhân có chiến lược PCI tiếp theo), có thể đảo ngược được bằng protamine sulfate khi cần thiết. Thêm vào đó, theo một nghiên cứu cộng gộp năm 2007 với hơn 27.000 bệnh nhân so sánh heparin TLPTT với heparin KPĐ, tỷ lệ chảy máu cao hơn ở nhóm sử dụng enoxaparine (2,6% so với 1,8%).
- Fondaparinux không được khuyến cáo cho những bệnh nhân được tiêu sợi huyết có kế hoạch PCI tiếp theo. Tuy nhiên, có thể sử dụng nếu bệnh nhân có nguy cơ chảy máu cao hoặc không có kế hoạch PCI sau đó.
- Bivalirudin cũng không được khuyến cáo sử dụng do làm tăng nguy cơ chảy máu so với heparin KPĐ trên các bệnh nhân được tiêu sợi huyết thông qua nghiên cứu HERO – 2. Đây là thử nghiệm với hơn 17.000 bệnh nhân bị NMCT cấp có ST chênh lên được tiêu sợi huyết bằng streptokinase được dùng kèm bivalirudin hoặc heparin KPĐ. Sau 30 ngày, không có sự khác biệt về tỷ lệ tử vong giữa hai nhóm, trong khi đó tỷ lệ chảy máu nhẹ và vừa có xu hướng cao hơn ở nhóm dùng bivalirudin.
a. Liều dùng:
Heparin không phân đoạn:
- Bolus tĩnh mạch: 60 UI/kg ( tới 4000 UI), sau đó duy trì 12 UI/kg/h ( tới 1000 UI) để đạt được APTT từ 50- 70 giây.
- Không phải chỉnh liều theo mức lọc cầu thận, do đó phù hợp để thay thế cho enoxaparin trong các trường hợp suy thận nặng (MLCT < 15 mL/phút), lọc máu chu kỳ.
Heparin trọng lượng phân tử thấp (dùng enoxaparine):
- Tuổi < 75: 30 mg bolus tĩnh mạch, sau đó 1mg/kg tiêm dưới da mỗi 12h.
- Tuổi > 75: không tiêm bolus, tiêm dưới da 0,75 mg/kg mỗi 12h.
- Chỉnh liều theo mức lọc cầu thận (MLCT):
- Nếu MLCT < 30 mL/phút và bệnh nhân < 75 tuổi: 30 mg bolus tĩnh mạch, sau đó 1mg/kg tiêm dưới da mỗi 24h.
- Nếu MLCT < 30 mL/phút và bệnh nhân >75 tuổi: chỉ tiêm dưới da 1 mg/kg mỗi 24h
Fondaparinux
- Với bệnh nhân không có kế hoạch PCI.
- Bolus 2,5 mg tĩnh mạch và duy trì 2,5mg/24h sau đó.
b. Thời gian sử dụng:
Trong trường hợp tiêu sợi huyết đơn thuần, nếu bệnh nhân được PCI thì theo hướng dẫn của phần 3.2
- Heparin không phân đoạn: thêm 2 ngày sau tiêu sợi huyết.
- Heparin TLPTT hoặc fondaparinux: đến 8 ngày sau tiêu sợi huyết hoặc đến khi ra viện.
Điều trị nội khoa đơn thuần
- Có bằng chứng chứng minh hiệu quả của các thuốc chống đông cho bệnh nhân bị NMCT cấp có ST chênh lên không sử dụng các biện pháp tái thông ĐMV. Heparin KPĐ hoặc heparin TLPTT được khuyến cáo sử dụng, trong khi không có khuyến cáo cho fondaparinux hoặc bivalirudin.
- Nghiên cứu CREATE với 3325 sử dụng Reviparin cho thấy hiệu quả làm giảm tỷ lệ tử vong, NMCT, đột quỵ so với giả dược ( 15,0 % sơ với 18,3 %).
- Nghiên cứu TETAMI so sánh heparin KPĐ với enoxaparin, kết cục sau 30 ngày giữa hai nhóm không có sự khác biệt có ý nghĩa.
a. Liều dùng:
Heparin không phân đoạn:
- Bolus tĩnh mạch 50 – 70 UI/kg ( tới 5000 UI),sau đó duy trì 12 UI/kg/h để đạt được APTT từ 50 đến 75 giây.
Heparin trọng lượng phân tử thấp và Fondaparinux: giống với liều dùng trong tiêu sợi huyết.
b. Thời gian sử dụng: giống với bệnh nhân được tiêu sợi huyết
THUỐC KHÁNG KẾT TẬP TIỂU CẦU
(xem thêm chương 8)
Phân loại
Các thuốc kháng kết tập tiểu cầu dùng trong điều trị NMCT cấp có ST chênh lên bao gồm ba nhóm:
- Aspirin: ngăn chặn con đường hoạt hóa tiểu cầu của thromboxane A2 bằng việc acetyl hóa không hồi phục enzyme cyclooxygenase.
- Các thuốc ức chế thụ thể P2Y12: gồm clopidogrel, ticagrelor, prasugrel, cangelor.
- Các thuốc kháng thụ thể GP IIb/IIIa: gồm abciximab, tirofiban, eptifibatide.
Lựa chọn thuốc kháng kết tập tiểu cầu
a. Nguyên tắc:
-
Một khi được chẩn đoán xác định, tất cả các bệnh nhân đều phải được sử dụng aspirin (liều nạp 162 – 325 mg) càng sớm càng tốt,
bệnh nhân được cho uống tại khoa Cấp cứu hoặc ngay trên xe cấp cứu.
- Lựa chọn thuốc ức chế thụ thể P2Y12 dựa trên chiến lược tái thông động mạch vành. Một số bệnh nhân được tiến hành PCI có thể có lợi nếu dùng thêm thuốc kháng thụ thể GP IIb/IIIa.
b. Thuốc kháng kết tập tiểu cầu ở bệnh nhân được tiêu sợi huyết:
- Ngoài aspirin, tất cả các bệnh nhân được tiêu sợi huyết có hay không được PCI sau đó cần được dùng thêm thuốc kháng thụ thể P2Y12. Clopidogrel là thuốc có nhiều bằng chứng nhất khi kết hợp cùng aspirin trên các đối tượng này thông qua các nghiên cứu COMMIT/CCS – 2, CLARITY TIMI – 28. Các nghiên cứu này so sánh cho thấy hiệu quả làm giảm tỷ lệ tử vong khi sử dụng phối hợp thuốc so với aspirin đơn độc, đồng thời nguy cơ chảy máu không tăng thêm ở các bệnh nhân sử dụng hai thuốc kết hợp.
Bảng 17.2: Liều nạp các thuốc ức chế thụ thể P2Y12
| Tái thông ĐMV | Phương pháp | Tuổi | Thuốc phù hợp (liều nạp) |
| Có | PCI | Tất cả | 180 mg ticagrelor hoặc 60 mg prasugrel nếu không có chống chỉ định*. |
| 300 – 600 mg clopidogrel ( nên dùng 600 mg) ở bệnh nhân không phù hợp dùng ticagrelor hoặc prasugrel. | |||
| Tiêu sợi huyết | < 75 | 300 mg clopidogrel | |
| ≥ 75 | 75 mg clopidogrel | ||
| Không | Tất cả | 180 mg ticagrelor |
*Chống chỉ định tuyệt đối với prasugrel: tiền sử bị đột quỵ nhồi máu não hoặc xuất huyết não.
Chống chỉ định tương đối với prasugrel gồm: < 65 kg và > 75 tuổi
- Nghiên cứu TREAT với 3799 bệnh nhân trẻ hơn 75 tuổi nhằm đánh giá tính an toàn của ticagrelor so sánh với clopidogrel. Kết quả sau 30 ngày tỷ lệ chảy máu nặng (đánh giá theo TIMI) không có sự khác biệt giữa hai nhóm ( 0,73 % so với 0,69%), tại thời điểm 12 tháng tỷ lệ chảy máu cũng cho kết quả tương tự. Tỷ lệ các biến cố MACE cũng tương đương (6,7% so với 7,3%, HR 0,93, CI 95% 0,73-1,18). Do vậy, với các bệnh nhân dưới 75 tuổi chúng ta có thể chuyển từ clopidogrel sang ticagrelor sau tiêu sợi huyết 12-24h. Một nghiên cứu cộng gộp ( bao gồm nghiên cứu TREAT và thử nghiệm PLATO) cho thấy sử dụng aspirin và ticagrelor kéo dài cho các bệnh nhân sau tiêu sợi huyết giúp giảm 13% các biến cố tim mạch sau 1 năm (RR 0,87, CI 95% 0,76- 0,99).
- Hiện tại chưa có bằng chứng ủng hộ dùng thuốc kháng thụ thể GP IIb/IIIa ở các bệnh nhân được tiêu sợi huyết.
- Liều dùng:
+ Liều nạp: xem bảng 17.2.
+ Liều duy trì: xem mục 4.2.3
c. Thuốc kháng kết tập tiểu cầu ở bệnh nhân được can thiệp ĐMV qua da thì đầu:
- Bên cạnh aspirin, tất cả các bệnh nhân được PCI thì đầu cần được sử dụng thuốc kháng thụ thể P2Y12. Hiện nay các hướng dẫn của ESC 2017, AHA/ACC 2013 đều khuyến cáo ưu tiên sử dụng ticagrelor hoặc prasugrel hơn clopidogrel (do khả năng ức chế kết tập tiểu cầu cao hơn) trên các bệnh nhân được PCI. Thuốc kháng thụ thể GP IIb/IIIa không nên sử dụng thường quy.
Clopidogrel:
- Hiện tại chưa có nghiên cứu ngẫu nhiên nào được thiết kế để đánh giá hiệu quả ngắn hạn của liệu pháp kết tập tiểu cầu kép so với aspirin đơn thuần trên các bệnh nhân bị NMCT cấp có ST chênh lên. Các bằng chứng về hiệu quả của việc phối hợp clopidogrel và aspirin đến từ các phân tích dưới nhóm từ nghiên cứu CLARITY – TIMI 28.
- Liều dùng:
- Liều nạp: xem bảng 17.2. Liều 600 mg được khuyến cáo ưu tiên sử dụng so với liều 300 mg (từ nghiên cứu CURRENT – OASIS 7 và HORIZONS AMI).
- Liều duy trì: 75 mg/ 1 lần/24h.
Prasugrel:
- Nghiên cứu TRITON – TIMI 38 so sánh hiệu quả của prasugrel với clopidogrel, với 13608 bệnh nhân bị HCMVC được PCI, trong đó có 3534 bệnh nhân bị NMCT cấp có ST chênh lên. Sau thời gian theo dõi trung bình 15 tháng, prasugrel làm giảm tỷ lệ tử vong do tim mạch, NMCT không tử vong, đột quỵ không tử vong so với clopidogrel (10 % so với 12,4%, HR 0,79, CI 95% 0,65- 0,97), thêm vào đó tỷ lệ huyết khối trong stent cũng giảm ở nhóm dùng prasugrel (1,6% so với 2,8%). Tỷ lệ chảy máu nặng không có sự khác biệt giữa hai nhóm (HR 1,11; CI 95%: 0,7 – 1,77).
- Liều dùng:
- Liều nạp: xem bảng 17.2.
- Liều duy trì: 10 mg/1 lần/24h.
Ticagrelor:
- Nghiên cứu PLATO so sánh hiệu quả của ticagrelor với clopidogrel với 18.000 bệnh nhân bị HCMVC, trong đó có 38% bệnh nhân bị NMCT cấp có ST chênh lên được PCI. Với những bệnh nhân này, ticagrelor cho hiệu quả làm giảm tỷ lệ biến cố MACE ( 9,4% so với 10,8%, HR 0,87, 95% CI 0,75 – 1,01). Không có sự khác biệt về tỷ lệ chảy máu nặng không liên quan đến phẫu thuật bắc cầu nối chủ vành (CABG) giữa hai thuốc ( HR 1,09, 95% CI 0,8 -1,48).
- Đến thời điểm này, có hai nghiên cứu so sánh trực tiếp hiệu quả điều trị của ticagrelor và prasugrel. Nghiên cứu PRAGUE – 18 với 1.230 bệnh nhân bị HCMVC được dùng ngẫu nhiêu ticagrelor hoặc prasugrel trước khi chụp ĐMV qua da. Nghiên cứu này đã bị dừng sớm do tính vô nghĩa của nó khi không có sự khác biệt về tỷ lệ biến cố MACE và tỷ lệ chảy máu giữa hai thuốc. Nghiên cứu thứ 2 là thử nghiệm ISAR- REACT 5 với 4018 bệnh nhân bị HCMVC (41% bị NMCT cấp có ST chênh lên), các bệnh nhân cũng được dùng ngẫu nhiên một trong hai thuốc này. Kết quả cho thấy ở nhóm sử dụng ticagrelor có tỷ lệ biến cố MACE cao hơn nhóm còn lại ( 9,3% so với 6,9%, HR 1,36, 95%CI 1,09 – 1,7), tỷ lệ chảy máu nặng (từ mức độ 3 theo thang điểm BARC) không có sự khác biệt giữa hai nhóm. Tuy nhiên, nghiên cứu này có một vài hạn chế như nhãn mở, theo dõi bệnh nhân qua điện thoại. Hiện tại cả hai thuốc đều được ESC và AHA/ACC khuyến cáo sử dụng với mức độ như nhau, tuy nhiên lựa chọn sử dụng ticagrelor hay prasugrel cần dựa trên nguồn lực sẵn có và chống chỉ định kèm theo.
- Liều dùng:
- Liều nạp: xem bảng 17.2.
- Liều duy trì: 90 mg x 2 lần/24h.
Cangrelor:
- Đây là thuốc kháng thụ thể P2Y12 dạng tiêm tĩnh mạch duy nhất.
- Có ba nghiên cứu so sánh hiệu quả của cangrelor với clopidogrel hoặc giả dược. Các bằng chứng từ những nghiên cứu này đã thuyết phục được FDA và các hội tim mạch ESC, AHA/ACC đưa vào khuyến cáo. Hiện nay, chỉ định dùng thuốc khi bệnh nhân được PCI nhưng chưa được nạp hiệu quả các thuốc ức chế P2Y12 khác hoặc khi không dùng thuốc ức chế thụ thể GP IIb/IIIa.
- Liều dùng:
- Liều nạp: 30 µg/kg tiêm bolus trong 1 phút trước khi PCI.
- Liều duy trì: 4 µg/kg/phút truyền ít nhất 2h hoặc trong khi làm can thiệp.
Các thuốc ức chế thụ thể GP IIb/IIIa:
- Khuyến cáo không sử dụng thường quy, hiện nay, chỉ định các thuốc này đã thu hẹp lại. Nên xem xét sử dụng thuốc ức chế GP IIb/IIIa như biện pháp cứu trợ trong các trường hợp không có dòng chảy ĐMV hoặc biến chứng do huyết khối, gánh nặng huyết khối lớn. Cũng có thể cân nhắc dùng thuốc này nếu thời gian dùng thuốc ức chế thụ thể P2Y12 trước PCI quá ngắn ( < 45 phút).
- Các loại thuốc và liều: có hai loại loại hiện nay đang được dùng phổ biến:
- Eptifibatide (Integrilin): liều dùng tấn công 180 μg/kg tiêm tĩnh mạch sau đó truyền tĩnh mạch 1,3 – 2,0 μg/kg/phút trong 12h tiếp theo.
- Tirofiban (Aggrastat): liều dùng tấn công 25 µg/kg/phút truyền TM trong 3 phút, sau đó truyền TM 0,15 µg/kg/phút tối đa đến 18h.
d. Thuốc kháng kết tập tiểu cầu ở bệnh nhân chỉ điều trị nội khoa đơn thuần
- Khuyến cáo tất cả bệnh nhân được sử dụng thuốc ức chế thụ thể P2Y12 phối hợp aspirin. Từ nghiên cứu COMMIT/CCS–2 so sánh clopidogrel với giả dược, đến nghiên cứu PLATO cho các bằng chứng ủng hộ sử dụng phối hợp clopidogrel, ticagrelor với aspirin trên bệnh nhân bị NMCT cấp có ST chênh lên. Ticagrelor nên được ưu tiên sử dụng, trong khi đó prasugrel không chứng minh được sự vượt trội so với clopidogrel.
- Không sử dụng thuốc kháng thụ thể GP IIb/IIIa trên các đối tượng này. Nghiên cứu TETAMI sử dụng tirofiban so sánh với giả dược không cho thấy được hiệu quả của thuốc trên những bệnh nhân này.
e. Thuốc kháng kết tập tiểu cầu ở bệnh nhân được phẫu thuật bắc cầu nối chủ vành (CABG)
- Một số bệnh nhân bị NMCT cấp có ST chênh lên có giải phẫu ĐMV không phù hợp để PCI, CABG cần được thực hiện sớm. Những bệnh nhân này nếu sử dụng liệu pháp kháng kết tập tiểu cầu kép làm tăng nguy cơ chảy máu khi phẫu thuật. Nguy cơ chảy máu khi sử dụng thuốc ức chế thụ thể P2Y12 được đánh giá qua hai thử nghiệm.
- Thử nghiệm CURE cho thấy việc sử dụng clopidogrel trong vòng 7 ngày trước phẫu thuật làm tăng không có ý nghĩa thống kê nguy cơ chảy máu nặng, nguy hiểm đến tính mạng. Tuy nhiên, ở những bệnh nhân dừng clopidogrel trước cuộc mổ 5 ngày, nguy cơ chảy máu là tương đương với giả dược ( 4,4 % so với 5,3%).
- Ở nghiên cứu TRITON – TIMI 38 nguy cơ chảy máu liên quan đến CABG tăng lên ở các bệnh nhân sử dụng prasugrel so với clopidogrel (13,4% so với 3,2%). Ở nghiên cứu PLATO, nguy cơ này là tương đương ở các bệnh nhân sử dụng ticagrelor so với clopidogrel (7,4% so với 7,9%).
- Do đó với những bệnh nhân chờ đợi để CABG, nên dừng thuốc ức chế P2Y12 trước 5 ngày để giảm nguy cơ chảy máu.
f. Một số chú ý đặc biệt khi sử dụng thuốc kháng kết tập tiểu cầu (KTTC)
Thời gian dùng thuốc:
- Như đã nêu ở trên, các thuốc kháng KTTC cần được dùng sớm nhất có thể. Hầu hết bệnh nhân dùng clopidogrel sẽ đạt được hoạt độ ức chế tiểu cầu hiệu quả sau 8h. Trong khi ticagrelor và prasugrel sẽ đạt được hoạt độ ức chế tiểu cầu hiệu quả sau khi uống liều nạp 2h.
Cách uống thuốc:
- Việc uống nguyên viên thuốc có vẻ làm chậm việc đạt được hoạt tính ức chế tiểu cầu cần thiết, thậm chí ảnh hưởng đến kết cục lâm sàng so với việc nghiền thuốc, mặc dù chưa có nghiên cứu nào chứng minh điều này. Do đó, trong một vài trường hợp như cần PCI cấp hoặc bệnh nhân không nuốt được (bệnh nhân hôn mê, thở máy) có thể nghiền thuốc trước khi cho bệnh nhân uống.
Thời gian duy trì:
- Thời gian duy trì kháng kết tập tiểu cầu kép (DAPT) và kháng kết tập tiểu cầu đơn tiếp theo, theo chiến lược dựa trên đánh giá nguy cơ chảy máu và đông máu của người bệnh:
- Với bệnh nhân có tiền sử chảy máu (tiêu hóa, đột quỵ xuất huyết não…) hoặc trong thời gian dùng DAPT có chảy máu; kèm theo thiếu máu, người già yếu, gầy gò hoặc đánh giá thang điểm PRECISE-DAPT ≥ 25 (tham khảo trang www.precisedaptscore.com)… thì nên rút ngắn thời gian dùng kháng kết tập tiểu cầu kép (DAPT) trong 6 tháng thậm chí 3 tháng sau đó chỉ dùng một loại kháng kết tập tiểu cầu đơn (aspirin).
- Với bệnh nhân nguy cơ chảy máu thấp (không có các yếu tố trên) và nguy cơ tắc mạch cao nhất là bệnh nhân có tổn thương ĐMV phức tạp, được đặt stent thân chung ĐMV trái, đặt nhiều stent hoặc có tiền sử huyết khối trong stent… thì nên dùng DAPT kéo dài, có thể trên 12 tháng và lâu hơn nữa nếu có thể.
- Có thể cân nhắc chiến lược chuyển đổi: “lên thang” hoặc “xuống thang”.
Chuyển đổi giữa các thuốc ức chế thụ thể P2Y12:
- Có khoảng 10% bệnh nhân bị NMCT cấp có ST chênh lên được PCI và dùng ticagrelor hoặc prasugrel chuyển sang dùng clopidogrel trước khi ra viện. Sau ra viện lại có khoảng 10% bệnh nhân lại thực hiện sự chuyển đổi tiếp. Lý do chung chủ yếu là do sự xuất hiện các biến cố chảy máu và giá thuốc.
- Ticagrelor gắn có hồi phục với thụ thể P2Y12 tại vị trí khác với vị trí gắn của prasugrel và clopidogrel – 2 thuốc này gắn không hồi phục với thienopyridine ở trung tâm. Vì vậy khi chuyển từ ticagrelor sang clopidogrel, vị trí trung tâm thienopyridine còn trống nên phải sử dụng liều nạp clopidogrel. Trong khi đó nếu chuyển từ prasugrel sang clopidogrel không cần phải nạp lại do vị trí trung tâm thienopyridine đã bị ức chế.
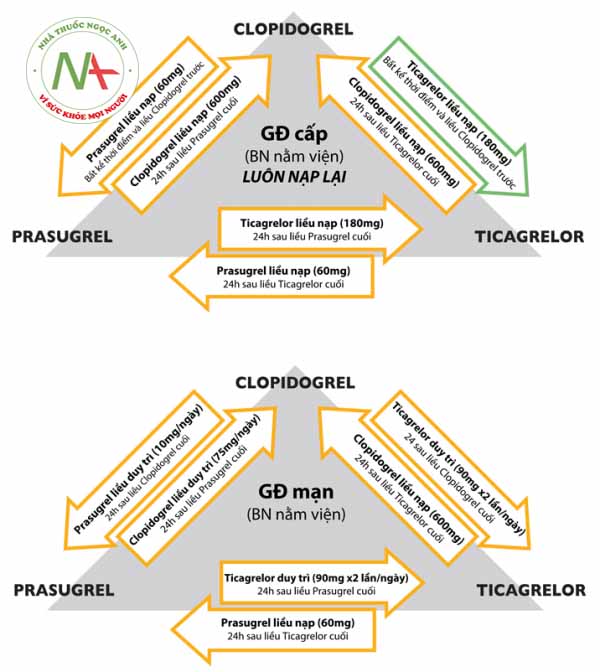
GĐ: Giai đoạn, BN: Bệnh nhân
- Nghiên cứu CAPITAL OPTI – CROSS đánh giá dược động học của việc chuyển đổi từ ticagrelor sang clopidogrel trên 60 bệnh nhân bị HCMVC, các bệnh nhân sau chuyển đổi hoặc dùng 600 mg clopidogrel liều nạp, duy trì 75 mg/24h hoặc chỉ dùng 75 mg/24h. Kết quả ở nhóm có dùng liều nạp sau chuyển đổi, hoạt tính ức chế tiểu cầu cao hơn nhóm chỉ dùng duy trì clopidogrel từ đầu. Tuy nhiên những lợi ích của việc giảm thiểu biến cố tim mạch liên quan đến thiếu máu cơ tim của ticagrelor và prasugrel, các khuyến cáo chỉ nên chuyển sang dùng clopidogrel chỉ khi có lo ngại về nguy cơ xuất huyết.
- Trong trường hợp bệnh nhân HCMVC đã dùng clopidogrel trước đó có thể được chuyển sang ticagrelor ngay sau khi nhập viện với liều nạp 180 mg bất kể thời điểm và liều nạp clopidogrel, trừ khi có chống chỉ định với ticagrelor (Khuyến cáo IB).
- Chuyển đổi cụ thể các thuốc ức chế P2Y12 trong giai đoạn nằm viện ( giai đoạn cấp) và sau ra viện (giai đoạn mạn): xem hình 17.3.
Thay đổi chế độ dùng thuốc kháng kết tập tiểu cầu khi có xuất huyết:
- Tỷ lệ xuất huyết khi sử dụng thuốc kháng kết tập tiểu cầu khoảng 5%/năm, chảy máu có thể chỉ ở mức độ nhẹ như bầm tím ngoài da, chảy máu chân răng hoặc nguy hiểm đến tính mạng như xuất huyết não.
- Tác dụng của DAPT trên giảm thiểu các biến cố do thiếu máu cơ tim là không thể bàn cãi, tuy nhiên một khi xảy ra xuất huyết chúng ta cần có các tiếp cận phù hợp để cân bằng giữa lợi ích và nguy cơ thiếu máu. Hình dưới đây trình bày tóm tắt về chiến lược điều trị cho các bệnh nhân bị xuất huyết khi đang sử dụng DAPT.
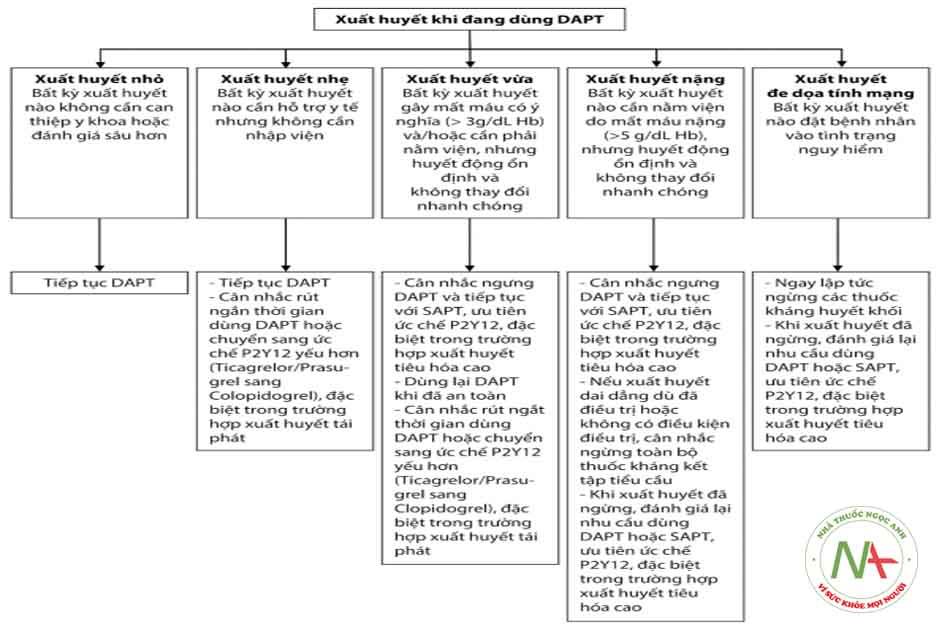
DAPT: Liệu pháp kháng kết tập tiểu cầu kép; SAPT: Liệu pháp kháng kết tập tiểu cầu đơn
Bệnh nhân có chỉ định sử dụng thuốc chống đông đường uống:
-
- Nếu bệnh nhân bị NMCT cấp có ST chênh lên có các chỉ định phải dùng thuốc chống đông đường uống (OAC) như: rung nhĩ, huyết khối buồng tim, van tim cơ học hoặc thuyên tắc huyết khối tĩnh mạch, việc sử dụng OAC cũng cần thiết như việc sử dụng aspirin hoặc thuốc ức chế thụ thể P2Y12. Tuy nhiên, sử dụng ba thuốc phối hợp sẽ làm nguy cơ chảy máu tăng lên rõ rệt khi so sánh với chỉ sử dụng OAC hoặc thuốc kháng kết tập tiểu cầu đơn thuần.
- Xử trí khi bệnh nhân nhập viện:
-
- Sử dụng OAC là chống chỉ định khi lựa chọn bệnh nhân tiêu sợi huyết, vì vậy tất cả bệnh nhân nên được xem xét PCI.
- Sử dụng các thuốc chống đông đường tiêm bất kể thời gian từ liều OAC cuối cùng. Không nên dừng hẳn các OAC đang uống trước đó.
- Lựa chọn thuốc ức chế thụ thể P2Y12: Clopidogrel là lựa chọn tối ưu, liều nạp 600 mg. Ticagrelor và prasugrel không được khuyến cáo do tăng nguy cơ chảy máu.
- Bảo vệ dạ dày bằng thuốc ức chế bơm proton.
- Xử trí sau thời điểm ban đầu:
-
- Việc dùng OAC ở bệnh nhân đang sử dụng DAPT nên được đánh giá cẩn thận và chỉ nên tiếp tục nếu có bằng chứng thuyết phục. Cần cân bằng giữa lợi ích phòng ngừa các biến cố tim mạch và hạn chế nguy cơ chảy máu.
- Với phần lớn bệnh nhân, liệu pháp ba thuốc (OAC, aspirin và clopidogrel) nên được dùng trong 6 tháng đầu. Sau đó, OAC phối hợp với aspirin hoặc clopidogrel nên được tiếp tục trong 6 tháng nữa. Sau 1 năm, chỉ cần duy trì OAC đơn độc. Trong trường hợp có nguy cơ chảy máu rất cao, liệu pháp ba thuốc có thể giảm thời gian xuống còn 1 tháng sau NMCT, liệu pháp kép (OAC cộng với aspirin hoặc clopidogrel) tối đa 1 năm và sau đó chỉ OAC đơn độc.
CÁC THUỐC CÓ TÁC DỤNG CẢI THIỆN TIÊN LƯỢNG LÂU DÀI CỦA BỆNH NHÂN
Thuốc chẹn beta giao cảm
(xem thêm chương 1)
- Sử dụng chẹn beta giao cảm sớm giúp giới hạn diện tích vùng nhồi máu, giảm tỷ lệ tử vong và rối loạn nhịp nguy hiểm sớm. Những bệnh nhân được hưởng lợi nhiều nhất gồm:
-
- Có nhịp nhanh xoang và tăng huyết áp.
- Tiếp tục hoặc tái diễn đau ngực/tái nhồi máu cơ tim.
- Rối loạn nhịp nhanh, ví dụ rung nhĩ.
- Bắt đầu sớm trong vòng 24 giờ ngay khi nhập viện ở những bệnh nhân được can thiệp tái tưới máu nếu không có chống chỉ định bằng các thuốc chẹn beta đường tĩnh mạch (metoprolol 1 – 2 mg/lần, nhắc lại mỗi 1 – 2 phút, liều tối đa 15 – 20 mg) theo dõi điện tâm đồ và huyết áp liên tục.
- Không chỉ định ở những bệnh nhân tụt huyết áp, suy tim cấp, block nhĩ thất hay nhịp chậm rõ rệt.
- Mục tiêu:
-
- Nhịp tim 55 – 60 nhịp/phút
- Huyết áp tâm thu 100 – 110 mmHg.
- Nếu huyết động ổn định tiếp tục sau liều tĩnh mạch cuối cùng 15 – 30 phút, bắt đầu metoprolol 25 mg, 1 – 2 lần/24h. Esmolol là thuốc có tác dụng rất ngắn, có thể được sử dụng nếu nghi ngờ bệnh nhân không dung nạp được chẹn beta giao cảm.
- Thuốc chẹn beta giao cảm nên được duy trì đường uống sớm ngay trong giai đoạn nằm viện và kéo dài liên tục cho tất cả các bệnh nhân nếu không có chống chỉ định.
- Các thuốc có thể cân nhắc: bisoprolol, metoprolol, carvedilol. Lưu ý hiện tại nebivolol chưa được phê duyệt cho chỉ định nhồi máu cơ tim, trừ trường hợp kèm theo suy tim.
Bảng 17.3: Các thuốc chẹn beta giao cảm trong nhồi máu cơ tim
| Liều dùng | Cách dùng | |
| Bisoprolol | 1,25 – 10 mg | 1 lần/24h |
| Metoprolol | 12,5 – 200 mg | 1 lần/24h |
| Carvedilol | 3,125 – 25 mg | 2 lần/24h |
Thuốc ức chế men chuyển/ức chế thụ thể (xem thêm chương 2)
- Tất cả bệnh nhân nhồi máu cơ tim cấp có ST chênh lên nên được sử dụng thuốc ƯCMC trong vòng 24h.
- Người được hưởng lợi nhiều nhất bao gồm:
-
- Nhồi máu cơ tim cấp nguy cơ cao hoặc nhồi máu cơ tim diện rộng, đặc biệt là nhồi máu thành trước.
- Tiền sử đã nhồi máu cơ tim.
- Người lớn tuổi, suy tim, suy thất trái trên siêu âm tim.
- Bệnh nhân không dung nạp thuốc ƯCMC nên được dùng thuốc ƯCTT. Valsartan đã được chứng minh là không thua kém captopril trong thử nghiệm VALIANT.
- Liều dùng: xem chương 2
Các thuốc hạ lipid máu (xem thêm chương 6 và chương 16)
- Lợi ích của statin trong phòng ngừa thứ phát đã được chứng minh một cách rõ ràng và các thử nghiệm đã cho thấy lợi ích của việc điều trị statin sớm và tích cực trong HCMVC. Một phân tích tổng hợp các thử nghiệm làm giảm LDL –C nhiều bằng liệu pháp statin tích cực hơn đã làm giảm thiểu có ý nghĩa nguy cơ tử vong do tim mạch, NMCT không gây tử vong, đột quỵ do thiếu máu cục bộ.
- Do đó, statin được khuyến cáo sử dụng ở tất cả các bệnh nhân bị NMCT, không phân biệt nồng độ cholesterol ban đầu. Điều trị hạ lipid máu nên được bắt đầu càng sớm càng tốt, vì điều này làm tăng sự tuân thủ điều trị của bệnh nhân sau khi xuất viện đồng thời điều trị với cường độ cao từ đầu vì điều này có liên quan đến lợi ích lâm sàng sớm và bền vững. Các bệnh nhân đang điều trị statin với cường độ nhẹ – vừa cũng nên được trị liệu statin mạnh mẽ hơn trừ khi có tiền sử không dung nạp với điều trị statin cường độ cao hoặc có các bệnh lý ảnh hưởng đến sự an toàn khi dùng statin.
- Mục tiêu: nồng độ LDL-C <1,8 mmol/L (<70 mg/dL) hoặc giảm ít nhất 50% LDL-C nếu mức LDL-C ban đầu là 1,8 – 3,5 mmol/L. Tuy nhiên, cũng nên cân nhắc sử dụng liệu pháp statin cường độ thấp ở bệnh nhân có nguy cơ xảy ra tác dụng phụ của statin (người già, suy gan hoặc thận, tác dụng phụ trước đó).
- Sau NMCT, nồng độ lipid máu có sự biến đổi, với sự giảm nhẹ nồng độ cholesterol toàn phần, LDL-C và HDL-C và tăng triglyceride trong vòng 24h. Vì vậy, xét nghiệm lipid máu nên được thực hiện càng sớm càng tốt (có thể không cần nhịn ăn) sau khi nhập viện đối với NMCT cấp có ST chênh lên. Xét nghiệm lipid máu nên được kiểm tra lại 4 – 6 tuần sau NMCT để đánh giá đã đạt được mục tiêu hay chưa , đánh giá vấn đề an toàn, để điều chỉnh liệu trình điều trị sau đó.
- Nếu bệnh nhân không dung nạp với statin ở bất kỳ liều điều trị nào nên chuyển sang dùng ezetimibe.
- Dữ liệu từ các thử nghiệm pha I – III gần đây, cho thấy chất ức chế proprotein convertase subtilisin/kexin type 9 (PCSK9) làm giảm LDL-C tới 60%, dưới dạng đơn trị liệu hoặc phối hợp với statin và cũng như có tác dụng đối với triglyceride và HDL -C. Phân tích tổng hợp các thử nghiệm hiện tại với hơn 10.000 bệnh nhân cho thuốc làm giảm đáng kể (HR 0,45, CI 95% 0,23 – 0,86) tỷ lệ tử vong. Trong nghiên cứu FOURIER trên 27.564 bệnh nhân có bệnh lý tim mạch liên quan đến xơ vữa có LDL ≥70 mg/dL (1,8 mmol/L), các bệnh nhân dù đã được điều trị bằng statin cường độ trung bình hoặc tiếp tục được tiêm evolocumab rồi so sánh với giả dược, kết quả tỷ lệ tử vong do tim mạch, NMCT, đột quỵ, nhập viện vì đau thắt ngực không ổn định hoặc tái thông mạch vành giảm 15% tỷ lệ tương đối và 1,5% theo tỷ lệ tuyệt đối. Không có sự khác biệt về tỷ lệ tử vong do mọi nguyên nhân hoặc tử vong do tim mạch và không có sự khác biệt đáng kể về các tác dụng phụ. Do tác dụng vừa phải trong 2 năm và không làm giảm tỷ lệ tử vong chung, nên thuốc này chỉ được chỉ định chọn lọc cho những bệnh nhân có nguy cơ cao.
- Cũng nên cân nhắc dùng thêm các thuốc hạ lipid khác ngoài statin cho các bệnh nhân nguy cơ cao chưa đạt được mục tiêu điều trị sau NMCT mặc dù đã sử dụng liều statin tối đa dung nạp được.
- Liều dùng các thuốc: xem chương 6
Thuốc chẹn kênh canxi
- Một phân tích tổng hợp 17 thử nghiệm liên quan đến sử dụng thuốc chẹn kênh canxi sớm trong NMCT cấp có ST chênh lên cho thấy thuốc có tác dụng không có lợi do làm tăng tỷ lệ tử vong hoặc tái NMCT, đặc biệt với nifedipine. Do đó, việc sử dụng chẹn kênh canxi ở giai đoạn cấp không được chỉ định thường quy. Chống chỉ định trong trường hợp có suy giảm chức năng thất trái nặng.
- Amlodipine an toàn đối với các bệnh nhân sau nhồi máu cơ tim có suy giảm chức năng thất trái. Tuy nhiên việc sử dụng dihydropyridine thường không cho thấy lợi ích sau NMCT cấp có ST chênh lên và do đó chúng chỉ nên được kê đơn khi có chỉ định rõ ràng như có tăng huyết áp hoặc còn đau thắt ngực sau NMCT.
- Ở giai đoạn mạn tính, một thử nghiệm lâm sàng ngẫu nhiên trên 1.775 bệnh nhân bị NMCT điều trị bằng verapamil (không dùng chẹn beta giao cảm) hoặc giả dược cho thấy thuốc làm giảm tỷ lệ tử vong và tái NMCT.
- Vì vậy, ở những bệnh nhân có chống chỉ định với thuốc chẹn beta, đặc biệt khi có hen phế quản hoặc bệnh phổi tắc nghẽn mạn tính giai đoạn nặng, thuốc chẹn kênh canxi là lựa chọn hợp lý cho bệnh nhân có chức năng thất trái bình thường.
Thuốc kháng thụ thể aldosterone
- Thuốc được khuyến cáo ở những bệnh nhân bị rối loạn chức năng thất trái (EF ≤40%) và suy tim sau NMCT. Eplerenone, một thuốc đối kháng thụ thể aldosterone chọn lọc, đã được chứng minh là làm giảm tỷ lệ mắc bệnh và tử vong ở những bệnh nhân này qua nghiên cứu EPHESUS.
- Hiện đã có hai nghiên cứu cho các kết quả khả quan về vai trò của thuốc kháng thụ thể aldosterone trên các bệnh nhân bị NMCT nhưng có chức năng thất trái bình thường (nghiên cứu REMINDER và ALBASTROSS). Tuy nhiên, cần có thêm các nghiên cứu trong tương lai để khẳng định tác dụng của thuốc trên các đối tượng này.
- Thận trọng khi sử dụng thuốc ở các bệnh nhân có suy giảm chức năng thận ( creatinine > 221 mmol/L (2,5 mg/dL) ở nam giới và > 177 mmol/L (2,0 mg/dL) ở nữ giới), đồng thời cần theo dõi định kỳ nồng độ kali máu.
- Liều dùng: xem chương 4 – phần thuốc lợi tiểu giữ kali.
ĐIỀU TRỊ CÁC RỐI LOẠN NHỊP TRONG NMCT
- Rối loạn nhịp tim và rối loạn dẫn truyền rất phổ biến trong những giờ đầu của NMCT và là yếu tố quan trọng ảnh hưởng đến tiên lượng bệnh nhân. Tác dụng của các thuốc chống loạn nhịp ở bệnh nhân NMCT còn khá hạn chế và có thể ảnh hưởng tiêu cực đến tỷ lệ tử vong sớm đã được chứng minh trong vài nghiên cứu. Vì vậy cần sử dụng thận trọng các thuốc chống loạn nhịp đồng thời nên áp dụng chiến lược ‘chờ và xem’ đối với các rối loạn nhịp không hoặc chỉ ảnh hưởng huyết động ở mức độ nhẹ – vừa.
- Điều chỉnh thăng bằng điện giải và sử dụng sớm các thuốc chẹn beta giao cảm, thuốc ƯCMC/ƯCTT và statin cũng giúp giảm thiểu nguy cơ xảy ra các rối loạn nhịp.
Các rối loạn nhịp trên thất
- Rung nhĩ thường gặp nhất với tần suất khoảng 21% ở các bệnh nhân bị NMCT cấp có ST chênh lên. Sự xuất hiện của rung nhĩ làm tăng nguy cơ xảy ra biến chứng, tắc mạch, tăng diện nhồi máu, làm nặng suy tim và nguy cơ tái NMCT.
- Một số khuyến cáo của ESC 2017 liên quan đến thuốc điều trị rung nhĩ trong NMCT:
-
- Sử dụng beta giao cảm đường tĩnh mạch để kiểm soát tần số tim, ngoại trừ các trường hợp tụt huyết áp, shock tim, suy tim cấp (I – C). Tuy nhiên, chẹn beta (bao gồm cả sotalol) và chẹn kênh canxi không được sử dụng để chuyển nhịp trong trường hợp rung nhĩ mới khởi phát (III – B).
- Amiodarone đường tĩnh mạch có thể sử dụng để kiểm soát tần số tim nếu có suy tim cấp không có tụt huyết áp (I – C). Thuốc cũng được sử dụng trước sốc điện để tạo thuận/dự phòng tái phát rung nhĩ sau shock (I – C).
- Digoxin đường tĩnh mạch để kiểm soát tần số tim nếu có suy tim cấp có tụt huyết áp (IIa-B). Tuy nhiên thuốc không được sử dụng để chuyển nhịp xoang trong trường hợp rung nhĩ mới khởi phát (III – A).
- Nếu rung nhĩ mới xuất hiện, việc sử dụng DOAC lâu dài cần được đánh giá dựa trên điểm CHA2DS2 – VASc (IIa-C).
Các rối loạn nhịp thất
- Khoảng 6-8% bệnh nhân bị NMCT cấp có ST chênh lên xuất hiện rối loạn nhịp thất (nhịp nhanh thất và rung thất). Các rối loạn này có thể xảy ra ở bất kỳ thời điểm nào, ngay cả khi bệnh nhân đang được tái thông ĐMV và ảnh hưởng đến tiên lượng sớm (30 ngày đầu) của các bệnh nhân nhưng ít tác động đến nguy cơ rối loạn nhịp về sau.
- Một số khuyến cáo của ESC 2017 liên quan đến thuốc điều trị rối loạn nhịp thất trong NMCT:
-
- Chẹn beta giao cảm đường tĩnh mạch nên được sử dụng cho các bệnh nhân bị nhịp nhanh thất đa dạng/ rung thất trừ khi có chống chỉ định (I – B).
- Amiodarone đường tĩnh mạch được khuyến cáo cho các trường hợp nhịp nhanh thất đa dạng tái phát (I – C). Thuốc cũng được dùng trong trường hợp nhịp nhanh thất tái phát có huyết động ổn định dù đã shock điện nhiều lần (IIa – C).
- Thuốc chống rối loạn nhịp không nên sử dụng nếu rối loạn nhịp thất không triệu chứng hoặc không ảnh hưởng đến huyết động (III – C) và để dự phòng rối loạn nhịp (III – B).
Nhịp chậm xoang và rối loạn đường dẫn truyền các mức độ
- Không cần xử lý nếu chỉ nhịp chậm xoang đơn thuần không triệu chứng. Nếu có tụt huyết áp có thể dùng atropin tiêm tĩnh mạch.
- Block nhĩ thất cấp 1 và cấp 2 Mobitz I có thể điều trị bằng atropin tiêm tĩnh mạch. Hạn chế sử dụng các thuốc ảnh hưởng đến dẫn truyền như chẹn beta giao cảm, amiodarone, verapamil, diltiazem.
- Block nhĩ thất độ cao (từ Mobitz II trở lên) : sử dụng các thuốc như epinephrine, vasopressin, cân nhắc atropin, đồng thời cần tiến hành đặt tạo nhịp tạm thời và tái thông ĐMV càng sớm càng tốt.
PHẦN III. HỘI CHỨNG ĐỘNG MẠCH VÀNH CẤP KHÔNG CÓ ST CHÊNH LÊN
Việc điều trị hội chứng động mạch vành cấp không có ST chênh lên (bao gồm nhồi máu cơ tim cấp không có ST chênh lên và đau thắt ngực không ổn định) có sự khác biệt cơ bản so với nhồi máu cơ tim cấp có ST chênh lên ở cách tiếp cận, phân tầng nguy cơ, yếu tố thời gian và đặc biệt là không sử dụng thuốc tiêu sợi huyết để tái thông động mạch vành. Trong khuôn khổ cuốn sách này chúng tôi chỉ trình bày về phần điều trị nội khoa bằng thuốc đơn thuần, các vấn đề về chẩn đoán, phân tầng nguy cơ, tái thông mạch vành độc giả có thể tham khảo ở cuốn “Lâm sàng tim mạch học”.
Xử trí ban đầu ngay khi chẩn đoán được bệnh cần được nhanh chóng tiến hành để đạt được các mục tiêu điều trị sau:
- Giảm đau do thiếu máu cục bộ.
- Đánh giá huyết động của bệnh nhân và điều chỉnh các bất thường. Cần chú ý đến tình trạng tăng huyết áp và nhịp tim nhanh nếu có vì có thể gây tăng nhu cầu oxy cơ tim.
- Sử dụng sớm các thuốc chống huyết khối (bao gồm thuốc chống kết tập tiểu cầu và thuốc chống đông) để ngăn ngừa huyết khối tiến triển hoặc hình thành mới từ các mảng xơ vữa nứt vỡ không ổn định.
Theo sau đó, cần sử dụng các thuốc có ảnh hưởng đến tiên lượng lâu dài của bệnh nhân như:
- Thuốc kháng KTTC lâu dài để dự phòng huyết khối ĐMV trong tương lai và tắc stent với bệnh nhân được can thiệp ĐMV qua da.
- Thuốc điều trị rối loạn lipid máu.
- Thuốc ƯCMC/ƯCTT ở những bệnh nhân có nguy cơ cao.
- Thuốc chống đông đường uống (AVK hoặc DOAC) trên các bệnh nhân có chỉ định.
GIẢM ĐAU DO THIẾU MÁU CƠ TIM
Nitrate và morphin
(xem mục 1 phần II)
Thuốc chẹn beta giao cảm:
- Thuốc làm giảm nhu cầu oxy của cơ tim thông qua nhiều cơ chế (xem thêm chương 1) do đó làm giảm triệu chứng cơn đau thắt ngực.
- Nhiều nghiên cứu đã được tiến hành nhằm đánh giá hiệu quả của thuốc chẹn beta giao cảm trên các bệnh nhân bị NMCT cấp. Tuy nhiên, cho đến nay chưa có nghiên cứu ngẫu nhiên riêng biệt nào về tác dụng của thuốc trên các bệnh nhân bị HCMVC không có ST chênh lên.
- Đặc biệt lưu ý không dùng thuốc chẹn beta giao cảm cho các bệnh nhân đau ngực nghi ngờ do co thắt ĐMV (do nguy cơ làm tăng co thắt do ức chế hệ beta giao cảm ở mạch vành có tác dụng giãn mạch – đối kháng với alpha giao cảm vốn đóng vai trò chính trong co thắt ĐMV).
- Chỉ định và liều dùng thuốc: xem mục 5.1 phần II
Các thuốc khác
- Verapamil và diltiazem có tác dụng giảm cơn đau thắt ngực tương đương với thuốc chẹn beta giao cảm. Nghiên cứu so sánh verapamil và giả dược cho thấy verapamil làm giảm tỷ lệ tử vong, tái nhồi máu cơ tim trên các bệnh nhân bị NMCT cấp có chức năng thất trái bảo tồn.
- Nghiên cứu MERLIN trên 3279 bệnh nhân bị HCMVC không ST chênh lên sử dụng ranolazine cho thấy thuốc làm giảm các cơn đau thắt ngực tái phát nhưng không cải thiện được các biến cố tim mạch chính – MACE.
- Chỉ định sử dụng thuốc chẹn kênh canxi non–dihydropiridine và ranolazine cho các bệnh nhân còn đau ngực sau PCI và không đáp ứng với thuốc chẹn beta giao cảm.
THUỐC CHỐNG ĐÔNG
(Xem thêm mục 3 Phần II)
- Thuốc chống đông phải được sử dụng càng sớm càng tốt ở bệnh nhân bị HCMVC không có ST chênh lên. Tuy nhiên, việc lựa chọn thuốc phù hợp cần dựa vào chiến lược phân tầng nguy cơ và tái tưới máu cho bệnh nhân, cụ thể gồm:
-
- Bệnh nhân được tái thông ĐMV bằng PCI.
- Bệnh nhân chỉ điều trị nội khoa đơn thuần.
Phân loại
(xem mục 3.1 phần II)
Thuốc chống đông ở bệnh nhân điều trị nội khoa đơn thuần
- Đối với những bệnh nhân này, fondaparinux hoặc heparin trọng lượng phân tử thấp (Heparin TLPTT) được ưu tiên sử dụng hơn bivalirudin hoặc heparin không phân đoạn (Heparin KPĐ).
- Trong khi bivalirudin chưa có đủ bằng chứng về hiệu quả và an toàn trên đối tượng này thì heparin KPĐ đường tĩnh mạch cần phải theo dõi và chỉnh liều sát sao hơn heparin TLPTT tiêm dưới da. Thêm vào đó, heparin TLPTT đã chứng minh được hiệu quả so với heparin KPĐ thông qua các nghiên cứu trên các bệnh nhân bị HCMVC điều trị bảo tồn:
-
- Nghiên cứu ESSENCE với 3171 bệnh nhân bị HCMVC được điều trị bảo tồn, các bệnh nhân được sử dụng ngẫu nhiên heparin TLPTT hoặc heparin KPĐ trong 8 ngày. Sau 30 ngày, nhóm dùng heparin TLPTT có tỷ lệ biến cố MACE ít hơn ý nghĩa so với nhóm dùng heparin KPĐ (19,8% so với 23,3%), trong khi tỷ lệ chảy máu tương đương giữa hai nhóm. Kết quả này vẫn được duy trì sau 1 năm theo dõi.
- Kết quả tương tự cũng được thể hiện trong nghiên cứu TIMI 11B với 3.190 bệnh nhân bị HCMVC được điều trị bảo tồn.
- Lựa chọn giữa fondaparinux và heparin TLPTT phụ thuộc vào nguồn lực sẵn có và chi phí. Đối với những bệnh nhân có nguy cơ chảy máu cao, từ nghiên cứu OASIS -5, một số tác giả khuyến cáo sử dụng fondaparinux thay vì heparin TLPTT.
a. Liều dùng
- Enoxaparin: không cần liều nạp, tiêm dưới da liều 1 mg/kg mỗi 12h và 1 mg/kg/24h nếu MLCT < 30 mL/phút
- Fondaparinux: tiêm dưới da 2,5 mg/ 24h.
b. Thời gian sử dụng
- Với các bệnh nhân đang điều trị bằng thuốc kháng KTTC kép, thuốc chống đông nên sử dụng tối thiểu 48h.
Bệnh nhân được tái thông động mạch vành
- Với các bệnh nhân có kế hoạch tái thông ĐMV sớm trong vòng 48h, heparin KPĐ được ưu tiên sử dụng so với bivalirudin, Heparin TLPTT hoặc fondaparinux. Mặc dù hiệu quả của heparin KPĐ và bivalirudin trên các bệnh nhân này tương đương nhưng heparin KPĐ có lợi thế hơn về giá cả. Trong khi đó, nếu bệnh nhân đang được sử dụng fondaparinux có kế hoạch tái thông ĐMV, bắt buộc phải chuyển sang dùng bivalirudin hoặc heparin KPĐ để giảm thiểu nguy cơ huyết khối trong ống thông.
a. So sánh giữa heparin KPĐ và heparin TLPTT
(xem thêm mục 3.2-b phần II)
- Nghiên cứu SYNERGY trên 10.027 bệnh nhân bị HCMVC không có ST chênh lên so sánh hiệu quả và tính an toàn của heparin TLPTT và heparin KPĐ. Kết quả sau 6 tháng và 1 năm theo dõi, không có sự khác biệt về tỷ lệ biến cố MACE và tỷ lệ tử vong giữa hai thuốc. Tuy nhiên, tỷ lệ chảy máu trong viện cao hơn ở nhóm dùng heparin TLPTT ( 9,1% so với 7,6%).
b. So sánh giữa heparin KPĐ và bivalirudin
(xem thêm mục 3.2-a phần II )
- Heparin KPĐ được ưu tiên sử dụng hơn so với bivalirudin nếu bệnh nhân đang sử dụng ticagrelor hoặc prasugrel không chỉ vì chênh lệch giá cả mà còn vì tỷ lệ huyết khối trong stent cao hơn ở nhóm dùng bivalirudin. Với bệnh nhân sử dụng clopidogrel, cả heparin KPĐ hoặc bivalirudin đều có thể sử dụng, đặc biệt nếu bệnh nhân có nguy cơ chảy máu cao hoặc can thiệp qua đường ĐM đùi bivalirudin được khuyến cáo dùng ưu tiên.
- Các kết luận trên được rút ra từ các nghiên cứu ACUITY, ISAR – REACT 4, MATRIX và VALIDATE- SWEDEHEART 2017. Các nghiên cứu đều nhận thấy không có sự khác biệt về tỷ lệ tử vong, biến cố tim mạch giữa heparin KPĐ và bivalirudin, mặc dù có tăng nhẹ tỷ lệ huyết khối trong stent ở nhóm dùng bivalirudin (nghiên cứu MATRIX).
c. Fondaparinux
- Mặc dù được khuyến cáo sử dụng ưu tiên trên các bệnh nhân bị HCMVC không có ST chênh lên có nguy cơ chảy máu cao (nghiên cứu OASIS – 5) nhưng với các bệnh nhân có dự định tái thông ĐMV, thuốc không được sử dụng thường quy do nguy cơ huyết khối trong ống thông.
- Nghiên cứu OASIS – 5 so sánh giữa fondaparinux với enoxaparin cho thấy nhóm sử dụng fondaparinux có tỷ lệ huyết khối trong ống thông cao hơn ( 0,9% so với 0,4%). Do đó bắt buộc phải sử dụng heparin KPĐ với các bệnh nhân đang dùng fondaparinux có kế hoạch PCI.
d. Liều dùng:
Bệnh nhân được can thiệp ĐMV cấp:
- Heparin KPĐ: bolus tĩnh mạch 60 UI/kg ( tối đa 5000 UI) sau đó 12 UI/kg/h ( tối đa 1000 UI) duy trì APTT 50 – 75 giây.
- Bivalirudin:
-
- Tại phòng cấp cứu: Bolus tĩnh mạch 0,1mg/kg sau đó 0,25 mg/kg/h.
- Tại phòng can thiệp tại thời điểm PCI: Bolus tĩnh mạch 0,75 mg/kg sau đó 1,75 mg/kg/h.
Bệnh nhân được can thiệp ĐMV trì hoãn:
- Nếu bệnh nhân đang truyền heparin KPĐ:
- Nếu không có thuốc kháng thụ thể GP IIb/IIIa: sau khi mở đường vào mạch máu thành công, thêm heparin KPĐ để ACT từ 250 – 300 giây.
- Nếu có thuốc kháng thụ thể GP IIb/IIIa: thêm heparin KPĐ để ACT từ 200 – 250 giây.
- Nếu bệnh nhân đang dùng enoxaparin, liều chống đông phụ thuộc thời gian từ liều tiêm dưới da cuối cùng:
-
- < 8h: Không cần thêm chống đông.
- > 8h: Tiêm tĩnh mạch 0,3 mg/kg enoxaparin.
- Nếu bệnh nhân đang dùng fondaparinux: bolus 85 UI/kg heparin KPĐ.
e. Thời gian sử dụng
- Nên dừng ngay sau PCI nếu không có biến chứng. Tuy nhiên, có thể kéo dài thời gian sử dụng nếu có các tình huống sau:
-
- Liên quan đến thủ thuật: gánh nặng huyết khối lớn, dòng chảy chậm, stent dài, can thiệp thân chung, chỗ chia đôi.
- Các chỉ định phải dùng thuốc chống đông: rung nhĩ, van cơ học, huyết khối buồng tim…
- Nếu bệnh nhân đang dùng bivalirudin và chỉ mới dùng thuốc kháng KTTC ngay trước thủ thuật thì tiếp tục truyền bivalirudin 1,75mg/kg thêm 4h.
THUỐC KHÁNG KẾT TẬP TIỂU CẦU
Phân loại (xem mục 4.1 phần II)
Lựa chọn thuốc kháng kết tập tiểu cầu
a. Nguyên tắc
- Tất cả bệnh nhân nên được dùng 150 đến 300 mg aspirin càng sớm càng tốt sau khi được chẩn đoán. Liều đầu tiên nên được nhai hoặc nghiền nát trước khi uống.
- Dù chiến lược điều trị tiếp theo là can thiệp hay nội khoa bảo tồn, tất cả bệnh nhân nên được dùng thuốc ức chế thụ thể P2Y12.
- Thuốc ức chế thụ thể P2Y12 có thể được sử dụng sớm ở các bệnh nhân chưa có kế hoạch chụp và can thiệp ĐMV sớm và không có nguy cơ chảy máu cao.
- Đối với những bệnh nhân chỉ điều trị nội khoa bảo tồn, ticagrelor 180 mg là thuốc được khuyến cáo sử dụng.
- Phần lớn bệnh nhân không cần dùng thuốc ức chế glycoprotein IIb/IIIa tiêm tĩnh mạch. Chỉ định sử dụng nhóm này bao gồm:
-
- Bệnh nhân có bằng chứng thiếu máu cục bộ liên tục dù đang điều trị bằng kháng KTTC kép và có kế hoạch can thiệp ĐMV.
- Bệnh nhân có nguy cơ cao khi PCI như gánh nặng huyết khối lớn, huyết khối xuất hiện trong khi đang PCI mà bệnh nhân chưa được dùng prasugrel hoặc ticagrelor trước đó.
- Đối với những bệnh nhân có tiền sử xuất huyết tiêu hóa nên dùng thêm thuốc ức chế bơm proton.
b. Thuốc kháng kết tập tiểu cầu cho bệnh nhân có kế hoạch can thiệp
(xem thêm mục 4.2-c phần II):
- Tất cả các bệnh nhân bị HCMVC không có ST chênh lên có kế hoạch PCI đặt stent cần phải sử dụng thuốc KTTC kép. Trong đó ticagrelor và prasugrel được chỉ định ưu tiên hơn so với clopidogrel. Tuy nhiên, đối với các bệnh nhân có kế hoạch can thiệp sớm, nên sử dụng thuốc P2Y12 (prasugrel, ticargrelor, clopidogrel) khi biết rõ tổn thương động mạch vành (trên phim chụp ĐMV qua da hoặc MSCT).
- Bằng chứng ủng hộ cho việc chỉ định ưu tiên của ticagrelor và prasugrel đến từ thử nghiệm PLATO và TRITON – TIMI 38. Trong khi đó, nghiên cứu ISAR – REACT 5 so sánh đối đầu trực tiếp ticagrelor và prasugrel cho kết quả ủng hộ cho prasugrel; đồng thời, do hiệu quả của prasugrel trên chức năng nội mạc, hiện nay khuyến cáo ESC 2020 nên ưu tiên sử dụng prasugrel so với ticagrelor ở nhóm bệnh nhân HCMVC không có ST chênh lên được tiến hành can thiệp ĐMV. Lưu ý lựa chọn theo thời gian từ lúc chẩn đoán đến khi được PCI đã nêu ở phần nguyên lý.
- Cangrelor: xem mục 4.2-c phần II
- Thuốc kháng thụ thể GP IIb/IIIa:
-
- Không được chỉ định thường quy, chỉ được dùng trong một số trường hợp (xem phần nguyên lý).
- Nghiên cứu ISAR – REACT 2 cho các bằng chứng về giảm tỷ lệ biến cố MACE của abciximab trên các bệnh nhân bị HCMVC không có ST chênh lên được PCI. Nhưng đến nghiên cứu ACUITY Timing và EARLY ACS với eptifibatide dùng thường quy trong PCI không cho thấy hiệu quả vượt trội trong khi tỷ lệ chảy máu tăng lên có ý nghĩa. Do vậy sử dụng thuốc kháng thụ thể GP IIb/IIIa chỉ hạn chế trong các trường hợp đặc biệt.
c. Thuốc kháng kết tập tiểu cầu cho bệnh nhân điều trị nội khoa bảo tồn
- Trong khi nghiên cứu PLATO ủng hộ cho việc sử dụng ticagrelor hơn clopidogrel trên các bệnh nhân này, thì prasugrel thất bại trong việc tìm bằng chứng ủng hộ sử dụng sau khi nghiên cứu TRILOGY ACS cho thấy thuốc không cải thiện các kết cục lâm sàng mà còn làm tăng tỷ lệ chảy máu so với clopidogrel.
- Vì vậy khuyến cáo sử dụng thuốc ức chế P2Y12 trên đối tượng này bao gồm:
-
- Ticagrelor được ưu tiên sử dụng ngay tại thời điểm chẩn đoán.
- Nếu không thể sử dụng ticagrelor ( do nguy cơ chảy máu quá cao, không có sẵn) có thể sử dụng clopidogrel thay thế.
- Không sử dụng prasugrel trừ khi bệnh nhân có chỉ định can thiệp ĐMV.
- Không sử dụng GP IIb/IIIa trừ khi bệnh nhân có bằng chứng thiếu máu cơ tim liên tục và có kế hoạch PCI.
d. Thuốc kháng kết tập tiểu cầu trên bệnh nhân được phẫu thuật bắc cầu nối chủ vành
(xem mục 4.2-e phần II)
e. Liều dùng các thuốc:
- Aspirin:
-
- Liều nạp: 150 – 300 mg.
- Liều duy trì: 75 – 100 mg/24h.
- Ticagrelor:
-
- Liều nạp: 180 mg.
- Liều duy trì: 90 mg x 2 lần/24h.
- Prasugrel:
-
- Liều nạp: 60 mg.
- Liều duy trì: 10 mg/24h.
- Chống chỉ định: Bệnh nhân có tiền sử xuất huyết, quỵ não (tuyệt đối) , tuổi > 75, cân nặng < 60 kg (tương đối).
- Clopidogrel:
-
- Liều nạp: 300 – 600 mg (ưu tiên liều 600 mg).
- Liều duy trì: 75 mg/24h.
- Cangrelor:
-
- Liều nạp: 30 µg/kg tiêm bolus trong 1 phút trước khi PCI.
- Liều duy trì: 4 µg/kg/phút truyền ít nhất 2h hoặc trong khi làm can thiệp.
- Các thuốc kháng thụ thể GP IIb/IIIa (xem mục 4.2-c phần II)
f. Một số chú ý đặc biệt khi sử dụng thuốc kháng KTTC
Thời gian:
- Như đã đề cập ở trên, các thuốc kháng KTTC nên được cho ngay sau khi thiết lập chẩn đoán. Tuy nhiên, có nhiều tình huống trên lâm sàng khiến cho bác sĩ có lý do để trì hoãn việc dùng thuốc như:
-
- Bệnh nhân có nguy cơ chảy máu cao.
- Bệnh nhân cần phải phẫu thuật tim mở do có bệnh đồng mắc: bệnh lý van tim, biến chứng cơ học của NMCT.
- Bệnh nhân có nguy cơ thấp: men tim không tăng, điện tâm đồ không biến đổi.
Cách uống thuốc và thời gian duy trì: xem mục 4.2-f phần II.
Chuyển đổi giữa các thuốc ức chế thụ thể P2Y12, thay đổi chế độ dùng các thuốc kháng kết tập tiểu cầu khi có xuất huyết:
Có thể cân nhắc giảm bậc điều trị của nhóm thuốc ức chế P2Y12 (ví dụ chuyển từ prasugrel hay ticagrelor sang clopidogrel), đặc biệt ở bệnh nhân có HCMVC được đánh giá là không phù hợp để dùng KNTTC hoạt lực mạnh. Giảm bậc điều trị có thể được tiến hành dựa trên đánh giá lâm sàng hoặc chỉ dẫn bằng xét nghiệm chức năng tiểu cầu hoặc xét nghiệm gen CYP2C19 phụ thuộc vào tiền sử bệnh và sự sẵn có của các xét nghiệm trên.
Sử dụng kết hợp các thuốc chống đông đường uống (xem thêm mục 4.2-f phần II ):
- Bệnh nhân có can thiệp đặt stent ĐMV: khoảng 6 – 8% bệnh nhân có kế hoạch PCI có các chỉ định sử dụng thuốc chống đông đường uống (OAC) kéo dài như rung nhĩ, bệnh lý van tim, huyết khối buồng tim. Các bệnh nhân này là những đối tượng đặc biệt do nguy cơ chảy máu lẫn tắc mạch đều rất cao. Các khuyến cáo điều trị theo ESC 2015 cho các bệnh nhân này bao gồm:
-
- Bệnh nhân có chỉ định dùng OAC nên phối OAC với thuốc kháng kết tập tiểu cầu ( I – C).
- Có kế hoạch chụp ĐMV sớm (trong vòng 24h) ở các bệnh nhân nguy cơ vừa – cao theo phân tầng để nhanh chóng có kế hoạch điều trị ( nội khoa – stent – CABG) và chiến lược dùng chống KTTC kể cả khi bệnh nhân đang dùng OAC trước đó ( IIa – C).
- Không dùng thuốc kháng KTTC kép với OAC trước khi bệnh nhân được chụp ĐMV ( III – C).
- Trong quá trình can thiệp ĐMV, cần cho chống đông đường tĩnh mạch nếu INR <2,5 bất kể thời gian từ liều OAC cuối cùng (I – C).
- Không dừng các thuốc OAC trong quá trình chuẩn bị và làm thủ thuật ( IIa – C).
- Một số lưu ý trong quá trình PCI để giảm thiểu nguy cơ chảy máu: xem bảng 17.4.
- Sử dụng thuốc kháng kết tập tiểu cầu sau thủ thuật: xem bảng 17.5
- Nếu sử dụng phác đồ 3 thuốc (triple therapy) cần duy trì PT- INR từ 2,0 -2,5 với thuốc kháng vitamin K và dùng liều thấp nhất với các thuốc chống đông mới theo các khuyến cáo mà vẫn có tác dụng dự phòng thuyên tắc.
- Thời gian và các mốc chuyển liệu trình thuốc (1 – 2 – 3 thuốc kết hợp): xem hình 17.5.
Bảng 17.4: Chiến lược tiếp cận giúp giảm nguy cơ chảy máu trong PCI ở các bệnh nhân dùng OAC
| Liều chống đông được điều chỉnh theo cân nặng và chức năng thận đặc biệt ở bệnh nhân nữ giới và bệnh nhân cao tuổi. |
| Ưu tiên can thiệp đường động mạch quay. |
| Thuốc ức chế bơm proton ở bệnh nhân sử dụng kháng kết tập tiểu cầu kép có nguy cơ xuất huyết tiêu hóa cao (tiền sử loét/xuất huyết đường tiêu hóa, sử dụng chống đông, sử dụng NSAID/ corticosteroid dài ngày hoặc có hai hoặc nhiều hơn hai các yếu tố sau: tuổi ≥ 65, trào ngược dạ dày thực quản, chậm tiêu, nhiễm HP, sử dụng rượu dài ngày). |
| Bệnh nhân sử dụng OAC· Tiến hành PCI mà không cần dừng kháng vitamin K hoặc DOAC.
· Bệnh nhân sử dụng kháng vitamin K không cần dùng thêm heparin không phân đoạn nếu INR > 2,5. · Ở bệnh nhân sử dụng DOAC, dùng thêm chống đông đường tiêm liều thấp (enoxaparin 0,5mg/kg hoặc heparin KPĐ 60 IU/kg) bất kể thời gian từ lần sử dụng DOAC cuối cùng. . Aspirin được chỉ định nhưng không nên điều trị trước với các thuốc ức chế thụ thể P2Y12. · Ức chế GPIIb/IIIa chỉ sử dụng cho những thủ thuật phức tạp. |
Bảng 17.5: Sử dụng thuốc chống đông và thuốc kháng kết tập tiểu cầu trên bệnh nhân bị HCMVC không có ST chênh lên được đặt stent ĐMV
| Khuyến cáo | Nhóm | Mức |
| Nếu nguy cơ chảy máu thấp (HAS-BLED ≤ 2), liệu pháp 3 thuốc với OAC, aspirin (75 – 100 mg/ngày) và clopidogrel 75mg/ngày nên được cân nhắc trong 6 tháng sau đó là OAC và aspirin 75 – 100 mg hoặc clopidogrel 75mg/ngày tiếp tục đến 12 tháng | IIa | C |
| Nếu nguy cơ chảy máu cao (HAS-BLED ≥ 3), liệu pháp 3 thuốc với OAC, aspirin (75 – 100 mg/ngày) và clopidogrel 75mg/ngày nên được cân nhắc trong vòng 1 tháng, sau đó là OAC và aspirin 75 – 100mg/ngày hoặc clopidogrel (75 mg/ngày) tiếp tục tới 12 tháng bất kể loại stent (stent trần hoặc stent phủ thuốc) | IIa | C |
| Kháng tiểu cầu kép bao gồm ức chế P2Y12 nên được cân nhắc thay thế liệu pháp 3 thuốc sau khi đặt stent ở bệnh nhân NMCT không ST chênh kèm rung nhĩ nếu điểm CHA2DS2 – VASc là 1 ở nam hoặc 2 ở nữ | IIa | C |
| Liệu pháp 2 thuốc với OAC và clopidogrel 75 mg/ngày có thể cân nhắc thay thế liệu pháp 3 thuốc ở những bệnh nhân chọn lọc (HAS-BLED ≥ 3 và nguy cơ huyết khối trong stent thấp) | IIb | B |
| Sử dụng ticagrelor hoặc prasugrel trong liệu pháp 3 thuốc không được khuyến cáo | III | C |
- Bệnh nhân phẫu thuật bắc cầu nối chủ vành hoặc điều trị nội khoa đơn thuần:
-
- Các bệnh nhân được CABG nếu vẫn sử dụng OAC như thường lệ sẽ làm tăng nguy cơ chảy máu lên rất nhiều lần, vì vậy trong trường hợp phẫu thuật có chuẩn bị cần tạm dừng OAC trước (48h với các DOAC). Trong trường hợp cần CABG cấp cứu cần truyền các yếu tố đông máu hoặc huyết tương tươi với các bệnh nhân dùng thuốc kháng vitamin K lẫn DOAC mặc dù tác dụng còn hạn chế
- Sau CABG nếu kiểm soát được tình trạng chảy máu cần cho ngay aspirin kết hợp DOAC
- Chỉ cần 1 loại thuốc KTTC (aspirin hoặc clopidogrel) kết hợp với OAC cho các bệnh nhân chỉ điều trị nội khoa đơn thuần ( IIa – C).
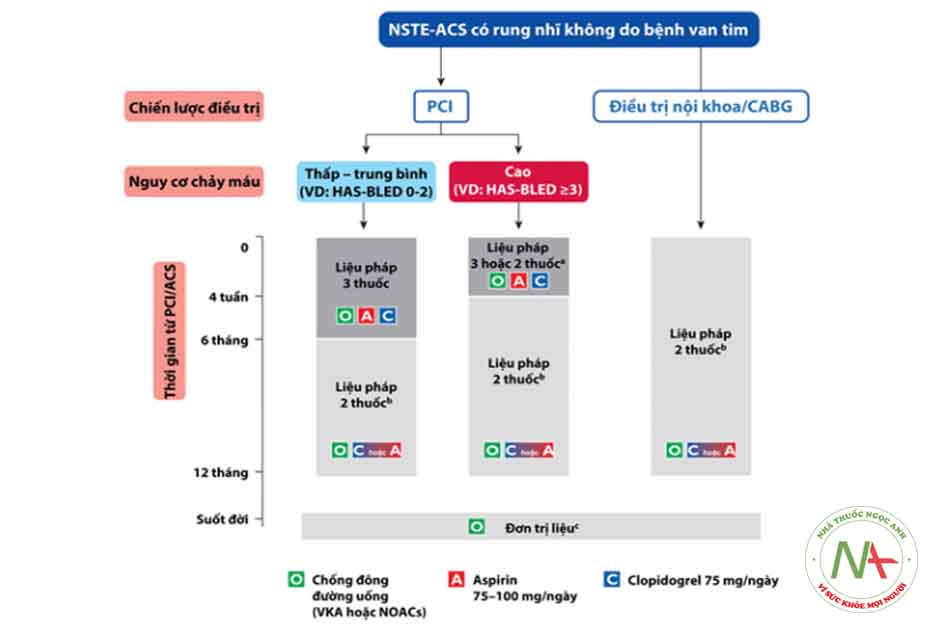
a, Liệu pháp hai thuốc gồm chống đông đường uống và clopidogrel có thể cân nhắc ở một số bệnh nhân (nguy cơ thiếu máu cục bộ thấp).
b, Aspirin có thể cân nhắc thay thế clopidogrel ở bệnh nhân sử dụng 2 thuốc (ví dụ: Chống đông đường uống kết hợp 1 thuốc kháng tiểu cầu); liệu pháp 3 thuốc có thể xem xét dùng đến 12 tháng cực kỳ chọn lọc ở bệnh nhân có nguy cơ biến cố cao (ví dụ: Huyết khối stent trước đó trong khi đã dùng đủ phác đồ kháng tiểu cầu, đặt stent ở thân chung động mạch vành trái hoặc còn nhánh động mạch vành thương tổn có ý nghĩa, nhiều stent ở đoạn gần động mạch vành, phương pháp 2 stent ở chỗ chia đôi, hoặc bệnh nhiều thân mạch vành lan tỏa đặc biệt ở bệnh nhân đái tháo đường).
c, Liệu pháp 2 thuốc với chống đông đường uống và 1 thuốc kháng tiểu cầu (aspirin hoặc clopidogrel) có thể cân nhắc dùng trên 1 năm ở bệnh nhân có nguy cơ biến cố mạch vành rất cao. Ở bệnh nhân đã đặt stent động mạch vành, liệu pháp kháng tiểu cầu kép có thể thay cho liệu pháp 3 thuốc hoặc kết hợp chống đông đường uống với 1 thuốc kháng tiểu cầu nếu điểm CHA2DS2-VASc là 1 (nam) hoặc 2 (nữ).
CÁC THUỐC CÓ TÁC DỤNG ẢNH HƯỞNG LÂU DÀI ĐẾN BỆNH NHÂN
Các thuốc hạ lipid máu
(xem chương 6, chương 16 và mục 5.3 phần II chương 17)
Thuốc chẹn beta giao cảm
- Ngoài tác dụng giảm cơn đau thắt ngực do thiếu máu cơ tim, thuốc còn giúp cái thiện tiên lượng ở các bệnh nhân suy tim EF thấp (< 40%) do NMCT.
- Chưa có nghiên cứu ngẫu nhiên nào đánh giá hiệu quả của thuốc trên các bệnh nhân bị HCMVC không có ST chênh lên không có suy tim.
- Các thuốc và liều dùng: xem mục 5.1 phần II.
Thuốc ức chế men chuyển và chẹn thụ thể
- Được chỉ định cho các trường hợp rối loạn chức năng thất trái do suy tim, tăng huyết áp, đái tháo đường.
- Sử dụng thuốc ƯCTT nếu bệnh nhân không dung nạp với thuốc ƯCMC.
- Các thuốc và liều dùng: xem chương 2.
Thuốc kháng thụ thể aldosteron
(Xem mục 5.5 phần II)
Điều trị rối loạn nhịp tim ở các bệnh nhân bị HCMVC không có ST chênh lên:
- Các rối loạn nhịp thất và trên thất có thể xảy ra trong giai đoạn cấp và các giai đoạn sau đó ở bệnh nhân bị NMCT cấp không có ST chênh lên.
- Xử trí giống trong trường hợp NMCT cấp có ST chênh lên: xem mục 6 phần II.
Xem thêm:
TÀI LIỆU THAM KHẢO
- Bertram G. Katzung. Basic & Clinical Pharmacology, Fourteenth Edition 2018, by McGraw-Hill Education.
- Lionel H. Opie, Bernard J. Gersh. Drugs for the Heart, 8th Ed 2013, by Elsevier Inc
- Kanu Chatterjee, Eric J Topol. Cardiac Drugs, Second Edition 2015, by Jaypee Brothers Medical Publishers
- Fihn SD, Gardin JM, Abrams J, et al. 2012 ACCF/AHA/ACP/AATS/PCNA/SCAI/STS guideline for the diagnosis and management of patients with stable ischemic heart disease: executive summary: a report of the American College of Cardiology Foundation/American Heart Association task force on practice guidelines, and the American College of Physicians, American Association for Thoracic Surgery, Preventive Cardiovascular Nurses Association, Society for Cardiovascular Angiography and Interventions, and Society of Thoracic Surgeons. Circulation 2012; 126:3097.
- Fihn SD, Blankenship JC, Alexander KP, et al. 2014 ACC/AHA/AATS/PCNA/SCAI/STS focused update of the guideline for the diagnosis and management of patients with stable ischemic heart disease: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines, and the American Association for Thoracic Surgery, Preventive Cardiovascular Nurses Association, Society for Cardiovascular Angiography and Interventions, and Society of Thoracic Surgeons. J Am Coll Cardiol 2014; 64:1929.
- Meisel SR, Dagan Y, Blondheim DS, et al. Transient ST-elevation myocardial infarction: clinical course with intense medical therapy and early invasive approach, and comparison with persistent ST-elevation myocardial infarction. Am Heart J 2008; 155:848.
- O’Gara PT, Kushner FG, Ascheim DD, et al. 2013 ACCF/AHA guideline for the management of ST-elevation myocardial infarction: a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines. Circulation 2013; 127:e362.
- Juhani Knuuti, William Wijns, Antti Saraste, et al. 2019 ESC Guidelines for the diagnosis and management of chronic coronary syndromes: The Task Force for the diagnosis and management of chronic coronary syndromes of the European Society of Cardiology (ESC). European Heart Journal, Volume 41, Issue 3, 14 January 2020, 407–477.
- Borja Ibanez, Stefan James, Stefan Agewall, et al. 2017 ESC Guidelines for the management of acute myocardial infarction in patients presenting with ST-segment elevation: The Task Force for the management of acute myocardial infarction in patients presenting with ST-segment elevation of the European Society of Cardiology (ESC). European Heart Journal, Volume 39, Issue 2, 07 January 2018, 119–177.
- Marco Roffi, Carlo Patrono, Jean-Philippe Collet, et al. 2015 ESC Guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation: Task Force for the Management of Acute Coronary Syndromes in Patients Presenting without Persistent ST-Segment Elevation of the European Society of Cardiology (ESC). European Heart Journal, Volume 37, Issue 3, 14 January 2016, 267–315.