COVID-19
Rối loạn cân bằng nước điện giải và thăng bằng kiềm toan thường gặp trong covid-19
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
Tác giả: Nguyễn Văn Huy, Hoàng Bùi Hải
Bài viết RỐI LOẠN CÂN BẰNG NƯỚC ĐIỆN GIẢI VÀ THĂNG BẰNG KIỀM TOAN được trích từ chương 11 trong phần 3 “Hồi sức ở bệnh nhân nặng và nguy kịch” sách Chẩn đoán và điều trị COVID-19, Nhà xuất bản Đại học Quốc gia Hà Nội.
1. SINH LÝ CÂN BẰNG NƯỚC
Trong điều kiện sinh lý, Natri chủ yếu ở dịch ngoại bào và có vai trò chính quyết định áp lực thẩm thấu hiệu dụng của dịch ngoại bào. Khi áp lực thẩm thấu hiệu dụng dịch ngoại bào thay đổi sẽ kéo theo sự thay đổi phân bố nước trong cơ thể. Nước trong cơ thể được phân bố ở dịch nội bào, dịch khoảng kẽ, dịch lòng mạch và một phần rất ít ở các khoang ảo. Áp lực thẩm thấu hiệu dụng dịch ngoại bào tăng sẽ làm nước di chuyển từ nội bào ra ngoại bào. Ngược lại, nước sẽ di chuyển vào nội bào.
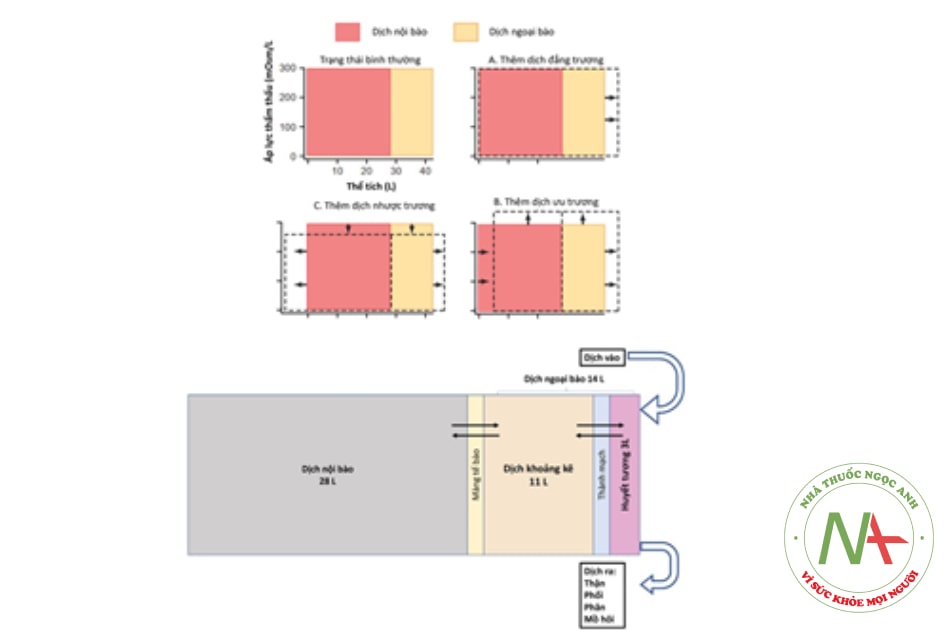
Nồng độ Natri huyết thanh được duy trì bởi 4 yếu tố: (1) lượng nước đưa vào, (2) cơ chế khát nước, (3) arginine vasopressin (AVP, hay antidiuretic hormone – ADH) của tuyến yên, và (4) thận – đáp ứng thay đổi cô đặc nước tiểu với vasopressin. Tăng áp lực thẩm thấu huyết thanh ở mức 290-295 mOsm/kg sẽ kích thích trung tâm khát ở vùng dưới đồi (hypothalamus). Nếu hoạt động thần kinh của trung tâm khát tốt sẽ kích thích cảm giác khát và người đó sẽ uống nước để giảm áp lực thẩm thấu về bình thường. Đáp ứng bình thường với lượng nước uống vào (thường nhược trương) là bài tiết nước tiểu ở trạng thái hòa loãng tối đa (ALTT nước tiểu < 100 mOsm/kg). Khởi đầu bằng nhận cảm tình trạng nhược trương huyết thanh bởi các tế bào vùng hạ đồi. Sau đó, các nhân vùng hạ đồi giảm bài tiết ADH và nồng độ ADH trong máu giảm xuống. ADH thấp làm giảm các kênh nước ở ống góp của thận và giảm tái hấp thu nước. Do đó nước tiểu thải ra giảm cô đặc.
Một điểm quan trọng nữa là áp lực thẩm thấu huyết thanh không phải là yếu tố duy nhất ảnh hưởng đến nồng độ ADH (hay AVP). Tụt huyết áp là yếu tố kích thích tiết ADH mạnh mẽ. Đáp ứng với các receptor áp lực này là cơ chế quan trọng để bảo vệ trong tình huống bị giảm thể tích. Thậm chí, tác dụng khi kích thích receptor áp lực còn mạnh hơn tác dụng của áp lực thẩm thấu khi kích thích giải phóng ADH. Do đó, một bệnh nhân có tụt huyết áp thì nồng độ ADH cao ngay cả khi áp lực thẩm thấu thấp. Ngoài ra, nồng độ ADH còn tăng khi đau, stress, nôn, giảm oxy, tăng CO2 máu, và thuốc như adrenalin và opioids.
2. RỐI LOẠN ĐIỆN GIẢI THƯỜNG GẶP TRONG COVID-19
2.1. HẠ NATRI MÁU
Tỷ lệ hạ Na máu ở bệnh nhân COVID-19 ghi nhận từ 10-60% tùy từng nghiên cứu. Hạ Na máu ở bệnh nhân COVID-19 có thể có nguyên nhân đa dạng, cần chẩn đoán được các thể lâm sàng và nguyên nhân hạ Na máu để có điều trị phù hợp. Theo các dữ liệu hiện tại, nguyên nhân hạ Natri máu thường gặp ở bệnh nhân COVID-19 là SIADH (40-50%) và mất Natri qua đường tiêu hóa do nôn và tiêu chảy. Tuy nhiên 2 nguyên nhân này lại có chiến lược xử trí khác biệt hoàn toàn. Do đó, cần xác định được nguyên nhân trước khi điều trị.
Hạ Na máu được định nghĩa là tình trạng giảm nồng độ Na huyết thanh < 135 mEq/L.
Hạ Na máu nặng khi Na < 115 mmol/L có thể đe dọa tính mạng, đặc biệt khi diễn biến nhanh.
Hạ Na máu đẳng trương (giả hạ Na máu) là tình trạng xét nghiệm Na huyết thanh thấp, nhưng áp lực thẩm thấu bình thường (280-295 mOsm/kg). Đây là sai số xét nghiệm do phương pháp quang kế ngọn lửa khi bệnh nhân có các tình trạng tăng triglyceride máu, tăng protein huyết tương, hòa loãng mẫu trước đó. Hiện nay, hầu hết các khoa hóa sinh đều dùng phương pháp điện cực chọn lọc ion để định lượng Na, do đó sẽ khắc phục được tình trạng này.
Hạ Na máu ưu trương là tình trạng hạ Natri máu thật sự, nhưng có lượng lớn chất tạo áp lực thẩm thấu khác trong dịch ngoại bào (ví dụ: glucose, mannitol, glycerol). Lúc này, đồng thời có cả hạ Natri máu (không phải giả hạ Natri), tăng áp lực thẩm thấu dịch ngoại bào và giảm thể tích dịch nội bào xảy ra.
Hạ Na máu nhược trương là tình trạng xảy ra khi thận giảm khả năng thải lượng dịch tương ứng với lượng dịch vào. Xảy ra khi uống vào một lượng lớn dịch nhược trương vượt quá khả năng thải dịch hòa loãng của thận hoặc khả năng hòa loãng nước tiểu của thận bị giảm. Phân biệt bằng cách đo áp lực thẩm thấu (ALTT) niệu. ALTT niệu < 100 mOsm/kg ở bệnh nhân hạ natri máu nhược trương do lượng dịch vào quá nhiều. ALTT niệu > 100 mOsm/ kg ở bệnh nhân hạ natri máu nhược trương là do giảm khả năng hòa loãng nước tiểu. Tình trạng nước tiểu cô đặc phản ánh nồng độ ADH trong máu ở mức cao. Bên cạnh đó, ADH bị ảnh hưởng bởi cả ALTT máu và huyết động, do đó cần đánh giá tình trạng dịch ngoại bào của bệnh nhân. Đồng thời xảy ra 3 tình trạng giảm, bình thường và tăng dịch ngoại bào. Đây là 3 thể lâm sàng của hạ Na máu nhược trương.
2.1.1. Triệu chứng lâm sàng
Có các biểu hiện của tình trạng phù tế bào não (ví dụ: Hạ Na máu nặng có tăng áp lực nội sọ).
Hạ Natri máu nhược trương được chia thành: đẳng tích, tăng thể tích, và giảm thể tích máu.
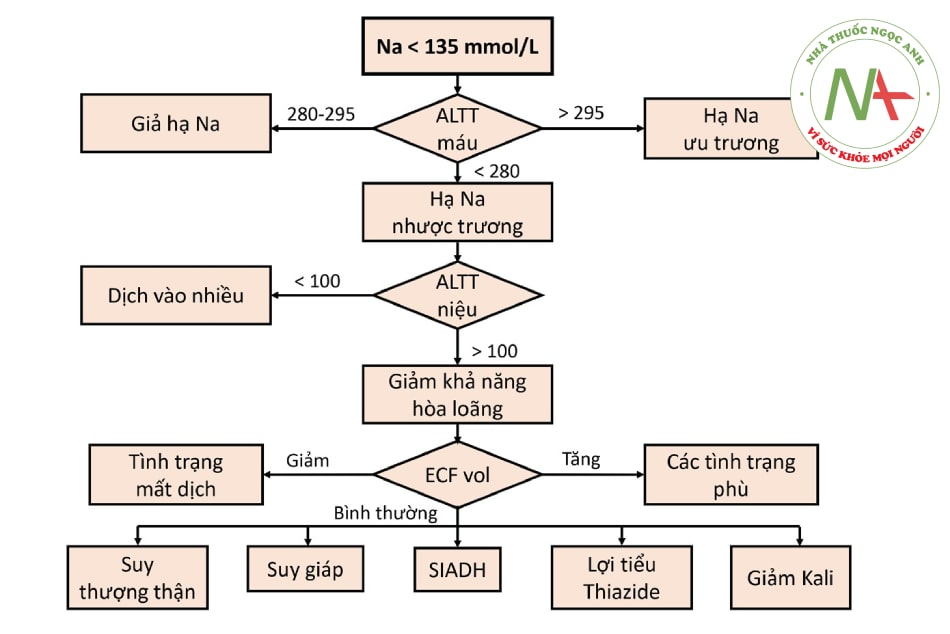
Chú thích: ECF vol (extracellular fluid volume status): tình trạng dịch ngoại bào; ALTT: áp lực thẩm thấu; SIADH: Hội chứng tăng tiết ADH không thích hợp.
a. Hạ Na máu giảm thể tích
Bảng 11.1. Đặc trưng và nguyên nhân hạ Na giảm thể tích
| Đặc trưng | Giảm chức năng hòa loãng nước tiểu khi giảm thể tích do 2 cơ chế: giảm lượng dịch tới nephron và giải phóng ADH thông qua cơ chế huyết động học. |
| Nguyên nhân | – Các nguyên nhân có thể quan sát (vd: mất máu, nôn, tiêu chảy, đái nhiều). Ở bệnh nhân COVID-19, hiện tượng mất Natri do nôn và tiêu chảy là một trong các nguyên nhân thường gặp, do đó cần đặc biệt lưu ý trên lâm sàng.– Mất qua thận (vd: do dùng lợi tiểu): Na niệu cao > 20 mEq/L, FENa > 1%.
– Mất ngoài thận: có biểu hiện bảo tồn Na (Na niệu < 10 mEq/L, FENa < 1%). – Não mất muối (CSW – hay mất muối do não): các bệnh lý nội sọ (vd: chấn thương, u, chảy máu). Cần phân biệt với SIADH, CSW có đặc trưng chính là giảm dịch ngoại bào và Na niệu bài tiết không phù hợp với tình trạng dịch. |
Chú thích: SIADH: Hội chứng tăng tiết ADH không thích hợp.
b. Hạ Na máu tăng thể tích
Bảng 11.2. Đặc trưng và nguyên nhân hạ Na tăng thể tích
| Đặc trưng | – Không thể bài tiết Na bình thường (tăng tổng lượng Na) vì suy thận nặng (Na niệu > 20 mEq/L) hoặc có bệnh lý gây ra tình trạng phù (ví dụ: suy tim, xơ gan, và hội chứng thận hư) (Na niệu< 10 mEq/L, FENa < 1%).
– Ở những BN có phù, có tình trạng giảm thể tích tuần hoàn hiệu dụng (mặc dù thể tích dịch lòng mạch ở mức cao), do đó kích thích bài tiết ADH và làm giảm khả năng hòa loãng nước tiểu. |
| Nguyên nhân | – Suy thận mạn và tổn thương thận cấp giai đoạn vô niệu: có xu hướng bị hạ Na.– Bệnh nhân suy tim mất bù.
– Bệnh nhân xơ gan có biến chứng. |
c. Hạ Na máu thể tích bình thường
Bảng 11.3. Đặc trưng và nguyên nhân hạ Na thể tích bình thường
| Đặc trưng | Bản chất hạ Na là có thừa nước đơn độc và tổng lượng Na bình thường, tuy nhiên trên lâm sàng có thể thấy hình ảnh “đẳng tích” do lượng nước thừa được phân bố cả dịch nội bào (chiếm 2/3) và ngoại bào. Do đó, biểu hiện trên lâm sàng có tăng nhẹ lượng dịch nội mạch là có giảm ure máu và giảm acid uric máu. |
| Nguyên nhân | – SIADH (Hội chứng bài tiết ADH không thích ứng): có tăng nồng độ ADH trong máu không phù hợp với các kích thích do ALTT và huyết động. ALTT niệu > 100 mOsm/kg. Có 5 nhóm nguyên nhân của SIADH: do các bất thường nội sọ, bất thường trong lồng ngực, khối u, các thuốc, và vô căn. Trên quần thể bệnh nhân COVID-19, có báo cáo đã ghi nhận có tương quan tỷ lệ nghịch giữa nồng độ IL-6 và nồng độ Natri máu. IL-6 được xem đóng vai trò quan trọng trong cơ chế bệnh sinh gây ra SIADH, thông qua kích thích các tế bào thần kinh nội tiết bài tiết ADH. Có một số yếu tố kèm theo có thể gây tăng bài tiết ADH như bệnh nhân thông khí nhân tạo áp lực dương (kích thích bài tiết ADH không thông qua cơ chế áp lực thẩm thấu), sử dụng corticoid, và kháng sinh ( ví dụ: fluoroquinolon, cefoperazone/ sulbactam, azithromycin).– Suy thượng thận. Ở bệnh nhân có dùng glucocorticoid kéo dài (vì điều trị bệnh trước đó hoặc điều trị COVID-19) có thể gây ra tình trạng suy thượng thận. Bệnh nhân thường có hạ natri và hạ kali máu phối hợp. Xét nghiệm sàng lọc Cortisol 8 giờ sáng. Các xét nghiệm chuyên sâu khác như: định lượng ACTH, nghiệm pháp kích thích ACTH. Cần điều trị suy thượng thận bằng liệu pháp thay thế hormone để điều chỉnh natri và kali máu. Với nhóm này, cần phối hợp với bác sĩ chuyên khoa Nội tiết để theo dõi điều trị suy thượng thận sau này.
– Suy giáp – Hạ Na ở vận động viện tập các môn thể thao sức bền: 15% vận động viên marathon có Na < 135 mmol/L. Yếu tố nguy cơ gồm: BMI < 20, thời gian racing > 4 giờ, uống nhiều nước trong lúc chạy. |
1.2. Điều trị hạ Na máu
Điều trị hạ Na chỉ cần thiết khi có tình trạng giảm áp lực thẩm thấu. Khi điều trị cần xem xét bốn yếu tố: (1) triệu chứng lâm sàng (các triệu chứng phù tế bào não), (2) thời gian diễn biến cấp hay mạn. Hạ Na máu mạn tính mà bù Na quá nhanh sẽ có nguy cơ dẫn đến hội chứng tiêu myelin do áp lực thẩm thấu (ODS). (3) xử trí nguyên nhân. Hạ Na ưu trương cần xử lý nguyên nhân, ví dụ như tình trạng tăng glucose máu. (4) Theo dõi sát tránh bù quá mức.
Xác định nguyên nhân hạ Natri máu ở bệnh nhân COVID-19 rất quan trọng. Vì dựa trên các dữ liệu hiện có các nguyên nhân thường gặp gồm có SIADH và mất Natri qua đường tiêu hóa (nôn và tiêu chảy). Chiến lược điều trị cho hai nguyên nhân này rất khác nhau. Cụ thể, với SIADH, chiến lược hạn chế dịch đáp ứng tốt trên bệnh nhân này, bên cạnh đó, bệnh nhân mất natri qua đường tiêu hóa cần được bù lại lượng điện giải mất.
Hội chứng tiêu myelin do áp lực thẩm thấu (Osmotic demyelination syndrome- ODS): nguyên nhân do điều chỉnh Na quá nhanh, đặc biệt ở người có hạ Na mạn (đã có quá trình thích nghi thể tích nội bào hoàn toàn). Đặc trưng của ODS là có các tổn thương thần kinh không phục hồi (ví dụ: rối loạn vận ngôn, rối loạn nuốt, rối loạn hành vi, rối loạn thăng bằng, liệt tứ chi, hôn mê) sau 3-10 ngày sau khi điều trị. Các yếu tố nguy cơ của ODS gồm có hạ Na trước đó, suy dinh dưỡng, lạm dụng rượu, cao tuổi, giới nữ, và sau phẫu thuật. Để tránh ODS, cần theo dõi sát Na máu để trách bù quá mức. Điều chỉnh Na ≤ 10 mmol/L/ngày.
NaCl 3% (có nồng độ Na 513 mmol/L), pha 23 ống NaCl 10% 5mL (115mL) với 385 mL NaCl 0,9%.
Bảng 11.4. Tóm tắt điều trị hạ Natri máu.
| Hạ Na máu cấp nặng | – Ví dụ: vận động viên marathon, sau phẫu thuật, dùng “thuốc lắc”.– Đặc điểm: diễn biến trong 24 giờ, nặng, có các triệu chứng tăng áp lực nội sọ nguy cơ tụt kẹt.
– Xử trí: Bolus tĩnh mạch 100 mL NaCl 3% trong ít nhất 10 phút. |
| Hạ Na máu mạn có triệu chứng | – Đặc điểm: > 48 giờ hoặc không rõ diến biến, mức độ nặng.– Mục tiêu: tăng Na máu ≤ 6 mmol/L trong 6 giờ đầu. |
| Hạ Na máu mạn không có triệu chứng | – Điều trị nguyên nhân.– Hạn chế lượng nước vào (duy trì bilan âm ~ 10 mL/kg).
– Điều chỉnh Na tăng ≤ 0,5 mEq/L/giờ. – Thuốc đối kháng receptor vasopressin (V2) (VRA): conivaptan (TM) và tolvaptan (uống). Dùng trong trường hợp SIADH không đáp ứng với hạn chế nước, hạ Na máu ở bệnh nhân suy tim mất bù. – Demeclocycline |
| Hạ Na giảm thể tích | – Bù dịch lòng mạch bằng NaCL 0,9% (sẽ giảm tiết ADH và tăng lượng nước tới thận, thận thải nước và Na sẽ được điều chỉnh).– Điều trị nguyên nhân |
| Hạ Na máu ở bệnh nhân có phù | – Hạn chế muối, nước– Lợi tiểu
– ACEIs, làm tăng thể tích máu động mạch hiệu dụng. – VRA |
Chú thích: SIADH: Hội chứng tăng tiết ADH không thích hợp; ACEIs: thuốc ức chế men chuyển.
Sự thay đổi Na máu khi bù nước có thể ước tính theo công thức:
Nồng độ Na thay đổi = (Na dịch truyền – [Na hiện tại]) / (Tổng lượng nước cơ thể + 1(Lít))
Trong đó:
Lượng nước cơ thể = Trọng lượng cơ thể x 0,6 (nam).
Trọng lượng cơ thể x 0,5 (nữ).
Trọng lượng cơ thể x 0,5 (nam – cao tuổi)
Trọng lượng cơ thể x 0,45 (nữ – cao tuổi)
Dung dịch NaCl 3% Có Na 513 mmol/L
Chú ý: Công thức trên chưa bao gồm lượng nước và Na tiếp tục mất đi.
2.2. TĂNG NATRI MÁU
Tăng Na máu là khi nồng độ Na huyết thanh > 145 mmol/L. Tỷ lệ tăng Na máu ở bệnh nhân COVID-19 chưa được thống kê đầy đủ, tuy nhiên có các ghi nhận tăng Na máu ở nhóm bệnh nhân COVID-19 nặng.
Các thay đổi phân bố nước ở bệnh nhân tăng Na máu được tóm tắt trong hình ảnh dưới đây:
Sơ đồ tiếp cận chẩn đoán & nguyên nhân Tăng Na máu
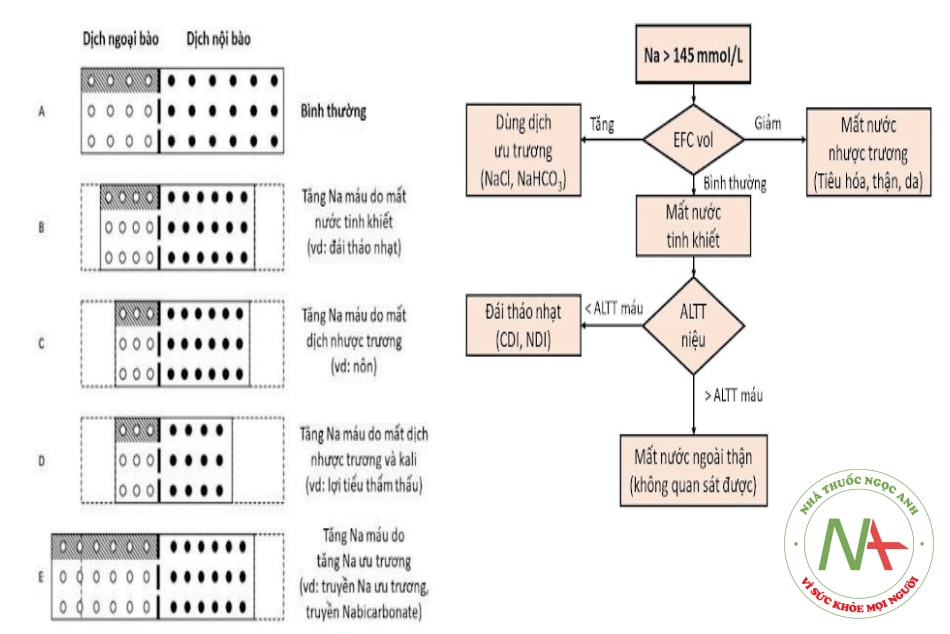
Chú thích: ECF vol (extracellular fluid volume status): tình trạng dịch ngoại bào; ALTT: áp lực thẩm thấu; CDI: đái tháo nhạt trung ương; NDI: đái tháo nhạt do thận.
Lượng mất ngoài thận (không quan sát được) ước tính 10 mL/kg trong điều kiện bình thường. Ở những người trong môi trường nóng, có sốt, thở nhanh sẽ mất tới 20 mL/kg.
2.2.1. Triệu chứng
Lâm sàng
- Toàn thân: khát, khó chịu.
- Thần kinh: yếu cơ, lú lẫn, mê sảng, co giật, hôn mê, co cứng, tăng phản xạ.
- Tiêu hóa: buồn nôn và nôn.
- Dấu hiệu thay đổi thể tích dịch ngoại bào
- Tăng natri máu có giảm thể tích (sụt cân, da niêm mạc khô, tĩnh mạch xẹp, nhịp tim nhanh, CVP giảm).
- Tăng natri máu có tăng thể tích (tăng cân, phù ngoại bào, tĩnh mạch cổ nổi, CVP tăng).
Triệu chứng cận lâm sàng
- Na máu tăng > 145 mmol/L
- ALTT máu tăng
- ALTT niệu < 800 mOsm/kg ở người thiếu ADH
- Na niệu: thay đổi phụ thuộc vào các thể lâm sàng.
2.2.2. Điều trị
Điều trị tăng Na máu phụ thuộc vào tình trạng dịch của bệnh nhân. Cần theo dõi điện giải đồ mỗi 4-6 giờ trong giai đoạn điều trị tăng Na máu nặng vì các công thức ước tính và phân tích có thể sẽ gặp sai số. Đồng thời, cần điều trị nguyên nhân như ngừng hút dịch dạ dày, giảm sốt, xử trí tăng glucose máu và glucose niệu, ngừng thụt và dùng lợi tiểu, xử trí tăng canxi máu và hạ kali máu.
- Mục tiêu điều trị tăng Na máu là đưa Na máu về 145 mmol/L. Và dùng thể tích dịch ít nhất có thể để xử lý tăng Na máu, vì thể tích truyền nhiều làm tăng nguy cơ phù não.
- Mục tiêu điều trị tăng Na máu đẳng trương (mất nước tinh khiết): (1) hạn chế và/hoặc bù lượng dịch đang tiếp tục mất, và (2) bù lượng dịch đã mất.
- Mục tiêu điều trị tăng Na máu tăng thể tích: (1) giảm thể tích dịch ngoại bào và nội bào, (2) bù lại lượng nước thiếu. Lưu ý, có thể gặp quá tải thể tích khi bù quá Do đó, trên lâm sàng thường cần phối hợp giữa dùng furosemid (tạo ra nước tiểu tương đương với muối nửa) và truyền glucose 5% để điều chỉnh tình trạng tăng Na máu.
- Với điều trị tăng Na máu giảm thể tích, với các biểu hiện tụt huyết áp, nhịp tim nhanh và giảm tưới máu mô cần truyền tĩnh mạch NaCl 0,9% bất kể mức độ tăng Na máu. Khi đã bù đủ thể tích dịch ngoại bào, sau đó mới xem xét đến tổng lượng nước thiếu.
Tốc độ bù nước cần tương xứng với mức độ nhanh của tiến triển tăng Na máu. Nếu tăng Na máu diễn biến nhanh trong vài giờ (ví dụ: sau phẫu thuật) cần điều chỉnh nhanh hơn. Ngược lại, tăng Na máu diễn biến nhiều ngày hoặc không rõ thời gian, cần hiệu chỉnh chậm, tránh gây phù não. Tốc độ bù nước sao cho nồng độ Na thay đổi < 10 mmol/L trong 24 giờ.
Sự thay đổi Na máu khi bù nước có thể ước tính theo công thức:
Nồng độ Na thay đổi = (Na dịch truyền – [Na hiện tại]) / (Tổng lượng nước cơ thể + 1(Lít))
Trong đó:
Lượng nước cơ thể = Trọng lượng cơ thể x 0,6 (nam).
Trọng lượng cơ thể x 0,5 (nữ).
Trọng lượng cơ thể x 0,5 (nam – cao tuổi)
Trọng lượng cơ thể x 0,45 (nữ – cao tuổi)
Chú ý: Công thức trên chưa ước tính lượng dịch tiếp tục bị mất đi theo thời gian.
Bảng 11.5. Đặc điểm của các loại dịch truyền thường dùng.
| Loại dịch truyền | [Na dịch truyền] | Phân bố ở dịch ngoại bào % |
| Glucose 5% | 0 | 40% |
| NaCl 0,45% | 77 | 73% |
| Ringer’s lactate | 130 | 97% |
| NaCl 0,9% | 154 | 100% |
Cần chọn loại dịch truyền trước khi tính toán theo công thức, chọn loại dịch tùy vào
Các sai lầm thường gặp khi điều chỉnh tăng Na máu:
- Sử dụng NaCl 0,9% để xử lý tăng Na máu. Ví dụ một bệnh nhân nam 50 tuổi có Na máu 162 mmol/L và nặng 70 kg (lượng nước cơ thể là 42 lít). Khi truyền 1 lít NaCl 0,9% sẽ giảm Na đi 0,2 mmol/L ([154-162]/[42+1]= -0,2). Mặc dù nồng độ Na của dịch truyền thấp hơn Na máu, tuy nhiên mức giảm không đủ để giải quyết tăng Na máu. Hơn thể nữa, hiện tượng mất dịch nhược trương tiếp tục vượt quá mức truyền vào và làm tăng Na máu nặng hơn. NaCl 0,9% chỉ nên được sử dụng trong trường hợp tăng Na máu có rối loạn huyết động (nhịp nhanh, huyết áp tụt, thiếu máu mô).
- Bù quá nhanh và/hoặc quá mức có thể gây ra phù não.
2.3. TĂNG KALI MÁU
Kali máu bình thường 3,5–5,0 mmol/L. Kali chủ yếu (98%) nằm trong nội bào, khác với Na có nồng độ cao ở dịch ngoại bào và được duy trì nhờ bơm Na-K-ATPase ở màng tế bào.
Tăng kali máu khi K+ > 5,0 mmol/L. Tăng kali máu nặng khi K+ > 6,5 mmol/L và có biểu hiện trên điện tâm đồ.
Giả tăng kali máu: tan máu khi lấy mẫu, để mẫu quá lâu, mẫu bị giữ trong nhiệt độ lạnh.
Bảng 11.6. Tóm tắt tiếp cận tăng kali máu
| Tăng kali cấp cứu | Tăng kali ổn định (kéo dài vài ngày) |
| Tình huống: Lần đầu tiếp nhận bệnh nhân, kali máu cao (> 6,5 mmol/L).– Lập tức làm điện tâm đồ để tìm các dấu hiệu tăng kali máu. Nếu có cần điều trị cấp cứu ngay.
– Đồng thời lấy mẫu xét nghiệm (gửi Khoa Hóa sinh): điện giải đồ, glucose, ure, creatinine, và công thức máu. |
|
| – Đánh giá nước tiểu: quan sát màu sắc đánh giá tiêu cơ vân, tan máu. | Chú thích: GFR: mức lọc cầu thận,PC: cortisol huyết tương đã kích thích, PA: aldosteron huyết tương đã kích thích. |
| – Kiểm tra lại chế độ ăn và thuốc là nguồn kali: dịch truyền, kali uống, truyền chế phẩm máu, dùng chế phẩm cardioplegic. | |
| – Thuốc khác: digoxin, succinylcholine, truyền chế phẩm máu. |
2.3.1. Triệu chứng tăng kali máu
Lâm sàng: khi đã có tình trạng nguy kịch như rối loạn nhịp nhanh, rung thất, ngừng tuần hoàn.
Xét nghiệm: sinh hóa kali máu > 5 mmol/L.
Điện tim:
- Nhẹ: Sóng T cao nhọn, đối xứng, biên độ ≥ 2/3 sóng R ở chuyển đạo trước tim.
- Vừa – nặng: Kéo dài khoảng PR, sóng P dẹt, QRS giãn rộng, dạng sóng hình sin, rối loạn nhịp thất, vô tâm
Các xét nghiệm khác chẩn đoán nguyên nhân.
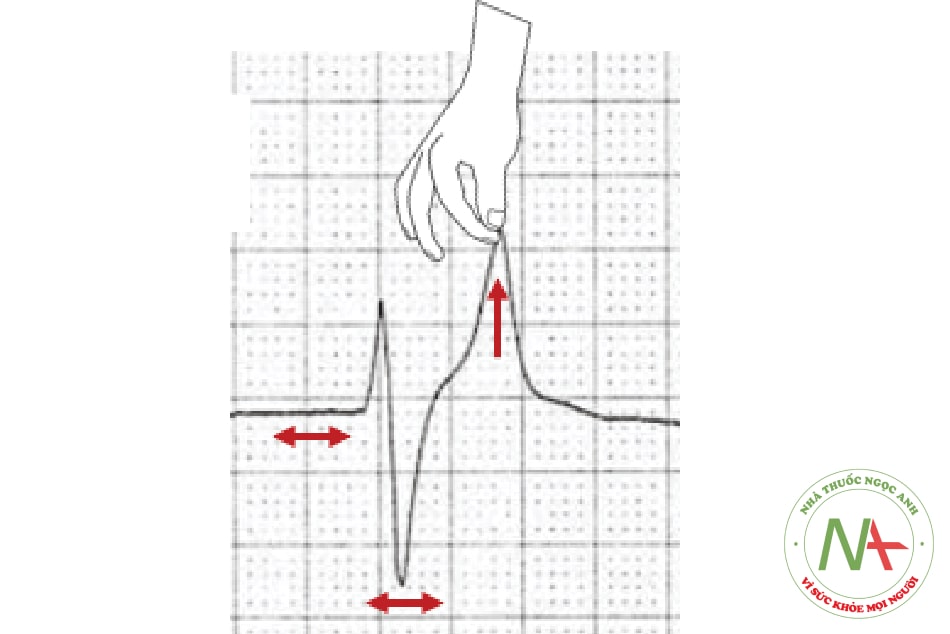
2.3.2. Các lựa chọn điều trị tăng kali máu
Bảng 11.7. Tóm tắt các thuốc xử trí tăng kali máu.
| THUỐC XỬ TRÍ TĂNG KALI MÁU | |
| Calci Clorid hoặc calci gluconat tiêm tĩnh mạch | Tác dụng: Ổn định màng tế bào cơ tim. Không làm giảm kali máu.Liều: 0,5-2 g
Thời gian tác dụng: khởi phát ngay và kéo dài 30-60 phút. |
| Insulin & glucose | Tác dụng: vận chuyển kali từ ngoại bào vào nội bào. Cần phối hợp insulin và glucose để tránh hạ glucose máu. |
| Liều: 10 IU insulin nhanh (TM) + 12,5-25 g glucose (vd: 250 ml glucose 10%)Tác dụng: bắt đầu sau 10-20 phút, đạt đỉnh sau 30-40 phút và kéo dài 2-4 giờ. Đa phần có tác dụng giảm 0,5-1,0 mmol/L. | |
| Albuterol khí dung | Tác dụng: là chất cường β2, giảm kali do kích thích bơm Na-K ATPase.Tác dụng: là 1 giải pháp có hiệu quả, tác dụng sau 30 phút. Kéo dài 3-6 giờ. Đặc biệt nếu phối hợp với insulin sẽ có tác dụng hiệp đồng. |
| Natri bicarbonate | Tác dụng: làm tăng pH và có tác dụng di chuyển kali vào nội bào. Thuốc này có tác dụng giảm kali máu kém nhất. Nên chỉ dùng trong trường hợp có phối hợp tăng kali máu và toan chuyển hóa. |
| Furosemide | Tác dụng: Thải kali qua nước tiểu. Tuy nhiên sẽ kém hiệu quả ở những người suy thận kém đáp ứng với lợi tiểu. |
| Kayexalate(nhựa trao đổi cation) | Tác dụng: kali liên kết với nhựa trao đổi cation, ngăn kali hấp thu qua ruột vào máu, và đào thải qua phân.Thời gian tác dụng: Sau 1-2 giờ, và kéo dài 4-6 giờ. |
| Lọc máu cấp cứu ngắt quãng | Tác dụng: Lọc máu IHD có tác dụng thải kali hiệu quả. Lọc CVVH, CVVHD, CVVHDF cũng có tác dụng tuy nhiên chậm hơn.Thời gian: IHD sau 30 phút. |
Chú thích: IHD: lọc máu ngắt quãng; CVVH, CVVHD, CVVHDF: các chế độ lọc máu liên tục qua đường tĩnh mạch.
2.3.3. Điều trị tăng kali máu
Bảng 11.8. Tóm tắt điều trị tăng kali máu
| Rối loạn điện tim | Không rối loạn điện tim |
| 1. Calciclorua 0,5g tiêm tĩnh mạch 2-3 phút. Có thể lặp lại sau 5 phút.2. Insulin và glucose.3. Albuterol 10-20 mg khí dung hoặc 0,5 mg pha truyền tĩnh mạch. 4. Natri bicarbonat 4,2% truyền 45 mol khi pH < 7,15. 5. Furosemide 40-60 mg tiêm tĩnh mạch. 6. Kayexalate (kalimate 5g) uống 15-30 g kèm 50 g sorbitol. 7. Lọc máu cấp cứu khi kém đáp ứng với lợi tiểu hoặc có vô niệu, thiểu niệu, thừa dịch, kết hợp toan chuyển hóa nặng pH < 7,10. |
1. Kayexalate (kalimate 5 g) 15-30 g và sorbitol 50 g. 2. Furosemide 40-60 mg tiêm tĩnh mạch. 3. Lọc máu cấp cứu khi kém đáp ứng với lợi tiểu. |
| Tìm và xử trí nguyên nhân. Lưu ý trong trường hợp toan ceton và tăng áp lực thẩm thấu do đái tháo đường cần xử lý các nguyên nhân này là chính! | |
2.4. HẠ KALI MÁU
Kali máu bình thường 3,5-5,0 mmol/L, hạ kali máu khi kali < 3,5 mmol/L. Có nghiên cứu ghi nhận tỉ lệ hạ kali máu ở bệnh nhân COVID-19 lên đến 41%, yếu tố nguy cơ là giới nữ và sử dụng lợi tiểu.
Bảng 11.9. Tóm tắt tiếp cận hạ kali máu
| Hạ kali máu cấp cứu | Hạ kali máu mạn |
| Các tình huống cần điều trị cấp cứu:– Có các triệu chứng tim mạch và thần kinh cơ.
– Hạ kali máu nặng < 2,0 mmol/L dù không có triệu chứng lâm sàng. – Hạ kali máu trung bình (kali < 3,0 mmol/L) ở người có dùng digoxin, nhồi máu cơ tim (nguy cơ rối loạn nhịp). Khai thác các nguy cơ hạ kali: thuốc tăng vận chuyển vào tế bào (dùng insulin, dùng các thuốc cường β-adrenergic), tăng đồng hóa (vd: dinh dưỡng tĩnh mạch), và tiền sử liệt chu kỳ. |
Hình 11.6. Tóm tắt tiếp cận hạ kali máu mạn Chú thích: UkV: bài xuất kali trong 24 giờ; PA: aldosteron huyết tương đã kích thích; UClV: bài xuất Cl trong 24 giờ; RTA: toan ống thận. |
2.4.1. Lâm sàng
- Yếu cơ (cơ tứ chi, cơ hô hấp), đau cơ, co rút cơ, tiêu cơ vân.
- Mạch yếu, tiếng tim nhỏ có thể có tiếng thổi tâm thu, có thể có ngất.
- Bụng chướng, giảm nhu động ruột, táo bón, buồn nôn, nôn.
2.4.2. Cận lâm sàng
- Xét nghiệm kali máu < 3,5 mmol/L.
- Điện tâm đồ: có sóng U, sóng T dẹt, ST chênh xuống, QT kéo dài, nhịp thanh thất, xoắn đỉnh.
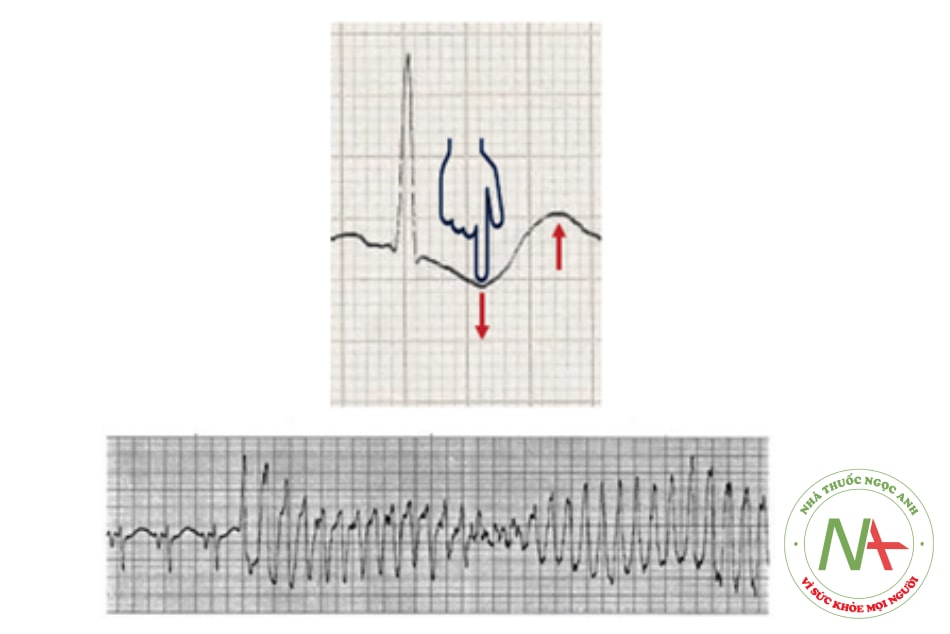
2.4.3. Chẩn đoán xác định:
xét nghiệm kali máu < 3,5 mmol/L.
Bảng 11.10. Phân độ hạ kali máu
| Mức độ nhẹ | Không có triệu chứng lâm sàng và rối loạn điện tim. Kali máu từ 2,5–3,5 mmol/L. |
| Mức độ vừa | Có chướng bụng, chuột rút. Điện tâm đồ có sóng T dẹt, đoạn ST chênh xuống nhưng không có các triệu chứng nặng trên điện tim và liệt thần kinh cơ. |
| Mức độ nặng | Có rối loạn nhịp, yếu cơ, hội chứng tiêu cơ vân cấp.Kali ≤ 2,5 mmol/L (< 3,0 mmol/L với người đang dùng digoxin). |
2.4.4. Xử trí hạ kali máu
Bảng 11.11. Tóm tắt xử trí hạ kali máu
| Theo dõi: | |
| Hạ kali máu nhẹ: kali 2,5-3,5 mmol/L VÀ không có triệu chứng.Xử trí: Uống hoặc truyền tĩnh mạch KCl 10-20 mmol (1-1,5g) mỗi 6 giờ.
Hạ kali máu vừa – nặng: Kali ≤ 2,5 mmol/L (< 3,0 mmol/L với người đang dùng digoxin) – Mức độ nặng: có dấu hiệu liệt cơ và dấu hiệu nặng trên điện tim: dùng KCl 13-20 mmol/giờ (1-1,5 g) truyền qua tĩnh mạch trung tâm trong 3 giờ, sau đó xét nghiệm lại rồi phân loại lại. |
– Trường hợp có biến đổi điện tim, cần theo dõi Monitor điện tim– Theo dõi xét nghiệm kali máu. Mức độ nặng 3 giờ/lần, mức độ vừa 6 giờ/lần, mức độ nhẹ 24 giờ/lần cho đến khi kali máu về bình thường
Chú ý: – 1 gram kali clorua có 13,6 mmol kali. – pH tăng 0,1 tương ứng kali giảm 0,4 mmol/L. – Tốc độ bù kali clorua không quá 26 mmol/giờ (2 gram). – Nồng độ kali clorua pha quá 40 mmol/L (3 gram) thì cần dùng đường truyền trung tâm, không dùng đường ngoại biên do gây khó chịu và viêm mạch. – Truyền glucose sẽ tăng nguy cơ hạ kali máu. |
3. CÁC TRƯỜNG HỢP RỐI LOẠN ĐIỆN GIẢI KHÁC
3.1. HẠ PHOSPHO MÁU
Định nghĩa hạ phospho máu khi nồng độ phosphate huyết thanh < 3 mg/dL.
Bảng 11.12. Phân loại mức độ hạ phospho máu
| Giảm nhẹ | 2,5-3 mg/dL |
| Giảm vừa | 1-2,5 mg/dL |
| Giảm nặng | < 1 mg/dL |
Ở bệnh nhân hồi sức, thường gặp ở người có toan ceton đái tháo đường và sepsis. Hạ phospho nhẹ tới vừa thường không có triệu chứng, tuy nhiên hạ phospho nặng làm tăng tỷ lệ tử vong. Bệnh nhân có phospho máu < 1 mg/ dL có tỷ lệ tử vong do tất cả các nguyên nhân khoảng 30%.
Bảng 11.13. Các nguyên nhân hạ phospho máu
| Các nguyên nhân thường gặp của hạ phospho máu | |
| Vận chuyển vào tế bào – Hội chứng cho ăn trở lại– Kiềm hô hấp– Sử dụng insulin |
Mất qua thận – Dùng lợi tiểu– Truyền dịch nhiều– Lợi tiểu thẩm thấu– Cường cận giáp (nguyên phát và thứ phát) – Các bất thường về chức năng ống lượn gần – Hội chứng Fanconi |
| Tình trạng dị hóa quá mức – Bỏng– Chấn thương– Sepsis |
Rối loạn hấp thu qua tiêu hóa – Suy dinh dưỡng– Các thuốc kháng acid gắn phosphate– Thiếu vitamin D– Tiêu chảy mạn – Tiêu chảy mỡ – Hút dịch dạ dày – Nôn – Hội chứng rối loạn hấp thu
|
Bệnh nhân toan ceton đái tháo đường có nguy cơ cao với tình trạng thiếu hụt phosphate. Mặc dù xét nghiệm có thể bình thường nhưng tổng dự trữ của toàn cơ thể thường giảm do tình trạng toan chuyển hóa – gây dịch chuyển phosphate ra ngoại bào và mất qua thận do có tình trạng lợi tiểu thẩm thấu. Khi bệnh nhân được điều trị với insulin, tình trạng toan chuyển hóa cải thiện và đẩy phosphate từ huyết tương vào tế bào, và gây ra tình trạng hạ phospho máu.
Bảng 11.14. Triệu chứng lâm sàng của hạ phospho máu nặng
| Các triệu chứng lâm sàng của hạ phospho máu nặng (<1,0 mg/dL) | |
| Hệ hô hấp
– Suy hô hấp cấp – Phụ thuộc máy thở |
Hệ cơ và xương – Yếu cơ– Tiêu cơ vân– Mất khoáng trong xương |
| Hệ tạo máu – Tan máu– Các rối loạn chức năng thực bào và hóa ứng động của bạch cầu |
Hệ thần kinh – Thay đổi ý thức– Mất khả năng giữ thăng bằng– Dị cảm |
| Hệ tim mạch – Bệnh cơ tim– Giảm sức bóp cơ tim– Rối loạn nhịp tim |
|
Hạ phospho máu gây ra tình trạng giảm ATP của tế bào cơ tim, gây ra các triệu chứng về tim mạch. Tương tự, làm giảm lực cơ của cơ hoành và phụ thuộc máy thở.
Điều trị
Điều trị hạ phospho máu nặng (nồng độ phosphate < 1 mg/dL) cần bù bằng đường tĩnh mạch. Khuyến cáo dùng truyền liên tục kali phosphate 9 mmol (279 mg) trong thời gian 12 giờ. Tùy theo mức độ nặng sẽ tính liều từ 0,08 mmol/kg (2,5 mg/kg) hoặc 0,16 mmol/lg (5 mg/kg) trong 6 giờ. Lưu ý thận trọng ở bệnh nhân suy thận.
Với hạ phospho mức độ nhẹ – vừa, có thể bổ sung qua đường uống. Nguồn bổ sung: sữa tách bơ (skim milk), cung cấp 900 mg/L phosphate vô cơ. Nếu bệnh nhân không dung nạp, xem xét bổ sung Natri phosphate (chứa 250 mg phosphate mỗi viên).
3.2. HẠ MAGIE MÁU
Magie máu bình thường 1,8-2,3 mg/dL (1,5-1,9 mEq/L hoặc 0,7-1,0 mmol/L).
Magie trong máu có 2 dạng: 20-30% gắn với protein, dạng tự do chiếm 70- 80% có thể được lọc qua thận. Magie di chuyển vào tế bào rất chậm do đó bù magie phải bù kéo dài.
3.2.1. Nguyên nhân hạ magie máu
Bảng 11.15. Nguyên nhân hạ magie máu ở hồi sức
| Giảm hấp thu qua tiêu hóa | Dinh dưỡng tĩnh mạch hoàn toàn Chế độ ăn thiếu magie Hội chứng ruột ngắn, hội chứng kém hấp thu.
Lạm dụng rượu |
| Tăng mất qua tiêu hóa | Tiêu chảy mạn, rò dịch tiêu hóa và dịch mật, hút dịch dạ dày liên tục, nôn. |
| Mất qua thận nội sinh | Bệnh thận kẽ, sau ghép thận, giai đoạn đái trở lại sau suy thận cấp. |
| Mất qua thận do thuốc | Dùng lợi tiểu quai và thiazid, aminoglycosides, amphotericin B. |
| Nguyên nhân nội tiết và chuyển hóa | Cường giáp, cường cận giáp, SIADH, toan ceton, hạ canxi, hạ albumin, hạ phospho. |
| Rối loạn phân bố magie | Viêm tụy cấp, dùng adrenalin, insulin, truyền máu lượng lớn, hội chứng nuôi dưỡng trở lại (refeeding syndrome). |
| Nguyên nhân khác | Lọc máu liên tục, ECMO, bỏng nặng |
Chú thích: SIADH: Hội chứng tăng tiết ADH không thích hợp;ECMO: oxy hóa máu qua màng ngoài cơ thể.
Ở bệnh nhân hồi sức, hạ magie thường do phối hợp nhiều nguyên nhân. Các nguyên nhân có thể gộp thành 4 nhóm chính: (1) giảm lượng hấp thu, (2) mất qua thận, (3) mất ngoài thận và (4) tái phân bố. Để chẩn đoán phân biệt nguyên nhân tại thận hay ngoài thận có thể đo lượng magie nước tiểu 24 giờ hoặc tính phân suất thải magie (FEMg):
FEMg= [UMg × Pcr] / [(0,7×PMg)×UCr] ×100
Trong đó: UMg, PMg là nồng độ Mg niệu và máu.
UCr, PCr là nồng độ creatinin niệu và máu.
Hạ magie máu do mất qua thận: Mg niệu 24 giờ > 25mg/24 giờ hoặc FEMg > 2%.
3.2.2. Triệu chứng hạ magie
Hạ magie máu thường không có triệu chứng và phát hiện thông qua xét nghiệm.
Biểu hiện điện tâm đồ của hạ magie tương tự với hạ kali: sóng T dẹt, sóng U, khoảng QT kéo dài. Rung nhĩ, nhịp nhanh nhĩ đa ổ, nhanh thất, hoặc xoắn đỉnh.
Hạ magie thường gặp kèm với hạ kali, hạ canxi.
- Do magie là một co-enzym với Na+/K+-ATPase ở mô cơ Hạ magie cũng được đi kèm với nhiều rối loạn nhịp khác như rung nhĩ, nhịp nhanh nhĩ đa ổ, nhanh thất hoặc xoắn đỉnh. Bù magie tĩnh mạch là thuốc đầu tay cho xoắn đỉnh và được dùng hỗ trợ điều trị rối loạn nhịp thất kháng trị.
- Hạ magie thường đi kèm với cả hạ kali và hạ canxi. Các thuốc và các thay đổi nội môi ảnh hưởng tới magie đồng thời ảnh hưởng tới kali. Do đó, có trường hợp hạ kali không đáp ứng với bù kali nếu không bù Tương tự với hạ canxi, vì hạ magie ức chế giải phóng PTH và hoạt động của hormone này. Kết quả là, hạ canxi không đáp ứng với bù canxi nếu không bù magie.
3.2.3. Điều trị hạ magie
Điều trị hạ magie cần điều trị nguyên nhân và bù Magie
Bảng 11.16. Các tình huống lâm sàng hạ magie máu.
| Trường hợp có xoắn đỉnh, rung thất, hoặc co giật hạ magie | Liều: 2 g MgSO4 tiêm tĩnh mạch chậm trong vài phút. |
| Có triệu chứng | MgSO4 6 g truyền trong 24 giờ, sau đó 3-4 g/ngày trong 5 ngày tiếp theo. |
| Không triệu chứng | Bù đường uống MgCl2 500 mg viên giải phóng chậm, 10-12 viên mỗi ngày. |
| Bệnh nhân suy thận | Không dùng liều bolus. |
Chú ý:
- Cần truyền kéo dài do quá trình vận chuyển magie vào tế bào chậm và bị thải qua nước tiểu một phần. Nếu truyền trong thời gian ngắn sẽ bị thải qua nước tiểu và không đạt được mục tiêu điều trị. Nên truyền kéo dài 8-12 giờ.
- Tuy nhiên, cần lưu ý trong trường hợp có suy thận có thể gây ra tình trạng tăng magie nặng. Giảm liều 50% – 75% và xét nghiệm theo dõi Mg máu.
3.3. RỐI LOẠN CANXI MÁU: HẠ CANXI MÁU & TĂNG CANXI MÁU
3.3.1. Hạ canxi máu
Nồng độ canxi toàn phần huyết thanh bình thường 8,5–10,5 mg/dL (2,12-2,62 mmol/L). Hạ canxi máu khi nồng độ canxi toàn phần huyết thanh < 2,12 mmol/L. Canxi ion có nồng độ bình thường 1,1-1,3 mmol/L (4,4-5,2 mg/dL).
Canxi tồn tại 2 dạng trong máu: gắn với protein (~ 40%) và canxi có khả năng di chuyển qua màng bán thấm (~60%). Dạng gắn với protein không thể di chuyển qua màng bán thấm được, nên trơ về mặt sinh lý. Dạng có thể di chuyển qua màng bán thấm, bản chất gồm 50% là dạng ion thực sự và có hoạt tính sinh học và 10% là dạng liên kết với các anion citrate, phosphate, và lactate.
Cahiệu chỉnh = Caxét nghiệm + 0,8*(4,0 – Albbệnh nhân (g/dL))
Tỷ lệ Ca toàn phần/Ca ion phụ thuộc 2 yếu tố: pH và albumin. pH thấp làm tăng chuyển Ca gắn protein thành Ca ion và gây ra tăng Ca ion tương đối. pH cao làm tăng gắn Ca vào albumin, gây ra giảm Ca ion tương đối, mặc dù Ca toàn phần không đổi. Hạ albumin máu làm giảm Ca toàn phần. Mỗi 1 gam albumin gắn với 0,8 mg canxi ở điều kiện pH sinh lý. Tuy nhiên Ca hiệu chỉnh không tương quan với nồng độ Ca ion có hoạt tính sinh lý ở bệnh nhân hồi sức. Do nhiều yếu tố như các rối loạn kiềm toan, nồng độ acid béo tự do trong máu cao, truyền heparin, bicarbonate, citrate. Do đó khuyến cáo đo trực tiếp Ca ion ở bệnh nhân hồi sức.
a. Nguyên nhân hạ canxi
Bảng 11.17. Nguyên nhân hạ canxi
| Suy cận giápMắc phải:
Sau mổ cắt tuyến cận giáp Bệnh ác tính Bẩm sinh Vô căn |
Rối loạn phân bố– Mất vào mô
• Viêm tụy cấp • Tiêu cơ vân cấp – Tạo phức • Môi trường kiềm • Truyền chế phẩm máu được citrate hóa • Chống đông citrate trong CRRT • Thay huyết tương bằng ly tâm • Truyền bicarbonate điều trị toan chuyển hóa |
| Thiếu vitamin D– Suy dinh dưỡng
– Giảm hấp thu – Bệnh gan – Bệnh thận |
| Thuốc– Cis-platinum
– Bisphosphonates – Plicamycin |
• Phosphate
• Hội chứng ly giải u • Tiêu cơ vân cấp • Thuốc thụt Fleet enemas (chứa phosphate) và các thuốc thụt chứa phosphat khác. – EDTA |
| Phối hợp– Sepsis/SIRS
– Hạ magie – Tổn thương thận cấp |
Chú thích: CRRT: lọc máu liên tục.
Nguyên nhân hạ canxi ở bệnh nhân hồi sức rất hiếm khi có suy cận giáp nguyên phát, mà thường là kết quả của nhiều yếu tố khác như giảm khả năng tiết và hoạt động PTH, thiếu và kháng vitamin D, canxi bị tạo phức, giảm khả năng huy động Ca2+ từ xương. Một số tình trạng thường được ghi nhận tại hồi sức như hạ canxi kèm với các tình trạng Sepsis, SIRS, do làm giảm tiết và hoạt động của PTH và giảm tổng hợp canxitriol. Một ví dụ khác, suy thận có thể gây ra hạ canxi thông qua cơ chế giảm sản xuất canxitriol và tăng phospho máu và tạo phức với canxi ion. Bên cạnh đó, việc sử dụng lọc máu liên tục sẽ làm mất magie và canxi rõ rệt. Một số nguyên nhân khác gây giảm canxi ion như nhiễm kiềm (làm tăng gắn Ca2+ với albumin), dùng thuốc (điều trị co giật, kháng sinh, thuốc cản quang), truyền máu lượng lớn, sepsis, và viêm tụy cấp.
b. Triệu chứng của hạ canxi máu
Hạ canxi máu thường không có triệu chứng và các triệu chứng đặc hiệu cũng khó đánh giá rõ ràng trong tình trạng hồi sức.
Bảng 11.18. Triệu chứng lâm sàng hạ canxi máu
| Triệu chứng thần kinhDị cảm Co giật
Giảm trí nhớ Chuột rút Dấu hiệu Chvostek Dấu hiệu Trousseau Co thắt cơ |
Triệu chứng tim mạch
|
- Các dấu hiệu thần kinh (dị cảm, co giật, giảm trí nhớ) và tim mạch (tụt huyết áp, giảm sức bóp cơ tim, rối loạn nhịp) có thể gặp khi nồng độ Ca2+huyết thanh < 1,0 mmol/L. Các triệu chứng thần kinh cơ của hạ canxi nặng bao gồm có chuột rút, co thắt cơ.
- Dấu hiệu kinh điển của hạ canxi máu bao gồm dấu hiệu Chvostek và dấu hiệu Trousseau, là các dấu hiệu co thắt cơ tiềm ẩn. Dấu hiệu Chvostek là dấu hiệu co các cơ mặt không chủ đích cùng bên khi gõ nhẹ vào dây thần kinh mặt để kích thích dây thần kinh mặt (điểm trước tai, ngay dưới xương gò má). Tuy nhiên, có thể không xuất hiện ở bệnh nhân có hạ canxi mạn tính. Dấu hiệu Trousseau là dấu hiệu co quắp cơ cẳng bàn tay do giảm lưu lượng máu tới tay, xuất hiện ở bệnh nhân hạ canxi máu khi bơm cuff của máy đo huyết áp lên mức 20 mmHg trong 3 phút. Dấu hiệu Trousseau không đặc hiệu và có thể không xuất hiện ở 1/3 bệnh nhân có hạ canxi máu.
- Rối loạn nhịp tim, như nhịp nhanh thất, kéo dài khoảng QT, và có block tim là các biến chứng nguy hiểm của hạ canxi máu. Bên cạnh đó, giảm cung lượng tim và tụt huyết áp, đặc biệt là kháng trị với các thuốc vận mạch và truyền dịch cần được điều trị bù canxi nếu có tình trạng hạ
c. Điều trị hạ canxi
Chỉ định điều trị khi Ca ion < 0,8 mmol/L và có triệu chứng hạ canxi.
Mỗi 200 mg canxi nguyên tố có thể nâng canxi toàn phần huyết thanh lên 1 mg/dL.
Thuốc:
- Canxi gluconate 10% 10 mL (90 mg canxi) tiêm tĩnh mạch chậm từ 5-10 phút, sau đó truyền canxi gluconate (500-1000 mg trong 500ml glucose 5% kéo dài 6 giờ).
- Canxi clorua 10% (272 mg canxi).
Trường hợp hạ Ca nhẹ (canxi ion > 0,8 mmol), bù đường uống. Nhu cầu 1-4 g canxi nguyên tố/ngày, phối hợp thêm vitamin D tăng khả năng hấp thu tại ruột.
- Ngưỡng điều trị bù canxi có nhiều phác đồ khác nhau, nhưng nhiều phác đồ dùng ngưỡng Ca ion < 0,8 mmol/L (3,2 mg/dL) và có triệu chứng hạ canxi là cần được điều trị ở bệnh nhân hồi sức. Điều trị ở bệnh nhân có canxi ion > 0,8 mmol/L và không có triệu chứng thường không cần thiết và có thể gây hại trong một số tình huống như sepsis và giảm oxy tế bào.
- Bù canxi bằng canxi đường tĩnh mạch. Có 2 chế phẩm thường dùng là canxi clorid 10% (chứa 27 mg/mL muối canxi và 1,36 mEq/mL canxi) và canxi gluconate 10% (9 mg/mL muối canxi và 0,46 mEq/mL canxi). Một lượng 200 mg canxi nguyên tố có thể nâng tổng lượng canxi huyết thanh lên 1 mg/dL. Do tiêm tĩnh mạch canxi có tác dụng ngắn, nên có thể phải truyền canxi nếu cần. Canxi clorid không được truyền đường ngoại vi do có thể gây hoại tử mô, viêm tắc tĩnh mạch nếu đường truyền bị chệch
- Bệnh nhân huyết động không ổn định ở hồi sức và có kèm theo hạ canxi máu có thể cải thiện huyết áp và/hoặc tăng cung lượng tim thoáng qua nếu bù Do tác dụng tăng sức bóp cơ tim. Tuy nhiên, có thể làm xấu đi tình trạng thiếu oxy nội bào. Nhưng ở những bệnh nhân có bệnh cảnh hạ canxi và xuất hiện thêm huyết động không ổn định (đặc biệt đã cần vận mạch) thì cần đảm bảo bù đủ canxi.
3.3.2. Tăng canxi máu
Là tình trạng hiếm gặp ở hồi sức. Định nghĩa là tình trạng tăng canxi huyết thanh > 10,4 mg/dL (2,60 mmol/L), thường do tái hấp thu quá mức từ xương. Thường gặp nhất do cường cận giáp và tăng canxi trong bệnh ác tính (ví dụ: đa u tủy xương). Các nguyên nhân ít gặp hơn gồm sarcoidosis, bất động kéo dài, và dùng thuốc (ví dụ: lợi tiểu thiazid).
Tăng canxi nhẹ thường không có triệu chứng. Khi canxi ion > 12 mg/dL có thể có các dấu hiệu lẫn lộn, sảng, các rối loạn tâm thần, và hôn mê. Các dấu hiệu có thể gặp như buồn nôn, nôn, táo bón, đau bụng, giảm nhu động ruột. Các ảnh hưởng trên hệ tim mạch gồm tụt huyết áp, giảm thể tích, khoảng QT ngắn. Tình trạng yếu nặng cơ vân, co giật đã được ghi nhận.
Điều trị gồm có điều trị trực tiếp tình trạng bệnh tiềm ẩn. Truyền dịch Natriclorid 0,9% và lợi tiểu được chỉ định khi canxi tăng trên 14 mg/dL (3,5 mmol/L). Trường hợp đa u tủy xương có thể kết hợp calcitonin và hydrocortisone.
4. RỐI LOẠN THĂNG BẰNG KIỀM TOAN
4.1. ĐỊNH NGHĨA
Nhiễm toan khi pH < 7,35 – Tăng [H+] trong dịch ngoại bào. Nhiễm kiềm khi pH > 7,45 – Giảm [H+] trong dịch ngoại bào.
Rối loạn thăng bằng kiềm toàn gồm: rối loạn nguyên phát và bù trừ.
Bảng 11.19. Hậu quả của rối loạn kiềm toan nặng
| CÁC TẠNG | NHIỄM TOAN (PH < 7,20) | NHIỄM KIỀM (PH > 7,60) |
| Tim mạch | Giảm co bóp cơ tim, giãn tiểu động mạch.Giảm HA trung bình và cung lượng tim
Giảm đáp ứng với vận mạch Tăng nguy cơ rối loạn nhịp |
Co tiểu động mạchGiảm lưu lượng máu vành
Tăng nguy cơ rối loạn nhịp |
| Hô hấp | Tăng thông khí, mệt cơ hô hấp | Giảm thông khí |
| Chuyển hóa | Tăng kali máu | Giảm kali, Ca ion, Mg, PO4 |
| Thần kinh | Rối loạn ý thức | Rối loạn ý thức, co giật. |
Phân tích rối loạn toan kiềm (có thể dùng ứng dụng MDCalc trên điện thoại và web):
Bước 1: Xác định rối loạn tiên phát: pH, PaCO2, HCO3.
Quy tắc 1: Rối loạn chuyển hóa tiên phát khi pH và PaCO2 thay đổi cùng chiều. Quy tắc 2: Rối loạn hô hấp khi PaCO2 cao hơn giá trị ước tính (hỗn hợp).
Quy tắc 3: Rối loạn hô hấp tiên phát khi PaCO2 bất thường và PaCO2 và pH ngược chiều.
Bảng 11.20. Các rối loạn nguyên phát
| RL nguyên phát | Vấn đề | pH | PaCO2 | HCO3 |
| Toan chuyển hóa | Tăng H+ hoặc mất HCO3 | ↓ | ↓ | ↓ ↓ |
| Kiềm chuyển hóa | Tăng HCO3 hoặc mất H+ | ↑ | ↑ | ↑ ↑ |
| Toan hô hấp | Giảm thông khí | ↓ | ↑ | ↑ ↑ |
| Kiềm hô hấp | Tăng thông khí | ↑ | ↓ | ↓ ↓ |
Bước 2: Xác định xem mức độ bù trừ đã phù hợp chưa? (Quy tắc 4: sử dụng bảng)
Bảng 11.21. Mức bù trừ cho các rối loạn toan kiềm
| Rối loạn nguyên phát | Mức bù trừ phù hợp | Thời gian |
| Toan chuyển hóa | PaCO2 = (1,5*HCO3) + 8 ± 2 (Winter -1967)Hoặc ↓PaCO2 = 1,25*ΔHCO3 | 12–24 giờ |
| Kiềm chuyển hóa | ↑PaCO2 = 0,7* ΔHCO3 | 24-36 giờ |
| Toan hô hấp cấp | ↑ HCO3 = 0,1*ΔPaCO2(↓pH = 0,008* ΔPaCO2) | < 6 giờ |
| Toan hô hấp mạn | ↑ HCO3 = 0,4*ΔPaCO2(↓pH = 0,003* ΔPaCO2) | 2–5 ngày |
| Kiềm hô hấp cấp | ↓ HCO3=0,2* ΔPaCO2 (↑pH =0,008*ΔPaCO2) | < 6 giờ |
| Kiềm hô hấp mạn | ↓ HCO3 =0,4* ΔPaCO2 | 2-5 ngày |
Chú ý: Kí hiệu ↑,↓,Δ thể hiện sự thay đổi, ví dụ ΔPaCO2 = PaCO2 đo được – 40mmHg, hay ΔHCO3 = HCO3 – 24.
Bước 3: Xác định rối loạn hỗn hợp kèm theo (có > 1 rối loạn nguyên phát):
- Mức độ bù trừ ít hơn hoặc nhiều hơn so với ước tính:
PaCO2 quá thấp → có thêm kiềm hô hấp
PaCO2 quá cao → có thêm toan hô hấp
HCO3 quá thấp → có thêm toan chuyển hóa
HCO3 quá cao → có thêm kiềm chuyển hóa
- pH bình thường nhưng…
↑PaCO2 + ↑HCO3 → toan hô hấp và kiềm chuyển hóa
↓PaCO2 + ↓HCO3 → kiềm hô hấp + toan chuyển hóa
PaCO2 và HCO3 bình thường, nhưng ↑AG → Toan chuyển hóa tăng AG + kiềm hô hấp.
PaCO2, HCO3 và AG bình thường → Không có rối loạn hoặc toan chuyển hóa non-AG + kiềm hô hấp.
- Không có phối hợp giữa toan hô hấp (tăng thông khí) và kiềm hô hấp (giảm thông khí).
4.2. TOAN CHUYỂN HÓA
Đặc trưng: Giảm HCO3–, phản ánh tăng các acid cố định hoặc tình trạng mất kiềm.
Nguyên nhân
Bảng 11.22. Nguyên nhân gây toan chuyển hóa
| Toan chuyển hóa tăng AG Ghi nhớ (GOLD MARK) | Toan chuyển hóa không tăng AG (Toan chuyển hóa tăng Clo) |
| – G: glycerol– O: Oxoproline
– L: L-lactate – D: D-lactate – M: methanol – A: Aspirin – R: Renal failure (tăng ure máu), Rhabdomyolysis (tiêu cơ vân). – K: Ketoacidosis (rượu, ĐTĐ) |
Tại thận– Giảm thải H+: toan ống thận xa (distal RTA type 1)
– Giảm tái hấp thu HCO3–: toan ống thận gần (proximal RTA type 4) – Mất các anion hữu cơ qua nước tiểu: toan ceton, ngộ độc toluen. Ngoài thận – Mất HCO3 qua tiêu hóa: ỉa chảy, rò tụy. – Truyền dịch nhiều Cl: NaCl, KCl, NH4Cl, CaCl2 |
Chú thích: AG (anion gap): khoảng trống anion; ĐTĐ: đái tháo đường.
Chẩn đoán: Cần đánh giá rối loạn chung như đã trình bày ở trên. Sau đó tiếp tục đánh giá các chỉ số về rối loạn toan chuyển hóa. (có thể dùng ứng dụng MDCalc để hỗ trợ tính toán).
Bảng 11.23. Tiếp cận chẩn đoán toan chuyển hóa.
| Tính khoảng trống Anion (anion gap – AG) = [Na+] – [Cl-] – [HCO3-] | |||
| Anion gap bình thườngTính AG niệu, nếu pH niệu > 6,5 hoặc [Na+] nước tiểu < 20 mmol/L, cần tính OG niệu | Tăng Anion gap(ví dụ: lactate, ceton, ngộ độc rượu) | ||
| AG niệu: âm (Ví dụ: ỉa chảy, truyền NaCl, toan ống thận gần (proximal RTA) –thường hạ phospho máu, tăng ure máu, tăng glucose niệu. | AG niệu: dương Toan ống thận (RTA)Type 1: Kali máu giảm, pH niệu > 5,5
Type 4: Kali máu tăng, pH niệu > 5,5 |
Tính OGOG > 10
mOsm/kg Ví dụ: ngộ độc rượu. |
Tính Δ – ΔToan ceton:
ΔAG – ΔHCO3- Toan lactic: 0,6*ΔAG – ΔHCO3- Nếu Δ – Δ từ -5 đến 5: Chỉ có toan CH tăng AG. Nếu Δ – Δ > 5 mmol/L: Toan chuyển hóa tăng AG và kiềm chuyển hóa. Nếu Δ – Δ < -5 mmol/L: Toan chuyển hóa tăng AG và Toan chuyển hóa non-AG. |
Chú thích: OG: khoảng trống áp lực thẩm thấu.
Xử trí: Cần xử trí nguyên nhân, truyền Nabicarbonate, lọc máu.
4.3. KIỀM CHUYỂN HÓA
Đặc trưng: Tăng nồng độ bicarbonate trong máu.
Nguyên nhân: Được chia thành 2 nguyên nhân: mất acid (qua thận hoặc ngoài thận) và đưa thêm bicarbonate.
Bảng 11.24. Một số nguyên nhân kiềm chuyển hóa thường gặp.
| Giảm thể tích dịch lòng mạch | Tăng thể tích dịch lòng mạch |
| Mất acid qua đường tiêu hóa– Nôn, hút dịch dạ dày
– Ỉa chảy dịch nhiều clo Mất acid qua thận – Lợi tiểu (quai, thiazid) – Hội chứng Bartter – Hội chứng Gitelman – Mất magie – Sau tăng CO2 – Suy tim (giảm thể tích hiệu dụng) – Xơ gan/cổ trướng (giảm thể tích hiệu dụng) |
– Hẹp động mạch thận– U tiết renin
– Cường aldosteron nguyên phát – Hội chứng Cushing – Dùng corticoid – Hội chứng Liddle |
Các nguyên nhân kiềm chuyển hóa có giảm thể tích lòng mạch thường đáp ứng với bù dịch NaCl 0,9%, còn được gọi là kiềm chuyển hóa đáp ứng với clo.
Chẩn đoán: Dựa vào khí máu động mạch.
Nhiễm kiềm có giảm thể tích lòng mạch (đáp ứng với clo): có giảm thể tích dịch và xét nghiệm Clo niệu < 10 mEq/L.
Nhiễm kiềm không giảm thể tích lòng mạch: Clo niệu > 20 mEq/L, hiếm gặp.
Xử trí
Nhiễm kiềm đáp ứng với clo:
- Truyền NaCl 0,9%.
- Acetazolamide 250-500 mg mỗi 8 giờ, khi chức năng thận tốt.
Nhiễm kiềm kháng clo: điều trị nguyên nhân.
4.4. TOAN HÔ HẤP
Đặc trưng: Do giảm thải CO2 ở phổi. Gồm 2 loại: cấp và mạn, dựa trên mức độ tăng HCO3-. Các nguyên nhân gồm:
- Ức chế hệ thần kinh trung ương (thuốc, nhiễm trùng, tổn thương não).
- Bệnh thần kinh cơ (hội chứng Guillain-Barré, bệnh cơ)
- Bệnh phổi: Đợt cấp COPD, hen phế quản, bệnh phổi hạn chế, viêm phổi…
Lâm sàng: kích động, hoa mắt, đau đầu, phù gai thị, ngủ gà, hôn mê, tăng huyết áp, nhịp nhanh, suy tim, rối loạn nhịp.
Chẩn đoán: dựa trên khí máu động mạch.
Xử trí: Xử trí nguyên nhân. Không khuyến cáo dùng Natri bicarbonat.
4.5. KIỀM HÔ HẤP
Đặc trưng: Do thải quá mức CO2 ở phổi (tăng thông khí) hoặc hệ thống ECMO.
Bảng 11.25. Nguyên nhân gây kiềm hô hấp
| Thần kinh trung ương: u não, viêm não màng não | Có thai |
| Tâm lý: đau, vật vã, lo lắng,… | Cường giáp |
| Xơ gan | Giảm oxy: sống ở vùng cao, thiếu máu nặng |
| Bệnh phổi: các tình trạng tạo shunt | Điều chỉnh quá nhanh toan chuyển hóa mạn |
| Thuốc: salicylate, progesteron |
Triệu chứng: chóng mặt, rối loạn cảm giác, tetani, ngất, co giật, rối loạn nhịp.
Chẩn đoán: Dựa trên khí máu động mạch.
Xử trí: Điều trị nguyên nhân. Thường không cần xử trí cấp cứu trừ khi pH > 7,50.
Đối với bệnh nhân có thở máy mode kiểm soát, cần giảm thông khí phút (MV), ước tính điều chỉnh thông khí phút theo công thức:
PaCO2ban đầu × MVban đầu= PaCO2cần đạt × MVcần đạt
Khi giảm MV thì PaCO2 sẽ tăng lên, giảm MV bằng cách giảm tần số và/ hoặc Vt.
Với bệnh nhân thở máy mode hỗ trợ, cần giảm mức hỗ trợ xuống.
4.6. MỘT SỐ ĐẶC ĐIỂM RỐI LOẠN KIỀM TOAN Ở BỆNH NH N COVID-19
Báo cáo ghi nhận rối loạn kiềm toan ở bệnh nhân COVID-19 lên đến 79,7% ở nhóm bệnh nhân nhập viện. Trong đó kiềm chuyển hóa (33,6%), kiềm hô hấp (30,3%), kiềm hỗn hợp (9,4%), toan hô hấp (3,3%), toan chuyển hóa (2,8%) và nhóm có rối loạn hỗn hợp (3,6%).
TÀI LIỆU THAM KHẢO
- Gheorghe G, Ilie M, Bungau S, Stoian AMP, Bacalbasa N, Diaconu CC. Is There a Re- lationship between COVID-19 and Hyponatremia? . Medicina (Kaunas). 2021;57(1):55. Published 2021 Jan 9. doi:10.3390/medicina57010055
- Horacio J. Adrogué, Nicolaos E. Madias. Management of life-threatening acid- base disorders. The New England Journal of Medicine
- Horacio J. Adrogué, Nicolaos E. Madias. Hypernatremia. The New England Journal of Medicine
- Kenrick Berend, Aiko J de Vries, Rijk O.B Gans. Physiological approach to assessment of acid- base disturbances. The New England Journal of Medicine 2014.
- Marc S. Sabatine. Pocket medicine fourth
- Joseph E. Parrillo, R. Phillip Dellinger. Critical care medicine: Principles of Diagnosis and Management in the Adult. Fifth
- Jean-Louis Vincent, Edward Abraham, Frederick Moore, Patrick M. Kochanek, Mitch- ell P. Fink. Textbook of Critical care, 7th Edition.
- Bộ Y Tế. Hướng dẫn chẩn đoán và xử trí hồi sức tích cực.
- Alfano G, Ferrari A, Fontana F, et al. Hypokalemia in Patients with COVID-19. Clin Exp Nephrol. 2021;25(4):401-409. doi:10.1007/s10157-020-01996-4
- Alfano G, Fontana F, Mori G, et al. Acid base disorders in patients with COVID-19 [published online ahead of print, 2021 Jun 11]. Int Urol Nephrol. 2021;1-6. doi:10.1007/ s11255-021-02855-1.
- Berni A, Malandrino D, Parenti G, Maggi M, Poggesi L, Peri A. Hyponatremia, IL- 6, and SARS-CoV-2 (COVID-19) infection: may all fit together?. J Endocrinol Invest. 2020;43(8):1137-1139. doi:10.1007/s40618-020-01301-w.
