Bệnh da liễu
Nám: Nguyên nhân gây nám, chẩn đoán và điều trị
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
Tác giả: Jae Dong Lee
Dịch: Bs. Trương Tấn Minh Vũ
nhathuocngocanh.com – Để tải file PDF của bài viết Nám: Nguyên nhân gây nám, chẩn đoán và điều trị, xin vui lòng click vào link ở đây.
Giới thiệu
Định nghĩa nám
Nám là một tình trạng tăng sắc tố da thường xảy ra ở những vùng da tiếp xúc nhiều với ánh nắng, đặc biệt là mặt. Nám hiếm khi xảy ra trước tuổi dậy thì và thường được thấy ở phụ nữ, đặc biệt là phụ nữ trong độ tuổi sinh đẻ. Nám cũng được thấy ở 10% nam giới. Nám mới thường phát sinh và tình trạng nám hiện có có thể nặng hơn khi mang thai. Các triệu chứng biểu hiện dưới dạng các dát màu nâu với bờ không đều và xuất hiện đối xứng ở vùng da tiếp xúc ánh sáng mặt trời trên mặt, thường được hợp nhất thành một hình dạng lưới. Nám bị tối màu đi bởi ánh sáng mặt trời, trở nên tệ hơn vào mùa hè và cải thiện trong mùa đông, tức là có sự thay đổi theo mùa. Nám phổ biến ở phụ nữ châu Á và gốc Tây Ban Nha sống ở những nơi có ánh nắng mạnh, xảy ra thường xuyên ở bệnh nhân có loại da IV, V và VI theo Fitzpatrick [1].
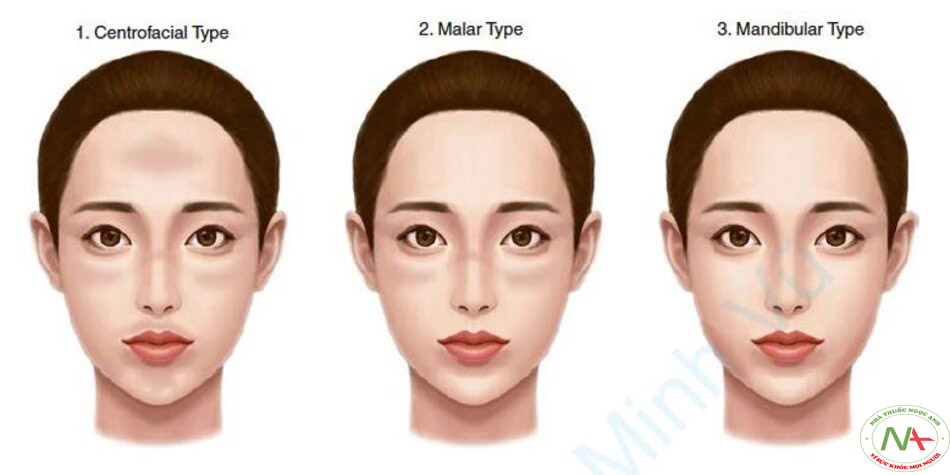
Nám có thể được phân loại thành ba loại theo các kiểu hình trên khuôn mặt: giữa mặt, má và hàm dưới (Hình 12.1). Kiểu hình giữa mặt chiếm 63% trường hợp và ảnh hưởng đến trán, mũi, cằm và môi trên. Kiểu hình ở má chiếm 21% và chỉ giới hạn ở mũi và má. Kiểu hình hàm dưới chiếm 16% các trường hợp và xuất hiện dọc theo hàm dưới. Một kiểu hình mới hơn được gọi là nám ở bên ngoài mặt, có thể xảy ra trên các bộ phận không phải trên mặt, gồm cổ, xương ức và chi trên [1]. Việc phân loại nám theo phân bố dường như không có ý nghĩa về mặt lâm sàng, tuy nhiên, theo kinh nghiệm chúng tôi thấy rằng nám dưới mắt có khả năng kháng trị.
Nám cũng có thể được phân thành ba loại theo mô học, theo độ sâu của sắc tố melanin: biểu bì, bì và hỗn hợp. Đèn Wood dùng để phân biệt giữa nám biểu bì và nám bì, nám biểu bì nổi lên trong khi nám bì thì không. Nám biểu bì đáp ứng tốt hơn với điều trị tại chỗ so với nám bì [1].
Lee và cộng sự đã nghiên cứu 411 bệnh nhân bị nám tại năm bệnh viện đại học ở Hàn Quốc [3]. Nám được phân thành ba loại. Các bờ bình thường với màu nâu được phân loại là nám biểu bì. Các bờ không đều với màu hơi xanh được phân loại là nám bì. Khi có cả hai loại biểu bì và bì thì được phân loại là nám hỗn hợp. Theo nghiên cứu này, 36% (145 bệnh nhân) có nám biểu bì, 64% (235 bệnh nhân) có nám hỗn hợp, nhưng không có nám bì. Kar và cộng sự thực hiện sinh thiết trên bệnh nhân nám ở Ấn Độ [4]; 51,66% (31 bệnh nhân) là loại biểu bì, 48,33% (29 bệnh nhân) là loại hỗn hợp và không có loại bì. Kết quả tương tự như nghiên cứu ở trên. Dựa trên kết quả của cả hai nghiên cứu, tôi cho rằng nám hỗn hợp chiếm tỷ lệ cao trong tổng số bệnh nhân bị nám, do đó, việc điều trị nám thường khó và tốn nhiều thời gian. Tôi cũng nghĩ rằng không có nhiều trường hợp nám bì.
Chẩn đoán phân biệt nám
Chẩn đoán phân biệt đối với nám bao gồm bớt Ota, bớt Hori (ABNOM), tăng sắc tố da do thuốc, hồng ban rối loạn sắc tố (EDP), lichen planus sắc tố, ranh giới giữa vết bỏng da và vùng da sáng hơn sau đó, lichenoid bùng phát do thuốc, bệnh hắc tố Riel, tăng sắc tố sau viêm (PIH), rối loạn sắc tố trưởng thành, tăng sắc tố quanh hốc mắt, acanthosis nigricans, tàn nhang, đốm nâu, tăng sắc tố ngoại sinh, v.v. [5].
Rodriques và cộng sự đã đề cập đến hai đặc điểm của nám giúp phân biệt với các rối loạn sắc tố khác [5]. Đầu tiên, nám xuất hiện ở bờ ổ mắt và hiếm khi ở vùng hàm dưới. Thứ hai, nám không tối màu như tăng sắc tố do thuốc hoặc hồng ban rối loạn sắc tố (EDP), cũng không có màu xám như xi măng. Tuy nhiên, trên thực tế, rất khó để chẩn đoán phân biệt tình trạng nám.
Các vấn đề về nám da
Điều trị nám bằng laser có thể gây ra ba vấn đề. Đầu tiên, nám da tiềm ẩn có thể chuyển thành nám thực sự. Thứ hai, tình trạng nám da hiện tại có thể trở nên tồi tệ hơn. Thứ ba, sau khi điều trị bằng laser, tình trạng nám da có thể xảy ra ngay cả ở những vùng không được chiếu tia laser. Chúng tôi sẽ xem xét lần lượt ba vấn đề này.
Đầu tiên, khi IPL được dùng phổ biến trong phòng mạch tư nhân, các sắc tố sau IPL tương tự như nám da thường được ghi nhận. Negishi và cộng sự đã nghiên cứu hiện tượng này bằng cách so sánh ảnh bình thường với ảnh chụp bằng máy ảnh tia UV [6]. Một khảo sát trên 223 phụ nữ Nhật Bản cho thấy 63 (28,3%) bị nám mà không thể nhìn thấy dưới ánh sáng bình thường nhưng có thể nhìn thấy dưới tia UV. Đó là, các vết nám tiềm ẩn đã được quan sát thấy. Ngoài ra, trên lâm sàng cho thấy ở những bệnh nhân bị nám tiềm ẩn được phát hiện bằng tia UV, nám mới xuất hiện trên cùng vị trí sau IPL. Trong quá trình điều trị bằng laser, điều quan trọng cần lưu ý là mặc dù chúng ta không thể nhìn thấy tình trạng nám trên mặt của bệnh nhân khi nhìn bằng mắt thường, nhưng luôn có khả năng có tình trạng nám tiềm ẩn.
Thứ hai, khi điều trị nám bằng các thông số laser đã được biết có hiệu quả đối với các rối loạn sắc tố khác, ban đầu nám có vẻ biến mất nhưng trở nên sẫm màu hơn theo thời gian, sau đó với một lần điều trị bằng laser khác, nó có thể biến mất tiếp và trở lại sẫm màu hơn, như vòng luẩn quẩn. Nếu tình trạng nám không được chẩn đoán chính xác và điều trị giống như một chứng rối loạn sắc tố khác, tình trạng nám có thể trở nên tồi tệ hơn. Vì vậy, chẩn đoán chính xác rất quan trọng trong điều trị nám.
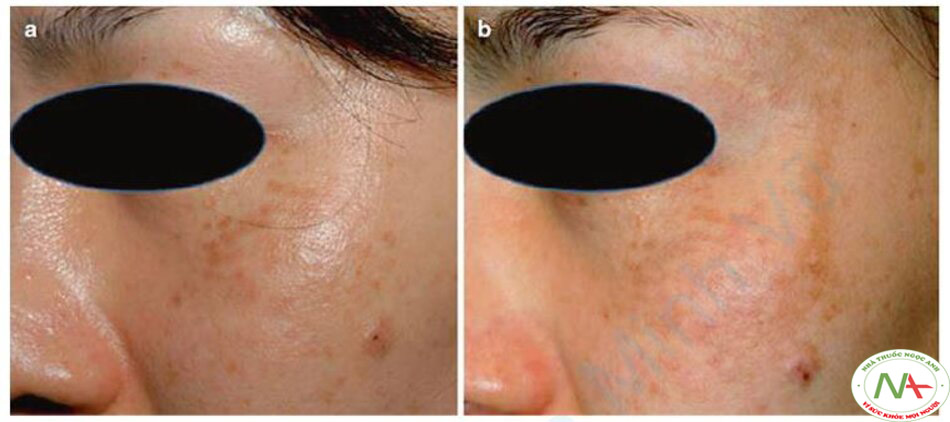
Thứ ba, sau khi điều trị bằng laser, tình trạng nám có thể xảy ra ngay cả ở những vùng không được chiếu tia laser. Lee và cộng sự đã điều trị cho một bệnh nhân nữ 37 tuổi bị ABNOM bằng laser Q-switched Nd: YAG 1064 nm năm lần, cách nhau 4 tuần [7]. Một tháng sau nám được ghi nhận xung quanh ABNOM. Nám xuất hiện ở những vùng không được chiếu tia laser (Hình 12.2).
Ba vấn đề đã được xem xét ở trên — Nám tiềm ẩn chuyển thành nám thực sự. Tình trạng nám hiện tại ngày càng nặng hơn. Nám mới xuất hiện sau khi điều trị các rối loạn sắc tố khác như ABNOM — có thể xảy ra trong quá trình điều trị bằng laser ở phòng mạch tư nhân. Những tình huống này đã gây khó khăn cho cả bác sĩ và bệnh nhân. Vì vậy, trước đây laser là chống chỉ định trong điều trị nám.
Mặc dù không được đề cập rõ ràng trong các tài liệu, tôi tin rằng các melanocyte được kích hoạt là vấn đề gốc cho những nguyên nhân này.
Nguyên nhân và học thuyết về nám
Lý do tại sao điều này xảy ra? Cơ chế bệnh sinh của nám vẫn chưa được biết rõ, nhưng các melanocyte có hoạt tính sinh học, nguyên nhân di truyền, ảnh hưởng của nội tiết tố và tia UV được biết là quan trọng [8]. Tôi đặc biệt tin rằng các melanocyte được kích hoạt là vấn đề gốc. Các nguyên nhân khác có thể bao gồm thuốc tránh thai, liệu pháp thay thế estrogen, rối loạn chức năng tuyến giáp hoặc buồng trứng nhẹ, khối u buồng trứng, mỹ phẩm, dinh dưỡng, nhiễm độc ánh sáng, thuốc gây dị ứng ánh sáng và thuốc động kinh [8].
Tuy nhiên, các tài liệu gần đây đã công bố trái ngược với các nguyên nhân gây ra nám hiện có. Đầu tiên, một nghiên cứu trên 324 bệnh nhân tại 12 cơ sở y tế ở 9 quốc gia cho thấy chỉ có khoảng 50% bệnh nhân bị nám có tiền sử gia đình [9]. Nám thường xuất hiện ở độ tuổi 20 và 30, nhưng một số xuất hiện ở độ tuổi 40 (14%) và 50 (6%). Nám xuất hiện sớm ở làn da sáng màu hơn trong khi xuất hiện muộn ở loại da tối màu hơn (loại da Fitzpatrick loại V, VI), một số thậm chí sau khi mãn kinh. Như vậy, nhiều khả năng nguyên nhân chủng tộc là nguyên nhân gây nám da hơn nguyên nhân gia đình. Về tác động của nội tiết tố, chỉ có 20% bệnh nhân bị nám xuất hiện nám khi mang thai và các thuốc tránh thai có ảnh hưởng nhỏ đến sự xuất hiện của nám. Và mặc dù bức xạ tia UV được biết đến là nguyên nhân chính gây tái phát nám, nhưng sự tái phát nám đã được ghi nhận ở nhiều bệnh nhân nám có bôi kem chống nắng kỹ lưỡng. Gần đây có báo cáo rằng ánh sáng nhìn thấy chứ không phải là tia cực tím (UVB) là một nguyên nhân khác làm tăng sắc tố da, đặc biệt là ở loại da Fitzpatrick IV – VI. Do đó, có những lập luận cho rằng kem chống nắng có tác dụng ngăn ngừa hạn chế và kem chống nắng có màu (như kem BB) ngăn chặn ánh sáng nhìn thấy có thể hiệu quả hơn trong việc ngăn ngừa nám tái phát.
Điều thú vị là mỹ phẩm là một trong những nguyên nhân gây ra nám. Kenichirou Kasai, tác giả của “Skin spots treatment clinics,” cho rằng nguyên nhân của nám da là do “sự phá vỡ các hàng rào da gây ra bởi quá trình kích thích mãn tính (chà xát quá nhiều)” [10]. Nói cách khác, có giả thuyết cho rằng nám xảy ra theo cơ chế giống như PIH để bảo vệ da khi hàng rào bảo vệ da bị phá vỡ do quá trình kích thích mãn tính do mỹ phẩm gây ra. Kasai, một bác sĩ y khoa Nhật Bản hành nghề tư nhân, đã kiểm tra các bệnh nhân bị nám, và phát hiện ra các xu hướng thú vị (kích thích mãn tính) ở các bệnh nhân bị nám. Ông quan sát thấy rằng luôn có “hàng rào da bị phá hủy” ở vùng tổn thương nám và không có “hàng rào da bị phá hủy” ở vùng không bị nám. Ngoài ra, người ta quan sát thấy rằng khi thực hiện các biện pháp làm giảm sự phá vỡ hàng rào da, nám da sẽ thuyên giảm và khi thực hiện các biện pháp làm hàng rào da trở nên tệ hơn thì tình trạng nám cũng trở nên tồi tệ hơn. Ngoài ra, độ tuổi xuất hiện nám cũng trùng với độ tuổi mà người ta “dùng mỹ phẩm”. Không có hiện tượng nám da ở trẻ em hay người già, là những người không dùng mỹ phẩm.
Kasai cho rằng việc trang điểm và tẩy trang hàng ngày là nguyên nhân chính khiến hàng rào bảo vệ da bị phá hủy. Ngoài ra, việc bôi và tẩy các loại mỹ phẩm khác nhau để che giấu vết nám, càng phá hủy hàng rào bảo vệ da và khiến tình trạng nám trở nên trầm trọng hơn. Do đó, lý do mà nhiều vấn đề về da (ví dụ, viêm da tiếp xúc dị ứng, ban đỏ, bong tróc da, v.v.) thường gặp ở bệnh nhân nám có thể được giải thích là do hàng rào da bị phá hủy. Vì lý do này, Kasai suy đoán rằng các phương pháp điều trị nám tại chỗ có thể gây ra các triệu chứng kích ứng và tác dụng phụ thường xuyên.
Tuy nhiên, vì những suy đoán này chỉ là giả thuyết dựa trên những quan sát đơn giản, Kasai cho biết anh đã xuất bản một cuốn sách có tên “Skin spots treatment clinics” với hy vọng rằng các thế hệ tương lai sẽ xác nhận rằng giả thuyết là đúng. Bây giờ chúng ta sẽ xem xét các tài liệu khác nhau để xem liệu giả thuyết của Kasai có đúng hay không, tức là liệu sự phá hủy hàng rào bảo vệ da do kích thích mãn tính có thể là nguyên nhân gây ra nám da hay không.
Bệnh học nám
Để tìm hiểu nguyên nhân gây nám da, chúng ta sẽ điểm qua các đặc điểm mô học của nám trong các nghiên cứu khác nhau.
Grimes và cộng sự so sánh kiểm tra mô học của vùng da bị nám và vùng da bình thường xung quanh ở 21 bệnh nhân bị nám [11]. Kết quả cho thấy có sự thâm nhiễm nhẹ bạch cầu lympho ở 75% các vùng tăng sắc tố. Các vùng tăng sắc tố cho thấy sự lắng đọng của melanin tăng lên ở lớp biểu bì và lớp bì trong tất cả các trường hợp. Có sự gia tăng có ý nghĩa thống kê về hàm lượng của melanin biểu bì. Không có sự gia tăng số lượng melanocyte trong các vùng da tăng sắc tố. Tuy nhiên, các melanocyte trong các vùng tăng sắc tố là các melanocyte lớn hơn, nhuộm đậm với các đuôi gai nổi bật. Kính hiển vi điện tử cho thấy nhiều melanosomes hơn trong keratinocyte, melanocyte và đuôi gai ở vùng da bị nám so với vùng da không bị nám. Số lượng đuôi gai trên mỗi melanocyte tăng lên so với da bình thường (da bình thường 5,28 ± 1,85, da nám 7,55 ± 2,53, p <0,05). Kết quả của nghiên cứu này cho thấy rằng nám là hậu quả của việc các melanocyte “tăng hoạt động” với sự gia tăng tạo melanin, dẫn đến tăng melanin biểu bì và melanin lớp bì.
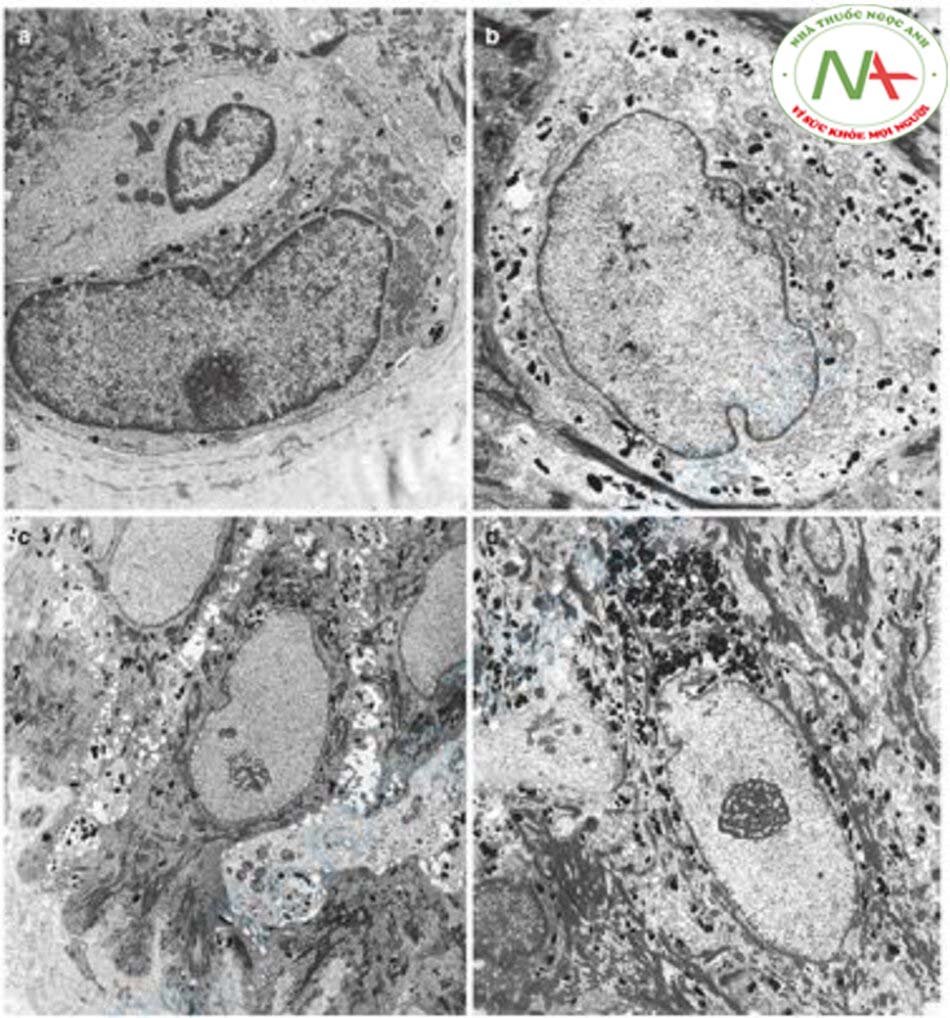
Kang và cộng sự so sánh kết quả kiểm tra mô học của vùng da bị nám và vùng da bình thường xung quanh ở 56 bệnh nhân bị nám Hàn Quốc [12]. Kết quả cho thấy, hắc tố melanin được gia tăng đáng kể ở lớp biểu bì, đặc biệt là ở lớp đáy. Ngoài ra, sự gia tăng có ý nghĩa thống kê tình trạng solar elastosis được ghi nhận ở da nám so với da bình thường. Kết quả hiển vi điện tử cho thấy các melanocyte trong da nám có nhiều ti thể, bộ máy Golgi, mạng lưới nội chất thô và ribosome hơn các melanocyte bình thường (Hình 12.3). Nói cách khác, melanocyte ở vùng da bị nám là “melanocyte kích động” hoạt động nhiều hơn bình thường để tạo ra sắc tố melanin và thực sự tạo ra nhiều melanosome hơn.
Kang và cộng sự quan sát nám da thông qua kính hiển vi tiêu điểm phản xạ (RCM) và so sánh kết quả với mô học [13]. Kết quả như sau. Đầu tiên, so với da bình thường, da nám có sự gia tăng sắc tố melanin và các gờ rete bị phẳng. Các gờ rete phẳng là hiện tượng được thấy khi da lão hóa. Thứ hai, số lượng đuôi gai trên mỗi melanocyte được tăng lên trong các melanocyte được kích hoạt. Thứ ba, các melanocyte được xem như là các tế bào bị rơi từ lớp biểu bì xuống lớp bì (melanocyte nhô ra ngoài). Thứ tư, melanophages được quan sát thấy ở lớp bì. Thứ năm, có sự gia tăng đáng kể trong tình trạng solar elastosis và các mạch máu ở lớp bì, đây là dấu hiệu của sự lão hóa và viêm nhiễm. Cuối cùng, melanophages được tìm thấy ở lớp bì, nhưng chỉ ở một phần da bị nám. Sự phân bố rất không đồng nhất khi quan sát bằng kính hiển vi.
Các nghiên cứu gần đây về nám
Bây giờ chúng ta sẽ xem xét một số nghiên cứu gợi ý các nguyên nhân gây ra nám.
Noh và cộng sự đã khảo sát các đặc điểm viêm của nám [14]. 197 phụ nữ bị nám đã hoàn thành một bảng câu hỏi liên quan đến các yếu tố kích hoạt hoặc làm trầm trọng thêm. Những trường hợp này được chia thành các nhóm “không viêm” và “viêm”. Bảng câu hỏi đã kiểm tra 31 yếu tố bao gồm các yếu tố làm trầm trọng thêm và các yếu tố phản ứng viêm. Các phản ứng viêm được phân thành bảy loại: ngứa / cảm giác châm chích, khô, ban đỏ/ giãn mạch (Bảng 12.1). Nếu bệnh nhân có hơn năm trong số bảy phản ứng, họ được xếp vào nhóm “viêm”.
Bảng 12.1 Mục phản ứng viêm trong bảng câu hỏi.
| Cảm giác ngứa / châm chích |
|
| Khô |
|
| Ban đỏ/giãn mạch |
|
Trong số 197 đối tượng, 50 bệnh nhân (25,4%) được xếp vào nhóm viêm. Sinh thiết cho thấy nhóm viêm có sự phá vỡ màng đáy, gờ rete phẳng, tăng sắc tố lớp đáy, thâm nhiễm tế bào viêm và tình trạng solar elastosis có ý nghĩa thống kê so với nhóm không viêm. Hóa mô miễn dịch cho thấy tế bào melanophages CD68+ và tế bào mast CD117+ (tế bào viêm) và bạch cầu LCA+ đã tăng lên đáng kể trong nhóm viêm. Do đó, Noh cho rằng viêm nhiễm nên được coi là nguyên nhân chính gây ra nám, như tia UV và hormone, vốn đã được coi là nguyên nhân chính gây ra nám. Noh và cộng sự cũng có ý kiến cho rằng nên chia nám da thành nám viêm và nám không viêm và cách điều trị đối với hai loại nám này cũng khác nhau.
Kang và cộng sự thu mẫu da mặt có tổn thương và không có tổn thương của 52 phụ nữ Hàn Quốc bị nám [15]. Phân tích hóa mô miễn dịch và phản ứng chuỗi polymerase phiên mã ngược (RT-PCR) được thực hiện để xác định sự biểu hiện của yếu tố tế bào gốc (stem cell factor, SCF) và c-kit trong bệnh nám. SCF được biết đến như một cytokine để tạo hắc tố melanin. SCF được quan sát thấy trong các tế bào sừng ở lớp biểu bì và trong các nguyên bào sợi ở lớp bì.
- SCF của lớp bì là 0,014 ± 0,012 ở da nám và 0,005 ± 0,004 ở da bình thường. Tức là, SCF của lớp bì tăng lên ở da nám (p <0,001). SCF của lớp biểu bì là 0,48 ± 0,11 ở da nám và 0,43 ± 0,19 ở da bình thường, không có ý nghĩa thống kê (p = 0,5).
- C-kit của biểu bì là 0,14 ± 0,017 ở da nám và 0,08 ± 0,06 ở da bình thường. Tức là c-kit tăng lên ở lớp biểu bì của da nám (p <0,005). Ngoài ra, nồng độ c-kit trên một đơn vị diện tích của lớp biểu bì là 25.375 ± 1023 ở da nám và 18.124 ± 1044 ở da bình thường. Tức là, nồng độ c-kit tăng lên có ý nghĩa thống kê trong lớp biểu bì của da nám (p <0,005). Tuy nhiên, không có sự khác biệt về nồng độ c-kit trong lớp bì của da nám và da bình thường, lần lượt là 3,13 ± 6,0 và 2,75 ± 4,8 cm-1 ở da nám và da bình thường.
Nói cách khác, melanin sản xuất bởi SCF được quan sát thấy trong các nguyên bào sợi ở lớp bì. Việc phát hiện ra SCF trong lớp bì có liên quan đến tình trạng viêm. Các nguyên bào sợi ở lớp bì được biết là tiết ra SCF để phản ứng với tình trạng viêm. Ngược lại, c-kit, thụ thể cho SCF, chỉ được tìm thấy ở lớp biểu bì, không phải lớp bì. Kết luận, có thể giả định rằng SCF tăng lên ở lớp bì do viêm lớp bì và liên kết với c-kit của tế bào sừng biểu bì và gây ra tạo melanin ở biểu bì.
Gần đây, các nguyên bào sợi lão hoá được báo cáo là có liên quan đến nám cũng như đốm nâu. Nguyên bào sợi khi lão hoá được biết là tiết ra nhiều protein liên quan đến lão hóa da (skin aging-associated secreted proteins, SAAP) hơn nguyên bào sợi bình thường. SAAP không chỉ bao gồm các yếu tố được tiết ra để điều chỉnh chất nền ngoại bào mà còn bao gồm cytokine tạo hắc tố melanin tạo nên các sắc tố như yếu tố tế bào gốc (SCF), yếu tố tăng trưởng tế bào sừng (keratinocyte growth factors, KGF) và yếu tố tăng trưởng tế bào gan (hepatocyte growth factors, HGF). Kim và cộng sự thu mẫu da mặt có tổn thương và không có tổn thương của 38 phụ nữ bị nám và kiểm tra tế bào bằng máy làm lão hóa p16INK4A [16]. Kết quả cho thấy không có sự khác biệt về số lượng tế bào p16INK4A ở lớp biểu bì của da nám và da bình thường, ngược lại số lượng tế bào ở lớp bì của da nám cao hơn của da bình thường (5,58 ± 4,55 so với 2,05 ± 1,71, p <0,001). Đặc biệt, hầu hết các tế bào tập trung ở lớp bì nông gần lớp nối biểu bì-bì chứ không phải lớp bì sâu. Tức là trong nám, chúng ta có thể thấy các tế bào lão hoá được tích tụ ở lớp bì. Để loại bỏ các nguyên bào sợi lão hoá, Kim và cộng sự đã dùng kim RF lưỡng cực xâm lấn (SYLFIRM ™, Viol, Gyeonggi, Hàn Quốc) trên ba bệnh nhân bằng phương pháp lặp lại và so sánh kết quả. Các bệnh nhân được điều trị 5 lần cách nhau 2 tuần với mức độ 2, độ sâu của kim 1.5 mm, với đầu 25 kim cách điện ở 2 MHz. Kết quả cho thấy nám cải thiện về mặt lâm sàng và cải thiện giá trị độ sáng (54,67 ± 6,20 so với 60,87 ± 4,32). Về mặt mô học, số lượng tế bào p16INK4A giảm và tăng procollagen-1 liên quan đến giảm sắc tố biểu bì. Sắc tố biểu bì do nhuộm Fontana-Masson cũng giảm.
Dựa trên kết quả của hai nghiên cứu này, có thể giả định rằng tình trạng viêm lớp bì và nguyên bào sợi lão hoá tạo nên sắc tố biểu bì. Cũng có thể giả định rằng các mô biểu bì và bì đều tham gia vào quá trình sản xuất sắc tố biểu bì.
Kim và cộng sự đã khảo sát yếu tố tăng trưởng nội mô mạch máu (vascular endothelial growth factor, VEGF), yếu tố tạo mạch chính của da ở bệnh nhân nám [17]. Đầu tiên, giá trị a* cho thấy mức độ ban đỏ được đo bằng máy đo màu. Thứ hai, vùng nám và vùng bình thường được so sánh bằng sinh thiết ở 50 bệnh nhân nữ Hàn Quốc bị nám. Thứ ba, kháng nguyên liên quan đến yếu tố VIIIa và VEGF được đo bằng hóa mô miễn dịch. Kết quả như sau. Giá trị a* ở má phải và trái của da bình thường lần lượt là 10,24 ± 1,35 và 10,53 ± 1,73, giá trị a* ở má phải và trái của da nám lần lượt là 12,92 ± 1,96 và 12,78 ± 2,19. Giá trị a* cao hơn ở da bị nám (p <001). Ngoài ra so với da thường, da nám có độ dày mạch máu (16,28%), mật độ mạch máu (33,89%), và diện tích mạch máu (68,75%) cao hơn. Số lượng mạch máu và mức độ hình thành sắc tố nám có mối tương quan có ý nghĩa thống kê. Cuối cùng, so sánh diện tích nhuộm trên một đơn vị diện tích biểu bì của VEGF cho thấy da bình thường là 0,137 ± 0,132 và da nám là 0,270 ± 0,237, cho thấy nồng độ VEGF cao hơn (p = 0,034). Kim và cộng sự đề xuất các ý kiến sau bằng cách phân tích các kết quả trên. Tăng cường tạo mạch là một đặc điểm đặc trưng của quá trình lão hóa, vì vậy nám có thể được coi không chỉ là một rối loạn sắc tố biểu bì mà còn là một kiểu hình độc đáo của tổn thương do ánh sáng [17]. Như vậy, điều trị nám không chỉ cần các phương pháp điều trị sắc tố mà còn phải điều trị chống lão hóa, chống tạo mạch.
Hernadez-Barrera và cộng sự đã đánh giá các tế bào mast và vùng bị solar elastosis trong sinh thiết của 27 bệnh nhân nám bằng cách sử dụng phân tích hình ảnh có sự hỗ trợ của máy tính [18]. Da nám có nhiều vật chất đàn hồi hơn so với da thường (13,3 ± 2,8% so với 10,2 ± 2,9%, p <0,001). Tế bào mast ưu thế hơn ở vùng solar elastosis của da bị nám (173 ± 57% so với 145 ± 57%, p = 0,04). Nghiên cứu này cho thấy rằng solar elastosis được thấy ở lớp bì và các tế bào mast cũng tăng lên, như trong Sect. 12.3.1. Solar elastosis được biết đến có nguyên nhân chủ yếu là lão hoá do ánh sáng, vì vậy có thể coi quá trình lão hoá do ánh sáng đóng một vai trò quan trọng trong việc xuất hiện nám. Trong nghiên cứu trên, hiện tượng tăng mạch máu cũng được cho là do lão hoá do ánh sáng. Tuy nhiên, tôi nghĩ rằng solar elastosis và sự gia tăng các mạch máu trong nám không chỉ do tia UV gây ra mà còn do lớp bì bị tổn thương bởi nhiều kích ứng và viêm khác nhau.
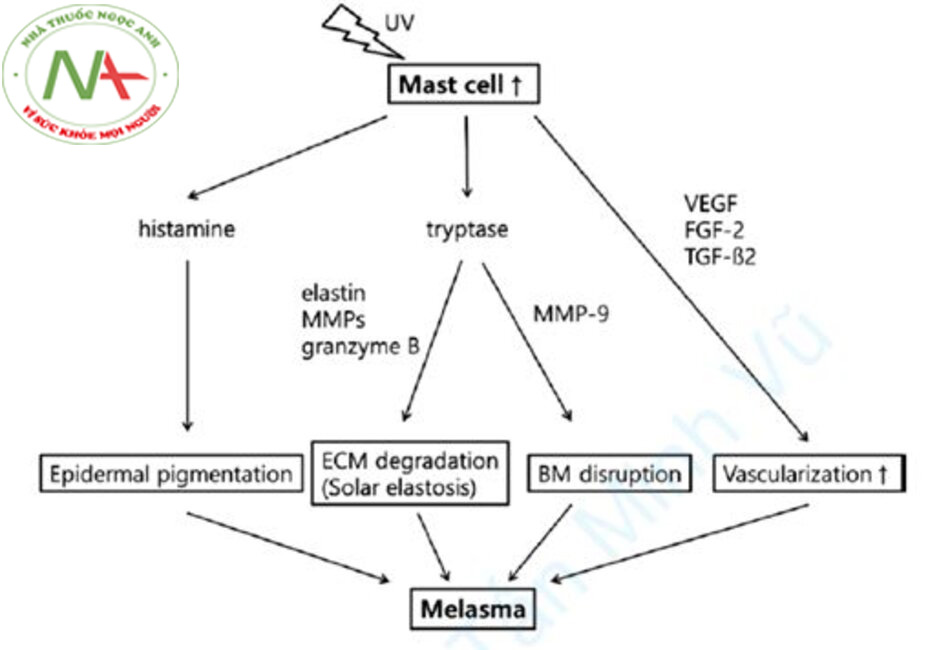
Vai trò của các tế bào mast trong tình trạng nám vẫn chưa được biết đến, nhưng một số nghiên cứu đã chỉ ra rằng histamine có vai trò trong quá trình hình thành hắc tố melanin [19, 20]. Nói cách khác, tia UV làm tăng tiết histamine trong tế bào mast và histamine thúc đẩy sự tăng sinh và di cư của melanocyte. Có một nghiên cứu về mối quan hệ giữa các tế bào mast và quá trình lão hoá do ánh sáng, cho thấy rằng có sự gia tăng đáng kể các tế bào mast trong da lão hoá do ánh sáng. Do đó, một số nghiên cứu coi vai trò của các tế bào mast là quan trọng trong nám da, Hình 12.4 [20].
Chức năng hang rào bị khiếm khuyết và mất kiểm soát sắc tố
Lee và cộng sự so sánh vùng da tổn thương và vùng quanh da bình thường của 16 bệnh nhân bị nám [21]. Độ ẩm của lớp sừng ở da tổn thương cao hơn đáng kể so với da bình thường xung quanh. Không có sự khác biệt đáng kể giữa da tổn thương và da bình thường về mức độ mất nước qua biểu bì (transepidermal water loss, TEWL). Tuy nhiên, tỷ lệ TEWL sau khi hàng rào da xáo trộn cao hơn đáng kể ở da tổn thương và tốc độ phục hồi hàng rào bị trì hoãn đáng kể (Hình 12.5). Sinh thiết được thực hiện trên 11 trong số 16 bệnh nhân, và lớp sừng ở vùng da nám mỏng hơn so với da bình thường (nám, 10,4 ± 2,9 μm; bình thường, 14,5 ± 5,5 μm, p = 0,052). Hơn nữa, điều này có tương quan với tỷ lệ phục hồi hàng rào (hệ số tương quan, 0,721). Sáu trong số 11 bệnh nhân được làm sinh thiết cho thấy thụ thể alpha (PPAR-α) kích hoạt peroxisome thấp hơn, một yếu tố quan trọng đối với chuyển hóa lipid.
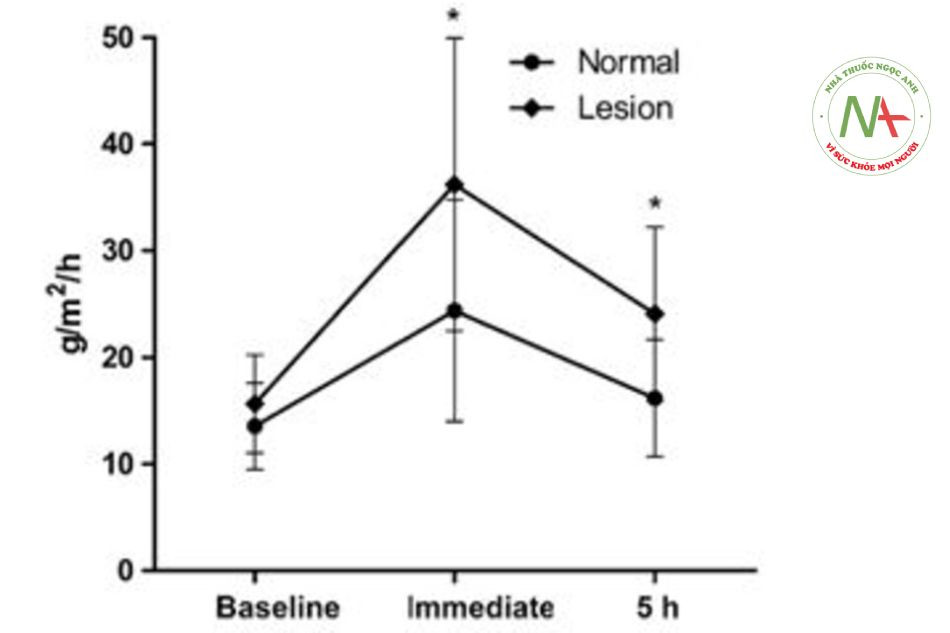
Các nghiên cứu trước đó cho thấy rằng chức năng hàng rào bảo vệ của da bị nám bị suy giảm, đặc biệt là tỷ lệ phục hồi hàng rào.
Shin và cộng sự báo cáo một case report của hai bệnh nhân có phát hiện mô học bất thường [22].
Bệnh nhân đầu tiên cho thấy các phát hiện mô học của các melanocyte hoặc keratinocyte nhô vào lớp bì. Bệnh nhân thứ hai có biểu hiện tăng melanocyte lớp bì, tức là melanocyte hiện diện ở lớp bì, giống như bớt Ota hoặc ABNOM. Tuy nhiên, không giống như các melanocyte nằm ở độ sâu 1,3 ± 0,1 mm trong bớt Ota, các melanocyte của bệnh nhân này nằm ở độ sâu 0,35 mm, rất nông hơn khi so sánh. Kết quả mô học kết hợp của hai bệnh nhân cho thấy phơi nắng kéo dài biến các melanocyte biểu bì thành các melanocyte lơ lửng, cuối cùng rơi vào lớp bì, dẫn đến tăng melanocyte lớp bì. Do đó, các tác giả của bài báo này kết luận rằng dựa trên những phát hiện mô học này, cần có các phương pháp điều trị khác nhau cho biểu bì, bì và màng đáy.
Torres-Alvarez và cộng sự đánh giá các tổn thương nám và so sánh chúng với da xung quanh và da được bảo vệ khỏi ánh sáng [23]. Họ đã lấy mẫu từ da bị tổn thương và được bảo vệ khỏi ánh sáng (mông) ở 24 bệnh nhân (nhóm A). Ở 24 bệnh nhân khác, họ lấy mẫu sinh thiết da tổn thương và da xung quanh (cách vết nám 10 mm) (nhóm B). Ở nhóm A, kiểm tra mô học bằng phương pháp nhuộm Periodic acid-Schiff (PAS) cho thấy ba trong số 24 bệnh nhân không có màng đáy (12,5%) và 87,5%, màng đáy bị thiếu hoặc bị vỡ một phần. Tỷ lệ mất màng đáy trên mỗi lần sinh thiết là 25,85 ± 11%. Ở nhóm B, sự thiếu hoàn toàn màng đáy được quan sát thấy ở 3 bệnh nhân (12,5%). Ở da nám, 95,8% mô có biểu hiện mất màng đáy, cao hơn vùng da xung quanh (58,3%). Ngoài ra, mất màng đáy trên mỗi mô là 23 ± 2%, cao hơn có ý nghĩa thống kê so với vùng da bình thường xung quanh (15 ± 7%) (p <0,002) (Hình 12.6). Hóa mô miễn dịch của anti- collagen IV cho thấy tỷ lệ mất màng đáy ở da nám là 83%, cao hơn da bình thường (66%) (Hình 12.7). Ngoài ra, tỷ lệ mất màng đáy trên mỗi mô ở da nám là 19,3 ± 14,4%, cao hơn có ý nghĩa thống kê so với da bình thường (10 ± 14,8%) (p <0,054).
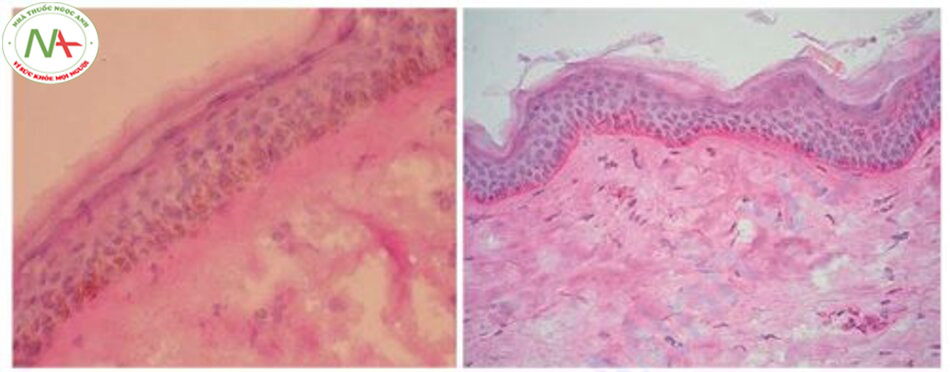
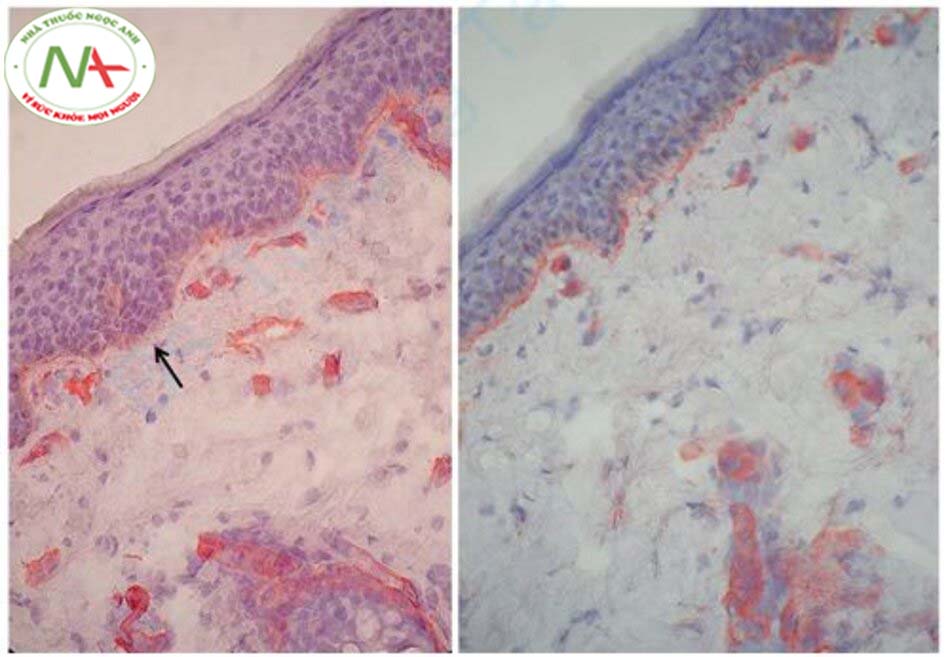
Mất kiểm soát sắc tố là một hiện tượng mô học của sự tích tụ melanin ở lớp bì nông [24]. Bình thường, không có sắc tố ở lớp bì. Lý do tích tụ melanin ở lớp bì có liên quan đến sự tổn thương lớp đáy của biểu bì và màng đáy. Do lớp đáy bị viêm, lớp đáy và màng đáy trở nên bị tổn thương và các melanocyte hoặc keratinocyte có melanin rơi vào lớp bì. Về mặt mô học, melanocyte và melanophage (melanosomes được thực bào bởi đại thực bào) được quan sát thấy ở lớp bì.
Trong các nghiên cứu trước đó, sự mất kiểm soát sắc tố cũng được thấy trong bệnh nám. Nám có thể được phân thành ba loại theo mô học, theo độ sâu của sắc tố melanin: biểu bì, bì và hỗn hợp. Xem xét tình trạng mất kiểm soát sắc tố ở bệnh nám, tôi suy đoán rằng nám ban đầu có thể chỉ xuất hiện ở loại biểu bì và sau đó tiến triển thành loại hỗn hợp hoặc bì do mất kiểm soát sắc tố. Đây có lẽ là lý do tại sao nám biểu bì và hỗn hợp lại phổ biến hơn nám lớp bì. Ngoài ra do lớp màng đáy bị tổn thương và mất kiểm soát sắc tố nên việc điều trị nám gặp nhiều khó khăn và tình trạng nám tái phát là phổ biến. Vì vậy, cần có những thủ thuật có thể phục hồi màng đáy để ngăn ngừa tái phát và cải thiện kết quả lâu dài.
Da nhạy cảm
Trong một cuốn sách về laser, nám da được giải thích như sau [25]. “Nám da được đặc trưng bởi tình trạng viêm không có triệu chứng, tức là viêm nhẹ, không nhìn thấy được, không triệu chứng lâm sàng. Nói cách khác, nám là da nhạy cảm”. Tôi cũng quan sát thấy rằng những bệnh nhân bị nám có làn da nhạy cảm hơn những bệnh nhân khác. Và trong số những bệnh nhân bị nám, những bệnh nhân có làn da nhạy cảm không đáp ứng tốt với điều trị. Ngoài ra, tôi đã gặp phải trường hợp nám xảy ra ở những bệnh nhân có làn da nhạy cảm, và do đó, những bệnh nhân có làn da nhạy cảm như thể họ bị nám, mặc dù họ không bị nám.
Nguyên nhân có thể gây ra nám
Tôi đã tóm tắt các phát hiện mô học ở bệnh nám, trong Bảng 12.2. Các nguyên nhân và cơ chế có thể gây ra nám được tóm tắt trong Bảng 12.3. Dựa trên các nội dung cho đến nay, tôi nghĩ rằng cơ chế có thể xảy ra của nám như sau. “Ở những bệnh nhân có làn da nhạy cảm do di truyền hoặc nội tiết tố, có thể bị viêm do kích ứng mãn tính, như tia UV hoặc mỹ phẩm, điều này có thể phá vỡ hàng rào biểu bì, dẫn đến màng đáy bị tổn thương và viêm ở lớp bì. Để bảo vệ vùng da bị tổn thương, các sắc tố xuất hiện trên lớp biểu bì, từ đó xuất hiện tình trạng nám da”.
| Các phát hiện mô học trong nám |
|
Bảng 12.3 Nguyên nhân và cơ chế có thể của nám
| Nguyên nhân có thể gây ra nám | Cơ chế có thể gây ra nám |
| Melanocyte kích động
Di truyền, hormone, tia UV, mỹ phẩm, v.v. Viêm |
|
Vậy chúng ta nên điều trị nám như thế nào? Đầu tiên, chúng ta không thể thay đổi yếu tố di truyền, nhưng vì nám có liên quan đến estrogen, thuốc tránh thai estrogen liều thấp (ví dụ: Yaz®) nên khuyên dùng cho bệnh nhân đang dùng thuốc tránh thai. Ngoài ra, cần chống tia UV triệt để, không để da bị kích ứng. Thứ hai, lớp biểu bì, màng đáy và lớp bì phải được tái tạo để phục hồi da bị tổn thương. Tình trạng viêm của lớp bì cũng sẽ được giảm bớt. Tức là toàn bộ làn da cần được cải thiện. Cuối cùng, hoạt động của các melanocyte nên được giảm, không tạo ra sắc tố mới và cần loại bỏ sắc tố đã hình thành. Các chi tiết cụ thể sẽ được xem xét sau.
Giống như Kenichirou Kasai, tôi cũng thấy “sự phá vỡ các hàng rào gây ra bởi quá trình kích thích mãn tính (chà xát quá nhiều)” là nguyên nhân chính gây ra nám da. Ngoài giả thuyết của Kasai, tôi thêm các nghiên cứu kết quả mô học của nám và nghiên cứu gợi ý nguyên nhân gây ra nám. Nhưng tất cả vẫn chỉ là giả thuyết. Nó chỉ là một bước nữa từ Kasai. Giống như Kasai, tôi cũng đang hành nghề tư nhân và gặp khó khăn khi thực hiện các nghiên cứu lâm sàng hoặc thực nghiệm. Tôi cũng mong muốn được nhìn thấy cơ chế chính xác của nám thông qua các nghiên cứu trong tương lai.
Điều trị nám
Đồng thuận về điều trị nám
Ba lựa chọn điều trị chính cho bệnh nám như sau [1]. Đầu tiên, chống tia UV và các loại thuốc làm trắng da tại chỗ như hydroquinone (HQ), tretinoin, axit azelaic, rucinol và axit kojic. Liệu pháp phối hợp ba thuốc (công thức Kligman) là sự kết hợp của hydroquinone, tretinoin và steroid, và là phương pháp điều trị chính bôi tại chỗ. Thứ hai, lột da bằng hóa chất. Thứ ba, điều trị bằng laser có thể hữu ích, nhưng có thể xảy ra hiện tượng tăng sắc tố. Đôi khi việc tránh các yếu tố làm trầm trọng thêm như tiếp xúc với tia UV và kích thích nội tiết tố có thể là đủ để điều trị nám.
Như trong Bảng 12.4, có thể thấy rằng các loại thuốc làm trắng khác nhau bao gồm cả liệu pháp kết hợp ba thành phần đều có hiệu quả đối với nám. Lột da bằng hóa chất và thuốc uống cũng có hiệu quả. Có một nghiên cứu cho rằng laser toning và laser fractional CO2 là phương pháp điều trị nám hiệu quả. Điều thú vị là có những tranh cãi về hiệu quả của laser Er: Glass, một loại laser phân đoạn không bóc tách được FDA Hoa Kỳ phê duyệt để điều trị nám. Có hai nghiên cứu ủng hộ hoặc không ủng hộ hiệu quả của laser Er: Glass trong trị nám. Ngoài ra còn có một nghiên cứu ủng hộ IPL để điều trị nám, được biết đến như là một chống chỉ định trong hành nghề tư nhân [27].
Bảng 12.4 Các phương pháp điều trị nám, cơ chế hoạt động và tác dụng phụ
| Phương
pháp |
Điều trị | Cơ chế hoạt động | Tác dụng phụ |
| Bôi tại chỗ | Iron oxide | Cản ánh sáng khả kiến và UV | Kích ứng |
| Hydroquinone, Azelaic
acid, ascorbic acid, Kojic acid |
Chất ức chế tyrosinase | Kích ứng, tăng sắc tố do hydroquinone | |
| Tretinoin | Tăng luân chuyển tế bào sừng | Kích ứng, mẩn đỏ | |
| Corticosteroid | Chống viêm với ức chế không
chọn lọc sự hình thành hắc tố |
Giãn mạch, teo biểu bì, trứng
cá do steroid, rạn, giảm sắc tố |
|
| Ascorbic acid | Ức chế các loại oxy phản ứng | Không đáng kể | |
| Niacinamide | Ức chế chuyển melanosome | Kích ứng | |
| Uống | Tranexamic acid | Ức chế con đường plasminogen / plasmin → ức chế tổng hợp melanin
Giảm sự tăng sinh mạch máu |
Đầy bụng, kinh nguyệt không đều, đau đầu, huyết khối tĩnh mạch sâu |
| Polypodium leucotomos, | Ức chế các loại oxy phản ứng | Không đáng kể | |
| Thủ thuật | Laser Q-switched ruby,
laser Q-switched Nd:Yag |
Phá hủy melanosome | Bỏng, thay đổi sắc tố sau viêm |
| Laser không bóc tách
Laser phân đoạn |
Quá trình quang nhiệt phân
đoạn dẫn đến loại bỏ melanin |
Bỏng, thay đổi sắc tố sau viêm | |
| Lột da bằng hóa chất | Tăng luân chuyển tế bào sừng | Bỏng, bong tróc, thay đổi sắc
tố sau viêm |
|
| Microneedling | Vận chuyển thuốc qua da | Ban đỏ, phù nề, vết kim, thay
đổi sắc tố sau viêm |
|
| IPL | Loại bỏ melanosome | Bỏng, thay đổi sắc tố sau viêm | |
| RF | Kích thích sinh học tế bào
Vận chuyển thuốc qua da |
Bỏng |
Từ các phương pháp điều trị khác nhau, điều trị hiệu quả nhất là gì? Trong một nghiên cứu của Trivedi và cộng sự, các phương pháp điều trị sau đây đã được khuyến nghị cho bệnh nám da [28]. Lựa chọn đầu tay nên là thuốc bôi ngoài da bao gồm HQ. Đối với lựa chọn thứ hai, lột da bằng hóa chất được khuyến khích. Và đối với lựa chọn thứ ba, liệu pháp laser và ánh sáng bao gồm IPL đã được khuyến khích. Rivas và cộng sự đã công bố một nghiên cứu tổng quan về điều trị nám [29]. Phương pháp điều trị bằng laser tạo ra nhiều kết quả khác nhau, với việc tăng nguy cơ kích ứng và tăng sắc tố sau đó, đặc biệt ở những người da tối màu. Do đó, laser nên được coi là liệu pháp thứ ba khi điều trị nám da ở những người da tối màu.
Từ những nghiên cứu trước đó, chúng ta có thể thấy nhiều nghiên cứu nghi ngờ về việc điều trị nám bằng laser. Nhưng những kết luận này có đáng tin cậy không? Trong những thập kỷ qua, phương pháp điều trị nám da ngày càng phát triển. Trước khi bắt đầu sử dụng laser, chỉ có thuốc và lột da bằng hóa chất là những lựa chọn điều trị nám da. Và qua nhiều nghiên cứu, giờ đây chúng ta đã biết được liều lượng và loại thuốc điều trị nám tối ưu. Vì phương pháp điều trị nám bằng laser tương đối mới, có thể vấn đề là chúng ta không biết loại laser và năng lượng tối ưu để điều trị nám.
Tôi nghĩ rằng ưu điểm lớn nhất của laser là tính đặc hiệu của chúng. Chỉ nám hoặc sắc tố có thể điều trị chọn lọc. Mặt khác, thuốc hoặc lột da bằng hóa chất không có tính chọn lọc. Nhưng tôi không nghĩ rằng điều trị bằng laser là phương pháp điều trị nám hiệu quả nhất. Không có phương pháp điều trị duy nhất nào là hiệu quả nhất đối với bệnh nám. Tôi nghĩ việc điều trị kết hợp giữa dùng thuốc, lột da hóa chất, laser theo cơ chế hiệu quả là quan trọng nhất trong điều trị nám.
Đồng thuận về điều trị bằng thuốc và lột da bằng hóa chất
Điều trị nám bằng thuốc và lột da bằng hóa chất đã được sử dụng từ lâu trong các phương pháp điều trị nám. Như vậy, liều lượng, loại thuốc và phương pháp điều trị nám tối ưu đã được thiết lập. Vậy thuốc và lột da bằng hóa chất hiệu quả nhất để điều trị nám da là gì?
Vào năm 2006, Pigmentary Disorders Academy đã xem xét các nghiên cứu liên quan đến điều trị nám trong hai thập kỷ qua và phân loại chúng từ I đến IV theo chất lượng bằng chứng (chỉ ra rằng nghiên cứu được thiết kế khách quan tốt, số càng nhỏ thì chất lượng càng cao) và từ A đến E theo mức độ bằng chứng (càng gần A, bằng chứng càng cao) [30] (Bảng 12.5).
Kết quả cho thấy trong số các chất bôi ngoài da, chất duy nhất có chất lượng bằng chứng I và mức độ bằng chứng A là công thức Kligman. 4% hydroquinone, 0,1% tretinoin, sự kết hợp của 4% hydroquinone và GA 10%, và axit azelaic 20% có chất lượng bằng chứng I và mức độ bằng chứng B. Không có chất lượng bằng chứng I ở nghiên cứu về lột da bằng hóa chất. Chất lượng bằng chứng cao nhất là II-i với mức độ bằng chứng B của sự kết hợp giữa 20–30% GA lột da và 4% hydroquinone, và 70% GA lột da. Chất lượng bằng chứng và mức độ bằng chứng cho cả điều trị bằng laser và mài mòn da đều thấp.
Bảng 12.5 Mức độ và chất lượng của bằng chứng của các liệu pháp trị nám
| Phương pháp | Chất lượng
bằng chứng |
Mức độ
bằng chứng |
| Bôi tại chỗ | ||
| 2% HQ | II-ii | C |
| 4% HQ | I | B |
| 0.1% tretinoin (RA) | I | B |
| 0.05% tretinoin (RA) | I | C |
| 0.05% isotretinoin | II-ii | C |
| 4% N-acetyl-4-S-cysteaminylphenol | III | C |
| 5% HQ + 0.1–0.4% RA + 7% lactic acide/10% ascorbic acid | III | C |
| 3% HQ + 0.1% RA | III | C |
| 4% HQ + 0.05% RA + 0.01% fluocinolone acetonide | I | A |
| 2% HQ + 0.05% RA + 0.01% dexamethasone (modified kligman) | III | C |
| 2% HQ + 0.05% RA + 0.01% dexamethasone (modified kligman) +
30% ~ 40% GA peel |
III | B |
| 5% HQ + 0.1% RA, and 1% hydrocortisone | III | C |
| 4% HQ + 5% RA | II-ii | B |
| 4% KA + 5% RA | II-ii | B |
| 2% KA + 2% HQ + 10% GA | II-iii | C |
| 2% HQ + 10% GA | II-iii | C |
| 4% HQ + 10% GA | I | B |
| 20% Azelaic acid | I | B |
| 20% Azelaic acid +0.05% RA | III | C |
| Vitamin C iontophoresis | II-i | C |
| Adapalene | II-ii | B |
| Lột da bằng hoá chất | ||
| 10–50% GA | II-ii/ III | C |
| 10% GA + 2% HQ + 20–70% GA | II-ii | C |
| 20–30% GA + 4% HQ | II-i | B |
| 70% GA | II-i | B |
| Jessner’s solution | II-i | C |
| 20–30% salicylic acid | III | C |
| 1–5% RA | III | C |
| 50% GA + 10% KA | III | C |
| Laser (+Lột da bằng hoá chất và Bôi tại chỗ) | ||
| Laser Q-switched ruby | IV | C |
| Laser Pulsed CO2 + Q-switched alexandrite | C |
| Laser Q-switched alexandrite | IV | C |
| Laser Q-switched alexandrite laser +15–25% TCA peel + Jessner’s
solution |
III | C |
| Laser Erbium:YAG | III | D |
| Mài mòn da | II-iii | E |
GA- Glycolic acid, HQ- hydroquinone, KA- kojic acid, KF- Kligman’s formula, RA- retinoic acid, TCA- trichloroacetic acid.
Năm 2014, Shankar và cộng sự đã phân tích một số bài báo liên quan đến lột da bằng hóa chất [31]. Kết quả cho thấy không có thử nghiệm ngẫu nhiên có đối chứng (RCTs) và lột da bằng GA có mức độ khuyến cáo cao nhất (Bảng 12.6).
Bảng 12.6 Mức độ bằng chứng và độ mạnh khuyến cáo đối với các chất lột tẩy trên da dân tộc
| Phân loại | Hoạt chất | Mức độ bằng chứng | Độ mạnh
khuyến cáo |
| Peel bề mặt | Phytic acid | Ý kiến chuyên gia | C |
| Lactic acid | Nghiên cứu không đối chứng | B | |
| Glycolic acid | Nghiên cứu đối chứng không ngẫu
nhiên |
A | |
| Salicylic acid | Nghiên cứu không đối chứng | B | |
| Jessner’s solution | Nghiên cứu không đối chứng | B | |
| Peel bề mặt-trung bình | Pyruvic acid | Ý kiến chuyên gia | C |
| Peel trung bình-sâu | Trichloroacetic acid | Nghiên cứu không đối chứng | B |
A: Có bằng chứng tốt hỗ trợ việc sử dụng thủ thuật, B: Có bằng chứng hợp lý hỗ trợ việc sử dụng thủ thuật, C: Có ít bằng chứng hỗ trợ việc sử dụng thủ thuật.
Có nhiều loại thuốc và hóa chất lột da khác nhau, nhưng trong cuốn sách này, tôi sẽ thảo luận ngắn gọn về những điều sau: liệu pháp kết hợp ba thành phần, axit tranexamic và lột da bằng GA.
Liệu pháp kết hợp ba thành phần
Liệu pháp kết hợp ba thành phần (triple combination therapy, TCT) được thực hiện bởi Tiến sĩ Albert M. Kligman (1916–2010) vào năm 1975 [2]. Còn được gọi là công thức Kligman, công thức ban đầu này sử dụng dexamethasone 0,1% kết hợp với 0,1% tretinoin và 5% hydroquinone. Công thức Kligman đã được sửa đổi theo một số cách trong nhiều năm (Hình 12.8).
Thuốc có cơ chế hoạt động chính được cho là HQ, có tác dụng ức chế tyrosinase, đây là loại enzym quan trọng nhất trong quá trình tổng hợp melanin. Đây là lý do tại sao TCT cho thấy hiệu quả làm trắng mạnh mẽ. HQ là chất oxy hóa liên kết và phản ứng nhanh với oxy nên khó tạo dạng ổn định. Tretinoin ngăn chặn quá trình oxy hóa hydroquinone, tăng cường sự thâm nhập vào biểu bì, loại bỏ sắc tố và tăng sinh tế bào sừng. Cuối cùng, steroid tại chỗ có tác dụng làm giảm chuyển hóa tế bào, ức chế tổng hợp melanin và giảm kích ứng do thuốc.

Chan và cộng sự so sánh hiệu quả và độ an toàn của TCT (fluocinolone acetonide 0,01%, HQ 4%, tretinoin 0,05%) so với HQ 4% sau 8 tuần điều trị nám da mặt từ trung bình đến nặng ở 240 bệnh nhân châu Á [32]. TCT có hiệu quả vượt trội so với HQ về chỉ số mức độ nghiêm trọng của nám (64,2% so với 39,4%), nhưng không có 100%. Nhiều bệnh nhân có các tác dụng phụ liên quan đến TCT hơn so với HQ (48,8% so với 13,7%). Các tác dụng phụ thường gặp nhất là ban đỏ (24,0% so với 4,6%), kích ứng da (10,9% so với 3,8%), bong tróc da (5,4% so với 0,8%), khó chịu trên da (6,2% so với 1,5%), nhưng hầu hết đều nhẹ và không nặng.
TCT nên được sử dụng mỗi ngày một lần trong 12 tuần đầu tiên và hai lần một tuần trong 12 tuần tiếp theo đồng thời theo dõi chặt chẽ sự tuân thủ của bệnh nhân và các tác dụng phụ.
TCT là thuốc đã được sử dụng từ lâu và đã được chứng minh hiệu quả, nhưng như trong Sect. 5.2.8 trong “Chap. 5” mặc dù khả năng là thấp, nhưng nó có thể gây ra tăng sắc tố ngoại sinh do HQ. Và thông qua các thí nghiệm trên động vật gặm nhấm, người ta cho rằng HQ có thể là chất gây ung thư. Hơn hết, nó có thể gây kích ứng da và ban đỏ và gây ra PIH. Đặc biệt, sự tuân thủ của bệnh nhân thấp và thường được sử dụng không đúng cách. Đây là lý do tại sao tôi kê đơn axit tranexamic, thay vì TCT.
Axit tranexamic
Axit tranexamic (TA) bắt đầu được chú ý vào năm 1979 sau khi Nijo Sadako (Nhật Bản) sử dụng nó để điều trị bệnh mày đay mãn tính và tình cờ thấy rằng mức độ nám của bệnh nhân đó đã giảm đáng kể [33]. Kể từ đó, TA đã được sử dụng rộng rãi trong điều trị nám ở Nhật Bản và nhiều nghiên cứu khác nhau về TA đã được xuất bản.
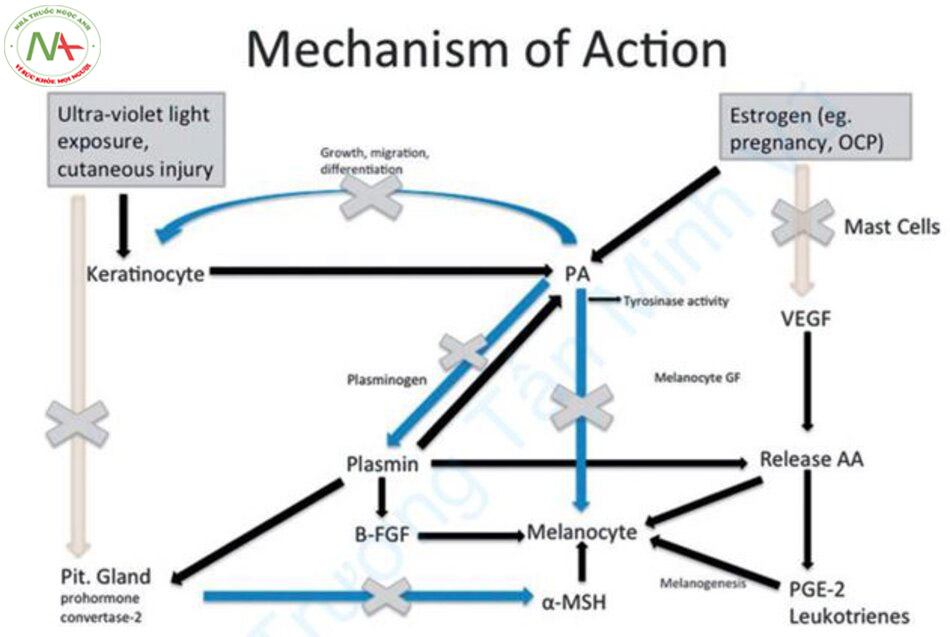
TA là một chất ức chế plasmin và đã được sử dụng như một loại thuốc để kiểm soát chảy máu bằng cách ức chế chất hoạt hóa plasminogen (plasminogen activator, PA).
Tế bào sừng tạo ra PA và plasminogen, và plasminogen thúc đẩy sự tổng hợp melanin bởi tia UV (Hình 12.9). Plasmin cũng tham gia vào quá trình tiết yếu tố tăng trưởng nguyên bào sợi (fibroblast growth factor, FGF), một yếu tố tăng trưởng cho melanocyte. TA ngăn chặn có thể đảo ngược vị trí liên kết lysine của plasminogen và ức chế sự chuyển đổi plasminogen thành plasmin bằng cách ức chế PA [33]. Trong các thí nghiệm trên động vật, TA làm giảm sự hình thành sắc tố bởi tia UV gây ra bằng cách liên kết plasminogen với keratinocyte và giảm hoạt hóa tyrosinase trong melanocyte. Trong một nghiên cứu, TA can thiệp vào xúc tác của tyrosinase, do đó ức chế sắc tố [34]. Các nghiên cứu khác đã chỉ ra rằng TA làm giảm α-melanocytestimulation hormone (α-MSH), là chất kích thích tổng hợp melanin.
Liều khuyến cáo của TA đường uống như sau: 250 mg 2-3 lần một ngày. Cần dùng thuốc ít nhất 1 tháng để thuốc phát huy tác dụng. Thời gian dùng thuốc dài hơn được biết là có hiệu quả hơn so với liều lượng thuốc cao hơn. Bên cạnh TA đường uống, còn có phương pháp tiêm trong da, tuy nhiên hiệu quả vẫn chưa được chứng minh. Việc sử dụng tại chỗ rất khó khăn vì các triệu chứng kích ứng và thiếu các sản phẩm thương mại hóa. TA có thể xâm nhập vào da bằng phương pháp điện di, nhưng hiệu quả vẫn chưa được chứng minh. Vào năm 2007 ở Đài Loan, tiêm tĩnh mạch (IV) 500 mg axit tranexamic với axit ascorbic trong khoảng thời gian từ 2 đến 4 tuần đã phổ biến với tên thương mại là “làm trắng da”. Nhưng không có nghiên cứu nào liên quan đến việc tiêm và nồng độ rất thấp, điều này cũng đặt ra câu hỏi về hiệu quả của nó. Ngoài ra, do tiêm tĩnh mạch nên có nguy cơ bị viêm tĩnh mạch hoặc các bệnh về tim mạch.
Liều TA để kiểm soát chảy máu là 0,5–1,5 g, 3 lần một ngày. Ngay cả ở liều cao như vậy, không thấy sự thay đổi của các yếu tố đông máu và tỷ lệ huyết khối không tăng. Vì vậy, tôi cho rằng liều lượng sử dụng cho bệnh nám 0,5–0,75 g/ngày là liều lượng rất an toàn. Nó không ảnh hưởng đến thai nhi hoặc dị tật thai nhi vì không qua hàng rào máu não (BBB) và nhau thai nhưng vẫn chống chỉ định trong thời kỳ mang thai hoặc cho con bú. Ngoài ra, những bệnh nhân bị bệnh mạch vành hoặc rối loạn đông máu, những bệnh nhân đang dùng thuốc làm tan huyết khối như aspirin, những bệnh nhân có kỳ vọng quá cao vào kết quả điều trị cũng là những chống chỉ định [33].
Wu và cộng sự đã đánh giá sự cải thiện sắc tố và giảm kích thước vết nám ở 74 bệnh nhân nữ dùng 250 mg TA 2 lần/ngày trong 6 tháng [35]. Kết quả cho thấy sự cải thiện đáng kể về sắc tố là 82,4% trong tháng đầu tiên, tăng lên 94,6% trong 2 tháng và 95,9% trong 6 tháng (10,8% xuất sắc, 54% tốt, 31,1% khá, 4,1% kém). Các tác dụng phụ bao gồm buồn nôn, tiêu chảy, đau bụng, giảm kinh, phát ban trên da, rụng tóc, buồn ngủ và giảm ham muốn tình dục, nhưng nhẹ và tỷ lệ mắc thấp. Điều thú vị là tình trạng nám da được cải thiện trong suốt thời gian điều trị, nhưng không có sự khác biệt ở các sắc tố khác như đốm nâu và tàn nhang. Karn và cộng sự so sánh hiệu quả của TA uống trong điều trị nám bằng cách so sánh hai nhóm [36]. Nhóm đầu tiên (A) được cho uống TA (liều 250 mg 2 lần một ngày) và bôi HQ tại chỗ trong 3 tháng trong khi nhóm thứ hai (B) chỉ được điều trị với bôi HQ tại chỗ trong 3 tháng. Điểm Melasma Area Severity Index (MASI) và chỉ số hài lòng của bệnh nhân được đo ở tuần thứ 8 và 12. Nhóm A cho thấy chỉ số nám giảm có ý nghĩa thống kê ở tuần thứ 8 và 12. Chỉ số nám da giảm có ý nghĩa thống kê ở 8 tuần ở nhóm B, nhưng không giảm ở 12 tuần. Chỉ số hài lòng của bệnh nhân là 82,3% ở nhóm A và 40,8% ở nhóm B. Các tác dụng phụ bao gồm chậm kinh nhẹ, ợ hơi, đau quặn bụng, đánh trống ngực và nổi mề đay. Điều thú vị là có một sự cải thiện đáng kể trong tình trạng tăng sắc tố do hydroquinone ở hai bệnh nhân dùng TA.
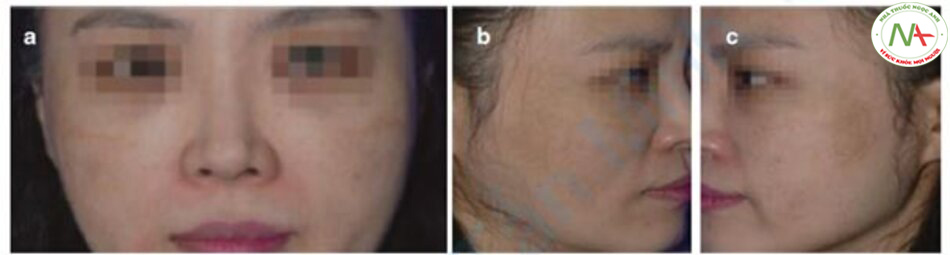
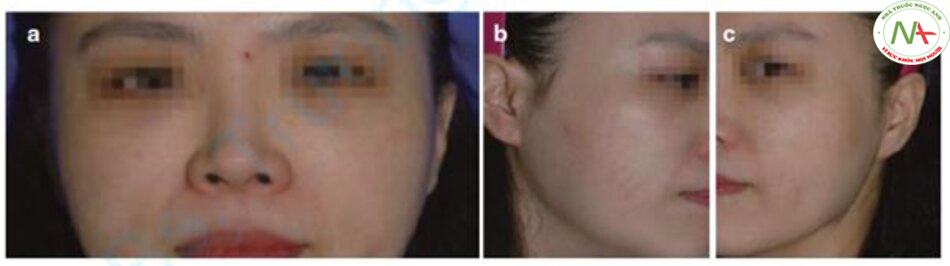
Tôi chỉ kê đơn uống TA 250 mg cho bệnh nhân bị nám (Hình 12.10 và 12.11) và thẩm thấu TA qua da bằng phương pháp điện di. Thỉnh thoảng, tôi sử dụng “tiêm căng bóng da”, kết hợp TA với axit hyaluronic và tiêm vào lớp bì.
Lột da bằng glycolic acid
Alpha-hydroxy acid (AHA) là một loại acid hữu cơ được tìm thấy trong trái cây và sữa trong tự nhiên, có tác dụng dưỡng ẩm và tẩy tế bào chết. Glycolic acid (GA) là một đại diện cho AHA lột da và được chiết xuất từ đường mía. GA được biết là có trọng lượng phân tử nhỏ nhất và có thể xâm nhập sâu hơn vào lớp biểu bì [37].
GA lột da đã được sử dụng rộng rãi như một chất lột tẩy từ cuối những năm 1980. GA lột da không làm hoà tan keratinocyte như lột da bằng TCA nhưng làm thay đổi sự gắn kết của keratinocyte để loại bỏ lớp sừng. Nó cũng kích thích lớp mầm và nguyên bào sợi và được biết là có tác dụng chống viêm và chống oxy hóa. GA lột da được biết là có hiệu quả cả ở lớp biểu bì và lớp bì.
Ưu điểm của việc GA lột da như sau. Đầu tiên, nó không làm suy yếu chức năng hàng rào bảo vệ da. Mất nước qua biểu bì (TEWL) không tăng so với da bình thường và không có dấu hiệu viêm. Thứ hai, không có sự hoại tử hoặc thoái hóa của các mô, và các chức năng phục hồi hàng rào được ghi nhận, như tăng tiết các thể phiến. Thứ ba, không phân biệt độ sâu, GA lột da tác động đến lớp bì và kích thích các nguyên bào sợi của lớp bì, dẫn đến tổng hợp và tăng sinh collagen, elastin, glycosaminoglycans, … Thứ tư, thời gian phục hồi ngắn, tốt trong điều trị thẩm mỹ. Thứ năm, nó có thể dùng cho mọi loại da và cũng có thể sử dụng cho da nhạy cảm.
Những ưu điểm của GA lột da có thể hữu ích cho tình trạng nám. GA lột da có thể phục hồi chức năng hàng rào bảo vệ da, được cho là nguyên nhân gây nám. Nó không gây viêm và cải thiện lớp bì. Nó cũng có thể dùng cho da nhạy cảm, có rất nhiều ở bệnh nhân bị nám. Cuối cùng, không cần thời gian nghỉ dưỡng. Đây là lý do tại sao tôi sử dụng GA lột da để trị nám.
Tuy nhiên, có rất nhiều nhược điểm của việc GA lột da. Đầu tiên, cường độ dùng cho điều trị thay đổi tùy thuộc vào nhiều biến số như nồng độ, pH và thời gian sử dụng. Vì vậy, GA lột da phải được thực hiện một cách thận trọng và quy trình phải được thống nhất. Thứ hai, do mức độ thâm nhập không đồng nhất và có thể thay đổi tùy thuộc vào tình trạng hoặc vị trí của da, điều quan trọng là phải đào tạo các chuyên gia thẩm mỹ để trung hoà GA lột da ngay lập tức nếu phản ứng bất lợi xảy ra. Thứ ba, GA lột da cần trung hòa [38].
Một số nghiên cứu đánh giá GA lột da hiệu quả ở da dân tộc [37]. Javaheri và cộng sự sử dụng GA 50% lột da trên 25 phụ nữ Ấn Độ bị nám cách nhau hàng tháng trong tổng thời gian 3 tháng, đã được chứng minh là có hiệu quả trong 91%. Ngoài một phụ nữ bị tăng sắc tố trên lông mày, không có tác dụng phụ. GA lột da được coi là hiệu quả và an toàn. Ưu điểm mà GA lột da hơn các loại lột tẩy khác là an toàn cho những người có làn da dân tộc, những người có làn da nhạy cảm. GA lột da cũng được biết là có hiệu quả đối với bệnh trứng cá đỏ vì nó ngăn chặn sự bám của mạt demodex vào nang lông.
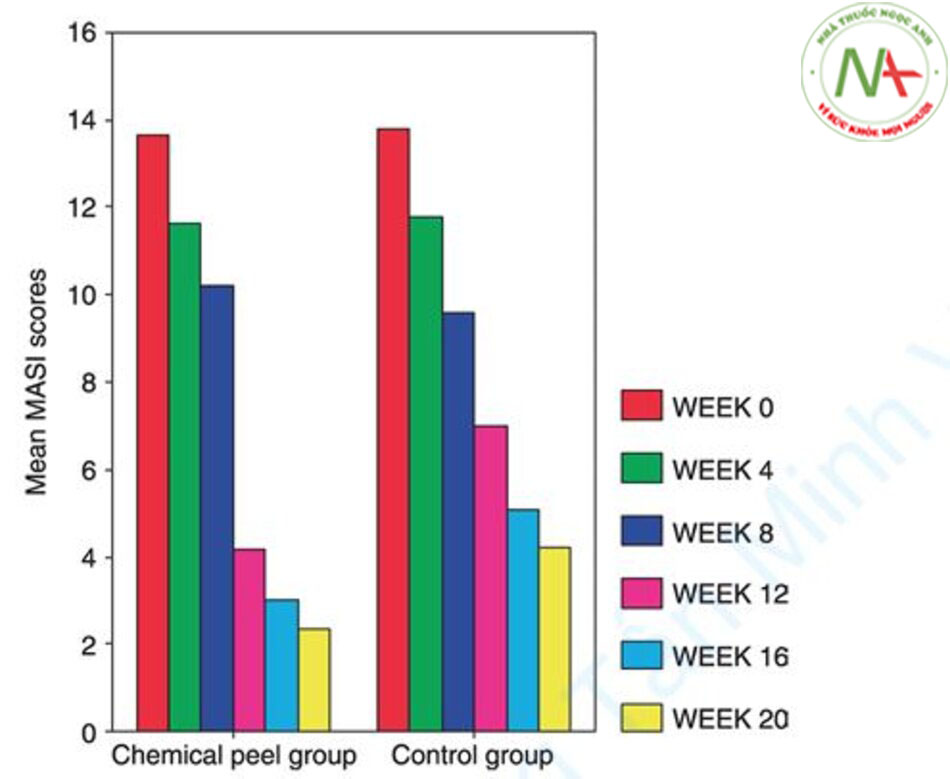
Erbil và cộng sự thu nhận 28 bệnh nhân bị nám kháng trị và chia thành hai nhóm [39]. Nhóm lột da bằng hóa chất được bôi GA kết hợp với axit azelaic và adapalene tại chỗ trong khi nhóm đối chứng chỉ bôi axit azelaic và adapalene tại chỗ. Quá trình lột GA được thực hiện 2 tuần một lần, và nồng độ được tăng lên từng chút một mỗi tháng.
Kết quả cho thấy khi sử dụng GA 50% lột da, sự giảm điểm MASI nổi bật hơn so với nhóm đối chứng (Hình 12.12). Đây là lý do tại sao tôi chọn sử dụng nồng độ 50% trong quá trình lột GA.
Tiếp theo, chúng ta sẽ điểm qua các phương pháp điều trị nám bằng laser. Đặc biệt, xem xét laser toning, được sử dụng rộng rãi trong phòng khám tư nhân. Chúng ta cũng sẽ xem xét nguyên tắc và sự lựa chọn của laser trong các rối loạn sắc tố và xem xét chiến lược điều trị sắc tố. Cuối cùng, chúng ta sẽ điểm qua nguyên lý và sự lựa chọn của laser trong điều trị nám.
Laser toning
Laser toning thông thường
Trước khi dùng laser toning, laser không được sử dụng để điều trị nám. Laser được chống chỉ định trong điều trị nám do các tác dụng phụ như tăng sắc tố ngược lại và giảm sắc tố [40]. Tuy nhiên, từ năm 2005, các phòng khám tư nhân ở Đông Á đã phát hiện ra laser Q-switched Nd: YAG 1064-nm (“laser toning”) có hiệu quả trong điều trị nám. Vì vậy, “laser toning” đầu tiên bắt đầu trong phòng khám tư nhân và sau đó được nghiên cứu trong bệnh viện đại học.
Chung và cộng sự đã sử dụng laser Q-switched Nd: YAG 1064-nm có mật độ năng lượng thấp ở 27 bệnh nhân bị nám. 17 bệnh nhân (58,8%) cho thấy cải thiện sắc tố trên 50–75% [40]. Nghiên cứu này là nghiên cứu đầu tiên về “laser toning.” Các thông số khác với những gì được sử dụng cho điều trị sắc tố thông thường: spot size lớn, năng lượng thấp, nhiều pass, thực hiện hàng tuần, nhiều lần. Phương pháp điều trị này được gọi là “laser toning.” Trong nghiên cứu, nó được gọi là “laser Q-switch Nd: YAG mật độ năng lượng thấp” hoặc “laser Q-switch Nd: YAG liều thấp”. Tuy nhiên, tôi sẽ sử dụng thuật ngữ “laser toning” trong cuốn sách này.
Các thông số của laser toning thông thường được sử dụng trong phòng khám tư nhân và ghi lại trong các nghiên cứu như sau. Đầu tiên, laser Q-switch Nd: YAG 1064- nm được sử dụng. Thứ hai, năng lượng tương đối thấp 1,6–3,5 J/cm2 được sử dụng. Thứ ba, spot size tương đối lớn từ 6–8 mm được sử dụng. Thứ tư, nhiều pass được thực hiện ở tần số 10 Hz dẫn đến hơn 1000 lần bắn. Thứ năm, điều trị được thực hiện với khoảng thời gian rất ngắn cứ 1-2 tuần một lần. Thứ sáu, cần điều trị 5–10 lần thay vì chỉ một lần. Thứ bảy, end point là ban đỏ.
Các thông số này có đúng không? Bây giờ chúng ta sẽ xem xét các khía cạnh chung của laser toning, và sau đó, tôi sẽ nhận xét về bảy thông số của laser toning.
Quang nhiệt chọn lọc dưới tế bào
Trong Sect. 3.1.3 trong “Chap. 3” chúng ta đã xem xét các nghiên cứu về “quang nhiệt chọn lọc dưới tế bào”, cơ sở của laser toning.
Sau đây là tóm tắt các điểm quan trọng trong nghiên cứu về quá trình quang nhiệt chọn lọc dưới tế bào (Bảng 12.7) [41]. Đầu tiên, để đáp ứng lý thuyết quang nhiệt chọn lọc dưới tế bào, mật độ năng lượng phải tương đối thấp hơn mật độ năng lượng được sử dụng trong điều trị sắc tố thông thường. Thứ hai, cửa sổ điều trị rất hẹp vì chỉ có 0,4 J/cm2 được thấy là có hiệu quả từ các mật độ năng lượng khác nhau dao động từ 0,3 đến 0,9 J/cm2 ở cá ngựa vằn. Thứ ba, chỉ được bắn một lần. Thứ tư, tái phát xảy ra ngay cả với laser toning.
Bảng 12.7 Các điểm quan trọng và biện pháp đối phó của quá trình quang nhiệt chọn lọc dưới tế bào
| Các điểm quan trọng của quá trình
quang nhiệt chọn lọc dưới tế bào |
Biện pháp đối phó |
| Mật độ năng lượng tương đối thấp | Tìm mật độ năng lượng trong trị liệu |
| Cửa sổ trị liệu rất hẹp | Mật độ năng lượng < cửa sổ trị liệu |
| Chỉ một lần bắn | 1 shot toning |
| Tái phát | Thay đổi hành vi, ngăn chặn sự tổng hợp
melanin, cải thiện lớp bì, lặp lại laser toning? |
Đây là suy nghĩ của tôi về bốn điểm trên. Đầu tiên, chúng ta không biết chính xác mật độ năng lượng của “mật độ năng lượng tương đối thấp”. Do đó, năng lượng thích hợp phải được tìm cho laser toning thông thường với nhiều pass và nhiều lần bắn. Năng lượng của one-shot toning mà tôi hiện đang sử dụng được đề cập trong Sect. 3.1.3 trong “Chap. 3” và không có thông số tuyệt đối. Năng lượng phải được điều chỉnh tùy theo bệnh nhân. Năng lượng nên được điều chỉnh để năng lượng là “tổn thương tối màu yếu, tổn thương sáng màu mạnh.” Thứ hai, phạm vi điều trị rất hẹp. Ngay cả khi năng lượng thích hợp được tìm thấy, nó vẫn rất nguy hiểm. Sẽ an toàn hơn nếu sử dụng ít hơn năng lượng đầy đủ vì nó chỉ kém hiệu quả hơn là có tác dụng phụ. Thứ ba, trong nghiên cứu “quang nhiệt chọn lọc dưới tế bào”, các tác giả chỉ sử dụng một lần bắn [42]. Ngay cả khi “one shot toning” mà tôi đã đề cập không được sử dụng, tốt hơn là nên xác định trước số lần bắn muốn thực hiện ở một bên mặt. Thứ tư, cần có các biện pháp ngăn ngừa tái phát. Phần này đòi hỏi sự hiểu biết về các nguyên nhân cơ bản gây ra nám. Điều này sẽ được giải thích một lần nữa dưới đây.
Hiệu quả của laser toning
Tiếp theo, chúng ta sẽ xem xét hai nghiên cứu tác động của laser toning.
Mun và cộng sự thực hiện laser toning bằng laser Q-switched Nd: YAG 1064-nm trên 16 bệnh nhân và quan sát tổn thương nám bằng kính hiển vi điện tử và tái tạo thành hình ảnh 3D [43].
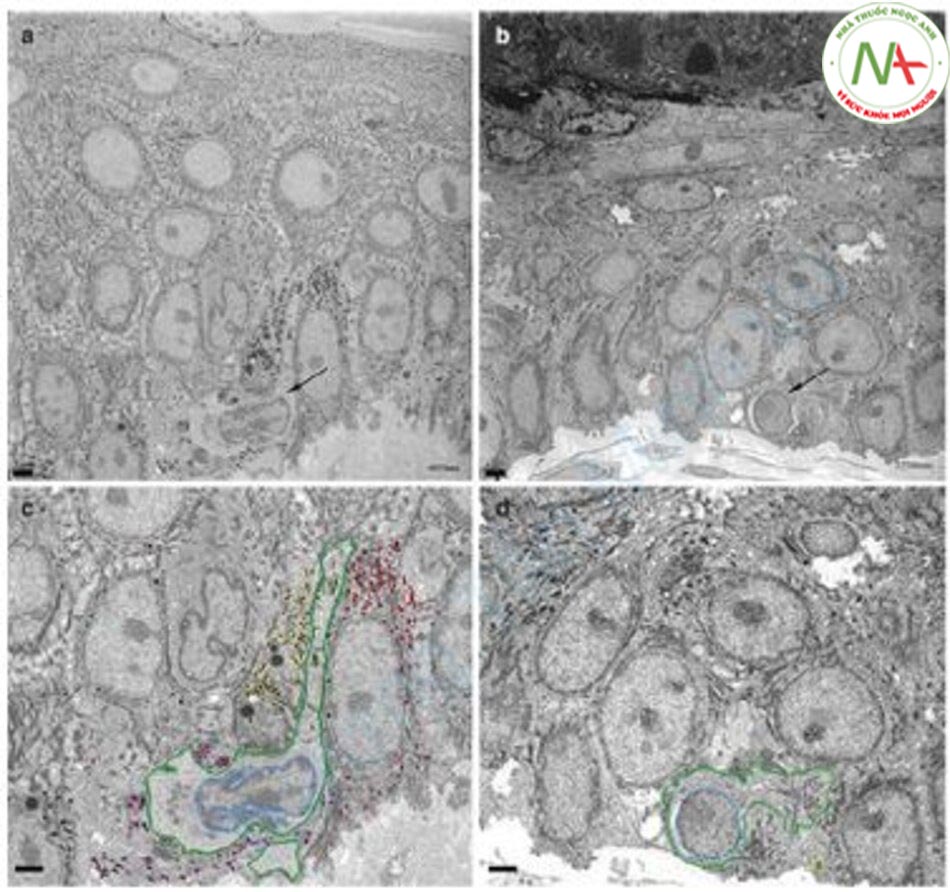
Kết quả như sau. Đầu tiên, thể tích của các melanocyte bị giảm và số lượng các melanosome cũng giảm (Hình 12.13). Thứ hai, ghi nhận hiện tượng “dendrectomy”, dendrite (đuôi gai) của melanocyte bị giảm (Hình 12.14). Thứ ba, các melanosome trưởng thành ở giai đoạn IV giảm, và thứ tư, melanosome bị thoái hóa và các vết được quan sát thấy. Thứ năm, các melanosome chưa trưởng thành ở giai đoạn I và II không thay đổi (Hình 12.15).
Điều thú vị về nghiên cứu này là hiện tượng “dendrectomy”, là hiện tượng giảm các dendrite của melanocyte. Các tác giả của nghiên cứu này cho rằng lý do của điều này là do các melanosome ở giai đoạn IV nằm trên dendrite nhiều hơn bất kỳ phần nào khác của melanocyte, do đó, do hiệu ứng nhiệt phân giải của laser, dendrite biến mất [43]. Tôi nghĩ rằng hiện tượng này là do “sự bất hoạt của melanocyte.” Vai trò quan trọng nhất của melanocyte là tạo ra các melanosome và đưa chúng đến các keratinocyte. Do đó, các dendrite giảm đi ngụ ý rằng vai trò của các melanocyte đã không còn nữa. Tôi nghĩ rằng laser toning gây ra sự bất hoạt melanocyte. Ngoài ra, sau khi điều trị bằng laser, các melanosome trong melanocyte biến mất, thể tích melanocyte nhỏ hơn và sự phân chia nhân giảm như trong Hình 12.13, mà tôi tin rằng tất cả đều là dấu hiệu của sự bất hoạt melanocyte.
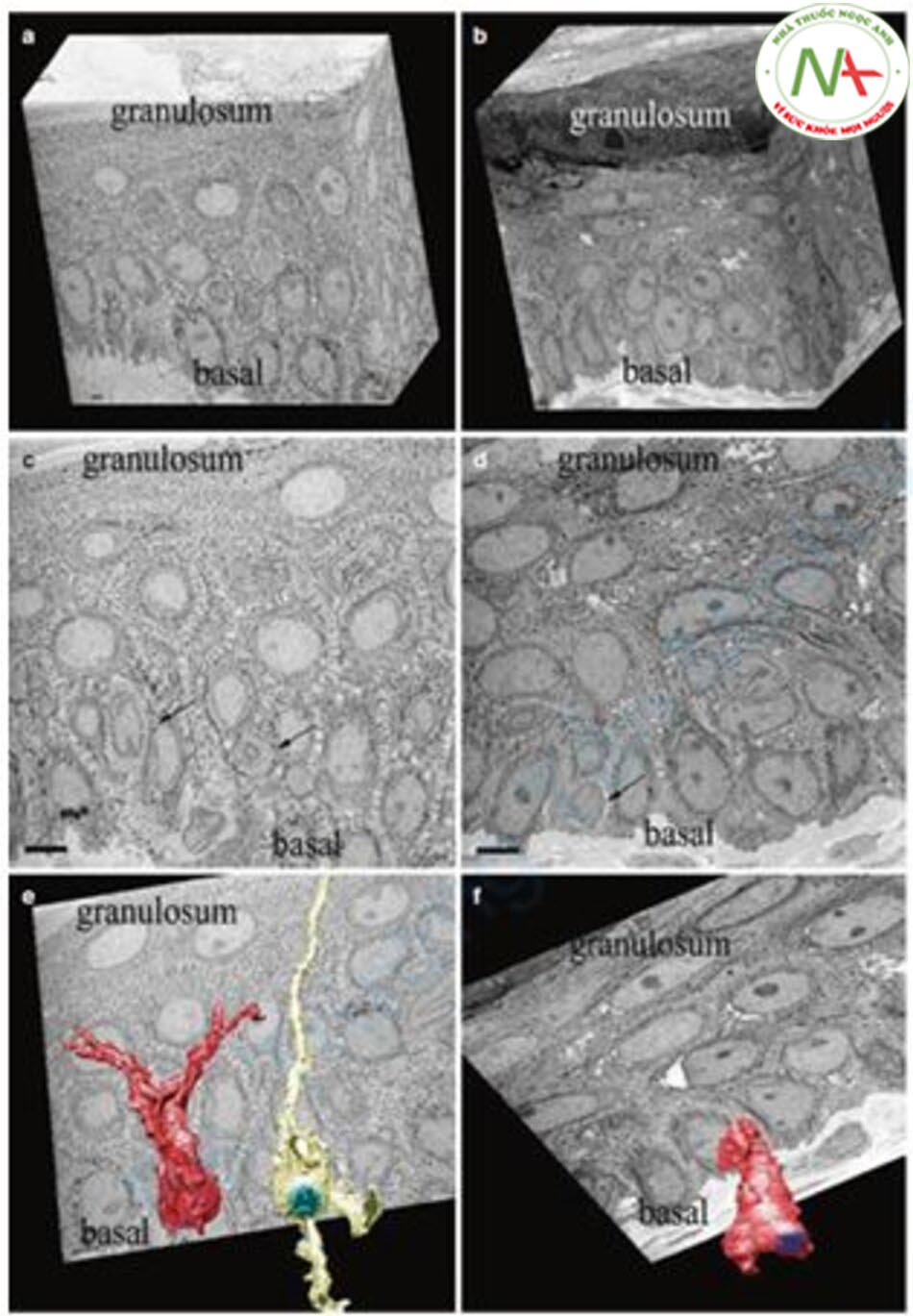
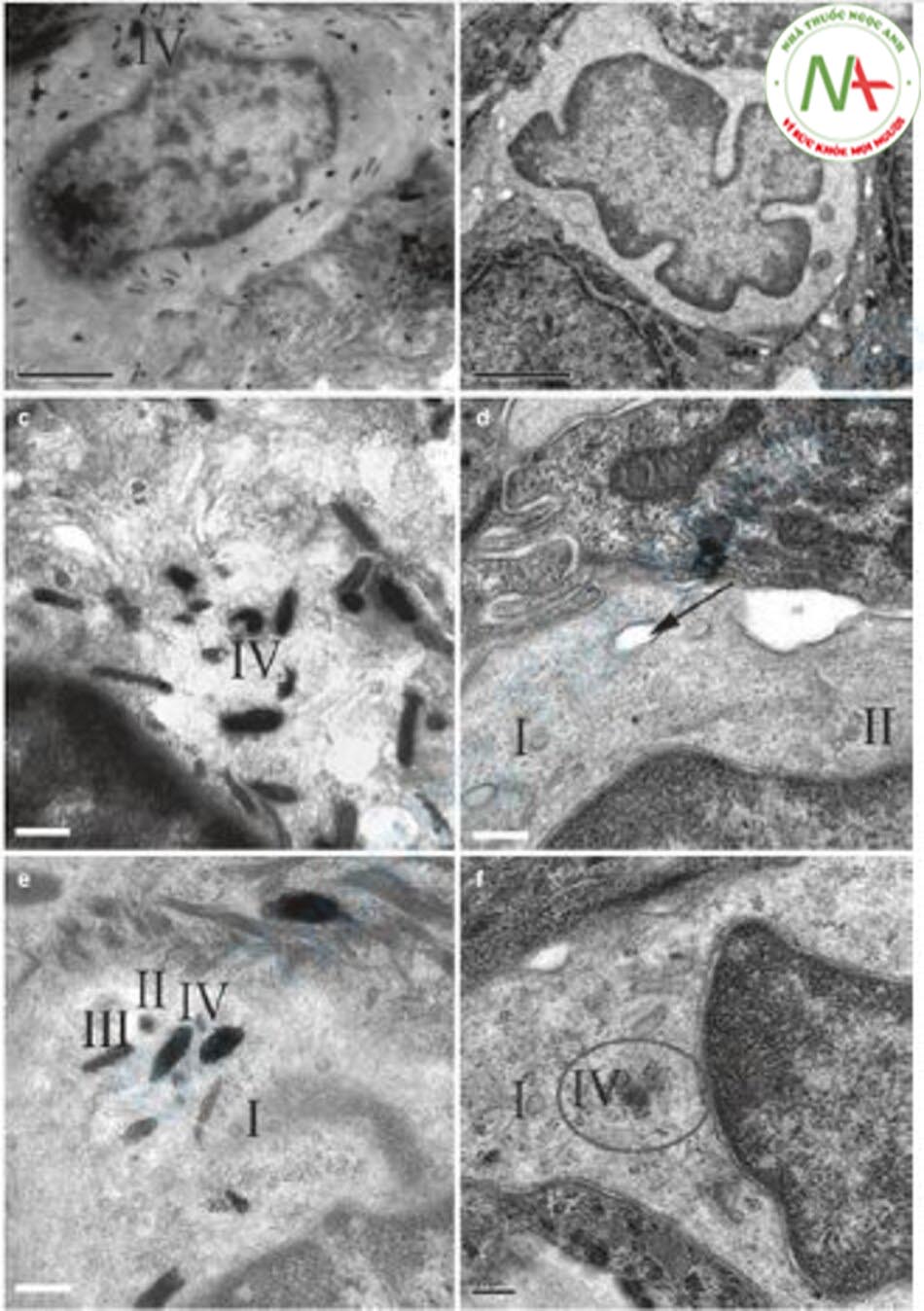
Tôi cũng tin rằng cơ chế của việc làm sáng nám bằng laser toning là do cắt bỏ đuôi gai chứ không phải do phá vỡ melanosome. Trong nghiên cứu “quang nhiệt chọn lọc dưới tế bào”, các melanosome của cá ngựa vằn đã bị phá vỡ bởi laser toning. Nhưng nếu melanosome vỡ bên trong tế bào, liệu điều này có làm cho sắc tố nám da tổng thể sáng hơn không? Các melanosome bị phá vỡ bởi laser toning không biến mất khỏi tế bào mà mảnh vỡ vẫn ở bên trong keratinocyte hoặc melanocyte. Khi sắc tố melanin bị vỡ ra và lan rộng, nó có vẻ sáng dưới kính hiển vi, nhưng tổng lượng melanin vẫn không thay đổi. Nói cách khác, không có sự khác biệt lớn khi nhìn bằng mắt. Đây là lý do tại sao chúng ta không thể thấy sự sáng lên ngay lập tức sau khi laser toning trên lâm sàng. Tôi nghĩ rằng việc phá vỡ đuôi gai ngăn không cho các melanocyte phân phối các melanosome đến các keratinocyte trong ít nhất 2 tuần, vì vậy trong quá trình luân chuyển biểu bì, các keratinocyte phát triển không có melanosome và khuôn mặt sáng lên. Đây là lý do tại sao laser toning không cải thiện tình trạng nám ngay lập tức, nhưng làm da mặt sáng lên sau 4 tuần, sau quá trình thay đổi biểu bì.
Một điều nữa cần đề cập là nhiều người nghĩ rằng laser toning chỉ làm tổn thương các melanosome trong melanocyte. Tuy nhiên, hầu hết các melanosome nằm trong keratinocyte và các melanocyte có các melanosome trưởng thành trong đuôi gai, phần sẽ biến mất sau dendrectomy trong khi các melanosome chưa trưởng thành (giai đoạn I, II) không bị ảnh hưởng bởi laser toning, tức là các melanocyte không trở nên sáng hơn hoặc biến mất. Do đó, laser toning không chỉ giúp cải thiện sự xuất hiện của nám mà còn làm sáng toàn bộ khuôn mặt.
Kim và cộng sự quan sát được những thay đổi trước và sau khi điều trị bằng laser toning qua kiểm tra mô bệnh học [44]. So với vùng da không bị nám, các mẫu da tổn thương nám cho thấy tăng phản ứng ở melanin và các protein liên quan quá trình tạo melanin, bao gồm hormone kích thích tế bào hắc tố α (α-melanocyte-stimulating hormone, α-MSH), tyrosinase, protein liên quan đến tyrosinase (tyrosinase-related protein TRP) -1, TRP-2, yếu tố tăng trưởng thần kinh (nerve growth factor, NGF) và yếu tố tế bào gốc (stem cell factor, SCF). Sau khi điều trị bằng laser, vùng da bị nám có biểu hiện giảm số lượng các melanosome và giảm biểu hiện của các protein liên quan đến hình thành melanin.
Nghiên cứu này cho thấy rằng laser toning làm giảm các protein liên quan đến quá trình hình thành melanin. Nói cách khác, laser toning không chỉ đơn giản là phá vỡ các melanosome, mà còn ức chế sự tổng hợp melanin, không phải là vĩnh viễn, nhưng quá trình sản xuất melanin tạm thời ngừng lại, dẫn đến sáng da.
Dựa trên hai nghiên cứu trước đó, tác dụng làm sáng da của laser toning là do, thứ nhất, ức chế tổng hợp melanin và thứ hai, ngăn chặn sự truyền melanosome.
Tiên lượng của laser toning
Zhou và cộng sự thu nhận 55 bệnh nhân và thực hiện laser Q-switched Nd: YAG 1064 nm ở mức năng lượng thấp hàng tuần trong chín lần [45]. Sự hài lòng của bệnh nhân, chỉ số melanin (MI), vùng nám và chỉ số mức độ nghiêm trọng (MASI) được đo. Kết quả như sau: thứ nhất, sự hài lòng của bệnh nhân là 84% và không phải tất cả bệnh nhân đều hài lòng; thứ hai, điểm MASI trung bình giảm 61,3% và chỉ có 10% đạt 100%. Hầu hết bệnh nhân vẫn bị nám sau khi dùng laser toning (Hình 12.16). Thứ ba, tình trạng nám da không cải thiện ngay sau khi sử dụng laser toning mà được cải thiện sau 4-6 tuần, và dần dần được cải thiện khi lặp lại laser toning. Thứ tư, các tác dụng phụ nhỏ như ban đỏ, cảm giác nóng, ngứa ran, sưng tấy và ban xuất huyết xảy ra, nhưng không có tác dụng phụ nghiêm trọng nào được ghi nhận. Thứ năm, khi ngừng điều trị, tỷ lệ tái phát sau 3 tháng là 64%, khá cao.
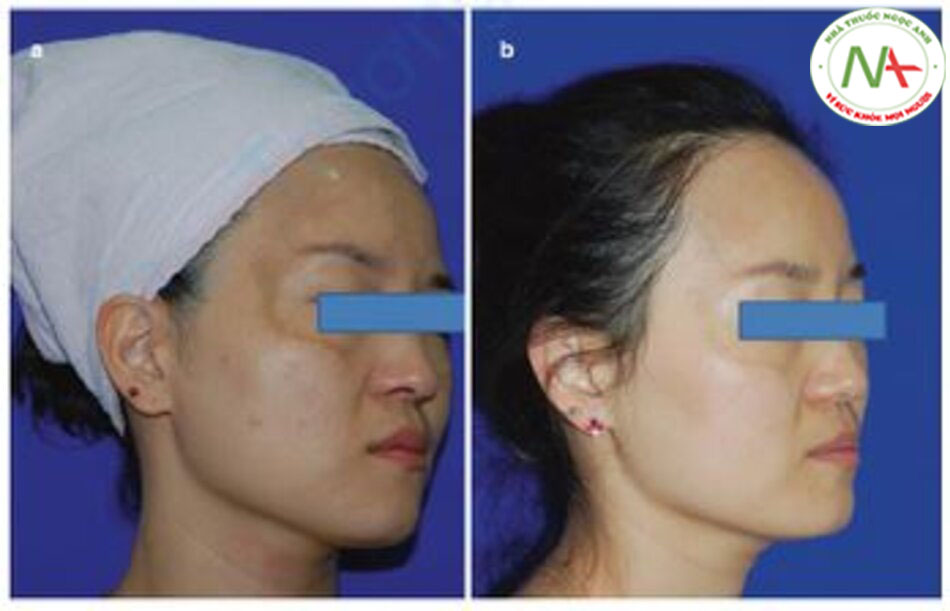
Mặc dù mật độ năng lượng của nghiên cứu này cao hơn một chút so với thông số laser toning thông thường (2,5–3,4 J/cm2), nhưng nghiên cứu này cho thấy tác dụng điển hình và sự tiến triển của laser toning.
Tác dụng phụ của laser toning
Khi các tác dụng của quang nhiệt chọn lọc dưới tế bào và laser toning đã được chứng minh, laser toning đã trở nên phổ biến trong hành nghề tư nhân. Tuy nhiên, nhiều quy trình laser toning dẫn đến các tác dụng phụ thường xuyên của laser toning. Các tác dụng phụ của laser toning được tóm tắt trong Bảng 12.8 [46].
Các tác dụng phụ được liệt kê ở phía bên trái của Bảng 12.8 là tạm thời và thường không phải là vấn đề lớn, nhưng các tác dụng phụ ở bên phải là tác dụng phụ vĩnh viễn nghiêm trọng.
Bảng 12.8 Các tác dụng phụ của laser toning
| Các tác dụng phụ của laser toni | ng |
| Tác dụng phụ nhẹ | Tác dụng phụ nghiêm trọng |
| Khô da | Không đáp ứng (10–20%) |
| Hình thành milium | Tái phát |
| Mày đay cơ học | Tăng sắc tố ngược |
| Phát ban mụn trứng cá | Bạch biến |
| Đốm xuất huyết | Giảm sắc tố dạng đốm (1,6%) |
| Làm trắng lông tơ mặt | |
| Tái kích hoạt herpes simplex |
Nếu chúng ta xem qua những tác dụng phụ nhẹ thì đầu tiên là tình trạng khô da. Điều này được cho là có liên quan đến việc giảm bã nhờn, một tác dụng của laser toning [47]. Sự hình thành milium hoặc tái kích hoạt herpes simplex được cho là rất hiếm vì tôi chưa bao giờ thấy nó. Phát ban mụn trứng cá thường thấy, nhưng sau khi dùng laser triệt lông với laser alexandrite xung dài 755 nm thì tần số đã được giảm bớt. Tôi nghĩ rằng phát ban mụn trứng cá là do cháy lông bởi laser toning. Trong một số trường hợp, mày đay được ghi nhận sau điều trị bằng laser mà không có bất kỳ tiền sử cụ thể nào. Trong trường hợp này, phân biệt nổi mày đay do các nguyên nhân khác bằng cách hỏi tiền sử và khám. Hầu hết lặn trong vòng vài phút. Nguyên nhân chính xác vẫn chưa được biết, nhưng tôi nghĩ điều này có thể là do sự phá vỡ các tế bào mast và giải phóng histamine (nổi mề đay cơ học). Nếu đốm xuất huyết xuất hiện sau khi điều trị bằng laser, năng lượng được coi là quá cao. Tôi cũng không quan sát thấy điều này vì tôi thực hiện laser toning với năng lượng tương đối thấp.
Các tác dụng phụ nghiêm trọng của laser toning như sau. Không đáp ứng (10– 20%), tái phát, tăng sắc tố ngược và giảm sắc tố. Đặc biệt, giảm sắc tố dạng đốm là một tác dụng phụ nghiêm trọng và được thấy trong khoảng 1,6% [48]. Tiếp theo, chúng ta hãy xem xét kỹ hơn những tác dụng phụ nghiêm trọng này.
Tái phát
Zhou và cộng sự thực hiện laser toning ở 55 bệnh nhân bị nám trong 9 tuần và sau 3 tháng theo dõi thấy rằng 64% bị tái phát [45]. Gokalp và cộng sự đã thực hiện laser toning ở 34 bệnh nhân bị nám từ sáu đến mười lần (trung bình là tám lần) trong khoảng thời gian 2 tuần, và sau 1 năm theo dõi, 58,8% (20 bệnh nhân) cho thấy tái phát, tương tự như nghiên cứu của Zhou và cộng sự [49]. Do đó, Gokalp và cộng sự kết luận rằng mặc dù các phương pháp điều trị mới đã xuất hiện trong điều trị nám nhưng không có tiêu chuẩn vàng nào trong điều trị bằng laser có hiệu quả lâu dài, do đó “một lần là nám, luôn là nám”.
Phải biết nguyên nhân gây nám thì mới có thể ngăn ngừa được tình trạng nám da. Tuy nhiên, vì nguyên nhân chính xác của nám vẫn chưa được xác định, nên không có cách nào nhất định để ngăn ngừa bệnh tái phát. Tuy nhiên, xét đến một số nguyên nhân gây nám da, tôi nghĩ những biện pháp này có thể ngăn ngừa nám tái phát. Đầu tiên, cần có liệu pháp hành vi để ngăn chặn tia UV và bảo vệ da. Thứ hai, các loại thuốc ức chế sản xuất melanosome phải được tiếp tục. Thứ ba, phải thực hiện các biện pháp phục hồi da, đặc biệt là cải thiện lớp bì. Thứ tư, nên lặp lại quá trình điều trị bằng laser toning.
Tăng sắc tố ngược
Sau khi dùng laser toning, có thể xảy ra hiện tượng như tối màu da bị nám. Hiện tượng này đã được ghi nhận ngay cả trước khi laser toning được giới thiệu. Năng lượng quá cao được cho là lý do. Năng lượng thấp hơn nên được sử dụng và thực hiện các biện pháp để tìm ra năng lượng thích hợp. Năng lượng thích hợp sẽ được thảo luận ở phần sau, trong Sect. 12.6.6.
Giảm sắc tố da dạng đốm (Bạch biến dạng đốm)
Kim và cộng sự đã thực hiện laser toning trên tổng số 259 phụ nữ Hàn Quốc và tình trạng giảm sắc tố dạng đốm xảy ra ở 3 bệnh nhân (1,6%) [48]. Điều thú vị là giảm sắc tố dạng đốm xảy ra sau hai lần điều trị bằng laser toning ở hai bệnh nhân và năm lần bằng laser toning ở một bệnh nhân.
Tác dụng phụ nghiêm trọng nhất sau khi dùng laser toning là giảm sắc tố dạng đốm. Giảm sắc tố dạng đốm là hiện tượng cho thấy nhiều mảng giảm sắc tố hình tròn nhỏ đến hình bầu dục có ranh giới rõ ràng (Hình 12.17).
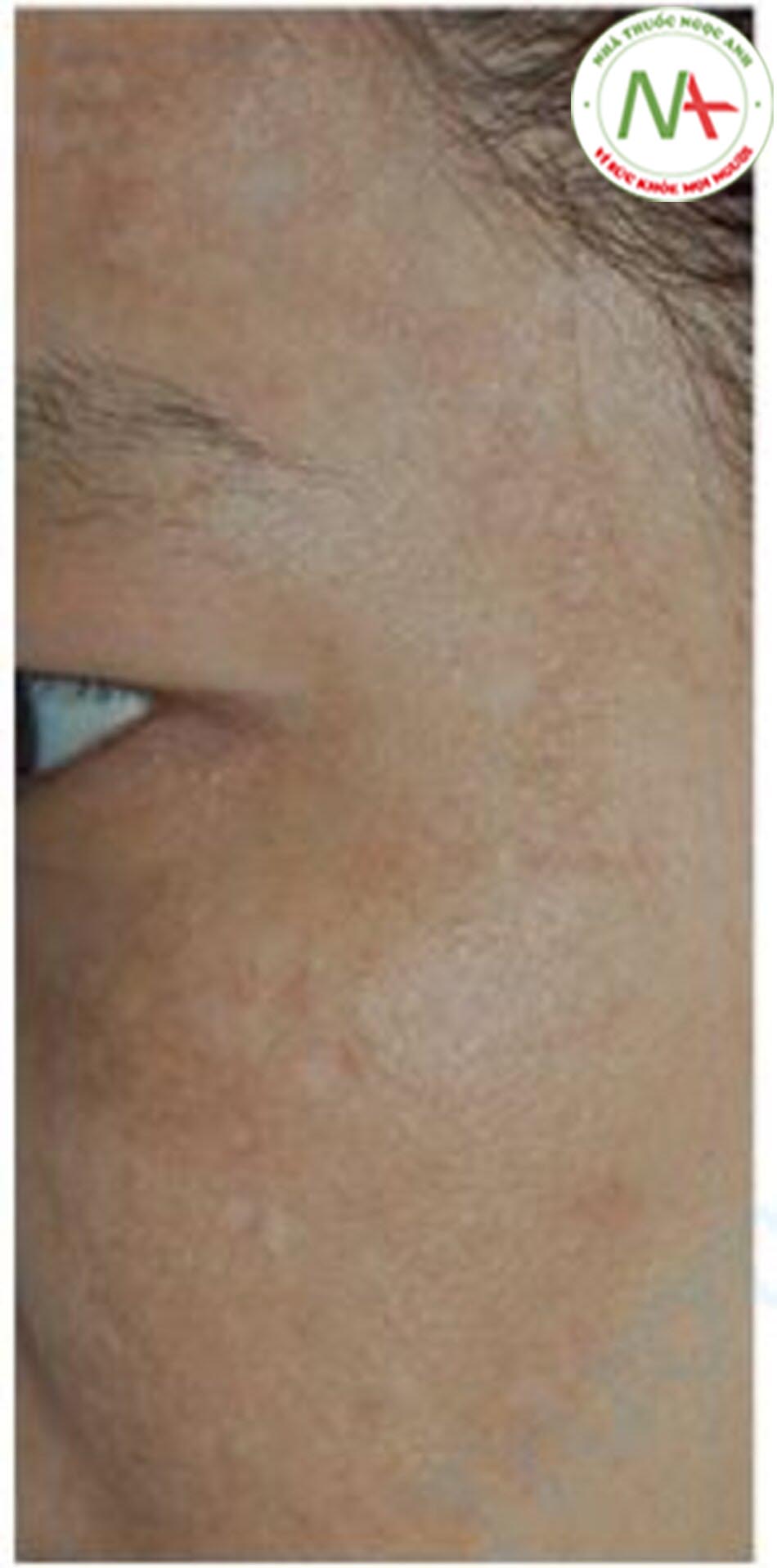
Khó có thể coi giảm sắc tố dạng đốm như một tác dụng phụ của laser toning vì các mảng giảm sắc tố xảy ra ở một số vị trí mặc dù laser được chiếu đều trên vết nám. Ngoài ra, sự tương phản giữa các mảng giảm sắc tố và nám khiến chúng trở nên rõ ràng hơn và không mong muốn. Mặc dù hiếm gặp (1,6%), cần lưu ý rằng giảm sắc tố dạng đốm có thể xảy ra khi thực hiện laser toning. Nó có thể xuất hiện rất nhanh, ngay cả giai đoạn đầu thực hiện điều trị bằng laser toning (chỉ sau hai lần), vì vậy cần phải theo dõi cẩn thận ở mọi lần điều trị.
Mặc dù không có sự đồng thuận về quá trình giảm sắc tố dạng đốm, hầu hết được biết là lâu dài và khó phục hồi. Do đó, cơ chế xảy ra hiện tượng giảm sắc tố dạng đốm và việc ngăn ngừa bằng cơ chế đó là rất quan trọng.
Giảm sắc tố da dạng đốm còn được gọi là bệnh bạch biến dạng đốm (punctate leukoderma). Bạch biến dạng đốm là một thuật ngữ đã được sử dụng ngay cả trước khi điều trị bằng laser. Bạch biến dạng đốm lần đầu tiên được thấy sau khi điều trị một số bệnh ngoài da: dùng 4-isopropylcatechol điều trị bệnh sắc tố, điều trị bằng tia UV sau khi dùng psoralen để điều trị bệnh bạch biến (tiếp xúc với tia UV mặt trời, PUVASOL hoặc PUVA) và tia UVB điều trị bệnh vẩy nến [50]. Falabella đã quan sát thấy nhiều hiện tượng giảm sắc tố ở 13 bệnh nhân bạch biến được điều trị bằng PUVASOL và lần đầu tiên mô tả nó là “leukoderma perfata” [51]. Cơ chế bệnh sinh của bạch biến dạng đốm được cho là do ngộ độc ánh sáng, như tia UV gây ra tổn thương melanocyte [50].
Các phát hiện mô học về giảm sắc tố dạng đốm được mô tả trong một số nghiên cứu. Wong và cộng sự quan sát thấy rằng ở các vị trí tăng sắc tố, sắc tố melanin tăng lên, số lượng melanocyte vẫn bình thường, và quá trình đuôi gai được phát triển, giống như các vị trí nám [52]. Mặt khác, vị trí giảm sắc tố có số lượng sắc tố melanin giảm, số lượng melanocyte và quá trình đuôi gai đều giảm (melanocytopenia). Ryu và cộng sự báo cáo khác [46]. Kết quả kiểm tra mô học qua phương pháp nhuộm H&E, nhuộm MART và nhuộm S-100 cho thấy số lượng melanocyte vẫn bình thường và chỉ có giảm melanin (tức là giảm hắc tố melanopenic chứ không phải giảm tế bào hắc tố melanocytopenic). Trong một nghiên cứu, kính hiển vi điện tử đã được sử dụng để quan sát vị trí giảm sắc tố. Sắc tố melanin giảm. Melanocyte đã được quan sát thấy, nhưng là melanocyte đang hoạt động bất thường (Hình 12.18) [44]. Jang và cộng sự cũng quan sát thấy rằng vị trí giảm sắc tố có biểu hiện gp100 cao hơn so với vùng da bị nám hoặc da bình thường [53]. Biểu hiện gp100 cao có nghĩa là hoạt động sản xuất melanosome của các melanocyte bị suy giảm, điều này ngăn cản các melanocyte tạo ra các melanosome trưởng thành.
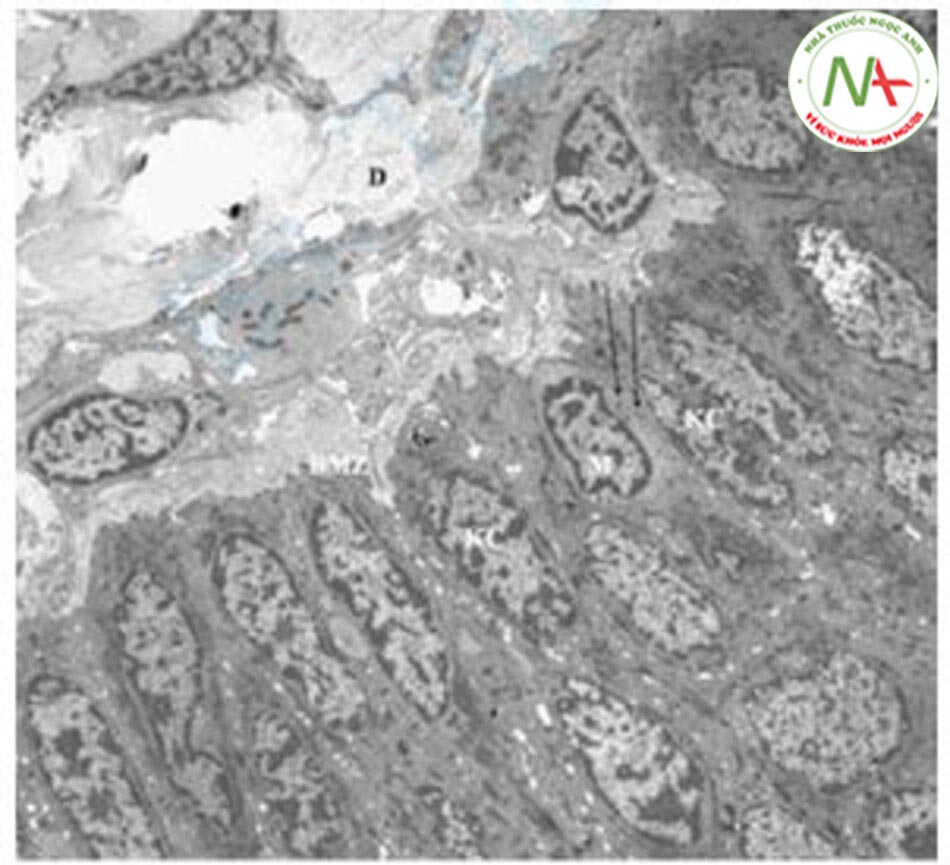
Cơ chế chính xác của giảm sắc tố dạng đốm do laser toning vẫn chưa được biết. Tuy nhiên, dựa trên cơ chế tạo bạch biến dạng đốm do tia UV gây ra và kết quả mô học của sự giảm sắc tố dạng đốm sau khi điều trị bằng laser, có thể ước tính như sau. Cơ chế chính được cho là ngộ độc ánh sáng tích lũy của melanocyte [51]. Cụ thể, quá trình quang nhiệt chọn lọc dưới tế bào nói rằng “có một mức năng lượng chỉ có thể phá vỡ các melanosome mà không làm tổn thương các tế bào,” nhưng trong chứng giảm sắc tố dạng đốm, các melanocyte cũng bị tổn thương như các melanosome. Tôi nghĩ nếu tổn thương quá mức thì số lượng melanocyte giảm đi, nhưng nếu tổn thương không quá mức thì số lượng melanocyte vẫn bình thường, nhưng chuyển thành melanocyte bị bất thường không có khả năng tạo ra hắc tố.
Lý do tại sao giảm sắc tố da xảy ra ở đây và được cho là như sau. Thứ nhất, vì bản thân nám không đồng nhất, có chỗ phản ứng mạnh với cùng một mức năng lượng. Thứ hai, chùm tia laser Q-switched Nd: YAG được cho là ở chế độ top-hat, nhưng chúng có thể không hoàn toàn đồng nhất [51]. Tôi cũng nghĩ rằng do nhiều pass trong quá trình thực hiện laser toning, một số phần tích lũy nhiều năng lượng hơn. (xem Sect. 12.6.8).
Cần lưu ý số lượng melanocyte. Nếu số lượng melanocyte vẫn bình thường và chỉ giảm melanin (melanopenia), chức năng của melanocyte sẽ trở lại, sản sinh melanin và tình trạng giảm sắc tố sẽ trở lại bình thường. Nhưng nếu số lượng melanocyte bị giảm (giảm tế bào hắc tố) thì không chắc rằng tình trạng giảm sắc tố sẽ trở lại bình thường. Do đó, năng lượng của laser toning phải là “năng lượng chỉ phá vỡ các melanosome” chứ không phải “năng lượng làm giảm các melanocyte.”
Xem xét cơ chế “ngộ độc ánh sáng tích lũy”, liều tích lũy được coi là một yếu tố nguy cơ đối với giảm sắc tố dạng đốm. Chúng ta sẽ tính đến liều lượng tích lũy và xem xét các thông số trong các nghiên cứu về giảm sắc tố dạng đốm để tìm ra thông số nào có vấn đề.
Kim và cộng sự quan sát thấy hiện tượng giảm sắc tố dạng đốm sau khi điều trị laser toning ở một phụ nữ Hàn Quốc 42 tuổi. Mật độ năng lượng là 2,5 J/cm2, cao hơn so với các thông số laser toning thông thường [50]. Kim và cộng sự đã thực hiện laser toning ở 8 phụ nữ Hàn Quốc, và tình trạng giảm sắc tố dạng đốm xảy ra ở 7 bệnh nhân [44]. Các thông số là 2000–3000 shot, 6–8 pass mỗi lần. Vấn đề dường như là quá nhiều shot và quá nhiều pass. Tian và cộng sự phân tích hồi cứu 23 bệnh nhân trải qua laser toning ba lần một tuần trong 2 tháng [54]. Tất cả các bệnh nhân đều có biểu hiện giảm sắc tố dạng đốm. Tian và cộng sự kết luận rằng 2 tuần là đủ cho khoảng thời gian giữa các liệu trình laser toning.
Khi “ngộ độc ánh sáng tích lũy” và các nghiên cứu trên được kết hợp cùng nhau, năng lượng cao, nhiều pass, nhiều lần bắn và khoảng thời gian giữa quá ngắn dường như là các yếu tố nguy cơ đối với chứng giảm sắc tố dạng đốm [44]. Do đó, nếu phát hiện thấy hiện tượng giảm sắc tố dạng đốm, nên ngừng sử dụng laser toning ngay lập tức để không làm tăng lượng năng lượng tích luỹ [46].
Các yếu tố nguy cơ khác cũng được đề cập [44]. Vùng quanh mắt ở những bệnh nhân dễ bị ban đỏ, tiền sử viêm da tiếp xúc dị ứng, ban đỏ và viêm ngứa sau laser, tiền sử ban đỏ kéo dài, da mỏng như vùng quanh mắt và da Fitzpatrick loại V được coi là các yếu tố nguy cơ.
Giảm sắc tố dạng đốm không phải là một tác dụng phụ phổ biến, vì vậy hầu hết các nghiên cứu là báo cáo trường hợp của một số ít bệnh nhân. Chiến lược điều trị giảm sắc tố dạng đốm như sau [51]. Đầu tiên, vị trí giảm sắc tố cần trở nên tối màu hơn, và thứ hai, vị trí tăng sắc tố cần trở nên nhạt màu hơn. Dựa trên hai khía cạnh này của chiến lược, chúng ta hãy xem xét các nghiên cứu liên quan đến việc điều trị chứng giảm sắc tố dạng đốm.
Chang và cộng sự chỉ thoa kem chống nắng có SPF100 trên da bình thường và da bị nám và chiếu UVB dải hẹp hàng tuần trên vùng da giảm sắc tố [51]. Tất cả năm bệnh nhân cho thấy sự cải thiện về mặt lâm sàng. Wong và cộng sự đã bôi thuốc mỡ tacrolimus 0,1% tại chỗ cho ba bệnh nhân, một bệnh nhân có cải thiện nhìn thấy được, một bệnh nhân không cải thiện và một bệnh nhân chỉ có cải thiện nhẹ [52]. Kim và cộng sự sử dụng laser bromua đồng 578-nm 5 lần trong khoảng thời gian 2 tuần [48]. Cải thiện tình trạng nám da và giảm sự khác biệt về màu sắc tổng thể, dẫn đến sự cải thiện chung. Ryu và cộng sự bôi GA 50% lột da vào các khoảng thời gian hàng tuần và kem tretinoin 0,025% vào mỗi buổi tối trong 3 tháng trên một bệnh nhân nữ 49 tuổi, và sự cải thiện đáng kể đã được ghi nhận [46]. Kim và cộng sự thực hiện laser excimer 308 nm trên các vị trí giảm sắc tố và một pass laser Q-switched Nd: YAG 1064 nm ở 0,7 J/cm2 trên các vị trí tăng sắc tố [55]. Sau 15 lần thực hiện cách nhau 2 tuần, sự cải thiện đáng kể đã đạt được.
Dựa trên các nghiên cứu này và các phát hiện mô học về giảm sắc tố dạng đốm, việc điều trị giảm sắc tố dạng đốm được khuyến nghị như sau.
Đầu tiên, vùng giảm sắc tố cho thấy các phát hiện mô học tương tự như bệnh bạch biến. Do đó, như được trình bày trong các báo cáo trước đó, có thể sử dụng phương pháp điều trị bằng tia UV (NB-UVB), thuốc mỡ 0,1% tacrolimus và kem tretinoin 0,025%, có hiệu quả trong điều trị bệnh bạch biến, có thể được sử dụng. Nhưng có một hạn chế về mặt kỹ thuật vì không dễ dàng điều trị chọn lọc vùng giảm sắc tố chỉ có kích thước từ 2– 3 mm. Đây là lý do tại sao laser excimer với kích thước điểm có thể điều chỉnh được được cho là phù hợp nhất. Ngoài ra, phương pháp điều trị hiệu quả nhất cho bệnh bạch biến được biết là laser excimer.
Thứ hai, vùng sắc tố xung quanh cần được làm sáng hơn. Nhưng như đã thấy trong các báo cáo trên, mặc dù có thể sử dụng kem chống nắng, thuốc bôi HQ, GA 50% lột da, kem tretinoin 0,025% nhưng việc điều trị chọn lọc vùng da sắc tố là rất khó. Vì vùng sắc tố ban đầu là vùng nám, nên nghịch lý là, phương pháp điều trị nám bằng laser toning hiệu quả nhất có thể được coi là an toàn. Tuy nhiên, do giảm sắc tố dạng đốm xảy ra với năng lượng được sử dụng ban đầu, nên sử dụng năng lượng thấp hơn năng lượng ban đầu. Do đó, 1 pass toning không chồng xung của Kim và cộng sự có ý nghĩa trong khía cạnh này. Có thể thử dùng laser mạch máu như laser đồng bromua. GA 50% lột da có thể làm tăng sự luân chuyển của biểu bì, có thể hữu ích cho vùng sắc tố xung quanh, và tretinoin 0,025% có thể không có tác dụng rõ ràng nhưng có thể thử.
Cuối cùng, chúng ta có thể coi vùng sắc tố chỉ là sắc tố và sử dụng laser để điều trị sắc tố biểu bì theo nguyên lý của laser. Vùng giảm sắc tố không có sắc tố; do đó, laser không thể phát huy tác dụng trên vùng này, tức là laser có thể nhắm mục tiêu một cách có chọn lọc vào vùng sắc tố. Nhưng laser an toàn nhất phải được sử dụng và năng lượng cũng phải được hạ thấp. Mặc dù không được công bố trong bài báo, tôi đã cố gắng điều trị chứng giảm sắc tố dạng đốm bằng laser alexandrite xung dài 755 nm, là loại laser an toàn nhất cho sắc tố biểu bì.
Thông số vàng
Có một số tài liệu liên quan đến tác dụng của laser toning, nhưng như đã thảo luận trước đó, cũng có nhiều tác dụng phụ. Có thông số vàng cho laser toning hiệu quả mà không có tác dụng phụ không? Một cuốn sách về laser đề xuất 3.0 J/cm2 ở chế độ PTP và 1.5 J/cm2 ở chế độ thông thường là các thông số vàng [56]. Nhưng tôi nghĩ rằng năng lượng này vẫn còn cao.
Choi và cộng sự thực hiện laser toning với laser Q-switched Nd: YAG 1064-nm trên 30 bệnh nhân bị nám nặng hơn sau liệu pháp điều trị trước đó như laser toning, IPL, laser phân đoạn, và lột da bằng hóa chất [57]. Các thông số là spot size 6 mm, 10 Hz, 2,1– 2,5 J/cm2 ở chế độ PTP, và endpoint là ban đỏ nhẹ. Sau khi laser toning, kỹ thuật genesis được thực hiện bằng cách sử dụng laser Nd: YAG 1064 nm xung dài ở 15–17 J/cm2 ở spot size 7 mm, 5 Hz và 0,3 ms. Mười lần laser toning được thực hiện cách nhau hàng tuần. Kết quả cho thấy chỉ số vùng nám và mức độ nghiêm trọng (mMASI) được điều chỉnh giảm từ 10,48 ± 3,64 xuống 3,22 ± 1,45 2 tháng sau khi hoàn thành 10 lần điều trị (p <0,001). 24 bệnh nhân (80%) có đánh giá của bác sĩ (PGA) mức độ 4 (cải thiện 76– 100%) và sáu bệnh nhân (20%) có PGA mức độ 3 (cải thiện 51–75%). Tất cả 30 bệnh nhân đều không có dấu hiệu nặng hơn của nám hoặc giảm sắc tố dạng đốm. Sau 1-3 năm theo dõi, tất cả 30 bệnh nhân không bị tái phát.
Trong nghiên cứu này, 30 bệnh nhân cho thấy sự cải thiện mà không có bất kỳ tác dụng phụ nào, mặc dù các bệnh nhân đã bị nám trầm trọng hơn sau liệu pháp điều trị trước đó như laser toning. Mười hai bệnh nhân (40% tổng số bệnh nhân) bị giảm sắc tố dạng đốm do các phương pháp điều trị khác đã cải thiện hình ảnh của vùng giảm sắc tố dạng đốm do giảm ở vùng sắc tố, làm giảm sự khác biệt màu sắc giữa vùng sắc tố và vùng giảm sắc tố dạng đốm.
Trước đó trong Sect. 12.6.2, chúng tôi đã xem xét rằng phạm vi điều trị của laser toning rất hẹp. Chúng tôi cũng đã xem xét lại rằng ngay cả khi năng lượng thích hợp được tìm thấy, nó vẫn rất nguy hiểm. Vì vậy, sẽ an toàn hơn nếu sử dụng mức thấp hơn năng lượng đủ vì nó sẽ ít hiệu quả hơn là có tác dụng phụ. Đây là lý do tại sao tôi nghĩ rằng mật độ năng lượng 2,1– 2,5 J/cm2 ở chế độ PTP và 1–1,25 J/cm2 ở chế độ thông thường là thông số vàng của điều trị nám.
Nám bì và nám hỗn hợp
Trong số các tác dụng phụ của laser toning, không đáp ứng là 10–20%. Có nhiều nguyên nhân có thể xảy ra, nhưng tôi tin rằng nám bì và nám hỗn hợp là một trong những nguyên nhân. Điều gì xảy ra với các vết nám ở lớp bì sau khi dùng laser toning? Tôi không thể tìm thấy bất kỳ bài báo nào liên quan đến vấn đề này, nhưng trong một cuốn sách, tôi có thể thấy bức ảnh và mô tả về ảnh hiển vi điện tử của Kim [25]. Kim đã quan sát thấy sự phá hủy một số lượng lớn các melanosome trong lớp bì sau khi điều trị bằng laser, và sau đó các melanin này biến mất bởi các melanophages.
Nói cách khác, quá trình phá vỡ và biến mất các melanosome bằng laser toning tương tự như điều trị hình xăm. Đại thực bào nuốt chửng các melanosome và sau đó biến mất theo hệ thống bạch huyết. Đó là quá trình tương tự như các sắc tố biến mất khỏi lớp bì.
Hai kết quả có thể được dự đoán. Đầu tiên, thời gian để sắc tố ở lớp bì biến mất ít nhất là 1–3 tháng, thời gian dẫn lưu bạch huyết, đối với hình xăm cũng vậy. Được biết, số lần điều trị xóa xăm cần thiết là 5 lần đối với hình xăm nghiệp dư và 10–15 lần đối với hình xăm chuyên nghiệp. Nám da tuy không đậm màu như hình xăm nhưng ước tính sẽ cần một thời gian khá dài để loại bỏ. Thứ hai, các melanosome ở lớp bì có thể hiện diện dưới dạng melanosome đơn lẻ, nhưng hầu hết hiện diện trong melanocyte hoặc melanophages. Để phá hủy các melanosome trong các tế bào này, năng lượng phải là “năng lượng chỉ làm tổn thương các tế bào mà không ảnh hưởng đến các tế bào xung quanh.” Nhưng như chúng ta đã xem xét trong quá trình quang nhiệt chọn lọc dưới tế bào, năng lượng được sử dụng để làm laser toning là “năng lượng phá vỡ các melanosome mà không làm tổn thương tế bào”. Ngoài ra, bởi vì tia laser di chuyển từ bên ngoài vào trong da, các photon giảm dần khi chúng đi vào da. Do đó, năng lượng dùng cho laser toning có thể phá vỡ các melanosome của nám biểu bì bên trong tế bào, nhưng sẽ không thể phá hủy các melanocyte hay melanophages của nám lớp bì. Vì vậy, để điều trị nám lớp bì cần tăng cường năng lượng. Tuy nhiên, điều này sẽ dẫn đến sự phá vỡ các tế bào ở lớp biểu bì và gây ra các tác dụng phụ. Vậy chúng ta có thể điều trị nám lớp bì bằng cách nào?
Có hai cách để điều trị sắc tố lớp bì, chẳng hạn như hình xăm (xem Sect. 7.2.4 trong “Chương 7”). Đầu tiên, các hạt mực xăm được phát nổ bởi tia laser Q-switched Nd: YAG và sau đó nguyên bào sợi thực bào hạt mực xăm, các melanocyte có melanosome và melanophages bị phá hủy. Thứ hai, bằng liệu pháp laser phân đoạn hoặc liệu pháp bắn đục lỗ, các hạt mực xăm hoặc hắc tố melanin được đông tụ hoặc hóa hơi trực tiếp và sau đó thải ra ngoài da thông qua các mảnh vụn biểu bì hoại tử cực nhỏ (MEND), còn được gọi là vận chuyển melanin. Như đã giải thích trước đó, phương pháp đầu tiên có vấn đề và phương pháp thứ hai cũng không được khuyến khích vì nám nhạy cảm với các kích thích và có thể trầm trọng hơn nếu đông tụ hoặc hóa hơi bằng laser Er: Glass hoặc laser CO2. Được giải thích chi tiết trong Sect. 12.9.3.
Vậy có một phương pháp khác? Có một chiến lược, không phải một phương pháp. Chiến lược đầu tiên là loại bỏ sắc tố biểu bì và sau đó loại bỏ sắc tố lớp bì, tức là thực hiện quy trình tuần tự. Cụ thể, các melanosome của lớp biểu bì đầu tiên được điều trị bằng laser toning, và khi tình trạng nám biểu bì được cải thiện đáng kể, nám bì có thể được điều trị bằng cách nâng cao năng lượng. Tuy nhiên, vẫn chưa rõ điều trị nám biểu bì cần dùng laser toning bao nhiêu lần. Ngoài ra, laser toning không thể loại bỏ hoàn toàn nám biểu bì và rất khó phân biệt nám bì bằng mắt thường. Đây là lý do tại sao tôi chưa có một tiêu chuẩn rõ ràng cho việc này.
Dựa trên những điều trên, tôi có kế hoạch điều trị nám da hỗn hợp và nám bì như sau. Mười lần điều trị bằng laser toning đầu tiên được thực hiện cách nhau 1–2 tuần với “mức năng lượng chỉ có thể phá vỡ các melanosome mà không làm tổn thương tế bào”, chỉ điều trị nám biểu bì. 10–20 lần laser toning tiếp theo được thực hiện cách nhau 1–2 tháng với “mức năng lượng chỉ làm tổn thương các tế bào đích mà không gây tổn thương các tế bào xung quanh” điều trị nám hỗn hợp và bì. Phương án điều trị này có thể cải thiện hoàn toàn tình trạng nám bì và nám hỗn hợp, tuy nhiên tình trạng nám tái phát không thể ngăn chặn 100% và cũng cần thời gian rất dài nên tôi không gặp nhiều trường hợp.
Đề xuất thông số laser
Tiếp theo, hãy xem liệu bảy thông số của laser toning thông thường được thực hiện tại phòng khám tư nhân có đúng theo nguyên lý của laser hay không (Bảng 12.9).
Bảng 12.9 So sánh giữa các thông số laser toning thông thường và các thông số laser toning của tôi
| Thông số | Thông số laser toning thông thường | Thông số laser toning của tôi |
| Laser | Laser Q-switched Nd:YAG 1064-nm | Laser Q-switched Nd:YAG 1064-nm |
| Mật độ năng lượng | 1.6–3.5 J/cm2 | £ 2–2.5 J/cm2 (chế độ PTP)
£ 3–3.5 J/cm2 (chế độ 1 shot toning) |
| Spot size | 6-8 mm | Spot lớn nhất, 4 mm (1 shot toning) |
| Pass, shot | Nhiều pass, >1000 shot | £ 1000 shot, 1 shot toning |
| Khoảng nghỉ | 1-2 tuần | ³ 2 tuần |
| Số lần | 5-10 lần | 5/10 lần |
| End point | Ban đỏ xung quanh ngay lập tức | Ban đỏ xung quanh chậm |
Đầu tiên, tôi tin rằng việc sử dụng bước sóng 1064 nm để làm laser toning là đúng vì hiệu ứng bỏ qua biểu bì (xem “Chương 5”). Bước sóng an toàn cho lớp biểu bì là 755 nm do hệ số hấp thụ thấp, nhưng tôi nghĩ 1064 nm với hệ số hấp thụ thấp hơn là an toàn nhất cho nám.
Thứ hai, mặc dù các thông số thông thường sử dụng năng lượng 1,6–3,5 J/cm2, tôi tin rằng năng lượng thấp hơn là phù hợp vì phạm vi điều trị của laser toning hẹp và phạm vi điều trị có thể khác nhau đối với từng bệnh nhân; sử dụng 2,0–2,5 J/cm2 ở chế độ PTP hoặc 1,0–1,25 J/cm2 ở chế độ thông thường hoặc mật độ năng lượng thấp hơn được khuyến cáo. Đối với 1 shot toning, tôi sử dụng mật độ năng lượng nhỏ hơn 4 J/cm2, cụ thể là 3,0–3,5 J/cm2.
Thứ ba, thông số thông thường sử dụng spot size từ 6–8 mm, nhưng spot size lớn hơn có thể được sử dụng để thực hiện nhanh hơn. Tôi sử dụng spot size lớn nhất có thể trong năng lượng đó. Tại sao spot size lớn nên được sử dụng cho laser toning? Một trong những nguyên tắc của laser là spot size càng lớn thì độ xuyên sâu quang (OPD) càng sâu. Vậy chúng ta có đang sử dụng spot size lớn trong laser toning để điều trị melanosome ở lớp bì bằng cách làm sâu OPD không? Có ba yếu tố liên quan đến OPD (Bảng 1.8), đó là spot size, bước sóng và mật độ công suất. Điều quan trọng nhất trong số này là bước sóng (xem Phần 6.4 trong “Chương 6”). Hầu hết các loại laser toning sử dụng laser Q-switched Nd: YAG 1064-nm, vì vậy không cần phải lo lắng về OPD. Nếu vậy, tại sao lại sử dụng spot size lớn? Ưu điểm của spot size lớn không chỉ là OPD sâu hơn mà thời gian thủ thuật cũng ngắn hơn. Nếu spot size nhỏ hơn được sử dụng cho toàn bộ khuôn mặt, thì sẽ cần nhiều lần bắn và thời gian dài hơn. Ngoài ra, bởi vì laser toning chỉ yêu cầu năng lượng thấp, spot size lớn có thể thực hiện được. Tôi cũng sử dụng spot size lớn nhất có thể, thay vì spot size 6–7 mm của laser toning thông thường.
Vậy thì nhược điểm của spot size lớn là gì? Để chiếu tia toàn bộ khuôn mặt không bị thiếu sót, chồng xung là điều không thể tránh khỏi. Khi spot size trở nên lớn hơn, có nhiều vùng chồng xung hơn (Hình 12.19). Trong khu vực chồng xung, năng lượng có thể được tích lũy. Khi thực hiện nhiều lần, năng lượng cao có thể tích tụ ở một số khu vực nhất định, gây ra các tác dụng phụ, như giảm sắc tố dạng đốm. Vì vậy, khi sử dụng spot size lớn, nên tránh nhiều pass hoặc shot. Ngoài ra, để chỉ chiếu tia một khu vực nhỏ, như vết nám hoặc đốm nâu, nên sử dụng spot size nhỏ hơn mà không bị chồng xung. Đó là lý do tại sao trong 1 shot toning, tôi sử dụng spot size nhỏ hơn là 4 mm mà không bị chồng xung.
Thứ tư, thông số thông thường hơn 1000 shot với nhiều pass ở tần số 10 Hz. Nhưng như chúng tôi đã xem xét trong Sect. 12.6.5.3, nhiều pass và nhiều shot không được khuyến khích. Khi thực hiện điều trị bằng laser thông thường, tôi sử dụng ít hơn 1000 shot và chỉ sử dụng một shot toning trên vùng tổn thương.
Thứ năm, các khoảng nghỉ thông thường rất ngắn, thường là 1–2 tuần. Cũng được xem xét trong Sect. 12.6.5.3, khoảng thời gian nghỉ ngắn là một yếu tố nguy cơ, đó là lý do tại sao tôi thực hiện laser toning với khoảng thời gian nghỉ hơn 2 tuần.
Thứ sáu, thông số lặp lại điều trị thông thường lên đến năm đến mười lần. Tôi khuyến cáo nên sử dụng laser toning năm lần cho mỗi 10 lần điều trị, nhưng sau mười lần điều trị, tôi tăng khoảng thời gian nghỉ của laser toning lên 1–2 tháng.
Thứ bảy, thông số thông thường coi end point là “ban đỏ xung quanh”. Nhưng tôi nghĩ rằng end point là “ban đỏ xung quanh muộn.” Như đã xem xét trong quá trình quang nhiệt chọn lọc dưới tế bào, nếu đó là “mức năng lượng chỉ có thể phá vỡ các melanosome mà không làm tổn thương tế bào”, thì tại sao ban đỏ lại xảy ra? Không có lý do rõ ràng nào được viết trong sách laser về lý do tại sao ban đỏ xuất hiện sau laser. Tôi xem xét lý do của ban đỏ sau khi laser như sau. Đầu tiên, trong trường hợp laser xung dài mili giây, nhiệt dư vẫn còn và xuất hiện ban đỏ để bù đắp cho điều này. Trong trường hợp laser Q- switched nano giây, ban đỏ có thể xảy ra do một phần năng lượng được chuyển hóa thành nhiệt. Nhưng phần lớn năng lượng được sử dụng cho hiệu ứng quang cơ, do đó sẽ ít xuất hiện ban đỏ hơn. Thứ hai, ban đỏ có thể xảy ra do viêm. Khi năng lượng của laser Q- switched cao và thành tế bào bị phá vỡ do hiệu ứng quang cơ, axit arachidonic được tiết ra và bị oxy hóa, đồng thời tiết ra các cytokine như prostaglandin (PG) và leukotriene (LT). Các cytokine này gây ra ban đỏ thông qua sự giãn nở của mao mạch và tăng tính thấm thành mạch. Thứ ba, tôi nghĩ nếu hiệu ứng quang cơ phá vỡ thành tế bào và màng đáy, đồng thời làm tổn thương thành mạch ở lớp bì, thì thành mạch sẽ giãn nở theo phản ứng. Trường hợp thứ hai là đặc biệt có vấn đề. Tình trạng viêm có thể dẫn đến PIH, thay vì kết thúc bằng ban đỏ và làm trầm trọng thêm tình trạng nám da. Kinh nghiệm cho thấy PIH ít xảy ra hơn nếu ban đỏ không nặng sau khi điều trị bằng laser.
Dựa trên những điều trên, tôi nghĩ rằng trong một “mức năng lượng chỉ có thể phá vỡ các melanosome mà không làm tổn thương tế bào” thì ban đỏ không nên xảy ra. Ít nhất là ban đỏ phát triển sau một thời gian, chứ không phải ngay sau thủ thuật laser, sẽ an toàn hơn. Đây là lý do tại sao tôi coi end point lâm sàng của điều trị bằng laser là “ban đỏ xung quanh muộn”. Ngược lại, “ban đỏ xung quanh tức thời” được coi là “end point cảnh báo” có nghĩa là tác dụng phụ.
Wattanakrai và cộng sự thu nhận 22 bệnh nhân bị nám và thực hiện laser toning và HQ 2% cho một bên mặt và chỉ HQ 2% cho bên còn lại. Mật độ năng lượng là 3,0–3,8 J/cm2, và end point lâm sàng là sắc tố sáng lên ngay lập tức hoặc ban đỏ nhẹ không có chấm xuất huyết [58]. Kết quả cho thấy vùng mặt được điều trị bằng laser toning kết hợp với HQ có sự cải thiện cao hơn (p <0,001), nhưng 3 người có giảm sắc tố dạng đốm phát triển và 4 người bị tăng sắc tố ngược. Sau 12 tuần, tất cả 22 bệnh nhân đều tái phát nám. End point trong nghiên cứu này đáng chú ý. Không chỉ mật độ năng lượng của laser toning rất cao, mà end point lâm sàng cũng được đặt không chính xác. Theo kinh nghiệm cá nhân của tôi, sắc tố sáng lên ngay lập tức hoặc ban đỏ nhẹ cho thấy năng lượng quá cao.
Nguyên tắc và lựa chọn laser trong điều trị nám
Nếu chúng ta coi nám da là một tình trạng sắc tố, theo nguyên lý và chiến lược của laser sắc tố (xem Sect 7.8 trong “Chương 7”), tôi sử dụng các chiến lược điều trị nám sau đây.
Hãy bắt đầu bằng suy nghĩ về các chiến lược điều trị nám biểu bì. Mô cạnh tranh của nám biểu bì là mô biểu bì bình thường. Đầu tiên, vì mối liên hệ ngang, quang nhiệt có chọn lọc là chiến lược chính. Trong lý thuyết của quá trình quang nhiệt chọn lọc, bước sóng là quan trọng. Hiệu ứng bỏ qua biểu bì yêu cầu laser sắc tố biểu bì sử dụng laser có bước sóng nhỏ hơn 800 nm. Laser gần 800 nm hiệu quả và an toàn. Tuy nhiên, không giống như các tình trạng sắc tố biểu bì, nám là “tế bào hắc tố hoạt động” và có tác dụng phụ nghiêm trọng. Do đó, laser Nd: YAG 1064 nm với hệ số hấp thụ thấp hơn nhiều sẽ an toàn hơn mặc dù không hiệu quả. Đây là lý do tại sao lần đầu tiên tôi sử dụng laser Q- switch Nd: YAG 1064-nm để làm laser toning. Và để điều trị nám biểu bì nhanh hơn, laser alexandrite xung dài 755 nm được sử dụng. Laser xung dài được sử dụng vì hiệu ứng quang nhiệt an toàn hơn hiệu ứng quang cơ khi xem xét thời gian xung. Tuy nhiên, mật độ năng lượng được sử dụng trong sắc tố biểu bì có thể làm trầm trọng thêm tình trạng nám, do đó, nên giảm mật độ năng lượng xuống 50% so với mật độ năng lượng được sử dụng trong sắc tố biểu bì. Bởi vì hệ số hấp thụ thay đổi theo nồng độ của sắc tố, năng lượng nên được điều chỉnh để năng lượng là “yếu với tổn thương tối màu, mạnh với tổn thương sáng màu”. Laser Q-switched có thời gian xung cố định, nhưng khi sử dụng laser xung dài, trước tiên nên sử dụng thời gian xung dài hơn bởi tính nhiệt động học chọn lọc, sau đó các tổn thương không đáp ứng nên được xử lý tuần tự bằng cách sử dụng thời gian xung ngắn.
Thứ hai, việc làm mát biểu bì là không cần thiết. Vì làm mát biểu bì làm giảm nhiệt độ của cả mô bình thường và mô đích, nên mật độ năng lượng phải được tăng lên để có hiệu quả. Vì vậy, làm mát là vô nghĩa khi điều trị sắc tố biểu bì.
Thứ ba, có phương pháp laser phân đoạn hoặc đục lỗ. Tuy nhiên, không nên sử dụng laser CO2 hoặc laser Er: YAG vì có thể gây tổn thương các mô xung quanh do hiện tượng hóa hơi. Mặt khác, laser phân đoạn không bóc tách được coi là an toàn vì cơ chế của chúng là đông tụ. Tuy nhiên, tôi có băn khoăn về việc điều trị nám bằng laser phân đoạn không bóc tách. Điều này sẽ được giải thích sau trong Sect. 12.9.3.
Bây giờ chúng ta hãy nghĩ về các chiến lược điều trị nám lớp bì. Mô cạnh tranh của mô bì là mô biểu bì bình thường. Làm mát biểu bì có vẻ quan trọng nhất vì nó là một mối liên quan theo chiều đứng, nhưng trên thực tế, làm mát biểu bì không có ích lợi gì vì việc sử dụng laser Q-switched trong điều trị sắc tố da.
Theo chiến lược này, đầu tiên, nên sử dụng laser có bước sóng 800 nm trở lên theo lý thuyết về sự phân giải quang nhiệt có chọn lọc và hiệu ứng bỏ qua biểu bì. Để nhắm các tế bào mục tiêu, cần sử dụng laser Q-switched nano giây. Do đó, chỉ có thể sử dụng laser Q-switch Nd: YAG 1064-nm. Đây là lý do tại sao tôi sử dụng laser Q-switched Nd: YAG để điều trị nám lớp bì. Tuy nhiên, năng lượng nên được tăng lên vì melanocyte ở lớp bì hoặc melanophage phải bị phá vỡ. Đối với 1 shot tonig, mật độ năng lượng được tăng lên 4–6 J/cm2. Vì ABNOM, Nevus of Ota và nám bì hiện diện trong các tế bào riêng biệt, lý thuyết năng lượng “yếu với tổn thương tối màu, mạnh với tổn thương sáng màu” là không phù hợp.
Thứ hai, như đã đề cập trước đó, làm mát biểu bì là vô nghĩa.
Thứ ba, ban đầu, sắc tố lớp bì yêu cầu sử dụng chủ động laser phân đoạn hoặc phương pháp đục lỗ. Nhưng tôi không khuyến khích các phương pháp này trong điều trị ABNOM hoặc nám lớp bì. Điều này cũng sẽ được giải thích sau trong Sect. 12.9.3.
Cuối cùng, laser tiến từ bên ngoài da vào lớp biểu bì và bì, vì vậy trước tiên nên loại bỏ các tổn thương biểu bì sau đó thực hiện từng bước một để điều trị các tổn thương ở lớp bì. Vì vậy, đầu tiên tôi điều trị nám biểu bì sau đó tăng năng lượng laser Q-switched Nd: YAG 1064-nm để điều trị nám lớp bì.
Các vấn đề trong các nghiên cứu gần đây về điều trị nám bằng laser
Nhiều nghiên cứu đã được công bố rằng sử dụng laser để điều trị nám, nhưng chúng có một số vấn đề. Đầu tiên, nám xảy ra ở nhiều loại da và mọi chủng tộc trên khắp thế giới, nhưng hầu hết các nghiên cứu chủ yếu về một hoặc hai loại da và một chủng tộc. Thứ hai, các phương pháp đánh giá khác nhau được sử dụng cho mỗi nghiên cứu. Ví dụ, một số nghiên cứu sử dụng chỉ số mức độ nghiêm trọng của vùng nám (MASI) và một số bài báo sử dụng chỉ số mức độ nghiêm trọng của vùng nám đã sửa đổi (mMASI). Do đó, việc so sánh giữa các bài nghiên cứu gặp nhiều khó khăn. Ngoài ra, vẫn chưa có một cách đánh giá tình trạng nám nào khách quan và chính xác. Thứ ba, ít nghiên cứu đối chứng ngẫu nhiên. Do đó, việc xác định kết quả khách quan gặp nhiều khó khăn. Thứ tư, vấn đề lớn nhất là các nhà nghiên cứu không biết nguyên lý hoạt động của laser và chỉ sử dụng một số thông số nhất định, nên dù sử dụng cùng một laser nhưng kết quả vẫn khác nhau, tức là có hiệu quả trong một số nghiên cứu nhưng trong một số nghiên cứu thì chỉ tác dụng phụ xảy ra. Vì vậy, chúng ta nên xem xét các nghiên cứu về điều trị nám dựa trên nguyên lý của laser.
Một nghiên cứu tổng hợp sử dụng IPL trong điều trị nám [28]. Wang và cộng sự (2004) so sánh HQ 4% (nhóm chứng) và sự kết hợp giữa HQ và IPL (nhóm điều trị). 17 bệnh nhân đã trải qua 4 lần IPL trong 16 tuần. Kết quả cho thấy chỉ số melanin giảm 11,6% ở nhóm đối chứng, trong khi giảm 39,8% ở nhóm điều trị. Nhóm điều trị cho thấy sự cải thiện có ý nghĩa thống kê (p <0,05). Tuy nhiên, hai bệnh nhân đã phát triển PIH. Goldman và cộng sự (2011) so sánh ở 56 bệnh nhân, bôi TCT gồm HQ và IPL ở một bên của khuôn mặt (bên điều trị), và dùng giả dược và IPL ở bên còn lại (bên đối chứng) của khuôn mặt. Sau 10 tuần, 57% bên điều trị sáng lên hoặc gần sáng, nhưng chỉ 23% bên đối chứng sáng lên. Figueedlyo và Trancoso và cộng sự (2012) so sánh 62 bệnh nhân dùng TCT với IPL và chỉ dùng TCT. Sau 6 tháng, điểm MASI cải thiện 49,4% và duy trì ở mức 44,9% sau 12 tháng.
Dựa vào ba nghiên cứu trên, chúng tôi có thể kết luận rằng “IPL có tác dụng vừa phải đối với nám và có thể là một lựa chọn ở những người không đáp ứng với thuốc bôi ngoài da. Tuy nhiên, PIH cũng có thể xảy ra, vì vậy cần phải thận trọng”. Nhưng không có đề cập đến các thông số ở đây. Vì vậy, tôi đã tìm kiếm tất cả các tài liệu để tìm các thông số cụ thể (Bảng 12.10).
Bảng 12.10 Các thông số IPL trong ba nghiên cứu khác nhau
| Wang et al. [59] | Goldman [60] | Figueiredo et al. [61] | |
| IPL | Vasculight, ESC/
Sharplan, Israel |
Lumenis One, Lumenis,
Santa Clara, CA |
Limelight, Cutera,
Brisbane, CA, USA |
| Kính lọc | 570 nm | 560 nm | 560 nm |
| Mật độ năng lượng | 26–33 J/cm2 | 14–18 J/cm2 | 12–22 J/cm2 |
| PD (delay)
PD |
3–4 (30–35)
4–5 (ms) |
3–3.5 (10–30)
3–3.5 (ms) |
|
| Lần điều trị thứ 2 | Kính lọc 590–615 | Mật độ năng lượng cao hơn 10% so với lần điều
trị đầu tiên |
|
| End point | Ban đỏ nhẹ xung quanh và các tổn thương da
xám lại |
Sậm màu da nhẹ, không tạo dấu ban đỏ | Một số ban đỏ nhẹ, thoáng qua, sau đó là
sậm màu nhẹ |
| Khoảng nghỉ | 4 buổi cách nhau 4 tuần | Vào tuần thứ 2 và thứ 6 | Một lần |
Trong số ba nghiên cứu, Wang và cộng sự đã sử dụng mật độ năng lượng cao nhất. Nói chung, mật độ năng lượng từ 15–20 J/cm2 được sử dụng khi điều trị sắc tố biểu bì bằng kính lọc 560 nm. Vì vậy, mặc dù Wang đã sử dụng bộ lọc 570 nm, mật độ năng lượng 26–33 J/cm2 vẫn còn rất cao. Điểm kết thúc lâm sàng của IPL khi điều trị sắc tố biểu bì thường là “ban đỏ xung quanh”, nhưng trong bài báo của Wang nó là “màu xám của các tổn thương da,” cũng ngụ ý rằng họ sử dụng năng lượng cao hơn. Do đó, có thể ước tính rằng đây là lý do tại sao PIH xảy ra, so với hai nghiên cứu còn lại. Nếu mật độ năng lượng không cao và vừa phải, tôi tin rằng IPL có thể được sử dụng để điều trị nám mà không có bất kỳ tác dụng phụ cụ thể nào. Và mặc dù IPL có thể không hiệu quả lắm, nó vẫn có thể có hiệu quả trung bình. Tuy nhiên, tôi nghĩ sẽ an toàn khi sử dụng ít năng lượng hơn so với năng lượng được sử dụng để điều trị sắc tố biểu bì vì vấn đề của nám là “tế bào hắc tố hoạt động”.
Điều trị nám bằng laser
Tiếp theo, chúng ta sẽ xem xét một số nghiên cứu về laser được biết là tương đối hiệu quả trong điều trị nám.
Laser alexandrite xung dài
Lee và cộng sự sử dụng laser alexandrite xung dài 755 nm để điều trị nám [62]. Thông số điều trị là 60–80 J/cm2 mà không có thiết bị làm mát động, sử dụng spot size 15 mm của tay cầm phân đoạn, với thời gian xung 0,5–1 ms. Một tia có kích thước 400 μm và 130 tia được chiếu. Mật độ năng lượng 60 J/cm2 với spot size 15 mm của tay cầm phân đoạn tương đương với năng lượng 9,5 J. End point lâm sàng là “ban đỏ xung quanh và / hoặc hình thành lớp vi mài màu xám nhạt.” Kết quả cho thấy điểm mMASI trung bình được cải thiện sau 2 tháng sau đợt điều trị cuối cùng và điểm tự đánh giá của bệnh nhân cao. Có ban đỏ nhẹ, cảm giác nóng rát, vi mài, nhưng không có tác dụng phụ đặc biệt. PIH phát triển ở một bệnh nhân nhưng cải thiện một cách tự nhiên sau 2 tháng theo dõi.
Nghiên cứu này nói về điều trị nám bằng laser alexandrite xung dài. Kết quả tương đối hài lòng. Vì khi điều trị sắc tố biểu bì, quá trình làm mát biểu bì không được thực hiện và thời gian xung tương đối ngắn (0,5-1 ms). Vì thời gian giãn nhiệt (TRT) của lớp đáy được biết là 0,1–0,4 ms, tôi nghĩ có thể tốt hơn nếu giảm nó xuống 0,2 hoặc 0,3 ms.
Điều thú vị ở nghiên cứu này là việc sử dụng tay cầm phân đoạn, tôi tin rằng việc sử dụng tay cầm phân đoạn ở bước sóng mà nước không phải là mục tiêu và xảy ra hiện tượng tán xạ là không thích hợp cho quá trình quang nhiệt phân đoạn. Phương pháp quang nhiệt phân đoạn không chiếu laser toàn bộ da, mà thay vào đó chiếu laser ở chỗ này và chỗ kia và để lại mô bình thường giữa các tia, giảm được tác dụng phụ bằng cách tái tạo nhanh chóng các mô bị hoại tử từ các mô bình thường xung quanh. Tuy nhiên, trong bước sóng ở nơi có sự tán xạ xảy ra, sự hấp thụ xảy ra không chỉ ở nơi laser được chiếu mà còn cả ở những phần không được chiếu laser do sự tán xạ. Đây là lý do tại sao tôi tin rằng tay cầm phân đoạn ở bước sóng mà tại đó sự tán xạ xảy ra không thích hợp cho quá trình quang nhiệt phân đoạn, mà chỉ có tác dụng (1) năng lượng thấp hơn, (2) spot size nhỏ hơn và độ sâu thâm nhập nông hơn, và (3) năng lượng mạnh ở nơi được chiếu laser được chiếu trực tiếp làm tăng khả năng xảy ra các tác dụng phụ.
Trong nghiên cứu này, có một bức tranh thú vị về một bệnh nhân có tiền sử giảm sắc tố dạng đốm do điều trị bằng laser trong phòng khám tư nhân, nhưng tình trạng giảm sắc tố dạng đốm được cải thiện khi sắc tố da trở nên đồng đều sau laser alexandrite xung dài. Hiện tượng giảm sắc tố vẫn thấy dưới đèn Wood, nhưng sau khi vùng sắc tố được cải thiện thì có thể thấy sự cải thiện toàn bộ sắc tố trên khuôn mặt.
Cheng và cộng sự thực hiện laser alexandrite xung dài 4 lần cách nhau hàng tháng trên 23 bệnh nhân bị nám [63]. Các thông số là 0,25 ms, spot size 8 mm với 6–7 J/cm2, và 2-4 pass được thực hiện cho đến khi xuất hiện ban đỏ nhẹ. Điểm số mMASI giảm đáng kể và 10 bệnh nhân (43,5%) mô tả sự cải thiện của họ là rõ rệt và xuất sắc (cải thiện > 60%). Các phương pháp điều trị được chịu đựng tốt với chỉ phản ứng nhẹ trên da với 83,7% phàn nàn về cơn đau nhẹ và hai bệnh nhân phàn nàn về cơn đau dữ dội. Một bệnh nhân bị bóng nước biến mất tự nhiên trong vòng một tuần. Một bệnh nhân phát triển PIH sau điều trị đầu tiên và bị loại khỏi nghiên cứu.
Nghiên cứu này cũng nói về điều trị nám bằng laser alexandrite xung dài. Tương tự như laser toning, hiệu quả tương đối vừa phải, cho thấy sự cải thiện dần dần của nám. Mật độ năng lượng tương đối thấp ở 6–7 J/cm2, nhưng năng lượng dự kiến sẽ cao hơn vì sự chồng xung của hai đến bốn pass. End point lâm sàng cũng là ban đỏ nhẹ, cho thấy rằng năng lượng được sử dụng tương tự như năng lượng được sử dụng để điều trị sắc tố biểu bì. Nghiên cứu này, giống như nghiên cứu trước, cũng có một bệnh nhân bị PIH. Một lần nữa, tôi nghĩ tốt hơn là chỉ nên bắn một shot để có độ chính xác và giảm năng lượng.
Laser phân đoạn không bóc tách
Laser phân đoạn Er: Glass 1550-nm đã được FDA Hoa Kỳ phê duyệt vào năm 2005 để điều trị nám. Tuy nhiên, đối với laser, không phải lúc nào sự chấp thuận của FDA Hoa Kỳ cũng có nghĩa là laser đó an toàn và hiệu quả. Có một quan niệm sai lầm về sự chấp thuận của FDA Hoa Kỳ: sự chấp thuận của FDA Hoa Kỳ đối với các loại thuốc là rất khắt khe, và các loại thuốc được FDA Hoa Kỳ chấp thuận là an toàn, hiệu quả và đáng tin cậy. Nhưng sự chấp thuận của FDA Hoa Kỳ đối với laser không đòi hỏi khắt khe như đối với thuốc. Laser được FDA chấp thuận nếu nó có thể chứng minh được độ an toàn và các nguyên tắc của nó. Do đó, không nên cho rằng bất kỳ loại laser nào đã được FDA Hoa Kỳ chấp thuận là luôn có hiệu quả. Tuy nhiên, chỉ có hai loại laser được biết đến là được FDA Hoa Kỳ phê duyệt để điều trị nám: laser phân đoạn Er: Glass 1550 nm (Fraxel) và laser Q-switched Nd: YAG 1064 nm (Spectra, Lutronic) [28].
Có rất nhiều nghiên cứu về laser phân đoạn không bóc tách 1550-nm (nonablational fractional laser, NAFL) vì đã xuất hiện từ lâu [28]. Chúng ta hãy xem xét một số nghiên cứu này. Kroon và cộng sự (2011) thu nhận 20 bệnh nhân và sử dụng TCT trong 8 tuần (nhóm chứng) và NAFL bốn lần trong khoảng thời gian nghỉ 2 tuần (nhóm điều trị). Cả hai nhóm đều cho thấy sự cải thiện tương tự, nhưng sự hài lòng của bệnh nhân cao hơn ở nhóm điều trị. Sáu tháng sau, cả hai nhóm đều có 50% tái phát, và không có tác dụng phụ cụ thể nào ngoại trừ PIH. Do đó, các tác giả khuyến cáo chỉ sử dụng NAFL ở những bệnh nhân không hiệu quả hoặc không thể sử dụng thuốc bôi làm trắng da. Wind và cộng sự (2010) so sánh nhóm được xử lý với NAFL 1550-nm từ bốn đến năm lần với nhóm sử dụng TCT. Sự hài lòng ở người đánh giá và của bệnh nhân đều cao hơn ở nhóm dùng laser, nhưng PIH xảy ra 31%. Các tác giả của nghiên cứu này cho rằng nguyên nhân gây ra PIH cao hơn nguyên nhân của Kroon và cộng sự (2011) vì mật độ năng lượng đã tăng từ 10 đến 15 mJ. Tourlaki và cộng sự (2014) so sánh NAFL 1540-nm với TCT ở 176 bệnh nhân. Sau 1 tháng điều trị, 67,1% bệnh nhân cải thiện trên 75%, và 21% bệnh nhân cải thiện 51–75%. Tuy nhiên, sau 6 tháng chỉ có 21,1% bệnh nhân duy trì sự cải thiện hơn 75%.
Bây giờ chúng ta sẽ xem xét các tài liệu đã sử dụng NAFL 1927-nm để điều trị nám [28]. Polder và Bruce (2012) đã thực hiện laser phân đoạn 1972-nm từ 3 đến 4 lần vào khoảng thời gian nghỉ hàng tháng trên 14 bệnh nhân. Các thông số là 10–20 mJ với tổng mật độ là 252–784 MTZ/cm2. Theo dõi tại thời điểm 1, 3 và 6 tháng sau khi điều trị cho thấy điểm MASI được cải thiện lần lượt là 51%, 33% và 34%. Lee và cộng sự (2013) đã thực hiện laser phân đoạn 1927 nm trên một nửa khuôn mặt của 25 phụ nữ phương Đông, trong đó có tám bệnh nhân bị nám, ba lần cách nhau 3 tuần. Các thông số là 10 mJ với mật độ mức 3. Điểm MASI cải thiện 5% đối với nửa khuôn mặt không được điều trị bằng laser và 33% đối với nửa khuôn mặt được điều trị bằng laser, ngụ ý rằng điều trị bằng laser là trị nám hiệu quả. Sáu tháng sau, một nửa khuôn mặt không được điều trị bằng laser duy trì điểm số MASI ở mức 12%, trong khi nửa khuôn mặt được điều trị bằng laser duy trì ở mức 28%. Niwa Massaki và cộng sự (2013) điều tra hồi cứu 20 bệnh nhân được điều trị một lần bằng laser phân đoạn 1927-nm. Các thông số là 10–20 mJ/cm2 với độ phủ 60–70% diện tích bề mặt dẫn đến tổng năng lượng là 1,72–4,42 kJ. Một tháng sau khi điều trị, kem HQ 4% được sử dụng như một liệu pháp duy trì. Kết quả cho thấy cải thiện hơn 50% ở 60% bệnh nhân chỉ với một lần điều trị. Điểm MASI cải thiện 53,8%. Nhưng trung bình 10,2 tháng, 33,3% bị tái phát một phần và 13% bị tái phát toàn bộ. Ngoài ra, PIH xảy ra ở hai bệnh nhân.
Đánh giá chung về NAFL về điều trị nám như sau [28].
Thứ nhất, thời gian tái phát của nám sau NAFL muộn hơn so với laser IPL hoặc Q- switched. IPL hoặc laser Q-switched tái phát trong vòng ba tháng sau khi kết thúc điều trị, trong khi NAFL tái phát trong vòng 3-6 tháng. Lý do cho sự tái phát muộn trong NAFL có thể liên quan đến sự cải thiện của lớp bì. Laser Q-switched và IPL chỉ điều trị sắc tố biểu bì, nhưng NAFL cũng có thể cải thiện lớp bì và dẫn đến trẻ hóa, có thể hữu ích cho việc điều trị nám. Nhưng ngay cả khi chúng ta không có NAFL, chúng ta có thể sử dụng một loại laser khác giúp trẻ hóa kết hợp với IPL hoặc laser Q-switched không? Đây là lý do tại sao sau khi laser toning, tôi sử dụng kỹ thuật Genesis với laser Nd: YAG xung dài 1064-nm.
Thứ hai, tương tự như IPL, số lần điều trị là khoảng 3 đến 4 lần, ít hơn so với điều trị bằng laser Q-switched, được thực hiện khoảng tám đến mười lần. Đặc biệt, NAFL 1927-nm hiệu quả hơn các phương pháp điều trị khác chỉ với một lần điều trị.
Thứ ba, laser IPL hoặc Q-switched chỉ được khuyến nghị cho các loại da Fitzpatrick I, II và III, nhưng NAFL cũng có thể được sử dụng cho III và IV. Tôi không đồng ý với điều này, vì IPL hoặc laser Q-switched cũng có thể được sử dụng trên da Fitzpatrick loại III và IV nếu năng lượng được giảm xuống. Trên thực tế, laser toning với laser Q-switched Nd: YAG được sử dụng cho các loại da III, IV, và thậm chí cả V. Vì vậy, đây chỉ là một khuyến nghị chung đã được sử dụng trong quá khứ. Ngược lại, NAFL cũng có thể gây ra nhiều tác dụng phụ khác nhau, bao gồm cả viêm nang lông, nếu da nhạy cảm bất kể loại da Fitzpatrick nào.
Nhận xét về laser phân đoạn không bóc tách
Bởi vì NAFL gây ra đông tụ, và đông tụ là một phản ứng an toàn, NAFLs có ít tác dụng phụ hơn các loại laser khác. Sự xuất hiện của PIH với NAFL trong các nghiên cứu có lẽ là do mật độ năng lượng cao. Để giảm tác dụng phụ và hiệu quả trẻ hóa, các thông số của NAFL nên là “mật độ năng lượng cao và mật độ thấp”. Nhưng đối với bệnh nám, tôi nghĩ rằng mật độ năng lượng cũng nên được giảm bớt. Do đó, nên sử dụng “mật độ năng lượng thấp và mật độ thấp”.
Tuy nhiên, tôi có một số lo lắng về lý thuyết về việc điều trị nám da bằng NAFLs. Đầu tiên, laser phân đoạn với bước sóng 1550 nm tạo ra sự đông tụ đối với lớp biểu bì, màng đáy và lớp bì, và mô được loại bỏ bởi các mảnh vụn biểu bì hoại tử cực nhỏ (MEND). Tôi lo ngại rằng nếu lớp màng đáy đông tụ và vỡ ra, có thể xảy ra hiện tượng không kiểm soát sắc tố, dẫn đến tình trạng nám da trở nên trầm trọng hơn [64].
Thứ hai, cơ chế của laser phân đoạn giúp cải thiện tình trạng nám da là làm đông tụ và giải phóng sắc tố, nhưng nếu thông số này được đặt ở mật độ thấp để an toàn, cải thiện nám sẽ không đáng kể và số lần điều trị sẽ tăng lên. Mặt khác, ưu điểm của NAFL thâm nhập sâu như 1550 nm là làm đông tụ lớp bì sâu hơn, do đó, các ban đỏ kèm theo nám được cải thiện và hiệu quả cải thiện lớp bì cũng có thể nhìn thấy được.
Thứ ba, trong trường hợp 1927 nm, hệ số hấp thụ đối với nước cao, vì vậy nó được coi là an toàn hơn 1550 nm vì không xuyên sâu. Nhưng vì sự đông tụ của màng đáy giống nhau nên tôi tin rằng không có sự khác biệt về kết quả. Thay vào đó, do hệ số hấp thụ đối với nước cao, năng lượng tăng nhẹ có thể gây ra hiện tượng hóa hơi dẫn đến các phản ứng phụ cao hơn. Do đó, việc giảm mật độ năng lượng là quan trọng hơn trong laser 1927 nm so với laser 1550 nm.
Laser mạch máu
Vì có các tổn thương mạch máu trong nám da, cũng có giả thuyết cho rằng điều trị mạch máu có thể có hiệu quả đối với nám da (Hình 12.20). Bây giờ chúng ta sẽ xem xét các nghiên cứu sử dụng laser mạch máu trong điều trị nám.
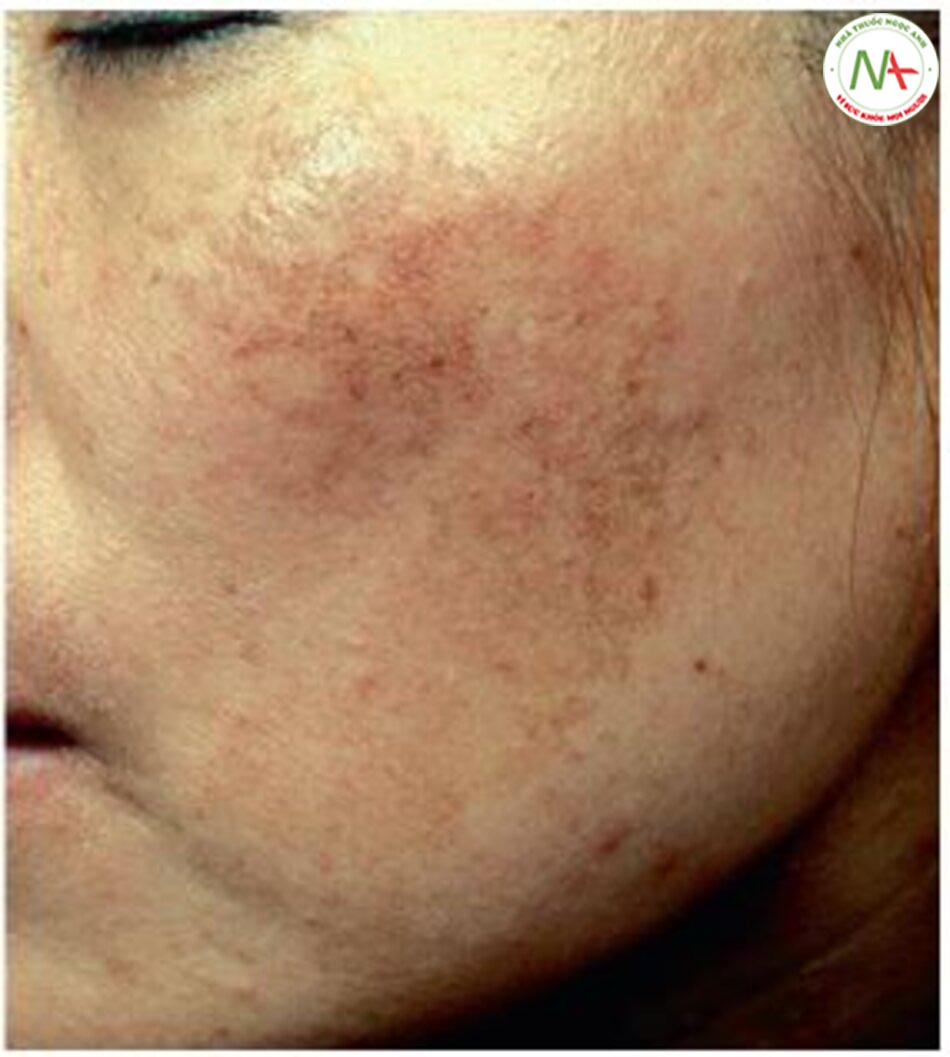
Passeron và cộng sự đã sử dụng TCT (Tri-Luma) mỗi ngày một lần trong 4 tháng ở 18 phụ nữ da trắng bị nám [65]. Điều trị bằng laser nhuộm xung (PDL) (V-beam; Candela Corporation) được bắt đầu sau 1 tháng dùng TCT. Ba phiên PDL được thực hiện trong khoảng thời gian nghỉ 3 tuần trên nửa mặt được chỉ định ngẫu nhiên. Kết quả cho thấy hiệu quả cao hơn đối với các phương pháp điều trị kết hợp. Nhưng chỉ bệnh nhân Fitzpatrick da loại II và III bị ảnh hưởng, và không có sự khác biệt ở bệnh nhân loại da Ba bệnh nhân nhận PDL đã phát triển PIH, tất cả đều thuộc loại da Fitzpatrick IV. Mặc dù bài báo này gợi ý rằng laser mạch máu có thể có hiệu quả đối với nám da, PIH đã được phát triển ở tất cả bệnh nhân loại da Fitzpatrick IV. Đây là lý do tại sao tôi nghĩ rằng việc sử dụng PDL như một laser mạch máu có vẻ không phù hợp với tình trạng nám da ở người Hàn Quốc. Có nhiều loại da Fitzpatrick IV và V ở người Hàn Quốc. Các laser mạch máu khác nên được xem xét.
Một phụ nữ 28 tuổi, đã tham gia vào nghiên cứu trên, đến khám 3 năm sau đó [66]. Kiểm tra cho thấy bên trái điều trị chỉ bằng TCT tái phát, nhưng bên phải điều trị kết hợp với PDL không tái phát (Hình 12.21). Phân tích bề mặt đỏ RBX và kính hiển vi bằng laser cho thấy các mạch máu giảm ở mặt phải được điều trị bằng PDL. Do đó, Passeron cho rằng điều trị bằng mạch máu trong điều trị nám có thể ngăn ngừa sự tái phát của nám.
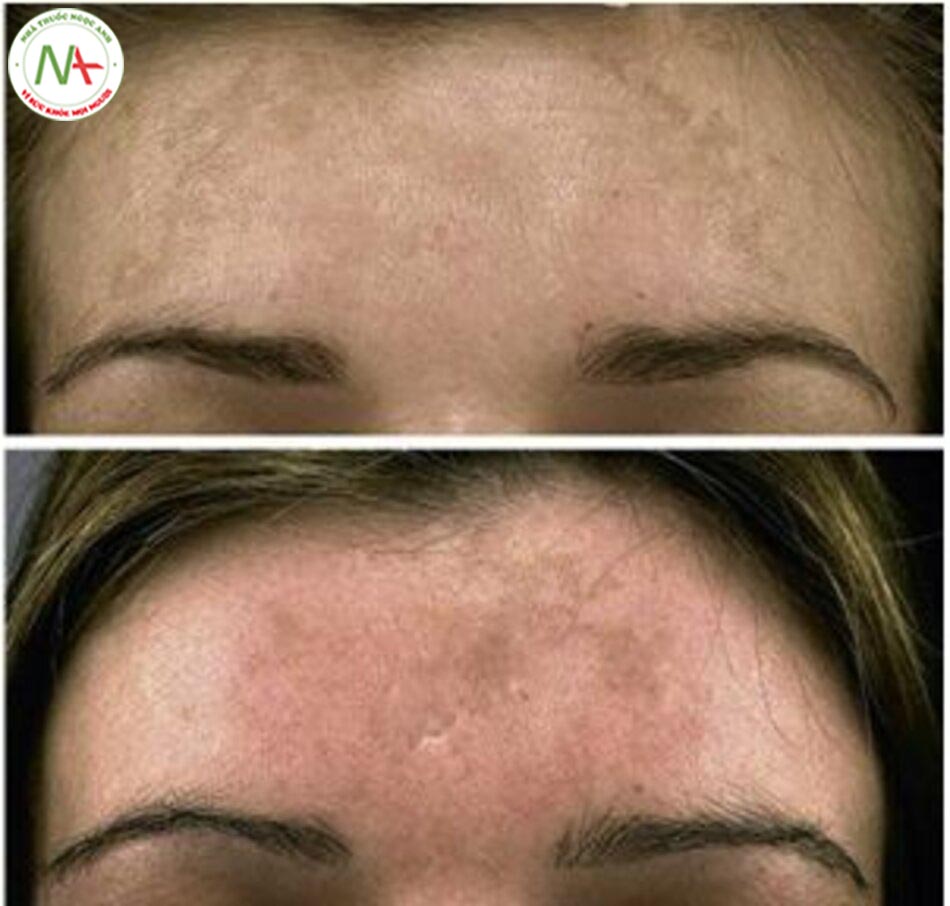
Các tổn thương mạch máu là nguyên nhân hay ảnh hưởng của nám da vẫn còn gây tranh cãi, nhưng nghiên cứu trên cho thấy liệu pháp mạch máu có thể giúp cải thiện tình trạng nám da và ngăn ngừa tái phát. Tuy nhiên, do hiệu ứng bỏ qua biểu bì, PDL, được gọi là laser mạch máu tốt nhất, có nguy cơ gây PIH ở người Hàn Quốc do bước sóng ngắn. Tôi nghĩ rằng laser mạch máu có bước sóng dài nhất, laser Nd: YAG xung dài 1064 nm an toàn hơn PDL, và do đó sử dụng kỹ thuật Genesis.
Ngoài PDL, laser bromua đồng cũng như một laser mạch máu. Lee và cộng sự thực hiện laser bromua đồng trên bệnh nhân bị nám [67]. Kết quả cho thấy điểm MASI trung bình giảm đáng kể sau khi điều trị. Các giá trị của L* phản ánh cường độ của sắc tố tăng lên và các giá trị của a* khi đo lường độ đỏ giảm sau khi điều trị. Sinh thiết cho thấy Melan-A, đại diện cho melanosome, giảm, CD34 và endothelin-1, đại diện cho tế bào nội mô mạch máu giảm, và yếu tố tăng trưởng nội mô mạch máu (VEGF) cũng giảm. Tuy nhiên, có những nghiên cứu trái ngược với kết quả của bài báo trên. Eimpunth và cộng sự (2014) đã sử dụng laser bromua đồng một mình trong điều trị nám da và Hammami Ghorbel và cộng sự (2015) kết hợp laser bromua đồng và TCT trong điều trị nám da, và cả hai đều không có tác dụng [28]. Nói cách khác, hiệu quả của phương pháp điều trị nám bằng laser bromua đồng vẫn còn nhiều tranh cãi.
Picolaser
Với sự ra đời gần đây của picolasers (laser sub-nanosecond), sự quan tâm đến việc điều trị nám da bằng cách sử dụng picolasers đã tăng lên. Tuy nhiên, vẫn chưa có nhiều nghiên cứu được công bố.
Lee và cộng sự thực hiện picolaser ở ba bệnh nhân, hai bệnh nhân bị nám và một bệnh nhân với PIH [68], được xử lý bằng picolaser alexandrite 755 nm. Tất cả bệnh nhân đều là người Hàn Quốc với loại da IV và không còn đáp ứng với phương pháp điều trị bằng laser Q-switched. Sau nhiều đợt điều trị, một bệnh nhân báo cáo cải thiện khá và hai bệnh nhân báo cáo cải thiện tốt. Bởi vì nghiên cứu này là case report, rất khó để kết luận rằng picolasers có hiệu quả đối với nám và PIH, nhưng chúng cho thấy tiềm năng trong điều trị nám. Kết quả sinh thiết cũng cho thấy picolasers xử lý sắc tố tốt hơn và có ít tác dụng phụ lên biểu bì hơn so với laser Q-switched Nd: YAG 532 nm.
Lee và cộng sự so sánh các picolaser 755 nm và laser Q-switched Nd: YAG 1064 nm trong điều trị nám [69]. Bên phải mặt của mỗi bệnh nhân được dùng picolaser 755 nm và bên mặt còn lại được dùng laser Q-switched Nd: YAG 1064 nm. End point lâm sàng của cả hai loại laser là “ban đỏ nhẹ và sưng không có chấm xuất huyết”. Sau 3 tháng theo dõi, mức độ sạch cao hơn được thấy ở phía picolaser 755 nm so với phía Q-switched Nd: YAG 1064 nm. Nghiên cứu này so sánh các picolasers và laser Q-switch Nd: YAG. Tuy nhiên, người ta không biết liệu hai loại laser có cung cấp năng lượng giống nhau cho các melanosome hay không. Các end point lâm sàng là giống nhau, nhưng nhiệt độ chính xác không được biết. Do đó, còn quá sớm để kết luận rằng picolasers hiệu quả hơn laser Q- switch Nd: YAG.
Khi xem xét các phản ứng laser-mô (xem “Chương 2”), tôi tin rằng tác dụng của cả hai laser là tương tự nhau vì cả hai laser đều phá vỡ các melanosome. Tuy nhiên, tác dụng phụ của picolasers sẽ ít hơn so với laser Q-Switch Nd: YAG. Nhưng điều này không có nghĩa là picolasers không có bất kỳ tác dụng phụ nào.
Điều trị kết hợp
Như đã nói ở trên, có nhiều phương pháp điều trị nám khác nhau, nhưng không có phương pháp điều trị đơn lẻ nào hiệu quả. Do đó, một số bài báo cho rằng điều trị kết hợp là cách tốt nhất để điều trị nám, tôi cũng đồng ý [5, 70].
Nhưng chỉ đơn giản trộn tất cả các phương pháp hiệu quả thì có thể gây ra tác dụng phụ do các quy trình chồng nhau của cùng một cơ chế. Ví dụ, laser alexandrite xung dài và laser lột da đều làm tổn thương lớp biểu bì và làm tăng sự luân chuyển của biểu bì, do đó, tác dụng phụ dễ xảy ra hơn khi chúng được kết hợp với nhau. Vì vậy, sẽ rất lý tưởng nếu phân loại các phương pháp điều trị theo cơ chế của chúng và kết hợp các phương pháp điều trị thích hợp mà không bị chồng chéo. Chiến lược điều trị nám có thể được chia thành ba loại, xem xét trên quá trình sản xuất melanin. Đầu tiên, hoạt động của các melanocyte nên giảm. Thứ hai, sự hình thành melanosome nên bị ức chế. Thứ ba, quá trình thoái hóa melanosome nên được thúc đẩy (Bảng 12.11).
Bảng 12.11 Chiến lược điều trị nám
| Chiến lược điều trị nám |
| 1. Giảm hoạt động của melanocyte
2. Ức chế sự hình thành melanosome 3. Thúc đẩy sự thoái hoá melanosome A. Loại bỏ melanin biểu bì B. Loại bỏ melanin lớp bì |
Hầu hết các laser không ức chế sản xuất melanin như HQ, nhưng chúng thúc đẩy quá trình loại bỏ melanin ở biểu bì tương tự như lột da bằng hóa chất. Laser được sử dụng trong điều trị sắc tố có thể chỉ loại bỏ một cách chọn lọc các sắc tố gây nám da và không làm tổn thương các mô xung quanh. Ngược lại, lột da bằng hóa chất không đặc hiệu, gây tổn thương không chỉ vùng nám mà còn cả các mô xung quanh. Do đó, tôi tin rằng laser an toàn và hiệu quả hơn phương pháp lột da bằng hóa chất trong điều trị nám.
Liệu pháp hiệu quả
Kết hợp các cơ chế gây nám, nguyên lý laser và các tài liệu về tác dụng của điều trị nám, tôi tin rằng các phương pháp sau đây có thể hữu ích trong việc điều trị nám (Bảng 12.12).
Bảng 12.12 Nguyên nhân và liệu pháp điều trị nám hiệu quả
| Nguyên nhân – di truyền, hormone, tia UV, mỹ phẩm, v.v. |
| 1. Rối loạn chức năng hàng rào biểu bì — Kem dưỡng ẩm, điện di
2. Sự phá vỡ màng đáy — Lột da hoá chất bề mặt (GA 50%), kỹ thuật genesis 3. Viêm lớp bì — Trẻ hóa không bóc tách, kỹ thuật genesis, ‘tiêm căng bóng’ 4. Tăng sắc tố 1. Giảm hoạt động của melanocyte — Laser toning 2. Ức chế sự hình thành melanosome — Axit tranexamic, Vit C, glabridin 3. Thúc đẩy sự thoái hoá melanosome I. Loại bỏ melanin biểu bì — Laser toning, laser xung dài 755 nm II. Loại bỏ melanin lớp bì — Laser Q-Switched 1064-nm |
Thứ nhất, do không biết 100% nguyên nhân gây ra nám nên chúng ta không thể trị nám 100%. Nhưng nếu bệnh nhân dùng thuốc tránh thai, chuyển họ sang thuốc tránh thai estrogen liều thấp (ví dụ: Yaz®) có thể hữu ích. Ngoài ra, điều trị nguyên nhân như tránh kích ứng mãn tính (ví dụ: mỹ phẩm) và chống nắng kỹ là điều quan trọng nhất để điều trị nám.
Thứ hai, vùng da bị tổn thương cần được sửa chữa. Lớp biểu bì sẽ được hưởng lợi từ chất dưỡng ẩm và điện di. Màng đáy sẽ được hưởng lợi từ việc bong tróc ít gây kích ứng như GA 50% và kỹ thuật genesis. Để cải thiện lớp bì, laser không bóc tách, kỹ thuật genesis và tiêm axit hyaluronic trong da, còn được gọi là “tiêm căng bóng” có thể hữu ích.
Thứ ba, để giảm hoạt động của các melanocyte, laser toning có tác dụng cắt bỏ đuôi gai của melanocyte. Thuốc làm trắng da tại chỗ để ngăn chặn sản xuất melanin có thể hữu ích. Axit tranexamic, axit ascorbic (vitamin C) và glabridin là lựa chọn giá rẻ mà không có tác dụng phụ.
Cuối cùng, sắc tố đã có trên da được coi là sắc tố tự có và được loại bỏ bằng laser sắc tố. Tuy nhiên, vì laser có thể làm tình trạng nám trở nên trầm trọng hơn, nên chọn loại laser thích hợp, không có tác dụng phụ và năng lượng phải yếu. Tôi sử dụng laser toning và laser alexandrite xung dài 755 nm để điều trị nám biểu bì. Laser toning được thực hiện trên toàn bộ khuôn mặt với chế độ PTP 2,1–2,5 J/cm2, và sau đó một shot toning được thực hiện ở 4 J/cm2 hoặc thấp hơn. Trong “Chap. 7 ” chúng ta đã đánh giá rằng loại laser an toàn nhất cho sắc tố biểu bì là laser alexandrite xung dài. Năng lượng được sử dụng cho sắc tố biểu bì trong laser alexandrite xung dài thường là 16–20 J/cm2, nhưng tôi sử dụng 8–10 J/cm2, và tôi coi end point lâm sàng là ban đỏ xung quanh muộn, thường xảy ra khi bệnh nhân kết thúc điều trị và sẵn sàng để về nhà. Các sắc tố vẫn tồn tại ngay cả sau khi điều trị nám biểu bì kéo dài hoặc các sắc tố có màu xám hoặc xanh được coi là nám lớp bì và có thể được điều trị bằng laser Q-switched Nd: YAG 1064-nm bằng cách tăng năng lượng, tương tự như điều trị hình xăm.
Lời khuyên về điều trị nám
Tôi đã điều trị nám hơn chục năm nay và học được rất nhiều điều qua quá trình thử và sai. Sau đây là danh sách những lời khuyên có thể hữu ích cho những ai mới điều trị nám.
Trước tiên, khi một bệnh nhân nám lần đầu đến khám, bạn nên kiểm tra xem trước đó đã từng điều trị gì chưa. Bạn cũng nên hỏi xem phương pháp điều trị có hiệu quả không hoặc có bất kỳ tác dụng phụ nào không. Nếu không có tác dụng phụ và có hiệu quả, và chỉ có vấn đề tái phát thì có thể lặp lại quy trình tương tự. Nhưng nếu có tác dụng phụ, cần cân nhắc thay đổi phương pháp điều trị. Ví dụ, nếu trước đây đã từng thực hiện phương pháp điều trị nám bằng laser và giảm sắc tố dạng đốm thì không nên thử dùng lại phương pháp điều trị nám bằng laser và có thể dự đoán rằng nó sẽ không dễ dàng cải thiện bằng phương pháp điều trị nám thông thường.
Thứ hai, không nên nói với bệnh nhân rằng nám có thể chữa khỏi 100%. Dù đã áp dụng tất cả các phương pháp điều trị nám, bao gồm cả liệu pháp hành vi, dùng thuốc và điều trị bằng laser, nhưng nám vẫn không thể điều trị khỏi 100%. Ngoài ra, cần phải điều trị nhiều lần. Gần đây tôi nghĩ rằng nên thực hiện laser toning 20–30 lần thay vì 10 lần khi điều trị nám da.
Thứ ba, không nên nhấn mạnh vào việc làm sáng toàn bộ khuôn mặt mà là cải thiện sắc tố đen để phù hợp với tông màu tổng thể của khuôn mặt. Điều này áp dụng cho tất cả các phương pháp trị sắc tố, kể cả nám. Để làm sáng tone cho cả khuôn mặt không phải là điều dễ dàng. Sẽ dễ hơn khi làm cho các đốm nâu tối màu hoặc nám sáng trở nên sáng hơn và điều này cũng có ít tác dụng phụ hơn.
Thứ tư, cần phối hợp các phương pháp điều trị. Có rất nhiều nguyên nhân và cơ chế gây ra nám và không có một phương pháp điều trị nám da duy nhất. Tuy nhiên, như đã giải thích trước đó, cơ chế nền tảng của mỗi phương pháp điều trị cần được xem xét để các cơ chế này không bị chồng chéo.
Thứ năm, không phải tất cả mọi người đều đáp ứng như nhau đối với mỗi lần điều trị. Một số bệnh nhân có thể xuất hiện các tác dụng phụ. Vì vậy, bệnh nhân cần được theo dõi cẩn thận bất cứ khi nào thực hiện điều trị để xem có bất kỳ dấu hiệu cải thiện hoặc tác dụng phụ nào không.
Thứ sáu, nám tái phát. Vì vậy, điều trị duy trì cần được chuẩn bị trước. Phòng ngừa thông qua liệu pháp hành vi cũng là cần thiết, và cần tư vấn đầy đủ với bệnh nhân liên quan đến cải thiện môi trường da và lặp lại laser toning.
Tài liệu tham khảo
- Goldsmith LA, Katz SI, Gilchrest BA, Paller AS, Leffell DJ, Wolff K et al (2012) Fitzpatrick’s dermatology in general McGraw-Hill Professional, New York
- Jeong JY, Koo BS, Kim JH, Lee JD, Jang JM, Jung JW et al (2019) Melasma (Korean). MDworld, Seoul
- Lee MH, Noh TK, Lee JH, Roh MR, Im Na J, Jung EC et al (2016) Clinicoepidemiological features of melasma in Korean patients at five university hospitals: a cross-sectional multicenter study. Korean J Dermatol 54(7):532–537
- Kar HK, Gupta L, Chauhan A (2012) A comparative study on efficacy of high and low fluence Q- switched Nd: YAG laser and glycolic acid peel in melasma. Indian J Dermatol Venereol Leprol 78(2): 165–171
- Rodrigues M, Pandya AG (2015) Melasma: clinical diagnosis and management options. Australas J Dermatol 56(3):151–163
- Negishi K, Kushikata N, Tezuka Y, Takeuchi K, Miyamoto E, Wakamatsu S (2004) Study of the incidence and nature of “very subtle epidermal melasma” in relation to intense pulsed light Dermatol Surg 30(6):881–886. discussion 6
- Lee WJ, Kim YJ, Noh TK, Chang SE (2013) Formation of new melasma lesions in the periorbital area following high-fluence, 1064-nm, Q-switched Nd/YAG J Cosmet Laser Ther 15(3):163– 165
- Kang S, Fitzpatrick TB (2019) Fitzpatrick’s McGraw-Hill Education, New York
- Passeron T (2013) Melasma pathogenesis and influencing factors – an overview of the latest J Eur Acad Dermatol Venereol 27(Suppl 1):5–6
- Kasai K (2007) Skin spots treatment clinics (Korean edition). Shinheung Med Science, Seoul
- Grimes PE, Yamada N, Bhawan J (2005) Light microscopic, immunohistochemical, and ultrastructural alterations in patients with Am J Dermatopathol 27(2):96–101
- Kang WH, Yoon KH, Lee ES, Kim J, Lee KB, Yim H et al (2002) Melasma: histopathological characteristics in 56 Korean Br J Dermatol 146(2):228–237
- Kang HY, Bahadoran P, Suzuki I, Zugaj D, Khemis A, Passeron T et al (2010) In vivo reflectance confocal microscopy detects pigmentary changes in melasma at a cellular level resolution. Exp Dermatol 19(8):e228–e233
- Noh TK, Choi SJ, Chung BY, Kang JS, Lee JH, Lee MW et al (2014) Inflammatory features of melasma lesions in Asian skin. J Dermatol 41(9):788–794
- Kang HY, Hwang JS, Lee JY, Ahn JH, Kim JY, Lee ES et al (2006) The dermal stem cell factor and c-kit are overexpressed in Br J Dermatol 154(6):1094–1099
- Kim M, Kim SM, Kwon S, Park TJ, Kang HY (2019) Senescent fibroblasts in melasma Exp Dermatol 28(6):719–722
- Kim EH, Kim YC, Lee ES, Kang HY (2007) The vascular characteristics of melasma. J Dermatol Sci 46(2):111–116
- Hernandez-Barrera R, Torres-Alvarez B, Castanedo-Cazares JP, Oros-Ovalle C, Moncada B (2008) Solar elastosis and presence of mast cells as key features in the pathogenesis of melasma. Clin Exp Dermatol 33(3):305–308
- Kwon S, Park K (2014) Clues to the pathogenesis of melasma from its histologic findings. Pigment Disord 1(141):2
- Kwon SH, Hwang YJ, Lee SK, Park KC (2016) Heterogeneous pathology of melasma and its clinical Int J Mol Sci 17(6):824
- Lee DJ, Lee J, Ha J, Park KC, Ortonne JP, Kang HY (2012) Defective barrier function in melasma J Eur Acad Dermatol Venereol 26(12):1533–1537
- Shin JH, Kang WH (2006) Two cases of melasma with unusual histopathologic findings. J Korean Med Sci 21(2):368–370
- Torres-Alvarez B, Mesa-Garza IG, Castanedo-Cazares JP, Fuentes-Ahumada C, Oros-Ovalle C, Navarrete-Solis J et al (2011) Histochemical and immunohistochemical study in melasma: evidence of damage in the basal Am J Dermatopathol 33(3):291–295
- Textbook compilation committee in Korean Dermatological Association (2014) Text book of dermatology, 6th edn. (Korean). Daehanuihak, Seoul
- Committee C, Sl C, Kim IH, Kang JS, Park SH, Chung KY et al (2016) Laser and light treatment in Asian Koonja, Paju
- Oluwatobi A, Ogbechie-Godec EN (2017) Melasma: an up-to-date comprehensive Dermatol Ther J 7(3):305–318
- Ball Arefiev KL, Hantash BM (2012) Advances in the treatment of melasma: a review of the recent Dermatol Surg 38(7 Pt 1):971–984
- Trivedi MK, Yang FC, Cho BK (2017) A review of laser and light therapy in Int J Womens Dermatol 3(1):11–20
- Rivas S, Pandya AG (2013) Treatment of melasma with topical agents, peels and lasers: an evidence- based Am J Clin Dermatol 14(5):359–376
- Rendon M, Berneburg M, Arellano I, Picardo M (2006) Treatment of J Am Acad Dermatol 54(5 Suppl 2):S272–S281
- Shankar K, Godse K, Aurangabadkar S, Lahiri K, Mysore V, Ganjoo A et al (2014) Evidence-based treatment for melasma: expert opinion and a Dermatol Ther (Heidelb) 4(2):165–186
- Chan R, Park KC, Lee MH, Lee ES, Chang SE, Leow YH et al (2008) A randomized controlled trial of the efficacy and safety of a fixed triple combination (fluocinolone acetonide 01%, hydroquinone 4%, tretinoin 0.05%) compared with hydroquinone 4% cream in Asian patients with moderate to severe melasma. Br J Dermatol 159(3):697–703
- Tse TW, Hui E (2013) Tranexamic acid: an important adjuvant in the treatment of J Cosmet Dermatol 12(1):57–66
- Bala HR, Lee S, Wong C, Pandya AG, Rodrigues M (2018) Oral tranexamic acid for the treatment of melasma: a Dermatol Surg 44(6):814–825
- Wu S, Shi H, Wu H, Yan S, Guo J, Sun Y et al (2012) Treatment of melasma with oral administration of tranexamic Aesthet Plast Surg 36(4):964–970
- Karn D, Kc S, Amatya A, Razouria EA, Timalsina M (2012) Oral tranexamic acid for the treatment of Kathmandu Univ Med J (KUMJ) 10(40):40–43
- Tosti A, Grimes PE, Padova MP (2012) Color atlas of chemical Springer-Verlag, Heidelberg: New York 38. Jeong JY (2010) Clinical skin care (Korean). Seoul, MDworld
- Erbil H, Sezer E, Tastan B, Arca E, Kurumlu Z (2007) Efficacy and safety of serial glycolic acid peels and a topical regimen in the treatment of recalcitrant J Dermatol 34(1):25–30
- Se YJ, Sung EC, Bak H, Choi JH, Kim I-H (2008) New melasma treatment by collimated low fluence Q-switched Nd: YAG Korean J Dermatol 46(9):1163–1170
- Kim JH, Kim H, Park HC, Kim IH (2010) Subcellular selective photothermolysis of melanosomes in adult zebrafish skin following 1064-nm Q-switched Nd:YAG laser J Invest Dermatol 130(9):2333–2335
- Kim JH, Jeong SY, Shin JB, Hc P, Kim IH (2008) Subcellular selective photothermolysis in zebrafish: an electron microscopic evidence after Q-switched Nd:YAG laser ablation. Korean J Dermatol 46(20):187
- Mun JY, Jeong SY, Kim JH, Han SS, Kim IH (2011) A low fluence Q-switched Nd:YAG laser modifies the 3D structure of melanocyte and ultrastructure of melanosome by subcellular-selective J Electron Microsc 60(1):11–18
- Kim JE, Chang SE, Yeo UC, Haw S, Kim IH (2013) Histopathological study of the treatment of melasma lesions using a low-fluence Q-switched 1064-nm neodymium:yttrium-aluminium-garnet Clin Exp Dermatol 38(2):167–171
- Zhou X, Gold MH, Lu Z, Li Y (2011) Efficacy and safety of Q-switched 1,064-nm neodymium- doped yttrium aluminum garnet laser treatment of Dermatol Surg 37(7):962–970
- Ryu HJ, Kim J (2013) A case of mottled hypopigmentation after low-fluence 1,064-nm Q-switched neodymium-doped yttrium aluminum garnet laser J Cosmet Laser Ther 15(5):290–292
- Lee MC, Hu S, Chen MC, Shih YC, Huang YL, Lee SH (2009) Skin rejuvenation with 1,064-nm Q- switched Nd:YAG laser in Asian patients. Dermatol Surg 35(6):929–932
- Kim MJ, Kim JS, Cho SB (2009) Punctate leucoderma after melasma treatment using 1064-nm Q- switched Nd:YAG laser with low pulse J Eur Acad Dermatol Venereol 23(8):960–962
- Gokalp H, Akkaya AD, Oram Y (2016) Long-term results in low-fluence 1064-nm Q-Switched Nd:YAG laser for melasma: is it effective? J Cosmet Dermatol 15(4):420–426
- Kim T, Cho SB, Oh SH (2010) Punctate leucoderma after 1,064-nm Q-switched neodymium-doped yttrium aluminum garnet laser with low-fluence therapy: is it melanocytopenic or melanopenic? Dermatol Surg 36(11):1790–1791
- Chan NP, Ho SG, Shek SY, Yeung CK, Chan HH (2010) A case series of facial depigmentation associated with low fluence Q-switched 1,064 nm Nd: YAG laser for skin rejuvenation and Lasers Surg Med 42(8):712–719
- Wong Y, Lee SS, Goh CL (2015) Hypopigmentation induced by frequent low-fluence, large-spot- size QS Nd: YAG laser treatments. Ann Dermatol 27(6):751–755
- Jang YH, Park JY, Park YJ, Kang HY (2015) Changes in melanin and melanocytes in mottled hypopigmentation after low-Fluence 1,064-nm Q-switched Nd: YAG laser treatment for melasma. Ann Dermatol 27(3):340–342
- Tian B (2017) The Asian problem of frequent laser toning for melasma. J Clin Aesthet Dermatol 10(7):40–42
- Kim HS, Jung HD, Kim HO, Lee JY, Park YM (2012) Punctate leucoderma after low-fluence 1,064- nm quality-switched neodymium-doped yttrium aluminum garnet laser therapy successfully managed using a 308-nm excimer Dermatol Surg 38(5):821–823
- Park SH, Yeo WC, Koh WS, Park JW, Noh NK, Yoon CS (2014) Laser dermatology plastic surgery, 2nd (Korean). Koonja, Seoul
- Choi CP, Yim SM, Seo SH, Ahn HH, Kye YC, Choi JE (2015) Retreatment using a dual mode of low-fluence Q-switched and long-pulse Nd: YAG laser in patients with melasma aggravation after previous therapy. J Cosmet Laser Ther 17(3):129–134
- Wattanakrai P, Mornchan R, Eimpunth S (2010) Low-fluence Q-switched neodymium-doped yttrium aluminum garnet (1,064 nm) laser for the treatment of facial melasma in Asians. Dermatol Surg 36(1): 76–87
- Wang CC, Hui CY, Sue YM, Wong WR, Hong HS (2004) Intense pulsed light for the treatment of refractory melasma in Asian Dermatol Surg 30(9):1196–1200
- Goldman MP, Gold MH, Palm MD, Colon LE, Preston N, Johnson LA et al (2011) Sequential treatment with triple combination cream and intense pulsed light is more efficacious than sequential treatment with an inactive (control) cream and intense pulsed light in patients with moderate to severe Dermatol Surg 37(2):224–233
- Figueiredo Souza L, Trancoso SS (2012) Single-session intense pulsed light combined with stable fixed-dose triple combination topical therapy for the treatment of refractory melasma. Dermatol Ther 25(5):477–480
- Lee MK, Min KS, Park EJ, Kim KH, Kim KJ (2016) A retrospective analysis of the treatment of melasma using a fractional long-pulsed alexandrite laser in Korean Dermatol Surg 42(8):952–960
- Cheng CY, Huang YL, Lee MC, Chang SL, Lin YF, Hu S (2017) Pulsed alexandrite laser for treatment of melasma in Asian patients. J Cosmet Laser Ther 19(4):210–214
- Choi JR, Won CH, Oh ES, An J, Chang SE (2013) Does altered basement membrane of melasma lesion affect treatment outcome in Asian skin? Am J Dermatopathol 35(1):137–138
- Passeron T, Fontas E, Kang HY, Bahadoran P, Lacour JP, Ortonne JP (2011) Melasma treatment with pulsed-dye laser and triple combination cream: a prospective, randomized, single-blind, split- face Arch Dermatol 147(9):1106–1108
- Passeron T (2013) Long-lasting effect of vascular targeted therapy of J Am Acad Dermatol 69(3): e141–e142
- Lee HI, Lim YY, Kim BJ, Kim MN, Min HJ, Hwang JH et al (2010) Clinicopathologic efficacy of copper bromide plus/yellow laser (578 nm with 511 nm) for treatment of melasma in Asian Dermatol Surg 36(6):885–893
- Lee YJ, Shin HJ, Noh TK, Choi KH, Chang SE (2017) Treatment of melasma and post-inflammatory hyperpigmentation by a picosecond 755-nm alexandrite laser in Asian patients. Ann Dermatol 29(6):779–781
- Lee MC, Lin YF, Hu S, Huang YL, Chang SL, Cheng CY et al (2018) A split-face study: comparison of picosecond alexandrite laser and Q-switched Nd: YAG laser in the treatment of melasma in Lasers Med Sci 33(8):1733–1738
- Li JY, Geddes ER, Robinson DM, Friedman PM (2016) A review of melasma treatment focusing on laser and light Semin Cutan Med Surg 35(4):223–232
Bài viết về nám khá chi tiết của bác sĩ Jae Dong Lee, tác giả cuốn sách rất hay về laser trong da liễu “Principles and Choice of Laser Treatment in Dermatology- With Special Reference to the Asian Population”.
- Điểm đặc biệt của bác sĩ Jae Dong Lee là tác giả có kiến thức nền tảng về vật lý laser, hiểu rõ cơ chế của laser trong da liễu nên tác giả có những đánh giá cũng như phản biện rất đáng tham khảo về các nghiên cứu trước đó, đặc biệt nhất là sự chia sẻ rất tâm huyết những kinh nghiệm riêng của bản thân và tổng hợp tài liệu khá toàn diện.
- Các bài về nám đã xuất bản hiện nay khá nhiều, đa số là những nghiên cứu nhỏ, một số bài tổng hợp nhưng cũng chỉ được một số khía cạnh trong nám, riêng bài này có lẽ toàn diện nhất cho đến hiện nay.
- Hy vọng bài này giúp ích được mọi người trong hành trình điều trị nám cho bệnh nhân cũng như cho bản thân.

