Bệnh huyết học
Tiếp cận – đánh giá – xử trí các rối loạn về Acid Base, dịch và điện giải
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
Sách Acid – Base, Fluids, and Electrolytes Made Ridiculously Simple – tái bản lần thứ 3 của tác giả là bác sĩ Richard A. Preston được biên dịch thành tiếng Việt Nam bởi nhóm bác sĩ: Nguyễn Thế Bảo, Nguyễn Thế Thời, Đặng Gia Uyên được đào tạo tại Trường Đại học Y Dược Cần Thơ và bác sĩ Liêu Minh Huy được đào tạo tại Đại học Y Dược Thành phố Hồ Chí Minh.
Lời ngỏ:
Không thể phủ nhận rằng, tiếp cận – đánh giá – xử trí các rối loạn về Acid Base, dịch và điện giải đã trở nên quá quen thuộc và thiết yếu trong công tác thực hành hằng ngày ở mọi cơ sở lâm sàng. Có thể nói, đây là một kỹ năng cần được chú tâm trau chuốt dù cho bạn có lựa chọn chuyên khoa nào của y học. Công tác này không chỉ quan trọng khi bệnh nhân thể hiện dấu hiệu của những rối loạn rõ rệt mà còn là một bước đánh giá bắt buộc trước khi thực hiện một số phương pháp điều trị.
Để giúp cho quý bạn đọc, đặc biệt là các bạn sinh viên y khoa Việt Nam mong muốn tiếp cận với tài liệu từ những nền y học phát triển trên thế giới, nhóm dịch xin giới thiệu bản dịch của quyển sách “Acid-base, Fluids, and Electrolytes Made Ridiculously Simple” – tái bản lần thứ 3 của tác giả là bác sĩ Richard A. Preston. Quyển sách này được nhóm dịch cân nhắc chọn lựa vì nó mang đến kiến thức về các quá trình không chỉ sinh lý mà còn sinh lý bệnh của các rối loạn toan-kiềm, dịch và điện giải thường gặp trên lâm sàng. Thêm vào đó, quyển sách còn được thiết kế để mang đến kiến thức một cách cô đọng, rõ ràng, dễ ghi nhớ. Ngoài ra, hệ thống bài tập minh họa theo sau mỗi chương sách vừa giúp bạn đọc hình dung rõ bối cảnh lâm sàng của rối loạn, vừa giúp các bạn ghi nhớ và vận dụng các kỹ năng mà sách giới thiệu. Một các chủ quan, nhóm dịch nhận định rằng quyển sách mang đến nhiều quan điểm độc đáo, khác biệt nhưng hiệu quả, rất thích hợp cho các bạn sinh viên chập chững tiếp cận đến lĩnh vực này.
Dù chỉ mang tới một bản dịch không chuyên, nhưng nhóm dịch đã nỗ lực rất nhiều để mang đến cho các bạn bản dịch hoàn chỉnh của sách. Với hy vọng có thể giúp quý bạn đọc củng cố kiến thức bằng nguồn tài liệu ngoại văn, nhóm dịch đã và đang cố gắng để hoàn thành bản dịch sớm nhất có thể. Trước mắt, kế hoạch của nhóm là gửi đến bạn đọc bản dịch theo từng chương mà nhóm hoàn thành, sau đó sẽ tập hợp lại thành một quyển hoàn chỉnh. Sản phẩm này được hình thành hoàn toàn từ tâm huyết và nỗ lực của các thành viên nhóm dịch, với mục đích đã nêu rõ ở trên. Song, do nhiều nguyên nhân khách quan và chủ quan mà không thể phủ nhận là sự không chuyên trong công tác dịch thuật của nhóm, sai sót trong quá trình thực hiện là không tránh khỏi. Mong nhận được sự đón nhận và phản hồi của quý đọc giả. ĐÂY LÀ BẢN MỚI NHẤT, ĐƯỢC DỊCH TRỰC TIẾP TỪ QUYỂN GỐC, HIỆN KHÔNG CÓ BẢN TIẾNG ANH MIỄN PHÍ. Mọi ý kiến đóng góp của anh/chị và các bạn vui lòng gửi về mail: ntbao.y41@student.ctump.edu.vn.
Các khái niệm cơ bản
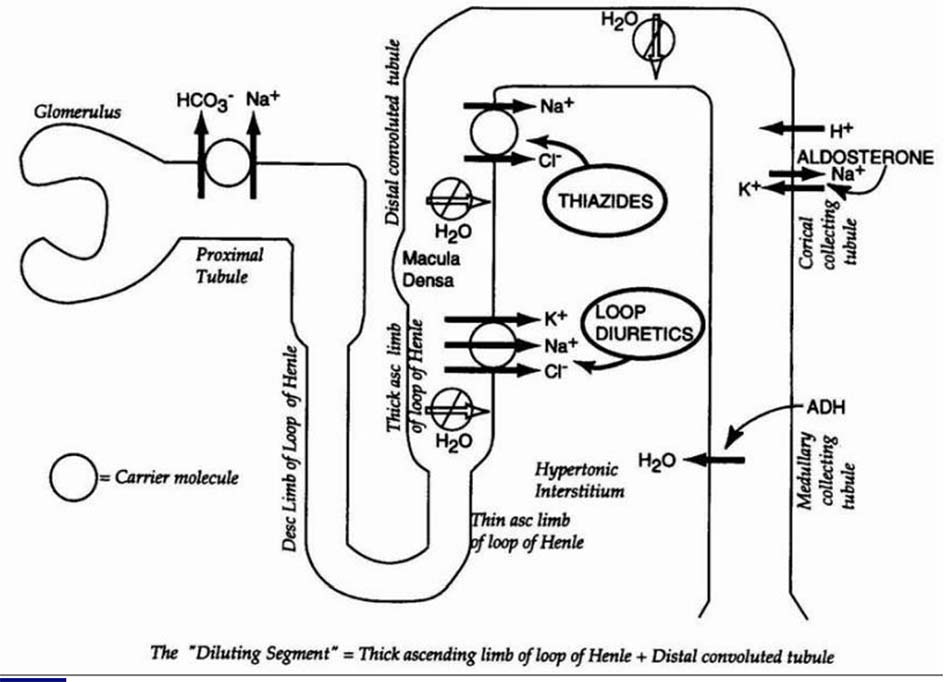
Phần này sẽ giới thiệu ngắn gọn về sinh lý học, cũng chính là chìa khóa để hiểu về các rối loạn của nước, điện giải và acid-base trên lâm sàng. Chương tổng quan này sẽ giúp bạn xây dựng nền móng cho sự hiểu biết đầy đủ hơn về sinh lý bệnh, chẩn đoán và điều trị các rối loạn sẽ được thảo luận trong các chương sau. Bảng tóm tắt ngắn gọn về sinh lý ống thận được trình bày ở Hình. 1-1.
CÁC NGĂN DỊCH TRONG CƠ THỂ
Tổng lượng nước trong cơ thể (total body water-TBW) chiếm khoảng 60% trọng lượng cơ thể ở nam giới và khoảng 50% ở nữ giới (xem Bảng 1-2). Tỷ lệ này giảm dần theo tuổi và tỉ lệ nghịch với lượng mỡ trong cơ thể. Dịch trong cơ thể được chia làm 2 ngăn: nội bào và ngoại bào. Nội bào chiếm 2/3 tổng lượng dịch cơ thể và tạo nên thể tích dịch nội bào (intracellular fluid volume-ICFV). 1/3 tổng lượng dịch còn lại nằm ở ngăn ngoại bào và tạo nên thể tích dịch ngoại bào (extracellular fluid volume-ECFV), trong đó thể tích ở khoảng kẽ hay gian bào chiếm 3/4, còn lại huyết tương chiếm 1/4 ECFV. Nước di chuyển tự do và nhanh chóng giữa tất cả các ngăn này để đáp ứng với sự thay đổi nồng độ chất tan nhằm duy trì trạng thái cân bằng thẩm thấu giữa các ngăn trong cơ thể.
| Bảng 1-2: Các ngăn dịch của cơ thể | |
| ECFV (1/3 TBW) | ICFV (2/3 TBW) |
| Natri 135-145 mEq/L . Kali 3.5-5.0 mEq/L. Clo 95-105 mEq/L. Bicarbonate 22-26 mEq/L. Glucose 90-120 mg/dl. Canxi 8.5-10.0 mg/dl. Magie 1.4-2.1 mEq/L. Urea Nitrogen 10-20 mg/dl. |
Natri 10-20 mEq/L. Kali 130-140 mEq/L. Magie 20-30 mEq/L. Urea Nitrogen 10-20 mg/dl. |
| Ở nữ giới: TBW = 0.5 x trong lượng cơ thể (kg). Ở nam giới: TBW = 0.6 x trọng lượng cơ thể (kg). Thể tích dịch nội bào = 2/3 TBW. Thể tích dịch ngoại bào = 1/3 TBW. Độ thẩm thấu tính được (Calculated osmolal) = 2 x [natri] + [glucose/18] + [Urea Nitrogen trong máu hay BUN]/2.8 Osmolal gap = OSM(đo được) – OSM(tính được) |
|
SINH LÝ BỆNH HỌC VỀ NATRI VÀ NƯỚC
Cách tiếp cận về sinh bệnh học của natri và nước dưới đây có thể sẽ khác với những gì bạn đã biết trước đó, Tác giả tin rằng việc đánh giá riêng biệt tình trạng natri (yếu tố quyết định thể tích dịch ngoại bào) cũng như của nước (yếu tố quyết định nồng độ natri huyết thanh) là rất quan trọng. Do đó, các vấn đề quan trọng cần được làm rõ trên lâm sàng là bệnh nhân có 1) vấn đề của natri, 2) vấn đề của nước hoặc 3) vấn đề của cả natri và nước. Đây là khái niệm sẽ được triển khai trong chương này và cũng được sử dụng để giải quyết những vấn đề ở những chương sau của quyển sách.
Các hệ thống điều chỉnh lượng natri và nước trong cơ thể hoạt động cùng nhau để:
- Giữ nồng độ natri ngoại bào trong khoảng hẹp (135-145 mEq/L).
- Giữ thể tích ngăn dịch ngoại bào trong khoảng giới hạn thích hợp.
Sinh lý về Natri – điều hòa thể tích dịch ngoại bào
Natri là cation ngoại bào chủ yếu và có vai trò hết sức quan trọng để duy trì nồng độ thẩm thấu và thể tích dịch ngoại bào.
Nếu tổng lượng natri ở ngoại bào tăng thì sẽ làm gia tăng thể tích dịch ngoại bào, thậm chí có thể gây quả tải. Những ví dụ điển hình cho thấy tăng lượng natri ở ngoại bào dẫn đến quá tải thể tích dịch ngoại bào (có thể gọi đơn giản là quá tải thể tích) như tình trạng phù trong suy tim, xơ gan và hội chứng thận hư. Tăng lượng natri ngoại bào dẫn đến sự tăng cao của thể tích dịch ngoại bào và biểu hiện trên lâm sàng qua triệu chứng phù. Ngoài ra, các biểu hiện lâm sàng khác của quá tải ECFV là tràn dịch màng phổi, phù phổi và báng bụng.
Nếu tổng lượng natri trong ngăn dịch ngoại bào giảm, thì ngược lại thể tích dịch ngoại bào sẽ giảm, từ đó gây thiếu hụt thể tích dịch ngoại bào. Giảm thể tích dịch ngoại bào (gọi đơn giản là giảm thể tích) biểu hiện: giảm độ căng của dạ, nhịp tim nhanh và hạ huyết áp tư thế. Quá tải ECFV là hậu quả của việc quá dư thừa natri ngoại bào và giảm ECFV là hậu quả của việc thiếu hụt đáng kể lượng natri ngoại bào. Trên thực hành lâm sàng, nhiều bệnh nhân có giảm thể tích hoặc quá tải thể tích nhẹ có thể không có bất kỳ biểu hiện điển hình nào. Thường có những trường hợp quá tải hay giảm thể tích, mà ngay cả với những bác sĩ lâm sàng dày dặn kinh nghiệm cũng khó có thể phát hiện được.
Bởi vì natri phần lớn bị giới hạn ở ngăn ngoại bào nên lượng natri ở ngăn ngoại bào được đề cập như tổng lượng natri cơ thể. Thuật ngữ này đúng một cách tương đối vì chỉ một lượng nhỏ natri nằm ở nội bào và một lượng đáng kể natri liên kết với các proteoglycan ở khoảng gian bào thì không tham gia vào hoạt động thẩm thấu. Nếu tổng lượng natri cơ thể tăng, thể tích dịch ngoại bào sẽ tăng và thậm chí có thể gây phù. Ngược lại, nếu tổng lượng natri cơ thể giảm từ đó gây thiếu hụt thể tích dịch ngoại bào.
Sự cân bằng giữa lượng natri nhập và lượng natri bài xuất qua thận giúp xác định được lượng natri trong ngăn ECF và qua đó biết được ECFV. Bình thường, thận sẽ chịu trách nhiệm điều chỉnh sự bài tiết của natri để giữ cho lượng ECFV nằm trong giới hạn chấp nhận được. Khi lượng ECFV tăng, thận sẽ tăng bài xuất natri để ngăn chặn quá tải ECFV. Khi ECFV giảm, thận sẽ giảm bài xuất natri để ngăn chặn việc thiếu hụt ECFV.
Có ba hệ thống chính điều hòa tổng lượng natri và từ đó điều hòa kích thước của ECFV. Mỗi một hệ thống đều có con đường hướng tâm (nhận cảm) và con đường ly tâm (đáp ứng) để kiểm soát natri. Nhánh hướng tâm sẽ nhận cảm kích thước của ECFV và nhánh ly tâm có hiệu lực tương ứng làm tăng hay giảm lượng natri bài xuất.
- Các thụ thể nằm trong các tế bào cạnh cầu thận giúp nhận cảm sự thay đổi trong tưới máu thận và đáp ứng bằng cách tạo ra những thay đổi trong việc giải phóng renin, từ đó kích hoạt hệ thống renin-angiotensin-aldosterone. Renin được bài tiết để đáp ứng với tình trạng giảm áp lực tưới máu tiểu động mạch đến của thận, giảm lượng Na+ và Cl- đến ống lượn xa của thận và bởi kích thích hệ thần kinh giao cảm. Renin xúc tác chuyển angiotensinogen thành angiotensin I, sau đó angiotensin I lại chuyển thành angiotensin II bởi men chuyển. Angiotensin II trực tiếp thúc đẩy quá trình giữ natri ở thận và kích thích giải phóng aldosterone bởi lớp cầu của tuyến thượng thận. Aldosteron có vai trò giúp tái hấp thu natri tại ống lượn xa của thận.
- Các thụ thể nhận cảm thể tích nằm trong các tĩnh mạch lớn và trong tâm nhĩ. Chúng nhạy cảm với những thay đổi nhỏ về thể tích dịch trong quá trình đưa máu về tĩnh mạch và đổ đầy tâm nhĩ. Khi lượng máu đổ về tâm nhĩ tăng cao, các thụ thể này sẽ được kích hoạt và giải phóng các chất kích thích bài xuất natri ra nước tiểu, giúp tăng bài xuất natri qua thận.
- Các thụ thể nhận cảm áp lực của máu phân bố ở động mạch chủ và xoang động mạch cảnh. Những thụ thể này nhạy cảm với sự giảm thể tích dịch ngoại bào, từ đó kích hoạt hệ thần kinh giao cảm, giúp thận giữ lại natri.
Đây là một số con đường quan trọng cho thấy mối liên kết giữa việc thay đổi về kích thước của ECFV (được xác định bằng tổng lượng natri của ECFV) với sự thay đổi về bài tiết natri của thận. Vấn đề đáng lưu ý là thông thường khi ECFV tăng, cơ chế tăng bài tiết natri được kích hoạt để ngăn chặn quá tải ECFV; và khi ECFV giảm, các con đường được kích hoạt để thúc đẩy thận giữ natri để ngăn chặn sự thiếu hụt của ECFV.
Các bàn luận trước đây về sự điều hòa natri không đề cập đến nồng độ natri ngoại bào. Nồng độ natri ngoại bào được xác định bởi các cơ chế kiểm soát nước, từ đó kiểm soát lượng nước liên quan mật thiết đến lượng natri ở ngăn ngoại bào. Việc đo nồng độ natri huyết thanh trên thực tế lâm sàng không cho chúng ta biết bất cứ thông tin đáng tin cậy nào về tổng lượng natri trong khoang dịch ngoại bào hoặc kích thước của thể tích dịch ngoại bào. Nồng độ natri huyết thanh chỉ cho chúng ta biết về lượng nước so với lượng natri. Tại thời điểm này còn quá sớm, nhưng tác giả vẫn muốn đề cập rằng: việc thiếu hụt thể tích đáng kể có thể làm tăng sự tái hấp thu nước tại thận do kích hoạt giải phóng ADH. Qua đó, việc giữ nước có thể dẫn đến giảm nồng độ natri huyết thanh nhanh chóng và nguy hiểm ở những bệnh nhân có thiếu hụt thể tích nhưng vẫn tiếp tục bổ sung nước hoặc được truyền nước tự do qua đường tĩnh mạch.
Nồng độ thẩm thấu và trương lực
Chất tan chính của ECFV bao gồm natri, glucose và ure. Độ thẩm thấu huyết thanh có thể được tính toán gần đúng bằng công thức: OSM(tính được)=2 X [nồng độ natri] + [nồng độ glucose]/18+[BUN]/2.8
Trong đó, nồng độ natri huyết thanh tính bằng mEq/L, nồng độ glucose và lượng nitơ có trong ure (Blood Urea Nitrogen-BUN) được tính bằng mg/dL. Nồng độ natri có trong dịch ngoại bào được xác định thông qua lượng nước có natri ở trong ngăn ngoại bào. Về mặt định lượng, nồng độ natri cho đến nay là yếu tố đóng góp chính vào tổng nồng độ thẩm thấu của huyết thanh. Nồng độ natri bất thường cho chúng ta biết rằng có sự bất thường trong việc điều hòa lượng nước trong ngăn ngoại bào.
Việc phân biệt rõ về nồng độ thẩm thấu và tính trương lực có ý nghĩa quan trọng. Nồng độ thẩm thấu được xác định bằng tổng nồng độ chất tan trong một ngăn chứa chất lỏng. Trương lực là tổng hợp tác dụng của tất cả các chất tan để tạo ra động lực thẩm thấu gây ra chuyển động của nước từ ngăn này sang ngăn khác (lời của dịch giả: hiểu một cách đơn giản, trương lực (tonicity) chính là nồng độ thẩm thấu CÓ HIỆU QUẢ, tức là nồng độ thẩm thấu tạo ra sự di chuyển của nước). Để tăng trương lực ở ngoại bào, chất tan phải được giữ lại ở trong ngăn ngoại bào. Tức là, chất tan không có khả năng di chuyển từ ngăn ngoại bào qua ngăn nội nào, do đó làm tăng áp suất thẩm thấu và nước di chuyển vào ngăn ngoại bào. Nước di chuyển từ nội bào ra ngoại bào sẽ giúp thiết lập trạng thái cân bằng thẩm thấu. Các chất hòa tan có khả năng gây ra chuyển động của nước bao gồm natri, glucose, mannitol và sorbitol, và do đó những chất này được gọi là “chất thẩm thấu hiệu quả”. Natri chiếm phần lớn trong ngăn ngoại bào vì nó được bơm Natri-Kali-ATPase bơm ra khỏi tế bào, do đó việc bổ sung thêm natri vào dịch ngoại bào làm cho nước di chuyển ra khỏi tế bào và làm tế bào bị teo lại. Vì vậy, natri là một chất thẩm thấu hiệu quả vì nó có khả năng tác động lên sự di chuyển của nước.
Nồng độ natri ngoại bào là yếu tố chính quyết định trương lực của huyết tương. Do đó, khi độ trương lực tăng, thường là do nồng độ natri ngoại bào tăng. Trương lực tăng là tác nhân chính gây khát và tăng tiết hormone chống bài niệu (ADH), những yếu tố quan trọng quyết định tổng lượng nước cơ thể. Nếu nồng độ natri tăng lên sẽ kích thích gây khát nước (dẫn đến tăng lượng nước nhập) và tiết ADH (dẫn đến tái hấp thu nước bởi thận). Nồng độ natri tăng cao cho chúng ta biết rằng có quá ít nước so với natri.
Glucose là một chất thẩm thấu hiệu quả nhưng thường được hấp thu vào tế bào. Do đó, bình thường glucose không đóng góp nhiều vào nồng độ thẩm thấu hay trương lực huyết thanh. Tuy nhiên, khi đường huyết không được kiểm soát tốt ở bệnh nhân đái tháo đường, nồng độ glucose trong huyết tương tăng cao một cách nghiêm trọng có thể tạo môi trường ưu trương đáng kể trong huyết tương và do đó nước di chuyển từ nội bào ra ngoại bào.
Urê góp phần vào nồng độ thẩm thấu, nhưng nó đi qua màng tế bào dễ dàng và do đó sẽ phân bổ đồng đều ở các ngăn dịch trong tổng lượng nước cơ thể. Bởi vì urê di chuyển tự do từ ngăn này sang ngăn khác theo gradient nồng độ của chính nó, nên không tác động lên sự di chuyển của nước qua lại giữa các ngăn dịch. Do đó, urê không góp phần vào độ trương lực và không phải là chất thẩm thấu hiệu quả. Urê sẽ làm tăng độ thẩm thấu huyết thanh đo được, nhưng nó đi qua màng tế bào dễ dàng và không góp phần vào sự di chuyển của nước hoặc co rút tế bào.
Việc điều hòa trương lực giúp ổn định trạng thái hydrat hóa của tế bào và từ đó ổn định kích thước tế bào. Tế bào não được đặc biệt quan tâm. Hầu hết các triệu chứng quan trọng và dấu hiệu do bất thường về trương lực là do não trương lên (phù não) để đáp ứng với tình trạng hạ natri máu hoặc co lại do tăng natri máu. Nếu trương lực của ECFV giảm đột ngột, nước sẽ di chuyển vào ngăn nội bào, dẫn đến tế bào sẽ phình to. Ngược lại, khi trương lực của ECFV tăng nhanh thì nước sẽ di chuyển khỏi tế bào và não sẽ co.
Osmolal gap (khoảng trống thẩm thấu)
Sự khác biệt giữa nồng độ thẩm thấu đo được và nồng độ thẩm thấu tính toán được gọi là osmolal gap: OSM GAP = OSM(đo được)-OSM(tính toán).
Giá trị OSM gap lớn hơn 10 mOsm/L là bất thường và cho thấy có sự hiện diện của một chất ngoại sinh. Sự gia tăng đáng kể osmolal gap có ý nghĩa giúp gợi ý có sự hiện diện của nhiều loại hợp chất ngoại sinh không góp phần vào chỉ số nồng độ thẩm thấu tính toán nhưng lại có hoạt động thẩm thấu nên khi xét nghiệm sẽ được đo lường. Hiểu biết về osmolal gap có thể hữu ích trong bệnh cảnh cấp cứu nhằm tầm soát những chất nghi ngờ mà bệnh nhân nuốt phải. Natri, glucose và ure không làm tăng osmolal gap vì chúng ảnh hưởng đến cả độ thẩm thấu đo được và tính toán được. Bảng 1-3 liệt kê một số chất quan trọng làm tăng osmolal gap.
| Bảng 1-3: Các nguyên nhân tăng osmolal gap |
| Ethanol. Isopropanol. Methanol. Ethylene glycol*. Propylene glycol*. Sorbitol Mannitol. *Đồng thời cũng gây toan chuyển hóa tăng Anion gap |
Sinh lý nước – điều hòa nồng độ natri huyết thanh (trương lực)
Nồng độ natri huyết thanh từ trước đến nay vẫn luôn là nhân tố quan trọng nhất tham gia vào trương lực của ngoại bào. Do đó, trương lực ngoại bào phần lớn được xác định bởi nồng độ natri ngoại bào. Các cơ chế điều hòa nội môi sẽ thêm vào hoặc loại bỏ nước khỏi cơ thể để đáp ứng với những thay đổi về trương lực (nồng độ natri) của ngăn dịch ngoại bào và giữ trương lực huyết tương không đổi. Điều này có ý nghĩa quan trọng trong việc giữ ổn định về trạng thái hydrat hóa và kích thước tế bào. Việc nhập đủ lượng nước được đảm bảo thông qua cơ chế khát còn nguyên vẹn và khả năng cung cấp nước (nguồn nước sẵn có). Tăng nồng độ natri ngoại bào thường là nguyên nhân gây tăng trương lực ngoại bào, dẫn đến cảm giác khát. Hệ thống điều hòa này được tóm lược như sau: Sự gia tăng nồng độ thẩm thấu của dịch ngoại bào dù chỉ vài mOsm/L nhưng sẽ tạo cảm giác khát đáng kể. Các kích thích khác gây khát như tăng angiotensin II và suy giảm đáng kể ECFV. Khát nước là một tác nhân kích thích mạnh mẽ đến nỗi nếu một người có cơ chế khát bình thường và có khả năng tiếp cận được với nguồn nước thì ít khi tiến triển đến tăng natri máu.
Vai trò điều hòa nước của thận
Thận đáp ứng với sự thay đổi trương lực dịch ngoại bào bằng cách điều chỉnh lượng nước được bài xuất. Trong trường hợp tăng trương lực dịch ngoại bào, thận sẽ giảm bài xuất nước bằng cách cô đặc nước tiểu lại so với huyết tương. Khi có thiếu hụt cơ chế cô đặc nước tiểu, thì thận sẽ mất đi khả năng dự trữ nước lại thích hợp (tái hấp thu nước), từ đó gây mất nước và tăng natri máu.
Ngược lại, trong trường hợp giảm trương lực dịch ngoại bào, thận sẽ tăng bài xuất nước bằng cách tạo ra nước tiểu loãng hơn so với huyết tương. Nếu cơ chế làm loãng nước tiểu bị thiếu hụt thì thận sẽ mất khả năng bài xuất nước, từ đó gây giữ nước và hạ natri máu.
Để giữ cho trương lực của ECFV (nồng độ natri) không đổi, cần phải có:
- Cơ chế gây khát nước còn nguyên vẹn.
- Độ lọc cầu thận (GFR) thích hợp.
- Sự phân bố nước đến cả phân đoạn có chức năng cô đặc và pha loãng của quai Henle và ở ống lượn xa.
- Cơ chế cô đặc và pha loãng còn nguyên vẹn ở các ống thận.
- Sự kích hoạt và ức chế thích hợp của ADH.
- Khả năng đáp ứng của thận với ADH.
Thực tế, tất cả các rối loạn lâm sàng gây tăng và giảm natri máu có thể hiểu được và ghi nhớ bằng cách dựa vào các bất thường trên một số cơ chế tham gia điều hòa nước.
Độ lọc cầu thận (GFR)
Cả sự cô đặc nước tiểu (dẫn đến giữ lại nước) hay sự pha loãng (dẫn đến tăng cường bài xuất nước) đều cần có một mức GFR thích hợp. Giả sử, nước và các chất hòa tan không được lọc vào các ống thận, thì bằng cách nào thận có thể cô đặc hay pha loãng nước tiểu để điều hòa sự cân bằng nước? GFR chỉ cần giảm 20% so với bình thường thì thận đã bắt đầu gặp vấn đề trong việc cô đặc hay pha loãng nước tiểu.
Sự phân bố nước đến vị trí pha loãng nước tiểu của quai Henle và ống lượn xa.
Nếu một lượng lớn dịch lọc cầu thận được tái hấp thu ở ống lượn gần, thì không đủ nước để có thể bài xuất ở ống lượn xa. Việc tăng tái hấp thu nước ở ống lượn gần dẫn đến giữ nước và gây hạ natri máu. Hai tình huống gây tăng tái hấp thu nước ở ống lượn gần và là nguyên nhân quan trọng gây hạ natri máu là: Sự thiếu hụt thể tích (thường do bệnh nhân uống nhiều nước liên tục sau nôn ói), dẫn đến tăng tái hấp thu nước ở ống lượn gần. Các trường hợp gây phù: suy tim sung huyết, xơ gan và hội chứng thận hư cũng gây tăng tái hấp thu nước ở ống lượn gần.
Cơ chế cô đặc nước tiểu ở thận
Ngoài việc tái hấp thu 20-30% lượng natri đã lọc, ngành lên quai Henle còn tạo nên tính ưu trương của mô kẽ tủy thận và gradient nồng độ ở tủy thận cần thiết cho sự cô đặc của nước tiểu. Natri được bơm từ quai Henle nhờ vào kênh đồng vận chuyển Na+ -K+ -Cl- vào mô kẽ tủy, cung cấp thêm độ thẩm thấu cần thiết để tạo ra gradient nồng độ ưu trương ở tủy thận. Gradient nồng độ ưu trương ở vùng tủy thận cần thiết cho sự tái hấp thu nước từ ống góp và từ đó giúp nước tiểu được cô đặc thích hợp. Nhờ vào tác động của ADH, ống góp trở nên thấm nước (lời dịch giả: nhờ vào tác động lên các kênh aquaporin để tăng vận chuyển nước). Khi dịch lọc đi qua ống góp, nước sẽ rời khỏi lòng ống và đi vào khoảng kẽ ưu trương theo chiều gradient nồng độ của nó và nhờ đó được tái hấp thu. Kết quả là nước tiểu được cô đặc. Thuốc lợi tiểu quai ức chế sự tái hấp thu natri ở quai Henle và làm suy giảm sự hình thành gradient nồng độ của vùng tủy thận. Do đó, thuốc làm giảm khả năng cô đặc nước tiểu của thận. Nhiều bệnh nhân mắc bệnh thận mãn tính, đặc biệt là các bệnh ống thận – mô kẽ, cũng có thể gây ra các thiếu hụt đáng kể về khả năng cô đặc nước tiểu ở thận.
Cơ chế pha loãng nước tiểu ở thận
Cả ngành lên của quai Henle ở đoạn vỏ thận và ống lượn xa đều tái hấp thu natri và để lại nước bởi vì tế bào biểu mô ống thận ở vùng này không thấm nước. Kết quả là natri được bơm đi trong khi nước vẫn được giữ lại ở lại lòng ống, làm cho dịch lọc trong lòng ống trở nên loãng hơn.
Ở quai Henle, natri, clo và kali được vận chuyển ra khỏi lòng ống bởi kênh đồng vận chuyển Na+ -K+ -2Cl- và không vận chuyển nước. Cơ chế của thuốc lợi tiểu quai là ức chế kênh này. Tại ống lượn xa, natri và clo cũng được vận chuyển ra ngoài lòng ống bởi kênh đồng vận chuyển Na+ -Cl- . Đây là cơ chế quan trọng trong việc pha loãng nước tiểu. Ống lượn xa tạo ra nước tiểu loãng bằng cách bơm natri và clo ra khỏi lòng ống và giữ lại nước. Thuốc lợi tiểu Thiazid ức chế kênh đồng vận chuyển này và do đó làm giảm khả năng pha loãng nước tiểu của thận. Nhóm thuốc lợi tiểu quai làm giảm khả năng pha loãng nước tiểu ít hơn nhóm lợi tiểu thiazide bởi vì ống lượn xa có thể vượt qua được tác dụng của thuốc lợi tiểu quai và tiếp tục thực hiện nhiệm vụ pha loãng của mình dù có sự hiện diện của thuốc lợi tiểu quai. Việc thuốc lợi tiểu quai ức chế sự tái hấp thu natri tại quai Henle có thể làm giảm gradient nồng độ ở đoạn tủy thận, dẫn đến suy giảm khả năng cô đặc nước tiểu của thận.
ADH
Sự hiện diện hay vắng mặt của ADH là điều kiện quan trọng nhất để quyết định xem cuối cùng nước tiểu cô đặc hay pha loãng. Khi trương lực tại ECFV tăng nhẹ cơ thể sẽ đáp ứng bằng cách tiết ra ADH. Mà nồng độ natri là yếu tố chính yếu quyết định trương lực nên sự thay đổi nồng độ natri cũng là tác nhân kích thích cơ thể tiết ADH. ADH làm tăng tính thấm của ống góp đối với nước và cho phép nước di chuyển theo gradient nồng độ của nó để được tái hấp thu vào mô kẽ ở vùng tủy có tính ưu trương. Bên cạnh đó do thận tái hấp thu nước dưới tác dụng của ADH sẽ làm giảm trương lực của ECFV. Sự bài tiết ADH rất nhạy cảm. Chỉ một thay đổi nhỏ tầm vài mOsm/L có thể kích thích osmoreceptor ở vùng hạ đồi và dẫn đến tăng tiết ADH. Khi có mặt ADH, độ thẩm thấu nước tiểu có thể cao đến 1200 mOsm/L và có thể thấp cỡ 50 mOsm/L khi ADH vắng mặt. Một số chất kích thích không thẩm thấu có thể gây tiết ADH, mặc dù trương lực ECFV không tăng.
ECFV giảm trầm trọng có thể “vượt qua” sự kiểm soát thẩm thấu của ADH. Khi thể tích dịch giảm sâu, thì thậm chí với nồng độ natri máu bình thường hoặc ngay cả khi hạ natri máu thì vẫn có thể kích thích tiết ADH. Khi thể tích dịch giảm đáng kể có hiện diện đồng thời với hạ natri máu, thì việc bù dịch có thể làm cho hiệu lực của ADH bị “dập tắt”, từ đó làm điều hòa thể tích nhanh chóng và gây ra hiện tượng bài tiết một lượng lớn nước tiểu. Do vậy mà nồng độ natri huyết thanh cũng được điều hòa trở lại. Như chúng ta thấy, việc điều chỉnh quá nhanh nồng độ natri huyết thanh có thể đi kèm với cái gọi là Hội chứng hủy myelin thẩm thấu, gây tổn thương thần kinh một cách đáng kể. Do đó, quan trọng là cần phải điều chỉnh việc giảm thể tích một cách cẩn thận và giám sát chặt chẽ nồng độ natri ở những bệnh nhân có suy giảm thể tích và hạ natri máu. Một số rối loạn lâm sàng và thuốc có thể làm tăng tiết ADH hoặc tăng cường hoạt động của nó tại ống góp. Những chất tăng tiết không thẩm thấu hoặc chất cường ADH có thể gây giữ nước và là nguyên nhân quan trọng dẫn đến hạ natri máu. Hội chứng lâm sàng gây giải phóng các chất không thẩm thấu hoặc tăng cường hoạt động của ADH dẫn đến giữ nước và hạ natri máu bệnh lý được gọi là hội chứng tăng tiết ADH không thích hợp (SIADH) hay hội chứng tăng tiết hormone chống bài niệu không thích hợp.
Mặc khác, sự vắng mặt hay thiếu hụt ADH có thể dẫn đến mất khả năng cô đặc nước tiểu thích hợp ở thận. Việc này có thể do mất quá nhiều nước ở thận và gây tăng natri máu. Hội chứng thiếu hụt ADH dẫn tới mất lượng lớn nước ở thận được gọi là đái tháo nhạt trung ương.
Sự đáp ứng của ống góp với ADH
Một số rối loạn liên quan đến sự không đáp ứng của ống thận với ADH, làm mất khả năng cô đặc nước tiểu ở thận, từ đó gây mất rất nhiều nước. Hội chứng này gọi là đái tháo nhạt do thận. Thậm chí khi có đủ mức ADH lưu hành, ống góp vẫn không thể tăng tính thấm một cách thích hợp để cho phép tái hấp thu nước, điều này dẫn đến hậu quả là nước mất quá nhiều ở thận và có khả năng gây tăng natri máu. Ngược lại, có những tình trạng và một số loại thuốc mà chúng có tác dụng giống ADH hoặc làm tăng độ nhạy cảm của ADH tới ống góp. Trong những bệnh cảnh này có thể gây ra SIADH và dẫn đến tình trạng giữ nước không thích hợp cũng như hạ natri máu.
Các guideline hướng dẫn giải quyết các vấn đề lâm sàng về natri và nước
Việc duy trì nồng độ natri ngoại bào trong khoảng hẹp (135-145 mEq/L) và kích thước ECFV trong khoảng chấp nhận được đối với cơ thể rất quan trọng. Về nguyên tắc, các cơ chế kiểm soát việc xuất nhập nước ảnh hưởng đến kích thước của ECFV ở một mức độ nào đó, nhưng cơ chế kiểm soát lượng natri xuất nhập thì quan trọng hơn nhiều bởi natri là cation chính ở ngoại bào và đóng góp động lực thẩm thấu duy trì ECFV. Trên lý thuyết, thì nồng độ natri ngoại bào có thể bị ảnh hưởng bởi lượng natri xuất nhập nhưng cơ chế kiểm soát lượng nước xuất nhập thì lại quan trọng hơn trong việc xác định nồng độ natri ngoại bào.
- Trên thực hành lâm sàng, trường hợp có bất thường kích thước ECFV (quá tải thể tích hay thiếu hụt thể tích) hữu ích nhất là xem xét đến các vấn đề trong cơ chế điều hòa nồng độ natri.
- Trên thực hành lâm sàng, trường hợp nồng độ natri ngoại bào bất thường, hữu ích nhất là xem xét các vấn đề với cơ chế điều hòa thể tích nước.
Có những tình trạng bất thường về cả về nồng độ natri (có vấn đề về điều hòa nước) và kích thước ECFV (có vấn đề về điều hòa natri), được coi là bất thường ở cả cơ chế kiểm soát nước và kiểm soát natri, do đó chẩn đoán và điều trị phải tập trung vào việc tìm ra và khắc phục những điều này (xem Bảng 1-4). Bạn đọc không cần ghi nhớ Bảng 1 -4. Nó được đưa vào để tham khảo, minh họa nhiều sự kết hợp có thể xảy ra và các tình trạng lâm sàng liên quan đến việc ECFV bất thường (có nghĩa là cơ chế kiểm soát natri bất thường) và nồng độ natri ngoại bào bất thường (có nghĩa là cơ chế kiểm soát nước bất thường). Đừng lo lắng, nếu những quan điểm này không được rõ ràng hoàn toàn ở thời điểm hiện tại. Chúng sẽ được mở rộng và diễn giải rõ hơn qua một số ví dụ và bài tập bạn nhé.
| Bảng 1-4 : Các tình trạng bất thường ECFV và nồng độ natri ở ngoại bào | |||
| Những rối loạn | Ý nghĩa | Vấn đề nguyên phát (bắt đầu từ đâu) | Các ví dụ về nguyên nhân lâm sàng phổ biến |
| Hạ natri máu ECFV bình thường | Nước dư thừa so với natr | Bất thường sự kiểm soát nước (quá nhiều nước so với natri) | SIADH |
| Tăng natri máu ECFV bình thường | Nước thiếu hụt so với natr | Bất thường sự kiểm soát nước (quá ít nước so với natri) | Đái tháo nhạt. Thất thoát không nhìn thấy được |
| Nồng độ natri bình thường ECFV tăng | Tăng tổng lượng natri cơ thể | Bất thường sự kiểm soát natri (quá nhiều natri) | Suy tim sung huyết. Xơ gan. Hội chứng thận hư. Suy thận. |
| Nồng độ natri bình thường ECFV giảm | Giảm tổng lượng natri cơ thể | Bất thường sự kiểm soát natri (quá ít natri) | Nôn ói. Tiêu chảy. Thuốc lợi tiểu quai. |
| Hạ natri máu với ECFV tăng | Nước dư thừa so với natri và tăng tổng lượng natri cơ thể | Bất thường sự kiểm soát nước (quá nhiều nước so với natri) và bất thường sự kiểm soát natri (quá nhiều natri) | Suy tim sung huyết (CHF). Xơ gan. Hội chứng thận hư. Suy thận. |
| Hạ natri máu với ECFV giảm | Nước dư thừa so với natri và giảm tổng lượng natri cơ thể | Bất thường sự kiểm soát nước (quá nhiều nước so với natri) và bất thường sự kiểm soát natri (quá ít natri) | Nôn ói. Thuốc lợi tiểu Thiazid. |
| Tăng natri máu với ECFV tăng | Nước thiếu hụt so với natri và tăng tổng lượng natri cơ thể | Bất thường sự kiểm soát nước (quá ít nước so với natri) và bất thường sự kiểm soát natri (quá nhiều natri) | Sử dụng các dung dịch natri ưu trương hoặc NaHCO3 (do điều trị) |
| Tăng natri máu với ECFV giảm | Nước thiếu hụt so với natri và giảm tổng lượng natri cơ thể | Bất thường sự kiểm soát nước (quá ít nước so với natri) và bất thường sự kiểm soát natri (quá ít natri) | Lợi tiểu thẩm thấu. Tiêu chảy. |
KALI – SINH LÝ VÀ SINH LÝ BỆNH
Kali là cation chính ở nội bào. Việc duy trì ổn định nồng độ kali huyết tương là thiết yếu để giữ cho chức năng tế bào được bình thường, giữ nhịp tim và dẫn truyền thần kinh cơ thích hợp. Nồng độ kali trong nội bào tầm 130-140 mEq/L, tương phản rõ rệt với con số chỉ 3.5-5.0 mEq/L ở ngoại bào. Tổng kali toàn cơ thể phân bố 98% trong nội bào và 2% ngoài ngoại bào. Hậu quả là, chỉ một thay đổi nhỏ trong sự phân bố này có thể đưa đến hạ kali máu hoặc tăng kali máu, kể cả khi tổng lượng kali dự trữ toàn cơ thể ở mức bình thường.
Sự chuyển dịch kali qua lại màng tế bào và tăng đưa kali vào tế bào
Phần lớn gradient của kali xuyên bào được duy trì bởi bơm Na+ -K+ -ATPase nằm trên màng tế bào. Bơm sử dụng năng lượng để vận chuyển natri ra khỏi tế bào và đồng thời bơm kali vào trong nội bào với tỷ lệ 3 Na+ /2 K+ . Dưới đây là những nhân tố cực kỳ quan trọng, cả về sinh lý và sinh lý bệnh, tác động đến sự phân bố kali cũng như nồng độ kali trong huyết tương.
- Insulin làm kali di chuyển vào trong tế bào. Khi thiếu hụt insulin sẽ làm giảm quá trình đưa kali vào tế bào và có nguy cơ tiến triển tới tăng kali máu.
- pH. Thay đổi pH dịch ngoại bào có thể gây thay đổi sự dịch chuyển kali qua tế bào. Khi nhiễm toan tế bào có xu hướng đẩy các ion kali rời khỏi tế bào để trao đổi lấy các ion hydro và do đó làm tăng nồng độ kali trong huyết tương; nhiễm kiềm thì ngược lại. Trong nhiễm toan chuyển hóa, phần lớn ion hydro dư thừa sẽ được đệm bởi nội bào. Sự trung hòa về điện thế được bảo toàn nhờ vào sự di chuyển của kali, tùy thuộc vào loại nhiễm toan ở hiện tại. Các acid vô cơ có xu hướng làm cho kali di chuyển ra khỏi tế bào, dẫn đến tăng nồng độ kali trong huyết tương. Các acid hữu cơ như ceton và acid lactic không có xu hướng tạo ra sự thay đổi kali qua tế bào vì những lý do phức tạp.
- Kích thích receptor beta2 adrenergic làm kali di chuyển vào trong nội bào. Sự di chuyển này tăng lên một phần bởi sự kích hoạt bơm Na+ -K+ -ATPase. Mặt khác, chất đối vận receptor beta2 adrenergic cũng có thể góp một vai trò nhỏ để kali di chuyển ra ngoại bào.
- Kích thích receptor alpha adrenergic sẽ ức chế bơm Na+ -K+ -ATPase, hậu quả làm kali di chuyển ra ngoài tế bào.
- Các bệnh lý có tăng nồng độ thẩm thấu nghiêm trọng như trong tăng đường huyết nặng có thể đưa kali ra ngoài ngăn ngoại bào và làm tăng nồng độ kali huyết tương. Cơ chế chuyển dịch kali từ các tế bào này được gấp bội lên là nhờ vào: Dòng nước di chuyển ra khỏi tế bào để đáp ứng với tình trạng ưu trương ở ECFV, từ đó tăng nồng độ kali nội bào và sau đó kali di chuyển ra khỏi tế bào. Hướng thứ hai là do sự lôi kéo chất hòa tan (hiện tượng solvent drag), theo đó nước mang kali cùng xuyên qua màng tế bào.
- Hormone thyroid làm tăng hoạt động của bơm Na+ -K+ -ATPase, kết quả làm tăng chuyển kali vào nội bào.
- Digitalis ức chế bơm Na+ -K+ -ATPase, khi dùng quá liều digitalis có thể làm kali di chuyển ra ngoại bào, đủ dẫn tới tăng kali máu nghiêm trọng.
Nguồn kali
Thông thường, lượng kali nhập vào trong khẩu phần ăn “khớp” với lượng kali thải ra qua nước tiểu và phân. Trung bình mỗi bữa ăn, kali chiếm 1 mEq/kg cân nặng/ngày, tương đương khoảng 70 mEq/ngày ở một người 70 kg. Bình thường kali được bài tiết 90% qua nước tiểu và 10% qua phân. Có những nguồn cung cấp kali tiềm ẩn quan trọng khác mà bạn cần nhớ: • Sự phá hủy mô, chẳng hạn như tiêu cơ vân, tan máu và sau khi hóa trị một số bệnh bạch cầu và u lympho. • Truyền máu • Xuất huyết tiêu hóa với sự hấp thụ kali • Kali trong dịch truyền tĩnh mạch, nuôi ăn tĩnh mạch và nuôi ăn qua sonde quá mức. • Kali từ các thuốc điều trị. • Do thận có khả năng bài tiết kali tốt nên tăng kali thường không phổ biến trừ khi có khiếm khuyết chức năng bài xuất ở thận.
Sự bài tiết kali ở thận
Cho đến nay, con đường thải trừ kali dư thừa quan trọng nhất là bài xuất qua thận. Thận bài xuất một lượng lớn kali dư thừa. Trong trường hợp thiếu kali, thì chức năng thận bình thường có thể làm giảm lượng kali thất thoát qua nước tiểu hàng ngày xuống còn 10 mEq/24 giờ hoặc ít hơn để bảo tồn kali. Trong khi đó, nếu kali tăng lên từ nguồn ngoại sinh từ thức ăn hay nội sinh ở cơ, lượng kali bài xuất mỗi ngày có thể lên tới 8-10 mEq/kg cân nặng/24 giờ. (Ví dụ, 560-700 mEq/24 giờ ở người nặng 70 kg). Suy thận làm giảm GFR và khả năng bài xuất kali dư thừa ở thận. Khi GFR giảm dưới 20% mức bình thường, thận sẽ gặp khó khăn khi bài xuất lượng kali trong chế độ ăn mỗi ngày và có thể dẫn tới tăng kali máu. Kali được lọc tự do qua cầu thận và khoảng 10% lượng kali đã lọc đến được ống góp. Đó là những gì cuối cùng còn lại tới ống góp (và ống nối) quyết định lượng kali được bài xuất bởi thận. (Lời dịch giả: ống nối hay connecting tubule là vùng nối giữa ống lượn xa và ống góp).
Tế bào chính của ống góp (Hình. 1-5) có các bơm Na+ -K+ -ATPase trên màng đáy. Những cái bơm này giúp duy trì nồng độ natri thấp và nồng độ kali cao ở trong tế bào. Kênh natri biểu mô (ENaC) nằm trên bờ tiếp xúc với lòng ống. Aldosterone có tác dụng làm tăng số lượng kênh natri biểu mô mở ra và do đó thúc đẩy tái hấp thu natri. Aldosterone cũng làm tăng hoạt động của bơm Na+ -K+ -ATPase.
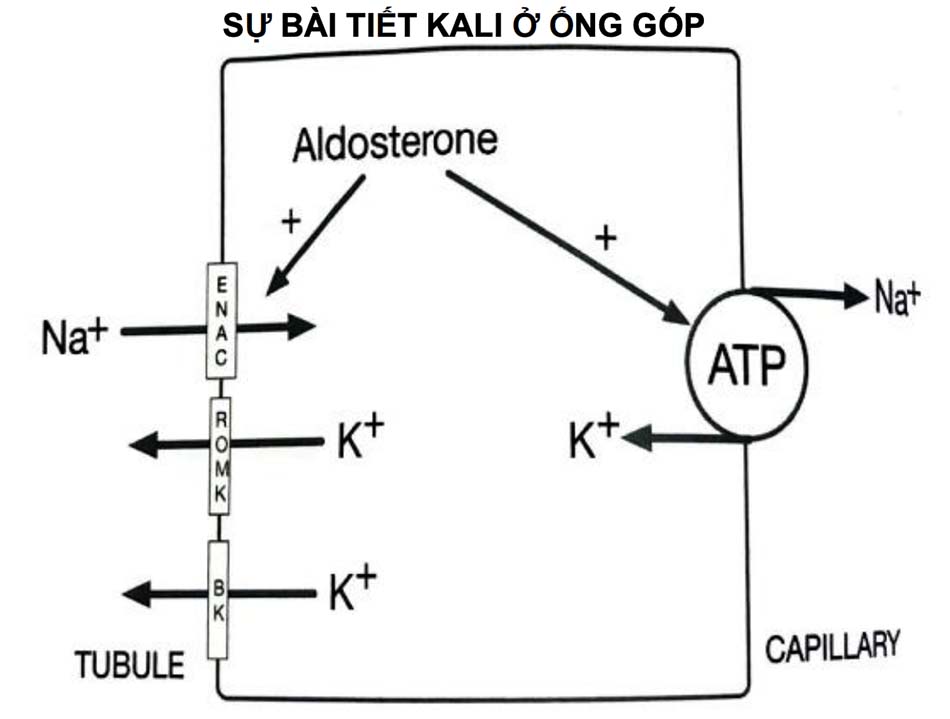
Tế bào chính có hai loại kênh kali. Kênh kali ngoài tủy thận (ROMK) được kích hoạt bởi lượng kali nhập vào và nồng độ kali huyết thanh tăng lên. Kênh này cho phép kali thoát ra khỏi tế bào biểu mô theo chiều gradient nồng độ và điện thế của nó. Trong tế bào chính còn có các kênh kali đặc biệt gọi là BK, nhạy cảm với dòng chảy của ống và bài tiết kali vào lòng ống khi tốc độ dòng chảy của ống tăng lên. Sự bài tiết kali phụ thuộc vào trình tự sau:
- Natri xâm nhập vào tế bào từ lòng ống qua các kênh natri biểu mô.
- Clo được tái hấp thu rất chậm trong ống góp qua con đường cạnh tế bào thay vì nhanh chóng qua các kênh của nó. Natri rời khỏi lòng ống vào tế bào qua kênh natri biểu mô, do đó làm lòng ống tích điện âm. Khả năng tạo ra sự chênh lệch điện thế âm này là rất quan trọng đối với cả quá trình bài tiết ion kali và hydro.
- Sự chênh lệch điện thế âm thúc đẩy kali rời khỏi tế bào biểu mô và vào trong lòng ống qua kênh ROMK và BK theo chiều gradient nồng độ và điện thế của nó.
- Natri vào trong tế bào ống thận thì được bơm ra khỏi màng đáy của tế bào (vào dịch kẽ rồi vào máu), cuối cùng được tái hấp thu. Kali vào trong lòng ống thận thì được bài xuất ra ngoài theo nước tiểu.
- Nhiều nguyên nhân giảm bài xuất kali từ đó làm tăng kali máu là do cản trở các yếu tố tham gia vào những cơ chế bài tiết này.
- Các tình trạng trên lâm sàng và các loại thuốc ức chế sản xuất aldosteron, ngăn cản ống thận đáp ứng với aldosteron, can thiệp vào các kênh natri ENaC, hoặc làm suy giảm sự tạo ra chênh lệch điện thế âm đều có thể dẫn đến bệnh lý gọi là nhiễm toan ống thận loại IV (lan tỏa), đây là một bệnh rất quan trọng và là nguyên nhân phổ biến của tăng kali máu.
Những nhân tố quan trọng ảnh hưởng đến sự bài tiết kali của ống góp và ống nối:
- Lượng kali nhập vào và nồng độ kali huyết thanh. Chính bản thân nồng độ kali huyết thanh là một động lực điều hòa mạnh mẽ cho sự bài tiết kali trong điều kiện bình thường.
- Aldosterone làm tăng trao đổi natri-kali và tăng lượng kali trong nước tiểu, tùy thuộc vào hàm lượng natri / thể tích được đưa đến ống lượn xa. Aldosterone được kích thích bài tiết bởi hệ thống renin-angiotensin và khi kali máu tăng. Khi aldosterone tiết ra quá nhiều sẽ gây mất kali ở thận, dẫn đến hạ kali huyết. Ngược lại, kali được giữ lại ở thận quá mức gây tăng kali huyết là hậu quả của việc thiếu hụt aldosteron.
- Natri được đưa đến ống góp càng nhiều thì sẽ càng làm tăng lượng kali được bài tiết bởi sự trao đổi natri-kali. Ví dụ, các thuốc lợi tiểu quai và thiazid, lợi tiểu thẩm thấu, và dịch truyền saline sẽ làm tăng lượng natri phân bố đến ống góp do đó gây tăng bài tiết kali.
- Tốc độ chảy trong lòng ống cao sẽ tăng hoạt động của kênh trung gian đặc biệtBK và tăng lượng kali bài tiết.
- Sự hiện diện của anion kém hấp thu. Ví dụ, trong trường hợp kiềm chuyển hóa, HCO3- tăng do không thể tái hấp thu bởi ống lượn gần và do đó sẽ “mang” natri cùng tới ống góp như một cation đi kèm. Qua đó, tăng trao đổi natri-kali và tăng lượng kali được đào thải ra nước tiểu.
- Trạng thái acid-base. Nhiễm toan ức chế bài tiết kali và nhiễm kiềm làm tăng bài tiết kali.
Thất thoát kali ngoài thận
Mất kali trong mồ hôi thường là tối thiểu: mồ hôi chứa khoảng 9 mEq/L kali và lượng mồ hôi tiết ra khoảng 200 ml/24 giờ ở người ít vận động. Lượng kali mất qua mồ hôi hằng ngày chỉ khoảng 9 mEq/L X 0.2 L = 1.8 mEq/ngày. Tuy nhiên, khi hoạt động gắng sức và thời tiết nóng, mồ hôi tiết ra khoảng 10 L/ngày và qua đó lượng kali thất thoát cũng tăng lên 9 mEq/L X 10L = 90 mEq/ngày. Kali mất qua phân bình thường khoảng 10% lượng kali ăn vào, nhưng có thể mất nhiều hơn khi có tiêu chảy. Lượng này cũng tăng lên ở bệnh nhân suy thận mạn bởi cơ chế bù trừ của cơ thể để ngăn tình trạng tăng kali máu xảy ra.
SINH LÝ VÀ SINH LÝ BỆNH LIÊN QUAN ĐẾN H+
pH máu được duy trì chính xác trong khoảng hẹp 7.35-7.45 và được điều hòa bởi sự cân bằng ion H+ . Nồng độ ion H+ được quyết định bởi tỉ số của hai chất: nồng độ HCO3-, được điều chỉnh bởi thận và PCO2, được kiểm soát bởi phổi. Mối quan hệ này được biểu diễn như sau: CO2 + H2O ↔ H2CO3 ↔ HCO3- + H+ [H+] α (PCO2/HCO3-)
Phương trình này mô tả hoạt động của hệ đệm CO2- HCO3- , là hệ đệm chính của dịch ngoại bào. Tỷ số PCO2 và nồng độ HCO3- quyết định nồng ion H+ . Chú ý rằng nồng độ ion H+ có thể tăng khi PCO2 tăng (toan hô hấp) hay HCO3- giảm (toan chuyển hóa). Nồng độ ion H+ có thể giảm khi PCO2 giảm (kiềm hô hấp) hay HCO3- tăng (kiềm chuyển hóa). Bình thường, phổi giúp điều hòa giữ nồng độ PCO2 khoảng 40 mmHg và thận tham gia giữ nồng độ HCO3- trong khoảng 24-26 mEq/L. Phổi và thận giúp giữ pH cơ thể trong giới hạn ổn định, tránh sự tăng và giảm ion H+ . Khi cơ thể mất một ion HCO3- , thì một ion H+ sẽ được giữ ở lại. Kết quả cuối cùng là có thêm một ion H+ tự do trong cơ thể. Do đó, mất một HCO3- cũng đồng nghĩa với tăng thêm một ion H+ . Ngược lại, tăng thêm một HCO3- cũng đồng nghĩa với mất đi một ion H+ . Trong điều kiện bình thường, có hai nguồn ion H+ mà cơ thể cần đào thải:
- Mỗi ngày phổi thải ra khoảng 15,000 mmols CO2 từ quá trình chuyển hóa carbohydrate và chất béo của cơ thể. Mặc dù CO2 không phải là acid nhưng khi nó kết hợp với H2O sẽ tạo ra H2CO3; do đó acid sẽ tích tụ rất nhanh nếu CO2 không được đào thải đầy đủ bởi phổi (toan hô hấp).
- Mỗi ngày có khoảng 1 mEq/kg (50-100 mEq) acid không bay hơi được tạo ra qua quá trình chuyển hóa protein. Ion H+ từ nguồn acid này được gọi là acid “cố định” bởi vì chúng không đào thải được qua phổi. Chúng được đệm bởi HCO3- ở dịch ngoại bào. HCO3- được sử dụng để đệm cho ion H+ mỗi ngày là 50-100 mEq có thể dẫn đến sự thiếu hụt HCO3- và dẫn tới toan chuyển hóa trừ khi thận có khả năng tạo ra lượng bicarbonate mới bù vào. Thận tạo ra HCO3- mới bằng cách loại bỏ những ion H+ từ cơ thể, mỗi một HCO3- sẽ được thêm vào dịch ngoại bào thay cho một ion H+ đào thải. Lưu ý rằng, mỗi một ion H+ mất đi sẽ để lại một ion HCO3- . Thận bài xuất 50-100 mEq H+ /ngày để giữ nồng độ HCO3- trong khoảng hẹp từ 24-26 mEq/L.
Hệ đệm của cơ thể
Hệ thống đệm của cơ thể là tuyến đầu phòng thủ chống lại những thay đổi nồng độ ion H+ một cách cấp tính. Ion H+ được đệm bởi cả nội bào và ngoại bào. Hệ đệm nội bào gồm phosphate và protein bào tương. Hệ đệm chính ở ngoại bào là CO2- HCO3- . Những hệ đệm này được đánh giá qua xét nghiệm “khí máu động mạch” trong phòng thí nghiệm. Xét nghiệm này đo được PO2 (áp lực riêng phần của oxy trong máu động mạch, đơn vị là mmHg), PCO2 (áp lực riêng phần của CO2 trong máu động mạch, đơn vị là mmHg) và pH. Xét nghiệm khí máu động mạch thông qua cân bằng Henderson-Hasselbalch, pH và PCO2 đo được cũng sẽ cho ta biết giá trị nồng độ HCO3- .
Sự điều chỉnh nồng độ HCO3- của thận
Có hai cơ chế rất khác nhau để thận điều chỉnh [HCO3- ] nhằm duy trì [HCO3- ] trong giới hạn (24-26 mEq/L):
- Ống lượn gần tái hấp thu hầu hết lượng HCO3- đã lọc Hầu hết HCO3- được lọc bởi cầu thận đều được tái hấp thu trở lại ở ống lượn gần (xem Hình 1-6). Quá trình này được thực hiện với công suất cao bởi vì mỗi ngày có một lượng lớn HCO3- được lọc qua thận và cần được tái hấp thu: 180 L/ngày (GFR) X 25 mEq/L (nồng độ lọc) = 4500 mEq/ngày lượng HCO3- cần tái hấp thu.
Quá trình này không thêm HCO3- vào ECFV và cũng không bài xuất ion H+ vào nước tiểu. Nó không tác động đến tình trạng acid-base: tổng ion H+ không đổi. Quá trình này cũng ngăn không cho HCO3- mất qua nước tiểu và do đó ngăn chặn được tình trạng toan chuyển hóa. Nồng độ HCO3- sau khi được tái hấp thu hoàn toàn từ dịch lọc (huyết tương) ở khoảng 24-26 mEq/L hoặc thấp hơn. Tuy nhiên nếu nồng độ vượt “ngưỡng” 24-26 mEq/L thì lượng HCO3- tới ống lượn gần đã vượt quá khả năng tái hấp thu HCO3- của ống thận và hệ thống này sẽ bị quá tải. Ống lượn gần không thể tái hấp thu hết lượng HCO3- đã lọc và do đó lượng HCO3- không được tái hấp thu sẽ bị “tràn” vào trong nước tiểu. Kết quả là, HCO3- huyết tương tăng cao sẽ có xu hướng lặp lại giá trị ngưỡng của nồng độ HCO3- . Những nhân tố quan trọng làm ống lượn gần tăng tái hấp thu HCO3- :
- Tình trạng ECFV. Ống lượn gần sẽ tăng tái hấp thu HCO3- khi ECFV giảm bởi vì ECFV giảm là nhân tố quan trọng để duy trì nồng độ HCO3- cao ở bệnh nhân kiềm chuyển hóa. Ống lượn gần tăng tái hấp thu NaHCO3 duy trì kiềm chuyển hóa cho đến khi sự giảm ECFV được cải thiện.
- Angiotensin II tăng làm tăng tái hấp thu HCO3- ở ống lượn gần.
- Khi PCO2 tăng, ống lượn gần sẽ bù trừ bằng cách tăng tái hấp thu HCO3- và nồng độ HCO3- huyết tương sẽ tăng theo. Khi PCO2 giảm thì ngược lại. Sự bù trừ này cực kỳ quan trọng để đáp ứng lại với tình trạng toan hô hấp (PCO2 tăng) hay kiềm hô hấp (PCO2 giảm).
- Nguồn kali dự trữ giảm trầm trọng (hạ kali máu) cũng là một nguyên nhân thúc đẩy ống lượn gần tăng tái hấp thu HCO3- . Cơ chế này thì phức tạp. Ngược lại với tăng kali máu.
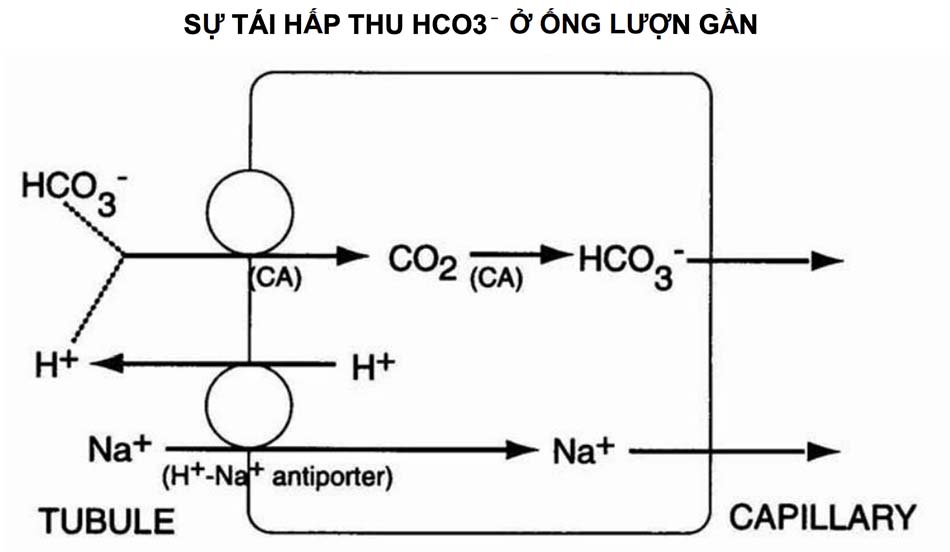
Khi có khiếm khuyết trong tái hấp thu HCO3- ở ống lượn gần, nồng độ HCO3- sẽ giảm do mất qua nước tiểu. Hậu quả là gây toan chuyển hóa. Hội chứng toan chuyển hóa gây ra bởi sự bất thường tái hấp thu HCO3- của ống lượn gần được gọi là toan hóa ống lượn gần type II.
Sự bài xuất ion hydro của thận
Cơ chế thứ hai giúp thận điều hòa nồng độ HCO3- huyết tương là đảm bảo sao cho lượng ion H+ được đào thải tương đương với lượng acid được tạo ra mỗi ngày (xem Hình 1-7). Ghi nhớ rằng, việc loại bỏ một ion H+ đồng nghĩa với việc thu giữ lại một ion HCO3- . Thận loại bỏ ion H+ để thay bằng HCO3- mới nhằm bù đắp cho lượng 50-100 mEq HCO3- /ngày được dùng để đệm cho lượng acid cố định. Hai cơ chế của quá trình này:
- Việc bài tiết ion H+ được thực hiện nhờ “bơm” proton cần năng lượng ATP ở ống góp. Mỗi HCO3- được tạo ra thay cho mỗi ion H+ được bài tiết. Bơm H+ này tăng hoạt động khi có sự có mặt của aldosteron.
- NH4+ (được đào thải ra nước tiểu) và HCO3- (trở lại ECFV) được tạo ra từ sự thủy phân glutamine ở ống lượn gần. Quá trình amoni hóa này sẽ giải phóng ion H+ miễn là ion NH4+ được bài xuất ra nước tiểu. Cơ chế chính xác của quá trình giúp tăng tạo cũng như đào thải NH4+ rất phức tạp và sẽ không được diễn giải chi tiết ở đây.
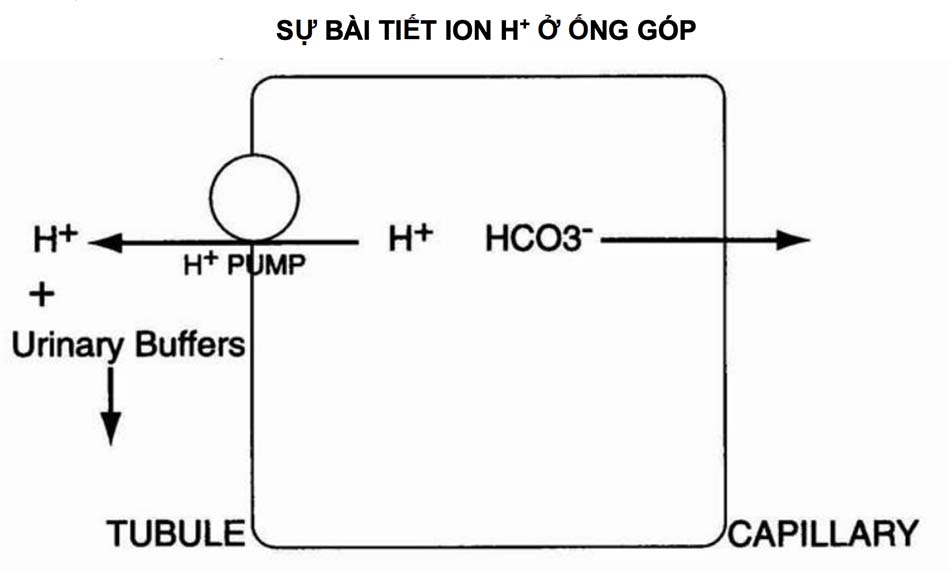
Sự bài tiết NH4+ về mặt định lượng quan trọng hơn việc bài xuất ion H+ để tạo ra HCO3- . Con đường chính để thận đáp ứng với tình trạng toan hóa (quá nhiều ion H+ ) là tăng sản xuất và đào thải NH4+ .
Khi có một bất thường trong việc đào thải H+ ở thận, nồng độ HCO3- sẽ giảm xuống để trung hòa với lượng H+ được tạo ra mỗi ngày và hậu quả là dẫn đến toan chuyển hóa. Hội chứng toan chuyển hóa gây ra bởi bất thường bài tiết ion H+ bởi ống thận gọi là toan hóa ống thận xa loại I.
Anion gap (khoảng trống anion)
Tính anion gap là mấu chốt để phân tích rối loạn acid-base một cách chính xác. Dịch ngoại bào có hiện tượng trung hòa điện tích: Tổng nồng độ của các ion mang điện tích dương phải cân bằng với tổng nồng độ ion mang điện tích âm. Điều này được mô tả qua cân bằng sau: Na+ + UC = Cl- + HCO3- + UA.
Trong đó UC (unmeasured cations là các cation không định lượng) được nói đến là tổng điện tích dương mà không phải là natri và UA (unmeasured anions là các anion không định lượng) là tổng của tất cả điện tích âm ngoài trừ Clo và Bicarbonate. UC chính là kali, canxi, magie và một số gamma globulin. UA chính là albumin, sulfate, phosphate và nhiều loại anion hữu cơ. Phương trình trên có thể được sắp xếp lại để biểu thị anion gap (AG) như sau: AG = UA – UC = [Na+] – ([Cl-] + [HCO3-]).
Một số loại ion H+ được thêm vào bởi tình trạng toan chuyển hóa có liên quan đến các anion không đo được ở ngoại bào.Thêm vào acid (H-Anion) ảnh hướng đến cả hai vế của phương trình AG. Ion H+ được đệm bởi HCO3- cho nên HCO3- sẽ giảm và anion thêm vào sẽ làm tăng AG vì nó sẽ cộng vào phần anion không định lược được. Kết quả này còn gọi là toan hóa tăng anion gap. Ở quyển sách này, tác giả sử dụng giá trị anion gap bình thường trung bình là 6 mEq/L với độ lệch chuẩn 2SD trong khoảng 2-10 mEq/L. Tất nhiên, khoảng bình thường này phụ thuộc vào từng bệnh viện và phòng xét nghiệm. Giá trị của khoảng trống anion bình thường thấp hơn so với giá trị mà chúng ta đã sử dụng trước đây, có thể là do những thay đổi trong phương pháp xác định giá trị các thành phần điện phân riêng lẻ tạo nên khoảng trống anion. Tuy nhiên, lời giải thích vì sao giá trị bình thường và phạm vi dao động của anion gap lại thấp hơn so với thực tế không hoàn toàn giải đáp một cách thỏa đáng với tác giả, vì vậy tác giả đã yêu cầu giám đốc trung tâm nghiên cứu của ông xác minh điều này với khoảng 4000 mẫu: giá trị anion gap trung bình trong phòng xét nghiệm của tác giả là 6 mEq/L với khoảng 2SD là 2- 10 mEq/L. Nhấn mạnh lại một lần nữa, giá trị này có thể thay đổi đáng kể từ phòng xét nghiệm này đến phòng xét nghiệm khác.
Trong thực hành lâm sàng, chúng ta chia toan chuyển hóa thành hai loại: tăng anion gap và anion gap bình thường (toan hóa anion gap bình thường còn được gọi là toan không tăng anion gap hay toan tăng hóa clo máu). Có một số hướng dẫn chung về cách chẩn đoán toan chuyển hóa tăng anion gap. Nếu anion gap tăng trên khoảng 25 mEq/L hoặc cao hơn thì toan chuyển hóa tăng anion gap luôn luôn xuất hiện bất kể giá trị của pH, PCO2 và [HCO3- ] là bao nhiêu. Nếu anion gap tăng trong khoảng 15-25 mEq/L thì rất có khả năng có toan chuyển hóa tăng anion gap bất kể giá trị của pH, PCO2 và [HCO3-] là bao nhiêu. Chúng ta sẽ bàn luận thêm về điều này sau. Rối loạn acid-base sẽ được bàn luận ở chương 7, 8 và 9.
Bài tập
Các bài tập cuối mỗi bài được thêm vào nhằm mục đích giúp bạn mở rộng thêm về nội dung của bài và giới thiệu những kiến thức mới thông qua các tình huống lâm sàng.
1. Tính tổng lượng nước trong cơ thể ở người phụ nữ cân nặng 50 kg:
Trả lời: 0.5 X 50 = 25 lít. Tổng lượng này có thể thấp hơn ở phụ nữ lớn tuổi (có thể 20 lít).
2. Tính tổng lượng nước trong cơ thể ở người nam cân nặng 100 kg.
Trả lời: 0.6 X 100 = 60 lít. Tăng hơn gấp đôi ở người nữ 50 kg. Tổng lượng nước có thể thấp hơn ở người nam lớn tuổi (có thể 50 lít).
3. Tính ECFV ở người nữ nặng 50 kg.
Trả lời: Tổng lượng nước trong cơ thể: 0.5 X 50 = 25 lít. ECFV khoảng ⅓ của tổng lượng nước: 25/3 = 8.3 lít
4. Tính ECFV ở người nam nặng 100 kg.
Trả lời: Tổng lượng nước trong cơ thể: 0.6 X 100 = 60 lít. ECFV khoảng ⅓ của tổng lượng nước: 60/3 = 20 lít.
5. Tính tổng natri ở ECF ở người nữ 50 kg.
Trả lời: Tổng lượng nước trong cơ thể: 0.5 X 50 = 25 lít. ECFV khoảng ⅓ của tổng lượng nước: 25/3 = 8.3 lít. Bây giờ nhân với nồng độ natri ngoại bào (bình thường khoảng 140 mEq/L): 8.3 L X 140 mEq/L = 1162 mEq.
6. Tính tổng natri ECF ở người nam nặng 100 kg
Trả lời: Tổng lượng nước trong cơ thể: 0.6 X 100 = 60 lít. ECFV khoảng ⅓ của tổng lượng nước: 60/3 = 20 lít. Bây giờ nhân với nồng độ natri ngoại bào (bình thường khoảng 140 mEq/L): 20 L X 140 mEq/L = 2800 mEq.
7. Đánh giá lại các câu trả lời từ 1-6.
Chú ý rằng có sự khác biệt lớn giữa một người phụ nữ nặng 50 kg so với người đàn ông nặng 100 kg. Nguyên tắc đầu tiên về điện giải đồ và sinh lý acid-base trên lâm sàng cần lưu ý là hầu hết các bệnh nhân không thuộc “tiêu chuẩn” người nam nặng 70 kg. Đây chính là điểm quan trọng cần ghi nhớ khi tính toán bù điện giải và lập kế hoạch điều trị với truyền dịch tĩnh mạch.
8. Bệnh nhân có kết quả xét nghiệm sau: natri 140 mEq/L, glucose 180 mg/dl, BUN 28 mg/dl. Mỗi thông số trên sẽ đóng góp bao nhiêu vào độ thẩm thấu?
Trả lời: Natri (cùng với Clo và các anion khác) đóng góp 2 X 140 = 280 mOsm/L.
Glucose đóng góp 180/18 = 10 mOsm/L.
Ure đóng góp 28/2.8 = 10 mOsm/L.
9. Bệnh nhân suy thận có kết quả xét nghiệm như sau: natri 130 mEq/L, glucose 100 mg/dl, BUN 120 mg/dl. Tính độ thẩm thấu. Bạn có dự đoán được rằng liệu với nồng độ thẩm thấu này có làm tăng cảm giác khát không?
Trả lời: Độ thẩm thấu tính được là 2 X 130 + 100/18 + 120/2.8 = 308. Độ thẩm thấu tăng do tăng ure, mà ure không phải là chất thẩm thấu hiệu quả. Do đó, ECF của bệnh nhân không ưu trương và bệnh nhân sẽ không tăng cảm giác khát.
10. Bệnh nhân đái tháo đường có kết quả xét nghiệm sau: natri 140 mEq/L, glucose 900 mg/dl, BUN 28 mg/dl. Nồng độ thẩm thấu này thể hiện được điều gì? Bệnh nhân này có tình trạng ưu trương không?
Trả lời: Độ thẩm thấu tính được: 340. Đúng vậy, bệnh nhân này có ưu trương, bởi vì glucose là một chất thẩm thấu hiệu quả và có khả năng làm chuyển dịch nước.
11. Glucose đóng góp bao nhiêu vào độ thẩm thấu trong ví dụ trên?
Trả lời: 900/18 = 50 mOsm/L.
12. Bệnh nhân đang nằm tại phòng cấp cứu với các chỉ số xét nghiệm sau: natri 140 mEq/L, glucose 360 mg/dl, BUN 28 mg/dl, nồng độ thẩm thấu đo được là 360. Tính osmolal gap. Các chất tan nào làm tăng osmolal gap? Glucose đóng góp bao nhiêu vào việc tăng osmolal gap trong trường hợp này?
Trả lời: Độ thẩm thấu tính được: 2 X 140 + 360/18 + 28/2.8 = 310. Osmolal gap là 50 (bình thường thấp hơn 10). Các chất ngoại sinh có thể gây tăng osmolal gap là mannitol, ethanol, isopropanol, methanol, ethylene glycol và sorbitol. Chúng ta cần nhiều thông tin hơn để biết chính xác đâu là thủ phạm chính. Glucose đóng góp 360/18 = 20 vào cả độ thẩm thấu tính được và đo được và do đó không ảnh hưởng đến osmolal gap.
13. Bệnh nhân 42 tuổi với nồng độ natri là 120 mEq/L. Bạn hiểu như thế nào về cơ chế điều hòa nước trên bệnh nhân này? Và tổng lượng natri toàn cơ thể của bệnh nhân này như thế nào?
Trả lời: Nồng độ natri huyết thanh thấp nói lên rằng có sự bất thường về điều hòa nước. Về mục tiêu lâm sàng, rối loạn nồng độ natri, cả tăng natri máu hay hạ natri máu, đều có thể được xem rằng chúng bắt nguồn từ những bất thường trong điều hòa cân bằng nội môi của nước. Sự bất thường về nồng độ natri sẽ hướng chúng ta điều tra để trả lời câu hỏi: tại sao sự điều hòa nước lại bất thường? Trong trường hợp hạ natri máu, có quá nhiều nước so với natri bởi vì thận không bài xuất nước một cách hợp lý. Nồng độ natri không cho chúng ta bất cứ thông tin đáng tin cậy nào về tổng lượng natri cơ thể rằng nó giảm hay bình thường.
Chúng ta không có bất kỳ thông tin nào về kích thước của ECFV. Vì thế, chúng ta không thể nói bất kỳ điều gì về liệu tổng natri của bệnh nhân tăng, giảm hay bình thường. Để đánh giá về tổng lượng natri của cơ thể, ta phải đánh giá về kích thước của ECFV trên lâm sàng, bởi vì thông số này được quyết định bởi tổng natri cơ thể. Các dấu hiệu cho thấy có sự thiếu hụt ECFV, từ đó phản ánh có giảm tổng lượng natri cơ thể, bao gồm: giảm độ căng của dạ, niêm mạc khô, hạ huyết áp tư thế, tăng nhịp tim khi chuyển sang tư thế đứng. Ngược lại, các dấu hiệu cho thấy có sự quá tải về ECFV, cho thấy có sự dư thừa natri trong cơ thể bao gồm: tĩnh mạch cổ nổi, rale phổi, tràn dịch màng phổi, tiếng gallop S3, và tất nhiên là cũng có phù trước xương chày.
14. Một bệnh nhân nhập viện với tình trạng phù nhiều ở bàn chân và bụng báng. Nồng độ natri trong máu bệnh nhân là 140 mEq/L. Bệnh nhân này có rối loạn về cơ chế điều hòa nước, natri hay cả hai?
Trả lời: Ở bệnh nhân này có rối loạn điều hòa natri. Nếu mục đích hướng về giải quyết các vấn đề ở bệnh nhân này trên lâm sàng, thì cần cân nhắc đến khả năng có bất thường về kích thước ECFV do bất thường về lượng natri cơ thể. Đánh giá lâm sàng về ECFV cho ta biết một cách tương đối liệu tổng lượng natri cơ thể là tăng, giảm hay bình thường. Ở bệnh nhân này, rõ ràng có tăng ECFV, biểu hiện với phù ở bàn chân và bụng báng. Vì thế, tổng lượng natri trong cơ thể cũng tăng đáng kể. Các tình trạng phù (như trong suy tim sung huyết, xơ gan với báng bụng và phù; hội chứng thận hư) có thể được xem như có sự tích lũy quá nhiều natri trong cơ thể. Từ đó cho biết có rối loạn kiểm soát natri.
Nồng độ natri máu cho ta biết có rối loạn trong điều hòa nước. Nếu như nồng độ natri bình thường, tức không có vấn đề đáng kể nào trên lâm sàng trong việc điều hòa nước. Ở bệnh nhân này có vấn đề trong việc đào thải nước và có thể tiến triển đến hạ natri máu nếu nhập thêm một lượng lớn nước, tuy nhiên nồng độ natri máu lại bình thường; chính vì thế sẽ không biểu hiện các rối loạn đáng kể nào về mặt lâm sàng trong điều hòa thăng bằng nước. Vấn đề quan trọng ở đây cần nhấn mạnh là không cần thiết phải hạn chế nước ở những bệnh nhân có suy tim sung huyết, xơ gan hay hội chứng thận hư nếu nồng độ natri huyết thanh trong giới hạn bình thường.
15. Một bệnh nhân nam có nồng độ natri máu là 125 mEq/L. Bạn nhận định tổng lượng natri trong cơ thể của bệnh nhân này như thế nào? Natri của anh ấy có giảm thấp không?
Trả lời: Chúng ta không thể khẳng định bất cứ điều gì đáng tin cậy về tình trạng tổng natri cơ thể của bệnh nhân khi chỉ dựa vào nồng độ natri máu có giá trị thấp. Chúng ta không có thêm thông tin lâm sàng nào về tình trạng của ECFV, vì thế chúng ta không thể nói bất cứ điều gì về tình trạng tổng natri cơ thể. Nồng độ natri chỉ đơn giản là một nồng độ, không phải tổng lượng đo được. Bản thân nồng độ natri không nói lên được bất cứ điều gì đáng tin cậy cho chúng ta về tình trạng của tổng lượng natri toàn cơ thể. Nồng độ natri không nói lên gì cho dù tổng lượng natri cơ thể tăng, giảm hay bình thường. Trên lâm sàng, tổng lượng natri cơ thể có thể được ước tính thông qua kích thước của ECFV bởi vì lượng natri toàn cơ thể là yếu tố quyết định chính của kích thước ECFV.
Bệnh nhân này có vấn đề với kiểm soát nước bởi vì có bất thường nồng độ natri huyết thanh. Nồng độ natri 125 mEq/L nói lên rằng nước quá thừa so với natri trong ECFV và do đó có sự bất thường trong việc điều hòa nước. Tóm lại: Bất thường ECFV có nghĩa là bất thường tổng lượng natri cơ thể. Bất thường nồng độ natri có nghĩa là bất thường trong sự điều hòa nước.
16. Bệnh nhân nam, 23 tuổi nhập viện với tình trạng phù chi, ran phổi và tiếng T3 ở tim (T3). Nồng độ natri của anh ấy là 120 mEq/L. Có phải anh ấy có vấn đề trong việc điều hòa natri hay điều hòa nước hay cả hai?
Trả lời: Cả hai. ECFV tăng (rối loạn điều chỉnh natri) cùng với nồng độ natri bất thường (rối loạn điều chỉnh nước). Bệnh nhân có vấn đề rất nghiêm trọng trong việc điều chỉnh natri. Ta có thể thấy bệnh nhân có tình trạng quá tải ECFV (biểu hiện với phù, ran phổi, T3) do tình trạng suy tim sung huyết và do đó quá tải tổng lượng natri trong cơ thể. Hạ natri máu còn chỉ ra rằng ở bệnh nhân này còn tồn tại sự bất thường về điều hòa nước. Natri huyết thanh thấp có nghĩa là có quá nhiều nước so với natri. Bệnh nhân có bất thường về khả năng bài xuất nước tiểu để loại bỏ lượng nước dư thừa. Do vậy, cần sử dụng lợi tiểu quai cũng như hạn chế natri để giảm tổng natri cơ thể và bên cạnh đó cũng cần hạn chế nước để khắc phục tình trạng hạ natri máu.
17. Bệnh nhân nhập viện với tình trạng giảm độ căng của dạ và nhịp tim nhanh. Hạ huyết áp khi chuyển sang tư thế đứng.Nồng độ natri máu là 130 mEq/L. Anh ấy có vấn đề về điều hòa natri, điều hòa nước hay cả hai?
Trả lời: Cả hai. Đánh giá lâm sàng về ECFV đại khái sẽ cho biết tổng lượng natri trong cơ thể tăng, giảm hoặc bình thường. Ở bệnh nhân này ta thấy có giảm ECFV. Do đó, tổng lượng natri trong cơ thể bệnh nhân giảm. Sự thiếu hụt ECFV trên lâm sàng do giảm lượng lớn natri toàn cơ thể. Hạ natri máu do hiện tượng giữ nước bất thường ở thận; lượng nước quá nhiều so với natri vì thận không pha loãng đủ lượng nước tiểu để bài xuất lượng nước dư thừa ra ngoài trong khi lượng nước nhập vào lại tiếp tục tăng. Bệnh nhân này có các rối loạn lâm sàng quan trọng về cả sự điều hòa natri lẫn sự điều hòa nước. Cả hạ natri máu và thiếu hụt ECFV nên được bù với dung dịch NaCl đẳng trương. Dịch truyền tĩnh mạch sẽ được giới thiệu ở bài viết: Dịch truyền tĩnh mạch: Tính chất và chỉ định.
18. Chất nào sau đây sẽ làm tăng nồng độ thẩm thấu đo được khi thêm chúng vào dịch ngoại bào?
- Urea.
- Glucose.
- Sodium.
- Ethanol.
- Methanol.
- Isopropanol.
- Ethylene glycol.
- Mannitol Sorbitol.
Trả lời: Tất cả các chất trên đều làm tăng nồng độ thẩm thấu khi được thêm vào dịch ngoại bào.
19. Chất nào sau đây sẽ làm tăng nồng độ thẩm thấu tính toán khi thêm chúng vào dịch ngoại bào?
- Urea.
- Glucose.
- Sodium.
- Ethanol.
- Methanol.
- Isopropanol.
- Ethylene glycol.
- Mannitol Sorbitol.
Trả lời: Chỉ có ure, glucose và natri nằm trong công thức tính nồng độ thẩm thấu. Do đó, chỉ có ure, glucose và natri sẽ làm nồng độ thẩm thấu tăng lên khi được thêm vào dịch ngoại bào.
20. Chất nào sau đây sẽ làm tăng osmolal gap khi thêm chúng vào dịch ngoại bào?
- Urea.
- Glucose.
- Sodium.
- Ethanol.
- Methanol.
- Isopropanol.
- Ethylene glycol.
- Mannitol Sorbitol.
Trả lời: OSM GAP = OSM(đo được) – OSM(tính được) Cả ure, glucose và natri đều nằm trong công thức tính nồng độ thẩm thấu. Chúng sẽ thêm vào cả độ thẩm thấu tính được và nồng độ thẩm thấu đo được và do đó sẽ không làm thay đổi osmolal gap nếu được thêm vào dịch ngoại bào. Còn những hợp chất khác sẽ làm tăng nồng độ thẩm thấu đo được nhưng không làm tăng nồng độ thẩm thấu tính được, khi đó sẽ làm tăng osmolal gap.
Thực tế osmolal gap có ý nghĩa lâm sàng quan trọng. Methanol, ethanol, ethylene glycol và isopropanol là những loại rượu quan trọng và phổ biến gây ngộ độc thường thấy trong phòng cấp cứu. Tăng osmolal gap có thể là manh mối quan trọng chứng tỏ có sự hiện diện của một trong những loại rượu này.
21. Mức GFR khoảng bao nhiêu sẽ khiến bệnh nhân gặp vấn đề trong việc đào thải kali nhập mỗi ngày? Ở mức này, bệnh nhân sẽ bắt đầu có cân bằng kali dương tính, gây tăng kali máu.
Trả lời: Giới hạn trên khả năng bài xuất kali tỉ lệ thuận một cách tương đối với GFR. Nếu GFR bình thường 100%, Lượng kali tối đa được bài xuất mỗi ngày là khoảng 10 mEq/ kg cân nặng. Tức là khoảng 70 X 10 = 700 mEq ở người 70 kg. Nếu GFR giảm xuống còn 50% mức bình thường, lượng kali tối đa được bài xuất có thể giảm xuống khoảng 50% X 700 = 350 mEq. Đó chỉ là khoảng ước tính lượng kali được bài xuất tối đa bởi vì còn có cơ chế bù trừ như sẽ tăng lượng kali bài xuất qua thận và tăng lượng kali mất qua phân như cách cơ thể tự bảo vệ chính mình khỏi tình trạng tăng kali máu. Nếu GFR giảm hơn 20% mức bình thường, lượng kali bài xuất tối đa sẽ hạ thấp xuống khoảng 140 mEq/ngày (20% của 700 mEq/ngày).
Chế độ ăn trung bình khoảng 1 mEq kali trên 1 kg cân nặng tức khoảng 70 mEq/ngày ở người 70 kg. Với khẩu phần ăn 70 mEq/ngày, GFR cần giảm còn khoảng 70/700 = 10% mức bình thường trước khi tăng kali máu xảy ra. Trên thực tế, GFR thường thấp hơn mức đó khi có tăng kali máu dựa trên mức nhập kali thông thường. Tăng kali máu có thể tiến triển trong bệnh cảnh suy thận nhẹ nếu tăng lượng kali nhập vào hay có tăng thêm lượng kali tiềm ẩn. Ví dụ, một người có chế độ ăn nhiều kali sẽ có tăng kali máu nếu GFR suy giảm. Một bệnh nhân với GFR ở mức 15% so với bình thường sẽ tiến triển đến tăng kali máu nếu kali vượt khoảng 15% X 700 = 105 mEq/ngày trong khẩu phần ăn hằng ngày. Như đã đề cập ở trên, đó chỉ là khoảng ước tính mức kali tối đa được bài xuất.
Một điểm cần chú ý trên lâm sàng, nếu bệnh nhân có suy thận nhẹ đến trung bình cùng với tình trạng tăng kali máu, thì không nên chỉ xem nguyên nhân của tăng kali máu là do suy thận đơn thuần mà cần nỗ lực tìm kiếm các nguyên nhân khác.
22. Có bao nhiêu kali trong ECFV ở một người nam có cân nặng 70 kg?
Trả lời: Bản chất rất tinh tế của sự phân bố kali qua màng tế bào được trình bày ở phép tính dưới đây:
- TBW = 0.6 X 70 kg = 42 L.
- ECFV = ⅓ X 42 L = 14 L .
- Nồng độ kali trong ECFV: 4.0 mEq/L.
- Tổng kali trong ECFV: 4.0 mEq/L X 14 L = 56 mEq.
Lượng kali tính được trong toàn bộ ECFV (56 mEq) thấp hơn lượng kali chứa trong 3 liều KCl 20 mEq hoặc thấp hơn lượng kali có trong 4 ly nước cam ép! Thậm chí chỉ tăng một ít kali ngoại bào cũng có thế gây tăng lượng lớn nồng độ kali ngoại bào. Hậu quả của thêm 56 mEq vào ECFV là nồng độ kali tăng từ 4.0 mEq/L tới 8.0 mEq/L. May mắn thay, nồng độ kali của chúng ta sẽ không tăng gấp đôi sau khi uống 4 ly cam ép bởi vì cơ chế cân bằng nội môi sẽ duy trì sự chênh lệch lớn giữa nồng độ kali trong và ngoài tế bào, do đó lượng kali ở ECFV sẽ không tăng cao.
23. Có bao nhiêu kali trong ECFV ở người nữ nặng 40 kg?
Trả lời:
- ECFV = ⅓ X 20 L = 6.7 L.
- Nồng độ kali trong ECFv: 4.0 mEq/L.
- Tổng kali trong ECFV: 4.0 mEq/L X 6.7 L = 26.8 mEq.
Lượng kali tính được trong ECFV là khoảng một liều KCl bổ sung.
24. Tính tổng lượng HCO3- có trong ECFV ở người nữ nặng 50 kg với nồng độ HCO3- ngoại bào là 25 mEq/L.
Trả lời: TBW: 0.5 X 50 = 25 lít. ECFV xấp xỉ ⅓ của TBW: 25/3 = 8.3 lít. Bình thường, HCO3- dự trữ ở ECF là 25 mEq/L X 8.3 L = 207.5 mEq! Điều này tương ứng với khoảng 4 ống NaHCO3 tiêu chuẩn.
Mỗi ngày có bao nhiêu HCO3- được tái hấp thu tại ống lượn gần của thận, giả sử GFR là 100 ml/phút?
Trả lời:Tổng lượng lọc = tổng lượng tái hấp thu bởi ống lượn gần: 100 ml/phút X 1440 phút/ngày X 25 mEq/L = 3600 mEq/ngày! Con số này gấp khoảng 17 lần bicarbonate trong ECF.
25. Để minh họa môt phần về tầm quan trọng trong khả năng đệm của nước tiểu, phép tính độ pH sau đây sẽ cho biết pH của nước tiểu sẽ là bao nhiêu nếu như không được đệm. Tác giả không đặt mục tiêu là bạn phải biết cách tính. Nó chỉ được đưa vào cho mục đích minh họa.
Bình thường, lượng ion H+ bài xuất ra một ngày xấp xỉ 50-100 mmol/ngày và chính bằng với lượng acid cố định được tạo ra do quá trình chuyển hóa thức ăn. Giả định, ion H+ bài xuất là 100 mmol trong 24 giờ, trong 1 L thể tích nước tiểu, khi đó độ pH trong nước tiểu sẽ là: pH = -log(H+) = -log(100 mmol/L) = -log(0.100 mmol/ml) = 1
Trông thật tệ dù chỉ tưởng tượng nếu pH là 1! So sánh pH =1 này với pH trung bình bình thường của nước tiểu là 4.5. Hệ đệm tiết niệu cho phép tăng bài tiết ion H+ lớn (200-300 mmol / ngày) ở trạng thái tăng tải lượng ion H+ mà không làm giảm đáng kể pH nước tiểu. Cơ chế chính để thận loại bỏ ion H+ dư thừa của cơ thể là bằng cách tăng quá trình tạo muối amoni (NH4+ ) ở thận. Trong các tình huống mà khi có lượng ion H+ dư thừa được thêm vào cơ thể, thận sẽ đáp ứng bằng cách tăng sản xuất và bài tiết NH4+ .
Nội dung chính của Tiếp cận – đánh giá – xử trí các rối loạn về Acid Base, dịch và điện giải
Tổng cộng có 10 chương, mời các bạn click vào từng phần để đọc tài liệu chi tiết:
1. CÁC KHÁI NIỆM CƠ BẢN.
2. DỊCH TRUYỀN TĨNH MẠCH TÍNH CHẤT VÀ CHỈ ĐỊNH.
3. HẠ NATRI MÁU.
4. TĂNG NATRI MÁU.
5. HẠ KALI MÁU.
6. TĂNG KALI MÁU.
7. TOAN CHUYỂN HÓA.
8. KIỀM CHUYỂN HÓA.
9. BA BƯỚC ĐỂ CHẨN ĐOÁN RỐI LOẠN TOAN KIỀM.
10. NHỮNG VÍ DỤ LÂM SÀNG.
Để tải đầy đủ sách Tiếp cận – đánh giá – xử trí các rối loạn về Acid Base, dịch và điện giải pdf mời các bạn click vào link ở đây.

