Bệnh huyết học
Ba bước để chẩn đoán rối loạn toan kiềm và 6 ca lâm sàng
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
Nhà thuốc Ngọc Anh – Bài viết Ba bước để chẩn đoán rối loạn toan kiềm và 6 ca lâm sàng được dịch từ: Chapter 9, 10 của. Hyponatremia, Textbook: Acid-Base, Fluids and Electrolytes made ridiculously simple, 3rd edition, Richard A.Preston bởi bởi nhóm bác sĩ: Nguyễn Thế Bảo, Nguyễn Thế Thời, Đặng Gia Uyên được đào tạo tại Trường Đại học Y Dược Cần Thơ và bác sĩ Liêu Minh Huy được đào tạo tại Đại học Y Dược Thành phố Hồ Chí Minh. Để tải file pdf bài viết này mời các bạn click vào link ở đây.
Cũng như cách tiếp cận có hệ thống khi phân tích X quang ngực hay ECG, thì việc tiếp cận phân tích có hệ thống các rối loạn kiềm toan cũng rất quan trọng. Chương này sẽ miêu tả một cách đơn giản, tuần tự các bước một về cách tiếp cận mỗi khi phân tích kết quả khí máu.
Rối loạn toan kiềm hỗn hợp là những trường hợp mà trong đó có nhiều rối loạn kiềm toan độc lập với nhau xảy ra cùng một lúc. Tiếp cận theo từng bước rất quan trọng bởi vì nhiều rối loạn xảy ra đồng thời như vậy có thể che giấu lẫn nhau. Ví dụ: rối loạn toan chuyển hóa và kiềm chuyển hóa có thể bù đắp cho nhau, dẫn tới pH và [HCO3⁻] gần như bình thường. Hay trong trường hợp khác, một rối loạn nặng, ưu thế hơn có thể che lấp một rối loạn khác nhẹ hơn. Và rồi chúng ta sẽ nhận ra rằng, các rối loạn kiềm toan nguy hiểm có thể bị bỏ sót nếu như không được tiếp cận một cách có hệ thống, tuần tự theo từng bước.
3 BƯỚC TIẾP CẬN ĐỂ CHẨN ĐOÁN RỐI LOẠN TOAN KIỀM
3 bước tiếp cận kiềm toan (xem bảng 9-1) sẽ được miêu tả cụ thể hơn trong phần còn lại của chương này:
Bước 1: Xác định rối loạn biểu hiện rõ ràng nhất (toan chuyển hóa, kiềm chuyển hóa, toan hô hấp hay kiềm hô hấp) bằng cách đánh giá pH, pCO2 và [HCO3⁻]. Nếu có nhiều hơn một rối loạn hiện diện rõ ràng ngay ban đầu thì hãy chọn rối loạn “nặng hơn” để bắt đầu tiếp cận. Nếu tất cả đều có vè nghiêm trọng thì sao? Cứ việc chọn đại một cái. Ưu điểm của cách tiếp cận này là dù bạn bắt đầu ở đâu thì kết quả thu được cũng như nhau.
Bước 2: Áp dụng công thức để đánh giá sự bù trừ cho rối loạn đã xác định có đủ hay không, từ dó sẽ biết được có rối loạn thứ hai kèm theo không. Một khi đã xác định được một rối loạn thì câu hỏi chung là: Rối loạn này được bù đủ chưa?
- Trong các rối loạn về chuyển hóa, biểu hiện [HCO3⁻] bất thường và chúng ta muốn đánh giá thử có rối loạn hô hấp kèm theo không. Chúng ta sẽ đặt ra câu hỏi: sau khi bù trừ thì pCO2 nên bằng bao nhiêu? Nếu pCO2 khác biệt một cách đáng kể so với giá trị dự đoán tính được bằng công thức thì có rối loạn hô hấp kèm theo.
- Trong rối loạn của hô hấp, pCO2 bất thường và chúng ta sẽ đánh giá có rối loạn chuyển hóa kèm theo không. Bằng cách dặt ra câu hỏi: [HCO3⁻] nên bằng bao nhiêu sau khi bù trừ? Nếu [HCO3⁻] khác biệt một cách đáng kể so với giá trị dự đoán tính được bằng công thức thì có rối loạn chuyển hóa kèm theo.
Áp dụng công thức cho rối loạn bạn đã xác định được để xem sự bù trừ có đủ không. Nếu sự bù trừ không giống như dự đoán từ công thức thì có rối loạn khác kèm theo.
Bước 3: Tính anion gap. Anion gap bình thường bằng khoảng 6 với khoảng giới hạn là là 2-10 mEq/L. Khoảng giới hạn bình thường này tất nhiên sẽ phụ thuộc vào từng bệnh viện và phòng xét nghiệm riêng. Nếu anion gap bình thường, việc của bạn đã xong. Còn nếu không thì khi anion gap tăng sẽ là dấu chứng rất mạnh để chẩn đoán toan chuyển hóa. Nếu anion gap tăng trên 15 mEq/L thì có thể có toan chuyển hóa tăng anion gap bất kể giá trị pH và [HCO3⁻] như thế nào. Nếu anion gap tăng trên 25 mEq/L thì gần như chắc chắn có toan chuyển hóa tăng anion gap bất kể giá trị pH và [HCO3⁻] như thế nào.
Nếu anion gap tăng do toan acid lactic hay toan ketone thì việc so sánh sự biến thiên của anion gap với sự biến thiên của nồng độ bicarbonate có thể sẽ có ích. Bằng cách này chúng ta có thể phát hiện được rối loạn chuyển hóa bị “che giấu”, đó có thể là kiềm chuyển hóa hoặc toan chuyển hóa không tăng anion gap.
| Bảng 9-1: Ba bước tiếp cận rối loạn kiềm toan | |||
| Bước 1: Xác định rối loạn biểu hiện rõ ràng nhất | |||
| Rối loạn | pH | pCO2 | HCO3- |
| Toan chuyển hóa
Kiềm chuyển hóa Toan hô hấp Kiềm hô hấp |
↓
↑ ↓ ↑ |
↓ (thứ phát)
↑ (thứ phát) ↑ (nguyên phát) ↓ (nguyên phát) |
↓ (nguyên phát)
↑ (nguyên phát) ↑ (thứ phát) ↓ (thứ phát) |
| Bước 2: Áp dụng công thức để xem sự bù trừ có đủ không Nếu không, có kèm theo rối loạn thứ hai | |||
| Toan chuyển hóa: 𝑝𝐶𝑂2 = 1,5 × [𝐻𝐶𝑂3⁻] + 8 Kiềm chuyển hóa: 𝑝𝐶𝑂2 = 40 + 0,7 × ([𝐻𝐶𝑂3⁻đ𝑜 đượ𝑐 ] − [𝐻𝐶𝑂3⁻𝑏ì𝑛ℎ 𝑡ℎườ𝑛𝑔]) .
Toan hô hấp:
Kiềm hô hấp :
|
|||
| Bước 3: Tính anion gap | |||
| AG= [Na⁺]-([Cl⁻]+[HCO3⁻]).
AG bình thường bằng xấp xỉ 6 với khoảng giới hạn là 2-10 mEq/L. Nếu AG > 15 mEq/L thì có thể có toan hóa máu tăng AG. Nếu AG > 25 mEq/L thì gần như chắc chắn có toan hóa máu tăng AG. Với toan acid lactic, tỉ số giữa lượng anion gap tăng và bicarbonate giảm là khoảng 1,5. Với toan ketone, tỉ số giữa lượng tăng anion gap và bicarbonate giảm là khoảng 1,0. |
|||
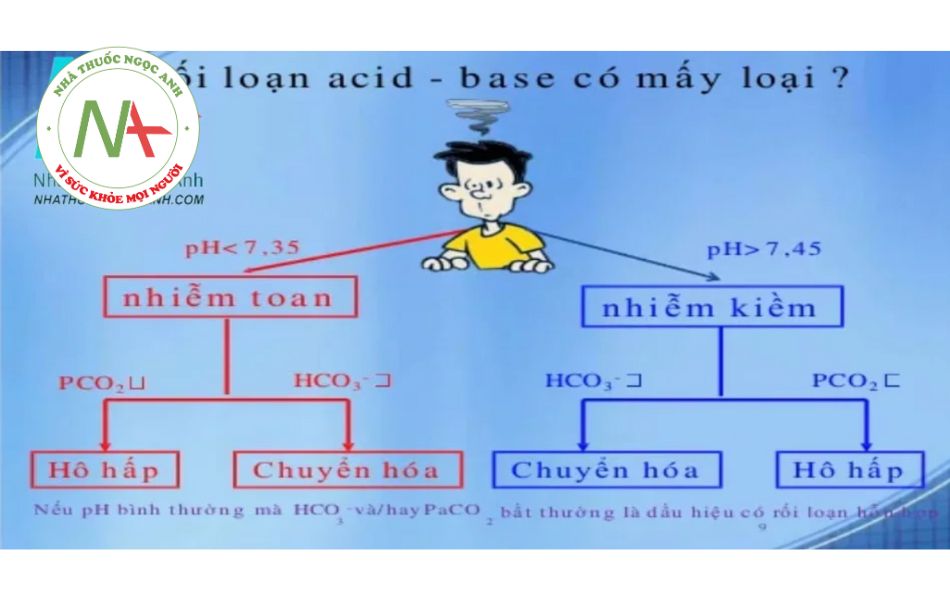
Bước 1: Xác định trước một loại rối loạn Đánh giá pH, pCO2 và [HCO3⁻] để xác định loại rối loạn kiềm toan biểu hiện rõ ràng nhất. Nhìn chung:
- Nếu pH thấp (<7,35) có thể có toan chuyển hóa hoặc toan hô hấp; nếu [HCO3⁻] thấp: toan chuyển hóa; nếu pCO2 cao: toan hô hấp.
- Nếu pH cao (>7,45), có thể có kiềm chuyển hóa hoặc kiềm hô hấp; nếu [HCO3⁻] cao: kiềm chuyển hóa; nếu pCO2 thấp: kiềm hô hấp .
- Nếu pH bình thường, nhưng [HCO3⁻] hoặc pCO2 hoặc cả hai đều bất thường, thì chọn cái bất thường nhất giữa [HCO3⁻] và pCO2. Ví dụ: pH=7,4, pCO2 = 60 mmHg, HCO3⁻ = 36 mEq/L. pCO2 và [HCO3⁻] đều bất thường. Bởi vì pH bình thường trong trường hợp này nên bạn có thể chẩn đoán ban đầu là kiềm chuyển hóa ( [HCO3⁻]= 36 mEq/L) hoặc toan hô hấp (pCO2 = 60mmHg) đều được. Dù hướng nào thì phương pháp này cũng sẽ có hiệu quả.
Bước 2: Áp dụng công thức để xem bù trừ có đủ không
Sử dụng công thức tính giá trị bù trừ mong đợi (expected compensation) để xác định xem có rối loạn khác xuất hiện không. Phần này sẽ đi cụ thể vào sử dụng công thức nào cho từng loại rối loạn nào và ý nghĩa của chúng. Một khi bạn đã xác định được một rối loạn rồi thì hãy áp dụng công thức phù hợp để xem bù trừ có đủ không. Với rối loạn chuyển hóa, hãy đặt ra câu hỏi: pCO2 nên bằng bao nhiêu sau khi bù trừ? Với rối loạn hô hấp, hãy đặt ra câu hỏi: [HCO3⁻] nên bằng bao nhiêu sau khi bù trừ? Các công thức sẽ cho ra giá trị bù trừ mong đợi của các rối loạn toan kiềm. Nếu sự bù trừ thực tế không giống với công thức thì có rối loạn thứ hai hiện diện. Lưu ý dùng các giá trị pCO2 và [HCO3⁻] từ kết quả khí máu động mạch (aterial blood gas – ABG) để xác định bù trừ có đủ không (Bước 2). Và sử dụng kết quả từ xét nghiệm huyết thanh để tính anion gap (Bước 3). Ở các trường hợp trong sách thì bicarbonate trong huyết thanh và bicarbonate tính được từ kết quả khí máu hầu như luôn bằng nhau, nhưng điều này có thể không xảy ra trên thực tế lâm sàng.
Toan chuyển hóa Nồng độ của ion H+ trong dịch ngoại bào được quyết định bởi tỉ lệ giữa PCO2 (được kiểm soát bởi phổi) và [HCO3⁻] (được kiểm soát bởi thận), tương quan theo: [𝐻 +] ∝ 𝑃𝐶𝑂2/[𝐻𝐶𝑂3 −](∝:𝑡ỉ𝑙ệ)
Toan chuyển hóa là quá trình gây ra sự giảm nguyên phát [HCO3⁻]. Hô hấp bù trừ cho toan chuyển hóa bằng cách làm tăng thông khí, từ đó giảm PCO2 thứ phát. Điều này giúp điều chỉnh tỉ lệ PCO2/[HCO3⁻] và do đó cũng điều chỉnh luôn nồng độ H+ về bình thường. Thông thường, phổi không chuyển nồng độ H+ về hẳn luôn giá trị bình thường mà chỉ tiệm cận khoảng đó. Vậy giá trị của PCO2 bằng bao nhiêu sau khi bù trừ? Đáp án của câu hỏi trên có thể trả lời bằng cách sử dụng công thức giá trị bù trừ hô hấp dự đoán của toan chuyển hóa. Theo đó, giá trị PCO2 bằng với 𝑃𝐶𝑂2 = 1.5 × [𝐻𝐶𝑂3 −] + 8
Nếu PCO2 đo được khác với giá trị PCO2 dự đoán thì có ý nghĩa gì? Sự khác biệt đáng kể mang ý nghĩa có rối loạn hô hấp kèm theo toan chuyển hóa, bởi vì PCO2 không biểu hiện như chúng ta mong đợi. Nếu PCO2 đo được cao hơn giá trị dự đoán thì có kèm theo tình trạng toan hô hấp. Nếu PCO2 đo được thấp hơn dự đoán thì sẽ kèm theo tình trạng kiềm hô hấp. Công thức này chỉ mang tính tương đối, và chúng ta nên cho PCO2 đo được dao động ± 2 mmHg so với giá trị dự đoán. Tuy nhiên, sự chênh lệch đáng kể so với giá trị dự đoán theo chiều nào cũng gợi ý rối loạn loạn hô hấp kèm theo sự toan chuyển hóa.
Kiềm chuyển hóa
Nồng độ của ion H+ trong dịch ngoại bào được quyết định bởi tỉ lệ giữa PCO2 (được kiểm soát bởi phổi) và [HCO3⁻] (được kiểm soát bởi thận) theo quan hệ [𝐻 +] ∝ 𝑃𝐶𝑂2/[𝐻𝐶𝑂3⁻](∝:𝑡ỉ 𝑙ệ)
Kiềm chuyển hóa là quá trình gây ra sự tăng nguyên phát [HCO3⁻]. Hô hấp bù trừ cho kiềm chuyển hóa bằng cách giảm thông khí, gây ra sự tăng thứ phát pCO2. Điều này giúp điều chỉnh tỉ lệ PCO2/[HCO3⁻] và do đó cũng điều chỉnh luôn nồng độ H+ về bình thường. Thông thường, phổi không chuyển nồng độ H+ về hẳn luôn giá trị bình thường mà chỉ tiệm cận khoảng đó. Vậy giá trị của PCO2 bằng bao nhiêu sau khi bù trừ? Đáp án của câu hỏi trên có thể trả lời bằng cách sử dụng công thức giá trị bù trừ hô hấp mong đợi của kiềm chuyển hóa ( expected respiratory compensation for a metabolic alkalosis). Theo đó, giá trị PCO2 nên bằng với: 𝑝𝐶𝑂2 = 40 + 0,7 × ([𝐻𝐶𝑂3⁻đ𝑜 đượ𝑐 ] − [𝐻𝐶𝑂3⁻𝑏ì𝑛ℎ 𝑡ℎườ𝑛𝑔].
Trong đó [𝐻𝐶𝑂3⁻đ𝑜 đượ𝑐 ] là bicarbonate đo được của bệnh nhân và [𝐻𝐶𝑂3⁻𝑏ì𝑛ℎ 𝑡ℎườ𝑛𝑔 ] là nồng độ bicarbonate bình thường, khoảng 24-26 mEq/L. Nếu PCO2 đo được khác với giá trị PCO2 dự đoán thì có ý nghĩa gì? Sự khác biệt đáng kể mang ý nghĩa có rối loạn hô hấp kèm theo kiềm chuyển hóa, bởi vì PCO2 không biểu hiện như chúng ta mong đợi. Nếu PCO2 đo được cao hơn giá trị dự đoán thì sẽ có kèm theo tình trạng toan hô hấp. Nếu PCO2 đo được thấp hơn dự đoán thì sẽ kèm theo tình trạng kiềm hô hấp. Chú ý rằng công thức này chỉ mang tính tương đối và các đáp ứng của hô hấp ở từng bệnh nhân với kiềm chuyển hóa hết sức đa dạng. Do đó, đối với kiềm chuyển hóa, chúng ta nên cho phép pCO2 được dao động khoảng ± 5 mmHg so với giá trị mong đợi tính được. Tuy nhiên sự chênh lệch đáng kể theo chiều nào cũng gợi ý rằng có rối loạn hô hấp kèm theo kiềm chuyển hóa.
Giá trị tối đa pCO2 có thể đạt được để bù trừ cho kiềm chuyển hóa khoảng 55 mmHg. pCO2 > 55 mmHg nhìn chung sẽ gợi ý tới toan hô hấp kèm theo, bất kể giá trị [HCO3⁻].
Rối loạn hô hấp
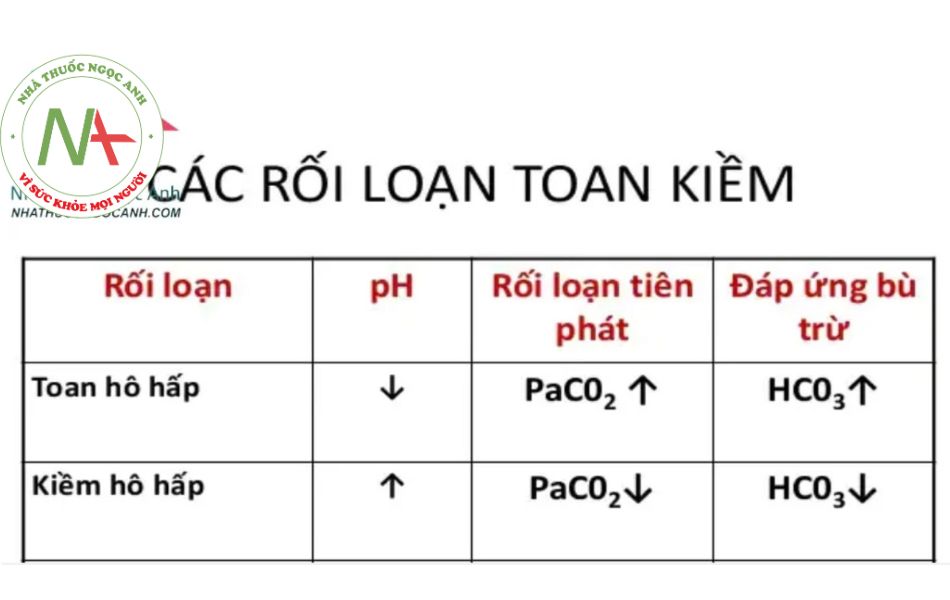
Toan hô hấp là quá trình gây ra sự tăng nguyên phát pCO2. Kiềm hô hấp là quá trình gây ra sự giảm nguyên phát pCO2. Rối loạn hô hấp được chia ra thành cấp và mạn. Cấp là từ vài phút tới vài giờ, mạn có nghĩa là kéo dài hơn 24-48 giờ. Lý do cho sự phân biệt này là bởi sự bù trừ hoàn toàn của thận cho rối loạn hô hấp thường mất ít nhất 24-48 giờ. Cụ thể hơn, khi toan chuyển hóa hình thành, sự gia tăng thông khí phút bù trừ của hệ hô hấp xảy ra rất nhanh và pCO2 hạ ngay lập tức. Còn trong rối loạn hô hấp, thận mất ít nhất 24-48 giờ để hoàn thành điều chỉnh [HCO3⁻] tới giá trị mới để bù trừ. Nói ngắn gọn là phổi điều chỉnh pCO2 nhanh hơn thận điều chỉnh [HCO3⁻] rất nhiều.
Ví dụ, trong trường hợp toan hô hấp, rối loạn nguyên phát là tăng pCO2. Sự bù trừ của thận cho toan hô hấp dẫn tới sự tăng thứ phát trong [HCO3⁻]. Mặc dù thận có xu hướng khởi đầu tăng [HCO3⁻] ngay lập tức nhưng sẽ mất khoảng ít nhất 24-48 giờ để thận tăng [HCO3⁻] tới giá trị ổn định mới. Do đó, công thức dự đoán bù trừ hô hấp phụ thuộc vào rối loạn này là cấp (vài phút tới khoảng 1 tiếng) hay mạn (24- 48 tiếng hoặc hơn – khoảng thời gian cần thiết để thận bù trừ hoàn toàn). Trong toan hô hấp cấp, nồng độ HCO3⁻ trong huyết thanh tăng khoảng 1 mEq/L cho mỗi 10 mmHg pCO2 tăng thêm. Với toan hô hấp mạn (sau 24-48 tiếng), nồng độ HCO3⁻ trong huyết thanh tăng khoảng 3,5 mEq/L cho mỗi 10 mmHg pCO2 tăng thêm. Với kiềm hô hấp, pCO2 sẽ giảm, do đó [HCO3⁻] sẽ giảm theo để bù trừ. Vậy giảm khoảng bao nhiêu ? Với kiềm hô hấp cấp (vài phút tới khoảng 1 tiếng), nồng độ HCO3⁻ trong huyết thanh sẽ giảm khoảng 2 mEq/L cho mỗi 10 mmHg pCO2 giảm đi. Với kiềm hô hấp mạn (sau 24-48 tiếng), nồng độ HCO3⁻ trong huyết thanh sẽ giảm khoảng 5 mEq/L cho mỗi 10 mmHg pCO2 giảm đi. Tóm tắt lại, với rối loạn hô hấp:
Toan hô hấp:
- Cấp: pCO2 tăng 10 mmHg thì [HCO3⁻] tăng 1 mEq/L.
- Mạn: pCO2 tăng 10 mmHg thì [HCO3⁻] tăng 3,5 mEq/L.
Kiềm hô hấp :
- Cấp: pCO2 giảm 10 mmHg thì [HCO3⁻] giảm 2 mEq/L.
- Mạn: pCO2 giảm 10 mmHg thì [HCO3⁻] giảm 5 mEq/L.
Ví dụ 1: pCO2 của bệnh nhân tăng từ 40 lên 60 mmHg trong toan hô hấp mạn. Trong rối loạn này, [HCO3⁻] trong huyết thanh sẽ tăng 3,5 mEq/L cho mỗi 10 mmHg pCO2 tăng thêm. Vậy sự bù trừ sẽ làm [HCO3⁻] tăng thêm 2 × 3,5 = 7 𝑚𝐸𝑞/𝐿. Nhân cho 2 là do pCO2 tăng lên 20 (= 𝟐 × 10).
Ví dụ 2: Bệnh nhân có pCO2 = 40 mmHg và [HCO3⁻]= 24 mEq/L. Bệnh nhân xuất hiện tình trạng kiềm hô hấp và pCO2 giảm xuống 20 mmHg. [HCO3⁻] nên bằng bao nhiêu sau khi bù trừ? Đáp án: [HCO3⁻] nên giảm đi 2 × 2 = 4 𝑚𝐸𝑞/𝐿. Nhân cho 2 là do pCO2 giảm 20 mmHg = 𝟐 × 10. Nồng độ [HCO3⁻] nên bằng với 24 − 4 = 20 𝑚𝐸𝑞/𝐿 sau khi bù trừ cho kiềm hô hấp cấp.
Ví dụ 3: Bệnh nhân có pCO2 = 40 mmHg và [HCO3⁻]= 24 mEq/L. Bệnh nhân xuất hiện tình trạng toan hô hấp cấp và pCO2 tăng lên 70 mmHg. {HCO3⁻] nên bằng bao nhiêu sau khi bù trừ? Đáp án: [HCO3⁻] nên tăng thêm 𝟑 × 1 = 3 𝑚𝐸𝑞/𝐿. Nhân cho 3 là do pCO2 tăng thêm 30 𝑚𝑚𝐻𝑔 = 𝟑 × 10. [HCO3⁻] nên bằng 24 + 3 = 27 𝑚𝐸𝑞/𝐿 sau khi bù trừ cho toan hô hấp cấp.
Ví dụ 4: Bệnh nhân có pCO2 = 40 mmHg và [HCO3⁻] = 24 mEq/L. Bệnh nhân xuất hiện tình trạng toan hô hấp mạn và pCO2 tăng lên 70 mmHg. [HCO3⁻] nên bằng bao nhiêu sau khi bù trừ (>24-48 giờ) Đáp án: [HCO3⁻] nên tăng thêm 𝟑 × 3,5 = 10,5 𝑚𝐸𝑞/𝐿. Nhân cho 3 là do pCO2 tăng thêm 30 𝑚𝑚𝐻𝑔 = 𝟑 × 10. [HCO3⁻] nên bằng 24 + 10,5 = 34,5 𝑚𝐸𝑞/𝐿 sau khi bù trừ cho toan hô hấp mạn.
Bước 3: Tính anion gap
AG= [Na⁺]-([Cl⁻] + [HCO3⁻])
Giá trị bình thường của anion gap sử dụng trong sách là 6 với khoảng giới hạn là từ 2-10 mEq/L. Nếu anion gap bình thường thì coi như bạn đã hoàn tất và tổng kết lại những rối loạn toan kiềm bạn đã xác định được. Sự hiện diện của tình trạng tăng anion gap là dấu chứng mạnh mẽ để chẩn đoán toan chuyển hóa. Sau đây là một vài hướng dẫn chung để ứng dụng AG trong chẩn đoán toan chuyển hóa tăng anion gap:
- Nếu anion gap ≥ 25 mEq/L thì có toan chuyển hóa tăng anion gap, bất kể giá trị của [HCO3⁻] và pH.
- Nếu anion gap > 15 mEq/L thì có khả năng có tình trạng toan chuyển hóa tăng anion gap, bất kể giá trị của [HCO3⁻] và pH.
- Anion gap trong khoảng 10-15 mEq/L là bất thường, nhưng có thể do những nguyên nhân khác ngoài toan chuyển hóa tăng anion gap
- Nếu anion gap bình thường, thì bạn đã hoàn thành từ bước trước đó.

Điều chỉnh anion gap trong tình trạng hạ albumin
Vì albumin chiếm phần lớn trong các anion không định lượng nên albumin cũng sẽ chiếm phần lớn trong anion gap. Khi albumin máu giảm, anion gap sẽ thấp hơn mong đợi, do đó tình trạng hạ albumin có thể che giấu toan chuyển hóa tăng anion gap. Vì vậy, khi albumin thấp hơn bình thường thì nên điều chỉnh anion gap theo lượng albumin hạ để có thể xác định chính xác hơn toan chuyển hóa tăng anion gap. Cách hiệu chỉnh theo albumin là tăng anion gap thêm 2,5 cho mỗi 1 g/dL albumin giảm dưới 4,5 g/dL.
Ví dụ: AG = 10 và albumin = 2,5 g/dL. AG hiệu chỉnh sẽ bằng 10 + 2,5 × (4,5 − 2,5) = 15 𝑚𝐸𝑞/𝐿. Do đó chúng ta sẽ phải nghĩ nhiều tới có tình trạng toan chuyển hóa tăng anion gap.
So sánh sự thay đổi anion gap với sự thay đổi bicarbonate
Nếu bạn có thể thực hiện được 3 bước nêu trên thì bây giờ bạn đã được trang bị khá đầy đủ để phân tích các rối loạn kiềm toan hỗn hợp trên lâm sàng. Nhưng còn thêm một bước bổ sung nữa sẽ giúp ích trong những trường hợp toan chuyển hóa tăng anion gap do toan acid lactic hay toan ketone. Bước này thỉnh thoảng sẽ hữu ích trong việc phát hiện các rối loạn chuyển hóa bị “che giấu”.
Nếu ở bước 3 bạn đã chẩn đoán toan chuyển hóa tăng anion gap do acid lactic hay ketone thì việc so sánh sự thay đổi giữa AG và [HCO3⁻] có thể sẽ hữu ích. Có quan điểm cho rằng trong toan chuyển hóa tăng anion gap sẽ có sự liên quan giữa anion gap tăng gây ra bởi tăng anion trong dịch ngoại bào và do giảm bicarbonate, gây ra bởi sự trung hòa với H+. Căn cứ vào phương trình: AG= [NA⁺]-([Cl⁻] + [HCO3⁻])
thì theo logic thông thường, anion gap tăng bao nhiêu thì HCO3⁻ sẽ giảm bấy nhiêu. Chẳng hạn như, toan acid lactic hay toan ketone đái tháo đường làm tăng anion lên 15 mEq/L thì nồng độ HCO3⁻ hi vọng sẽ giảm tương đương bằng 15 mEq/L.
Nhưng sự tương quan một – một này giữa lượng anion gap tăng và bicarbonate giảm thường không xảy ra trong thực tế. Có giả thuyết cho rằng đó là do ngoài HCO3⁻ thì H+ còn được đệm bởi hệ đệm nội bào và bởi xương. Hay nói một cách đơn giản là HCO3⁻ không phải đệm hết lượng ion H+ một mình mà sẽ nhận được sự “trợ giúp” từ các hệ đệm khác. Do đó [HCO3⁻] thường sẽ giảm ít hơn mức tăng của anion gap.
Với toan lactic, tỉ lệ giữa độ tăng anion gap và độ giảm [HCO3⁻] thường không phải là 1 mà khoảng 1,5 nhờ các hệ đệm ngoại bào khác. Do đó, với toan acid lactic thì gần như:
Lượng AG thay đổi/ Lượng {HCO3⁻] thay đổi = 1,5
Hoặc chuyển vế, ta có:
Lượng [HCO3⁻] thay đổi = Lượng AG thay đổi / 1,5
Sử dụng công thức đơn giản này thì chúng ta sẽ dự đoán được nếu trong toan acid lactic, AG tăng một khoảng 15 mEq/L thì [HCO3⁻] phải giảm một khoảng AG/1,5=15/1,5=10 mEq/L chứ không phải 15 mEq/L Với toan ketone, tỉ số này gần với 1 hơn có lẽ là do ketone (gây ra sự tăng anion gap) có thể bị đào thải qua nước tiểu. Do đó trong toan ketone thì có thể xem như:
Lượng [HCO3⁻] thay đổi = Lượng AG thay đổi

Phải nhấn mạnh lại rằng đây là cách rất tương đối để dự đoán độ giảm [HCO3⁻] dựa vào AG trong trường hợp toan acid lactic hay toan ketone. Còn trong trường hợp với toan ure máu và các nguyên nhân toan chuyển hóa tăng anion gap khác, tỉ số này không thể dự đoán được.
Vậy câu hỏi đặt ra là ta sẽ ứng dụng điều đã nói ở trên như thế nào? Trong bệnh cảnh toan lactic hoặc toan ketone, [HCO3⁻] đo được nếu cao hơn số dự đoán dựa trên AG sẽ gợi ý có tình trạng kiềm chuyển hóa tiềm ẩn kèm theo. Ngược lại [HCO3⁻] đo được thấp hơn giá trị dự đoán thì gợi ý có tình trạng toan chuyển hóa không tăng anion gap tiềm ẩn kèm theo.
- [HCO3⁻] đo được nếu cao hơn số dự đoán dựa trên AG sẽ gợi ý có tình trạng kiềm chuyển hóa tiềm ẩn kèm theo.
- [HCO3⁻] đo được thấp hơn giá trị dự đoán thì gợi ý có tình trạng toan chuyển hóa không tăng anion gap tiềm ẩn kèm theo.
Ví dụ 1: Một bệnh nhân với [HCO3⁻] huyết thanh = 24 mEq/L và AG= 6 mEq/L. Bà ta xuất hiện tình trạng toan acid lactic và AG tăng từ 6 lên 16. Bạn sẽ hi vọng [HCO3⁻] bằng khoảng bao nhiêu? Đáp án: 10 mEq/L H+ được đệm không chỉ bởi bicarbonate ngoại bào mà còn có các hệ đệm nội bào và xương. Nồng độ [HCO3⁻] hi vọng sẽ giảm xuống khoảng: Lượng AG thay đổi /1,5 = 6,7 mEq/L. Do đó [HCO3⁻] mong đợi bằng 24 – 6,7 = 17,3 mEq/L. Sự tăng AG thêm 10 mEq/L sẽ kèm theo sự giảm [HCO3⁻] 6,7 mEq/L. Tác giả nhận thức được rằng việc không làm tròn các chữ số thập phân trong nồng độ [HCO3⁻] sẽ trông có vẻ lạ lùng, nhất là khi đây là một phương pháp rất tương đối. Nhưng tác giả vẫn sẽ để lại chữ số thập phân cho các bạn đọc tiện theo dõi mặc dù biết là bàn luận về [HCO3⁻] = 17,3 mEq/L không có nhiều ý nghĩa lắm.
Ví dụ 2: Bệnh nhân ban đầu có [HCO3⁻] huyết thanh = 24 mEq/L và AG= 6 mEq/L. Sau khi xuất hiện tình trạng toan ketone thì AG tăng từ 6 lên 20 mEq/L. Kết quả [HCO3⁻] nên bằng bao nhiêu? Đáp án: AG tăng lên một khoảng bằng 14 mEq/L. Do đó [HCO3⁻] nên giảm khoảng 14 mEq/L (nhớ rằng Lượng AG thay đổi/Lượng [HCO3⁻] thay đổi bằng khoảng 1 trong toan ketone). Do đó bicarbonate mong chờ sẽ giảm 14 mEq/L từ 24 mEq/L (24- 14=10 mEq/L). Sự tăng AG nên đi kèm với sự giảm ngược lại của [HCO3⁻].
Ví dụ 3: Bệnh nhân ban đầu có AG= 6 mEq/L, [HCO3⁻] huyết thanh = 24 mEq/L. Kết quả khí máu động mạch pH= 7,40, [HCO3⁻] = 24 mEq/L, pCO2= 40 mmHg. Sau khi xuất hiện tình trạng toan acid lactic thì AG sẽ tăng từ 6 lên 26 mEq/L. Nhưng [HCO3⁻] không giảm và vẫn giữ nguyên 24 mEq/L. pH và pCO2 cũng giữ nguyên 7,4 và 40. Chuyện gì đã xảy ra? Đáp án: Bắt đầu với 3 bước tiếp cận
Bước 1: Mọi thứ trông có vẻ bình thường. Hiện tại vẫn chưa thấy có rối loạn toan kiềm.
Bước 2: pCO2 bình thường và phù hợp với [HCO3⁻] bình thường (24). Do đó không có rối loạn hô hấp.
Bước 3: AG tăng lên một khoảng 20 mEq/L. Dựa trên sự thay đổi AG thì [HCO3⁻] dự đoán sẽ giảm vào khoảng: Lượng AG thay đổi / 1,5 = 20/1,5 = 13,3 mEq/L. [HCO3⁻] mong đợi sẽ bằng 24 – 13,3 = 10,7 mEq/L. Nhưng [HCO3⁻] của bệnh nhân không giảm và vẫn giữ nguyên mức 24 mEq/L. Tại sao? Phải có thứ gì đó “đẩy” [HCO3⁻] tăng lên 13,3 mEq/L. Thứ đó là gì? Trả lời: Đó là kiềm chuyển hóa. Tình trạng toan chuyển hóa tăng AG nặng được “che giấu” bởi tình trạng kiềm chuyển hóa với mức độ tương đương. Nếu chúng ta không tính AG và so sánh lượng bicarbonate giảm dự đoán (dựa trên lượng AG tăng) với giá trị giảm thực tế, chúng ta có thể bỏ qua hai rối loạn độc lập và nghiêm trọng. À, tôi quên nói với các bạn là bệnh nhân này đã nôn ói suốt 2 ngày qua trong suốt quá trình có toan acid lactic. Ví dụ 4: Bệnh nhân ban đầu có AG = 6 mEq/L, [HCO3⁻] huyết thanh =24.
Ví dụ 4: Bệnh nhân ban đầu có AG = 6 mEq/L, [HCO3⁻] huyết thanh =24.
Khí máu động mạch pH = 7,40, [HCO3⁻]= 24 mEq/L, pCO2= 40 mmHg. Sau khi hình thành toan acid lactic thì kết quả mới là AG = 22, [HCO3⁻] = 22 mEq/L, pCO2= 39 mmHg, pH = 7,37. Bệnh nhân có các rối loạn nào?
Đáp án:
Bước 1: pH và [HCO3⁻] cùng giảm: toan chuyển hóa. Nhìn sơ thì tình trạng này có vẻ rất nhẹ.
Bước 2: pCO2 nên bằng bao nhiêu sau khi bù trừ? Sử dụng công thức bảng 9-1. Giá trị pCO2 nên bằng với 1,5 × 22 + 8 = 41. pCO2 của bệnh nhân là 39. Giá trị này nằm trong khoảng dự đoán của pCO2. Do đó không có rối loạn hô hấp.
Bước 3: Anion gap tăng lên một khoảng 16 mEq/L. Nếu chỉ có toan chuyển hóa tăng anion gap thì chúng ta sẽ mong chờ [HCO3⁻] giảm một lượng tương đương với : Lượng AG thay đổi/1,5 = 16/1,5 = 10,7 mEq/L. Nồng độ [HCO3⁻] mong chờ sẽ bằng với 24 – 10,7 = 13,3 mEq/L Nhưng bicarbonate của bệnh nhân là 22 mEq/L, cao hơn đáng kể so với dự đoán. Vậy có thứ gì đó “đẩy” HCO3⁻ lên. Đó là kiềm chuyển hóa. So sánh lượng anion gap tăng (16 mEq/L) với lượng bicarbonate giảm (chỉ có 2 mEq/L) giúp chúng ta xác định được tình trạng kiềm chuyển hóa tiềm ẩn.
Ví dụ 5: Bệnh nhân ban đầu AG = 8, [HCO3⁻] huyết thanh = 24 mEq/L. Khí máu động mạch: pH= 7,4, [HCO3⁻] = 24 mEq/L, pCO2= 40 mmHg. Sau đó hình thành tình trạng toan ketone. Giá trị mới AG = 18 mEq/L, [HCO3⁻] = 4 mEq/L, pH = 7,08. Có tình trạng gì đang xảy ra?
Đáp án:
Bước 1: Bicarbonate và pH cùng giảm. Có tình trạng toan chuyển hóa nặng.
Bước 2: pCO2 nên bằng bao nhiêu sau khi bù trừ? Sử dụng công thức trong bảng 9- 1: 1,5 × 4 + 8 = 14 . Sự giảm pCO2 phù hợp với sự bù trừ của toan chuyển hóa. Do đó, không có rối loạn hô hấp kèm theo.
Bước 3: AG tăng thêm 10 mEq/L. Sự giảm [HCO3⁻] mong đợi tương ứng với sự tăng AG 10 mEq/L do toan ketone sẽ vào khoảng 10 mEq/L, nên chúng ta sẽ mong đợi [HCO3⁻] vào khoảng 24-10= 14 mEq/L. Nhưng [HCO3⁻] chỉ có 4 mEq/L, thấp hơn 10 mEq/L so với giá trị dự đoán. Có thứ gì đó đang “kéo” [HCO3⁻] xuống. Thứ đó là gì?
Trả lời: Có sự rối loạn toan chuyển hóa thứ hai. Rối loạn toan hóa thứ hai bị “ẩn giấu” là dạng không tăng anion gap. Bệnh nhân này có hai toan chuyển hóa độc lập nhau: toan chuyển hóa tăng anion gap và toan chuyển hóa không tăng anion gap. Khi chúng ta nghĩ kĩ về nó thì việc bệnh nhân có DKA (toan chuyển hóa tăng anion gap) kèm theo bệnh toan hóa ống thận (toan chuyển hóa không tăng anion gap) hoặc tiêu chảy cấp mức độ nặng cũng không có gì là quá xa lạ. Hãy xem lại bảng 7-1, Chúng ta sẽ thấy có nhiều tình trạng có thể kết hợp và có thể dẫn tới toan chuyển hóa tăng anion gap xảy ra cùng lúc với toan chuyển hóa không tăng anion gap.
Ví dụ 6: Bệnh nhân trong phòng cấp cứu biểu hiện sốc nhiễm trùng kèm theo: anion gap tăng lên từ 6 tới 24 (lượng AG thay đổi bằng 18) và [HCO3⁻] huyết thanh giảm từ 26 xuống 4 (lượng AG thay đổi bằng 22). Kết quả khí máu động mạch: pCO2 giảm từ 40 xuống 15, [HCO3⁻] giảm xuống 4, và pH giảm từ 7,40 xuống 7,05. Chẩn đoán của bạn là gì?
Đáp án:
Bước 1: pH và [HCO3⁻] đều giảm: có toan chuyển hóa.
Bước 2: pCO2 nên bằng bao nhiêu? 𝑝𝐶𝑂2 = 1,5 × 4 + 8 = 14. pCO2 đo được phù hợp với pCO2 dự đoán. Do đó, không có rối loạn hô hấp.
Bước 3: Toan chuyển hóa tăng anion gap xảy ra ở trong sốc nhiễm trùng có khả năng là toan acid lactic. Lượng AG thay đổi là 18. Chúng ta sẽ mong chờ [HCO3⁻] giảm đi một lượng khoảng 18/1,5 = 12 mEq/L. Do đó [HCO3⁻] mong chờ sẽ bằng với 26-12=14 mEq/L. Nhưng [HCO3⁻] đo được giảm xuống 4 mEq/L. [HCO3⁻] thực tế thấp hơn giá trị dự đoán khi có toan chuyển hóa tăng anion gap. Có gì đó đang kéo [HCO3⁻] xuống thêm 10 mEq/L. Sự giảm [HCO3⁻] này là do có tình trạng toan chuyển hóa không tăng anion kèm theo.
Các ví dụ trên đã chỉ ra cách ứng dụng anion để xác định rối loạn chuyển hóa “tiềm ẩn” kèm theo trong trường hợp toan acid lactic và toan ketone. Trên thực tế, sử dụng anion gap để dự đoán thay đổi của bicarboante chỉ là phương pháp rất tương đối. Nhưng, sự sai lệch đáng kể so với giá trị dự đoán cũng mang ý nghĩa gợi ý có rối loạn chuyển hóa kèm theo. Cụ thể là:
- Nếu nồng độ bicarbonate cao hơn đáng kể so với giá trị dự đoán từ lượng AG tăng lên thì có rối loạn kiềm chuyển hóa “tiềm ẩn” kèm theo.
- Nếu nồng độ bicarbonate thấp hơn đáng kể so với giá trị dự đoán từ lượng AG tăng lên thì có rối loạn toan chuyển hóa không tăng anion gap “ tiềm ẩn” kèm theo.
Bài tập tổng hợp
Để tiện theo dõi thì tất cả các bệnh nhân sau đều có kết quả khí máu động mạch nền bằng pH=7,40, pCO2= 40 mmHg, [HCO3⁻]= 24 mEq/L, AG= 6 mEq/L. Tất cả các thay đổi và tính toán để phân tích ca lâm sàng sẽ dựa vào giá trị nền này.
1. Bệnh nhân có kết quả khí máu động mạch như sau pH= 7,15, [HCO3⁻] tính được là 6 mEq/L. pCO2= 18 mmHg, AG= 8 mEq/L
Đáp án:
Bước 1: Bệnh nhân này có toan chuyển hóa rất nặng.
Bước 2: Đối với toan chuyển hóa thì pCO2 nên bằng bao nhiêu? Chúng ta đang muốn xem thử rằng đây chỉ là rối loạn toan chuyển hóa đơn thuần hay có kèm thêm rối loạn hô hấp. Câu hỏi đặt ra là: pCO2 nên bằng bao nhiêu sau khi bù trừ? Chúng ta sẽ trả lời được câu hỏi này bằng cách áp dụng công thức bù trừ hô hấp mong đợi cho kiềm chuyển hóa. 𝑝𝐶𝑂2 = 1,5 × 6 + 8 = 9 + 8 = 17
pCO2 của bệnh nhân đo được gần với giá trị bù trừ của hô hấp mong đợi là 17. Do đó, chúng ta được phép kết luận rằng không có rối loạn hô hấp kèm theo.
Bước 3: AG = 8 mEq/L (bình thường). Vậy chúng ta đã xong. Không cần làm thêm bước nào nữa khi AG không gợi ý toan chuyển hóa tăng AG. Kết luận: Toan chuyển hóa không tăng anion gap. Các chẩn đoán phân biệt được liệt kê ở bảng 7-1.
2. Bệnh nhân có kết quả khí máu động mạch như sau pH= 7,08, [HCO3⁻] = 10 mEq/L. pCO2= 35 mmHg, AG= 8 mEq/L
Đáp án:
Bước 1: [HCO3⁻] là 10 và pH là 7,08. Có tình trạng toan chuyển hóa nặng.
Bước 2: pCO2 nên bằng bao nhiêu? pCO2 nên bằng với 𝑝𝐶𝑂2 = 1,5 × 10 + 8 = 23 𝑚𝑚𝐻𝑔
pCO2 đo được là 35 mmHg, cao hơn giá trị chúng ta mong đợi! Do đó, có thứ gì đó đang đẩy pCO2 lên. Đó là tình trạng toan hô hấp kèm theo. Vậy có tình trạng toan chuyển hóa kèm theo toan hô hấp.
Bước 3: AG = 8 trong giới hạn bình thường. Chúng ta đã xong. Kết luận: Toan chuyển hóa không tăng anion gap kèm theo toan hô hấp. pCO2 của bệnh nhân là 35. Cao hơn rất nhiều so với giá trị dự đoán được từ công thức. Do đó, bệnh nhân phải có toan hô hấp, có thể được hiểu là sự “đuối sức” của hệ hô hấp bệnh nhân dẫn tới giảm khả năng bù trừ cho toan chuyển hóa. Sự gia tăng pCO2 là một dấu hiệu nguy hiểm trong toan chuyển hóa, bởi vì lượng pCO2 tăng thêm có thể dẫn tới giảm pH đột ngột.
Một lưu ý về khía cạnh lâm sàng về khả năng bù trừ tối đa trong toan chuyển hóa: Ở bệnh nhân trẻ tuổi, hệ hô hấp có khả năng bù trừ tối đa (giá trị pCO2 thấp nhất có thể đạt được) vào khoảng 10-15 mmHg. Giá trị này sẽ vào khoảng 20 mmHg ở người lớn tuổi hơn, cho thấy có sự giới hạn khả năng tăng thông khí bù trừ. Do đó, có sự giới hạn trong khả năng bù trừ của hệ hô hấp trong toan chuyển hóa. Một bệnh nhân với [HCO3⁻]=3 mEq/L và sự bù trừ của hệ hô hấp đã đạt tối đa sẽ có pCO2 xấp xỉ bằng 0,5 × 3 + 8 = 12,5 𝑚𝑚𝐻𝑔. Giá trị này chỉ là xấp xỉ bởi vì đường cong bù trừ không tuyến tính hoàn toàn khi giá trị [HCO3⁻] quá thấp. pH tính được với [HCO3⁻] và pCO2 như trên sẽ bằng 7,00. Để giữ pCO2 ở mức 12,5 mmHg cần phải gắng sức rất nhiều. Liệu bệnh nhân sẽ thể duy trì được tình trạng thở nhanh sâu được bao lâu để giữ pCO2 ở mức 12,5 mmHg? Giả sử như cơ hô hấp bệnh nhân bắt đầu mỏi và pCO2 tăng lên 20 mmHg. pH lúc đó sẽ rơi thẳng xuống 6,80!
Vậy trên lâm sàng nếu có bệnh nhân trẻ tuổi bị toan chuyển hóa nặng và pCO2 vào khoảng 10-15 mmHg hoặc 20 mmHg ở bệnh nhân già hơn thì sự bù trừ lúc này đã đạt tới “tối đa”, dù chỉ một lượng nhỏ pCO2 tăng thêm hoặc [HCO3⁻] gảm đi sẽ nhanh chóng làm nặng hơn tình trạng lâm sàng của bệnh nhân rất nhiều!
3. Bệnh nhân có kết quả khí máu động mạch như sau pH= 7,49 , [HCO3⁻] = 35 mEq/L. pCO2= 48 mmHg, AG= 8 mEq/L
Đáp án:
Bước 1: pH và [HCO3⁻] đều tăng nên có tình trạng kiềm chuyển hóa.
Bước 2: Giá trị pCO2 nên bằng bao nhiêu? Chúng ta đang muốn xem thử rằng có rối loạn hô hấp kèm theo kiềm chuyển hóa không. Giả sử giá trị bình thường của [HCO3⁻] là 24 và pCO2 bình thường là 40, đáp án sẽ là 𝑝𝐶𝑂2 = 40 + 0,7 × (35 − 24) = 47,7 𝑚𝑚𝐻𝑔. pCO2 của bệnh nhân là 48, phù hợp với giá trị bù trừ của hô hấp đối với kiềm chuyển hóa đơn thuần. Do đó không có rối loạn hô hấp kèm theo.
Bước 3: Anion gap bằng 8 (bình thường) Kết luận: Kiềm chuyển hóa.
4. Bệnh nhân có kết quả khí máu động mạch như sau pH= 7,68 , [HCO3⁻] = 40 mEq/L. pCO2= 35 mmHg, AG= 8 mEq/L
Đáp án:
Bước 1: [HCO3⁻] và pH cùng tăng. Có tình trạng kiềm chuyển hóa.
Bước 2: pCO2 nên bằng bao nhiêu? Đáp án là 𝑝𝐶𝑂2 = 40 + 0,7 × (40 − 24) = 51,2 𝑚𝑚𝐻𝑔. pCO2 đo được của bệnh nhân thấp hơn dự đoán rất nhiều, dù đã tính thêm khoảng dao động ± 5 mmHg do đáp ứng bù trừ khác nhau của từng bệnh nhân. Do đó, có tình trạng kiềm hô hấp kèm theo kiềm chuyển hóa.
Bước 3: Anion gap = 8 mEq/L (bình thường). Chúng ta đã xong. Có hai rối loạn toan kiềm riêng biệt tồn tại song song, mỗi loại có những nguyên nhân riêng. Bệnh nhân có kiềm chuyển hóa do một trong những nguyên nhân được liệt kê ở bảng 8-1 cộng thêm kiềm hô hấp. Nguyên nhân của từng loại rối loạn nên được xem xét riêng lẻ với nhau.
5. Bệnh nhân trước đó ổn định 25 phút trước biểu hiện suy hô hấp có kết quả khí máu động mạch như sau pH= 7,26 , [HCO3⁻] = 26 mEq/L. pCO2= 60 mmHg, AG= 6 mEq/L
Đáp án:
Bước 1: pCO2 tăng và pH giảm. Do đó có tình trạng toan hô hấp. Từ bệnh sử ta thấy được tình trạng này là cấp tính.
Bước 2: Với rối loạn hô hấp, chúng ta phải đặt ra câu hỏi: [HCO3⁻] nên bằng bao nhiêu? Hãy nhớ rằng sự bù trừ của chuyển hóa được tính toán dựa trên sự thay đổi tương ứng với 10 đơn vị pCO2. pCO2 tăng thêm 20 tức là 𝟐 × 10. Với toan hô hấp cấp, [HCO3⁻] nên giảm 1 mEq/L với mỗi 10 mmHg pCO2 tăng thêm. Do đó [HCO3⁻] nên biến đổi 𝟐 × 1 𝑚𝐸𝑞/𝐿 = 2 𝑚𝐸𝑞/𝐿. Sử dụng giá trị bình thường = 24, [HCO3⁻] nên bằng với 24 + 2 = 26. Do đó sự bù trừ là đầy đủ và không có rối loạn chuyển hóa kèm theo.
Bước 3: AG trong khoảng bình thường. Chúng ta đã xong Kết luận: Toan hô hấp cấp tính.
6. Bệnh nhân biểu hiện lo âu, có cảm giác “hít không đủ dưỡng khí” trong 4 ngày qua. Có kết quả khí máu động mạch như sau pH= 7,42 , [HCO3⁻] = 19 mEq/L. pCO2= 30 mmHg, AG= 8 mEq/L
Đáp án:
Bước 1: pCO2 giảm, pH tăng. Có tình trạng kiềm hô hấp. Bệnh sử gợi ý tới kiềm hô hấp mạn tính.
Bước 2: [HCO3⁻] nên bằng bao nhiêu? Hãy nhớ rằng sự bù trừ của chuyển hóa được tính toán dựa trên sự thay đổi tương ứng với 10 đơn vị pCO2. pCO2 của bệnh nhân giảm 10 đơn vị, tức là 𝟏 × 10. Với kiềm chuyển hóa mạn tính, [HCO3⁻] nên giảm xuống 5 với mỗi 10 mmHg pCO2 giảm đi. Do đó trong trường hợp này, [HCO3⁻] nên giảm đi 𝟏 × 5. [HCO3⁻] nên bằng với 24 − 5 = 19. Do đó sự bù trừ là đầy đủ và không có rối loạn chuyển hóa.
Bước 3: AG trong khoảng bình thường. Chúng ta đã xong. Kết luận: Kiềm hô hấp mạn tính. Có một điều thú vị là kiềm hô hấp mạn tính là rối loạn đơn thuần duy nhất mà sự bù trừ có thể mang pH trở về khoảng bình thường (trong trường hợp này là 7,42)
7. Bệnh nhân biểu hiện khó thở trong 2 tuần qua. Có kết quả khí máu động mạch như sau pH= 7,38 , [HCO3⁻] = 40 mEq/L. pCO2= 70 mmHg, AG= 8 mEq/L
Đáp án:
Bước 1: pCO2 tăng cao. Có tình trạng toan hô hấp. Dựa vào bệnh sử: tình trạng này mạn tính.
Bước 2: [HCO3⁻] nên bằng bao nhiêu? pCO2 tăng lên một khoảng 30 tức là 𝟑 × 10. Với toan hô hấp mạn tính, [HCO3⁻] nên tăng thêm một khoảng bằng 𝟑 × 3,5 = 10,5. Sử dụng giá trị bình thường bằng 24, [HCO3⁻] nên bằng 24 + 10,5 = 34,5. Nói ngắn gọn là: với toan hô hấp mạn tính thì [HCO3⁻] nên bằng 24 + (3 × 3,5) = 34,5. [HCO3⁻] của bệnh nhân cao hơn giá trị mong muốn. Do đó có tình trạng kiềm chuyển hóa nhẹ kèm theo. [HCO3⁻] tăng cao không chỉ là do bù trừ của tình trạng toan hô hấp mà còn gây ra bởi một rối loạn toan-kiềm riêng lẻ: kiềm chuyển hóa.
Bước 3: AG trong khoảng bình thường.
Kết luận: Toan hô hấp mạn tính kèm theo kiềm chuyển hóa.
Có hai rối loạn toan kiềm riêng biệt cùng tồn tại trên bệnh nhân. Cả hai đều là do bệnh lý chứ không phải do bù trừ nhau, mặc dù pH gần như bình thường. Nói cách khác, trên cơ thể bệnh nhân có hai quá trình diễn ra song song có xu hướng bù đắp lẫn nhau: Kiềm chuyển hóa do các nguyên nhân được liệt kê ở bảng 8-1 kèm theo toan hô hấp. Nguyên nhân của hai loại rối loạn nên được xem xét một cách riêng lẻ.
8. Bệnh nhân tương tự câu 7
Đáp án Hãy thử tiếp cận lại trường hợp này bằng một cách khác, khởi đầu với kiềm chuyển hóa.
Bước 1: [HCO3⁻] cao: có tình trạng kiềm chuyển hóa.
Bước 2: Với kiềm chuyển hóa, pCO2 nên bằng bao nhiêu? Đáp án là 40 + 0,7 × (40 − 24) = 51. pCO2 cao hơn giá trị này rất nhiều. Có gì đó đang đẩy nó lên: đó là tình trạng toan hô hấp. (Lưu ý thêm rằng khi bù trừ cho kiềm chuyển hóa, pCO2 không nên cao quá 55 mHg: Nếu cao hơn 55 mmHg thì gợi ý có tình trạng toan hô hấp).
Bước 3: AG trong khoảng bình thường Kết luận: Kiềm chuyển hóa kèm theo toan hô hấp. pH thường gần với giá trị bình thường trong các trường hợp tồn tại nhiều rối loạn có khả năng bù đắp lẫn nhau. Mỗi loại rối loạn sẽ đẩy pH theo chiều trái ngược nhau. Nếu được lựa chọn tiếp cận các trường hợp rối loạn hô hấp và chuyển hóa tồn tại cùng lúc với mức độ nặng tương đương nhau, bản thân tác giả sẽ thường bắt đầu phân tích dữ liệu có được theo hướng bắt đầu với rối loạn chuyển hóa trước. Nó sẽ bớt được việc suy nghĩ xem nên áp dụng công thức cấp hay mạn. Nhưng phương pháp 3 bước sẽ hiệu quả dù bạn bắt đầu tiếp cận theo hướng rối loạn chuyển hóa hay rối loạn hô hấp. Tác giả chỉ nhận thấy rằng bắt đầu với rối loạn chuyển hóa thỉnh thoảng sẽ bớt cồng kềnh hơn.
9. Bệnh nhân có kết quả khí máu động mạch như sau pH= 7,68 , [HCO3⁻] = 40 mEq/L. pCO2= 35 mmHg, AG= 11 mEq/L
Đáp án:
Bước 1: pH và [HCO3⁻] cùng tăng: có tình trạng kiềm chuyển hóa.
Bước 2: pCO2 nên bằng bao nhiêu? Áp dụng công thức cho kiềm chuyển hóa: 𝑝𝐶𝑂2 = 40 + 0,7 × (𝐻𝐶𝑂3 −đ𝑜 đượ𝑐− 𝐻𝐶𝑂3 −𝑏ì𝑛ℎ 𝑡ℎườ𝑛𝑔) = 40 + 0,7 × (40 − 24) = 40 + 11,2 = 51,2. pCO2 của bệnh nhân là 35, giảm đáng kể so với giá trị mong đợi. Do đó, có tình trạng kiềm hô hấp làm kéo giá trị này xuống.
Bước 3: AG là 11. Giá trị này bất thường nhưng vẫn dưới 15 nên chúng ta không thể khẳng định được có sự toan chuyển hóa tăng AG. Vậy chúng ta đã xong nhưng vẫn nên phải chú ý theo dõi sát AG của bệnh nhân Kết luận: Kiềm chuyển hóa kèm theo kiềm hô hấp. pH thường rất bất thường khi các rối loạn khác nhau cùng đẩy pH về chung một hướng.
10. Bệnh nhân biểu hiện khó thở được 3 ngày. Có kết quả khí máu động mạch như sau pH= 7,45 , [HCO3⁻] = 44 mEq/L. pCO2= 65 mmHg, AG= 8 mEq/L
Đáp án:
Bước 1: Cả pCO2 và [HCO3⁻] đều rất cao. pH nằm trong khoảng bình thường. Hãy tạm xem đây là kiềm chuyển hóa vì pH hơi tăng.
Bước 2: pCO2 nên bằng bao nhiêu? Với kiềm chuyển hóa, pCO2 nên bằng với 40 + 0,7 × (44 − 24) = 54. pCO2 của bệnh nhân là 65, cao hơn 11 mmHg so với giá trị mong đợi. Do đó có tình trạng toan hô hấp.
Bước 3: AG bình thường Kết luận: Toan hô hấp và kiềm chuyển hóa. Chú ý rằng pH nằm trong khoảng bình thường, trong khi pCO2 và [HCO3⁻] đều rất bất thường. Điều này cho chúng ta thấy ngay có rối loạn hỗn hợp, bởi vì sự bù trừ của bệnh nhân không thể đưa pH về bình thường hoàn toàn ngoại trừ trường hợp kiềm hô hấp mạn tính. Đây là một ví dụ cho trường hợp hai rối loạn bù đắp cho nhau; có nghĩa là các rối loạn có xu hướng triệt tiêu nhau khi đẩy pH về hai hướng trái nhau. Nếu bạn chỉ nhìn sơ nồng độ các chất thì bạn có thể nghĩ rằng bệnh nhân chỉ có toan hô hấp đơn thuần với sự bù trừ của chuyển hóa. Các dữ liệu nhìn có vẻ như chỉ có một loại rối loạn. Bước 2 cho chúng ta thấy rằng đây không phải là toan hô hấp đơn thuần với sự bù trừ của chuyển hóa. Bệnh nhân này có hai rối loạn riêng biệt.
11. Bệnh nhân tương tự như ca số 10, nhưng hãy phân tích bắt đầu từ rối loạn hô hấp. Biểu hiện khó thở được 3 ngày. Có kết quả khí máu động mạch như sau pH= 7,45 , [HCO3⁻] = 44 mEq/L. pCO2= 65 mmHg, AG= 8 mEq/L
Đáp án:
Bước 1: Cả pCO2 và [HCO3⁻] đều bất thường. pH nằm trong khoảng bình thường. Hãy tạm xem đây là toan hô hấp – mạn tính vì bệnh sử gợi ý tình trạng này đã tồn tại được 3 ngày.
Bước 2: [HCO3⁻] nên bằng bao nhiêu? Với toan hô hấp mạn tính, [HCO3⁻] nên bằng với 24 + (2,5 × 3,5) = 24 + 8,75 = 32,75. [HCO3⁻] của bệnh nhân là 44 mEq/L, quá cao. Do đó có kiềm chuyển hóa.
Bước 3: AG bình thường Kết luận: Toan hô hấp và kiềm chuyển hóa.
12. Bệnh nhân có kết quả khí máu động mạch như sau pH= 7,65 , [HCO3⁻] = 32 mEq/L. pCO2= 30 mmHg, AG= 24 mEq/L Bệnh nhân có nhiệt độ là 102°F (39°C) và huyết áp 80/50. Biểu hiện vã mồ hôi. Xét nghiệm nước tiểu thấy số lượng lớn bạch cầu và vi khuẩn. Cetone niệu âm tính trên xét nghiệm tổng phân tích nước tiểu
Đáp án:
Bước 1: pH và [HCO3⁻] cùng tăng (kiềm chuyển hóa) và pCO2 giảm (kiềm hô hấp). Hãy bắt đầu bằng kiềm chuyển hóa trước vì chọn thế nào cũng ra được kết quả.
Bước 2: Với kiềm chuyển hóa thì pCO2 nên bằng bao nhiêu? 𝑝𝐶𝑂2 = 40 + 0,7 × (32 − 24) = 45,6. Bệnh nhân có pCO2 là 30, thấp hơn giá trị 45,6 mong đợi. Do đó kiềm hô hấp cũng hiện diện và đẩy pH lên.
Bước 3: Anion gap là 24. Do đó, cũng có tình trạng toan chuyển hóa tăng anion gap. Hiện tại chúng ta đã có tới 3 rối loạn. Khi đạt tới 3 rối loạn rồi bạn có thể dừng lại. Ba là số lượng tối đa các rối loạn bạn có thể tìm được khi áp dụng phương pháp này. Tình trạng toan chuyển hóa tăng anion gap ở bệnh nhân này có thể do toan acid lactic.
Để thỏa trí tò mò thì lượng anion gap thay đổi là 24-6=18. Chúng ta hãy so sánh giá trị này với lượng [HCO3⁻] thay đổi. Sự giảm [HCO3⁻] mong đợi sẽ tầm khoảng: Lượng AG thay đổi/1,5 = 18/1,5 = 12. [HCO3⁻] không giảm mà còn tăng lên 8 mEq/L. Cao hơn giá trị mong đợi. Điều này có nghĩa là có tình trạng kiềm chuyển hóa nặng đẩy [HCO3⁻] lên khoảng 20 mEq/L kèm theo toan chuyển hóa kéo [HCO3⁻] xuống khoảng 12 mEq/L. Kiềm chuyển hóa và toan chuyển hóa có xu hướng bù trừ cho nhau, nhưng cả hai đều ở mức độ nặng. Chú ý rằng đây là những rối loạn riêng biệt và độc lập. Mỗi tình trạng đều có những chẩn đoán phân biệt riêng cần phải cân nhắc.
Kết luận: Kiềm chuyển hóa (nặng), toan chuyển hóa tăng AG (nặng) và kiềm hô hấp (trung bình tới nặng). Chú ý rằng [HCO3⁻]=32 mEq/L nhìn sơ thì trông có vẻ không tệ lắm, nhưng tình trạng kiềm chuyển hóa cũng rất nặng. Tính khoảng AG và việc so sánh lượng AG tăng với lượng [HCO3⁻] giảm tỏ ra hữu ích trong trường hợp này.
13. Bệnh nhân bị toan cetone đái tháo đường, có kết quả khí máu động mạch như sau pH= 6,95 , [HCO3⁻] = 6 mEq/L. pCO2= 28 mmHg, AG= 26 mEq/L
Đáp án:
Bước 1: Toan chuyển hóa. pH trường hợp này thấp tới nỗi có thể gây trụy mạch.
Bước 2: pCO2 nên bằng bao nhiêu 𝑝𝐶𝑂2 = 1,5 × 6 + 8 = 17 . Bệnh nhân này có pCO2 đo được cao hơn rất nhiều giá trị mong đợi trong tình trạng toan chuyển hóa. pCO2 cao gợi ý tới tình trạng toan hô hấp, có lẽ do mỏi cơ hô hấp. Một số tác giả có thể gọi đây là “bù trừ không đủ” thay vì toan hô hấp bởi vì giá trị của pCO2 thấp chứ không cao. Quan điểm này cũng đúng phần nào đó, nhưng hãy cứ theo thuật ngữ ban đầu của chúng ta để không làm kẹt mọi thứ lại. Vậy bệnh nhân có toan hô hấp. Hãy nhớ rằng bệnh nhân không thể duy trì pCO2 trong khoảng 10-20 mà không dẫn tới đuối sức. Vậy bệnh nhân này có toan chuyển hóa và toan hô hấp do mỏi cơ hô hấp.
Bước 3: Khoảng AG là 26. Do đó, có tình trạng toan chuyển hóa tăng anion gap. Lượng anion gap tăng lên là 20 mEq/L, phù hợp với chẩn đoán toan chuyển hóa tăng anion gap. Lượng [HCO3⁻] giảm xuống dự đoán sẽ vào khoảng 20 mEq/L. Lượng [HCO3⁻] giảm thực tế là 18, rất gần với 20. Do đó [HCO3⁻] gần với giá trị mong đợi trong toan ketone đơn thuần, và không có rối loạn kiềm toan “tiềm ẩn” nào.
Kết luận: Toan chuyển hóa tăng anion gap do toan ketone đái tháo đường, toan hô hấp có lẽ do mỏi cơ hô hấp. Với nguyên nhân của toan hô hấp chúng ta cũng có thể cân nhắc giữa nguyên nhân sử dụng thuốc gây ức chế hô hấp và một quá trình tổn thương phổi độc lập.
14. Bệnh nhân bị nhiều đợt tắc ruột với tình trạng đau bụng nặng nề và nôn ói. Có kết quả khí máu động mạch như sau: pH= 7,33 , [HCO3⁻] = 18 mEq/L. pCO2= 35 mmHg, AG= 27 mEq/L Xét nghiệm cetone trên que nhúng âm tính. Huyết áp là 82/54 và nhịp tim 116.
Đáp án:
Bước 1: [HCO3⁻] và pH đều giảm. Toan chuyển hóa. Nghĩ nhiều do toan acid lactic. Nhìn sơ trông có vẻ rất nhẹ
Bước 2: pCO2 nên bằng bao nhiêu? (1,5 × 18) + 8 = 35. Không có rối loạn hô hấp kèm theo
Bước 3: Anion gap bằng 27 cho thấy có tình trạng toan chuyển hóa tăng anion gap. Lượng anion gap tăng lên bằng 21. Lượng [HCO3⁻] giảm xuống nên vào khoảng 21/1,5=14 trong trường hợp toan acid lactic, nhưng thực tế chỉ có 6. Do đó, có lẽ có tồn tại một tình trạng kiềm chuyển hóa “ tiềm ẩn” làm “đẩy” nồng độ bicarbonate lên cao hơn.
15. Bệnh nhân đái tháo đường 21 tuổi nôn ói nhiều có kết quả khí máu động mạch như sau: pH= 7,75 , [HCO3⁻] = 32 mEq/L. pCO2= 24 mmHg, AG= 24 mEq/L Xét nghiệm cetone trong tổng phân tích nước tiểu và trong huyết thanh đều dương tính mạnh.
Đáp án:
Bước 1: pH tăng rất cao. [HCO3⁻] cũng tăng còn pCO2 giảm. Cả hai tình trạng đều làm đẩy pH lên. Đây là ví dụ cho loại rối loạn mà pH bị đẩy cùng một chiều bởi cả pCO2 và [HCO3⁻]. Bệnh nhân này có hạ kali máu đe dọa tính mạng. Bạn có thể bắt đầu phân tích bằng pCO2 hoặc [HCO3⁻] trong trường hợp này. Nhưng tác giả thích bắt đầu với kiềm chuyển hóa hơn.
Bước 2: pCO2 nên bằng bao nhiêu? 40 + 0,7 × (32 − 24) = 45,6 𝑚𝑚𝐻𝑔. pCO2 của bệnh nhân là 24, thấp hơn rất nhiều so với mong đợi. Có tình trạng kiềm hô hấp nặng kèm theo kiềm chuyển hóa.
Bước 3: AG là 24. Có tình trạng toan chuyển hóa tăng anion gap. Một khi đã tìm ra 3 loại rối loạn thì bạn có thể dừng lại. Đó là số lượng tối đa đối với phương pháp này. Nhưng hãy khám phá thêm tí nữa, lượng AG tăng lên là 18. Nồng độ [HCO3⁻] nên tương ứng nên vào khoảng 18 mEq/L, xuống 6 mEq/L. Nhưng nó lại tăng lên tới 32 !! [HCO3⁻] tăng chứ không giảm. Có thứ gì đó đang đẩy [HCO3⁻] từ 6 mEq/L lên 32 mEq/L. Ban đầu khi nhìn sơ qua [HCO3⁻] gợi ý tình trạng kiềm chuyển hóa này là “nhẹ” nhưng giờ ta có thể thấy nó rất nặng nề.
Kết luận: Kiềm hô hấp (nặng), toan chuyển hóa tăng AG (nặng), kiềm chuyển hóa (nặng). Hẳn 3 rối loạn. Nếu bạn theo dõi chương này được tới đây thì bạn làm tốt lắm.
16. Đây hoàn toàn là câu hỏi không bắt buộc: Hãy đọc những bình luận về bù trừ của hô hấp trong trường hợp toan chuyển hóa ở ca số 2. Làm sao tác giả lại biết được pH = 7,00 ở bệnh nhân có [HCO3⁻]=3 mEq/L và pCO2 = 12,5 mmHg sẽ giảm xuống 6,80 nếu pCO2 tăng lên mức 20 mmHg?
Đáp án:
Tác giả đã sử dụng phương trình Henderson-Hasselbalch:
𝑝𝐻 = 6,1 + 𝑙𝑜𝑔 ( [𝐻𝐶𝑂3⁻] / 0,03 / 𝑝𝐶𝑂2 )
Và chỉ đơn giản là thay
[HCO3⁻]= 3 mEq/L và pCO2= 20 mmHg vào. 𝑝𝐻 = 6,1 + 𝑙𝑜𝑔 ( 3/ 0,03 / 20)
𝑝𝐻 = 6,1 + 𝑙𝑜𝑔 ( 3 / 0,6 ) = 6,1 + 𝑙𝑜𝑔(5) = 6,1 + 0,70 = 6,80
Phương trình này hữu ích trong trường hợp xem thử các kết quả pH, [HCO3⁻] và pCO2 có phù hợp với nhau không, hay đã có sai sót ở phòng xét nghiệm trong khâu đo lường các đại lượng này. Công thức này được nêu ra là bởi thỉnh thoảng nó sẽ là phương pháp hữu ích để xác định xem kết quả pH, [HCO3⁻] và pCO2 có chính xác không và dự đoán xem chuyện gì sẽ xảy ra với pH khi thay đổi [HCO3⁻] và pCO2.
Có một phương pháp xấp xỉ không cần sử dụng tới logarit nhưng phương trình Henderson-Hasselbalch là đơn giản nhất đối với tác giả. Nên tôi chỉ biết cắn răng chịu đựng và tính ra. Công thức này được đưa vào bởi nó có thể giúp ích cho bạn vào một ngày nào đó, nhưng nó không quan trọng cho việc phân tích các bài tập trong cuốn sách này.
Những ví dụ lâm sàng
Ca số 1
Bệnh nhân nam 50 tuổi, nặng 70 kg có tiền căn nghiện rượu, bệnh được 4 ngày với những biểu hiện: buồn nôn, nôn, đau bụng mức độ trung bình, xuất hiện sau một tuần uống rượu nhiều. Bệnh nhân không thể ăn. Khám lâm sàng ghi nhận niêm mạc khô, có hạ huyết áp tư thế và nhịp tăng khi thay đổi tư thế Kết quả cận lâm sàng: Na⁺ =140 mEq/L, K⁺ = 3,1 mEq/L, [HCO3⁻] = 20 mEq/L, Cl⁻= 92 mEq/L, glucose 86 mg/dL, BUN = 52 mg/dL, Cr = 1,4 mg/dL, amylase hiện chưa có, cetone huyết tương dương tính mạnh. Khí máu động mạch: pH = 7,32, pCO2= 40 mmHg, [HCO3⁻] = 20 mEq/L. Natri niệu = 30 mEq/L, Clorua niệu = 5 mEq/L (thấp), cetone niệu: tăng cao. Chẩn đoán của bạn là gì và bạn sẽ tiếp cận bệnh nhân này như thế nào?
Đáp án: Bệnh sử và kết quả cận lâm sàng gợi ý tới toan ketone do rượu kèm theo hạ natri máu thứ phát (không rõ tác giả có nhầm không?) do giảm thể tích dịch (nôn ói) và hạ kali máu thứ phát do nôn ói và toan ketone. Còn có thể có thêm tình trạng viêm tụy cấp. Đây là một rối loạn toan kiềm phức tạp, mặc dù pH chỉ giảm một ít.
1. Rối loạn toan-kiềm phức tạp
Bước 1: pH chỉ giảm nhẹ, [HCO3⁻] cũng giảm: có tình trạng toan chuyển hóa. pCO2 trong giá trị “bình thường” .
Bước 2: Đối với toan chuyển hóa thì pCO2 nên bằng bao nhiêu? 𝑝𝐶𝑂2 = (1,5 × 20) + 8 = 38. pCO2 đo được là 40 mmHg, rất gần với giá trị dự đoán nên không có rối loạn hô hấp kèm theo.
Bước 3: Anion gap tính được là 140 − (20 + 92) = 28!. Do đó có tình trạng toan chuyển hóa tăng anion gap. Giờ hãy so sánh sự biến đổi anion gap (28 – 6= 22) với sự biến đổi của [HCO3⁻] (=4). Lượng [HCO3⁻] giảm dự đoán đối với toan ketone phải vào khoảng 22 mEq/L. Nhưng [HCO3⁻] chỉ biến đổi 4 thay vì 22 mEq/L. Do đó, tồn tại tình trạng kiềm chuyển hóa làm đẩy [HCO3⁻] lên cùng với toan chuyển hóa tăng anion gap nặng làm kéo [HCO3⁻] xuống. Chúng có xu hướng bù trừ lẫn nhau, nhưng cả hai đều ở mức độ nặng. Vậy, đáp án của tình trạng rối loạn kiềm toan là:
- Toan chuyển hóa tăng anion gap do toan ketone do rượu (xem lại bảng 7-1 cho những nguyên nhân khác).
- Kiềm chuyển hóa do nôn ói (xem lại bảng 8-1 cho những nguyên nhân khác).
Tác giả thường lưu ý cân nhắc ngộ độc ethylene glycol và methanol ở những bệnh nhân nghiện rượu có toan chuyển hóa tăng AG.
2. Hạ kali máu
Tình trạng hạ kali máu nhiều khả năng là thứ phát sau nôn ói và toan ketone. Tỉ lệ kali trên creatinin trong mẫu nước tiểu một thời điểm > 20 mEq/g sẽ gợi ý tình trạng mất kali qua thận (hãy nhớ lại rằng hạ kali máu trong nôn ói và toan ketone đều là do mất qua nước tiểu). Nồng độ kali trong huyết tương = 3,1 mEq/L gợi ý có sự thiếu hụt kali nhiều, khoảng 400 mEq. Nồng độ kali có thể sẽ hạ khi được truyền glucose, do đó việc bù kali nên được bắt đầu ngay khi bạn xác định được bệnh nhân không bị vô niệu và nồng độ kali nên được kiểm tra lại mỗi 2-3 tiếng. Nếu nồng độ kali giảm thì nên tăng thêm lượng bù (nếu kali giảm nhanh thì nên tạm ngưng saline có chứa glucose và thay bằng saline 0,9% nếu cần thiết). Việc đo nồng độ magie cũng rất quan trọng trong bệnh cảnh này. Phải nhớ rằng không thể bù kali hiệu quả cho tới khi tình trạng thiếu hụt magie được điều chỉnh.
3. Điều trị
Bệnh nhân toan ketone do rượu cần phải bổ sung glucose cùng với saline đẳng trương để đảo ngược tình trạng tăng tạo ketone. Ngoài ra cũng nên bổ sung thêm các loại vitamine, thiamine và folate ở những bệnh nhân này. Sử dụng glucose đường tĩnh mạch có thể gây bệnh não Wernicke cấp tính trên bệnh nhân này nếu như chưa dùng thiamine (100mg TB) trước đó. Cho nên, ở bệnh nhân nghiện rượu thì đầu tiên cho thiamine, sau đó mới bắt đầu truyền dịch. Y lệnh dịch truyền tĩnh mạch có thể là:
100 mg thiamine TM ngay lập tức. Sau đó lặp lại mỗi 6-12 tiếng mỗi ngày trong ít nhất 3 ngày .
Lít dịch truyền đầu tiên: saline D5 0,9% kèm theo 30 mEq/L KCl, 5mg folate, 1 ống multivitamin; tốc độ truyền 250 cc/h.
Lít dịch truyền thứ 2: saline D5 0,9% kèm theo 30 mEq/L KCl, 5mg folate, 1 ống multivitamin; tốc độ truyền 175 cc/h.
Lít dịch truyền thứ 3: saline D5 0,9% kèm theo 30 mEq/KCl; tốc độ truyền 175 cc/h Y lệnh truyền dịch sẽ không được hoàn chỉnh nếu thiếu chỉ định theo dõi: cân nặng mỗi ngày. Glucose, natri, kali, clorua, bicarbonate, BUN, creatinin (Cr) sau 3 tiếng, 6 tiếng và 9 tiếng, và mỗi sáng sớm. Nếu nồng độ kali giảm thì nên tăng thêm lượng bù.
Ca số 2
Bệnh nhân nam 26 tuổi, tiền căn đái tháo đường biểu hiện tiểu nhiều, khát nhiều, buồn nôn và nôn, xuất hiện sau một đợt “cúm”. Bệnh nhân khai rằng không thể giữ lại được gì sau ăn do nôn ói nhiều trong 2 ngày nay. Nhiệt độ của bệnh nhân là 102°F (38,9°C), huyết áp và nhịp tim ở tư thế nằm lần lượt là 118/74 và 100. Khi ngồi thõng chân xuống giường thì huyết áp là 90/60, nhịp tim 120. Bệnh nhân có biểu hiện khó thở và co kéo cơ hô hấp phụ. Khám phổi ghi nhận có khò khè và ran ở đáy phổi 2 bên. Kết quả cận lâm sàng: Na⁺ =140 mEq/L, K⁺ = 4,5 mEq/L, [HCO3⁻] = 15 mEq/L, Cl⁻= 98 mEq/L, glucose 325 mg/dL, BUN = 30 mg/dL, Cr = 1,2 mg/dL, pH= 7,15, pCO2= 45 mmHg. Công thức máu: Hgb/Hct= 12/36, WBC = 15 000. Xét nghiệm nước tiểu: protein (1+), cetone dương tính mạnh, soi cặn lắng nước tiểu âm tính, Nồng độ cetone trong huyết tương dương tính mạnh Chẩn đoán của bạn là gì và bạn sẽ tiếp cận bệnh nhân này như thế nào?
Đáp án :
1. Rối loạn toan kiềm
Bước 1: Toan chuyển hóa (pH và [HCO3-] cùng giảm).
Bước 2: Giá trị pCO2 nên bằng bao nhiêu? pCO2 nên bằng = (1,5 × 15) + 8 = 30,5. pCO2 đo được là 45 mmHg. Cao hơn đáng kể so với giá trị mong đợi. Tình trạng toan hô hấp làm cho bệnh nhân không thể bù trừ toan chuyển hóa đủ được. Toan hô hấp gây ra bởi bệnh lý đồng mắc ở phổi (viêm phổi/viêm phế quản/ mỏi cơ hô hấp?). Lưu ý rằng sự bù trừ thất bại của hô hấp trong toan chuyển hóa là một yếu tố tiên lượng xấu.
Bước 3: Anion gap tính được là 140 − (15 + 98) = 27 𝑚𝐸𝑞/𝐿. Do đó có tình trạng toan chuyển hóa tăng anion gap. Giờ hãy so sánh sự biến đổi anion gap (27 – 6= 21) với sự biến đổi của [HCO3⁻] (24-15=9). Lượng [HCO3-] giảm thấp hơn 12 mEq so với giá trị mong đợi. Sự chênh lệch giữa lượng anion gap tăng và bicarbonate giảm đủ để chắc chắn rằng có tình trạng kiềm chuyển hóa kèm theo. Vậy có 3 tình trạng rối loạn kiềm toan là:
- Toan ketone đái tháo đường (AG=27), có thể khởi phát do tình trạng nhiễm trùng hô hấp của bệnh nhân.
- Toan hô hấp do bệnh lý ở phổi hiện chưa được chẩn đoán.
- Kiềm chuyển hóa. Tình trạng này không dễ nhìn ra được cho tới khi chúng ta so sánh sự biến đổi của anion gap với bicarbonate. Khi khai thác bệnh sử kĩ hơn, bệnh nhân khai rằng tình trạng nôn ói rất nặng.
2. Sự thiếu hụt kali
Nồng độ kali = 4,5 mEq/L nhiều khả năng biểu thị cho sự thiếu hụt kali trầm trọng bị ẩn giấu ở bệnh nhân toan ketone đái tháo đường có pH máu = 7,15 kèm theo nôn ói nhiều ngày. Cần phải bù kali ngay khi xác nhận bệnh nhân không bị vô niệu.
3. Cân nhắc điều trị
pH máu bằng 7,15 và bệnh nhân có biểu hiện những dấu hiệu rối loạn hô hấp cùng với không có khả năng bù trừ đủ cho tình trạng toan chuyển hóa. Ở những bệnh nhân này nếu giảm tần số thở đi, pH sẽ tụt thẳng xuống và có thể rơi vào tình trạng ngưng tim. Trong những trường hợp này, tác giả sẽ cân nhắc tới bù HCO3-, mặc dù có nhiều lý do không ủng hộ việc bù HCO3- ngay ở bệnh nhân này:
- Ketone sẽ được chuyển thành HCO3- tại gan khi tình trạng tăng tạo ketone được đảo ngược bởi insulin và dịch truyền.
- Có nguy cơ xuất hiện kiềm chuyển hóa ngược lại.
- HCO3- có thể nâng pH lên quá nhanh, làm kali di chuyển vào tế bào. Nếu nồng độ kali của bệnh nhân này thấp hơn, chẳng hạn như khoảng 3,5, thì càng phải cân nhắc tới yếu tố này hơn.
- Có lẽ quan trọng hơn việc bù bicarbonate là bệnh nhân có thể cần phải được đặt nội khí quản và thở máy cùng với theo dõi sát để nhanh chóng quản lý tình trạng bệnh ở phổi của bệnh nhân.
Bệnh nhân nên được điều trị với insulin đường tĩnh mạch, KCl và saline 0,9%. Một khi đã xác nhận được không có tình trạng vô niệu, nên chỉ định dịch truyền ban đầu là: saline 0,9% kèm theo 30-40 mEq/L KCl; tốc độ truyền 250 ml/h. Ion đồ và khí máu động mạch nên được kiểm tra lại mỗi 1-2 tiếng. Tùy theo kết quả xét nghiệm, có thể cần phải tăng tốc độ bù kali nhanh hơn. Nồng độ calci, magie, phosphate vô cơ huyết tương cũng nên được kiểm tra ở bệnh nhân này và nên bổ sung thêm các loại vitamin, folate vào trong lít dịch truyền đầu tiên. Nên bổ sung thêm cả Thiamine. Chẩn đoán và điều trị phù hợp tình trạng bệnh lý gây toan hô hấp ở phổi cùng với theo dõi tình trạng hô hấp và pH sẽ là mấu chốt trong ca này. Nếu hô hấp bị mất bù nặng, có thể cần phải đặt nội khí quản và thở máy.
Ca số 3
Bệnh nhân nữ 75 tuổi nhập viện vì đau lưng. Kết quả cận lâm sàng: Na⁺ =124 mEq/L, K⁺ = 4,2 mEq/L, [HCO3⁻] = 24 mEq/L, Cl⁻= 100 mEq/L, glucose 90 mg/dL, BUN = 28 mg/dL Bạn có suy nghĩ gì về bệnh nhân này?
Đáp án:
Bạn đã tính anion gap, đúng chứ? Tất nhiên là đúng rồi. Anion gap giảm thấp (=0) là dấu hiệu gợi ý tới đa u tủy. Ở một vài bệnh nhân, những paraprotein được tích điện dương và làm tăng thêm lượng cation không định lượng được (unmeasured cation -UC) nên anion gap sẽ giảm căn cứ theo phương trình AG= UA-UC. Nồng độ protein của bệnh nhân này là 12g/dL và tình trạng hạ natri máu là giả do tăng paraprotein máu trong đa u tủy. Phòng xét nghiệm của bệnh viện vì một lý do nào đó mà không sử dụng điện cực natri. Áp lực thẩm thấu huyết tương bình thường. Bệnh nhân này không có tình trạng tăng trương lực (nồng độ thẩm thấu đo được là 285 mOsm/L). Bệnh nhân có hạ natri máu giả sẽ có tình trạng tăng osmolal gap. Osmolal gap bằng với:
285 − (248 + 90/18 + 28/2,8) = 22 𝑚𝑂𝑠𝑚/𝐿
Tác giả bổ sung thêm bài tập này chủ yếu là vì bạn có thể sẽ gặp lại cô này trong đề thi. Và tác giả cũng cần tự nhắc nhở bản thân phải tính anion gap trên mọi điện giải đồ.
Ca số 4
Bệnh nhân nữ 65 tuổi biểu hiện giảm trí nhớ nhẹ. Cô ấy hiện đang sống với chồng mình là Fred và những chú mèo của họ, Sidney và Tabbert. Bệnh nhân đã không đi khám bệnh 25 năm nay. Kết quả cận lâm sàng: Na⁺ =124 mEq/L, K⁺ = 4,2 mEq/L, [HCO3⁻] = 24 mEq/L, Cl⁻= 90 mEq/L, glucose 90 mg/dL, BUN = 14 mg/dL, Cr = 0,8 mg/dL Bạn có suy nghĩ gì về bệnh nhân này?
Đáp án:
Hãy xem lại bảng 3-1 và 3-2 cùng với phần Chẩn đoán hạ natri máu trong chương 3. Bạn sẽ muốn biết thêm áp suất thẩm thấu đo được. Giá trị đó bằng 260 mOsm/L, và osmolal gap bằng 2 mOsm/L. Bệnh nhân này có hạ natri máu với áp suất thẩm thấu giảm. Hạ natri máu đi kèm với áp suất thẩm thấu giảm luôn là do sự giảm thải nước cùng với lượng nước nhập quá mức. Tiếp cận theo hệ thống theo các bước:
- Có bệnh thận mạn hay tổn thương thận cấp? Nồng độ creatinin bình thường. Bệnh nhân có thể vẫn có bệnh thận mạn nhưng mức độ vẫn chưa đủ để hạ natri máu mà không tăng lượng nước nhập lớn.
- Có bằng chứng của tăng hay giảm thể tích dịch ngoại bào không? Phải cẩn thận tìm tình trạng phù hoặc dấu thiếu nước. Trong ca này thì không có. Khi tiến hành đo nồng độ natri trong nước tiểu thì có kết quả là 45 mEq/L, không phù hợp với thiếu dịch và phù.
- Bệnh nhân có sử dụng thuốc thiazide không? Ở bệnh nhân nữ lớn tuổi, hạ natri máu có thể do sử dụng lợi tiểu thiazide để điều trị tăng huyết áp. Bệnh nhân không có tiền căn này.
- Bệnh nhân có sử dụng thuốc có khả năng gây ra SIADH không (xem kỹ lại bảng 3-2).
- Có bằng chứng của suy thượng thận hay suy giáp không? Khi nghi ngờ nên xét nghiệm kĩ thêm.
- Xem bệnh nhân ăn theo chế độ “tea and toast” không.
- Cân nhắc tình trạng tăng lượng nước nhập mặc dù bệnh sử không gợi ý bệnh nhân là vận động viên, nghiện bia rượu, tâm thần phân liệt hay sử dụng thuốc phiện. Nhưng mặt khác thì có lẽ bạn cũng không thể nào biết chính xác được.
Nếu sự đào thải chất tan thấp và lượng nước nhập đủ lớn ở bệnh nhân có rối loạn pha loãng nước tiểu thì có thể gây ra hạ natri máu. Ở người Mỹ trưởng thành, lượng chất tan nhập trung bình vào khoảng 600-900 mOsm, bao gồm chủ yếu là urea và điện giải (hầu hết là natri và kali). Bệnh nhân lớn tuổi, ăn uống thiếu đạm và muối có thể giảm thải nước do giảm bài xuất chất tan. Lượng chất tan nhập vào trường hợp này có thể vào khoảng 300 mOsm/ngày. Tăng nhập chất tan sẽ giúp đào thải nước và đưa nồng độ natri huyết tương về giá trị bình thường. Việc nhận diện bệnh nhân sử dụng chế độ ăn “tea and toast” rất quan trọng vì khi những bệnh nhân này tăng lượng chất tan nhập vào sẽ có nguy cơ gây điều chỉnh tình trạng hạ natri máu mạn quá nhanh và nên được theo dõi kỹ càng.
Ca số 5
Bệnh nhân nữ 45 tuổi có tiền căn đái tháo đường, nhập viện do tăng kali máu. Bệnh nhân cảm giác vẫn ổn. Bệnh sử không ghi nhận yếu cơ. Thuốc bệnh nhân đang dùng hiện tại gồm: captopril 25 mg 3 lần ngày, ibuprofen 400 mg khi cần thiết, glyburide 10 mg mỗi ngày và các loại vitamin. Bệnh nhân khai rằng gần đây mới bắt đầu tập luyện để chuẩn bị cho kì thi thể thao. Kết quả cận lâm sàng: Na⁺ =138 mEq/L, K⁺ = 7,3 mEq/L, [HCO3⁻] = 20 mEq/L, Cl⁻= 100 mEq/L, glucose 160 mg/dL, BUN = 35 mg/dL, Cr = 2,1 mg/dL. Tổng phân tích nước tiểu: protein (1+), glucose (2+). Soi cặn lắng âm tính Bạn sẽ tiếp cận chẩn đoán và xử lý bệnh nhân này như thế nào?
Đáp án:
- Ngưng sử dụng tất cả nguồn nhập kali.
- Đo ECG ngay lập tức. Nếu có dấu hiệu của tăng kali máu trên ECG thì nên bổ sung calcium gluconate để bù trừ lại tác động điện thế trên tim của tăng kali máu. Có thể kèm theo glucose/insulin hay thuốc đồng vận β2 đường khí dung(Bảng 6- 2).
- Liệt kê nhanh trong đầu những nguồn kali “tiềm ẩn” và các nguyên nhân có thể gây tăng kali như: Penicillin kali, Muối thay thế (có thể chứa KCl), Tán huyết do truyền máu, Xuất huyết tiêu hóa, Ly giải cơ, Bỏng, Đại phẫu, Các loại thuốc có thể gây tăng kali máu.
- Kiểm tra lại nồng độ kali (dặn bệnh nhân không nắm chặt tay lúc lấy máu để hạn chế khả năng tán huyết) .
- Xem xét những thuốc bệnh nhân đang sử dụng.
- Xác định nguyên nhân gây tăng kali máu.
Các nguyên nhân tăng kali máu được liệt kê ở bảng 6-1. Bệnh nhân này có thể có hội chứng thiếu hụt aldosterone hạ renin máu (syndrome of hyporeninemic hypoaldosteronism -SHH) được làm nặng thêm bởi ibuprofen và captopril. Cũng nên cân nhắc thêm suy thượng thận nguyên phát và hội chứng ống thận không đáp ứng với aldosterone. Nồng độ creatinin bằng 2,1 mg/dL gợi ý bệnh nhân có bệnh thận mạn, có thể góp phần vào sự giảm đào thải kali. Nhớ rằng các nguyên nhân tăng kali máu có thể phối hợp với nhau nên bệnh nhân có thể có nhiều tình trạng gây tăng kali máu. Chỉ định điều trị khẩn cấp cho bệnh nhân này phụ thuộc vào việc có biểu hiện tăng kali máu đáng kể trên ECG không và mức độ tăng kali máu. Điều trị kéo dài cho bệnh nhân khởi đầu bằng việc ngưng các thuốc ảnh hưởng tới bệnh, nhịn ăn và sử dụng chế độ ăn hạn chế kali, bởi vì căn nguyên của vấn đề là sự giữ kali của thận. Tình trạng tăng kali máu trong hội chứng SHH thường sẽ đáp ứng với thuốc lợi tiểu quai.
Ca số 6
Bệnh nhân nữ 50 tuổi nhập viện vì buồn nôn, nôn kéo dài và đau bụng. X quang bụng cho thấy có tình trạng tắc ruột, được điều trị với: hút dịch dạ dày và truyền tĩnh mạch (0,9% saline kèm theo 30 mEq/L KCl). Bệnh nhân khai rằng tình trạng đau bụng, ban đầu đã khỏi sau khi hút dịch dạ dày và truyền tĩnh mạch, nay đã xuất hiện trở lại. Nhiệt độ hiện tại của bệnh nhân là 101,6°F (38,7°C), huyết áp hạ từ 130/86 xuống còn 86/52. Khám ghi nhận bụng ấn đau và mất âm ruột Kết quả cận lâm sàng: Na⁺ =140 mEq/L, K⁺ = 4,5 mEq/L, [HCO3⁻] = 25 mEq/L, Cl⁻= 86 mEq/L, pH = 7,40, pCO2 = 40 mmHg.
Đáp án:
Tình trạng rối loạn toan kiềm phức tạp:
Bước 1: Nhìn sơ qua thì không có rối loạn toan kiềm nào rõ ràng. pH, pCO2 và [HCO3-] đều trong khoảng bình thường.
Bước 2: Vì không có rối loạn toan kiềm rõ ràng nên sự bù trừ có phù hợp không không quan trọng.
Bước 3: Anion gap tính được là 140 − (25 + 86) = 29 !. Do đó có tình trạng toan chuyển hóa tăng anion gap nặng (nhiều khả năng là do lactic) Sự toan chuyển hóa này có khả năng là hậu quả của thiếu máu thành ruột. Vậy tại sao [HCO3⁻] lại bình thường? Đó là bởi có một tình trạng kiềm chuyển hóa với mức độ tương đương làm “che giấu” toan chuyển hóa. Chúng ta phải tính sự biến đổi của anion gap và so sánh với sự biến đổi của [HCO3-]. Sự biến đổi của anion gap là 29-6= 23. Do đó, trong tình trạng toan acid lactic, [HCO3-] nên vào khoảng 25-23/1,5 = 25-15,3= 9,7! Do đó có tình trạng kiềm chuyển hóa đẩy [HCO3-] lên khoảng 15,3 ở ca này, vậy tuy nồng độ [HCO3- ] bình thường nhưng có tới hai rối loạn toan kiềm nặng ở bệnh nhân này:
- Toan chuyển hóa tăng anion gap do thiếu máu thành ruột.
- Kiềm chuyển hóa do nôn ói và hút dịch dạ dày.
Việc bám sát 3 bước khi đánh giá bất kì bộ kết quả toan kiềm nào là hết sức quan trọng, thậm chí là khi mọi thứ ban đầu trông có vẻ bình thường. Tính anion gap và so sánh sự biến đổi với bicarbonate là mấu chốt để giải quyết ca này.
* Chú thích của dịch giả: chỗ này em dịch nguyên văn theo tác giả, nhưng em nghĩ là [HCO3-] mong đợi nên = 24 – 23/1,5 = 8,7 mới chính xác theo quy ước từ những chương trước, do đó có tình trạng kiềm chuyển hóa đẩy [HCO3-] lên một khoảng = 25 – 8,7= 16,3.
Câu hỏi lâm sàng
Câu 1
Nam 36 tuổi được đưa tới khoa cấp cứu do lú lẫn, buồn nôn và giảm tỉnh táo. Anh ta không thể trả lời các câu hỏi và không thể khai thác thêm bệnh sử. Thân nhiệt 36.7 độ C, mạch 86 lần/phút, nhịp thở 22 lần/phút. Khí máu và kết quả điện giải đồ của anh ta: pH 7.21, PaO2 96 mmHg, PaCo2 28 mmHg, Natri 136 mEq/L, Kali 3.6 mEq/L, Clo 90 mEq/L, Hco3- 12 mmHg, BUN 30 mg/dL, Creatinine huyết thanh 1.2 m/dL. Rối loạn toan kiềm nguyên phát nhiều khả năng nhất ở bệnh nhân này là gì?
- Nhiễm toan chuyển hóa không có khoảng trống anion.
- Nhiễm toan chuyển hóa có khoảng trống anion.
- Nhiễm kiềm chuyển hóa.
- Nhiễm kiềm hô hấp.
- Nhiễm toan hô hấp.
Đáp án đúng là B: Rối loạn toan kiềm nguyên phát ở bệnh nhân này là nhiễm toan chuyển hóa có khoảng trống anion. Bằng chứng là pH < 7.35, giảm nặng Hco3- (<24 mEq/L). Thông thường, khoảng trống anion được tạo ra bởi các phân tử tích điện âm (protein, citrate, phosphate, sulffate) thường thấy trong huyết thanh. Những phân tử này được tính và cho ra khoảng trống anion thông thường từ 10-14 mEq/L. Khoảng trống anion (AG) có thể được tính dựa theo công thức sau:
AG= Ion dương (Các cation đo được) – Ion âm (Các anion đo được).
Do đa số các ion dương trong huyết thanh là Natri và đa số ion âm trong huyết thanh là Clo- và Hco3- cho nên công thức tính AG huyết tương có thể tính đơn giản là = Natri – (hco3 + clo).
Bệnh nhân này tính được AG =136-(90+12) = 34 mEq/L, giá trị này tăng bất thường, Sự tăng AG chỉ ra sự xuất hiện của acid không phải chloride trong dịch ngoại bào (phosphate, sulfate), nội bào (keton, lactat, các anion uremic hữu cơ), các chất ngoài cơ thể (salicylat hoặc nhiễm độn các acid hữu cơ mà cơ thể sản xuất) hoặc các anion chưa xác định
Các nguyên nhân chính của toan chuyển hóa có khoảng trống anion và các anion không đo được tương ứng đáp ứng gây ra khoảng trống anion đó là:
- Nhiễm toan lactat (lactate)
- Nhiễm toan keton (butyrate beta-hydroxyl, acetoacetic acid)
- Nhiễm độc meTăng huyết ápnol/ formaldehyde (acid formic)
- Nhiễm độc ethylen glycol (acid glycolic, acid oxalic)
- Nhiễm độc salicylate (salicylic, lactic, acid sulfuric và acid phosphoric)
- Tăng ure máu (bệnh thận giai đoạn cuối) (bất thường trong đào thải H+)
Tổng kết: AG tương ứng với nồng độ của các anion không đo được trong huyết thanh. Trong toan chuyển hóa có khoản trống anion thì AG tăng bởi sự xuất hiện của các acid không phải chloride trong huyết thanh.
Câu 2
Bệnh nhân nữ 45 tuổi được đưa tới bác sĩ sau khi cô ta thấy buồn nôn, sốt và chướng vùng bụng trên. Tiền sử bao gồm trầm cảm nặng, đau nửa đầu và viêm khớp dạng thấp. Bệnh nhân nói rằng thấy ù tai (tinnitus) và chóng mặt (vertigo) nhiều. Cô ta thừa nhận rằng đã sử dụng quá liều thuốc vào vài tiếng trước. Thân nhiệt 38,1 độ C, huyết áp 120/78 mmHg, mạch 115 lần/phút và nhịp thở 26 lần/phút. Các thăm khám còn lại không có gì đáng chú ý. Dấu hiệu nào sau đây có nhiều khả năng nhất xuất hiện trên kết quả phân tích khí máu động mạch của cô ta?
| pH | PaCO2 | HCO3- | |
| A | 7.3 | 27 | 13 |
| B | 7.32 | 50 | 25 |
| C | 7.39 | 20 | 12 |
| D | 7.4 | 40 | 24 |
| E | 7.42 | 54 | 32 |
Đáp án đúng là C: Bệnh nhân có ù tai, sốt, thở nhanh, buồn nôn và kích ứng đường tiêu hóa sau sử dụng quá liều thuốc. Những biểu hiện này gợi ý tình trạng ngộ độc Salicylate (do aspirin để điều trị viêm khớp dạng thấp hoặc đau nửa đầu). Ngộ độc salicylat cấp dẫn tới nhiễm kiềm hô hấp thông qua kích thích trung tâm hô hấp ở hành não và gây thở nhanh (dẫn tới PaCo2 thấp do Co2 bị thở ra ngoài nhiều), nó sau đó gây ra “khoảng trông anion toan chuyển hóa” do không gắn với các chất phosphoryl oxi hóa trong ty thể dẫn tới chuyển hóa kị khí (dẫn tới giảm hco3- do tích tụ acid). Do đó, khí máu động mạch trong trường hợp nhiễm độc salicylate thường thể hiện:
- Giảm PaCo2: Do nhiễm kiềm hô hấp nguyên phát (và bù trừ bằng toan chuyển hóa).
- Giảm hco3-: Do nhiễm toan chuyển hóa nguyên phát (và bù trừ bằng kiềm hô hấp).
- pH động mạch gần như bth: khi 2 rối loạn cân bằng acid-base nguyên phát kia cân bằng nhau.
Khí máu động mạch của bệnh nhân này cho kết quả gần-bình-thường 7.39 với rối loạn kiềm hô hấp và toan chuyển hóa hỗn hợp. Hco3- giảm trong đáp án (Hco3-=12 mEq/L) chỉ ra sự toan chuyển hóa. Dựa trên công thức tương ứng cho bù trừ hô hấp (công thức Winter), PaCO2 mong đợi = (1.5*hco3-) + 8 +/- 2 (trong trường hợp này tính được là 26 +/- 2 mmHg). Bởi vì PaCo2 thực tế thấp hơn PaCo2 mong đợi nên có tình trạng nhiễm kiềm hô hấp đi kèm.
Một sai lầm thường thấy trong quản lý bệnh nhân nhiễm độc salicylat là thấy pH gần 7.4 và không nhận ra rối loạn acid-base hỗn hợp dẫn tới kết quả là điều trị (bằng kiềm hóa hoặc lọc máu) chậm trễ bởi nhầm tưởng bệnh nhân đã bù trừ thích hợp bằng toan. Tuy nhiên theo thời gian toan chuyển hóa nặng dần, bệnh nhân sẽ đạt tới điểm mà không thể thông khí đủ nhanh để bù trừ.
Đáp án A: Toan máu (pH 7.3) với hco3- (13 mEq/L) giảm gợi ý nhiễm toan chuyển hóa nguyên phát kết hợp với giảm paco2 bù trừ, bù trù trong trường hợp này là phù hợp (PaCo2 mong đợi = 1.5*13+8+/-2=27.5+/-2). Nhiễm toan chuyển hóa nguyên phát đơn độc hiếm khi thấy ở ng trưởng thành bị nhiễm độc aspirin và không đúng với bệnh nhân đã trải qua vài tiếng sau uống thuốc.
Đáp án B: Toan hóa máu (pH 7.32) với paCo2 cao (50 mmHg) gợi ý nhiễm toan hô hấp, bù trừ bằng chuyển hóa là phù hợp (hco3- =25, Ahco3- = 0.1*APaCQ2 =1 (lấy PaCO2 trung bình là 40).
Đáp án D: Kết quả khí máu này này thể hiện tình trạng kiềm toan bình thường.
Đáp án E: pH bình thường trong bệnh cảnh rối loạn toan-kiềm (PaCo2 và Hco3- bất thường) chỉ ra rối loạn hô hấp và chuyển hóa hỗn hợp. Trong trường hợp này, hco3- cao (32 mEq/L) gợi ý nhiễm kiềm chuyển hóa, paCQ2 (54 mmHg) cao hơn paCo2 mong đợi với bù trừ hô hấp nên đây là nhiễm toan hô hấp (APaCQ2=0.7*Ahco3-=5.6 (lấy hco3- trung bình là 24). Với khoảng Paco2 bình thường là 33-45 nên PaCo2 mong đợi sẽ là 39-51. Đây là rối loạn hỗn hợp kiềm chuyển hóa và toan hô hấp. Khởi đầu với toan hô hấp và tính toán mức bù trừ mong đợi cũng sẽ cho kết quả tương tự.
Tổng kết: Nhiễm độc aspirin nên được nghi ngờ ở các bệnh nhân có tam chứng sốt, ù tai và thở nhanh. Ng trưởng thành bị ngộ độc aspirin mắc kiềm hô hấp và toan chuyển hóa có khoảng trốíng anion. pH bình thường trong bệnh cảnh rối loạn toan-kiềm thường chỉ ra rối loạn toan-kiềm hỗn hợp.
Câu 3
Một nam giới 60 tuổi được đưa tới khoa cấp cứu do sốt, rét run và lú lẫn. Bệnh nhân đang đi câu cá trên biển vào hôm qua và bị đứt chân do cứa vào đá khi đang đi qua vùng nước nông. Anh ta không thể thể làm sạch vết thương ngay lúc đó và đêm qua nó trở nên sưng đỏ dần và đau. Bệnh nhân tỉnh dậy vài lần do sốt, rét run và sáng nay, vợ anh ta thấy chồng mình không còn nhận biết được. Tiền sử y khoa bao gồm Tăng huyết áp. Thân nhiệt 38.8 độ C, huyết áp 86/62 mmHg, mạch 118 lần/phút, nhịp thở 24 lần/phút. Thăm khám thấy bệnh nhân rối loạn mức độ vừa, tiếng tim nhanh, đều và không có tiếng thổi. Phổi trong, tiếng thở nhanh và nông. Chân phải thấy vết rách có mủ và máu chảy ra tới cẳng chân. Kết quả khí máu động mạch: pH 7.08, PaO2 86 mmHg, PaCo2 42 mmHg, Hco3- 12 mEq/L. Mô tả nào sau đây đúng nhất với tình trạng toan-kiềm ở bệnh nhân này?
- Toan chuyển hóa còn bù
- Toan hô hấp còn bù
- Toan chuyển hóa và toan hô hấp hỗn hợp
- Toan chuyển hóa và kiềm hô hấp hỗn hợp
- Kiềm chuyển hóa và toan hô hấp hỗn hợp
Đáp án đúng là C: Rối loạn toan kiềm hỗn hợp bao gồm >= 2 rối loạn nguyên phát và có thể được gợi thông qua giá trị pH rất bất thường (<7.2 hoặc >7.6) hoặc gần giá trị bình thường nhưng giá trị hco3- và paco2 bất thường. Tình trạng toan-kiềm được theo dõi tốt nhất qua các bước sau:
- Theo dõi pH (bình thường là 7.4). Bệnh nhân này 7.08 là có nhiễm toan.
- Xác định cơ chế khởi phát ban đầu: Phân tích vai trò của chuyển hóa trong cân bằng toan kiềm qua nồng độ hco3- huyết Tăng huyết ápnh (bình thường 24 mEq/L) và sự bù trừ hô hấp qua PaCO2 (bình thường:40 mmHg). Sự chuyển dịch của cân bằng này đưa ra giải thích về sự Tăng huyết ápy đổi của pH trong rối loạn nguyên phát. Bệnh nhân này có hco3- huyết Tăng huyết ápnh giảm (chuyển dịch về phía toan) chỉ ra toan chuyển hóa.
- Xác định sự bù trừ: rối loạn chuyển hóa nguyên phát nhanh chóng được bù trừ bằng việc điều chỉnh sự thông khí và lượng co2 đào thải ra ngoài. Bù trừ được mong đợi ở bệnh nhân toan chuyển hóa là kiềm hô hấp với paCo2 khoảng 26 (tương ứng với công
thức Winter: 1.5*12+8+/-2). Tuy nhiên, PaCo2 của bệnh nhân này là 42 cao hơn mức mong đợi chỉ ra rối loạn toan hô hấp là rối loạn thứ phát.
Thăm khám các biểu hiện lâm sàng nên được thực hiện để chắc chắn về rối loạn nguyên phát. Bệnh nhân này có nhiễm khuẩn do viêm mô tế bào chi dưới (sốt, huyết động không ổn định) giải thích cho toan chuyển hóa do nhiễm toan acid lactic. Sự tăng acid gây ra bởi nhiễm khuẩn nặng gây ra tăng thông khí nhưng bệnh nhân này lại thở nhanh nông biểu hiện sự mệt cơ hô hấp và giảm thông khí cái gây nên suy hô hấp và cuối cùng là nhiễm toan hô hấp. Cần dùng kháng sinh và bù dịch để điều trị nhiễm khuẩn và những bệnh nhân như này thường được đặt nội khí quản và thở máy.
Tổng kết: Rối loạn toan-kiềm hỗn hợp gồm >=2 rối loạn trở lên và có thể được phát hiện thông qua sự bù trừ rối loạn ban đầu không phù hợp. Nhiễm khuẩn kèm suy hô hấp là nguyên nhân chủ yếu gây toan chuyển hóa và hô hấp kết hợp.
Câu 4
Nam 56 tuổi mắc đái tháo đường được đưa tới khoa cấp cứu do nôn và buồn nôn. Trong khi đang thăm khám thì một nữ điều dưỡng hỏi liệu sự xác định tình trạng toan kiềm sẽ giúp xác định nguyên nhân và bước quản lý tiếp theo cho vấn đề của bệnh nhân. Cặp giá trị cận lâm sàng nào sau đây sẽ giúp có bức tranh tốt nhất về tình trạng toan kiềm của bệnh nhân?
- pH và PaCO2
- pH và PaO2
- PaO2 và PaCo2
- pH nước tiểu và PaCo2
- pH nước tiểu và Hco3-
Đáp án đúng là A Hệ đệm chính ngoài tế bào ở cơ thể người là hệ đệm CO2-HCO3, cái có pK là 6.1. Mất cân bằng toan-kiềm ở những bệnh nhân được chẩn đoán theo giá trị pH và sự thay đổi của cả nồng độ hco3- huyết thanh và áp lực riêng phần của CO2. Thông thường, tình trạng toan- kiềm của hệ đệm có thể được xác định bằng cách sử dụng công thức Henderson-Haselblach với 3 biến của nó pH, Acid và baso liên hợp:
pH= pK + log ([base liên hợp]/[acid])
Trong trường hợp cặp hệ đệm CO2-HCO3 thì CO2 là acid còn HCO3- là base liên hợp nên công thức trên sẽ là:
pH = pK + log(base/acid) =6.1+(Hco3- / (0.03*PaCo2)).
Sử dụng công thức này thì ta có thể tính được bất kỳ biến nào nếu cho trước giá trị của hai biến. Do đó, bằng cách áp dụng công thức trên nếu cho pH và PaCO2 thì ta có thể tính được HCO3- và với những dữ kiện này ta có thể xác định được tình trạng toan-kiềm của bệnh nhân.
Đáp án B, C, D và E: PO2 đưa thông tin về tình trạng oxy của bệnh nhân. pH nước tiểu có thể thay đổi từ 4.5 tới 8 – có thể đưa thông tin về sự điều chỉnh toan kiềm tại thận nhưng không thể sử dụng để xác định tình trạng toan-kiềm huyết thanh của bệh nhân như cách mà pH, HCO3- và PaCO2 có thể.
Tổng kết: Với bất kỳ bệnh nhân nào, pH và PaCo2 là hai giá trị xét nghiệm cần cung cấp để có được cái nhìn tốt nhất về tình trạng toan kiềm của bệnh nhân, hco3- có thể tính được từ các đại lượng khác bằng việc sử dụng công thức Henderson-Hassebalch.
Xem thêm: Hạ Natri máu: Nguyên nhân, chẩn đoán và điều trị – Bác sĩ Nguyễn Thế Bảo

