Bệnh da liễu
Hội chứng Stevens-Johnson: Nguyên nhân, chẩn đoán và hướng dẫn điều trị theo BMJ
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
Nhà thuốc Ngọc Anh – Để tải bài viết Hội chứng Stevens-Johnson: Nguyên nhân, chẩn đoán và hướng dẫn điều trị theo BMJ file PDF xin vui lòng click vào link ở đây.
Tóm tắt
- Hội chứng Stevens-Johnson (SJS) và hoại tử biểu bì nhiễm độc (TEN) có thể liên quan đến tiền sử dùng thuốc, thường gặp nhất là thuốc chống co giật, thuốc kháng sinh và thuốc kháng viêm không steroid. Các yếu tố liên quan khác bao gồm nhiễm trùng.
- Bệnh nhân có thể có dấu hiệu Nikolsky, lớp biểu bì dễ bị bong tróc khi ấn lực vào khu vực phồng rộp hoặc ban đỏ.
- Chẩn đoán dựa trên biểu hiện lâm sàng và được xác nhận bằng sinh thiết da.
- Khi chẩn đoán, nên dừng sử dụng thuốc gây tổn thương. Sau đó, điều trị hỗ trợ.
- Bệnh nhân phục hồi tốt nhất khi được chuyển đến trung tâm bỏng để chăm sóc vết thương ngay sau khi nghi ngờ hoặc chẩn đoán xác định.
- Đa số bệnh nhân SJS có thể hồi phục (tỷ lệ tử vong từ 1% đến 5%). SJS có thể tái phát với cùng loại thuốc hoặc với loại thuốc khác.
- TEN có tỷ lệ tử vong cao hơn (25% đến 30%).
- Về lâu dài, bệnh nhân cần đảm bảo không phơi nhiễm các thuốc kích hoạt và cẩn thận khi tự dùng thuốc. Bệnh nhân nên tránh ánh sáng mặt trời trong quá trình chữa lành và chú ý dưỡng ẩm da.
- Hiện tại, những bệnh nhân có nguy cơ có thể cần sàng lọc HLA (kháng nguyên bạch cầu ở người) nếu bệnh nhân sử dụng các loại thuốc như carbamazepine, allopurinol hoặc trimethoprim/sulfamethoxazol.
Thông tin cơ bản
Định nghĩa
Hội chứng Stevens-Johnson (SJS) là chứng bong tróc da nghiêm trọng cùng biến chứng niêm mạc.[1] Đây là một phản ứng miễn dịch với kháng nguyên bên ngoài. SJS là dạng nghiêm trọng hơn hồng ban đa dạng nặng và có biểu hiện nhẹ hơn hoại tử biểu bì nhiễm độc (TEN).[2] Phân loại tùy thuộc vào tỷ lệ phần trăm ảnh hưởng đến da: SJS ảnh hưởng <10% diện tích bề mặt toàn thân (TBSA); SJS/TEN ảnh hưởng đến từ 10% đến 30% TBSA; và TEN ảnh hưởng >30% TBSA.[3] [4] [5] [6] [7] [8] [9]
Dịch tễ học
Hội chứng Stevens-Johnson (SJS) và hoại tử biểu bì nhiễm độc (TEN) được coi là các bệnh hiếm gặp và chưa có thử nghiệm lâm sàng đối chứng tốt hoặc chưa có nghiên cứu dịch tễ nào để xác định tỷ lệ hiện mắc và tỷ lệ mới mắc chính xác của các tình trạng này. Ước tính tỷ lệ mới mắc SJS là từ 1 đến 6 ca/triệu năm-người và đối với TEN là 0,4 đến 1,2 ca/ triệu năm-người, ở tất cả các chủng tộc, độ tuổi và giới tính.[10] Một nghiên cứu bệnh chứng xác định rằng trong các loại thuốc gây SJS và TEN, thì sulfonamide kháng khuẩn có nguy cơ vượt quá 4,5 ca bệnh/triệu người phơi nhiễm/tuần.[10] Tỷ lệ mới mắc và tỷ lệ hiện mắc tăng trong các nhóm nhỏ cụ thể sử dụng các loại thuốc cụ thể, như thuốc chống co giật ở bệnh nhân bị co giật, thuốc kháng HIV ở bệnh nhân dương tính với HIV, so với nhóm người không dùng các loại thuốc này. Bệnh nhân dương tính với HIV có tổng tỷ lệ mới mắc SJS và TEN là 1/1000 năm-người.[11] [12]
Một đánh giá phát hiện rằng ước tính nguy cơ dựa trên số lượng toa thuốc hoặc liều dùng hàng ngày trong khoảng từ 1 đến 10/10.000 người mới dùng carbamazepine, lamotrigine, phenobarbital và phenytoin và có mức axit valproic thấp.[13] [14] Các yếu tố nguy cơ khác gây mắc SJS/TEN là xạ trị, bệnh mạch máu collagen, cấy ghép và nhiễm vi-rút herpes.[10]
Các nghiên cứu dược lý học di truyền cho thấy sắc tộc và loại HLA có thể khiến bệnh nhân có phản ứng thuốc bất lợi.[15] [16] [17] [18] [19] Alen HLA-B*1502 có liên hệ mật thiết đến SJS và TEN do carbamazepine gây ra ở tộc người Hán Trung Quốc; tại Hoa Kỳ, FDA (Cơ quan Quản lý Thực phẩm và Dược phẩm) khuyến cáo nên xét nghiệm cho tất cả người dân châu Á trước khi kê loại thuốc này.[16] HLA-A*0206 và HLA-B*4403 có liên quan đến bệnh SJS và TEN do thuốc cảm gây ra.[19] HLA-A*3101 có liên hệ mật thiết đến SJS và TEN ở mắt và các biến chứng khác, bất kể sắc tộc.[15] Tất cả các cá nhân có HLA-B*5801 đều có nguy cơ mắc SJS/TENS do allopurinol gây ra.[20]
Sự hiện diện của các alen HLA-B*1502, HLA-C*0602 hoặc HLA-C*0801 có liên quan đến SJS/TEN do trimethoprim/ sulfamethoxazole gây ra.[2] [21] Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ khuyến cáo cần sàng lọc alen HLA- B*5701 cho bệnh nhân trước khi bắt đầu điều trị abacavir cho nhiễm HIV.[22] [Fig-2]
Bệnh căn học
Hội chứng Stevens-Johnson (SJS) có thể là hậu quả của một quá trình bệnh hoặc sử dụng thuốc kháng sinh, thuốc chống co giật hoặc các loại thuốc khác. Cần xem xét kỹ tiền sử điều trị.
Một số yếu tố bệnh căn học tồn tại.
Nhiễm trùng
SJS có thể là di chứng của một số tình trạng, bao gồm:[4]
- Nhiễm trùng đường hô hấp trên
- viêm họng
- Viêm tai giữa
- Mycoplasma pneumoniae
- Herpes
- EBV (virus Epstein-Barr)
- Cytomegalovirus.[23]
Tiêm vắc-xin:
- Tiêm vắc-xin ngừa bệnh đậu mùa có thể gây hồng ban đa dạng hoặc SJS.[24] [25]
Thuốc
Các loại thuốc thường gặp nhất có liên quan đến SJS và hoại tử biểu bì nhiễm độc (TEN) bao gồm:[3] [4] [10] [12] [14] [19] [26] [27] [28] [29] [30] [31] [32] [33] [34] [35] [36] [37]
- Thuốc chống co giật (ví dụ: carbamazepine, phenobarbital, phenytoin, axit valproic, lamotrigine)
- Thuốc kháng sinh (ví dụ: sulfonamide, aminopenicillin, quinolone, cephalosporin)
- Thuốc kháng nấm
- Thuốc kháng retrovirus (ví dụ: nevirapine, abacavir) và thuốc kháng vi-rút (ví dụ: telaprevir, aciclovir)
- Thuốc diệt giun
- Thuốc giảm đau (ví dụ: paracetamol)
- Thuốc kháng viêm không steroid (NSAID) và thuốc ức chế COX-2 chọn lọc
- Thuốc chống sốt rét
- Azathioprine
- Sulfasalazine
- Allopurinol
- Axit tranexamic
- Corticosteroids
- Thuốc hướng tâm thần
- Chlormezanone
- Các loại thuốc điều trị ung thư (ví dụ: bendamustine, busulfan, chlorambucil)
- Các thuốc retinoid.
Sinh lý bệnh học
Mặc dù có sự đồng thuận chung rằng hội chứng Stevens-Johnson (SJS) và hoại tử biểu bì nhiễm độc (TEN) là do sự đáp ứng miễn dịch, nhưng sinh lý bệnh học chính xác của các tương tác giữa thuốc, các chất chuyển hóa, vi-rút, cytokine, tế bào lympho, xu hướng di truyền, dược lý học di truyền và tế bào chết keratin theo chương trình chưa được giải thích rõ ràng.
Cả SJS và TEN có đặc trưng là sự bong tróc biểu bì khỏi lớp hạ bì nhú ở lớp nằm giữa biểu bì-hạ bì, biểu hiện dưới dạng phát ban dát sẩn và bọng nước do kết quả của tế bào chết keratin theo chương trình.[38] [39][Fig-3]
Tế bào chết keratin theo chương trình được trung gian bởi tế bào lympho T gây độc tế bào (CD8) trong SJS và TENS được điều chỉnh bởi TNF-alpha và interferon-gamma trong huyết tương, tăng lên ở bệnh nhân mắc SJS và TEN.[8] [40] Theo giả thiết hiện nay, quy trình này có thể xảy ra qua 3 con đường: tương tác phối tử Fas-Fas; perforin/granzyme B; và qua trung gian granulysin.[3] [8] [9] [41] [42] [43] Con đường chính được cho là qua trung gian granulysin, tuy nhiên vấn đề vẫn còn gây tranh cãi và khả năng ảnh hưởng của một hoặc một số con đường chưa được giải quyết.
Tiến trình mô tả sinh lý bệnh học của SJS/TEN đã giải quyết các yếu tố nguy cơ có thể tương tác với tế bào tiêu diệt tự nhiên (NK) và tế bào T gây độc tế bào, như cấu trúc thuốc và cơ chế chuyển hóa (CYP), và đặc tính sinh miễn dịch của các phân tử HLA.[2]
Có nhiều con đường tùy thuộc vào sắp xếp di truyền của bệnh nhân và/hoặc loại thuốc gây đáp ứng miễn dịch.
Phân loại
Phổ ảnh hưởng đến da – phân loại được chấp nhận về mặt lâm sàng[5] [6]
Không có phân loại chính thức. Người ta cho rằng có một phổ bệnh gây tróc da, với dạng nhẹ là hồng ban đa dạng nặng, dạng nặng là hoại tử biểu bì nhiễm độc (TEN) và hội chứng Stevens-Johnson (SJS) là mức giữa. Phân loại này hiện đã trở thành định nghĩa được chấp nhận về mặt lâm sàng và là phân loại phổ bệnh.
Hồng ban đa dạng nặng
- Tổn thương đích (liên quan đến vi-rút herpes)
SJS (hội chứng Stevens-Johnson)
- Ảnh hưởng đến <10% diện tích bề mặt toàn thân (TBSA). Nguyên nhân bao gồm Mycoplasma pneumoniae, nhiễm vi-rút và vắc-xin hoặc liên quan đến thuốc.
Trùng lấp SJS-TEN
- Ảnh hưởng đến TBSA 10% đến 30%. Chủ yếu liên quan đến thuốc.
TEN (hoại tử biểu bì nhiễm độc)
- Ảnh hưởng đến TBSA >30%. Liên quan tới thuốc
Ngăn ngừa thứ cấp
Bệnh nhân đã chữa khỏi SJS hoặc TEN cần tránh dùng các loại thuốc kích hoạt bệnh.
Bệnh nhân cần cảnh giác với các vết loét trợt niêm mạc hoặc viêm loét hay phát ban. Bệnh nhân cần khám bác sĩ trong thời gian sớm nhất do SJS được cho là có thể tái phát vài lần trên cùng một bệnh nhân.
Do có thể có xu hướng di truyền, những bệnh nhân này không được tự uống thuốc kháng sinh hoặc các loại thuốc bán không cần đơn khi chưa được bác sĩ cho phép.
Bác sĩ mới khám lần đầu cần được cảnh báo về tình trạng bệnh nhân đã từng được điều trị SJS hoặc TEN.
Chẩn đoán
Tiền sử ca bệnh
Tiền sử ca bệnh #1
Một nam thanh niên 27 tuổi bị AIDS có biểu hiện phát ban trong 4 ngày qua, sau khi sử dụng các liều thuốc dự phòng trimethoprim/sulfamethoxazole trong 19 ngày để điều trị số lượng CD4 <200 tế bào lympho. 20% da trên diện tích bề mặt toàn thân (TBSA) bệnh nhân bị bong tróc với nhiều mảng bong tróc rải rác khắp thân và tứ chi. Trừ ban đỏ màng kết, bệnh nhân không bị ảnh hưởng đến niêm mạc. Sau khi điều trị thành công, bệnh nhân đã xuất viện sau 12 ngày. Khoảng 2 tháng sau khi xuất viện, bệnh nhân uống ‘thuốc kháng sinh điều trị cảm lạnh và bệnh nấm miệng’. Bệnh nhân có biểu hiện sốt, ban đỏ lan rộng trên da và ngứa. Bệnh nhân nhập viện 4 giờ sau khi dùng thuốc, với huyết áp là 80/40mmHg, nhiệt độ 40°C (104°F), nhịp thở 22 nhịp/phút và nhịp tim là 96 bpm. “Kháng sinh” được sử dụng là trimethoprim/sulfamethoxazole.
Tiền sử ca bệnh #2
Một bé trai 14 tuổi có tiền sử sốt, chứng sợ ánh sáng, ớn lạnh, ho, amidan sưng to và môi nứt nẻ chảy máu đã 1 ngày. Bệnh nhân bị phát ban đỏ lan tỏa, bao gồm lòng bàn tay và lòng bàn chân, chiếm tới 57% TBSA. Trong vòng 24 giờ, phát ban tiến triển ảnh hưởng đến 87% TBSA và bệnh nhân cần được thông khí nhân tạo do suy hô hấp. Bệnh nhân có tiền sử hen suyễn và đã dùng ibuprofen để điều trị viêm đường hô hấp trên bị từ 2 tuần trước.[Fig-1]
Các bài trình bày khác
Các đặc điểm rất cụ thể khác bao gồm tổn thương đích không điển hình (có thể hợp nhất), các vệt, tổn thương ban xuất huyết có thể sờ thấy hoặc dấu hiệu Nikolsky dương tính (lớp biểu bì dễ bị bong tróc khi tác động lực vào vùng bị ảnh hưởng). Ngoài ra, bệnh nhân có thể bị sốt, khó chịu, tổn thương mắt, viêm dạ dày, sưng lưỡi, tiêu chảy, nôn, chứng khó tiểu, hạch bạch huyết sưng to, đau khớp, viêm khớp, viêm phế quản, SOB (khó thở), thở khò khè, tổn thương bộ phận sinh dục, hạ huyết áp và mất nước.
Cách tiếp cận chẩn đoán từng bước
Biểu hiện lâm sàng đặc trưng và kết quả sinh thiết da đủ để chẩn đoán tình trạng này.
Tiền sử
Hội chứng Stevens-Johnson (SJS) có thể là hậu quả của một quá trình bệnh hoặc sử dụng thuốc kháng sinh hoặc loại thuốc khác để điều trị tình trạng này.[33] Cần xem xét kỹ tiền sử, tập trung vào việc dùng thuốc gần đây, nhiễm vi khuẩn hoặc virus gần đây và tiêm vắc-xin gần đây. Các yếu tố tiền sử thường gặp liên quan đến SJS và hoại tử biểu bì nhiễm độc (TEN) bao gồm các bệnh đồng mắc như co giật, SLE,[44] AIDS, bệnh mạch máu collagen và ung thư, và các phương pháp điều trị nhất định bao gồm xạ trị[45] [46] và ghép tủy xương.
Các loại thuốc thường gặp nhất liên quan đến SJS và TEN bao gồm:[3] [4] [10] [12] [14] [19] [26] [27] [28] [29] [30] [31] [32] [33] [34] [35] [36] [37]
- Thuốc chống co giật (ví dụ: carbamazepine, phenobarbital, phenytoin, axit valproic, lamotrigine)
- Thuốc kháng sinh (ví dụ: sulfonamide, aminopenicillin, quinolone, cephalosporin)
- Thuốc kháng nấm
- Thuốc kháng retrovirus (ví dụ: nevirapine, abacavir) và thuốc kháng vi-rút (ví dụ: telaprevir, aciclovir)
- Thuốc diệt giun
- Thuốc giảm đau (ví dụ: paracetamol)
- Thuốc kháng viêm không steroid (NSAID) và thuốc ức chế COX-2 chọn lọc
- Thuốc chống sốt rét
- Azathioprine
- Sulfasalazine
- Allopurinol
- Axit tranexamic
- Corticosteroids
- Thuốc hướng tâm thần
- Chlormezanone
- Các loại thuốc điều trị ung thư (ví dụ: bendamustine, busulfan, chlorambucil)
- Các thuốc retinoid.
Đánh giá lâm sàng
Khi phát hiện ở giai đoạn sớm của bệnh, các dấu hiệu và triệu chứng có thể xuất hiện tương đối nhẹ. Tuy nhiên, tình trạng thường tiến triển sau một số ngày, do đó cần theo dõi chặt chẽ và đánh giá lại thường xuyên. Nên xem xét chuyển các ca bệnh nặng hơn sang trung tâm bỏng.
Những bệnh nhân phát hiện muộn hoặc mắc bệnh nặng hơn có thể ở tình trạng nghiêm trọng hơn. Ở các bệnh nhân này, đặc biệt cần đánh giá tình trạng hô hấp khi nhập viện. Một trong những biến chứng tiềm ẩn của SJS/TEN là ảnh hưởng đến niêm mạc của đường hô hấp trên và dưới, hình thành mụn nước, loét và bong tróc niêm mạc thực tế có thể dẫn đến chứng thở rít ở thanh quản, cùng với tình trạng co rút và phù nề mũi họng. Nếu bị suy hô hấp hoặc phù nề các mô hầu họng, có thể cần đặt nội khí quản để duy trì đường thở.[47] Khí máu động mạch và bão hoà oxy sẽ giúp xác định tình trạng hô hấp lâm sàng của bệnh nhân.
Thông thường, các triệu chứng bao gồm phát ban đột ngột hoặc phát ban xuất hiện sau khi bắt đầu dùng thuốc mới. Mụn nước hoặc nốt sẩn và các tổn thương dạng bia bắn dẹt không điển hình, ban đỏ lan tỏa và dấu hiệu Nikolsky (lớp biểu bì dễ dàng tróc ra khi tác động lực vào vùng bị ảnh hưởng) có thể được ghi nhận.[6] Tổn thương ở niêm mạc với vết loét trợt hoặc viêm loét mắt, môi, miệng, hầu họng, thực quản, đường GI (tiêu hóa), thận, gan, hậu môn, bộ phận sinh dục hoặc niệu đạo.
Các triệu chứng khác bao gồm sốt, phù nề lưỡi, tiêu chảy, nôn, khó tiểu, hạch bạch huyết sưng to, đau khớp, viêm khớp, viêm phế quản, khó thở, thở khò khè, hạ huyết áp và mất nước.
Nên khám cho bệnh nhân như bệnh nhân bỏng, chủ yếu đánh giá tình trạng đường thở, hô hấp và tuần hoàn (ABC).
Đánh giá tỷ lệ phần trăm diện tích da bề mặt cơ thể bị ảnh hưởng là yếu tố quan trọng để phân loại SJS hay TEN, và nhiều phương pháp khác nhau đã được sử dụng. Khoảng một bàn tay (lòng bàn tay và ngón tay) bệnh nhân tương đương với 1% diện tích da toàn thân (TBSA), hoặc bác sĩ có thể sử dụng “quy tắc 9s” [Wallace rule of 9s] hoặc biểu đồ ước tính tình trạng bỏng Lund-Browder,[48] cho phép tính tỷ lệ phần trăm bề mặt cơ thể bị ảnh hưởng. Một nghiên cứu so sánh độ tin cậy của các ước tính này cho thấy quy tắc của kỹ thuật 9s thường ước tính quá mức kích thước bỏng và thay đổi nhiều hơn, tuy nhiên có thể thực hiện nhanh hơn so với phương pháp Lund và Browder.[49] Hệ thống tính điểm SCORTEN được đưa ra để cung cấp dự báo chính xác về tỷ lệ tử vong ở bệnh nhân mắc TEN.[50] [Fig-4]
Quy tắc 9s của Wallace
Phương pháp này cung cấp nhanh ước tính diện tích vùng da bị bỏng gần đúng.[48] Giá trị này có thể tùy ý chia cơ thể thành các đơn vị diện tích bề mặt chia hết cho 9, trừ đáy chậu. Thông thường, biểu đồ diện tích thường có ở hầu hết các đơn vị về bỏng. [Wallace rule of 9s]
Ở người lớn, dưới đây là tỷ lệ phần trăm tương ứng của diện tích bề mặt toàn thân (TBSA):
- Cả mặt trước và sau của đầu và cổ: 9%
- Cả mặt trước và sau của mỗi tay: 9%
- Lồng ngực và vùng bụng phía trước: 18%
- Lồng ngực và vùng bụng phía sau: 18%
- Đáy chậu: 1%
- Cả mặt trước và sau của mỗi chân: 18%
Quy tắc 9s tương đối chính xác cho người lớn nhưng không chính xác đối với trẻ em, do sự không cân xứng tương đối của diện tích bề mặt bộ phận-cơ thể.
Bề mặt lòng bàn tay
Diện tích lòng bàn tay bệnh nhân (bao gồm các ngón tay) chiếm khoảng 0,8% diện tích bề mặt toàn thân. Có thể sử dụng bề mặt lòng bàn tay để ước tính các vết bỏng tương đối nhỏ (<15% tổng diện tích bề mặt) hoặc vết bỏng rất lớn (>85%, khi tính diện tích da không bị bỏng). Đối với các vết bỏng kích thước trung bình, phương pháp này không chính xác.[51]
Biểu đồ ước tính tình trạng bỏng Lund-Browder
Biểu đồ này bù trừ cho sự thay đổi về hình dạng cơ thể theo độ tuổi, do đó có thể đưa ra đánh giá chính xác về diện tích bỏng ở trẻ em.[48] [49]
SCORTEN
Điểm độ nặng của bệnh được hỗ trợ để dự đoán nguy cơ tử vong cho bệnh nhân mắc SJS/TEN, trong vòng 5 ngày nằm viện đầu tiên. Bệnh nhân nhận 1 điểm cho mỗi tiêu chí sau:[52] [53]
- >40 tuổi
- Ung thư
- Nhịp tim nhanh >120 bpm
- Thương tổn >10% diện tích da
- Urê huyết thanh >10 mmol/L
- Glucose huyết thanh >14 mmol/L
- Bicarbonate <20 mmol/L.
Mặc dù nhóm bắt nguồn từ điểm SCORTEN, và một số phương pháp khác, có thể thấy hệ thống thang điểm hữu ích,[54] [50] hệ thống không hữu ích với các nhóm khác.[55]
Nhiều khả năng, việc sử dụng globulin miễn dịch qua đường tĩnh mạch gần đây thường xuyên hơn ở những bệnh nhân này đã ảnh hưởng đến một số hiệu lực của hệ thống thang điểm này dành cho TEN.
Các xét nghiệm chẩn đoán
Các xét nghiệm bao gồm:
- Công thức máu
- Cấy máu: nên được thực hiện nhằm loại trừ nhiễm Tụ cầu khuẩn hoặc Liên cầu khuẩn gây ra hội chứng sốc do độc tố hay hội chứng tróc vảy da
- LFT (xét nghiệm chức năng gan): được chỉ định để loại trừ tổn thương gan
- Khí máu động mạch và độ bão hoà oxy, để đánh giá tình trạng suy giảm hô hấp
- Bề mặt cơ thể bị ảnh hưởng, là yếu tố dự đoán tốt nhất về sự hiện diện của nhiễm trùng đường máu[56]
- Urê và điện giải đồ để đánh giá tình trạng giảm thể tích máu lưu hành
- Mức creatinine: để loại trừ suy thận.
Xét nghiệm xác định SJS, trùng lặp SJS/TEN và TEN là phương pháp sinh thiết da (được đánh giá kết hợp với biểu hiện lâm sàng).[4] Bác sĩ da liễu cần tiến hành sinh thiết tại điểm chuyển tiếp mụn nước để đánh giá mức độ bóc vẩy da. Tình trạng bong tróc sẽ xảy ra ở lớp nằm giữa lớp biểu bì-nhú bì, với sự xuất hiện của tế bào hoại tử và tế bào lympho. Có thể thực hiện miễn dịch huỳnh quang trực tiếp khi sinh thiết da ở hoặc quanh vùng tổn thương để loại trừ bệnh mụn nước tự miễn.[2]
Các yếu tố nguy cơ
Thường gặp
Thuốc chống co giật
- Các loại thuốc chống co giật thường gặp nhất gây SJS và TEN bao gồm carbamazepine, phenobarbital, phenytoin, lamotrigine và axit valproic.[10] [14] SJS và TEN thường xuất hiện ở những bệnh nhân đã bắt đầu sử dụng một loại thuốc mới từ 1 đến 14 ngày; nếu dùng thuốc trong nhiều tháng hoặc nhiều năm thì nguy cơ mắc SJS và TEN thường xảy ra trong 2 tháng điều trị đầu tiên.[3] [10] Ngày chỉ số xuất hiện SJS và TEN thường không quá một tháng sau ngày bắt đầu dùng thuốc (15 ngày đối với carbamazepine, 24 ngày đối với phenytoin, 17 ngày đối với phenobarbital).[3] Các yếu tố di truyền cũng có thể là nguyên nhân khiến những bệnh nhân này phản ứng với thuốc.
Nhiễm trùng gần đây
- Mycoplasma pneumoniae có liên quan đến sự xuất hiện của SJS ảnh hưởng đến <10% diện tích bề mặt toàn thân (TBSA). Các loại nhiễm vi-rút có thể gây SJS và hồng ban đa dạng nặng bao gồm: herpes, EBV và CMV (cytomegalovirus). Chúng có thể xuất hiện dưới dạng nhiễm trùng tai, mũi và cổ họng, hoặc có các triệu chứng toàn thân.[4]
Gần đây dùng thuốc kháng sinh
- Bệnh nhân cần điều trị nhiễm trùng có nguy cơ xảy ra phản ứng bất lợi với nhiều loại thuốc kháng sinh, đặc biệt là những thuốc có chứa chất dẫn xuất sulfa. Nguy cơ lớn nhất là do sử dụng trimethoprim/sulfamethoxazole và các loại thuốc kháng sinh sulfonamide khác, cũng như các aminopenicillin, quinolone và cephalosporin.[2] [10] [21] các loại thuốc khác
- Các loại thuốc khác có thể gây nguy cơ cho bệnh nhân bao gồm: thuốc kháng nấm, thuốc kháng vi-rút (như telaprevir, aciclovir),[31] thuốc kháng retrovirus (như nevirapine, abacavir),[12] [27] [28] thuốc diệt giun, thuốc giảm đau (như paracetamol),[26] thuốc kháng viêm không steroid (NSAID), thuốc ức chế COX-2 chọn lọc,[29] [30] thuốc chống sốt rét, corticosteroid[10] azathioprine, trimethoprim/sulfamethoxazole, sulfasalazine,[35] allopurinol, axit tranexamic,[34] thuốc hướng tâm thần,[32] chlormezanone,[19] [36] các loại thuốc điều trị ung thư (ví dụ: bendamustine, busulfan, chlorambucil),[36] và các retinoid.[37]
- Các ca thường gặp là SJS, trùng lặp SJS/TEN và TEN; không kèm hồng ban đa dạng nặng.[6] Có thể xảy ra tương tác miễn dịch với các thuốc được sử dụng để điều trị SLE (lupus ban đỏ hệ thống), như corticosteroid và isoniazid.[10] Cơ chế này thường do thuốc, tuy nhiên bệnh nhân cũng có thể có khuynh hướng di truyền dễ phản ứng với thuốc. Đôi khi rất khó để xác định xem hoại tử biểu bì dạng tấm là do SLE hay SJS/TEN.[44]
AIDS
- Bệnh nhân bị suy giảm miễn dịch và xảy ra nhiều phản ứng thuốc với thuốc điều trị HIV.[11] [12] [22] Việc sử dụng trimethoprim/sulfamethoxazole để điều trị dự phòng nhằm ngăn ngừa viêm phổi do nấm Pneumocystis jirovecii có thể làm tăng nguy cơ mắc.
Xạ trị
- Thường xuất hiện ở bệnh nhân ung thư mới dùng thuốc chống co giật trong quá trình chiếu xạ sọ.[45] Amifostine, được sử dụng để bảo vệ các mô bình thường trong quá trình chiếu xạ và hóa trị liệu, cũng có liên quan đến SJS và TEN.[46] Bệnh nhân bị suy giảm miễn dịch do hóa trị liệu và quá trình mắc bệnh.
HLA và xu hướng di truyền
- Các nghiên cứu dược lý học di truyền cho thấy sắc tộc và loại HLA có thể khiến bệnh nhân có phản ứng thuốc bất lợi.[15] [16] [17] [18] [19] Alen HLA-B*1502 có liên hệ mật thiết đến SJS và TEN do carbamazepine gây ra ở tộc người Hán Trung Quốc; FDA khuyến cáo nên xét nghiệm cho tất cả người dân châu Á trước khi kê loại thuốc này.[16] HLA-A*0206 và HLA-B*4403 có liên quan đến bệnh SJS và TEN do thuốc cảm gây ra.[19] HLA- A*3101 có liên hệ mật thiết đến SJS và TEN ở mắt và các biến chứng khác, bất kể sắc tộc.[15].[Fig-2]
Tất cả các cá nhân có HLA-B*5801 đều có nguy cơ mắc SJS/TENS do allopurinol gây ra.[20]
- Sự hiện diện của các alen HLA-B*1502, HLA-C*0602 hoặc HLA-C*0801 có liên quan đến SJS/TEN do trimethoprim/sulfamethoxazole gây ra.[2] [21] Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ khuyến cáo cần sàng lọc alen HLA-B*5701 cho bệnh nhân trước khi bắt đầu điều trị abacavir cho nhiễm HIV.[22]
Tiêm vắc-xin bệnh đậu mùa
- Hiếm khi tiêm vắc-xin bệnh đậu mùa, tuy nhiên đã có tài liệu ghi nhận đây có thể là nguyên nhân gây SJS, có thể tiến triển thành TEN.[24] [25]
Không thường gặp
Cấy ghép tủy xương
- Trong trường hợp này, cần phân biệt SJS với bệnh lý mảnh ghép chống lại vật chủ (GVHD) cấp có thể xảy ra.[4] Triệu chứng ban đầu của cả hai tình trạng đều là phát ban. Tuy nhiên, ở GVHD, da không bị bong tróc như khi mắc SJS hoặc TEN. SJS hoặc TEN có thể do phản ứng thuốc, trong khi GVHD phát triển sau khi tế bào lympho vật chủ tấn công các cơ quan hoặc mô được hiến. Thông thường khó có thể phân biệt giữa GVHD và TEN, đặc biệt do cả hai bệnh có thể xuất hiện ở cùng một bệnh nhân trong cùng khoảng thời gian. Mặc dù trường hợp này rất hiếm gặp, tuy nhiên hầu hết các ca bệnh đều có tỷ lệ tử vong cao. Trong các trường hợp này, SJS/TEN thường liên quan đến thuốc.
Các yếu tố về tiền sử và thăm khám
Các yếu tố chẩn đoán chủ yếu
Có các yếu tố nguy cơ (thường gặp)
- Các yếu tố nguy cơ chính bao gồm sử dụng thuốc chống co giật và sử dụng một số loại thuốc khác, bao gồm dùng thuốc kháng sinh gần đây; nhiễm trùng gần đây; các tình trạng như SLE và AIDS; xạ trị; tiêm vắc-xin bệnh đậu mùa; loại HLA và sắc tộc người Trung Quốc hoặc Nhật Bản.
Phát ban (thường gặp)
- Phát ban đột ngột và phát ban xuất hiện sau khi bắt đầu dùng loại thuốc mới.
Ảnh hưởng đến niêm mạc (thường gặp)
- Vết loét trợt hoặc viêm loét mắt, môi, miệng, hầu họng, thực quản, đường GI, thận, gan, hậu môn, bộ phận sinh dục hoặc niệu đạo. Thường gặp ở hội chứng Stevens-Johnson (SJS) hơn so với hoại tử biểu bì nhiễm độc (TEN).
Dấu hiệu Nikolsky (thường gặp)
- Lớp biểu bì dễ bong tróc khi tác động lực vào vùng bị ảnh hưởng. Thường gặp ở TEN hơn so với SJS.
Mụn nước (không thường gặp)
- Mụn nước hoặc nốt sẩn và các tổn thương dạng bia bắn dẹt không điển hình, ban đỏ lan tỏa. Thường gặp ở TEN hơn so với SJS.[Fig-4]
Xét nghiệm chẩn đoán
Xét nghiệm thứ nhất cần yêu cầu
| Xét nghiệm | Kết quả |
| Sinh thiết da
• Xét nghiệm xác định để chẩn đoán. Cần tiến hành sinh thiết da sớm nhất có thể nếu nghi bệnh nhân có thể mắc hội chứng Stevens-Johnson (SJS) hoặc hoại tử biểu bì nhiễm độc (TEN). • Vùng bong tróc có thể chứa một số tế bào lympho T CD8 dương tính và hạ bì có thể chứa tế bào lympho T CD4 dương tính và đại thực bào, tùy thuộc vào giai đoạn bệnh khi tiến hành sinh thiết.[4][Fig-3] |
Gây chết tế bào keratin theo chương trình cùng với ly biểu bì da |
| Cấy máu
• Cần loại trừ hội chứng sốc độc và hội chứng da tróc vảy, các hội chứng này có thể cho thấy nuôi cấy dương tính với các loài Tụ cầu khuẩn hoặc Liên cầu khuẩn. |
Âm tính với SJS/TEN |
| Công thức máu
• Nếu FBC cho thấy bạch cầu ái toan, xem xét hội chứng quá mẫn ([DRESS] phát ban do thuốc với bạch cầu ái toan và triệu chứng toàn thân). Số lượng WBC có thể tăng nếu bị nhiễm trùng vết thương hoặc nhiễm khuẩn huyết. |
Kết quả tùy theo giai đoạn bệnh khi xét nghiệm và mức độ mất da. Bệnh nhân TEN có thể xuất hiện nhiễm khuẩn huyết và số lượng WBC (số lượng bạch cầu) tăng. |
| Urê
• Mức urê tăng cho thấy có thể bị giảm thể tích máu lưu hành. |
Có thể tăng |
| Xét nghiệm chức năng gan
• Những bất thường chính xác trong kết quả LFT tùy thuộc một phần vào độc tính của thuốc gây SJS hoặc TEN, cũng như tỷ lệ phần trăm diện tích bề mặt toàn thân (TBSA) bị ảnh hưởng. Tùy theo độ nặng của SJS hoặc TEN, phản ứng viêm do cytokine gây ra dưới dạng phản ứng với những thương tổn có thể tương tự với tình trạng xảy ra ở vết thương do nhiệt: gan nhiễm mỡ, tế bào gan chết theo chương trình và hoại tử. |
Các bất thường thay đổi |
| Khí máu động mạch và độ bão hòa oxy
• Khí máu động mạch và độ bão hoà oxy sẽ giúp xác định tình trạng hô hấp của bệnh nhân trên lâm sàng. Một trong những biến chứng của SJS/TEN là ảnh hưởng đến niêm mạc của đường hô hấp trên và dưới, hình thành mụn nước, loét và bong tróc niêm mạc thực tế có thể dẫn đến chứng thở rít ở thanh quản, có thể bị tình trạng co rút và phù nề mũi họng. |
Giảm oxy máu, nhiễm toan |
Các xét nghiệm khác cần cân nhắc
| Xét nghiệm | Kết quả |
| Điện giải đồ
• Mức kali và natri thấp cho thấy có thể bị giảm thể tích máu lưu hành. |
Hạ kali máu, hạ natri máu |
| Creatinine huyết thanh
• Mức creatinine huyết thanh cao cho thấy có thể bị suy thận hoặc bệnh thận. |
Có thể tăng |
| Miễn dịch huỳnh quang trực tiếp
• Được thực hiện khi sinh thiết da ở hoặc quanh vùng tổn thương để loại trừ bệnh mụn nước tự miễn.[2] |
Âm tính |
Chẩn đoán khác biệt
| Tình trạng | Các dấu hiệu/triệu chứng khác biệt | Các xét nghiệm khác biệt |
| Hội chứng phát ban do thuốc với bạch cầu ái toan và các triệu chứng toàn thân (DRESS) |
|
Sinh thiết da và biểu hiện lâm sàng; công thức máu có thể cho thấy tăng bạch cầu ái toan; xét nghiệm chức năng gan có thể tăng men gan nếu bị viêm gan. |
| Hội chứng bong vảy da do tụ cầu | • Bệnh ở trẻ sơ sinh hoặc trẻ nhỏ (bệnh Ritter).
• Nội độc tố của vi khuẩn phá vỡ lớp biểu bì nhưng không gây hoại tử hoặc viêm.[3] |
Công thức máu, nuôi cấy máu và vết thương và sinh thiết da. |
| Hội chứng sốc độc | • Tụ cầu khuẩn hoặc Liên cầu khuẩn có thể là nguồn gây nhiễm trùng, biểu hiện ở các dấu hiệu nhiễm khuẩn huyết và phát ban giống như bị cháy nắng. | Công thức máu, nuôi cấy máu và vết thương và sinh thiết da. |
| Bệnh lý mảnh ghép chống lại vật chủ | • Bệnh nhân xuất hiện phát ban, nhưng da trong bệnh lý mảnh ghép chống lại vật chủ không bong tróc nhanh như ở hội chứng Stevens-Johnson (SJS) hoặc hoại tử biểu bì nhiễm độc (TEN).
• Bệnh nhân đã được cấy ghép xuất hiện phát ban do tình trạng thải ghép thay vì phản ứng do thuốc, mặc dù biểu hiện da cấp độ IV có thể nặng như ở TEN. Các tổn thương mắt thường hiếm gặp.[3] |
Công thức máu và sinh thiết da. |
| Nhiễm độc chất gây sưng tấy/ mụn nước | • Các ảnh hưởng lâm sàng như ban đỏ và mụn nước sẽ xuất hiện ngay với phosgene oxime hoặc lewisite, hay xuất hiện trễ từ 2 đến 24 giờ với khí mù tạt.[60] | Sinh thiết da. |
| Ban đỏ đa dạng | • Tổn thương dạng bia bắn thường do vi-rút herpes kích hoạt.[5] [6] | Sinh thiết da. |
| Bỏng, da | • Kết quả chấn thương với mức độ tổn hại lớp biểu bì và hạ bì khác nhau.[4] | Sinh thiết da nếu không có bệnh sử rõ ràng. |
| Bệnh pemphigus cận ung thư | • Bệnh mụn nước có bệnh đồng mắc ác tính.[4] | Sinh thiết da và miễn dịch huỳnh quang trực tiếp. |
| Ban đỏ nhiễm sắc cố định bọng nước toàn thân (GBFDE) | • Tiền sử tái phát ở cùng một vùng khi dùng lại thuốc gây bệnh; nếu có, ít triệu chứng toàn thân; các đám mụn nước hoặc ban đỏ tròn.[61] [62] | Sinh thiết da. |
| Hội chứng ngoại ban mụn mủ toàn thân cấp tính (AGEP) | • Sốt, tăng bạch cầu trung tính, mụn mủ vô trùng cấp tính, ban đỏ, phù mặt.[63] | Sinh thiết da. |
| Coxsackievirus A6 | • Không dung nạp thuốc; sốt; nổi mụn nước ở tay, lưỡi, mông, loét miệng.[64] | Sinh thiết da; vi-rút ở da và dịch mụn nước. |
Các tiêu chí chẩn đoán
Hồng ban đa dạng nặng, SJS và TEN
Hồng ban đa dạng nặng
- Tổn thương đích (liên quan đến vi-rút herpes)
SJS (hội chứng Stevens-Johnson)
- Ảnh hưởng đến <10% diện tích da toàn thân (TBSA) Trùng lấp SJS-TEN
- Ảnh hưởng đến từ 10% đến 30% TBSA
TEN (hoại tử biểu bì nhiễm độc)
- Ảnh hưởng đến >30% TBSA
Điều trị
Cách tiếp cận điều trị từng bước
Hội chứng Stevens-Johnson (SJS) và hoại tử biểu bì nhiễm độc (TEN) tương tự như bỏng cấp độ hai xét về các ảnh hưởng sinh lý. Các đơn vị chuyên khoa bỏng có thể chăm sóc vết thương, cung cấp dinh dưỡng, chăm sóc chuyên sâu và kiểm soát cơn đau tối ưu.
Việc điều trị chính xác tùy thuộc vào mức độ da bị ảnh hưởng, tuy nhiên cả SJS và TEN đều áp dụng các nguyên tắc chung giống nhau. Nên bắt đầu điều trị dựa trên ca bệnh cụ thể, tùy theo biểu hiện của từng bệnh nhân.[65] [66]
Cả hai tình trạng có xu hướng tiến triển sau vài ngày, do đó nên theo dõi chặt chẽ tất cả bệnh nhân. Nếu phát ban tiến triển nhanh hoặc tình trạng bệnh nhân xấu hơn, nên chuyển bệnh nhân đến một đơn vị chuyên khoa bỏng để chăm sóc nếu không ở đó.[67]
Chăm sóc ngay
Sau khi chẩn đoán, nên loại bỏ ngay tác nhân gây bệnh. Các loại thuốc thường gặp nhất liên quan đến SJS và TEN bao gồm:[3] [4] [10] [12] [14] [19] [26] [27] [28] [29] [30] [31] [32] [33] [34] [35] [36] [37]
- Thuốc chống co giật (ví dụ: carbamazepine, phenobarbital, phenytoin, axit valproic, lamotrigine)
- Thuốc kháng sinh (ví dụ: sulfonamide, aminopenicillin, quinolone, cephalosporin)
- Thuốc kháng nấm
- Thuốc kháng retrovirus (ví dụ: nevirapine, abacavir) và thuốc kháng vi-rút (ví dụ: telaprevir, aciclovir)
- Thuốc diệt giun
- Thuốc giảm đau (ví dụ: paracetamol)
- Thuốc kháng viêm không steroid (NSAID) và thuốc ức chế COX-2 chọn lọc
- Thuốc chống sốt rét
- Azathioprine
- Sulfasalazine
- Allopurinol
- Axit tranexamic
- Corticosteroids
- Thuốc hướng tâm thần
- Chlormezanone
- Các loại thuốc điều trị ung thư (ví dụ: bendamustine, busulfan, chlorambucil)
- Các thuốc retinoid.
Khi nhập viện, bệnh nhân được khám để đánh giá tình trạng đường thở, hô hấp và tuần hoàn (ABC). Khi nhập viện, phải xác định xem bệnh nhân có bị suy hô hấp không. Khí máu động mạch và độ bão hoà oxy sẽ giúp xác định tình trạng hô hấp của bệnh nhân. Một trong những biến chứng của SJS/TEN là ảnh hưởng đến niêm mạc của đường hô hấp trên và dưới, hình thành mụn nước, loét và bong tróc niêm mạc thực tế có thể dẫn đến chứng thở rít ở thanh quản, có thể bị tình trạng co rút và phù nề mũi họng. Nếu bị suy hô hấp hoặc phù nề các mô hầu họng, nên sử dụng phương pháp đặt nội khí quản để duy trì đường thở.[47]
Cần tiến hành đánh giá ngay diện tích da toàn thân (TBSA) bị ảnh hưởng. Khoảng một bàn tay (lòng bàn tay và các ngón tay) của bệnh nhân tương đương với 1% TBSA, hoặc sử dụng “quy tắc 9s”. Tỷ lệ phần trăm TBSA bị ảnh hưởng càng lớn thì cần lượng dịch càng nhiều. Nên xem xét các tiêu chí bỏng khi tính toán. [Wallace rule of 9s] [48] [49] [51] Nên liên hệ tư vấn hoặc có thể chuyển bệnh nhân đến các trung tâm bỏng chuyên chăm sóc tích cực cho những bệnh nhân này.[67]
Thay băng
Nên thay băng và các chất kháng khuẩn bôi ngoài da để che phủ các vết thương đã được vệ sinh nhằm tránh nhiễm trùng. Việc lựa chọn thay băng thường tùy theo quyết định của bác sĩ và tình trạng khả dụng của băng gạc. Tùy theo thay băng và tình trạng vết thương, nên thay băng 1 đến 2 lần mỗi ngày, hoặc tối đa 2 đến 3 ngày một lần.[8] [9] [51]
Các lựa chọn thay băng bao gồm ghép ngoại lai (da lợn), ghép mô (da người chết) và băng gạc tổng hợp. Có thể sử dụng gạc có thuốc mỡ bacitracin và có thể sử dụng kem, như sulfadiazine bạc, kết hợp với thay băng Băng gạc tổng hợp thấm bạc có thể hữu ích đối với những bệnh nhân bị ảnh hưởng >30% diện tích bề mặt toàn thân (TBSA). Bạc giúp ngăn nhiễm trùng và duy trì hoạt tính trong từ 3 đến 4 ngày, giúp giảm số lần thay băng gạc.
Khi da đã được tái tạo (sau khoảng 2 đến 3 tuần), thuốc làm mềm có thể hữu ích để giúp da mềm và ngăn khô da.
Bệnh nhân hiếm khi thực sự cần ghép da
Kiểm soát dịch
Nếu bệnh nhân thường xuyên bị nôn, có thể xảy ra tình trạng mất nước. Bên cạnh đó, tùy theo mức độ bong tróc da, bệnh nhân có thể mất một lượng dịch đáng kể qua bề mặt da bị bóc.
Nếu bệnh nhân có thể bù dịch qua đường uống, nên khuyến khích phương pháp này. Nếu không, nên bắt đầu sử dụng qua đường tĩnh mạch như dung dịch Ringer lactate hoặc NaCl 0,9% để bù dịch cho bệnh nhân. Một nghiên cứu trên hàng loạt ca bệnh chỉ ra rằng khoảng 2 mL/kg/% TBSA là đủ nếu không có biến chứng khác.[68]
Bất kể lượng dịch cần thiết theo tính toán, đánh giá lâm sàng về đáp ứng của bệnh nhân đặc biệt quan trọng. Theo dõi bù dịch trong hồi sức thông qua lượng nước tiểu. Lưu ý lượng nước tiểu của người lớn là 0,5 mL/kg/giờ (30 đến 50 mL/giờ) và trẻ em có cân nặng <30kg có lượng nước tiểu là 1 mL/kg/giờ.
Có thể tăng hoặc giảm bù dịch trong hồi sức dựa trên lượng nước tiểu.
Kiểm soát đau
Nên cho dùng thuốc giảm đau theo mức độ nặng của triệu chứng. Không nên sử dụng thuốc kháng viêm không steroid (NSAID) trừ khi các loại thuốc khác như opioid hoặc paracetamol không có tác dụng. Bệnh nhân sẽ cần thêm thuốc giảm đau khi thay băng.
Globulin miễn dịch đường tĩnh mạch (IVIg)
Không có chỉ định rõ ràng về việc cho dùng IVIg. Một số bác sĩ lâm sàng chỉ định IVIg cho bệnh nhân có phát ban tiến triển nhanh ảnh hưởng ít nhất 6% TBSA. Một số khác chỉ cho dùng IVIg khi 20% TBSA bị ảnh hưởng. Không có thử nghiệm ngẫu nhiên có đối chứng xác định nào để hướng dẫn điều trị. Các tài liệu khoa học hiện tại bao gồm hàng loạt nghiên cứu tiền cứu và tiến cứu nhỏ. Các đánh giá của những thử nghiệm lâm sàng nhỏ này đã chỉ ra một số lợi ích và không có biến chứng nghiêm trọng nào khi sử dụng IVIg.[2] [3] [8] [9] [69] [70] [71]
Tổn thương ở miệng
Ở những bệnh nhân bị viêm miệng không thể ăn bằng miệng, nên cung cấp hỗ trợ về dinh dưỡng cho bệnh nhân ăn qua đường miệng hoặc ăn qua ống thông. Không nên sử dụng phương pháp nuôi dưỡng qua đường tĩnh mạch trừ khi bắt buộc. Nên sử dụng loại nước súc miệng dịu nhẹ để vệ sinh miệng đối với những bệnh nhân bị tổn thương niêm mạc miệng.
Tổn thương ở mắt
Tất cả bệnh nhân có dấu hiệu và triệu chứng của SJS/TEN cần được hội chẩn nhãn khoa và khám toàn diện sau khi nhập viện, nhằm bảo vệ thị lực và giảm thiểu các biến chứng.[72]
Việc dùng màng ối che phủ toàn bộ bề mặt mắt cùng với corticosteroid bôi ngoài da tăng cường trong thời gian ngắn, trong giai đoạn cấp tính của SJS và TEN đã được chứng minh là có tác dụng duy trì thị lực tốt và bề mặt mắt nguyên vẹn.[72]
Trong hàng loạt ca bệnh tiến cứu, 79 bệnh nhân đã được đánh giá, điều trị và theo dõi trong ba tháng sau khi xuất viện. Các ca bệnh được phân loại là nhẹ hoặc trung bình được điều trị nội khoa Các ca bệnh được phân loại là nặng hoặc rất nặng sẽ được điều trị nội khoa và ghép màng ối khẩn cấp. Việc phân loại dựa trên mức độ nhuộm fluorescein của viền mí mắt, giác mạc và/hoặc kết mạc.[72]
Liệu pháp chức năng và vật lý trị liệu
Do bệnh nhân có thể bị hạn chế về khả năng di chuyển và giảm sức mạnh, bệnh nhân cần đi lại hàng ngày và tập luyện trong phạm vi khả năng với nhà vật lý trị liệu và chuyên gia liệu pháp chức năng, nếu cần.
Tổng quan về các chi tiết điều trị
Tham khảo cơ sở dữ liệu dược địa phương của quý vị để biết thông tin toàn diện về thuốc, bao gồm các chống chỉ định, tương tác giữa các loại thuốc, và liều dùng thay thế.
| Cấp tính (tóm tắt) | ||
| Nhóm bệnh nhân | Tx line | Điều trị |
| Tất cả bệnh nhân | 1 | Đánh giá khẩn cấp + dừng tác nhân gây bệnh |
| Thêm | Thay băng + thuốc kháng khuẩn bôi ngoài da + thuốc làm mềm | |
| Thêm | Khám nhãn khoa | |
| Bổ sung | Truyền dịch qua IV ± hỗ trợ dinh dưỡng | |
| Bổ sung | Vệ sinh răng miệng | |
| Bổ sung | Thuốc giảm đau | |
| Bổ sung | Globulin miễn dịch đường tĩnh mạch (IVIg) | |
| Bổ sung | Bao phủ mắt bằng màng ối | |
| Bổ sung | Phương pháp vật lý trị liệu và liệu pháp chức năng | |
Các lựa chọn điều trị
| Cấp tính | ||
| Nhóm bệnh nhân | Tx line | Điều trị |
| Tất cả bệnh nhân | 1 | Đánh giá khẩn cấp + dừng tác nhân gây bệnh |
| » Khi chẩn đoán, nên loại bỏ ngay tác nhân gây bệnh. Các loại thuốc thường gặp nhất liên quan đến SJS và TEN bao gồm: thuốc chống co giật (ví dụ: carbamazepine, phenobarbital, phenytoin, axit valproic, lamotrigine), thuốc kháng sinh (ví dụ: sulfonamide, aminopenicillin, quinolone, cephalosporin), thuốc kháng nấm, thuốc kháng retrovirus (ví dụ: nevirapine), thuốc kháng vi-rút (ví dụ: telaprevir, aciclovir), thuốc diệt giun, thuốc giảm đau (ví dụ: paracetamol), thuốc kháng viêm không steroid (NSAID), chất ức chế COX-2 chọn lọc, thuốc chống sốt rét, azathioprine, sulfasalazine, allopurinol, axit tranexamic, corticosteroid, thuốc hướng tâm thần, thuốc điều trị ung thư (như bendamustine, busulfan, chlorambucil), chlormezanone và các retinoid.[2] [3] [4] [10] [12] [14] [19] [26] [27] [28] [29] [30] [31] [32] [33] [34] [35] [36] [37]
» Khi nhập viện, bệnh nhân được khám để đánh giá tình trạng đường thở, hô hấp và tuần hoàn (‘ABC’). Phải xác định xem bệnh nhân có bị suy hô hấp không. Khí máu động mạch và độ bão hoà oxy sẽ giúp xác định tình trạng hô hấp của bệnh nhân. Một trong những biến chứng của SJS/TEN là ảnh hưởng đến niêm mạc của đường hô hấp trên và dưới, hình thành mụn nước, loét và bong tróc niêm mạc thực tế có thể dẫn đến chứng thở rít ở thanh quản, và có thể bị tình trạng co rút và phù nề mũi họng: có thể cần đặt nội khí quản cho bệnh nhân để duy trì đường thở.[47] » Cần tiến hành đánh giá ngay diện tích da toàn thân (TBSA) bị ảnh hưởng. Khoảng một bàn tay (lòng bàn tay và các ngón tay) của bệnh nhân tương đương với 1% TBSA, hoặc sử dụng “quy tắc 9s”. Tỷ lệ phần trăm TBSA bị ảnh hưởng càng lớn thì cần lượng dịch càng nhiều. Nên xem xét các tiêu chí bỏng khi tính toán. [Wallace rule of 9s] [48] [49] [51] Nên liên hệ tư vấn hoặc có thể chuyển bệnh nhân đến các trung tâm bỏng chuyên chăm sóc tích cực cho những bệnh nhân này.[67] |
||
| Thêm | Thay băng + thuốc kháng khuẩn bôi ngoài da + thuốc làm mềm | |
| » Thay băng và thuốc kháng sinh bôi ngoài da để che phủ các vết thương đã được vệ sinh để tránh nhiễm trùng. Việc lựa chọn băng gạc thường tùy theo quyết định của bác sĩ và tình trạng khả dụng của băng gạc. Tùy theo băng gạc và tình trạng vết thương, nên thay băng 1 đến 2 lần mỗi ngày, hoặc 2 đến 3 lần một ngày
» Các lựa chọn thay băng bao gồm ghép ngoại lai (da lợn), ghép mô (da người chết) và băng gạc tổng hợp. Có thể sử dụng gạc có thuốc mỡ bacitracin và có thể sử dụng kem, như sulfadiazine bạc, kết hợp với thay băng Băng gạc tổng hợp thấm bạc có thể hữu ích đối với những bệnh nhân bị ảnh hưởng >30% diện tích bề mặt toàn thân (TBSA). Bạc giúp ngăn nhiễm trùng và duy trì hoạt tính trong từ 3 đến 4 ngày, giúp giảm số lần thay băng gạc. » Khi da đã được tái tạo (sau khoảng 2 đến 3 tuần), thuốc làm mềm có thể hữu ích để giúp da mềm và ngăn khô da. Các lựa chọn sơ cấp » bacitracin bôi ngoài da: bôi vào (các) vùng tổn thương hai hoặc ba lần mỗi ngày HOẶC Các lựa chọn sơ cấp » sulfadiazine bạc bôi ngoài da: (1%) bôi vào (các) vùng bị ảnh hưởng một hoặc hai lần mỗi ngày |
||
| Thêm | Khám nhãn khoa | |
| » Tất cả bệnh nhân có dấu hiệu và triệu chứng của SJS/TEN cần được hội chẩn nhãn khoa và khám toàn diện sau khi nhập viện, nhằm bảo vệ thị lực và giảm thiểu các biến chứng.[72] | ||
| Bổ sung | Truyền dịch qua IV ± hỗ trợ dinh dưỡng | |
| » Bệnh nhân có thể bù dịch qua đường uống nên được khuyến khích sử dụng phương pháp này. Nếu không, cần bắt đầu truyền dịch tĩnh mạch
» Tỷ lệ phần trăm diện tích da toàn thân (TBSA) bị tổn thương càng lớn thì cần lượng dịch càng nhiều. Bệnh nhân bị bong tróc da từ 15% đến 20% TBSA trở lên hơn cần được bù dịch hồi sức do bỏng. Đối với người lớn và trẻ em >14 tuổi, >40 kg: 2 đến 4 mL dung dịch Ringer có lactate (LR) X kg trọng lượng X % TBSA; đối với trẻ em <14 tuổi, <40 kg: 3 mL dung dịch LR x kg trọng lượng x % TBSA; và đối với trẻ sơ sinh <10 kg: dextrose 5% trong dung dịch Ringer có lactate. Năm mươi lăm phần trăm lượng dịch đã tính phải được cung cấp trong 8 giờ đầu và phần còn lại được chia sử dụng trong 16 giờ tiếp theo.» Bệnh nhân bị viêm miệng không thể ăn uống bình thường cần được hỗ trợ dinh dưỡng trong thời gian sớm nhất bằng cách cho ăn qua đường miệng hoặc qua ống thông. Có thể cần nuôi dưỡng tĩnh mạch nếu không thể cho ăn qua đường ruột. » Do tình trạng dị hóa và tăng chuyển hóa cao hơn, những bệnh nhân này cần được bổ sung dinh dưỡng có nhiều calo: đối với người lớn 30 đến 35 calo/kg/ ngày, và protein từ 1,5 đến 2 g/kg/ngày cho người lớn và tối đa 3 g/kg/ngày đối với trẻ em. Bệnh nhân cũng cần được bổ sung nhiều loại vitamin, kẽm, vitamin C, và khi cần là magie và canxi. » Nếu >40% TBSA, xem xét cho dùng oxandrolone để giảm thiểu việc mất khối lượng cơ và thúc đẩy quá trình khôi phục cân nặng và chữa lành.[73] |
||
| Bổ sung | Vệ sinh răng miệng | |
| » Nên sử dụng loại nước súc miệng dịu nhẹ (như lidocaine) để vệ sinh miệng đối với những bệnh nhân bị tổn thương niêm mạc miệng.
Các lựa chọn sơ cấp » lidocaine tại chỗ: (dung dịch nhớt 2%) 15 mL mỗi 3 giờ khi cần (súc xung quanh trong miệng và nhổ ra), tối đa 8 liều/ngày |
||
| Bổ sung | Thuốc giảm đau | |
| » Liều lượng được điều chỉnh theo độ nặng của triệu chứng và tùy theo bác sĩ và ưu tiên của tổ chức. Không nên sử dụng thuốc kháng viêm không steroid (NSAID) trừ khi các loại thuốc khác như opioid hoặc paracetamol không có tác dụng.
» NSAID và paracetamol cũng bị coi là tác nhân gây bệnh. » Bệnh nhân sẽ cần thêm thuốc giảm đau khi thay băng gạc. » Bệnh nhân có thể được cấp bơm thuốc giảm đau do bệnh nhân kiểm soát (PCA), nếu thích hợp. Các lựa chọn sơ cấp » Paracetamol: trẻ em: 10-15 mg/kg uống mỗi 4-6 giờ khi cần, tối đa 75 mg/kg/ngày; người lớn: 500-1000 mg uống mỗi 4-6 giờ khi cần, tối đa 4000 mg/ngày HOẶC Các lựa chọn sơ cấp » morphine sulfate: trẻ em: 0,05 đến 0,2 mg/kg đường uống/tĩnh mạch sau mỗi 2-4 giờ khi cần; người lớn: 7,5 đến 10 mg đường uống/tĩnh mạch mỗi 4 giờ khi cần |
||
| Bổ sung | Globulin miễn dịch đường tĩnh mạch (IVIg) | |
| » Không có chỉ định rõ ràng liên quan đến việc cho dùng IVIg; một số bác sĩ lâm sàng có thể sử dụng biện pháp điều trị này tùy theo biểu hiện của từng bệnh nhân.» Một số bác sĩ lâm sàng chỉ định IVIg cho bệnh nhân có phát ban tiến triể’n nhanh ảnh hưởng đến >6% diện tích bề mặt toàn thân (TBSA). Một số khác chỉ cho dùng IVIg khi 20% TBSA bị ảnh hưởng. Không có thử nghiệm ngẫu nhiên có đối chứng xác định nào để hướng dẫn điều trị.
» IVIg dành riêng cho những bệnh nhân có tiến triển nhanh các dấu hiệu và triệu chứng niêm mạc da; các bệnh đồng mắc cũng xác định loại điều trị mà bệnh nhân sẽ tiếp nhận. » Đối với bệnh nhân có trùng lặp SJS/TEN và TEN, nhiều trung tâm bỏng chỉ định IVIg khi có phát ban tiến triển nhanh và khi bệnh nhân được coi là ứng viên phù hợp về mặt lâm sàng. » Đặc biệt thận trọng đối với bệnh nhân suy thận.[2] [67] [71] » Liều lượng sử dụng rất khác nhau và dựa trên báo cáo ca bệnh theo tài liệu khoa học, tường thuật tình huống và các chuỗi bằng chứng nhỏ.[9] [69] [70] [71] Các lựa chọn sơ cấp » globulin miễn dịch thông thường ở người: tham khảo ý kiến chuyên gia để có hướng dẫn về liều dùng |
||
| Bổ sung | Bao phủ mắt bằng màng ối | |
| » Việc dùng màng ối che phủ toàn bộ bề mặt mắt cùng với corticosteroid bôi ngoài da tăng cường trong thời gian ngắn, trong giai đoạn cấp tính của SJS và TEN đã được chứng minh là có tác dụng duy trì thị lực tốt và bề mặt mắt nguyên vẹn.[72]
» Trong hàng loạt ca bệnh tiến cứu, 79 bệnh nhân đã được đánh giá, điều trị và theo dõi trong ba tháng sau khi xuất viện. Các ca bệnh được phân loại là nhẹ hoặc trung bình được điều trị nội khoa Các ca bệnh được phân loại là nặng hoặc rất nặng sẽ được điều trị nội khoa và ghép màng ối khẩn cấp. Việc phân loại dựa trên mức độ nhuộm fluorescein của viền mí mắt, giác mạc và/hoặc kết mạc.[72] |
||
| Bổ sung | Phương pháp vật lý trị liệu và liệu pháp chức năng | |
| » Do bệnh nhân có thể bị hạn chế về khả năng di chuyển và giảm sức mạnh, bệnh nhân cần được đi lại hàng ngày và tập luyện trong phạm vi khả năng với nhà vật lý trị liệu và chuyên gia liệu pháp chức năng, nếu cần. | ||
Giai đoạn đầu
Corticosteroids
Việc sử dụng corticosteroid ở hội chứng Stevens-Johnson (SJS)/hoại tử biểu bì nhiễm độc (TEN) còn gây nhiều tranh cãi. Bác sĩ phẫu thuật bỏng xem xét chống chỉ định liệu pháp corticosteroid ở TEN khi bị mất lượng da lớn (>20% diện tích bề mặt toàn thân [TBSA]), đặc biệt do các corticosteroid có thể gây SJS/TEN.[4] Một nghiên cứu không có đối chứng đã sử dụng liệu pháp dexamethasone liều cao trên 6 bệnh nhân ở các giai đoạn đầu của SJS/TEN. Các nghiên cứu ca bệnh, chủ yếu là tiền cứu, đã phát hiện rằng corticosteroid có thể hữu ích trong một số ngày đầu sau khi xuất hiện phát ban.[65] [66] [67] [74] [75]
Lọc huyết tương
Đã thử tiến hành thay huyết tương ở những bệnh nhân mắc TEN, tuy nhiên kết quả không rõ ràng do có ít bằng chứng và nghiên cứu. Trong vòng 9 năm, 16 bệnh nhân đã được điều trị TEN: 10 bệnh nhân tiếp nhận liệu pháp hỗ trợ thông thường và 6 bệnh nhân được điều trị bằng lọc huyết tương; không có bệnh nhân được lọc huyết tương nào tử vong; trong khi đó ở nhóm còn lại có 2 bệnh nhân tử vong vì nhiễm khuẩn huyết và 2 bệnh nhân bị ngừng tim phổi.[76] Độ tuổi trung bình của bệnh nhân là 42,4 tuổi; tỷ lệ TBSA trung bình là 51,5% và thời gian nằm viện là 14,8 ngày.[76] Một nghiên cứu khác sử dụng thành công phương pháp lọc huyết tương bên ngoài đơn vị về bỏng, trên 13 bệnh nhân với từ 17% đến 100% TBSA và từ 1 đến 4 tổn thương màng niêm mạc.[77] Những bệnh nhân này đã được thực hiện từ 2 đến 5 phiên lọc huyết tương (trung bình là 3,4 phiên, trao đổi trung bình 10 L huyết tương, được thực hiện khoảng hai ngày một lần). Ba bệnh nhân đã tử vong và 10 bệnh nhân đã hồi phục.[77] Một nghiên cứu so sánh phương pháp lọc huyết tương với 2 loạt đã công bố (không lọc huyết tương) làm cơ sở đối chứng, tuy nhiên ở cùng độ tuổi, tỷ lệ phần trăm TBSA, thời gian nằm viện và thời gian biểu mô hóa như nhau thì tỷ lệ tử vong tương tự nhau (12,5%) với 8 bệnh nhân tiếp nhận trung bình 5,5 đợt điều trị lọc huyết tương.[78]
Ciclosporin
Một số báo cáo ca bệnh rời rạc cho thấy việc điều trị TEN thành công bằng ciclosporin.[65] Một nghiên cứu nhỏ ở các bệnh nhân mắc TEN nặng (n=11; trung bình 83% TBSA bị ảnh hưởng) cho thấy điều trị bằng ciclosporin giúp ngưng tiến triển bệnh nhanh hơn, thời gian tái biểu mô hóa ngắn hơn, giảm suy phủ tạng và tình trạng giảm bạch cầu nhẹ hơn so với điều trị bằng cyclophosphamide và corticosteroid.[79] Trong đánh giá sơ đồ tiền cứu cho 71 bệnh nhân mắc SJS/TEN, ciclosporin liên quan đến giảm số trường hợp tử vong hơn mức dự kiến (tỷ lệ tử vong chuẩn là 0,43) trong khi globulin miễn dịch qua đường tĩnh mạch (IVIg) liên quan đến tăng tỷ lệ tử vong (tỷ lệ tử vong chuẩn là 1,43).[80] Kết quả từ một thử nghiệm nhãn mở giai đoạn II nhỏ (n=29) cho thấy ciclosporin có thể giảm tỷ lệ tử vong và tiến triển của tình trạng bong tróc da ở bệnh nhân SJS/TEN.[81] Trong nghiên cứu nhỏ trên 12 bệnh nhân có TBSA trung bình là 77% được điều trị bằng ciclosporin A và lọc huyết tương, có một ca tử vong.[82]
Cyclophosphamide
Bốn bệnh nhân đã được điều trị thành công bằng prednisolone và cyclophosphamide.[83] Cơ chế này đã được chứng minh khả năng ức chế nhiễm độc tế bào qua trung gian tế bào.[83]
Phủ tấm biểu mô niêm mạc miệng đã nuôi cấy lên bề mặt mắt
Việc ghép tấm biểu mô niêm mạc miệng đã nuôi cấy cung cấp phương pháp thay thế khả thi đối với các bệnh về bề mặt mắt nghiêm trọng do TEN, hóa chất, nhiệt và các thương tích khác.[84] [85]
Thuốc ức chế yếu tố hoại tử u (TNF)-alpha
Các báo cáo ca bệnh chỉ ra lợi ích của etanercept và infliximab.[86] [87]
Liên lạc theo dõi
Khuyến nghị
Giám sát
Không có khuyến cáo cụ thể do tình trạng sức khỏe của mỗi bệnh nhân khi nhập viện sẽ quyết định việc điều trị tiếp theo.
Nếu ảnh hưởng đến mắt, bệnh nhân cần khám bác sĩ chuyên khoa mắt và tùy theo tổn thương phủ tạng khác, bệnh nhân có thể cần được theo dõi bởi bác sĩ chuyên khoa như bác sĩ chuyên khoa hô hấp, bác sĩ chuyên khoa thận, bác sĩ chuyên khoa dị ứng, bác sĩ chuyên khoa tiêu hóa hoặc bác sĩ chuyên khoa bỏng.[2]
Những bệnh nhân nữ chưa đến tuổi mãn kinh cần được bác sĩ phụ khoa theo dõi và thực hiện thăm khám vùng chậu để loại trừ chứng dính âm đạo trong vòng vài tháng sau khi xuất viện. Chứng dính âm đạo không được chẩn đoán có thể ảnh hưởng đến việc quan hệ tình dục hoặc sinh thường. Việc phòng ngừa các biến chứng này rất quan trọng.[2] [95]
Bệnh nhân mắc chứng khó nuốt hoặc viêm niêm mạc cần khám bác sĩ chuyên khoa tai-mũi-họng.[2]
Do bệnh nhân có thể bị hạn chế về khả năng di chuyển và giảm sức mạnh, bệnh nhân cần được đi lại hàng ngày và tập luyện trong phạm vi khả năng với nhà vật lý trị liệu và chuyên gia liệu pháp chức năng, nếu cần.
Hướng dẫn dành cho bệnh nhân
Cũng cần tư vấn cho bệnh nhân đeo vòng loại MedicAlert.
Bệnh nhân điều trị khỏi hội chứng Stevens-Johnson (SJS) hoặc hoại tử biểu bì nhiễm độc (TEN) cần tránh dùng các loại thuốc kích hoạt bệnh.
Bệnh nhân cần tránh tiếp xúc với ánh nắng và tránh bị cháy nắng trong ít nhất 1 năm để thúc đẩy quá trình chữa lành da, đặc biệt là các vùng bị ảnh hưởng bởi phát ban, mụn nước hoặc bong tróc. Bệnh nhân nên sử dụng kem dưỡng ẩm.
Các biến chứng
| Các biến chứng | Khung thời gian | Khả năng |
| Mất nước | Ngắn hạn | Cao |
| Khi nhập viện, cần đánh giá tình trạng bù nước của bệnh nhân. Nếu bệnh nhân bị viêm miệng, buồn nôn hoặc nôn, bệnh nhân có nguy cơ bị mất nước. Bên cạnh đó, tùy theo mức độ bong tróc da, bệnh nhân có thể mất một lượng dịch đáng kể qua bề mặt da bị bóc.
Nếu bệnh nhân có thể bù dịch qua đường uống, nên khuyến khích phương pháp này. Nếu không, nên bắt đầu sử dụng qua IV (đường tĩnh mạch) như dung dịch Ringer có lactate hoặc NaCl 0,9% để bù nước cho bệnh nhân. Nếu bệnh nhân bị bong tróc da từ 15% đến 20% diện tích bề mặt toàn thân (TBSA) trở lên, bệnh nhân cần được bù dịch hồi sức do bỏng chứa: 2 đến 4 mL dung dịch Ringer có lactate (LR) X kg trọng lượng X % TBSA đối với người lớn và trẻ em >14 tuổi, >40 kg; 3 mL dung dịch LR x kg trọng lượng x % TBSA đối với trẻ em <14 tuổi, <40 kg; và dextrose 5% trong dung dịch Ringer có lactate cho trẻ sơ sinh <10 kg. Năm mươi lăm phần trăm lượng dịch đã tính phải được cung cấp trong 8 giờ đầu và phần còn lại được chia sử dụng trong 16 giờ tiếp theo. Bất kể lượng dịch cần thiết theo tính toán, đánh giá lâm sàng về đáp ứng của bệnh nhân đặc biệt quan trọng. Theo dõi bù dịch trong hồi sức thông qua lượng nước tiểu. Lưu ý lượng nước tiểu của người lớn là 0,5 mL/kg/giờ (30 đến 50 mL/giờ) và trẻ em có cân nặng <30 kg có lượng nước tiểu là 1 mL/kg/giờ. Có thể tăng hoặc giảm bù dịch trong hồi sức dựa trên lượng nước tiểu.[51] |
||
| Sắc tố da bất thường | Dài hạn | Trung bình |
| Nên khám bác sĩ da liễu để được chẩn đoán và khuyến cáo. | ||
| Hội chứng chèn ép khoang cấp | Dài hạn | Trung bình |
| Biến chứng này hiếm gặp nhưng có thể xảy ra trên tứ chi hoặc thân.[98] | ||
| Nhiễm trùng | Biến thiên | Cao |
| Việc mất bề mặt da làm lộ lớp hạ bì và làm tăng nguy cơ nhiễm trùng. Cần theo dõi các dấu hiệu sinh tồn và cung cấp dịch bằng truyền tĩnh mạch. Cần vệ sinh họng miệng và phần môi nứt nẻ sạch sẽ nhất có thể.
Không nên dùng băng dính trên các bề mặt da tổn thương hở. Nên cấy máu, đờm và các bề mặt da hở và điều trị phù hợp với độ nhạy cảm kháng sinh Nếu vùng da bong tróc bị nhiễm trùng, chỉ định cắt lọc, vệ sinh, dùng thuốc kháng sinh và thay băng gạc.[51] Cần theo dõi các dấu hiệu sinh tồn và cung cấp dịch qua IV. Cần đặt nội khí quản và hỗ trợ máy thở nếu được chỉ định. Nên theo dõi chụp x-quang ngực để biết thông tin về quá trình lành bệnh. |
||
| Các biến chứng về mắt | Biến thiên | Cao |
| Các biến chứng về mắt bao gồm viêm kết mạc màng giả, mất chức năng ống lệ, viêm loét giác mạc, viêm màng bồ đào trước, thoát vị túi lệ, lộn mí, chứng lông quặm và dính mi cầu. Báo cáo cho thấy bệnh nhân được điều trị bằng phương pháp ghép màng ối cho viền mí mắt, kết mạc mi và bề mặt của mắt trong giai đoạn cấp tính của SJS hoặc TEN có thể giảm đáng kể nguy cơ biến chứng ở mắt.[72] Trong nhóm người Brazil gốc Pardo và châu Âu bị mắc SJS/TEN, HLA-A*66:01 có thể là nguyên nhân gây biến chứng mắt nặng; HLA-B*44:03 và HLA-C*12:03 có thể là chất chỉ điểm cho những biến chứng này ở nhóm hậu duệ của người châu Âu.[92]Nên khám bác sĩ chuyên khoa mắt để được chẩn đoán và khuyến cáo. |
||
| Mất đĩa móng | Biến thiên | Trung bình |
| Phải bảo vệ phần nền móng cho đến khi tái tạo đĩa móng. | ||
| Suy gan cấp tính | Biến thiên | Trung bình |
| Đây có thể là phản ứng với thuốc mà bệnh nhân đang dùng hoặc phản ứng với sự xuất hiện của hội chứng Stevens- Johnson (SJS) hoặc hoại tử biểu bì nhiễm độc (TEN). Tùy theo độ nặng của SJS hoặc TEN, phản ứng viêm do cytokine gây ra dưới dạng phản ứng với những thương tổn có thể tương tự với tình trạng xảy ra ở vết thương do nhiệt: gan nhiễm mỡ, tế bào gan chết theo chương trình và hoại tử. Cơ chế đối với tế bào chết theo chương trình chưa được xác định rõ. Vết thương hoại tử có thể do giảm tưới máu hoặc tái tưới máu do thiếu máu cục bộ. Tổn thương gan cũng có thể là một phần của nhiều tình trạng suy đa phủ tạng, đặc biệt khi bị nhiễm khuẩn huyết.[8] [9] [93]Cần theo dõi enzym để xác định xem bệnh nhân có đang hồi phục không và tiến hành sinh thiết gan nếu được chỉ định, dựa trên tiến triển của bệnh nhân trong khi nằm viện | ||
| Suy thận cấp | Biến thiên | Trung bình |
| Tổn thương thận xảy ra, dẫn đến hoạt tử ống thận cấp và suy thận do giảm tưới máu hoặc do dược phẩm, như thuốc kháng sinh mà bệnh nhân cần dùng, đặc biệt khi bị nhiễm khuẩn huyết.
Cần theo dõi urê và creatinine để xác định xem bệnh nhân có đang hồi phục không và tiến hành sinh thiết thận nếu được chỉ định, dựa trên tiến triển của bệnh nhân trong khi nằm viện.[8] [9] [94] |
||
| Hạ thân nhiệt | Biến thiên | Trung bình |
| Nếu mất từ 15% đến 20% TBSA trở lên do bong tróc da, bệnh nhân sẽ bị mất khả năng điều chỉnh nhiệt qua bề mặt da. Bệnh nhân sẽ bị hạ thân nhiệt và cần được làm ấm bên ngoài. Hạ thân nhiệt có thể gây ảnh hưởng đến hệ tuần hoàn, hệ đông máu và lành vết thương. Có thể làm ấm cho bệnh nhân bằng cách tăng nhiệt độ bên ngoài và sử dụng chăn nhựa bơm khí ấm (‘Bair Huggers’). | ||
| Dính âm đạo | Biến thiên | Trung bình |
| Bệnh nhân nằm viện cần khám bác sĩ phụ khoa. Những bệnh nhân chưa đến tuổi mãn kinh cần được bác sĩ theo dõi và thực hiện thăm khám vùng chậu để loại trừ chứng dính âm đạo trong vòng vài tháng sau khi xuất viện. Việc không điều trị dính âm đạo có thể ảnh hưởng đến việc quan hệ tình dục hoặc sinh thường.[2] [95] | ||
| Biến chứng phổi | Biến thiên | Trung bình |
| Có khoảng 13 đến 16 ca được báo cáo bị biến chứng phổi mạn tính, bao gồm viêm phế quản, viêm tắc tiểu phế quản và giãn phế quản.[96] | ||
Tiên lượng
Tiên lượng tốt nhất khi:
- Bệnh nhân <50 tuổi
- Diện tích bề mặt toàn thân (TBSA) bị ảnh hưởng thấp
- Bệnh nhân đã được chuyển đến trung tâm bỏng
- Bệnh nhân không bị nhiễm khuẩn huyết
- Bệnh nhân không cần dùng thuốc kháng sinh.
Một nghiên cứu trên các bệnh nhi mắc SJS hoặc TEN đã nhập viện tại một bệnh viện Hoa Kỳ từ năm 2000 đến 2007 cho thấy 18% bệnh nhân bị tái phát SJS trong vòng 7 năm sau đợt đầu tiên và 47% để lại di chứng lâu dài. Tỷ lệ tử vong thấp hơn so với báo cáo trên người lớn.[88] [89]
Một nghiên cứu hồi cứu trên 189 bệnh nhi mắc SJS trong thời gian 29 năm tại Thái Lan cho thấy 20% ca bệnh bị biến chứng.[90]
Hội chứng Stevens-Johnson (SJS)
Phần lớn bệnh nhân hồi phục, mặc dù bệnh nhân có thể bị một số biến chứng về mắt hoặc nội tạng do bệnh; tỷ lệ tử vong từ 1% đến 5%.
Trùng lấp SJS-TEN
Phần lớn bệnh nhân hồi phục, mặc dù bệnh nhân có thể bị một số biến chứng về mắt hoặc ở nội tạng.
TEN (hoại tử biểu bì nhiễm độc)
Phần lớn bệnh nhân hồi phục, mặc dù bệnh nhân có thể bị một số biến chứng về mắt hoặc nội tạng do bệnh; tỷ lệ tử vong từ 25% đến 35%.
Trong một nghiên cứu đa trung tâm trên 199 bệnh nhân bị hoại tử biểu bì nhiễm độc (TEN), 64 bệnh nhân đã tử vong. Trong số các ca tử vong, một phần ba số trường hợp do nhiễm khuẩn huyết, một phần ba do suy đa phủ tạng, 14% do các biến chứng tim phổi và 16% ca tử vong do các nguyên nhân khác. Trong 135 ca hồi phục, 66% bệnh nhân đã được về nhà, 14% được chuyển đến bộ phận phục hồi chức năng, 7,3% được chuyển đến cơ sở chăm sóc trung cấp và 7,3% được chuyển đến bác sĩ giới thiệu.[91]
Hướng dẫn điều trị
Châu Âu
European guidelines on the use of high-dose intravenous immunoglobulin in dermatology
Nhà xuất bản: European Dermatology Forum
Xuất bản lần cuối: 2017
UK guidelines for the management of Stevens-Johnson syndrome/toxic epidermal necrolysis in adults
Nhà xuất bản: British Association of Dermatologists
Xuất bản lần cuối: 2016
Quốc tế
Guidelines for the management of Stevens-Johnson syndrome/toxic epidermal necrolysis: an Indian perspective
Nhà xuất bản: The Indian Association of Dermatologists, Venereologists and Leprologists
Xuất bản lần cuối: 2016
Nguồn trợ giúp trực tuyến
- Wallace rule of 9s (external link)
Các bài báo chủ yếu
- Dodiuk-Gad RP, Chung WH, Valeyrie-Allanore L, et al. Stevens-Johnson syndrome and toxic epidermal necrolysis: an update. Am J Clin Dermatol. 2015;16:475-493. Tóm lược
- Mockenhaupt M. Stevens-Johnson syndrome and toxic epidermal necrolysis: clinical patterns, diagnostic considerations, etiology, and therapeutic management. Semin Cutan Med Surg. 2014;33:10-16. Tóm lược
- Bastuji-Garin S, Rzany B, Stern RS, et al. Clinical classification of cases of toxic epidermal necrolysis, Stevens-Johnson syndrome, and erythema multiforme. Arch Dermatol. 1993 Jan;129(1):92-6. Tóm lược
- Schwartz RA, McDonough PH, Lee BW. Toxic epidermal necrolysis. Part I: introduction, history, classification, clinical features, systemic manifestations, etiology, and immunopathogenesis. J Am Acad Dermatol. 2013;69:173. Tóm lược
- Schwartz RA, McDonough PH, Lee BW. Toxic epidermal necrolysis. Part II: prognosis, sequelae, diagnosis, differential diagnosis, prevention, and treatment. J Am Acad Dermatol. 2013;69:187. Tóm lược
- Guegan S, Bastuji-Garin S, Poszepczynska-Guigne E, et al. Performance of the SCORTEN during the first five days of hospitalization to predict the prognosis of epidermal necrolysis. J Invest Dermatol. 2006;126:272-276. Tóm lược
- Gregory DG. New grading system and treatment guidelines for the acute ocular manifestations of Stevens-Johnson syndrome. Ophthalmology. 2016;123:1653-1658. Tóm lược
Tài liệu tham khảo
- Bộ Y tế, Hướng dẫn chẩn đoán và điều trị các bệnh da liễu, truy cập ngày 2/1/2024.
- Stevens AM, Johnson FC. A new eruptive fever associated with stomatitis and ophthalmia. Am J Dis Child. 1922;24:526-533.
- Dodiuk-Gad RP, Chung WH, Valeyrie-Allanore L, et al. Stevens-Johnson syndrome and toxic epidermal necrolysis: an update. Am J Clin Dermatol. 2015;16:475-493. Tóm lược
- Mockenhaupt M. Stevens-Johnson syndrome and toxic epidermal necrolysis: clinical patterns, diagnostic considerations, etiology, and therapeutic management. Semin Cutan Med Surg. 2014;33:10-16. Tóm lược
- Roujeau JC, Stern RS. Severe adverse cutaneous reactions to drugs. N Engl J Med. 1994 Nov 10;331(19):1272-85. Tóm lược
- Bastuji-Garin S, Rzany B, Stern RS, et al. Clinical classification of cases of toxic epidermal necrolysis, Stevens-Johnson syndrome, and erythema multiforme. Arch Dermatol. 1993 Jan;129(1):92-6. Tóm lược
- Auquier-Dunant A, Mockenhaupt M, Maldi L, et al. Correlations between clinical patterns and causes of erythema multiforme majus, Stevens-Johnson syndrome, and toxic epidermal necrolysis: results of an international prospective study. Arch Dermatol. 2002;138:1019-1024. Tóm lược
- Lyell A. Toxic epidermal necrolysis: an eruption resembling scalding of the skin. Br J Dermatol. 1956;68:355-361. Tóm lược
- Schwartz RA, McDonough PH, Lee BW. Toxic epidermal necrolysis. Part I: introduction, history, classification, clinical features, systemic manifestations, etiology, and immunopathogenesis. J Am Acad Dermatol. 2013;69:173. Tóm lược
- Schwartz RA, McDonough PH, Lee BW. Toxic epidermal necrolysis. Part II: prognosis, sequelae, diagnosis, differential diagnosis, prevention, and treatment. J Am Acad Dermatol. 2013;69:187. Tóm lược
- Roujeau JC, Kelly JP, Naldi L, et al. Medication use and the risk of Stevens-Johnson syndrome or toxic epidermal necrolysis. N Engl J Med. 1995;333:1600-1608. Toàn văn Tóm lược
- Coopman SA, Johnson RA, Platt R, et al. Cutaneous disease and drug reactions in HIV infection. N Engl J Med. 1993;328:1670-1674. Toàn văn Tóm lược
- Mittmann N, Knowles SR, Koo M, et al. Incidence of toxic epidermal necrolysis and Stevens-Johnson Syndrome in an HIV cohort: an observational, retrospective case series study. Am J Clin Dermatol. 2012;13:49-54. Tóm lược
- Mockenhaupt M, Messenheimer J, Tennis P, et al. Risk of Stevens-Johnson syndrome and toxic epidermal necrolysis in new users of antiepileptics. Neurology. 2005;64:1134-1138. Tóm lược
- Calabrese JR, Sullivan JR, Bowden CL, et al. Rash in multicenter trials of lamotrigine in mood disorders: clinical relevance and management. J Clin Psychiatry. 2002 Nov;63(11):1012-9. Tóm lược
- Yip VL, Alfirevic A, Pirmohamed M. Genetics of immune-mediated adverse drug reactions: a comprehensive and clinical review. Clin Rev Allergy Immunol. 2015;48:165-175. Tóm lược
- Chang CC, Too CL, Murad S, et al. Association of HLA-B*1502 allele with carbamazepine-induced toxic epidermal necrolysis and Stevens-Johnson syndrome in the multi-ethnic Malaysian population. Int J Dermatol. 2011;50:221-224. Tóm lược
- Chung WH, Hung SI. Genetic markers and danger signals in stevens-johnson syndrome and toxic epidermal necrolysis. Allergol Int. 2010;59:325-332. Tóm lược
- Leckband SG, Kelsoe JR, Dunnenberger HM, et al. Clinical Pharmacogenetics Implementation Consortium guidelines for HLA-B genotype and carbamazepine dosing. Clin Pharmacol Ther. 2013;94:324-328. Toàn văn Tóm lược
- Ueta M, Sawai H, Sotozono C, et al. IKZF1, a new susceptibility gene for cold medicine-related Stevens- Johnson syndrome/toxic epidermal necrolysis with severe mucosal involvement. J Allergy Clin Immunol. 2015;135:1538-1545. Tóm lược
- Hershfield MS, Callaghan JT, Tassaneeyakul W, et al. Clinical Pharmacogenetics Implementation Consortium guidelines for human leukocyte antigen-B genotype and allopurinol dosing. Clin Pharmacol Ther. 2013;93:153-158. Toàn văn Tóm lược
- Kongpan T, Mahasirimongkol S, Konyoung P, et al. Candidate HLA genes for prediction of co-trimoxazole-induced severe cutaneous reactions. Pharmacogenet Genomics. 2015;25:402-411. Tóm lược
- Tangamornsuksan W, Lohitnavy O, Kongkaew C, et al. Association of HLA-B*5701 genotypes and abacavir- induced hypersensitivity reaction: a systematic review and meta-analysis. J Pharm Pharm Sci. 2015;18:68-76. Toàn văn Tóm lược
- Nethercott JR, Choi BC. Erythema multiforme (Stevens Johnson syndrome) chart review of 123 hospitalized patients. Dermatologica. 1985;171:383-396. Tóm lược
- Centers for Disease Control and Prevention. Smallpox fact sheet – information for clinicians: adverse reactions following smallpox vaccination. 2008. http://emergency.cdc.gov.
- Morantz C. CDC releases guidelines for treating adverse reactions to smallpox vaccination. Am Fam Physician. 2003;67:1827, 1829-1830, 1833-1834. Tóm lược
- Levi N, Bastuji-Garin S, Mockenhaupt M, et al. Medications as risk factors of Stevens-Johnson syndrome and toxic epidermal necrolysis in children: a pooled analysis. Pediatrics. 2009;123:e297-e304. Tóm lược
- Rotunda A, Hirsch RJ, Scheinfeld N, et al. Severe cutaneous reactions associated with the use of human immunodeficiency virus medications. Acta Derm Venereol. 2003;83:1-9. Tóm lược
- Borras-Blasco J, Navarro-Ruiz A, Borras C, et al. Adverse cutaneous reactions associated with the newest antiretroviral drugs in patients with human immunodeficiency virus infection. J Antimicrob Chemother. 2008;62:879-888. Toàn văn Tóm lược
- La Grenade L, Lee L, Weaver J, et al. Comparison of reporting of Stevens-Johnson syndrome and toxic epidermal necrolysis in association with selective COX-2 inhibitors. Drug Saf. 2005;28:917-924. Tóm lược
- Layton D, Marshall V, Boshier A, et al. Serious skin reactions and selective COX-2 inhibitors: a case series from prescription-event monitoring in England. Drug Saf. 2006;29:687-696. Tóm lược
- Roujeau JC, Mockenhaupt M, Tahan SR, et al. Telaprevir-related dermatitis. JAMA Dermatol. 2013;149:152-158. Toàn văn Tóm lược
- Mufaddel A, Osman OT, Almugaddam F. Adverse cutaneous effects of psychotropic medications. Exp Rev Dermatol. 2013;8:681-692.
- Mockenhaupt M, Viboud C, Dunant A, et al. Stevens-Johnson syndrome and toxic epidermal necrolysis: assessment of medication risks with emphasis on recently marketed drugs. The EuroScar-Study. J Invest Dermatol. 2008;128:35-44. Tóm lược
- Irazabal MP, Martin LM, Gil LA, et al. Tranexamic acid-induced toxic epidermal necrolysis. Ann Pharmacother. 2013;47:e16. Tóm lược
- Tremblay L, de Chambrun GP, De Vroey B, et al. Stevens-Johnson syndrome with sulfasalazine treatment: report of two cases. J Crohns Colitis. 2011;5:457-460. Tóm lược
- Rosen AC, Balagula Y, Raisch DW, et al. Life-threatening dermatologic adverse events in oncology. Anticancer Drugs. 2014;25:225-234. Toàn văn Tóm lược
- Mawson AR, Eriator I, Karre S. Stevens-Johnson syndrome and toxic epidermal necrolysis (SJS/TEN): could retinoids play a causative role? Med Sci Monit. 2015;21:133-143. Toàn văn Tóm lược
- Paul C, Wolkenstein PC, Adle H, et al. Apoptosis as a mechanism of keratinocyte death in toxic epidermal necrolysis. Br J Dermatol. 1996;134:710-714. Tóm lược
- Le Cleach L, Delaire S, Boumsell L, et al. Blister fluid T lymphocytes during toxic epidermal necrolysis are functional cytotoxic cells which express human natural killer (NK) inhibitory receptors. Clin Exp Immunol. 2000;119:225-230. Tóm lược
- Caproni M, Torchia D, Schincaglia E, et al. Expression of cytokines and chemokine receptors in the cutaneous lesions of erythema multiforme and Stevens-Johnson syndrome/toxic epidermal necrolysis. Br. J Dermatol. 2006;155:722-728. Tóm lược
- Viard I, Wehrli P, Bullani R, et al. Inhibition of toxic epidermal necrolysis by blockade of CD95 with human intravenous immunoglobulin. Science. 1998;282:490-493. Tóm lược
- Chung WH, Hung SI, Yang JY, et al. Granulysin is a key mediator for disseminated keratinocyte death in Stevens-Johnson syndrome and toxic epidermal necrolysis. Nat Med. 2008;14:1343-1350. Tóm lược
- Abe R, Shimizu T, Shibaki A, et al. Toxic epidermal necrolysis and Stevens-Johnson syndrome are induced by soluble Fas ligand. Am J Pathol. 2003;162:1515-1520. Toàn văn Tóm lược
- Ziemer M, Kardaun SH, Liss Y, et al. Stevens-Johnson syndrome and toxic epidermal necrolysis in patients with lupus erythematosus: a descriptive study of 17 cases from a national registry and review of the literature. Br J Dermatol. 2012;166:575-600. Tóm lược
- Vern-Gross TZ, Kowal-Vern A. Erythema multiforme, Stevens Johnson syndrome, and toxic epidermal necrolysis syndrome in patients undergoing radiation therapy: a literature review. Am J Clin Oncol. 2014;37:506-513. Tóm lược
- Demiral AN, Yerebakan O, Simsir V, et al. Amifostine-induced toxic epidermal necrolysis during radiotherapy: a case report. Jpn J Clin Oncol. 2002;32:477-479. Toàn văn Tóm lược
- de Prost N, Mekontso-Dessap A, Valeyrie-Allanore L, et al. Acute respiratory failure in patients with toxic epidermal necrolysis: clinical features and factors associated with mechanical ventilation. Crit Care Med. 2014;42:118-128. Tóm lược
- Lund CC, Browder NC. The estimation of areas of burns. Surg Gynecol Obst. 1944;79:352-358.
- Wachtel TL, Berry CC, Wachtel EE, et al. The inter-rater reliability of estimating the size of burns from various burn area chart drawings. Burns. 2000;26:156-170. Tóm lược
- Cartotto R, Mayich M, Nickerson D, et al. SCORTEN accurately predicts mortality among toxic epidermal necrolysis patients treated in a burn center. J Burn Care Res. 2008;29:141-146. Tóm lược
- Hettiaratchy S, Papini R. Initial management of a major burn: II – assessment and resuscitation. BMJ. 2004;329:101-103. Toàn văn Tóm lược (Bản PDF chủ đề BMJ Best Practice (Thực tiễn Tốt nhất của BMJ) này 3 dựa trên phiên bản trang mạng được cập nhật lần cuối vào: Mar 21, 2018).
- Sekula P, Liss Y, Davidovici B, et al. Evaluation of SCORTEN on a cohort of patients with Stevens-Johnson Syndrome and toxic epidermal necrolysis included in the RegiSCAR Study. J Burn Care Res. 2011;32:237-245. Tóm lược
- Guegan S, Bastuji-Garin S, Poszepczynska-Guigne E, et al. Performance of the SCORTEN during the first five days of hospitalization to predict the prognosis of epidermal necrolysis. J Invest Dermatol. 2006;126:272-276. Tóm lược
- George SM, Harrison DA, Welch CA, et al. Dermatological conditions in intensive care: a secondary analysis of the Intensive Care National Audit and Research Centre (ICNARC) Case Mix Programme Database. Crit Care. 2008;12(suppl 1):S1-S10. Toàn văn Tóm lược
- Imahara SD, Holmes JH, Heimbach DM, et al. SCORTEN overestimates mortality in the setting of a standardized treatment protocol. J Burn Care Res. 2006;27:270-275. Tóm lược
- de Prost N, Ingen-Housz-Oro S, Duong T, et al. Bacteremia in Stevens-Johnson syndrome and toxic epidermal necrolysis: epidemiology, risk factors, and predictive value of skin cultures. Medicine (Baltimore). 2010;89:28-36. Tóm lược
- Husain Z, Reddy BY, Schwartz RA. DRESS syndrome: Part I. Clinical perspectives. J Am Acad Dermatol. 2013;68:693. Tóm lược
- Husain Z, Reddy BY, Schwartz RA. DRESS syndrome: Part II. Management and therapeutics. J Am Acad Dermatol. 2013;68:709. Tóm lược
- Baba M, Karakas M, Aksunger VL, et al. The anticonvulsant hypersensitivity syndrome. J Eur Acad Dermatol Venereol. 2003;17:399-401. Tóm lược
- Centers for Disease Control and Prevention. Toxic syndrome description: vesicant/blister agent poisoning. April 2013. http://www.emergency.cdc.gov (last accessed 23 September 2017). Toàn văn
- Sehgal V, Srivastava G. Fixed drug eruption (FDE): changing scenario of incriminating drugs. Int J Dermatol. 2006; 45:897-908. Tóm lược
- Lipowicz S, Sekula P, Ingen-Housz-Oro S, et al. Prognosis of generalized bullous fixed drug eruption: comparison with Stevens-Johnson syndrome and toxic epidermal necrolysis. Br J Dermatol. 2013; 168:726-732. Tóm lược
- Thienvibul C, Vachiramon V, Chanprapaph K. Five-year retrospective review of acute generalized exanthematous pustulosis. Dermatol Res Pract. 2015;2015:260928. Toàn văn Tóm lược
- Chung WH, Shih SR, Chang CF, et al. Clinicopathologic analysis of coxsackievirus A6 new variant induced widespread mucocutaneous bullous reactions mimicking severe cutaneous adverse reactions. J Infect Dis. 2013;208:1968-1978. Toàn văn Tóm lược
- Zimmermann S, Sekula P, Venhoff M, et al. Systemic immunomodulating therapies for Stevens-Johnson syndrome and toxic epidermal necrolysis: a systematic review and meta-analysis. JAMA Dermatol. 2017;153:514-522. Tóm lược
- Schneider JA, Cohen PR. Stevens-Johnson syndrome and toxic epidermal necrolysis: a concise review with a comprehensive summary of therapeutic interventions emphasizing supportive measures. Adv Ther. 2017;34:1235-1244. Toàn văn Tóm lược
- Herndon DN, ed. Total burn care. 4th ed. Philadelphia, PA: Elsevier; 2012.
- Shiga S, Cartotto R. What are the fluid requirements in toxic epidermal necrolysis? J Burn Care Res. 2010;31:100-104. Tóm lược
- Barron SJ, Del Vecchio MT, Aronoff SC. Intravenous immunoglobulin in the treatment of Stevens-Johnson syndrome and toxic epidermal necrolysis: a meta-analysis with meta-regression of observational studies. Int J Dermatol. 2015;54:108-115. Toàn văn Tóm lược
- Aires DJ, Fraga G, Korentager R, et al. Early treatment with nonsucrose intravenous immunoglobulin in a burn unit reduces toxic epidermal necrolysis mortality. J Drugs Dermatol. 2013;12:679-684. Tóm lược
- Enk A, Hadaschik E, Eming R, et al. European Guidelines (S1) on the use of high-dose intravenous immunoglobulin in dermatology. J Dtsch Dermatol Ges. 2017;15:228-241. Tóm lược
- Gregory DG. New grading system and treatment guidelines for the acute ocular manifestations of Stevens-Johnson syndrome. Ophthalmology. 2016;123:1653-1658. Tóm lược
- Saffle R, Hildreth M. Metabolic support of the burned patient. In: Herndon DN, ed. Total burn care. 2nd ed. New York: W.B. Saunders; 2002:271-287.
- Creamer D, Walsh SA, Dziewulski P, et al. UK guidelines for the management of Stevens-Johnson syndrome/toxic epidermal necrolysis in adults 2016. Br J Dermatol. 2016;174:1194-1227. Toàn văn Tóm lược
- Gupta LK, Martin AM, Agarwal N, et al. Guidelines for the management of Stevens-Johnson syndrome/toxic epidermal necrolysis: an Indian perspective. Indian J Dermatol Venereol Leprol. 2016;82:603-625. Toàn văn Tóm lược
- Egan CA, Grant WJ, Morris SE, et al. Plasmapheresis as an adjunct treatment in toxic epidermal necrolysis. J Am Acad Dermatol. 1999;40:458-461. Tóm lược
- Bamichas G, Natse T, Christidou F, et al. Plasma exchange in patients with toxic epidermal necrolysis. Ther Apher. 2002;6:225-228. Tóm lược
- Furubacke A, Berlin G, Anderson C, et al. Lack of significant treatment effect of plasma exchange in the treatment of drug-induced toxic epidermal necrolysis? Intensive Care Med.1999;25:1307-1310. Tóm lược
- Arevalo JM, Lorente JA, Gonzalez-Herrada C, et al. Treatment of toxic epidermal necrol80. Kirchhof MG, Miliszewski MA, Sikora S, et al. Retrospective review of Stevens-Johnson syndrome/toxic epidermal necrolysis treatment comparing intravenous immunoglobulin with cyclosporine. J Am Acad Dermatol. 2014;71:941-947. Tóm lược
- Valeyrie-Allanore L, Wolkenstein P, Brochard L, et al. Open trial of ciclosporin treatment for Stevens-Johnson syndrome and toxic epidermal necrolysis. Br J Dermatol. 2010;163:847-853. Tóm lược
- Giudice G, Maggio G, Bufano L, et al. Management of toxic epidermal necrolysis with plasmapheresis and cyclosporine A: our 10 years’ experience. Plast Reconstr Surg Glob Open. 2017;5:e1221. Toàn văn Tóm lược
- Heng MC, Allen SG. Efficacy of cyclophosphamide in toxic epidermal necrolysis. Clinical and pathophysiologic aspects. J Am Acad Dermatol. 1991;25:778-786. Tóm lược
- Satake Y, Higa K, Tsubota K, et al. Long-term outcome of cultivated oral mucosal epithelial sheet transplantation in treatment of total limbal stem cell deficiency. Ophthalmology. 2011;118:1524-1530. Tóm lược
- Sotozono C, Inatomi T, Nakamura T, et al. Cultivated oral mucosal epithelial transplantation for persistent epithelial defect in severe ocular surface diseases with acute inflammatory activity. Acta Ophthalmol. 2014;92:e447-e453. Toàn văn Tóm lược
- Wojtkiewicz A, Wysocki M, Fortuna J, et al. Beneficial and rapid effect of infliximab on the course of toxic epidermal necrolysis. Acta Derm Venereol. 2008;88:420-421. Toàn văn Tóm lược
- Scott-Lang V, Tidman M, McKay D. Toxic epidermal necrolysis in a child successfully treated with infliximab. Pediatr Dermatol. 2014;31:532-534. Tóm lược
- Finkelstein Y, Soon GS, Acuna P, et al. Recurrence and outcomes of Stevens-Johnson syndrome and toxic epidermal necrolysis in children. Pediatrics. 2011;128:723-728. Tóm lược
- Del Pozzo-Magana BR, Lazo-Langner A. Stevens Johnson Syndrome and toxic epidermal necrolysis in children: a literature review of current treatments. EMJ Dermatol. 2016;4:83-89. Toàn văn
- Singalavanija S, Limpongsanurak W. Stevens-Johnson syndrome in Thai children: a 29-year study. J Med Assoc Thai. 2011;94(suppl 3):85-90. Tóm lược
- Palmieri TL, Greenhalgh DG, Saffle JR, et al. A multicenter review of toxic epidermal necrolysis treated in U.S. burn centers at the end of the twentieth century. J Burn Care Rehabil. 2002;23:87-96. Tóm lược
- Wakamatsu TH, Ueta M, Tokunaga K, et al. Human leukocyte antigen class I genes associated with Stevens- Johnson syndrome and severe ocular complications following use of cold medicine in a Brazilian population. JAMA Ophthalmol. 2017;135:355-360. Tóm lược
- Jeschke MG, Finnerty CC. The hepatic response to a thermal injury. In: Herndon DN, ed. Total burn care. 4th ed. Philadelphia, PA: Elsevier; 2012:301-312.
- Goverman J, Fagan SP. Renal failure in association with thermal injuries. In: Herndon, DN, ed. Total burn care. 4th ed. Philadelphia, PA: Elsevier; 2012:369-376.
- Kaser DJ, Reichman DE, Laufer MR. Prevention of vulvovaginal sequelae in Stevens-Johnson syndrome and toxic epidermal necrolysis. Rev Obstet Gynecol. 2011;4:81-85. Toàn văn
- Kamada N, Kinoshita K, Togawa Y, et al. Chronic pulmonary complications associated with toxic epidermal necrolysis: report of a severe case with anti-Ro/SS-A and a review of the published work. J Dermatol. 2006;33:616-622. Tóm lược
- Baccaro LM, Sakharpe A, Miller A, et al. The first reported case of ureteral perforation in a patient with severe toxic epidermal necrolysis syndrome. J Burn Care Res. 2014;35:e265-e268. Tóm lược
- Kamal T, Elnikety S, Mashaly H, et al. Acute compartment syndrome of the forearm as a rare complication of toxic epidermal necrolysis: a case report. J Med Case Rep. 2012;6:84. Toàn văn Tóm lược
Hình ảnh
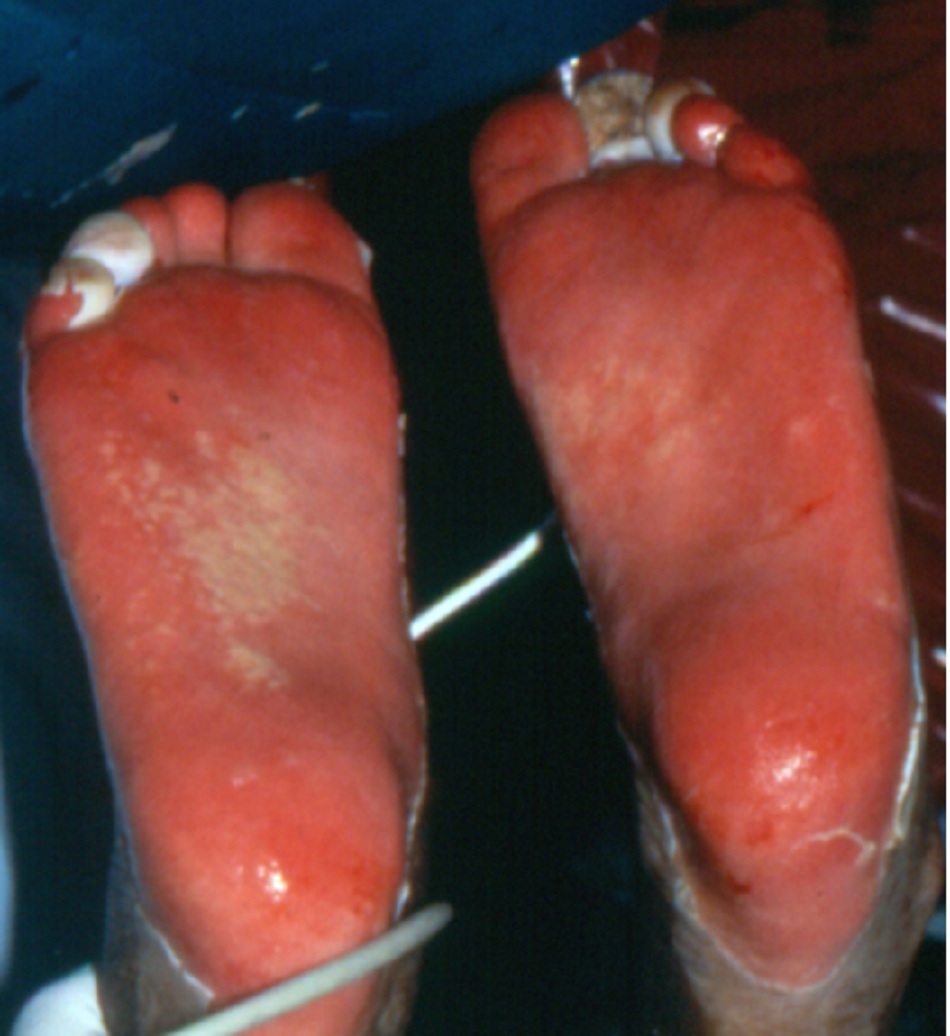
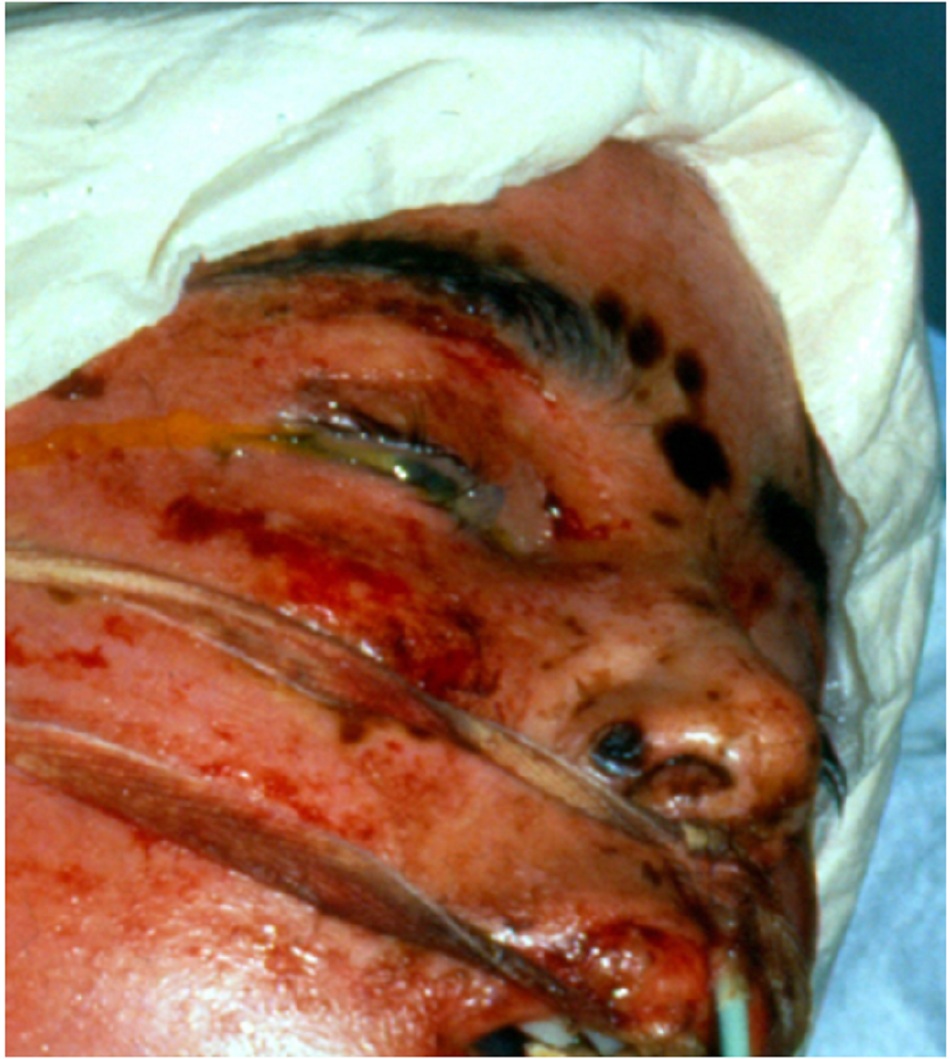
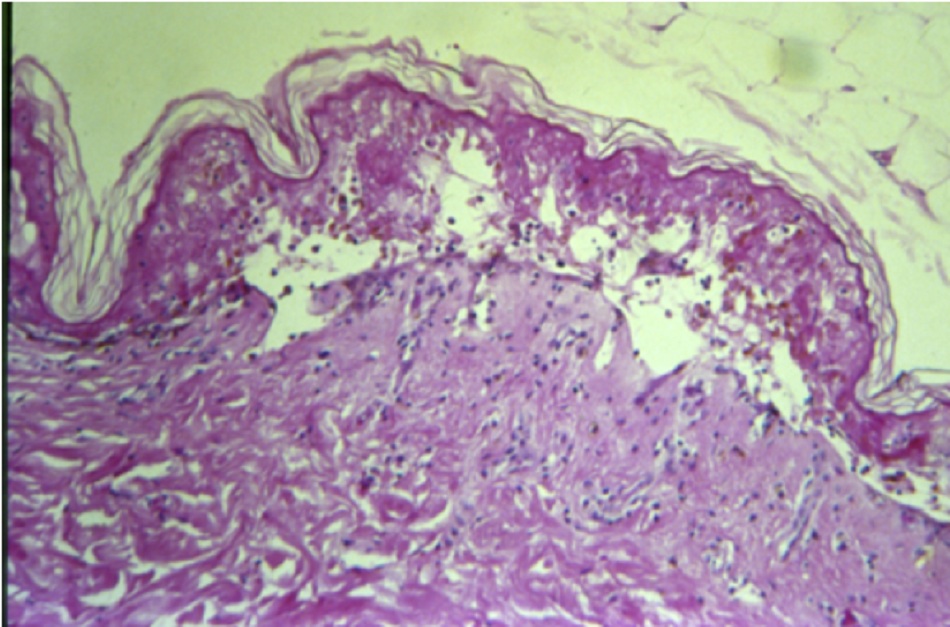
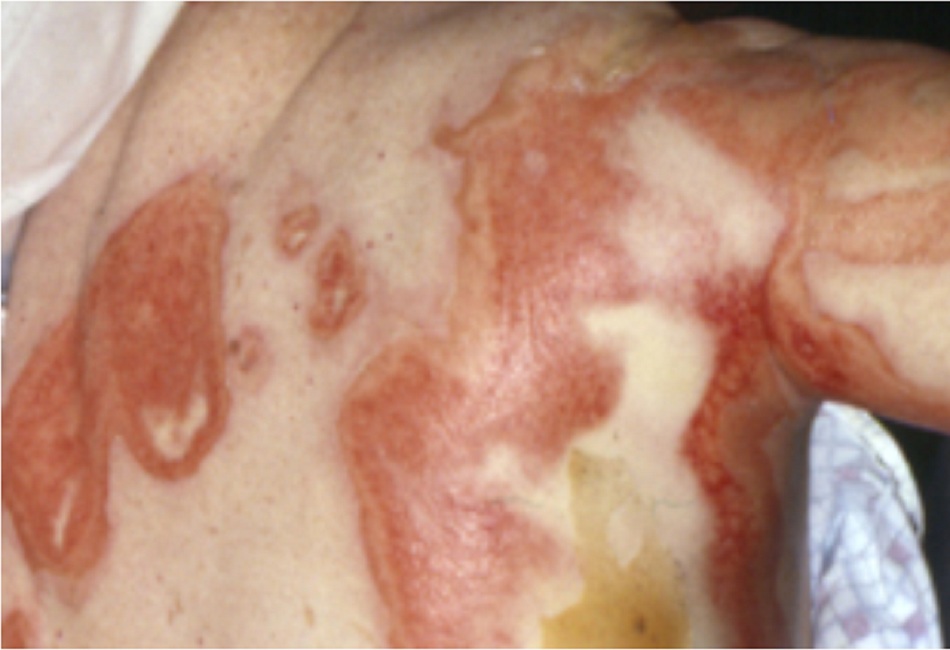
Những người có đóng góp
// Các tác giả:
Areta Kowal-Vern, MD
Assistant Professor
Department of Surgery, Rush University Medical Center, Chicago, IL
CÔNG KHAI THÔNG TIN: AK-V has received compensation for reviewing manuscripts for Rubriq from Research
Square on a variety of topics, including erythema multiforme, Stevens-Johnson syndrome and toxic epidermal necrolysis. She is also a manuscript reviewer for several journals, without renumeration.
// Những Người Bình duyệt:
Barbara A. Latenser, MD
Director Burn Unit
Department of Surgery, University of Iowa Hospitals, Iowa City, IA
CÔNG KHAI THÔNG TIN: BAL declares that she has no competing interests.
Tina Palmieri, MD
Assistant Chief of Burns
Shriners Hospital, UC Davis, Sacramento, CA
CÔNG KHAI THÔNG TIN: TP declares that she has no competing interests.
Venkat Gudi, MB BS
Consultant Dermatologist
Department of Dermatology, West Suffolk Hospital, Bury St. Edmunds, UK
CÔNG KHAI THÔNG TIN: VG declares that he has no competing interests.
Xem thêm:
Hội chứng Behcet: Nguyên nhân, chẩn đoán và điều trị theo BMJ

