Bệnh tiêu hóa
Bệnh do Clostridium difficile: Triệu chứng, chẩn đoán, điều trị và cách phòng ngừa theo BMJ
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
Link PDF: https://nhathuocngocanh.com/wp-content/uploads/2021/12/Bệnh-do-Clostridium-difficile.pdf
Tóm tắt
◊ Bệnh nhân thường có biểu hiện tiêu chảy, đau bụng và tăng bạch cầu, và có tiền sử dùng thuốc kháng sinh gần đây. Các triệu chứng thường gặp khác bao gồm sốt, tăng cảm giác vùng bụng và chướng bụng.
◊ Chỉ nên xét nghiệm ở những bệnh nhân bị tiêu chảy không rõ nguyên nhân, khởi phát lần đầu tiên (được xác định là từ 3 lần đại tiện không thành khuôn trong vòng 24 giờ). Khuyến nghị xét nghiệm phân tử đơn độc hoặc trong một nhóm xét nghiệm đa bước tùy thuộc vào phác đồ của cơ sở địa phương. Có thể thấy bằng chứng của giả mạc khi nội soi đại tràng sigma hoặc nội soi đại tràng ở một số bệnh nhân.
◊ Điều trị là ngưng dùng thuốc kháng sinh gây kích thích và bắt đầu điều trị bằng vancomycin hoặc fidaxomicin qua đường uống. Có thể cần phẫu thuật ở ca bệnh tối cấp.
◊ Khoảng 5% đến 50% bệnh nhân được điều trị bị tái phát sau khi ngưng điều trị, nhưng hầu hết đáp ứng với đợt điều trị thứ hai. Có thể khuyến nghị bổ sung vi sinh vật trong phân ở những bệnh nhân tái phát nhiều lần.
Thông tin cơ bản
Định nghĩa
Nhiễm trùng đại tràng do vi khuẩn Clostridium difficile gây ra. Có đặc trưng là tình trạng viêm đại tràng và hình thành giả mạc. Xảy ra ở những bệnh nhân có hệ vi khuẩn thường trú trong ruột bị rối loạn do sử dụng thuốc kháng sinh gần đây.
Còn gọi là viêm đại tràng giả mạc, nhiễm khuẩn Clostridium difficile (NKCD) hay bệnh do Clostridium difficile (BDCD). Chủ đề này chỉ bao gồm chẩn đoán và điều trị ở người lớn.
Viện Tiêu chuẩn Lâm sàng và Phòng thí nghiệm Hoa Kỳ đã công bố thay đổi danh pháp của tên loài từ Clostridium difficile sang Clostridioides difficile vào năm 2018; tuy nhiên, tên này vẫn chưa được chấp nhận rộng rãi.[1]
Dịch tễ học
Nhiễm khuẩn Clostridium difficile đã trở thành nguyên nhân thường gặp nhất gây nhiễm trùng liên quan đến chăm sóc y tế tại bệnh viện Hoa Kỳ, với ước tính là 500.000 ca nhiễm trùng và 29.000 ca tử vong (trong vòng 30 ngày kể từ lần chẩn đoán đầu tiên) trong số các bệnh nhân tại Hoa Kỳ trong một năm. Khoảng 65% ca bệnh có liên quan đến chăm sóc y tế (bao gồm viện dưỡng lão và các bệnh nhân đã đến cơ sở ngoại trú), nhưng chỉ 24% ca bệnh khởi phát trong khi ở bệnh viện. Tỷ lệ mắc mới các ca nhiễm trùng liên quan đến chăm sóc y tế là 92,8 trên 100.000 người, trong khi tỷ lệ mắc mới các ca nhiễm trùng có liên quan đến cộng đồng là 48,2 trên 100.000 người. Người da trắng, giới tính nữ và bệnh nhân từ 65 tuổi trở lên có tỷ lệ mắc mới các ca nhiễm trùng cao hơn.[4] Một nghiên cứu tiến cứu đã phát hiện ra rằng nhiễm khuẩn C difficile chiếm khoảng 10% bệnh nhân đến phòng cấp cứu với biểu hiện tiêu chảy và không nôn, và hơn một phần ba các bệnh nhân này không có các yếu tố nguy cơ nhiễm trùng truyền thống.
Dịch tễ học đã thay đổi vào những năm 2000 do sự xuất hiện của chủng thuộc điện di gel trường xung loại 1 độc hại hơn tại Bắc Mỹ (NAP1) (còn gọi là chủng dịch bệnh theo PCR định loại ribo 027).[6] [7] [8] Các đợt bùng phát xảy ra tại Bắc Mỹ, Anh Quốc, châu Âu và châu Á. Chủng NAP1 đã giảm tỷ lệ xuất hiện kể từ lần đầu tiên được phân lập, nhưng vẫn còn là một vấn đề nghiêm trọng tại Hoa Kỳ. Sự xuất hiện của chủng này có thể là kết quả của việc sử dụng rộng rãi fluoroquinolone.[9] Chủng NAP1 phổ biến hơn ở các ca nhiễm trùng liên quan đến chăm sóc y tế.[4]
Tỷ lệ tái phát được báo cáo là từ 5% đến 50%, mặc dù một nghiên cứu đã phát hiện rằng có ít nhất một lần tái phát ở 21% ca nhiễm trùng liên quan đến chăm sóc y tế và 14% ca nhiễm trùng liên quan đến cộng đồng.[4] Nguy cơ tái phát lần đầu tiên sau đợt nhiễm trùng đầu tiên là 25%, với nguy cơ tái phát lần thứ hai là 38%, nguy cơ tái phát lần thứ ba là 29%, và nguy cơ tái phát lần thứ tư là 27%. Nguy cơ nhiễm trùng nặng giảm theo mỗi lần tái phát sau đó.[10] Tỷ lệ tái nhiễm nhiều lần hàng năm đã tăng trong những năm gần đây. Các yếu tố nguy cơ của tái nhiễm bao gồm giới tính nữ, tuổi cao, bệnh thận mạn tính, chẩn đoán tại viện dưỡng lão và gần đây sử dụng corticosteroid hoặc thuốc ức chế bơm proton.[11]
Clostridium difficile gây ra 48% ca nhiễm trùng đường tiêu hóa liên quan đến chăm sóc y tế tại các bệnh viện chăm sóc cấp tính trên khắp châu Âu.[12] Tại Anh Quốc, đã có báo cáo về 5038 ca bệnh từ tháng Một, 2017 đến tháng Một, 2018 ở các bệnh nhân 2 tuổi trở lên (chỉ các ca bệnh được phân định đáng tin cậy).[13] Đã có báo cáo rằng tỷ lệ mắc mới ở châu Á tương tự tỷ lệ mắc mới ở châu Âu và Bắc Mỹ.[14]
Bệnh căn học
Thuốc kháng sinh phổ rộng làm phá vỡ hệ vi khuẩn thường trú trong ruột, các loại thuốc gây bệnh thường gặp nhất là ampicillin, cephalosporin, clindamycin, carbapenem và fluoroquinolone.[15]Clostridium difficile sinh sôi trên hệ vi khuẩn đường ruột bị rối loạn sau khi nuốt phải bào tử kháng nhiệt, chuyển đổi thành dạng sinh dưỡng trong đại tràng.
Lây truyền trong cơ sở y tế rất có thể là do lây lan trực tiếp qua đường phân – miệng (ví dụ: qua tay của nhân viên y tế), đồ vật có nguy cơ truyền bệnh cao (ví dụ: bô đi vệ sinh của bệnh nhân hoặc nhiệt kế trực tràng), hoặc tiếp xúc trực tiếp với môi trường nhiễm bệnh. Bệnh nhân có vi khuẩn cư trú không có triệu chứng cũng có thể góp phần lây lan bệnh.[2]
Sinh lý bệnh học
Thời gian ủ bệnh thường từ 2 đến 3 ngày, nhưng có thể là hơn một tuần.[2]Clostridium difficile là trực khuẩn gram dương, kỵ khí, hình thành bào tử, tạo ra các độc tố A và B. Những độc tố này gây ra phản ứng viêm ở ruột già, dẫn đến tăng tình trạng tăng tính thấu mao mạch và hình thành giả mạc.[3] Giả mạc tại đại tràng có đặc trưng phân biệt là các mảng màu vàng và trắng bám dính với niêm mạc bị viêm, và chứa bạch cầu trung tính, fibrin, chất nhầy và mảnh vụn tế bào.[3]
Độc tố A được coi là đóng vai trò quan trọng hơn độc tố B trong sinh bệnh học vì độc tố A được phát hiện thấy là gây ra tổn thương mô nặng hơn và tích tụ dịch trong các mẫu động vật thí nghiệm. Độc tố B được cho là đóng vai trò chỉ sau khi niêm mạc đại tràng đã bị độc tố A làm tổn thương.[3]
Tùy thuộc vào đáp ứng miễn dịch ở vật chủ và vào việc liệu chủng C difficile có sinh độc tố không, mà xảy ra tình trạng người mang mầm bệnh không có triệu chứng hoặc bệnh do C difficile. Người mang mầm bệnh không có triệu chứng ít có khả năng có bằng chứng hình thành độc tố.
Biểu hiện lâm sàng thường xảy ra vào các ngày từ 4 đến 9 trong quá trình điều trị kháng sinh, nhưng có thể xảy ra đến tối đa 8 tuần sau khi ngưng dùng thuốc kháng sinh.[16]
Bệnh nhân bị suy nhược có thể không tạo miễn dịch immunogammaglobulin với độc tố A.[16]
Phân loại
Giám sát ca bệnh
Khởi phát tại cơ sở y tế:
• Nhiễm khuẩn Clostridium difficile được xác định trên xét nghiệm xảy ra kéo dài hơn 3 ngày sau khi được tiếp nhận vào cơ sở (tức là vào ngày thứ 4 trở đi). Các cơ sở y tế cần theo dõi các ca bệnh này để phát hiện sự tăng số lượng các ca bệnh và bùng phát.
Khởi phát tại cộng đồng, có liên quan đến cơ sở y tế:
• Nhiễm khuẩn C difficile xảy ra trong vòng 28 ngày sau khi ra khỏi cơ sở y tế. Có liên quan đến cộng đồng:
• Nhiễm khuẩn C difficile ở bệnh nhân không có hồ sơ lưu trú qua đêm tại cơ sở y tế trong 12 tuần trước.
Phòng ngừa
Ngăn ngừa sơ cấp
Sử dụng thuốc kháng vi đúng cách và ngưng dùng chúng ngay khi có thể giúp làm giảm thay đổi về hệ vi khuẩn trong ruột, do đó có thể làm giảm nguy cơ mắc phải Clostridium difficile. Ngoài ra, sử dụng men vi sinh có thể hữu ích trong phòng ngừa ban đầu. Một nghiên cứu tổng quát và phân tích tổng hợp 31 thử nghiệm ngẫu nhiên có đối chứng (8672 bệnh nhân) đã phát hiện rằng có bằng chứng khá thuyết phục rằng men vi sinh an toàn và hiệu quả trong việc phòng ngừa tiêu chảy do C difficile khi sử dụng thuốc kháng sinh ở bệnh nhân không bị suy giảm miễn dịch hoặc bị suy k nặng.[32] Đã có phát hiện rằng việc cho dùng men vi sinh gần với liều thuốc kháng sinh đầu tiên làm giảm hơn 50% nguy cơ nhiễm khuẩn C difficile ở người lớn nhập viện. Tuy nhiên, hướng dẫn của Hoa Kỳ không khuyến nghị sử dụng men vi sinh để phòng ngừa bên ngoài phạm vi các ca thử nghiệm do không đủ dữ liệu.[2]
Tư vấn kiểm soát lây nhiễm và rửa tay bằng xà phòng và nước sẽ giúp ngăn ngừa lây nhiễm giữa các bệnh nhân. Tổ chức Y tế Thế giới đưa ra hướng dẫn về kỹ thuật rửa tay đúng cách. Đã có phát hiện rằng kỹ thuật rửa tay theo quy tắc có hiệu quả hơn kỹ thuật không theo quy tắc trong việc phòng ngừa C difficile.[34] [WHO: guidelines on hand hygiene] Bệnh nhân cần được chăm sóc kèm theo biện pháp phòng ngừa tiếp xúc trong ít nhất 48 tiếng sau khi tiêu chảy có tình trạng cải thiện.[35]
Vệ sinh môi trường trong các bệnh viện là cần thiết để phòng ngừa việc đưa vào hoặc lây lan mầm bệnh.[36] [37] Các thuốc giải phóng clo hiệu quả hơn chất tẩy trong việc tiêu diệt các bào tử do C difficile tạo ra.[38] [39] [40] Các thử nghiệm chỉ ra rằng hệ thống khử trùng bằng hydrogen peroxide dạng sương mù khô hiệu quả hơn dung dịch sodium hypochlorite 0,5% trong việc loại trừ bào tử C difficile, và nó được coi là phương pháp mới để khử trùng các phòng của bệnh nhân nhiễm khuẩn C difficile.[41]
Một phương pháp mới là công nghệ khử nhiễm phòng hoàn toàn tự động, linh hoạt, sử dụng chiếu xạ tia cực tím C để tiêu diệt mầm bệnh.[42] Mặc dù các chiến lược vệ sinh tăng cường được chứng tỏ là cải thiện tính đầy đủ và hiệu quả của việc vệ sinh, điều này đã không dẫn đến việc giảm tỷ lệ mắc mới của nhiễm khuẩn C difficile trong một thử nhiệm.[43]
Quản lý kháng sinh nên là yếu tố trọng tâm của các chương trình kiểm soát nhiễm khuẩn C difficile.[17] Các lợi ích của chương trình quản lý bao gồm giảm hiệu ứng bất lợi và cải thiện kết quả của bệnh nhân. Các khuyến nghị bao gồm:[2]
• Giảm thiểu tần suất và thời gian dùng thuốc kháng sinh nguy cơ cao, cũng như số lượng thuốc kháng sinh được kê đơn, để làm giảm nguy cơ nhiễm khuẩn C difficile
• Thực hiện chương trình quản lý thuốc kháng sinh
• Cân nhắc hạn chế fluoroquinolone, clindamycin và cephalosporin (ngoại trừ dự phòng trong phẫu thuật).
Một phân tích tổng hợp đã phát hiện ra rằng các chương trình quản lý đã chứng minh là làm giảm đáng kể tỷ lệ mắc mới C difficile đến 32% ở các bệnh nhân nội trú, và hiệu quả hơn khi được thực hiện với các biện pháp kiểm soát lây nhiễm.[18]
Không có đủ bằng chứng để khuyến nghị ngưng dùng thuốc ức chế bơm proton nhằm ngăn ngừa nhiễm khuẩn C difficile; tuy nhiên, cần ngưng dùng chúng nếu không cần thiết.[2]
Ngăn ngừa thứ cấp
Cần thận trọng khi sử dụng thuốc kháng sinh được biết là gây ra (hoặc nghi ngờ gây ra) nhiễm khuẩn Clostridium difficile (ví dụ: ampicillin, cephalosporin, clindamycin, carbapenem và fluoroquinolone), đặc biệt ở các nhóm bệnh nhân cụ thể (ví dụ như người già, bệnh nhân nhập viện và bệnh nhân ức chế miễn dịch). Cần tuân thủ nghiêm ngặt quy trình rửa tay.
Các chiến lược biện pháp dự phòng cấp 2 (ví dụ: men vi sinh, dự phòng vancomycin hoặc fidaxomicin) ở bệnh nhân cần điều trị kháng sinh cho một chỉ định khác sau khi điều trị C difficile chưa được nghiên cứu trong các thử nghiệm ngẫu nhiên có đối chứng.
Chẩn đoán
Tiền sử ca bệnh
Tiền sử ca bệnh #1
Một người đàn ông da trắng 72 tuổi có tiền sử 5 ngày đau bụng, buồn nôn, tiêu chảy nặng, sốt và mệt mỏi. Ông đã được bắt đầu cho dùng levofloxacin để điều trị viêm phổi cộng đồng 2 tuần trước khi các triệu chứng ở phổi có cải thiện. Thăm khám thấy sốt 38,3°C (101°F) và chướng bụng nhẹ với cảm giác đau khi chạm vào ở mức tối thiểu. Xét nghiệm trong phòng thí nghiệm cho thấy số lượng bạch cầu ngoại vi là 12.000/mm³ và xét nghiệm máu ẩn guaiac phân cho kết quả dương tính nhẹ.
Các bài trình bày khác
Các triệu chứng có thể từ tiêu chảy nhẹ xảy ra một lần cho đến liên tục, nhiều nước kèm theo đau bụng nặng và số lượng tế bào bạch cầu (WBC) ngoại vi cao. Viêm đại tràng đe dọa tính mạng có thể xảy ra, đặc biệt ở người cao tuổi. Tăng đột ngột số lượng TBBC ở bệnh nhân bị tiêu chảy và tiền sử gần đây có dùng thuốc kháng sinh có thể là chỉ báo viêm đại tràng tối cấp sắp xảy ra.
Cách tiếp cận chẩn đoán từng bước
Chẩn đoán dựa trên việc lấy tiền sử chính xác, khám thực thể và xác nhận qua xét nghiệm phù hợp. Cần cân nhắc chẩn đoán ở bệnh nhân có tiền sử gần đây dùng thuốc kháng sinh và có biểu hiện tiêu chảy. Chỉ nên xét nghiệm ở những bệnh nhân bị tiêu chảy không rõ nguyên nhân, khởi phát lần đầu tiên (được xác định là từ 3 lần đại tiện không thành khuôn trong vòng 24 giờ). Khuyến nghị xét nghiệm phân tử đơn độc hoặc là một phần của phương cách đa bước tùy thuộc vào phác đồ của cơ sở địa phương.
Tiền sử
Các bệnh nhân cao tuổi, có tiền sử gần đây sử dụng thuốc kháng sinh, có bệnh lý kèm theo (ví dụ: bệnh viêm ruột, bệnh thận mạn tính, nhiễm HIV), nằm viện kéo dài, sống tại viện dưỡng lão, có tiền sử dùng thuốc ức chế a-xít, có tiền sử ghép tạng đặc hoặc ghép tế bào gốc tạo máu, hoặc có tiền sử bị bệnh do Clostridium đặc biệt có nguy cơ. Các thuốc kháng sinh thường gặp nhất bao gồm ampicillin, cephalosporin, clindamycin, carbapenem và fluoroquinolone, đặc biệt là trong 3 tháng trước.[15] [16] Các bệnh nhân thường có biểu hiện sốt, tiêu chảy, đau bụng, buồn nôn hoặc nôn.
Khám lâm sàng
Có thể biểu hiện từ cảm giác đau nhẹ hay không tăng cảm giác vùng bụng cho đến các dấu hiệu của đau bụng cấp tính.
Các triệu chứng toàn thân của sốc bao gồm hạ huyết áp và nhịp tim nhanh, kèm theo đau bụng nặng và cảm giác đau khi chạm vào cho thấy nguy cơ viêm đại tràng tối cấp. Bệnh tối cấp được xác định là ca nhiễm khuẩn C difficile nặng có biến chứng kèm theo nguy cơ tử vong cao.
Các xét nghiệm ban đầu
Cần thực hiện xét nghiệm công thức máu có phân biệt trong đánh giá ban đầu, thường chỉ ra tăng bạch cầu. Nếu số lượng bạch cầu rất cao (30.000 đến 50.000/mm³), bệnh nhân có nguy cơ viêm đại tràng tối cấp.
Cần chụp X-quang vùng bụng ở bệnh nhân bị chướng bụng hoặc có các triệu chứng và dấu hiệu cho thấy nguy cơ nhiễm khuẩn. Điều này có thể chỉ ra tình trạng giãn đại tràng.[16]
Cần lấy mẫu phân trong xét nghiệm ban đầu và kiểm tra sự xuất hiện của máu ẩn trong phân.
Phân biệt giữa nhiễm khuẩn C difficile và tình trạng cư trú của vi khuẩn C difficile là một thách thức trong chẩn đoán, và hiện đang thiếu sự đồng thuận về phương pháp chẩn đoán tốt nhất. Các xét nghiệm phát hiện chính vi sinh vật (tức là xét nghiệm khuếch đại axit nucleic [NAATs], như phản ứng chuỗi polymerase đối với mẫu phân, thử nghiệm miễn dịch enzym glutamate dehydrogenase [GDH], hoặc nuôi cấy vi khuẩn tạo độc tố) hoặc các độc tố chính (tức là thử nghiệm miễn dịch enzym độc tố A và B, xét nghiệm trung hòa khả năng nhiễm độc tế bào bằng nuôi cấy tế bào) trực tiếp trong phân. Xét nghiệm phân tử, phương pháp chẩn đoán thường gặp nhất, không phân biệt giữa nhiễm khuẩn và tình trạng cư trú của vi khuẩn. Xét nghiệm này có độ nhạy cao và độ đặc hiệu thấp/trung bình. Do đó, vì lợi ích của quản lý chẩn đoán tốt, khuyến cáo chỉ nên xét nghiệm cho các bệnh nhân bị tiêu chảy không rõ nguyên nhân, khởi phát lần đầu tiên (được xác định là 3 lần đại tiện không thành khuôn trong vòng 24 giờ) và đang không dùng thuốc nhuận tràng; tuy nhiên, khuyến cáo này dựa trên bằng chứng rất kém thuyết phục. Nếu nhân viên bệnh viện và phòng thí nghiệm thống nhất về tiêu chuẩn lấy mẫu phân này, khuyến cáo dùng đơn độc xét nghiệm NAATs là phương pháp chẩn đoán có độ nhạy cao nhất cho các mẫu phân từ các bệnh nhân có nguy cơ nhiễm khuẩn C difficile dựa vào các triệu chứng lâm sàng. Tuy nhiên, nếu không có thống nhất trước về tiêu chuẩn gửi mẫu phân của bệnh nhân, thì khuyến cáo xét nghiệm độc tố trong mẫu phân như một phần của phương cách đa bước (ví dụ như GDH kết hợp với độc tố; GDH kết hợp với độc tố, được đánh giá bởi xét nghiệm NAAT; hoặc xét nghiệm NAAT kết hợp với độc tố) hơn là một mình xét nghiệm . Không nên lặp lại xét nghiệm trong vòng 7 ngày trong cùng đợt tiêu chảy, và không nên xét nghiệm cho các bệnh nhân không có triệu chứng.[2]
Hướng dẫn của châu Âu khuyến nghị phương cách hai buớc, bắt đầu với xét nghiệm có độ nhạy cao (ví dụ: xét nghiệm NAAT, hoặc xét nghiệm miễn dịch enzym để phát hiện GDH) và nếu dương tính, xác nhận bằng xét nghiệm có độ đặc hiệu cao (xét nghiệm miễn dịch enzym để phát hiện độc tố A/B). Ngoài ra, có thể sàng lọc các mẫu bằng cả xét nghiệm miễn dịch enzym để phát hiện GDH và độc tố A/B.
Các xét nghiệm tiếp theo
Chỉ định nội soi đại tràng sigma hoặc nội soi đại tràng nếu điều trị thất bại, hoặc ở bệnh nhân có xét nghiệm miễn dịch enzym âm tính, hoặc nếu nghi ngờ các nguyên nhân khác viêm đại tràng do thiếu máu cục bộ.
Chỉ định chụp cắt lớp vi tính vùng bụng ở bệnh nhân bị chướng bụng, cơn đau nặng hơn, hoặc không có âm nhu động ruột.
Xét nghiệm mới
Các chất chỉ điểm trong phân như calprotectin và lactoferrin, ngày càng được sử dụng để phân biệt giữa các nguyên nhân gây ra tiêu chảy do tình trạng viêm và các nguyên nhân không do tình trạng viêm. Không có đủ bằng chứng để khuyến nghị sử dụng các chất chỉ điểm sinh học này trong việc chẩn đoán nhiễm khuẩn C difficile tại thời điểm này.[2]
Các yếu tố nguy cơ
Mạnh
Dùng thuốc kháng sinh
• Các thuốc kháng sinh thường gặp nhất có liên quan là ampicillin, cephalosporin, clindamycin, carbapenem và fluoroquinolone, đặc biệt là trong 3 tháng trước.
• Hạn chế sử dụng fluoroquinolone có vẻ làm giảm tỷ lệ mắc mới nhiễm khuẩn Clostridium difficile tại nước Anh. Quản lý kháng vi sinh vật cần là yếu tố trọng tâm của các chương trình kiểm soát nhiễm khuẩn C difficile.[17] Một phân tích tổng hợp đã phát hiện ra rằng các chương trình quản lý đã chứng minh là làm giảm đáng kể tỷ lệ mắc mới C difficile đến 32% ở các bệnh nhân nội trú, và hiệu quả hơn khi được thực hiện với các biện pháp kiểm soát lây nhiễm.[18]
Cao tuổi
• Bệnh nhân tuổi cao tăng nguy cơ nhiễm khuẩn C difficile
Nhập viện hoặc sống tại viện dưỡng lão
• Nhiễm khuẩn C difficile là nguyên nhân thường gặp nhất của tiêu chảy tại bệnh viện ở người lớn.
• Người mang C difficile sinh độc tố làm tăng nguy cơ nhiễm khuẩn ở các bệnh nhân khác tại bệnh viện.[19] Nguy cơ nhiễm khuẩn tăng theo thời gian nằm viện.
Tiền sử mắc bệnh do Clostridium difficile
• Tỷ lệ tái phát được báo cáo là từ 5% đến 50%, mặc dù một nghiên cứu đã phát hiện rằng có ít nhất một lần tái phát ở 21% ca nhiễm trùng liên quan đến chăm sóc y tế và 14% ca nhiễm trùng liên quan đến cộng đồng.[4]
• Một số lượng nhỏ bệnh nhân bị tái phát nhiều lần, đòi hỏi phải có nhiều lần điều trị, hoặc thử nghiệm liều xung hoặc giảm dần vancomycin.[15]
Sử dụng thuốc ức chế a-xít
• Thuốc ức chế bơm proton có liên quan đến việc tăng nguy cơ nhiễm khuẩn C difficile. Cũng có thể thấy ảnh hưởng khi dùng chất đối kháng thụ thể H2.
Bệnh viêm ruột
• Bệnh nhân mác bệnh viêm ruột tăng nguy cơ nhiễm khuẩn C difficile nguyên phát và bệnh tái phát, cũng như tăng tỷ lệ mắc bệnh và tỷ lệ tử vong do nhiễm khuẩn.
Người nhận ghép tạng đặc
• Tỷ lệ nhiễm khuẩn C difficile cao hơn 5 lần ở nhóm đối tượng này so với bệnh nhân nội khoa nói chung.
Người nhận ghép tế báo gốc tạo máu
• Tỷ lệ nhiễm khuẩn C difficile cao hơn 9 lần trong nhóm đối tượng này so với bệnh nhân nhập viện nói chung.
Bệnh thận mạn tính (CKD)
• Tỷ lệ nhiễm khuẩn C difficile cao hơn từ 2 đến 2,5 lần ở nhóm đối tượng này, tăng nguy cơ ở bệnh nhân bị bệnh thận giai đoạn cuối.[28]
Nhiễm HIV
• Bệnh nhân tăng nguy cơ do bệnh ức chế miễn dịch có sẵn, tiếp xúc với cơ sở y tế và thuốc kháng sinh, hoặc kết hợp các yếu tố này.[29]
Yếu
Thuốc ức chế miễn dịch hoặc hóa trị liệu
• Kết hợp giữa sử dụng thuốc ức chế miễn dịch và mắc bệnh trạng.[30]
Phẫu thuật dạ dày – ruột
• Liên quan giữa phẫu thuật dạ dày – ruột
Các yếu tố về tiền sử và thăm khám
Các yếu tố chẩn đoán chủ yếu
Có các yếu tố nguy cơ (thường gặp)
• Các yếu tố nguy cơ chính bao gồm dùng thuốc kháng sinh, tuổi cao, nhập viện hoặc cư trú tại viện dưỡng lão, và tiền sử bị bệnh do Clostridium difficile.
Tiêu chảy (thường gặp)
• Có thể từ phân lỏng đến tiêu chảy nặng; không có tiêu chảy có thể có liên quan đến phình đại tràng nhiễm độc hoặc bệnh liệt ruột.
Đau bụng (thường gặp)
• Có thể nhẹ hoặc không , nhưng có thể nặng, đặc biệt ở trường hợp viêm đại tràng tối cấp.
Các yếu tố chẩn đoán khác
Sốt (thường gặp)
• Có thể ở cấp độ thấp trong các ca bệnh nhẹ.
Tăng cảm giác đau vùng bụng (thường gặp)
• Thường xuất hiện, đặc biệt ở vùng bụng dưới.
Buồn nôn và nôn mửa (không thường gặp)
• Có thể không .
Chướng bụng (không thường gặp)
• Có thể không .
Các triệu chứng của sốc (không thường gặp)
• Các triệu chứng toàn thân của sốc bao gồm hạ huyết áp và nhịp tim nhanh, kèm theo đau bụng nặng và tăng cảm cho thấy nguy cơ viêm đại tràng tối cấp.
Xét nghiệm chẩn đoán
Xét nghiệm thứ nhất cần yêu cầu
| Xét nghiệm Kết quả | |
| Công thức máu
• Được chỉ định định kỳ. Xét nghiệm không nhạy và không đặc hiệu. Xét nghiệm không loại trừ chẩn đoán nếu kết quả bình thường. • Có thể cao đến 30.000 đến 50.000/mm³ trong trường hợp viêm đại tràng tối cấp. |
Tăng tế bào bạch cầu () |
| Xét nghiệm dựa trên guaiac đối với mẫu phân (xét nghiệm máu ẩn trong phân)
• Được thực hiện thường xuyên để loại trừ các chẩn đoán phân biệt. Các kết quả thường dương tính, nhưng kết quả dương tính không đặc hiệu chẩn đoán. |
dương tính đối với máu ẩn |
| CPR mẫu phân
• Được khuyến cáo là xét nghiệm duy nhất nếu nhân viên bệnh viện và phòng thí nghiệm thống nhất về tiêu chuẩn gửi mẫu phân sau đây: tiêu chảy không rõ nguyên nhân, khởi phát lần đầu tiên (được xác định là 3 lần đại tiện không thành khuôn trở lên trong vòng 24 giờ) ở bệnh nhân đang không dùng thuốc nhuận tràng.[2] • Được khuyến nghị như một phần của phương cách đa bước nếu không có đồng thuận trước về tiêu chuẩn gửi mẫu phân của bệnh nhân.[44] [2] • Độ nhạy cao và độ đặc hiệu thấp/trung bình. |
dương tính |
| Xét nghiệm miễn dịch phân để phát hiện glutamate dehydrogenase
• Phát hiện sự xuất hiện của Clostridium difficile trong ruột mặc dù nó không xác nhận tình trạng nhiễm khuẩn. • Được khuyến nghị như một phần của phương cách đa bước nếu không có đồng thuận trước về tiêu chuẩn gửi mẫu phân của bệnh nhân.[44] [2] |
dương tính |
| Xét nghiệm mẫu phân để phát hiện độc tố A và B
• Được khuyến nghị như một phần của phương cách đa bước nếu không có đồng thuận trước về tiêu chuẩn gửi mẫu phân của bệnh nhân • Kết quả có trong vòng vài giờ với độ nhạy từ 65% đến 85% và độ đặc hiệu từ 95% đến 100%.[3] • Có thể được lặp lại tối đa 3 lần để cải thiện độ nhạy, mặc dù bằng chứng của việc lặp lại xét nghiệm hấp thụ miễn dịch liên kết với enzym (ELISA) là không nhất quán.[45] |
dương tính |
| Chụp x-quang bụng
• Được chỉ định nếu bị chướng bụng rõ rệt. |
không khí trong ruột, giãn đại tràng |
Các xét nghiệm khác cần cân nhắc
| Xét nghiệm Kết quả | |
| thử nghiệm trung hòa khả năng nhiễm độc tế bào bằng nuôi cấy tế bào
• Được chỉ định nếu có bùng phát hoặc các ca bệnh cần được theo dõi về mặt dịch tễ học. • Kết quả có thể không có trong khoảng thời gian lên tới 48 giờ. • Xét nghiệm có độ nhạy từ 80% đến 90% và độ đặc hiệu từ 99% đến 100%.[3] |
dương tính đối với khả năng nhiễm độc tế bào |
| Xét nghiệm Kết quả | |
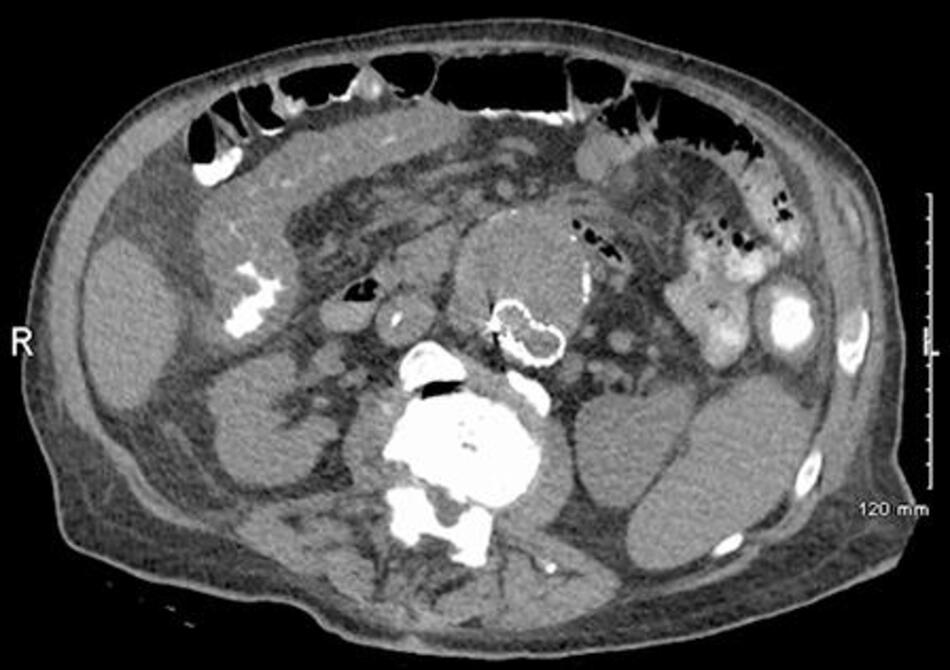
| Chụp CT bụng
• Được chỉ định nếu bệnh nhân bị chướng bụng, cơn đau nặng hơn hoặc mất nhu động ruột. |
giãn đại tràng và dày đại tràng lan tỏa |
| Nội soi đại tràng sigma hoặc nội soi đại tràng
• Loét và hình thành giả mạc được chẩn đoán |
giả mạc ở đại tràng và viêm đại tràng |
Các xét nghiệm giai đoạn đầu
| Xét nghiệm Kết quả | |
| lactoferrin hoặc calprotectin trong phân
• Các chất chỉ điểm trong phân ngày càng được sử dụng để phân biệt giữa các nguyên nhân gây ra tiêu chảy do tình trạng viêm và các nguyên nhân không do tình trạng viêm. Không có đủ bằng chứng để khuyến nghị sử dụng các chất chỉ điểm sinh học này trong việc chẩn đoán nhiễm khuẩn C difficile tại thời điểm này.[2] |
Tăng |
Chẩn đoán khác biệt
| Tình trạng | Các dấu hiệu/triệu chứng khác biệt | Các xét nghiệm khác biệt |
| Tiêu chảy do thuốc kháng sinh (TCDTKS) | • TCDTKS bao gồm tiêu chảy thẩm thấu do dùng thuốc kháng sinh. Biểu hiện buồn nôn và tiêu chảy. Không có sốt. | • Tất cả các xét nghiệm đều nằm trong giới hạn bình thường. Xét nghiệm phát hiện độc tố của Clostridium difficile âm tính. |
| Viêm đại tràng do thiếu máu cục bộ | • Tiền sử đột quỵ, hạ huyết áp, suy tim, đái tháo đường hoặc phơi nhiễm phóng xạ vùng bụng. Các triệu chứng bao gồm tiêu chảy ra máu, đau bụng, nôn và sốt. | • Nội soi đại tràng cho thấy viêm bề mặt niêm mạc hoặc loét do thiếu máu cục bộ. Chụp mạch máu chỉ ra tình trạng gián đoạn lưu lượng động mạch. |
| Viêm dạ dày-ruột do vi-rút hoặc vi khuẩn | • Tiền sử đi lại, ăn thức ăn bị nhiễm bẩn, hoặc các thành viên gia đình cũng bị ốm.
• Có thể có tiền sử đại tiện ra máu. |
• Nuôi cấy máu cũng như phân để phát hiện nhiễm khuẩn xâm lấn cho kết quả dương tính. |
| Bệnh viêm ruột | • Tiêu chảy mạn tính có thể có máu kèm biểu hiện ngoài ruột. | • Nội soi đại tràng hoặc bệnh lý gợi ý nguy cơ bệnh viêm ruột. |
Các tiêu chí chẩn đoán
Xác định ca bệnh
Định nghĩa về ca bệnh được khuyến nghị giám sát yêu cầu:
• Xuất hiện tiêu chảy hoặc bằng chứng phình đại tràng hoặc liệt ruột nặng; và
• Kết quả xét nghiệm chẩn đoán trong phòng thí nghiệm dương tính hoặc bằng chứng giả mạc khi nội soi hoặc xét nghiệm mô bệnh học.
Ca mắc bệnh mới:
• Đợt khởi phát triệu chứng nguyên phát mới (không có đợt khởi phát triệu chứng với kết quả dương tính trong 8 tuần trước) và kết quả xét nghiệm dương tính.
Ca bệnh tái phát:
• Đợt khởi phát triệu chứng và kết quả thử nghiệm dương tính sau đợt mắc bệnh trong 2 đến 8 tuần trước.
Điều trị
Cách tiếp cận điều trị từng bước
Mục tiêu chính của điều trị là ngưng dùng thuốc kháng vi sinh vật được chỉ định và bắt đầu điều trị phù hợp.
Cần nhập viện cho tất cả bệnh nhân chưa được nhập viện trừ khi họ không có triệu chứng toàn thân và rối loạn chức năng cơ quan, trong trường hợp này, có thể điều trị các bệnh nhân nhân này như bệnh nhân ngoại trú. Hầu hết các khuyến nghị trong phần này dựa trên các hướng dẫn của Hiệp hội Bệnh truyền nhiễm Hoa Kỳ (IDSA)/Hiệp hội Dịch tễ học Y tế Hoa Kỳ (SHEA) đã được công bố vào đầu năm 2018.
Phòng ngừa và kiểm soát nhiễm khuẩn
Cần cách ly các bệnh nhân nhập viện được xác nhận hoặc nghi ngờ nhiễm khuẩn trong phòng riêng với nhà vệ sinh riêng để giảm nguy cơ lây nhiễm các bệnh nhân khác. Tại các cơ sở có số lượng phòng riêng hạn chế, cần ưu tiên cho các bệnh nhân bị đại tiện không tự chủ. Điều quan trọng là cần áp dụng các biện pháp phòng ngừa khi tiếp xúc với các bệnh nhân nghi ngờ nhiễm khuẩn trước khi có kết quả xét nghiệm. Cần tiếp tục sử dụng các biện pháp phòng ngừa khi tiếp xúc trong ít nhất 48 giờ sau khi tiêu chảy cải thiện, và cho đến khi xuất viện nếu tỷ lệ nhiễm khuẩn Clostridium difficile vẫn cao.
Các chuyên gia y tế cần mặc áo choàng và đeo găng tay khi bước vào phòng khi chăm sóc cho bệnh nhân. Cần vệ sinh tay trước và sau khi tiếp xúc với bệnh nhân và sau khi tháo găng tay. Cần sử dụng xà phòng và nước hoặc sản phẩm chứa cồn.
Cần khuyến khích bệnh nhân rửa tay và tắm vòi sen để giảm tải lượng bào tử trên da. Ưu tiên dùng thiết bị dùng một lần cho bệnh nhân nếu sẵn có (không khuyến nghị nhiệt kế trực tràng).[2]
Tổ chức Y tế Thế giới đưa ra hướng dẫn về kỹ thuật rửa tay đúng cách. Đã có phát hiện rằng kỹ thuật rửa tay theo quy tắc có hiệu quả hơn kỹ thuật không theo quy tắc trong việc phòng ngừa C difficile.[34] [WHO: guidelines on hand hygiene]
Ngưng dùng thuốc gây bệnh
Đề xuất đầu tiên của chẩn đoán là ngưng dùng (các) thuốc kháng sinh kích thích ngay khi có thể.[2]nbspNếu không thể ngưng dùng thuốc kháng sinh, thì nên thay thế bằng một loại thuốc kháng sinh ít có nguy cơ gây nhiễm khuẩn C difficile hơn. Cụ thể, cần tránh dùng ampicillin, cephalosporin, clindamycin, carbapenem và fluoroquinolone.
Chăm sóc hỗ trợ
Đầu tiên cần đánh giá bệnh nhân về tình trạng dịch, đặc biệt nếu bệnh nhân nằm viện. Nếu cần, nên bắt đầu bù nước và bổ sung điện giải. Sử dụng các thuốc kháng nhu động, bao gồm opioid và loperamide, mặc dù không có bằng chứng hỗ trợ khuyến cáo này.
Điều trị kháng sinh
Cần bắt đầu điều trị kháng sinh theo kinh nghiệm nếu có nguy cơ trì hoãn đáng kể (>48 giờ) kết quả xét nghiệm hoặc nhiễm khuẩn tối cấp. Đối với các bệnh nhân khác, có thể bắt đầu điều trị kháng sinh sau khi chẩn đoán để giới hạn việc lạm dụng thuốc kháng sinh. Phác đồ khuyến cáo dựa trên mức độ nghiêm trọng của bệnh và liệu đợt bệnh này là đợt đầu tiên hay tái phát.
Hướng dẫn của Hoa Kỳ khuyến cao dùng vancomycin hay fidaxomicin qua đường uống là lựa chọn đầu tiên để điều trị đợt nhiễm khuẩn C difficile đầu tiên. Trước đây, metronidazole đường uống là thuốc kháng sinh được lựa chọn; tuy nhiên, hiện nay thuốc này chỉ được khuyến nghị tại các cơ sở có hạn chế trong việc tiếp cận với thuốc bậc một.[2]
Đợt đầu tiên: không nghiêm trọng
• Dữ liệu lâm sàng hỗ trợ: tăng bạch cầu với số lượng bạch cầu ≤15.000 tế bào/mL và creatinine huyết thanh <0,13 mmol/l (<1,5 mg/dL)
• Điều trị bậc 1: vancomycin hoặc fidaxomicin đường uống trong 10 ngày
• Phương án điều trị thay thế: metronidazole qua đường uống trong 10 ngày Khởi phát ban đầu: nặng
• Dữ liệu lâm sàng hỗ trợ: tăng bạch cầu với số lượng bạch cầu ≥15.000 tế bào/mL và creatinine huyết thanh >0,13 mmol/l (>1,5 mg/dL)
• Điều trị bậc 1: vancomycin hoặc fidaxomicin đường uống trong 10 ngày Khởi phát đầu tiên: tối cấp (nặng, nhiễm khuẩn có biến chứng)
• Dữ liệu lâm sàng hỗ trợ: hạ huyết áp, sốc, liệt hoặc phình đại tràng
• Điều trị bậc 1 vancomycin qua đường uống (ở liều cao hơn liều điều trị nhiễm khuẩn tối cấp). Nếu bị liệt ruột, có thể cân nhắc đặt vancomycin trực tràng. Cần cho dùng metronidazole qua đường tĩnh mạch kèm theo vancomycin qua đường uống hoặc trực tràng, đặc biệt nếu bị liệt ruột vì có thể ảnh hưởng đến việc cung cấp vancomycin qua đường uống đến trực tràng
• Phương án điều trị thay thế: tigecycline hoặc globulin miễn dịch đã được sử dụng ở bệnh nhân không đáp ứng với điều trị bậc 1, nhưng chưa có thử nghiệm có đối chứng.
Hướng dẫn quốc tế vẫn có thể khuyến nghị cho dùng metronidazole như thuốc bậc 1 cho bệnh không nặng. Ví dụ, hướng dẫn của châu Âu vẫn còn khuyến cáo dùng metronidazole làm thuốc bậc 1 để điều trị bệnh không nặng (với vancomycin hoặc fidaxomicin làm phương án điều trị thay thế), và vancomycin làm thuốc bậc 1 cho bệnh nặng.[46] Cơ quan Y tế Công cộng Anh tại Anh Quốc cũng ủng hộ những khuyến nghị này. Công bố những hướng dẫn này xảy ra trước khi các hướng dẫn IDSA/SHEA được công bố vào đầu năm 2018. Cần phải tham khảo khuyến cáo tại địa phương.
Một phân tích gộp cũng cho thấy bằng chứng thuyết phục nhất chỉ ra là fidaxomicin tốt hơn hẳn so với vancomycin trong việc chữa khỏi triệu chứng lâu dài (được xác định bằng số bệnh nhân khỏi tiêu chảy trừ đi số bệnh nhân bị tái phát hoặc tử vong) ở người lớn bị nhiễm tái phát không có sự nhân lên của vi khuẩn. Vì vậy, nó được xem là lựa chọn điều trị tốt hơn vancomycin ở tất cả bệnh nhân ngoại trừ những người bị nhiễm trùng nặng. Tỷ lệ chữa khỏi bằng metronidazole thấp hơn đáng kể so với vancomycin và fidaxomicin.[48]
Một đánh giá Cochrane đã phát hiện ra bằng chứng khá thuyết phục gợi ý vancomycin ưu việt hơn metronidazole, và fidaxomicin ưu việt hơn vancomycin, để chữa khỏi triệu chứng ở bệnh nhân nhiễm khuẩn C difficile, mặc dù khác biệt về tính hiệu lực không quá lớn. Không thể đưa ra kết luận chắc chắn về hiệu quả của điều trị kháng sinh trong trường hợp bệnh nặng vì hầu hết các nghiên cứu loại trừ những bệnh nhân này. Không thể rút ra kết luận về sự cần thiết phải điều trị kháng sinh ở bệnh nhân nhiễm khuẩn nhẹ, ngoài ngừng thuốc kháng sinh gây bệnh, do thiếu nhóm chứng không điều trị trong đánh giá. Dữ liệu cho thấy fidaxomicin có thể hiệu quả trong việc điều trị nhiễm khuẩn C difficile nhẹ đến vừa, và thuốc này ưu việt hơn vancomycin đường uống trong việc duy trì đáp ứng lâm sàng và giảm tái phát.
Vancomycin hoặc fidaxomicin là thuốc ưa dùng ở những bệnh nhân đang mắc bệnh viêm ruột . Những bệnh nhân này cũng thường cần phải nhập viện để kiểm soát tích cực. Cần đưa ra quyết định dừng hoặc tiếp tục thuốc ức chế miễn dịch ở bệnh nhân bị bệnh viêm ruột trong đợt nhiễm khuẩn cấp tính theo từng ca bệnh
Nitazoxanide và a-xít fusidic có thể hiệu quả trong việc điều trị đợt nhiễm khuẩn C difficile đầu tiên, nhưng có ít dữ liệu hỗ trợ. Không có bằng chứng ủng hộ việc sử dụng rifaximin, tigecycline hoặc bacitracin để điều trị đợt khởi phát đầu tiên.
Phẫu thuật
Có thể cần đến phẫu thuật trong trường hợp bệnh tối cấp ở những bệnh nhân không đáp ứng với điều trị kháng sinh. Bệnh tối cấp không được đánh giá như là bệnh đe dọa tính mạng vì thiếu nhận thức về mức độ nghiêm trọng của bệnh và hội chứng lâm sàng không cụ thể. Chẩn đoán và điều trị sớm là thiết yếu để có kết quả tốt, và cần cân nhắc can thiệp sớm bằng phẫu thuật ở bệnh nhân không đáp ứng với điều trị thuốc hoặc những người đã tăng số lượng tế bào bạch cầu hoặc nồng độ lactate. Thủ thuật phẫu thuật lựa chọn là cắt bỏ một phần đại tràng kèm theo bảo tồn trực tràng. Mở thông hồi tràng có chuyển hướng đoạn ruột (với rửa dạ dày, sau đó là rửa thuận chiều bằng vancomycin) là một phương pháp thay thế.[2]
Nhiễm trùng tái phát
Tỷ lệ tái phát được báo cáo là từ 5% đến 50%, mặc dù một nghiên cứu đã phát hiện rằng có ít nhất một lần tái phát ở 21% ca nhiễm trùng liên quan đến chăm sóc y tế và 14% ca nhiễm trùng liên quan đến cộng đồng.[4] Khoảng 25% bệnh nhân đuợc điều trị bằng vancomycin cho đợt đầu tiên bị ít nhất một đợt tái phát.[60] [50]
Lựa chọn điều trị tùy thuộc vào điều trị được sử dụng cho đợt đầu tiên. Có thể điều trị đợt tái phát đầu tiên bằng các phác đồ kháng sinh sau:[2]
• Một phác đồ liều giảm dần và liều xung vancomycin qua đường uống (nếu vancomycin qua đường uống đã được sử dụng cho đợt đầu tiên)
• Một đợt điều trị tiêu chuẩn 10 ngày bằng fidaxomicin (nếu vancomycin qua đường uống đã được sử dụng cho đợt đầu tiên)
• Một đợt điều trị tiêu chuẩn 10 ngày bằng vancomycin qua đường uống (nếu metronidazole đã được sử dụng cho đợt đầu tiên).
Các nghiên cứu đã cho thấy có thể giảm tái phát ở bệnh nhân bằng chủng thuộc điện di trường xung loại 1 không phải B1 được cách ly từ người ở Bắc Mỹ khi được điều trị bằng fidaxomicin so với vancomycin.
Có thể điều trị các đợt tái phát sau đó bằng các phác đồ kháng sinh sau đây:[2]
• Một phác đồ vancomycin đường uống liều giảm dần và liều xung
• Một đợt điều trị tiêu chuẩn 10 ngày bằng vancomycin qua đường uống, sau đó là rifaximin trong 20 ngày
• Một đợt tiêu chuẩn 10 ngày bằng fidaxomicin.
Ghép vi sinh vật trong phân (GVSVTP) là một tùy chọn ở những bệnh nhân tái phát ít nhất hai lần và đã thất bại trong điều trị kháng sinh.[2] Thủ thuật bao gồm ghép phân đã được xử lý từ người hiến tặng khỏe mạnh vào đường ruột của bệnh nhân nhiễm khuẩn để khắc phục tình trạng mất cân bằng hệ khuẩn ruột. Có thể sử dụng một đợt vancomycin trong thời gian ngắn để giảm tải lượng C difficile ở những bệnh nhân đang không được điều trị kháng sinh trước khi nhận GVSVTP theo kế hoạch.
Các thử nghiệm ngẫu nhiên có đối chứng đã chứng minh tỷ lệ thành công cao. Một nghiên cứu tổng quát về các thử nghiệm ngẫu nhiên có đối chứng đã phát hiện rằng có bằng chứng khá thuyết phục chỉ ra rằng GVSVTP hiệu quả hơn vancomycin hoặc giả dược. GVSVTP dạng đóng băng hiệu quả như GVSVTP dạng tươi trong việc đạt được tình trạng cải thiện của tiêu chảy, và cung cấp qua đường tiêu hóa dưới có thể hiệu quả hơn cung cấp qua đường tiêu hóa trên.GVSVVTP có thể dung nạp tốt, nhưng các tác dụng bất lợi có thể bao gồm sốt, tăng cảm giác vùng bụng hoặc khó chịu, đầy hơi, buồn nôn/nôn, tiêu chảy/táo bón và nhiễm khuẩn. Các hậu quả dài hạn còn chưa rõ.
Không có đủ bằng chứng để khuyến nghị GVSVTP cho bệnh nặng, và phương pháp này có thể kém hiệu quả hơn trong việc loại bỏ nhiễm khuẩn C difficile ở bệnh nhân bị bệnh viêm ruột. Cần tiến hành thêm nghiên cứu về điều trị này vì ít có báo cáo về các thành phần chính của can thiệp bằng GVSVTP.[70]
Bezlotoxumab, một kháng thể đơn dòng ở người gắn kết độc tố B của C difficile, được phê duyệt tại Hoa Kỳ và châu Âu để làm giảm tái phát nhiễm khuẩn C difficile ở người lớn đang điều trị kháng khuẩn cho nhiễm khuẩn C difficile và người có tỷ lệ tái phát cao. Tuy nhiên, vị trí của liệu pháp này hiện vẫn chưa rõ và vẫn còn được coi là một điều trị mới nổi.
Tổng quan về các chi tiết điều trị
Tham khảo cơ sở dữ liệu dược địa phương của quý vị để biết thông tin toàn diện về thuốc, bao gồm các chống chỉ định, tương tác giữa các loại thuốc, và liều dùng thay thế. ( xem Tuyên bố miễn trách nhiệm )
| Cấp tính | ( tóm tắt ) | |
| Đợt đầu tiên: không nặng | ||
| 1 | Vancomycin hoặc fidaxomicin hoặc metronidazole qua đường uống | |
| thêm | Ngưng dùng tác nhân gây bệnh | |
| thêm | Chăm sóc hỗ trợ | |
| thêm | Các biện pháp kiểm soát nhiễm trùng | |
| Đợt ban đầu: nặng | ||
| 1 | Vancomycin hoặc fidaxomicin đường uống | |
| thêm | Ngưng dùng tác nhân gây bệnh | |
| thêm | Chăm sóc hỗ trợ | |
| thêm | Các biện pháp kiểm soát nhiễm trùng | |
| Đợt đầu tiên: tối cấp | ||
| 1 | Vancomycin kết hợp metronidazole, hoặc tigecycline, hoặc globulin miễn dịch qua đường tĩnh mạch () | |
| thêm | Ngưng dùng tác nhân gây bệnh | |
| thêm | Chăm sóc hỗ trợ | |
| thêm | Các biện pháp kiểm soát nhiễm trùng | |
| bổ sung | Phẫu thuật | |
| Tiếp diễn ( tóm tắt ) |
| Tái phát lần đầu tiên |
| 1 lặp lại điều trị kháng sinh |
| Tái phát tiếp theo |
| 1 Lặp lại điều trị kháng sinh
2 Ghép vi sinh vật trong phân (GVSVTP) |
Các lựa chọn điều trị
| Cấp tính | ||
| Đợt đầu tiên: không nặng | 1 | Vancomycin hoặc fidaxomicin hoặc metronidazole qua đường uống
Các lựa chọn sơ cấp » vancomycin: 125 mg đường uống bốn lần mỗi ngày trong 10 ngày Dạng bào chế uống có thể cần được điều chế đặc biệt tại một số quốc gia. HOẶC » fidaxomicin: 200 mg qua đường uống hai lần mỗi ngày trong 10 ngày Các lựa chọn thứ cấp » metronidazole: 500 mg đường uống ba lần hàng ngày trong 10 ngày » Dữ liệu lâm sàng hỗ trợ: tăng bạch cầu với số lượng bạch cầu ≤15.000 tế bào/mL và creatinine huyết thanh <0,13 mmol/l (<1,5 mg/dL). » Cần bắt đầu điều trị kháng sinh theo kinh nghiệm nếu có nguy cơ trì hoãn đáng kể (>48 giờ) kết quả xét . Đối với các bệnh nhân khác, có thể bắt đầu điều trị kháng sinh sau khi chẩn đoán để giới hạn việc lạm dụng thuốc kháng sinh. » Vancomycin hoặc fidaxomici đường uống được khuyến nghị làm thuốc bậc một cho đợt đầu tiên nhiễm khuẩn Clostridium difficile không nặng. Hiện nay Metronidazole chỉ được khuyến nghị tại các cơ sở có hạn chế trong việc tiếp cận với thuốc bậc một. Tuy nhiên, hướng dẫn quốc tế vẫn có thể khuyến nghị cho dùng metronidazole như thuốc bậc một. » Một phân tích gộp cũng cho thấy bằng chứng thuyết phục nhất chỉ ra là fidaxomicin tốt hơn đáng kể so với vancomycin trong vệc chữa khỏi triệu chứng lâu dài ở người lớn bị nhiễm trùng tái phát không có sự nhân lên của vi khuẩn Vì vậy, fidaxomicin được xem là lựa chọn điều trị tốt hơn vancomycin ở tất cả bệnh nhân ngoại trừ những người bị nhiễm trùng nặng. Tỷ lệ chữa khỏi bằng metronidazole thấp hơn đáng kể so với vancomycin và fidaxomicin.[48] |
| thêm | Ngưng dùng tác nhân gây bệnh
» Đề xuất đầu tiên của chẩn đoán là ngưng dùng (các) thuốc kháng sinh kích thích ngay khi có thể. » Nếu không thể ngưng thuốc kháng sinh, thì nên thay thế bằng một loại thuốc kháng sinh ít có nguy cơ gây nhiễm khuẩn C difficile hơn. Cụ thể, tránh dùng ampicillin, cephalosporin, clindamycin, carbapenem và fluoroquinolone. |
|
| thêm | Chăm sóc hỗ trợ
» Đầu tiên cần đánh giá bệnh nhân về tình trạng dịch, đặc biệt nếu bệnh nhân được nhập viện. Nếu cần, nên bắt đầu bù nước và bổ sung điện giải. |
|
| thêm | Các biện pháp kiểm soát nhiễm trùng
» Cần cách ly bệnh nhân trong phòng riêng với nhà vệ sinh riêng. Cần ưu tiên cho các bệnh nhân đại tiện không tự chủ. Cần dùng biện pháp phòng ngừa khi tiếp xúc với bệnh nhân nghi ngờ nhiễm khuẩn trước khi có kết quả xét nghiệm. Cần tiếp tục sử dụng các biện pháp phòng ngừa khi tiếp xúc trong ít nhất 48 giờ sau khi đã hết tiêu chảy, và cho đến khi xuất viện nếu tỷ lệ nhiễm khuẩn C difficile vẫn cao. » Các chuyên gia y tế cần mặc áo choàng và đeo găng tay khi bước vào phòng. Cần vệ sinh tay trước và sau khi tiếp xúc với bệnh nhân và sau khi tháo găng tay. Cần sử dụng xà phòng và nước hoặc sản phẩm chứa cồn. Cần khuyến khích bệnh nhân rửa tay và tắm vòi sen để giảm tải lượng bào tử trên da. Ưu tiên dùng thiết bị dùng một lần cho bệnh nhân nếu sẵn có (không khuyến nghị nhiệt kế đặt tại trực tràng).[2] » Tổ chức Y tế Thế giới đưa ra hướng dẫn về kỹ thuật rửa tay đúng cách.[34] [WHO: guidelines on hand hygiene] |
|
| Đợt ban đầu: nặng | 1 | Vancomycin hoặc fidaxomicin đường uống
Các lựa chọn sơ cấp » vancomycin: 125 mg đường uống bốn lần mỗi ngày trong 10 ngày Dạng bào chế uống có thể cần được điều chế đặc biệt tại một số quốc gia. HOẶC » fidaxomicin: 200 mg qua đường uống hai lần mỗi ngày trong 10 ngày » Dữ liệu lâm sàng hỗ trợ: tăng bạch cầu với số lượng bạch cầu ≥15.000 tế bào/mL và creatinine huyết thanh >0,13 mmol/l (>1,5 mg/dL). » Cần bắt đầu điều trị kháng sinh theo kinh nghiệm nếu có nguy cơ trì hoãn đáng kể (>48 giờ) kết quả xét . » Vancomycin hoặc fidaxomicin qua đường uống được khuyến nghị làm thuốc bậc 1 cho đợt đầu tiên nhiễm khuẩn CC difficile nặng |
| thêm | Ngưng dùng tác nhân gây bệnh
» Đề xuất đầu tiên của chẩn đoán là ngưng dùng (các) thuốc kháng sinh kích thích ngay khi có thể.[2] » Nếu không thể ngưng thuốc kháng sinh, thì nên thay thế bằng một loại thuốc kháng sinh ít có nguy cơ gây nhiễm khuẩn C difficile hơn. Cụ thể, tránh dùng ampicillin, cephalosporin, clindamycin, carbapenem và fluoroquinolone |
|
| thêm | Chăm sóc hỗ trợ
» Đầu tiên cần đánh giá bệnh nhân về tình trạng dịch, đặc biệt nếu bệnh nhân được nhập viện. Nếu cần, nên bắt đầu bù nước và bổ sung điện giải. |
|
| thêm | Các biện pháp kiểm soát nhiễm trùng
» Cần cách ly bệnh nhân trong phòng riêng với nhà vệ sinh riêng. Cần ưu tiên cho các bệnh nhân đại tiện không tự chủ. Cần dùng biện pháp phòng ngừa khi tiếp xúc với bệnh nhân nghi ngờ nhiễm khuẩn trước khi có kết quả xét nghiệm. Cần tiếp tục sử dụng các biện pháp phòng ngừa khi tiếp xúc trong ít nhất 48 giờ sau khi đã hết tiêu chảy, và cho đến khi xuất viện nếu tỷ lệ nhiễm khuẩn C difficile vẫn cao. » Các chuyên gia y tế cần mặc áo choàng và đeo găng tay khi bước vào phòng. Cần vệ sinh tay trước và sau khi tiếp xúc với bệnh nhân và sau khi tháo găng tay. Cần sử dụng xà phòng và nước hoặc sản phẩm chứa cồn. Cần khuyến khích bệnh nhân rửa tay và tắm vòi sen để giảm tải lượng bào tử trên da. Ưu tiên dùng thiết bị dùng một lần cho bệnh nhân nếu sẵn có (không khuyến nghị nhiệt kế đặt tại trực tràng). » Tổ chức Y tế Thế giới đưa ra hướng dẫn về kỹ thuật rửa tay đúng cách.[34] [WHO: guidelines on hand hygiene] |
|
| Đợt đầu tiên: tối cấp | 1 | Vancomycin kết hợp metronidazole, hoặc tigecycline, hoặc globulin miễn dịch qua đường tĩnh mạch
Các lựa chọn sơ cấp » vancomycin: 500 mg qua đường uống (hoặc qua ống thông mũi – dạ dày) bốn lần mỗi ngày; hoặc 500 mg trong 100 mL nước muối sinh lý qua trực tràng (dưới dạng thụt giữ) mỗi 6 giờ Dạng bào chế uống có thể cần được điều chế đặc biệt tại một số quốc gia. » metronidazole: 500 mg đường tĩnh mạch mỗi 8 giờ một lần Các lựa chọn thứ cấp » Tigecycline: 100 mg đầu tiên qua đường tĩnh mạch dưới dạng liều nạp, sau đó là 50 mg mỗi 12 giờ hoặc » globulin miễn dịch thông thường ở người: 150-400 mg/kg qua đường tĩnh mạch dưới dạng liều đơn » Dữ liệu lâm sàng hỗ trợ: hạ huyết áp, sốc, liệt hoặc phình đại tràng Còn gọi là nhiễm khuẩn nặng, có biến chứng. » Vancomycin qua đường uống (ở liều cao hơn liều được sử dụng để điều trị nhiễm khuẩn không tối cấp) là điều trị bậc 1 được khuyến nghị. Nếu bị liệt, có thể cân nhắc đặt vancomycin tại trực tràng. Cần cho dùng metronidazole qua đường tĩnh mạch kèm theo vancomycin qua đường uống hoặc trực tràng, cụ thể nếu bị liệt vì liệt có thể ảnh hưởng đến việc cung cấp vancomycin qua đường uống đến trực tràng.[2] » Ở bệnh nhân không đáp ứng với liệu pháp bậc một, tigecycline hoặc IVIG nên được sử dụng, nhưng chưa tiến hành thử nghiệm có đối chứng nào.[2] IVIG có hiệu quả ở một số lượng bệnh nhân nhỏ bị bệnh tối cấp, có thể là bằng cách cung cấp các kháng thể trung hòa kháng lại độc tố A và B. Có thể cân nhắc IVIG cho bệnh tối cấp ở bệnh nhân có rủi ro phẫu thuật cao; tuy nhiên, không có dữ liệu hoặc hướng dẫn xác định để hỗ trợ khuyến cáo này. |
| thêm | Ngưng dùng tác nhân gây bệnh
» Đề xuất đầu tiên của chẩn đoán là ngưng dùng (các) thuốc kháng sinh kích thích ngay khi có thể.[2] » Nếu không thể ngưng thuốc kháng sinh, thì nên thay thế bằng một loại thuốc kháng sinh ít có nguy cơ gây nhiễm khuẩn C difficile hơn. Cụ thể, tránh dùng ampicillin, cephalosporin, clindamycin, carbapenem và fluoroquinolone. |
| thêm | Chăm sóc hỗ trợ |
| » Đầu tiên cần đánh giá bệnh nhân về tình trạng dịch, đặc biệt nếu bệnh nhân được nhập viện. Nếu cần, nên bắt đầu bù nước và bổ sung điện giải. | |
| » Sử dụng các thuốc kháng nhu động, bao gồm opioid và loperamide, mặc dù không có bằng chứng hỗ trợ khuyến cáo này. | |
| thêm | Các biện pháp kiểm soát nhiễm trùng |
| » Cần cách ly bệnh nhân trong phòng riêng với nhà vệ sinh riêng. Cần ưu tiên cho các bệnh nhân đại tiện không tự chủ. Cần dùng biện pháp phòng ngừa khi tiếp xúc với bệnh nhân nghi ngờ nhiễm khuẩn trước khi có kết quả xét nghiệm. Cần tiếp tục sử dụng các biện pháp phòng ngừa khi tiếp xúc trong ít nhất 48 giờ sau khi đã hết tiêu chảy, và cho đến khi xuất viện nếu tỷ lệ nhiễm khuẩn C difficile vẫn cao. | |
| » Các chuyên gia y tế cần mặc áo choàng và đeo găng tay khi bước vào phòng. Cần vệ sinh tay trước và sau khi tiếp xúc với bệnh nhân và sau khi tháo găng tay. Cần sử dụng xà phòng và nước hoặc sản phẩm chứa cồn. Cần khuyến khích bệnh nhân rửa tay và tắm vòi sen để giảm tải lượng bào tử trên da. Ưu tiên dùng thiết bị dùng một lần cho bệnh nhân nếu sẵn có (không khuyến nghị nhiệt kế đặt tại trực tràng).[2] | |
| » Tổ chức Y tế Thế giới đưa ra hướng dẫn về kỹ thuật rửa tay đúng cách.[34] [WHO: guidelines on hand hygiene] | |
| bổ sung | Phẫu thuật |
| » Chẩn đoán và điều trị sớm là thiết yếu để có kết quả tốt, và cần cân nhắc can thiệp sớm bằng phẫu thuật ở bệnh nhân không đáp ứng với liệu pháp y tế hoặc những người đã tăng số lượng bạch cầu hoặc nồng độ lactate. | |
| » Thủ thuật phẫu thuật lựa chọn là cắt bỏ một phần đại tràng kèm theo bảo vệ trực tràng. Mở thông hồi tràng có chuyển hướng đoạn ruột (với rửa dạ dày, sau đó là rửa thuận chiều bằng vancomycin) là một phương pháp thay thế.[2] | |
| Tiếp diễn | |
| Tái phát lần đầu tiên | |
| 1 | Lặp lại điều trị kháng sinh |
| Các lựa chọn sơ cấp |
| Tiếp diễn | ||
| 1 | » vancomycin: phác đồ tiêu chuẩn: 125 mg qua đường uống bốn lần mỗi ngày trong 10 ngày; phác đồ liều giảm dần và liều xung: 125 mg qua đường uống bốn lần mỗi ngày trong 10-14 ngày, sau đó là 125 mg hai lần mỗi ngày trong 7 ngày, sau đó là 125 mg mỗi ngày một lần trong 7 ngày, tiếp theo là 125 mg mỗi 2-3 ngày trong 2-8 tuần
Dạng bào chế uống có thể cần được điều chế hoặc » fidaxomicin: 200 mg qua đường uống hai lần mỗi ngày trong 10 ngày » Lựa chọn điều trị tùy thuộc vào điều trị được sử dụng cho đợt đầu tiên.[2] » Nếu điều trị 10 ngày bằng vancomycin đường uống cho đợt đầu tiên: khuyến cáo phác đồ vancomycin qua đường uống liều giảm dần kéo dài và liều xung hoặc điều trị tiêu chuẩn 10 ngày bằng fidaxomicin. » Nếu sử dụng metronidazole cho đợt đầu tiên: khuyến nghị điều trị tiêu chuẩn 10 ngày bằng vancomycin qua đường uống. |
|
| Tái phát tiếp theo | 1 | Lặp lại điều trị kháng sinh
Các lựa chọn sơ cấp » vancomycin: phác đồ liều giảm dần và liều xung: 125 mg qua đường uống bốn lần mỗi ngày trong 10-14 ngày, sau đó là 125 mg hai lần mỗi ngày trong 7 ngày, tiếp theo là 125 mg mỗi ngày một lần trong 7 ngày, rồi đến 125 mg mỗi 2-3 ngày trong Dạng bào chế uống có thể cần được điều chế đặc biệt tại một số quốc gia. hoặc » vancomycin: phác đồ tiêu chuẩn: 125 mg qua đường uống bốn lần mỗi ngày trong 10 ngày Dạng bào chế uống có thể cần được điều chế đặc biệt tại một số quốc gia. » Rifaximin: 400 mg qua đường uống ba lần hàng ngày trong 20 ngày; bắt đầu sau khi kết thúc tiến trình điều trị 10 ngày bằng vancomycin hoặc » fidaxomicin: 200 mg qua đường uống hai lần mỗi ngày trong 10 ngày » Có thể điều trị các đợt tái phát tiếp theo bằng phác đồ kháng sinh sau đây: phác đồ vancomycin qua đường uống liều giảm dần kéo dài và liều xung; điều trị tiêu chuẩn 10 ngày bằng vancomycin qua đường uống, sau đó là rifaximin trong 20 ngày; hoặc điều trị tiêu chuẩn 10 ngày bằng fidaxomicin. |
| 2 | Ghép vi sinh vật trong phân (GVSVTP)
» GVSVTP là một tùy chọn ở những bệnh nhân tái phát ít nhất hai lần và đã thất bại trong điều trị kháng sinh.[2] » Bao gồm ghép phân đã được xử lý từ người hiến tặng khỏe mạnh vào đường ruột của bệnh nhân nhiễm khuẩn để khắc phục tình trạng mất cân bằng hệ khuẩn ruột. » Có thể sử dụng tiến trình đưa vào vancomycin trong thời gian ngắn để giảm tải lượng C difficile ở những bệnh nhân đang không được điều trị kháng sinh trước khi nhận GVSVTP theo kế hoạch. » Các thử nghiệm ngẫu nhiên có đối chứng đã chứng minh tỷ lệ thành công cao. Một nghiên cứu tổng quát về các thử nghiệm ngẫu nhiên có đối chứng đã phát hiện rằng có bằng chứng khá thuyết phục chỉ ra rằng GVSVTP hiệu quả hơn vancomycin hoặc giả dược.[64] » GVSVTP dạng đóng băng hiệu quả như GVSVTP dạng tươi trong việc đạt được tình trạng cải thiện của tiêu chảy,[62] [65]nbspvà cung cấp qua đường tiêu hóa dưới có thể hiệu quả hơn cung cấp qua đường tiêu hóa trên.[66] » GVSVVTP có thể dung nạp tốt, nhưng các tác dụng bất lợi có thể bao gồm sốt, tăng cảm vùng bụng hoặc khó chịu, đầy hơi, buồn nôn/nôn, tiêu chảy/táo bón và nhiễm khuẩn. Các hậu quả dài hạn còn chưa rõ. » Không có đủ bằng chứng để khuyến nghị GVSVTP cho bệnh nặng, và phương pháp này có thể kém hiệu quả hơn trong việc loại bỏ nhiễm khuẩn C difficile ở bệnh nhân bị bệnh viêm ruột. |
Giai đoạn đầu
Bezlotoxumab
Một kháng thể đơn dòng ở người gắn kết độc tố B của Clostridium difficile. Kháng thể này đã được phê duyệt tại Hoa Kỳ và châu Âu để làm giảm tái phát nhiễm khuẩn C difficile ở người lớn đang được điều trị kháng khuẩn cho nhiễm khuẩn C difficile và người có tỷ lệ tái phát cao. Thuốc này không được chỉ định để điều trị nhiễm khuẩn C difficile và không phải là thuốc kháng khuẩn. Một liều đơn bezlotoxumab qua đường tĩnh mạch (được cho dùng kết hợp với điều trị kháng sinh tiêu chuẩn) cho nhiễm khuẩn C difficile nguyên phát hoặc tái phát gắn với tỷ lệ nhiễm trùng tái phát thấp hơn là 38% so với riêng điều trị kháng sinh trong 2 thử nghiệm giai đoạn III. Đã đạt được tình trạng khỏi bệnh bền vững (không có nhiễm trùng tái phát trong 12 tuần) ở 64% bệnh nhân so với 54% bệnh nhân trong nhóm giả dược. Tác dụng bất lợi thường gặp nhất là buồn nôn và tiêu chảy, và thuốc có thông tin về tác dụng bất lợi tương tự với giả dược.[71] Hiện vẫn chưa rõ vị trí của thuốc trong điều trị. Hướng dẫn của Hiệp hội Bệnh truyền nhiễm Hoa Kỳ/Hiệp hội Dịch tễ Y tế Hoa Kỳ năm 2017 không đưa ra bất kỳ khuyến nghị nào về việc sử dụng thuốc này, nhưng lưu ý là thuốc này sẽ được đề cập trong các cập nhật hướng dẫn tiếp theo.[2] Viện Y tế và Chăm sóc Quốc gia khuyến nghị rằng cần bàn bạc về các lợi ích và rủi ro của liệu pháp bezlotoxumab với bệnh nhân vì một số người có thể không muốn tiêm truyền qua đường tĩnh mạch, đặc biệt nếu họ không có yếu tố nguy cơ tái phát (ví dụ: độ tuổi >65 tuổi, bị suy giảm miễn dịch, tiền sử trước đây nhiễm khuẩn C difficile, hiện nhiễm khuẩn nặng).[72]
Cadazolid
Thuốc kháng sinh mới thuộc nhóm oxazolidinone. Đã có phát hiện rằng thuốc này ức chế tổng hợp protein của C difficile, dẫn đến ức chế hình thành bào tử và độc tố. Trong các nghiên cứu tiền lâm sàng, cadazolid đã tỏ ra có hiệu quả trong hoạt tính kháng C difficile trong ống nghiệm. Hấp thụ Cadazolid không đáng kể, dẫn đến nồng độ trong lòng ruột cao và phơi nhiễm toàn thân thấp.[73] Một nghiên cứu giai đoạn II đã phát hiện ra rằng cadazolid được dung nạp tốt và có tỷ lệ đáp ứng lâm sàng bền vững cao hơn so với vancomycin.[50] Một thử nghiệm giai đoạn III đang được tiến hành.
Teicoplanin
Một loại thuốc kháng sinh glycopeptide bán tổng hợp. Một đánh giá Cochrane đã phát hiện rằng duy trì chữa khỏi triệu chứng cải thiện khi dùng teicoplanin so với vancomycin;[49] tuy nhiên, độ thuyết phục của bằng chứng về việc sử dụng thấp, và thuốc hiện không sẵn có tại Hoa Kỳ.
Ridinilazole
Một thuốc kháng khuẩn mới có phổ hoạt động nhắm mục tiêu cao, có khả năng bảo vệ hệ vi sinh vật thường trú trong đường ruột. Thuốc này đã hoàn thành thử nghiệm giai đoạn II và cho thấy khả năng điều trị nhiễm khuẩn C difficile ,[74] nhưng cần tiến hành nghiên cứu thêm.
Surotomycin
Một loại lipopeptide vòng, diệt khuẩn chọn lọc, được hấp thu tối thiểu, dùng qua đường uống đang được nghiên cứu về khả năng điều trị nhiễm khuẩn C difficile. Surotomycin và vancomycin có tỷ lệ chữa khỏi lâm sàng tương tự nhau, và tỷ lệ tái phát thấp hơn khi dùng surotomycin trong một thử nghiệm ngẫu nhiên có đối chứng giai đoạn II.[75]
Resin
Cholestyramine và colestipol gắn kết độc tố của C difficile và đã được sử dụng để điều trị bệnh tái phát kèm theo hay không kèm theo vancomycin. Các loại thuốc này cũng gắn kết vancomycin, và đã không được nghiên cứu
nhiều.[15]nbspĐơn trị liệu bằng các thuốc gắn kết độc tố trong lòng ruột này đã được chứng tỏ là thua kém hơn liệu pháp tiêu chuẩn bằng metronidazole và vancomycin.
Vắc-xin
Vắc-xin kháng C difficileare đang được phát triển. VLA84 đã được chứng minh là an toàn và hiệu quả trong thử nghiệm giai đoạn I.[77]nbspCho đến nay, thuốc đã hoàn thành các thử nghiệm giai đoạn II và sẵn sàng cho giai đoạn III.
Tái khám
Khuyến nghị
Giám sát
Không yêu cầu theo dõi cụ thể. Không khuyến nghị lặp lại xét nghiệm phân thường xuyên vì bệnh nhân được theo dõi về sự cải thiện lâm sàng. Cần tái kiểm tra bệnh nhân tái phát tiêu chảy.
Hướng dẫn dành cho bệnh nhân
Cần tư vấn cho bệnh nhân tìm kiếm chăm sóc y tế nếu bệnh nhân xuất hiện lại các triệu chứng. Với tiêu chảy nói chung, bệnh nhân cần tránh thức ăn nhiều dầu mỡ; ở tiêu chảy kéo dài, việc tham khảo ý kiến chuyên gia dinh dưỡng có thể giúp tư vấn bệnh nhân về chế độ ăn uống.[78] [CDC: Clostridium difficile infection]
Các biến chứng
| Các biến chứng | Khung thời gian | Khả năng |
| Tắc ruột | Ngắn hạn | Thấp |
| Bệnh nhân bị buồn nôn và nôn nặng hơn.
Chụp X-quang vùng bụng cho thấy giãn ruột nhẹ. Chỉ định đặt ống thông mũi – dạ dày và điều trị hỗ trợ cho đến khi khỏi liệt. Cần theo dõi thủng, viêm phúc mạc và phình đại tràng nhiễm độc. |
||
| Thủng và viêm phúc mạc | ngắn hạn | thấp |
| Bệnh nhân có biểu hiện đau bụng cấp tính, đau và phản ứng thành bụng. Họ bị sốt cao, hạ huyết áp và nhịp tim nhanh.
Cần cho dùng điều trị hỗ trợ, metronidazole qua đường tĩnh mạch và vancomycin qua trực tràng hoặc vancomycin qua ống thông mũi – dạ dày. Có thể cần đến thủ thuật mở bụng kèm cắt bỏ đại tràng trong trường hợp cấp cứu. |
||
| Phình đại tràng nhiễm độc | ngắn hạn | thấp |
Tiên lượng
Đáp ứng với điều trị dự kiến là việc cải thiện nhanh sốt và tiêu chảy trong vòng 4 đến 6 ngày. Đa số bệnh nhân đáp ứng với điều trị lần đầu tiên.
Chủng dịch bệnh mới (Chủng thuộc điện di gel trường xung loại 1 được cách ly từ người ở Bắc Mỹ/ Clostridium difficile B1) đã dẫn đến bệnh nặng hơn và kháng trị cao hơn. Do đó, đã tăng tỷ lệ phình đại tràng nhiễm độc và tăng ca tử vong liên quan đến C difficile.
Tỷ lệ tái phát thay đổi tùy thuộc vào biểu hiện, chức năng miễn dịch, mức độ nghiêm trọng của bệnh và loại và thời gian điều trị. Đã có báo cáo về tỷ lệ tái phát là từ 5% đến 50%, mặc dù một nghiên cứu đã phát hiện rằng ít nhất một lần tái phát ở 21% ca nhiễm trùng liên quan đến chăm sóc y tế và 14% ca nhiễm trùng liên quan đến cộng đồng.[4] Một số lượng nhỏ bệnh nhân bị tái phát lại, đòi hỏi phải có một số đợt điều trị, hoặc thử nghiệm liều xung hoặc giảm dần.[15] Nguy cơ tái phát lần đầu tiên sau đợt nhiễm trùng đầu tiên là 25% trong một nghiên cứu, với nguy cơ tái phát lần thứ hai là 38%, nguy cơ tái phát lần thứ ba là 29%, và nguy cơ tái phát lần thứ tư là 27%. Nguy cơ nhiễm trùng nặng giảm theo mỗi lần tái phát sau đó
Hướng dẫn chẩn đoán
Guidance document on the prevention of Clostridium difficile infection in acute health care settings
Nhà xuất bản: European Society of Clinical Microbiology and Infectious Diseases Xuất bản lần cuối: 2018
Clinical practice guidelines for Clostridium difficile infection in adults and children: 2017 update
Nhà xuất bản: Infectious Diseases Society of America; Society for Healthcare Epidemiology of America
Xuất bản lần cuối: 2018
Guidelines for diagnosis, treatment, and prevention of Clostridium difficile infections
Nhà xuất bản: American College of Gastroenterology Xuất bản lần cuối: 2013
Hướng dẫn điều trị
Infection prevention and control
Nhà xuất bản: National Institute for Health and Care Excellence Xuất bản lần cuối: 2014
Faecal microbiota transplant for recurrent Clostridium difficile infection
Nhà xuất bản: National Institute for Health and Care Excellence Xuất bản lần cuối: 2014
Update of the treatment guidance document for Clostridium difficile infection
Nhà xuất bản: European Society of Clinical Microbiology and Infectious Diseases Xuất bản lần cuối: 2014
Updated guidance on the management and treatment of Clostridium difficile infection
Nhà xuất bản: Public Health England Xuất bản lần cuối: 2013
Clinical practice guidelines for Clostridium difficile infection in adults and children: 2017 update
Nhà xuất bản: Infectious Diseases Society of America; Society for Healthcare Epidemiology of America
Xuất bản lần cuối: 2018
Guidelines for diagnosis, treatment, and prevention of Clostridium difficile infections
Nhà xuất bản: American College of Gastroenterology Xuất bản lần cuối: 201
Nguồn trợ giúp trực tuyến
1. WHO: guidelines on hand hygiene (external link)
2. CDC: Clostridium difficile infection (external link)
Câu hỏi lâm sàng
Câu 1
Bệnh nhân nữ 67 tuổi nhập viện vì nhiễm trùng huyết thứ phát do nhiễm trùng đường tiết niệu. Tiền căn ghi nhận tăng huyết áp, đái tháo đường týp 2, đột quỵ thiếu máu cục bộ và bàng quang thần kinh được đặt Foley. Bệnh nhân nhập vào khoa ICU và điều trị bằng dịch truyền tĩnh mạch và kháng sinh phổ rộng. Cấy máu và nước tiểu phát triển Escherichia coli nhạy cảm với tất cả các loại kháng sinh được thử nghiệm. Tình trạng của bệnh nhân dần dần được cải thiện sau quá trình điều trị và thuốc kháng sinh được đổi thành ciprofloxacin đường uống vào ngày thứ 3 kể từ khi nhập viện. Ngày thứ 7, bệnh nhân lú lẫn dần, đi ngoài 6 lần, phân lỏng kèm đau vùng bụng dưới. Nhiệt độ là 38 C (100,4 F), huyết áp là 111/89 mmHg và mạch là 108 lần/phút. Bụng mềm và ấn đau nhẹ 1/4 bụng dưới trái với nhu động ruột bình thường. Không dấu đề kháng hoặc phản ứng dội. X-quang ngực cho thấy không có thâm nhiễm mới. Xét nghiệm ghi nhận số lượng bạch cầu là 14.200/mm3 so với 8.700/mm3 ở 2 ngày trước đó. Xét nghiệm lại nước tiểu cho thấy thỉnh thoảng có nấm men (yeasts). Điều nào sau đây là bước tiếp theo tốt nhất trong quản lý bệnh nhân này?
- Thay Foley và bắt đầu dùng fluconazole
- Gửi lại cấy máu và bắt đầu tiêm tĩnh mạch gentamicin
- Gửi xét nghiệm phân và bắt đầu uống vancomycin
- Ngừng ciprofloxacin và bắt đầu tiêm tĩnh mạch vancomycin
- Tư vấn phẫu thuật khẩn cấp
Bệnh nhân nữ, 67 tuổi, nhập viện vì nhiễm trùng huyết
- Nhiễm trùng huyết từ nhiễm trùng tiêu hóa trên do E. Coli, đáp ứng kháng sinh
- N7: thay đổi tri giác, tiêu chảy, tăng bạch cầu
Hỏi: Điều nào sau đây là bước tiếp theo tốt nhất trong quản lý bệnh nhân này?
Đáp án: B: Gửi xét nghiệm phân và bắt đầu uống vancomycin
Bệnh nhân này có biểu hiện lú lẫn và tăng bạch cầu mới khởi phát, liên quan đến việc sử dụng kháng sinh gần đây, tiêu chảy và đau bụng nhẹ, cho thấy có thể nhiễm Clostridioides (trước đây là Clostridium) (CDI – Clostridioides difficle infection). Các yếu tố nguy cơ đối với CDI bao gồm nhập viện gần đây, tuổi cao hoặc sử dụng kháng sinh (phổ biến nhất là fluoroquinolones, penicillin, cephalosporin và clindamycin). Tăng bạch cầu không rõ nguyên nhân ở bệnh nhân nhập viện nên nghi ngờ về CDI, ngay cả khi không bị tiêu chảy. CDI có thể từ tiêu chảy nhẹ đến viêm đại tràng tối cấp với phình đại tràng nhiễm độc.
Chẩn đoán thường được xác nhận bằng xét nghiệm phân tìm độc tố C difficiie (ví dụ, PCR). Các phương pháp điều trị ban đầu bao gồm vancomycin đường uống hoặc fidaxomicin. Bệnh nhân mắc bệnh tối cấp (ví dụ: hạ huyết áp, tắc ruột, phình đại tràng) nên được điều trị bằng vancomycin đường uống liều cao và metronidazole tiêm tĩnh mạch; nếu có tắc ruột, vancomycin có thể dùng đường hậu môn.
(Lựa chọn A) Nấm đường niệu không triệu chứng phổ biến ở những bệnh nhân đặt ống thông tiểu lâu ngày, nhưng nhiễm trùng đường tiết niệu do nấm có triệu chứng là không bình thường- Trong trường hợp nấm niệu không triệu chứng không biến chứng, ống thông có thể được thay thế, nhưng thuốc kháng nấm theo kinh nghiệm nói chung là không cần thiết.
(Lựa chọn B) Aminoglycosides (ví dụ, gentamicin) điều trị vi khuẩn gram âm kháng thuốc. Tuy nhiên, bệnh nhân này đang cải thiện lâm sàng và có Escherichia coli nhạy cảm với ciprofloxacin.
Việc sử dụng kháng sinh và các triệu chứng tiêu hóa của bệnh nhân này làm cho viêm đại tràng do C difficile dễ xảy ra hơn là làm nặng thêm tình trạng nhiễm trùng đường tiết niệu.
(Lựa chọn D) Ở những bệnh nhân bị CDI, nên ngừng sử dụng kháng sinh (ví dụ: ciprofloxacin) càng sớm càng tốt, với những bệnh nhân chuyển sang dùng kháng sinh ít liên quan đến CDI hơn. Vancomycin tiêm tĩnh mạch được sử dụng để điều trị các vi khuẩn gram dương kháng thuốc. Tuy nhiên, điều này sẽ không điều trị được bệnh nhiễm khuẩn huyết E coli của cô ấy. Ngoài ra, vancomycin tiêm tĩnh mạch không được bài tiết vào đại tràng và không có hiệu quả chống lại CDI.
(Lựa chọn E) Tư vấn phẫu thuật là cần thiết ở những bệnh nhân có CDI tối cấp (ví dụ: hạ huyết áp, tắc ruột, phình đại tràng nhiễm độc). Tuy nhiên, bệnh nhân này bị viêm đại tràng nhẹ đến trung bình mà không có dấu hiệu phúc mạc cấp tính khi thăm khám
Kết luận:
Nên nghi ngờ viêm đại tràng difficile do Clostridioides (trước đây là Clostridium) ở bất kỳ bệnh nhân nào đã dùng kháng sinh và bị tiêu chảy và/hoặc đau bụng. Các xét nghiệm phân tìm độc tố C difficile nên được thực hiện để xác định chẩn đoán. Các phương pháp điều trị cho giai đoạn đầu bao gồm vancomycin đường uống hoặc fidaxomicin đường uống. Bệnh nhân mắc bệnh tối cấp (ví dụ: hạ huyết áp, tắc ruột, phình đại tràng) nên được điều trị bằng vancomycin đường uống liều cao và metronidazole đường tĩnh mạch; nếu có tắc ruột, vancomycin có thể được dùng đường hậu môn.
Câu 2
Bệnh nhân, nam 28 tuổi, tái nhập khoa cấp cứu do đau quặn bụng và tiêu chảy. Bệnh nhân có tiền sử viêm loét đại tràng 3 năm và lần đầu tiên xuất hiện cách đây 2 tuần với triệu chứng đau bụng và đi ngoài ra máu. Anh ta đã được nhập viện và nội soi đại tràng ghi nhận viêm đại tràng đang hoạt động ở trực tràng, đại tràng sigma và đại tràng xuống. Các triệu chứng của anh ấy dần dần được cải thiện khi điều trị và anh ấy đã được xuất viện cùng với điều trị prednisone và 5—aminosalicylic acid. Các triệu chứng của bệnh nhân đã khỏi hoàn toàn, nhưng hiện anh ta bị đau quặn bụng nhẹ và tiêu chảy nhiều nước 2 ngày nay mặc dù đã uống thuốc theo chỉ định.
Anh ấy không có vấn đề y khoa khác. Nhiệt độ là 37,9 C (100,2 F), huyết áp là 124/76 mm Hg, mạch là 78 l/phút và nhịp thở là 12 lần/phút, không thay đổi khi đứng. Bệnh nhân có cảm giác đau nhẹ khi ấn khắp bụng, không ghi nhận phản ứng dội hoặc dấu đề kháng. Nhu động bình thường. Kết quả xét nghiệm như sau:
Complete blood count
| Hemoglobin | 12.4 g/dL |
| Platelets | 380,000/mm3 |
| Leukocytes | 16,000./mm3 |
| Neutrophils | 80% |
Serum chemistry
| Sodium | 136 mEq/L |
| Potassium | 3.8 mEq/L |
| Bicarbonate | 22 mEq/L |
| Creatinine | 0.7 mg/dL |
Bước tiếp theo nào là tốt nhất trong điều trị bệnh nhân này?
- Chụp CT bụng có cản quang
- Lặp lại nội soi đại tràng với sinh thiết
- Đo mỡ trong phân
- Xét nghiệm phân tìm độc tố Clostridioides difficile
- Liệu pháp tumor necrosis factor inhibitor
Đáp án: D: Xét nghiệm phân tìm độc tố Clostridioides difficile
Bệnh nhân này gần đây đã nhập viện vì đợt bùng phát viêm loét đại tràng ở trực tràng và đại tràng sigma/đại tràng xuống. Phân lẫn máu của anh ấy đã được giải quyết, nhưng sau đó anh ấy đã xuất hiện phân nước lượng nhiều kèm tăng bạch cầu, làm tăng lên nghi ngờ về nhiễm trùng Clostridioides difficile (CDI). Mặc dù việc sử dụng kháng sinh là yếu tố nguy cơ lớn nhất đối với CDl, nhưng các yếu tố nguy cơ khác được xác đinh rõ ràng gồm việc nhập viện gần đây và bệnh nặng đi kèm như bệnh viêm ruột.
CDI thường được đánh dấu bằng tiêu lỏng (23 đợt trong 24 giờ) không có máu hoặc phân đen (không giống như viêm loét đại tràng, thường gây ra phân có máu với lượng nhỏ). Bệnh nhân bị CDI cũng thường xuyên bị đau quạng, sốt nhẹ và buồn nôn. Bụng thường mềm và xét nghiệm thường cho thấy tăng bạch cầu. Các trường hợp nghi ngờ cần phải đề phòng tiếp xúc và xét nghiệm phân để tìm độc tố C difficile. Điều trị bằng van nhưng nhiều trường hợp tái phát.
(Lựa chọn A) Chụp CT bụng thường không quan trọng ở những người nghi ngờ bị viêm đại tràng C difficile nhưng có thể cần thiết cho những người bị CDI nặng (ví dụ: chướng bụng, giảm thể tích tuần hoàn) hoặc nghi ngờ thủng (ví dụ: phản ứng dội).
(Lựa chọn B) Bệnh nhân bị CDI thường không nên tiến hành nội soi do nguy cơ thủng trong quá trình bơm hơi. Nội soi có thể được chỉ định nếu xét nghiệm phân tìm độc tố C difficile âm tính và chẩn đoán vẫn chưa rõ ràng.
(Lựa chọn C) Đo lượng chất béo trong phân có thể giúp chẩn đoán bệnh tiêu chảy kém hấp thu, thường xảy ra trong bối cảnh nhiễm trùng đường ruột non (ví dụ, bệnh giardia), vi khuẩn phát triển quá mức hoặc viêm tụy mạn tính. Bệnh nhân thường bị tiêu chảy phân nước nhiều, nhợt nhạt, có mùi khắm, nhưng thường không bị sốt nhẹ và tăng bạch cầu. Ngoài ra, bệnh nhân này mới nhập viện gần đây và có tiền sử bệnh viêm ruột làm cho CDI có nhiều khả năng xảy ra hơn.
(Lựa chọn E) Thuốc tumor necrosis factor inhibitors thường được sử dụng cho viêm loét đại tràng dai dẳng. Tuy nhiên, viêm loét đại tràng thường gây ra phân có máu với lượng nhỏ chứ không phải phân nước với lượng nhiều. Do đó, xét nghiệm CDI là cần thiết trước khi xem xét các liệu pháp khác.
Kết luận:
Nhiễm trùng Clostridioides difficile nên được nghi ngờ ở những bệnh nhân mới nhập viện bị tiêu chảy nhiều nước, sốt nhẹ và tăng bạch cầu. Xét nghiệm phân tìm độc tố C difficile giúp chẩn đoán. Các yếu tố nguy cơ khác bao gồm sử dụng kháng sinh, bệnh nặng kèm theo (ví dụ: bệnh viêm ruột) và tuổi cao.
Tài liệu tham khảo
Các bài báo chủ yếu
• McDonald LC, Gerding DN, Johnson S, et al. Clinical practice guidelines for Clostridium difficile infection in adults and children: 2017 update by the Infectious Diseases Society of America (IDSA) and Society for Healthcare Epidemiology of America (SHEA). Clin Infect Dis. 2018 Mar 19;66(7):e1-48. Toàn văn Tóm lược
• Beinortas T, Burr NE, Wilcox MH, et al. Comparative efficacy of treatments for Clostridium difficile infection: a systematic review and network meta-analysis. Lancet Infect Dis. 2018 Jul 16. pii: S1473-3099(18)30285-8. Tóm lược
• Nelson RL, Suda KJ, Evans CT. Antibiotic treatment for Clostridium difficile-associated diarrhoea in adults. Cochrane Database Syst Rev. 2017;(3):CD004610. Toàn văn Tóm lược
Tài liệu tham khảo
1. Lawson PA, Citron DM, Tyrrell KL, et al. Reclassification of Clostridium difficile as Clostridioides difficile (Hall and O’Toole 1935) Prévot 1938. Anaerobe. 2016 Aug;40:95-9. Tóm lược
2. McDonald LC, Gerding DN, Johnson S, et al. Clinical practice guidelines for Clostridium difficile infection in adults and children: 2017 update by the Infectious Diseases Society of America (IDSA) and Society for Healthcare Epidemiology of America (SHEA). Clin Infect Dis. 2018 Mar 19;66(7):e1-48. Toàn văn Tóm lược
3. Poutanen SM, Simor AE. Clostridium difficile-associated diarrhea in adults. CMAJ. 2004 Jul 6;171(1):51-8. Toàn văn Tóm lược
4. Lessa FC, Mu Y, Bamberg WM, et al. Burden of Clostridium difficile infection in the United States. N Engl J Med. 2015 Feb 26;372(9):825-34. Toàn văn Tóm lược
5. Abrahamian FM, Talan DA, Krishnadasan A, et al; EMERGEncy ID NET Study Group. Clostridium difficile infection among US emergency department patients with diarrhea and no vomiting. Ann Emerg Med. 2017 Jul;70(1):19-27;e4. Tóm lược
6. Bartlett JG, Perl TM. The new Clostridium difficile – what does it mean? N Engl J Med. 2005 Dec 8;353(23):2503-5. Tóm lược
7. Loo VG, Poirier L, Miller MA, et al. A predominantly clonal multi-institutional outbreak of Clostridium difficile- associated diarrhea with high morbidity and mortality. N Engl J Med. 2005 Dec 8;353(23):2442-9. Toàn văn Tóm lược
8. McDonald LC, Killgore GE, Thompson A, et al. An epidemic, toxin gene-variant strain of Clostridium difficile. N Engl J Med. 2005 Dec 8;353(23):2433-41. Toàn văn Tóm lược
9. Bartlett JG. Narrative review: the new epidemic of Clostridium difficile-associated enteric disease. Ann Intern Med. 2006 Nov 21;145(10):758-64. Tóm lược
10. Sheitoyan-Pesant C, Abou Chakra CN, Pépin J, et al. Clinical and healthcare burden of multiple recurrences of Clostridium difficile infection. Clin Infect Dis. 2016 Mar 1;62(5):574-80. Toàn văn Tóm lược
11. Ma GK, Brensinger CM, Wu Q, et al. Increasing incidence of multiply recurrent Clostridium difficile infection in the United States: a cohort study. Ann Intern Med. 2017 Aug 1;167(3):152-8. Tóm lược
12. European Centre for Disease Prevention and Control (ECDC). Point prevalence survey of healthcare-associated infections and antimicrobial use in European acute care hospitals. 2011-2012. July 2013 [internet publication]. Toàn văn
13. Public Health England. Clostridium difficile infection: monthly data by NHS acute trust. March 2018 [internet publication]. Toàn văn
14. Borren NZ, Ghadermarzi S, Hutfless S, et al. The emergence of Clostridium difficile infection in Asia: a systematic review and meta-analysis of incidence and impact. PLoS One. 2017 May 2;12(5):e0176797. Toàn văn Tóm lược
15. Treatment of Clostridium difficile infection. Med Lett Drugs Ther. 2011 Feb 21;53(1358):14-5. Tóm lược
16. Schroeder MS. Clostridium difficile-associated diarrhea. Am Fam Physician. 2005 Mar 1;71(5):921-8. Toàn văn Tóm lược
17. Dingle KE, Didelot X, Quan TP, et al. Effects of control interventions on Clostridium difficile infection in England: an observational study. Lancet Infect Dis. 2017 Apr;17(4):411-21. Toàn văn Tóm lược
18. Baur D, Gladstone BP, Burkert F, et al. Effect of antibiotic stewardship on the incidence of infection and colonisation with antibiotic-resistant bacteria and Clostridium difficile infection: a systematic review and meta- analysis. Lancet Infect Dis. 2017 Sep;17(9):990-1001. Tóm lược
19. Blixt T, Gradel KO, Homann C, et al. Asymptomatic carriers contribute to nosocomial Clostridium difficile infection: a cohort study of 4508 patients. Gastroenterology. 2017 Apr;152(5):1031-41;e2. Tóm lược
20. Cunningham R, Dale B, Undy B, et al. Proton pump inhibitors as a risk factor for Clostridium difficile diarrhoea. J Hosp Infect. 2003 Jul;54(3):243-5. Tóm lược
21. US Food and Drug Administration. Clostridium difficile associated diarrhea can be associated with stomach acid drugs known as proton pump inhibitors (PPIs). August 2012 [internet publication]. Toàn văn
22. Arriola V, Tischendorf J, Musuuza J, et al. Assessing the risk of hospital-acquired clostridium difficile infection with proton pump inhibitor use: a meta-analysis. Infect Control Hosp Epidemiol. 2016 Dec;37(12):1408-17. Toàn văn Tóm lược
23. Nguyen GC, Kaplan GG, Harris ML, et al. A national survey of the prevalence and impact of Clostridium difficile infection among hospitalized inflammatory bowel disease patients. Am J Gastroenterol. 2008 Jun;103(6):1443-50. Tóm lược
24. Razik R, Rumman A, Bahreini Z, et al. Recurrence of Clostridium difficile infection in ptients with inflammatory bowel disease: the RECIDIVISM study. Am J Gastroenterol. 2016 Aug;111(8):1141-6. Tóm lược
25. Donnelly JP, Wang HE, Locke JE, et al. Hospital-onset Clostridium difficile infection among solid organ transplant recipients. Am J Transplant. 2015 Nov;15(11):2970-7. Toàn văn Tóm lược
26. Paudel S, Zacharioudakis IM, Zervou FN, et al. Prevalence of Clostridium difficile infection among solid organ transplant recipients: a meta-analysis of published studies. PLoS One. 2015 Apr 17;10(4):e0124483. Toàn văn Tóm lược
27. Zacharioudakis IM, Ziakas PD, Mylonakis E. Clostridium difficile infection in the hematopoietic unit: a meta- analysis of published studies. Biol Blood Marrow Transplant. 2014 Oct;20(10):1650-4. Toàn văn Tóm lược
28. Phatharacharukul P, Thongprayoon C, Cheungpasitporn W, et al. The risks of incident and recurrent Clostridium difficile-associated diarrhea in chronic kidney disease and end-stage kidney disease patients: a systematic review and meta-analysis. Dig Dis Sci. 2015 Oct;60(10):2913-22. Tóm lược
29. Sanchez TH, Brooks JT, Sullivan PS, et al; Adult/Adolescent Spectrum of HIV Disease Study Group. Bacterial diarrhea in persons with HIV infection, United States, 1992-2002. Clin Infect Dis. 2005 Dec 1;41(11):1621-7. Toàn văn Tóm lược
30. Anand A, Glatt AE. Clostridium difficile infection associated with antineoplastic chemotherapy: a review. Clin Infect Dis. 1993 Jul;17(1):109-13. Tóm lược
31. Southern WN, Rahmani R, Aroniadis O, et al. Postoperative Clostridium difficile-associated diarrhea. Surgery. 2010 Jul;148(1):24-30. Toàn văn Tóm lược
32. Goldenberg JZ, Yap C, Lytvyn L, et al. Probiotics for the prevention of Clostridium difficile-associated diarrhea in adults and children. Cochrane Database Syst Rev. 2017;(12):CD006095. Toàn văn Tóm lược
33. Shen NT, Maw A, Tmanova LL, et al. Timely use of probiotics in hospitalized adults prevents Clostridium difficile infection: a systematic review with meta-regression analysis. Gastroenterology. 2017 Jun;152(8):1889-900;e9. Toàn văn Tóm lược
34. Deschênes P, Chano F, Dionne LL, et al. Efficacy of the World Health Organization-recommended handwashing technique and a modified washing technique to remove Clostridium difficile from hands. Am J Infect Control. 2017 Aug 1;45(8):844-8. Tóm lược
35. Banach DB, Bearman G, Barnden M, et al. Duration of contact precautions for acute-care settings. Infect Control Hosp Epidemiol. 2018 Feb;39(2):127-44. Toàn văn Tóm lược
36. Rutala WA, Weber DJ. Sterilization, high-level disinfection, and environmental cleaning. Infect Dis Clin North Am. 2011 Mar;25(1):45-76. Tóm lược
37. National Institute for Health and Care Excellence. Infection prevention and control. April 2014 [internet publication]. Toàn văn
38. Macleod-Glover N, Sadowski C. Efficacy of cleaning products for C. difficile: environmental strategies to reduce the spread of Clostridium difficile-associated diarrhea in geriatric rehabilitation. Can Fam Physician. 2010 May;56(5):417-23. Toàn văn Tóm lược
39. Kundrapu S, Sunkesula V, Jury LA, et al. Daily disinfection of high-touch surfaces in isolation rooms to reduce contamination of healthcare workers’ hands. Infect Control Hosp Epidemiol. 2012 Oct;33(10):1039-42. Tóm lược
40. Louh IK, Greendyke WG, Hermann EA, et al. Clostridium difficile infection in acute care hospitals: systematic review and best practices for prevention. Infect Control Hosp Epidemiol. 2017 Apr;38(4):476-82. Toàn văn Tóm lược
41. Barbut F, Menuet D, Verachten M, et al. Comparison of the efficacy of a hydrogen peroxide dry-mist disinfection system and sodium hypochlorite solution for eradication of Clostridium difficile spores. Infect Control Hosp Epidemiol. 2009 Jun;30(6):507-14. Tóm lược
42. Nerandzic MM, Cadnum JL, Pultz MJ, et al. Evaluation of an automated ultraviolet radiation device for decontamination of Clostridium difficile and other healthcare-associated pathogens in hospital rooms. BMC Infect Dis. 2010 Jul 8;10:197. Toàn văn Tóm lược
43. Ray AJ, Deshpande A, Fertelli D, et al. A multicenter randomized trial to determine the effect of an environmental disinfection intervention on the incidence of healthcare-associated Clostridium difficile infection. Infect Control Hosp Epidemiol. 2017 Jul;38(7):777-83. Tóm lược
44. Tschudin-Sutter S, Kuijper EJ, Durovic A, et al. Guidance document for prevention of Clostridium difficile infection in acute healthcare settings. Clin Microbiol Infect. 2018 Mar 2 [Epub ahead of print]. Toàn văn Tóm lược
45. Deshpande A, Pasupuleti V, Pant C, et al. Potential value of repeat stool testing for Clostridium difficile stool toxin using enzyme immunoassay? Curr Med Res Opin. 2010 Nov;26(11):2635-41. Toàn văn Tóm lược
46. Debast SB, Bauer MP, Kuijper EJ. European Society of Clinical Microbiology and Infectious Diseases: update of the treatment guidance document for Clostridium difficile infection. Clin Microbiol Infect. 2014 Mar;20(suppl 2):1-26. Toàn văn Tóm lược
47. Public Health England. Clostridium difficile infection: guidance on management and treatment. June 2013 [internet publication]. Toàn văn
48. Beinortas T, Burr NE, Wilcox MH, et al. Comparative efficacy of treatments for Clostridium difficile infection: a systematic review and network meta-analysis. Lancet Infect Dis. 2018 Jul 16. pii: S1473-3099(18)30285-8. Tóm lược
49. Nelson RL, Suda KJ, Evans CT. Antibiotic treatment for Clostridium difficile-associated diarrhoea in adults. Cochrane Database Syst Rev. 2017;(3):CD004610. Toàn văn Tóm lược
50. Louie TJ, Miller MA, Mullane KM, et al. Fidaxomicin versus vancomycin for Clostridium difficile infection. N Engl J Med. 2011 Feb 3;364(5):422-31. Toàn văn Tóm lược
51. Cornely OA, Crook DW, Esposito R, et al; OPT-80-004 Clinical Study Group. Fidaxomicin versus vancomycin for infection with Clostridium difficile in Europe, Canada, and the USA: a double-blind, non-inferiority, randomised controlled trial. Lancet Infect Dis. 2012 Apr;12(4):281-9. Tóm lược
52. Drekonja DM, Butler M, MacDonald R, et al. Comparative effectiveness of Clostridium difficile treatments: a systematic review. Ann Intern Med. 2011 Dec 20;155(12):839-47. Toàn văn Tóm lược
53. Crook DW, Walker AS, Kean Y, et al. Fidaxomicin versus vancomycin for Clostridium difficile infection: meta- analysis of pivotal randomized controlled trials. Clin Infect Dis. 2012 Aug;55(suppl 2):S93-103. Toàn văn Tóm lược
54. Lancaster JW, Matthews SJ. Fidaxomicin: the newest addition to the armamentarium against Clostridium difficile infections. Clin Ther. 2012 Jan;34(1):1-13. Tóm lược
55. Whitman CB, Czonowski QA. Fidaxomicin for the treatment of Clostridium difficile infections. Ann Pharmacother. 2012 Feb;46(2):219-28. Tóm lược
56. Cornely OA, Miller MA, Louie TJ, et al. Treatment of first recurrence of Clostridium difficile infection: fidaxomicin versus vancomycin. Clin Infect Dis. 2012 Aug;55(suppl 2):S154-61. Toàn văn Tóm lược
57. Goldstein EJ, Citron DM, Sears P, et al. Comparative susceptibilities to fidaxomicin (OPT-80) of isolates collected at baseline, recurrence, and failure from patients in two phase III trials of fidaxomicin against Clostridium difficile infection. Antimicrob Agents Chemother. 2011 Nov;55(11):5194-9. Toàn văn Tóm lược
58. Khanna S, Shin A, Kelly CP. Management of Clostridium difficile infection in inflammatory bowel disease: expert review from the Clinical Practice Updates Committee of the AGA Institute. Clin Gastroenterol Hepatol. 2017 Feb;15(2):166-74. Toàn văn Tóm lược
59. Jaber MR, Olafsson S, Fung WL, et al. Clinical review of the management of fulminant Clostridium difficile infection. Am J Gastroenterol. 2008 Dec;103(12):3195-203;quiz 3204. Tóm lược
60. Stevens VW, Nelson RE, Schwab-Daugherty EM, et al. Comparative effectiveness of vancomycin and metronidazole for the prevention of recurrence and death in patients with Clostridium difficile infection. JAMA Intern Med. 2017 Apr 1;177(4):546-53. Tóm lược
61. van Nood E, Vrieze A, Nieuwdorp M, et al. Duodenal infusion of donor feces for recurrent Clostridium difficile. N Engl J Med. 2013 Jan 31;368(5):407-15. Toàn văn Tóm lược
62. Lee CH, Steiner T, Petrof EO, et al. Frozen vs fresh fecal microbiota transplantation and clinical resolution of diarrhea in patients with recurrent Clostridium difficile infection: a randomized clinical trial. JAMA. 2016 Jan 12;315(2):142-9. Toàn văn Tóm lược
63. Hota SS, Sales V, Tomlinson G, et al. Oral vancomycin followed by fecal transplantation versus tapering oral vancomycin treatment for recurrent Clostridium difficile infection: an open-label, randomized controlled trial. Clin Infect Dis. 2017 Feb 1;64(3):265-71. Toàn văn Tóm lược
64. Moayyedi P, Yuan Y, Baharith H, et al. Faecal microbiota transplantation for Clostridium difficile-associated diarrhoea: a systematic review of randomised controlled trials. Med J Aust. 2017 Aug 21;207(4):166-72. Toàn văn Tóm lược
65. Tang G, Yin W, Liu W. Is frozen fecal microbiota transplantation as effective as fresh fecal microbiota transplantation in patients with recurrent or refractory Clostridium difficile infection: a meta-analysis? Diagn Microbiol Infect Dis. 2017 Aug;88(4):322-9. Tóm lược
66. Furuya-Kanamori L, Doi SA, Paterson DL, et al. Upper versus lower gastrointestinal delivery for transplantation of fecal microbiota in recurrent or refractory Clostridium difficile infection: a collaborative analysis of individual patient data from 14 studies. J Clin Gastroenterol. 2017 Feb;51(2):145-50. Tóm lược
67. Wang S, Xu M, Wang W, et al. Systematic review: adverse events of fecal microbiota transplantation. PLoS One. 2016 Aug 16;11(8):e0161174. Toàn văn Tóm lược
68. Chapman BC, Moore HB, Overbey DM, et al. Fecal microbiota transplant in patients with Clostridium difficile infection: a systematic review. J Trauma Acute Care Surg. 2016 Oct;81(4):756-64. Tóm lược
69. Khoruts A, Rank KM, Newman KM, et al. Inflammatory bowel disease affects the outcome of fecal microbiota transplantation for recurrent Clostridium difficile infection. Clin Gastroenterol Hepatol. 2016 Oct;14(10):1433-8. Toàn văn Tóm lược
70. Bafeta A, Yavchitz A, Riveros C, et al. Methods and reporting studies assessing fecal microbiota transplantation: a systematic review. Ann Intern Med. 2017 Jul 4;167(1):34-9. Tóm lược
71. Wilcox MH, Gerding DN, Poxton IR, et al. Bezlotoxumab for prevention of recurrent Clostridium difficile infection. N Engl J Med. 2017 Jan 26;376(4):305-17. Toàn văn Tóm lược
72. National Institute for Health and Care Excellence. Preventing recurrence of Clostridium difficile infection: bezlotoxumab. June 2017 [internet publication]. Toàn văn
73. Locher HH, Seiler P, Chen X, et al. In vitro and in vivo antibacterial evaluation of cadazolid, a new antibiotic for treatment of Clostridium difficile infections. Antimicrob Agents Chemother. 2014;58(2):892-900. Toàn văn Tóm lược
74. Vickers RJ, Tillotson GS, Nathan R, et al. Efficacy and safety of ridinilazole compared with vancomycin for the treatment of Clostridium difficile infection: a phase 2, randomised, double-blind, active-controlled, non-inferiority study. Lancet Infect Dis. 2017 Jul;17(7):735-44. Toàn văn Tóm lược
75. Lee CH, Patino H, Stevens C, et al. Surotomycin versus vancomycin for Clostridium difficile infection: phase 2, randomized, controlled, double-blind, non-inferiority, multicentre trial. J Antimicrob Chemother. 2016 Oct;71(10):2964-71. Toàn văn Tóm lược
76. McCoy RM, Klick A, Hill S, et al. Luminal toxin-binding agents for Clostridium difficile infection. J Pharm Pract. 2016 Aug;29(4):361-7. Tóm lược
77. Bézay N, Ayad A, Dubischar K, et al. Safety, immunogenicity and dose response of VLA84, a new vaccine candidate against Clostridium difficile, in healthy volunteers. Vaccine. 2016 May 17;34(23):2585-92. Tóm lược
78. Almroth S, Mohale M, Latham MC. Grandma ahead of her time: traditional ways of diarrhoea management in Lesotho. J Diarrhoeal Dis Res. 1997 Sep;15(3):167-72. Tóm lược
Tuyên bố miễn trách nhiệm
Bên ngoài Hoa Kỳ và Canada. BMJ Publishing Group Ltd (”BMJ Group”) nỗ lực để đảm bảo rằng các thông tin được cung cấp là chính xác và cập nhật, nhưng chúng tôi và cả những người cấp giấy phép của chúng tôi, là những người cung cấp các nội dung nhất định có liên kết với nội dung của chúng tôi hoặc có thể truy cập được từ nội dung của chúng tôi, đều không đảm bảo điều đó. BMJ Group không ủng hộ hay xác nhận việc sử dụng bất kỳ loại thuốc hay trị liệu nào trong đó và BMJ Group cũng không thực hiện chẩn đoán cho các bệnh nhân. Các chuyên gia y tế cần sử dụng những cân nhắc chuyên môn của mình trong việc sử dụng thông tin này và chăm sóc cho bệnh nhân của họ và thông tin trong này không được coi là sự thay thế cho việc đó.
các phương pháp chẩn đoán, điều trị, liên lạc theo dõi, thuốc và bất kỳ chống chỉ định hay phản ứng phụ nào. Ngoài ra, các tiêu chuẩn và thực hành y khoa đó thay đổi khi có thêm số liệu, và quý vị nên tham khảo nhiều nguồn khác nhau. Chúng tôi đặc biệt khuyến nghị người dùng nên xác minh độc lập các chẩn đoán, điều trị và theo dõi liên lạc được đưa ra, đồng thời đảm bảo rằng thông tin đó là phù hợp cho bệnh nhân trong khu vực của quý vị. Ngoài ra, liên quan đến thuốc kê toa, chúng tôi khuyên quý vị nên kiểm tra trang thông tin sản phẩm kèm theo mỗi loại thuốc để xác minh các điều kiện sử dụng và xác định bất kỳ thay đổi nào về liều dùng hay chống chỉ định, đặc biệt là nếu dược chất được cho sử dụng là loại mới, ít được sử dụng, hay có khoảng trị liệu hẹp. Quý vị phải luôn luôn kiểm tra rằng các loại thuốc được dẫn chiếu có giấy phép để sử dụng cho mục đích được nêu và trên cơ sở được cung cấp trong tình trạng “hiện có” như được nêu, và trong phạm vi đầy đủ được pháp luật cho phép BMJ Group và những người cấp giấy phép của mình không chịu bất kỳ trách nhiệm nào cho bất kỳ khía cạnh chăm sóc sức khỏe nào được cung cấp với sự hỗ trợ của thông tin này hay việc sử dụng nào khác của thông tin này.
Xem đầy đủ Các Điều khoản và Điều kiện Sử dụng Trang Web. Liên hệ với chúng tôi
+ 44 (0) 207 111 1105
support@bmj.com
BMJ
BMA House Tavistock Square London
WC1H 9JR UK