Bệnh huyết học
Tiếp cận điều trị rối loạn lipid máu theo từng bước
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
Nhà thuốc Ngọc Anh – Bài viết Tiếp cận điều trị rối loạn lipid máu theo từng bước được biên soạn bởi bác sĩ Nguyễn Thế Bảo – Trường Đại học Y Dược Cần Thơ để tải về file pdf mời các bạn click vào link ở đây.
I. CHẨN ĐOÁN RỐI LOẠN LIPID MÁU
1. Lâm sàng:
– Khai thác tiền sử gia đình về rối loạn lipid máu.
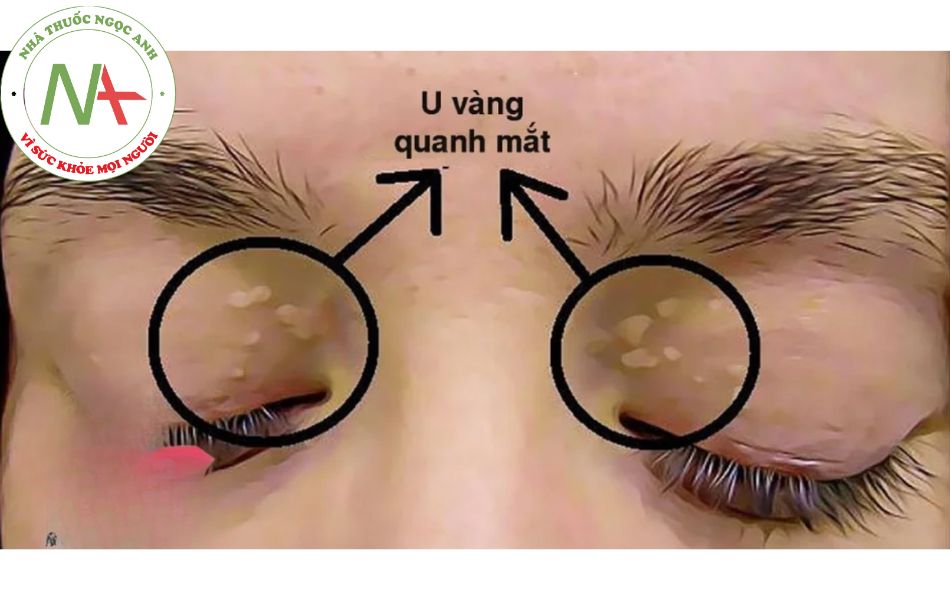
– Triệu chứng thường không đặc hiệu: có thể thấy u vàng ở mi mắt, da, gân Achiles, dây chằng cân cơ (xanthelasma) trong rối loạn lipid máu có tính chất gia đình.
– Tìm các yếu tố nguy cơ như các bệnh đồng mắc (tăng huyết áp, đái tháo đường, béo phì), chế độ ăn uống, lối sống tĩnh tại, hút thuốc, uống rượu…
– Tìm các bệnh lý gây rối loạn lipid máu thứ phát (nếu có): suy giáp, đái tháo đường, hội chứng thận hư hay do thuốc (corticosteroid, estrogen, progestin, steroid, androgen, cyclosporine, retinoid…).
– Các triệu chứng khi đã có biến chứng (bệnh do xơ vữa động mạch): bệnh lý động mạch vành, mạch ngoại vi, mạch não.
2.Xét nghiệm:
Chẩn đoán rối loạn lipid máu khi có một trong các tiêu chuẩn sau:
- Tăng cholesterol: ≥ 200 mg/dl (5,2 mmol/l) – Tăng LDL-C: ≥ 130 mg/dl (3,4 mmol/l).
- Giảm HDL-C: < 40 mg/dl (1 mmol/l).
- Tăng triglyceride: ≥ 200 mg/dl (2,3 mmol/l).
Rối loạn kiểu hỗn hợp: khi tăng cholesterol + tăng triglyceride.
3.Thời điểm tầm soát:
Khi ≥ 20 tuổi, thực hiện bilan lipid máu (cholesterol toàn phần, LDL-c, HDL-c, triglyceride) sau khi nhịn đói 12 giờ → thực hiện lại mỗi 5 năm nếu trong giới hạn bình thường và không có biến cố tim mạch.
Bệnh nhân nhập viện với hội chứng vành cấp thì nên xét nghiệm bilan lipid máu trong vòng 24 giờ nếu chưa rõ giá trị các thông số lipid máu gần đây.
II. CHIẾN LƯỢC TIẾP CẬN ĐIỀU TRỊ RỐI LOẠN LIPID MÁU
1. Nắm vững nguyên tắc điều trị
Tiến hành phân tầng nguy cơ bệnh nhân → Từ đó xác định đích điều trị VÀ chiến lược điều trị.
Loại trừ nguyên nhân rối loạn lipid máu và kiểm soát tốt các yếu tố nguy cơ gây rối loạn lipid máu.
Khi điều trị bằng thuốc, dựa trên các bằng chứng lâm sàng hiện tại để đạt hiệu quả tối ưu: Vai trò của STATIN vẫn là cốt lõi điều trị giảm biến cố BTMXV.
Có kế hoạch theo dõi:
- Về tuân thủ điều trị.
- Về hiệu quả điều trị: Theo dõi diễn tiến của các bệnh lý, biến chứng kèm theo + kết quả xét nghiệm lipid máu để chỉnh liều và thay đổi thuốc.
- Về tác dụng không mong muốn của thuốc.
2. Thực hiện các bước như trên:
Bước 1: Phân tầng nguy cơ bệnh nhân
Nguy cơ rất cao:
- Có bằng chứng của bệnh tim mạch xơ vữa: . Trên lâm sàng: hội chứng vành cấp, tiền sử NMCT, cơn đau thắt ngực ổn định, tiền căn tái thông động mạch, đột quỵ não, cơn TIA hoặc bệnh động mạch ngoại biên do xơ vữa . Trên hình ảnh học: mảng xơ vữa lớn khi chụp mạch vành hoặc trên CT-scan (bệnh mạch vành đa nhánh với 2 nhánh động mạch lớn ở ngoại tâm mạc hẹp trên 50%) hoặc mảng xơ vữa lớn khi siêu âm động mạch cảnh.
- Đái tháo đường có tổn thương cơ quan đích: microalbumin niệu, bệnh thận do đái tháo đường, bệnh thần kinh do đái tháo đường.
- Bệnh thận mạn với GFR <30 ml/phút/m2 da + Tính theo thang điểm SCORE ≥ 10% về nguy cơ tử vong tim mạch trong 10 năm.
- Tiền căn RL lipid máu gia đình có bệnh tim mạch xơ vữa (BTMXV) hoặc kèm YTNC quan trọng khác.
Nguy cơ cao:
- Có kèm một trong các yếu tố sau: TC > 8 mmol/L (>310 mg/dl), LDL-c >4,9 mmol/L (190 mg/dl) hoặc huyết áp ≥ 180/110 mmHg.
- Đái tháo đường chưa có tổn thương cơ quan đích, mà thời gian mắc ĐTĐ >10 năm hoặc có kèm YTNC khác.
- Bệnh thận mạn với GFR từ 30-50 ml/phút/m2 da.
- Điểm SCORE từ 5-10% + Tiền căn RL lipid máu gia đình không kèm YTNC quan trọng khác.
Nguy cơ trung bình:
- Bệnh nhân trẻ tuổi có mắc ĐTĐ (type 1 < 35 tuổi, type 2 < 50 tuổi) mà thời gian mắc <10 năm và không kèm YTNC khác.
- Điểm SCORE từ 1-5% – Nguy cơ thấp: Điểm SCORE <1%.
Bước 2: Xác định đích điều trị và chiến lược điều trị:
Xác định đích điều trị:
- LDL-c là đích điều trị chính.
- Có kế hoạch can thiệp khi có tăng triglyceride nhiều.
- Non HDL và Apo-B là mục tiêu phụ (lưu ý: mục tiêu của non-HDL được tính bằng mục tiêu của LDL-c tương ứng + 0,8 mmol/L).
- Đích điều trị: Nhóm nguy cơ rất cao: LDL < 1,4 mmol/l (55 mg/dl) . Nhóm nguy cơ cao: LDL < 1,8 mmol/l (70 mg/dl) . Nhóm nguy cơ vừa: LDL < 2,6 mmol/l (100 mg/dl) . Nhóm nguy cơ thấp: LDL < 3 mmol/l (116 mg/dl) Lưu ý: Khi bệnh nhân đang điều trị liều statin tối đa dung nạp được mà xảy ra biến cố tim mạch lần 2 (không cần phải cùng loại biến cố lần đầu) trong vòng 2 năm => cân nhăc LDL < 1 mmol/L.
Xác định chiến lược điều trị (tóm gọn những tình huống quan trọng trong bảng của ESC 2019)
- Nguy cơ rất cao => *Kết hợp điều trị thuốc + thay đổi lối sống khi LDL >1,4 mmol/L.
- Nguy cơ cao => *Kết hợp điều trị thuốc + thay đổi lối sông khi LDL >1,8 mmol/L.
- Nguy cơ trung bình => *Kết hợp điều trị thuốc + thay đổi lối sống khi LDL >3 mmol/L.
- Nguy cơ thấp => *Kết hợp điều trị thuốc + thay đổi lối sống khi LDL >4,9 mmol/l Lưu ý: *có thể cân nhắc điều trị thuốc ở ngưỡng LDL thấp hơn tùy cá thể hóa từng bệnh nhân.
Bước 3: Loại trừ nguyên nhân thứ phát và kiểm soát các yếu tố nguy cơ
Có kế hoạch điều chỉnh, loại trừ, kiểm soát tốt các nguyên nhân thứ phát gây RL lipid máu đã kể trên Kiểm soát các yếu tố nguy cơ. Mục tiêu thay đổi lối sống như sau:
- Bỏ thuốc lá.
- Hạn chế rượu bia tối đa.
- Chế độ ăn kiêng, giảm tiêu thụ chất béo bão hòa, tăng khẩu phần ăn hoa quả, rau, các loại đậu và cá; giảm ăn ngọt, nước uống có đường, mỡ động vật.
- Tập thể dục: 30-60 phút mỗi ngày, ít nhất 5 lần/tuần, không được nghỉ liên tục 2 ngày.
- Kiểm soát cân nặng, vòng bụng: BMI duy trì 20-25 kg/m2, vòng bụng <94 cm (với nam) và < 80 cm (với nữ).
- Kiểm soát huyết áp < 140/90 mmHg.
- Kiểm soát HbA1C <7%.
Bước 4: Điều trị bằng thuốc:
Trước khi đi vào vấn đề chính, dưới đây là những thông tin cơ bản về một số thuốc trong điều trị rối loạn lipid máu (xem kĩ nhóm statin và nhóm fibrate nhé!!).
Thuốc ức chế men HMG-coA reductase (nhóm statin):
- Cơ chế: ức chế enzyme HMG-coA reductase (chịu trách nhiệm chuyển đổi HMG-coA thành tiền chất của sterol, bao gồm cholesterol) → giảm tổng hợp cholesterol ở gan + kích thích tổng hợp thụ thể LDL ở gan → giảm LDL trong máu.
- Dược động học: tất cả statin được hấp thu nhanh, tối đa 4 giờ. Atorvastatin và rosuvastatin có thời gian bán hủy dài hơn → hiệu quả giảm cholesterol kéo dài cả ngày; statin chuyển hóa tại gan thông qua hệ CYP P450; không dùng thuốc quá gần bữa ăn và có thể dùng 1 lần trong ngày trước khi đi ngủ.
- Phân loại statin theo mức độ giảm LDL-c:
| Bảng phân loại statin theo mức độ giảm LDL-c | ||
| Statin cường độ cao (giảm 50% LDL-c) | Statin cường độ trung bình (giảm 30- 50% LDL-c) | Statin cường độ thấp (giảm 30% LDLc) |
| Rosuvastatin 20-40mg | Rosuvastatin 5-10mg | |
| Atorvastatin 40-80mg | Atorvastatin 10-20mg | |
| Simvastatin 20-40mg | Simvastatin 10mg | |
| Pravastatin 20-40mg | Pravastatin 10-20mg | |
| Lovastatin 40mg | Lovastatin 20mg | |
| Pitavastatin 2-4mg | Pitavastatin 1mg | |
| Fluvastatin 80mg | Fluvastatin 20-40mg | |
- Chống chỉ định: Phụ nữ mang thai và cho con bú, Bệnh gan giai đoạn hoạt động/tăng men gan kéo dài chưa giải thích được.
- Tác dụng không mong muốn: Tổn thương cơ (nói rõ ở bước 5), Tổn thương gan (nói rõ ở bước 5), Tăng nguy cơ mắc đái tháo đường: cơ chế làm giảm tiết insulin ở tụy và giảm nhạy cảm insulin ở ngoại biên.
- Một số statin quan trọng trên lâm sàng: Atorvastatin: khởi đầu liều 10-20 mg hoặc cao hơn (tối đa 80 mg) tùy theo cường độ statin cần dùng để điều trị, Sử dụng liều duy nhất bất cứ lúc nào trong ngày, không phân biệt thời gian bữa ăn → xét nghiệm bilan lipid máu và chỉnh liều mỗi 2-4 tuần. Không cần chỉnh liều trên bệnh nhân suy thận, tránh dùng chung với cyclosporine, thuốc ức chế protease HIV. Khi dùng chung với clarithromycin, itraconazole → giới hạn liều ở mức 20mg/ngày . Rosuvastatin: khởi đầu liều 5-20 mg, hoặc cao hơn (tối đa 40mg) tùy theo cường độ statin cần dùng để điều trị. Sử dụng liều duy nhất bất cứ lúc nào trong ngày, không phân biệt thời gian bữa ăn → XN bilan lipid máu và chỉnh liều mỗi 2-4 tuần. Chuyển hóa qua men CYP450-2C9 nên ít tương tác thuốc hơn. Lưu ý ở bệnh nhân suy thận với GFR <30ml/phút/m2 da → bắt đầu liều 5mg/ngày và không quá 10mg/ngày.
Thuốc nhóm fibrate:
- Là liệu pháp đầu tiên cho BN tăng triglyceride máu nặng.
- Cơ chế: ức chế tổng hợp acid béo + tăng dị hóa acid béo + giảm sản xuất triglyceride và giảm VLDL.
- Có 2 thuốc chính: Gemfibrozil: hấp thu hoàn toàn sau uống, đạt đỉnh 1-2h sau dùng thuốc, nên dùng trước ăn 30 phút; thời gian bán thải # 1h. Liều dùng: 600 mg 2 lần/ngày, trước ăn sáng và tối 30 phút (giảm còn 600mg/ngày khi GFR <60 ml/phút và không dùng khi chạy thận nhân tạo), thận trọng và giảm liều thuốc chống đông máu khi dùng chung. Fenofibrate: bài tiết 60% qua nước tiểu, 25% qua phân, chuyển hóa bởi CYP P450, thời gian bán hủy # 20h. Liều dùng ban đầu với acid fenofibric là 135 mg mỗi ngày một lần (giảm liều khi GFR <60 và không nên dùng khi GFR <30 ml/phút/m2 da).
- Chống chỉ định: . Tiền sử bệnh gan đang hoạt động, suy thận nặng, bệnh túi mật . Chống chỉ định kết hợp gemfibrozil với thuốc hạ đường huyết . Chống chỉ định fibrate trong thai kỳ và cho con bú.
- Tác dụng không mong muốn: . Tổn thương cơ: đặc biệt khi kết hợp chung với statin . Tăng men gan → theo dõi định kỳ và ngừng điều trị nếu > 3 lần giới hạn trên . Fenofibrate làm tăng nồng độ creatinin → theo dõi định kỳ ở bệnh nhân suy thận.
Thuốc Ezetimibe:
- Cơ chế: Ức chế hấp thụ cholesterol ở ruột non.
- Dược động học: chuyển hóa chủ yếu ở ruột non và gan; thời gian bán hủy # 22 giờ, bài tiết phần lớn qua phân và một phần qua nước tiểu. Đáp ứng tối đa thường đạt trong 2 tuần và duy trì trong suốt thời gian điều trị.
- Chỉ định: có thể dùng phối hợp với statin để giảm thêm LDL-c.
- Chống chỉ định: Suy gan trung bình/nặng (Child-pugh >7) .
- Phụ nữ mang thai: Liều dùng: 10 mg mỗi ngày một lần. Không cần chỉnh liều ở BN suy gan hoặc suy thận nhẹ hay ở BN lớn tuổi + Tác dụng không mong muốn: triệu chứng đường tiêu hóa, đau cơ…
Thuốc gắn acid mật:
- Cơ chế: liên kết acid mật và muối mật trong ruột non, làm mất vai trò hấp thu chất béo của các chất này → giảm hấp thu cholesterol, đồng thời làm tăng chuyển hóa cholesterol ở gan thành acid mật + tăng thụ thể LDL ở gan → giảm cholesterol máu.
- Chỉ định: đơn trị liệu giảm LDL hoặc kết hợp statin ở BN tăng lipid máu nguyên phát.
- Chống chỉ định: Tiền sử tắc ruột, tắc mật, tăng triglyceride ≥ 500 mg/dl, tiền sử viêm tụy do triglyceride, phụ nữ có thai…
- Liều dùng và tác dụng không mong muốn: các bạn tự tham khảo thêm.
Niacin:
- Cơ chế tác dụng: giảm hoạt hóa lipase → giảm acid béo tự do giải phóng từ tế bào mỡ cho gan để sản xuất triglyceride và VLDL → giảm LDL.
- Hiện nay không còn dùng nhóm này trong điều trị rối loạn lipid máu.
Thuốc dạng kháng thể đơn dòng ức chế enzyme PCSK9:
- Cơ chế tác dụng: tương tác với vị trí gắn của enzyme PCSK9 (vai trò thoái giáng thụ thể LDL ở gan) trên thụ thể LDL → tăng bộc lộ thụ thể LDL → giảm nồng độ LDL trong máu.
- Thuốc hiện có: Alirocumab và Evolocumab.
- Chỉ định: tăng cholesterol máu gia đình loại đồng hợp tử; rối loạn lipid máu tiên phát khó đáp ứng với thuốc khác; kiểm soát nồng độ LDL khó khống chế bởi statin đơn thuần và dự phòng biến cố tim mạch thứ phát.
- Liều dùng: Alirocumab (Praluent) 75-150 mg mỗi 2 tuần dạng bút tiêm hoặc Evolocumab (Repatha) 140mg mỗi 2 tuần hay 420mg mỗi tháng.
- Tác dụng không mong muốn: Tác dụng phụ trên da: phát ban, mày đay, sưng, đau, viêm mạch, bầm tím, Triệu chứng thần kinh: lú lẩn, ngủ gà, khó tập trung, Cảm lạnh, cúm, đau lưng,… Tăng đề kháng insulin và đái tháo đường.
Ngoài ra, hiện còn có một số thuốc mới đang trong quá trình nghiên cứu như: Thuốc ức chế enzyme CETP, thuốc ức chế trực tiếp apoB, thuốc ức chế MTP,…
Vì sao vai trò của statin là cốt lõi trong điều trị giảm biến cố BTMXV?
- Các bằng chứng lâm sàng từ các thử nghiệm, nghiên cứu cho thấy việc giảm LDL-C bằng liệu pháp statin để phòng ngừa tiên phát cũng như phòng ngừa thứ phát rất có hiệu quả trong việc giảm các biến cố tim mạch.
- Statin khuyến cáo là lựa chọn đầu tay để điều trị rối loạn lipid máu ở bệnh nhân đái tháo đường có nồng độ LDL-c cao.
- Statin hoặc statin kết hợp ezetimibe ở bệnh nhân CKD giai đoạn 3-5 không phụ thuộc lọc máu (do được xếp vào nhóm nguy cơ tim mạch cao hoặc rất cao).
- Statin làm giảm nguy cơ đột quỵ trong phòng ngừa tiên phát và thứ phát nhồi máu não, không làm tăng nguy cơ xuất huyết não và mức độ nặng của xuất huyết não.
- Statin làm giảm triệu chứng đau cách hồi, giảm tỷ lệ tái thông mạch máu ngoại biên và giảm tỷ lệ cắt cụt chi ở bệnh lý động mạch ngoại biên do xơ vữa.
Từ các bằng chứng trên, ta cần nhớ 4 tình huống nên bắt đầu liệu pháp statin:
- Bệnh nhân có BTMXV trên lâm sàng: Theo chiến lược tiếp cận như trên thì mục tiêu điều trị là LDL giảm ≥ 50% so với nền (khi chưa điều trị) hoặc LDL < 1,4 mmol/l. Sử dụng statin cường độ cao → khi statin đã đạt liều tối đa (hoặc liều cao nhất bệnh nhân có thể dung nạp được) mà chưa đạt mục tiêu → cân nhắc bổ sung thêm ezetimibe trước khi dùng thuốc ức chế PCSK9.
- LDL-c ≥ 190 mg/dL: Theo chiến lược tiếp cận như trên thì mục tiêu điều trị là LDL giảm ≥ 50% so với nền (khi chưa điều trị) hoặc LDL < 1,8 mmol/L. Sử dụng statin cường độ cao → các bước sau tương tự trường hợp trên.
- Đái tháo đường từ 40-75 tuổi kèm LDL > 1,8 mmol/L: Sử dụng statin cường độ cao, đích điều trị đánh giá theo phân tầng như trên tùy theo đái tháo đường có tổn thương cơ quan đích hay chưa.
- Bệnh nhân từ 40-75 tuổi với nguy cơ mắc BTMXV kèm LDL từ 1,8-4,9 mmol/L => Cân nhắc điều trị statin cường độ trung bình hoặc cường độ cao cá thể hóa tùy theo mức độ nguy cơ mắc BTMXV và mức LDL của BN.
Một số tình huống thường gặp khác:
Ở bệnh nhân lớn tuổi:
- Dự phòng thứ phát khi đã mắc BTMXV giống như ở người trẻ tuổi.
- Ở BN >75 tuổi có thể ngừng statin khi chức năng sống của BN (bao gồm thể chất và nhận thức) suy giảm, có nhiều bệnh đồng mắc, kỳ vọng sống không cao.
Bệnh thận tiến triển cần phải lọc máu và đang sử dụng statin => vẫn tiếp tục dùng nhưng nếu chưa dùng trước đó thì không nên khởi trị liệu pháp statin trên nhóm BN này.
Bệnh nhân có kèm tăng triglyceride máu:
- Là yếu tố nguy cơ độc lập với tim mạch.
- Thường thấy trong hội chứng chuyển hóa và có rất nhiều nguyên nhân tiềm ẩn như béo phì, suy thận, đái tháo đường, sử dụng corticosteroid, beta-blocker.
- Phân mức độ: Bình thường <150 mg/dl, Bình thường cao: 150-199 mg/dl, Cao: 200-499 mg/dl, Rất cao: >=500 mg/dl. Theo Endocrine Society thì phân thêm 2 độ nữa: Nghiêm trọng: 1000-1999 mg/dl (từ mức này nguy cơ cao mắc viêm tụy cấp do tăng triglyceride), Rất nghiêm trọng: ≥ 2000 mg/dl.
- Điều trị: . Từ mức rất cao (500 mg/dl) trở lên sẽ kết hợp điều trị bằng chế độ ăn hạn chế tối đa chất béo, tăng cường luyện tập thể lực, giảm cân và kết hợp thuốc (fibrate, omega-3) . Dưới mức rất cao: vẫn lấy LDL là đích điều trị chính!
Bệnh nhân có kèm giảm HDL-c: Chủ yếu thay đổi lối sống và điều chỉnh các nguyên nhân (đặc biệt là các thuốc gây giảm HDL-c).
Bước 5: Theo dõi điều trị
*Theo dõi sự tuân thủ của bệnh nhân về thuốc và thay đổi lối sống
*Theo dõi hiệu quả điều trị:
- Trước khi đạt mục tiêu: Xét nghiệm bilan lipid máu mỗi 4-12 tháng sau khi khởi trị hoặc sau mỗi lần thay đổi/phối hợp thuốc hạ lipid máu. Khi đã đạt mục tiêu: Xét nghiệm bilan lipid máu hàng năm (trừ khi BN bỏ trị hoặc có các bệnh lý đi kèm/nguy cơ khác cần phải theo dõi thường xuyên hơn).
*Theo dõi tác dụng không mong muốn:
- Bệnh cơ do statin/fibrate: Theo dõi các triệu chứng: đau mỏi, căng cứng cơ, đái đỏ (đái myoglobin).
- Theo dõi xét nghiệm CK: Trước khi điều trị (nếu CK tăng > 4 lần giới hạn trên thì không khởi trị → tìm nguyên nhân, giải quyết nguyên nhân và XN lại) => không cần theo dõi thường quy, chỉ XN theo dõi khi BN có các triệu chứng kể trên.
- Cần đặc biệt lưu ý trên các đối tượng có nguy cơ cao: người lớn tuổi, nhiều bệnh lý nội khoa, bệnh gan, thận, cơ kèm theo bất kể nồng độ CK là bao nhiêu!.
- Cách xử trí khi có triệu chứng ở cơ/tăng CK . CK > 10 lần so với giới hạn trên => ngưng statin + kiểm tra chức năng thận + đo lại CK mỗi 2 tuần . 4 lần < CK < 10 lần + không triệu chứng => tiếp tục sử dụng + kiểm tra lại CK mỗi 2-6 tuần . 4 lần < CK < 10 lần + có triệu chứng => ngưng statin + kiểm tra lại CK => chỉ bắt đầu lại statin với liều thấp hơn (hoặc đổi statin khác hay kết hợp với nhóm thuốc khác) khi CK đã trở về bình thường . CK tăng nhưng < 4 lần: nếu không có triệu chứng => tiếp tục dùng; nếu có triệu chứng thì theo dõi CK thường xuyên, khi triệu chứng vẫn còn tiếp diễn => ngưng và đánh giá sử dụng lại sau 6 tuần
Tăng nồng độ AST/ALT:
- Không phản ánh tổn thương hủy tế bào gan thực sự và hầu như không bao giờ tiến triển gây ảnh hưởng đến chức năng gan => Không khuyến cáo theo dõi định kỳ ở BN không có triệu chứng.
- Theo dõi tiến hành 1 lần duy nhất sau 8-12 tuần kể từ khi khởi trị/sau khi nâng liều statin.
- Cách xử trí khi có tăng men gan: Nếu ALT tăng < 3 lần => tiếp tục dùng và kiểm tra lại sau 4-6 tuần, Nếu ALT tăng >= 3 lần => ngưng statin hoặc giảm liều và theo dõi men gan trong 4-6 tuần => sử dụng lại với liều thấp hơn một cách thận trọng khi men gan về bình thường.
Xem thêm: Hạ Natri máu: Nguyên nhân, chẩn đoán và điều trị – Bác sĩ Nguyễn Thế Bảo
Tài liệu tham khảo:
2019 ESC/EAS Guidelines for the management of dyslipidaemias . Basic and clinical pharmacology 13th.
(2018), Bertram G. Katzung.
Lâm sàng tim mạch học (2019), PGS. Phạm Mạnh Hùng.
The Washington Manual of Medical Therapeutics 36th (2019).
Thuốc tim mạch trong thực hành lâm sàng (2020), PGS. Phạm Mạnh Hùng.