


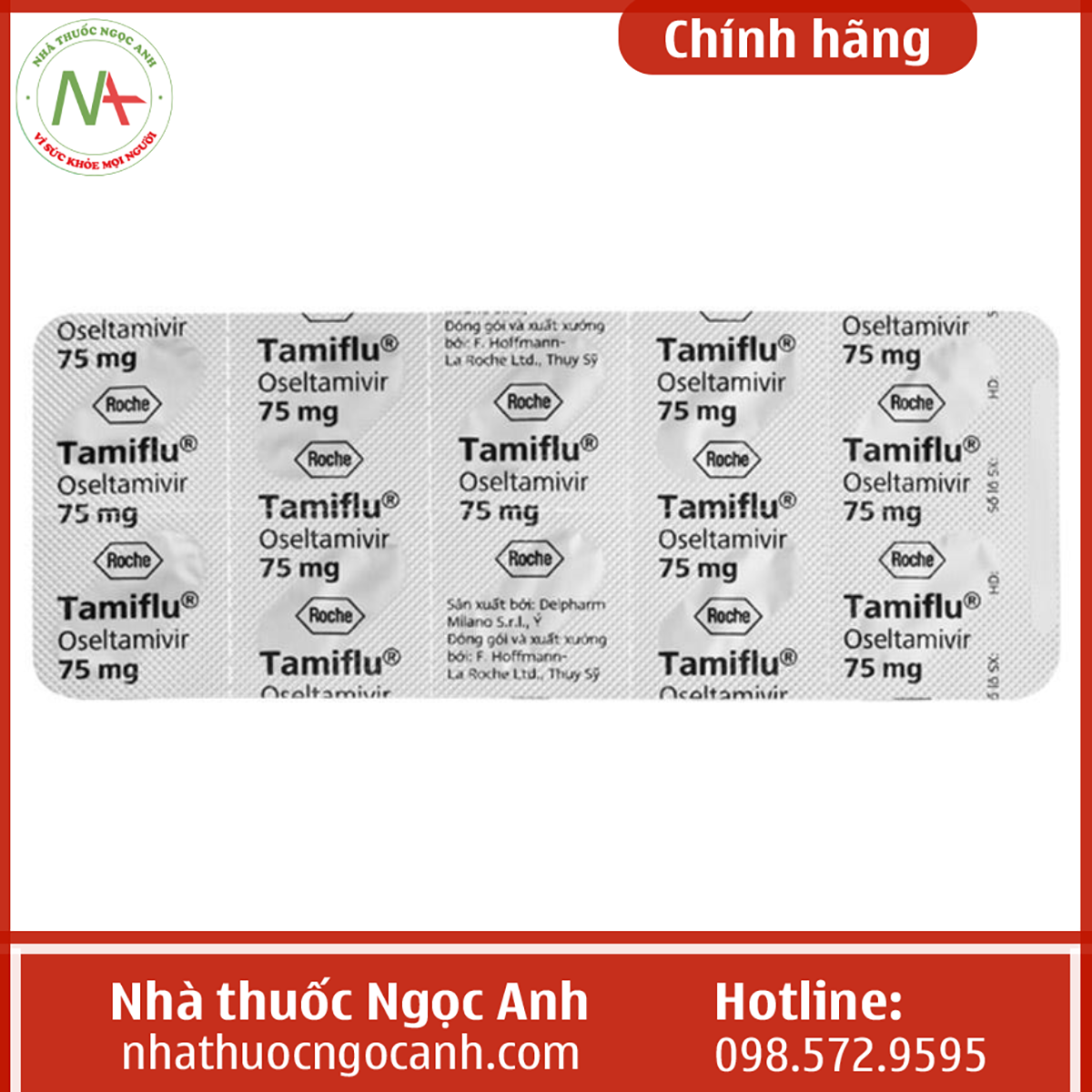
Tamiflu 75 mg
Thuốc kê đơn
Thành phần Oseltamivir
Hàm lượng 75mg
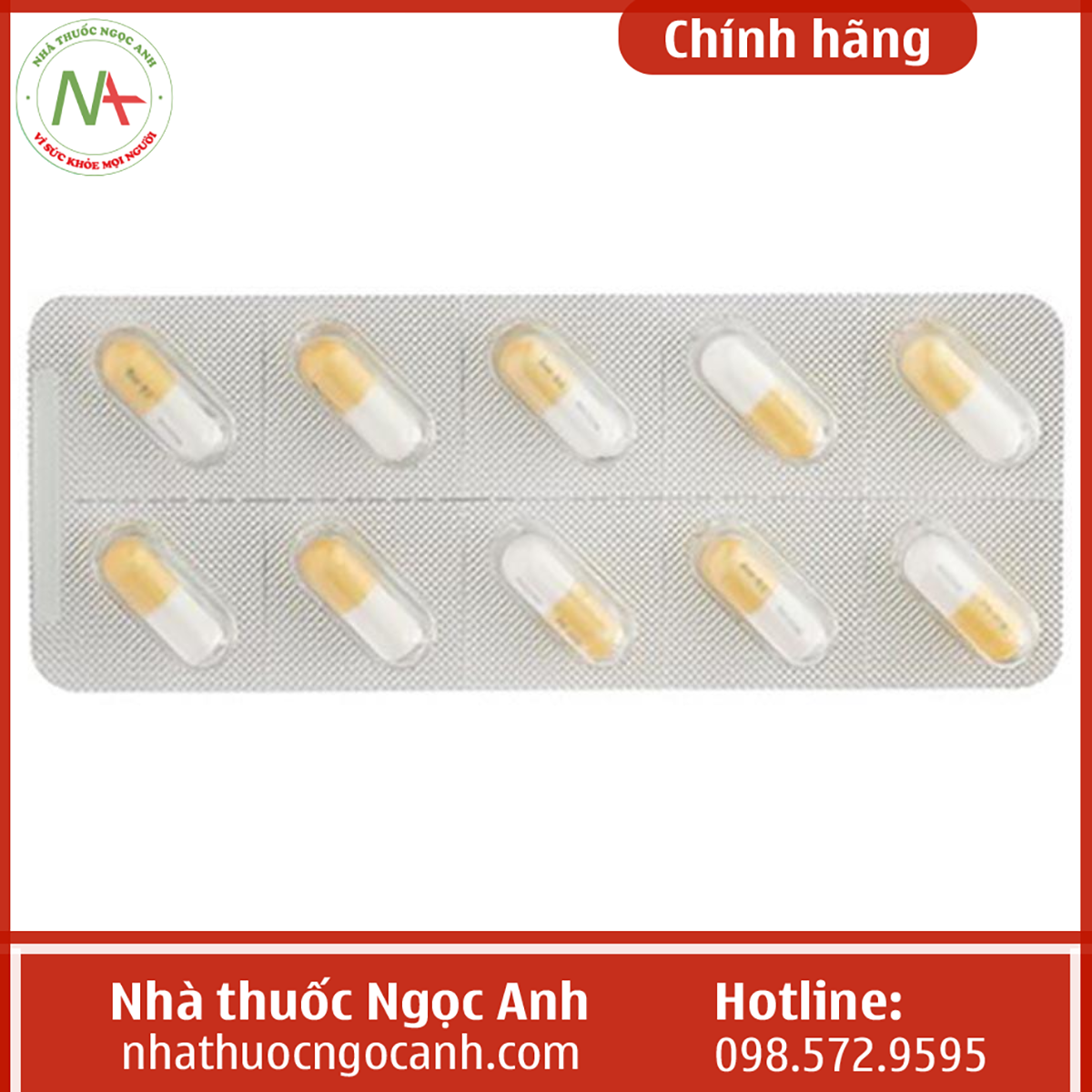
Dạng bào chế Viên nang cứng
Công ty đăng ký Roche
Số đăng ký VN-22143-19
Delpharm Milano S.r.l
Tiêu chuẩn sản xuất Tiêu chuẩn sản xuất
Xuất xứ Ý
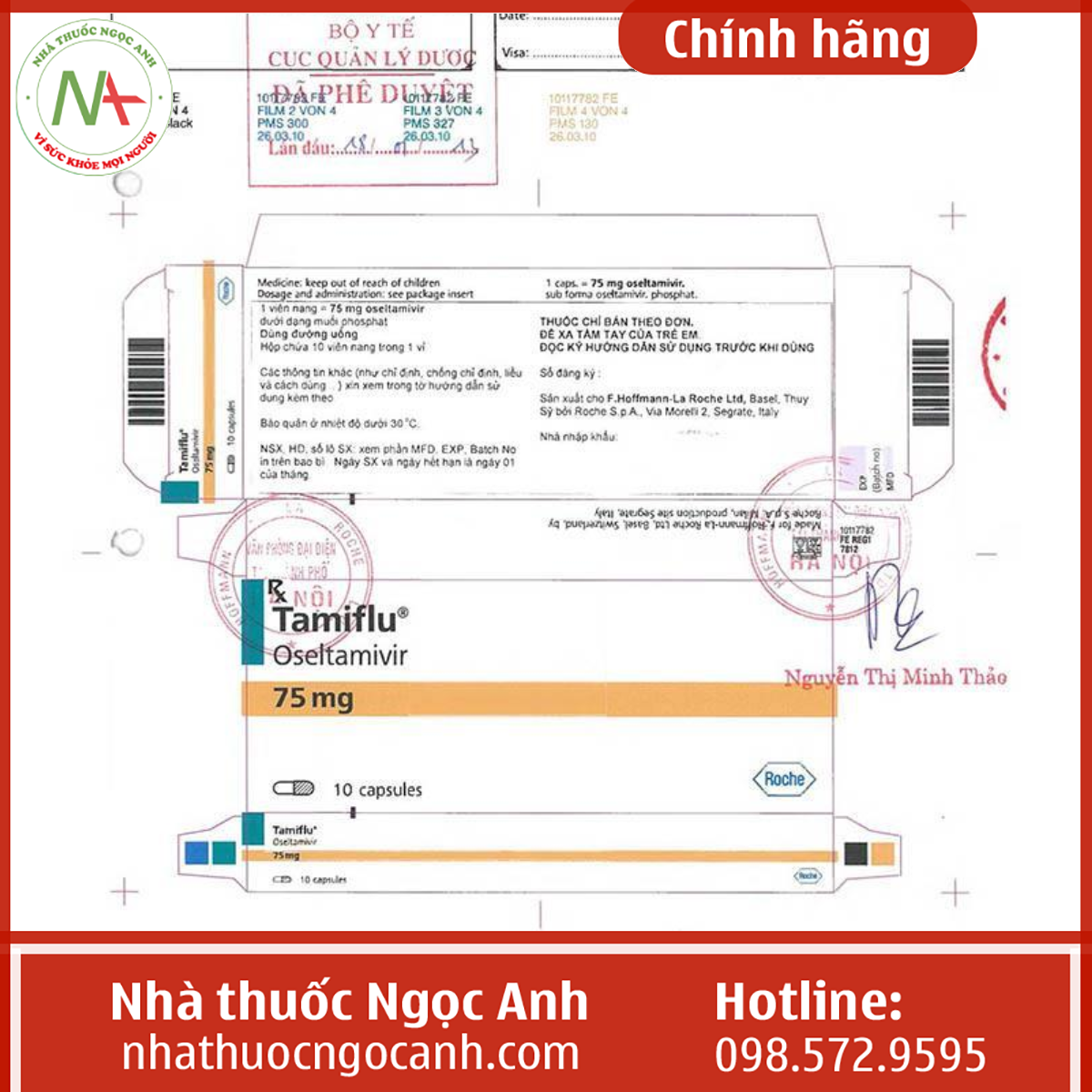
Quy cách đóng gói Hộp 1 vỉ x 10 viên
Hạn sử dụng 84 tháng kể từ ngày sản xuất
Mã sản phẩm tamiflu-75-mg
- Chi tiết
- Hỏi & Đáp 0
- Đánh giá 1
Trên thị trường hiện nay có rất nhiều thông tin về thuốc Tamiflu 75 mg tuy nhiên còn chưa đầy đủ. Trong bài viết này Nhà thuốc Ngọc Anh xin được trả lời cho bạn các câu hỏi: Tamiflu 75 mg là thuốc gì? Thuốc Tamiflu 75 mg có tác dụng gì? Thuốc Tamiflu 75 mg giá bao nhiêu? Dưới đây là thông tin chi tiết.
Tamiflu 75 mg là thuốc gì?
Tamiflu 75 mg là một loại thuốc kháng vi rút. Đây là thuốc dùng trong điều trị và dự phòng mắc cúm, với hoạt chất là Oseltamivir phosphate.
- Dạng bào chế: Viên nang cứng
- Quy cách đóng gói: Hộp 1 vỉ × 10 viên nang
- Xuất xứ: Ý
- Công ty sản xuất: Delpharm Milano S.r.l
- Công ty đăng ký: F.Hoffmann-La Roche Ltd
- Số đăng ký: VN-22143-19
Thành phần
Mỗi viên nang 75mg chứa 98,5mg oseltamivir phosphate, tương đương với 75mg oseltamivir.
Ngoài ra còn có các tá dược khác vừa đủ 1 viên nang bao gồm Pre-gelatinized starch, Povidone K 30, Croscarmellose sodium, Talc, Sodium stearyl fumarate.
Tác dụng của thuốc Tamiflu 75 mg
Oseltamivir phosphate chuyển hóa thành oseltamivir carboxylate ức chế chọn lọc lên enzym neuraminidase của vi rút cúm tuýp A và B. Enzym này vừa giúp vi rút xâm nhập vào những tế bào lành, vừa giúp giải phóng vi rút mới được tạo thành từ các tế bào bị nhiễm làm quá trình lây lan nhiễm vi rút nhanh.
Oseltamivir carboxylate ức chế men neuraminidase của vi rút cúm cả 2 type A và B. Oseltamivir carboxylate vừa ức chế sự lây nhiễm và sao chép của vi rút cúm, vừa ức chế sự sao chép và ngăn chặn việc gây bệnh của vi rút cúm.
Theo nghiên cứu của nhóm tác giả T Jefferson năm 2014, trong các thử nghiệm điều trị trên người lớn, oseltamivir làm giảm thời gian giảm các triệu chứng đầu tiên xuống 16,8 giờ (khoảng tin cậy 95% 8,4 đến 25,1 giờ, P <0,001). Không có ảnh hưởng ở trẻ em bị hen suyễn, nhưng có ảnh hưởng ở trẻ em khỏe mạnh khác (chênh lệch trung bình 29 giờ, khoảng tin cậy 95% từ 12 đến 47 giờ, P = 0,001). Trong các thử nghiệm điều trị, không có sự khác biệt về số lần nhập viện ở người lớn (chênh lệch nguy cơ 0,15%, khoảng tin cậy 95% -0,91% đến 0,78%, P = 0,84) và dữ liệu thưa thớt ở trẻ em và trong điều trị dự phòng. Trong các thử nghiệm điều trị cho người lớn, oseltamivir làm giảm viêm phổi chưa được xác minh qua trung gian điều tra viên (chênh lệch nguy cơ 1,00%, 0,22% đến 1,49%; số cần thiết để điều trị để có lợi (NNTB) 100, khoảng tin cậy 95% 67 đến 451). Hiệu quả không có ý nghĩa thống kê trong năm thử nghiệm sử dụng hình thức chẩn đoán chi tiết hơn cho “viêm phổi” và không có báo cáo nghiên cứu lâm sàng nào báo cáo xác nhận trong phòng thí nghiệm hoặc chẩn đoán về “viêm phổi”. Hiệu quả đối với viêm phổi chưa được xác minh ở trẻ em và điều trị dự phòng là không đáng kể.
Công dụng – Chỉ định của thuốc Tamiflu 75 mg
- Điều trị bệnh cúm: Tamiflu được chỉ định để điều trị bệnh cúm cho cả trẻ em trên 1 tuổi và người lớn có các triệu chứng điển hình của bệnh cúm trong mùa cúm cộng đồng. Hiệu quả điều trị đạt được trong vòng 2 ngày sau khi các triệu chứng cúm đầu tiên xuất hiện.
- Phòng ngừa bệnh cúm: Dự phòng bệnh cúm ở trẻ nhỏ từ 1 tuổi trở lên có nguy cơ mắc cúm khi tiếp xúc với người mắc cúm hoặc đang trong mùa dịch (trong vòng 48 giờ sau khi phơi nhiễm và trong thời gian có dịch cúm) và phòng ngừa cho người lớn và trẻ em từ 13 tuổi trở lên đã từng tiếp xúc với người bị cúm.
=> Tham khảo: Thuốc Tefostad T300 có tốt không? Giá bao nhiêu? Mua ở đâu?
Dược động học
Hấp thu
Oseltamivir được hấp thu hầu hết qua đường tiêu hóa. Nồng độ thuốc trong huyết tương đạt đỉnh 2 – 3 giờ sau khi dùng thuốc và cao hơn đáng kể. Có khoảng 75% lượng thuốc uống vào được tuần hoàn dưới dạng chất chuyển hóa có hoạt tính. Sự hấp thu thuốc không bị ảnh hưởng bởi thức ăn.
Phân bố
Sau khi thuốc được hấp thu vào tuần hoàn, thuốc sẽ phân bố rộng khắp các mô, dịch cơ thể. Chất chuyển hóa có hoạt tính có thể tích phân bố trung bình khoảng 23 lít. Tỷ lệ gắn kết với protein huyết tương của chất chuyển hóa là không đáng kể (xấp xỉ 3%). Tỷ lệ gắn kết của tiền chất với protein huyết tương là 42%.
Chuyển hóa
Một phần lớn thuốc được chuyển hóa qua gan lần đầu thành chất có hoạt tính nhờ enzym esterase ở gan, enzym này có mặt chủ yếu ở gan.
Thải trừ
Oseltamivir thải trừ khoảng 90% thành chất chuyển hóa có hoạt tính, sau đó thải trừ qua nước tiểu. Thuốc còn hoạt tính được thải trừ khoảng 99% qua thận. Thấp hơn 20% liều có đóng dấu phóng xạ được thải trừ qua phân.
Hướng dẫn sử dụng thuốc Tamiflu 75 mg hiệu quả
Liều dùng
Liều dùng để điều trị cúm
Nên dùng thuốc vào ngày đầu hoặc ngày thứ 2 khi thấy có các biểu hiện cúm
- Người lớn và thanh thiếu niên: Liều dùng cho trẻ trên 13 tuổi, trẻ nặng trên 40kg và người lớn: 1 ngày dùng 2 lần, mỗi lần 75mg. thời gian dùng thuốc kéo dài 5 ngày
- Trẻ em:
- Liều dùng cho trẻ em trên 1 tuổi: thời gian dùng thuốc kéo dài 5 ngày, mỗi ngày dùng 2 lần. Liều cho trẻ cân nặng dưới 15kg là 30mg; liều cho trẻ cân nặng từ 15 đến 23kg là 45mg; liều cho trẻ từ 23kg đến 40kg là 60mg.
- Liều dùng cho trẻ em từ 6-12 tháng tuổi: thời gian dùng thuốc trong 5 ngày. Mỗi ngày dùng 2 lần với liều 3mg/kg cân nặng.
Liều dùng để dự phòng mắc bệnh cúm
Nên dùng thuốc vào ngày đầu hoặc ngày thứ 2 sau khi tiếp xúc với nguồn nhiễm cúm
- Liều dùng cho người lớn và trẻ trên 13 tuổi, trẻ em có cân nặng trên 40kg: thời gian dùng thuốc kéo dài 10 ngày, mỗi ngày dùng 1 lần liều 75mg
- Liều dùng cho trẻ em trên 1 tuổi: thời gian dùng thuốc kéo dài 10 ngày, mỗi ngày dùng 2 lần. Liều cho trẻ cân nặng dưới 15kg là 30mg; liều cho trẻ cân nặng từ 15 đến 23kg là 45mg; liều cho trẻ từ 23kg đến 40kg là 60mg.
Liều dùng trên một số bệnh nhân đặc biệt
Bệnh nhân suy thận
Điều trị bệnh cúm
- Những bệnh nhân có độ thanh thải creatinine trên khoảng 60 ml/phút không cần thiết phải chỉnh liều.
- Những bệnh nhân có độ thanh thải creatinine khoảng 30-60 ml/phút, phải giảm liều dùng còn 30mg/ lần, uống 2 lần/ ngày trong vòng 5 ngày.
- Những bệnh nhân có độ thanh thải creatinine khoảng 10-30 ml/phút, phải giảm liều dùng còn 30mg/ lần, uống 1 lần/ngày trong vòng 5 ngày.
- Đối với những bệnh nhân đang trong quá trình thẩm phân máu định kỳ, khi triệu chứng cúm bắt đầu xuất hiện trong vòng 48 giờ giữa hai đợt thẩm phân máu, thì dùng liều khởi đầu 30 mg trước khi bắt đầu quá trình thẩm phân máu. Đề nồng độ thuốc nằm trong khoảng trị liệu thì nên dùng với liều 30 mg sau mỗi lần thẩm phân máu. Trường hợp thẩm phân ở phúc mạc cần dùng liều 30 mg trước quá trình thẩm phân máu và bổ sung liều 30 mg trong 5 ngày.
Phòng ngừa mắc bệnh cúm
- Những bệnh nhân có độ thanh thải creatinine trên khoảng 60 ml/phút không cần điều chỉnh liều.
- Những bệnh nhân có độ thanh thải creatinine khoảng 30-60 ml/phút, cần giảm liều còn 30mg/ lần, uống 1 lần/ngày.
- Những bệnh nhân có độ thanh thải creatinine khoảng 10-30 ml/phút, cần giảm liều còn 30mg/ lần, uống cách ngày một lần.
- Đối với những bệnh nhân đang thẩm phân máu định kỳ, nên dùng liều khởi đầu 30 mg trước quá trình thẩm phân máu. Để nồng độ thuốc nằm trong khoảng trị liệu, nên dùng liều 30 mg sau 1 lần thẩm phân máu xen kẽ. Trường hợp thẩm phân tại phúc mạc thì nên dùng với liều 30 mg trước quá trình thẩm phân máu và tiếp tục bổ sung liều 30 mg trong vòng 7 ngày.
Bệnh nhân suy gan
Ở những bệnh nhân rối loạn chức năng gan từ nhẹ đến vừa không cần phải điều chỉnh liều khi điều trị hoặc ngăn ngừa cúm.
Bệnh nhân suy giảm hệ miễn dịch
Thời gian khuyến cáo dự phòng cúm cho những bệnh nhân suy giảm miễn dịch từ 1 tuổi trở lên là trước 12 tuần trước khi vào mùa cúm và không cần phải điều chỉnh liều.
Người già
Không cần điều chỉnh liều cho người già khi được điều trị hoặc phòng ngừa bệnh cúm
Trẻ em
Theo những dữ liệu dược động học, trẻ từ 6 đến 12 tháng tuổi dung liều 3 mg/kg uống 2 lần/ ngày có hiệu quả lâm sàng tương tự ở trẻ lớn hơn và người lớn. Chưa có dữ liệu lâm sàng để đưa ra liều khuyến cáo cho trẻ dưới 6 tháng tuổi.
Cách dùng thuốc Tamiflu 75 mg hiệu quả
Thuốc có thể sử dụng chung với thức ăn hoặc không. Ở một số trường hợp, nếu dùng chung với thức ăn làm tăng dung nạp của thuốc.
Thuốc được bào chế ở dạng viên nang và được dùng đường uống. Khi uống không nên nhai nát viên thuốc, phải uống cả viên với nước đun sôi để nguội.
Hướng dẫn pha chế Tamiflu cho trẻ em, người khó nuốt
Người lớn, thanh thiếu niên không thể nuốt hoặc trẻ em dùng liều thấp có thể sử dụng Tamiflu dạng huyền dịch thay vì viên nang.
Huyền dịch uống Tamiflu tốt nhất nên được pha chế tại hiệu thuốc bởi dược sĩ có kinh nghiệm trước khi đưa cho bệnh nhân. Đưa thuốc cho bệnh nhân kèm ống lấy thuốc và tờ hướng dẫn.
Các bước pha chế huyền dịch như sau:
- Vỗ nhẹ lọ đựng thuốc vài lần giúp bột tơi hơn.
- Sử dụng cốc đong có sẵn đong vừa đủ 55 ml nước theo mức đã được chỉ định.
- Đổ lượng nước vừa đong vào lọ bột thuốc, đóng kín, lắc kỹ trong 15 giây.
- Mở nắp lọ (loại nắp bảo vệ tránh trẻ em) sau đó ấn bộ phận tiếp hợp vào cổ lọ thuốc.
- Đóng chặt nắp bảo vệ giúp cố định bộ phận tiếp hợp ở lọ thuốc. Nhãn thuốc cần ghi ngày hết hạn của huyền dịch đã pha.
Trường hợp không có sẵn Tamiflu huyền dịch uống, vẫn có thể pha hỗn dịch uống từ viên nang Tamiflu (Nồng độ sau khi pha cần đạt 6 mg/mL). Huyền dịch 6mg/ml có thể pha từ viên nang Tamiflu 30 mg, 45 mg hoặc 75 mg cùng dung dịch chứa 0.05% sodium benzoate (chất bảo quản).
Tổng thể tích huyền dịch cần pha để sử dụng trong một đợt điều trị kéo dài 5 ngày được tính theo cân nặng như sau:
| Cân nặng người bệnh (kg) | Thể tích cần pha (ml) |
| < 6kg | 25 |
| 6 – (dưới) 7kg | 30 |
| 7 – 10kg | 50 |
| 10 – 15kg | 50 |
| trên 15 – 23kg | 75 |
| trên 23 – 40kg | 100 |
| trên 40kg | 125 |
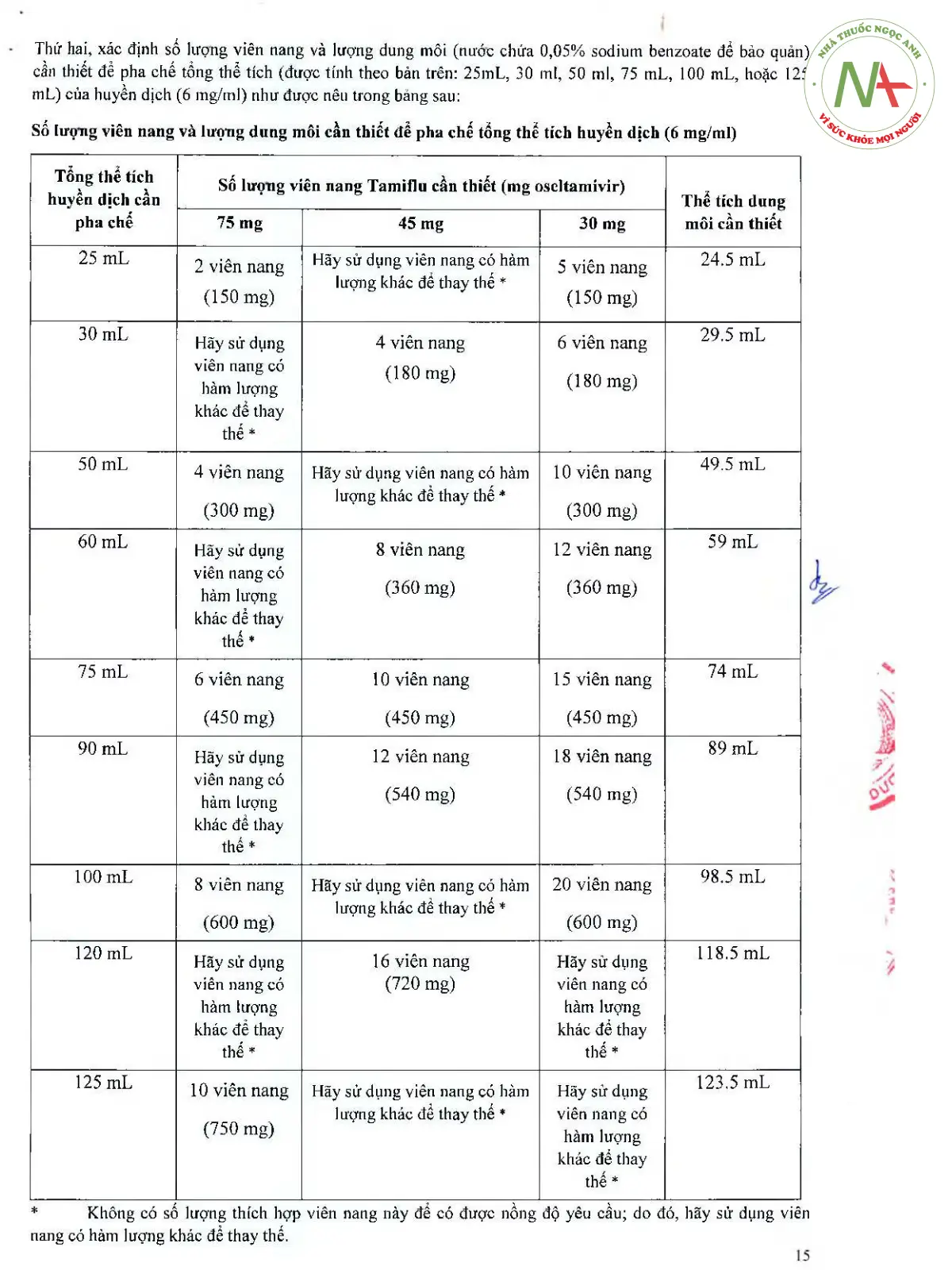
Tương ứng với tổng thể tích huyền dịch cần pha ở bảng trên, số lượng viên nang Tamiflu và dung môi cần thiết là:
| Thể tích huyền dịch cần pha (ml) | Số lượng viên nang cần thiết | Thể tích dung môi cần dùng (ml) | ||
| Viên 75mg | Viên 45mg | Viên 30mg | ||
| 25 | 2 viên (150mg) | 5 viên | 24.5 | |
| 30 | 4 viên (180mg) | 6 viên | 29.5 | |
| 50 | 4 viên (300mg) | 10 viên | 49.5 | |
| 60 | 8 viên (360mg) | 12 viên | 59 | |
| 75 | 6 viên (450mg) | 10 viên | 15 viên | 74 |
| 90 | 12 viên (540) | 18 viên | 89 | |
| 100 | 8 viên (600mg) | 20 viên | 98.5 | |
| 120 | 16 viên (720mg) | 118.5 | ||
| 125 | 10 viên (750) | 123.5 | ||
Quy trình pha chế huyền dịch (6 mg/ml) từ viên nang Tamiflu bao gồm các bước:
- Chuyển lượng viên nang và dung dịch sodium benzoate được tính theo bảng trên vào chai.
- Đậy kín nắp chai, sau đó lắc đều trong khoảng 2 phút.
- Chai cần được dán nhãn phụ ghi rõ lưu ý “Lắc nhẹ trước khi dùng”. Bên cạnh đó, cần dán nhãn hạn dùng theo từng điều kiện bảo quản (3 tuần khi bảo quản ở nhiệt độ phòng dưới 25 độ C, 6 tuần khi bảo quản lạnh từ 2 – 8 độ C).
Dược sĩ khi đưa thuốc cần hướng dẫn người chăm sóc bỏ đi phần dung dịch còn thừa sau khi bệnh nhân kết thúc đợt điều trị.
Tác dụng phụ của thuốc Tamiflu 75 mg
Trong quá trình thuốc được thử nghiệm lâm sàng
Một số nghiên cứu sử dụng Tamiflu điều trị cúm cho người lớn và thanh thiếu niên, các phản ứng không mong muốn thường gặp nhất là buồn nôn, nôn mửa, chóng mặt, đau đầu. Hầu hết các phản ứng này xảy ra trong ngày đầu tiên điều trị hoặc ngày thứ hai điều trị và thường tự hết trong vòng 1-2 ngày. Trong nghiên cứu sử dụng Tamiflu để dự phòng cúm cho người lớn và thanh thiếu niên, phần lớn các phản ứng không mong muốn được báo cáo là buồn nôn, nôn ói, đau đầu, chóng mặt.
Ở trẻ em, phản ứng không mong muốn thường xảy ra nhất là nôn ói.
Hầu hết những bệnh nhân khi gặp các phản ứng phụ trên không cần thiết phải ngưng sử dụng Tamiflu.
Sau khi thuốc được lưu hành trên thị trường
Trong quá trình sử dụng Tamiflu sau khi lưu hành thuốc, phát hiện những phản ứng không mong muốn có thể xảy ra sau đây:
- Tác dụng phụ trên da và các mô dưới da: những phản ứng da dị ứng xảy ra như viêm da, nổi ban, chàm đỏ, mề đay, sưng phù mặt, hội chứng Stevens-Johnson và có thể xảy ra hoại tử biểu bì.
- Tác dụng phụ trên gan – mật: viêm gan, men gan tăng cao.
- Tác dụng phụ trên hệ thần kinh: Co giật và mê sảng (các triệu chứng bao gồm thay đổi ý thức, hoang tưởng, ảo giác, bồn chồn, lo lắng, ác mộng).
- Tác dụng trên hệ tiêu hóa: Xuất huyết tiêu hóa thường gặp là viêm đại tràng xuất huyết, thường triệu chứng sẽ thuyên giảm khi ngừng sử dụng Tamiflu.
Ngoài ra có thể gặp một số phản ứng không mong muốn khác như:
- Nhiễm trùng, nhiễm ký sinh trùng như viêm xoang, viêm họng mũi, viêm đường hô hấp trên, nhiễm Herpes simplex.
- Hô hấp: ho, sổ mũi, viêm họng.
Trong quá trình điều trị, bệnh nhân nhận thấy xuất hiện bất cứ biểu hiện bất thường nào nghi ngờ rằng do sử dụng thuốc thì bệnh nhân cần xin ý kiến của dược sĩ hoặc bác sĩ điều trị để có thể xử trí kịp thời và chính xác.
Chống chỉ định
Không sử dụng thuốc Tamiflu 75 mg cho người có tiền sử mẫn cảm với bất kì thành phần nào có trong thuốc.
Lưu ý khi sử dụng và bảo quản thuốc Tamiflu 75 mg
Lưu ý và thận trọng
- Thận trọng và tham khảo ý kiến bác sĩ trước khi dùng Tamiflu cho bệnh nhân là phụ nữ đang mang bầu hoặc đang thời kì nuôi con bằng sữa mẹ.
- Thận trọng và chú ý giảm liều theo hướng dẫn của bác sĩ đối với bệnh nhân chức năng gan, thận kém, bệnh nhân là người lớn tuổi.
- Trong thời gian sử dụng thuốc, người bệnh tuyệt đối tuân thủ theo chỉ định về liều của bác sĩ điều trị, tránh việc tăng hoặc giảm liều để đẩy nhanh thời gian điều trị bệnh.
- Trước khi ngưng sử dụng thuốc, bệnh nhân cần xin ý kiến của bác sĩ điều trị.
- Nếu nhận thấy thuốc xuất hiện các dấu hiệu lạ như đổi màu, biến dạng, chảy nước thì bệnh nhân không nên sử dụng thuốc đó nữa.
- Không thể sử dụng Tamiflu với mục đích thay thế tiêm vắc xin phòng cúm. Nên chủ động lên kế hoạch tiêm phòng vắc xin cúm để tăng hiệu quả chống dịch cúm khi sắp bước vào mùa cúm.
- Khi có các phản ứng bất thường khi sử dụng Tamiflu cần ngưng sử dụng và đến nơi cơ sở y tế gần nhất để giải quyết kịp thời.
Phụ nữ mang thai và phụ nữ cho con bú có sử dụng thuốc Tamiflu 75 mg được không?
Đối với phụ nữ có thai
Nguy cơ thai kỳ thuộc nhóm B
Chưa có thử nghiệm lâm sàng có đối chứng về việc sử dụng Oseltamivir cho phụ nữ mang thai, rất ít dữ liệu được báo cáo sau khi lưu hành thuốc và các nghiên cứu quan sát hồi cứu. Các dữ liệu này kết hợp những nghiên cứu trên động vật, không thấy các tác hại trực tiếp hoặc gián tiếp lên thai kỳ. Do vậy, phụ nữ có thai có thể uống Tamiflu sau khi đã cân nhắc về những thông tin an toàn sẵn có với mức độ gây bệnh của chủng vi rút cúm hiện hành và tình trạng sức khỏe của người phụ nữ đang mang thai.
Đối với phụ nữ cho con bú
Có rất ít thông tin về việc Oseltamivir bài tiết vào sữa mẹ, các dữ liệu này đã cho thấy rằng oselamivir và chất chuyển hoá có hoạt tính của nó có trong sữa mẹ ở nồng độ thấp. Theo khuyến cáo, bà mẹ đang cho con bú có thể sử dụng oseltamivir sau cân nhắc tính gây bệnh của các chủng vi rút cúm đang hiện hành và tình trạng sức khỏe của bà mẹ cho con bú.
Lưu ý đối với người lái xe hoặc người vận hành máy móc
Thuốc không gây ra các ảnh hưởng bất lợi cho người lái xe hay người vận hành máy móc
Bảo quản
- Bảo quản nơi khô ráo, thoáng mát, tránh ẩm, tránh ánh nắng trực tiếp.
- Để nơi có nhiệt độ dưới 30 độ C.
- Tránh xa tầm tay của trẻ nhỏ.
- Hạn sử dụng: 48 tháng kể từ ngày sản xuất.
Tương tác thuốc
| Thuốc | Tương tác |
| Thuốc ngừa thai dùng đường uống | Một số nghiên cứu in vitro cho thấy oseltamivir phosphate và chất chuyển hóa có hoạt tính đều không phải là chất nền tốt của men oxidase có chức năng hỗn hợp P450 hoặc cho men glucuronyl transferases. Không có cơ sở nào về mặt cơ chế cho thấy có sự tương tác với thuốc ngừa thai dùng đường uống. |
| Cimetidine | Cimetidine không có ảnh hưởng đến nồng độ Oseltamivir hoặc chất chuyển hóa có hoạt tính của nó. |
| Probenecid | Dùng Oseltamivir đồng thời probenecid làm nồng độ các chất chuyển hóa có hoạt tính tăng lên lên gần gấp đôi do sự bài tiết chủ động của ống thận giảm đi. Tuy nhiên không cần phải điều chỉnh liều Oseltamivir khi dùng đồng thời với probenecid vì giới hạn an toàn của chất chuyển hóa có hoạt tính rất rộng. |
| Amoxicillin, Paracetamol | Dùng chung Oseltamivir với amoxicillin đều không gây ra sự thay đổi nồng độ hai thuốc trong huyết tương. |
| Thuốc ức chế men chuyển (enalapril, captopril), các thiazide lợi tiểu (bendrofluazide), kháng sinh (penicillin, cephalosporin, azithromycin, erythromycin và doxycycline), thuốc chẹn thụ thể H2 (ranitidine, cimetidine), chẹn beta (propranolol), các xanthine (theophylline), thuốc giống giao cảm (pseudoephedrine), chế phẩm thuốc phiện (codeine), corticosteroids, thuốc giãn phế quản dạng hít, và thuốc giảm đau (aspirin, ibuprofen và paracetamol). | Trong một số nghiên cứu lâm sàng để dự phòng và điều trị pha III, cho dùng đồng thời Tamiflu với các thuốc này. Ta không thấy phản ứng phụ hoặc các tương tác gì. |
Thuốc Tamiflu 75 mg có tốt không?
Ưu điểm
- Được phép lưu hành rộng rãi với cấp phép từ Bộ y tế.
- Được sản xuất tại nhà máy hiện đại, có chứng nhận GMP. Với độ ngũ nhân viên kinh nghiệm cao, chất lượng được đảm bảo suốt cả quá trình sản xuất cho đến tay khách hàng.
- Thành phần chứa Oseltamivir phosphate là thuốc điều trị cảm cúm. Có thể dùng được cho trẻ từ 1 tuổi trở lên.
- Dạng thuốc viên dễ dùng.
Nhược điểm
Thuốc có thể gây ra các phản ứng phụ khi dùng.
Cách xử trí quá liều, quên liều thuốc Tamiflu 75 mg
Quá liều
Các biểu hiện khi uống quá liều thuốc khá giống với các triệu chứng của tác dụng phụ. Bên cạnh đó, bệnh nhân có thể gặp phải tình trạng nhiễm độc gan, thận. Bệnh nhân cần được theo dõi kĩ các biểu hiện trên da, mặt, huyết áp và đề phòng vì tình trạng nguy hiểm có thể diễn biến rất nhanh. Tốt nhất, tình trạng của bệnh nhân cần được thông báo với bác sĩ điều trị để có hướng xử trí kịp thời
Quên liều
Tránh quên liều; nếu quên liều, bệnh nhân cần bỏ qua liều đã quên, không uống chồng liều với liều tiếp theo.
Không nên bỏ liều quá 2 lần liên tiếp.
=> Đọc thêm: Thuốc Mocrea Tenofovir 300mg là thuốc gì, giá bao nhiêu, mua ở đâu.
Thuốc Tamiflu 75 mg có giá bán bao nhiêu?
Thuốc Tamiflu 75 mg giá bao nhiêu? Một hộp thuốc Tamiflu 75 mg được bán phổ biến tại các cơ sở bán thuốc trên toàn quốc với giá dao động khoảng 950.000 VNĐ/ hộp 1 vỉ chứa 10 viên nang hoặc có thể thay đổi tùy vào từng nhà thuốc.
Mua thuốc Tamiflu 75 mg ở đâu uy tín, chính hãng?
Thuốc Tamiflu 75 mg là thuốc bán theo đơn, bệnh nhân mua thuốc cần mang theo đơn thuốc của bác sĩ. Cần liên hệ những cơ sở uy tín để mua được sản phẩm thuốc Tamiflu 75 mg tốt nhất, tránh thuốc kém chất lượng. Hiện nay thuốc đang được bán tại Nhà thuốc Ngọc Anh, bạn có thể liên hệ qua hotline hoặc nhắn tin qua website để được các Dược sĩ có chuyên môn tư vấn.
Nguồn tham khảo
Tờ hướng dẫn sử dụng. Tải tờ hướng dẫn tại đây.















*Mọi thông tin của website chỉ mang tính chất tham khảo, không thể thay thế lời khuyên của bác sĩ. Nếu có bất cứ thắc mắc nào vui lòng liên hệ hotline: 098.572.9595 hoặc nhắn tin qua ô chat ở góc trái màn hình.


SO SÁNH VỚI SẢN PHẨM TƯƠNG TỰ

Công ty cổ phần dược phẩm Agimexpharm
1 đánh giá cho Tamiflu 75 mg
Sorry, no reviews match your current selections
Hỏi & Đáp
Gửi câu hỏi
Cẩu hỏi của bạn sẽ được trả lời từ những chuyên gia hàng đầu trong lĩnh vực.
Thank you for the question!
Your question has been received and will be answered soon. Please do not submit the same question again.
Error

An error occurred when saving your question. Please report it to the website administrator. Additional information:
Add an answer
Thank you for the answer!
Your answer has been received and will be published soon. Please do not submit the same answer again.
Error

An error occurred when saving your question. Please report it to the website administrator. Additional information:







my Đã mua hàng
Thuốc có hiệu quả tốt ạ
Dược sĩ Anh Thư Quản trị viên
Cảm ơn bạn đã tin dùng sản phẩm của Nhà thuốc Ngọc Anh