Bệnh sản phụ khoa
Các bệnh đường tiêu hóa khi mang thai: Bác sĩ chuyên khoa tiêu hóa cần biết những gì?
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
Biên dịch: Bác sĩ Vũ Tài – Học viện Quân y
nhathuocngocanh.com – Chủ đề: Các bệnh đường tiêu hóa khi mang thai: Bác sĩ chuyên khoa tiêu hóa cần biết những gì?
Bạn có thể tải file PDF Tại đây.
Tóm tắt
Thai kỳ được đặc trưng bởi vô số các thay đổi sinh lý có thể dẫn đến nhiều triệu chứng khác nhau và thường xuyên có các than phiền về đường tiêu hóa, như ợ nóng, buồn nôn và nôn hoặc táo bón. Các bệnh đường tiêu hóa mãn tính cần duy trì điều trị trong suốt giai đoạn này, đặt ra câu hỏi đầy thách thức liệu kết cục có lợi đối với mẹ có thể gây hại cho thai nhi hay không. Ngoài ra, một số bệnh, như gan nhiễm mỡ cấp tính thai kỳ, chì phát triển trong thai kỳ và có thể cần các thủ thuật khẩn cấp, như sinh thai. Mặc dù chúng không xuất hiện trong thực hành hàng ngày của chúng ta, kiến thức về các bệnh liên quan đến thai kỳ là nền tảng và sự hợp tác giữa bác sĩ chuyên khoa tiêu hóa và bác sĩ sản khoa thường là cần thiết. Trong tài liệu này, chúng tôi xem xét các bệnh liên quan đến thai kỳ và hệ thống hóa các lựa chọn điều trị thích hợp nhất theo các tài liệu và hướng dẫn gần đây, đề bài báo có thể phục vụ như một hướng dẫn cho bác sĩ chuyên khoa tiêu hóa tiếp cận nội khoa đối với các bệnh gan và tiêu hóa liên quan đến thai kỳ và quản lý điều trị chúng.
Giới thiệu
Thai kỳ là một giai đoạn đầy thử thách đối với bác sĩ chuyên khoa tiêu hóa. Mặc dù nhiều than phiền về đường tiêu hóa có thể xảy ra trong thai kỳ (trào ngược dạ dày thực quán, táo bón, v.v.) nhưng hầu hết các than phiền này đều ở mức độ nhẹ đến trung binh, thường được bác sĩ sản khoa quân lý và do đó bác sĩ chuyên khoa tiêu hóa hiếm khi được nhờ can thiệp. Tuy nhiên, một số biến chứng của thai kỳ, như các bệnh gan đặc hiệu, quản lý thai phụ bị bệnh viêm ruột (IBD), hoặc cần phải nội soi trong thai kỳ, có thể cần đến sự can thiệp của bác sĩ chuyên khoa tiêu hóa; do đó, điều cần thiết là bác sĩ chuyên khoa tiêu hóa phải luôn cập nhật các biến chứng thường gặp nhất và các chẩn đoán phân biệt tiềm năng của thai kỳ. Dưới đây, chúng tôi xem xét toàn diện các biến chứng tiêu hóa phổ biến nhất của thai kỳ, cung cấp hướng dẫn có thể hữu ích cho bác sĩ chuyên khoa tiêu hóa trong việc quản lý, chẩn đoán và tiếp cận những tình huống này.
Tài liệu và phương pháp
Một tìm kiếm điện từ trên PubMed được thực hiện nhằm xác định các tài liệu liên quan về sinh lỷ bệnh, biểu hiện lâm sàng, điều trị, kết cục của mẹ và thai nhi đổi với cá bệnh tiêu hóa và gan trong thai kỳ; tìm kiếm này đã được bổ sung bởi các hướng dần gần đây nhất hiện có (ECCO, ACG, EASL, Royal College of Obstetrics and Gynaecology).
Thay đổi sinh lý trong thai kỳ
Thai kỳ được đặc trưng bởi tình trạng pha loãng máu gây ra bởi sự mở rộng thể tích do giữ muối và nước. Do đó, nồng độ hemoglobin và albumin giảm, số lượng tiểu cầu có thế giảm, nhưng thường vần trong giới hạn bình thường. Alkaline phosphatase (AP) có thể tăng 3-4 lần do nhau thai sản xuất. Aspartate aminotransferase, alanine aminotransferase (ALT), gama-glutamyl transferase (GGT), bilirubin và thời gian prothrombin (PT) vần nam trong phạm vi bình thường của chúng. Tuy nhiên, nồng độ yếu tố đông máu bị ảnh hướng bời thai kỳ, với giảm nhẹ antithrombin III, protein c và protein s, và tăng các yếu tố I đến XXII và fibrinogen gây nên trạng thái tiền đông máu [)].
Nồng độ hormone tăng cao, như progesterone, góp phần làm chậm quá trình làm rỗng dạ dày. Độ axit trong dạ dày tăng do nhau thai sàn xuất gastrin nhiều hơn [2], Sự tăng trưởng của thai trong tử cung cũng làm thay đổi mối quan hệ giải phẫu giữa các cơ quan trong ổ bụng: ví dụ, ruột thừa có thể di chuyển lên trên sau tháng thứ 3 [3],
Bệnh đường tiêu hóa
Các than phiền về đường tiêu hóa thường gặp:
Buồn nôn và nôn
Buồn nôn và nôn là những tình trạng nội khoa thường gặp nhất trong thai kỳ, ảnh hưởng đến 50-80% thai phụ [4]. Các triệu chứng này bắt đầu từ tuần thứ 4 đến tuần thứ 6, cao điểm từ tuần thứ 8 đến tuần thứ 12, và thường chấm dứt vào tuần thứ 20 [4]. Các triệu chứng đính điếm và việc dùng thuốc thường trùng với thời kỳ dễ bị tác dụng gây quái thai nhất. Cơ chế chính xác của buồn nôn và nôn chưa được hiểu biết hoàn toàn. Người ta tin rang progesterone có tác dụng ức chế cơ trơn môn vị và ruột non, làm giảm nhu động đường tiêu hóa và làm chậm quá trình làm rỗng dạ dày [4]. Đa thai và thai trứng có liên quan đến các triệu chứng nghiêm trọng hơn và thường xảy ra hơn, điều này có thể được giải thích là do nồng độ gonadotropin màng đệm người (HCG) cao hơn [5]. Cuối cùng, các yếu tố tâm !ỷ cùng có thể đóng một vai trò nào đó. Lo lắng, trầm cảm, mang thai ngoài ý muốn và mối quan hệ tiêu cực với các thành viên trong gia đình có liên quan đến tỷ lệ buồn nôn và nôn cao hơn [4].
Cách tiếp cận với buồn nôn và nón đòi hỏi phải loại trừ các nguyên nhân khác, đặc biệt nếu các triệu chứng này vẫn tồn tại trong tam cá nguyệt thứ hai và thú ba. Hầu hết thai phụ không cần điều trị bằng thuốc và có thể được quản lý bằng các lựa chọn thay thế và điều chỉnh chế độ ăn uống [6]. Các khuyến cáo về chế độ ăn uống bao gồm các chia nhỏ các bữa ăn và tránh thực phẩm nhiều chất béo và rau tươi có thế làm chậm quá trình làm rỗng dạ dày [4], Nên uống 1,5 L nước hoặc đồ uống có chứa glucose, muối và kali hàng ngày. Cà thiamine (vitamin Bl) và pyridoxine (vitamin B6) đã chứng minh được hiệu quả của chúng và được chỉ định làm chất bổ sung thường quy ở những bệnh nhân bị nôn kéo dài [4], Một tổng quan của Cochrane năm 2010 đánh giá 9 thử nghiệm ngẫu nhiên liên quan đến gừng [5]. Dựa trên kinh nghiệm của chuyên gia, gừng có thể được coi là một lựa chọn không dùng thuốc trong thai kỳ [7],
Liên quan đến điều trị bằng thuốc, thuốc chống nôn có thể là một lựa chọn cho những thai phụ bị buồn nôn và nôn dai dẳng.
Thuốc chẹn thụ thể histamin (kháng Hl), nhtr promethazine, cyclizine, cinnarizine, doxylamine và dimenhydrinate, được coi là điều trị đẩu tay, vì không có tác dụng bất lợi đối với thai nào được mó tà [4]. Doxylamine có ưu điểm là an toàn khí các triệu chứng mới bắt đầu (6-7 tuần). Trong một nhóm thuần tập gồm 608.385 thai kỳ, Pasternak và cộng sự đã đánh giá ondansetron, một chất chẹn thụ thể H3, và kết luận rằng nó không liên quan đến gia tăng đáng kể sảy thai tự phát, thai chết lưu, dị tật bẩm sinh lớn, sinh non hoặc trẻ nhỏ so với tuổi thai [8 ]. Tuy nhiên, có những nghiên cứu ghi nhận khiếm khuyết tim bẩm sinh, đặc biệt khi ondansetron được dùng trong tam cá nguyệt thứ nhất. Do đó, nó được khuyến cáo như là liệu pháp hàng thứ hai [9], Phenothiazines là một lựa chọn điều trị đầu tay khác, bao gồm prochlorperazine, chlorpromazine và perphenazine. Các nghiên cứu không cho thấy gia tăng nguy cơ bị các dị tật lớn [6]. Cuối cùng, metoclopramide, một chất đối kháng dopamin, cũng có thể được kè đơn một cách an toàn. Tuy nhiên, nó qua nhau thai và được coi là một lựa chọn điều trị hàng thứ hai, do tác dụng ngoại tháp tiềm ẩn của nó đối với câ thai nhi (tam cá nguyệt thứ ba) và mẹ (tam cá nguyệt thứ nhất) [9].
Bệnh trào ngược dạ dày thực quản (GERD)
GERD được báo cáo bới 40-85% thai phụ, thường bắt đầu vào cuối tam cá nguyệt thứ nhất và có thể làm giảm đáng kể chất lượng cuộc sống [10], Khi xuất hiện, GERD vẫn tồn tại trong suốt thai kỳ và thường khỏi sau khi sinh. Các biến chứng như viêm trợt thực quản, chảy máu hoặc chít hẹp hiếm khi được mô tả [4]. Đối với các triệu chứng nhẹ, khuyến cáo điều chỉnh lối sống và chế độ ăn uống [6]. Các biện pháp bảo tồn bao gồm tránh ăn khuya, kè cao đầu giường 10-15 cm và nằm nghiêng trái [10], Nếu các triệu chứng vần còn, có thể cần dùng thuốc. Điều trị đầu tay là thuốc kháng acid [10], Thuốc kháng axit có chứa canxi và magiê được coi là an toàn trong thai kỳ. Hơn nữa, bệnh nhân thích sử dụng thuốc này hơn vì nó làm giảm các triệu chứng ngay và có thể được dùng theo nhu cầu. Không quan sát thấy tác dụng gây quái thai của các thuốc này trong các nghiên cứu trên động vật [11], Nên tránh các thuốc có chứa bicarbonat, như natri bicarbonat, vì chúng có thế gây nhiễm kiềm chuyển hóa và quá tải dịch ờ mẹ và thai nhi [4,10]. Một mối lo ngại nữa đối với thuốc kháng axit có chứa nhôm là khả năng chậm phát triển được mô tả khi thai phụ dùng liều cao thuốc này [12], Khả năng gây độc cho thai nhi khi sử dụng sucralfate có liên quan đến thành phần nhôm của nó. Tuy nhiên, không có tác dụng bất lợi nào được ghi nhận ớ mẹ và thai, và do đó sucralfate thường được coi là an toàn trong thai kỳ [13], Thuốc đối kháng histamine type 2 thường là liệu pháp đầu tay. Cả cimetidine và ranitidine đã được sử dụng với dữ liệu an toàn tuyệt vời [4,10). Mặc dù có mối lo ngại về tinh an toàn đối với thuốc ức chế bơm proton (PPI), trong một phân tích gộp gần đày Gill và cộng sự không phát hiện gia tăng nguy cơ bị các dị tật bẩm sinh lớn khi dùng PPI trong thai kỳ [14], Tuy nhiên, một số nghiên cứu trước đây đã báo cáo tỷ lệ từ vong phôi và thai liên quan đến liều lượng trong các nghiên cứu trên động vật với omeprazole [4], Dữ liệu tiến cửu cho thay tính an toàn của thuốc này [15]. Pasternak và cộng sự, trong một nghiên cứu thuần tập, không phát hiện sự gia tăng đáng kể các dị tật bẩm sinh lớn khi phơi nhiễm với PPIs trong ba tháng đầu thai kỳ (odds ratio [OR] 1,10, Cl 95% [CI] 0,91-1,34) [16 ]. Trong một phân tích cá thề, không có mồi liên hệ đáng kể nào giữa việc sử dụng bất kỳ loại pp[ cụ thể nào và nguy cơ mắc các dị tật bẩm sinh lớn [16], Nhìn chung, PP1 ngày nay được coi là an toàn ở phụ nữ mang thai và thường chi dành cho các biến chứng GERD hoặc cho thai phụ không đáp ứng với các phương pháp điều trị trước đó [13], Tất cả các thuốc làm giảm độ axit trong dạ dày nén được sử dụng một cách thận trọng, vì chúng có thể làm giảm hấp thu sắt.
Táo bón

Táo bón thường xảy ra trong tam cá nguyệt thứ nhất và thứ hai, ánh hướng tương ứng đến 35% và 39% thai phụ. Tỉ lệ táo bón trong tam cá nguyệt thứ ba và sau sinh được ước tính lần 1ưọ1 là khoảng 20% và 17% [17]. Nguy cơ táo bón dường như cao hơn nếu được ghi nhận ở thai kỳ trước đó và có liên quan đến lượng sắt.
Tỉ lệ táo bón cao hơn ở giai đoạn đầu thai kỳ gợi ý rang hormone sinh dục là yếu tố có ảnh hương lớn. Progesterone gây giãn cơ trơn, dẫn đến giảm nhu động của ruột non và ruột già. Ngoài ra, có ý kiến cho rằng thai phụ có sự tăng hấp thu nước ở ruột già, được giải thích là do nồng độ aldosteron cao hơn gây ra bởi các hormone sinh dục nhtr estrogen và progesterone. Bổ sung sắt trong thai kỳ có thể làm trầm trọng thèm tình trạng táo bón. Cuối cùng, các yếu tố cơ học cũng có thể góp phần vào cuối thai kỳ. Các chuyền động kết hợp của đường ruột và từ cung được phát hiện lá có thể cản trở sự di chuyển về phía trước của phân rắn, cản trở việc đại tiện và gây táo bón [18,19], Mặc dù phần lớn thai phụ được phát hiện là bị táo bón cơ năng, điều quan trọng là phải loại trừ các nguyên nhân cơ học và đặc biệt chú ý đến khả năng mắc bệnh đái tháo đường hoặc suy giáp [ 18].
Quản lý táo bón không dùng thuốc bao gồm uổng đủ nước và chế độ ăn nhiều chất xơ. Lượng thức ăn có thể làm trầm trọng thêm các triệu chứng, đặc biệt là trong tam cá nguyệt thứ hai, và chia nhỏ các bữa ăn có thể là một lựa chọn thay thế [ 17,18]. Điều trị bằng thuốc chi dành cho các bệnh nhân kháng trị vì nó có thể liên quan đến các biển chửng. Thuốc làm tăng khối lượng phân chứa chất xơ (Metamucil®, Citrucel®) có lẽ là thuốc nhuận tràng an toàn nhất được dùng trong thai kỳ, vì chúng không được hấp thu toàn thân [18Ị. Tuy nhiên, chúng không làm giảm các triệu chứng cấp tính và có thể cần vài ngày để bắt đầu có tác dụng. Thuốc nhuận tràng thẩm thấu, nhir lactulose, polyethylene glycol (PEG), glycerol và sorbitol, được coi là an toàn và các nghiên cứu trên động vật cho thấy không có tác dụng gây quái thai [18], Trên thực tế, tuyên bố quan điểm của Hiệp hội Tiêu hóa Hoa Kỳ coi PEG là một loại thuốc cỏ nguy cơ thấp và là loại thuốc ưu tiên cho táo bón mạn tính trong thai kỳ [20,21]. Mặt khác, nên tránh dùng thuốc nhuận tràng kích thích, như sennosides và bisacodyl trong thai kỳ. Các loại thuốc không được khuyến cáo bao gồm dầu khoáng, dầu thầu dầu và các thuốc tăng áp lực thẩm thấu chứa muối [4,21], Table 2 tóm tắt các lựa chọn điều trị được khuyến cáo cho các than phiền đường tiêu hóa phổ biến.
Các bệnh đường tiêu hóa đặc hiệu trong thai kỳ
Ốm nghén nặng (HG)
HG là một dạng buồn nôn và nôn nặng kèm theo sụt cân > 5% trọng lượng trước khi mang thai, mất nước và mất cân bằng điện giải. HG thường xảy ra trước tuần thứ 22 của thai kỳ, ảnh hướng đến 0,3-2,0% thai kỳ và đôi khi cần phải nhập viện [22,23], Trong một nghiên cứu thuần tập dựa trên dân số Canada, Fell và cộng sự đã báo cáo về sự gia tăng nguy cơ HG liên quan đến rối loạn cường giáp, bệnh tâm thần, mang thai trứng trước đó, bệnh đái tháo đường và bệnh hen có tứ trước khi mang thai [24],
Hiện tại, ba căn nguyên chính được mô tả trong y văn. Đầu tiên, nồng độ HCG cao có thế có tác dụng kích thích quá trình bài tiết ở đường tiêu hóa trên. Sản xuất globulin gắn với tuyến giáp cũng tăng dưới sự kích thích của estrogen, dẫn đến giám thyroxine tự do (T4). Nồng độ T4 tự do giám thoáng qua gây kích thích tuyến giáp và bệnh nhân có thể bị nhiễm độc giáp thoáng qua khi mang thai, dẫn đến nôn. Thứ hai, HCG tương tự như hormone kích thích tuyến giáp (TSH) và có thể gầy nôn nhiều do kích thích thụ thể TSH [23], Thứ ba, có một mối quan hệ (-) giữa nồng độ prolactin và buồn nôn / nôn, trong khi estrogen có mối quan hệ (+). Do đó, lượng estrogen cao hon trong thai kỳ có thể làm tăng nguy cơ HG [25].
HG là một chẩn đoán loại trừ. Nó thường kèm theo hạ natri máu, hạ kali máu, ure huyết thanh thấp, hematocrit tăng, nhiễm kiềm chuyển hóa giâm cio máu và ceton niệu. Men gan có thể tăng trong 50% trường hợp. Bệnh nhân bị mất nước do không dung nạp dịch / thức ăn và sút cân do nôn kéo dài. Siêu âm đánh giá thai kỳ là bắt buộc, vì HG có thể liên quan đến đa thai và thai trứng [23],
Không có liệu pháp đơn lẻ nào có lợi đáng kể và cách tiếp cận nội khoa dựa trên điều chỉnh điện giải và ngăn ngừa mất nước [23]. Khi nhập viện, những thai phụ này thường cằn liệu pháp truyền dịch tĩnh mạch đề điều chỉnh rối loạn điện giải. Dung dịch nước muối 0.9% được khuyến cáo để điều chỉnh tình trạng hạ natri máu có thế xảy ra. Trong trường hợp buồn nôn và nôn không nghiêm trọng, thiamine (vitamin BI) và pyridoxine (vitamin B6) có thể thích hợp để ngăn ngừa các triệu chứng nặng. Thiamine cùng ngăn ngừa bệnh não Wernicke ở bệnh nhân nôn kéo dài. Neu bệnh nhân không đáp ứng với liệu pháp bảo tồn, thuốc chống nôn sẽ được chi định, bao gồm thuốc chẹn thụ thể histamin, phenothiazin và thuốc đối kháng dopamin. Suy dinh dưỡng có thể cần cho ăn qua đường ruột với ống thông mũi hỗng tràng, có hiệu quả trong việc kiểm soát triệu chứng và tăng cân ở bệnh nhân HG nặng. Dinh dưỡng toàn phần tĩnh mạch có thể được sir dụng ở những trường hợp đe dọa tính mạng [23],
Bệnh viêm ruột (IBD)
IBD ảnh hưởng đến phụ nữ trong độ tuổi sinh sản và ước tính có khoảng 50% được chẩn đoán trước 32 tuổi [26], IBD có thể liên quan đến kết cục thai kỳ tồi hơn; do đó, khuyến cáo rằng bác sĩ điều trị 1BD và bác sĩ sản khoa cần theo dõi chặt chẽ bệnh nhân. Điều này đặc biệt quan trọng vì nhiều bác sĩ sản khoa có thề không quen với thuốc điều trị IBD và có thể không tư vấn chính xác về việc duy trì thuốc trong thai kỳ.
Thai kỳ có thể ảnh hưởng đến diễn tiến của IBD. Trong một nghiên cứu thuần tập theo dõi kéo dài 10 năm, Riss và cộng sự kết luận rằng thai kỳ không ảnh hưởng đến kiểu hình bệnh hoặc tỷ lệ phẫu thuật, nhưng có liên quan đến việc giám số lần bùng phát trong những năm theo dõi [20], Ngược lại, IBD có thế liên quan đến kết cục tồi hơn trong thai kỳ, ngay cá khi bệnh ổn định [26]. Trong một tổng quan gần đây trên 3907 bệnh nhàn 1BD, Cornish và cộng sự kết luận rằng thai phụ bị IBD có nhiều khả năng sinh non, cân nặng khi sinh thấp và mổ lấy thai, đặc biệt trường hợp cuối cùng xảy ra trong bệnh Crohn. Tất cả kết cục này thường gặp hơn nhiều nếu bệnh hoạt động trong thai kỳ [27]. Thật vậy, hoạt động của bệnh lá yếu tố dự báo mạnh nhất về một kết cục thai kỳ bất lợi [26], Nếu thụ thai xảy ra trong thời gian bệnh ổn định, nguy cơ tái phát tương tự như ở phụ nữ bị IBD không mang thai. Bệnh nhân bị viêm loét đại tràng có 33% nguy cơ tái phát và bệnh nhân mắc bệnh Crohn có nguy cơ khoang 20% [26]. Ngược lại, nếu thụ thai xảy ra trong đợt cấp của bệnh, 2/3 sè mắc bệnh hoạt động dai dẳng và 2/3 trong số này sẽ tiến triển nặng hơn [20], Tương tự như vậy, bệnh hoạt động ở thời điểm thụ thai có liên quan đến nguy cơ sảy thai tự nhiên và sinh non cao hơn, trong khi đó bệnh bùng phát trong thai kỳ làm tăng nguy cơ sinh non, thai chết lưu và cân nặng khi sinh thấp. [26], Trong một nghiên cứu thuần tập trên 462 thai phụ bị 1BD, Mahadevan và cộng sự cùng nhận thấy tỷ lệ biến chứng thai kỳ cao hơn ở bệnh nhân IBD (OR 1,78, 95% Cl 1,13-2,81), như tiền sản giật hoặc vỡ ối sớm [28]. Do đó, thai phụ mắc IBD được khuyến cáo nên có thời gian thuyên giám kéo dài tứ 3 đến 6 tháng trước khi cố gắng mang thai. Nghiên cứu tiến cứu, đa trung tâm đang diễn ra “Pregnancy in Inflammatory Bowel Disease and Neonatal Outcomes” (PIANO) phát hiện tỳ ỉệ đợt cấp cao hơn ở bệnh nhân viêm loét đại tràng so với bệnh nhân Crohn trong thai kỳ [29],
Về phương thức sinh, đa số bệnh nhân có thể sinh thường khi đủ tháng. Bệnh nhân mắc bệnh Crohn có bệnh quanh hậu môn đang hoạt động hoặc trực tràng đang hoạt động nên mổ lấy thai; tương tự như vậy, mặc dù không phải là một chi định tuyệt đối, nhưng thường được khuyên rằng những thai phụ có túi hình chữ J nên mổ lấy thai đến bào tồn khả năng đại tiện tự chủ [26,30],
Một loạt các dấu ấn chẩn đoán có thể được sử dụng để đánh giá mức độ hoạt động của bệnh trong thai kỳ, bao gồm tốc độ lắng hồng cầu, huyết sắc tố, albumin và protein phản ứng c (CRP). Tuy nhiên, các thay đổi sinh lý trong thai kỳ ảnh hưởng đến các dấu ấn sinh học nảy, đặc biệt là CRP, albumin, hemoglobin và số lượng bạch cầu. Theo các nghiên cứu gần dây, nồng độ calprotectin trong phân (FC) không bị thay đổi ở thai phụ khỏe mạnh và do đỏ có thể được dùng để theo dõi hoạt động của bệnh trong thai kỳ [26,31,32], Trong một nghiên cứu quan sát đa trung tâm được thực hiện ờ Đan Mạch, Palsgaard và cộng sự đồ nghị sử dụng FC kết họp với đánh giá tổng thể của bác sĩ đề theo dõi mức độ hoạt động của bệnh trong tất cả các tam cá nguyệt [32]. Tuy nhiên, Meuwis và cộng sự không phát hiện thấy mối tương quan có ý nghĩa thống kê giữa FC đơn thuần và mức độ hoạt động của bệnh trong bất kỳ tam cá nguyệt nào của thai kỳ [33], cần thêm các nghiên cứu để xác định vai trò của FC trong thai kỳ ở thai phụ bị IBD, mặc dù nó có khả năng được sử dụng như dấu ấn sinh học của bệnh tiến triển. Nội soi đại tràng sigma chi nên áp dụng ở những trường hợp nặng, như những người bị chảy máu đường tiêu hóa dưới. Đau bụng và tiêu chảy là những chỉ định yếu hơn cho thủ thuật này [26,34]. Siêu âm. được sử dụng để theo dõi sự phát triển của thai nhi, là an toàn và tia X liều thấp gây nguy cơ tối thiểu cho thai nhi.
Điều trị IBD luôn phải được cân nhắc, vì bệnh hoạt động gây nguy cơ cao hơn đối với thai nhi và mẹ hơn là dùng thuốc [26], Nhìn chung, hầu hết các điều trị cỏ thề được sử dụng trong thai kỳ, ngoại trừ methotrexate và thalidomide, là những chất gây quái thai. 5-aminosalicylate được coi là an toàn trong thai kỳ, mặc dù sulfasalazine cản trở hấp thu axit folic và cần bổ sung liều cao hơn [6]. Azathioprine qua nhau thai và có liên quan đến thiếu máu ở trẻ sơ sinh [6,29]. Tuy nhiên, hầu hết các nghiên cứu cho rằng đó là một liệu pháp an toàn trong thai kỳ. Sè hợp lý hơn nếu tiếp tục đơn trị liệu bằng thioprine đề duy trì sự thuyên giảm IBD hơn là dừng nó và làm tăng nguy cơ bùng phát bệnh. Bằng chứng về việc sử dụng cyclosporine trong IBD chi giới hạn ở một số ít thai phụ có đợt tái phát nặng trong thai kỳ [26], ớ những bệnh nhân được ghép tạng, nó có liên quan đến cân nặng khi sinh thấp và sinh non, mặc dù phát hiện này không được mô tả ở những bệnh nhân IBD. Các thuốc chống yếu tố hoại tử khối u (anti- TNF) infliximab và adalimumab được coi là các thuốc có nguy cơ thấp. Một số nghiên cứu gợi ý rang infliximab không gây quái thai và không (lẫn đến sinh non hoặc cân nặng khi sinh thấp. Đối với adalimumab, dữ liệu hiện có còn hạn chế nhưng không cho thấy kết cục tồi hơn đối với thai kỳ phơi nhiễm với kháng thế này. Tuy nhiên, ảnh hưởng lâu dài khi phơi nhiễm trong từ cung với các thuốc ức chế miễn dịch này đối với sự phát triển hệ thống miễn dịch của trẻ sơ sinh vẫn chưa được biết rõ [6], Đồng thuận ECCO khuyến cáo ngừng liệu pháp kháng TNF trong ba tháng cuối thai kỳ [30], Tuy nhiên, Nguyen và cộng sự trong đồng thuận Toronto khuyến cáo duy tri liệu pháp kháng TNF trong tất cả các tam cá nguyệt [35]. Do đó, quyết định duy trì hoặc ngừng thuốc phải được cân bằng với nguy cơ tái phát, và nên được cá nhân hóa và điều chỉnh cho phù hợp với mong muốn của bệnh nhàn. Điều quan trọng là con cái của những người tham gia nghiên cứu PIANO bị phơi nhiễm với các thuốc sinh học không bị chậm phát triển so với những đứa trẻ không bị phơi nhiễm [29]. Mặt khác, liệu pháp kết hợp giữa kháng TNF và thiopurine có thể liên quan đến sinh non (OR 2,4, Ci 95% 1,3-4,3) và bất kỳ biến chứng thai kỳ nào (OR 1,7, ct 95% 1,0-2,2) [26,29 ]. Dữ liệu sơ bộ hiện có VC tính an toàn của vedolizumab trong thai kỳ vẫn còn hạn chế [26], Dữ liệu rất hạn chế dà được công bố về tính an toàn của ustekinumab trong bệnh Crohn [36], Corticosteroid có thế được dùng trong các đợt bùng phát bệnh, nhưng nên được giới hạn ở liều thấp nhất có hiệu quả và thời gian ngắn nhất để ngăn ngừa các biến chứng như đái tháo đường thai kỳ, tăng huyết áp và cân nặng khi sinh thấp. Mặc dù đã cố báo cáo rằng sử dụng corticosteroid trong ba tháng đầu có liên quan đến tăng nguy cơ dị tật ở mặt – miệng, một nghiên cứu dựa trên dân số gần đây cho thấy không có sự gia tăng nguy cơ này [6,37], Cuối cùng, metronidazol có liên quan đến sứt môi, hở hàm ếch và ciprofloxacin cản trở sự tăng trưởng trong tử cung. Nếu cần dùng kháng sinh, amoxicillin-clavulanic acid là lựa chọn ưu tiên trong thai kỳ [6,30], Quyết định ngừng thuốc nên được cá nhân hóa cho từng bệnh nhãn, có tính đến xác suất tái phát và kiểu hình của bệnh nhân, luôn phải luôn được chia sẻ với bệnh nhân.
Chỉ định phẫu thuật ở thai phụ bị IBD không khác với chỉ định ờ phụ nữ không mang thai [30], Không có thời điểm phẫu thuật cụ thể, vì nó phụ thuộc vào mức độ hoạt động của bệnh. Phẫu thuật tương đối an toàn trong tất cá các tam cá nguyệt, mặc dù có một số báo cáo về sảy thai tự nhiên trong tam cá nguyệt thứ nhất [6,38],
Bệnh gan
Các bệnh gan trong thai kỳ có thể được chia thành các rối loạn chi xay ra trong thai kỳ, các rối loạn xảy ra trúng hợp với thai kỳ và các bệnh gan có từ trước nặng hơn khi mang thai [39]. Chúng ta sẽ tập trung tháo luận về chẩn đoán phân biệt các bệnh chỉ xảy ra trong thai kỳ, với một lưu ý ngắn gọn về nhiễm VI rút viêm gan E (HEV).

Ứ mật trong gan của thai kỳ (ICP)
ICP là một rối loạn ứ mật trong gan lành tính ở cuối thai kỳ, đặc trưng bởi ngứa và tăng nồng độ axít mật ( > 10 pmol / L) và các aminotransferase huyết thanh. Đây là một dạng ứ mật ảnh hưởng bởi nội tiết tố, có thể đảo ngược và các triệu chứng sẽ tự thuyên giâm, thường xáy ra trong vòng 2-3 tuần sau khi sinh [40,41,42], Thời gian cần để bình thường hóa các xét nghiệm gan có thể lâu hơn, lên đến 6-8 tuần. ICP có xu hướng xảy ra ở thai phụ lớn tuổi, sinh nhiều lần và song thai. Tiền sử ICP trước đó, ứ mật trong khi dùng liệu pháp tránh thai đường uống, và tiền sử gia đình mắc cá ICP và ứ mật do thuốc tránh thai có liên quan đến tăng nguy cơ ICP [40].
Sinh lý bệnh có liên quan đến tình trạng nội tiết tố và khuynh hướng di truyền của bệnh nhân. Nồng độ estrogen và progesterone cao hon gây ứ mật do tiết axit mật ít hơn. Estrogen làm giảm tinh thấm của màng đáy bên của tế bào gan, trong khi progesterone gây ra sự kiện này bằng cách ức chế glucuronosyltransferase. Các nghiên cứu gần đây điều tra các gen vận chuyển gan mật. Các đột biến trong chất vận chuyển phospholipid ở gan (MDRD3, ABCB4) và bơm xuất muối mật (BSEP, ABCB11) đã được báo cáo ở thai phụ bị ICP [40],
Chẩn đoán dựa trên sự hiện diện của ngứa bắt đầu ở lòng bàn tay và lòng bàn chân vả thường nặng hơn vào buổi tối. Vàng da có thể xuất hiện trong vòng 1-4 tuần sau khi khởi phát ngứa. Có thể có phân nhiễm mỡ và hấp thu chất béo kém có thể dẫn đến thiếu vitamin K, dẫn đến PT kéo dài và băng huyết sau sinh [40], Các dấu hiệu cận lâm sàng được đặc trưng bơi tăng tổng lượng axit mật (> 12 mmol / L) và aminotransferase tăng 2-10 lần, cá biệt có trường hợp đạt tới 1000 UI / L. Tăng GGT gặp ở 1/3 số trường hợp. Neu GGT tăng, bệnh nhân có khả năng mắc bệnh gan có thành phần di truyền [43]. AP cùng có thể tăng gấp 4 lần, nhưng điều này không giúp ỉch gì cho việc chẩn đoán, vì AP tăng trong thai kỳ do nhau thai sản xuất. Tăng bilirubin máu hiếm khi đạt đến 6 mg / dL và gặp ờ 1/4 số bệnh nhãn. Mặc dù ICP được coi là một rối loạn lành tính đối với mẹ, nó có liên quan đến tăng nguy cơ sinh non, nước ổi nhuộm phân su, nhịp tim thai chậm, suy thai và thai chết lưu. Cơ chế bệnh sinh của những kết cục thai nhi này chưa được hiểu rõ hoàn toàn, nhưng người ta cho rằng nồng độ axit mật cao hơn có thể gây độc và dẫn đến sự phát triển đột ngột các rối loạn nhịp tim thai hoặc co thắt mạch bề mặt màng đệm nhau thai [41],
Phương pháp điều trị đối với ICP bao gồm làm giảm các triệu chứng của mẹ và quản lý sản khoa để ngăn ngừa suy thai. Axit ursodeoxycholic (UDCA) là một trong những thuốc được ưu tiên trong ICP. Cơ chế của UDCA vẫn chưa được biết rõ. Liều hàng ngày dao động từ 10-15 mg / kg có hiệu quả trong việc giảm ngứa, giảm tổng lượng acid mật huyết thanh, ALT và bilirubin, cho phép chấm dứt thai kỳ gần đủ tháng hơn [44], Chấm dứt thai kỳ sớm là lựa chọn duy nhất thực sự cải thiện kết cục lâm sàng. Đồng thuận chung cho rằng không nên trì hoãn chấm dứt thai kỳ sau tuần thứ 37 [42],
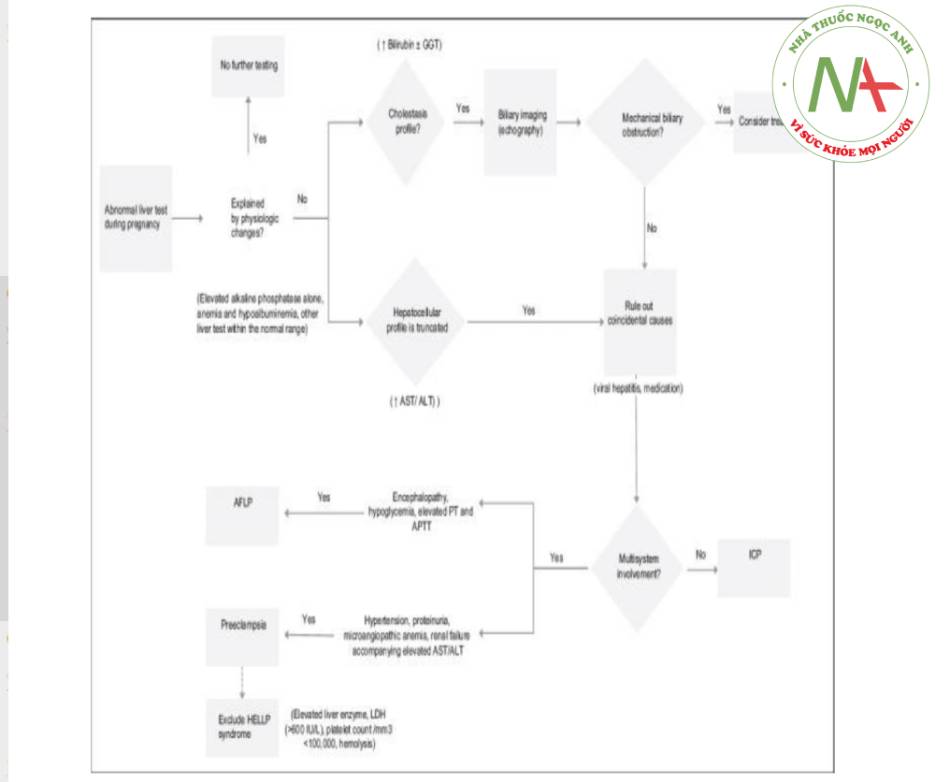
Đầu tiên, loại trừ các bất thường được giải thích do thay đổi sinh lý trong thai kỳ (tăng phosphatase kiềm). Sau đó, đối với tình trạng ứ mật, cần phải loại trừ các nguyên nhân cơ học gây tắc đường mật. Nếu chẩn đoán hình ảnh bình thường hoặc bệnh nhân có xét nghiệm tế bào gan, hãy loại trừ các nguyên nhàn trùng hợp ngẫu nhiên (thuốc, viêm gan vi rút). Đối với ảnh hưởng đến đa cơ quan trong các bệnh gan chi gặp trong thai kỳ, xem xét AFLP (các dấu hiệu rối loạn chức năng gan) hoặc tiền sản giật. Loại trừ hội chứng HELLP. Ngửa mà không liên quan đến đa cơ quan dẫn đến ICP.
AFLP, gan nhiễm mỡ cấp tính thai kỳ; HELLP, tan máu, tăng men gan và sổ hrợng tiểu cầu thấp; 1CP, ứ mật trong gan của thai kỳ; AST, aspartate aminotransferase; ALT, alanin aminotransferase; GGT, gama-glutamyl transferase; LDH, lactate dehydrogenase; PT, thời gian prothrombin; APTT, thời gian thromboplastin hoạt hóa từng phần
Hội chứng tán huyết, tăng men gan và số lượng tiểu cầu thấp (HELLP)
Mặc dù ỷ kiến này còn gây tranh cãi, một số người cho rằng HELLP là một dạng tiền sản giật nặng. Những người khác tin rằng nó là một thực thề riêng biệt [47], Hội chứng HELLP được xác định bởi sự hiện diện của tán huyết, tăng men gan và giảm tiểu cầu. Nó xảy ra ờ 0,17-0,85% thai kỳ, thường gặp hơn ở thai phụ da trang sinh nhiều lần, nhiều tuổi (> 34 tuổi). 70% trường hợp được chẩn đoán trước sinh, thường gặp nhất là từ tuần thứ 27 đến tuần thứ 37 của thai kỳ [48], 30% còn lại được chẩn đoán sau khi sinh. Trong số này, 90% bị TSG trong thai kỳ. Khoáng 5-10% thai phụ bị tiền sản giật nặng phát triển HELLP. Cơ chế bệnh sinh dường như tương tự như tiền sản giật, với tổn thương nội mô và vi mạch toàn thân dẫn đến thiếu máu vi mạch, hoại tử gan quanh khoáng cừa và giâm tiểu cầu [40],
Hầu hết bệnh nhân than phiền đau đầu, buồn nôn và nôn, rối loạn thị giác và đau vùng thượng vị, khám lâm sàng thấy đau vùng hạ sườn phải, tăng cân và phù toàn thân. Các dấu hiệu cận lâm sàng bao gồm tán huyết, đặc trưng bởi nồng độ lactate dehydrogenase cao (> 600 Uí / L) với giá trị haptoglobin giảm, tăng bilirubin máu không liên họp, tăng aminotransferase và giảm tiểu cầu.
Phân loại Mississippi được phát triển đề phân nhóm mức độ nặng của hội chứng HELLP (Table 3). Neu số lượng tiểu cầu < 50.000 / mm3, có thể kèm theo đông máu máu rải rác trong lòng mạch số lượng tiểu cầu không tăng sau 96 giờ kể từ lúc sinh cho thấy tiên lượng xấu hơn với khả năng tiến triển thành suy đa tạng [49], Thời gian PT và thời gian thromboplastin hoạt hóa từng phần (APTT) bình thường trong giai đoạn đầu. Do hậu quả của quá trình tiêu sợi huyết thứ phát và kết tập tiểu cầu, nồng độ các sản phẩm fibrin, d-dimer và phức hợp thrombin-antithrombin có thề cao. Một số bệnh nhân, thận cũng bị ảnh hưởng.
Suy gan cấp là một biển chửng hiếm gặp với tỷ lệ mắc là 5 í 100.000. Vờ gan tự phát xảy ra < 2% trường hợp. Bệnh nhân bị ảnh hưởng thường có biểu hiện đau vùng hạ sườn phải kèm theo buồn nôn, nôn, tăng huyết áp hoặc sốc giảm thể tích do vỏ bao Glisson (50). Siêu âm hoặc chụp cộng hưởng từ thường giúp chẩn đoán xuất huyết dưới bao hoặc trong nhu mô và vỡ gan [40]. Xử trí bao gồm cà lấy thai ra khẩn cấp và
phẫu thuật gan. Có thế cần ghép gan khi suy gan tối cấp hoặc xuất huyết không kiểm soát được trong quá trình phẫu thuật mở bụng [50],
Từ vong chu sinh thường do nhau bong non và ngạt trong tử cung. Tỷ lệ tử vong mẹ là 1 -3,5% do rối loạn đông máu và xuất huyết [49],
Quản lý những bệnh nhân này nên được thực hiện tại các Đơn vị Chăm sóc Đặc biệt và bao gồm lọc máu và hỗ trợ thở máy ở trường hợp nặng, thuốc chống huyết khối, aspirin liều thấp, prostacyclin, thuốc ức chế miễn dịch, steroid và huyết tương tươi đông lạnh. Tuy nhiên, chấm dứt thai kỳ là liệu pháp đặc hiệu duy nhất trong hội chứng HELLP [40],
Gan nhiễm mỡ cấp tính thai kỳ (ALFP)
ALFP là một rối hiếm gặp nhưng tiềm ẩn nguy hiểm xảy ra trong ba tháng cuối thai kỳ (giữa tuần thứ 30 và 38) hoặc đầu thời kỳ hậu sản [40], Ngày nay, tỉ lệ tử vong mẹ và tử vong chu sinh lần lượt là khoảng 18% và 25%. AFLP có thể do rối loạn chức năng ty thể trong gan của thai nhi. 3-hydroxyacyl-CoA dehydrogenase chuồi dài là một trong những thiếu hụt enzyme quan trọng nhất được ghi nhận. Thiếu hụt enzym này dẫn đến tích tụ của các axit béo chuỗi dài trong tuần hoàn của thai nhi và mẹ. Vì người mẹ là dị hợp tử đối với enzyme, quá trình chuyển hóa axit béo chuỗi dài bị suy giảm và trở nên độc hại với thâm nhiễm mỡ dạng vi hạt trong tế bào gan.
Bệnh nhân thường có các triệu chứng không đặc hiệu, như chán ăn, buồn nôn, nôn, đau đầu và đau bụng. Các dấu hiệu lâm sàng quan trọng nhất là sốt và vàng da, xảy ra ở 70% bệnh nhân. Khoảng 50% bệnh nhân có các dấu hiệu cùa TSG [40], Các dấu hiệu cận lâm sàng bao gồm số lượng bạch cầu tăng cao (> 15.000 / L) kèm theo hematocrit bình thường, trừ khi có xuất huyết hoặc tán huyết. PT và APTT đều kéo dài, với nồng độ fibrinogen thấp. Aminotransferase tăng cao, với mức tăng lên đến 300-500 UI / L, và có thể liên quan đến nhiễm toan lactic, tăng bilirubin và hạ đường huyết.
AFLP là chẩn đoán phân biệt cùa tiền sản giật, hội chứng HELLP, ICP và viêm gan vi rút. Xu hướng hạ đường huyết, tăng amoniac máu và thời gian PT và APTT kéo dài giúp phân biệt AFLP với HELLP [39). Xét nghiệm huyết thanh gan cũng nôn là một phần cùa thăm khám bổ sung.
AFLP là một cấp cứu sản khoa và nội khoa. Chấm dứt thai kỳ kịp thời và chăm sóc hỗ trợ tích cực là nền tảng trong quân lý AFLP [49].
Nhiễm vi rút viêm gan E (HEV)
HEV là một loại vi rút lây truyền qua đường ruột gây viêm gan rõ trên lâm sàng ở các nước đang phát triển như Ấn Độ, Châu Á, Châu Phi và Trung Mỹ. Nguồn lây truyền HEV chinh là nước uống bị ô nhiễm. Gằn đày, ngày càng có nhiều trường hợp mắc bệnh xuất hiện ở các nước phát triển do lây nhiễm từ động vật sang người [51 ]. Một trong những đặc điểm giúp phân biệt HEV với các loại virus gây bệnh ái tinh với gan khác là diễn tiến gày độc cùa nó trong thai kỳ, thường tiến triển thành suy gan tối cấp hơn. Tỷ lệ tử vong lên đến 10 – 20% ở thai phụ. Nhiêm HEV cấp tính đặc biệt nặng trong tam cá nguyệt thứ hai và ba [52].
Người ta đã công nhận ràng tỳ lệ từ vong cao hơn có liên quan đến những thay đổi về nội tiết tố và miễn dịch. Navaneethan và cộng sự báo cáo rằng có sự thay đổi rõ ràng từ mô hình tế bào Thl sang Th2 trong thai kỳ và nồng độ cùa hầu hết các cytokine đều giám, đặc biệt trong 20 tuần đầu tiên cùa thai kỳ [51], Ngoài ra, trong các nghiên cứu trên động vật, nồng độ progesterone, estrogen và [i-HCG cao hơn có liên quan đến tác dụng ức chế miễn dịch qua trung gian tế bào. Cả hai cơ chế này đều có thề dẫn đến nhạy cảm cao hơn đối với độc lực cùa HEV [51], Tuy nhiên, không có nghiên cứu nào xác nhận mối quan hệ nhân quả giữa những phát hiện sinh lý này và nhiễm HEV.
Hầu hết các nghiên cứu về HEV ở thai phụ được thực hiện ở các nước có tỷ lệ nhiễm HEV cao. Bệnh não là biến chứng phổ biến nhất của nhiễm HEV cấp tính trong thai kỳ, sau đó là xuất huyết tiêu hóa, suy thận và co giật. Thai phụ bị suy gan cấp tinh có tiên lượng xấu hơn những thai phụ chì bị viêm gan cấp tính, với tỷ lệ chết trong tử cung cao hơn (78,6% so với 11,4%), sinh non (65,7% so với 17,3%) và tử vong mẹ (56,2% so với . 0,9%) [53], Lây truyền dọc cũng đã được báo cáo và có thể xảy ra ở bất kỳ thời điểm nào trong thai kỳ. Tuy nhiên, nhiễm HEV thường tự giới hạn ở trẻ sơ sinh và viêm gan tối cấp rất hiếm gặp.
Mặc dù nhiễm HEV có thể nặng trong thai kỳ, nhưng điều trị chỉ mang tính chất hỗ trợ. Ghép gan có thế được xem xét trong một số trường hợp [54]. Cách tiếp cận tốt nhất là thông qua phòng ngừa. Hai loại vắc xin tái tổ hợp khác nhau đã được phát triển, nhưng vẫn chưa được chấp thuận.
Tiền sản giật / sản giật
Tiền sản giật được xác định bằng sự hiện diện của tăng huyết áp và protein niệu sau tuần thứ 20 của thai kỳ; có ảnh hưởng đến 2-8% thai kỳ. Sán giật được xem xét khi thai phụ bị tiền sản giật xuất hiện các cơn co giật mà không có bất kỳ giải thích nào khác. Tiền sản giật / sản giật là một rối loạn đa hệ thống đặc trưng bói đáp ứng bất thường cùa mạch máu đối với sự tăng trưởng của bánh nhau kèm theo co mạch, rối loạn chức năng nội mô, thay đổi chuyển hóa và tăng đáp ứng viêm [40,45]. Ảnh hưởng đến gan có thề được giải thích là do co thắt động mạch gan và lắng đọng fibrin trong khu vực khoảng cửa và quanh khoáng cửa cùa tiểu thùy gan, có thề dẫn đến thiếu máu cục bộ tiếu thùy và hoại từ tế bào gan.
Chẩn đoán dựa trên tăng huyết áp với huyết áp trên 140/90 mmHg ờ hai lần đo liên tiếp (cách nhau 6 giờ) và tý số protein niệu: protein nước tiểu > 0,3 g trong mẫu nước tiểu 24 giờ, tỷ số protein (mg / dL) / creatinine (mg / dL) > 0,3, hoặc protein que nhúng nước tiểu 1-e [40]. Thai phụ than phiền đau đầu dữ dội và dai dẳng kèm theo nôn, phù ngoại vi, nhìn đôi và nhìn mờ. Men gan bất thường gặp ờ 20% đến 30% các trường hợp, với mức độ tăng từ nhẹ đến trung bình (1,5-5 lần bình thường). Bilirubin liên hợp, albumin và PT có xu hướng vẫn trong giới hạn bình thường [47], Tiền sản giật được coi là nặng nếu có các đặc điểm sau: phù phổi, co giật, thiểu niệu, giám tiểu cầu (<100.000 ỉ pL), men gan bất thường kèm theo đau vùng thượng vị hoặc hạ sườn phải dai dẳng và các triệu chứng ở hệ thần kinh trung ương như đau đầu, nhìn mờ, mù hoặc thay đổi ý thức [44], Sinh non (15-65%) và thai chậm tăng trưởng (10-25%) là những hậu quả bất lợi thường gặp nhất đối với thai nhi [45],
Tình trạng gan liên quan đến tiền sản giật / sản giật không cần điều trị đặc hiệu và tiếp cận nội khoa dựa trên việc kiểm soát huyết áp, giảm các triệu chứng liên quan và điều trị kịp thời các cơn co giật [40], Sau 37 tuần, thai phụ bị tiền sản giật nên được chấm dứt thai kỳ [46], Trong các trường hợp TSG cỏ các tiêu chí mức độ nặng, nên cân nhắc sinh thai ở tuần 34 hoặc thậm chí sớm hơn (24-34 tuần), nếu tình trạng thai hoặc mẹ xấu đi.
Nội soi trong thai kỳ
Nội soi tiêu hóa thường được coi là một thủ thuật an toàn. Tuy nhiên, có nhiều nguy cơ tiềm ẩn liên quan đến nội soi trong thai kỳ [55], Mọt nghiên cứu thuần tập dựa trên dân số Thụy Điển gần đây phát hiện nội soi có liên quan đến tăng nguy cơ sinh non hoặc trẻ nhỏ so với tuổi thai, mặc dù không tìm thấy mối liên quan nào với dị tật bẩm sinh hoặc thai chết lưu [56],
Các chỉ định phổ biến nhất đề nội soi đường tiêu hóa trên ở thai phụ là xuất huyết tiêu hóa lớn hoặc liên tục, khó nuốt và buồn nôn và nón kháng trị. Nguyên nhân phổ biến nhất gây xuất huyết cấp tính không do giãn tĩnh mạch là vết rách Mallory-Weiss. Những thai phụ bị giãn tĩnh mạch thực quản hoặc bệnh gan nặng nên được tư vấn về nguy cơ vỡ búi giãn tĩnh mạch. Nội soi thường không được chỉ định trong trường hợp buồn nôn và nôn nhiều khi mang thai hoặc HG, nhưng nếu bệnh nhân buồn nôn và nôn nhiều, kèm theo đau bụng kháng trị với các điều trị nội khoa thì nội soi có thể là thích hợp để chẩn đoán loét dạ dày tá tràng lớn hoặc tắc nghẽn đường ra dạ dày. Tiêm epinephrine, nhiệt động và điện động đã được chứng minh là thành công ở tất cả bệnh nhàn trong thai kỳ, ngoại trừ những người cần phẫu thuật. Epinephrine có thề làm giảm lưu lượng máu đến thai nhi. Tuy nhiên, không có tác dụng bất lợi nào được báo cáo trong y vãn hiện có [34,57], Trong quá trình điện đông, nước ối có thế dẫn dòng điện đến thai nhi, do đó nên đặt một miếng đệm tiếp đất cách xa từ cung và áp dụng phương pháp đốt điện lưỡng cực để giám thiểu nguy cơ. Tuy nhiên, có rất ít dữ liệu liên quan đến việc cầm máu đối với chảy máu không do giãn tĩnh mạch ở bệnh nhân mang thai và kỹ thuật điều trị dựa trên ý kiến chuyên gia từ bệnh nhân không mang thai. Liệu pháp xơ hóa vá thắt vòng nội soi là những thủ thuật an toàn trong thai kỳ [55],
Nội soi đại tràng và nội soi đại tràng sigma được chi định trong đánh giá xuất huyết đường tiêu hóa dưới lớn, nghi ngờ khối u ở đại tràng và tiêu chảy nặng dai dẳng không rõ nguyên nhân [55], Nội soi đại tràng sigma được coi là an toàn và hiệu quả khi thực hiện tham vấn sản khoa. Có rất ít dữ liệu đánh giá tính an toàn và các biến cố bất lợi cùa nội soi đại tràng trong thai kỳ, vì vậy thủ thuật này chỉ được thực hiện khi thật sự cần thiết. Tuy nhiên, khi được yêu cầu trước phẫu thuật, nội soi đại tràng nên được thực hiện đề đánh giá nghi ngờ một khối u / ung thư đại tràng, xuất huyết nặng không kiểm soát được, chít hẹp đại tràng không rõ nguyên nhân. Tất cả các chi định tự chọn nên được trì hoãn cho đến sau khi sinh.
Mang thai có liên quan đến tăng nguy cơ sỏi mật. Các biến chứng tắc nghẽn ống mật chủ hoặc ống mật phụ có thể xảy ra, bao gồm viêm túi mật, sỏi đường mật và viêm tụy, mặc dù những biến chứng này rất hiếm gặp. vẫn còn tranh cãi về tính an toàn cùa phương pháp nội soi mật tụy ngược dòng (ERCP) trong thai kỳ, và dữ liệu còn hạn chế do phơi nhiễm tia xạ đối với thai nhi và nguy cơ cùa thú thuật đối với kết cục cùa mẹ [30]. Các chỉ định ERCP bao gồm cơn đau quặn mật tái phát, xét nghiệm chức năng gan bất thường và giãn ống mật trên siêu âm [58]. Sỏi ổng mật chủ, viêm tụy mật và viêm đường mật cùng là những chỉ định ERCP trong thai kỳ. Siêu âm nội soi không chống chỉ định trong thai kỳ và có thể làm giâm các can thiệp không cần thiết ở những bệnh nhân có xác suất sôi đường mật-ống mật chủ thấp hơn hoặc trung binh [55].
Thuốc an thần có thề được sử dụng an toàn trong thai kỳ. Hai nghiên cứu xác nhận meperidine không gây quái thai và có thể sử dụng trong giai đoạn này. Khi an thần chi với meperidine không dù, có thề dùng midazolam như là liệu pháp bổ trợ. Tuy nhiên, benzodiazepine thường không được khuyến cáo trong thai kỳ. Diazepam có liên quan đến tật hở hàm ếch và rối loạn hành vi thần kinh. Propofol dường như là một lựa chọn an toàn hơn so với benzodiazepin, vì không có báo cáo về tác dụng gây quái thai ờ động vật hoặc người [59]. Cà propofol và midazolam nên tránh trong ba tháng đầu thai ký. Fentanyl không nên được kê đơn [60].
Kết luận
Tiếp cận nội khoa đối với thai phụ là một thách thức. Các bác sĩ lâm sàng phải đánh giá khả năng mắc các bệnh đặc hiệu trong thai kỳ và lựa chọn chiến lược điều trị tốt nhất, lưu ý các lựa chọn không gây hại cho thai nhi. Trong bài tống quan này, chúng tôi đầ tóm tắt các chẩn đoán và xử trí cần thiết mà các bác sĩ chuyên khoa tiêu hóa cần xem xét khi tiếp cận một thai phụ, để cái thiện hướng dẫn lâm sàng cùa chúng tôi. Những cân nhắc cụ thế là cần thiết liên quan đến IBD vâ khám nội soi trong giai đoạn này. Chủng tôi cũng nhấn mạnh sự cần thiết cùa một tiếp cận đa chuyên khoa để ngăn ngừa các biến chứng thai kỳ và xác định chiến lược và thời điểm chấm dirt thai kỳ tốt nhất.
Tham khảo
- Ahmed KT, Ahnashhrawi AA, Rahman RN, Hammoud CM, Ibdah JA. Liver diseases in pregnancy: diseases unique to pregnancy. World J Gastroenterol 2013;19:7639-7646.
- Tan EK, ‘Tan EL. Alterations in physiology and anatomy during pregnancy. Best Pract Res Clin Obstet Gynaecol 2013;27:791 -802.
- Augustin G, Majerovic M. Non-obstetrical acute abdomen during pregnancy. Eur J Obstet Gynecol Reprod Biol 2007;131:4-12.
- Body c, Christie JA. Gastrointestinal diseases in pregnancy. Nausea, vomiting, hyperemesis gravidarum, gastroesophageal reflux disease, constipation, and diarrhea. Gastroenterol Clin North Am 2016;45:267-283.
- Matthews A, Hass DM, O’Mathuna DP, Dowswell T. interventions for nausea and vomiting in early pregnancy. Cochrane Database Syst Rev 2015; 8:CD007575.
- van der Woude CJ, Metselaar HJ, Danese s. Management of gastrointestinal and liver diseases during pregnancy. Gut 2014;63:1014-1023.
- Giacosa A, Morazzoni p, Bombardelli E, Riva A, Porro GB, Rondanelli M. Can nausea and vomiting be treated with ginger extract? Eur Rev Med Pharmacol Sci 2015;19:1291-1296.
- Pasternak B, Svanstrom H, Hviid A. Ondansetron in pregnancy and risk of adverse fetal outcomes. N Engl J Med 2013;368:814-823.
- Shehmar M, MacLean MA, Nelson-Piercy c, Gadsby R, O’Hara M. The management of nausea and vomiting of pregnancy and hyperemesis gravidarum. Royal College of Obstetricians and Gynaecologists Green-top Guideline No. 69,2016
- All RA, Egan LJ. Gastroesophageal reflux disease in pregnancy. Best Pract Res Clin Gastroenterol 2007;21:793-806.
- Ching C, Lam s. Antacids: indicationsand limitations. Drugs 1994;47:305-317.
- Tytgat GN, Heading RC, Miíller-Lissner s, et al. Contemporary understanding and management of reflux and constipation in the general population and pregnancy: a consensus meeting. Aliment Pharmacol Ther 2003;) 8:291-301.
- Richter JE. Review article: the management of heartbum in pregnancy. Aliment Pharmacol Ther 2005;22:749-757.
- Gill SK, O’Brien L, Einarson TR, Koren G. The safety of proton pump inhibitors (PPIs) in pregnancy: a meta-analysis. Am J Gastroenterol 2009; 104:1541- 1545; quiz 1540, 1546.
- Mahadevan u. Gastrointestinal medications in pregnancy. Best Pracl Res Clin Gastroenterol 2007;21:849-877.
- Pasternak B, Hviid A. Use of proton-pump inhibitors in early pregnancy and the risk of birth defects. N Eng! J Med 2010;363:2114-2123.
- Derbyshire E, Davies J, Costareili V, Dettmar p. Diet, physical inactivity and the prevalence of constipation throughout and after pregnancy. Matem Child Nutr 2006;2:127-134.
- Cullen G, O’Donoghue D. Constipation and pregnancy. Best Pract Res Clin Gastroenterol 2007;21:807-818.
- Wald A. Constipation, diarrhoea and symptomatic hemorrhoids during pregnancy. Gastroenterol Clin North Am 2003;32:309-322.
- Riis L, Vind I, Politi p, et al; European Collaborative study group on Inflammatory Bowel Disease. Does pregnancy change the disease course? A study in a European cohort of patients with inflammatory bowel disease. Am J Gastroenterol 2006;101:1539-1545.
- Bharucha AE, Dom SD, Lembo A, Pressman A; American Gastroenterological Association. American Gastroenterological Association medical position statement on constipation. Gastroenterology 2013; 144:211 -217
- Bailit J. Hyperemesis gravidarium: epidemiologic findings from a large cohort. Am J Obs Gynecol 2005; 193’811-814.
- Ismail SK, Kenny L. Review on hyperemesis gravidarum. Best Pract Res Clin Gastroenterol 2007;21:755-769.
- Fell DB, Dodds L, Joseph KS, Alien VM, B. B. Risk factors for hyperemesis gravidarum requiring hospital admission during pregnancy. Obstet Gynecol 2006; 107(2 Pt l):277-284.
- Lagiou PN, Tamimi R, Mucc LA, Trichopoulos D, H.o. A, Hsieh c Nausea and vomiting in pregnancy in relation to prolactin, estrogens, and progesterone: a prospective study. Obstet Gynecol 2003; 101:639-644.
- McConnell RA, Mahadevan u. Pregnancy and the patient with inflammatory bowel disease: fertility, treatment, delivery, and complications. Gastroenterol Clin North Am 2016;45:285-301.
- Cornish J, Tan E, Teare J, et al. A tneta-analysis on the influence of inflammatory bowel disease on pregnancy. Gut 2007;56:830-837.
- Mahadevan u, Sandborn WJ, Li DK, Hakitnian s, Kane s, Corley DA. Pregnancy outcomes in women with inflammatory bowel disease: a large communitybased study from Northern California. Gastroenterology 2007; 133:1106-1112.
- Mahadevan u, Martin CF, Sandler RS, et al. PIANO: A 1000 patient prospective registry of pregnancy outcomes in women with IBD exposed to immunomoduiators and biologic therapy. Gastroenterology 2012;142 Suppl LS-149.
- Van der Woude CJ, Ardizzone s, Bengtson MB, et al. The second European evidenced-based consensus on reproduction and pregnancy in inflammatory bowel disease. J Crohns Colitis 2015;9:107-124.
- Bálint A, Berényi A, Farkas K, et al. Pregnancy does not affect fecal calprotectin concentration in healthy women. Turk J Gastroenterol 2017,28:171-175.
- Julsgaard M, Hvas CL, Geaưy RB, et al. Fecal calprotectin is not affected by pregnancy: clinical implications for the management of pregnant patients with inflammatory bowel disease. Inflamm Bowel Dis 2017;23:1240-1246.
- Meuwis M, Vemier-Massouille G, Grimaud J, et al. Serum calprotectin as a biomarker for Crohn’s disease. J Crohns Colitis 2013;7:e678-e683.
- Qureshi WA, Rajan E, Adler DG, et al, American Society for Gastrointestinal Endoscopy. ASGE Guideline: Guidelines for endoscopy in pregnant and lactating women. Gastrointest Endosc 2005;61:357-362.
- Nguyen GC, Seow CH, Maxwell c, et al; Canadian Association of Gastroenterology. The Toronto consensus statements for the management of inflammatory bowel disease in pregnancy. Gastroenterology 2016;150:734-757.
- Levy RA, de Jesus GR, de Jesus NR, Kiumb EM. Critical review of the current recommendations for the treatment of systemic inflammatory rheumatic diseases during pregnancy and lactation. Autoimmun Rev 2016,15:955-963.
- Park-Wyllie L, Mazzotta p, Pastuszak A, et al. Birth defects after maternal exposure to corticosteroids: prospective cohort study and meta-analysis of epidemiological studies. Teratology 2000;62:385-392.
- Hill J, Clark A, Scott NA. Surgical treatment of acute manifestations of Crohn’s disease during pregnancy. J R Soc Med 1997;90:64-66.
- Schutt VA, Minuk GY. Liver diseases unique to pregnancy. Best Pract Res Clin Gastroenterol 2007;21:771-792.
- Pusl T, Betters u. (ntrahepatic cholestasis of pregnancy. Orphanet J Rare Dis 2007;2:26.
- Ozkan s, Ceylan Y, Ozkan ov, Yildirim s. Review of a challenging clinical issue: Intrahepatic cholestasis of pregnancy. World J Gastroenterol 2015;21:7134- 7141.
- Lammert F, Marschall HU, Glantz A, Matern s. Intrahepatic cholestasis of pregnancy: molecular pathogenesis, diagnosis and management. J Hepatol 2000;33:1012-1021.
- Glantz A, Marschall HU, Lammert F, Mattsson LA. Intrahepatic cholestasis of pregnancy: a randomized controlled trial comparing dexamethasone and ursodeoxycholic acid. Hepatology 2005;42:1399-1405.
- Sibai B, Dekker G, Kupferminc M. Pre-eclampsia. Lancet 2005;365:785-799.
- Tran TT, Ahn J, Reau NS. ACG Clinical Guideline: liver disease and pregnancy. Am J Gastroenterol 2016;l 11:176-194; quiz 196
- Rahman TM, Wendon J. Severe hepatic dysfunction in pregnancy. QJM 2002;95:343-357.
- Mihu D, Costin N, Mihu CM, Seicean A, Ciortea R. HELLP syndrome – A multisystemic disorder. J Gastrointestin Liver Dis 2007;16:419-424.
- O’Brien J, Buckley o, Munk p. Torreggiani w. An unusual case of elevated liver enzymes: hepatic necrosis following HELLP syndrome. Eur Radiol 2007;) 7:289- 291.
- Pavlis T, Aioizos s, Aravosita p, et al. Diagnosis and surgical management of spontaneous hepatic rupture associated with HELLP syndrome. J Suig Educ 2009;66:163-167.
- Navaneethan u, Al Mohajer M, Shata MT. Hepatitis E and pregnancy: understanding the pathogenesis. Liver Int 2008;28:l 190-1199.
- Shinde N, Patil T, Deshpande A, Gulhane R, Patil M, Bansod Y. Clinical profile, maternal and fetal outcomes of acute hepatitis e in pregnancy. Ann Med Health Sci Res 2014;4:S133-SI39.
- Rac MW, Sheffield JS. Prevention and management of viral hepatitis in pregnancy. Obstet Gynecol Clin North Am 2014;41:573-592.
- Shalimar, Acharya SK. Hepatitis E and acute liver failure it) pregnancy. J Clin Exp Hepatol 2013;3:213-224.
- Savas N. Gastrointestinal endoscopy in pregnancy. World J Gastroenterol 2014;20:15241-15252.
- Ludvigsson JF, Lebwohl B, Ekbom A, et al. Outcomes of pregnancies for women undergoing endoscopy while they were pregnant: a nationwide cohort study. Gastroenterology 2017; 152:554-563.
- O’Mahony s. Endoscopy in pregnancy. Best Pract Res Clin Gastroenterol 2007;21:893-899.
- Tang SJ, Mayo MJ, Rodriguez-Frias E, et al. Safety and utility of ERCP during pregnancy. Gastromtest Endosc 2009;69:453-461.
- Neuman G, Koren G. Safety of procedural sedation in pregnancy. J Obstet Gynaecol Can 2013;35:168-173.
- Shergill AK, Ben-Menachem T, Chandrasekhara V, et al, ASGE Standard of Practice Committee. Guidelines for endoscopy in pregnant and lactating women. Gastrointest Endosc 2012;76:18-24.

