Tác giả: Lê Thị Thanh Xuân, Nguyễn Thị Quỳnh
Bài viết Tổng quan về vaccine COVID-19 được trích từ chương 22 trong phần 5 “MỘT SỐ VẤN ĐỀ LƯU Ý TRONG COVID-19” sách Chẩn đoán và điều trị COVID-19.
COVID-19 đang là một khủng hoảng y tế công cộng toàn cầu; trong khi mọi nỗ lực đang tập trung vào việc phát triển vắc xin, phương pháp điều trị cũng như thực hiện các biện pháp y tế (đeo khẩu trang, rửa tay…) thì biến chủng vi rút mới không ngừng xuất hiện làm cho cuộc chạy đua ngày càng khốc liệt và khó tiên lượng. Trong khi dịch bệnh ngày càng diễn biến phức tạp thì vắc xin là chìa khóa trong việc giảm lây nhiễm, giảm tỷ lệ nhập viện và tử vong khi mắc COVID-19. Hiện nay nhờ ứng dụng nhiều tiến bộ trong khoa học, trên thế giới đã có nhiều nền tảng phát triển vắc xin cho phép rút ngắn thời gian sản xuất vắc xin COVID-19. Tuy nhiên kể cả với những công nghệ mới này, cuộc chạy đua giữa con người và vi rút vẫn còn nhiều thách thức. Vắc xin cũng không phải là “viên đạn bạc”, nên chúng ta cần phải kết hợp cả những biện pháp y tế công cộng để sớm đẩy lùi đại dịch COVID-19.
1. MỘT SỐ KHÁI NIỆM LIÊN QUAN ĐẾN VẮC XIN COVID-19
1.1. Vắc xin
Vắc xin là chế phẩm sinh học có tính kháng nguyên có nguồn gốc từ vi sinh vật gây bệnh hoặc vi sinh vật có cấu trúc kháng nguyên giống vi sinh vật gây bệnh, đã được bào chế đảm bảo độ an toàn cần thiết, giúp cơ thể tạo ra miễn dịch chủ động có tác dụng dự phòng mầm bệnh trong tương lai, giúp cơ thể không bị bệnh khi tiếp xúc tác nhân gây bệnh truyền nhiễm.
1.2. Miễn dịch cộng đồng
Miễn dịch cộng đồng là sự bảo vệ gián tiếp khỏi một bệnh truyền nhiễm khi một quần thể được miễn dịch thông qua tiêm chủng hoặc miễn dịch tự nhiên. Nếu chúng ta chọn cách tạo miễn dịch cộng đồng bằng cách mắc bệnh sẽ dẫn đến thiệt hại kinh tế, tinh thần và gây ra những trường hợp tử vong đáng tiếc. Trong khi con đường tiêm vắc xin cũng tạo ra những kháng thể giống như mắc bệnh, nhưng lại không làm chúng ta bị bệnh. Miễn dịch cộng đồng còn phụ thuộc vào hệ số lây lan (R) của dịch bệnh và hiệu quả (VE) của vắc xin mà cộng đồng đó tiêm chủng.
Bảng 22.1. Hiệu quả của một số vắc xin trong cộng đồng đối với biến chủng Alpha
| Vắc xin | Giảm lây nhiễm (%) | Giảm nhập viện (%) | Giảm tử vong (%) |
| Pfizer | 61 (51-69) | 43 (33-52) | 72 (19-100) |
| Moderna | 75 (67-81) | 60 (14-79) | – |
| Astrazeneca | 60 (41-73) | 94 (73-99) | – |
Hệ số lây lan của SARS-CoV-2 khoảng 2,5. Ví dụ: một cộng đồng tiêm vắc xin Moderna với VE = 75%, R = 2,5 thì 80% dân số tiêm vắc xin sẽ tạo ra miễn dịch cộng đồng. Hệ số lây lan phụ thuộc vào thói quen đeo khẩu trang, giãn cách xã hội và các chính sách phòng dịch ở mỗi nước.
Miễn dịch tự nhiên và miễn dịch từ vắc xin COVID-19
Hầu hết các vắc xin COVID-19 hiện nay hướng đến protein gai (protein S) có trên bề mặt của vi rút SARS-CoV-2 như vắc xin của Pfizer/BioNTech, Moderna, AstraZeneca, Johnson & Johnson, Sputnik V; hoặc sử dụng công nghệ bất hoạt để sản xuất vắc xin như Sinopharm hoặc Sinovac, Hayat – Vax để “huấn luyện” hệ miễn dịch của cơ thể làm quen với vi rút SARS-CoV-2. Trong khi đó khi bị nhiễm COVID-19 hệ miễn dịch sẽ có trí nhớ với nhiều loại protein (trong đó bao gồm cả protein gai). Những người đã bị nhiễm COVID 19 trước đó có nguy cơ tái nhiễm COVID-19 thấp hơn 11- 12,5 lần so với những người chưa mắc COVID-19 và khả năng bảo vệ kéo dài dao động từ 3 -12 tháng. Miễn dịch tự nhiên sẽ giảm theo thời gian, tuy nhiên, những người được tiêm thêm 1 liều vắc xin mRNA sẽ có nguy cơ tái nhiễm thấp hơn (10%) so với những người không được tiêm vắc xin (41%). Khi so sánh miễn dịch tự nhiên và miễn dịch sau tiêm vắc xin 2 liều vắc xin COVID-19 Pfizer, kết quả cho thấy những người tiêm vắc xin có nguy cơ bị nhiễm thấp hơn những người đã từng mắc COVID-19 trước đó. Vì vậy để ngăn ngừa dịch bệnh việc tiêm vắc xin COVID-19 là cần thiết.
2. MỘT SỐ VẮC XIN COVID 19 HIỆN NAY
Tính đến ngày 22 tháng 9 năm 2021, trên thế có 121 vắc xin đã và đang phát triển ở giai đoạn tiền lâm sàng và 194 vắc xin ở giai đoạn thử nghiệm lâm sàng, trong đó đã có 6 loại vắc xin được Tổ chức Y tế thế giới (WHO) phê chuẩn sử dụng khẩn cấp và một loại vắc xin đã được Cục quản lý thực phẩm và dược phẩm Hoa Kỳ (FDA) phê chuẩn đầy đủ. Tại Việt Nam có 8 loại vắc xin đã được Bộ Y tế cấp phép sử dụng khẩn cấp bao gồm: Vắc xin COVID-19 Astrazeneca, Vắc xin Gam-COVID-Vac (tên khác là SPUTNIK V), Vắc xin Vero Cell của Sinopharm, Vắc xin Comirnaty của Pfizer/BioNTech, Vắc xin Spikevax (tên khác là: COVID-19 Vắc xin Moderna), COVID-19 Vắc xin Janssen, vắc xin Hayat-Vax và vắc xin Abdala của Cuba.
2.1. Nhóm vắc xin được sản xuất theo công nghệ véc tơ vi rút
Trong các loại vắc xin COVID-19 hiện đang được WHO cấp phép sử dụng khẩn cấp có vắc xin COVID-19 Astrazeneca và Janssen được sản xuất theo công nghệ véc tơ vi rút. Adenovirus (vi rút gây cúm ở tinh tinh) đã được làm mất khả năng sao chép được sử dụng để mang kháng nguyên là protein gai bề mặt của vi rút COVID-19 xâm nhập vào cơ thể con người. Cơ thể sẽ nhận ra protein của COVID-19 là kháng nguyên và sinh kháng thể chống lại, sau đó sẽ tạo ra trí nhớ miễn dịch để bảo vệ cơ thể cho những lần tiếp xúc tác nhân gây bệnh sau đó.
2.1.1. Vắc xin COVID-19 Astrazeneca
Vắc xin COVID-19 Astrazeneca của hãng Astrazeneca được nghiên cứu và phát triển bởi đại học Oxford và được WHO thông qua chấp thuận sử dụng vắc xin trong trường hợp khẩn cấp vào ngày 15/2/2021. Tại Việt Nam vắc xin này cũng được phê duyệt sử dụng khẩn cấp vào ngày 01/02/2021.
- Tên vắc xin: COVID-19 Vắc xin Astrazeneca (ChAdOx1-S)
- Hãng sản xuất: Oxford-Astrazeneca
- Thành phần hoạt chất, nồng độ/hàm lượng: Mỗi liều (0,5 ml) chứa: vắc xin COVID-19 (ChAdOx1-S tái tổ hợp) 5 x 1010 hạt vi rút (vp).
- Liều lượng: 0,5 ml, tiêm 2 liều cách nhau từ 4 đến 12 tuần, tốt nhất nên là 8 đến 12 tuần.
- Quy cách đóng gói: Mỗi lọ chứa 8-10 liều tùy thuộc vào nước sản xuất (ví dụ của Anh sản xuất là 8 liều, còn lại đa số các nước là 10 liều một lọ), mỗi liều 0,5
- Dạng bào chế: dung dịch tiêm.
- Đường tiêm: tiêm vào bắp phần trên cánh
- Đối tượng: từ 18 tuổi trở lên.
Tính an toàn của vắc xin
Các phản ứng thông thường: đau tại chỗ tiêm, đau cơ, sốt, đau đầu…..phổ biến ở người dưới 56 tuổi hơn.
- Các phản ứng tại chỗ sau tiêm hai liều ở độ tuổi từ 18-55 là 88%, nhóm tuổi 56-69 là 65%, và 65% ở nhóm trên 70 tuổi.
- Các phản ứng bất lợi nghiêm trọng là rất hiếm gặp.
- Cơ quan Quản lý Dược phẩm châu Âu (EMA) đã đánh giá kỹ các dữ liệu về chất lượng, tính an toàn và hiệu quả của vắc xin, và đã khuyến cáo cấp phép lưu hành thị trường tạm thời cho những người từ 18 tuổi trở lên.
Tính hiệu quả của vắc xin
- Đối với biến chủng Delta, hai mũi vắc xin Astrazeneca có hiệu quả 67% trong ngăn ngừa lây nhiễm có triệu chứng, 92% trong ngăn ngừa bệnh nặng cần nhập viện và 91% trong ngăn ngừa tử
- Nghiên cứu cho thấy kéo dài khoảng cách giữa hai mũi vắc xin Astra- zeneca từ 8 đến 12 tuần có hiệu quả miễn dịch cao hơn và lâu dài hơn so với tiêm hai mũi vắc xin gần hơn.
2.1.2. Vắc xin COVID-19 Janssen của Johnson & Johnson
- Tên vắc xin: COVID-19 Janssen (Ad26.COV2.S).
- Hãng sản xuất: Johnson & Johnson.
- Liều lượng: 0,5 ml, tiêm một liều duy nhất.
- Dạng bào chế: hỗn dịch tiêm.
- Quy cách đóng gói: hộp chứa 10 lọ, mỗi lọ đa liều 2,5 ml chứa 5 liều.
- Đường tiêm: tiêm bắp phần trên cánh
- Đối tượng: từ 18 tuổi trở lên.
Tính an toàn của vắc xin
- Trong các thử nghiệm lâm sàng, các tác dụng không mong muốn thường xuất hiện trong 7 ngày sau khi tiêm chủng nhưng hầu hết là ở mức nhẹ, phổ biến ở người 18 đến 59 tuổi hơn so với những người từ 60 tuổi trở lên.
- Huyết khối và giảm tiểu cầu là phản ứng không mong muốn rất hiếm, gặp khoảng 7 trên 1 triệu phụ nữ từ 18 49 tuổi.
Tính hiệu quả của vắc xin
- Vắc xin ngừa COVID-19 của J&J/Janssen đạt hiệu quả 66,3% trong các thử nghiệm lâm sàng (tính hiệu lực) phòng ngừa bệnh COVID-19 ở người chưa mắc COVID-19 trước đó. Kháng thể đạt nồng độ cao nhất sau 2 tuần tiêm chủng.
- Vắc xin có hiệu quả cao trong việc giảm tỷ lệ nhập viện và tử vong ở bệnh nhân mắc COVID-19. Không ghi nhận trường hợp mắc COVID-19 nào phải nhập viện sau khi tiêm vắc xin ít nhất 4 tuần.
2.2. Nhóm vắc xin được sản xuất theo công nghệ mRNA
Một thử thách trong việc phát triển vắc xin chống lại vi rút như SARS-CoV-2 là việc các vi rút này không ngừng biến chủng và do vậy các vắc xin truyền thống có thể không đạt được hiệu quả như mong muốn. Trong bối cảnh đó, công nghệ mRNA được áp dụng vào sản xuất vắc xin thế hệ mới. Một vắc xin mRNA được tạo ra sao cho không có đủ thông tin mã hóa để sản xuất protein gây bệnh nhưng lại có đủ thông tin để “lừa gạt” hệ thống miễn dịch của con người nhận ra đó là một vi rút thật, và kích hoạt việc sản xuất ra kháng thể chống lại vi rút.
2.2.1. Vắc xin COVID-19 Pfizer-Biontech
Vắc xin Comirnaty của Pfizer-BioNTech được Tổ chức Y tế thế giới thông qua chấp thuận sử dụng vắc xin trong trường hợp khẩn cấp vào ngày 31/12/2020. Vắc xin này đã được nhiều quốc gia trên thế giới cấp phép lưu hành và sử dụng. Tại Việt Nam vắc xin này được cấp phép sử dụng khẩn cấp vào ngày 12/06/2021.
- Tên vắc xin: Vắc xin COVID-19 Comirnaty (BNT162b2).
- Hãng sản xuất: Pfizer –
- Liều lượng: 0,3 ml tiêm 2 mũi, cách nhau 21 ngày.
- Tiêm vào bắp phần trên cánh
- Đối tượng: Vắc xin Pfizer đã được phê duyệt sử dụng cho người lớn, và trẻ em từ 5 tuổi trở lên.
- Vắc xin được đóng 195 lọ (1.170 liều) trong 1 Mỗi khay có thể tích: 23 cm x 23 cm x 4 cm, mỗi lọ chứa 0,45 ml vắc xin dạng hỗn dịch đậm đặc pha tiêm, tương đương 6 liều vắc xin sau pha loãng với nước muối sinh lý 0,9 %.
Tính an toàn của vắc xin
- Các tác dụng phụ được báo cáo phổ biến nhất là đau, đỏ và sưng tại chỗ tiêm, mệt mỏi, nhức đầu, đau cơ hoặc khớp, ớn lạnh và sốt.
- Ngoài ra, tác dụng phụ nguy hiểm hiếm gặp của vắc xin này liên quan đến viêm cơ tim và viêm màng ngoài tim (myocarditis and pericarditis) chủ yếu trong vòng 7 ngày sau khi tiêm liều thứ Nguy cơ này cao hơn ở nam giới dưới 40 tuổi và cao nhất ở nam giới từ 12 đến 17 tuổi. Tất cả các trường hợp này đều đã hồi phục và thông tin này được ghi rõ trong phần cảnh báo nguy cơ của vắc xin.
Tính hiệu quả của vắc xin
- Trong thử nghiệm lâm sàng giai đoạn 3, vắc xin Comirnaty của Pfizer – BioNTech có hiệu lực bảo vệ trước tác nhân gây bệnh COVID-19 từ 95% đến 100% sau khi tiêm liều thứ 2 khoảng 7 ngày ở nhiều độ tuổi, chủng tộc, giới tính và hiệu quả ở cả những người có bệnh nền.
- Đối với biến chủng Delta, hai mũi vắc xin Pfizer có hiệu quả 88% trong ngăn ngừa lây nhiễm có triệu chứng, 96% trong ngăn ngừa bệnh nặng cần nhập viện và 90% trong ngăn ngừa tử vong.
2.2.2. Vắc xin Moderna
- Tên vắc xin: Moderna COVID-19 Vắc xin; Moderna mRNA-1273 Vắc xin; COVID-19 mRNA Vắc xin (nucleoside modified); Vắc xin SPIKEVAX.
- Hãng sản xuất: Moderna TX-Mỹ; Catalent Indiana, LLC-Mỹ; Lonza Bio- logics, Inc-Mỹ; Baxter-Mỹ; Rovi Pharma Industrial Services, SA-Tây Ban Nha; Moderna Biotech-Tây Ban Nha; Racipharm Monts-Pháp.
- Liều lượng: 0,5 ml.
- Số mũi tiêm: 2 mũi, cách nhau 28 ngày (4 tuần).
- Quy cách đóng gói: 1 lọ 14 liều, mỗi liều 0,5 ml.
- Vị trí tiêm: Tiêm vào bắp phần trên cánh tay.
- Đối tượng: người từ 18 tuổi trở lên.
Tính an toàn của vắc xin
- Phần lớn các phản ứng thông thường là nhẹ đến trung bình và hết sau 7 ngày sau tiêm.
- Phản ứng toàn thân phổ biến hơn sau khi tiêm liều thứ hai.
Tính hiệu quả của vắc xin
- Vắc xin đã được chứng minh là có hiệu quả tới 94,1% (dao động từ 89,3% đến 96,8% với độ tin cậy 95%). Hiệu quả được duy trì trên tất cả các nhóm tuổi (trên 18 tuổi) và không bị ảnh hưởng bởi giới tính hoặc dân tộc.
- Với biến chủng Delta, nghiên cứu thực tế cho thấy một mũi vắc xin có hiệu quả 84,8% trong ngăn ngừa lây nhiễm nói chung, 72% trong ngăn ngừa nhiễm có triệu chứng và 95% trong ngăn ngừa bệnh nặng cần nhập viện.
- Theo một số nghiên cứu về vắc xin phòng COVID-19 Moderna, hiệu quả sau liều đầu tiên đạt 91,9% bắt đầu từ 14 ngày sau tiêm với thời gian theo dõi trung bình là 28 ngày và thông tin về việc kháng thể tồn tại đến 6 tháng sau liều thứ hai đã được ghi nhận.
2.3. Nhóm vắc xin được sản xuất theo công nghệ bất hoạt
Vi rút đã được bất hoạt được tiêm vào cơ thể để kích thích sản xuất các kháng thể và làm cho cơ thể sẵn sàng để ứng phó với tình trạng nhiễm vi rút SARS-CoV-2. Thành phần của vắc xin này được bổ sung hydroxit nhôm để tăng cường phản ứng của hệ thống miễn dịch.
2.3.1. Vắc xin COVID-19 (Vero Cell) bất hoạt của Sinopharm
- Tên vắc xin: Vắc xin COVID-19 (Vero Cell) bất hoạt.
- Hãng sản xuất: Beijing Institute of Biological Products Co., Ltd., China National Biotec Group (CNBG)/ Sinopharm-Trung Quốc.
- Thành phần hoạt chất, nồng độ/hàm lượng: Mỗi liều (0,5 ml) chứa 6,5 U kháng nguyên.
- Dạng bào chế: dung dịch tiêm.
- Quy cách đóng gói: hộp 1 lọ hoặc 3 lọ, mỗi lọ chứa 1 liều 0,5 ml.
- Vắc xin COVID-19 (Vero Cell) bất hoạt của Sinopharm được chỉ định tiêm phòng cho người từ 18 tuổi trở lên với 2 mũi cách nhau từ 3-4 tuần.
- Liều lượng, đường tiêm: 0,5ml, tiêm bắp. Lắc lọ vắc xin trước khi sử dụng.
Tính an toàn: Cho đến nay dữ liệu về tính an toàn của vắc xin còn hạn chế. Các phản ứng sau tiêm thường ở mức độ nhẹ đến trung bình, phổ biến nhất là đau tại chỗ tiêm, mệt mỏi và đau đầu.
Tính hiệu quả: Dữ liệu về tính hiệu quả trong việc ngăn ngừa lây nhiễm COVID-19 của vắc xin là 78,1%, và hiệu quả trong việc giảm tỷ lệ nhập viện là 78,7% đối với biến chủng Alpha. Hiện tại chưa có đủ nghiên cứu trên thực tế về hiệu của của vắc xin này đối với biến chủng Delta..
2.3.2. Vắc xin COVID-19 Sinovac
- Tên vắc xin: Vắc xin COVID-19 Sinovac (CoronaVac).
- Hãng sản xuất: Công ty Sinovac Biotech-Trung Quốc.
- Liều lượng: 0,5 ml, tiêm 2 mũi cách nhau 2 đến 4 tuần.
- Thành phần: vi rút SARS-CoV-2 bất hoạt (chủng CZ02), nhôm hydroxit, dinatri hydro photphat dodecahydrat, natri dihydro photphat monohydrat và natri clorua.
- Tiêm vào bắp phần trên cánh tay.
- Đối tượng: trên 18 tuổi.
Tính an toàn
- Theo số liệu từ WHO, nghiên cứu được tiến hành tại Trung Quốc ghi nhận 49 ca trong 35,8 triệu liều có phản ứng phụ nghiêm trọng bao gồm: sốc phản vệ, xuất huyết não, viêm mạch máu, sưng cổ họng. Tại Brazil và Indonesia có 162 ca/17 triệu liều có phản ứng phụ nghiêm trọng bao gồm: sốt, đau đầu, khó thở, tử Tại Chile có 90/3,7 triệu liều có phản ứng phụ nghiêm trọng.
- Tuy nhiên dữ liệu về an toàn ở đối tượng trên 60 tuổi còn chưa rõ do số lượng đối tượng ít và các dữ liệu được công bố trên WHO mà không tìm thấy được dữ liệu gốc.
Tính hiệu quả:
Kết quả nghiên cứu quan sát tại Chile cho thấy, hiệu quả của vắc xin là 65,9% ngăn ngừa COVID-19, 87,5% trong giảm tỷ lệ nhập viện và 86,3% trong việc giảm tỷ lệ tử vong do COVID-19 đối với biến chủng Alpha. Dữ liệu về hiệu quả của vắc xin ở đối tượng trên 60 tuổi chưa rõ do số lượng ít. Hiện tại chưa có đủ nghiên cứu trên thực tế đối với biến chủng Delta.
2.4. Phản ứng sau tiêm của các vắc xin COVID-19
Mặc dù được phát triển trong thời gian ngắn, các vắc xin COVID-19 đều đã được kiểm duyệt bởi các tổ chức y tế uy tín như WHO, FDA, EMA về tính an toàn và hiệu quả. Tuy nhiên, bất kì một loại thuốc hay vắc xin nào thì đều có thể xảy ra một tỷ lệ các phản ứng không mong muốn. Các phản ứng này có thể do phản ứng với vắc xin hoặc thành phần có trong vắc xin, do các sự cố không mong muốn do không thực hiện đúng quy trình bảo quản hay tiêm chủng; ngoài ra, một số phản ứng sau tiêm cũng không thể xác định được nguyên nhân. Đáp ứng miễn dịch của mỗi cơ thể với các tác nhân lạ là khác nhau mà có thể xảy ra các phản ứng từ nhẹ cho đến các triệu chứng của phản vệ và sốc phản vệ. Tuy nhiên những lợi ích từ việc tiêm vắc xin vượt trội so với những rủi ro, nên việc bao phủ vắc xin vẫn là ưu tiên trong cuộc chiến với COVID-19.
2.4.1. Các phản ứng thông thường
- Sốt, mệt mỏi, đau đầu, ớn lạnh, đau cơ, đau khớp, tăng cảm giác đau, ngứa, sưng, đỏ, đau tại chỗ tiêm, bồn chồn là những phản ứng phổ biến sau khi tiêm vắc xin COVID-19, tuy nhiên đây là những phản ứng thông thường và sẽ tự hết sau 1 đến 2 ngày.
- Dấu hiệu thông thường diễn biến nặng lên: sốt cao ≥ 39ºC, sưng/đỏ lan rộng tại chỗ tiêm, đau cơ dữ dội, tăng huyết áp hoặc tụt huyết áp.
- Dấu hiệu nghiêm trọng: rất hiếm nhưng có thể xảy ra; nếu có, thường xuất hiện trong vòng vài giờ hoặc ngày đầu sau khi tiêm vắc xin phòng COVID-19.
- Ở miệng: tê quanh môi và/hoặc lưỡi…
- Ở da: phát ban, môi mẩn đỏ, tím tái hoặc đỏ da…
- Ở họng: ngứa, căng cứng, tắc nghẽn, khản đặc…
- Đường tiêu hóa: nôn, tiêu chảy, đau quặn bụng…
- Đường hô hấp: thở dốc, thở khò khè, thở rít, khó thở, cảm giác nghẹt thở, ho…
- Toàn thân: mạch yếu, chóng mặt, choáng/xây xẩm, cảm giác muốn ngã, chân tay co quắp…
Bảng 22.2. Tỷ lệ (%) phản ứng không mong muốn của một số vắc xin COVID-19
| Phản ứng phụ | Pfizer | Moderna | Astrazeneca |
| Sưng/đau tại vị trí tiêm | 78 | 90 | 67 |
| Sốt | 16 | 17 | 18 |
| Mệt | 59 | 68 | 70 |
| Đau đầu | 52 | 63 | 68 |
| Gai lạnh | 35 | 48 | 51 |
| Đau nhức cơ bắp | 37 | 6 | 60 |
| Đau khớp | 22 | 45 | 31 |
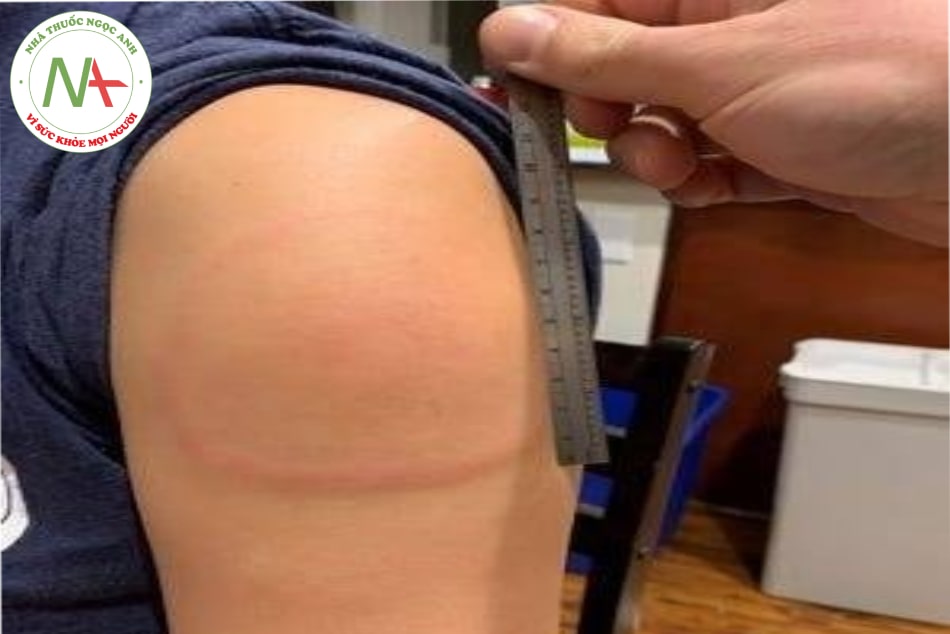
Hiện tượng cánh tay COVID-19: Đây là phản ứng quá mẫn muộn, tuy nhiên không nguy hiểm đến tính mạng và sẽ biến mất trong một vài ngày, hiện tượng đã được báo cáo khi tiêm vắc xin Moderna.
- Ngứa, có thể ngứa dữ dội.
- Phát ban đỏ/hoặc đổi màu vùng da quanh chỗ tiêm với các kích thước khác nhau. Trong một số trường hợp, phát ban có thể lan tới bàn tay hoặc ngón tay.
- Sưng tấy.
- Đau.
- Da vùng tiêm cảm thấy nóng ấm khi chạm vào.
- Xuất hiện các cục u cứng dưới da tại vị trí tiêm
2.4.2. Một số phản ứng đặc biệt
- Hội chứng Guillain-Barré (GBS) đã được báo cáo ở một số người sau khi tiêm vắc xin COVID-19. GBS là hội chứng rối loạn hiếm gặp, trong đó hệ miễn dịch của cơ thể gây tổn thương các tế bào thần kinh, gây yếu cơ và đôi khi là gây liệt. Hầu hết mọi người đều hồi phục sau khi bị GBS, chỉ có một vài trường hợp có để lại tổn thương thần kinh lâu dài. Sau khi tiêm hơn 14 triệu liều vắc-xin COVID-19 của J&J/Janssen đã có khoảng 167 báo cáo sơ bộ về hội chứng GBS. Phần lớn các ca này được báo cáo sau khoảng 2 tuần kể từ khi tiêm chủng và hầu hết xảy ra ở nam giới, trong đó có nhiều người từ 50 tuổi trở lên. Điều trị hội chứng GBS sau tiêm vắc xin không khác so với điều trị GBS thông thường.
- Viêm cơ tim và viêm màng ngoài tim: Các báo cáo cho thấy nguy cơ viêm cơ tim và viêm màng ngoài tim tăng lên, đặc biệt là sau khi sử dụng vắc xin phòng COVID-19 liều thứ Thông thường, các triệu chứng khởi phát trong vòng vài ngày sau tiêm chủng. Một nghiên cứu trên hơn 2 triệu đối tượng đã cho kết quả 0,02% người bị viêm cơ tim, 0,037% người bị viêm màng ngoài tim. Những triệu chứng này xuất hiện trung bình trong 3,5 ngày sau tiêm vắc xin COVID-19. Cần thận trọng khi chỉ định tiêm chủng vắc xin phòng COVID-19 cho các đối tượng có tiền sử viêm cơ tim hoặc viêm màng ngoài tim. Với những đối tượng có tiền sử này cần phải khám sàng lọc kĩ và theo dõi sau tiêm cẩn thận.
- Bell’s palsy (liệt mặt ngoại biên cấp tính): được báo cáo như là một biến chứng hiếm gặp sau khi tiêm vắc xin COVID-19. Một nghiên cứu bệnh chứng đã được tiến hành tại Hồng Kông đã ghi nhận 0,006% và 0,003% trường hợp xuất hiện tình trạng liệt dây thần kinh mặt ngoại biên cấp tính sau khi tiêm vắc xin CoronaVac và Pfizer.
- Hội chứng thuyên tắc huyết khối kèm giảm tiểu cầu: là biến chứng hiếm gặp và nguy hiểm sau khi tiêm vắc xin COVID-19. Trên những đối tượng có tiền sử rối loạn đông cầm máu/giảm tiểu cầu cần tư vấn kỹ về các dấu hiệu như đau đầu, đau bụng dữ dội, mờ mắt, khó thở, đau tức ngực và sưng đau phù nề cẳng chân sau khi tiêm vắc xin để đến cơ sở y tế gần nhất kịp thời. Đây là hội chứng có tỷ lệ tử vong cao và thường xảy ra ở những phụ nữ dưới 55 tuổi sau khi tiêm vắc xin COVID-19 trong vòng 2 tuần. Sau khi xuất hiện 6 trường hợp xuất hiện rối loạn đông cầm máu sau khi tiêm vắc xin COVID-19 Janssen, Mỹ đã yêu cầu ngừng sử dụng vắc xin này để kiểm tra, tổng hợp các dữ liệu và đánh giá các phản ứng không mong muốn vào ngày 13 tháng 4 năm 2021. Tuy nhiên đến ngày 23 tháng 4 năm 2021, Trung tâm kiểm soát bệnh tật (CDC) và cục quản lý thực phẩm và dược phẩm Hoa Kỳ (FDA) đã khuyến cáo tiếp tục sử dụng vắc xin COVID-19 Janssen sau khi cân nhắc giữa lợi ích và nguy cơ. Riêng những phụ nữ trên 50 tuổi cần lưu ý rủi ro xảy ra hiện tượng huyết khối và giảm tiểu cầu sau khi tiêm vắc xin và có thể lựa chọn vắc xin khác để thay thế.
- Huyết khối (ví dụ: huyết khối tĩnh mạch não): Một số nước lo ngại về tính an toàn của vắc xin COVID-19 Astrazeneca sau khi xuất hiện những ca tử vong do đông máu. Ở Anh, tính đến cuối tháng 3/2021, có 79 bệnh nhân báo cáo chứng đông máu sau 20 triệu liều vắc xin Astrazeneca và 19 người đã tử Xác suất biến chứng đông máu sau khi tiêm vắc xin Astrazeneca là 1 trên 250000 người (Anh), 169/34 triệu liều (châu Âu lục địa), 1 trên 100000 người (Mỹ – EMA). EMA cũng cho rằng có thể vắc xin là nguyên nhân của biến chứng đông máu. Tuy nhiên, chúng ta cần phải so sánh với xác suất đông máu trong cộng đồng. Một nghiên cứu tiến hành phân tích tỷ lệ đông máu trên quần thể dân số chung cho thấy có 50 trên 100000 dân có phát sinh chứng đông máu. Ngoài ra, biến chứng đông máu trên bệnh nhân nhiễm COVID-19 là rất cao, dao động từ 5 đến 41,7%. Vì vậy có thể thấy rằng phản ứng đông máu sau tiêm của vắc xin COVID-19 là rất thấp, do vậy vắc xin vẫn an toàn.
3. ĐỐI TƯỢNG CẦN THẬN TRỌNG VÀ ƯU TIÊN TIÊM VẮC XIN COVID-19
Nhìn chung, luôn luôn cần phải cân nhắc giữa nguy cơ bệnh nặng do COVID-19 và nguy cơ từ các tác dụng phụ hoặc biến chứng sau tiêm vắc xin.
Các đối tượng cần được ưu tiên tiêm vắc xin COVID-19 có thể thay đổi trong từng giai đoạn, nhưng nhìn chung bao gồm các đối tượng nguy cơ nhiễm bệnh cao (nhân viên y tế, nhân viên tham gia chống dịch), nguy cơ bệnh nặng (người trên 65 tuổi, có bệnh nền mạn tính), những nhóm có vai trò thiết yếu trong xã hội (lực lượng quân đội, công an, nhóm cung cấp dịch vụ thiết yếu).
Các đối tượng cần thận trọng tiêm chủng và phải được khám sàng lọc kỹ lưỡng và thận trọng:
- Người có tiền sử dị ứng với các dị nguyên khác.
- Người có bệnh nền, bệnh mạn tính.
- Người mất tri giác, mất năng lực hành vi.
- Người có tiền sử giảm tiểu cầu và/hoặc rối loạn đông máu.
- Phụ nữ mang thai ≥ 13 tuần
- Phụ nữ mang thai cần được giải thích nguy cơ/lợi ích, cần cân nhắc tiêm vắc xin phòng COVID-19 cho phụ nữ mang thai ≥13 tuần khi lợi ích tiềm năng lớn hơn nguy cơ tiềm tàng đối với mẹ và thai nhi. Phụ nữ mang thai trên 13 tuần và cho con bú vẫn được tiêm vắc xin, tuy nhiên không dùng vắc xin Sputnik V.
- Người phát hiện thấy bất thường dấu hiệu sống:
- Nhiệt độ < 35,5°C và > 37,5 °C.
- Mạch: < 60 lần/phút hoặc > 100 lần/phút.
- Huyết áp tối thiểu < 60 mmHg hoặc > 90 mmHg và/hoặc huyết áp tối đa < 90 mmHg hoặc > 140 mmHg hoặc cao hơn 30 mmHg so với huyết áp hàng ngày (ở người có tăng huyết áp đang điều trị và có hồ sơ y tế)
- Nhịp thở > 25 lần/phút.
4. KHÁM SÀNG LỌC VÀ CHỈ ĐỊNH
Đảm bảo tiêm chủng an toàn ngay từ những giai đoạn đầu triển khai tiêm vắc xin sẽ tạo niềm tin ở người dân từ đó đặt nền tảng vững chắc cho việc phủ vắc xin và hình thành miễn dịch cộng đồng. Tính đến ngày 10 tháng 8 năm 2021 đã có nhiều quyết định thay thế nhau về hướng dẫn khám sàng lọc trước tiêm chủng vắc xin phòng COVID-19 theo hướng từ thận trọng để đánh giá phản ứng sau tiêm đến mở rộng dần đối tượng tùy thuộc vào nguồn vắc xin và tình hình dịch bệnh. Hiện nay tất cả các loại vắc xin COVID-19 đang được cấp phép sử dụng tại Việt Nam đều thực hiện khám sàng lọc theo quyết định 4355/QĐ-BYT ngày 10 tháng 9 năm 2021. Tuy nhiên do vắc xin COVID-19 là các vắc xin mới nên hướng dẫn khám sàng lọc của Bộ Y tế có thể sẽ được điều chỉnh và vì vậy các cán bộ Y tế cần cập nhật thường xuyên hướng dẫn của Bộ Y tế.
Các đối tượng đủ điều kiện tiêm chủng
- Người trong độ tuổi tiêm chủng theo khuyến cáo trong hướng dẫn sử dụng của nhà sản xuất và không quá mẫn với hoạt chất hoặc với bất kỳ tá dược nào trong thành phần của vắc
Các đối tượng trì hoãn tiêm chủng
- Có tiền sử rõ ràng đã mắc COVID-19 trong vòng 6 tháng.
- Đang mắc bệnh cấp tính.
- Phụ nữ mang thai dưới 13 tuần.
Chống chỉ định
- Tiền sử rõ ràng phản vệ với vắc xin phòng COVID-19 cùng loại (lần trước).
- Có bất cứ chống chỉ định nào theo công bố của nhà sản xuất.
4.1. Khám sàng lọc trước tiêm chủng
- Hỏi tiền sử bệnh: Tình trạng sức khỏe hiện tại.
- Khám sức khỏe hiện tại xem có sốt, hay đang mắc các bệnh cấp tính, bệnh mạn tính đang tiến triển, đặc biệt là tình trạng bệnh gợi ý COVID-19 không?
- Tiền sử tiêm vắc xin phòng COVID-19: Cần khai thác chính xác loại vắc xin COVID-19 đã tiêm và thời gian đã tiêm vắc xin.
- Tiền sử dị ứng: Đã từng có tiền sử dị ứng với bất kỳ dị nguyên nào, tiền sử dị ứng nặng, bao gồm cả phản vệ, tiền sử dị ứng với vắc xin và bất kỳ thành phần nào của vắc
- Tiền sử mắc COVID-19 trong vòng 6 tháng.
- Tiền sử suy giảm miễn dịch nặng, ung thư giai đoạn cuối, đang điều trị hóa trị, xạ trị.
- Tiền sử rối loạn đông máu/cầm máu hoặc đang dùng thuốc chống đông.
- Phụ nữ mang thai (nếu có) hoặc đang cho con bú:
- Phụ nữ mang thai: Hỏi tuổi thai, giải thích nguy cơ/lợi ích, chỉ nên cân nhắc tiêm vắc xin phòng COVID-19 cho phụ nữ mang thai ≥ 13 tuần khi lợi ích tiềm năng lớn hơn bất kỳ nguy cơ tiềm tàng nào đối với mẹ và thai nhi.
- Phụ nữ mang thai và đang cho con bú: chống chỉ định với vắc xin Sputnik V.
Đánh giá lâm sàng
- Phát hiện các bất thường về dấu hiệu sống:
- Đo thân nhiệt tất cả những người đến tiêm.
- Đo huyết áp đối với người có tiền sử tăng huyết áp/huyết áp thấp, người có bệnh nền liên quan đến bệnh lý tim mạch, người trên 65 tuổi.
- Đo mạch, đếm nhịp thở ở người có tiền sử suy tim hoặc phát hiện bất thường như đau ngực, khó thở….
Quan sát toàn trạng
- Đánh giá mức độ tri giác bằng cách hỏi những câu hỏi về bản thân người đến tiêm. Lưu ý những người có bệnh nền nặng nằm liệt giường, mất tri giác, mất năng lực hành vi.
- Ghi nhận bất kỳ biểu hiện bất thường nào quan sát thấy ở người đến tiêm để hỏi lại về tiền sử sức khỏe.
4.2. Lưu ý khám sàng lọc cho những người có bệnh nền
Để có thể bảo vệ cho những đối tượng có nguy cơ cao mắc COVID-19 như những người có bệnh nền mà vẫn đảm bảo được an toàn trong buổi tiêm chủng, bác sĩ khám sàng lọc cần quan sát tổng thể và khai thác kỹ lưỡng các nguy cơ của đối tượng đến tiêm chủng vắc xin COVID-19.
- Những đối tượng có bệnh lý tim mạch cần phải đếm mạch và đo huyết áp kết hợp với việc khai thác các chỉ số này hàng ngày, tình trạng sử dụng thuốc, kết quả khám định kỳ gần nhất… Khi phát hiện những bất thường như: huyết áp, mạch tăng quá cao, có cơn đau thắt ngực trong 2 tuần gần đây, khó thở… cần gửi đi khám chuyên khoa tim mạch và xin ý kiến của bác sĩ tim mạch về việc tiêm vắc xin COVID-19.
- Những đối tượng có bệnh lý hô hấp: bệnh phổi tắc nghẽn mạn tính, bệnh hen phế quản… bác sĩ khám sàng lọc cần nghe tim phổi để đánh giá tình trang hiện tại, khai thác kỹ tình trạng khó thở trong một tuần gần đây, tình trạng sử dụng thuốc theo bệnh… Nếu thấy bất thường cần gửi đi khám chuyên khoa hô hấp và xin ý kiến bác sĩ chuyên khoa về việc tiêm vắc xin COVID-19.
- Những đối tượng có các bệnh lý chuyển hóa: goute, đái tháo đường, rối loạn chuyển hóa lipid… cần khai thác kỹ đợt cấp của bệnh, nếu có thể yêu cầu đối tượng cho xem kết quả khám gần nhất để đánh giá tình trạng bệnh. Nếu phát hiện bất thường cần gửi đi khám chuyên khoa và xin ý kiến về việc tiêm vắc xin COVID-19.
- Những đối tượng đang mắc ung thư: cần quan sát toàn trạng của đối tượng, khai thác kỹ giai đoạn bệnh các biện pháp đang điều trị. Trong trường hợp đối tượng hóa trị và xạ trị nên cách ít nhất 14 ngày thì chỉ định tiêm vắc xin COVID-19.
- Các đối tượng mắc bệnh mạn tính đang trong tiến trình điều trị bệnh, bác sĩ khám sàng lọc cần có những hướng dẫn về việc có tiếp tục dừng thuốc hay không phụ thuộc vào mặt bệnh và cân nhắc giữa lợi ích và nguy cơ của việc tiêm vắc xin COVID-19. Hầu hết các bệnh mạn tính hiện nay như tăng huyết áp, đái tháo đường, viêm gan B… việc duy trì thuốc điều trị bệnh nền không làm giảm đáp ứng miễn dịch cũng như tăng các phản ứng sau tiêm chủng vắc xin COVID-19.
4.3. Kết luận sau khám sàng lọc
- Chỉ định tiêm chủng ngay cho những trường hợp đủ điều kiện tiêm chủng.
- Trì hoãn tiêm chủng cho những trường hợp có ít nhất một yếu tố phải trì hoãn tiêm chủng.
- Chuyển đến tiêm ở cơ sở y tế có đủ khả năng cấp cứu phản vệ cho những trường hợp có tiền sử phản vệ độ 3 với bất kỳ dị nguyên nào.
- Phụ nữ mang thai ≥ 13 tuần sau khi được giải thích nguy cơ/lợi ích nếu đồng ý tiêm chủng cần chuyển đến tiêm và theo dõi tại cơ sở y tế có khả năng cấp cứu sản khoa.
- Không chỉ định tiêm cho những người có chống chỉ định tiêm chủng.
5. CÁC TRƯỜNG HỢP ĐẶC BIỆT
5.1. Phụ nữ có thai
Các dữ liệu khoa học được thu thập cho đến hiện nay cho thấy rằng những người mang thai nếu mắc COVID-19 có nhiều khả năng phải nhập viện hơn những người cùng tuổi không mang thai. Trong các nghiên cứu về phụ nữ mang thai nhập viện khi mắc COVID-19, nguy cơ sinh non dao động từ 10% đến 25%, với tỷ lệ cao nhất là 60% khi bệnh trở nặng. Do vậy, nhiễm COVID-19 là yếu tố nguy cơ cho phụ nữ có thai và đặc biệt khi bệnh trở nặng sẽ ảnh hưởng xấu cho cả mẹ và thai nhi.
Một nghiên cứu tiến hành trên 7530 phụ nữ mang thai được tiêm vắc xin Pfizer và 7530 phụ nữ có thai không được tiêm vắc xin cho thấy vắc xin giảm nguy cơ lây nhiễm 42%. Một nghiên cứu khác trên 3958 người trong chương trình an toàn vắc xin (v-safe) cho thấy những phụ nữ mang thai được tiêm vắc xin Pfizer rất an toàn, tỷ lệ sảy thai, sinh non, thiếu cân…. tương đương với những người không tiêm vắc xin. Từ những bằng chứng khoa học có thể thấy phụ nữ có thai nên được ưu tiên tiêm vắc xin, vắc xin Pfizer được cho là an toàn và tiêm chủng vắc xin COVID-19 có thể tạo miễn dịch một cách gián tiếp cho trẻ qua chuyển kháng thể đến bào thai.
5.2. Phụ nữ cho con bú
Các vaccine COVID-19 đang được sử dụng hiện nay cho thấy khá an toàn với bà mẹ cho con bú. Đặc biệt là một số vắc xin sử dụng công nghệ sản xuất mRNA như của Pfizer/BioNTech hoặc Moderna cho thấy rất an toàn vì mRNA là phân tử không bền, rất dễ bị phân hủy sau khi đưa vào cơ thể và đã hoàn thành nhiệm vụ trình diện kháng nguyên S cho tế bào miễn dịch. Nghiên cứu sắp được công bố của nhóm nghiên cứu của Golan ở đại học California ở San Francisco sử dụng kỹ thuật RT-PCR để kiểm tra lượng mRNA có trong sữa từ người mẹ được tiêm vắc xin của Moderna hoặc Pfizer (sau khoảng 4-48 giờ) và cho thấy không đo được bất cứ lượng mRNA nào từ vắc xin; họ đưa ra kết luận rằng vắc xin không đi vào sữa mẹ và vì vậy việc cho con bú sau khi tiêm vắc xin COVID-19 là an toàn. Những loại vắc xin dùng vector Adenovirus như Astrazeneca hoặc Janssen (Johnson & Johnson) cho đến hiện nay cũng cho thấy khá an toàn và cũng chưa có bằng chứng nào cho thấy vắc xin có thể truyền qua sữa mẹ.
Trong khi đó, việc cho con bú sữa mẹ còn cung cấp kháng thể thụ động cho trẻ. Một nghiên cứu đã tìm thấy kháng thể trong sữa mẹ sau khi tiêm đủ 2 mũi vắc xin COVID-19 Moderna. Các dữ liệu đều cho thấy rằng trẻ em khi mắc COVID-19 sẽ có ít triệu chứng và biến chứng hơn, tuy nhiên những trẻ dưới 2 tuổi lại có tỷ lệ nhập viện cao hơn, có thể do hệ miễn dịch chưa đầy đủ. Trong khi vắc xin cho trẻ sơ sinh vẫn chưa có, việc truyền kháng thể từ mẹ đã được tiêm vắc xin cho con có thể sẽ giúp giảm tỷ lệ bệnh nặng và tử vong ở trẻ nhỏ. Từ những lợi ích mà vắc xin mang lại, WHO khuyến khích bà mẹ cho con bú đi tiêm vắc xin COVID-19 nếu đến lượt mình và không cần phải dừng cho con bú sau khi tiêm.
5.3. Trẻ em
- Nhìn chung tỷ lệ mắc COVID-19 ở trẻ em là thấp và nếu mắc thì triệu chứng và các biến chứng cũng nhẹ hơn nhiều so với người lớn. Do vậy, trong bối cảnh nguồn vắc xin vẫn chưa đầy đủ cho nhóm người có nguy cơ cao nhiễm và trở nặng khi mắc COVID-19 như người lớn tuổi, có bệnh nền nguy hiểm, nhân viên y tế… thì việc ưu tiên tiêm vắc xin COVID-19 cho người lớn vẫn là giải pháp phù hợp.Tính đến tháng 11/2021, vắc xin COVID-19 Pfizer-Biontech là vắc xin duy nhất được FDA phê chuẩn đầy đủ sử dụng cho trẻ từ 5 tuổi trở lên. Hãng dược Pfizer và BioNTech đã công bố những kết quả tích cực của thử nghiệm lâm sàng pha 2/3 trên nhóm đối tượng từ 5 đến 11 tuổi. Kết quả cho thấy khi trẻ được tiêm 2 liều vắc xin với liều lượng 0,1 ml và cách nhau 21 ngày thì tính an toàn, khả năng dung nạp và tính sinh miễn dịch là không thua kém so với người lớn.
- Ngoài Pfizer and BioNTech, các hãng dược khác như Moderna cũng đang tiến hành các nghiên cứu về vắc xin cho trẻ em.
- Dữ liệu về tính an toàn và hiệu quả ở trẻ dưới 5 tuổi còn đang được thu thập và nghiên cứu.
- Trong khi chưa có vắc xin cho trẻ em thì chúng ta nên thực hiện một số biện pháp để giảm rủi ro nhiễm COVID-19 cho nhóm đối tượng này:
- Khi trẻ em nhiễm COVID-19 thường ít xuất hiện các triệu chứng nặng nên cha mẹ cần theo dõi kỹ và khi phát hiện trẻ xuất hiện các biểu hiện bất thường như: sốt, mệt mỏi, sổ mũi, biếng ăn… cần liên hệ với cơ quan y tế để được làm xét nghiệm, theo dõi và điều trị kịp thời.
- Tiêm vắc xin COVID-19 cho tất cả những người lớn trong nhà để giảm thiểu sự lây lan cho trẻ. Hạn chế cho trẻ tiếp xúc với người chưa tiêm vắc xin phòng COVID-19.
- Đối với nhóm trẻ có bệnh lý nền như: hen suyễn, béo phì, tiểu đường… các bậc cha mẹ cần theo dõi sát, kiểm soát tốt bệnh nền và đảm bảo tiêm phòng đầy đủ các loại vắc xin khác cho trẻ, ví dụ như vắc xin cúm, phế cầu.
5.4. Người đã từng nhiễm SARS-CoV-2
Trong bối cảnh nguồn vắc xin còn hạn chế và tập trung chủ yếu ở các nước phát triển thì việc phân bổ vắc xin để đảm bảo công bằng đóng vai trò quan trọng trong việc phòng chống COVID-19. Việc ưu tiên tiêm vắc xin cũng cần dựa trên những phân tích về yếu tố nguy cơ. Đối với những người đã và đang mắc COVID-19 việc tiêm vắc xin nên cân nhắc thời gian hợp lý để tạo đáp ứng miễn dịch tốt nhất cũng như đảm bảo an toàn cho người bệnh.
Nghiên cứu mới nhất (Abu-Raddad 2021, JAMA) cho thấy miễn dịch tự nhiên (do từng nhiễm COVID-19) có thể giúp giảm nguy cơ nhiễm đột phá (breakthrough infection) sau khi tiêm vắc xin COVID-19. Ngoài ra, khoảng cách dài hơn giữa nhiễm COVID-19 và tiêm vắc xin cũng giúp giảm tỷ lệ nhiễm đột phá. Hiện tại chưa có đủ nghiên cứu để giải thích cho hiện tượng này. Với những dữ liệu khoa học hiện nay, những người đã mắc COVID-19 trong vòng sáu tháng nên trì hoãn tiêm vắc xin COVID-19.
Những người có triệu chứng nghi nhiễm vi rút SAR-CoV-2 thì cần sàng lọc kỹ trước khi tiêm vắc xin. Nếu tiêm vắc xin xong mới phát hiện ra tình trạng nhiễm vi rút SAR-CoV-2 trong tuần đầu tiên thì hướng xử trí và tiên lượng như người chưa tiêm vắc xin. Lý do sau khi tiêm vắc xin cơ thể chưa thể có miễn dịch tức thì mà thường phải sau 2 tuần mới có lượng kháng thể tối ưu nhất. Hiện nay chưa có dữ liệu đầy đủ về tiên lượng nặng và tử vong ở những người vừa tiêm vắc xin đã nhiễm bệnh. Trong trường hợp này, các cán bộ y tế cần theo dõi triệu chứng của các ca nhiễm sau khi tiêm vắc xin, đặc biệt là những bệnh nhân trẻ tuổi. Hướng dẫn người bệnh khi có các triệu chứng như sốt li bì, tụt huyết áp, mạch nhanh… cần phải nhập viện ngay lập tức.
5.5. Kết hợp các loại vắc xin COVID-19
Nhiều nghiên cứu đã chỉ ra rằng việc phối hợp các loại vắc xin COVID-19 khác nhau có thể giúp đáp ứng miễn dịch tốt hơn. Tuy nhiên câu trả lời về hiệu quả tại cộng đồng và tần suất xuất hiện các phản ứng sau tiêm là như thế nào thì vẫn chưa rõ.
Trong một nghiên cứu được tiến hành tại Tây Ban Nha đã cho thấy đáp ứng miễn dịch tốt ở nhóm đối tượng tiêm mũi một là vắc xin COVID-19 Astrazeneca và mũi hai là COVID-19 Pfizer. Tuy nhiên sự kết hợp này lại làm tăng tỷ lệ các phản ứng tại chỗ như đau tại chỗ tiêm, đau đầu, đau mỏi cơ, tê bì. Một nghiên cứu khác do David Hillus và cộng sự tiến hành so sánh khả năng sinh miễn dịch trên 340 đối tượng được tiêm hai liều vắc xin COVID-19 Pfizer hoặc liều đầu tiên là vắc xin COVID-19 Astrazeneca. Kết quả nghiên cứu cho thấy với cả 2 phác đồ thì đều đáp ứng miễn dịch tương đương nhau. Nghiên cứu thứ ba về phối hợp vắc xin được tiến hành tại Đức, kết quả cho thấy khi phối hợp vắc xin COVID-19 Astrazeneca và Pfizer sẽ sinh miễn dịch tốt hơn so với phác đồ hai liều vắc xin của Astrazeneca và cao tương đương khi tiêm hai liều vắc xin COVID-19 Pfizer.
Những nghiên cứu về việc phối hợp các loại vắc xin COVID-19 còn nhỏ lẻ và thời gian theo dõi còn ngắn nên vẫn chưa đánh giá được tính hiệu quả và an toàn. Vì vậy, trước khi có những kết quả đến từ các nghiên cứu rộng rãi và lâu dài hơn thì WHO vẫn khuyến cáo sử dụng cùng một loại vắc xin.
Tính đến thời điểm hiện tại ngày 23 tháng 9 năm 2021, Bộ Y tế Việt Nam đã tiếp nhận các loại vắc xin có công nghệ sản xuất khác nhau (Astrazeneca, Pfizer/BioNtech, Moderna, Sinopharm, Sputnik V…). Bộ Y tế hướng dẫn “những người đã tiêm mũi 1 vắc xin nào thì tốt nhất tiêm mũi 2 bằng vắc xin đó”. Tuy nhiên cần xem xét việc kết hợp nhiều loại vắc xin trong tình trạng khẩn cấp có thể sẽ đẩy nhanh độ bao phủ vắc xin toàn dân từ đó góp phần sớm đẩy lùi đại dịch COVID-19.
5.6. Liều tăng cường vắc xin COVID-19
Các nghiên cứu đã chỉ ra rằng, nhóm người có hệ miễn dịch bị suy giảm như: người ghép tạng, người mắc bệnh ung thư, người bị suy thận… đáp ứng miễn dịch với vắc xin COVID-19 không cao như người bình thường ngay từ những mũi đầu. Vì vậy việc bổ sung liều thứ 3 cho nhóm này nhanh chóng nhận được sự đồng thuận của giới chuyên gia. Tuy nhiên, hiện nay có nhiều tranh cãi về việc có nên tiêm liều tăng cường ở quần thể dân số bình thường hay không. Các chuyên gia của FDA đã đưa ra các lý luận như sau:
- Lượng kháng thể sẽ giảm dần từ khoảng tháng thứ 6 trở đi tùy từng loại vắc xin COVID-19 và hiệu quả bảo vệ có thể giảm đối với chủng Delta nhưng vẫn còn khả năng bảo vệ khá tốt ở những người đã tiêm đầy đủ 2 liều vắc Một nghiên cứu lớn trên bệnh nhân ở bang New York cho thấy hiệu quả của vắc xin chống lại tất cả các trường hợp nhiễm SAR-CoV-2 giảm từ 91,7% xuống còn 79,8% trong khoảng thời gian từ tháng 5 đến tháng 7 khi chủng Delta hoành hành trên thế giới. Tuy nhiên khả năng bảo vệ khỏi nhập viện đối với COVID-19 vẫn đạt gần 95%. Dữ liệu này cũng tương đồng với nghiên cứu tại Israel khi hiệu quả bảo vệ khỏi bệnh nặng vẫn lên tới 85% đến 92%. CDC Hoa Kỳ cũng công bố dữ liệu chứng minh những người đã tiêm đủ 2 mũi vắc xin có nguy cơ bị nhiễm bệnh thấp hơn 5 lần, nhập viện vì COVID-19 thấp hơn 10 lần và tử vong thấp hơn 11 lần so với những người chưa được tiêm chủng đầy đủ.
- Việc tiêm vắc xin mang lại lợi ích lớn hơn nhiều so với những phản ứng không mong muốn, và các phản ứng phụ nghiêm trọng cũng đã được làm rõ. Tuy nhiên việc bổ sung liều thứ 3 còn chưa được đánh giá kỹ lưỡng giữa lợi ích và nguy cơ.
- Việc tiêm liều bổ sung sẽ có ý nghĩa và hiệu quả hơn nhiều nếu chúng ta sử dụng các vắc xin cải tiến dựa trên các đặc điểm của biến chủng hiện hành.
- Việc tiêm liều bổ sung cho những người đã tiêm đủ 2 liều sẽ giúp tăng cường hệ miễn dịch nhưng sẽ cứu được nhiều người hơn nếu chúng ta dùng những liều đó cho những người chưa được tiêm. Đại dịch COVID-19 hiện nay là cuộc chiến của toàn nhân loại, việc các nước phát triển viện trợ vắc xin cho những nước nghèo không chỉ mang tính nhân văn hỗ trợ giữa con người với con người mà đó còn là hành động đem lại lợi ích chung cho mọi người bao gồm cả chính họ.
Chưa tổ chức, cá nhân nào khẳng định được mô hình dự đoán, chiến lược nào là đúng trong bối cảnh dịch bệnh COVID-19 vẫn đang diễn biến hết sức phức tạp và vắc xin COVID-19 vẫn còn mới. Việc tiêm liều bổ sung cũng cần phải linh hoạt và dựa vào tình hình thực tế của từng địa phương cũng như nguồn cung vắc xin.
6. BẢO QUẢN VẮC XIN
Các vắc xin sản xuất theo công nghệ bất hoạt hoặc véc tơ vi rút như COVID-19 Astrazeneca, Sinopharm… cần được bảo quản 2-8ºC và không được để đông băng vắc xin. Lọ vắc xin đã mở chỉ được sử dụng trong vòng 6 giờ kể từ khi mở và được bảo quản ở 2-8 ºC. Bảo quản tránh tiếp xúc trực tiếp dưới ánh sáng mặt trời. Với vắc xin COVID-19 Astrazeneca, lọ vắc xin chưa mở bảo quản ở 2-8ºC được phép sử dụng trong vòng 6 tháng kể từ ngày sản xuất, còn đối với vắc xin Vero cell của Sinopharm là 24 tháng kể từ ngày sản xuất.
Những vắc xin sản xuất theo công nghệ mRNA cần phải bảo quản ở nhiệt độ âm sâu:
6.1.Vắc xin Pfizer
Bảo quản vắc xin ở nhiệt độ âm sâu -90°C đến -60°
- Ở nhiệt độ -90ºC đến -60ºC vắc xin có thể được bảo quản cho đến ngày hết hạn sử dụng được ghi trên nhãn của lọ vắc xin (6 tháng kể từ ngày sản xuất).
- Trong trường hợp không có tủ âm sâu, có thể sử dụng thùng vận chuyển giữ nhiệt của Pfizer để tối đa hóa thời gian sử dụng. Thời gian bảo quản trong thùng vận chuyển được tối đa 30 ngày nếu được bổ sung đá khô thường xuyên theo định kỳ 5 ngày 1 lần. Không nên mở thùng vận chuyển giữ nhiệt quá 3 phút mỗi lần.
- Để lọ vắc xin thẳng đứng trong khay và tránh ánh sáng. Không mở khay lọ hoặc tháo lọ vắc xin ra cho đến khi sẵn sàng rã đông/sử dụng vắc
Bảo quản vắc xin trong buồng lạnh/tủ lạnh âm -25°C đến -15°C
- Vắc xin có thể được bảo quản trong buồng lạnh/tủ lạnh âm từ -25°C đến -15°C tối đa 2 tuần. Bất cứ khi nào vận chuyển vắc xin ở nhiệt độ -25°C đến -15°C thì thời gian vận chuyển đều được tính vào giới hạn 2 tuần. Tuy nhiên lưu ý vắc xin khi để ở nhiệt độ -25°C đến -15°C thì chỉ được bảo quản trở lại nhiệt độ âm sâu (-90ºC đến -60ºC) 1 lần.
- Ghi lại thời gian bắt đầu bảo quản vắc xin trong ở nhiệt độ “-25°C đến -15°C”.
- Nếu hết thời hạn 2 tuần bảo quản trong buồng lạnh/tủ lạnh âm, chuyển vắc xin sang tủ lạnh dương 2°C đến 8°C thì bảo quản thêm tối đa 1 tháng (31 ngày). Ghi thời gian bắt đầu bảo quản ở 2°C đến 8°C.
Bảo quản vắc xin trong buồng lạnh/tủ lạnh dương nhiệt độ 2°C đến 8°C
- Vắc xin có thể được bảo quản trong buồng lạnh/tủ lạnh dương từ 2°C đến 8°C tối đa 1 tháng (31 ngày). Bất cứ khi nào vận chuyển vắc xin ở nhiệt độ 2°C đến 8°C thì thời gian vận chuyển đều được tính vào giới hạn 1 tháng (31 ngày), tổng thời gian vận chuyển ở nhiệt độ 2°C đến 8°C không vượt quá 12 giờ. Vì vậy, cần phải kế hoạch triển khai tiêm vắc xin này trước khi lấy vắc xin từ buồng lạnh/tủ lạnh âm sâu để tránh việc vắc xin hết hạn và trả đủ 2 mũi vắc xin theo hướng dẫn của Bộ Y tế và thông tin kê toa của nhà sản xuất.
- Ghi ngày bắt đầu bảo quản ở nhiệt độ từ 2°C đến 8°C để theo dõi thời gian vắc xin đã được để trong buồng lạnh/tủ lạnh ở nhiệt độ này và không làm đông băng lại vắc xin.
Lưu ý: Khi chuyển khay/lọ vắc xin giữa các môi trường bảo quản:
- Không chạm vào lọ vắc xin cho đến khi có nhu cầu lấy chúng ra khỏi khay lọ để sử dụng hoặc chuyển môi trường bảo quản.
- Đeo găng tay bảo hộ khi chuyển các lọ vắc xin đông lạnh.
- Khi lấy lọ vắc xin ra khỏi khay không nên mang cả khay ra khỏi môi trường đông lạnh. Nếu khay lấy ra khỏi tủ âm từ -25°C đến -15°C, hãy để lại tủ đông trong vòng chưa đầy 1 phút.
- Sau khi lọ riêng lẻ được lấy ra khỏi khay ở nhiệt độ phòng, không được đưa trở lại bảo quản đông lạnh và nên được rã đông để sử dụng.
- Không làm đông lại các lọ đã rã đông.
- Bảo quản lọ vắc xin đã pha loãng ở nhiệt độ 2°C đến 8°C trên miếng xốp trong phích vắc xin. Vắc xin đã pha chỉ được sử dụng trong vòng 6 giờ. Bảo quản vắc xin sau khi pha loãng.
6.2. Vắc xin COVID-19 Moderna
Bảo quản ở nhiệt độ âm -50°C đến -15°C trong tủ lạnh âm
- Vắc xin có thể bảo quản ở nhiệt độ từ -50°C đến -15°C cho đến ngày hết hạn sử dụng được ghi trên nhãn của lọ vắc xin (7 tháng kể từ ngày sản xuất).
- Không bảo quản vắc xin phòng COVID-19 Moderna ở nhiệt độ dưới -50°C, sử dụng đá khô để bảo quản có thể làm nhiệt độ hạ dưới -50°C.
- Trong quá trình bảo quản vắc xin cần để lọ vắc xin thẳng đứng trong hộp và hạn chế tiếp xúc với ánh sáng. Vắc xin đã rã đông sẽ không bảo quản trở lại nhiệt độ đông băng do vậy không lấy lọ vắc xin ra khỏi tủ lạnh âm cho đến khi sẵn sàng rã đông và sử dụng vắc xin hoặc vận chuyển vắc
Bảo quản ở nhiệt độ 2°C đến 8°C
Vắc xin có thể bảo quản ở nhiệt độ từ 2°C đến 8°C trong thời gian tối đa 30 ngày, vì vậy cũng cần phải có kế hoạch triển khai tiêm vắc xin này trước khi lấy ra khỏi tủ lạnh âm sâu cũng như kế hoạch trả mũi 2 sau 4 tuần. Ghi lại thời gian bắt đầu bảo quản vắc xin ở nhiệt độ từ 2°C đến 8°C. Không được để đông băng lại vắc xin đã rã đông.
Nhiệt độ bảo quản khác
- Lọ vắc xin chưa mở có thể bảo quản ở nhiệt độ từ 8°C đến 25°C trong thời gian tổng cộng là 24 giờ.
- Lọ vắc xin đã mở có thể bảo quản ở nhiệt độ từ 2°C đến 25°C trong tối đa 12 giờ.
Bảng 22.3. Tóm tắt thông tin của một số vắc xin COVID-19
| Loại vắc xin | Bất hoạt | Véc tơ vi rút | Công nghệ mRNA | |||||
| Tên vắc xin | Vero Cell | Sinovac- Coronavac | Hayat-Vax | Janssen | Astrazeneca | Gmaleya | Moderna | Comirnaty |
| Hãng sản xuất | Sinor- pharm | Sinovac Biotech | Sino- pharm CNBG and Abu Dha-bi’s G42 | Johnson and John- son | Oxford-As- trazeneca | Sputnik V | Moderna | Pfizer – BioNTech |
| Số liều | 2 x 0,5 ml | 2 x 0,5 ml | 2 x 0,5 ml | 1 x 0,5 ml | 2 x 0,5 ml | 2 x 0,5 ml | 2 x 0,5 ml | 2 x 0,3 ml |
| Khoảng cách | 3- 4 tuần | 2 – 4 tuần | 3 – 4 tuần | 8 – 12 tuần | 3 tuần | 4 tuần | 3 tuần | |
| Thời gian đạt hiệu lực miễn dịch tối đa | Sau 2 tuần | Sau 2 tuần | Sau 2 tuần | Sau 2 tuần | Sau 2 tuần | Sau 2 tuần | Sau 2 tuần | Sau 2 tuần |
| Bảo quản | 2 đến 8ºC | 2 đến 8ºC | 2 đến 8ºC | 2 đến 8ºC (3 tháng) | 2 đến 8ºC (6 tháng) | 18,5ºC (dạng lỏng)
2 – 8ºC (dạng khô) |
-250 đến -15ºC (6 tháng) và 2 đến 8ºC (30 ngày) | -90 đến -60ºC (6 tháng)
-25 đến -15ºC (2 tuần) 2 đến 8ºC (31 ngày) |
| Hiệu quả bảo vệ (%) | 78,1 | 50,7 | 79,34 | 66,3 | 76 | 91,6 | 94,1 | 95 |
7. KỸ THUẬT TIÊM VẮC XIN COVID-19
Kỹ thuật tiêm vắc xin đúng đóng vai trò quan trọng trong việc tối ưu hóa khả năng sinh miễn dịch và giảm thiểu các tác dụng không mong muốn cho khách hàng, đảm bảo an toàn trong tiêm chủng.
Bảo quản vắc xin trong buổi tiêm chủng: Vắc xin phải được bảo quản trong dây chuyền lạnh (tủ lạnh/hòm lạnh/phích vắc xin) ở nhiệt độ từ 2 độ C đến 8 độ C. Không được để đông băng vắc xin. Tại bàn tiêm chủng bảo quản vắc xin trong phích vắc xin. Lọ vắc xin đã mở chỉ sử dụng trong vòng 6 giờ.
Kiểm tra vắc xin và dung môi (nếu có)
- Kiểm tra nhãn lọ vắc xin, dung môi. Nếu không có nhãn phải hủy bỏ.
- Kiểm tra hạn sử dụng lọ vắc xin và dung môi. Nếu quá hạn sử dụng phải hủy bỏ.
- Kiểm tra lọ vắc xin, hủy vắc xin nếu có thay đổi về màu sắc hoặc bất kỳ sự thay đổi bất thường nào khác.
- Sử dụng đúng loại vắc xin COVID-19 theo chỉ định của bác sĩ khám sàng lọc.
- Chỉ pha loãng khi có đối tượng đến tiêm chủng.
- Dung dịch pha loãng là nước muối sinh lý Natri clorua 0,9% được cấp phát kèm theo vắc Tại buổi tiêm chủng, bảo quản dung dịch pha loãng cùng với vắc xin ở nhiệt độ 2-8 độ C trong phích vắc xin.
- Sử dụng một lọ nước pha để pha cho một lọ vắc Sử dụng một bơm kim tiêm (5 ml hoặc 3 ml) vô trùng để pha vắc xin.
- Kiểm tra vắc xin/dung dịch pha loãng trước khi sử dụng
- Kiểm tra nhãn lọ vắc Nếu không có nhãn phải hủy bỏ. Trước khi pha loãng kiểm tra hạn sử dụng của vắc xin và dung dịch pha loãng. Không sử dụng vắc xin hoặc dung dịch pha loãng đã hết hạn.
Lưu ý:
- Đối với vắc xin của Pfizer-BioNTech thời hạn sử dụng của vắc xin sẽ phụ thuộc vào nhiệt độ bảo quản vắc xin. Vắc xin đã bảo quản ở nhiệt độ 2°C đến 8°C chỉ sử dụng tối đa trong vòng 31 ngày.
- Kiểm tra lọ vắc xin đã được rã đông trước khi pha loãng. Ở nhiệt độ 2ºC đến 8ºC, vắc xin được rã đông trong thời gian 3 giờ.
- Nhẹ nhàng đảo ngược lọ vắc xin theo chiều thẳng đứng 10 lần và không lắc lọ vắc Vắc xin có màu từ trắng đến trắng nhạt và có thể chứa các hạt đục. Không sử dụng nếu chất lỏng trong lọ vắc xin bị đổi màu.
- Cân bằng áp suất trong lọ vắc xin trước khi rút kim ra khỏi lọ bằng cách hút ngược lại 1,8 ml không khí từ lọ vắc xin vào bơm kim tiêm để loại bỏ không khí khỏi lọ vắc
- Tiếp tục lật nhẹ nhàng lọ vắc xin theo chiều thẳng đứng 10 lần.
Tiến hành tiêm:
- Sử dụng bơm kim tiêm vô trùng lấy đúng lượng vắc xin tùy từng loại.
Lưu ý: đối với vắc xin COVID-19 Astrazeneca không lắc lọ vắc xin để tránh tình trạng tạo bọt, các vắc xin sản xuất theo công nghệ mRNA không lắc lọ vắc xin để bảo toàn cấu trúc của phân tử vắc xin.
- Đề nghị người được tiêm ngồi xuống. Lưu ý cán bộ y tế ngồi tránh trực diện với đối tượng tiêm chủng để phòng lây nhiễm SARS-CoV-2.
- Đâm nhanh và thẳng kim xuyên qua da giữa các ngón tay làm cữ. Đâm sâu vào bắp thẳng góc 90 độ.
- Ấn pít tông bằng ngón cái đẩy vắc xin vào.
- Rút kim nhanh, nếu nơi tiêm bị chảy máu sử dụng bông khô vô khuẩn ấn vào chỗ tiêm.
Ghi chép thông tin sau khi tiêm vắc xin
- Ghi các thông tin (số liều, ngày tiêm) vào danh sách/phần mềm quản lý đối tượng được tiêm chủng vắc xin phòng COVID-19 tích hợp trên hệ thống thông tin tiêm chủng Quốc gia hoặc Ứng dụng Hồ sơ sức khỏe điện tử.
- Ghi đầy đủ các thông tin ngày tiêm, loại vắc xin, lô vắc xin, giờ tiêm vào giấy xác nhận đã tiêm vắc xin phòng COVID-19 và trả lại cho đối tượng tiêm chủng và hẹn lần tiêm chủng Phiếu tiêm chủng bắt buộc phải có chữ ký của bác sĩ chỉ định và điều dưỡng thực hiện tiêm vắc xin COVID-19.
Theo dõi sau tiêm vắc xin COVID-19
- Sau khi tiêm vắc xin COVID-19 chúng ta có thể gặp phải các phản ứng thông thường tại chỗ hay toàn thân: sưng, đau, nóng đỏ chỗ tiêm, đau đầu, mệt mỏi, đau cơ… Tuy nhiên đây là những phản ứng không nguy hiểm, báo hiệu hàng rào bảo vệ của cơ thể đang được hình thành. Khi gặp các phản ứng này sau khi tiêm vắc xin chúng ta chỉ cần nghỉ ngơi, tăng cường ăn uống, hạn chế vận động mạnh và không nên sử dụng các chất kích thích sau khi tiêm vắc xin.
- Các vắc xin được cấp phép sử dụng hiện nay đã được kiểm chứng về tính an toàn bởi các Tổ chức Y tế uy tín trên thế giới. Tuy nhiên vẫn có một tỷ lệ rất nhỏ có thể gặp phải các phản ứng nghiêm trọng sau khi tiêm: tức ngực, khó thở, phù mặt, phát ban, nổi mày đay khắp người. Các phản ứng nghiêm trọng này thường xảy ra một vài giờ đầu sau khi tiêm vì vậy nên theo dõi tại điểm tiêm từ 15 đến 30 phút. Trong trường hợp về nhà nếu xuất hiện các phản ứng nghiêm trọng cần phải đến cơ sở y tế gần nhất để thăm khám.
TÀI LIỆU THAM KHẢO
- Voysey M, Clemens SAC, Madhi SA, et al. Safety and efficacy of the ChAdOx1 nCoV- 19 vaccine (AZD1222) against SARS-CoV-2: an interim analysis of four randomised controlled trials in Brazil, South Africa, and the UK. Lancet (London, England). Jan 9 2021;397(10269):99-111. doi:10.1016/s0140-6736(20)32661-1
- World Health Organization. Development of new vaccines. https://www.euro.who.int/ en/health-topics/disease-prevention/vaccines-and-immunization/vaccines-and-immuni- zation/development-of-new-vaccines
- World Health Organization. Coronavirus disease (COVID-19): Herd immunity, lock- downs and COVID-19. Accessed 1 September 2021, https://www.who.int/news-room/q- a-detail/herd-immunity-lockdowns-and-covid-19.
- Vasileiou Eleftheria, Simpson Colin R, Shi Ting, et al. Interim findings from first-dose mass COVID-19 vaccination roll-out and COVID-19 hospital admissions in Scotland: a national prospective cohort study. The Lancet. 2021;397(10285):1646-1657.
- Sivan Gazit, Roei Shlezinger, Galit Perez, et al. Comparing SARS-CoV-2 natural immu- nity to vaccine-induced immunity: reinfections versus breakthrough infections. medRxiv. 2021;
- Ramasamy MN, Minassian AM, Ewer KJ, et al. Safety and immunogenicity of ChA- dOx1 nCoV-19 vaccine administered in a prime-boost regimen in young and old adults (COV002): a single-blind, randomised, controlled, phase 2/3 trial. Lancet (London, En- gland). Dec 19 2021;396(10267):1979-1993. doi:10.1016/s0140-6736(20)32466-1.
- Jara Alejandro, Undurraga Eduardo A, González Cecilia, et Effectiveness of an inacti- vated SARS-CoV-2 vaccine in Chile. New England Journal of Medicine. 2021;
- Polack Fernando P, Thomas Stephen J, Kitchin Nicholas, et al. Safety and efficacy of the BNT162b2 mRNA COVID-19 vaccine. New England Journal of Medicine. 2020;
- World Health The Pfizer BioNTech (BNT162b2) COVID-19 vaccine: What you need to know. Accessed 1 September 2021, https://www.who.int/news-room/fea– ture-stories/detail/who-can-take-the-pfizer-biontech-covid-19–vaccine
- ModernaTX A. A study to evaluate efficacy, safety, and immunogenicity of mRNA- 1273 vaccine in adults aged 18 years and older to prevent COVID-19. ClinicalTrials 2020;
- Centers for Disease Control and Prevention. FDA and CDC Lift Recommended Pause on Johnson & Johnson (Janssen) COVID-19 Vaccine Use Following Thorough Safety Re-
- GA Diaz, GT Parsons, SK Gering, et al. Myocarditis and Pericarditis After Vaccination for COVID-19. Jama. Sep 28 2021;326(12):1210-1212. doi:10.1001/jama.2021.13443
- Nicola Cirillo, Richard Doan. The association between COVID-19 vaccination and Bell’s palsy. The Lancet Infectious Diseases. 2021;
- CC Lai, WC Ko, CJ. Chen, et al. COVID-19 vaccines and thrombosis with thrombocy- topenia syndrome. Expert review of vaccines. Aug 2021;20(8):1027-1035. doi:10.1080/1 4760584.2021.1949294
- Pfizer và BioNTech. Pfizer và BioNTech announce positive topline results from piv- otal trial of COVID-19 vaccine in children 5 to 11 years. https://www.pfizer.com/news/ press-release/press-release-detail/pfizer-and-biontech-announce-positive-topline-re- sults?
- Quyết định 3802/QĐ-BYT ban hành hướng dẫn tạm thời khám sàng lọc trước tiêm chủng vaccine COVID-19
- Emily H Adhikari, Catherine Y Spong. COVID-19 vaccination in pregnant and lactating women. Jama. 2021;325(11):1039-1040.
- David Hillus, Tatjana Schwarz, Pinkus Tober-Lau, et al. Safety, reactogenicity, and immunogenicity of homologous and heterologous prime-boost immunisation with ChA- dOx1-nCoV19 and BNT162b2: a prospective cohort study. medRxiv. 2021;
- Merryn Voysey, Sue Ann Costa Clemens, et al. Safety and efficacy of the ChAdOx1 nCoV-19 vaccine (AZD1222) against SARS-CoV-2: an interim analysis of four randomised controlled trials in Brazil, South Africa, and the The Lancet. 2021;397(10269):99-111.
- Correspondence BNT162b2 and ChAdOx1 nCoV-19 Vaccine Effectiveness against Death from the Delta Variant. N Engl J Med 2021; 385:2195-2197 DOI: 10.1056/NE- JMc2113864
- Effectiveness of BNT162b2 and mRNA-1273 covid-19 vaccines against symptomatic SARS-CoV-2 infection and severe covid-19 outcomes in Ontario, Canada: test negative design BMJ 2021;374:n1943; 374 doi: https://doi.org/10.1136/bmj.n1943 (Pub- lished 20 August 2021)
- Viện Vệ Sinh Dịch Tễ Trung Ương. Hướng dẫn thực hành tiêm chủng vắc
