Bệnh Nội tiết - chuyển hóa
Giải phẫu, sinh lý, bệnh học, chẩn đoán và điều trị các bệnh lý tuyến giáp
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
Bài viết Giải phẫu, sinh lý, bệnh học, chẩn đoán và điều trị các bệnh lý tuyến giáp được lược dịch từ Chapter 7: The Thyroid gland, Textbook Greenspan’s Basic & Clinical Endocrinology 10th edition bởi 2 bác sĩ Nguyễn Thế Bảo – Nguyễn Đăng Sơn – Trường Đại học Y Dược Cần Thơ. Để tải file pdf phần 1 mời các click vào link ở đây, phần 2 ở đây.
Tuyến giáp là cơ quan nội tiết lớn nhất cơ thể. Vai trò chính của tuyến giáp là chế tiết các hormone tuyến giáp với nồng độ phù hợp, chủ yếu là thyroxine (T4), với một lượng nhỏ triiodothyronine (T3), phần lớn T3 còn lại được tạo thành từ quá trình loại bỏ iod từ T4 ở các cơ quan ngoại vi. Ở mô đích, T3 sẽ tương tác với các thụ thể T3 nằm trong nhân tế bào. Các hormone tuyến giáp có vai trò trong sự phát triển bình thường của bào thai, ở trẻ em, trong đó có hệ thần kinh trung ương; tham gia điều hòa nhịp tim, sự co và giãn của cơ tim; ảnh hưởng đến nhu động ống tiêu hóa và thanh thải nước ở thận; điều hòa nhu cầu sử dụng năng lượng của cơ thể, sự sinh nhiệt, điều hòa cân nặng và chuyển hóa lipid. Ngoài ra, tuyến giáp còn có các tế bào cạnh nang (còn gọi là tế bào C) sản sinh ra calcitonin, là một hormone có bản chất là peptide có vai trò ức chế sự hủy xương, nhưng vai trò sinh lý ở người thật sự không rõ ràng. Tuy nhiên, calcitonin về mặt lâm sàng lại có ý nghĩa quan trọng với vai trò là một marker khối u được sản xuất bởi các ung thư tuyến giáp có nguồn gốc từ vùng tủy giáp phát sinh từ các tế bào này (xem Chương 8).
NGUỒN GỐC PHÔI THAI, GIẢI PHẪU VÀ MÔ HỌC TUYẾN GIÁP
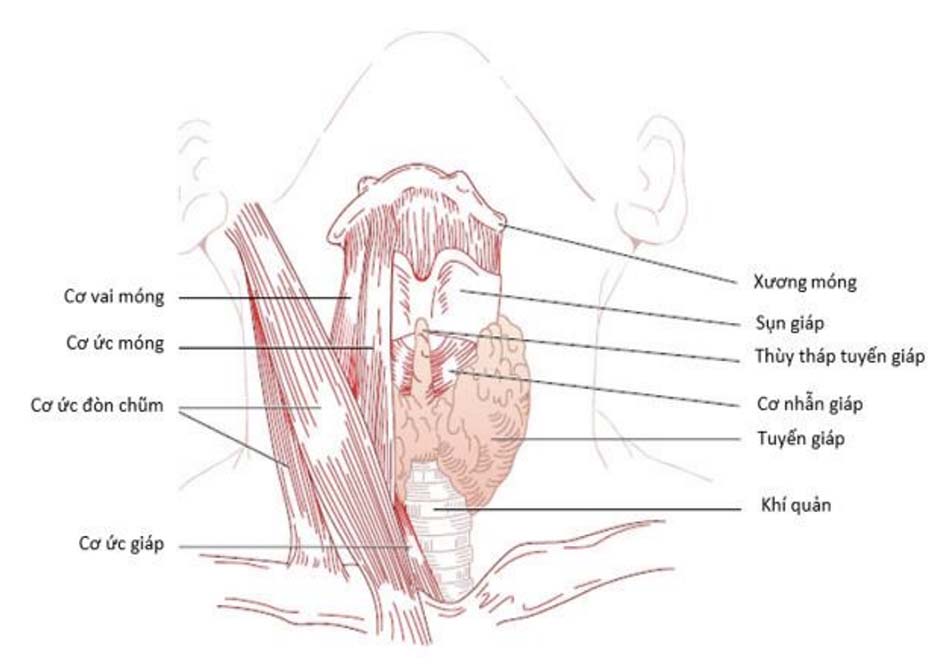
Tuyến giáp có nguồn gốc từ sự lõm vào của trung phôi bì trong nền hầu ở lỗ tịt, rồi đi xuống phía trước khí quản và chia làm hai phần, tạo thành hai thùy bên, mỗi thùy dài khoảng 4 cm, rộng khoảng 2 cm và dày khoảng 1 cm ở người trưởng thành. Mô giáp lạc chỗ có thể hiện diện ở bất cứ đâu dọc theo ống giáp lưỡi này, từ đáy lưỡi (tuyến giáp ở lưỡi) đến tận trung thất. Tận cùng phần đuôi của ống giáp lưỡi tạo thành thùy tháp của tuyến giáp, thùy này có thể sờ được trong những bệnh lý viêm giáp lan tỏa (Xem Hình 7.1).
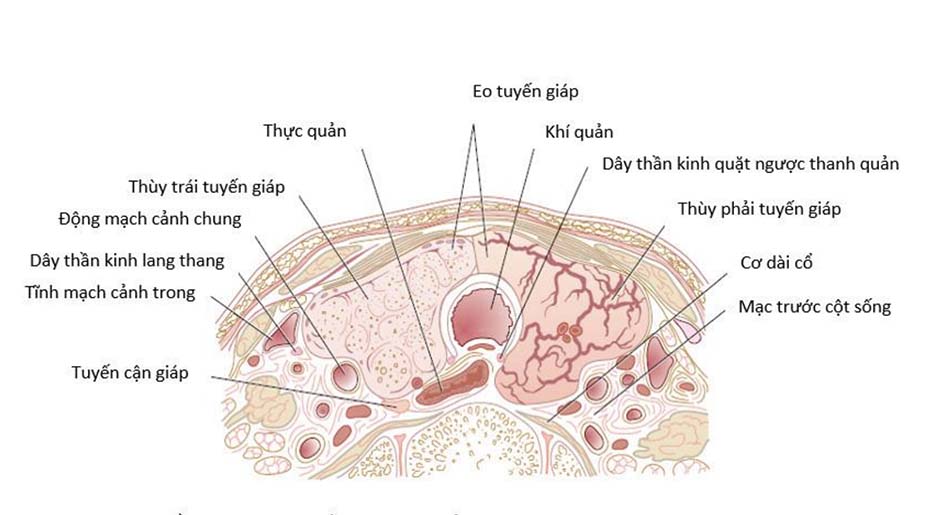
Vì phía sau tuyến giáp dính với mạc trước của khí quản, nên tuyến giáp cử động lên xuống theo nhịp nuốt. Khi tuyến giáp to, bờ dưới có thể phát triển đến tận trung thất trên (bướu giáp chìm sau xương ức), trong khi đó phần trên bị giới hạn lại do có cơ ức giáp bám vào sụn giáp. Tuyến giáp có liên hệ mật thiết về mặt giải phẫu, có ý nghĩa lâm sàng quan trọng với thần kinh quặt ngược thanh quản, chạy phía sau tuyến giáp, còn có 4 tuyến cận giáp nằm ở phần sau trên và sau giữa của các thùy tuyến giáp. Tuyến giáp được bọc quanh khí quản và rìa sau của mỗi thùy sẽ tiếp giáp với thực quản. Tất cả các cấu trúc này sẽ bị chèn ép khi tuyến giáp to, hay bị xâm lấn bởi các bệnh lý ác tính của tuyến giáp cũng như dễ bị tổn thương khi phẫu thuật tuyến giáp (Xem Hình 7.2).
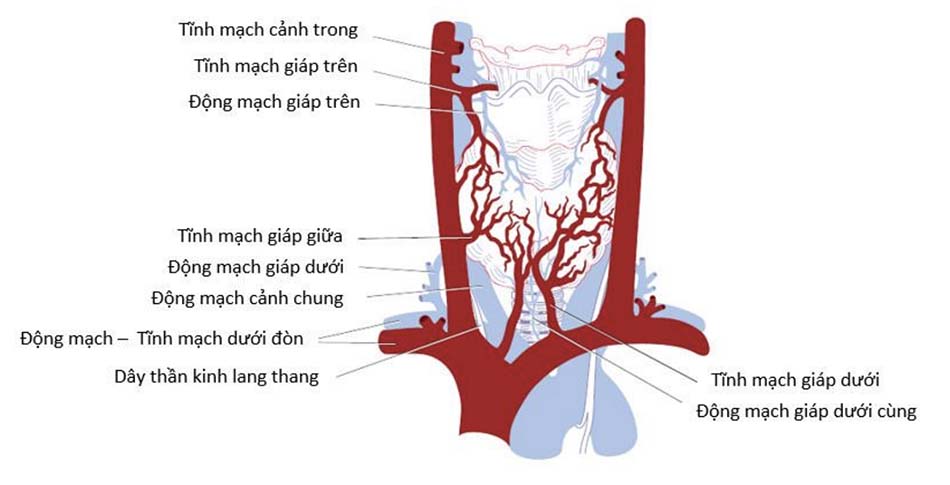
Tuyến giáp được cấp máu dồi dào (Xem Hình 7.3), và có thể phong phú hơn ở những bệnh nhân bị cường giáp, khám lâm sàng có thể nghe được âm thổi hoặc sờ được rung miu. Về mặt vi thể, các tế bào tuyến giáp tạo thành khối cầu rỗng (các nang) bao bọc xung quanh lòng ống ở giữa, trong lòng có chứa các thyroglobulin (TG) đã được iod hóa (keo giáp), chính là nơi dự trữ hormone tuyến giáp. (Lời dịch giả: Tuyến giáp được cấp máu chủ yếu bởi 2 động mạch: động mạch giáp trên là nhánh bên của động mạch cảnh ngoài; động mạch giáp dưới xuất phát từ động mạch thân giáp cổ, là nhánh của động mạch dưới đòn)
SINH LÝ TUYẾN GIÁP
CẤU TRÚC VÀ SINH TỔNG HỢP HORMONE TUYẾN GIÁP
Hormone tuyến giáp bản chất là iod hóa từ thyronine. Các tế bào nang giáp có khả năng tổng hợp phần lớn tiền chất của TG, bắt giữ iod từ tuần hoàn và biểu lộ thụ thể gắn TSH, đóng vai trò trong sự tăng trưởng và sinh tổng hợp các tế bào tuyến giáp.
CHUYỂN HÓA IOD
Iod là thành phần cấu trúc chính của hormone tuyến giáp. Vì thế, iod là một trong những vi chất thiết yếu có mặt trong thức ăn hay nước uống dưới dạng iodide hay iodate (sẽ được chuyển thành iodide ở dạ dày). WHO khuyến cáo nhu cầu iod nhập vào mỗi ngày là 150 µg ở người trưởng thành, 200 µg ở phụ nữ mang thai và cho con bú, 90 µg ở trẻ em. Vì hầu hết iod sẽ được đào thải qua thận, nên chỉ số iod niệu là một thông số rất có ích trong khảo sát lượng iod nhập.
TỔNG HỢP VÀ BÀI TIẾT HORMONE TUYẾN GIÁP
Tổng hợp T4 và T3 ở tuyến giáp gồm 6 bước: (1) vận chuyển chủ động iod qua màng đáy vào tế bào tuyến giáp (bắt giữ); (2): oxi hóa iod và iod hóa TG ở vị trí tyrosine (hữu cơ hóa); (3) liên kết các phân tử iodotyrosine bên trong TG để tạo thành T3 và T4 (bắt cặp); (4) ẩm bào và sau đó là phân giải TG để giải phóng iodothyronine và iodotyrosine vào tuần hoàn; (5) loại bỏ iod khỏi iodotyrosine ở bên trong tế bào tuyến giáp, biến đổi và tái sử dụng lại các iod được giải phóng này; và (6) loại bỏ iod ở vị trí 5’ bên trong tuyến giáp từ T4 để tạo T3. Quá trình tổng hợp hormone tuyến giáp cần NIS, TG và enzyme thyroid peroxidase (TPO). Xem Hình 7-6 và 7-7. Thyroglobulin
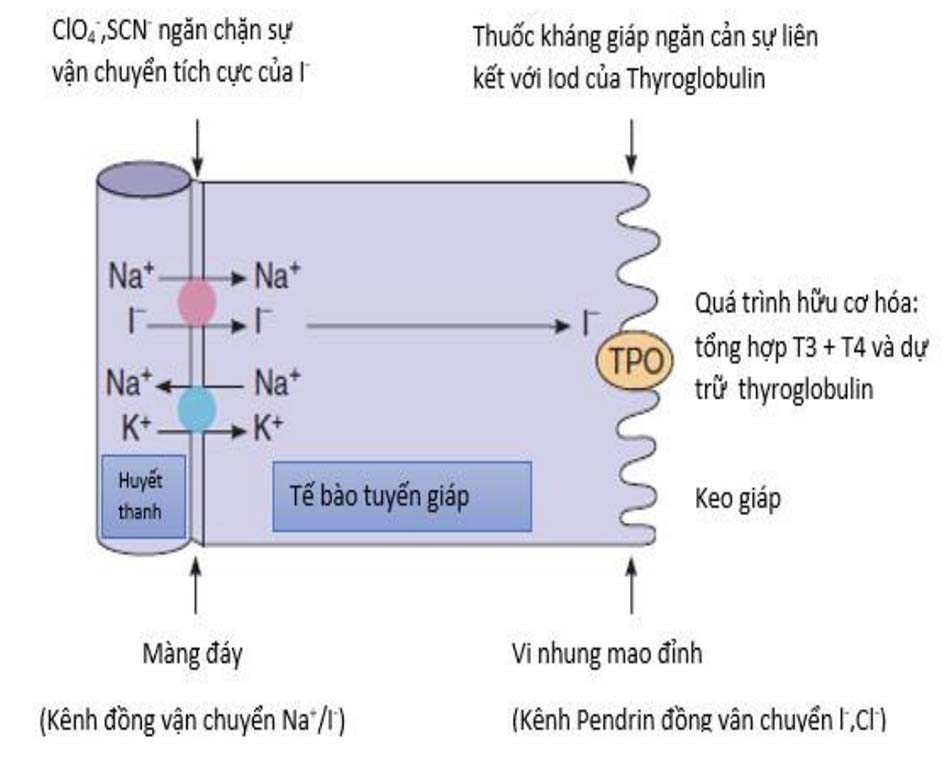
Vận chuyển Iodide
Iodide (I- ) được vận chuyển qua lại màng đáy của các tế bào tuyến giáp nhờ vào NIS (kênh đồng vận chuyển Na+ -I – ), sử dụng năng lượng từ bơm Na+ -K+ – ATPase, giúp duy trì nồng độ iod tự do ở bên trong tuyến giáp cao gấp 30-40 lần so với trong huyết tương. Bình thường, NIS được kích thích bởi TSH, bên cạnh đó cũng kích thích bởi các kháng thể kích thích thụ thể TSH có trong bệnh Graves. Ở tuyến nước bọt, dạ dày và vú cũng có kênh NIS này nên cũng giúp duy trì nồng độ iod tự do cao hơn nhưng không tham gia vào chức năng hữu cơ hóa và dự trữ iod, và cũng không bị kích thích bởi TSH. Tuy nhiên, nồng độ iod tập trung ở các mô này đủ để quan sát được trên hình ảnh học iod phóng xạ cũng như có thể gây ra các biến chứng viêm tuyến nước bọt, viêm dạ dày khi điều trị với iod phóng xạ.
Liều cao iod sẽ ức chế cả hoạt động và sự biểu lộ gene của NIS, gọi là cơ chế tự điều hòa iod (xem sau). Ion Perchlorate (ClO4 – ) cạnh tranh với iod ở kênh NIS; vì thế perchlorate cũng được sử dụng trong điều trị cường giáp.
Ở bờ đỉnh của tế bào tuyến giáp, còn có một kênh vận chuyển iod thứ hai nữa có tên là pendrin, giúp vận chuyển iodide qua mặt phân cách giữa màng tế bào và chất keo, nơi chúng sẽ trở thành cơ chất để tổng hợp hormone tuyến giáp (xem lại Hình 7-6 và 7-7). Các đột biến làm ảnh hưởng đến chức năng của pendrin sẽ gây ra hội chứng Pendred: bướu giáp và mất thính lực mắc phải ở trẻ sơ sinh và trẻ nhỏ.
Thyroid Peroxidase
TPO tham gia vào xúc tác quá trình oxi hóa iod và liên kết iod với tyrosine của TG. Sự biểu lộ gene TPO được kích thích bởi TSH
Iod hóa TG
Sự bắt cặp giữa các thành phần iodotyrosyl ở TG
Sự bắt cặp này cũng được xúc tác bởi enzyme TPO. Tại phân tử TG, hai phân tử diiodotyrosine (DIT) liên kết với nhau tạo thành T4, và hai phân tử monoiodotyrosine (MIT) và DIT liên kết với nhau tạo thành T3. Các thuốc thuộc nhóm thiocarbamide như methimazole, carbimazole và propylthiouracil (PTU), là các chất ức chế cạnh tranh với TPO. Từ đó giúp ức chế quá trình tổng hợp hormone tuyến giáp, đóng vai trò quan trọng trong điều trị cường giáp.
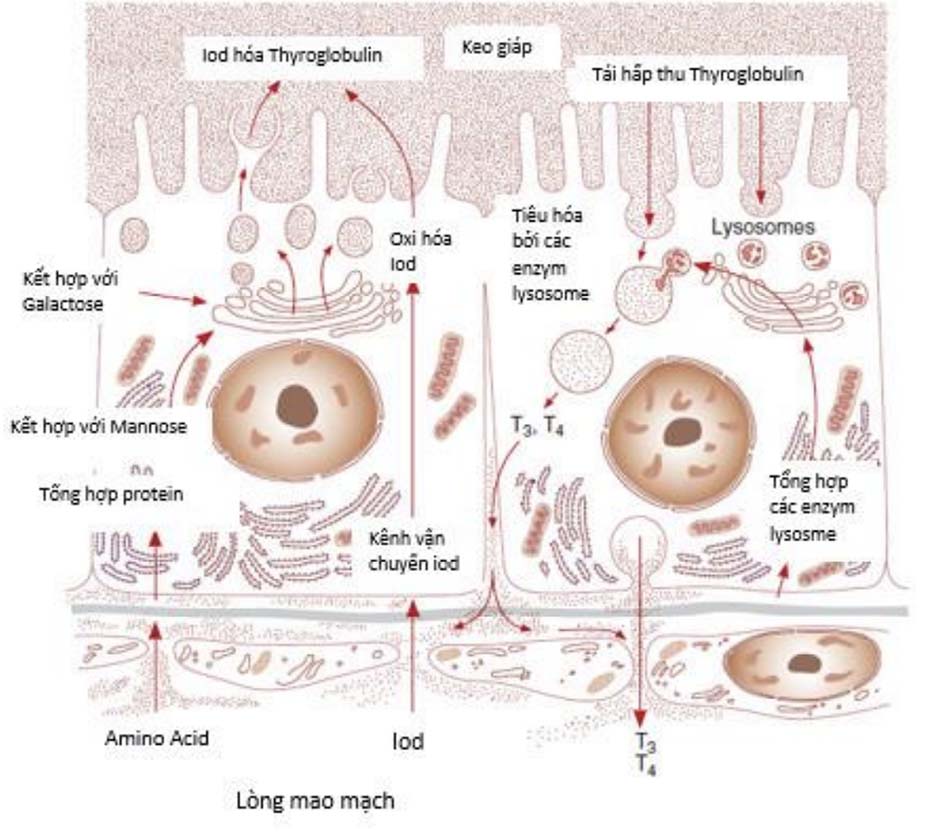
Sự phân giải Thyroglobulin và sự bài tiết hormone tuyến giáp
Quá trình phân giải và bài tiết TG trong quá trình tổng hợp hormone tuyến giáp được minh họa trong Hình 7-7. Ở bờ đỉnh của tế bào tuyến giáp, chất keo giáp được đóng gói trong các túi vận chuyển rồi được đưa vào bên trong tế bào bằng hình thức ẩm bào. Các lysosome có chứa các enzyme phân giải protein sẽ đến hòa màng với các túi chứa chất keo này. Từ đó phóng thích ra T4 và T3 ở dạng có hoạt tính sinh học đi vào tuần hoàn; còn DIT và MIT và iodide được giữ lại tái sử dụng. Sự bài tiết hormone tuyến giáp được kích thích bởi TSH và ức chế khi có quá nhiều iodide (xem sau) và lithium. Phân tử TG nguyên vẹn bình thường cũng được giải phóng khỏi tế bào tuyến giáp và lưu hành trong máu. Nồng độ TG huyết thanh tăng rõ rệt trong một số bệnh lý tuyến giáp như viêm giáp, bướu giáp nhân và bệnh Graves. Vì TG cũng được tổng hợp bởi hầu hết các bệnh lý ác tính phát sinh từ tế bào biểu mô tuyến giáp như ung thư tuyến giáp dạng nang hay ung thư tuyến giáp dạng nhú, nên nó có vai trò như một marker chỉ điểm khối u.
Quá trình loại bỏ iod ở bên trong tuyến giáp
Hầu hết iodide được giải phóng sẽ được tái sử dụng cho quá trình tổng hợp hormone, và chỉ có một lượng nhỏ bình thường sẽ được “rò rỉ” ra khỏi tuyến giáp vào máu (xem Hình 7-10). Enzyme 5’-deiodinase giúp chuyển đổi T4 thành T3 ở các mô ngoại vi cũng hiện diện ở tuyến giáp. Khi có sự thiếu hụt iodide và trong các bệnh lý gây cường giáp, hoạt tính của enzyme này sẽ tăng lên giúp bài tiết nhiều T3 hơn từ tuyến giáp, tăng hiệu quả chuyển hóa trong quá trình tổng hợp hormone.
CÁC BẤT THƯỜNG TRONG TỔNG HỢP VÀ GIẢI PHÓNG HORMONE TUYẾN GIÁP
Thiếu hụt iod trong khẩu phần ăn và các khiếm khuyết về mặt di truyền
Chế độ ăn rất ít iod và các khiếm khuyết di truyền ở các gen có vai trò mã hóa những protein cần thiết trong quá trình sinh tổng hợp hormone tuyến giáp (gây rối loạn tổng hợp hormone tuyến giáp) đều gây tổng hợp không hiệu quả. Để đáp ứng với tình trạng này, tuyến giáp sẽ tăng tỉ lệ MIT-DIT trong TG cũng như tăng tỉ lệ bài tiết T3 so với T4. Trục hạ đồi – tuyến yên – tuyến giáp cũng sẽ đáp ứng bằng cách tăng tiết TRH, từ đó tăng tiết TSH. Vì vậy, những bệnh nhân có tình trạng trên sẽ biểu hiện tình trạng phì đại tuyến giáp (bướu cổ), có thể có hiệu quả để bù trừ lại sự thiếu hụt kể trên; nhưng nếu không thì có thể tiến triển đến suy giáp. Trẻ sơ sinh và trẻ nhỏ bị ảnh hưởng có thể phải gánh chịu những hậu quả vĩnh viễn từ việc thiếu hụt hormone tuyến giáp trên sự phát triển của chúng, gây ra bệnh đần (cretinism).
Các tác động của thừa iod trên sinh tổng hợp Hormone
Mặc dù iod đóng vai trò thiết yếu trong sự tổng hợp hormone tuyến giáp, nhưng khi thừa iod cũng sẽ ức chế ba bước trong quá trình tổng hợp này: bắt giữ iod, iod hóa TG (hiệu ứng WolffChaikoff), và sự giải phóng hormone tuyến giáp. Các tác động ức chế này chỉ thoáng qua, thường tuyến giáp sẽ thoát khỏi hiệu ứng ức chế này sau 10 – 14 ngày nếu thừa iod. Nhờ vào cơ chế điều hòa tự động này mà iod giúp “cô lập” chức năng sinh lý của tuyến giáp trước những biến đổi về lượng iod nhập trong thời gian ngắn.
Những tác động của sự dư thừa iod cũng thường thấy trên lâm sàng, thỉnh thoảng có thể gây ra rối loạn chức năng tuyến giáp do iod. Nếu tuyến giáp bị tác động bởi tình trạng viêm giáp tự miễn hoặc một số rối loạn di truyền trong tổng hợp hormone thì chúng không có khả năng thoát khỏi hiệu ứng ức chế nói trên gây ra bởi iod trong thời gian dài, từ đó có thể dẫn đến suy giáp. Ngược lại, lượng iod nhập vào có thể gây cường giáp (hiệu ứng Jod-Basedow) ở một số bệnh nhân có bướu giáp đa nhân hay bệnh Graves tiềm ẩn, và hiếm khi xuất hiện ở người bình thường. Các hiệu ứng ức chế của iodide ở một số liều dược lý đã giúp nó trở thành một phương pháp điều trị hiệu quả trong kiểm soát tình trạng cường giáp trong thời gian ngắn, như trước phẫu thuật. Iodide cũng giúp ngăn chặn sự phơi nhiễm của tuyến giáp với phóng xạ ở những người tiếp xúc với môi trường có iod phóng xạ, chẳng hạn như sau thảm họa hạt nhân
VẬN CHUYỂN HORMONE TUYẾN GIÁP
Cả hai hormone tuyến giáp lưu hành trong máu chủ yếu gắn kết với các protein; chỉ có khoảng 0,04% T4 và 0,4% T3 ở dạng không gắn kết hay tự do (Xem Hình 7-11). Có 3 loại protein vận chuyển chính của hormone tuyến giáp: globulin gắn kết với thyroxine (TBG); transthyretin, còn gọi là prealbumin gắn kết với thyroxine (TBPA), và albumin (Hình 7-12). Nhờ các protein này giúp hormone tuyến giáp phần lớn lưu hành ở dạng không hoạt động, đảm bảo thời gian bán hủy ổn định khoảng 7 ngày trong huyết tương và sự phân bố đồng đều hormone tuyến giáp đến các mô đáp ứng
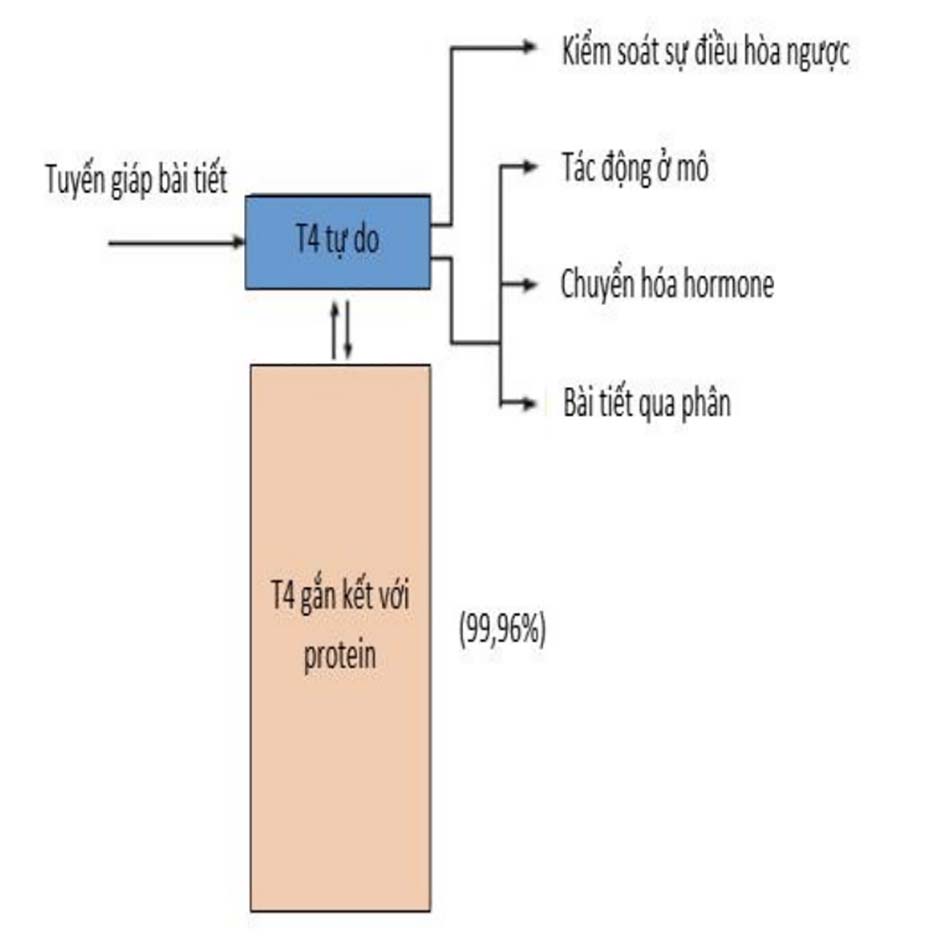
Globulin gắn kết Thyroxine (TBG)
Là glycoprotein có nguồn gốc từ gan, mỗi phân tử TBG có một vị trí gắn cho T4 hoặc T3, nồng độ bình thường trong huyết thanh từ 15 – 30 mcg/mL (280-560 nmol/L), nhờ có ái lực cao với T4 và T3 nên TBG vận chuyển đến 70% lượng hormone tuyến giáp lưu hành trong máu. • Trong trường hợp có thai, điều trị với estrogen sẽ làm tăng phần acid sialic trong phân tử TBG, từ đó làm giảm thanh thải TBG, làm tăng nồng độ chất này trong huyết thanh. Khi nồng độ TBG tăng sẽ làm tăng nồng độ T4 và T3 toàn phần, nhưng nồng độ hormone ở dạng tự do trong giới hạn bình thường nên bệnh nhân vẫn ở trạng thái bình giáp. Ngược lại, sự thanh thải TBG tăng trong hội chứng thận hư, mất protein qua đường tiêu hóa hay do các bệnh lý hệ thống nặng do bị phân cắt bởi enzyme leukocyte protease và do giảm ái lực của TBG với hormone tuyến giáp. Từ đó làm giảm nồng độ T3, T4 toàn phần (xem Bảng 7-1). Nồng độ TBG cũng giảm trong nhiễm độc giáp mãn, cường vỏ thượng thận và bệnh to đầu chi. Một số thuốc có thể làm giảm (androgenic steroid, glucocorticoid) hay tăng (estrogen, 5- fluourouracil) nồng độ TBG huyết tương. Một số loại thuốc khác như salicylates, phenytoin liều cao và furosemide đường TM có thể gắn kết với TBG, thay thế vị trí của T4 và T3. Trong trường hợp này, trục hạ đồi – tuyến yên – tuyến giáp (sẽ được bàn luận sau) giúp duy trì nồng độ hormone tự do bằng cách giảm nồng độ hormone tuyến giáp toàn phần trong huyết thanh. Tương tự như vậy, do sự kích thích heparin từ lipoprotein lipase sẽ giải phóng ra các acid béo tự do giành lấy vị trí của T3, T4 ở TBG. In vivo, sẽ làm giảm nồng độ hormone toàn phần tuyến giáp. Trong khi đó, in vitro, thì heparin làm tăng nồng độ T4 và T3 tự do.
Transthyretin (Prealbumin gắn kết với Thyroxine)
Transthyretin, gắn kết với khoảng 10% T4 lưu hành trong máu, ái lực của nó với T4 gấp 10 lần so với T3. Sự phân ly của Transthyretin với T3 và T4 nhanh chóng, nên nó cung cấp nguồn T4 sẵn có nhanh chóng cho mô khi cần. Một số bệnh lý tăng sản xuất transthyretin lạc chỗ: u tụy, u gan sẽ gây bình giáp nhưng tăng hormone tuyến giáp trong máu.
Albumin
Albumin gắn kết với T4 và T3 với ái lực thấp hơn so với transthyretin nhưng do nồng độ albumin trong huyết tương cao nên giúp vận chuyển khoảng 15% lượng T4 và T3 lưu hành. Hormone tuyến giáp sẽ phân ly nhanh chóng ra khỏi albumin khi cần nên giúp nó trở thành một nguồn cung cấp hormone tự do cho mô. Các bệnh lý làm giảm albumin máu như xơ gan, hội chứng thận hư thường làm giảm T3 và T4 toàn phần nhưng nồng độ hormone ở dạng tự do thì trong giới hạn bình thường.

BẢNG 7-1: Các nguyên nhân gây bất thường nồng độ Thyroxine huyết thanh ở một số bệnh nhân biểu hiện bình giáp
| Tình trạng bình giáp có tăng hormone giáp trong máu
↑ gắn kết protein huyết tương:
↓ chuyển hóa T4 sang T3:
|
| Tình trạng bình giáp có giảm hormone giáp trong máu
↓ gắn kết glubulin với thyroxine
Bệnh hệ thống. Thuốc.
|
CHUYỂN HÓA HORMONE TUYẾN GIÁP
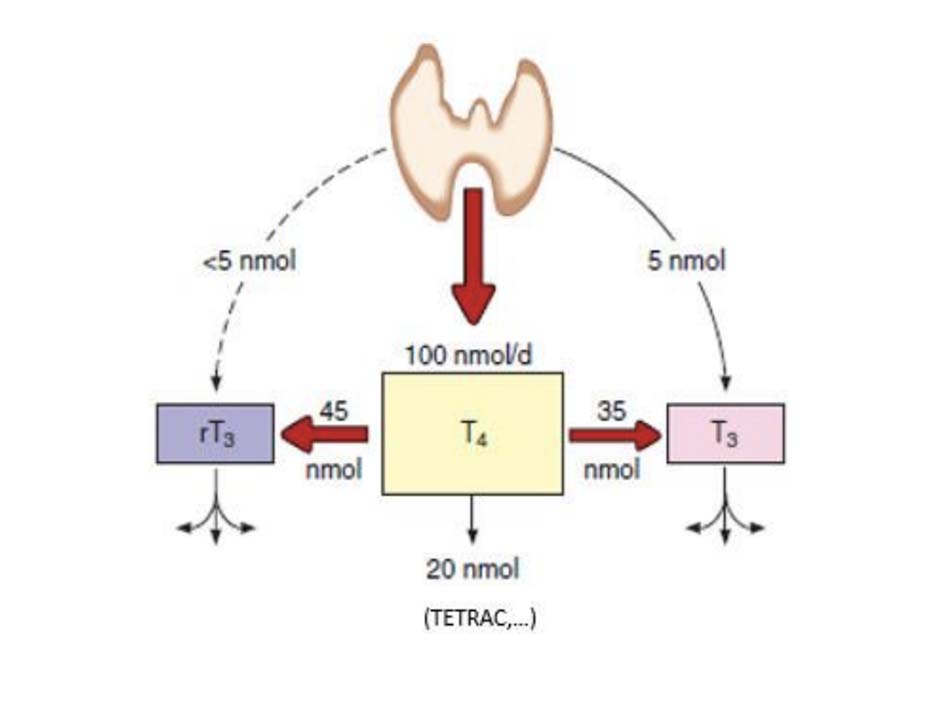
Tuyến giáp bình thường bài tiết khoảng 100 nmol T4 và chỉ 5 nmol T3 mỗi ngày; ít hơn 5 nmol dạng không hoạt tính của T3 (rT3) (Hình 7-13). Hầu hết T3 có mặt trong huyết tương có nguồn gốc từ sự loại bỏ một iod ở vị trí 5’ của T4 tại mô (ngoài tuyến giáp), chủ yếu ở gan, thận và cơ xương (Bảng 7-2). Có ba loại enzyme deiodinase xúc tác tham gia vào các phản ứng khác nhau ở từng mô, tóm tắt dưới Bảng 7-2.
- Type 1 5’-deiodinase là dạng nhiều nhất, chủ yếu ở gan và thận, và một ít ở tuyến giáp, xương, cơ tim và các mô khác. Vai trò chính của enzyme này là tăng biến đổi cung cấp T3 vào tuần hoàn. Enzyme này bị ức chế bởi thuốc kháng giáp nhóm thionamide như PTU nhưng không bị ức chế bởi methimazole. Enzyme còn bị ức chế bởi amiodarone và thuốc cản quang có chứa iod.
- Type 2 5’-deiodinase chủ yếu có ở não và tuyến yên, giúp duy trì nồng độ T3 nội bào trong hệ thần kinh trung ương. Enzyme này rất nhạy cảm với nồng độ T4 lưu hành, vì thế nếu T4 lưu hành thấp sẽ làm tăng nồng độ enzyme này ở não và ở tuyến yên, giúp duy trì nồng độ T3 nội bào và chức năng của các tế bào thần kinh. Enzyme này có vai trò đệm ở vùng hạ đồi và tuyến yên khi có sự thay đổi T4 lưu hành trong máu.
- Type 3 5’-deiodinasae có ở màng nuôi của nhau thai và các tế bào thần kinh đệm của hệ thần kinh trung ương, có vai trò bất hoạt T4 bằng cách chuyển T4 thành rT3 và bất hoạt T3 bằng cách chuyển T3 thành 3,3’ T2. Enzyme này tăng trong cường giáp và giảm trong suy giáp, giúp bảo vệ thai nhi trước tình trạng thừa hay thiếu T4. Cũng chính enzyme này giúp giải thích một phần vì sao phụ nữ mang thai có suy giáp thì cần tăng liều hormone T4 so với bình thường. Nhìn chung, các enzyme này giúp điều hòa hoạt động của hormone tuyến giáp ở từng tế bào và từng mô riêng lẻ, giúp cơ quan thích nghi với sự thay đổi của môi trường và giúp đảm bảo sự phát triển bình thường ở giai đoạn bào thai. Có khoảng 80% T4 được loại bỏ iod để tạo thành 35% T3 và 45% rT3 (Hình 7- 13). Phần còn lại chủ yếu được bất hoạt bởi phản ứng glucuronid hóa ở gan và được bài tiết qua mật hay phản ứng lưu huỳnh hóa ở gan và thận. Cuối cùng, có khoảng 10% T4 ở bên ngoài tuyến giáp được đào thải ra ngoài mỗi ngày, thời gian bán hủy của T4 trong huyết tương là khoảng 7 ngày. Vì ái lực của T3 với các protein trong huyết tương thấp hơn nên thời gian bán hủy T3 khoảng 1 ngày. Tổng lượng rT3 trong cơ thể gần bằng với T3, nhưng rT3 được chuyển hóa nhanh hơn, thời gian bán hủy chỉ khoảng 0,2 ngày.
| Bảng 7.2: Các loại Enzyme Lodothyronine Deiodinase và đặc điểm của chúng. | |||
| Loại Enzyme | D1 | D2 | D3 |
| Cơ chất | rT3 > T4 > T3 | T4 > rT3 | T3 > T4 |
| Phân bố ở mô | Gan, thận, tuyến giáp | Não, tuyến yên, cơ xương | Não, nhau thai, mô của thai nhi |
| Chức năng | Tổng hợp T3 huyết tương | Tổng hợp T3 tại chỗ và huyết tương | Thoái hóa T3 |
| Ức chế PTU (IC50, mcM) | 5 | > 1000 | > 1000 |
| Suy giáp | Giảm | Tăng | Giảm |
| Cường giáp | Tăng | Giảm | Tăng |
ĐIỀU HÒA CHỨC NĂNG VÀ HOẠT ĐỘNG CỦA HORMONE TUYẾN GIÁP
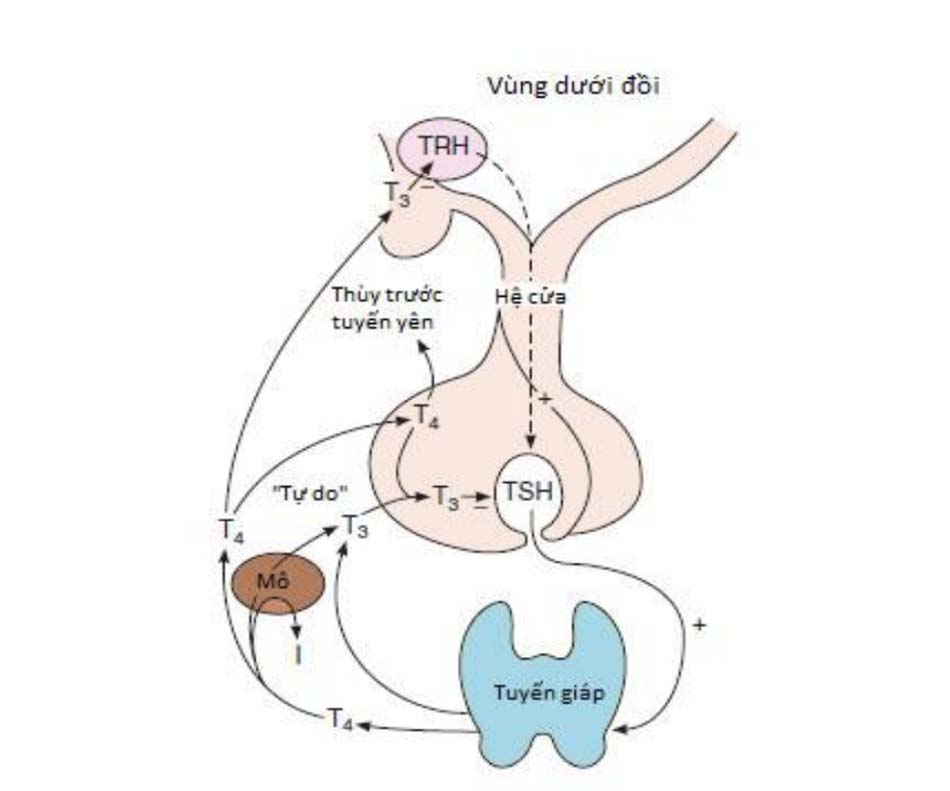
Hormone giải phóng thyrotropin (TRH)
TRH, là tripeptide được tổng hợp bởi các neuron ở nhân trên thị và nhân trên não thất của vùng hạ đồi. TRH được dự trữ ở lồi giữa của vùng hạ đồi, sau đó được vận chuyển qua hệ cửa hạ đồi – tuyến yên đến thùy trước tuyến yên, giúp điều hòa sự tổng hợp và bài tiết TSH. Ở thùy trước tuyến yên, TRH sẽ gắn với thụ thể màng đặc hiệu ở các tế bào tiết TSH và prolactin, kích thích tổng hợp và giải phóng các hormone tương ứng. Sự bài tiết TSH được kích thích bởi TRH theo xung động (pulsatile) (Xem Hình 7- 17), với trung bình mỗi xung là 0,6 mU/L mỗi 2 giờ. TSH còn được giải phóng theo nhịp ngày đêm, với đỉnh tiết vào khoảng giữa đêm đến 4 giờ sáng, giống với mô hình điều hòa sự tổng hợp TRH ở vùng hạ đồi. Các hormone tuyến giáp có cơ chế feedback âm lên sự tổng hợp của TSH ở tuyến yên, ví dụ ở bệnh nhân cường giáp thì cả xung tiết TSH và nhịp ngày đêm đều bị giảm. Nhiệt độ lạnh cũng kích thích bài tiết TRH và TSH. Một số loại hormone và thuốc như vasopressin, các chất đồng vận α-adrenergic cũng kích thích tổng hợp và giải phóng TRH. Leptin cũng tham gia điều hòa sự bài tiết TRH và TSH, nên có thể thấy nồng độ TSH tăng (có thể đảo ngược) ở một số bệnh nhân béo phì.
TRH còn được tìm thấy ở tế bào đảo tụy, ống tiêu hóa, nhau thai, tim, tiền liệt tuyến, tinh hoàn và buồng trứng. Tuy nhiên, sự tổng hợp TRH ở các mô ngoại biên này không bị ức chế bởi nồng độ T3; vai trò của TRH ở các cơ quan này cũng chưa được biết rõ.
Thyrotropin (Hormone kích thích tuyến giáp – TSH)
TSH kiểm soát sự tăng trưởng và tổng hợp hormone bằng cách gắn vào thụ thể TSH đặc hiệu trên màng đáy của các tế bào tuyến giáp. Rối loạn liên quan đến thụ thể TSH thường gặp nhất gây cường giáp là bệnh Graves, trong đó các tự kháng thể sẽ gắn và kích thích thụ thể TSH.
Các tác động của TSH trên tế bào tuyến giáp
A. Thay đổi trên hình thái của tế bào tuyến giáp
TSH làm biến đổi nhanh chóng các giả túc ở ranh giới của tế bào nang – chất keo, làm tăng hấp thu TG nhiều hơn. Lượng keo giáp giảm dần khi các giọt keo ở nội bào được hình thành, kích thích tăng tổng hợp lysosome, tăng ly giải TG và giải phóng hormone tuyến giáp.
B. Sự tăng trưởng của tế bào.
Từng tế bào tuyến giáp sẽ tăng phát triển về kích thước, hệ thống mạch máu theo thời gian, thậm chí có thể gây phì đại tuyến giáp hay bướu cổ.
C. Chuyển hóa iod
TSH kích thích tất cả các giai đoạn trong chuyển hóa iod. Hiệu ứng của TSH trên hàm lượng iod trong tế bào tuyến giáp diễn ra theo hai pha: ban đầu, giảm (dòng nhập iod) do sự gia tăng ly giải TG và phóng thích hormone, rò rỉ iod ra khỏi tuyến giáp một cách nhanh chóng; và sau đó khoảng vài giờ, sự bắt giữ của iod sẽ gia tăng.
D. Các tác động khác của TSH
TSH kích thích tuyến giáp tăng nhập glucose, tăng tiêu thụ oxy và oxi hóa glucose – các hiệu ứng này giúp tăng phát hiện tình trạng di căn của ung thư tuyến giáp bằng FDG PET scanning.
Điều hòa sự bài tiết TSH của tuyến yên
Có hai yếu tố chính tham gia điều hòa sự tổng hợp và bài tiết TSH: (1) nồng độ T3 bên trong các tế bào định hướng tiết hormone giáp, giúp điều hòa sự biểu lộ mRNA, dịch mã TSH và giải phóng hormone, và (2) TRH, kiểm soát sự glycosyl hóa hậu dịch mã và cũng kiểm soát sự giải phóng của TSH. Sự tổng hợp và bài tiết TSH bị ức chế bởi nồng độ cao T3 và T4 trong huyết thanh (nhiễm độc giáp) và kích thích bởi nồng độ thấp T3 và T4 (suy giáp). Nhiễm độc giáp có thể gây giảm nồng độ TSH dưới ngưỡng phát hiện được của xét nghiệm và sự phục hồi khả năng tiết của TSH cần mất vài tuần đến vài tháng sau khi đã khôi phục được nồng độ hormone tuyến giáp bình thường. Một số hormone và thuốc có khả năng ức chế sự bài tiết của TSH như somatostatin, dopamine, thuốc đồng vận dopamine như bromocriptine, nồng độ cao glucocorticoid. Các bệnh lý hệ thống nặng cũng ức chế sự bài tiết TSH, và có thể gây ra sự tăng tiết TSH trở lại khi bệnh nhân hồi phục.
Các yếu tố kích thích và điều hòa bài tiết hormone tuyến giáp khác
Các yếu tố tự tiết như prostaglandin, cytokine giúp điều hòa sự tăng trưởng và tổng hợp hormone của tế bào tuyến giáp. Một số bệnh lý có liên quan đến các yếu tố này như: bướu giáp nhân lành tính. Vùng nang giáp được cấp máu bởi một hệ thống mao mạch dồi dào, nên cũng được điều hòa bởi các sợi thần kinh noradrenergic từ hạch cổ trên và các sợi thần kinh tiết acetylcholine esterase từ dây X và hạch tuyến giáp. Tuy nhiên, vai trò của chúng vẫn chưa được hiểu rõ.
TÁC ĐỘNG SINH LÝ CỦA CÁC HORMONE TUYẾN GIÁP
Tác động trên sự tăng trưởng của thai nhi
Nồng độ iod ở tuyến giáp và TSH ở tuyến yên bắt đầu xuất hiện ở thời kỳ bào thai của người khoảng tuần thứ 11 của thai kỳ. Do ở thời kỳ này, nồng độ enzyme type 3 5’-deiodinase cao nên hầu hết T3 và T4 đều bị bất hoạt, chỉ có một lượng rất nhỏ hormone này ở dạng tự do trong tuần hoàn nhau thai. Tuy nhiên, lượng rất nhỏ được cung cấp từ mẹ này lại đóng vai trò quan trọng trong giai đoạn sớm của sự phát triển não của bào thai. Sau tuần thứ 15 – 18 của thai kỳ thì thai nhi đã có thể tự tiết được hầu hết hormone tuyến giáp. Suy giáp di truyền gây ra bệnh đần (cretinism), các đặc điểm của bệnh lý này bao gồm: chậm phát triển thần kinh và còi cọc.
Tác động trên nhu cầu tiêu thụ oxy, sinh nhiệt và tạo các gốc tự do
T3 làm tăng nhu cầu tiêu thụ oxy và tăng sinh nhiệt một phần do kích thích bơm Na+ -K+ -ATPase ở tất cả các mô ngoại trừ não, lách và tinh hoàn. Tác động này cũng làm gia tăng chuyển hóa cơ bản (tổng oxy tiêu thụ của cơ thể khi nghỉ ngơi), giải thích cho hiện tượng sợ nóng trong cường giáp và sợ lạnh trong suy giáp. Các hormone tuyến giáp cũng kích thích tạo ty thể, tăng khả năng oxi hóa của tế bào.
Tác động trên tim mạch
T3 làm tăng chức năng tâm thu của tim. Ở tế bào cơ tim, T3 thay đổi sự biểu lộ của dạng khác nhau của các gen Na+ -K+ – ATPase, làm tăng biểu lộ các thụ thể αadrenergic. Các hormone tuyến giáp làm giảm kháng lực mạch máu ngoại biên và tăng thể tích nội mạch, làm gia tăng cung lượng tim liên quan đến hoạt động hormone tuyến giáp. T3 cũng làm tăng sự khử cực và tái cực của nút xoang, làm tăng nhịp tim. Tóm lại, các hormone tuyến giáp có tác động inotrop và chronotrop (+), cùng với tăng sự tác động của hoạt tính adrenergic làm tăng lực co bóp và tăng nhịp tim, đặc biệt ở bệnh nhân cường giáp, và ngược lại ở bệnh nhân suy giáp.
Tác động giao cảm
Hormone tuyến giáp làm gia tăng số lượng thụ thể β-adrenergic ở tim và cơ xương, mô mỡ, các tế bào lympho. Nó cũng khuếch đại tác động của catecholamine ở vùng hậu thụ thể. Các biểu hiện lâm sàng của nhiễm độc giáp phản ánh sự tăng nhạy cảm với catecholamine. Nhờ vậy, điều trị với các thuốc ức chế β-adrenergic giúp kiểm soát tốt các triệu chứng giao cảm khi có tình trạng nhiễm độc giáp.
Tác động trên phổi
Hormone tuyến giáp giúp duy trì khả năng đáp ứng của thông khí với tình trạng giảm oxy hay tăng Co2 máu của trung tâm hô hấp ở não. Ở bệnh nhân suy giáp nặng, có thể xuất hiện giảm thông khí. Chức năng của cơ hô hấp cũng được điều hòa bởi hormone tuyến giáp, và có thể bị suy yếu trong cường giáp, gây tình trạng khó thở.
Các tác động trên hệ tạo máu
Tăng nhu cầu tiêu thụ O2 trong cường giáp làm tăng tổng hợp erythropoietin và tăng sản sinh hồng cầu. Tuy nhiên, thể tích máu thường không tăng do hiện tượng pha loãng máu và tăng thời gian chuyển hóa của hồng cầu. Hormone tuyến giáp cũng làm tăng hàm lượng 2,3- DPG trong các tế bào hồng cầu, cho phép tăng khả năng phân ly của O2 khỏi hemoglobin từ đó tăng trao O2 cho mô. Suy giáp gây tác động ngược lại.
Tác động trên hệ tiêu hóa
Hormone tuyến giáp làm gia tăng nhu động ruột, từ đó có thể gây tiêu chảy ở bệnh nhân cường giáp. Trái lại, có thể gây táo bón ở bệnh nhân suy giáp (Lời dịch giả: giải thích thêm là do sự tương tác với đám rối thần kinh nội tại ở ống tiêu hóa và sự bài tiết của các hormone địa phương).
Tác động trên xương
Hormone tuyến giáp kích thích chu chuyển xương, tăng sự thoái khoáng xương, và ở tăng nhẹ sự hình thành xương. Vì thế, cường giáp có thể gây tăng calci niệu, có thể có tăng calci máu nhưng ít gặp hơn. Những bệnh nhân nhiễm độc giáp mạn tính có thể gây thoái khoáng xương đáng kể trên lâm sàng và tăng nguy cơ gãy xương.
Tác động trên thần kinh – cơ
Ở bệnh nhân cường giáp có hiện tượng tăng chuyển hóa protein và tăng mất protein ở cơ xương, từ đó có thể gây yếu cơ gốc chi. Trong cường giáp có hiện tượng tăng tốc độ co và giãn của cơ, biểu hiện với tình trạng tăng phản xạ. Run nhẹ ở đầu chi ở bàn tay cũng thường gặp. Ở bệnh nhân cường giáp, có thể biểu hiện tình trạng lo lắng, tăng kích thích trong khi đó nhược giáp thường biểu hiện trầm cảm.
Tác động trên chuyển hóa lipid và carbohydrate
Cường giáp làm tăng tân tạo đường và tăng ly giải glycogen, đồng thời cũng tăng hấp thu glucose ở ruột, giảm nhạy cảm với insulin. Vì vậy, kiểm soát đường huyết khó khăn hơn ở bệnh nhân đái tháo đường có cường giáp. Hormone tuyến giáp cũng tăng kích thích tổng hợp và thoái giáng cholesterol, chủ yếu do tăng số lượng thụ thể LDL và tăng thanh thải LDL. Vì vậy, bệnh nhân suy giáp thường biểu hiện với tình trạng tăng cholesterol toàn phần và tăng LDL cholesterol máu. Ngược lại, ở bệnh nhân cường giáp có hiện tượng tăng ly giải mỡ, giải phóng nhiều acid béo và glycerol vào huyết tương.
Tác động trên hệ nội tiết
Hormone tuyến giáp làm thay đổi khả năng tổng hợp, đáp ứng và thanh thải một số hormone. Ở trẻ em có suy giáp, cũng làm suy yếu giải phóng hormone tăng trưởng (GH) làm chậm phát triển chiều cao. Bệnh nhân suy giáp có thể biểu hiện dậy thì muộn do giảm phóng thích GnRH. Ngược lại, suy giáp nguyên phát có thể gây dậy thì sớm, do nồng độ TSH tăng cao có tác động lên thụ thể của gonadotropin. Ở người trưởng thành, tình trạng suy giáp có thể làm tăng prolactin máu ở một số phụ nữ. Suy giáp cũng thường gây rong kinh và chu kỳ không rụng trứng, nặng hơn có thể gây vô sinh. Ở bệnh nhân suy giáp có hiện tượng giảm đáp ứng của trục hạ đồi – tuyến yên – vỏ thượng thận với stress do giảm thanh thải cortisol. Ở bệnh nhân cường giáp, có hiện tượng gia tăng thơm hóa androgen để tạo estrogen và tăng nồng độ globulin gắn hormone sinh dục, gây bệnh vú to và gia tăng nồng độ testosterone ở nam giới. Cường giáp cũng làm giảm suy yếu GnRH, khả năng điều hòa sự rụng trứng và điều hòa kinh nguyệt, từ đó gây vô sinh và vô kinh. Tất cả các rối loạn nội tiết gây ra bởi rối loạn chức năng tuyến giáp sẽ được phục hồi sau khi bệnh nhân được điều trị bình giáp trở lại.
NHỮNG THAY ĐỔI SINH LÝ ẢNH HƯỞNG CHỨC NĂNG TUYẾN GIÁP
CHỨC NĂNG TUYẾN GIÁP THỜI KỲ BÀO THAI
Giai đoạn đầu, sự phát triển của bào thai (đặc biệt là thần kinh) phụ thuộc vào hormone tuyến giáp từ tuần hoàn mẹ. Vào khoảng tuần thứ 11 của thai kỳ, khi hệ mạch cửa tuyến yên phát triển thì bắt đầu đo được nồng độ TSH và TRH. Cũng trong thời gian này, tuyến giáp của bào thai bắt đầu tham gia bắt iod. Hormone tuyến giáp ở bào thai bắt đầu được chế tiết từ tuần thứ 18-20 của thai kỳ. TSH tăng nhanh chóng và đạt đỉnh khoảng tuần 24-28, nồng độ T4 tăng cao nhất vào khoảng tuần thứ 35-40 của thai kỳ. Trong khi đó, nồng độ T3 vẫn duy trì ở mức thấp trong suốt thai kỳ do T4 ưu thế chuyển thành rT3 bởi sự hiện diện của enzyme 5’-deiodinase type 3 trong thời gian này. Sau khi sanh, có sự kích thích TSH tăng lên một cách đột ngột do thai tiếp xúc với môi trường lạnh ở bên ngoài tử cung, từ đó làm T4, T3 tăng cao, rT3 lúc này sụt giảm. Xu hướng này tương đối ổn định trong tháng đầu tiên của trẻ.
CHỨC NĂNG TUYẾN GIÁP KHI MANG THAI
Có nhiều thay đổi trong các thông số liên quan đến hormone tuyến giáp trong quá trình mang thai. Có sự tăng đào thải iode qua nước tiểu, vì thế ở những vùng chế độ ăn ít iod có thể gây ra bướu cổ ở mẹ, hoặc thậm chí có thể gây suy giáp. Trong quá trình mang thai, có sự gia tăng nồng độ TBG do tăng glycosyl hóa TBG ở gan thúc đẩy bởi estrogen, từ đó làm kéo dài thời gian đào thải chúng. Hệ quả là làm gia tăng nồng độ T4 toàn phần trong huyết tương, T3 cũng tăng nhưng ít hơn. Bên cạnh đó, trong thai kỳ cũng có sự gia tăng đáng kể nồng độ hCG (hormone này cũng có hoạt tính đồng vận thụ thể TSH nhưng yếu hơn), cũng góp phần làm tăng kích thước tuyến giáp. Nồng độ hCG trong máu mẹ đạt đỉnh vào khoảng tuần 12 của thai kỳ, làm gia tăng tạm thời nồng độ T4 tự do trong huyết thanh ở mức vừa phải và do đó feedback âm làm ức chế gây giảm nhẹ nồng độ TSH. Trong bệnh cảnh có sự gia tăng của nồng độ hCG, như trong bệnh lý nguyên bào nuôi (thai trứng, choriocarcinoma,…) có thể gây cường giáp thật sự. Ở những phụ nữ có triệu chứng buồn nôn dữ dội trong thai kỳ (gọi là nghén), là do sự gia tăng nồng độ hCG trong máu có thể biểu hiện tình trạng nhiễm độc giáp thoáng qua. Như đã nói ở phần trước, enzyme deiodinase type 3 từ nhau thai sẽ làm tăng đào thải T4 trong thai kỳ, chính vì thế khi bổ sung T4 ở những phụ nữ có suy giáp đòi hỏi phải tăng liều cao hơn. Ngoài ra, iod ở mẹ có thể qua được nhau thai, đóng vai trò tối cần thiết trong sự tổng hợp hormone tuyến giáp ở bào thai. Tuy nhiên, nếu bổ sung một lượng lớn iodide cũng có thể ức chế chức năng tuyến giáp ở bào thai (xem lại sinh lý ở phần trước), làm tuyến giáp phì đại đủ gây chuyển dạ tắc nghẽn. Ở phụ nữ mang thai có bệnh lý tuyến giáp tự miễn thì các kháng thể immunoglobulin từ mẹ gây kích thích hoặc ức chế thụ thể TSH có thể qua được nhau thai và gây rối loạn chức năng tuyến giáp ở bào thai. Hơn nữa, các thuốc kháng giáp sử dụng ở mẹ như methimazole và PTU cũng qua được nhau thai, khi sử dụng ở liều cao có thể gây suy giảm chức năng tuyến giáp ở bài thai (xem Chương 16)
SỰ THAY ĐỔI CHỨC NĂNG TUYẾN GIÁP THEO TUỔI GIẢ
Chu chuyển T4 cao nhất ở trẻ nhỏ và giảm dần ở người trưởng thành (sau tuổi dậy thì). Tuần hoàn T4 sau đó ổn định cho đến 60 tuổi, lúc này bắt đầu có sự sụt giảm dần. Vì thế, ở người lớn tuổi tốc độ đào thải T4 có thể giảm đến 50%, nên cần giảm liều điều trị T4 ở những đối tượng này khi có mắc suy giáp.
ẢNH HƯỞNG CỦA BỆNH LÝ CẤP VÀ MÃN TÍNH LÊN CHỨC NĂNG TUYẾN GIÁP (HỘI CHỨNG BÌNH GIÁP DO BỆNH LÝ)
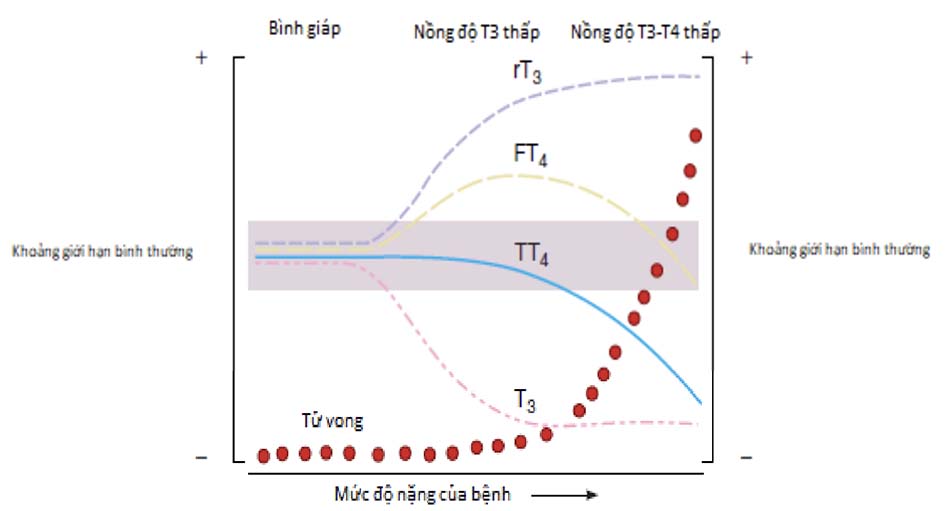
Bệnh lý cấp hay mãn tính đều có ảnh hưởng nhất định đến chức năng tuyến giáp. Tác động sớm nhất và thường gặp nhất là ức chế chuyển T4 thành T3, từ đó giảm nồng độ T3 lưu hành. Cùng với hiện tượng trên là sự gia tăng nồng độ rT3 trong huyết thanh. Những thay đổi trên có thể gặp trong các trường hợp thiếu năng lượng như suy dinh dưỡng, nhịn đói, chán ăn tâm thần và gặp ở các bệnh lý toàn thân cấp hay mãn tính (xem Bảng 7-3). BẢNG 7-3: Những bệnh lý và các yếu tố gây giảm biến đổi T4 hoặc T3.
| 1. Thời kỳ bào thai.
2. Thiếu năng lượng. 3. Bệnh lý của gan. 4. Bệnh lý toàn thân nặng. 5. Một số thuốc: Propylthiouracil Glucocorticoid Propranolol (ảnh hưởng nhẹ) Thuốc cản quang chứa iod (acid iopanoic, ipodate sodium) Amiodarone. 6. Thiếu hụt Selenium. |
Sinh bệnh học của hội chứng T3 thấp này được cho là do các cytokine như yếu tố hoại tử u, được tiết ra từ các tế bào viêm sẽ tham gia ức chế enzyme 5’-deiodinase type 1. Một số thuốc cũng ức chế enzyme này và làm giảm nồng độ T3 huyết thanh như: corticosteroid, amiodarone, thuốc cản quang có chứa iod, PTU, propanolol liều cao. Ban đầu, T3 huyết thanh thấp thường đi kèm với T4 tự do và toàn phần bình thường hay hơi tăng (xem Hình 7- 23). Khi bệnh ngày càng nặng, lúc này có sự sụt giảm cả T4 toàn phần và tự do. Có nhiều nguyên nhân gây ra hiện tượng này tùy thuộc vào bệnh nền. Ví dụ như trong hội chứng thận hư và bệnh gan nặng, nguyên nhân là do giảm nồng độ TBG lưu hành. Nồng độ acid béo tự do trong huyết tương tăng cũng có thể ngăn T4 gắn kết vào TBG, làm tăng nồng độ T4 tự do, từ đó feedback lên vùng hạ đồi và tuyến yên giảm tiết TSH và thành lập một cân bằng mới với nồng độ T4 toàn phần thấp hơn. TSH cũng có thể bị ức chế bởi các cytokine lưu hành ở các bệnh nhân mắc các bệnh lý nặng hay bởi dopamine, corticosteroid dùng để điều trị các bệnh nhân này. Cuối cùng, một trong những cơ chế khác chính là sự gia tăng đào thải T4 khi có bệnh lý. Tất cả những yếu tố kể trên đều có thể góp phần làm giảm nồng độ T4 toàn phần và T4 tự do khi định lượng bằng xét nghiệm miễn dịch (free-hormone immunoassay). Tuy nhiên, nồng độ T4 khi đo bằng phương pháp thẩm tách cân bằng (equilibrium dialysis) được báo cáo rằng bình thường trong hầu hết, tuy nhiên không phải tất cả các trường hợp. Hai câu hỏi lâm sàng đặt ra trong bối cảnh bệnh nhân có bệnh nền đồng thời với rối loạn chức năng tuyến giáp. Một là làm sao để phân biệt được rối loạn là do hội chứng bình giáp do bệnh lý hay là suy giáp thứ phát (từ nguyên nhân trục hạ đồi – tuyến yên); vì trong hai bệnh cảnh này thì T4 và TSH đều giảm. Lúc này, khai thác thêm lâm sàng có thể giúp ích, chẳng hạn tiền sử có bệnh lý tuyến yên hay tuyến giáp đã biết trước đó, chấn thương hay phẫu thuật sọ não, các biểu hiện khác của suy tuyến yên có thể có (tinh hoàn nhỏ ở nam giới). Đôi lúc cần chỉ định thêm một số xét nghiệm bổ sung khác. Như đã nói ở trên, định lượng T4 tự do huyết thanh bằng phương pháp thẩm tách cân bằng có thể cho nồng độ T4 trong giới hạn bình thường ở bệnh nhân bình giáp do bệnh lý. Định lượng nồng độ cortisol cũng có thể giúp ích, vì cortisol thường sẽ bình thường hoặc tăng cao ở những bệnh nhân có bệnh lý toàn thân nặng, vì vậy nếu kết quả là bình thường hoặc tăng thì có vẻ như không phải nguồn gốc bệnh lý từ hạ đồi – tuyến yên. Đôi lúc cần phải chỉ định một số cận lâm sàng hình ảnh học cấp cứu để đánh giá thêm vùng hạ đồi – tuyến yên. Các bất thường về chức năng tuyến giáp này thường trở về bình thường khi bệnh nhân hồi phục. Tuy nhiên, thỉnh thoảng cũng gây hiện tượng tăng TSH hồi ngược thoáng qua (rebound), làm nhầm lẫn với tình trạng suy giáp. Trong trường hợp này, nếu không xuất hiện các dấu hiệu suy giáp rõ thì không nên điều trị bổ sung hormone tuyến giáp mà nên đánh giá lại vài tuần sau khi bệnh nhân hồi phục. Câu hỏi thứ hai là liệu hội chứng bình giáp do bệnh lý có nên được điều trị luôn với hormone tuyến giáp hay không. Thật vậy, ở nhiều bệnh nhân có các bệnh lý nền nặng biểu hiện các triệu chứng liên quan đến suy giáp như hạ thân nhiệt, thay đổi cảm giác, rối loạn thông khí và rối loạn chức năng cơ tim, hạ natri máu. Từ đó dấy lên quan điểm rằng, việc bổ sung hormone tuyến giáp thay thế có thể mang lại lợi ích nhất định. Trái lại, những quan điểm khác cho rằng những thay đổi liên quan đến chức năng tuyến giáp này thực tế là do các cơ chế bù trừ để giảm bớt sự tiêu thụ oxy và dị hóa protein, vậy nếu bổ sung hormone tuyến giáp vào sẽ làm tình hình tệ hơn. Hơn nữa, các thử nghiệm lâm sàng nhỏ và một số thử nghiệm trên mô hình động vật đã thất bại trong việc chứng minh lợi ích của điều trị hormone tuyến giáp trong trường hợp này. Cuối cùng, các guideline hiện hành nhìn chung sẽ tạm không điều trị hormone tuyến giáp thay thế trong trường hợp này, trừ khi có bằng chứng thuyết phục về cả lâm sàng và cận lâm sàng cho thấy có tình trạng suy giáp thực sự.
CÁC XÉT NGHIỆM HORMONE TUYẾN GIÁP TRONG MÁU
Xét nghiệm định lượng nồng độ TSH
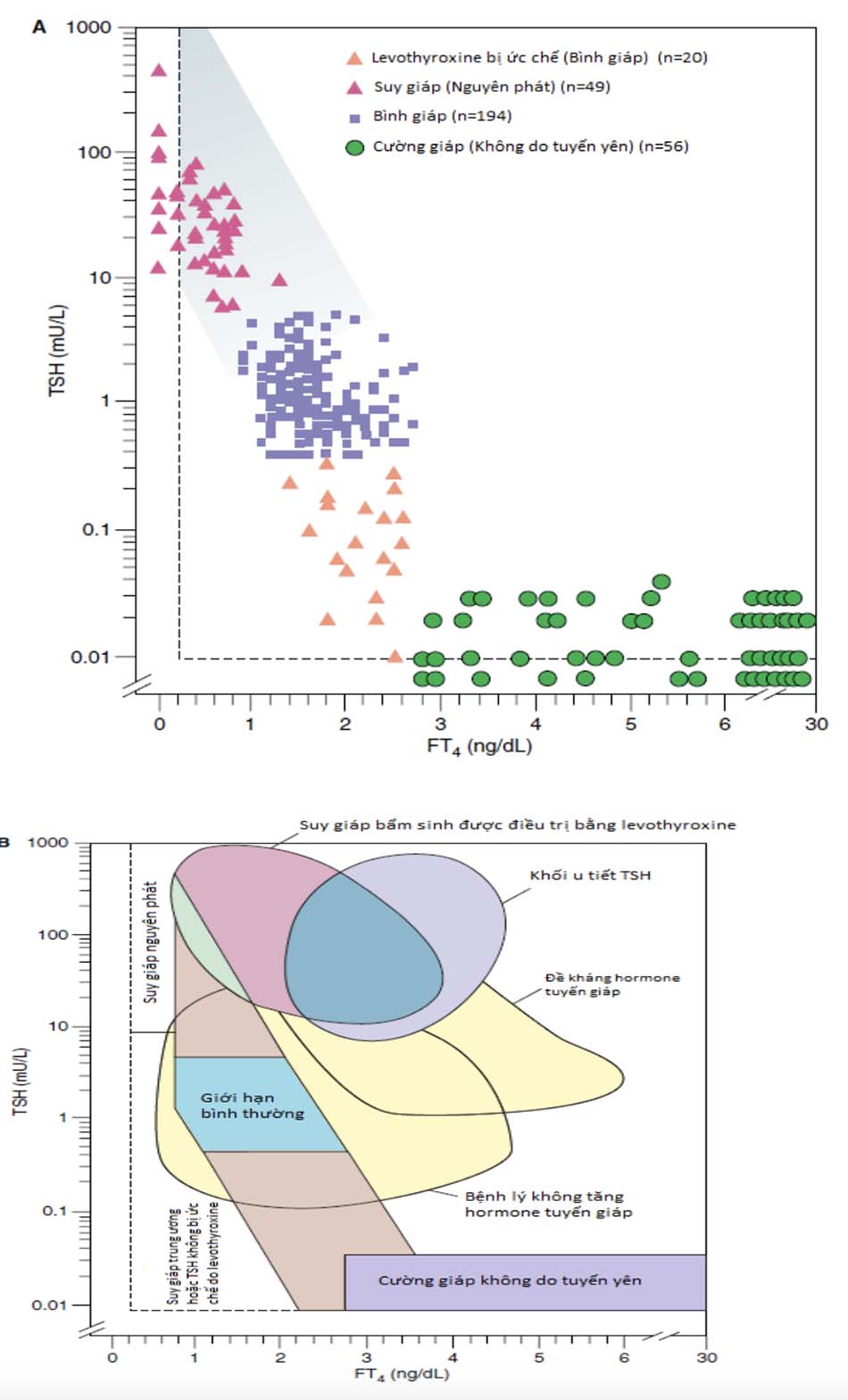
Vì chức năng tuyến giáp bị rối loạn thường xuất phát từ các rối loạn nguyên phát ngay tại tuyến giáp, vì thế định lượng nồng độ TSH trở thành một trong những test được sử dụng rộng rãi để xác định có hay không rối loạn chức năng tuyến giáp. Sự nhạy cảm của trục hạ đồi – tuyến yên – tuyến giáp đảm bảo rằng cả các rối loạn nguyên phát tại tuyến giáp và nhiễm độc giáp (do tuyến giáp hay do hormone giáp ngoại sinh) đều sẽ được phát hiện. Hơn nữa, dù rối loạn chức năng tuyến giáp ở mức độ nhẹ, nồng độ hormone tuyến giáp trong huyết thanh sụt giảm hay tăng như thế nào đó, thì vẫn đảm bảo rằng nằm trong khoảng tham chiếu có thể phát hiện được (chẳng hạn như rối loạn chức năng tuyến giáp nhẹ hoặc thể dưới lâm sàng). Sự tương quan logarit đảo ngược giữa nồng độ TSH huyết thanh và nồng độ T4 tự do ở các tình huống khác nhau được minh họa ở Hình 7-24A và Hình 7-24B. Nhìn chung, có hai phương pháp định lượng TSH (và T4, T3) được sử dụng: phương pháp miễn dịch (IMA) và miễn dịch phóng xạ (RIA). (Đến đây bạn đọc lưu ý đến giải đáp câu hỏi thường gặp trên lâm sàng: vì sao thường sử dụng TSH kết hợp với FT4 trên lâm sàng, mà không phải là các đại lượng khác, hay chỉ đơn độc từng cái, hay khi nào sẽ cần kết hợp nhiều đại lượng). Nếu chỉ sử dụng định lượng TSH đơn độc để chẩn đoán các rối loạn tuyến giáp thì sẽ có nhiều hạn chế. Đầu tiên, chúng ta sẽ bỏ qua các trường hợp suy giáp trung ương (thứ phát từ nguyên nhân ở trục hạ đồi – tuyến yên), chẳng hạn nếu bệnh nhân bị suy giáp do u tuyến yên, thì nồng độ TSH sẽ không tăng cao mà ngược lại còn giảm hay ở mức “bình thường, nhưng không phù hợp”. Chính vì thế, thường kết hợp thêm nồng độ T4 tự do song hành với định lượng TSH để chẩn đoán cũng như loại trừ các bệnh lý chung của tuyến giáp. Một số thuốc cũng ảnh hưởng đến nồng độ TSH, chẳng hạn như corticosteroid liều cao hay dopamine, gây ức chế giải phóng TSH (xem Bảng 7-4). Nhược điểm thứ hai là có nhiều nguyên nhân khác không liên quan đến tuyến giáp cũng gây gia tăng nồng độ TSH trong huyết thanh như được mô tả trong Bảng 7-4.
Xét nghiệm định lượng nồng độ T4 và T3
Nồng độ hormone toàn phần của tuyến giáp trong huyết thanh được sử dụng rộng rãi và đánh giá chính xác hầu hết các bệnh nhân có rối loạn chức năng tuyến giáp thật sự. Tuy nhiên, nhược điểm là có những trường hợp gây dương tính giả và âm tính giả khi có sự thay đổi nồng độ hay ái lực gắn kết của hormone tuyến giáp với protein. Ví dụ, phụ nữ mang thai có sự gia tăng nồng độ TBG do estrogen (xem lại phần trước) gây chẩn đoán nhầm thành cường giáp nếu như chỉ dựa vào định lượng nồng độ T4 toàn phần trong máu. Trái lại, ở bệnh nhân mang thai có suy giáp nguyên phát có thể bị bỏ sót do sự gia tăng TBG nói trên làm T4 toàn phần tăng lên trở về giới hạn “bình thường”. Vì vậy, kết hợp T4 toàn phần với TSH có thể cho kết quả chính xác hơn.
Các vấn đề kể trên sẽ được giải quyết bằng cách định lượng nồng độ T4 tự do bằng IMA, bằng thẩm tách cân bằng (ED) hay bằng phương pháp sắc ký lỏng ghép đầu dò khối phổ (LC/MS). Khi định lượng bằng chất đánh dấu tương tự T4 (T4 analog tracer) cạnh tranh gắn kết với kháng thể của xét nghiệm thay vì protein huyết tương, nên sẽ rất chính xác khi cần phân biệt có sự tái phân bố hormone tuyến giáp với TBG hay bất thường FT4 thực sự do rối loạn chức năng tuyến giáp. Tuy nhiên, chúng vẫn bị ảnh hưởng ít nhiều trong các trường hợp có biến đổi nồng độ T4 toàn phần (gây kết quả tăng giả trong trường hợp nhiễm độc giáp do rối loạn chức năng albumin hay gây giảm giả trong ba tháng cuối thai kỳ,…). Dù vậy, định lượng T4 tự do bằng IMA hiện nay vẫn là xét nghiệm được sử dụng rộng rãi nhất khi cần xác định nồng độ FT4 vì nó tương đối chính xác trong hầu hết các trường hợp, nhanh chóng, tự động và rẻ tiền. Phương pháp thẩm tách cân bằng (ED) tuy là tiêu chuẩn vàng trong xác định nồng độ FT4 trong máu nhưng đắt tiền và không sẵn có, nên không được xem là 1 st line trong định lượng FT4. Nhắc lại, vẫn phải thực hiện FT4 cùng với TSH, vì nếu FT4 dùng đơn độc để chẩn đoán các rối loạn chức năng tuyến giáp thì sẽ gặp nhiều vấn đề. Một là có những bệnh nhân lâm sàng bình giáp nhưng định lượng hormone tuyến giáp tự do tăng do bệnh nền, do thuốc ức chế chuyển T4 thành T3 (làm tăng nồng độ FT4) như thuốc cản quang chứa iod, amiodarone, glucocorticoid và propanolol. Trong những trường hợp này thì nếu làm xét nghiệm TSH, cho kết quả bình thường có thể loại trừ cường giáp. Ngược lại, sẽ có những bệnh lý mà nồng độ FT4 dưới mức bình thường dù bệnh nhân đó bình giáp. Ví dụ như các thuốc chống động kinh như phenytoin và carbamazepine gây nhiều tác động như ức chế tiết TSH và gia tăng tốc độ dị hóa T4, từ đó làm giảm nồng độ T4 toàn phần và T4 tự do. Lúc này, nồng độ TSH huyết tương bình thường sẽ giúp loại trừ. Về xét nghiệm nồng độ T3 tự do và toàn phần trong máu, nếu chỉ sử dụng nó thay cho nồng độ T4 thường sẽ không phản ánh chính xác, ví dụ để chẩn đoán suy giáp, nếu bệnh nhân chỉ mắc suy giáp nguyên phát mức độ nhẹ – trung bình thì nồng độ hormone T3 trong máu thường vẫn được duy trì ở mức bình thường nhờ cơ chế feedback âm (xem lại phần trước). Tuy vậy, xét nghiệm nồng độ T3 trong máu vẫn có vai trò trong các trường hợp (1) phát hiện những bệnh nhân có nhiễm độc giáp chỉ do tăng T3, thể nhẹ của cường giáp, trong đó T3 tăng nhưng T4 bình thường; (2) để đánh giá tốt hơn về mức độ nặng của cường giáp và theo dõi đáp ứng điều trị; và (3) để chẩn đoán phân biệt một số thể cường giáp. Vì trong bệnh Graves thì hầu hết bệnh nhân sẽ ưu thế tăng T3 (cũng gặp trong một số bướu giáp nhân độc), nên chỉ số T3/T4 huyết thanh (biểu hiện dưới ng/dl: μg/dL) thường > 20. Ngược lại, những nguyên nhân gây nhiễm độc giáp liên quan đến viêm giáp thì tỉ số T3/T4 thường < 20.
| BẢNG 7-4: Nguyên nhân làm nồng độ TSH huyết thanh không phù hợp |
Lâm sàng có biểu hiện cường giáp:
|
Lâm sàng có biểu hiện suy giáp:
|
| Lâm sàng có biểu hiện bình giáp.
Bệnh hệ thống (↓ trong giai đoạn cấp tính, ↑ trong khi phục hồi). Đề kháng với hormone tuyến giáp (đã bù trừ). Sai số do xét nghiệm:
Thuốc: dopamine, dobutamine, glucocorticoid. |
| BẢNG 7-5: Giá trị động học của iodothyronine ở người bình giáp | |||
| T4 | T3 | rT3 | |
Nồng độ trong huyết thanh
|
8(103)
1.5(19) |
0.12(1.84 )
0.28(4.3) |
0.04(0.51 )
0.24(3.69 ) |
| Chứa trong toàn cơ thể | 800(1023) | 46(70.7) | 40(61.5) |
| Thể tích phân bố (L) | 10 | 38 | 98 |
| Tỷ lệ đào thải qua chuyển hóa | 1 | 22 | 90 |
| (MCR) (L/ngày) | |||
| Tỷ lệ sản xuất (thải bỏ) MCR × nồng độ huyết thanh, μg/d (nmol/ngày ) | 80(103) | 26(34) | 36(46) |
| Thời gian bán hủy trong huyết tương (t1/2) (ngày) | 7 | 1 | 0,2 |
Lưu ý: T4 μg/dL × 12,87 = nmol/L; T3 μg/dL × 15,38 = nmol/.
Định lượng nồng độ TG đôi lúc được chỉ định cho mục đích: (1) phát hiện ung thư biểu mô tuyến giáp còn sót hay tái phát sau phẫu thuật (u nhú, u nang và carcinoma tế bào Hurthle); và (2): phân biệt với nhiễm độc giáp do hormone giáp ngoại sinh (trường hợp này TG sẽ bị giảm) với nguyên nhân nội sinh. Tuy nhiên cần lưu ý, TG không giúp ích trong việc phân biệt nhân giáp là lành hay ác tính.
XÉT NGHIỆM ĐÁNH GIÁ VỀ SINH TỔNG HỢP VÀ CHUYỂN HÓA IOD Ở TUYẾN GIÁP
Các xét nghiệm định lượng bắt iod đồng vị phóng xạ có thể được sử dụng để phân biệt giữa các nguyên nhân gây nhiễm độc giáp, đặc biệt khi kết hợp với hình ảnh học. Ở bệnh nhân cường giáp do bệnh Graves, phân suất bắt iod phóng xạ (RAIU) trong 24 giờ tăng rõ rệt (40%- 95%), khi chu chuyển iod quá nhanh thì phân suất bắt trong 5 giờ thậm chí có thể cao hơn so với 24 giờ (xem Hình 7-25).
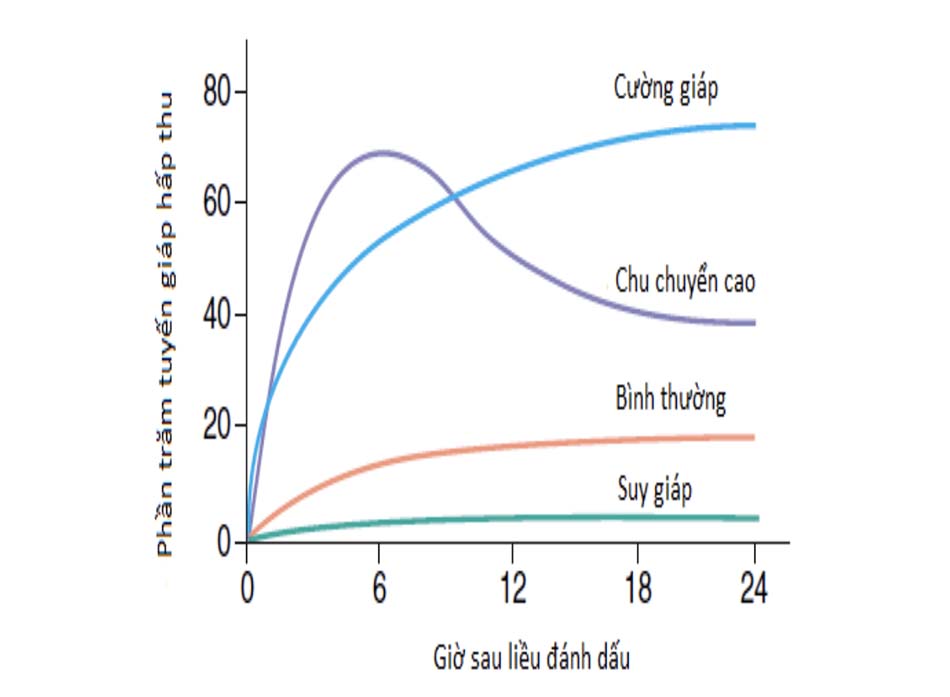
Tương tự, 24h-RAIU tăng ít hơn ở bệnh nhân bướu giáp nhân độc (30%-70%). Ngược lại, nhiễm độc giáp mà RAIU ở tuyến giáp thấp thường do các nguyên nhân: (1): viêm giáp bán cấp và do lympho bào (viêm giáp hậu sản, thầm lặng); (2) nhiễm độc giáp do sử dụng thừa hormone tuyến giáp; và (3) sau khi nhập một lượng lớn iodide đường uống hoặc đường tĩnh mạch, ví dụ như điều trị với amiodarone, hay sau khi chụp hình với thuốc cản quang. Ngoài ra, RAIU thấp “không phải ở vùng cổ trước” (vị trí thông thường của tuyến giáp) có thể gặp trong các bệnh lý tăng tiết hormone tuyến giáp lạc chỗ như ở nền lưỡi (giáp lưỡi), ở trung thất, u quái giáp ở buồng trứng hay trong trường hợp có di căn sang nơi khác sau phẫu thuật cắt tuyến giáp ở ung thư biểu mô tuyến giáp.
HÌNH ẢNH HỌC TUYẾN GIÁP
HÌNH ẢNH HỌC PHÓNG XẠ
123I và 99mTcO4 được sử dụng để đánh giá hoạt động chức năng và hình thái của tuyến giáp. Uống 123I (200-300 μCI) và đánh giá hình ảnh học sau 8-24 giờ sau đó. 99mTcO4 (1-10 mCi) được bắt lại bởi NIS nhưng không được biến đổi và giữ lại ở tuyến giáp, tiêm tĩnh mạch và đánh giá hình ảnh học sau đó 30-60 phút. Trên hình ảnh phóng xạ cung cấp thông tin về kích thước, hình dạng tuyến giáp cũng như sự phân bố thể hiện dưới hoạt động của chất đánh dấu bên trong tuyến giáp. Phương tiện này giúp phân biệt giữa các nguyên nhân gây nhiễm độc giáp. Ví dụ, bệnh nhân cường giáp với biểu hiện tuyến giáp phì đại, bắt iod mạnh và đồng nhất là các đặc tính của bệnh Graves. Ngược lại, khi biểu hiện một hay nhiều vùng với hoạt động bắt iod khác nhau, đặc biệt tương ứng với những vị trí nốt mà ta sờ được khi khám lâm sàng, cùng với sự ức chế của mô xung quanh nốt đó trên hình ảnh học là biểu hiện điển hình của bướu giáp nhân độc.
Hình ảnh học phóng xạ có vai trò hạn chế trong việc phân biệt các nhân giáp lành với ác tính. Khi bệnh nhân có nhân giáp, kèm với giảm nồng độ TSH trong máu, hình ảnh học phóng xạ thường biểu hiện với nhân nóng (tức là hoạt động làm ức chế các vùng xung quanh nhân đó), thường là nhân lành tính. Nhưng ngược lại, hầu hết các nhân giáp lành tính và ác tính là nhân lạnh, hay giảm chức năng thì lúc này không giúp ta phân biệt được.
Ngoài ra, đánh giá hình ảnh học phóng xạ toàn cơ thể giúp theo dõi điều trị ung thư tuyến giáp và để xác định các trường hợp mô giáp lạc chỗ như ở lưỡi (giáp lưỡi), ở giữa cổ (ống giáp lưỡi), ở trung thất (bướu giáp sau xương ức) hay ở vùng chậu (u quái giáp).
SIÊU ÂM TUYẾN GIÁP VÀ MỘT SỐ HÌNH ẢNH HỌC KHÁC
Kích thước và các đặc điểm sang thương của nhân giáp được đánh giá tốt nhất qua siêu âm có độ phân giải cao (Hình 7- 27). Siêu âm có thể phân biệt giữa nhân đặc với sang thương dạng nang và với một số nang có đặc điểm phức tạp (vừa có thành phần đặc, vừa có thành phần dạng nang). Một số đặc điểm nhất định của nhân thường gặp trong các tổn thương ác tính bao gồm: hồi âm giảm, vỏ bọc nhân không đều và có vi vôi hóa.
Bên cạnh đó các đặc điểm thường gợi ý lành tính như: đẳng âm hay tăng hồi âm, dạng bọt biển (spongiform) và thay đổi dạng nang.

Siêu âm còn có vai trò theo dõi kích thước tuyến giáp theo thời gian, dẫn đường để chọc hút nhân giáp bằng kim nhỏ, đánh giá các hạch bạch huyết vùng ở bệnh nhân ung thư tuyến giáp trước phẫu thuật và trong quá trình theo dõi lâu dài. Ngoài ra, siêu âm còn giúp đánh giá lưu lượng máu của tuyến giáp, giúp ích trong chẩn đoán phân biệt với nhiễm độc giáp do thuốc amiodarone gây ra. CT-scan và MRI thường sử dụng trong các tình huống đặc biệt, dùng để xác định khi tuyến giáp phát triển lớn ra sau cổ và xuống xương ức, khi có các biểu hiện đẩy lệch khí quản hay chèn ép. Bên cạnh đó, còn giúp đánh giá di căn ở những bệnh nhân ung thư tuyến giáp (phổi, gan). Tuy nhiên, cần nhớ rằng khi sử dụng chất cản quang có chứa iod để đánh giá trên CT-scan có thể gây ảnh hưởng đến việc đánh giá bằng hình ảnh học phóng xạ và ảnh hưởng đến điều trị trong vòng vài tháng. PET-scan có vai trò trong việc định vị nơi di căn ở những bệnh nhân ung thư tuyến giáp đã được điều trị khi nồng độ TG huyết thanh > 10 ng/ml.
Các nghiên cứu chỉ ra rằng xuất độ ung thư tuyến giáp ở những u giáp phát hiện một cách tình cờ khi khảo sát hình ảnh học cao như việc phát hiện ung thư tuyến giáp từ các nhân giáp sờ được trên lâm sàng, chính vì thế nên sinh thiết nếu đường kính > 1-1,5 cm và theo dõi nhiều lần trên siêu âm nếu kích thước nhỏ hơn.
SINH THIẾT TUYẾN GIÁP
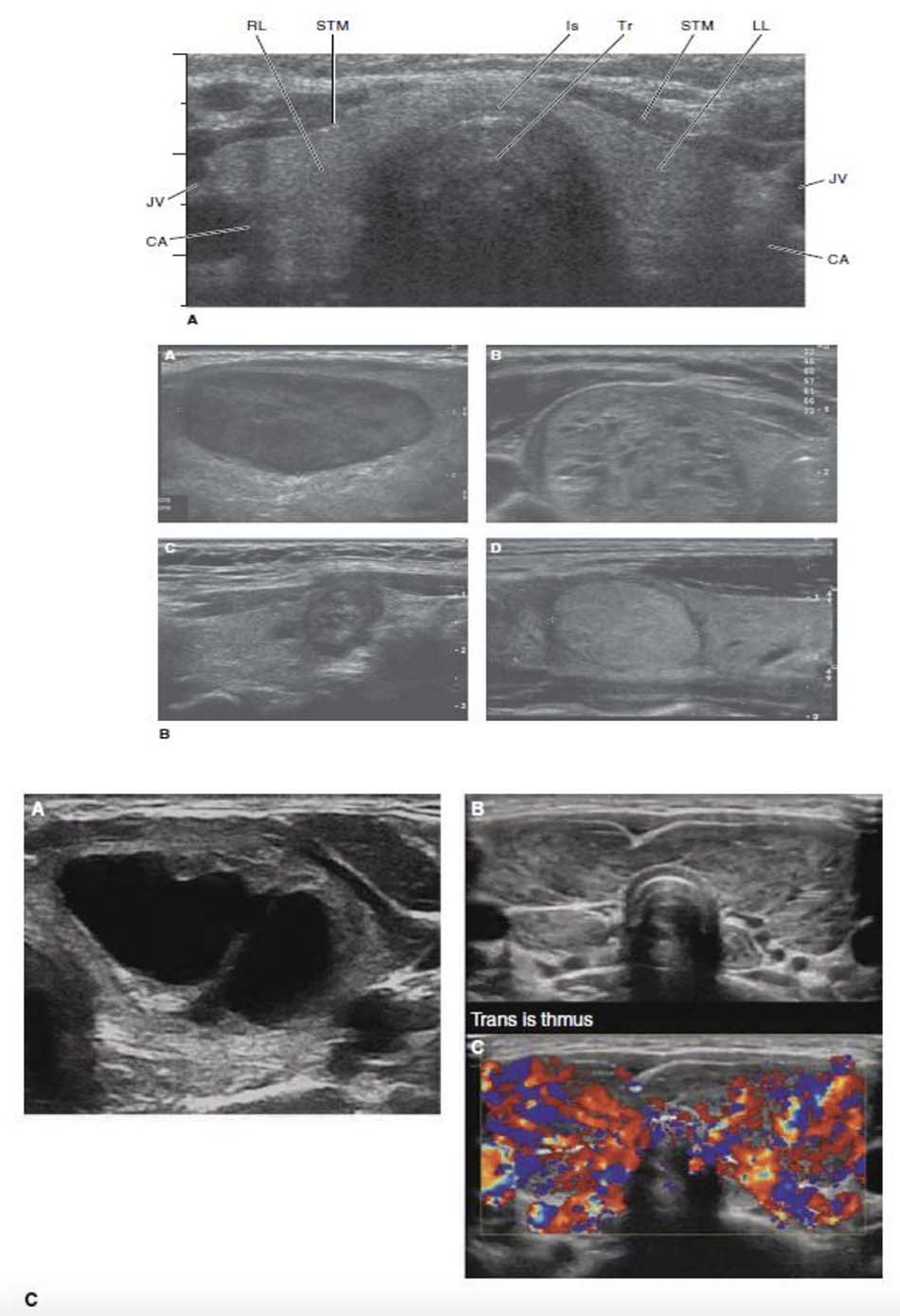
Sinh thiết bằng kim nhỏ (FNAB) nhân giáp là phương pháp tốt nhất để phân biệt giữa nhân giáp ác tính với nhân giáp lành tính và với bướu giáp lan tỏa. FNAB là một thủ thuật nhỏ có thể tiến hành ngoại trú, lúc bệnh nhân tỉnh, không cần nhịn đói, với kỹ thuật vô trùng thích hợp, có thể cần gây tê tại chỗ hoặc không. Thủ thuật thường được tiến hành bằng kim có kích thước 27 hoặc 25- gauge, chọc vào vùng nốt hay bướu, đưa vào đưa ra đến khi thu được một ít mẫu ở phần trung tâm của kim. Sau đó mẫu được trải lên một lam kính, nhuộm rồi quan sát.
Chẩn đoán trên tế bào học về sự ác tính của các nhân giáp rất chính xác. Độ nhạy trong phát hiện ung thư tuyến giáp (số trường hợp dương tính thật trên tổng số trường hợp nhân giáp đã được khẳng định là ung thư sau phẫu thuật) là 95- 98%, và độ đặc hiệu trong ung thư (số ca dương tính thật chia tổng số ca dương tính qua sinh thiết) lên đến 98%. Ngược lại, ở các nhân còn lại, khi biểu hiện với hình ảnh mô học lành tính thì có khả năng tiên đoán âm lên đến 97% (số kết quả âm tính thật chia cho tổng trường hợp cho kết quả âm tính). Tuy nhiên, có khoảng một phần ba số nhân giáp cho hình ảnh mô học không xác định được, chúng được chia thành các nhóm nhỏ như: không xác định được các trường hợp không điển hình (AUS), tân sản dạng nang hay nghi ngờ ác tính, ba phân nhóm này có nguy cơ ung thư ước tính lần lượt là 5-15%; 15-30% và 60-75%.
ĐỊNH LƯỢNG TỰ KHÁNG THỂ TUYẾN GIÁP
Xác định tự kháng thể kháng giáp giúp ích trong việc chẩn đoán các bệnh lý tuyến giáp tự miễn. Để chẩn đoán viêm giáp tự miễn (viêm giáp Hashimoto) ở bệnh nhân có bướu giáp lan tỏa hay có suy giáp thì có thể tiến hành xét nghiệm kháng thể anti-TPO hay ít nhạy hơn là anti-TG trong huyết thanh, có thể bằng phương pháp ngưng kết hồng cầu, ELISA hay RIA; trong đó RIA nhạy hơn, định lượng chính xác hơn và thường được ưu tiên hơn. Mặc dù các kháng thể này gặp trong hầu hết các bệnh nhân có viêm giáp tự miễn, nhưng nó cũng có mặt ở nhiều bệnh nhân mắc bệnh Graves và một số thể viêm giáp khác. Chính vì xuất độ mắc cao, đặc biệt ở giới nữ, nên dù kết quả dương tính cũng chưa đủ để loại trừ có thể mắc kèm với một bệnh lý tuyến giáp thứ hai. Các kháng thể kích thích, gắn kết hay ức chế thụ thể TSH cũng thường được xác định. TSI (còn gọi là TSAb), hiện diện trong khoảng 90% bệnh nhân có bệnh Graves và hầu như không bao giờ phát hiện được ở các bệnh nhân không mắc bệnh này cũng như không gặp trong các bệnh nhân mắc các bệnh lý tuyến giáp liên quan đến tự miễn khác. Xét nghiệm tìm TSI thường được sử dụng trong một số tình huống sau: (1) phụ nữ mang thai để xác định nguy cơ mắc cường giáp sau đó ở trẻ sơ sinh, (2) để phân biệt bệnh Graves với viêm giáp hậu sản ở phụ nữ cho con bú không thể thực hiện xét nghiệm bắt iod phóng xạ; (3) để chẩn đoán bệnh Graves ở các bệnh nhân bình giáp nhưng có biểu hiện bệnh ở mắt rõ có liên quan đến tuyến giáp; và (4) để dự đoán khả năng liệu bệnh nhân Graves đang điều trị với thuốc kháng giáp có tái phát nếu ngưng điều trị sau đó hay không. Ngoài ra, trong một số trường hợp có thể định lượng kháng thể gắn kết TSH. Kháng thể ức chế thụ thể TSH là nguyên nhân ít gặp gây suy giáp ở một số bệnh nhân; có thể truyền qua nhau thai gây suy giáp ở bào thai.
CÂU HỎI LÂM SÀNG
Một phụ nữ 22 tuổi đến phàn nàn vì không chịu được nóng, ra mồ hôi và đánh trống ngực. Cô cũng nói rằng kinh nguyệt không đều, chán ăn và tiêu chảy.
Mạch 102 l/ph và đều, HA 116/80 mmHg, nhiệt độ 37,2 (99F), nhịp thở 14 l/ph. Khám thấy tuyến giáp không đau, to lan tỏa. Nồng độ TSH 0,05 mU/L. Nồng độ T3 và T4 tự do tăng. Xạ hình iod phóng xạ 24h là 50%. Có thyroid stimulating immunoglobulin (TSI). Cô bắt đầu dùng propylthiouracil 300 mg mỗi ngày chia làm 3 liều. Sau 2 tuần, cô trở lại và phàn nàn về viêm họng. Mạch 98 l/ph và đều, nhiệt độ 38,6 C (101,5F), HA 115/76 mmHg, nhịp thở 15 l/ph. Khẩu cái mềm, hầu, và lưỡi đỏ và sưng. Bước tiếp theo phù hợp nhất trong quản lý bệnh nhân này là gì?
- Thêm propranolol
- Tăng liều propylthiouracil
- Dừng propylthiouracil
- Cấy họng
- Penicillin đường uống
- Acetaminophen
Đáp án đúng là C:
Thuốc kháng giáp trạng propylthiouracil (PTU) và methimazole (MMI) liên quan đến một lượng nhỏ, cũng như khả năng đe dọa tính mạng các tác dụng phụ. Giảm bạch cầu hạt là tác dụng phụ đáng sợ nhất, được thấy ở xấp xỉ 0,3% bệnh nhân được điều trị với thuốc kháng giáp trạng. Nó được gây ra bởi sự phá hủy miễn dịch bạch cầu hạt, phần lớn các trường hợp xảy ra trong vòng 90 ngày điều trị. Theo dõi định kì số lượng bạch cầu hạt không có hiệu quả và không được tán thành. Khuyến cáo hiện tại là một khi bệnh nhân phàn nàn về sốt và viêm họng, thuốc kháng giáp trạng nên được dừng lại ngay và đo số lượng bạch cầu. Số lượng bạch cầu toàn bộ thấp hơn 1000/mm3 báo động việc dừng thuốc lâu dài. Nếu số lượng bạch cầu toàn bộ nhiều hơn 150/mm3, ngộ độc thuốc kháng giáp trạng không có khả năng gây ra viêm họng và sốt.
Lựa chọn A: Propranolol có thể được sử dụng để giảm nhẹ triệu chứng, tuy nhiên, bước tiếp theo quan trọng nhất là dừng PTU và kiểm tra số lượng bạch cầu.
Lựa chọn B: Tăng liều propylthiouracil sẽ gây chết người ở bệnh nhân này.
Lựa chọn D, E và F: Điều trị giảm bạch cầu hạt do thuốc kháng giáp trạng gồm dừng thốc và truyền tĩnh mạch kháng sinh phổ rộng (đặc biệt cho Pseudomonas). Granulocyte colony stimulating factor có thể được sử dụng để làm tăng số lượng bạch cầu. Cấy họng, penicillin đường uống và acetaminophen không đảo ngược vấn đề tiềm ẩn của bệnh nhân này, và do đó không phải bước tiếp theo thích hợp.
Mục tiêu học tập:
Sốt và viêm họng ở bất kì bệnh nhân nào dùng thuốc kháng giáp trạng gợi ý giảm bạch cầu hạt. Thuốc kháng giáp trạng nên được dừng và kiểm tra số lượng bạch cầu. Đo số lượng bạch cầu định kì ở bệnh nhân dùng thuốc kháng giáp trạng không có hiệu quả.