Bệnh sản phụ khoa
Quản lý bệnh nguyên bào nuôi thai kỳ (SOGC-1/2021)
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
Biên dịch: Bs Vũ Tài
nhathuocngocanh.com – Tải File PDF bài viết Quản lý bệnh nguyên bào nuôi thai kỳ (SOGC-1/2021) TẠI ĐÂY.
GIỚI THIỆU
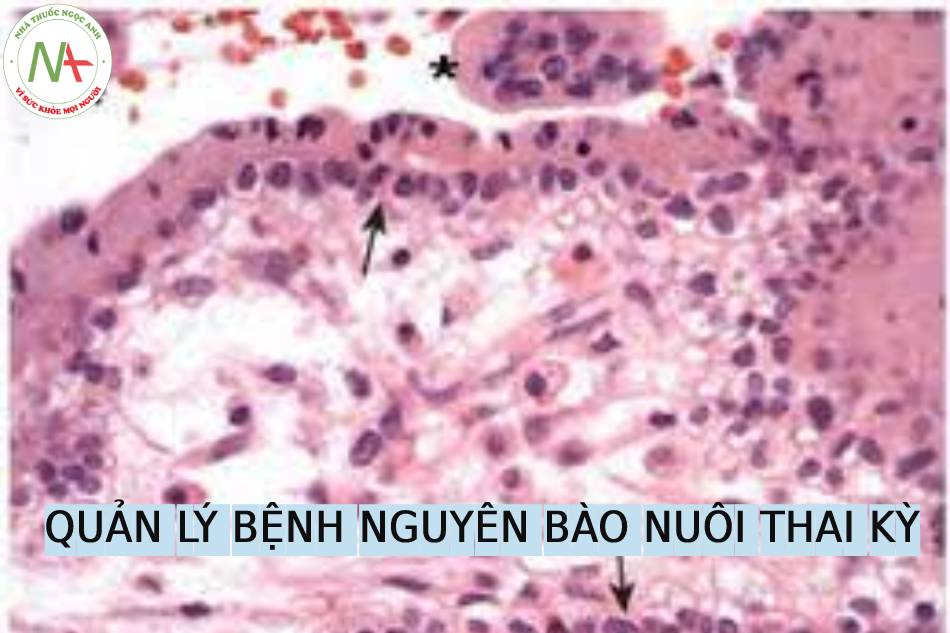
Bệnh nguyên bào nuôi thai kỳ (GTD) được đặc trưng bởi sự tăng sinh bất thường của nguyên bào nuôi nhau thai. Các nốt nơi nhau bám (Placental site nodules) và các khối u quá mức nơi nhau bám (exaggerated placental site tumours) là những thực thể không phải ung thư. Thai trứng toàn phần và bán phần được coi là tiền ác tính do chúng có khả năng tồn tại dai dẳng và xâm lấn. Các nốt nơi nhau bám không điển hình cũng có khả năng ác tính.1 Các tình trạng ác tính được phân loại là u nguyên bào nuôi thai kỳ (GTN). GTN có thể xảy ra sau thai trứng hoặc không phải thai trứng và bao gồm một số chẩn đoán: thai trứng xâm lấn (invasive moles), ung thư nguyên bào nuôi (choriocarcinomas), u nguyên bào nuôi nơi nhau bám (placental site trophoblastic tumours) và u nguyên bào nuôi dạng biểu mô (epithelioid trophoblastic tumours)
DI TRUYỀN
Thai trứng là kết quả của sự dư thừa bộ nhiễm sắc thể đơn bội của bố ở thai. Thai trứng toàn phần thường được đặc trưng bởi không có bộ nhiễm sắc thể đơn bội của mẹ và có 2 bộ nhiễm sắc thể đơn bội của bố (androgenesis) xảy ra từ sự thụ tinh của một trứng trống với một tinh trùng duy nhất, sau đó là sự nhân đôi bộ nhiễm sắc thể của nó (tức là: 46, XX) hoặc thông qua sự thụ tinh của 2 tinh trùng (tức là: 46, XX hoặc 46, XY). Thai trứng bán phần là kết quả của các quá trình tương tự nhưng chứa 1 bộ nhiễm sắc thể đơn bội của mẹ, dẫn đến thai tam bội (tức là 69, XXX, 69, XXY hoặc 69, XYY). Ở thai trứng bán phần, có thể có thai nhi hoặc các màng thai, nhưng thai nhi này không thể sống được. Điều này trái ngược với thai tam bội có 2 bộ NST đơn bội của mẹ và 1 bộ NST đơn bội của bố, trong đó thai tam bội không phải thai trứng có biểu hiện nhung mao thoái hóa nước nhưng không tăng sinh nguyên bào nuôi. Có thể nhuộm hóa mô miễn dịch sản phẩm gen p57KI12 của CDKN1C để phân biệt thai trứng toàn phần với thai trứng bán phần và sẩy thai phù nề. CDKN1C là một gen nằm trên bộ NST của bố nhưng có gen biểu hiện nằm trên bộ NST của mẹ. Sản phẩm gen p57KIP2 hoàn toàn không có trong nguyên bào nuôi nhung mao của thai trứng toàn phần vì nguồn gốc androgenetic của nó. Có một ngoại lệ với điều này đó là thai trứng toàn phần lưỡng bội có nguồn gốc từ cả bố và mẹ hậu quả từ thai trứng tái phát có tính chất gia đình. Tình trạng di truyền lặn trên NST thường này ảnh hưởng đến gen NLRP7 hoặc KHDC3L, gen NLRP7 là yếu tố góp phần quan trọng đối với dấu ấn di truyền của mẹ. Tình trạng này được chẩn đoán thông qua việc xác định kiểu gen vi vệ tinh huỳnh quang, trong đó xác định được sự đóng góp của cả bố và mẹ. Những bệnh nhân bị tình trạng không thể mang thai bình thường nếu không có sự hỗ trợ của việc cho trứng; chiếm 50% đến 80% số bệnh nhân có thai trứng tái phát.4 Các đột biến có hại hai alen gần đây đã được xác định trong các gen MEI1, TOP6BL / C1 lorf80 và REC114, có vai trò trong việc hình thành các đứt gãy sợi kép giảm phân ở phụ nữ bị thai trứng toàn phần androgenetic tái phát.5 Nghiên cứu xác định các gen đóng góp mới khác đang được tiến hành.4
GTN có thể xảy ra sau thai trứng, thai đủ tháng / non tháng, phá thai hoặc thai lạc chỗ. Ung thư nguyên bào nuôi sau sinh chứa bộ nhiễm sắc thể từ cả bố và mẹ giống hệt bộ nhiễm sắc thể của thai nhi, trong khi ung thư nguyên bào nuôi sau thai trứng toàn phần là androgenetic. Xác định kiểu gen có thể có lợi để loại trừ ung thư nguyên bào nuôi dạ dày, buồng trứng hoặc phổi nguyên phát, tùy thuộc vào tình huống lâm sàng, như không có khối vùng chậu hoặc thai kỳ trước đó. Ung thư nguyên bào nuôi không do thai kỳ hiếm gặp và có thể được phân biệt bằng cách không có DNA của bố.6 Chúng có liên quan đến đáp ứng điều trị kém và tiên lượng chung xấu.7
SINH BỆNH HỌC
u nguyên bào nuôi thai kỳ tiết ra gonadotropin màng đệm người (hCG). Ban đầu nó được tiết ra bởi đơn bào nuôi nguyên thủy chủ yếu là hyperglycosylated hCG cho đến tuần thứ 4. Sau tuần thứ 4, hầu hết hCG được tiết ra bởi lá nuôi hợp bào (một lớp có nguồn gốc từ lớp đơn bào nuôi xâm nhập). Lớp này mất dần khi thai trưởng thành, giảm dần từ khoảng tuần thứ 12 của thai kỳ cho đến khi đủ tháng. Bởi u nguyên bào nuôi nơi nhau bám phát sinh từ nguyên bào nuôi trung gian ở vị trí làm tổ, chúng chứa cực ít lá nuôi hợp bào và tiết ra lượng hCG rất thấp, u nguyên bào nuôi dạng biểu mô, phát sinh từ nguyên bào nuôi trung gian loại màng đệm, cũng tiết ra lượng hCG rất thấp. Mặt khác, nồng độ hCG huyết thanh tương quan cao với gánh nặng khối u và do đó là một dấu ấn quan trọng và hữu ích trong chẩn đoán và điều trị GTN.
Glycoprotein hCG được tạo thành từ một tiểu đơn vị beta độc nhất và một tiểu đơn vị alpha giống các hormone khác, bao gồm hormone kích thích tuyến giáp (TSH) và hormone hoàng thể hóa (LH). Sự kích thích quá mức do nồng độ hCG tăng cao (thường > 100 000 mlƯ/mL) có thể dẫn đến sự phát triển các nang hoàng tuyến của buồng trứng, ốm nghén nặng, tiền sản giật và cường giáp với nguy cơ kèm theo cơn bão giáp, đặc biệt là tại thời điểm nạo hút tử cung. Hầu hết các xét nghiệm hCG sử dụng kháng thể để phát hiện tiểu đơn vị beta, mà trong thai kỳ bình thường chủ yếu hiện diện ở dạng nguyên vẹn. Tuy nhiên, với sự biến đổi ác tính, phân tử hCG bị phá vỡ thành các mảnh như core hCG, nicked free-beta, và C-terminal peptide. Các dạng hyperglycosyl hóa cũng tăng lên. Các xét nghiệm hCG có sẵn trên thị trường phát hiện một số dạng hCG khác nhau, nhưng có sự khác biệt lớn về tỷ lệ tương đối mà mỗi xét nghiệm báo cáo. Điều này có thể gây ra sự khác biệt về nồng độ hCG được báo cáo nếu các xét nghiệm hCG khác nhau được sử dụng trong quá trình theo dõi bệnh nhân GTN.8
Chẩn đoán phân biệt nồng độ hCG cao bao gồm mang thai, GTD, sản xuất hCG từ tuyến yên, hCG bóng ma do phản ứng chéo với kháng thể dị ái lưu hành, hoặc sản xuất hCG lạc chỗ (ví dụ: ung thư nguyên bào nuôi không do thai kỳ).
DỊCH TỄ HỌC
Tỷ lệ mắc mới GTD thường được báo cáo là 1 trong 1000 thai kỳ; tuy nhiên, tỷ lệ này thay đổi theo quần thể. 910 Nghiên cứu duy nhất ở Canada báo cáo nguy cơ mắc thai trứng là 1 trong 454 thai kỳ ở Nova Scotia từ năm 1990 đến 2005 bằng cách sử dụng cơ sở dữ liệu về GTD, thai kỳ và sinh của tỉnh.11 GTDs phổ biến hơn ở bệnh nhân ở các cực của tuổi (< 20 tuổi hoặc > 40 tuổi) và đặc biệt ở phụ nữ trên 45 tuổi 11,12 Tỷ lệ mắc mới GTD dường như cao nhất ở dân số Châu Á.10 Nguy cơ bị thai trứng xâm lấn là 15% đến 20% sau thai trứng toàn phần và 0,5% đến 1% sau khi thai trứng bán phần.13”16 Nguy cơ thai trứng xâm lấn tăng lên 40% đến 50% ở những bệnh nhân có bất kỳ một trong các yếu tố nguy cơ sau: tuổi > 40, kích thước tử cung > 4 tuần cao hơn kỳ vọng so với tuổi thai, hCG > 100 000 mlU/mL và nang hoàng tuyến hai bên > 6 cm.17,18 Tỷ lệ mắc mới ung thư nguyên bào nuôi là khoảng 1 trong số 20.000 thai kỳ ở Bắc Mỹ những thay đổi trên toàn cầu. 19,20 The GTN hiếm khi được chẩn đoán nhất là u nguyên bào nuôi nơi nhau bám và u nguyên bào nuôi dạng biểu mô, chiếm < 1% tổng số GTN; chúng có thể xảy ra sau thai trứng và không phải thai trứng, thường là nhiều năm sau lần mang thai trước đó.
CHẨN ĐOÁN BỆNH NGUYÊN BÀO NUÔI THAI KỲ
Trước đây, bệnh nhân GTD thường có biểu hiện chảy máu âm đạo bất thường và tử cung lớn hơn so với tuổi thai và đôi khi có biểu hiện ốm nghén, tiền sản giật hoặc cường giáp. Tuy nhiên, từ khi siêu âm ba tháng được đầu thực hiện thường quy, GTD thường được xác định trên siêu âm trước khi bệnh nhân xuất hiện các triệu chứng lâm sàng khác ngoài xuất huyết âm đạo, hoặc trên mô học sau khi hút thai bất thường. Nếu các dấu hiệu trên siêu âm không thể chẩn đoán chắc chắn là thai trứng, nồng độ hCG đang tăng sẽ giúp phân biệt GTD với các chẩn đoán như trứng trống hoặc sẩy thai lưu.21 Cần cân nhắc đo hCG huyết thanh hoặc nước tiểu từ 4 đến 6 tuần sau bất kỳ chấm dứt thai kỳ nào, hút thai lưu hoặc sẩy thai tự phát nếu các triệu chứng mang thai vẫn tồn tại, như chảy máu liên tục hoặc vô kinh. Điều này sẽ giúp loại trừ sót các sản phẩm thụ thai hoặc mang thai mới ở những nơi mà các sản phẩm thụ thai không được gửi thường quy để làm giải phẫu bệnh và có thể xác định GTD, do đó tránh được chẩn đoán GTN muộn, có liên quan đến các biến chứng đe dọa tính mạng và cần can thiệp phẫu thuật và hóa trị.22 Các đặc điểm trên siêu âm của một thai trứng toàn phần bao gồm không có thai nhi và không có nước ối trong tử cung to. Tử cung có một khối hồi âm hỗn hợp, chủ yếu là hồi âm dày, có nhiều ổ giảm âm trong khối thường được mô tả là hình ảnh “bão tuyết”. Khối trong tử cung chứa nhiều nang (nhung mao thoái hóa nước) dẫn đến xuất hiện hình ảnh “chùm nho”. Khi thai kỳ tiến triển, các nang to ra và nhiều hơn. Ngoài các nang, khối này có thể chứa các ổ dịch không đều lớn hơn. Trong thai trứng toàn phần, có thể xuất hiện nang hoàng tuyến buồng trứng khi nồng độ hCG tăng cao do phân tử hCG nguyên vẹn có khả năng bắt chước hormone hoàng thể hóa ( LH). Thai trứng bán phần có thể biểu hiện dưới dạng túi thai trống hoặc túi thai chứa các bộ phận của thai nhi vô định hình hoặc thai chậm tăng trưởng / không thể sống được. Lượng nước ối giảm và nhau thai to so với kích thước của tử cung, với các nang thường được gọi là có dạng “pho mát Thụy Sĩ”. Túi thai ở thai trứng bán phần có thể có hình trứng, được xác định bằng tăng đường kính ngang (tỷ lệ đường kính ngang /đường kính trước trước sau > 1,5). Thường không có nang hoàng tuyến do nồng độ hCG thấp hơn. Có thể chẩn đoán sai thai trứng bán phần trong trường hợp hiếm gặp là song thai bao gồm một thai trứng và một thai lưỡng bội (có thể sống được).
Bất kỳ sản phẩm thụ thai nào trông bất thường tại thời điểm hút buồng tử cung nên được kiểm tra mô học. Bất kỳ kết quả giải phẫu bệnh nào gợi ý GTD đều nên được xem xét bởi bác sĩ giải phẫu bệnh phụ khoa để phân biệt thai trứng toàn phần, thai trứng bán phần và bệnh nguyên bào nuôi ác tính; sự khác biệt này sẽ ảnh hưởng đến việc theo dõi bệnh nhân và quản lý GTN.
Các việc cần làm khi nghi ngờ GTD bao gồm xem xét các cơ quan để xác định biến chứng như thiếu máu, tiền sản giật và cường giáp, hoặc các triệu chứng gợi ý bệnh di căn. Tuổi thai và kết cục của tất cả các lần mang thai trước nên được ghi lại như một phần của tiền sử sản khoa. Khám lâm sàng bao gồm đánh giá kích thước tử cung và sự hiện diện của các khối ở phần phụ hoặc di căn khác. Các xét nghiệm cận lâm sàng bao gồm công thức máu toàn bộ, điện giải đồ, chỉ số bình thường hóa quốc tế (INR), thời gian thromboplastin từng phần, creatinin, men gan, hormone kích thích tuyến giáp (TSH), định lượng hCG toàn phần và protein nước tiểu. Một phụ nữ trong độ tuổi sinh sản có nồng độ hCG tăng cao hoặc đang tăng không giải thích được nên được coi là mắc GTD cho đến khi chứng minh được là do nguyên nhân khác.
Chẩn đoán hình ảnh đối với bệnh nhân mang thai trứng thường chỉ là siêu âm vùng chậu, với các phương tiện chẩn đoán hình ảnh chuyên sâu hơn được điều chỉnh theo các triệu chứng. Chẩn đoán hình ảnh GTN sau thai trứng cần chụp X-quang ngực để tìm di căn phổi và siêu âm vùng chậu để đánh giá mức độ bệnh trong khung chậu. Trên X-quang phổi, có thể thấy được các tổn thương > 6 mm. Nếu kết quả chụp X- quang phổi âm tính, không cần làm thêm các chẩn đoán hình ảnh khác. Khả năng di căn có ý nghĩa trên lâm sàng là không đáng kể trong trường hợp không có di căn phổi hoặc âm đạo. Các vi di căn trong phổi được xác định trên CT scan ngực không ảnh hưởng đến kết cục lâm sàng của bệnh nhân mắc bệnh ở giai đoạn 1.23,24 Nếu kết quả chụp X-quang ngực nghi ngờ hoặc dương tính, khuyến cáo chụp CT ngực và bụng với thì động mạch qua gan. Nếu kết quả chụp X-quang ngực dương tính, cũng nên chụp cộng hưởng từ (MRI) não.
Trong trường hợp nghi ngờ ung thư nguyên bào nuôi hoặc GTN sau thai kỳ không phải thai trứng, khuyến cáo thực hiện các xét nghiệm chuyên sâu hơn vì tỷ lệ di căn có thể > 40% ,23 Siêu âm vùng chậu nên được dùng trong đánh giá ban đầu để xác định mức độ bệnh vùng chậu sau khi khám lâm sàng. Các xét nghiệm khác bao gồm chụp CT ngực và bụng (với thì động mạch qua gan) và MRI não.
Chụp cắt lớp phát xạ positron/chụp cắt lớp vi tính (PET/CT) không có ưu thế hơn so với hình ảnh thông thường trong phân giai đoạn khối u. Tuy nhiên, chụp cắt lớp phát xạ positron/chụp cắt lớp vi tính có thể hữu ích trong các trường hợp mơ hồ có nồng độ hCG tăng cao.
GTN di căn chủ yếu theo đường máu. Phổi và âm đạo là những vị trí di căn phổ biến nhất; não, gan và các vị trí khác ít gặp hơn nhiều. Các triệu chứng di căn trong GTN có thể bao gồm chảy máu âm đạo, khó thở, ho, đau ngực, ho ra máu, đau bụng, đại tiện phân đen, đau đầu, thay đổi thị giác, chóng mặt, co giật hoặc khiếm khuyết thần kinh. Suy hô hấp, bụng cấp tính, thiếu máu nặng hoặc đột quỵ có thể do xuất huyết từ các khối u giàu mạch máu này. Mặc dù đánh giá lâm sàng nên được thực hiện, bao gồm khám bụng và vùng chậu, chống chỉ định sinh thiết các tổn thương nghi ngờ vì nguy cơ xuất huyết đáng kể. Sau khi mang thai, bất kỳ tình trạng chảy máu dai dẳng nào > 6 tuần sau sinh nên được kiểm tra bằng xét nghiệm hCG và siêu âm vùng chậu.
Phụ nữ nghi ngờ có thai trứng có thể được giới thiệu đến khoa phụ để đánh giá và xử trí. Phụ nữ nghi ngờ GTN nên được chuyển thẳng đến khoa ung bướu phụ khoa để được phân giai đoạn và điều trị khẩn cấp.
ĐIỀU TRỊ THAI TRỨNG
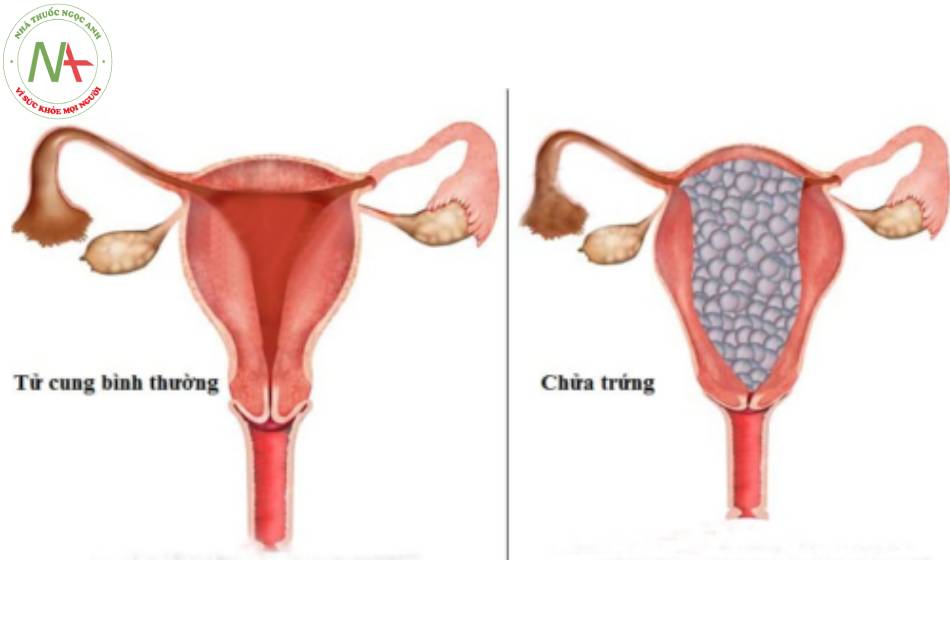
Dạng GTD phổ biến nhất là thai trứng. Lựa chọn quản lý ngoại khoa được khuyến cáo là hút buồng tử cung, nhung cắt bỏ tử cung là một lựa chọn thay thế có thể chấp nhận được. Các phương pháp phá thai nội khoa không được khuyến cáo.25 Phương pháp điều trị phải được điều chỉnh cho phù hợp với nhu cầu và mong muốn của bệnh nhân. Nếu cắt bỏ tử cung được lựa chọn, bệnh nhân phải lưu ý rằng họ vẫn sẽ cần phải theo dõi hCG nối tiếp vì GTN vẫn có thể xảy ra và cần điều trị toàn thân. Một phân tích gộp gần đây gợi ý rằng cắt bỏ tử cung thay vì hút buồng tử cung có thể là lựa chọn điều trị lý tưởng ở nhũng bệnh nhân trên 40 tuổi đã hoàn thành việc sinh con.26 Nếu các kết quả hình ảnh ủng hộ thai trứng, có thể xem xét cắt bỏ tử cung. Phẫu thuật phải được thực hiện bởi một phẫu thuật viên có kinh nghiệm. Tử cung phải được lấy bỏ nguyên vẹn (tức là không cắt nhở). Quá trình theo dõi cũng giống như những người hút buồng tử cung và điều trị phải dựa trên kết quả giải phẫu bệnh cuối cùng.
Hút buồng tử cung được thực hiện an toàn nhất trong phòng mổ, với nạo hút, lý tưởng là dưới hướng dẫn của siêu âm, để đảm bảo hút sạch hoàn toàn và giảm thiểu khả năng thủng tử cung do sơ ý. Đội ngũ bác sĩ gây mê và phòng mổ cần lưu ý khả năng xuất huyết đáng kể, cơn bão giáp, hoặc rối loạn chức năng hô hấp cấp tính do thuyên tắc nguyên bào nuôi. Chảy máu xối xả thường gặp khi cổ tử cung bị nong liên tiếp. Sau đó, một ống hút phù hợp với kích thước của tử cung được sử dụng để hút các chất trong tử cung và gửi đi làm giải phẫu bệnh. Dùng thìa nạo sắc chuyên dụng ở cuối thủ thuật để đảm bảo hút sạch hoàn toàn. Oxytocin có thể được dùng để làm tăng trương lực tử cung sau khi hút buồng tử cung. Xoa bóp đáy tử cung có thể là thích hợp nếu tử cung có kích thước > 12 đến 14 tuần. Chèn ép bằng bóng và thuyên tắc mạch đã được mô tả để bảo tồn tử cung trong các trường hợp xuất huyết nặng sau hút buồng tử cung. 27,28
Trước khi xuất viện, cần chỉ định bắt đầu ngay các biện pháp tránh thai hiệu quả. cần phải lên lịch theo dõi trước khi bệnh nhân xuất viện: yêu cầu định lượng hCG toàn phần trong huyết thanh hàng tuần (bắt đầu 2 tuần sau hút buồng tử cung và đều được thực hiện ở cùng một phòng xét nghiệm) và tái khám hậu phẫu từ 3 đến 6 tuần sau điều trị để xem xét kết quả giải bệnh lý và tuân thủ các biện pháp tránh thai, theo dõi hCG, và thực hiện khám vùng chậu để đảm bảo tử cung co hồi liên tục.
Globulin miễn dịch kháng D nên được tiêm cho tất cả các bệnh nhân Rh âm để dự phòng bất đồng miễn dịch. Mặc dù mô hoặc máu của thai nhi thường chỉ gặp ở thai trứng bán phần, nhưng không phải lúc nào cũng có thể phân biệt được thai trứng bán phần với thai trứng toàn phần trên lâm sàng tại thời điểm hút buồng tử cung. Điều trị dự phòng trong khoảng thời gian 72 giờ là thích hợp, globulin miễn dịch kháng D được khuyến cáo cho tất cả bệnh nhân Rh âm sau thủ thuật.
Không khuyến cáo hóa trị dự phòng cho tất cả bệnh nhân vì phần lớn bệnh nhân không cần thiết phải hóa trị toàn thân và các tác dụng bất lợi của nó và có thể gây kháng hóa trị ở những người tiếp tục phát triển bệnh dai dẳng. Hóa trị dự phòng có thể được xem xét ở một số bệnh nhân có nguy cơ cao, những người không có khả năng hoàn thành quá trình theo dõi.17,29-32
THEO DÕI THAI TRỨNG
Nếu kết quả giải phẫu bệnh khẳng định chẩn đoán thai trứng không có bệnh di căn, khuyến cáo theo dõi sát để đảm bảo bệnh thoái triển hoàn toàn. Định lượng hCG toàn phần trong huyết thanh nên được đo bằng các xét nghiệm có sẵn trên thị trường có khả năng đo nồng độ hCG < 5 mlU/mL và có khả năng phát hiện tất cả các dạng hCG, bao gồm beta-hCG, core hCG, C-terminal hCG, nicked-free beta, và beta core. Nên sử dụng cùng một xét nghiệm trong quá trình theo dõi để tránh sự khác biệt về kết quả giữa các phòng xét nghiệm. hCG nên được đo hàng tuần bắt đầu từ 2 tuần sau thủ thuật và tiếp tục cho đến khi không phát hiện được nồng độ hCG trong 3 tuần liên tiếp. Tiếp tục theo dõi hàng tháng trong 6 tháng đối với bệnh nhân có thai trứng toàn phần.33 Đối với bệnh nhân có thai trứng bán phần, hCG nên được đo 1 tháng sau kết quả không thể phát hiện được đầu tiên để xác nhận bệnh thoái triển.34 Có thể cân nhắc thời gian theo dõi ngắn hơn cho bệnh nhân có thai trứng toàn phần mong muốn có thai, đặc biệt phụ nữ > 35 tuổi và đặc biệt những người có tiền sử hiếm muộn. Một số nghiên cứu hồi cứu lớn thấy rằng nguy cơ GTN là < 1% sau thai trứng toàn phần hoặc bán phần khi hCG đạt đến mức không thể phát hiện được và nguy cơ thấp nhất ở những bệnh nhân có hCG trở về bình thường trong vòng 56 ngày đầu tiên.35-39 Phải sử dụng biện pháp tránh thai đáng tin cậy để tránh mang thai trong quá trình theo dõi vì mang thai sẽ gây khó khăn cho việc phiên giải kết quả hCG và làm phức tạp điều trị nếu có bệnh dai dẳng. Biện pháp tránh thai nội tiết là an toàn, có thể dùng ngay sau hút buồng tử’ cung và không làm tăng nguy cơ mắc bệnh dai dẳng. Thuốc tránh thai đường uống mang lại thêm lợi ích ức chế hormone hoàng thể hóa nội sinh, có thể cản trở việc đo hCG ở nồng độ thấp. 40 Nên tránh dùng các dụng cụ tránh thai trong tử cung cho đến khi nồng độ hCG huyết thanh trở về bình thường để giảm nguy cơ thủng tử cung.41
BỆNH NGUYÊN BÀO NUÔI THAI KỲ TRONG SONG THAI HOẶC ĐA THAI
Tỷ lệ mắc mới GTD trong song thai hoặc đa thai là rất hiếm. Nhũng bệnh nhân này tăng nguy cơ bị tiền sản giật, xuất huyết, nhiễm độc giáp, sinh non và GTN sau đó. Trong 72 trường hợp GTD mang song thai (trong số 12455 trường hợp GTD), 60% trường hợp tiếp tục thai kỳ dẫn đến sinh sống. Tiến triển thành GTN được quan sát thấy ở 46% bệnh nhân. Chấm dứt thai kỳ chủ động không làm thay đổi nguy cơ GTN sau đó. Chấm dứt thai kỳ vì các biến chứng như tiền sản giật hoặc chảy máu nhiều có khả năng cao tiến triển thành GTN, cũng như những người có nồng độ hCG cao hơn.42 Cần thảo luận cân bằng về nguy cơ và lợi ích khi tiếp tục thai kỳ, và nếu thai kỳ tiếp tục, phải được quản lý chung bởi bác sĩ chuyên khoa ung thư phụ khoa và chuyên gia y học mẹ và bào thai.
MANG THAI SAU KHI BỊ BỆNH NGUYÊN BÀO NUÔI THAI KỲ
Nguy cơ GTD tái phát là khoảng 1/100, hoặc cao hơn xấp xỉ 10 lần so với bệnh nhân không có tiền sử GTD trước đó. Ở những lần mang thai sau đó, khuyến cáo siêu âm sớm để khẳng định thai trong tử cung bình thường. Lúc sinh cần được kiểm tra kỹ lưỡng nhau thai và gửi làm giải phẫu bệnh nếu có bất thường lâm sàng. Trong trường hợp thai lạc chỗ hoặc phá thai dưới bất kỳ hình thức nào, các sản phẩm thụ thai phải được gửi đi làm giải phẫu bệnh. Nên giới thiệu bệnh nhân đi tư vấn và xét nghiệm di truyền khi chẩn đoán thai trứng tái phát để loại trừ thai trứng tái phát có tính chất gia đình.
CHẨN ĐOÁN U NGUYÊN BÀO NUÔI THAI KỲ SAU THAI TRỨNG
Trong quá trình theo dõi sau thai trứng, bệnh dai dẳng được chẩn đoán khi có bất kỳ tiêu chuẩn nào sau đây:
- Nồng độ hCG huyết thanh đang tăng, được xác định là tăng > 10% so với giá trị trước đó trong 2 tuần liên tiếp (được đo vào các ngày 1, 7 và 14) 43
- Nồng độ hCG huyết thanh bình nguyên, được xác định là thay đổi < 10% so với giá trị trước đó trong 3 tuần liên tiếp (được đo vào các ngày 1,7, 14 và 21)43
- Chẩn đoán giải phẫu bệnh ung thư nguyên bào nuôi (luu ý: không khuyến cáo sinh thiết lại)43
- Bằng chứng về bệnh di căn 44
- Nồng độ hCG huyết thanh > 20.000 mlU/mL > 4 tuần sau nạo hút 44
LƯU Ý: Tiêu chuẩn “hCG tăng cao trong 6 tháng sau nạo hút” không còn được liệt kê. Dường như là an toàn để theo dõi nồng độ hCG > 6 tháng miễn là nồng độ hCG đang giảm.
Bệnh nhân được chẩn đoán GTN nên được quản lý chủ yếu bởi bác sĩ chuyên khoa ung bướu phụ khoa hoặc bác sĩ chuyên khoa ung bướu nội khoa quan tâm đến bệnh ung bướu phụ khoa. Kết cục của bệnh nhân được cải thiện phụ thuộc vào việc chuyển tuyến và chuyển chăm sóc kịp thời để phân giai đoạn, chấm điểm nguy cơ và điều trị.
Trong quá trình theo dõi hCG huyết thanh sau thai trứng, phải đặc biệt xem xét để phát hiện nồng độ hCG thấp dai dẳng, một dấu hiệu có thể là GTN thực sự, “GTD yên lặng”, sản xuất hCG từ tuyến yên hoặc hCG dương tính giả (tức là, “hCG bóng ma”). Nồng độ hCG thấp dai dẳng được định nghĩa là hCG < 1000 mlU/mL trong > 3 tháng mà không có xu hướng tăng hoặc giảm rõ ràng và không có bằng chứng của bệnh.46 Đo tỷ lệ hyperglycosylated hCG (hCG-H) đã được đề xuất để phân biệt bệnh ác tính và GTD yên lặng vì đơn bào nuôi xâm lấn chịu trách nhiệm chính trong việc sản xuất hCG-H.47 Đo tỷ lệ tiểu đơn vị beta tự do đã được đề xuất như một phương tiện để xác định bệnh nhân có u nguyên bào nuôi nơi nhau bám 48 Việc sử dụng hCG-H và beta hCG tự do cần được xác nhận giá trị trong các nghiên cứu tiến cứu lớn để xác định vai trò của chúng trong việc quản lý GTN 49 Các trường hợp gợi ý bệnh ác tính phải được chuyển đến khoa ung thư phụ khoa để đánh giá thêm và quản lý. Bệnh nhân bị GTD yên lặng có hiệu giá hCG khoảng 55 mlU/mL và không cần xử trí tích cực ngoài việc theo dõi hCG thường xuyên. Sản xuất hCG từ tuyến yên là một hiện tượng sinh học được quan sát thấy ở một số phụ nữ quanh tuổi mãn kinh và mãn kinh và trung bình tương ứng là 10-11 mlU/mL và < 35 mlU/mL.50,51 Nó có thể bị ức chế bằng cách sử dụng thuốc tránh thai có chứa estrogen trong 3 tuần hoặc được phát hiện trong phòng thí nghiệm vì nó bị sulfat hóa. hCG bóng ma là kết quả xét nghiệm dương tính giả do kháng thể dị ái lưu hành. Hiện tượng này có thể được xác nhận bằng phân tích nước tiểu, đặc biệt là âm tính với hCG (kháng thể dị ái quá lớn để có trong nước tiểu); bằng cách sử dụng thử nghiệm pha loãng; hoặc được thực hiện bởi một xét nghiệm hCG chuyên biệt. Trong trường hợp không có thai hoặc bằng chứng bệnh ác tính, những phụ nữ có nồng độ hCG trong huyết thanh và nước tiểu cao dai dẳng (tức là, đã loại trù’ hCG dương tính giả) nên được theo dõi dài hạn dưới sự giám sát của chuyên gia quản lý GTN. Bất chấp các kết quả xét nghiệm ban đầu âm tính, 1/5 trong số nhũng phụ nữ này sẽ phát triển GTN vài tháng hoặc vài năm sau biểu hiện ban đầu. Trong trường hợp không xác định được bệnh, cần tránh việc điều trị.52
PH N GIAI ĐOẠN VÀ CHẤM ĐIỂM NGUY CƠ U NGUYÊN BÀO NUÔI THAI KỲ
Sau khi chẩn đoán GTN, bệnh nhân được phân giai đoạn và chấm điểm nguy cơ để lập kế hoạch điều trị. Bệnh thai trứng xâm lấn và ung thư nguyên bào nuôi thường rất nhạy cảm với hóa trị, trong khi u nguyên bào nuôi nơi nhau bám và u nguyên bào nuôi dạng biểu mô đáp ứng kém hơn nhiều. Trong cả hai trường hợp này, điều trị có thể cần kết hợp cả liệu pháp toàn thân và phẫu thuật.
Tối thiểu, bệnh nhân nên được chụp X-quang ngực và siêu âm vùng chậu, lý tưởng nhất là có Doppler (chỉ số xung Doppler có thể là một yếu tố dự báo độc lập về khả năng đề kháng đơn hóa trị methotrexate trong các trường hợp mắc bệnh nguy cơ thấp). 53 Mặc dù có tới 41% bệnh nhân chụp X-quang ngực bình thường có thể có bằng chứng vi di căn (< 6 mm) trên CT, không cần thực hiện thêm các chẩn đoán hình ảnh khác ở bệnh nhân có nguy cơ thấp vì di căn < 2 cm không ảnh hưởng đến đề kháng hóa trị hoặc thời gian thuyên giảm.54 Nếu di căn phổi được xác định trên X-quang ngực hoặc GTN được xác định sau thai kỳ không phải thai trứng hoặc nếu chẩn đoán giải phẫu bệnh là ung thư nguyên bào nuôi, u nguyên bào nuôi nơi nhau bám hoặc u nguyên bào nuôi dạng biểu mô hoặc trường hợp tái phát GTN đã được chẩn đoán trước đó, cần chụp CT ngực, bụng và vùng chậu cùng với MRI não. MRI vùng chậu cũng có thể được xem xét. cần chụp CT bụng thì động mạch để xác định chính xác di căn gan.
Các triệu chứng thần kinh có ở 87% đến 100% bệnh nhân di căn não. Nếu hình ảnh não không rõ ràng, chọc dịch não tủy thắt lưng có thể giúp chẩn đoán nếu tỷ lệ hCG trong dịch não tủy/huyết thanh > 1:60. Trong một loạt 27 bệnh nhân có di căn hệ thần kinh trung ương, 3 bệnh nhân (11,1%) có di căn hệ thần kinh trung ương là vị trí duy nhất của bệnh. Do đó, đối với những bệnh nhân bị ung thư nguyên bào nuôi không phải thai trứng, khuyến cáo chẩn đoán hình ảnh não bất kể vị trí thay thế của bệnh hoặc không có triệu chứng. Table 1 là bảng phân loại giai đoạn GTN của Liên đoàn Sản phụ khoa Quốc tế (FIGO), áp dụng cho tất cả các thể bệnh, bao gồm thai trứng xâm lấn, ung thư nguyên bào nuôi, u nguyên bào nuôi nơi nhau bám và u nguyên bào nuôi dạng biểu mô.
Bệnh nhân có thai trứng xâm lấn hoặc ung thư nguyên bào nuôi được coi là có nguy cơ thấp hoặc cao dựa trên hệ thống chấm điểm tiên lượng của Tổ chức Y tế Thế giới (WHO) được sửa đổi bởi FIGO. Bệnh nhân mắc bệnh nguy cơ thấp (điểm từ 0 đến 6) được đề nghị đơn hóa trị hoặc cắt bỏ tử cung (trong trường hợp không có bằng chứng của bệnh di căn). Bệnh nhân mắc bệnh nguy cơ cao (điểm > 7) được đề nghị đa hóa trị, ưu tiên dưới sự giám sát của bác sĩ chuyên khoa ung bướu có chuyên môn và quan tâm đặc biệt trong quản lý bệnh này. Phẫu thuật được tiến hành cho một số ít bệnh nhân kháng thuốc hoặc các biến chứng liên quan đến bệnh. Bệnh nhân có điểm nguy cơ > 12 được coi là nguy cơ cực cao với nguy cơ tử vong tăng, đặc biệt là tử vong sớm.57 Bệnh nhân có nguy cơ cực cao, thường có biểu hiện di căn gan và/hoặc não, cần được điều trị chuyên khoa, tốt nhất là tại trung tâm có chuyên môn về quản lý GTN với đội ngũ đa chuyên khoa (ví dụ: X quang can thiệp, phẫu thuật lồng ngực và thần kinh, đơn vị chăm sóc tích cực). Table 2 trình bày hệ thống chấm điểm tiên lượng sửa đổi của WHO được điều chỉnh bởi FIGO. Lưu ý, chỉ những tổn thương phổi có thể nhìn thấy trên X-quang ngực mới được tính điểm. Hệ thống chấm điểm tiên lượng của WHO không áp dụng cho u nguyên bào nuôi nơi nhau bám hoặc u nguyên bào nuôi dạng biểu mô, được xem xét riêng.
ĐIỀU TRỊ BỆNH NGUYÊN BÀO NUÔI NGUY CƠ THẤP
Các hóa chất chính được sử dụng trong đơn hóa trị cho GTN nguy cơ thấp là methotrexate và dactinomycin (Table 3). Trên toàn cầu, có một số phác đồ đang được sử dụng, bao gồm 5-tluorouracil, được sử dụng phổ biến ở Trung Quốc với hiệu quả tốt và độc tính thấp. Các cuộc tranh luận đang diễn ra về phác đồ hóa trị hiệu quả nhất, với các cân nhắc là tỷ lệ khỏi bệnh chính, sự thuận tiện của bệnh nhân và chất lượng cuộc sống, hồ sơ tác dụng bất lợi và chi phí. Nhóm Ung thư Phụ khoa đã tiến hành một thử nghiệm ngẫu nhiên có đối chứng về dactinomycin (1,25 mg/m2, liều tối đa 2 mg) được dùng 2 tuần một lần (tức là hai tuần một lần) so với methotrexate hàng tuần (30 mg/m2) và kết luận rằng dactinomycin hai tuần một lần thể hiện tính ưu việt với tỷ lệ đáp ứng hoàn toàn là 70% so với 53% của methotrexate (P = 0,01) ,58 Tỷ lệ này được so sánh với tỷ lệ đáp ứng hoàn toàn là 70,8% của methotrexate hàng tuần (50 mg/m2) và 69,5% của phác đồ methotrexate-folinic acid 8 ngày trong một nghiên cứu thuần tập không ngẫu nhiên. Nghiên cứu của Nhóm ung thư phụ khoa (GOG 275) so sánh dactinomycin hai tuần một lần với methotrexate 5 hoặc 8 ngày cho thấy tỷ lệ đáp ứng hoàn toàn và hồ sơ độc tính giữa các phác đồ tương tự nhau (với tỷ lệ rụng tóc tương tự), những nghiên cứu đã bị đóng sớm do các vấn đề tích lũy.60 Nhìn chung, không có sự khác biệt lớn trong hồ sơ độc tính của methotrexate và dactinomycin. Các tác dụng bất lợi thường gặp nhất là buồn nôn, mệt mỏi và thiếu máu. Tuy nhiên, rụng tóc phổ biến hơn với dactinomycin, trong khi viêm miệng phổ biến hơn với methotrexate.61 cần phải nghiên cứu thêm để xác định liệu có một phác đồ ưu tiên cho những bệnh nhân có nguy cơ thấp hay không và liệu những phác đồ khác, như kết hợp methotrexate và dactinomycin, có thể chứng minh có lợi ở một số bệnh nhân được lựa chọn hay không.
Những bệnh nhân mắc bệnh giai đoạn I đã hoàn thành việc sinh con có thể được đề nghị cắt bỏ tử cung, mặc dù có thể vẫn cần phải điều trị toàn thân nếu theo dõi sau phẫu thuật cho thấy bệnh dai dẳng. Một nghiên cứu hồi cứu gần đây cho thấy 82% phụ nữ có GTN nguy cơ thấp không di căn được điều trị cắt bỏ tử cung không cần hóa trị liệu cún nguy.62 Bệnh nhân < 35 tuổi có điểm tiên lượng dựa trên hệ thống chấm điểm tiên lượng được sửa đổi của WHO là < 4 cũng có thể được đề nghị nạo lần hai. Cách tiếp cận này có thể giúp hơn 40% bệnh nhân không cần phải hóa trị và có tỷ lệ thấp các biến chứng như thủng tử cung hoặc xuất huyết cấp tính. Tác động của cách tiếp cận này đối với khả năng sinh sản trong tương lai thì không rõ, và gia tăng quan ngại về nguy cơ dính tử cung với thủ thuật thứ hai.
Bệnh nhân đang điều trị cần theo dõi định lượng hCG huyết thanh hàng tuần để xác định kịp thời sự phát triển của bệnh kháng thuốc. Nên sử dụng xét nghiệm hCG có thể phát hiện tất cả các dạng hCG (ví dụ: beta-hCG, core hCG, C-terminal hCG, nicked- free beta, beta core) và khuyến cáo cùng một xét nghiệm (tức là cùng một phòng xét nghiệm ) để tránh sự khác biệt về kết quả giữa các phòng xét nghiệm. Bệnh kháng thuốc được chẩn đoán nếu nồng độ hCG tăng hoặc bình nguyên, theo tiêu chuẩn FIGO. Trong trường hợp kháng thuốc, phân lại giai đoạn và chấm điểm nguy cơ sẽ dẫn đến việc chuyển sang đơn hóa trị thay thế (điểm nguy cơ sửa đổi < 6) hoặc đa hóa trị. Điều trị được tiếp tục cho đến khi nồng độ hCG huyết thanh trở về bình thường, sau đó là 2 đến 3 chu kỳ (4 đến 6 tuần) củng cố.65 Tỷ lệ khỏi bệnh chung cho những bệnh nhân mắc bệnh nguy cơ thấp, kể cả với liệu pháp ban đầu hoặc sau đó, đều gần 100%.
Bệnh nhân có nguy cơ mắc bệnh kháng thuốc bao gồm những người có khối u tăng sinh mạch được thấy trên siêu âm Doppler,53 người có điểm tiên lượng theo WHO sửa đổi là 5 hoặc 6,57 người có nồng độ hCG trước khi điều trị > 400 000 mlU/mL, 65 người bị ung thư nguyên bào nuôi không phải thai trứng và những người có đáp ứng dưới mức tối ưu được xác định thông qua toán đồ/ phân tích động học hCG .66 Nguy cơ kháng methotrexate ở những bệnh nhân có điểm tiên lượng theo WHO sửa đổi là 6 và chỉ số xung động mạch tử cung < 1 là 100% so với 20% ở bệnh nhân có chỉ số xung động mạch tử cung > 1 (P <0,0001) ,43 Những phát hiện này rất hữu ích cho mục đích tiên lượng và tư vấn; tuy nhiên, cần phải nghiên cứu thêm để xác định xem những bệnh nhân nào trong số này có thể được hưởng lợi từ đa hóa trị liệu đầu tay.
ĐIỀU TRỊ BỆNH NGUYÊN BÀO NUÔI NGUY CƠ CAO
GTN nguy cơ cao được điều trị bằng hóa trị liệu kết hợp. Hai phác đồ thường được sử dụng với tỷ lệ khỏi bệnh cao và hồ sơ độc tính chấp nhận được là etoposide, methotrexate, dactinomycin, cyclophosphamide, vincristine (EMA-CO) và etoposide, methotrexate, dactinomycin, etoposide, cisplatin (EMA-EP). Các phác đồ này và các phác đồ thay thế được liệt kê trong Table 4. Các tác dụng độc hại cần quan tâm là suy tủy, có thể đáp úng với yếu tố kích thích dòng bạch cầu hạt (granulocyte colonystimulating factor) ; rụng tóc; viêm niêm mạc; và phát triển bệnh lý ác tính thứ hai. Tiếp tục theo dõi hCG hàng tuần cho đến khi nồng độ hCG huyết thanh trở về bình thường. Với bệnh nguy cơ cao, nên điều trị củng cố với 3 chu kỳ (6 tuần) hóa trị sau khi hCG trở về bình thường.
Nhũng bệnh nhân có nguy cơ cao với di căn gan và não hoặc nhũng bệnh nhân có số điểm theo WHO được sửa đổi bởi FIGO56 > 12 được coi là có nguy cơ cực cao. Nhũng bệnh nhân này có thể chết trong quá trình điều trị do xuất huyết cấp tính hoặc do biến chứng của bệnh lan rộng. Hóa trị liệu cảm ứng liều thấp với etoposide và cisplatin trong 1 đến 3 tuần, sau đó là hóa trị liệu EMA-EP hoặc EMA-CO, đã được chúng minh là giảm tử vong sớm ở nhũng bệnh nhân có nguy cơ cực cao (Table 4). Tiếp tục hóa trị liệu củng cố trong 8 tuần sau khi hCG huyết thanh trở về bình thường. Mặc dù không có dữ liệu ngẫu nhiên nào so sánh các phác đồ ở nhũng bệnh nhân có nguy cơ cực cao, những người bị di căn gan và não có thể hưởng lợi khi EMA-EP là phác đồ đa hóa trị đầu tay sau hóa trị liệu cảm ứng.67
Có thể cần các điều trị bổ trợ cho liệu pháp toàn thân để giải quyết các biến chứng đe dọa tính mạng và đạt được sự thuyên giảm. Thuyên tắc nội mạch bằng X quang can thiệp có thể được yêu cầu để kiểm soát xuất huyết ồ ạt.68 Có thể cần xạ trị lập thể đối với các di căn hệ thần kinh trung ương để ngăn ngừa xuất huyết hoặc suy giảm thần kinh, hoặc điều trị các ổ bệnh kháng thuốc. Tương tự, phẫu thuật phù hợp có thể được yêu cầu để ngăn ngừa tình trạng xấu đi cấp tính (ví dụ, phẫu thuật mở sọ để giải quyết tình trạng tăng áp lực nội sọ) hoặc để điều trị các ổ bệnh kháng thuốc (ví dụ, phẫu thuật mở ngực với cắt bỏ nhu phổi hình chêm). Khả năng khỏi bệnh ở những bệnh nhân có nguy cơ cao là 70% đến 95%. Trước đây, những người mắc bệnh nguy cơ cực cao có nguy cơ tử vong sớm, với tỷ lệ sống sót chỉ từ 25% đến 50%. Nếu được điều trị bằng hóa trị liệu cảm ứng, những bệnh nhân có nguy cơ cực cao này hiện có tiên lượng tương tự như những người mắc bệnh nguy cơ cao.
ĐIỀU TRỊ U NGUYÊN BÀO NUÔI NƠI NHAU BÁM VÀ U NGUYÊN BÀO NUÔI DẠNG BIỂU MÔ
Các khối u nguyên bào nuôi nơi nhau bám và u nguyên bào nuôi dạng biểu mô đáng chú ý vì chúng tăng trưởng chậm hơn, di căn muộn và khả năng kháng hóa trị liệu cao hơn. Những khối u này tiết ra mức hCG thấp hơn vì chúng có nguồn gốc từ nguyên bào nuôi trung gian. Hệ thống phân giai đoạn FIGO được sử dụng để mô tả mức độ của bệnh. Phân giai đoạn cần chụp CT ngực, bụng và vùng chậu cũng như siêu âm Doppler vùng chậu, MRI não, và nếu hình ảnh não không rõ ràng, chọc dịch não tủy thắt lưng để đo tỷ số hCG dịch não tủy/huyết thanh. Những người mắc bệnh giai đoạn I nên phẫu thuật, bao gồm cắt bỏ tử cung đơn giản, cân nhắc bảo tồn buồng trứng. Sự cần thiết của việc nạo vét hạch là không rõ ràng. Tỷ lệ di căn hạch là 5,9% trong một loạt 286 trường hợp.70 Tám tuần điều trị bổ trợ với EMA-EP hoặc paclitaxel-cisplatin / paclitaxel etoposide (TP/TE) nên được áp dụng cho những người có các yếu tố nguy cơ như mang thai trước đó hơn 48 tháng trước khi chẩn đoán.71 Nên kết hợp hóa trị với EMA-EP hoặc TP/TE và phẫu thuật cho bệnh nhân mắc bệnh giai đoạn II đến IV, mặc dù khả năng đáp ứng thấp. Bệnh còn sót lại đơn độc khi được được xác định ở những bệnh nhân như vậy cần phải cắt bỏ, và hóa trị liệu củng cố trong 8 tuần sau khi hCG trở về bình thường được khuyến cáo.
THEO DÕI SAU ĐIỀU TRỊ U NGUYÊN BÀO NUÔI THAI KỲ
Khi hoàn thành liệu pháp, hình ảnh được thực hiện để làm cơ sở so sánh với những lần sau. Có thể thấy các tổn thương còn sót lại, đặc biệt ở phổi, nhưng không cần cắt bỏ hoặc điều trị lại nếu nồng độ hCG vẫn không thể phát hiện được.72 Nguy cơ tái phát khoảng 3% và tái phát thường xảy ra trong 12 tháng đầu theo dõi.73 hCG huyết thanh được theo dõi hàng tuần trong 4 đến 6 tuần đầu tiên và sau đó hàng tháng trong tối thiểu 12 đến 24 tháng tương ứng với bệnh nguy cơ thấp và cao. Nhũng bệnh nhân có u nguyên bào nuôi nơi nhau bám và u nguyên bào nuôi dạng biểu mô có thể cần theo dõi lâu dài. Nên tránh mang thai trong thời gian theo dõi bằng cách sử dụng biện pháp tránh thai đáng tin cậy, bao gồm các biện pháp nội tiết tố và dụng cụ từ cung. Đặt dụng cụ tử cung chỉ có thể được chấp nhận sau khi hCG trở về bình thường. Một số nghiên cứu hạn chế đã được thực hiện về kết cục thai kỳ sau khi điều trị GTN bằng hóa trị.74,75 Một số nghiên cứu báo cáo nguy cơ kết cục bất lợi cao hơn ở thai kỳ được thụ thai < 6 tháng sau khi hoàn thành hóa trị, như sẩy thai, thai trứng tái phát, chuyển dạ sinh non, tiền sản giật, và bệnh nhau thai.75 Những nguy cơ này dường như thấp hơn đối với những thai kỳ được thụ thai > 1 năm sau khi hoàn thành hóa trị.
Mặc dù tiếp xúc với hóa trị liệu EMA-CO có thể dẫn đến mãn kinh sớm hơn, nhưng khả năng sinh sản dường như không bị ảnh hưởng và không tăng nguy cơ mắc dị tật bẩm sinh. Tăng nguy cơ phát triển ung thư thứ hai (ví dụ: bệnh bạch cầu, ung thư vú, ung thư đại tràng, u hắc tố), nhấn mạnh việc cần theo dõi lâu dài và đăng ký tập trung.
CÓ THAI TRONG THỜI GIAN THEO DÕI BỆNH NGUYÊN BÀO NUÔI THAI KỲ
Đôi khi, có thai sẽ xảy ra trong thời gian theo dõi sau nạo hút thai trứng hoặc điều trị GTN. Vì hCG huyết thanh là chất chỉ điểm chính được sử dụng trong theo dõi, mang thai trong thời gian theo dõi đặt ra một thách thức lâm sàng đáng kể. Quản lý những trường hợp này phải được cá thể hóa và thảo luận cân bằng về nguy cơ và lợi ích khi tiếp tục thai kỳ. Khuyến cáo giới thiệu đến chuyên khoa ung bướu phụ khoa và y học mẹ – bào thai. Tùy thuộc vào hoàn cảnh, lựa chọn và nguy cơ tái phát bệnh của từng bệnh nhân để đưa ra kế hoạch quản lý phù hợp. Nếu bệnh nhân mong muốn tiếp tục thai kỳ, khuyến cáo theo dõi chặt chẽ với hCG huyết thanh và siêu âm để xác định bằng chứng sớm của GTN.
U NGUYÊN BÀO NUÔI THAI KỲ TÁI PHÁT
GTN tái phát cần phân lại giai đoạn với chụp CT đầu, ngực, bụng và vùng chậu. Chụp cắt lóp phát xạ positron fluorodeoxyglucose có thể hữu ích trong việc xác định vị trí ổ bệnh kháng thuốc / tái phát và điều trị đích.77 GTN tái phát nên được chấm lại điểm nguy cơ bằng cách sử dụng hệ thống WHO sửa đổi được điều chỉnh bởi FIGO56 và các lựa chọn điều trị nguy cơ thấp hoặc cao. Đối với bệnh nguy cơ cao, các lựa chọn hóa trị bao gồm EMA-EP; TP / TE, ifosfamide, carboplatin và etoposide (ICE); và BEP, như được liệt kê trong Table 4. Đối với bệnh đa kháng thuốc, các liệu pháp mới có thể được chỉ định, bao gồm các thuốc nhắm đích như programmed death-ligand 1 inhibitors hoặc human epidermal growth factor receptor 2/neu receptor antagonists.78 Một thử nghiệm lâm sàng của avelumab trong GTN kháng hóa trị đang được thực hiện. Có thể cần phẫu thuật cắt bỏ đối với các ổ đơn độc của khối u dai dẳng. Thời gian bán thải của hCG khoảng 48 giờ và do đó có thể được sử dụng để đánh giá đáp ứng cấp tính với bất kỳ can thiệp phẫu thuật nào. Hóa trị liều cao kết hợp với ghép tủy xương tự thân hoặc tế bào gốc cũng có thể được xem xét. Bệnh nhân mắc bệnh đa kháng thuốc có nguy cơ tử vong liên quan đến bệnh, và do đó, chăm sóc chuyên biệt, phù hợp là bắt buộc để đạt được kết cục tốt nhất có thể.