Thông Tin Thuốc, Bệnh huyết học
Giảm bạch cầu trung tính do các thuốc không độc tế bào
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
Biên soạn: Dược sĩ Lê Minh Hồng, Khoa Dược Bệnh Viện 108.
Hiệu đính: ThS. Nguyễn Thị Thu Thủy, Bộ môn Dược lâm sàng, Đại học Dược Hà Nội.
1. Giới thiệu chung
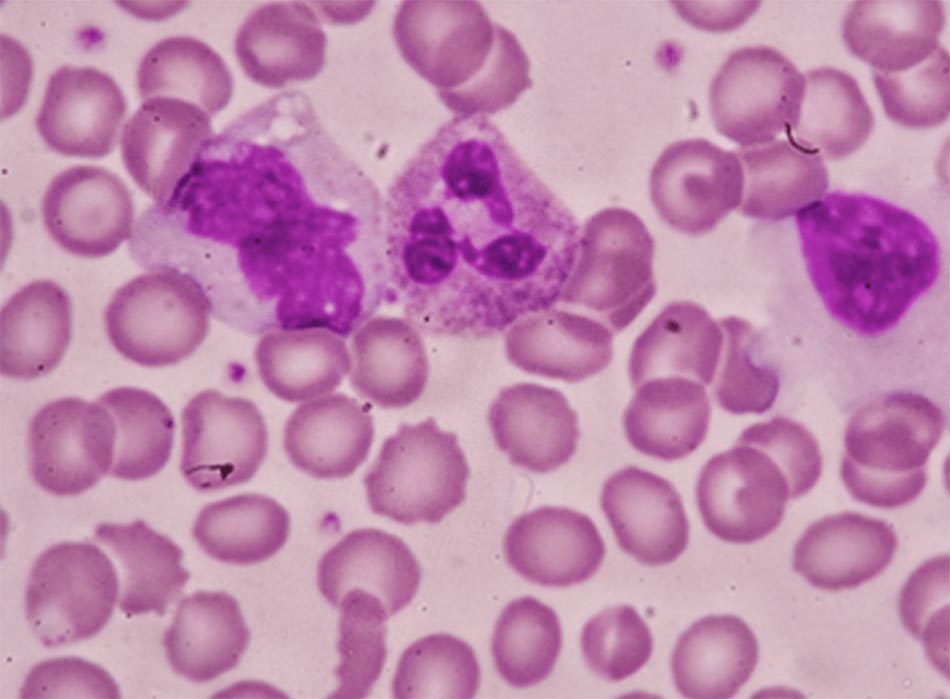
Bạch cầu trung tính có vai trò quan trọng trong việc chống lại các tác nhân lây nhiễm từ bên ngoài như vi khuẩn và nấm. Giảm bạch cầu trung tính có thể dẫn đến tình trạng nhiễm khuẩn nặng, ảnh hưởng nghiêm trọng đến tình trạng lâm sàng của bệnh nhân.
Giảm bạch cầu trung tính do thuốc có thể do giảm sản xuất hoặc tăng phá hủy tế bào bạch cầu trung tính. Giảm sản xuất thường là do các thuốc hóa trị liệu gây ức chế tế bào tiền thân ở tủy xương. Tăng phá hủy xảy ra trong trường hợp giảm bạch cầu trung tính do thuốc không độc tế bào (Non–chemotherapy idiosyncratic drug–induced neutropenia – IDIN) là phản ứng bất lợi đặc trưng của thuốc không độc tế bào. IDIN một trong những nguyên nhân dẫn đến tăng chi phí điều trị, làm nặng thêm tình trạng bệnh và tăng tỷ lệ tử vong ở bệnh nhân [1].
2. Các thuật ngữ và định nghĩa
Bạch cầu hạt bao gồm bạch cầu ưa base, bạch cầu ưa acid và bạch cầu trung tính. Bạch cầu trung tính chiếm nhiều nhất trong số lượng bạch cầu hạt và tổng số lượng tế bào bạch cầu trong máu.
Giảm bạch cầu trung tính được định nghĩa là số lượng bạch cầu trung tính tuyệt đối (absolute neutrophil count – ANC) < 1,5 G/L [1],[3]. Nguy cơ nhiễm khuẩn sẽ tăng lên khi ANC giảm xuống dưới 1,0 G/L, và có ý nghĩa lâm sàng nhất khi ANC < 0,5 G/L [1],[3]. Các thuật ngữ giảm bạch cầu (leukopenia) và giảm bạch cầu hạt (granulocytopenia) vẫn thường được sử dụng thay thế cho thuật ngữ giảm bạch cầu trung tính (neutropenia), mặc dù giữa chúng có sự khác biệt nhỏ [3].
Giảm bạch cầu trung tính nghiêm trọng được định nghĩa là khi ANC < 0,5 G/L, bệnh nhân giảm ANC < 0,1 G/L có nguy cơ nghiêm trọng làm tăng mức độ nặng của bệnh và tử vong do nhiễm khuẩn [1]. Mất bạch cầu hạt (agranulocytopenia) theo nghĩa đen là không có bạch cầu hạt (ANC = 0), tuy nhiên thuật ngữ này vẫn thường được sử dụng để chỉ giảm bạch cầu trung tính mức độ nghiêm trọng (ANC < 0,1; < 0,2 hoặc thậm chí < 0,5 G/L) [3].
3. Cơ chế
Các thuốc gây độc tế bào làm giảm bạch cầu trung tính do tính chất dược lý – dược lực của chúng. Do đó, những phản ứng này là phụ thuộc vào liều, có thể dự đoán trước được và có thể dự phòng. Trái lại, IDIN, gây ra bởi các thuốc không độc tế bào, là không thể dự đoán trước, không phụ thuộc vào liều và xảy ra với tần suất hiếm gặp nên việc thực hiện các nghiên cứu về cơ chế gây ra IDIN còn nhiều khó khăn. Tuy nhiên, cơ chế qua trung gian miễn dịch thường được đề xuất, mặc dù còn thiếu các bằng chứng mức độ mạnh ủng hộ cơ chế này.
Cơ chế miễn dịch phù hợp với biểu hiện lâm sàng của IDIN, bao gồm (1) thời gian xuất hiện muộn sau khi phơi nhiễm với thuốc, thường là 1 – 6 tháng [1],[2] tính từ liều khởi đầu (thời gian cần thiết để hình thành đáp ứng miễn dịch), (2) phản ứng khởi phát sớm khi dùng lại cùng một loại thuốc ở những bệnh nhân đã gặp IDIN trước đó (phù hợp với tính ghi nhớ của hệ miễn dịch) và (3) tăng bạch cầu ái toan và sự có mặt của các kháng thể kháng bạch cầu trung tính đặc hiệu với thuốc (drug-dependent neutrophil antibody) hoặc kháng thể tự miễn (auto antibody) [2].
Hai cơ chế qua trung gian miễn dịch thường được mô tả là giả thuyết hapten và giả thuyết tín hiệu nguy hiểm.
- Giả thuyết hapten: Hapten là các phân tử trọng lượng phân tử thấp không có khả năng tự tạo ra phản ứng miễn dịch, nhưng khi kết hợp với một phân tử vận chuyển lớn (thường là một protein) thì sẽ có khả năng tạo ra phản ứng miễn dịch. Thuốc khi đi vào cơ thể thường được chuyển hóa qua gan tạo thành các chất chuyển hóa tan trong nước, sau đó được thải trừ qua nước tiểu tránh tích lũy và gây độc tế bào. Mặc dù đa phần lượng thuốc chuyển hóa qua gan, cũng có một lượng thuốc chuyển hóa qua các tế bào khác, bao gồm bạch cầu trung tính. Các enzym trong bạch cầu trung tính chuyển hóa thuốc thành các chất chuyển hóa tái hoạt động (hapten) liên kết chặt chẽ với glycoprotein màng tế bào bạch cầu trung tính tạo thành các phức hợp hapten – protein. Phức hợp này sẽ kích thích sản xuất kháng thể đặc hiệu với thuốc, sau đó kháng thể đặc hiệu sẽ gắn với phức hợp hapten – protein màng tế bào gây tiêu diệt hoặc phá hủy tế bào bạch cầu trung tính.
- Giả thuyết tín hiệu nguy hiểm: Để kích thích sản xuất kháng thể đặc hiệu cần có các tế bào trình diện kháng nguyên (APC) trình diện các protein cho tế bào T hỗ trợ (tế bào Thelp) (tín hiệu 1). Nhưng APC cần được hoạt hóa bởi tín hiệu nguy hiểm (tín hiệu 2), nếu không có tín hiệu 2 thì sẽ xảy ra sự dung nạp miễn dịch. Tín hiệu 2 là tín hiệu nguy hiểm được sản xuất ra bởi các tế bào bị tổn thương (tế bào bạch cầu trung tính bị stress hoặc các tế bào khác) và kích hoạt đồng thời APC cùng tế bào Thelp. Như vậy, cả cơ chế hapten và cơ chế tín hiệu nguy hiểm đều cần thiết để tạo ra đáp ứng miễn dịch gây IDIN (hình 1).
![Giảm bạch cầu trung tính do các thuốc không độc tế bào 6 Hình 1. Cơ chế miễn dịch gây giảm bạch cầu trung tính do thuốc không độc tế bào [1]](https://nhathuocngocanh.com/wp-content/uploads/2022/01/hinh-1.jpeg)
4. Các thuốc liên quan IDIN
4.1 Các nhóm thuốc thường được báo cáo liên quan đến IDIN:
Đã có nhiều thuốc không độc tế bào được báo cáo liên quan đến IDIN, trong đó các nhóm thuốc có tần suất báo cáo thường xuyên hơn bao gồm các thuốc điều trị rối loạn tuyến giáp, các thuốc chống loạn thần không điển hình, các thuốc kháng sinh – kháng virus và các thuốc sinh học [1],[2]:
- Trong số các thuốc điều trị rối loạn tuyến giáp, propylthiouracil được báo cáo có tỷ lệ cao nhất liên quan đến mất bạch cầu hạt [2].
- Trong số các thuốc chống loạn thần không điển hình, clozapin là thuốc được báo cáo nhiều nhất liên quan đến IDIN. Clozapin cũng có thể được xem là thuốc có khả năng liên quan đến IDIN cao nhất trong tất cả các thuốc nói chung [1],[2]. Vì vậy, nhiều quốc gia đã triển khai các biện pháp dự phòng IDIN do clozapin, như Đức yêu cầu bác sĩ khi kê đơn clozapin phải thông báo nguy cơ IDIN đến bệnh nhân đồng thời kiểm tra công thức máu định kỳ mỗi tuần cho đến tuần thứ 18 và kiểm tra mỗi tháng sau đó cho đến tuần thứ 4 sau khi ngừng thuốc, Hoa Kỳ cũng triển khai chương trình nâng cao nhận thức và tự giám sát biến cố ở bệnh nhân sử dụng clozapin.
- Nhóm thuốc kháng sinh – kháng virus là nhóm thuốc có tỷ lệ báo cáo liên quan đến mất bạch cầu hạt cao nhất chỉ sau nhóm thuốc hóa trị liệu, đặc biệt là các b-lactam và một số chế phẩm kháng virus [1],[2]. Nhóm thuốc này thường có thời gian khởi phát IDIN sớm và có cấu trúc dễ bị chuyển hóa thành phân tử tái hoạt động (như b-lactam). Tuy nhiên, cũng có thể bệnh nhân khởi phát IDIN sớm do bệnh nhân đã sinh đáp ứng miễn dịch đặc hiệu với thuốc từ lần sử dụng trước.
- Trong số các thuốc sinh học không có chỉ định điều trị ung thư, các thuốc hay được báo cáo liên quan đến giảm bạch cầu trung tính và mất bạch cầu hạt là các sinh phẩm điều trị các bệnh tự viêm và bệnh tự miễn. Do cơ chế tác dụng của các thuốc này nên việc giảm bạch cầu trung tính không phải là ít gặp [2].
4.2 Các thuốc đã được báo cáo liên quan đến IDIN:
Các thuốc không độc tế bào đã được báo cáo liên quan đến IDIN trong các nghiên cứu quốc tế và hiện đang có trong danh mục thuốc của Bệnh viện TWQĐ 108 được trình bày trong bảng dưới đây, trong đó các thuốc có tần suất báo cáo cao hơn được in đậm và đánh dấu sao.
Bảng 1. Các thuốc không độc tế bào thường được báo cáo liên quan đến IDIN [1],[2],[4]
| Nhóm thuốc | Tên thuốc |
| Thuốc điều trị rối loạn tuyến giáp | Thiamazol |
| Thuốc chống loạn thần không điển hình | Chlopromazin, Clozapin**, Olanzapin**, Quetiapin* |
| Thuốc kháng sinh – kháng virus | Amoxicillin/acid clavulanic, Acyclovir, Cefepim*, Cefotaxim, Ceftriaxon*, Ciprofloxacin, Clarithromycin*, Clindamycin, Co-trimoxazol, Ganciclovir***, Imipenem/Cilastatin*, Isoniazid, Linezolid*, Meropenem*, Metronidazol, Piperacillin/Tazobactam, Rifampicin, Tobramycin, Valganciclovir***, Vancomycin |
| Thuốc sinh học | Imatinib***, Infliximab**, Rituximab***, Tocilizumab** |
| Thuốc giảm đau và NSAIDs | Diclofenac natri, Ibuprofen, Indomethacin, Naproxen |
| Thuốc điều trị động kinh | Carbamazepin, Phenytoin |
| Thuốc tim mạch | Captopril, Clopidrogel, Doxazosin, Methyldopa, Ramipril, Spironolacton, |
| Thuốc tiêu hóa | Cimetidin, Famotidin, Mesalamin, Omeprazol, Ranitidin |
| Các thuốc khác | Allopurinol, Levetiracetam, Sulfasalazin, Tacrolimus* |
| * Tần suất báo cáo liên quan IDIN theo tờ thông tin sản phẩm phê duyệt bởi Cơ quan quản lý Dược Châu Âu (EMA) hoặc Cục quản lý thuốc và thực phẩm Hoa Kỳ (FDA) ở mức ít gặp (từ ³1/1000 đến <1/100) ** Tần suất báo cáo liên quan IDIN theo tờ thông tin sản phẩm phê duyệt bởi Cơ quan quản lý Dược Châu Âu (EMA) hoặc Cục quản lý thuốc và thực phẩm Hoa Kỳ (FDA) ở mức thường gặp (từ ³1/100 đến <1/10) *** Tần suất báo cáo liên quan IDIN theo tờ thông tin sản phẩm phê duyệt bởi Cơ quan quản lý Dược Châu Âu (EMA) hoặc Cục quản lý thuốc và thực phẩm Hoa Kỳ (FDA) ở mức rất thường gặp (³1/10) |
|
| Trước khi kê đơn |
| Xác định thuốc đã được báo cáo gây IDIN (bảng 1) |
| Trong quá trình sử dụng thuốc |
| – Thông báo cho bệnh nhân và người nhà – Ghi chép thời điểm bắt đầu dùng thuốc – Kiểm tra công thức máu thường xuyên |
| Giảm ANC |
| Ngừng thuốc liên quan |
| Cân nhắc sử dụng G-CSF ở đối tượng phù hợp |
| Điều trị sốt và nhiễm khuẩn (nếu có) |
| Kiểm tra công thức máu thường xuyên cho đến khi số lượng bạch cầu hồi phục |
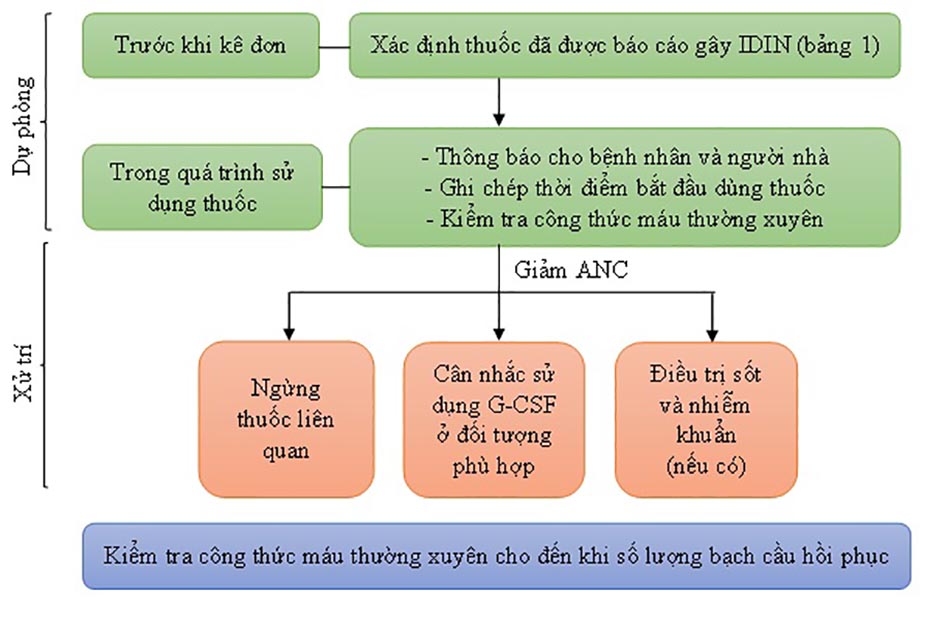
5. Biện pháp dự phòng và xử trí
5.1 Biện pháp dự phòng
IDIN là một biến chứng hiếm gặp khi dùng thuốc nhưng để lại hậu quả nghiêm trọng, vì vậy cần có các biện pháp dự phòng với các thuốc đã được báo cáo làm tăng nguy cơ này (trình bày trong bảng 1).
Trước khi kê đơn, xác định các thuốc có khả năng gây mất bạch cầu hạt và ghi chép lại thời gian bắt đầu dùng thuốc. Việc này giúp xác định thuốc có khả năng cao nhất gây giảm bạch cầu, đặc biệt khi bệnh nhân sử dụng nhiều thuốc. Bệnh nhân, người nhà bệnh nhân hoặc người chăm sóc bệnh nhân cũng cần được thông báo về nguy cơ IDIN cũng như các triệu chứng của mất bạch cầu hạt để thông báo với nhân viên y tế khi triệu chứng xuất hiện.
Khi bệnh nhân bắt đầu sử dụng thuốc, giám sát công thức máu chặt chẽ từ thời điểm khởi đầu, trong thời gian dùng thuốc và sau khi dùng thuốc cho đến thời điểm an toàn (biến chứng IDIN xuất hiện trong khoảng thời gian từ 1 – 6 tháng tính từ liều đầu tiên [1],[2]). Thông số quan trọng nhất cần giám sát là ANC. Nếu bệnh nhân gặp IDIN, cân nhắc biện pháp xử trí phù hợp tùy theo thuốc gây ra biến cố, mức độ giảm bạch cầu trung tính và tình trạng lâm sàng của bệnh nhân.
5.2 Ngừng sử dụng thuốc
Biện pháp xử trí quan trọng nhất là ngừng thuốc liên quan, trong trường hợp bệnh nhân dùng nhiều thuốc, quyết định ngưng sử dụng thuốc nào cần dựa trên các yếu tố:
- Thuốc đã được báo cáo có liên quan đến IDIN hay chưa và tần suất báo cáo ở mức độ nào? (trình bày trong bảng 1)
- Thời gian xuất hiện IDIN sau liều khởi đầu? Vì theo cơ chế trình bày ở mục 2, cần có một khoảng thời gian đủ để cơ thể sinh đáp ứng miễn dịch đặc hiệu với thuốc.
- Số lượng bạch cầu có hồi phục sau khi ngừng thuốc hay không? Sau khi ngừng thuốc, thông thường số lượng bạch cầu sẽ phục hồi theo thời gian và bệnh nhân chỉ cần điều trị triệu chứng như sử dụng kháng sinh để điều trị nhiễm khuẩn. Thời gian số lượng bạch cầu trung tính phục hồi hoàn toàn trung bình là 9 ngày (từ 9 đến 24 ngày) [1].
Riêng đối với các thuốc sinh học, do cơ chế tác dụng của chúng nên việc ANC còn 1,0 – 1,5 G/L là thường gặp, và bệnh nhân giảm ANC mức độ này vẫn có thể tiếp tục dùng thuốc dưới sự giám sát chặt chẽ của nhân viên y tế. Ở bệnh nhân giảm ANC còn 1,0 G/L, tạm ngừng thuốc cho đến khi ANC hồi phục còn 1,5 G/L, sau đó tiếp tục phác đồ điều trị. Các trường hợp giảm ANC < 0,5 G/L được báo cáo ít gặp hơn, bệnh nhân giảm ANC mức độ này cần được ngừng thuốc và chuyển sang dùng thuốc khác thay thế [2].
5.3 Sử dụng yếu tố kích thích tăng trưởng bạch cầu hạt
Bệnh nhân giảm bạch cầu trung tính kéo dài có thể được điều trị bổ sung bằng các yếu tố kích thích tăng trưởng bạch cầu hạt (G-CSF). Việc sử dụng G-CSF để điều trị bệnh nhân hạ bạch cầu trung tính nghiêm trọng vẫn còn nhiều tranh cãi.
Một số báo cáo cho thấy sử dụng G-CSF giúp rút ngắn thời gian giảm bạch cầu, thời gian điều trị bằng kháng sinh và thời gian nằm viện. Vài nghiên cứu gần đây cho kết quả G-CFS giúp rút ngắn thời gian mất bạch cầu 4 – 5 ngày và cải thiện tiên lượng bệnh [2]. Cũng đã có báo cáo thời gian bạch cầu trung tính phục hồi về mức bình thường được rút ngắn còn 8 ngày ở nhóm sử dụng G-CFS so với 9 ngày ở nhóm đối chứng [1]. Liều ở người lớn thường được báo cáo là tiêm dưới da 300 μg/ngày. Liều 0,5 μg/kg mỗi ngày cho đến khi số lượng bạch cầu trung tính hồi phục > 0,5 G/L cũng được đề xuất [1].
Tuy nhiên, vẫn còn thiếu các nghiên cứu chất lượng cao chứng minh G-CSF giúp rút ngắn thời gian giảm bạch cầu trung tính ở BN mất bạch cầu hạt. Thử nghiệm ngẫu nhiên, tiến cứu duy nhất cho đến nay không chứng minh được lợi ích của G-CSF, nhưng cỡ mẫu của thử nghiệm này bé (N=24) và liều G-CFS 100 – 200 μg/ngày trong thử nghiệm thấp hơn liều 300 μg/ngày (mức liều được một số chuyên gia khuyến cáo [1]).
Bệnh nhân có số lượng bạch cầu trung tính < 0,1 G/L đã được báo cáo có nhiều biến chứng nhiễm khuẩn và tử vong hơn các bệnh nhân khác, do vậy có thể sử dụng G-CFS 300 μg/ngày ở bệnh nhân có số bạch cầu trung tính £ 0,1 G/L bất kể tình trạng nhiễm khuẩn [1]. Mặc dù còn thiếu bằng chứng về hiệu quả của G-CFS đối với IDIN, độc tính của G-CFS trên bệnh nhân giảm bạch cầu trung tính là rất thấp nên có thể sử dụng liều 0,5 μg/kg theo kinh nghiệm ở bệnh nhân suy yếu hoặc nghi ngờ có giảm dự trữ tủy xương [3].
5.4 Các biện pháp xử trí khác
Ở bệnh nhân sốt, nếu ANC từ 0,5 – 1,5 G/L chỉ cần áp dụng các biện pháp hạ sốt thông thường, nếu ANC < 0,5 G/L phải theo dõi bệnh nhân trong điều kiện nội trú [3]. Ở các bệnh nhân này, dự phòng và điều trị nhiễm khuẩn theo hướng dẫn điều trị sốt giảm bạch cầu hiện hành, kháng sinh phổ rộng đường tĩnh mạch thường được lựa chọn [2].
Ngoài ra, thực hành vệ sinh tốt (good hygiene pratices) cũng cần áp dụng cho đến khi số lượng bạch cầu của bệnh nhân hồi phục [1].
5.5 Ví dụ thực tế lâm sàng
Trên thực tế lâm sàng, Ban Dược lâm sàng đã nhận được báo cáo một trường hợp bệnh nhân với chẩn đoán “Suy hô hấp do viêm phổi do A.baumannii đa kháng, viêm màng não” gặp biến cố giảm bạch cầu trung tính mức độ nghiêm trọng (ANC < 0,5 G/L).
Trong các thuốc bệnh nhân đang sử dụng xác định được vancomycin và ganciclovir là các thuốc đã được báo cáo liên quan đến IDIN, với tần suất lần lượt là hiếm gặp và rất thường gặp. Bệnh nhân đã sử dụng vancomycin đến ngày thứ 20 và sử dụng ganciclovir ngày 2. Mặc dù tần suất báo cáo liên quan đến IDIN của ganciclovir là rất thường gặp, cao hơn vancomycin nhưng thời gian bệnh nhân sử dụng ganciclovir chưa đủ để cơ thể sinh đáp ứng miễn dịch đặc hiệu với thuốc. Xét theo thời gian sử dụng thuốc và tình trạng lâm sàng của bệnh nhân, bác sĩ điều trị đã quyết định thay thế vancomycin bằng kháng sinh khác và sử dụng G-CSF. Sau 9 ngày ngừng thuốc số lượng bạch cầu của bệnh nhân hồi phục.
Vậy, sau ca lâm sàng này có thể thấy (1) bệnh nhân sử dụng vancomycin là một thuốc đã được báo cáo liên quan IDIN, (2) biến cố mất bạch cầu hạt khởi phát muộn sau khi bệnh nhân đã dùng thuốc được 20 ngày và (3) sau khi ngừng thuốc số lượng bạch cầu của bệnh nhân hồi phục. Dựa vào các yếu tố kể trên có thể kết luận vancomycin có liên quan đến biến cố mất bạch cầu hạt trên bệnh nhân.
6. Kết luận
Các báo cáo ADR bệnh nhân bị giảm bạch cầu trung tính do thuốc không độc tế bào đang có xu hướng gia tăng trong thời gian gần đây. Đây là một trong những tác dụng bất lợi nghiêm trọng nhất và có thể xảy ra với nhiều loại thuốc điều trị nhiều bệnh lý khác nhau. Thời gian khởi phát thường chậm và thường đe dọa tính mạng. Do đó, khi sử dụng một thuốc hay được báo cáo có liên quan đến IDIN, cần giám sát số lượng tế bào máu thường xuyên. Khi xảy ra giảm bạch cầu trung tính hoặc bạch cầu hạt, cần ngưng thuốc liên quan ngay lập tức, có thể cân nhắc sử dụng G-CSF tùy trường hợp cụ thể. Ở bệnh nhân mất bạch cầu hạt nghiêm trọng, có thể cân nhắc các biện pháp xử trí khác theo các hướng dẫn điều trị sốt giảm bạch cầu hiện hành.
Các nghiên cứu tổng quan về IDIN còn hạn chế, tỷ lệ xảy ra, tỷ lệ tử vong, thuốc liên quan, cơ chế còn chưa rõ ràng. Do đó, khi xảy ra giảm bạch cầu trung tính hoặc mất bạch cầu hạt do thuốc không độc tế bào, cần báo cáo đầy đủ đến Ban Dược lâm sàng để bổ sung những dữ liệu còn thiếu về nguy cơ này của thuốc, từ đó giúp tăng cường sử dụng thuốc an toàn hơn.
TÀI LIỆU THAM KHẢO
1. Tác giả: Curtis, Brian R. “Non-chemotherapy drug-induced neutropenia: key points to manage the challenges.” Hematology. American Society of Hematology. Education Program vol. 2017,1 (2017): 187-193. doi:10.1182/asheducation-2017.1.187, Ngày truy cập: 21 tháng 01 năm 2022.
2. Tác giả: Rattay, B., & Benndorf, R. A. (2021). Drug-Induced Idiosyncratic Agranulocytosis – Infrequent but Dangerous. Frontiers in pharmacology, 12, 727717. https://doi.org/10.3389/fphar.2021.727717, Ngày truy cập: 21 tháng 01 năm 2022.
3. Tác giả: Thomas D Coates. Drug-induced neutropenia and agranulocytosis. https://www.uptodate.com/, Ngày truy cập: 21 tháng 01 năm 2022.
4. Tờ thông tin sản phẩm thuốc đã được Cục quản lý dược châu Âu hoặc Cục quản lý dược phẩm & thực phẩm Hoa Kỳ phê duyệt, Ngày truy cập: 21 tháng 01 năm 2022.