Bệnh tiêu hóa, Bệnh truyền nhiễm
Viêm gan B: Nguyên nhân, chẩn đoán và hướng dẫn điều trị theo BMJ
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
Nhà thuốc Ngọc Anh – Để tải bài viết Viêm gan B: Nguyên nhân, chẩn đoán và hướng dẫn điều trị theo BMJ file PDF xin vui lòng click vào link ở đây.
Tóm tắt
◊ Hầu hết mọi người đều không có triệu chứng mặc dù một số người sẽ biểu hiện biến chứng như xơ gan, ung thư biểu mô tế bào gan hoặc suy gan.
◊ Những người ở các vùng dịch lưu hành (châu Á, châu Phi) hoặc tiêm chích ma túy và những người có hành vi tình dục nguy cơ cao có nguy cơ nhiễm trùng cao hơn.
◊ Các dấu ấn huyết thanh rất quan trọng trong chẩn đoán và đánh giá mức độ hoạt động của bệnh, bao gồm phân biệt giữa những người nhiễm trùng cấp và mạn tính và người mang mạn tính không triệu chứng.
◊ Điều trị nhiễm vi-rút cấp hầu như chỉ gồm điều trị hỗ trợ. Tuy nhiên, một số bệnh nhân nhiễm trùng cấp có thể tiến triển thành suy gan và những bệnh nhân này cần được chuyển sang trung tâm ghép gan.
◊ Thuốc điều trị nhiễm vi-rút mạn tính bao gồm các thuốc tương tự nucleoside/nucleotide và pegylated interferon- alfa.
Thông tin cơ bản
Định nghĩa
Virus Viêm gan B (HBV) là một virus ADN lây truyền qua da và niêm mạc. Nhiễm HBV cũng là bệnh lây truyền qua đường tình dục. Nhiễm virus có thể biểu hiện bệnh và tự khỏi mà không cần điều trị, đặc biệt là nhiễm virus mắc phải ở người lớn, nhưng cũng có thể dẫn tới tình trạng nhiễm virus mạn tính, đặc biệt là nếu mắc phải ở thời kỳ chu sinh hoặc trong những năm đầu đời.
[BMJ Best Practice podcast: hepatitis B – how to approach diagnosis and management of chronic infection]Dịch tễ học
Tổ chức Y tế Thế giới ước tính trên toàn cầu, có 257 triệu người bị nhiễm HBV (được định nghĩa là có kháng nguyên bề mặt viêm gan B dương tính).[9] Gần một nửa số người nhiễm bệnh sống ở các vùng dịch lưu hành cao tại Đông Nam Á (trừ Nhật Bản), Trung Quốc và châu Phi.[10] [11] Trong các khu vực dịch lưu hành này, >8% dân số mắc HBV mạn tính.[10] Trong các khu vực có mức độ lưu hành dịch thấp (ví dụ: Tây Âu, Bắc Mỹ, Úc), <2% dân số mắc HBV mạn tính. Ngoài ra, nguy cơ nhiễm HBV suốt đời cũng khác nhau trên thế giới, từ 80% ở các khu vực có mức độ lưu hành dịch cao đến <20% ở các khu vực có tỷ lệ mắc thấp. Trên toàn cầu, có 887.000 ca tử vong liên quan đến HBV năm 2015, chủ yếu là do các biến chứng như xơ gan và ung thư biểu mô tế bào gan.[9][Fig-1]
Theo lịch sử, Hoa Kỳ là vùng có tỷ lệ lưu hành bệnh thấp. Về tỷ lệ mắc mới, ước tính có 21.900 ca nhiễm HBV cấp tính mới tại Hoa Kỳ năm 2015.[12] Đối với nhiễm HBV mạn tính, Trung tâm Kiểm soát và Phòng chống Dịch bệnh (CDC) Hoa Kỳ ước tính có 850.000 người tại Hoa Kỳ mắc viêm gan B mặc dù họ cho cho rằng con số này có thể cao đến mức 2,2 triệu người.[12] Dữ liệu chưa công bố của CDC cho thấy một nửa số ca nhiễm HBV mạn tính tại Hoa Kỳ đến từ người gốc Á/Các đảo Thái Bình Dương và ba phần tư số ca nhiễm bệnh đến từ những người sinh ra bên ngoài Hoa Kỳ. Dữ liệu về tỷ lệ tử vong cũng cho thấy tỷ lệ cao hơn không tương xứng đối với người gốc Á/Đảo Thái Bình Dương.[12]
Theo cuộc Khảo sát Kiểm tra Sức khỏe và Dinh dưỡng Quốc gia lần thứ 2 (NHANES II), người Mỹ gốc Á và Dân đảo Thái bình Dương (APIA) chưa được đánh giá chính xác trong tổng số người nhiễm HBV tại Hoa Kỳ. Hơn nữa, đã xác định một số rào cản đối với chăm sóc HBV cho những người APIA. Nhìn chung, những rào cản này bao gồm rào cản liên quan tới việc cung cấp, bệnh nhân và nguồn lực dẫn tới sự chênh lệch về sức khỏe liên quan tới HBV ở người APIA. Vì thế, cần có những chiến lược hiệu quả để cung cấp dịch vụ chữa trị nhiễm HBV phù hợp cho nhóm dân số này.[13]
Nhóm Đặc trách về Dịch vụ Phòng bệnh của Hoa Kỳ khuyến cáo xét nghiệm HBV cho những người sinh ra tại các nước lưu hành dịch HBV.[14]
Bệnh căn học
HBV là virus DNA, thuộc họ hepadnaviruses, có vỏ envelope , không gây độc tế bào, có ái tính với gan và có khả năng lây nhiễm cao.[15] [16] Vỏ ngoài envelop của virus có chứa ba loại kháng nguyên bề mặt (HBsAg), trong đó nhiều nhất là protein S. Sự phát triển của miễn dịch tế bào và miễn dịch thể dịch đối với HBsAg mang tính bảo vệ. Bên trong envelope là nucleocapsid của virus, hay nhân, trong đó có chứa ADN mạch vòng xoắn kép một phần (HBcAg). Các peptide có nguồn gốc từ HBcAg gây ra đáp ứng miễn dịch tế bào chủ chủ yếu đối với HBV. HBeAg đóng vai trò là dấu ấn cho sự sao chép hoạt động, nhưng chức năng của nó chưa được xác định. Protein X (HBx) có thể có vai trò trong tiến triển của ung thư biểu mô tế bào gan. DNA polymerase có chức năng sao chép ngược để tổng hợp cả chuỗi âm và dương của ADN HBV .[15] [16]
Sinh lý bệnh học
Vi-rút không trực tiếp giết chết tế bào gan.[16] Đáp ứng miễn dịch của vật chủ với kháng nguyên vi-rút được coi là nguyên nhân gây tổn thương gan khi nhiễm HBV.[17] Đáp ứng miễn dịch tế bào, thay vì đáp ứng miễn dịch thể dịch, có vẻ liên quan chủ yếu tới quá trình bệnh sinh. Sự kích thích đáp ứng lymphocyte T đặc hiệu kháng nguyên được cho là xảy ra khi các tế bào lymphocyte T vật chủ nhận diện các epitope vi-rút thông qua các tế bào trình diện kháng nguyên tại các cơ quan bạch huyết. Các tế bào T đặc hiệu kháng nguyên này trưởng thành và lan rộng, sau đó di cư đến gan. Trong nhiễm HBV cấp tính, hầu hết HBV DNA được loại bỏ khỏi tế bào gan thông qua các tác dụng không độc tế bào của quá trình viêm bằng các sản phẩm của các tế bào TCD8+ được kích thích bởi lymphocyte T CD4+, đặc biệt là interferon¬gamma và yếu tố hoại tử khối u alfa. Điều này làm giảm quá trình sao chép của vi-rút và kích hoạt sự ly giải trực tiếp tế bào gan bị nhiễm bởi các tế bào T độc CD8+ đặc hiệu HBV.[18] Ngược lại, những người nhiễm HBV mạn tính biểu hiện đáp ứng tế bào T đặc hiệu HBV yếu, không thường xuyên và ít tập trung và phần lớn các tế bào đơn nhân trong gan của người nhiễm HBV mạn tính không đặc hiệu kháng nguyên.[19]
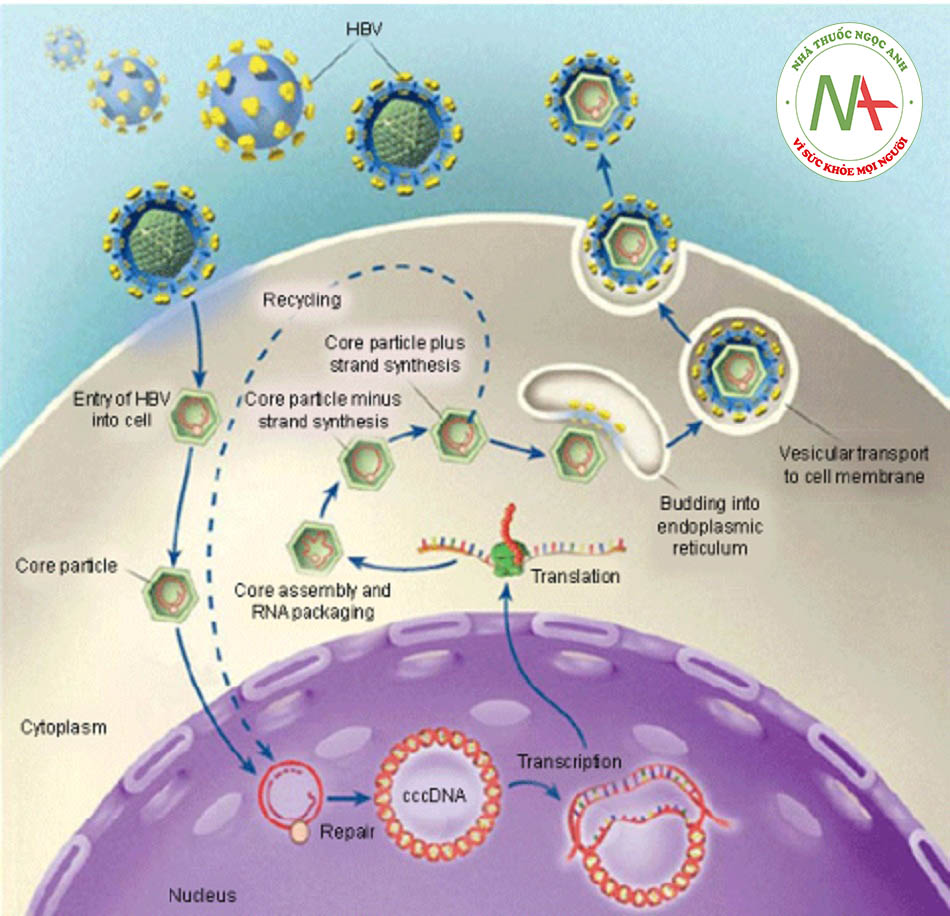
Do HBV hiện diện ở những vùng ngoài gan, cũng như sự có mặt của DNA vòng kín thông qua liên kết cộng hóa trị (covalently closed circular DNA, cccDNA) trong tế bào gan, việc loại trừ vi-rút là mục tiêu không thực tế với các loại thuốc sẵn có hiện nay. cccDNA đóng vai trò là khuôn mẫu để phiên mã RNA thông tin tiền gen, bước khởi đầu quan trọng trong quá trình sao chép HBV.[20] [21] [22] [23] Việc cccDNA liên tục có mặt trong tế bào gan được coi là dấu ấn của nhiễm vi-rút dai dẳng. Rất tiếc là các phương pháp điều trị hiện tại chưa hiệu quả để loại trừ cccDNA và chỉ có thể làm giảm nồng độ.[24] [25] [26] [27] [28] [29] [30] Sự tồn tại của nồng độ thấp cccDNA trong nhân tế bào gan đã cho thấy có tương quan với sự bùng phát vi-rút sau khi ngừng điều trị. Ngoài ra, việc HBV DNA tích hợp với nhân tế bào gan trong quá trình nhân lên có thể giải thích sự gia tăng nguy cơ mắc ung thư biểu mô tế bào gan. Hơn nữa, đồng nhiễm vi- rút viêm gan C (HCV) có thể làm tăng tỷ lệ xơ hóa, xơ gan và ung thư tế bào gan một cách hiệp đồng,[31] [32] [33] [34] vì cả HBV và HCV có thể nhiễm vào cùng tế bào gan một cách độc lập.[35]
Phân loại
Kiểu gen HBV[1]
Các kiểu gen HBV được xác định dựa trên 8% sự thay đổi trình tự nucleotide của toàn bộ bộ gen và được phân bố theo khu vực địa lý.[2] Dữ liệu cho thấy kiểu gen HBV có thể đóng vai trò trong tiến triển của bệnh gan liên quan tới HBV và đáp ứng với điều trị.[3] Nghiên cứu cho thấy mức chuyển đảo huyết thanh HBeAg tăng lên ở cả kiểu gen A và B,[4] [5] [6] [7] mặc dù một nghiên cứu cho thấy việc cải thiện chuyển đảo huyết thanh HBeAg chỉ giới hạn ở kiểu gen A.[8] Những cải thiện này trong đáp ứng điều trị được quan sát trong phác đồ pegylated IFN-alfa mà không thấy khi điều trị bằng nucleotide hay nucleoside, do đó cần tiến hành nghiên cứu thêm trước khi khuyến cáo xét nghiệm kiểu gen trong thực hành lâm sàng và liên quan với đáp ứng điều trị.[3]
- Kiểu gen A được tìm thấy ở Mỹ, Bắc Âu và châu Phi. Kiểu gen này cũng kèm theo tỷ lệ chuyển đảo huyết thanh HBeAg cao hơn với liệu pháp interferon-alfa so với kiểu gen B, C và D.
- Kiểu gen B và C được tìm thấy ở châu Á và Hoa Kỳ. Kiểu gen B kèm theo sự chuyển đảo huyết thanh HBeAg ở độ tuổi trẻ hơn, viêm gan hoại tử hoạt động ít hơn, đáp ứng điều trị bền vững hơn sau khi chuyển đảo huyết thanh HBeAg, tốc độ tiến triển thành xơ gan chậm hơn và tỷ lệ ung thư biểu mô tế bào gan thấp hơn so với kiểu gen C. Kiểu gen C là kiểu gen viêm gan B liên quan nhiều nhất đến xơ gan và ung thư gan.[3]
- Kiểu gen D được tìm thấy ở Mỹ, Nam Âu và Trung Đông.
- Kiểu gen E được tìm thấy ở châu Phi.
- Kiểu gen F và H được tìm thấy ở Trung và Nam Mỹ.
- Kiểu gen G được tìm thấy ở châu Phi.
Phòng ngừa
Ngăn ngừa sơ cấp
Biện pháp phòng ngừa cấp I là thông qua tiêm chủng thụ động với immunoglobulin viêm gan B (hepatitis B immunoglobulin, HBIG) hoặc tiêm chủng chủ động với vắc-xin viêm gan B (HBsAg bất hoạt tái tổ hợp).[49]
Tổ chức Y tế Thế giới khuyến cáo mọi trẻ nhũ nhi cần được tiêm loạt vắc-xin viêm gan B với mũi đầu tiên sớm nhất có thể ngay sau khi sinh, tốt nhất là trong vòng 24 giờ, sau đó là hai hoặc ba mũi nữa.[39] Tại Hoa Kỳ, Ủy ban Tư vấn về Thực hành Tiêm chủng (ACIP) khuyến cáo trẻ nhỏ nên tiêm mũi đầu tiên (vắc-xin viêm gan B đơn giá) trong vòng 24 giờ sau sinh, mũi thứ hai lúc trẻ được 1-2 tháng tuổi (sau mũi đầu tiên ít nhất là 4 tuần) và mũi thứ ba lúc trẻ được 6-18 tháng tuổi (ít nhất 8 tuần sau mũi thứ hai và ít nhất 16 tuần sau mũi thứ nhất). Nếu trẻ không được tiêm mũi nào lúc sinh, thì cần tiêm 3 mũi có chứa vắc-xin viêm gan B theo lịch lúc trẻ được 0, 1-2, và 6 tháng tuổi, bắt đầu ngay khi có thể. Cần dùng vắc-xin viêm gan B đơn giá cho mũi tiêm trước khi trẻ được 6 tuần tuổi. Cho phép tiêm loạt 4 mũi vắc-xin viêm gan B khi dùng vắc-xin kết hợp có chứa viêm gan B sau mũi lúc sinh. Cần tiêm mũi cuối cùng (thứ ba hoặc thứ tư) trong loạt vắc-xin viêm gan B khi trẻ đã đủ 24 tuần tuổi trở lên.[50] Tại Hoa Kỳ, trẻ có mẹ dương tính với HBsAg cần được tiêm vắc-xin viêm gan B đơn giá và globulin miễn dịch viêm gan B (HBIG) trong vòng 12 giờ sau sinh. Nếu chưa rõ tình trạng HBsAg của mẹ, trẻ cần được tiêm vắc-xin viêm gan B trong vòng 12 giờ sau sinh, và trẻ nhẹ hơn 2000 g cũng cần được tiêm HBIG. Đối với trẻ nặng hơn 2000 g, cần xác định tình trạng HBsAg của người mẹ và nếu dương tính, cần tiêm HBIG cho trẻ ngay khi có thể trong vòng 7 ngày. Trẻ nhỏ có mẹ dương tính với HBsAg cần được xét nghiệm HBsAg và anti-HBs lúc 9 đến 12 tháng tuổi, hoặc 1 đến 2 tháng sau khi tiêm xong loạt vắc-xin viêm gan B. Trẻ nhỏ có mẹ âm tính với HBsAg cần được tiêm một liều vắc-xin viêm gan B trong vòng 24 giờ sau khi sinh (nếu sức khỏe ổn định và cân nặng lúc sinh hơn 2000 g), hoặc một mũi lúc được 1 tháng tuổi hoặc xuất viện nếu cân nặng lúc sinh dưới 2000 g. [50]
Từ cuối năm 2017, tại Anh Quốc, chương trình tiêm chủng thường quy cho trẻ em sẽ bao gồm viêm gan B trong vắc-xin tổng hợp cho bạch hầu, uốn ván, ho gà, bại liệt và Haemophilus influenzae týp B (DTaP/IPV/Hib/HepB).[51] Khuyến cáo tiêm vắc-xin DTaP/IPV/Hib/HepB khi trẻ được 8, 12, và 16 tuần tuổi, nhưng trẻ có thể được tiêm từ 6 tuần tuổi cho đến 10 tuổi. Trẻ nhỏ có mẹ bị nhiễm viêm gan B cần được tiêm vắc-xin viêm gan B đơn giá lúc sinh (trong vòng 24 giờ) và lúc 4 tuần tuổi, sau đó là vắc-xin đa giá lúc 8 tuần tuổi, và vắc-xin đa giá bổ sung lúc 12 và 16 tuần tuổi; trẻ nhỏ được xét nghiệm HBsAg lúc được một tuổi và được tiêm thêm một liều vắc-xin viêm gan B đơn giá. Trẻ nhỏ có mẹ bị nhiễm viêm gan B cũng cần được tiêm HBIG trong vòng 24 giờ sau khi sinh, trừ khi người mẹ có HBsAg dương tính và kháng HBe dương tính đồng thời trẻ nặng hơn 1500 g.[51]
Những người có nguy cơ nhiễm HBV cao cần được tiêm vắc-xin HBV (ví dụ như những người sinh ra trong vùng có tỉ lệ lưu hành dịch cao, người có nguy cơ nghề nghiệp, đồng tính nam, người tiêm chích ma túy, bệnh nhân lọc máu, người nhiễm HIV, người có quan hệ tình dục và tiếp xúc trong gia đình với người mang HBV âm tính với các dấu ấn huyết thanh HBV.) Tiêm chủng vắc-xin HB trong khi mang thai dường như không gây ra dị tật bẩm sinh tới thai nhi hay liên quan tới sinh non hay sảy thai tự phát. Tuy nhiên, các nghiên cứu còn hạn chế do thiếu tính ngẫu nhiên hoặc cỡ mẫu nhỏ và độ mạnh thống kê thấp.[52] Tại Hoa Kỳ, ACIP khuyến cáo tiêm 3 mũi vắc-xin viêm gan B đơn giá lúc 0, 1, và 6 tháng. Người lớn cũng có thể được tiêm vắc-xin viêm gan A và B kết hợp (HepA-HepB) lúc 0, 1, và 6 tháng.[53]
Năm 2017, Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ đã phê duyệt Heplisav-B®, vắc-xin viêm gan B mới đầu tiên trong 25 năm. Vắc-xin này có chứa chất bổ trợ chuỗi kích thích miễn dịch mới. Heplisav-B® được chia thành hai mũi, tiêm cách nhau một tháng. Đây là vắc-xin hai liều duy nhất hiện có cho viêm gan B. ACIP khuyến cáo tiêm vắc-xin này cho người lớn >18 tuổi có nguy cơ mắc phải vi-rút viêm gan B (ví dụ như người có nguy cơ mắc bệnh lây truyền qua đường tình dục, người nhiễm HIV, người bị giam giữ, người tiêm chích ma túy). Độ an toàn chưa được thử nghiệm ở phụ nữ mang thai. Kháng thể bảo vệ trong huyết thanh cho kháng nguyên bề mặt viêm gan B có được ở 90% đến 100% bệnh nhân trong các thử nghiệm ngẫu nhiên, so với 70% đến 90% đối với Engerix-B®.[54]
Tại Anh Quốc, lịch tiêm nhanh được cung cấp cho hầu hết các nhóm nguy cơ, theo đó trẻ được tiêm vắc-xin lúc 0, 1, và 2 tháng, hoặc có thể tiêm theo lịch lúc 0, 1 và 6 tháng nếu không cần bảo vệ nhanh và có khả năng tuân thủ. Khuyến cáo xét nghiệm huyết thanh sau khi tiêm vắc-xin 1 đến 2 tháng sau lần tiêm cuối cùng.[55] Những người không đáp ứng về mặt huyết thanh cần được tiêm chủng lại.
Hướng dẫn của Ủy ban Cố vấn về Thực hành Tiêm chủng (Advisory Committee on Immunization Practices, ACIP) khuyến cáo rằng mọi bệnh nhân mắc tiểu đường (tuýp 1 hoặc 2) trong độ tuổi từ 19 đến 59 cần được tiêm vắc-xin HBV.[56] Với những người từ 60 tuổi trở lên, ACIP khuyến cáo tiêm chủng theo quyết định của bác sĩ lâm sàng điều trị do dữ liệu kém vững chắc hơn trong nhóm tuổi này.
Lịch tiêm chủng với liều vắc-xin được điều chỉnh và xét nghiệm huyết thanh thường xuyên để kiểm tra việc mất khả năng miễn dịch có thể cần được áp dụng với bệnh nhân tiểu đường đang lọc máu vì phân tích gộp đã chứng tỏ rằng những bệnh nhân này có đáp ứng miễn dịch thấp hơn đáng kể với tiêm chủng HBV so với bệnh nhân lọc máu không bị tiểu đường.[57] Tuy nhiên, không có mối liên hệ giữa khả năng đáp ứng miễn dịch với vắc-xin HBV và bệnh nhân dương tính với vi-rút viêm gan C (HCV) hoặc âm tính với HCV đang được lọc máu.[58] Những người có huyết thanh âm tính với HBV bị bệnh viêm ruột cần được tiêm chủng trước khi bắt đầu liệu pháp ức chế miễn dịch hoặc sinh học.[59] Có thể cần tăng liều vắc-xin viêm gan B cho bệnh nhân bị ức chế miễn dịch để đạt được khả năng miễn dịch.[31]
Khám sàng lọc
Sàng lọc người có nguy cơ cao có thể giảm tỷ lệ mắc mới và tỷ lệ lưu hành bệnh, và chẩn đoán và điều trị sớm có thể ngăn tiến triển thành xơ hóa và ung thư biểu mô tế bào gan. Những người có nguy cơ bao gồm trẻ sơ sinh có mẹ nhiễm HBV có nguy cơ lây nhiễm HBV qua niêm mạc từ máu hoặc chất dịch nhiễm bệnh trong khi sinh.[36] Quan hệ tình dục với bạn tình nhiễm bệnh là một cách lây nhiễm quan trọng. HBV xuất hiện với tải lượng lớn (10A8 đến 10A10 bản sao/ mL) trong huyết thanh của người nhiễm bệnh và có thể phát hiện thấy trong tinh trùng, nước bọt và bạch cầu.[15] Dùng chung kim tiêm khi tiêm chích có thể dẫn đến lây nhiễm qua da. Những người sinh ra tại khu vực lưu hành dịch (ví dụ như châu Á, châu Phi) có nhiều nguy cơ.[39] Bệnh nhân có tiền sử gia đình nhiễm HBV và/hoặc bệnh gan mạn tính hoặc ung thư biểu mô tế bào gan, cũng có nguy cơ nhiễm tăng cao. Tiếp xúc với dịch tiết nhiễm bệnh qua tổn thương da và bề mặt niêm mạc tình cờ, không rõ ràng, gần liên tục cũng được cho là phương thức lây nhiễm vì HBV vẫn tồn tại bên ngoài cơ thể trong khoảng thời gian dài.[46] Cũng cần đề xuất sàng lọc cho tất cả các bệnh nhân mắc bệnh viêm ruột trước khi họ bắt đầu điều trị.[59]
Ngăn ngừa thứ cấp
Tất cả những người nhiễm HBV mạn tính không có miễn dịch với viêm gan A cần được tiêm vắc-xin phòng viêm gan A. Bệnh nhân nhiễm HBV mạn tính cần tránh uống nhiều rượu (>20 g/ngày đối với phụ nữ và >30 g/ngày đối với nam giới) vì điều này có thể là yếu tố nguy cơ bổ sung cho việc tiến triển nhanh thành xơ gan.[147]
Bạn tình và tất cả những người tiếp xúc trong hộ gia đình của người có HBsAg dương tính cần được tiêm vắc-xin phòng HBV nếu họ có kết quả xét nghiệm âm tính đối với các dấu ấn huyết thanh HBV.
Người có HBsAg dương tính cần sử dụng biện pháp bảo vệ khi quan hệ tình dục nếu bạn tình của họ chưa được tiêm vắc-xin hay miễn dịch tự nhiên, không dùng chung bàn chải đánh răng hay dao cạo râu, và cần che các vết cắt hở và vết xước, dọn sạch vết máu vấy đổ bằng thuốc tẩy hay chất tẩy rửa, và không hiến máu, hiến tạng hay tinh trùng.[77]
Cần sử dụng globulin miễn dịch viêm gan B (HBIG) trong dự phòng sau phơi nhiễm cho bạn tình thông thường của bệnh nhân nhiễm HBV, sau đó là tiêm các mũi vắc-xin HBV.
Ở bệnh nhân đồng nhiễm vi-rút viêm gan C (HCV), điều trị HCV bằng thuốc kháng virus tác dụng trực tiếp có thể gây tái hoạt HBV.[31] Hầu hết bệnh nhân đồng nhiễm HBV/HCV và bệnh tiến triển cần được điều trị bằng chất tương tự nucleotide/nucleoside.[31]
Nguy cơ tái hoạt HBV ở những người được hóa trị liệu hay điều trị liệu pháp ức chế miễn dịch có thể cao, và cần đánh giá bệnh nhân về điều trị hay dự phòng.[31]
Khuyến cáo điều trị kéo dài bằng chất tương tự nucleotide/nucleoside mạnh để giảm HBV DNA trước khi ghép gan ở người có HBsAg dương tính bị xơ hóa tiến triển hay ung thư tế bào gan.[31] [148] [149] [150] [151] Bệnh nhân HBV sau ghép cần có biện pháp dự phòng kéo dài. Hiện tại, tiêu chuẩn chăm sóc khi tái phát HBV sau khi ghép gan bao gồm kết hợp HBIG và chất tương tự nucleoside/nucleotide.[31] [152]
Chẩn đoán
Tiền sử ca bệnh
Tiền sử ca bệnh #1
Một người đàn ông 40 tuổi không có triệu chứng đến khám sức khỏe với hoạt độ alanine aminotransferase (ALT) tăng cao (55 đơn vị quốc tế [IU]/mL). Mẹ ông đã qua đời vì ung thư biểu mô tế bào gan và ông có một chị gái ở tuổi trung niên “nhiễm viêm gan B”. Kết quả khám lâm sàng bình thường và không có dấu hiệu của bệnh gan mạn tính.
Các bài trình bày khác
Điều quan trọng là bác sĩ lâm sàng phải nhận ra viêm gan B có các biểu hiện lâm sàng khác nhau. Bệnh nhân có thể không có triệu chứng hoặc có thể có gan to hay bằng chứng về khối u ở gan, hoặc dấu hiệu bệnh gan mạn tính. Một số bệnh nhân có thể biểu hiện các triệu chứng viêm gan mạn tính lần đầu tiên. Bệnh nhân có triệu chứng lâm sàng (buồn nôn, nôn, đau bụng, vàng da, đau cơ) có thể có biểu hiện đợt cấp của bệnh mạn tính.
Cách tiếp cận chẩn đoán từng bước
Diễn biến tự nhiên của viêm gan B rất khác nhau, phức tạp và biến động. Phương pháp tốt nhất để chẩn đoán nhiễm HBV là nghi ngờ lâm sàng với những người có nguy cơ và đánh giá kết quả của các xét nghiệm cụ thể liên quan tới gan và huyết thanh HBV. Khoảng 70% bệnh nhân nhiễm HBV cấp không có triệu chứng, vì thế việc chẩn đoán thường gặp khó khăn. Bệnh nhân nhiễm viêm gan B mạn tính cũng có thể không có triệu chứng hoặc có các dấu hiệu và triệu chứng của bệnh gan mạn tính, bao gồm xơ gan và các biến chứng của bệnh, ung thư biểu mô tế bào gan (hepatocellular carcinoma, HCC) và suy gan.
Những người có nguy cơ
Trẻ sơ sinh có mẹ nhiễm HBV có nguy cơ lây nhiễm HBV qua niêm mạc từ máu hoặc chất dịch nhiễm bệnh trong khi sinh. Quan hệ tình dục với bạn tình nhiễm bệnh là một cách lây nhiễm quan trọng. HBV xuất hiện với tải lượng lớn (10A8 đến 10A10 bản sao/mL) trong huyết thanh của người nhiễm bệnh và có thể’ phát hiện thấy trong tinh trùng, nước bọt và bạch cầu. Dùng chung kim tiêm khi tiêm chích có thể dẫn đến lây nhiễm qua da. Trên toàn cầu, có khoảng 2 tỷ người nhiễm HBV, trong đó 400 triệu người mắc HBV mạn tính, gần một nửa trong số đó ở những vùng dịch lưu hành cao tại Đông Nam Á (trừ Nhật Bản), Trung Quốc và châu Phi. Nam giới có nguy cơ nhiễm HBV cao hơn 1,6 lần so với phụ nữ. Bệnh nhân có tiền sử gia đình nhiễm HBV và/hoặc bệnh gan mạn tính hoặc ung thư biểu mô tế bào gan, cũng có nguy cơ lây nhiễm tăng cao. Tiếp xúc với dịch tiết nhiễm bệnh qua tổn thương da hoặc bề mặt niêm mạc một cách vô ý, không rõ ràng, gần liên tục cũng được cho là phương thức lây nhiễm vì HBV vẫn tồn tại bên ngoài cơ thể trong khoảng thời gian dài.[46]
Các triệu chứng
Các triệu chứng chính liên quan đến nhiễm HBV cấp tính, đặc biệt là ở người lớn, là các triệu chứng của hội chứng giống như bệnh huyết thanh: sốt, rét run, khó chịu, đau khớp, và ban dát sẩn hoặc mề đay. Các triệu chứng khác có thể có bao gồm vàng da, buồn nôn, nôn và đau vùng gan (RUQ) xảy ra ở khoảng 30% bệnh nhân bị HBV cấp.[60] Đa số bệnh nhân bị HBV mạn tính không có triệu chứng cho đến khi phát triển HCC, xơ gan và biến chứng của xơ gan, hay suy gan.
Kết quả khám lâm sàng
Các dấu hiệu chính ở bệnh nhân bị HBV cấp có triệu chứng là gan to và đau vùng gan và vàng da. Tuy nhiên, bệnh nhân bị HBV mạn tính nhưng không xơ gan, suy gan hay HCC có thể có kết quả khám lâm sàng bình thường. Một số bệnh nhân bị HBV mạn tính có thể có bàn tay son và sao mạch, có hay không có dấu hiệu của tăng áp lực tĩnh mạch cửa, bao gồm cổ chướng, vàng da, và dấu hiệu run vỗ cánh (dấu hiệu của bệnh não gan).
Các xét nghiệm
Ban đầu, xét nghiệm công thức máu, bilan chuyển hóa cơ bản, và xét nghiệm chức năng gan (aspartate aminotransferase [AST], alanine aminotransferase [ALT], bilirubin, phosphatase kiềm, và albumin) được chỉ định. Sau đó cần lấy kết quả xét nghiệm huyết thanh HBV đầy đủ (HBsAg, anti-HBs, anti-HBc [IgM và IgG], HBeAg, anti-HBe, và ADN HBV).
Xét nghiệm huyết thanh hữu ích trong việc phân biệt giữa nhiễm HBV cấp và mạn tính.[49] [CDC: typical interpretation of serologic test results for hepatitis B virus infection.] Ví dụ, bệnh nhân có HBsAg dương tính và HBcIgM dương tính kèm theo ADN HBV được chẩn đoán là nhiễm HBV cấp. Tuy nhiên, một số bệnh nhân có thể tái hoạt cấp tình trạng mang bệnh không có triệu chứng hay bùng phát HBV mạn tính và có HBcIgM dương tính. Điều này đặc biệt có nhiều khả năng ở bệnh nhân có tiền sử HBsAg dương tính đã xác định, và những người đang điều trị hóa trị liệu hay thuốc ức chế miễn dịch khác.[61] [62] Khuyến cáo cần xét nghiệm HBsAg và anti-HBc total ở nhóm đối tượng này và tiêm vắc-xin cho những người có tình trạng huyết thanh HBV âm tính trước khi bắt đầu hóa trị liệu hay liệu pháp ức chế miễn dịch.[31] Cần lưu ý là có thể cần tăng liều ở bệnh nhân bị ức chế miễn dịch để có miễn dịch với viêm gan B.[31] Bệnh nhân bị nhiễm HBV mạn tính thường có HBsAg dương tính trong >6 tháng, HBcIgG dương tính và HBeAg dương tính hoặc HBeAg âm tính nhưng có HBV DNA có thể phát hiện.
Sau đó yêu cầu xét nghiệm amoniac trong huyết thanh, xét nghiệm đông máu(PT/INR), và alpha-fetoprotein (AFP) để đánh giá chức năng gan. AFP kết hợp với siêu âm cũng có thể phát hiện HCC.
Kiểu gen HBV có thể đóng vai trò quan trọng trong việc tiến triển bệnh gan liên quan đến HBV và đáp ứng điều trị, vì vậy việc xác định kiểu gen có giá trị tiên lượng, nhưng điều này cần xác nhận thêm bằng nghiên cứu bổ sung.[3]
Chẩn đoán hình ảnh
Cần yêu cầu siêu âm gan ban đầu để đánh giá xơ hóa tiến triển, xơ gan và tăng áp lực tĩnh mạch cửa, và HCC. Có thể chỉ định chụp CT có thuốc cản quang hay MRI có thuốc đối quang từ ổ bụng ba thì để chẩn đoán HCC nếu nó có khả năng, dựa trên tiền sử, khám lâm sàng, và xét nghiệm bao gồm cả tăng AFP. Hướng dẫn của Hiệp hội Nghiên cứu Bệnh Gan Hoa Kỳ (AASLD) khuyến cáo siêu âm gan mỗi 6 đến 12 tháng ở người mang HBV có nguy cơ cao và bệnh nhân xơ gan.[63] [64] Người mang HBV có nguy cơ cao bao gồm: nam giới châu Á >40 tuổi và phụ nữ châu Á >50 tuổi, bệnh nhân có tiền sử gia đình mắc HCC, người châu Phi >20 tuổi, và người mang HBV >40 tuổi bị tăng ALT dai dẳng hoặc từng đợt và/hoặc mức HBV DNA cao (>2000 IU/mL).[63] [64]
Sinh thiết gan
Có thể yêu cầu sinh thiết gan ở bệnh nhân bị HBV mạn tính để phân độ và phân giai đoạn bệnh gan trước khi bắt đầu điều trị. Tuy nhiên, sinh thiết gan có thể không cần thiết ở mọi bệnh nhân nhiễm HBV và có thể không được chỉ định nếu có bằng chứng lâm sàng, xét nghiệm, hay nội soi của xơ gan và nếu quyết định điều trị không bị ảnh hưởng.[31] Nhìn chung, chỉ định sinh thiết gan nếu có khả năng ảnh hưởng đến quyết định điều trị sau đó. Tuy nhiên, sinh thiết gan cũng được chỉ định nếu ALT tăng không tương xứng so với dự kiến ở bệnh nhân bị HBV mạn tính và để loại trừ bệnh gan đồng mắc có thể có khác, như bệnh gan nhiễm mỡ không do rượu. Ngoài ra, nếu có sự không tương xứng giữa ALT và HBV DNA, sinh thiết gan được chỉ định để xác định tình trạng viêm hoại tử và/hoặc xơ hóa từ vừa đến nặng.
Kích thước mảnh sinh thiết gan đóng vai trò rất quan trọng vì mảnh sinh thiết nhỏ có thể không đủ để đánh giá giai đoạn xơ hóa và bệnh gan.[65] Mặc dù có nguy cơ với sinh thiết gan qua da, nguy cơ biến chứng được báo cáo ở mức thấp, với một biến chứng trên mỗi 4.000 đến 10.000 thủ thuật.[66] Những người không muốn chịu rủi ro của thủ thuật xâm lấn có thể có các lựa chọn khác để đánh giá tổn thương gan như đo độ đàn hồi thoáng qua và dấu ấn huyết thanh.[31] [65] [67] [68] [69] [70] [71] [72] [73] [74] Tại châu Âu, đo độ đàn hồi thoáng qua là phương pháp phổ biến để xác định xơ gan; tuy nhiên, việc sử dụng phương pháp này bị hạn chế bởi dương tính giả do tình trạng viêm gan đáng kể và thiếu tiêu chuẩn thống nhất để tính toán độ cứng của gan.[31] [75] [76] Cần nghiên cứu bổ sung để chuẩn hóa xét nghiệm không xâm lấn cho đánh giá xơ gan.
Các giai đoạn lâm sàng của nhiễm vi rút
AASLD phân loại nhiễm HBV mạn tính thành bốn giai đoạn, thể hiện mối quan hệ giữa sự nhân lên và tiến hóa vi-rút và đáp ứng miễn dịch vật chủ.[3]
- Dung nạp miễn dịch: HBeAg dương tính; ALT bình thường; HBV DNA tăng cao (thường là >1 triệu IU/mL); sinh thiết gan cho thấy tình trạng viêm và xơ hóa rất ít.
- Hoạt động miễn dịch HBeAg dương tính: ALT tăng cao; HBV DNA tăng cao (>20.000 IU/mL); tình trạng viêm hoặc xơ hóa gan từ vừa đến nặng.
- Viêm gan B mạn tính không hoạt động: HBeAg âm tính và anti-HBe dương tính; ALT bình thường; HBV DNA thấp hoặc không thể phát hiện; sinh thiết gan cho thấy tình trạng viêm hoại tử rất ít và xơ hóa thay đổi (thể hiện tổn thương gan trong giai đoạn hoạt động miễn dịch HBeAg dương tính).
- Tái hoạt miễn dịch HBeAg âm tính: ALT tăng cao; HBV DNA tăng cao (>2.000 IU/mL); tình trạng viêm hoặc xơ hóa từ vừa đến nặng; trong số những người chuyển đảo huyết thanh từ HBeAg dương tính sang anti-HBe dương tính, 10% đến 30% có thể tiếp tục có ALT và HBV DNA tăng cao, và 10% đến 20% có thể tái hoạt sau nhiều năm bệnh không hoạt động.
Hướng dẫn của Hiệp hội Nghiên cứu Gan Châu Âu (EASL) chia HBV mạn tính thành năm giai đoạn theo dấu ấn huyết thanh và bệnh gan.
- Nhiễm HBV mạn tính HBeAg dương tính: ALT bình thường; HBV DNA tăng cao; sinh thiết gan cho thấy tình trạng viêm và xơ hóa rất ít; trước đây được gọi là giai đoạn ‘dung nạp miễn dịch’.
- Viêm gan B mạn tính có HBeAg dương tính: ALT tăng cao, HBV DNA tăng cao; tình trạng viêm hoại tử gan từ vừa đến nặng và tiến triển nhanh thành xơ hóa; ở hầu hết bệnh nhân, chuyển đảo huyết thanh HBeAg và ức chế HBV DNA xảy ra và bệnh nhân bước vào giai đoạn nhiễm trùng HBeAg âm tính, trong khi ở những bệnh nhân khác, việc kiểm soát HBV không diễn ra và họ tiến triển sang giai đoạn viêm gan B mạn HbeAg âm tính, có thể tồn tại nhiều năm; trước đây được gọi là giai đoạn ‘phản ứng miễn dịch HBeAg dương tính’.
- Nhiễm HBV mạn tính có HBeAg âm tính: anti-HBe dương tính; ALT bình thường; HBV DNA thấp hoặc không thể phát hiện; sinh thiết gan cho thấy tình trạng viêm hoại tử rất ít và xơ hóa thấp; trước đây được gọi là giai đoạn ‘người mang bệnh không hoạt động’.
- Viêm gan B mạn HBeAg âm tính: có anti-HBe; HBV DNA từ vừa đến nặng; ALT tăng cao (dai dẳng hoặc từng đợt); tình trạng viêm hoại tử và xơ hóa từ vừa đến nặng.
- HBsAg âm tính: bệnh nhân có HBsAg âm tính và anti-HBc dương tính, và có thể phát hiện được anti-HBe; ALT bình thường; HBV DNA thường không phát hiện được; ức chế miễn dịch ở những bệnh nhân này có thể dẫn đến tái hoạt; giai đoạn này còn được gọi là nhiễm HBV tiềm ẩn.
![Viêm gan B: Nguyên nhân, chẩn đoán và hướng dẫn điều trị theo BMJ 15 Hình 3: Các giai đoạn nhiễm viêm gan B mạn tính [AASLD = Hiệp hội Nghiên cứu Bệnh Gan Hoa Kỳ, EASL = Hiệp hội Nghiên cứu Gan Châu Âu; *cccDNA]](https://nhathuocngocanh.com/wp-content/uploads/2022/03/viem_gan_B_nguyen_nhan_chan_doan_dieu_tri_theo_bmj_hinh3.jpg)
Các yếu tố nguy cơ
Thường gặp
Phơi nhiễm chu sinh ở trẻ sơ sinh có mẹ nhiễm HBV
- Trẻ sơ sinh có mẹ nhiễm HBV có nguy cơ lây nhiễm HBV qua niêm mạc từ máu hoặc chất dịch nhiễm bệnh trong khi sinh.[36] Lây nhiễm qua nhau thai trong tử cung và khi cho con bú ít có khả năng là nguyên nhân lây nhiễm HBV. 90% số trẻ sơ sinh bị nhiễm bệnh không có dự phòng sau phơi nhiễm tiến triển thành HBV mạn tính.
Nhiều bạn tình
- Quan hệ tình dục với bạn tình nhiễm bệnh là một cách lây nhiễm quan trọng. Trong một nghiên cứu, 27% bệnh nhân nhiễm HBV cấp tính có quan hệ tình dục khác giới với một hay nhiều bạn tình nhiễm bệnh.[37] HBV xuất hiện với tải lượng lớn (10A8 đến 10A10 bản sao/mL) trong huyết thanh của người nhiễm bệnh và có thể’ phát hiện thấy trong tinh trùng, nước bọt và bạch cầu.[15]
Đồng tính nam (MSM)
- Quan hệ tình dục với bạn tình nhiễm bệnh là một cách lây nhiễm quan trọng. Trong một nghiên cứu, 13% số bệnh nhân nhiễm HBV cấp có quan hệ đồng tính nam.[37] HBV xuất hiện với tải lượng lớn (10A8 đến 10A10 bản sao/ mL) trong huyết thanh của người nhiễm bệnh và có thể phát hiện thấy trong tinh trùng, nước bọt và bạch cầu.[15]
Tiêm chích ma túy
- Dùng chung kim tiêm khi tiêm chích có thể dẫn đến lây truyền qua da. Tiêm chích được báo cáo ở trong 18% bệnh nhân ghi nhận nhiễm HBV cấp.[37]
Sinh ra tại khu vực có tỷ lệ lưu hành dịch cao
- Những người sinh ra tại khu vực có tỷ lệ mắc mới và tỷ lệ lưu hành bệnh cao (ví dụ như châu Á, châu Phi) có nguy cơ cao.[39]
Tiền sử gia đình mắc HBV và/hoặc bệnh gan mạn tính
- Bệnh nhân có tiền sử gia đình mắc HBV có nguy cơ nhiễm bệnh tăng cao.
Tiền sử gia đình mắc ung thư biểu mô tế bào gan (HCC)
- Những người có tiền sử gia đình mắc HCC có nguy cơ nhiễm HBV tăng cao vì nguy cơ mắc HCC cao do hậu quả của HBV.
Tiếp xúc với HBV trong gia đình
- Tại Hoa Kỳ vào cuối những năm 1990, tiếp xúc với người nhiễm bệnh trong gia đình chiếm khoảng 4% số ca nhiễm HBV cấp mỗi năm.[37] Tiếp xúc dịch tiết nhiễm vi rút qua tổn thương da hoặc bề mặt niêm mạc một cách vô ý, không rõ ràng, gần gũi, liên tục được cho là phương thức lây nhiễm vì HBV vẫn tồn tại bên ngoài cơ thể trong khoảng thời gian dài.[46] Trẻ em nhiễm bệnh mạn tính có thể vô tình gây nhiễm bẩn vào các bề mặt bên ngoài qua các vết cắt hoặc vết thương hở. Hình thức lây nhiễm này được coi là nguyên nhân của đa số các ca lây truyền ngang HBV ở trẻ em trong các vùng dịch lưu hành cao.[47]
Không thường gặp
Giới tính nam
- Nam giới có nguy cơ nhiễm HBV cao hơn 1,6 lần so với phụ nữ.[38]
Tiền sử bệnh lây qua đường tình dục
- Đa số các bệnh nhân da đen và da trắng mắc phải HBV do lây nhiễm qua đường tình dục khi trưởng thành.
Nhiễm HIV
- Có tới 10% người nhiễm HIV đồng nhiễm HBV mạn tính và 80% bệnh nhân HIV có bằng chứng huyết thanh phơi nhiễm với HBV.[40]
Nhiễm vi-rút viêm gan C (HCV)
- Khoảng 10% đến 15% bệnh nhân nhiễm HBV mạn tính đồng nhiễm HCV.[41]
- Điều trị HCV bằng thuốc kháng virus tác động trực tiếp có thể gây tái hoạt HBV ở bệnh nhân đồng nhiễm.[31]
Truyền máu hoặc các sản phẩm máu
- Tại Hoa Kỳ, tỷ lệ nhiễm HBV liên quan tới truyền máu hiện tại là khoảng 0,002% trên mỗi người được truyền máu.[42] Sàng lọc bắt buộc với các sản phẩm máu bắt đầu được tiến hành ở Hoa Kỳ và Vương Quốc Anh từ đầu những năm 1970.
Nhân viên y tế (HCW)
- Trong lịch sử, các nhân viên y tế (healthcare worker, HCW) và công chức tiếp xúc với máu và chất dịch cơ thể có tỷ lệ nhiễm HBV cao hơn so với cộng đồng chung do lây nhiễm HBV qua da hoặc qua niêm mạc. Tỷ lệ nhiễm HBV ở những nhân viên y tế được tiêm chủng hiện tại đã thấp hơn so với dân số nói chung.[43] Cũng đã có báo cáo về việc bác sĩ phẫu thuật bị nhiễm bệnh lây nhiễm HBV cho bệnh nhân.[44] [45]
Tiền sử bị giam giữ
- Do các yếu tố nguy cơ đi kèm (tiêm chích ma túy, hành vi tình dục không an toàn, xăm mình), các bệnh nhân với tiền sử bị giam giữ có nguy cơ phơi nhiễm với HBV cao hơn.
Lọc máu
- Đã phát hiện thấy HBV trên các bề mặt môi trường và trong máu rò rỉ ở các phiên lọc máu.[48] Tuy nhiên, hiện nay ít có trường hợp nhiễm HBV cấp được báo cáo ở bệnh nhân phải lọc máu thường xuyên.[38]
Các yếu tố về tiền sử và thăm khám
Các yếu tố chẩn đoán chủ yếu
Có các yếu tố nguy cơ (thường gặp)
- Các yếu tố nguy cơ chính bao gồm phơi nhiễm chu sinh, nhiều bạn tình, đồng tính nam, người tiêm chích ma túy, tiền sử gia đình bị HBV hoặc ung thư biểu mô tế bào gan, tiếp xúc trong gia đình với người nhiễm bệnh, và có nguồn gốc châu Á hay châu Phi.
Các yếu tố chẩn đoán khác
Khám lâm sàng bình thường (thường gặp)
- Khoảng 70% bệnh nhân nhiễm HBV cấp không có triệu chứng.
Chứng vàng da (không thường gặp)
- Biểu hiện ở khoảng 30% bệnh nhân bị nhiễm HBV cấp và bệnh nhân >30 tuổi có nhiều khả năng có triệu chứng hơn.[60] Cũng biểu hiện ở nhiễm HBV mạn tính với xơ gan hay suy gan.
Chứng gan to (không thường gặp)
- Thường gặp ở nhiễm HBV cấp hơn mạn tính.[60]
Cổ trướng (không thường gặp)
- Thường gặp ở bệnh nhân bị xơ gan liên quan đến HBV mạn tính.
Sốt/ớn lạnh (không thường gặp)
- Một phần hội chứng giống bệnh huyết thanh và biểu hiện ở một số bệnh nhân bị nhiễm HBV cấp.
Khó chịu (không thường gặp)
- Một phần hội chứng giống bệnh huyết thanh và biểu hiện ở một số bệnh nhân bị nhiễm HBV cấp.
Ban dát sẩn hoặc nổi mề đay (không thường gặp)
- Một phần hội chứng giống bệnh huyết thanh và biểu hiện ở một số bệnh nhân bị nhiễm HBV cấp.
Đau vùng gan (không thường gặp)
- Có thể biểu hiện ở bệnh nhân nhiễm HBV cấp hoặc mạn tính.
Mệt mỏi (không thường gặp)
- Biểu hiện ở bệnh nhân nhiễm HBV cấp hoặc mạn tính bao gồm xơ gan.
Buồn nôn/ nôn (không thường gặp)
- Một phần hội chứng giống bệnh huyết thanh và biểu hiện ở một số bệnh nhân bị nhiễm HBV cấp.
Đau khớp/viêm khớp (không thường gặp)
- Một phần hội chứng giống bệnh huyết thanh và biểu hiện ở một số bệnh nhân bị nhiễm HBV cấp.
Lòng bàn tay son (không thường gặp)
- Có thể biểu hiện ở bệnh nhân nhiễm HBV mạn tính bao gồm xơ gan.
Sao mạch (không thường gặp)
- Có thể biểu hiện ở bệnh nhân nhiễm HBV mạn tính bao gồm xơ gan.
Lách to (không thường gặp)
- Thường gặp ở bệnh nhân bị xơ gan liên quan đến HBV mạn tính.
Chứng suy tư thế vận động (không thường gặp)
- Thường gặp hơn ở bệnh nhân bị xơ gan liên quan đến HBV mạn tính bao gồm xơ gan mất bù.
Xét nghiệm chẩn đoán
Xét nghiệm thứ nhất cần yêu cầu
| Xét nghiệm | Kết quả |
| Xét nghiệm chức năng gan
• Đánh giá mức độ nặng của bệnh gan. Hoạt độ aminotransferase (alanine aminotransferase [ALT]/aspartate aminotransferase [AST]), phosphatase kiềm, hoặc bilirubin có thể tăng cao do HBV mạn tính và/hoặc xơ gan bao gồm xơ gan mất bù liên quan đến HBV. Nồng độ albumin có thể thấp. • Đáp ứng sinh hóa với điều trị được xác định là đưa hoạt độ ALT trở về bình thường dựa trên giá trị thông thường. Tuy nhiên, giới hạn trên của mức bình thường (ULN) cho ALT ở người khỏe mạnh thấp hơn các mức dựa trên dân số nói chung, bao gồm người bị bệnh gan cận lâm sàng,[3] và ALT cũng có thể biến động theo thời gian. Ít nhất cần theo dõi trong một năm với tần suất 3 tháng một lần để xác định đáp ứng sinh hóa sau điều trị.[31] |
Aminotransferase (ALT/AST), phosphat kiềm, và bilirubin tăng cao; albumin thấp |
| Công thức máu
• Bệnh nhân có thể tích trung bình hồng cầu thấp và haemoglobin thấp có thể bị xuất huyết do giãn tĩnh mạch liên quan tới xơ gan do HBV. Số lượng tiểu cầu thấp cho thấy tăng áp lực tĩnh mạch cửa do xơ gan liên quan đến HBV gây ra. |
Thiếu máu hồng cầu nhỏ và/ hoặc giảm tiểu cầu |
| Urê và điện giải đồ
• Bệnh nhân có thể bị hạ natri máu do quá tải thể tích hoặc sử dụng thuốc lợi tiểu ở bệnh nhân bị xơ gan liên quan đến HBV có cổ chướng. Mức urê có thể tăng thứ phát do tăng urê máu trước thận, suy thận cấp, suy thận mạn, hay hội chứng gan thận trong xơ gan. |
Hạ natri máu, urê máu cao |
| Xét nghiệm đông máu (PT, INR)
• Xét nghiệm ban đầu để đo PT/INR. Xét nghiệm này hữu ích trong việc xác định khả năng chức năng tổng hợp của gan. PT/INR tăng cao cho thấy bệnh nhân có thể bị xơ gan hay suy gan liên quan đến việc nhiễm HBV. |
Bình thường hoặc tăng cao |
| HBsAg huyết thanh
• Xuất hiện 2 đến 10 tuần sau khi phơi nhiễm với HBV. Ở các trường hợp nhiễm HBV cấp tự khỏi, HBsAg thường không phát hiện được sau 4 đến 6 tháng nhiễm bệnh. Việc HBsAg tồn tại dai dẳng trong >6 tháng cho thấy nhiễm HBV mạn tính. |
Dương tính |
| Anti-HBs huyết thanh
• Xuất hiện vài tuần sau khi HBsAg biến mất và cung cấp miễn dịch suốt đời ở hầu hết bệnh nhân, cho thấy đã hết nhiễm bệnh. Cũng có thể phát hiện ở người được tiêm vắc-xin HBV. |
Dương tính |
| Anti-HBc huyết thanh (IgM)
• Xuất hiện trong vòng vài tuần sau khi nhiễm cấp và vẫn có thể phát hiện trong 4 đến 8 tháng. Trong giai đoạn cửa sổ (vài tuần đến vài tháng) sau khi HBsAg biến mất và trước khi xuất hiện anti-HBs, việc phát hiện anti-HBc IgM có thể là cách duy nhất để chẩn đoán nhiễm HBV cấp. Một số bệnh nhân bị HBV mạn tính hoặc người mang HBV không hoạt động dương tính với kháng thể IgM trong các đợt bùng phát hay tái hoạt cấp, làm cho anti-HBc IgM dương tính không phải là dấu ấn hoàn toàn đáng tin cậy cho nhiễm HBV cấp. |
Dương tính |
| Anti-HBc huyết thanh (IgM + IgG)
• Có thể phát hiện ở hầu như mọi bệnh nhân từng phơi nhiễm HBV (nhiễm HBV cấp hay mạn tính). Nó không mang có miễn dịch bảo vệ. Nó có thể dương tính trong các trường hợp sau: 1) nhiễm HBV cấp: trong giai đoạn cửa sổ (hầu hết là anti-HBc IgM); và 2) nhiễm HBV mạn tính (anti-HBc IgG) khi HBsAg giảm xuống mức không thể phát hiện. Nó thường gặp ở khu vực có tỷ lệ lưu hành nhiễm HBV cao và ở những bệnh nhân đồng nhiễm HIV hoặc viêm gan C. Đây là xét nghiệm đơn độc tốt nhất để sàng lọc việc tiếp xúc trong gia đình với những người nhiễm HBV để xác định xem có cần tiêm vắc-xin hay không. |
Dương tính |
| HBeAg huyết thanh
• Đây là protein vi-rút hòa tan có trong huyết thanh ở giai đoạn đầu của nhiễm HBV cấp và thường biến mất khi hoặc ngay sau khi mức alanine aminotransferase (ALT) huyết thanh đạt đỉnh. HBeAg huyết thanh tồn tại >3 tháng sau khi khởi phát bệnh cho thấy nhiều khả năng tiến triển sang nhiễm HBV mạn tính. anti-HBe có trong huyết thanh của người mang HBsAg cho thấy tình trạng nhiễm cao với tải lượng vi-rút nhân lên cao. Đa số bệnh nhân nhiễm HBV mạn tính có HBeAg dương tính đều bị bệnh gan hoạt động; ngoại trừ trẻ em và người trẻ tuổi bị nhiễm HBV mắc phải ở giai đoạn chu sinh với ALT bình thường. Chuyển đảo huyết thanh tự phát từ HBeAg dương tính thành HBeAg âm tính với anti-HBe dương tính thường liên quan đến giảm HBV DNA (>3 log). Một số bệnh nhân (thường là người cao tuổi) có thể bị bệnh gan hoạt động với HBV DNA cao hoặc có thể phát hiện mà không có HBeAg trong huyết thanh, dẫn đến nhiễm HBV mạn tính có HBeAg âm tính. Cần kiểm tra định kỳ tình trạng HBeAg ở bệnh nhân có HBeAg dương tính trong quá trình điều trị nhiễm HBV mạn tính, đặc biệt nếu không thể phát hiện tải lượng HBV DNA trong huyết thanh, để theo dõi chuyển đảo huyết thanh. |
Dương tính |
| HBV DNA
• Có thể đo lường bằng xét nghiệm định lượng hoặc định tính. Thường sử dụng phản ứng khuếch đại PCR để đo tải lượng HBV DNA. Công nghệ PCR mới hơn cho phép cải thiện độ nhạy với khả năng phát hiện 5 đến 10 IU/mL và phạm vi dao động lớn hơn tối đa 8 đến 9 log10 IU/mL. Tổ chức Y tế Thế giới đã xác định tiêu chuẩn quốc tế chung để đo HBV DNA là đơn vị quốc tế mỗi millilit (1 IU/mL bằng khoảng 5,6 bản sao/mL). Người ta thường sử dụng tải lượng HBV DNA để đánh giá sự phù hợp cho liệu pháp kháng vi- rút và theo dõi đáp ứng điều trị. Hội nghị năm 2000 của NIH đã chọn giá trị thay đổi >20.000 IU/mL (>100.000 bảo sao/mL) làm tiêu chuẩn chẩn đoán nhiễm HBV mạn tính. Tuy nhiên, tải lượng HBV DNA có thể thay đổi nhiều ở bệnh nhân bị nhiễm HBV mạn tính (từ không phát hiện đến >2.000.000 IU/mL). Do đó, việc theo dõi liên tục quan trọng hơn là đánh giá một lần để tiên lượng và xác định nhu cầu điều trị. |
Không thể phát hiện hoặc tăng cao |
Các xét nghiệm khác cần cân nhắc
| Xét nghiệm | Kết quả |
| Anti-HBe huyết thanh
• Chuyển đảo huyết thanh từ HBeAg dương tính thành anti-HBe dương tính là chỉ điểm hữu ích về việc thải trừ vi-rút, cho thấy thải trừ HBV liên quan đến điều trị. Bệnh nhân chuyển đảo huyết thanh kéo dài thường có kết quả mô học gan cải thiện. Tuy nhiên, một số bệnh nhân sẽ tự có anti-HBe dương tính mà không thải trừ hết vi-rút do đột biến tiền nhân hoặc đột biến vùng điều hòa nhân (HBV mạn tính có HBeAg âm tính) hoặc chuyển sang trạng thái mang bệnh mạn tính không có triệu chứng. • Chuyển đảo huyết thanh có thể là hiện tượng tạm thời và cần được phân tích kết hợp với tải lượng HBV DNA huyết thanh. |
Dương tính |
| Kiểu gen HBV
• Tám kiểu gen của HBV đã được mô tả: A đến H. |
Dương tính |
| Siêu âm gản
• Được sử dụng để sàng lọc ung thư biểu mô tế bào gan (HCC), cùng với AFP. Độ nhạy của siêu âm để phát hiện HCC là 60% (CI 95% 44% đến 76%) và độ đặc hiệu 97% (CI 95% 95% đến 98%). |
Bờ không đều và nhu mô cản âm kém |
| Amoniac huyết thanh
• Thường tăng cao trong bệnh não gan thứ phát sau xơ gan hay suy gan tối cấp liên quan đến HBV cấp. |
Bình thường hoặc tăng cao |
| Sinh thiết gan
• Được sử dụng để đánh giá mức độ tổn thương gan và/hoặc xơ hóa và loại trừ nguyên nhân dẫn đến bệnh gan khác. Chỉ định sinh thiết gan rõ ràng nếu có khả năng ảnh hưởng đến quyết định điều trị. Tuy nhiên, sinh thiết gan có thể không cần thiết ở mọi bệnh nhân nhiễm HBV mạn tính, như các ca bệnh có bằng chứng lâm sàng, xét nghiệm, hay nội soi của xơ gan mà quyết định điều trị cho họ không bị ảnh hưởng. • Sinh thiết gan hữu ích nhất ở bệnh nhân không đáp ứng các tiêu chuẩn hiện tại của Hiệp hội Nghiên cứu Bệnh Gan Hoa Kỳ (AASLD) để bắt đầu điều trị nhiễm HBV mạn tính. • Cần cân nhắc sinh thiết ở bệnh nhân có giá trị alanine aminotransferase (ALT) gần giới hạn trên của mức bình thường và >40 tuổi, và bệnh nhân có tình trạng viêm hoại tử vừa và/hoặc các đặc điểm của bệnh gan tiến triển khi sinh thiết. |
Bệnh nhân có thể có: a) sinh thiết gan bình thường, không có tình trạng viêm hoại tử và/ hoặc xơ hóa, b) tình trạng viêm hoại tử từ nhẹ đến vừa có/ không có xơ hóa, c) tình trạng viêm hoại tử từ vừa đến nặng, có xơ hóa hoặc xơ gan tiến triển |
| Alpha-fetoprotein (AFP)
• Được sử dụng để sàng lọc ung thư biểu mô tế bào gan (HCC) kết hợp với siêu âm 6 đến 12 tháng/lần ở người mang HBV có nguy cơ cao. Mức AFP tăng cao ở 75% bệnh nhân bị HCC, nhưng cũng có thể bình thường. Độ nhạy nằm trong khoảng từ 41% đến 65% và độ đặc hiệu nằm trong khoảng từ 80% đến 94%. Mức AFP >400 nanogram/mL có độ đặc hiệu 95% đối với HCC. |
Bình thường hoặc tăng cao |
Các xét nghiệm giai đoạn đầu
| Xét nghiệm | Kết quả |
| Đo độ đàn hồi thoáng qua
• Phương án không xâm lấn để đánh giá tổn thương gan bằng cách đo độ cứng của gan khi siêu âm. Tại châu Âu, đo độ đàn hồi thoáng qua là phương pháp phổ biến để xác định xơ gan; tuy nhiên, việc sử dụng phương pháp này bị hạn chế do dương tính giả do tình trạng viêm gan đáng kể và thiếu tiêu chuẩn thống nhất để tính toán độ cứng của gan. Cần nghiên cứu bổ sung để chuẩn hóa xét nghiệm không xâm lấn này cho đánh giá xơ gan. |
Độ cứng của gan tăng |
Chẩn đoán khác biệt
| Tình trạng | Các dấu hiệu/triệu chứng khác biệt | Các xét nghiệm khác biệt |
| Nhiễm vi-rút viêm gan A (HAV) cấp | • Có thể không có các khác biệt về dấu hiệu và triệu chứng. | • Xét nghiệm huyết thanh sẽ dương tính đối với kháng thể HAV-IgM. |
| Nhiễm vi-rút viêm gan C (HCV) cấp | • Có thể không có các khác biệt về dấu hiệu và triệu chứng. | • Xét nghiệm huyết thanh sẽ dương tính đối với kháng thể HCV, và RNA-PCR sẽ dương tính đối với viêm gan C. Thông thường, bệnh nhân nhiễm HCV cấp có triệu chứng sẽ cho thấy mức alanine aminotransferase (ALT), aspartate aminotransferase (AST), và bilirubin rất cao. |
| Nhiễm HCV cấp | • Có thể không có các khác biệt về dấu hiệu và triệu chứng. | • Bệnh nhân có thể có chức năng gan bình thường hoặc tăng cao với kháng thể HCV và RNA- PCR HCV huyết thanh dương tính. |
| Đồng nhiễm vi-rút viêm gan D (HDV) và HBV | • Có thể không có các khác biệt về dấu hiệu và triệu chứng. Bệnh nhân có thể có kết quả tăng đột ngột trong xét nghiệm về gan. | • RNA viêm gan D huyết thanh và kháng thể IgM viêm gan D sẽ dương tính. |
| Nhiễm vi-rút viêm gan E
(HEV) cấp |
• Các triệu chứng và dấu hiệu có thể giống với viêm gan vi-rút cấp khác. Tình trạng này thường gặp nhất ở phụ nữ mang thai tại các nước đang phát triển có khí hậu nóng. | • Kháng thể HEV huyết thanh (IgM) sẽ dương tính, bao gồm cả PCR HEV RNA huyết thanh. |
| Viêm gan do cytomegalovirus (CMV) | • Có thể có tiền sử suy giảm miễn dịch bao gồm cả ghép tạng. | • Kháng thể CMV-IgM và PCR CMV DNA huyết thanh dương tính. |
| Viêm gan do vi-rút Epstein Barr (EBV) | • Bệnh nhân thường có sốt, mệt mỏi, viêm họng, tình trạng khó chịu, đau cơ, và hạch to (đặc biệt là hạch cổ sau). | • Xét nghiệm đơn điểm và kháng thể heterophile huyết thanh dương tính. Kháng thể EBV- IgM và PCR EBV DNA huyết thanh dương tính. |
| Viêm gan do vi-rút herpes simplex (HSV) | • Bệnh nhân có thể bị ức chế miễn dịch hay mang thai nhưng cũng có thể có miễn dịch bình thường. Bệnh nhân có thể biểu hiện như viêm gan vi-rút cấp có hoặc không có suy gan. | • Kháng thể IgM HSV và PCR HSV DNA huyết thanh dương tính. |
| Viêm gan cấp do rượu | • Có thể không có các khác biệt về dấu hiệu và triệu chứng. Tiền sử sử dụng rượu trung bình hoặc nhiều. | • Xét nghiệm huyết thanh âm tính đối với viêm gan vi-rút. Mức aspartate aminotransferase (AST) cao hơn alanine aminotransferase (ALT), với gamma glutamyl transferase tăng cao. Sinh thiết gan có thể cho thấy gan nhiễm mỡ, tế bào gan dạng thả bóng, tiểu thể Mallory, thâm nhiễm bạch cầu trung tính quanh tiểu thủy, có hoặc không có xơ hóa quanh tế bào. |
| Viêm gan do thuốc hoặc độc tố | • Có thể không có các khác biệt về dấu hiệu và triệu chứng. Có thể có tiền sử phơi nhiễm thuốc hay độc tố gây tổn thương cho gan. | • Sinh thiết gan có thể cho thấy các đặc điểm của dạng tổn thương tế bào gan, ứ mật hoặc kết hợp, bao gồm cả ứ mật. |
| Viêm gan tự miễn | • Có thể không có các khác biệt về dấu hiệu và triệu chứng. | • Nồng độ globulin huyết thanh, kháng thể kháng nhân, kháng thể kháng cơ trơn, kháng thể vi tiểu thể gan/thận, và/hoặc kháng thể chống lại kháng nguyên gan hòa tan/kháng nguyên tụy gan có thể tăng. Mô học gan có thể cho thấy viêm gan bề mặt cùng với thâm nhiễm tương bào. |
| tắc mật | • Triệu chứng liên quan đến tắc mật có thể bao gồm đau vùng gan, sốt/rét run, vàng da, ngứa, buồn nôn và nôn. | • Siêu âm, chụp CT hay chụp MRI đường mật có thể cho thấy giãn đường mật. Trong trường hợp tắc ác tính, có thể nhìn thấy khối u trong gan. |
| Di căn gan | • Bệnh nhân có thể không có triệu chứng hoặc có triệu chứng và dấu hiệu của bệnh ác tính tại các vị trí ban đầu, bao gồm cả đặc điểm tắc mật. | • Chụp CT hoặc MRI ổ bụng có thể cho thấy một hoặc nhiều khối u di căn trong gan. |
| Viêm gan thiếu máu cục bộ cấp | • Bệnh nhân có thể có triệu chứng thiếu máu cục bộ như suy tim cấp, sốc hay nhiễm trùng máu. | • Điện tâm đồ có thể cho thấy đặc điểm của thiếu máu cục bộ hoặc nhồi máu cơ tim. XQ ngực thẳng và siêu âm tim có thể cho thấy đặc điểm của suy tim xung huyết. Siêu âm Doppler gan có thể cho thấy huyết khối tĩnh mạch cửa hoặc tắc động mạch gan cấp. |
| Hội chứng Budd-Chiari | • Có thể không có các khác biệt về dấu hiệu và triệu chứng. | • Siêu âm Doppler có thể cho thấy huyết khối tĩnh mạch gan hoặc huyết khối tĩnh mạch chủ dưới. |
| Gan nhiễm mỡ cấp khi đang mang thai | • Phụ nữ mang thai có thể biểu hiện vàng da. | • Chẩn đoán loại trừ các bệnh
khác có triệu chứng và dấu hiệu đặc trưng ở phụ nữ mang thai. |
| Bệnh Wilson | • Có thể không có các khác biệt về dấu hiệu và triệu chứng. | • Nồng độ đồng niệu tăng,
ceruloplasmin huyết thanh giảm, và vòng Kayser-Fleischer khi khám mắt bằng đèn khe. |
| Bệnh thừa sắt | • Có thể không có các khác biệt về dấu hiệu và triệu chứng. | • Độ bão hòa sắt cao (>45% độ
bão hòa transferrin) và đột biến gen bệnh hemochromatosis. Sinh thiết gan chỉ ra tình trạng ứ sắt trong tế bào gan. |
Các tiêu chí chẩn đoán
Các giai đoạn nhiễm HBV mạn tính theo Hiệp hội Nghiên cứu Bệnh Gan Hoa Kỳ (AASLD)[3]
AASLD phân loại nhiễm HBV mạn tính thành bốn giai đoạn, thể hiện mối quan hệ giữa sự nhân lên và tiến hóa vi-rút và đáp ứng miễn dịch vật chủ.
- Dung nạp miễn dịch: dương tính HBeAg; alanine aminotransferase (ALT) bình thường; HBV DNA tăng cao (thường là >1 triệu IU/mL); sinh thiết gan cho thấy tình trạng viêm và xơ hóa rất ít.
- Hoạt động miễn dịch HBeAg dương tính: ALT tăng cao; HBV DNA tăng cao (>20.000 IU/mL); tình trạng viêm hoặc xơ hóa gan từ vừa đến nặng.
- Viêm gan B mạn tính không hoạt động: HBeAg âm tính và anti-HBe dương tính; ALT bình thường; HBV DNA thấp hoặc không thể phát hiện; sinh thiết gan cho thấy tình trạng viêm hoại tử rất ít và xơ hóa thay đổi (thể hiện tổn thương gan trong giai đoạn hoạt động miễn dịch HBeAg dương tính).
- Tái hoạt miễn dịch HBeAg âm tính: ALT tăng cao; HBV DNA tăng cao (>2.000 IU/mL); tình trạng viêm hoặc xơ hóa từ vừa đến nặng; trong số những người chuyển đảo huyết thanh từ HBeAg dương tính sang anti-HBe dương tính, 10% đến 30% có thể tiếp tục có ALT và HBV DNA tăng cao, và 10% đến 20% có thể tái hoạt sau nhiều năm bệnh không hoạt động.
Các giai đoạn nhiễm HBV mạn tính theo Hiệp hội Nghiên cứu Gan Châu Âu (EASL)[31]
Hướng dẫn của EASL chia HBV mạn tính thành năm giai đoạn theo dấu ấn huyết thanh và bệnh gan.
- Nhiễm HBV mạn tính HBeAg dương tính: ALT bình thường; HBV DNA tăng cao; sinh thiết gan cho thấy tình trạng viêm và xơ hóa rất ít; trước đây được gọi là giai đoạn ‘dung nạp miễn dịch’.
- Viêm gan B mạn tính có HBeAg dương tính: ALT tăng cao, HBV DNA tăng cao; tình trạng viêm hoại tử gan từ vừa đến nặng và tiến triển nhanh thành xơ hóa; ở hầu hết bệnh nhân, chuyển đảo huyết thanh HBeAg và ức chế HBV DNA xảy ra và bệnh nhân bước vào giai đoạn nhiễm trùng HBeAg âm tính, trong khi ở những bệnh nhân khác, việc kiểm soát HBV không diễn ra và họ tiến triển sang giai đoạn viêm gan B mạn HbeAg âm tính, có thể tồn tại nhiều năm; trước đây được gọi là giai đoạn ‘phản ứng miễn dịch HBeAg dương tính’.
- Nhiễm HBV mạn tính có HBeAg âm tính: anti-HBe dương tính; ALT bình thường; HBV DNA thấp hoặc không thể phát hiện; sinh thiết gan cho thấy tình trạng viêm hoại tử rất ít và xơ hóa thấp; trước đây được gọi là giai đoạn ‘người mang bệnh không hoạt động’.
- Viêm gan B mạn HBeAg âm tính: có anti-HBe; HBV DNA từ vừa đến nặng; ALT tăng cao (dai dẳng hoặc từng đợt); tình trạng viêm hoại tử và xơ hóa từ vừa đến nặng.
- HBsAg âm tính: bệnh nhân có HBsAg âm tính và anti-HBc dương tính, và có thể phát hiện anti-HBe; ALT bình thường; HBV DNA thường không phát hiện thấy; ức chế miễn dịch ở những bệnh nhân này có thể dẫn đến tái hoạt; giai đoạn này còn được gọi là nhiễm HBV tiềm ẩn.
![Viêm gan B: Nguyên nhân, chẩn đoán và hướng dẫn điều trị theo BMJ 15 Hình 3: Các giai đoạn nhiễm viêm gan B mạn tính [AASLD = Hiệp hội Nghiên cứu Bệnh Gan Hoa Kỳ, EASL = Hiệp hội Nghiên cứu Gan Châu Âu; *cccDNA]](https://nhathuocngocanh.com/wp-content/uploads/2022/03/viem_gan_B_nguyen_nhan_chan_doan_dieu_tri_theo_bmj_hinh3.jpg)
Điều trị
Cách tiếp cận điều trị từng bước
Điều trị nhiễm cấp
Bệnh nhân nhiễm HBV cấp thường chỉ cần điều trị hỗ trợ. Hơn 95% những người nhiễm HBV cấp sẽ có chuyển đảo huyết thanh với xuất hiện anti-HBs mà không cần điều trị.[31] [83]
Bệnh nhân tiến triển viêm gan tối cấp hay suy gan do HBV cấp có thể được điều trị bằng thuốc tương tự nucleoside/ nucleotide[31] [84] và cũng cần được đánh giá đồng thời việc ghép gan nếu nguy cơ tử vong cao liên quan đến suy gan mà không ghép gan.[85]
Điều trị nhiễm HBV mạn tính
Nhu cầu điều trị kháng vi-rút trong nhiễm HBV mạn tính được dựa trên hoạt độ alanine aminotransferase (ALT), tải lượng HBV DNA huyết thanh và mức độ nặng của bệnh gan, và cần theo dõi thường xuyên để xác định giai đoạn nhiễm trùng. Các yếu tố bổ sung cần được cân nhắc trước khi bắt đầu điều trị bao gồm độ tuổi bệnh nhân, khả năng đáp ứng, biến cố bất lợi tiềm ẩn, tiền sử gia đình về ung thư tế bào gan, và biểu hiện ngoài gan.[3] [31]
Mục tiêu cuối cùng của việc điều trị là cải thiện rối loạn chức năng gan và xuất hiện trạng thái không có bệnh, được đánh dấu bằng chuyển đảo huyết thanh từ HBsAg dương tính thành âm tính và sản sinh kháng thể HBs. Việc điều trị đôi khi có thể dẫn đến mất HBeAg và chuyển đảo huyết thanh HBeAg thành anti-HBe ở bệnh nhân HBV mạn tính HBeAg dương tính. Tuy nhiên, việc loại trừ hoàn toàn HBV là hiếm gặp với các phương pháp điều trị hiện có, vì vậy mục tiêu điều trị chính ở hầu hết bệnh nhân nhiễm HBV mạn tính là ức chế HBV DNA huyết thanh ở mức không phát hiện được lâu dài và bền vững.
Mức ức chế HBV DNA tỷ lệ nghịch với sự xuất hiện tình trạng kháng thuốc. Do đó, ức chế HBV DNA huyết thanh càng nhiều thì càng tốt cho kết quả lâu dài mà không dẫn đến tình trạng kháng vi-rút. Ức chế kéo dài có thể giảm tỷ lệ xơ hóa, suy gan và ung thư biểu mô tế bào gan (HCC) ở bệnh nhân bị HBV mạn tính (nhưng không loại bỏ hết nguy cơ).[86] [87] [88] [89] Tuy nhiên, không có thử nghiệm ngẫu nhiên nào hỗ trợ điều này (RCT như vậy sẽ tốn kém đến mức không thể thực hiện và kéo dài 20-30 năm).
Hiện có một số thuốc được phê duyệt để điều trị HBV mạn tính: interferon alfa 2b, peginterferon alfa 2a, và chất tương tự nucleoside/nucleotide. Chất tương tự nucleoside là entecavir và lamivudine. Chất tương tự nucleotide là tenofovir disoproxil và adefovir. Các lựa chọn ưu tiên về thuốc đơn trị liệu ban đầu là entecavir, peginterferon alfa-2a, và tenofovir disoproxil.[3] [31] [90] Entecavir và tenofovir disoproxil đều được biết đến như là các thuốc kháng vi- rút có hiệu quả cao,[91] mặc dù không có thử nghiệm nào trực tiếp so sánh 2 thuốc này. Tuy nhiên, các hướng dẫn điều trị HBV mạn tính được phát triển liên tục, đặc biệt là với việc ra đời các thuốc kháng vi-rút mới hiệu quả cao với nguy cơ kháng thuốc thấp hơn. Hướng dẫn có thể khác nhau theo từng nước và cần tham khảo hướng dẫn của địa phương.
Trong khi interferon thường được cho dùng trong thời gian định sẵn, thì chất tương tự nucleoside/nucleotide được dùng cho đến khi đạt được kết điểm cụ thể, có thể đồng nghĩa với việc điều trị lâu dài. Đối với bệnh nhân HBeAg dương tính, ức chế vi-rút có thể được duy trì bằng điều trị hiện tại ở 50% đến 90% bệnh nhân nếu dừng điều trị sau khi có chuyển đảo huyết thanh HBeAg.[92] Tuy nhiên, ở bệnh nhân HBeAg âm tính, tình trạng tái phát thường xảy ra, ngay cả khi ức chế HBV DNA xuống mức không phát hiện được trong hơn 1 năm, làm cho kết điểm điều trị trở nên không rõ ràng và có thể cần điều trị suốt đời. Hướng dẫn của Hiệp hội Nghiên cứu Bệnh Gan Hoa Kỳ (AASLD) khuyến cáo bệnh nhân có HBeAg dương tính (không có tình trạng xơ hóa) chuyển đảo huyết thanh thành anti-HBe có thể dừng điều trị bằng chất tương tự nucleoside/nucleotide sau thời gian củng cố 12 tháng (tức là 12 tháng có ALT bình thường liên tục và không phát hiện được HBV DNA huyết thanh).[3]
HBV không có tình trạng đồng nhiễm/bệnh đồng mắc
Phải bắt đầu điều trị ngay nếu bệnh nhân có vàng da hay mất bù, hoặc nếu sinh thiết gan cho thấy tình trạng viêm từ vừa đến nặng và/hoặc xơ hóa nghiêm trọng.[3]
Hướng dẫn của AASLD khuyến cáo điều trị kháng vi-rút cho người lớn nhiễm HBV mạn tính hoạt động miễn dịch, được xác định là những người có HBeAg dương tính, với mức HBV DNA>20.000 đơn vị quốc tế (IU)/mL và ALT cao hơn gấp đôi giới hạn trên của mức bình thường (ULN) hoặc bệnh mô học đáng kể; hoặc HBeAg âm tính, với HBV DNA >2000 IU/mL, và ALT cao hơn gấp đôi ULN hoặc bệnh mô học đáng kể.[3]
Kết điểm điều trị là chuyển đảo huyết thanh từ HBeAg dương tính thành HBeAg âm tính với việc sản sinh anti-HBe. Tuy nhiên, một số bệnh nhân chuyển đảo huyết thanh HBeAg thành anti-HBe vẫn có thể cho thấy HBV DNA thấp hay HBV DNA dao động trong thời gian dài. Những bệnh nhân này được theo dõi cẩn thận về bùng phát HBV và đảo ngược thành HBeAg dương tính. Trong tình huống này, những bệnh nhân này có thể cần được điều trị lại. Có thể cân nhắc peginterferon cho bệnh nhân HBeAg dương tính, bệnh gan bù hoàn toàn, đặc biệt với HBV kiểu gen A, ALT cao, và HBV DNA huyết thanh thấp,[8] [93] [94] [95] vì nó làm tăng tỷ lệ đáp ứng bền vững khi không điều trị. Một số nghiên cứu sử dụng thuốc uống và peginterferon cho thấy các thay đổi về nồng độ HBsAg định lượng trong quá trình điều trị có thể dự đoán việc chuyển đảo huyết thanh hay mất HBeAg.[96] [97] [98] Nghiên cứu cũng cho thấy việc giảm HBsAg có thể là yếu tố dự đoán việc mất HBsAg và đáp ứng virus bền vững khi không điều trị.[99] [100] [101] Nhiều nghiên cứu đã được thực hiện để kiểm tra tính hiệu quả của các dạng bào chế interferon khác nhau dưới dạng đơn trị liệu hay kết hợp với một chất tương tự nucleoside/nucleotide. Hiện tại, không có nhiều dữ liệu về tính an toàn và hiệu quả liên quan đến liệu pháp kết hợp giữa peginterferon và chất tương tự nucleotide/nucleoside và không khuyến cáo sử dụng phương pháp này.[3] [31]
Ưu điểm của điều trị bằng interferon/peginterferon alfa bao gồm thời gian điều trị ngắn, đáp ứng bền vững, và không có tình trạng kháng thuốc, nhưng có các tác dụng phụ khó chịu và đòi hỏi dùng thuốc ngoài đường uống và theo dõi thường xuyên. Ưu tiên peginterferon so với dạng không pegylated vì tính đơn giản.[3] Các yếu tố dự đoán mức đáp ứng interferon bao gồm:[102]
- ALT ban đầu >5 lần ULN
- HBV DNA ban đầu <20.000.000 IU/mL
- Kiểu gen HBV A hoặc B.
Bệnh nhân đã khẳng định bùng phát vi-rút có thể được chuyển sang điều trị kháng vi-rút khác có hàng rào kháng thuốc cao, hoặc có thể thêm điều trị kháng vi-rút thứ hai với xét nghiệm bổ sung kháng thuốc; hiện không có đủ bằng chứng để khuyến cáo phương pháp nào tốt hơn phương pháp nào.[3]
Xơ gan
Việc điều trị được thực hiện để cải thiện tỷ lệ sống sót và giảm tỷ lệ tàn tật và tỷ lệ tử vong liên quan đến gan bằng cách phòng ngừa suy gan hoặc đòi hỏi ghép gan. Đối với bệnh nhân xơ gan mất bù hay còn bù, lựa chọn điều trị tốt nhất là đơn trị liệu ở dạng entecavir hoặc tenofovir disoproxil. Điều này sẽ làm giảm nguy cơ kháng thuốc và cũng ức chế vi-rút nhanh trước khi ghép gan ở bệnh nhân mất bù.[3] Tránh dùng interferon và peginterferon alfa ở bệnh nhân có bằng chứng về xơ gan mất bù do báo cáo tỷ lệ cao biến chứng bất lợi nghiêm trọng, bao gồm sepsis và nguy cơ mất bù liên quan đến điều trị.[103] Chỉ có thể cân nhắc sử dụng peginterferon alfa cho bệnh nhân chọn lọc mắc xơ gan còn bù nhưng không bị tăng áp lực tĩnh mạch cửa.[31] [104] Adefovir có thể không phải là lựa chọn tốt nhất cho đơn trị liệu đối với bệnh nhân xơ gan mất bù vì nguy cơ kháng thuốc và độc tính trên thận có thể cao khi sử dụng kéo dài. Cũng không sử dụng một mình lamivudine cho nhóm bệnh nhân này do nguy cơ bùng phát và suy gan liên quan đến kháng lamivudine.[105] Một phân tích gộp gồm 22 nghiên cứu đánh giá kết cục về tính hiệu quả và an toàn của các chất tương tự nucleoside/nucleotide đường uống khác nhau ở bệnh nhân bị xơ gan HBV mất bù và thấy rằng, mặc dù tất cả các chất tương tự nucleoside/nucleotide đường uống cải thiện các thông số vi-rút học, sinh hóa và lâm sàng sau 1 năm, hiệu quả của lamivudine bị hạn chế do kháng thuốc trong khi hiệu quả của adefovir bị hạn chế do dược lực và thời gian khởi phát tác dụng chậm hơn.[106]
Hướng dẫn của AASLD khuyến cáo bệnh nhân bị xơ gan còn bù về mặt lâm sàng và HBV DNA <2000 IU/mL cần được điều trị kháng vi-rút bất kể hoạt độ ALT để giảm nguy cơ mất bù; bệnh nhân bị xơ gan còn bù và tải lượng HBV DNA >2.000 U/mL được điều trị theo khuyến cáo cho viêm gan B mạn tính hoạt động miễn dịch HBeAg dương tính và âm tính.[3] Nghiên cứu đã chỉ ra rằng việc ức chế ADN vi-rút HBV có thể dừng quá trình tiến triển tự nhiên của bệnh gan thành xơ gan mất bù[105] [107] và một số trường hợp cho thấy cải thiện về mô học gan.[108] Hiện không có bằng chứng về thời gian điều trị tối ưu cho xơ gan còn bù; nếu dừng điều trị, cần theo dõi bệnh nhân chặt chẽ.[3]
Ở bệnh nhân xơ gan mất bù bị HBV mạn tính, họ cần được giới thiệu đến trung tâm ghép gan. Chống chỉ định peginterferon đối với xơ gan mất bù.[31] Khuyến cáo tăng liều entecavir cho điều trị.[31] Tenofovir disoproxil là phương án điều trị thay thế cho bệnh nhân xơ gan mất bù.[31] Dữ liệu cho thấy cả hai thuốc này đều an toàn và hiệu quả,[109] [110] [111] mặc dù tình trạng nhiễm axit lactic xảy ra khi sử dụng lâu dài chất tương tự nucleoside như entecavir.[112]
Đồng nhiễm HIV
HBV không có ảnh hưởng đáng kể đến diễn biến tự nhiên nhiễm HIV, tuy nhiên việc nhiễm và điều trị HIV có thể ảnh hưởng đáng kể đến diễn biến tự nhiên của HBV. Tái hoạt HBV có thể xảy ra ở bệnh nhân nhiễm HIV.[113] Bệnh nhân đồng nhiễm HIV và HBV có thể có tỷ lệ chuyển đảo huyết thanh thấp hơn và tải lượng HBV DNA huyết thanh cao hơn.[114]
Hướng dẫn của Hoa Kỳ khuyến cáo bệnh nhân đồng nhiễm HIV và HBV nên điều trị kháng retrovirus (ART) bao gồm các thuốc có tác dụng kháng cả hai loại vi-rút bất kể số lượng tế bào CD4 hay nhu cầu cần điều trị HBV. Phác đồ ưu tiên là tenofovir disoproxil và emtricitabine. Hầu hết bệnh nhân nhận ART cần được điều trị HBV suốt đời. Các lựa chọn bị hạn chế nếu bệnh nhân từ chối ART; không nên sử dụng thuốc điều trị HBV có tác dụng trực tiếp nếu không dùng phác đồ ART ức chế đầy đủ do khả năng phát triển kháng ART của HIV.[114]
Đồng nhiễm viêm gan D
Viêm gan tối cấp thường được nhận thấy ở bệnh nhân mắc HBV đồng nhiễm HDV.[115] Kết điểm điều trị là việc ức chế nhân lên HDV, bình thường hóa ALT, và cải thiện mô học của gan. Interferon hiện là phương pháp điều trị chính.[3] Cần điều trị lâu dài; tuy nhiên, cần có thêm nghiên cứu để xác định thời gian điều trị ưu tiên.[115] [116] Một nghiên cứu cho thấy liều cao interferon alfa có đáp ứng về vi-rút học, mô học và sinh hóa cao hơn so với interferon alfa liều thấp.[117] Hầu hết bệnh nhân tái phát sau khi ngừng interferon alfa liều cao nhưng sẽ duy trì cải thiện mô học gan sau 10 năm.[118] Trước đây, peginterferon alfa 2b đã được phê chuẩn cho đồng nhiễm viêm gan D, nhưng đã bị dừng ở một số nước vì lý do thương mại (không phải vì lý do an toàn). Chất tương tự nucleoside hoặc nucleotide có kết quả gây thất vọng.
Mang thai và cho con bú
Cần cân nhắc điều trị kháng vi-rút nếu tải lượng vi-rút >200.000 IU/mL. Dữ liệu cho thấy tenofovir disoproxil là thuốc được lựa chọn cho bệnh nhân mang thai nhiễm HBV nhờ vào dữ liệu an toàn tuyệt vời và hàng rào kháng thuốc cao.[31] [119] Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) phân loại thuốc này thuộc nhóm B cho phụ nữ mang thai và thường được bắt đầu dùng trong ba tháng cuối thai kỳ. Trong một thử nghiệm đối chứng ngẫu nhiên và tổng quan hệ thống, tenofovir disoproxil được cho dùng trong ba tháng cuối thai kỳ đã được chứng minh là làm giảm tỷ lệ lây truyền từ mẹ sang con khi được cho dùng cùng với vắc-xin viêm gan B và globulin miễn dịch viêm gan B ở trẻ sơ sinh.[120] [121] Có thể cho dùng lamivudine trong ba tháng cuối thai kỳ và thuốc này cho thấy
tính an toàn và làm giảm việc lây truyền HBV chu sinh và trong tử cung khi được cho dùng cùng với vắc-xin viêm gan B và globulin miễn dịch viêm gan B lúc sơ sinh.[122] [123] [124] [125] [126] Phụ nữ mang thai khi đang dùng peginterferon hoặc entecavir cần được chuyển sang phác đồ an toàn hơn. Thời gian điều trị để dự phòng lây truyền chu sinh không được xác định rõ và có thể tiếp tục trong 3 tháng sau sinh hay dừng lúc sinh; việc dừng lúc sinh có thể có lợi vì nó không ảnh hưởng đến việc cho con bú.[31]
Theo đánh giá của 10 nghiên cứu, cho con bú sau khi dùng biện pháp dự phòng miễn dịch sơ sinh kịp thời không làm tăng tỷ lệ lây truyền so với việc không cho con bú.[127] Tính an toàn của việc dùng thuốc kháng vi-rút trong khi cho con bú chưa được nghiên cứu kỹ và mặc dù không có chống chỉ định, các nhà sản xuất thuốc có thể khuyến cáo tránh cho con bú.[3] [31]
Tại Hoa Kỳ, trẻ có mẹ dương tính với HBsAg cần được tiêm vắc-xin viêm gan B đơn giá và globulin miễn dịch viêm gan B (HBIG) trong vòng 12 giờ sau sinh. Nếu chưa rõ tình trạng HBsAg của mẹ, trẻ cần được tiêm vắc-xin viêm gan B trong vòng 12 giờ sau sinh, và trẻ nhẹ hơn 2000 g cũng cần được tiêm HBIG. Đối với trẻ nặng hơn 2000 g, cần xác định tình trạng HBsAg của người mẹ và nếu dương tính, cần tiêm HBIG cho trẻ ngay khi có thể trong vòng 7 ngày. Trẻ nhỏ có mẹ dương tính với HBsAg cần được xét nghiệm HBsAg và anti-HBs lúc 9 đến 12 tháng tuổi, hoặc 1 đến 2 tháng sau khi tiêm xong các mũi vắc-xin viêm gan B. Trẻ nhỏ có mẹ âm tính với HBsAg cần được tiêm một mũi vắc- xin viêm gan B trong vòng 24 giờ sau khi sinh (nếu sức khỏe ổn định và cân nặng lúc sinh hơn 2000 g), hoặc một mũi lúc được 1 tháng tuổi sinh lý hay xuất viện nếu cân nặng lúc sinh dưới 2000g.[50]
Trẻ em
Viêm gan B mạn tính xảy ra mà không có triệu chứng ở hầu hết trẻ em. Nhìn chung, phương pháp điều trị bảo tồn đối với HBV là có thể chấp nhận do dữ liệu lâm sàng và lựa chọn điều trị hạn chế. Theo kết luận của hội đồng chuyên gia Tổ chức Viêm gan B, không có chỉ định điều trị trong giai đoạn trạng thái mang bệnh không hoạt động, và chưa xác định được lợi ích của việc điều trị cho trẻ em ở giai đoạn dung nạp miễn dịch do nguy cơ phát triển kháng thuốc cao.[128] Theo hướng dẫn của AASLD, trẻ có ALT lớn hơn 1,3 lần ULN cần được cân nhắc điều trị nếu ALT vẫn tăng cao trong hơn 6 tháng cùng với việc tăng HBV DNA.[3] Tuy nhiên, nhìn chung tải lượng HBV DNA rất cao ở trẻ em; nếu có <10A4 IU/mL, có thể’ trì hoãn điều trị cho đến khi loại trừ nguyên nhân khác gây ra bệnh gan và chuyển đảo huyết thanh HBeAg nguyên phát.[3] Đối với trẻ ở giai đoạn hoạt động miễn dịch hay tái hoạt, sinh thiết gan có thể giúp hướng dẫn đưa ra quyết định điều trị và tiền sử gia đình về bệnh gan, đặc biệt là ung thư biểu mô tế bào gan có thể dẫn đến việc điều trị sớm trong một số ca bệnh.[128] Việc điều trị cần do bác sĩ có kinh nghiệm về điều trị cho trẻ em nhiễm HBV tiến hành.
Nếu cần điều trị, hướng dẫn của AASLD cho biết interferon alfa 2b được phê chuẩn cho trẻ > 1 tuổi, lamivudine và entecavir được phê chuẩn cho trẻ >2 tuổi, (mặc dù entecavir có liên quan đến nguy cơ kháng thuốc thấp hơn), và tenofovir disoproxil được phê chuẩn cho trẻ >12 tuổi.[3] Peginterferon alfa 2a được phê chuẩn cho trẻ >5 tuổi bị viêm gan C và có thể được cân nhắc cho việc sử dụng ngoài hướng dẫn nếu cần cho viêm gan B mạn tính.[3] Thời gian điều trị khuyến cáo bằng interferon alfa 2b là 24 tuần.[3] Theo hướng dẫn của AASLD, thời gian điều trị đã được nghiên cứu cho thuốc kháng vi-rút đường uống là 1 đến 4 năm; có thể sử dụng chuyển đảo huyết thanh HBeAg làm kết điểm điều trị cho thuốc kháng vi-rút đường uống, tiếp tục dùng thêm 12 tháng nữa (như ở người lớn).[3]
Cần theo dõi trẻ bị nhiễm HBV mạn tính cho đến khi trưởng thành.
Tổng quan về các chi tiết điều trị
Tham khảo cơ sở dữ liệu dược địa phương của quý vị để biết thông tin toàn diện về thuốc, bao gồm các chống chỉ định, tương tác giữa các loại thuốc, và liều dùng thay thế.
| Cấp tính (tóm tắt) | ||
| Nhiễm HBV cấp | ||
| 1 | Chăm sóc hỗ trợ | |
|
Bổ sung | Điều trị kháng vi-rút ± ghép gan |
| Tiếp diễn (tóm tắt) | ||
| Nhiễm HBV mạn tính: người lớn không mang thai, không có tình trạng đồng nhiễm hay bệnh đồng mắc | ||
| 1 | Điều trị kháng vi-rút hoặc peginterferon | |
| Nhiễm HBV mạn tính: người lớn không mang thai bị xơ gan | ||
|
1 | Điều trị kháng vi-rút hoặc peginterferon Liệu pháp |
|
1 | Kháng vi-rút |
| Bổ sung | Đánh giá ghép gan | |
| Nhiễm HBV mạn tính: người lớn không mang thai bị đồng nhiễm HIV | ||
| 1 | Liệu pháp kháng vi-rút kết hợp | |
| Nhiễm HBV mạn tính: người lớn không mang thai bị đồng nhiễm viêm gan D | ||
| 1 | Liệu pháp interferon | |
| Nhiễm HBV mạn tính: người lớn mang thai hoặc đang cho con bú | ||
| 1 | Đơn trị liệu kháng vi-rút | |
| thêm | Biện pháp dự phòng miễn dịch sơ sinh | |
| Nhiễm HBV mạn tính: trẻ em | ||
| 1 | Chăm sóc hỗ trợ | |
|
bổ sung | Interferon hoặc đơn trị liệu kháng vi-rút |
Các lựa chọn điều trị
| Cấp tính | ||
| Nhiễm HBV cấp | ||
| 1 | Chăm sóc hỗ trợ | |
| » Bệnh nhân nhiễm HBV cấp thường chỉ cần điều trị hỗ trợ. » Hơn 95% những người nhiễm cấp sẽ có chuyển đảo huyết thanh với xuất hiện anti-HBs mà cần không điều trị.[31] [83] |
||
|
Bổ sung | Điều trị kháng vi-rút ± ghép gan |
| Các lựa chọn sơ cấp » lamivudine: 100 mg đường uống mỗi ngày một lần HOẶC » entecavir: 0,5 mg đường uống một lần mỗi ngày HOẶC » tenofovir disoproxil: 300 mg uống mỗi ngày một lần » Bệnh nhân tiến triển viêm gan tối cấp hoặc suy gan do HBV cấp có thể được điều trị bằng chất tương tự nucleoside/nucleotide, đồng thời họ cần được đánh giá khả năng ghép gan do nguy cơ tử vong cao liên quan đến suy gan mà không ghép gan.[85] |
||
| Tiếp diễn | ||
| Nhiễm HBV mạn tính: người lớn không mang thai, không có tình trạng đồng nhiễm hay bệnh đồng mắc | ||
| 1 | Điều trị kháng vi-rút hoặc peginterferon | |
| điều trị kháng vi-rút hoặc peginterferon Các lựa chọn sơ cấp » entecavir: 0,5 mg đường uống một lần mỗi ngày trong 12 tháng, liên tục trong 6 tháng sau chuyển đảo huyết thanh HBeAg ở người có HBeAg dương tính, hoặc cho đến khi thải trừ hết HBsAg ở người có HBeAg âm tính HOẶC » tenofovir disoproxil: 300 mg đường uống một lần mỗi ngày trong điều trị kéo dài, liên tục trong 12 tháng sau chuyển đảo huyết thanh HBeAg ở người HBeAg dương tính, hoặc cho đến khi thải trừ hết HBsAg ở người có HBeAg âm tính HOẶC » peginterferon alfa 2a: 180 microgram tiêm dưới da mỗi tuần một lần trong 48 tuần » Hướng dẫn của Hướng dẫn của Hiệp hội Nghiên cứu Bệnh Gan Hoa Kỳ (AASLD) khuyến cáo điều trị kháng vi-rút cho người lớn nhiễm HBV mạn tính giai đoạn hoạt động miễn dịch, được xác định là những người có HBeAg dương tính, với tải lượng HBV DNA >20.000 đơn vị quốc tế (IU)/mL và alanine aminotransferase (ALT) lớn hơn gấp đôi giới hạn trên của mức bình thường (ULN) hoặc bệnh mô học đáng kể; hoặc HBeAg âm tính, với HBV DNA >2000 IU/ mL, và ALT lớn hơn gấp đôi ULN hoặc bệnh mô học đáng kể.[3] Mục tiêu cuối cùng của việc điều trị là cải thiện rối loạn chức năng gan và xuất hiện trạng thái không có bệnh, được đánh dấu bằng chuyển đảo huyết thanh từ HBsAg dương tính thành HBsAg âm tính và sản sinh kháng thể HBs. Việc điều trị đôi khi có thể dẫn đến mất HBeAg và chuyển đảo huyết thanh HBeAg thành anti-HBe ở bệnh nhân HBeAg dương tính. Tuy nhiên, việc loại bỏ hoàn toàn HBV là hiếm gặp với các phương pháp điều trị hiện nay, vì vậy mục tiêu điều trị chính ở hầu hết bệnh nhân bị nhiễm HBV mạn tính là ức chế HBV DNA huyết thanh ở mức không phát hiện được lâu dài và bền vững. » Có thể cân nhắc peginterferon cho bệnh nhân HBeAg dương tính, bệnh gan bù hoàn toàn, đặc biệt với HBV kiểu gen A, ALT cao, và HBV DNA huyết thanh thấp,[8] [93] [94] [95] vì nó làm tăng tỷ lệ đáp ứng bền vững khi không điều trị. Ưu điểm bao gồm thời gian điều trị ngắn, đáp ứng bền vững, và không có tình trạng kháng thuốc, mặc dù chúng có các tác dụng phụ khó chịu và đòi hỏi dùng thuốc không qua đường uống và theo dõi thường xuyên. » Lựa chọn điều trị khuyến cáo cho liệu pháp ban đầu là peginterferon, hoặc chất tương tự nucleoside/ nucleotide mạnh với hàng rào kháng thuốc cao (tức là entecavir hoặc tenofovir disoproxil ).[3] [31] Ưu tiên peginterferon so với dạng không pegylated vì tính đơn giản.[3] » Bệnh nhân đã khẳng định bùng phát vi-rút có thể’ được chuyể’n sang điều trị kháng vi-rút khác có hàng rào kháng thuốc cao, hoặc có thể’ thêm điều trị kháng vi-rút thứ hai với xét nghiệm bổ sung kháng thuốc; hiện không có đủ bằng chứng để’ khuyến cáo phương pháp nào tốt hơn phương pháp nào.[3] |
||
| Nhiễm HBV mạn tính: người lớn không mang thai bị xơ gan | ||
|
1 | Điều trị kháng vi-rút hoặc peginterferon Liệu pháp |
| Các lựa chọn sơ cấp » entecavir: 0,5 mg đường uống một lần mỗi ngày HOẶC » tenofovir disoproxil: 300 mg uống mỗi ngày một lần Các lựa chọn thứ cấp » peginterferon alfa 2a: 180 microgram tiêm dưới da mỗi tuần một lần » Hướng dẫn của Hiệp hội Nghiên cứu Bệnh Gan Hoa Kỳ (AASLD) khuyến cáo bệnh nhân bị xơ gan còn bù về mặt lâm sàng và HBV DNA <2000 IU/ mL cần được điều trị kháng vi-rút bất kể alanine aminotransferase (ALT) để giảm nguy cơ mất bù; bệnh nhân bị xơ gan còn bù và mức HBV DNA >2.000 U/mL được điều trị theo khuyến cáo cho viêm gan B mạn tính giai đoạn hoạt động miễn dịch có HBeAg dương tính và âm tính.[3] » Lựa chọn điều trị tốt nhất là đơn trị liệu ở dạng entecavir hoặc tenofovir disoproxil. Điều này sẽ làm giảm nguy cơ kháng thuốc và cũng ức chế vi-rút nhanh trước khi ghép gan ở bệnh nhân mất bù.[3] » Chỉ có thể cân nhắc sử dụng peginterferon alfa cho bệnh nhân chọn lọc mắc xơ gan còn bù nhưng không bị tăng áp lực tĩnh mạch cửa.[3] [31] [104] Hiện không có bằng chứng về thời gian điều trị tối ưu cho xơ gan còn bù; nếu dừng điều trị, cần theo dõi bệnh nhân chặt chẽ.[3] |
||
|
1 | Kháng vi-rút |
| Các lựa chọn sơ cấp » entecavir: 1 mg đường uống mỗi ngày một lần HOẶC » tenofovir disoproxil: 300 mg uống mỗi ngày một lần » Khuyến cáo tăng liều entecavir cho điều trị.[31] Tenofovir disoproxil là phương án điều trị thay thế cho bệnh nhân bị xơ gan mất bù.[31] Dữ liệu cho thấy cả hai thuốc này đều an toàn và hiệu quả,[31] [109] [110] [111] mặc dù tình trạng nhiễm axit lactic xảy ra khi sử dụng lâu dài chất tương tự nucleoside như entecavir.[31] [112] |
||
| Bổ sung | Đánh giá ghép gan | |
| Ở bệnh nhân bị HBV mạn tính hoặc xơ gan mất bù, họ cần được giới thiệu tới trung tâm ghép gan | ||
| Nhiễm HBV mạn tính: người lớn không mang thai bị đồng nhiễm HIV | ||
| 1 | Liệu pháp kháng vi-rút kết hợp | |
| Các lựa chọn sơ cấp » tenofovir disoproxil: 300 mg uống mỗi ngày một lần -và- » emtricitabine: 200 mg qua đường uống mỗi ngày một lần » Hướng dẫn của Hoa Kỳ khuyến cáo bệnh nhân đồng nhiễm HIV và HBV nên điều trị kháng retrovirus (ART) bao gồm các thuốc có tác dụng kháng cả hai loại vi-rút bất kể số lượng tế bào CD4 hay nhu cầu cần điều trị HBV. Phác đồ ưu tiên là tenofovir disoproxil và emtricitabine. Hầu hết bệnh nhân nhận ART cần được điều trị HBV suốt đời. Các lựa chọn bị hạn chế nếu bệnh nhân từ chối ART; không nên sử dụng thuốc điều trị HBV có tác dụng trực tiếp nếu không dùng phác đồ ART ức chế đầy đủ do khả năng phát triển kháng ART của HIV.[114] |
||
| Nhiễm HBV mạn tính: người lớn không mang thai bị đồng nhiễm viêm gan D | ||
| 1 | Liệu pháp interferon | |
| Các lựa chọn sơ cấp » peginterferon alfa 2a: tham khảo ý kiến chuyên gia để’ có hướng dẫn về liều dùng » Interferon hiện là phương pháp điều trị chính.[3] Cần điều trị lâu dài; tuy nhiên, cần có thêm nghiên cứu để’ xác định thời gian điều trị ưu tiên.[31] [115] [116] Một nghiên cứu cho thấy liều cao interferon alfa có đáp ứng về vi-rút học, mô học và sinh hóa cao hơn so với interferon alfa liều thấp.[117] Hầu hết bệnh nhân tái phát sau khi ngừng interferon alfa liều cao nhưng sẽ duy trì cải thiện mô học gan sau 10 năm.[118] Trước đây, peginterferon alfa 2b đã được phê chuẩn cho đồng nhiễm viêm gan D, nhưng đã bị dừng ở một số nước vì lý do thương mại (không phải vì lý do an toàn). Chất tương tự nucleoside hoặc nucleotide có kết quả gây thất vọng. |
||
| Nhiễm HBV mạn tính: người lớn mang thai hoặc đang cho con bú | ||
| 1 | Đơn trị liệu kháng vi-rút | |
| Các lựa chọn sơ cấp » tenofovir disoproxil: 300 mg uống mỗi ngày một lầnHOẶC » lamivudine: 100 mg đường uống mỗi ngày một lần » Cần cân nhắc điều trị kháng vi-rút nếu tải lượng vi-rút >200.000 IU/mL. Dữ liệu cho thấy tenofovir disoproxil là thuốc được lựa chọn cho bệnh nhân mang thai nhiễm HBV nhờ vào dữ liệu an toàn tuyệt vời và hàng rào kháng thuốc cao.[31] [119] Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) phân loại thuốc này thuộc nhóm B cho phụ nữ mang thai và thường được bắt đầu dùng trong ba tháng cuối thai kỳ. Trong một thử nghiệm đối chứng ngẫu nhiên và tổng quan hệ thống, tenofovir disoproxil được cho dùng trong ba tháng cuối thai kỳ đã được chứng minh là làm giảm tỷ lệ lây truyền từ mẹ sang con khi được cho dùng cùng với vắc-xin viêm gan B và globulin miễn dịch viêm gan B ở trẻ sơ sinh.[120] [121] » Có thể dùng lamivudine trong ba tháng cuối thai kỳ và thuốc này cho thấy tính an toàn và làm giảm việc lây truyền HBV chu sinh và trong tử cung khi được cho dùng cùng với vắc-xin viêm gan B và globulin miễn dịch viêm gan B ở trẻ sơ sinh.[122] [123] [124] [125] [126] Lamivudine là thuốc nhóm C theo FDA. Phụ nữ mang thai khi đang dùng peginterferon hoặc entecavir cần được chuyển sang phác đồ an toàn hơn. » Thời gian điều trị để phòng tránh lây truyền chu sinh không được xác định rõ và có thể tiếp tục trong 3 tháng sau sinh hay dừng lúc sinh; việc dừng lúc sinh có thể có lợi vì nó không ảnh hưởng đến việc cho con bú.[31] » Theo đánh giá của 10 nghiên cứu, cho con bú sau khi dùng biện pháp dự phòng miễn dịch sơ sinh kịp thời không làm tăng tỷ lệ lây truyền so với việc không cho con bú.[127] Tính an toàn của việc dùng thuốc kháng vi-rút trong khi cho con bú chưa được nghiên cứu kỹ và mặc dù không có chống chỉ định, các nhà sản xuất thuốc có thể khuyến cáo tránh cho con bú.[3] |
||
| thêm | Biện pháp dự phòng miễn dịch sơ sinh | |
| Các lựa chọn sơ cấp » vắc-xin viêm gan B: tham khảo quy trình tiêm chủng tại địa phương để biết lịch tiêm -và- » globulin miễn dịch viêm gan B: 0,5 mL tiêm bắp liều duy nhất » Tại Hoa Kỳ, trẻ có mẹ dương tính với HBsAg cần được tiêm vắc-xin viêm gan B đơn giá và globulin miễn dịch viêm gan B (HBIG) trong vòng 12 giờ sau sinh. Nếu chưa rõ tình trạng HBsAg của mẹ, trẻ cần được tiêm vắc-xin viêm gan B trong vòng 12 giờ sau sinh, và trẻ nhẹ hơn 2000 g cũng cần được tiêm HBIG. Đối với trẻ nặng hơn 2000 g, cần xác định tình trạng HBsAg của người mẹ và nếu dương tính, cần tiêm HBIG cho trẻ ngay khi có thể’ trong vòng 7 ngày. Trẻ nhỏ có mẹ dương tính với HBsAg cần được xét nghiệm HBsAg và anti-HBs lúc 9 đến 12 tháng tuổi, hoặc 1 đến 2 tháng sau khi tiêm xong các mũi vắc-xin viêm gan B. Trẻ nhỏ có mẹ âm tính với HBsAg cần được tiêm một mũi vắc-xin viêm gan B trong vòng 24 giờ sau khi sinh (nếu sức khỏe ổn định và cân nặng lúc sinh hơn 2000 g), hoặc một mũi lúc được 1 tháng tuổi sinh lý hay xuất viện nếu cân nặng lúc sinh dưới 2000 g.[50] |
||
| Nhiễm HBV mạn tính: trẻ em | ||
| 1 | Chăm sóc hỗ trợ | |
| » Nhìn chung, viêm gan B mạn tính xảy ra mà không có triệu chứng ở hầu hết trẻ em, và phương pháp điều trị bảo tồn là có thể chấp nhận do dữ liệu lâm sàng và lựa chọn điều trị hạn chế. Không có chỉ định điều trị trong giai đoạn trạng thái mang bệnh không hoạt động, và chưa xác định được lợi ích của việc điều trị cho trẻ em ở giai đoạn dung nạp miễn dịch do nguy cơ phát triển kháng thuốc cao.[128] | ||
|
bổ sung | Interferon hoặc đơn trị liệu kháng vi-rút |
| Các lựa chọn sơ cấp » entecavir: trẻ em >2 tuổi: tham khảo ý kiến chuyên gia để có hướng dẫn về liều dùng HOẶC » tenofovir disoproxil: trẻ em >12 tuổi: tham khảo ý kiến chuyên gia để có hướng dẫn về liều dùng HOẶC » interferon alfa 2b: trẻ em >1 tuổi: tham khảo ý kiến chuyên gia để có hướng dẫn về liều dùng HOẶC » peginterferon alfa 2a: trẻ em >5 tuổi: tham khảo ý kiến chuyên gia để có hướng dẫn về liều dùng Các lựa chọn thứ cấp » lamivudine: trẻ em >2 tuổi: tham khảo ý kiến chuyên gia để có hướng dẫn về liều dùng » Việc điều trị cần do bác sĩ có kinh nghiệm về điều trị cho trẻ em nhiễm HBV tiến hành.» Trẻ có alanine aminotransferase (ALT) >1,3 lần giới hạn trên của mức bình thường cần được cân nhắc điều trị nếu ALT vẫn tăng cao trong hơn 6 tháng cùng với việc tăng HBV DNA.[3] Tuy nhiên, nhìn chung tải lượng HBV DNA rất cao ở trẻ em; nếu có <10A4 IU/mL, có thể trì hoãn điều trị cho đến khi loại trừ nguyên nhân khác gây ra bệnh gan và chuyển đảo huyết thanh HBeAg nguyên phát.[3] Đối với trẻ ở giai đoạn hoạt động miễn dịch hay tái hoạt, sinh thiết gan có thể giúp hướng dẫn đưa ra quyết định điều trị và tiền sử gia đình về bệnh gan, đặc biệt là ung thư biểu mô tế bào gan có thể dẫn đến việc điều trị sớm trong một số ca bệnh.[128] » Nếu cần điều trị, hướng dẫn của Hiệp hội Nghiên cứu Bệnh Gan Hoa Kỳ (AASLD) cho biết interferon alfa 2b được phê chuẩn cho trẻ > 1 tuổi, lamivudine và entecavir được phê chuẩn cho trẻ >2 tuổi, (mặc dù entecavir có liên quan đến nguy cơ kháng thuốc thấp hơn), và tenofovir disoproxil được phê chuẩn cho trẻ >12 tuổi.[3] Peginterferon alfa 2a được phê chuẩn cho trẻ >5 tuổi bị viêm gan C và có thể được cân nhắc cho việc sử dụng ngoài hướng dẫn nếu cần cho viêm gan B mạn tính.[3] Thời gian điều trị khuyến cáo bằng interferon alfa 2b là 24 tuần.[3] Theo hướng dẫn của AASLD, thời gian điều trị đã được nghiên cứu cho thuốc kháng vi-rút đường uống là 1 đến 4 năm; có thể sử dụng chuyển đảo huyết thanh HBeAg làm kết điểm điều trị cho thuốc kháng vi-rút đường uống, tiếp tục dùng thêm 12 tháng nữa (như ở người lớn).[3] |
||
Giai đoạn đầu
Tenofovir alafenamide
Cơ quan Quản lý Thực phẩm và Dược phẩm (FDA) Hoa Kỳ đã phê duyệt tenofovir alafenamide, một loại tiền chất mới của tenofovir, để điều trị cho người lớn bị nhiễm HBV mạn tính bị bệnh gan còn bù. Thuốc này dẫn đến nồng độ nội bào cao hơn và nồng độ huyết tương thấp hơn của tenofovir chuyển hóa có hoạt tính so với tiền chất thế hệ thứ nhất (tenofovir disoproxil fumarate); do đó, cần liều thấp hơn. Tenofovir alafenamide đã được chứng minh là có hiệu quả tương tự như tenofovir disoproxil fumarate, nhưng cải thiện tác dụng trên xương và thận.[129] [130] Thuốc được Ủy ban Châu Âu phê chuẩn vào tháng 1 năm 2017,[131] và được hướng dẫn của Hiệp hội Nghiên cứu Gan Châu Âu (EASL) khuyến cáo sử dụng.[31] Hiệp hội Nghiên cứu Bệnh Gan Hoa Kỳ (AASLD) vẫn chưa đưa tenofovir alafenamide vào hướng dẫn hiện tại của họ.
Valtorcitabine
Chất tương tự L-nucleoside có khả năng ức chế tốt việc tổng hợp ADN phụ thuộc ARN. Chất này cho thấy khả năng ức chế mạnh HBV DNA ở bệnh nhân HBeAg dương tính. Sau 4 tuần điều trị, liệu pháp valtorcitabine cho thấy giảm 99,9% tải lượng vi-rút và có hồ sơ an toàn tương đương với giả dược trong một nghiên cứu.[132] Việc kết hợp valtorcitabine và telbivudine đang được nghiên cứu dựa theo dữ liệu mô hình động vật về tác dụng đồng vận có thể có trong việc ức chế sự nhân lên của HBV.[132]
Liệu pháp gen
Liệu pháp gen sử dụng phân tử antisense, ribozyme, và siRNA đã được xây dựng. Các phương pháp này được thiết kế để điều chỉnh giảm và ức chế tổng hợp HBV RNA bên trong tế bào gan. Các liệu pháp này đầy hứa hẹn trong các mô hình trong ống nghiệm và động vật nhưng chưa được thử nghiệm ở người.[133] Vấn đề tiềm ẩn với các thuốc này là phương thức cung cấp đến tế bào gan và sau đó đến vị trí nhân lên của HBV.[132] Các mối quan ngại khác liên quan đến tính an toàn: hoạt hóa đáp ứng miễn dịch không đặc hiệu, vấn đề về liệu pháp dựa trên gen, và khả năng bùng phát viêm gan B với kích hoạt miễn dịch. Một thử nghiệm lâm sàng giai đoạn I đang được tiến hành.
CẬP NHẬT ĐIỀU TRỊ VIÊM GAN B MẠN- WHO 2024
Bs Huỳnh Văn Trung – Phòng khám tiêu hoá gan mật – Trung tâm nội soi và phẫu thuật nội soi tiêu hoá- Bệnh viện Tâm Anh TPHCM
NHỮNG KHUYẾN CÁO MỚI ĐÁNG CHÚ Ý:
- MỞ RỘNG CHỈ ĐỊNH ĐIỀU TRỊ Ở BỆNH NHÂN VIÊM GAN B MẠN: khuyến cáo mới cập nhật mới 4 chỉ định điều trị ở bệnh nhân >=12 tuổi với viêm gan B mạn. Trước đây chỉ có khoảng 8-15% bệnh nhân HBsAg (+) cần điều trị, nay với cập nhật mới góp phần mở rộng ít nhất 50% bệnh nhân HBsAg (+) cần điều trị: BAO GỒM
- Tất cả bệnh nhân HBsAg (+) với xơ hoá gan đáng kể hoặc xơ gan (>=F2) dựa trên test đánh giá xơ hoá gan không xâm lấn như (APRI score >0.5 hoặc đo đàn hồi thoáng qua >7KPa) BẤT CHẤP nồng độ HBV DNA hoặc ALT
- Tất cả bệnh nhân HBsAg (+) với HBV DNA >2000 IU/ml VÀ ALT >ULN (giới hạn trên bình thường) (khuyến cáo trước đây HBV DNA >20.000 IU/ml)
- iii. Tất cả bệnh nhân HBsAg (+) với (1) đồng nhiễm HIV, HDV và HCV; (2) tiền căn gia đình ung thư gan hoặc xơ gan; (3) tình trạng suy giảm miễn dịch như dùng corticosteroid kéo dài, ghép tạng; (4) đồng mắc đái tháo đường hoặc bệnh gan nhiễm mỡ liên quan rối loạn chuyển hoá; (5) bất thường ngoài gan do HBV như viêm cầu thận hoặc viêm mạch máu BẤT CHẤP nồng độ HBV DNA và ALT
- Ở những cơ sở y tế không đánh giá được HBV DNA => tất cả bệnh nhân HBsAg(+) với ALT tăng dai dẵng (ALT >ULN x 2 lần liên tiếp trong thời gian 6-12 tháng) được chỉ định điều trị bất chấp APRI score
MỞ RỘNG CHỈ ĐỊNH PHÒNG NGỪA KHÁNG VIRUS Ở PHỤ NỮ MANG THAI
- Những cơ sở y tế thực hiện được xét nghiệm HBV DNA hoặc HBeAg => khuyến cáo kháng virus TDF phòng ngừa ở phụ nữ mang thai HBsAg (+) với HBV DNA >=200.000 IU/ml hoặc HBeAg (+) từ tam cá nguyện thứ 2 thai kỳ
- Cơ sở y tế không tiếp cận được xét nghiệm HBV DNA hoặc HBeAg =>khuyến cáo mở rộng chỉ định phòng ngừa kháng virus cho tất cả phụ nữ mang thai HBsAg (+) từ tam cá nguyệt thứ hai cho đến ít nhất sau sinh hoặc sau khi phòng ngừa đầy đủ globulin miễn dịch và vacxin viêm gan B
THÊM LIỆU PHÁP THAY THẾ TRONG ĐIỀU TRỊ VIÊM GAN B MẠN
- Tenofovir disoproxil fumarate (TDF) hoặc entecavir (ETV) vẫn là lựa chọn ưu tiên ở bệnh nhân viêm gan B mạn có chỉ định điều trị
- Tenofovir + lamivudine hoặc tenofovir + emtricitabine là liệu pháp thay thế như là một phần trong phác đồ điều trị ARV (khi không có TDF đơn trị liệu)
- Tenofovir alafenamide fumarate (TAF) là lựa chọn điều trị riêng ở bệnh nhân hiện có hoặc có nguy cơ suy thận hoặc loãng xương
Liên lạc theo dõi
Khuyến nghị
Giám sát
Ở bệnh nhân không đáp ứng tiêu chuẩn điều trị tại địa phương bằng liệu pháp kháng vi-rút, mục tiêu theo dõi là xác định sự thay đổi trong tình trạng lâm sàng cho thấy việc tiến triển thành trạng thái bệnh đòi hỏi phải được điều trị. Mục tiêu theo dõi ở những người đã được dùng liệu pháp kháng vi-rút là đánh giá đáp ứng điều trị, tác dụng phụ, và tiến triển hay tái hoạt bệnh.[3] [31] [39] [144] Các khuyến cáo sau đây chủ yếu dựa trên hướng dẫn của Hiệp hội Nghiên cứu Bệnh Gan Hoa Kỳ (AASLD);[3] [144] hướng dẫn địa phương có thể khác.
Bệnh nhân có HBeAg dương tính không được cân nhắc điều trị
- Alanine aminotransferase (ALT) được kiểm tra 3 đến 6 tháng một lần, và việc mất HBeAg và anti-HBe được kiểm tra 6 đến 12 tháng một lần. ALT và HBV DNA được đo thường xuyên hơn (1 đến 3 tháng một lần) nếu ALT tăng cao. Nếu bệnh nhân vẫn có HBeAg dương tính với HBV DNA>20.000 đơn vị quốc tế (IU)/mL và >40 tuổi, hoặc vẫn có HBeAg dương tính với HBV DNA>20.000 IU/mL có ALT tăng cao trung gian (dưới ngưỡng gấp đôi so với giới hạn trên của mức bình thường [ULN]) sau khoảng thời gian 3 đến 6 tháng, hoặc có tiền sử gia đình về ung thư biểu mô tế bào gan (HCC), thì có thể cân nhắc sinh thiết gan. Bắt đầu điều trị nếu sinh thiết gan cho thấy tình trạng viêm từ vừa đến nặng và/hoặc xơ hóa đáng kể.
Bệnh nhân có HBeAg âm tính không được cân nhắc điều trị
- ALT được xét nghiệm 3 tháng một lần trong năm đầu tiên và sau đó 6 đến 12 tháng một lần nếu ổn định.[144] Tuy nhiên, ở bệnh nhân có HBeAg âm tính với HBV DNA >2000 IU/mL (nhưng <20.000 IU/mL) và ALT lớn hơn mức ULN nhưng dưới ngưỡng gấp đôi ULN, thì cân nhắc sinh thiết gan và bắt đầu điều trị nếu sinh thiết cho thấy tình trạng viêm từ vừa đến nặng và/hoặc xơ hóa.[144]
Bệnh nhân đang được điều trị với liệu pháp interferon hoặc peginterferon
- Bệnh nhân cần kiểm tra công thức máu và xét nghiệm chức năng gan mỗi 4 tuần, và TSH và HBV DNA mỗi 12 tuần, và nếu ban đầu có HBeAg dương tính, cần đánh giá HBeAg/anti-HBe mỗi 24 tuần trong quá trình điều trị. Sau khi dừng điều trị, cần kiểm tra công thức máu, xét nghiệm chức năng gan, TSH, HBV DNA, và nếu ban đầu HBeAg dương tính, HBeAg/anti-HBe mỗi 12 tuần trong 24 tuần đầu tiên.
- Hồ sơ tác dụng phụ của interferon bao gồm biểu hiện giống cúm, sốt, rét run, đau đầu, tình trạng khó chịu, đau cơ, mệt mỏi, biếng ăn, giảm cân, và rụng tóc nhẹ.[3] [144] Thuốc này cũng có tác dụng ức chế tủy xương; tuy nhiên, thường không thấy giảm bạch cầu trung tính (<1000/mmA3) hay giảm tiểu cầu (<50.000/mmA3) đáng kể.[144]
- Tác dụng phụ khó chịu nhất của liệu pháp IFN bao gồm rối loạn cảm xúc bao gồm cáu kỉnh, lo âu, trầm cảm và thậm chí xu hướng muốn tự tử.[3] [144]
Bệnh nhân dùng chất tương tự nucleoside/nucleotide:
- Lamivudine thường được dung nạp tốt mặc dù việc tăng nhẹ ALT (gấp 2 đến 3 lần) đã được báo cáo.[144] Telbivudine cũng thường được dung nạp tốt; tuy nhiên, các ca bệnh về cơ và bệnh lý thần kinh ngoại biên đã được báo cáo.[145] [146]
- Tenofovir đã được báo cáo là gây ra hội chứng Fanconi và suy thận, cũng như chứng nhuyễn xương và giảm mật độ xương. Khuyến cáo theo dõi creatinine và phốt pho huyết thanh.[3]
- Xét nghiệm chức năng gan được theo dõi mỗi 12 tuần và HBV DNA mỗi 12 đến 24 tuần, và nếu ban đầu có HBeAg dương tính, HBeAg/anti-HBe mỗi 24 tuần trong quá trình điều trị. Nhìn chung, khuyến cáo bệnh nhân theo dõi thường xuyên ngay cả sau khi chuyển đảo huyết thanh vì tái hoạt HBV sau khi chuyển đảo huyết thanh được xác định xảy ra ở khoảng 20% bệnh nhân. Phải xét nghiệm creatinine huyết thanh mỗi 12 tuần đối với bệnh nhân dùng tenofovir. Cần theo dõi nồng độ axit lactic ở những người dùng entecavir hoặc tenofovir disoproxil nếu có mối quan ngại về mặt lâm sàng.[3]
Sàng lọc HCC định kỳ bằng siêu âm và alpha-fetoprotein (AFP) nếu muốn, 6 tháng một lần đối với bệnh nhân xơ gan và người mang HBV có nguy cơ cao (nam giới châu Á >40 tuổi, phụ nữ châu Á >50 tuổi, người có tiền sử gia đình
mắc HCC, người châu Phi >20 tuổi và người mang HBV >40 tuổi tăng ALT liên tục và/hoặc HBV DNA>2000 IU/ mL).[63] [64]
Hướng dẫn dành cho bệnh nhân
Người có HBsAg dương tính cần sử dụng biện pháp bảo vệ khi quan hệ tình dục nếu bạn tình của họ chưa được tiêm vắc-xin hay miễn dịch tự nhiên, không dùng chung bàn chải đánh răng hay dao cạo râu, và cần che các vết cắt hở và vết xước, dọn sạch vết máu vấy đổ bằng thuốc tẩy hay chất tẩy rửa, và không hiến máu, hiến tạng hay tinh trùng.[77]
Bệnh nhân cần tránh uống nhiều rượu (>20g/ngày đối với phụ nữ; >30g/ngày đối với nam giới).[147]
Bạn tình và tất cả những người tiếp xúc trong hộ gia đình của người có HBsAg dương tính cần được tiêm vắc-xin phòng HBV nếu họ có kết quả xét nghiệm âm tính đối với các dấu ấn huyết thanh HBV.
Các biến chứng
| Các biến chứng | Khung thời gian | Khả năng |
| Suy gan tối cấp | ngắn hạn | thấp |
| Người ta cho rằng đáp ứng miễn dịch tăng cao đối với HBV gây nên ly giải qua trung gian miễn dịch ồ ạt các tế bào gan nhiễm bệnh là nguyên nhân gây ra viêm gan tối cấp liên quan đến nhiễm viêm gan B cấp. Điều này xảy ra ở <1% (khoảng 0,1% đến 0,5%) số ca HBV cấp. Đồng nhiễm vi-rút viêm gan C hoặc D làm tăng nguy cơ phát triển viêm gan tối cấp. Cần chuyển tới nơi ghép gan để tránh tàn tật và tử vong. | ||
| Xơ gan | dài hạn | trung bình |
| Xơ gan xảy ra ở khoảng 20% bệnh nhân bị HBV mạn tính và được cho là do sự tấn công miễn dịch liên tục tế bào nhiễm bệnh trong gan, dẫn đến phát triển xơ hóa và các nốt tái tạo. Các yếu tố nguy cơ liên quan đến việc tiến triển thành xơ gan bao gồm tình trạng đồng nhiễm (viêm gan C hoặc D, và/hoặc HIV), tuổi cao, tải lượng HBV DNA cao, và thói quen uống rượu. Có thể bắt đầu điều trị ở hầu hết bệnh nhân bị HBV mạn tính và xơ gan. | ||
| Ung thư biểu mô tế bào gan | dài hạn | trung bình |
| Hiện nay, tỷ lệ mắc mới ung thư tế bào gan (HCC) liên quan đến HBV đang gia tăng và chiếm 50% tổng số ca HCC trên toàn cầu. Cần bắt đầu sàng lọc HCC theo gợi ý của khuyến cáo trong hướng dẫn. Người ta cho rằng HCC liên quan đến viêm gan B là hệ quả của viêm mạn tính và tái tạo tế bào gan. Xơ gan dường như là yếu tố nguy cơ lớn nhất gây nên HCC mặc dù 30% đến 50% số ca HCC liên quan đến HBV không có xơ gan. Nam giới, tuổi cao, đồng nhiễm viêm gan C, đột biến vùng điều hòa nhân, tiền sử gia đình mắc HCC, có HBeAg, và tải lượng HBV DNA cao là các yếu tố nguy cơ phát triển HCC. Có thể cân nhắc ghép gan ở giai đoạn đầu với HCC nhỏ và không có bằng chứng về di căn. | ||
| Viêm cầu thận liên quan đến viêm gan B | dài hạn | thấp |
| Viêm cầu thận liên quan đến HBV không phải là biến chứng thường gặp của nhiễm HBV và có nhiều tranh cãi về nguyên nhân gây ra viêm cầu thận ở bệnh nhân nhiễm HBV. Liệu pháp tối ưu cũng không được xác định rõ. Một tổng quan hệ thống và phân tích gộp đánh giá tính an toàn và hiệu quả của interferon và lamivudine ở bệnh nhân nhiễm HBV bị viêm cầu thận đã báo cáo việc thuyên giảm hội chứng viêm cầu thận với việc thanh thải sự nhân lên của HBV, cho thấy vai trò thông thường của HBV trong việc phát triển viêm cầu thận. | ||
Tiên lượng
Bệnh nhân HBeAg dương tính nhiễm HBV mạn tính
Kết điểm điều trị được xác định rõ ở nhóm bệnh nhân này dựa trên khả năng dự đoán và thời gian chuyển đảo huyết thanh sang anti-HBe. Khi dừng điều trị sau khi đạt được chuyển đảo huyết thanh, ức chế vi-rút được duy trì ở 50% đến 90% bệnh nhân. Chuyển đảo huyết thanh có liên quan đến việc duy trì cải thiện kéo dài về mô học gan.[134] Tuy nhiên, biện pháp chữa khỏi có hiệu quả thực sự (mất HBsAg và anti-HBs) chỉ xảy ra ở tỷ lệ rất thấp bệnh nhân được điều trị (1% đến 5%).[16] [135]
Bệnh nhân nhiễm HBV mạn tính HBeAg âm tính
Kết điểm điều trị cho nhóm bệnh nhân này được xác định kém. Do đó, thời gian điều trị kéo dài và có thể cần điều trị suốt đời. Ngoài ra, tái phát thường xảy ra ở nhóm bệnh nhân này ngay cả khi ức chế vi-rút hoàn toàn sau khi dừng thuốc (không phát hiện được HBV DNA) trong >1 năm.[3]
Hướng dẫn
Hướng dẫn chẩn đoán
Châu Âu
2017 European Guideline for the screening, prevention and initial management of hepatitis B
& C infections in sexual health settings
Nhà xuất bản: International Union against Sexually Transmitted Infections
Xuất bản lần cuối: 2017
EASL clinical practice guidelines on the management of hepatitis B virus infection
Nhà xuất bản: European Association For The Study Of The Liver
Xuất bản lần cuối: 2017
Hepatitis B (chronic): diagnosis and management Nhà xuất bản: National Institute for Health and Care Excellence
Xuất bản lần cuối: 2017
Quốc tế
Guidelines for the prevention, care and treatment of persons with chronic hepatitis B infection
Nhà xuất bản: World Health Organization
Xuất bản lần cuối: 2015
Bắc Mỹ
Hepatitis B vaccination, screening, and linkage to care: best practice advice from the American College of Physicians and the Centers for Disease Control and Prevention
Nhà xuất bản: American College of Physicians and Centers for Disease Control and Prevention
Xuất bản lần cuối: 2017
AASLD guidelines for treatment of chronic hepatitis B Nhà xuất bản: American Association for the Study of Liver Disease
Xuất bản lần cuối: 2015
Sexually transmitted diseases treatment guidelines, 2015: viral hepatitis
Nhà xuất bản: Centers for Disease Control and Prevention
Xuất bản lần cuối: 2015
Châu Á
Asian-Pacific clinical practice guidelines on the management of hepatitis B: a 2015 update
Nhà xuất bản: Asian Pacific Association for the Study of the Liver
Xuất bản lần cuối: 2015
Hướng dẫn điều trị
Châu Âu
EASL clinical practice guidelines on the management of hepatitis B virus infection
Nhà xuất bản: European Association for the Study of the Liver
Xuất bản lần cuối: 2017
2017 European Guideline for the screening, prevention and initial management of hepatitis B
& C infections in sexual health settings
Nhà xuất bản: International Union against Sexually Transmitted Infection Xuất bản lần cuối: 2017
Hepatitis B (chronic): diagnosis and management Nhà xuất bản: National Institute for Health and Care Excellence
Xuất bản lần cuối: 2017
United Kingdom national guideline on the management of the viral hepatitides A, B and C
Adefovir dipivoxil and pegylated interferon alpha for the treatment of chronic hepatitis B: an
updated systematic review and economic evaluation Nhà xuất bản: Health Technology Assessment Programme
Xuất bản lần cuối: 2009
Telbivudine for the treatment of chronic hepatitis B Nhà xuất bản: National Institute for Health and Care Excellence
Xuất bản lần cuối: 2008
Entecavir for the treatment of chronic hepatitis B Nhà xuất bản: National Institute for Health and Care Excellence
Xuất bản lần cuối: 2008
Quốc tế
Global hepatitis report, 2017
Nhà xuất bản: World Health Organization
Xuất bản lần cuối: 2017
Guidelines for the prevention, care and treatment of persons with chronic hepatitis B infection
Nhà xuất bản: World Health Organization
Xuất bản lần cuối: 2015
Bắc Mỹ
Recommended immunization schedule for adults aged 19 years or older – United States, 2018
Nhà xuất bản: Centers for Disease Control and Prevention
Xuất bản lần cuối: 2018
Recommended immunization schedule for children and adolescents aged 18 years or younger – United States, 2018
Nhà xuất bản: Centers for Disease Control and Prevention
Xuất bản lần cuối: 2018
Prevention of hepatitis B virus infection in the United States: recommendations of the
Advisory Committee on Immunization Practices
Nhà xuất bản: Centers for Disease Control and Prevention
Xuất bản lần cuối: 2018
Hepatitis B vaccination, screening, and linkage to care: best practice advice from the
American College of Physicians and the Centers for Disease Control and Prevention
Nhà xuất bản: American College of Physicians and Centers for Disease Control Xuất bản lần cuối: 2017 and Prevention
Canadian immunization guide. Part 4 – active vaccines: hepatitis B vaccine
Nhà xuất bản: Public Health Agency of Canada
Xuất bản lần cuối: 2017
AASLD guidelines for treatment of chronic hepatitis B
Nhà xuất bản: American Association for the Study of Liver Diseases
Xuất bản lần cuối: 2015
Sexually transmitted diseases treatment guidelines, 2015: viral hepatitis
Nhà xuất bản: Centers for Disease Control and Prevention
Xuất bản lần cuối: 2015
Sexually transmitted diseases treatment guidelines, 2015: clinical prevention guidance
Nhà xuất bản: Centers for Disease Control and Prevention
Xuất bản lần cuối: 2015
Sexually transmitted diseases treatment guidelines, 2015: special populations
Nhà xuất bản: Centers for Disease Control and Prevention
Xuất bản lần cuối: 2015
CDC guidance for evaluating healthcare personnel for hepatitis B virus protection and for administering postexposure management
Nhà xuất bản: Centers for Disease Control and Prevention
Xuất bản lần cuối: 2013
Recommendations for identification and public health management of persons with chronic hepatitis B virus infection
Nhà xuất bản: National Center for HIV/AIDS, Viral Hepatitis, STD, and TB
Xuất bản lần cuối: 2008
Prevention
Viral hepatitis in pregnancy
Nhà xuất bản: American Congress of Obstetricians and Gynecologists
Xuất bản lần cuối: 2007
Serological testing for suspected viral hepatitis Nhà xuất bản: Alberta Clinical Practice Guidelines
Xuất bản lần cuối: 2006
A comprehensive immunization strategy to eliminate transmission of hepatitis B virus infection in the United States. Recommendations of the Advisory Committee on Immunization Practices (ACIP) part 2: immunization of adults
Nhà xuất bản: Centers for Disease Control and Prevention
Xuất bản lần cuối: 2006
A comprehensive immunization strategy to eliminate transmission of hepatitis B virus infection in the United States. Recommendations of the Advisory Committee on Immunization Practices (ACIP) part 1: immunization of infants, children, and adolescents
Nhà xuất bản: Centers for Disease Control and Prevention
Xuất bản lần cuối: 2005
Châu Á
Asian-Pacific clinical practice guidelines on the management of hepatitis B: a 2015 update
Nhà xuất bản: Asian Pacific Association for the Study of the Liver
Xuất bản lần cuối: 2015
Consensus recommendations on immunization
Nhà xuất bản: Indian Academy of Paediatrics
Châu Đại Dương
Management of hepatitis B in pregnancy
Nhà xuất bản: Royal Australian and New Zealand College of Obstetricians and
Xuất bản lần cuối: 2016 Gynaecologists
Nguồn trợ giúp trực tuyến
- BMJ Best Practice podcast: hepatitis B – how to approach diagnosis and management of chronic infection (external link)
- CDC: typical interpretation of serologic test results for hepatitis B virus infection. (external link)
Các bài báo chủ yếu
- Terrault NA, Bzowej NH, Chang KM, et al. AASLD guidelines for treatment of chronic hepatitis B. Hepatology. 2016 Jan;63(1):261-83. Toàn văn Tóm lược
- European Association for the Study of the Liver. EASL 2017 clinical practice guidelines on the management of hepatitis B virus infection. J Hepatol. 2017 Aug;67(2):370-98. Toàn văn Tóm lược
Ca lâm sàng
Ca 1
Bệnh nhân nữ 34 tuổi nhập cư từ Trung Quốc vào Mỹ thực hiên xét nghiệm để nhập học trường điều dưỡng. Tiền căn bệnh lý và dùng thuố’c chưa ghi nhận bất thường. Bệnh nhân hiện đang trong một mối quan hệ một vợ một chồng và không dùng chất cấm. Bệnh nhân tin rằng mình luôn bổ sung các mũi tiêm ngừa đầy đủ. Bệnh nhân mang kết quả xét nghiệm đến phòng khám như sau:
| HBsAg | Negative |
| Anti-HBs | Positive |
| Anti-HBc | Positive |
| HBeAg | Negative |
| Anti-HBe | Negative |
Điều nào sau đây giải thích phù hợp cho kết quả xét nghiệm trên?
- Nhiễm viêm gan B cấp tính
- Nhiễm viêm gan B mạn tính
- Nhiễm viêm gan B trong giai đoạn phục hồi
- Nhiễm viêm gan B đã khỏi
- Tiêm ngừa giúp chống lại nhiễm viêm gan B
Đáp án: D: Nhiễm viêm gan B đã khỏi
Bệnh nhân có kết quả xét nghiêm phù hợp với nhiễm viêm gan B đã khỏi. Những người có miễn dịch do nhiễm HBV tự nhiên thường có kết quả anti-HBs dương tính và HBsAg âm tính. Họ cũng có thể dương tính với IgG anti-HBc bởi vì kháng thể giúp chống lại trực tiếp kháng nguyên lõi của HBV. Vaccine HBV có chứa HbsAg giúp kích thích sinh anti-HBs và tạo miễn dịch cho vật chủ. Tuy nhiên, vaccine không chưa kháng nguyên lõi vì vậy không thể tạo kháng thể chống lại và bệnh nhân sẽ có anti-HBc âm tính (Lựa chọn E) Các marker huyết thanh cho HBV bao gồm
- HbsAg: là marker huyết thanh đầu tiên được xác định sau khi tiêm ngừa. Nó cũng xuất hiện trước khi khởi phát triệu chứng lâm sàng và tăng men gan. HbsAg vẫn còn xác định được trong suốt giai đoạn có triệu chứng của viêm gan siêu vi B cấp và gợi ý nhiễm trùng.
- Anti-HBs: xuất hiện trong huyết thanh sau khi tiềm người HBV hoặc đào thải HbsAg và xác định được trong suốt cuộc đời của phần lớn bệnh nhân. Nó giúp xác định tình trạng không nhiễm trùng hoặc miễn dịch. Tuy nhiên, có một khoảng thời gian nằm giữa lúc HbsAg biến mất và anti-HBs xuất hiện được gọi là giai đoạn cửa sổ
- HbcAg: là marker không được xác đinh trong huyết thanh vì thường được lớp áo HbsAg che dấu.
- Anti-HBc: IgM xuất hiện trong một giai đoạn ngắn sau khi xuất hiện HBsAg và có thể là marker duy nhất xuất hiện trong nhiễm HBV cấp trong giải đoạn cửa sổ. IgG vẫn còn được xác định trong giai đoạn hồi phục nhiễm HBV cấp hoặc giai đoạn tiến triển đến nhiễm mạn tính.
- HbeAg: Kháng nguyên này được xác đinh trong một thời gian ngắn sau khi HBsAg xuất huyết và cho thấy khả năng sao chép cảu virus. Marker này có liên quan đến HBV DNA. HbeAg biến mất nhanh sau khi men gan đạt đến đỉnh và trước khi HBsAg được đào thải. Sau đó là sự xuất hiện của anti-Hbe. Anti-Hbe: là marker cho thấy sự ngưng sao chép và khả năng lấy nhiễm thấp
(Lựa chọn A và B) Nhiễm HBV cấp tính biểu hiện bằng sự xuất hiện của HbsAg và IgM anti-HBc. Ngược lại, nhiễm HBV mạn được xác định khi có sự xuất hiện HBsAg trong huyết thanh > 6 tháng.
(Lựa chọn C) Nhiễm HBV giai đoạn hồi phục biểu hiện bằng sự xuất hiện của anti-HBs, anti-HBc (ưu thế IgG), và anti-Hbe.
Ca 2
Bệnh nhân nữ, 42 tuổi đi khám vì mệt mỏi và nước tiểu màu vàng sậm. Cô ấy cũng cảm thấy chán ăn, buồn nôn, đau bụng nhẹ và thiếu sức sống. Bệnh nhân không biết chắc thời điểm bắt đầu triệu chứng nhưng cô ấy vẫn cảm thấy bình thường vào kỳ nghỉ 4 tuần trước. Chưa ghi nhận tiền căn bệnh lý và tiền căn dùng thuốc. Bệnh nhân không sử dụng rượu bia, thuốc lá và các chất cấm. Tuy nhiên, cô ấy có quan hệ tình dục không dùng biện pháp bảo vệ với 6 bạn tình khác nhau trong năm qua. Bệnh nhân không nhớ rõ tiền căn tiêm ngừa viêm gan B. Xét nghiệm ban đầu ghi nhận:
| Bilirubin toàn phần | 5.3 mg/dL |
| ALP | 170 U/L |
| AST | 992 U/L |
| ALT | 1290 U/L |
Xét nghiệm nào sau đây phù hợp để chẩn đoán viêm gan siêu vi B?
- HBcAg.
- HBeAg.
- HBsAg và anti-HBs.
- HBsAg và IgM anti-HBc.
- Hepatitis B virus DNA.
Bệnh nhân nữ, 42 tuổi, đi khám vì mệt mỏi:
- Đau bụng, mệt mỏi, nước tiểu vàng sậm.
- Tiền căn: Quan hệ tình dục không an toàn, không dùng biện pháp bảo vệ.
- Xét nghiệm: AST, ALT tăng cao > 10 ULN, AST/ALT < 1, tăng bilirubin toàn phần.
Đáp án: D: HbsAg và IgM anti-HBc
Các triệu chứng mới khởi phát của bệnh nhân này (ví dụ: mệt mỏi, buồn nôn/đau bụng, nước tiểu sẫm màu) và xét nghiệm chức năng gan bất thường (ví dụ: tăng transaminase, tăng bilirubin máu) kèm theo tiền căn quan hệ tình dục không an toàn với nhiều bạn tình, do đó bệnh có thể là do nhiễm viêm gan siêu vi B cấp. Marker đầu tiền xuất hiện trong huyết thanh là HBsAg, thường xuất hiện 4-8 tuần sau khi nhiễm bệnh. lgM anti-HBc xuất hiện ngay sau đó, đây cũng là lúc xuất hiện các triệu chứng lâm sàng và tăng nồng độ aminotransferase trong gan (thường > 25 lần giới hạn bình thường).
Giai đoạn cửa sổ (vài tuần đến vài tháng) là giai đoạn mà không tìm thấy HBsAg và anti-HBs chưa đủ để phát hiện. IgM anti-HBc có thể là dấu hiệu duy nhất có thể phát hiện được đối với nhiễm viêm gan B cấp tính trong giai đoạn này. Như vậy, HBsAg và anti-HBc là các xét nghiệm chẩn đoán thích hợp nhất cho viêm gan B cấp tính vì cả hai đều tăng trong quá trình nhiễm trùng ban đầu và anti-HBc sẽ vẫn tăng giai đoạn cửa sổ.
(Lựa chọn A) HBcAg không thể phát hiện được trong huyết thanh, do đó không hữu ích để xác định chẩn đoán.
(Lựa chọn B) HBeAg là một chỉ số tốt về khả năng lây nhiễm nhưng là một xét nghiệm kém đối với viêm gan B cấp tính vì nồng độ thường giảm sớm.
(Lựa chọn C) Xét nghiệm HBsAg và anti—HBs có thể bỏ sót chẩn đoán nhiễm viêm gan B cấp tính ở những bệnh nhân đang trong giai đoạn cửa sổ.
(Lựa chọn E) Mặc dù HBV DNA có thể được phát hiện trước khi xuất hiện HBsAg hoặc HBeAg, nhưng xét nghiệm này thường không được thực hiện để chẩn đoán nhiễm trùng cấp tính. Thay vào đó, HBV DNA thường được thực hiện ở bệnh nhân viêm gan B mạn tính để xác định khả năng điều trị bằng thuốc kháng vi-rút hoặc theo dõi đáp ứng với điều trị.
Kết luận:
HBsAg và anti-HBc là những xét nghiệm chẩn đoán thích hợp nhất đối với nhiễm viêm gan B cấp tính vì cả hai đều tăng trong thời gian nhiễm bệnh ban đầu và anti-HBc sẽ duy trì ở mức cao trong suốt thời kỳ cửa sổ.
Ca 3
Bệnh sử
Bệnh nhân nam 22 tuổi đến khám vì mệt mỏi và chán ăn khoảng 1 tuần. Bệnh nhân nôn ói 1 lần, không có máu. Bệnh nhân cảm thấy sốt nhưng không đo nhiệt độ. Khoảng 2 tuần nay, bệnh nhân đau nhức đầu gối, khuỷu tay và cổ tay nhưng không có phù khớp. Bệnh nhân không thấy bất thường về nước tiểu và phân.
Cách đây 5 năm, bệnh nhân bị sốt tuyến đã chẩn đoán xác định bằng huyết thanh học. Bệnh nhân hút 25 điếu thuốc lá mỗi ngày và uống 20-40 đơn vị rượu mỗi tuần. Bệnh nhân dùng cần sa (marijuana) và thuốc lắc (ecstasy) vài lần trong 2 năm qua và nhiều loại thuốc viên hoặc thuốc hỗn hợp tại các câu lạc bộ mà không chắc về thành phần. Bệnh nhân phủ nhận dùng ma túy qua đường tĩnh mạch. Bệnh nhân có quan hệ đồng tính không thường xuyên nhưng luôn luôn dùng biện pháp bảo vệ. Bệnh nhân khai có xét nghiệm âm tính HIV 6 tháng trước. Bệnh nhân không du lịch nước ngoài trong 2 năm qua.
Bệnh nhân đang thất nghiệp và sống trong 1 căn hộ cùng 3 người khác. Không có tiền sử gia đình liên quan.
Khám lâm sàng
Bệnh nhân có nhiệt độ 38.6°C và trông không khỏe. Bệnh nhân vàng da nhẹ. Bệnh nhân đau nhẹ vùng hạ sườn phải. Khám khớp và cơ quan khác đều bình thường.
Cận lâm sàng
| Bình thường | |
| Haemoglobin 14.1 g/dL
Thể tích trung bình hồng cầu (MCV) 85 fL Số lượnghồngcầu 11.5 X 109/L Số lượng tiểu cầu 286 X 109/L Prothrombin time(PT) 17 s Natri 135 mmol/L Kali 3.5 mmol/L Urea 3.2 mmol/L Creatinine 64 pmol/L Bilirubin 50 mmol/L Alkaline phosphatase 376IU/L Alanine aminotransferase 570IU/L Đường huyết lúc đói 4.1 mmol/L |
13.3-17.7 g/dL
80-99fL 3.9-10.6 X 109/L 150-440 X 109/L 10-14s 135-145 mmol/L 3.5- 5.0 mmol/L 2.5- 6.7 mmol/L 70-120 pmol/L 3-17 mmol/L 30-300IU/L 5-35IU/L 4.0-6.0 mmol/L |
Câu hỏi
- Giải thích các thông tin của ca lâm sàng?
- Chẩn đoán phù hợp là gì?
- Điều trị thế nào?
Trả lời
Chẩn đoán sơ bộ viêm gan siêu vi cấp. Kết quả các dấu ấn sinh hóa cho thấy xét nghiệm chức năng gan bình thường với thay đổi chủ yếu là transaminase, gợi ý bệnh lý trong tế bào gan hơn là vấn đề tắc nghẽn trong gan. Có thể do viêm gan siêu vi A, B hoặc C. Tăng số lượng bạch cầu phù hợp với tình trạng viêm gan cấp. Quan hệ đồng tính và lạm dụng ma túy dạng tiêm là các yếu tố nguy cơ viêm gan B và C. Cũng có thể nhiễm các virus khác như cytomegalo virus và herpes simplex. Do tiền sử sử dụng thuốc kích thích không rõ ràng, nên nghi ngờ viêm gan do thuốc. Các triệu chứng tiền triệu ở khớp gợi ý nguyên nhân do nhiễm siêu vi và thường gặp nhất là viêm gan B. Xét nghiệm huyết thanh học có thể làm để phát hiện các kháng thể immunoglobulin M (IgM) cho thấy nhiễm trùng cấp tính với 1 trong những virus này. Nên đo tải lượng virus. Xét nghiệm HIV âm tính 6 tháng trước nên ít nghĩ nguyên nhân do HIV, mặc dù tự bệnh nhân khai đã xét nghiệm HIV không phải lúc nào cũng đáng tin cậy và cũng nên cân nhắc chuyển đổi huyết thanh HIV
Bệnh nhân này bị viêm gan B cấp. Khoảng 30% trường hợp diễn tiến vàng da. Điều trị chủ yếu trong pha cấp. Thuốc kháng virus không được chỉ định trong hầu hết viêm gan B cấp. Thời gian prothrombin trên bệnh nhân này tăng nhẹ nhưng không đủ để lo ngại hoặc là dấu hiệu bệnh rất nặng. Nên đo chức năng gan để theo dõi enzym trong gan nhằm điều trị tiếp. Nên ngưng rượu và các thuốc gây độc gan cho đến khi chức năng gan trở về bình thường. Các biến chứng hiếm gặp của bệnh cấp tính là suy gan tối cấp, thiếu máu bất sản, viêm cơ tim và viêm mạch máu. Cầ n có cơ hội tư vấn cho bệnh nhân về tác hại tiềm tàng của thuốc lá, ma túy và rượu, cũng như các bệnh lây truyền qua đường tình dục. HBV có thể tồn tại ngoài cơ thể trong một thời gian nên khuyên bạn cùng phòng của bệnh nhân không dùng chung dao cạo râu hoặc bàn chảy đánh răng. Bệnh nhân đi tiêm vaccine viêm gan B. Chỉ 5% bệnh nhân trưởng thành mắc viêm gan B diễn tiến thành nhiễm trùng mạn tính. Bệnh nhân mắc bệnh gan do rượu kèm với viêm gan B sẽ tiên lượng nghèo nàn.
Ý chính
- Viêm gan do siêu vi thường liên quan các trệu chứng tiền triệu như đau khớp và triệu chứng giống cúm.
- Cần tìm bằng chứng xác nhận kết quả xét nghiệm HIV mà bệnh nhân khai.
- Lây truyền qua đường tình dục và dùng ma túy dạng tiêm là các con đường lây truyền chính của viêm gan B ở người trưởng thành ở các nước phát triển.
- Nhiễm trùng viêm gan B cấp tính là bệnh phổ biến ở Anh.
Tài liệu tham khảo
- Chu CJ, Keeffe EB, Han SH, et al. Hepatitis B virus genotypes in the United States: results of a nationwide study. Gastroenterology. 2003;125:444-451. Tóm lược
- Mohanty SR, Kupfer SS, Khiani V. Treatment of chronic hepatitis B. Nat Clin Pract Gastroenterol Hepatol. 2006;3:446-458. Tóm lược
- Terrault NA, Bzowej NH, Chang KM, et al. AASLD guidelines for treatment of chronic hepatitis B. Hepatology. 2016 Jan;63(1):261-83. Toàn văn Tóm lược
- Chu CJ, Lok AS. Clinical significance of hepatitis B virus genotypes. Hepatology. 2002;35:1274-1276. Toàn văn Tóm lược
- Erhardt A, Blondin D, Hauck K, et al. Response to interferon alfa is hepatitis B virus genotype dependent: genotype A is more sensitive to interferon than genotype D. Gut. 2005;54:1009-1013. Toàn văn Tóm lược
- Janssen HL, van Zonneveld M, Senturk H, et al. Pegylated interferon alfa-2b alone or in combination with lamivudine for HBeAg-positive chronic hepatitis B: a randomised trial. Lancet. 2005;365:123-129. Tóm lược
- Kao JH, Wu NH, Chen PJ, et al. Hepatitis B genotypes and the response to interferon therapy. J Hepatol. 2000;33:998-1002. Tóm lược
- Lau GK, Piratvisuth T, Luo KX, et al. Peginterferon alfa-2a, lamivudine, and the combination for HBeAg-positive chronic hepatitis B. N Engl J Med. 2005 Jun 30;352(26):2682-95. Tóm lược
- World Health Organization. Hepatitis B: fact sheet. July 2017 [internet publication]. Toàn văn
- Alter MJ. Epidemiology of hepatitis B in Europe and worldwide. J Hepatol. 2003;39 Suppl 1:S64-9. Tóm lược
- Gish RG, Gadano AC. Chronic hepatitis B: current epidemiology in the Americas and implications for management. J Viral Hepat. 2006 Dec;13(12):787-98. Tóm lược
- Centers for Disease Control and Prevention. Surveillance for viral hepatitis – United States, 2015. June 2017 [internet publication]. Toàn văn
- Hu KQ. Hepatitis B virus (HBV) infection in Asian and Pacific Islander Americans (APIAs): how can we do better for this special population? Am J Gastroenterol. 2008 Jul;103(7):1824-33. Tóm lược
- LeFevre ML; US Preventive Services Task Force. Screening for hepatitis B virus infection in nonpregnant adolescents and adults: U.S. Preventive Services Task Force recommendation statement. Ann Intern Med. 2014 Jul 1;161(1):58-66. Toàn văn Tóm lược
- Lee WM. Hepatitis B virus infection. N Engl J Med. 1997 Dec 11;337(24):1733-45. Tóm lược
- Ganem D, Prince AM. Hepatitis B virus infection – natural history and clinical consequences. N Engl J Med. 2004 Mar 11;350(11):1118-29. Tóm lược
- Guidotti LG, Rochford R, Chung J, et al. Viral clearance without destruction of infected cells during acute HBV infection. Science. 1999 Apr 30;284(5415):825-9. Tóm lược
- Guidotti LG, Ishikawa T, Hobbs MV, et al. Intracellular inactivation of the hepatitis B virus by cytotoxic T lymphocytes. Immunity. 1996 Jan;4(1):25-36. Tóm lược
- Chisari FV, Ferrari C. Hepatitis B virus immunopathogenesis. Annu Rev Immunol. 1995;13:29-60. Tóm lược
- Tuttleman JS, Pourcel C, Summers J. Formation of the pool of covalently closed circular viral DNA in hepadnavirus-infected cells. Cell. 1986 Nov 7;47(3):451-60. Tóm lược
- Seeger C, Mason WS. Hepatitis B virus biology. Microbiol Mol Biol Rev. 2000 Mar;64(1):51-68. Toàn văn Tóm lược
- Seeger C, Ganem D, Varmus HE. Biochemical and genetic evidence for the hepatitis B virus replication strategy. Science. 1986 Apr 25;232(4749):477-84. Tóm lược
- Newbold JE, Xin H, Tencza M, et al. The covalently closed duplex form of the hepadnavirus genome exists in situ as a heterogeneous population of viral minichromosomes. J Virol. 1995 Jun;69(6):3350-7. Toàn văn Tóm lược
- Zoulim F. New insight on hepatitis B virus persistence from the study of intrahepatic viral cccDNA. J Hepatol. 2005 Mar;42(3):302-8. Tóm lược
- Yuen MF, Wong DK, Sum SS, et al. Effect of lamivudine therapy on the serum covalently closed-circular (ccc) DNA of chronic hepatitis B infection. Am J Gastroenterol. 2005 May;100(5):1099-103. Tóm lược
- Wursthorn K, Lutgehetmann M, Dandri M, et al. Peginterferon alpha-2b plus adefovir induce strong cccDNA decline and HBsAg reduction in patients with chronic hepatitis B. Hepatology. 2006 Sep;44(3):675-84. Tóm lược
- Wong DK, Yuen MF, Ngai VW, et al. One-year entecavir or lamivudine therapy results in reduction of hepatitis B virus intrahepatic covalently closed circular DNA levels. Antivir Ther. 2006;11(7):909-16. Tóm lược
- Werle-Lapostolle B, Bowden S, Locarnini S, et al. Persistence of cccDNA during the natural history of chronic hepatitis B and decline during adefovir dipivoxil therapy. Gastroenterology. 2004 Jun;126(7):1750-8. Tóm lược
- Sung JJ, Wong ML, Bowden S, et al. Intrahepatic hepatitis B virus covalently closed circular DNA can be a predictor of sustained response to therapy. Gastroenterology. 2005 Jun;128(7):1890-7. Tóm lược
- Bourne EJ, Dienstag JL, Lopez VA, et al. Quantitative analysis of HBV cccDNA from clinical specimens: correlation with clinical and virological response during antiviral therapy. J Viral Hepat. 2007 Jan;14(1):55-63. Tóm lược
- European Association for the Study of the Liver. EASL 2017 clinical practice guidelines on the management of hepatitis B virus infection. J Hepatol. 2017 Aug;67(2):370-98. Toàn văn Tóm lược
- Chu CJ, Lee SD. Hepatitis B virus/hepatitis C virus coinfection: epidemiology, clinical features, viral interactions and treatment. J Gastroenterol Hepatol. 2008 Apr;23(4):512-20. Toàn văn Tóm lược
- Donato F, Boffetta P, Puoti M. A meta-analysis of epidemiological studies on the combined effect of hepatitis B and C virus infections in causing hepatocellular carcinoma. Int J Cancer. 1998 Jan 30;75(3):347-54. Toàn văn Tóm lược
- Jamma S, Hussain G, Lau DT. Current concepts of HBV/HCV coinfection: coexistence, but not necessarily in harmony. Curr Hepat Rep. 2010;9(4):260-269. Toàn văn Tóm lược
- Bellecave P, Gouttenoire J, Gajer M, et al. Hepatitis B and C virus coinfection: a novel model system reveals the absence of direct viral interference. Hepatology. 2009 Jul;50(1):46-55. Toàn văn Tóm lược
- Ghendon Y. Perinatal transmission of hepatitis B virus in high-incidence countries. J Virol Methods. 1987 Aug;17(1-2):69-79. Tóm lược
- Goldstein ST, Alter MJ, Williams IT, et al. Incidence and risk factors for acute hepatitis B in the United States, 1982-1998: implications for vaccination programs. J Infect Dis. 2002 Mar 15;185(6):713-9. Tóm lược
- Wasley A, Miller JT, Finelli L. Surveillance for acute viral hepatitis: United States, 2005. MMWR Surveill Summ. 2007 Mar 16;56(3):1-24. Tóm lược
- World Health Organization. Guidelines for the prevention, care and treatment of persons with chronic hepatitis B infection. March 2015 [internet publication]. Toàn văn
- Thio CL. Hepatitis B in the human immunodeficiency virus-infected patient: epidemiology, natural history, and treatment. Semin Liver Dis. 2003 May;23(2):125-36. Tóm lược
- Strader DB. Understudied populations with hepatitis C. Hepatology. 2002 Nov;36(5 Suppl 1):S226-36. Tóm lược
- Dodd RY, Notari EP, Stramer SL. Current prevalence and incidence of infectious disease markers and estimated window-period risk in the American Red Cross blood donor population. Transfusion. 2002 Aug;42(8):975-9. Tóm lược
- Mahoney FJ, Stewart K, Hu H, et al. Progress toward the elimination of hepatitis B virus transmission among health care workers in the United States. Arch Intern Med. 1997 Dec 8-22;157(22):2601-5. Tóm lược
- Harpaz R, Von Seidlein L, Averhoff FM, et al. Transmission of hepatitis B virus to multiple patients from a surgeon without evidence of inadequate infection control. N Engl J Med. 1996 Feb 29;334(9):549-54. Tóm lược
- Lettau LA, Smith JD, Williams D, et al. Transmission of hepatitis B with resultant restriction of surgical practice. JAMA. 1986 Feb 21;255(7):934-7. Tóm lược
- Bond WW, Favero MS, Petersen NJ, et al. Survival of hepatitis B virus after drying and storage for one week. Lancet. 1981 Mar 7;1(8219):550-1. Tóm lược
- Davis LG, Weber DJ, Lemon SM. Horizontal transmission of hepatitis B virus. Lancet. 1989 Apr 22;1(8643):889-93. Tóm lược
- Cendoroglo Neto M, Draibe SA, Silva AE, et al. Incidence of and risk factors for hepatitis B virus and hepatitis C virus infection among hemodialysis and CAPD patients: evidence for environmental transmission. Nephrol Dial Transplant. 1995;10(2):240-6. Tóm lược
- Mast EE, Weinbaum CM, Fiore AE, et al. A comprehensive immunization strategy to eliminate transmission of hepatitis B virus infection in the United States: recommendations of the Advisory Committee on Immunization Practices (ACIP) part II: immunization of adults. MMWR Recomm Rep. 2006 Dec 8;55(RR-16):1-33. Toàn văn Tóm lược
- Robinson CL, Romero JR, Kempe A, et al. Advisory Committee on Immunization Practices Recommended Immunization Schedule for Children and Adolescents Aged 18 Years or Younger – United States, 2018. MMWR Morb Mortal Wkly Rep. 2018 Feb 9;67(5):156-157. Toàn văn Tóm lược
- Public Health England. Hepatitis B: the green book, chapter 18. June 2017 [internet publication]. Toàn văn
- Makris MC, Polyzos KA, Mavros MN, et al. Safety of hepatitis B, pneumococcal polysaccharide and meningococcal polysaccharide vaccines in pregnancy: a systematic review. Drug Saf. 2012 Jan 1;35(1):1-14. Tóm lược
- Kim DK, Riley LE, Hunter P. Advisory Committee on Immunization Practices Recommended Immunization Schedule for Adults Aged 19 Years or Older – United States, 2018. MMWR Morb Mortal Wkly Rep. 2018 Feb 9;67(5):158-160. Toàn văn Tóm lược
- Schillie S, Harris A, Link-Gelles R, et al. Recommendations of the advisory committee on immunization practices for use of a hepatitis B vaccine with a novel adjuvant. MMWR Morb Mortal Wkly Rep. 2018 Apr 20;67(15):455-458. Toàn văn Tóm lược
- Pham H, Geraci SA, Burton MJ, et al. Adult immunizations: update on recommendations. Am J Med. 2011 Aug;124(8):698-701. Tóm lược
- Centers for Disease Control and Prevention (CDC). Use of hepatitis B vaccination for adults with diabetes mellitus: recommendations of the Advisory Committee on Immunization Practices (ACIP). MMWR Morb Mortal Wkly Rep. 2011 Dec 23;60(50):1709-11. Toàn văn Tóm lược
- Fabrizi F, Dixit V, Martin P, et al. Meta-analysis: the impact of diabetes mellitus on the immunological response to hepatitis B virus vaccine in dialysis patients. Aliment Pharmacol Ther. 2011 Apr;33(7):815-21. Tóm lược
- Fabrizi F, Dixit V, Martin P, et al. Hepatitis C virus and the immunological response to hepatitis B virus vaccine in dialysis patients: meta-analysis of clinical studies. J Viral Hepat. 2011 Dec;18(12):871-6. Tóm lược
- Rahier JF, Ben-Horin S, Chowers Y, et al. European evidence-based consensus on the prevention, diagnosis and management of opportunistic infections in inflammatory bowel disease. J Crohns Colitis. 2009 Jun;3(2):47-91. Tóm lược
- McMahon BJ, Alward WL, Hall DB, et al. Acute hepatitis B virus infection: relation of age to the clinical expression of disease and subsequent development of the carrier state. J Infect Dis. 1985 Apr;151(4):599-603. Tóm lược
- Lok AS, Liang RH, Chiu EK, et al. Reactivation of hepatitis B virus replication in patients receiving cytotoxic therapy. Report of a prospective study. Gastroenterology. 1991 Jan;100(1):182-8. Tóm lược
- Ostuni P, Botsios C, Punzi L, et al. Hepatitis B reactivation in a chronic hepatitis B surface antigen carrier with rheumatoid arthritis treated with infliximab and low dose methotrexate. Ann Rheum Dis. 2003 Jul;62(7):686-7. Tóm lược
- Bruix J, Sherman M; Practice Guidelines Committee, American Association for the Study of Liver Diseases. Management of hepatocellular carcinoma. Hepatology. 2005;42:1208-1236. Toàn văn Tóm lược
- Heimbach J, Kulik LM, Finn R, et al. AASLD guidelines for the treatment of hepatocellular carcinoma. Hepatology. 2018 Jan;67(1):358-380. Toàn văn Tóm lược
- Bedossa P, Dargère D, Paradis V. Sampling variability of liver fibrosis in chronic hepatitis C. Hepatology. 2003 Dec;38(6):1449-57. Toàn văn Tóm lược
- West J, Card TR. Reduced mortality rates following elective percutaneous liver biopsies. Gastroenterology. 2010 Oct;139(4):1230-7. Toàn văn Tóm lược
- Cardoso AC, Carvalho-Filho RJ, Marcellin P. Transient elastography in chronic viral hepatitis: a critical appraisal. Gut. 2011 Jun;60(6):759-64. Tóm lược
- Cardoso AC, Carvalho-Filho RJ, Stern C, et al. Direct comparison of diagnostic performance of transient elastography in patients with chronic hepatitis B and chronic hepatitis C. Liver Int. 2012 Apr;32(4):612-21. Tóm lược
- Castéra L. Transient elastography and other noninvasive tests to assess hepatic fibrosis in patients with viral hepatitis. J Viral Hepatol. 2009 May;16(5):300-14. Tóm lược
- Castéra L, Bernard PH, Le Bail P, et al. Transient elastography and biomarkers for liver fibrosis assessment and follow-up of inactive hepatitis B carriers. Aliment Pharmacol Ther. 2011 Feb;33(4):455-65. Toàn văn Tóm lược
- Fraquelli M, Branchi F. The role of transient elastography in patients with hepatitis B viral disease. Dig Liver Dis. 2011 Jan;43 Suppl 1:S25-31. Tóm lược
- Marcellin P, Ziol M, Bedossa P, et al. Non-invasive assessment of liver fibrosis by stiffness measurement in patients with chronic hepatitis B. Liver Int. 2009 Feb;29(2):242-7. Tóm lược
- Myers RP, Tainturier MH, Ratziu V, et al. Prediction of liver histological lesions with biochemical markers in patients with chronic hepatitis B. J Hepatol. 2003 Aug;39(2):222-30. Tóm lược
- Poynard T, Morra R, Halfon P, et al. Meta-analyses of FibroTest diagnostic value in chronic liver disease. BMC Gastroenterol. 2007;7:40. Toàn văn Tóm lược
- Arena U, Vizzutti F, Corti G, et al. Acute viral hepatitis increases liver stiffness values measured by transient elastography. Hepatology. 2008 Feb;47(2):380-4. Toàn văn Tóm lược
- Tsochatzis EA, Gurusamy KS, Ntaoula S, et al. Elastography for the diagnosis of severity of fibrosis in chronic liver disease: a meta-analysis of diagnostic accuracy. J Hepatol. 2011 Apr;54(4):650-9. Tóm lược
- Centers for Disease Control and Prevention. Public Health Service inter-agency guidelines for screening donors of blood, plasma, organs, tissues, and semen for evidence of hepatitis B and hepatitis C. MMWR Recomm Rep. 1991 Apr 19;40(RR-4):1-17. Tóm lược
- Saldanha J, Gerlich W, Lelie N, et al; WHO Collaborative Study Group. An international collaborative study to establish a World Health Organization international standard for hepatitis B virus DNA nucleic acid amplification techniques. Vox Sang. 2001 Jan;80(1):63-71. Tóm lược
- Lok AS, Heathcote EJ, Hoofnagle JH. Management of hepatitis B: 2000 – summary of a workshop. Gastroenterology. 2001 Jun;120(7):1828-53. Tóm lược
- Colli A, Fraquelli M, Casazza G, et al. Accuracy of ultrasonography, spiral CT, magnetic resonance, and alpha-fetoprotein in diagnosing hepatocellular carcinoma: a systematic review. Am J Gastroenterol. 2006 Mar;101(3):513-23. Tóm lược
- Gupta S, Bent S, Kohlwes J. Test characteristics of alpha-fetoprotein for detecting hepatocellular carcinoma in patients with hepatitis C. A systematic review and critical analysis. Ann Intern Med. 2003 Jul 1;139(1):46-50. Tóm lược
- Soresi M, Magliarisi C, Campagna P, et al. Usefulness of alpha-fetoprotein in the diagnosis of hepatocellular carcinoma. Anticancer Res. 2003 Mar-Apr;23(2C):1747-53. Tóm lược
- Tassopoulos NC, Papaevangelou GJ, Sjogren MH, et al. Natural history of acute hepatitis B surface antigen-positive hepatitis in Greek adults. Gastroenterology. 1987 Jun;92(6):1844-50. Tóm lược
- Tillmann HL, Hadem J, Leifeld L, et al. Safety and efficacy of lamivudine in patients with severe acute or fulminant hepatitis B, a multicenter experience. J Viral Hepat. 2006 Apr;13(4):256-63. Tóm lược
- Lee WM, Larson AM, Stravitz RT. AASLD position paper: the management of acute liver failure: update 2011. 2011 [internet publication]. Toàn văn
- Papatheodoridis GV, Lampertico P, Manolakopoulos S, et al. Incidence of hepatocellular carcinoma in chronic hepatitis B patients receiving nucleos(t)ide therapy: A systematic review. J Hepatol. 2010 Aug;53(2):348-56. Tóm lược
- Wong GL, Yiu KK, Wong VW, et al. Meta-analysis: reduction in hepatic events following interferon-alfa therapy of chronic hepatitis B. Aliment Pharmacol Ther. 2010 Nov;32(9):1059-68. Toàn văn Tóm lược
- Sung JJ, Tsoi KK, Wong VW, et al. Meta-analysis: treatment of hepatitis B infection reduces risk of hepatocellular carcinoma. Aliment Pharmacol Ther. 2008 Nov 1;28(9):1067-77. Tóm lược
- Miyake Y, Kobashi H, Yamamoto K. Meta-analysis: the effect of interferon on development of hepatocellular carcinoma in patients with chronic hepatitis B virus infection. J Gastroenterol. 2009;44(5):470-5. Tóm lược
- Keeffe EB, Dieterich DT, Han SH, et al. A treatment algorithm for the management of chronic hepatitis B virus infection in the United States: an update. Clin Gastroenterol Hepatol. 2006 Aug;4(8):936-62. Tóm lược
- Woo G, Tomlinson G, Nishikawa Y, et al. Tenofovir and entecavir are the most effective antiviral agents for chronic hepatitis B: a systematic review and Bayesian meta-analyses. Gastroenterology. 2010 Oct;139(4):1218-29. Toàn văn Tóm lược
- Gish RG, Lok AS, Chang TT, et al. Entecavir therapy for up to 96 weeks in patients with HBeAg-positive chronic hepatitis B. Gastroenterology. 2007 Nov;133(5):1437-44. Tóm lược
- Wong DK, Cheung AM, O’Rourke K, et al. Effect of alpha-interferon treatment in patients with hepatitis B e antigen-positive chronic hepatitis B. A meta-analysis. Ann Intern Med. 1993 Aug 15;119(4):312-23. Tóm lược
- Lin SM, Sheen IS, Chien RN, et al. Long-term beneficial effect of interferon therapy in patients with chronic hepatitis B virus infection. Hepatology. 1999 Mar;29(3):971-5. Tóm lược
- Flink HJ, van Zonneveld M, Hansen BE, et al. Treatment with Peg-interferon alpha-2b for HBeAg-positive chronic hepatitis B: HBsAg loss is associated with HBV genotype. Am J Gastroenterol. 2006 Feb;101(2):297-303. Tóm lược
- Zoulim F, Carosi G, Greenbloom S, et al. Quantification of HBsAg in nucleos(t)ide-naive patients treated for chronic hepatitis B with entecavir with or without tenofovir in the BE-LOW study. J Hepatol. 2015 Jan;62(1):56-63. Tóm lược
- Marcellin P, Buti M, Krastev Z, et al. Kinetics of hepatitis B surface antigen loss in patients with HBeAg-positive chronic hepatitis B treated with tenofovir disoproxil fumarate. J Hepatol. 2014 Dec;61(6):1228-37. Tóm lược
- Sonneveld MJ, Hansen BE, Piratvisuth T, et al. Response-guided peginterferon therapy in hepatitis B e antigen-positive chronic hepatitis B using serum hepatitis B surface antigen levels. Hepatology. 2013 Sep;58(3):872-80. Toàn văn Tóm lược
- Brunetto MR, Moriconi F, Bonino F, et al. Hepatitis B virus surface antigen levels: a guide to sustained response to peginterferon alfa-2a in HBeAg-negative chronic hepatitis B. Hepatology. 2009 Apr;49(4):1141-50. Tóm lược
- Moucari R, Mackiewicz V, Lada O, et al. Early serum HBsAg drop: a strong predictor of sustained virological response to pegylated interferon alfa-2a in HBeAg-negative patients. Hepatology. 2009 Apr;49(4):1151-7. Toàn văn Tóm lược
- Moucari R, Martinot-Peignoux M, Mackiewicz V, et al. Influence of genotype on hepatitis B surface antigen kinetics in hepatitis B e antigen-negative patients treated with pegylated interferon-alpha2a. Antivir Ther. 2009;14(8):1183-8. Tóm lược
- Carosi G, Rizzetto M, Alberti A, et al. Treatment of chronic hepatitis B: update of the recommendations from the 2007 Italian Workshop. Dig Liver Dis. 2011 Apr;43(4):259-65. Tóm lược
- Perrillo R, Tamburro C, Regenstein F, et al. Low-dose, titratable interferon alfa in decompensated liver disease caused by chronic infection with hepatitis B virus. Gastroenterology. 1995 Sep;109(3):908-16. Tóm lược
- Buster EH, Hansen BE, Buti M, et al; HBV 99-01 Study Group. Peginterferon alpha-2b is safe and effective in HBeAg-positive chronic hepatitis B patients with advanced fibrosis. Hepatology. 2007 Aug;46(2):388-94. Toàn văn Tóm lược
- Liaw YF, Sung JJ, Chow WC, et al. Lamivudine for patients with chronic hepatitis B and advanced liver disease. N Engl J Med. 2004 Oct 7;351(15):1521-31. Toàn văn Tóm lược
- Singal AK, Fontana RJ. Meta-analysis: oral anti-viral agents in adults with decompensated hepatitis B virus cirrhosis. Aliment Pharmacol Ther. 2012 Mar;35(6):674-89. Tóm lược
- Papatheodoridis GV, Dimou E, Dimakopoulos K, et al. Outcome of hepatitis B e antigen-negative chronic hepatitis B on long-term nucleos(t)ide analog therapy starting with lamivudine. Hepatology. 2005 Jul;42(1):121-9. Toàn văn Tóm lược
- Chang TT, Liaw YF, Wu SS, et a. Long-term entecavir therapy results in the reversal of fibrosis/cirrhosis and continued histological improvement in patients with chronic hepatitis B. Hepatology. 2010 Sep;52(3):886-93. Toàn văn Tóm lược
- Liaw YF, Raptopoulou-Gigi M, Cheinquer H, et al. Efficacy and safety of entecavir versus adefovir in chronic hepatitis B patients with hepatic decompensation: a randomized, open-label study. Hepatology. 2011 Jul;54(1):91-100. Toàn văn Tóm lược
- Liaw YF, Sheen IS, Lee CM, et al. Tenofovir disoproxil fumarate (TDF), emtricitabine/TDF, and entecavir in patients with decompensated chronic hepatitis B liver disease. Hepatology. 2011 Jan;53(1):62-72. Toàn văn Tóm lược
- Shim JH, Lee HC, Kim KM, et al. Efficacy of entecavir in treatment-naive patients with hepatitis B virus-related decompensated cirrhosis. J Hepatol. 2010 Feb;52(2):176-82. Tóm lược
- Lange CM, Bojunga J, Hofmann WP, et al. Severe lactic acidosis during treatment of chronic hepatitis B with entecavir in patients with impaired liver function. Hepatology. 2009 Dec;50(6):2001-6. Toàn văn Tóm lược
- Altfeld M, Rockstroh JK, Addo M, et al. Reactivation of hepatitis B in a long-term anti-HBs-positive patient with AIDS following lamivudine withdrawal. J Hepatol. 1998 Aug;29(2):306-9. Tóm lược
- Centers for Disease Control and Prevention; National Institutes for Health; HIV Medicine Association of the Infectious Diseases Society of America. Guidelines for the prevention and treatment of opportunistic infections in HIV-infected adults and adolescents: hepatitis B virus infection. August 2017 [internet publication]. Toàn văn
- Yurdaydin C, Idilman R, Bozkaya H, et al. Natural history and treatment of chronic delta hepatitis. J Viral Hepat. 2010 Nov;17(11):749-56. Tóm lược
- Hughes SA, Wedemeyer H, Harrison PM. Hepatitis delta virus. Lancet. 2011 Jul 2;378(9785):73-85. Tóm lược
- Farci P, Mandas A, Coiana A, et al. Treatment of chronic hepatitis D with interferon alfa-2a. N Engl J Med. 1994 Jan 13;330(2):88-94. Tóm lược
- Farci P, Roskams T, Chessa L, et al. Long-term benefit of interferon alpha therapy of chronic hepatitis D: regression of advanced hepatic fibrosis. Gastroenterology. 2004 Jun;126(7):1740-9. Tóm lược
- Bzowej NH. Hepatitis B therapy in pregnancy. Curr Hepat Rep. 2010 Nov;9(4):197-204. Toàn văn Tóm lược
- Pan CQ, Duan Z, Dai E, et al; China Study Group for the Mother-to-Child Transmission of Hepatitis B. Tenofovir to prevent hepatitis B transmission in mothers with high viral load. N Engl J Med. 2016 Jun 16;374(24):2324-34. Tóm lược
- Hyun MH, Lee YS, Kim JH, et al. Systematic review with meta-analysis: the efficacy and safety of tenofovir to prevent mother-to-child transmission of hepatitis B virus. Aliment Pharmacol Ther. 2017 Jun;45(12):1493-505. Tóm lược
- Han GR, Cao MK, Zhao W, et al. A prospective and open-label study for the efficacy and safety of telbivudine in pregnancy for the prevention of perinatal transmission of hepatitis B virus infection. J Hepatol. 2011 Dec;55(6):1215-21. Tóm lược
- Shi Z, Yang Y, Ma L, et al. Lamivudine in late pregnancy to interrupt in utero transmission of hepatitis B virus: systematic review and meta-analysis. Obstet Gynecol. 2010 Jul;116(1):147-59. Tóm lược
- Su GG, Pan KH, Zhao NF, et al. Efficacy and safety of lamivudine treatment for chronic hepatitis B in pregnancy. World J Gastroenterol. 2004 Mar 15;10(6):910-2. Tóm lược
- van Zonneveld M, van Nunen AB, Niesters HG, et al. Lamivudine treatment during pregnancy to prevent perinatal transmission of hepatitis B virus infection. J Viral Hepat. 2003 Jul;10(4):294-7. Tóm lược
- Xu WM, Cui YT, Wang L, et al. Lamivudine in late pregnancy to prevent perinatal transmission of hepatitis B virus infection: a multicentre, randomized, double-blind, placebo-controlled study. J Viral Hepat. 2009 Feb;16(2):94-103. Tóm lược
- Shi Z, Yang Y, Wang H, et al. Breastfeeding of newborns by mothers carrying hepatitis B virus: a meta-analysis and systematic review. Arch Pediatr Adolesc Med. 2011 Sep;165(9):837-46. Tóm lược
- Jonas MM, Block JM, Haber BA, et al. Treatment of children with chronic hepatitis B virus infection in the United States: patient selection and therapeutic options. Hepatology. 2010 Dec;52(6):2192-205. Toàn văn Tóm lược
- Chan HLY, Fung S, Seto WK, et al. Tenofovir alafenamide versus tenofovir disoproxil fumarate for the treatment of HBeAg-positive chronic hepatitis B virus infection: a randomised, double-blind, phase 3, non-inferiority trial. Lancet Gastroenterology & Hepatology. 2016;3:185-195.
- Buti M, Gane E, Seto WK, et al. Tenofovir alafenamide versus tenofovir disoproxil fumarate for the treatment of patients with HBeAg-negative chronic hepatitis B virus infection: a randomised, double-blind, phase 3, non-inferiority trial. Lancet Gastroenterology & Hepatology. 2016;3:196-206.
- Gilead. European Commission grants marketing authorization for Gilead’s Vemlidy® (tenofovir alafenamide, TAF) for the treatment of chronic hepatitis B virus infection. January 2017. http://www.gilead.com/ (last accessed 25 July 2017). Toàn văn
- Keeffe EB, Marcellin P. New and emerging treatment of chronic hepatitis B. Clin Gastroenterol Hepatol. 2007;5:285-294. Tóm lược
- McCaffrey AP, Nakai H, Pandey K, et al. Inhibition of hepatitis B virus in mice by RNA interference. Nat Biotechnol. 2003;21:639-644. Tóm lược
- Niederau C, Heintges T, Lange S, et al. Long-term follow-up of HBeAg-positive patients treated with interferon alfa for chronic hepatitis B. N Engl J Med. 1996;334:1422-1427. Tóm lược
- Gish RG, Chang TT, Lai CL, et al. Loss of HBsAg antigen during treatment with entecavir or lamivudine in nucleoside-naive HBeAg-positive patients with chronic hepatitis B. J Viral Hepat. 2010;17:16-22. Tóm lược
- Yim HJ, Lok AS. Natural history of chronic hepatitis B virus infection: what we knew in 1981 and what we know in 2005. Hepatology. 2006;43(suppl 1):S173-S181. Tóm lược
- El-Serag HB. Epidemiology of viral hepatitis and hepatocellular carcinoma. Gastroenterology. 2012;142:1264-1273. Toàn văn Tóm lược
- Bosch FX, Ribes J, Cleries R, et al. Epidemiology of hepatocellular carcinoma. Clin Liver Dis. 2005;9:191-211. Tóm lược
- Yang HI, Lu SN, Liaw YF, et al. Hepatitis B e antigen and the risk of hepatocellular carcinoma. N Engl J Med. 2002;347:168-174. Tóm lược
- Iloeje UH, Yang HI, Su J, et al. Predicting cirrhosis risk based on the level of circulating hepatitis B viral load. Gastroenterology. 2006;130:678-686. Tóm lược
- Smedile A, Farci P, Verme G, et al. Influence of delta infection on severity of hepatitis B. Lancet. 1982;2:945-947. Tóm lược
- Feray C, Gigou M, Samuel D, et al. Hepatitis C virus RNA and hepatitis B virus DNA in serum and liver of patients with fulminant hepatitis. Gastroenterology. 1993;104:549-555. Tóm lược
- Fabrizi F, Dixit V, Martin P. Meta-analysis: anti-viral therapy of hepatitis B virus-associated glomerulonephritis. Aliment Pharmacol Ther. 2006;24:781-788. Tóm lược
- Lok AS, McMahon BJ. Chronic hepatitis B. Hepatology. 2007 Feb;45(2):507-39. Toàn văn Tóm lược
- Lai CL, Gane E, Liaw YF, et al. Telbivudine versus lamivudine in patients with chronic hepatitis B. N Engl J Med. 2007 Dec 20;357(25):2576-88. Toàn văn Tóm lược
- Liaw YF, Gane E, Leung N, et al. 2-Year GLOBE trial results: telbivudine Is superior to lamivudine in patients with chronic hepatitis B. Gastroenterology. 2009 Feb;136(2):486-95. Tóm lược
- Chevillotte G, Durbec JP, Gerolami A, et al. Interaction between hepatitis b virus and alcohol consumption in liver cirrhosis. An epidemiologic study. Gastroenterology. 1983 Jul;85(1):141-5. Tóm lược
- Grellier L, Mutimer D, Ahmed M, et al. Lamivudine prophylaxis against reinfection in liver transplantation for hepatitis B cirrhosis. Lancet. 1996 Nov 2;348(9036):1212-5. [Erratum in: Lancet 1997 Feb 1;349(9048):364.] Tóm lược
- Papatheodoridis GV, Cholongitas E, Archimandritis AJ, et al. Current management of hepatitis B virus infection before and after liver transplantation. Liver Int. 2009 Oct;29(9):1294-305. Toàn văn Tóm lược
- Samuel D. Management of hepatitis B in liver transplantation patients. Semin Liver Dis. 2004;24 Suppl 1:55-62. Tóm lược
- Schiff E, Lai CL, Hadziyannis S, et al; Adefovir Dipivoxil Study 45 International Investigators Group. Adefovir dipivoxil for wait-listed and post-liver transplantation patients with lamivudine-resistant hepatitis B: final long-term results. Liver Transpl. 2007 Mar;13(3):349-60. Toàn văn Tóm lược
- Cholongitas E, Goulis J, Akriviadis E, et al. Hepatitis B immunoglobulin and/or nucleos(t)ide analogues for prophylaxis against hepatitis b virus recurrence after liver transplantation: a systematic review. Liver Transpl. 2011 Oct;17(10):1176-90. Tóm lược
Hình ảnh
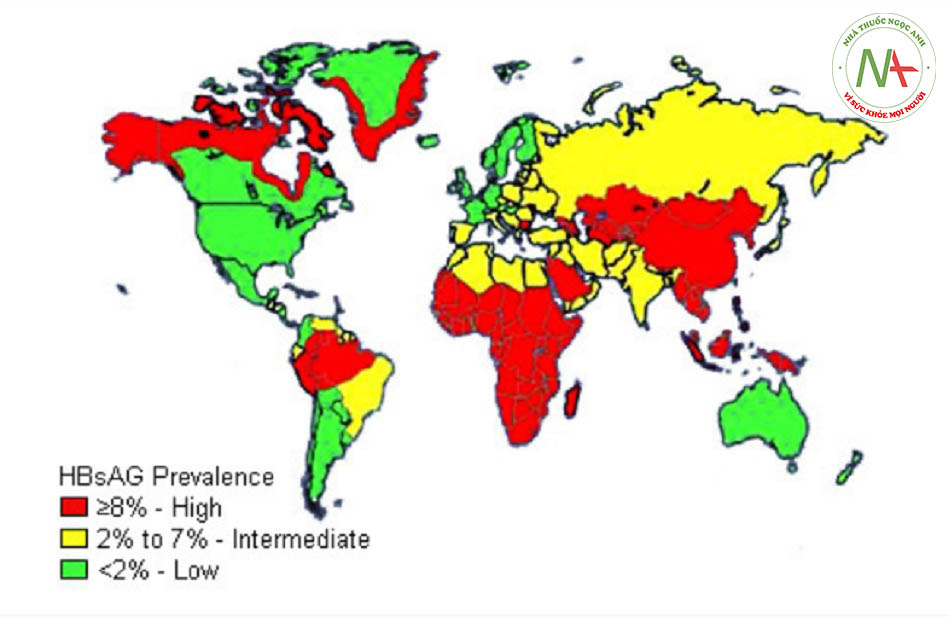

![Viêm gan B: Nguyên nhân, chẩn đoán và hướng dẫn điều trị theo BMJ 15 Hình 3: Các giai đoạn nhiễm viêm gan B mạn tính [AASLD = Hiệp hội Nghiên cứu Bệnh Gan Hoa Kỳ, EASL = Hiệp hội Nghiên cứu Gan Châu Âu; *cccDNA]](https://nhathuocngocanh.com/wp-content/uploads/2022/03/viem_gan_B_nguyen_nhan_chan_doan_dieu_tri_theo_bmj_hinh3.jpg)
Những người có đóng góp
// Các tác giả:
Jawad Ahmad, MD, FRCP, FAASLD
Professor of Medicine
Division of Liver Diseases, Mount Sinai Hospital, New York, NY CÔNG KHAI THÔNG TIN: JA declares that he has no competing interests.
// Lời cảm ơn:
Dr Jawad Ahmad would like to gratefully acknowledge Dr Sateesh R. Prakash, Dr Siddarth Verma, Dr Smruti R. Mohanty, and Dr Jared Hossack, previous contributors to this monograph. SRP, SV, and JH declare that they have no competing interests. SRM serves as a speaker bureau for Bristol-Myers Squibb regarding the use of entecavir for the treatment of chronic hepatitis B.
// Những Người Bình duyệt:
George Y. Wu, MD, PhD
Chief
Hepatology Section, Department of Medicine, University of Connecticut Health Center, Farmington, CT
CÔNG KHAI THÔNG TIN: GYW is on the medical advisory boards of Gilead Sciences and Bristol-Myers Squibb.
Lucieni Oliveira Conterno, MD, PhD
Director
Clinical Epidemiology Unit, Marilia Medical School, Sao Paulo, Brazil CÔNG KHAI THÔNG TIN: LOC declares that she has no competing interests.
Mamun-Al-Mahtab, MB BS, MSc, MD
Chairman
Bangladesh Primary Care Research Network, Dhaka, Bangladesh CÔNG KHAI THÔNG TIN: MAM declares that he has no competing interests.
Xem thêm:
Viêm gan A: Nguyên nhân, chẩn đoán và hướng dẫn điều trị theo BMJ