Tin Tức
Tổng quan về rối loạn nhịp tim chậm: Nguyên nhân, đánh giá, phương pháp hồi sức
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
Nhà thuốc Ngọc Anh – Bài viết Tổng quan về rối loạn nhịp tim chậm: Nguyên nhân, đánh giá, phương pháp hồi sức do Ths.Bs Phạm Hoàng Thiên biên dịch, để tải file PDF bài viết xin vui lòng click vào link ở đây.
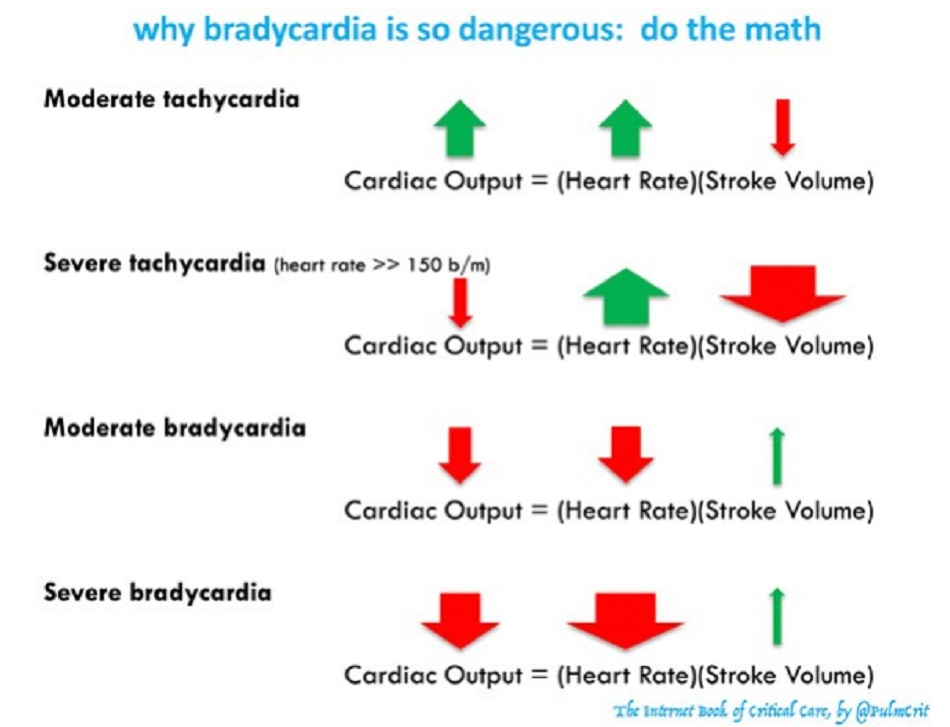
Tại sao nhịp tim chậm là nguy hiểm
Ảnh hưởng của nhịp tim nhanh lên cung lượng tim thường bị ước tính quá mức
- Nhịp tim nhanh có tác động hỗn hợp đến cung lượng tim:
- Tăng nhịp tim có xu hướng làm tăng cung lượng tim.
- Giảm thời gian đổ đầy có xu hướng làm giảm thể tích nhát bóp, làm giảm cung lượng tim.
- Nhịp tim nhanh ở mức độ nhẹ-trung bình nói chung sẽ làm tăng cung lượng tim. Đây là một phản ứng sinh lý bình thường đối với stress. Ảnh hưởng của việc tăng nhịp tim chiếm ưu thế ở đây.
- Nhịp tim nhanh nghiêm trọng (tần số > 150 lần/phút) có thể làm giảm cung lượng tim do tim không có thời gian đổ đầy máu trong thời kỳ tâm trương, gây giảm thể tích nhát bóp.
- Ảnh hưởng có hại của nhịp tim lên cung lượng tim thường bị ước tính quá mức. Ví dụ, nếu một bệnh nhân bị rung nhĩ với tần số tim là 150 lần/phút, không chắc chắn rằng việc chuyển nhịp hoặc kiểm soát tần số sẽ cải thiện cung lượng tim. Thông thường, làm chậm một nhịp tim nhanh mức độ trung bình sẽ khiến tình trạng xấu đi.
Ảnh hưởng của nhịp tim chậm lên cung lượng tim thường được ước tính dưới mức (under-estimated)
- Nhịp tim chậm trực tiếp kéo cung lượng tim xuống, có khả năng gây sốc.
- Làm chậm nhịp tim có thể gây ra một sự gia tăng rất nhỏ trong đổ đầy tâm trương, do đó làm tăng thể tích nhát bóp. Tuy nhiên, yếu tố bù trừ này còn yếu và cực kỳ hạn chế. Ví dụ, nếu nhịp tim giảm một đi một nửa, thì thể tích nhát bóp không thể tăng gấp đôi.
- Trong trường hợp nhịp tim chậm nghiêm trọng, cung lượng tim phải thấp. Đây là một phép toán đơn giản.
- Sốc tim được định nghĩa là cung lượng tim không đủ để hỗ trợ chức năng cơ quan (cung / cầu không phù hợp). Một số bệnh nhân có thể bù trừ cho cung lượng tim thấp mà không bị sốc. Tuy nhiên, với nhịp tim chậm ngày càng nghiêm trọng, thì ngày càng lo ngại về sốc tim..
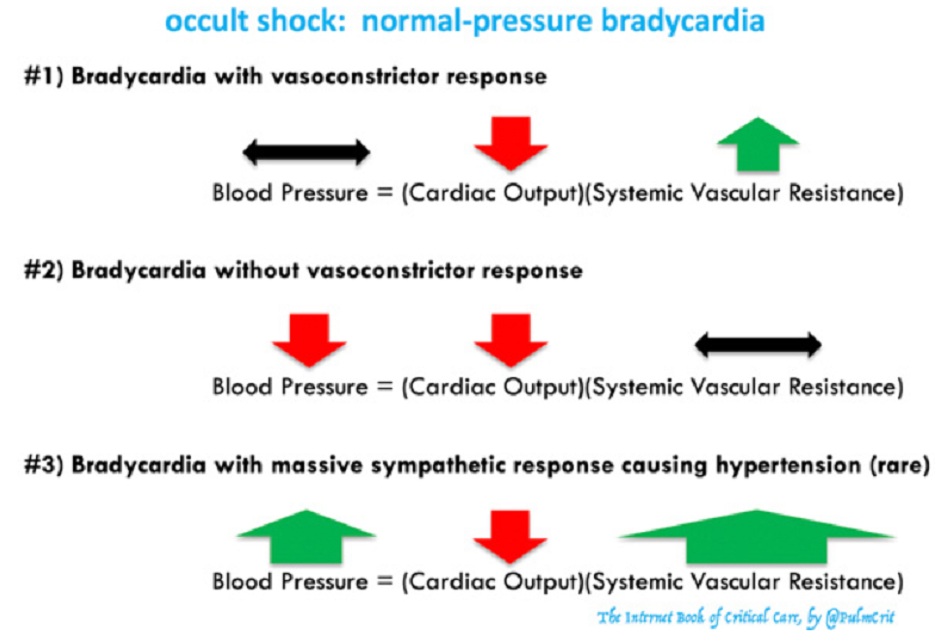
Đừng để bị đánh lừa bởi nhịp tim chậm có huyết áp bình thường
- “Nhịp tim là 25 lần/phút, nhưng huyết áp vẫn ổn… Tôi nghĩ chúng ta có thể đưa cô ấy lên khoa phòng”
- Một số bệnh nhân nhịp tim chậm sẽ duy trì một huyết áp bình thường, do phản ứng giao cảm nội sinh gây co mạch. Mặc dù huyết áp bình thường, những bệnh nhân này vẫn có cung lượng tim thấp và vẫn có thể bị sốc.
- Những bệnh nhân hiếm gặp có thể có nhịp tim chậm nghiêm trọng và tăng huyết áp nặng (# 3 trong hình trên). Tăng huyết áp được gây ra bởi một phản ứng giao cảm rất mạnh, khi cơ thể đấu tranh để bù đắp cho nhịp tim chậm. Tình huống nguy hiểm này phải được quản lý một cách chu đáo, bởi vì phản ứng giao cảm thực sự là giữ cho bệnh nhân sống còn. Việc giãn mạch tích cực để điều trị “cơn tăng huyết áp cấp cứu” sẽ gây suy sụp huyết động. Xử trí nên tập trung vào việc điều chỉnh nhịp tim chậm. Một khi nhịp tim bình thường, phản ứng giao cảm nội sinh sẽ dịu đi và mọi thứ sẽ được giải quyết.
Nhịp tim chậm tiến triển thường là báo hiệu của cái chết
- Nhịp tim chậm nặng dần lên thường được thấy ngay trước khi tử vong (“bệnh nhân đang suy sụp”).
- Nếu nhịp tim của bệnh nhân liên tục giảm trước mắt bạn, đừng chỉ đứng đó – hãy lấy một ít epinephrine. Nhanh lên nào.
- Chẩn đoán phân biệt nhịp tim chậm ở đây rộng hơn bình thường và có thể bao gồm các thực thể như giảm oxy máu nặng và suy thất phải do PE diện rộng. Đánh giá ngay lập tức nên tập trung vào các yếu tố ABC: đường thở, hô hấp và tuần hoàn (siêu âm tim tại giường).
Thêm một lý do để sợ nhịp tim chậm: xoắn đỉnh
- Xoắn đỉnh là một rối loạn nhịp tim phụ thuộc vào thời gian tạm ngừng – có nhiều khả năng xảy ra ở nhịp tim chậm hơn. Hơn nữa, bản thân nhịp tim chậm có thể kéo dài khoảng QT.1 2 Việc để bệnh nhân ở trạng thái nhịp tim chậm nghiêm trọng có thể làm tăng nguy cơ xoắn đỉnh.
Các nguyên nhân phổ biến
Medication/intoxication (Thuốc/độc chất):
- Beta-blocker hoặc calcium-channel blocker.
- Central alpha-2 agonist (ví dụ: clonidine, dexmedetomidine, guanfacine).
- Cholinergic agent.
- Digoxin, các thuốc chống loạn nhịp.
- Propofol infusion syndrome.
- Alpha-blockers (ví dụ: prazosin).
- Ngộ độc benzodiazepines, alcohol, hoặc opioids có thể giảm nhịp tim phần nào, nhưng đây thường không phải là đặc điểm chính của ngộ độc.
Metabolic (Chuyển hóa):
- Tăng kali máu, BRASH syndrome.
- Tăng Magie máu.
- Suy giáp (hôn mê suy giáp).
- Hạ thân nhiệt.
- Hạ glucose máu.
- Giảm oxy máu nghiêm trọng / tăng CO2 / toan máu (nhịp chậm xoang là một con đường phổ biến dẫn đến tử vong do bất kỳ nguyên nhân nào).
MI – nhồi máu cơ tim
Thảm họa thần kinh
- Phản xạ Cushing do tăng áp lực nội so.
- Sốc thần kinh.
Nhiễm trùng:
- Bệnh Lyme, giang mai.
- Viêm nội tâm mạc van động mạch chủ với áp xe vòng (block dẫn truyền).
Sự thoái hóa ở tuổi già của nút xoang hoặc hệ thống dẫn truyền.
Hỏng máy tạo nhịp tim vĩnh viễn.
Đánh giá
Thăm khám lâm sàng
Trọng tâm chính là sự tưới máu đầy đủ.
- Sốc rõ do nhịp tim chậm: tình trạng ý thức bị thay đổi.
- Sốc ẩn giấu do nhịp tim chậm: Huyết áp và tình trạng ý thức không thay đổi, nhưng đầu chi lạnh và lượng nước tiểu kém.
Kiểm tra tim phổi với siêu âm
- Tình trạng thể tích?
- Bằng chứng của nhồi máu cơ tim (ví dụ như bất thường vận động của thành dưới)?
- Bằng chứng về sung huyết phổi (ví dụ: B-lines trên khắp các trường phổi)?
Thăm khám thần kinh/ngộ độc
- Bằng chứng về tăng áp lực nội sọ (ví dụ như lơ mơ – stupor, đường kính dây thần kinh thị lớn – widened optic nerve sheath)?
- Đồng tử hình đinh ghim có thể gợi ý ngộ độc (ví dụ như clonidine hoặc cholinergic)
ECG: Tập trung vào 3 điểm
- Chẩn đoán nhịp tim (ví dụ: nhịp tim chậm xoang vs block tim)
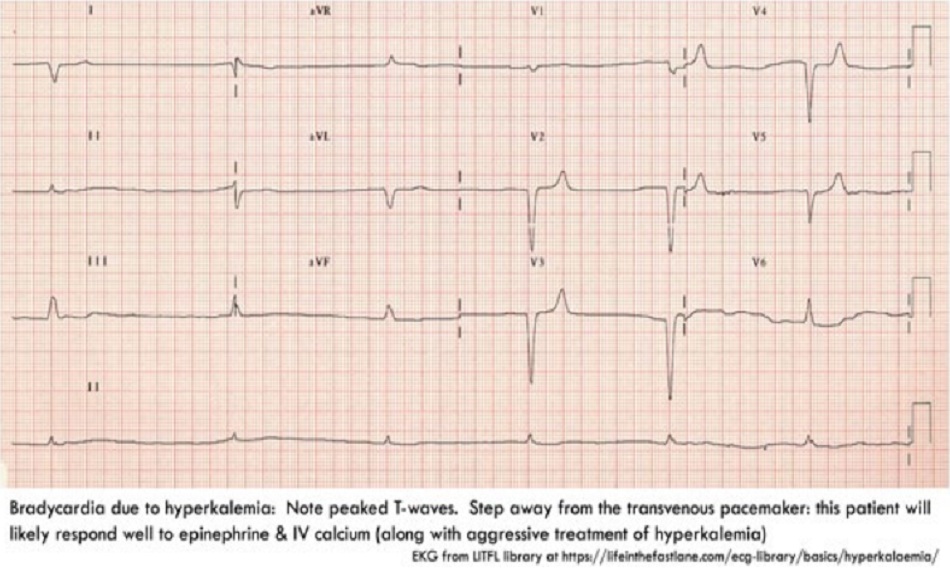
- Các dấu hiệu của tăng kali máu (ví dụ như sóng T cao nhọn)
- Các dấu hiệu của thiếu máu cục bộ
Xem xét các thuốc đang sử dụng
Danh sách thuốc đang sử dụng?
Những thay đổi thuốc gần đây, bao gồm cả việc thay đổi liều lượng?
- Một số loại thuốc có thể gây ra nhịp tim chậm (ví dụ: donepezil, tizanadine).3 Vì vậy, nếu bệnh nhân mới bắt đầu dùng một thuốc nào đó, hãy kiểm tra xem nó có thể gây ra nhịp tim chậm hay không.
- Ngay cả thuốc nhỏ mắt có đặc tính giống giao cảm cũng có thể đủ gây nhịp tim chậm ở bệnh nhân cao tuổi.4
Tương tác?
Thuốc thải qua thận cộng với tổn thương thận cấp tính?
Các xét nghiệm
- Glucose mao mạch nếu tình trạng ý thức thay đổi
- Sinh hóa bao gồm Ca & Mg
- Troponin, nếu nghi ngờ MI từ bệnh sử/ECG
- Nồng độ Digoxin, đối với bệnh nhân đang dùng digoxin
- Cân nhắc kiểm tra TSH, huyết thanh Lyme.
Tổng quan hồi sức
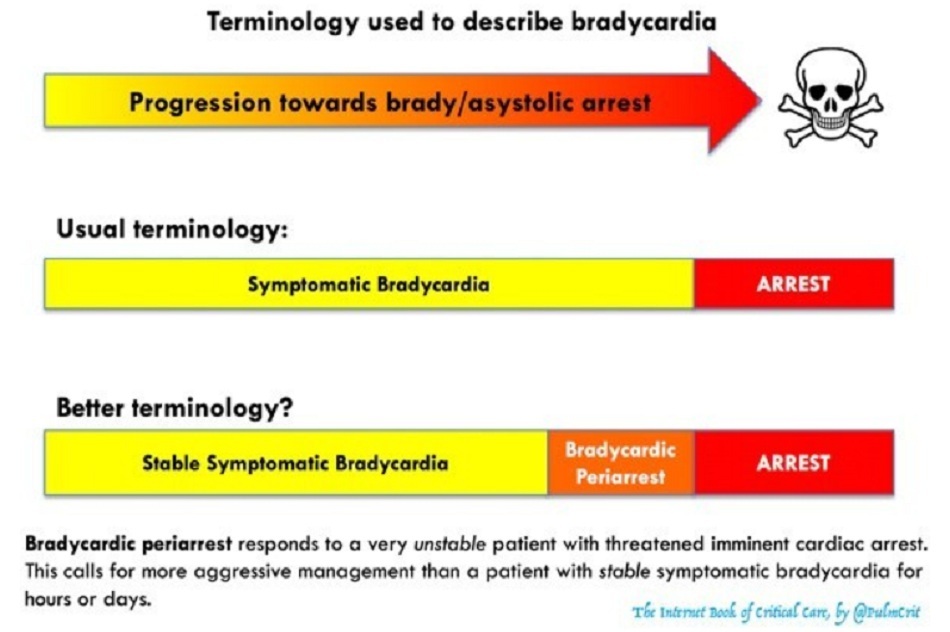
Tổng quan: phác đồ xử trí nhịp chậm dọa ngừng tim
Nhịp chậm dọa ngừng tim có thể được định nghĩa một cách lỏng lẻo là nhịp tim chậm nghiêm trọng với biểu hiện sốc rõ rệt và lo ngại về việc ngừng tim ngay lập tức. Phác đồ dưới đây cho thấy một chiến lược tích cực tối đa được thiết kế để ngăn chặn tình trạng xấu dẫn đến ngừng tim.
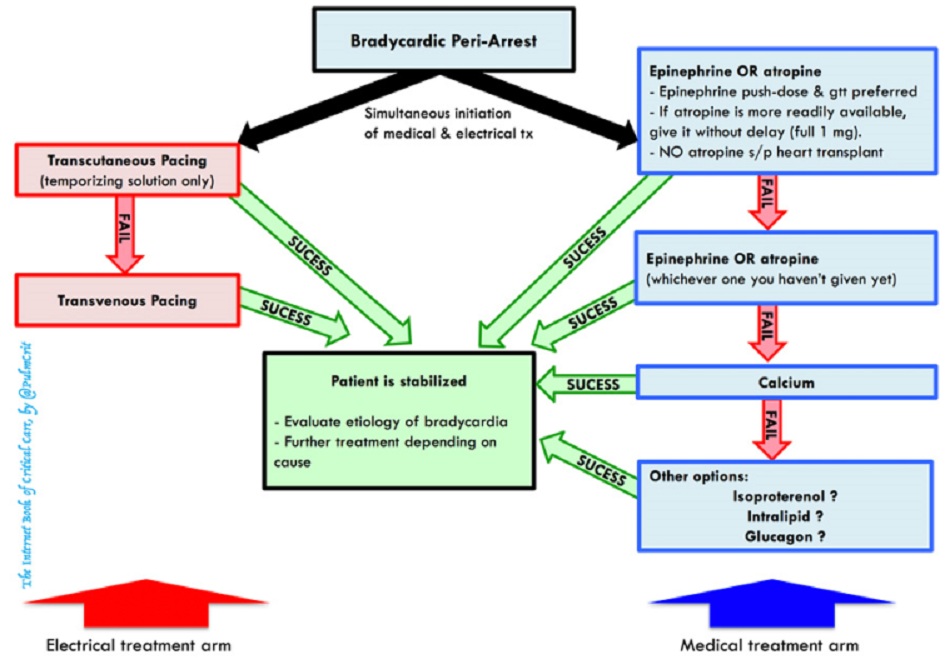
- Có hai “nhánh” trị liệu: điện & thuốc.
- Thật khó để dự đoán bệnh nhân nào sẽ đáp ứng tốt nhất với liệu pháp thuốc hay liệu pháp điện.
- Tiến hành đồng thời cả hai nhánh trị liệu càng nhanh càng tốt cho đến khi bệnh nhân ổn định.
Đối với những bệnh nhân có dấu hiệu nhẹ của giảm tưới máu cơ quan (ví dụ huyết áp bình thường nhưng lượng nước tiểu kém), thì cách tiếp cận dần dần và từng bước có thể là thích hợp nhất. Ví dụ, chỉ cần bắt đầu truyền epinephrine thường sẽ cải thiện nhịp tim và tưới máu.
Hồi sức bằng thuốc
Atropine
Những vấn đề với atropine
- Ở liều thấp, atropine có thể gây ra nhịp tim chậm nghịch lý.5 6 7 8
- Atropine hoạt động bằng cách ức chế thần kinh phế vị, vì vậy nó chỉ có hiệu quả đối với nhịp tim chậm qua trung gian của trương lực phế vị quá mức. Có thể đoán trước là nó sẽ thất bại trong các trường hợp block AV cao độ.
- Chống chỉ định ở những bệnh nhân đã được cấy ghép tim vì atropine có thể thúc đẩy vô tâm thu.5
- Atropine có thể ổn định bệnh nhân trong 30-60 phút, nhưng sau đó sẽ mất tác dụng. Điều này ban đầu có thể làm cho bệnh nhân có vẻ ổn định, chỉ là sau đó sẽ xấu đi (một khi mọi người không còn chú ý nhiều đến bệnh nhân nữa).
Chiến lược khi nào dùng atropine?
Nếu atropine là loại thuốc có sẵn ngay lập tức nhất, thì hãy cho nó. Ngoài ra, nếu bạn có thể sử dụng epinephrine ngay lập tức, thì có thể sẽ hiệu quả hơn nếu chuyển thẳng sang dùng epinephrine.
- Atropine theo truyền thống là thuốc hàng đầu. Tuy nhiên, đối với những bệnh nhân rất không ổn định, epinephrine có hiệu quả đáng tin cậy hơn và có thể thích hợp hơn.
Bắt đầu với atropine 1mg, các liều bổ sung có thể được đưa ra với liều tối đa là ~ 3 mg.
Nhìn chung, chỉ có ~ 25% bệnh nhân đáp ứng hoàn toàn với atropine, vì vậy đừng trì hoãn các liệu pháp khác trong khi chờ atropine phát huy tác dụng.
- Đừng cho atropine rồi ngồi lại và hy vọng rằng nó sẽ khắc phục được mọi thứ. Cho atropine đồng thời chuẩn bị epinephrine và tạo nhịp qua da, với dự tính khả năng rằng atropine thường sẽ thất bại.
Epinephrine
Những ưu điểm của epinephrine
Có sẵn ở mọi nơi, có thể lấy nhanh chóng.
Không giống như atropine, epinephrine kích thích toàn bộ cơ tim. Điều này cho thấy epinephrine có một phổ hiệu quả rộng hơn cho các cơ chế nhịp tim chậm khác nhau.11
- Epinephrine là piperacillin-tazobactam của loạn nhịp chậm.
- An toàn khi tiêm truyền ngoại vi (không phải lo lắng về tình trạng thoát mạch extravasation, bạn không cần phải đặt một đường truyền trung tâm).
Chiến lược sử dụng epinephrine
Bolus cho bệnh nhân dọa ngừng tim
- Đối với bệnh nhân sắp ngừng tim, bolus với liều ~ 20-50 mcg epinephrine. o Liều bolus sẽ ổn định bệnh nhân trong vài phút, nhưng đây chỉ là cầu nối tạm thời đến epinephrine truyền liên tục.
Truyền epinephrine
- Liều thông thường là 2-10 mcg / phút (nhưng không có giới hạn trên cố định ở bệnh nhân nguy kịch).
- Chiến lược dùng thuốc tùy thuộc vào mức độ không ổn định của bệnh nhân. Đối với những bệnh nhân không ổn định nặng hơn, bắt đầu ở liều cao và giảm dần khi bệnh nhân đáp ứng. Đối với những bệnh nhân còn khá ổn định, bắt đầu ở liều thấp và tăng dần.
Tìm ra cách đạt được điều này tại đơn vị của bạn:
- Nếu bạn có ngay các túi epinephrine đã pha sẵn, hãy biết cách sử dụng chúng (biết nồng độ của chúng và cần bao nhiêu ml để cung cấp epinephrine liều push-dose).
- Nếu bạn không có ngay các túi epinephrine pha sẵn, thì hãy đọc tiếp…
Tạo ra & dùng “dirty epi drip” (tạm dịch: cách pha truyền epinephrine không chính quy)
Pha một túi epinephrine rất dễ dàng. Điều này thường được gọi là “dirty epi drip”,
nhưng nếu được thực hiện đúng cách thì đó là một cách an toàn và chính xác để cung
cấp epinephrine.
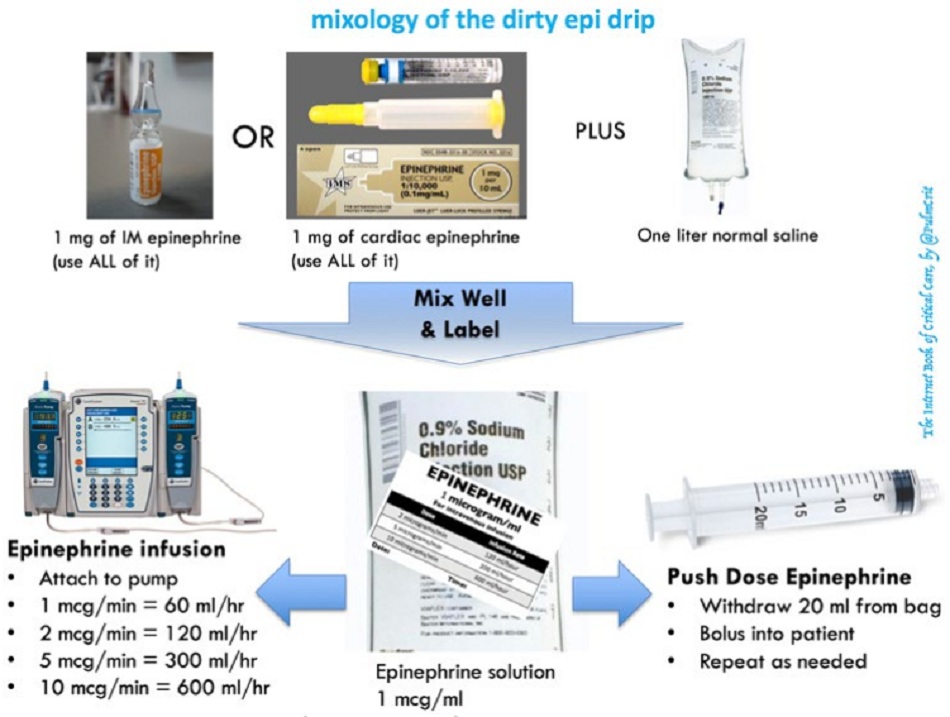
Bước #1: tạo túi chứa epinephrine
- Tiêm 1mg epinephrine vào một lít nước muối sinh lý bình thường. Có thể lấy một miligam epinephrine từ một ống tiêm epinephrine tim nguyên vẹn (1: 10.000) hoặc một lọ epinephrine IM nguyên vẹn (1: 1000).
- Xịt/bơm xung quanh túi để trộn đều.
- Dán nhãn cho túi. Cách tốt nhất để làm điều này là sử dụng nhãn in sẵn bao gồm hướng dẫn định liều như hình dưới đây. Nhưng rõ ràng điều này không cần thiết.
Bước #2: epinephrine liều push dose
- Đối với một bệnh nhân sắp ngừng tim, bạn sẽ muốn bolus những liều nhỏ epinephrine cho đến khi bệnh nhân ổn định.
- Hút đầy một ống tiêm 20cc rỗng với epinephrine pha loãng (1 mcg / ml) từ túi một lít của bạn.
- Bolus 20 ml dung dịch này, sẽ cung cấp một lượng 20 mcg epinephrine.
- Hút đầy ống tiêm 20ml của bạn lần nữa và bolus lặp lại nếu cần.
- Epinephrine liều push-dose là một giải pháp tạm thời. Ngay sau khi bệnh nhân ổn định, bắt đầu truyền epinephrine.
Bước #3: truyền epinephrine
Gắn túi epinephrine của bạn vào một máy bơm tiêm điện và đặt tốc độ. Ví dụ:
- Truyền với tốc độ 60ml / giờ để đạt được 1 mcg / phút o Truyền với tốc độ 240ml / giờ để đạt được 4 mcg / phút o Truyền với tốc độ 600ml / giờ để đạt được 10 mcg / phút
Những ưu điểm của chiến lược “dirty epi” bolus & drip:
Tương đối dễ dàng. Miễn là bạn trộn đều và dán nhãn lên túi, thì sẽ rất khó để mắc lỗi liều lượng:
- Bất kể bạn sử dụng loại epinephrine nào, bạn cũng sẽ ổn (1: 1.000 hoặc 1: J0.000 đều có tác dụng).
- về mặt thực tế, không thể bolus một liều epinephrine gây chết người sau khi nó đã được pha loãng thành 1 mcg / ml (bạn sẽ cần một ống tiêm > 100ml, mà loại ống tiêm này không tồn tại).
- Ngay cả khi bạn cho chảy nhanh túi dịch chứa epinephrine, bạn sẽ chỉ cung cấp khoảng ~ 30 mcg / phút epinephrine – vì vậy một lần nữa, về cơ bản là không thể cung cấp một liều epinephrine cao đến mức gây tử vong..
Khuyến khích chuyển đổi nhanh chóng từ epinephrine liều push-dose sang epinephrine truyền (đến cuối cùng thì đây là một chiến lược an toàn hơn và có kiểm soát hơn).
Cách tiếp cận khả thi khi thiếu epinephrine:
- Dễ dàng thực hiện với epinephrine 1: 1000, nếu khoa của bạn hết epinephrine 1: 10.000.
- Một ống epinephrine có thể được sử dụng cho cả pushes & drip, duy trì.
Calcium
Cùng với epinephrine, canxi là một loại thuốc thường được sử dụng dưới mức (under-utilized) trong rối loạn nhịp chậm. Canxi IV có khả năng hiệu quả đối với nhiều nguyên nhân khác nhau được liệt kê dưới đây. Canxi khá an toàn (trừ khi nó thoát mạch), vì vậy khi các liệu pháp khác thất bại, bạn nên thử dùng một ít canxi.
Các rối loạn nhịp chậm đáp ứng với calcium:
- Tăng kali máu
- Hạ calci máu
- Tăng magnesi máu
- Thuốc chẹn kênh canxi
- Thuốc chẹn beta (có thể hiệu quả)
Liều dùng
- Nhịp tim chậm không rõ nguyên nhân: Thử một liều canxi (1 gam canxi clorua hoặc 3 gam canxi gluconat).
- Tăng kali máu đã biết hoặc nghi ngờ: Bắt đầu với 1 gam canxi clorua hoặc 3 gam canxi gluconat. Nếu không hiệu quả và bệnh nhân không ổn định một cách nguy hiểm, hãy cân nhắc bổ sung canxi. Liều tối đa của canxi là không xác định trong tình huống này. Theo dõi xét nghiệm sinh hóa tại giường bằng iSTAT có thể hữu ích, giúp phát hiện tình trạng tăng calci máu vừa phải (ví dụ mức canxi ion là 2¬3 mM).
Các thuốc khác
Dobutamine
Dobutamine chủ yếu là chất chủ vận beta, có hoạt tính alpha-adrenergic rất yếu. Không giống như epinephrine, dobutamine có xu hướng gây giãn mạch toàn thân:
- Dobutamine có thể hoàn hảo cho bệnh nhân nhịp tim chậm và huyết áp bình thường / tăng cao, khi bạn đang cố gắng tăng cung lượng tim (mà không làm tăng huyết áp).
- Dobutamine không phải là một lựa chọn tốt cho bệnh nhân nguy kịch, bị tụt huyết áp. Nếu dobutamine không làm tăng nhịp tim được thì nó có thể chỉ hoạt động như một loại thuốc giãn mạch, và do đó gây ra tình trạng hạ huyết áp trầm trọng hơn.
Dobutamine có thể không hoàn toàn an toàn khi tiêm truyền ngoại vi như epinephrine. Nếu bạn đang sử dụng dobutamine để truyền dịch ngoại vi kéo dài, hãy theo dõi kỹ vị trí đó và tránh tiêm truyền ở tĩnh mạch bàn tay / cổ tay.
Isoproterenol
Đây là một loại thuốc tuyệt vời cho nhịp tim chậm nếu bạn có thể hiểu/kiểm soát được nó.
Isoproterenol là một chất chủ vận beta thuần khiết, an toàn khi tiêm truyền ngoại vi. Isoproterenol dường như mạnh hơn epinephrine một chút (dường như có một số bệnh nhân không đáp ứng với epinephrine sẽ đáp ứng với isoproterenol).
Hạn chế chính của isoproterenol là về mặt kinh tế và sự sẵn có. Isoproterenol rất đắt ở Hoa Kỳ (một lần truyền có thể tốn vài nghìn đô la). Nhiều bệnh viện không có nó. Ngay cả khi bệnh viện của bạn có nó, thường sẽ mất thời gian để lấy nó từ nhà thuốc. Tìm hiểu thêm thông tin về isoproterenol từ Dược sĩ Scott Dietrich ở đây here.
Dopamine
Dopamine có một hồ sơ ghi chép dài về việc sử dụng trong rối loạn nhịp tim chậm có triệu chứng. Ưu điểm chính của dopamine là ổn định ở nhiệt độ phòng, vì vậy nó có thể có sẵn nhiều hơn trong các túi đã pha sẵn (ví dụ như trong xe cứu thương).
Nhược điểm của dopamine so với epinephrine:
- Dopamine có thể gây hoại tử da khi tiêm truyền kéo dài.
- Ở liều cao, dopamine có thể hoạt động chủ yếu như một chất co mạch. Điều này có thể là không mong muốn nếu bạn chủ yếu mong đợi vào chronotropy.Nếu dopamine là tác nhân sẵn có nhất, thì hãy sử dụng nó. Khi bạn có thời gian, hãy cân nhắc chuyển sang truyền epinephrine.
Điều trị độc chất nâng cao
Local Anesthesia Systemic Toxicity (LAST)
- Nghi ngờ ở bất kỳ bệnh nhân nhịp tim chậm nào khi đang truyền lidocain hoặc gần đây được điều trị bằng thuốc phong bế thần kinh.
- Liệu pháp hàng đầu là nhũ tương lipid.
Ngộ độc thuốc chẹn beta và / hoặc thuốc chẹn kênh canxi
- Các phương pháp điều trị độc chất nâng cao chủ yếu hữu ích cho những bệnh nhân bị quá liều nghiêm trọng. Tuy nhiên, những liệu pháp này cũng có thể được xem xét đối với những bệnh nhân bị nhịp tim chậm do rủi ro/tai biến của điều trị.
- Điều trị có thể bao gồm insulin liều cao, glucagon hoặc nhũ tương lipid.
Hồi sức bằng điện
Máy tạo nhịp qua da
Tạo nhịp qua da thường là chiến lược nhanh nhất để tăng nhịp tim. Ngay cả khi nó không tạo được nhịp, sự khó chịu có thể đủ để kích hoạt phản ứng giao cảm giúp bệnh nhân sống sót. Dù bằng cách nào, đây cũng là một biện pháp tạm thời cho đến khi có thể có liệu pháp điều trị ổn định dứt khoát hơn (ví dụ: máy tạo nhịp đường tĩnh mạch).
Cài đặt pad
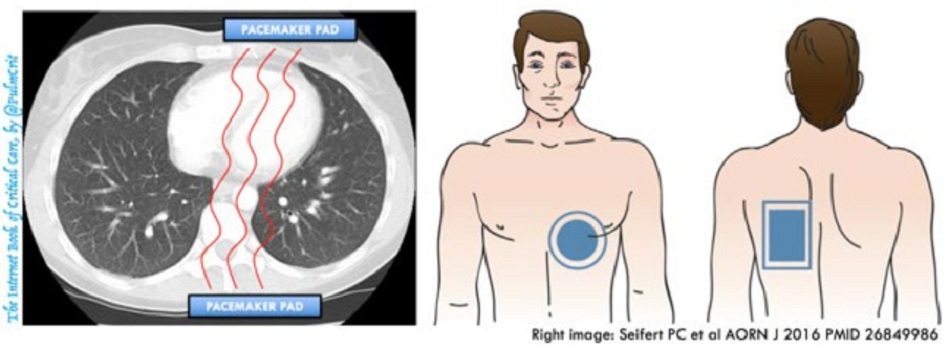
Khí là chất dẫn điện kém, vì vậy việc đặt các pad đè lên trên vùng phổi là một chiến lược tồi.
Vị trí đặt pad trước-sau có thể được ưu tiên hơn (hình trên)12 13
- Pad trước nằm ở bên trái phần dưới của xương ức, phủ lên “cửa sổ cạnh ức trái” của tim. Dựa trên kinh nghiệm siêu âm tim, đây là nơi tiếp xúc đáng tin cậy nhất giữa tim và mô mềm của lồng ngực.
Điện thế
Nếu bệnh nhân nguy kịch, hãy bắt đầu ở mức điện thế tối đa và giảm dần sau khi bệnh nhân đã ổn định.
Nếu bệnh nhân ổn định, hãy bắt đầu ở mức điện thế thấp và tăng dần.
- Nếu bệnh nhân vẫn ổn, thì có thể bạn sẽ không thực sự muốn thực hiện tạo nhịp qua da. Tuy nhiên, nó có thể hữu ích để xác định xem bệnh nhân có đáp ứng với tạo nhịp qua da hay không. Việc chứng minh rằng máy tạo nhịp tim qua da sẽ tạo được nhịp tim có thể giúp bạn quyết định liệu việc đặt máy tạo nhịp qua đường tĩnh mạch có cần thiết cho một bệnh nhân ở cận kề nguy hiểm (borderline) hay không.
Tiếp tục tăng mức điện thế lên 10-20 mA trên mức năng lượng tối thiểu cần thiết để tạo được nhịp.
Thường cần ~ 40-80 mA để đạt được tạo nhịp (có thể cao hơn ở bệnh nhân béo phì hoặc bệnh phổi tắc nghẽn).14
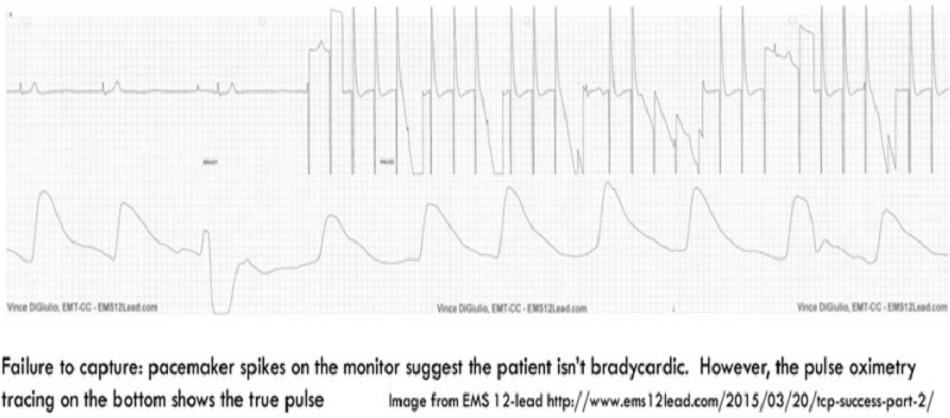
Nhận ra nhịp giả
Nhịp giả là khi máy tạo nhịp tim không tạo được nhịp cho cơ tim, nhưng monitor hiển thị một nhịp tim ngang bằng với máy tạo nhịp qua da. Điều này mang lại cảm giác an toàn giả tạo vì monitor trông rất tuyệt.
Luôn xác nhận rằng máy tạo nhịp tim đang tạo được nhịp tim hiệu quả thông qua một trong các phương pháp sau:
- Dạng sóng đo oxy xung mạch (pulse oximetry waveform) cho thấy mạch trùng khớp với máy tạo nhịp tim (hình trên)
- Siêu âm tim tại giường xác nhận co cơ tim theo nhịp
- Nhịp mạch đập, tốt nhất là cách xa lồng ngực (ví dụ: nhịp đập ở đùi hoặc mu bàn chân, để tránh bị đánh lừa bởi sự giật của cơ ngực)
Gây mê/an thần?
Có thể bị hạn chế bởi sự không ổn định của bệnh nhân. Fentanyl và/hoặc ketamine liều thấp có lẽ là hợp lý.
An thần sâu & đặt nội khí quản cho phép chịu đựng tạo nhịp qua da là một cách tiếp cận phổ biến, nhưng có lẽ không phải là tốt nhất. Sự không ổn định gây ra bởi thuốc an thần và đặt nội khí quản có thể làm mất đi lợi ích của việc tạo nhịp qua da. Ngoài ra, nếu bệnh nhân bị căng phồng quá mức (hyperinflated) khi máy thở, điều này về mặt lý thuyết có thể dẫn đến việc mất sự tạo nhịp tim từ máy tạo nhịp qua da..
Tạo nhịp qua đường tĩnh mạch
Tạo nhịp qua đường tĩnh mạch là chiến lược xâm lấn nhất, nhưng cũng hiệu quả nhất (với tỷ lệ thành công > 95%).15 Các chỉ định đại khái như sau:
- Nhịp tim chậm không ổn định không đáp ứng với các biện pháp can thiệp khác (ví dụ: epinephrine).
- Block AV cao độ khiến bệnh nhân có nguy cơ suy thoái liên tục (ví dụ Mobitz II, block tim mức độ 3 với nhịp thoát phức bộ rộng).
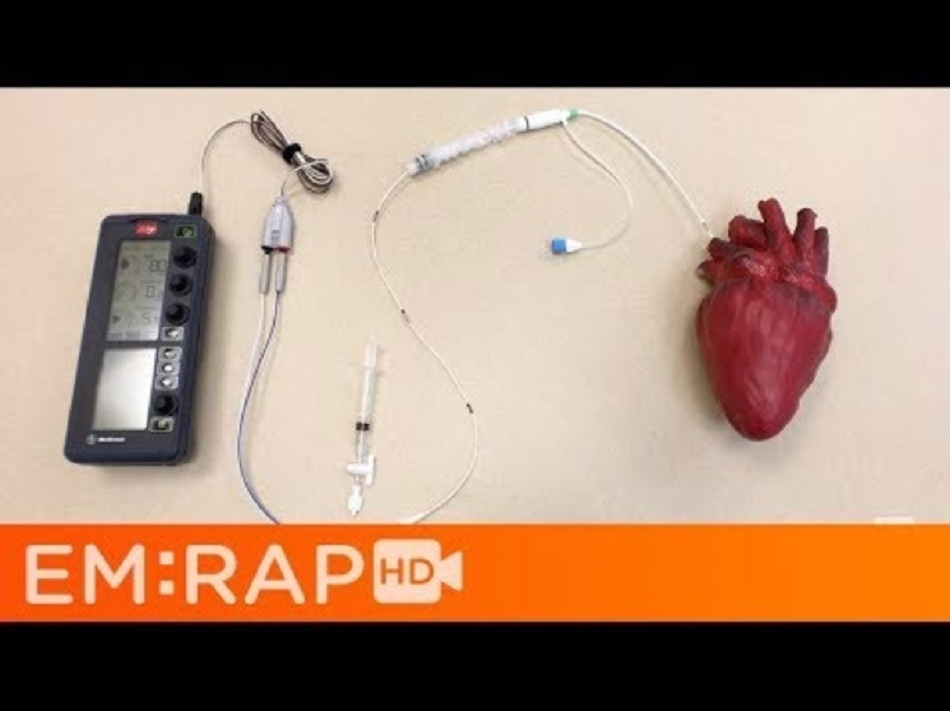
Có một bộ dụng cụ, biết bộ dụng cụ của bạn, yêu bộ dụng cụ của bạn
Đơn vị của bạn phải có mọi thứ cần thiết cho máy tạo nhịp đường tĩnh mạch ở một vị trí cụ thể (ví dụ: một hộp hoặc ngăn kéo lớn trong xe đẩy hồi sức). Bao gồm bản thân máy tạo nhịp tim đường tĩnh mạch, sheath tĩnh mạch, máy phát điện tạo nhịp tim/máy phát nhịp (pacing generator), các dây wire và adapter pins.
Sử dụng sheath tĩnh mạch có kích thước thích hợp cho máy tạo nhịp tim:
- Nếu bạn yêu cầu một sheath tĩnh mạch ngẫu nhiên, bạn có thể sẽ được cấp một sheath 8,5 French được thiết kế để phù hợp một catheter Swan-Ganz. Sheath này không thể được sử dụng để đặt dây wire máy tạo nhịp tim, nó sẽ quá lớn (dẫn đến rò rỉ máu ra khỏi sheath hoặc không khí bị tắc nghẽn trong sheath). Pacer sheath sẽ nhỏ hơn.
Điểm mấu chốt của quy trình này là làm quen với bộ dụng cụ tạo nhịp có sẵn trong đơn vị của bạn. Tốt nhất là nên có sẵn một bộ dụng cụ không tiệt trùng (non-sterile) cho mục đích thực hành. Trong trường hợp cấp cứu, trí nhớ về cách lắp ráp tất cả các bộ phận sẽ là vô giá.
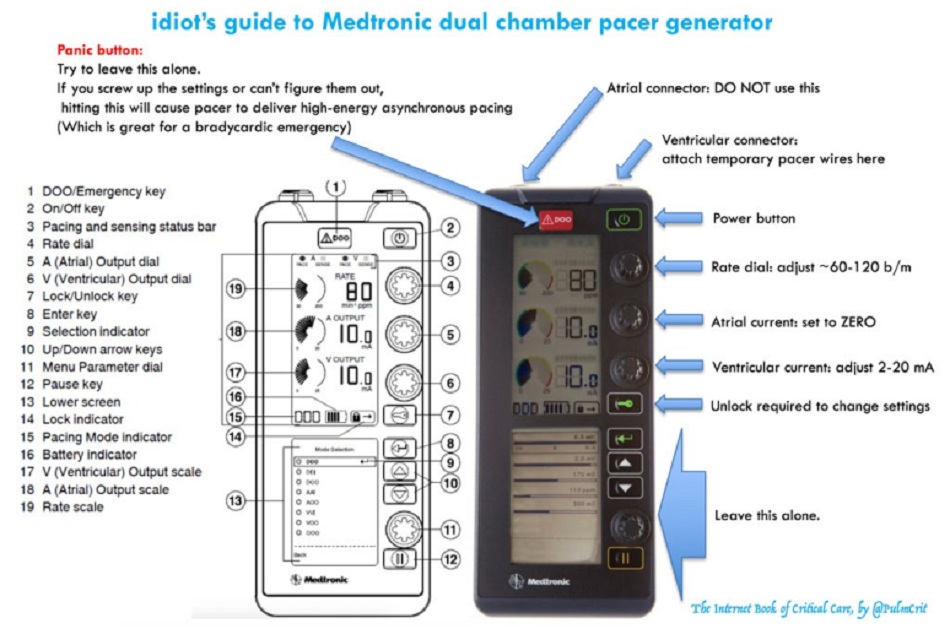
Cũng biết cách làm việc của máy phát nhịp. Máy phát nhịp kỹ thuật số mới hơn được thiết kế cho các nhà điện sinh lý, vì vậy chúng có thể gây nhầm lẫn. Đảm bảo rằng bạn đã quen thuộc với các thiết bị của bệnh viện..
Vị trí đặt máy
Nói chung, các vị trí cho phép máy tạo nhịp tim trôi nổi (floating) dễ dàng nhất là:
- 1st choice: Tĩnh mạch cảnh trong phải (straight shot into the RV – đi thẳng vào trong thất phải)
- 2nd choice: tĩnh mạch dưới đòn trái (smooth arc through the larger vessels into the heart – đi vòng 1 cách uyển chuyển qua các mạch máu lớn vào trong tim)
Điện thể thích hợp trong khi thả nổi (floating) dây wire
Tùy thuộc vào mức độ không ổn định của bệnh nhân, có hai chiến lược để đặt máy tạo nhịp tim tạm thời:
Honey Badger Mode: Khi bạn đang thả nổi dây wire, hãy tăng dòng điện lên 20 mA. Điều này sẽ tạo nhịp tim nhanh nhất có thể, điều này tốt hơn nếu bệnh nhân đang hấp hối. Vấn đề là sự tạo nhịp có thể xảy ra khi dây wire ở trong tâm nhĩ, vì vậy cách tiếp cận này không phải lúc nào cũng dẫn đến vị trí lý tưởng của máy tạo nhịp tim tạm thời. Mục đích ở đây là ổn định bệnh nhân càng sớm càng tốt, bạn có thể mày mò đặt máy tạo nhịp tim sau đó.
Kỹ thuật thông thường: Đối với bệnh nhân không hấp hối, thả nổi máy tạo nhịp tim với biên độ thấp hơn (ví dụ: 5 mA). Điều này thường sẽ không tạo nhịp được cho cơ tim cho đến khi bạn gần đến cơ tim thất phải. Chiến lược này tốt hơn để tối ưu hóa vị trí lý tưởng của máy tạo nhịp tim. Sau khi đã tạo nhịp được, hãy tiến thêm thêm vài mm và làm xẹp quả bóng balloon – điều này thường sẽ giúp đặt nó ở vị trí tối ưu, nằm dựa vào tâm thất phải.
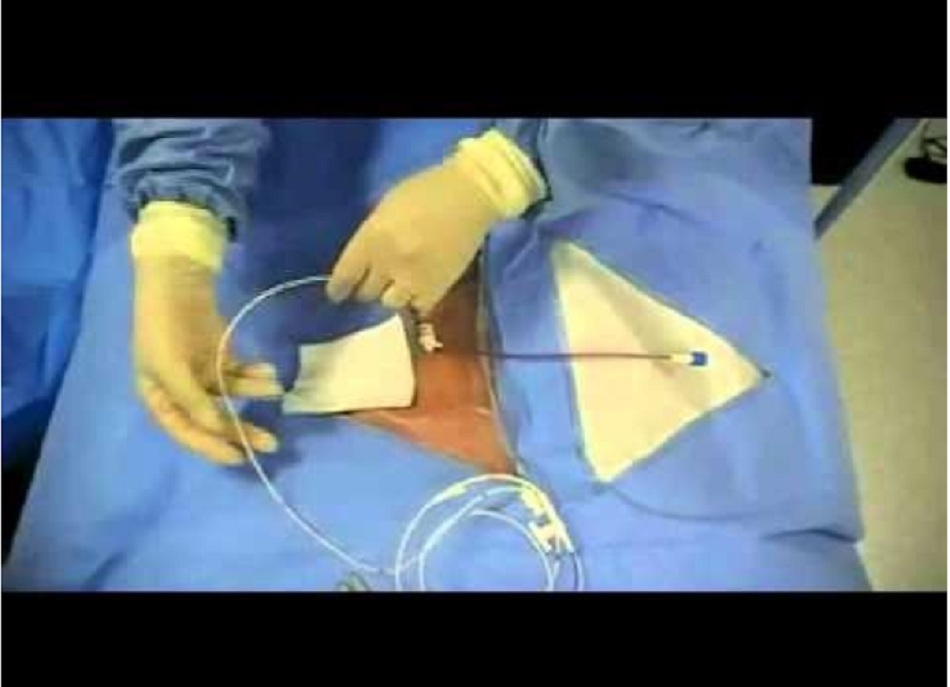
Siêu âm hướng dẫn
Không cần thiết, nhưng có thể hữu ích. Cần một bác sĩ thứ hai tiếp cận dưới tấm drap vô trùng và định vị bằng siêu âm. Lý tưởng nhất là bác sĩ này nên có kỹ năng siêu âm.
Tầm nhìn bốn buồng (ví dụ: 4 buồng dưới sườn) nói chung là tốt nhất, điều này có thể cho phép nhìn thấy dây dẫn đang đi vào tâm nhĩ và tâm thất phải.
Giá trị tiềm năng:
- Nếu bạn đưa dây pacer wire vào hơn ~ 30cm và không thấy nó ở tâm nhĩ phải, thì có lẽ dây đã đi thẳng vào tĩnh mạch chủ dưới. Làm xẹp bóng balloon, kéo lùi lại ~ 15 cm và thử thả nổi một lần nữa.
- Siêu âm cho phép tinh chỉnh quy trình đặt. Ví dụ, khi bạn đã đi thông qua van ba lá, bạn có thể đi chậm lại – bạn chỉ còn vài cm nữa là đến.
- Nếu bạn thấy dây dẫn trong tâm thất phải nhưng không bắt tạo được nhịp thì có thể có vấn đề với hộp tạo nhịp (pacer box). Đảm bảo rằng tất cả các dây wire được kết nối chính xác và cài đặt chính xác.
Các biến chứng
Hầu hết các biến chứng liên quan đến việc đặt sheath pacemaker trong tĩnh mạch (ví dụ như tràn khí màng phổi hoặc chảy máu).
Nguy cơ tràn máu màng tim rất nhỏ, nhưng có (< 0,6%).16
- Điều này có thể giảm bớt bằng cách đặt dây wire cẩn thận với hướng dẫn của siêu âm.
- Nếu bệnh nhân xấu đi sau khi đặt máy tạo nhịp tim tạm thời đường tĩnh mạch, siêu âm nên được thực hiện để loại trừ tràn máu màng tim.
Dual pacing là một chiến lược dự phòng
Một số bệnh nhân sẽ hoàn toàn phụ thuộc vào máy tạo nhịp tim (họ không có nhịp nội tại nào cả). Điều này khá đáng sợ, vì nếu quá trình tạo nhịp điện không thành công dù chỉ một phút, bệnh nhân sẽ bị ngừng tim. Máy tạo nhịp tạm thời đường tĩnh mạch đôi khi bị hỏng, vì vậy đây có thể là một vấn đề thực sự. Để tránh bệnh nhân tử vong nếu máy tạo nhịp tim tạm thời đường tĩnh mạch của họ không hoạt động, có thể sử dụng dual pacing:
Bệnh nhân được gắn đồng thời cả máy tạo nhịp đường tĩnh mạch và máy tạo nhịp qua da.
Máy tạo nhịp đường tĩnh mạch được điều chỉnh theo cách thông thường:
- Đặt tần số ở mức hợp lý (ví dụ: 60-80 lần/phút, hoặc có thể cao hơn nếu bệnh nhân bị sốc).
- Đây phải là máy tạo nhịp điều khiển nhịp tim của bệnh nhân.
Máy tạo nhịp tim qua da được gắn và bật, với các cài đặt sau:
- Đặt tần số 20 lần/phút thấp hơn máy tạo nhịp đường tĩnh mạch (ví dụ: 40 lần/phút).
- Đặt điện thế ở mức đủ cao để tạo được nhịp cho cơ tim.
- Tối ưu hóa vị trí đặt miếng pad.
- Máy tạo nhịp tim này lý tưởng là không nên làm gì.
Máy tạo nhịp qua da được sử dụng ở đây hoàn toàn như một thiết bị dự phòng. Nếu máy tạo nhịp đường tĩnh mạch bị trục trặc, máy tạo nhịp qua da sẽ tạo nhịp mà không bị mất nhịp nào. Tất nhiên, điều này sẽ gây đau đớn cho bệnh nhân (vì đột nhiên họ sẽ bị sốc điện). Tuy nhiên, tạo nhịp qua da thích hợp hơn khi ngừng tim đột ngột.
Phác đồ
Tiếp cận bệnh nhân nhịp chậm dọa ngừng tim
Bảng cheat máy tạo nhịp tim
Cạm bẫy
- Đừng cho rằng bởi vì huyết áp bình thường, thì bệnh nhân sẽ tưới máu đầy đủ và ổn định. Một số bệnh nhân co mạch và duy trì huyết áp bình thường, dù vậy đã có tình trạng giảm tưới máu cơ quan.
- Đối với một bệnh nhân không ổn định, đừng cố chấp vào bất kỳ can thiệp cụ thể nào. Tiếp tục thực hiện một loạt các liệu pháp điện và cơ học cho đến khi có tác dụng (hình bên dưới).
- Đừng ngại sử dụng epinephrine liều push dose và truyền epinephrine ngoại vi cho bệnh nhân không ổn định.
- Đừng quên khai thác tốt bệnh sử/tiền sử dùng thuốc, tập trung vào những lần thay đổi thuốc gần đây và những loại thuốc có thể tích tụ trong suy giảm chức năng thận (ví dụ: digoxin, atenolol).
- Đừng để bị lừa bởi nhịp giả của máy tạo nhịp qua da. Thực tế là lồng ngực co giật và monitor hiển thị nhịp tim bình thường không có ý nghĩa gì cả – vẫn có khả năng là cơ tim vẫn chưa được tạo nhịp.
- Hãy nhớ rằng nhịp tim chậm có thể do nhồi máu cơ tim và các loại ngộ độc khác nhau – vì vậy việc điều chỉnh nhịp tim có thể không đủ để ổn định bệnh nhân.
- Hãy thử tưởng tượng từng phần của bộ dụng cụ máy tạo nhịp tim qua đường tĩnh mạch của bạn và cách chúng được lắp ráp. Nếu bạn không thể làm điều này, bạn cần phải thực hành với bộ dụng cụ. Tình trạng ngừng thủ thuật phổ biến nhất là do không quen thuộc với bộ dụng cụ và máy phát nhịp tim.
Mạch chậm, suy thận, block nút nhĩ thất, sốc và tăng Kali máu: Một hội chứng quan trọng cần phát hiện
(Tác giả Chui King Wong, Mohd Johar Jaafar – Dịch bởi BS. Thanh Sơn)
Tóm tắt
Hội chứng BRASH là một hội chứng đặc trưng bởi mạch chậm, suy thận, sử dụng thuốc chẹn nút nhĩ thất (AV), sốc và tăng kali máu (BRASH). Nó thường thấy hơn ở các bệnh nhân có nhiều bệnh đồng mắc như bệnh tim mạch, suy giảm chức năng thận, tăng huyết áp cần thuốc chẹn nút AV. Các bất thường dẫn truyền thường gây ra bởi tăng kali máu nặng. Tuy nhiên, nó cũng có thể xảy ra khi kali máu tăng ở mức nhẹ tới vừa và kèm sử dụng thuốc chẹn nút AV do tác dộng cộng gộp giữa hai yếu tố trên trong bệnh cảnh suy giảm chức năng thận. Nhà lâm sàng phải xác định được hội chứng BRASH bởi cách điều trị có thể khác so với phác đồ hồi sức tim mạch tiêu chuẩn (ACLS). Chúng tôi báo cáo hai ca bệnh có biểu hiện hội chứng BRASH mà không đáp ứng với phác đồ ACLS tiêu chuẩn.
Từ khóa
Thuốc chẹn nút nhĩ thất, mạch chậm, tăng kali máu, suy thận, sốc.
Tổng quan
Thuật ngữ hội chứng BRASH xuất hiện lần đầu năm 2016 khi Josh Farkas mô tả hội chứng viết tắt cho mạch chậm, suy thận, thuốc chẹn nút nhĩ thất, sốc và tăng kali máu (BRASH) trong Pilmcrit [1]. Nó được mô tả là một vòng luẩn quẩn giữa mạch chậm và sốc gây ra bởi tác dụng cộng gộp của tăng kali máu và sử dụng thuốc chẹn nút nhĩ thất (AV) thứ phát gây suy thận. Các đặc điểm của hội chứng này được mô tả trong nhiều tài liệu trước đây, nhưng nó còn chưa được xem là một hội chứng riêng biệt [2- 4]. Hội chứng BRASH thường thấy ở các bệnh nhân mắc bệnh tim mạch từ trước và suy thận mạn đã điều trị trong thời gian dài với thuốc chẹn nút AV. Các yếu tố nguy cơ đã được xác định cho tình trạng bệnh nguy kịch cấp tính như sepsis, giảm thể tích, tăng số lượng thuốc uống tại nhà (các lợi tiểu giữ kali) và bất kỳ nguyên nhân nào khác gây tổn thương thận cấp. Việc xác định hội chứng lâm sàng này là quan trọng bởi điều trị theo ACLS tiêu chuẩn có thể thất bại trong việc cải thiện mạch chậm và sốc ở những bệnh nhân này.
Báo cáo ca bệnh
Ca 1
Một phụ nữ 62 tuổi mắc đái tháo đường, tăng huyết áp và rối loạn mỡ máu tới phòng cấp cứu do có nhiều cơn ngất xỉu. Khai thác bệnh sử thêm cho thấy bà ta có nhiều lần nôn và tiêu chảy trước đó. Bà ta không đau ngực, khó thở hay bất kỳ triệu chứng nào khác. Bà ta uống Telmisartan 40mg một lần một ngày, atenolol 50mg một lần một ngày, diltiazem 60mg 3 lần một ngày, metformin 1g hai lần một ngày, aspirin 75 mg một lần một ngày và atorvastatin 20mg trước khi đi ngủ. Bà ta than phiền về thuốc và không có bệnh sử về việc sử dụng quá liều. Khi thăm khám, bệnh nhân lơ mơ và đầu chi lạnh và mạch đập yếu. Huyết áp đo được là 105/41 mmHg, nhịp tim là 40 lần/phút. Các dấu hiệu thực thể khác là không đáng chú ý. Điện tâm đồ (ECG) thấy nhịp bộ nối chậm với tần số 40 lần/phút [Hình 1]. Xét nghiệm chức năng thận thấy: Kali 6.3 mmol/L (giá trị bình thường 3.3-5.1 mmol/1), Ure: 10.9 mmol/1 (giá trị bình thường: 1.7-8.3 mmol/1), Creatinine: 175 umol/1 (giá trị bình thường: 60-120 μmol/1). Bắt đầu truyền tĩnh mạch bolus 20ml/kg dịch muối đẳng trương và dùng hai liều atropine 0.5mg đường tĩnh mạch nhưng không thấy cải thiện. Chúng tôi đã tiến hành cho 10ml calcium gluconat 10% đường tĩnh mạch, 50ml dextrose 50% và 10UI insulin pha truyền tĩnh mạch. Bà ta cần truyền catecholamine và dopamine với liều 20 ug/kg/phút và adrenaline 5μg/phút. Sau khi tryền xong dextrose/insulin đầu tiên, kali trong khí máu quay trở về mức 5.6 mmol/1. Chúng tôi đã cho truyền dextrose/insulin lần thứ hai, và bà ta đã có cải thiện đáng kể khi có nhịp xoang trở lại và nhịp tim là 75 1/ph [Hình 2]. Catecholamine được giảm liều dần dần. Kali máu làm lại quay trở lại mức 3.5 mmol/1.
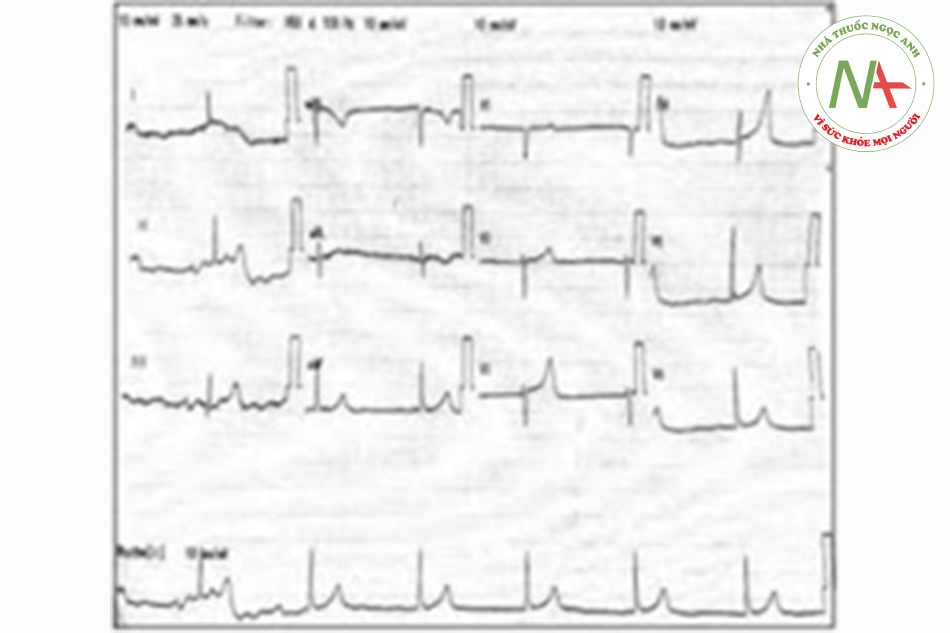
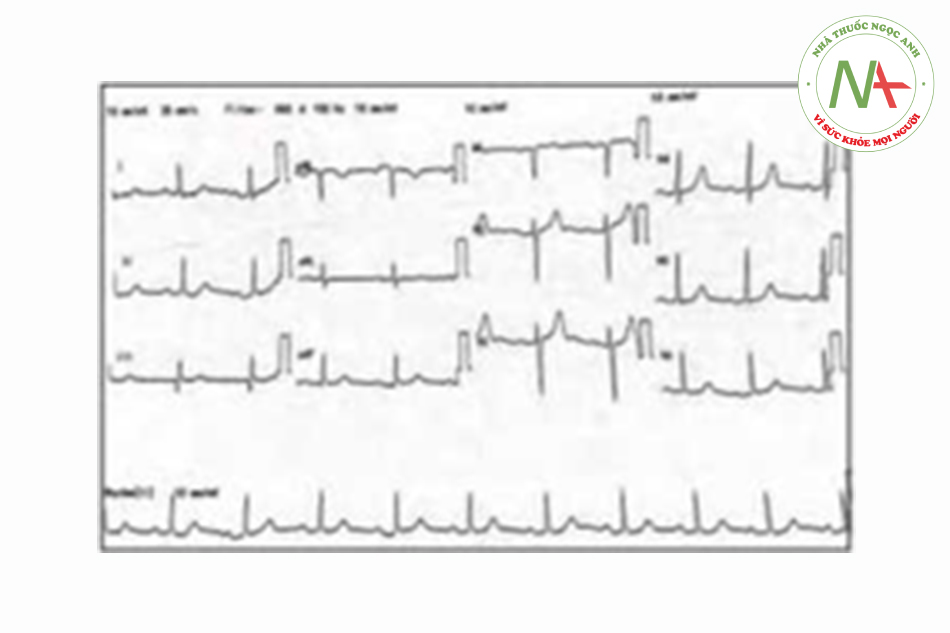
Ca 2
Ca thứ hai là một phụ nữ 44 tuổi mắc bệnh thận mạn, tăng huyết áp, và đái tháo đường tới với chúng tôi vì có một cơn ngất xỉu. Không thấy có biểu hiện động kinh. Bà ta không đau ngực, khó thở, tiêu chảy hoặc nôn. Thuốc đang dùng bao gồm uống diltiazem 30mg 3 lần một ngày, furosemide 80mg 3 lần một ngày, metoprolol lOOmg hai lần một ngày, felodipine 10mg hai lần một ngày, spriolactone 25mg hai lần một ngày, aspirin 75mg một lần một ngày, vidagliptin 50mg một lần một ngày, sắt fumarate 200mg hai lần một ngày, và vitamin c 5mg một lần một ngày. Khi nhập viện, bệnh nhân lơ mơ với điểm GSC 14 (E3V5M6), huyết áp 88/52 mmHg, nhịp tim 48 lần/phút, và spO2 96% khí phòng. Mạch nẩy yếu, thời gian đổ đầy mao mạch là 3 giây, và chi lạnh. Thăm khám phổi thấy bình thường, thăm khám tim mạch không thấy tiếng thổi. Thăm khám thần kinh không có gì đáng chú ý. ECG thấy nhịp thoát bộ nội với các nhịp rơi ngẫu nhiên [Hình 3]. 1.5mg Atropine truyền tĩnh mạch và bệnh nhân được pha truyền dopamine liều 20 ug/kg/phút. Không thấy cải thiện, bệnh nhân được thở máy và an thần để đặt máy tạo nhịp qua da. Tại thời điểm này, kali máu trở về mức 5.5 mmol/1 (giá trị bình thường 3.3-5.1 mmol/1), và chúng tôi cho dùng 10ml calcium gluconate 10% đường tĩnh mạch kèm 50ml dextrose 50% pha với 10UI insulin truyền tĩnh mạch. Các đánh giá khác cho thấy ure tăng từ 16.2 mmol lên 21.2 mmol/1 (giá trị bình thường: 1.7-8.3 mmol/1) và creatinine tăng từ 132 umol/1 lên 257 μmol/1 (giá trị bình thường: 60-120 μmol/1). Các men tim, điện giải khác, xét nghiệm chức năng gan, và công thức máu toàn phần đều bình thường. Làm lại kali máu sau điều trị cho kết quả 4.3 mmol/1 và ECG quay trở lại nhịp xoang [Hình 4]. Dopamine và máy tạo nhịp được dừng từ từ, và bệh nhân được rút ống vào ngày tiếp sau. Sự đồng ý bằng văn bản đã được cả hai bệnh nhân xác nhận.
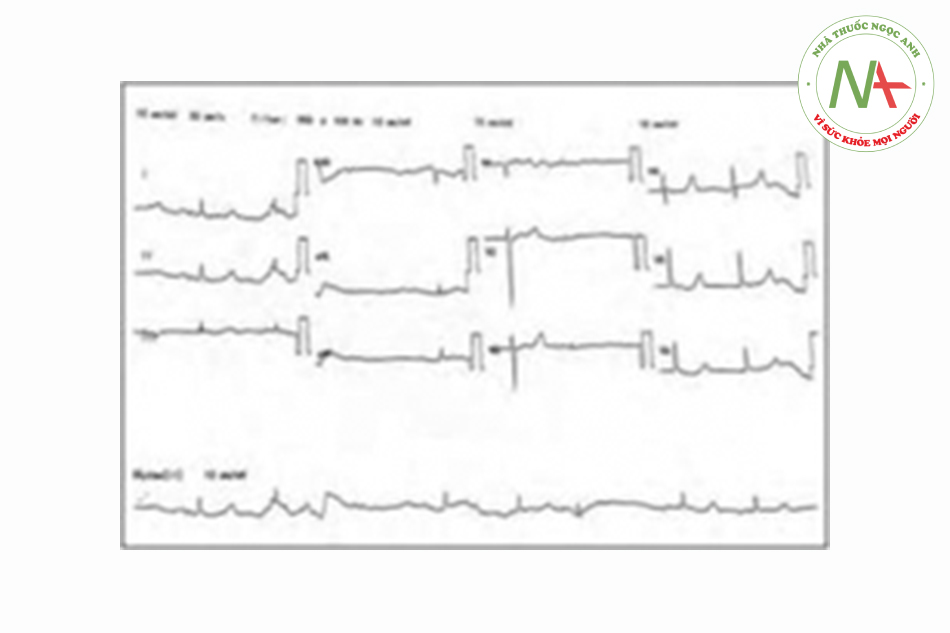
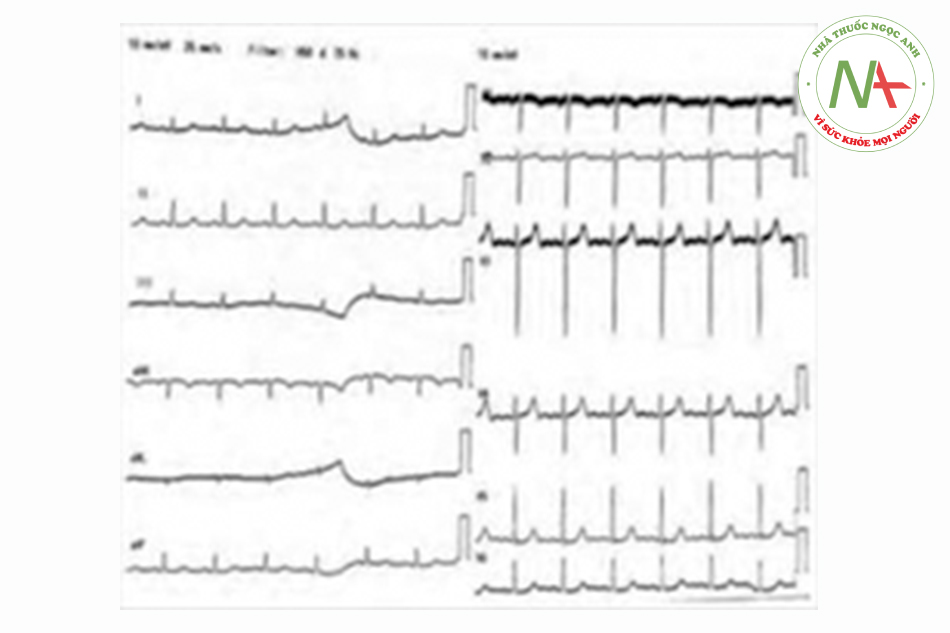
Bàn luận
Bệnh học của hai ca bệnh ở trên có thể là do tăng kali máu tác động cộng gộp với thuốc chẹn nút AV dẫn tới giảm sức co cơ tim và tụt huyết áp. Điều này dẫn tới giảm tưới máu và suy thận, điều này có thế tạo điều kiện cho tăng kali máu và tích tụ các thuốc trong cơ thể tạo ra một vòng tròn bệnh lý. [5] Tác động của tăng kali máu có thể phản ánh qua ECG và sự thay đổi phụ thuộc vào tốc độ tăng và nồng độ kali máu. Mối liên quan giữa nồng độ kali máu và sự thay đổi ECG có thể là đa dạng nhưng hầu hết bệnh nhân có bất thường trên ECG tại mức kali máu là 6.7 mmol/L [6] Ngừng xoang với việc mất sóng p trên ECG là một thay đổi hiếm gặp bởi các sợi của nút xoang có tính đề kháng với tăng kali máu cao hơn so với các cơ nhĩ. Có thể có một số thay đổi trên ECG do tăng kali máu ở mức tăng vừa (kali máu 6-6.5 mmol/1) như T cao nhọn, QRS rộng và PR kéo dài nhưng ngừng xoang thường xảy ra khi tăng kali máu nặng khi kali máu đã gần tới 8-9 mmol/1. [7] Trong hội chứng BRASH, mạch chậm xảy ra khi tăng kali máu ở mức nhẹ hoặc vừa do tác động cộng gộp của thuốc chẹn nút AV và tăng kali máu. [1] Điều này được ủng hộ bởi một nghiên cứu của Hegazi và cộng sự [8] cho thấy verapamil có thể gây nhịp bộ nối chậm thậm chí ở mức tăng kali máu nhẹ. Các đặc điểm phân biệt khác giữa tăng kali máu đơn thuần với hội chứng BRASH là có biểu hiện của nhịp bộ nối chậm mà không có các dấu hiệu về tăng kali máu trên điện tâm đồ. [3] Bonvinin và cộng sự [2] cũng thấy rằng tăng kali máu mức độ vừa có thể biểu hiện ngừng xoang mà không có bất kỳ dấu hiệu trên điện tâm đồ nào khác trong bệnh cảnh sử dụng thuốc chẹn kênh canxi và chẹn beta.
Việc xác định hội chứng lâm sàng này là quan trọng do lưu đồ ACLS tiêu chuẩn bao gồm atropine và đặt máy tạo nhịp có thể không có hiệu quả trong điều trị ở những bệnh nhân mắc hội chứng BRASH. Điều trị nên đặt mục tiêu là giảm kali máu, xác định và điều trị nguyên nhân tổn thương thận và đôi khi là điều trị ngộ độc thuốc chẹn beta hay chẹn kênh canxi. Tăng kali máu nên được điều trị bằng Calcium đường tĩnh mạch để ổn định màng tế bào cơ tim và truyền insulin kèm glucose để chuyển kali vào trong tế bào. Các phương thức khác như albuterol cũng có thế hữu ích trong điều trị mạch chậm. Vì bệnh nhân BRASH thường biểu hiện giảm thể tích, bù dịch là tối quan trọng cho những bệnh nhân này. cần đặc iệt quan tâm đến những bệnh nhân suy thận vô niệu bởi có thể có tình trạng quá tải dịch. Đào thải kali qua nước tiểu bằng lợi tiếu thải kali như furosemide có thể được cân nhắc để tạo điều kiện loại bỏ kali qua nước tiểu. Lọc máu cấp cứu nên được tiến hành nếu các phương thức trên thất bại. Truyền catecholamine nên được dùng nếu bệnh nhân có bất thường huyết động kéo dài [1,5]. Duy trì tái tưới máu thận phù hợp là quan trọng trong khi chờ các thuốc nói trên bị đào thải [9]. Các lựa chọn catecholamine là epinephrine, dopamine và ispproterenol. Điều trị ngộ độc chẹn beta hoặc chẹn kênh canxi bằng insulin liều cao và glucagon đôi khi có thể cần thiết
Kết luận
Hai trường hợp lâm sàng này nhấn mạnh tầm quan trọng của việc chẩn đoán hội chứng BRASH, đặc biệt ở những người có nhiều bệnh đồng mắc. Việc hiểu bệnh học của bệnh có thể hỗ trợ nhà lâm sàng điều trị những bệnh nhân này hiệu quả hơn. Việc điều trị hội chứng BRASH khác với lưu đồ ACLS tiêu chuẩn, và nó có thể dẫn tới việc sử dụng quá mức máy tạo nhịp nếu chúng ta tuân thủ mù quáng phác đồ ACLS.
Tài liệu tham khảo
- Ashworth S, Levsky M, Marley C, Kang C. Bradycardia-associated torsade de pointes and the long-QT syndromes: a case report and review of the literature. Mil Med. 2005;170(5):381-386. [PubMed]
- Namboodiri N. Bradycardia-induced Torsade de Pointes – An arrhythmia Less Understood. Indian Pacing Electrophysiol J. 2010;10(10):435-438. [PubMed]
- Cortes J, Hall B, Redden D. Profound symptomatic bradycardia requiring transvenous pacing after a single dose of tizanidine. J Emerg Med. 2015;48(4):458- 460. [PubMed]
- Wung S. Bradyarrhythmias: Clinical Presentation, Diagnosis, and Management. Crit Care Nurs Clin North Am. 2016;28(3):297-308. [PubMed]
- Bernheim A, Fatio R, Kiowski W, Weilenmann D, Rickli H, Brunner-La R. Atropine often results in complete atrioventricular block or sinus arrest after cardiac transplantation: an unpredictable and dose-independent phenomenon. Transplantation. 2004;77(8):1181-1185. [PubMed]
- Carron M, Veronese S. Atropine sulfate for treatment of bradycardia in a patient with morbid obesity: what may happen when you least expect it. BMJ Case Rep. 2015;2015. [PubMed]
- Chin K, Seow S. Atrioventricular conduction block induced by low-dose atropine. Anaesthesia. 2005;60(9):935-936. [PubMed]
- Maruyama K, Mochizuki N, Hara K. High-degree atrioventricular block after the administration of atropine for sinus arrest during anesthesia. Can J Anaesth. 2003;50(5):528-529. [PubMed]
- For bradycardia due to cholinergic poisoning, much higher doses of atropine may be needed.
- Brady W, Swart G, DeBehnke D, Ma O, Aufderheide T. The efficacy of atropine in the treatment of hemodynamically unstable bradycardia and atrioventricular block: prehospital and emergency department considerations. Resuscitation. 1999;41(1):47- 55. [PubMed]
- Vavetsi S, Nikolaou N, Tsarouhas K, et al. Consecutive administration of atropine and isoproterenol for the evaluation of asymptomatic sinus bradycardia. Europace. 2008;10(10):1176-1181. [PubMed]
- There doesn’t seem to be solid clear data on this. This arrangement is consistent with most references and makes a reasonable amount of sense. Based on echocardiography and anatomy, the location of the left parasternal window is fairly uniform. In contrast, the apex of the heart is highly variable. Therefore, trying to place a pad on the apex of the heart is error-prone.
- Seifert P, Yang Z, Reines H. Crisis Management of Unstable Bradycardia in the OR. AORNJ. 2016;103(2):215-223. [PubMed]
- Deal N. Evaluation and management of bradydysrhythmias in the emergency department. EmergMedPract. 2013;15(9):1-15; quiz 15-16. [PubMed]
- Sodeck G, Domanovits H, Meron G, et al. Compromising bradycardia: management in the emergency department. Resuscitation. 2007;73(1):96-102. [PubMed]
- Metkus T, Schulman S, Marine J, Eid S. Complications and Outcomes of Temporary Transvenous Pacing: An Analysis of > 360,000 Patients From the National Inpatient Sample. Chest. 2019;155(4):749-757.
https://www.ncbi.nlm.nih.gov/pubmed/3 0543 806.
Xem thêm:
Chàm là bệnh gì? Triệu chứng, nguyên nhân, cách điều trị và phòng ngừa bệnh theo BMJ