Bệnh sản phụ khoa
TỔNG QUAN VỀ RỐI LOẠN NHỊP TIM THAI (FETAL ARRHYTHMIAS)
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
Bài viết TỔNG QUAN VỀ RỐI LOẠN NHỊP TIM THAI (FETAL ARRHYTHMIAS) – tải pdf tại đây.
Biên dịch: Bác sĩ Vũ Tài.
GIỚI THIỆU
Nhờ những tiến bộ về công nghệ siêu âm nên hiện nay chúng ta đã có thề chẩn đoán trước sinh được hầu hết các bất thường nhịp tim. Siêu âm 2D, bao gồm hình ảnh thang xám thông thường và M-mode, ngoài ra, Doppler màu và xung cũng đóng vai trò quan trọng trong việc chẩn đoán các rối loạn nhịp tim thai phức tạp và theo dõi sự thành công của các can thiệp điều trị trước sinh. Kết hợp Doppler mô và chụp cộng hưởng từ tim thai (magnetocardiographỵ) với siêu âm thông thường giúp hiểu biết rõ hơn về sinh lý bệnh của các rối loạn nhịp tim thai, từ đó có phương pháp điều trị đặc hiệu cho các tình trạng này.
Các bất thường nhịp tim thai rất phổ biến với tỷ lệ 1% đen 2% thai kỳ (I). Nhịp tim thai không đều là ]ý do chuyền tuyến phổ biến nhất ờ các trung tâm siêu âm tim thai vì rối loạn nhịp, và phần lớn đó là ngoại tâm thu nhĩ lành tinh (benign atria) ectopic beats). Rối loạn nhịp tim thai chậm hoặc nhanh dai dẳng, có thể làm tăng tý lệ bệnh tật và từ vong ỡ trê sơ sinh nhưng chi chiếm < 10% các trường hợp chuyến tuyến (2). Chương này thảo luận về các phương thức chẩn đoán hiện có để đánh giá các bất thường/rối loạn nhịp tim thai khác nhau, cũng như tác động cùa chúng đối với kết cục cùa thai nhi và trê sơ sinh và quản lý chúng.
ĐÁNH GIÁ NHỊP TIM THAI
Siêu âm tim M-mode
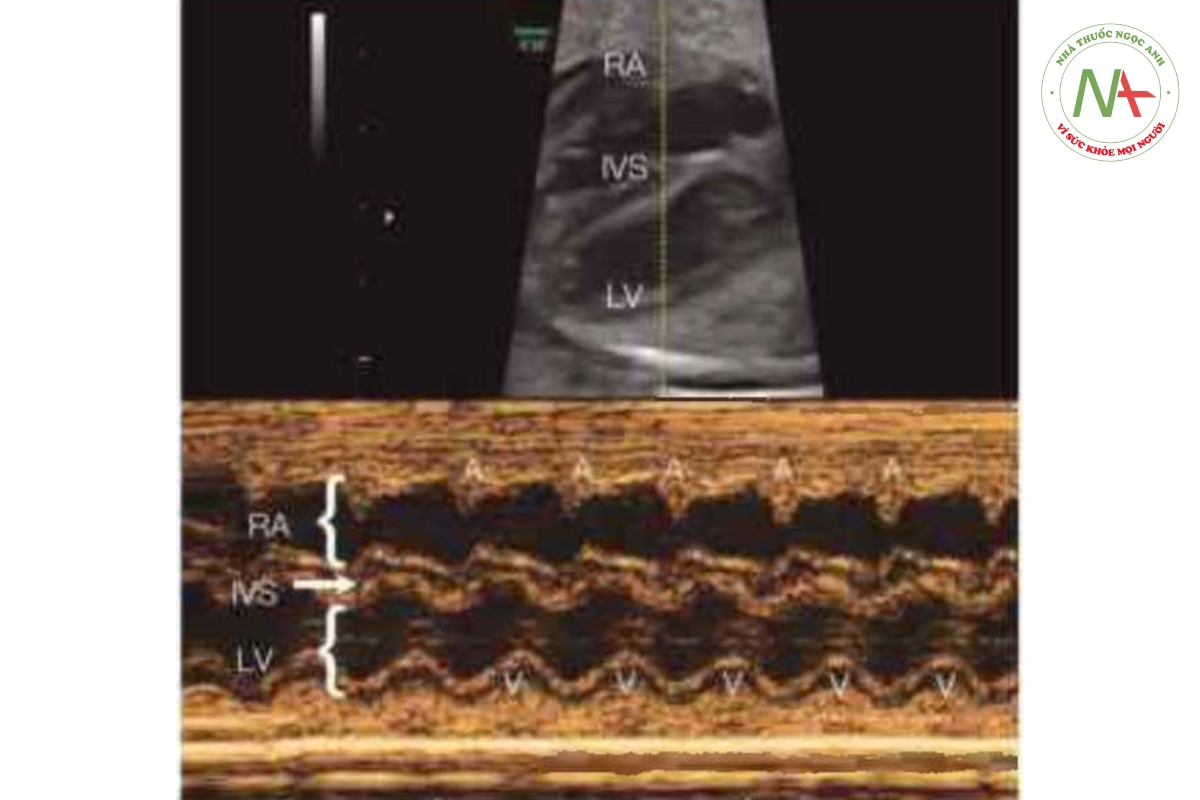
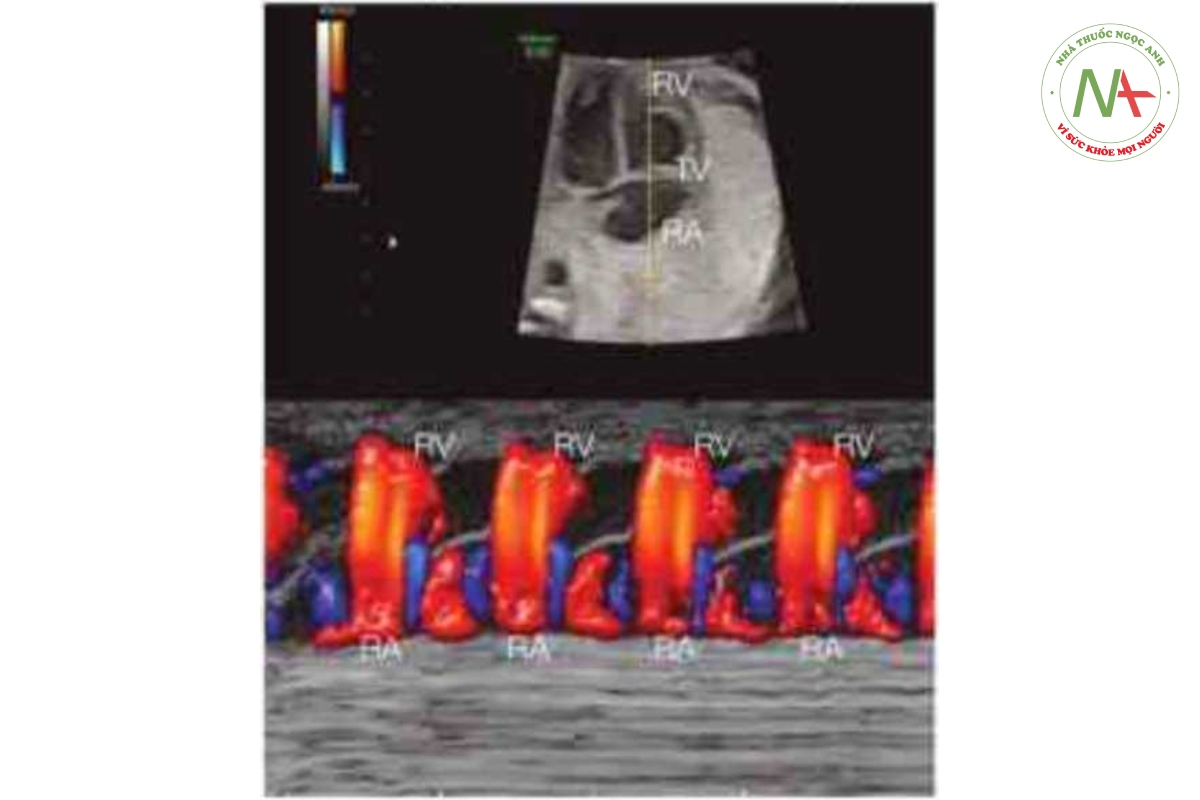
Siêu âm tim M-mode (Mode chuyển động) thu được bằng cách ghi lại sóng phản hồi (reflections) của chùm sóng siêu âm liên quan đến thời gian và độ sâu từ đầu dò. Do đó, bàn ghi M-mode được biểu diễn dưới dạng đường thắng cùa các cấu trúc tim lân cận như một hàm của thời gian. Trong thực hành lâm sàng, đầu tiên cần có hình ảnh siêu âm 2D tim thai và thanh định hướng (cursor) M-mode được đặt ở vị trí mong muốn trong tim. Do độ phân giải thời gian (temporal resolution) ngày càng tăng nên biểu diễn dưới dạng đường thắng của siêu âm tim M-mode cho phép đo kích thước các buồng tim và đường kính đại động mạch chính xác hơn và có thể tái tạo lại (reproducible). Vì siêu âm tim M-mode phát hiện chuyển động của các cấu trúc theo thời gian nên các sự kiện điện (electrical events) của tim được suy ra lừ chuyển động đó, và do đó, siêu âm tim M-mode thường được dùng để đánh giá rối loạn nhịp tim thai nhi và chuyển động của các van tim khác nhau. Thanh định hướng M-mode thường được đặt cắt qua tâm nhĩ và tâm thất để ghi lại tương quan của các nhát tâm nhĩ-tâm thất co bóp (Hình 46.1). Trên M-mode, vì thời điểm bắt đầu (onset) và định của các nhát tâm nhĩ và tâm thất co bóp không được xác định rõ ràng nên không thể đo được khoảng thời gian (time intervals) nhì thất (AV), và đây là một nhược điểm lớn của M-mode khi đánh giá bất thường nhịp tim thai. Hơn nữa, khả năng ứng dụng lâm sàng của M-mode thường bị hạn chế bởi chất lượng tín hiệu kém và tư the thai nhi không thuận lợi (suboptimal fetal positions). M-mode giải phẫu (Anatomic M-mode) là một ứng dụng tương đối mới của M-mode, bằng cách tái tạo lại (reconstructing) M- rnode từ vòng lặp (cine loop) hình ảnh 2D trong xử lý hậu kỳ nên không phụ vào tư thế thai nhi (3) (Hình. 15.19), và đây là một lợi thế đáng kể so với M-mode thông thường. Tuy nhiên, trong M-mode giải phẫu, độ phân giải thời gian bị giảm đáng kể khi so sánh với M-mode thông thường vì M-mode giải phẫu phụ thuộc vào chất lượng của dữ liệu kỹ thuật số được lưu trữ (stored digita) data). Kết hợp Doppler màu vào M- mode (Hình 46.2) sẽ cho biết thêm dòng máu vào và ra qua các van và có thể hữu ích trong việc tăng cường khả năng ứng dụng và diễn giải M-mode. Độc giả tham khảo Chương 15 để thảo luận chi tiết hơn về vai trò của M-mode trong siêu âm tim thai.
Siêu âm tim Doppier xung
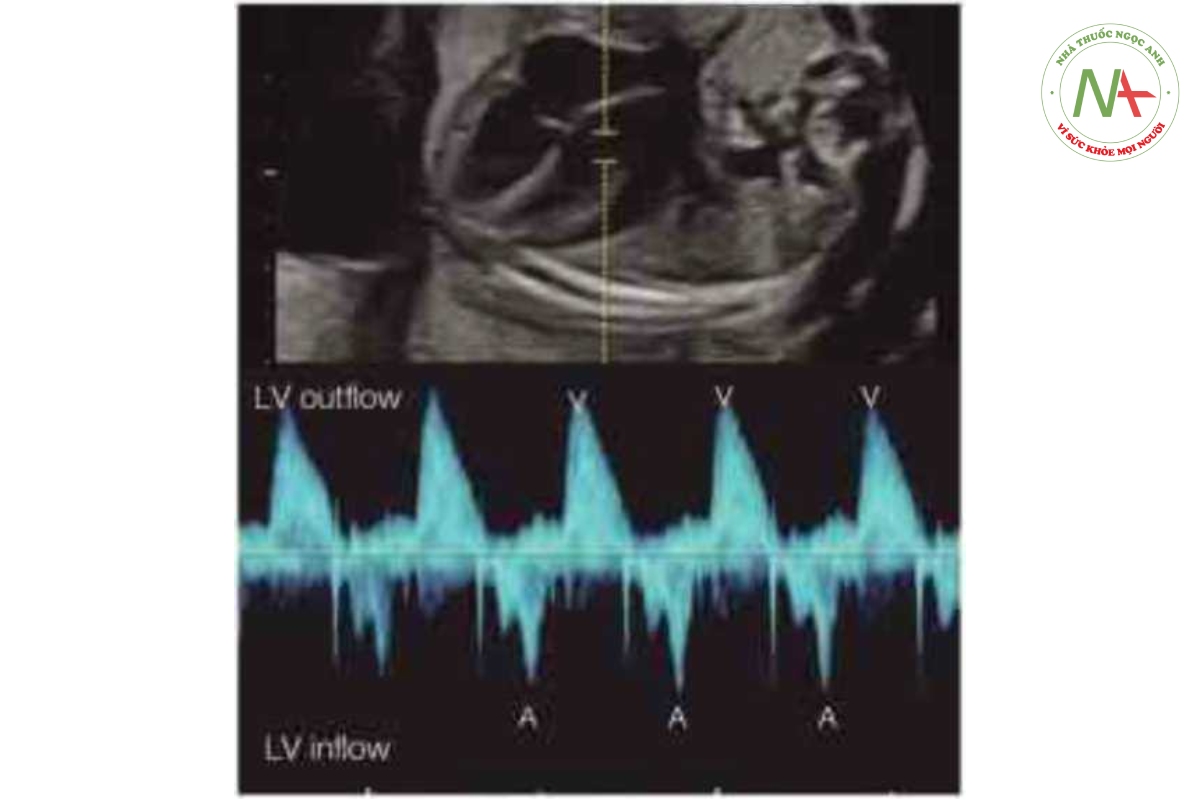
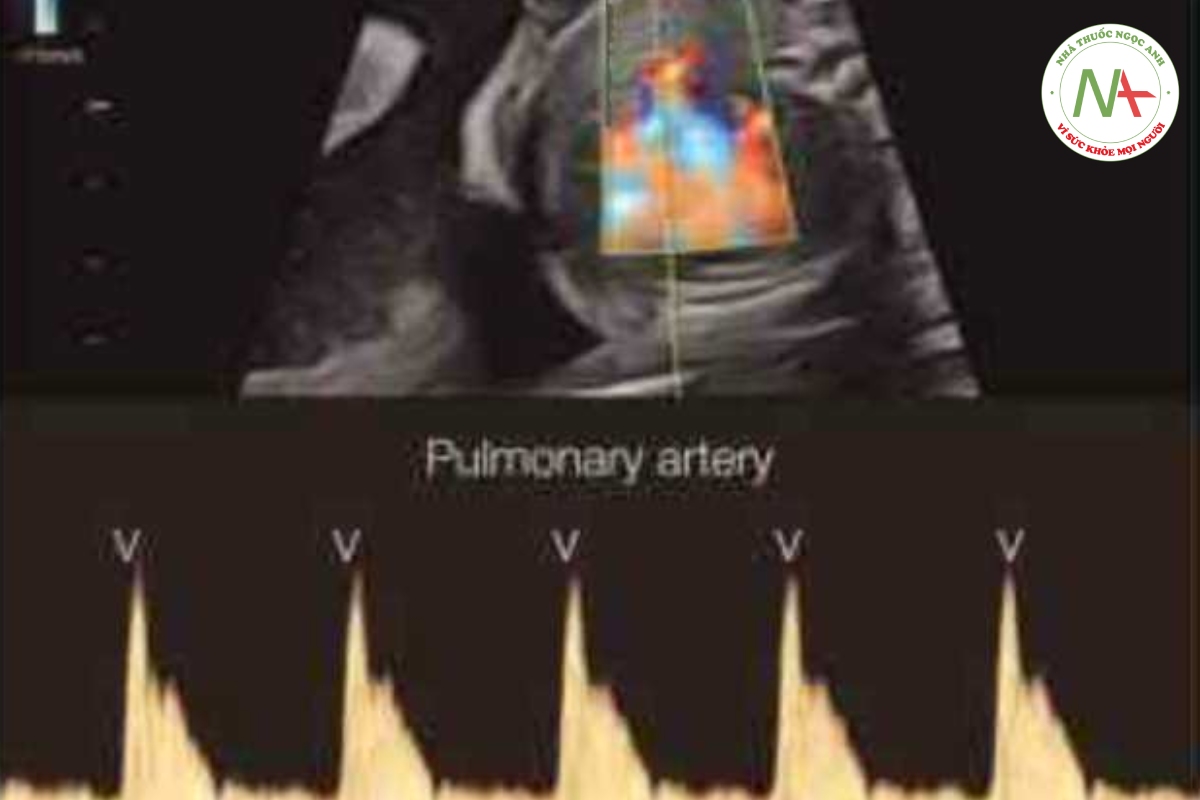
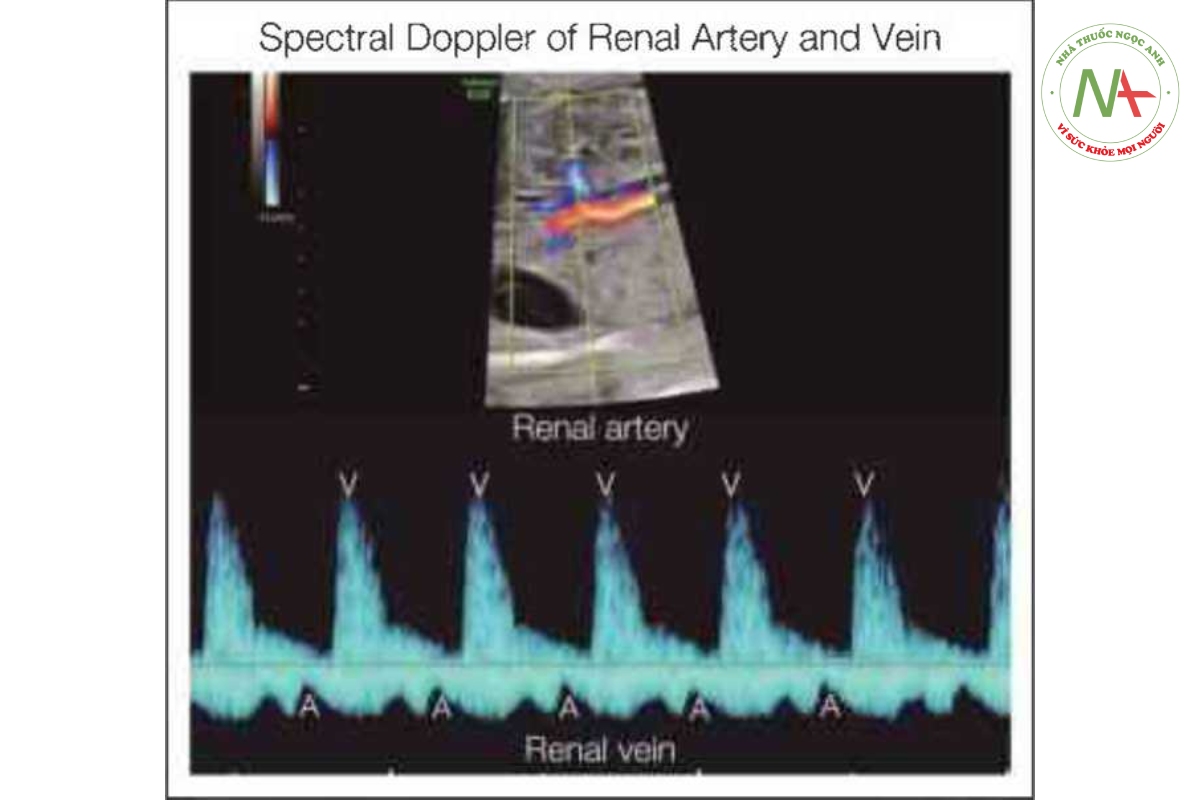
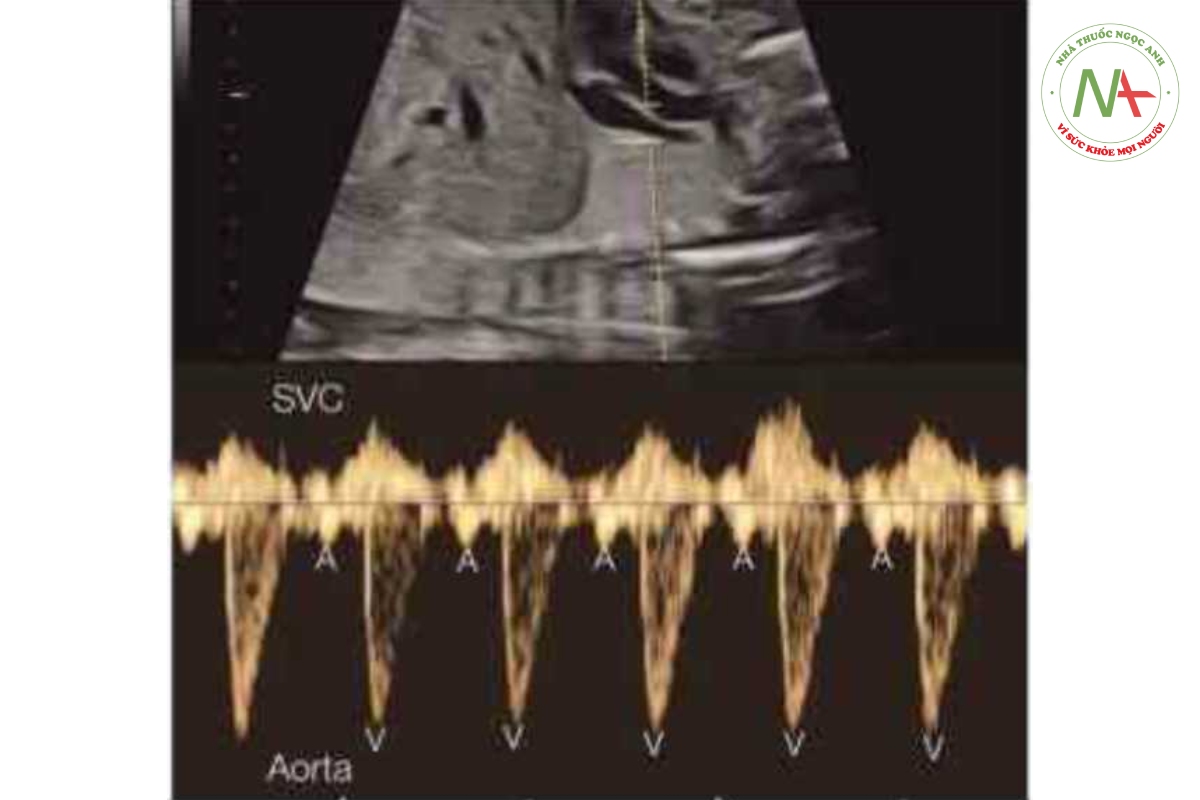
Siêu âm tim Doppler xung có thể cung cấp các thông tin rất quan trọng giúp đánh giá các bất thường nhịp tim thai và là phương thức được ưa chuộng hiện nay, bên cạnh siêu âm tim M-mode. Doppler xung có khả năng thu được các tín hiệu đồng thời khi tâm nhĩ và tâm thất co, do đó xác định được các sự kiện trong chu chuyền tim và các khoảng thời gian khác nhau, đây là một thông số rất cần thiết giúp phân loại các rối loạn nhịp úm khác nhau. Có thể thu được các thông tin trên khi cửa số (gatc) Doppler xung được đặt qua van hai lá và van động mạch chủ (Hình 46.3), động mạch và tĩnh mạch phổi (Hình 46.4), động mạch và tĩnh mạch thận (Hình 46.5), hoặc tĩnh mạch chủ trên và động mạch chủ (Hình 46.6) (4-6). Khi cửa sổ Doppler được đặt đồng thời qua tĩnh mạch chủ trên và động mạch chủ. dòng chảy ngược trong tĩnh mạch chủ trên đánh dấu thời điểm tâm nhĩ bắt đầu có, và dòng chảy xuôi dòng trong động mạch chủ đánh dấu thời điểm tâm thất bắt đầu có (Hình 46.6), vì vậy cũng có thể đánh giá khoảng PR cơ học bằng Doppler xung (xem phần sau của chương này) (7).
Điện tim thai nhi
ECG thai nhi (ECG) ghi lại các tín hiệu điện của tim thai qua thành bụng thai phụ, đã được báo cáo và giới thiệu cách đây khoảng 20 năm. Khó khăn của kỹ thuật này liên quan đến khả năng cô lập các tín hiệu ECG cùa thai nhi khỏi các tín hiệu ECG của mẹ chồng lên. Lĩnh vực này đang có những tiến bộ đáng kế và nhờ sự cái tiến công nghệ trong tương lai sẽ nhanh chóng thúc đẩy ứng dụng ECG thai nhi vào việc phân loại rối loạn nhịp tim.
=> Đọc thêm: Nghiên cứu các bất thường của thai thụ tinh trong ống nghiệm.
Doppler mô cơ tim
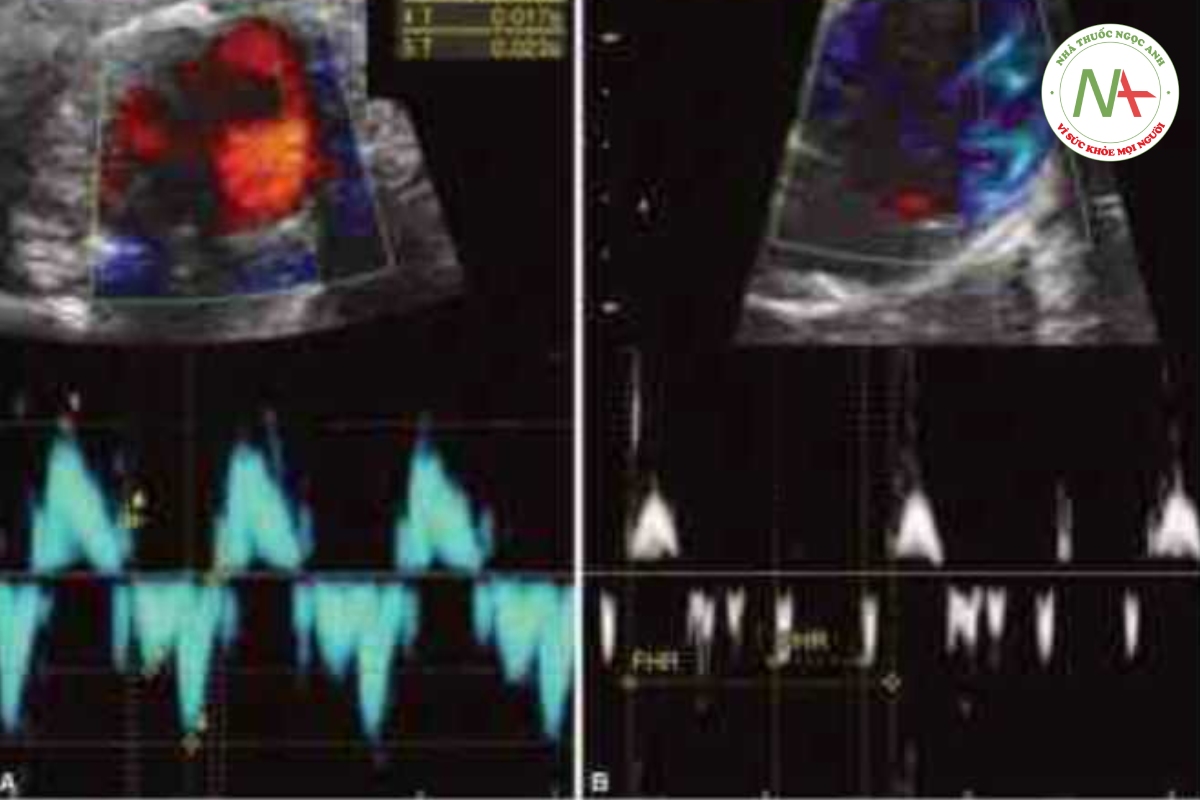
Doppler mô cơ tim là một kỹ thuật cho phép phân tích trực tiếp vận động thành của tim thai theo từng phần (vận tốc cơ tim) ở bất kỳ vùng nào trong cùng một chu chuyển tím (8). Kỹ thuật này cung cấp một bản đo các cấu trúc tim được mã hóa màu và vận động của chúng (Hình 46.7), đồng thời có iru điểm hơn siêu âm tim Doppler xung trong việc đánh giá trình tự thời gian của các sự kiện trong chu chuyền tim. Đánh giá khoảng thời gian AV bằng Doppler xung có nguồn gốc gián tiếp từ các phép đo lưu lượng nên bị ảnh hưởng bởi tiền tải/hậu tải, đặc tính cơ tim nội tại, tần số tim và tốc độ truyền ám (3). Tuy nhiên, khi đặt các số Doppler mô vào thành tâm nhĩ và tâm thất đang vận động, Doppler mô có thể cung cấp số đo chính xác về các khoảng thời gian của tim (cardiac intervals) và vận tốc của thành tim (Hình 46.7) (3). Do sự sẵn có của thiết bị Doppler mô rất hạn chế đã làm giới hạn khả năng ứng dụng lâm sàng của kỹ thuật này. Bằng cách điều chỉnh gain và vận tốc của siêu âm Doppler màu và Doppler xung, có thể thu được hình ảnh Doppler mô cơ tim với thiết bị siêu âm tiêu chuẩn (9). Thông tim chi tiết về cách tối ưu hóa hiển thị Doppler mô được trình bày trong Chương 18.
Chụp cộng hưởng từ tim thai
Chụp cộng hưởng từ tiền thai nhi (fMCG) ghi lại từ trường được tạo ra bởi hoạt động điện của tim thai và sử dụng trung bình tín hiệu để tạo ra các dạng sóng rất giống với các dạng sóng thu được trên ECG. Trong thập kỷ qua, đã có những tiến bộ đáng kể về việc ứng dụng lâm sàng của IMCG trong đánh giá các bất thường nhịp tim thai phức tạp. Một ưu điểm lớn của IMCG là khả năng đánh giá sự tái cực, điều này không thể phát hiện được bằng các phương thức cơ học trên siêu âm tim. Hơn nữa, IMCG cho phép theo dõi tim thai kéo dài và do đó có thể hữu ích trong việc đánh giá các bất thường nhịp tim thai phức tạp mà có thể thay đổi theo thời gian. Hạn chế của công nghệ này bao gồm giá thành, không sẵn có ở nhiều trung tâm và cần một phòng cản từ tính (10,11). Đã có báo cáo về việc sử dụng thành công công nghệ này trong môi trường thông thường (12), và trong tương lai, với sự cài tiến về công nghệ FMCG, và FMCG được ứng dụng rộng rãi sẽ giúp chẩn đoán các bất thường nhịp tim thai chính xác hơn.
PHÂN LOẠI RỐI LOẠN NHỊP VÀ QUẢN LÝ
Phân loại rối loạn nhịp tim ờ trẻ sơ sinh, trẻ em và người lớn dựa vào các tiêu chí rõ ràng, chủ yếu bằng các dấu hiệu trên ECG. Vì ECG không thể thực hiện được ở thai nhi nên một cách phân loại thực tế hơn được áp dụng, dựa vào các công nghệ trên siêu âm, chẳng hạn như M-mode và Doppler xung và Doppler mô cơ tim. Rối loạn nhịp tim thai nhi được phân thành 3 nhóm chính: nhịp tim thai không đều, rối loạn nhịp tim thai chậm (<110 nhịp/phút) và rối loạn nhịp tim thai nhanh (> 180 nhịp/phút).
Nhịp tim thai không đều
Nhịp tim không đều là lý do chuyển tuyến phổ biến nhất vì rối loạn nhịp tim thai, gặp ở khoảng 1% đến 2% thai kỳ (13), và có thể được phân loại thành ngoại tâm thu nhĩ và ngoại tâm thu thất.
Ngoại tâm thu nhĩ
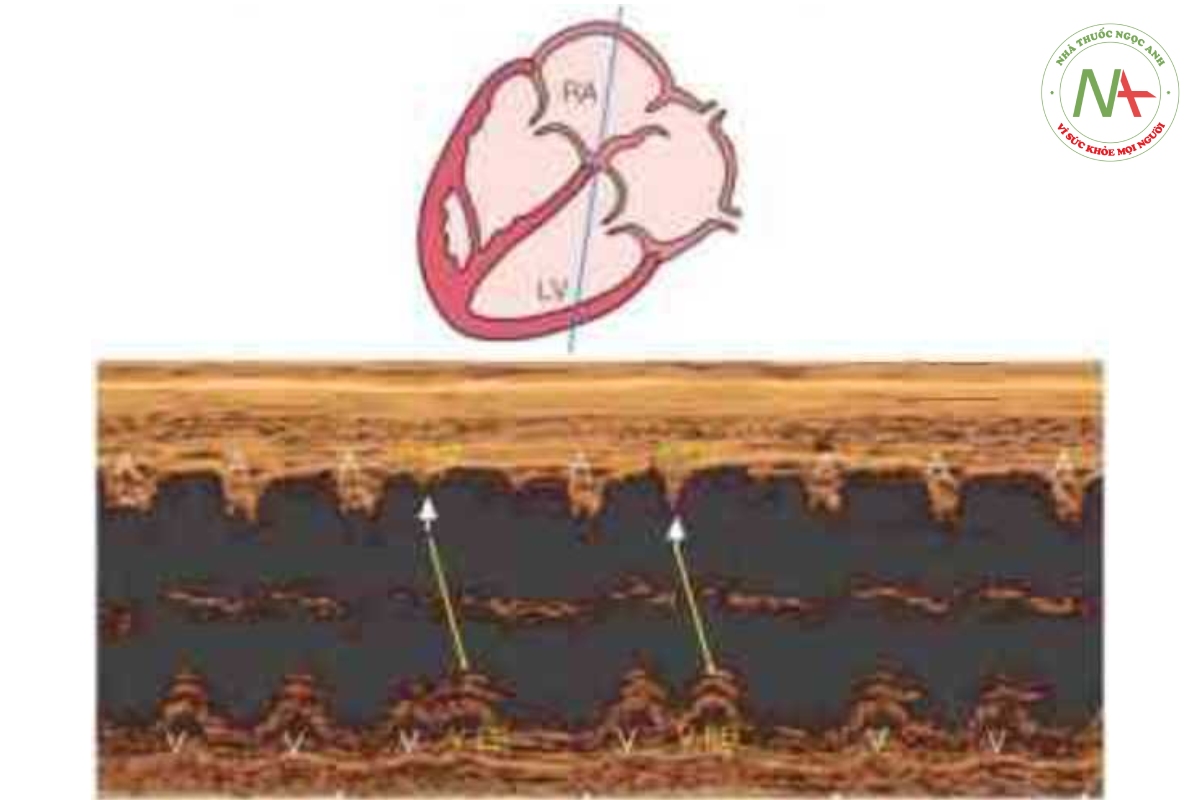
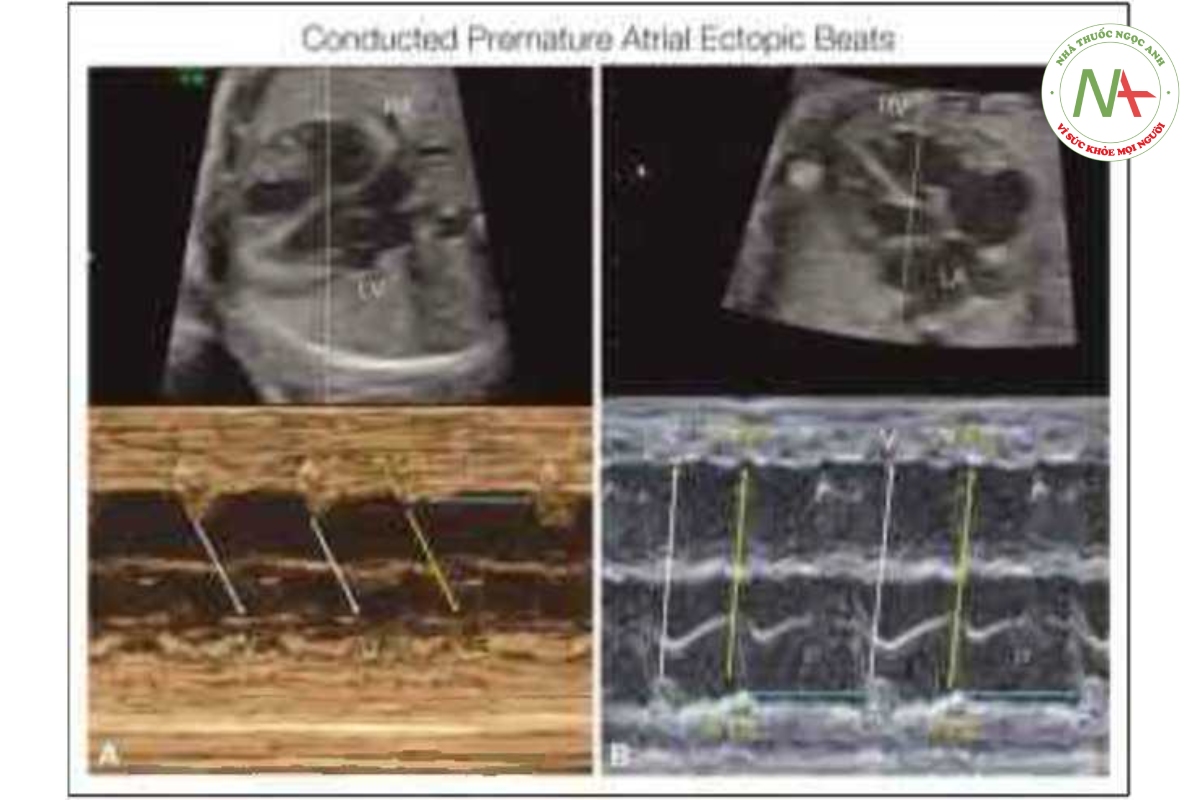
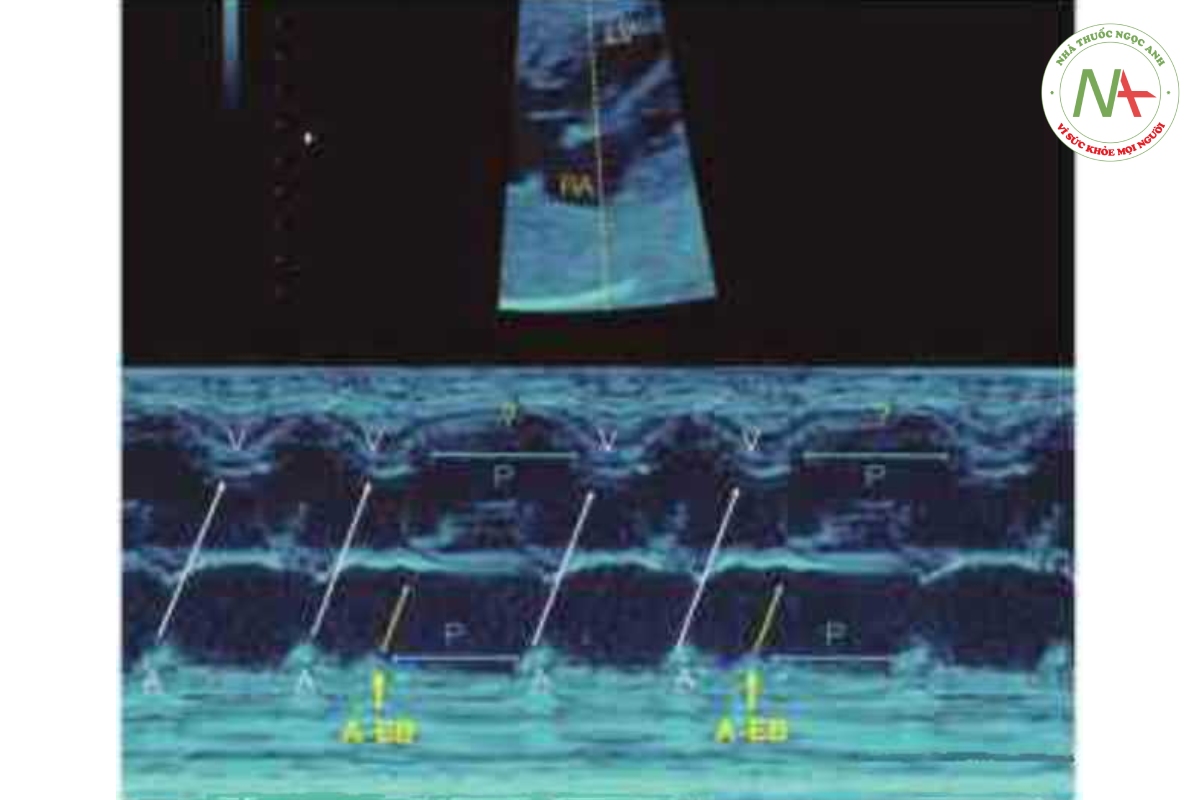
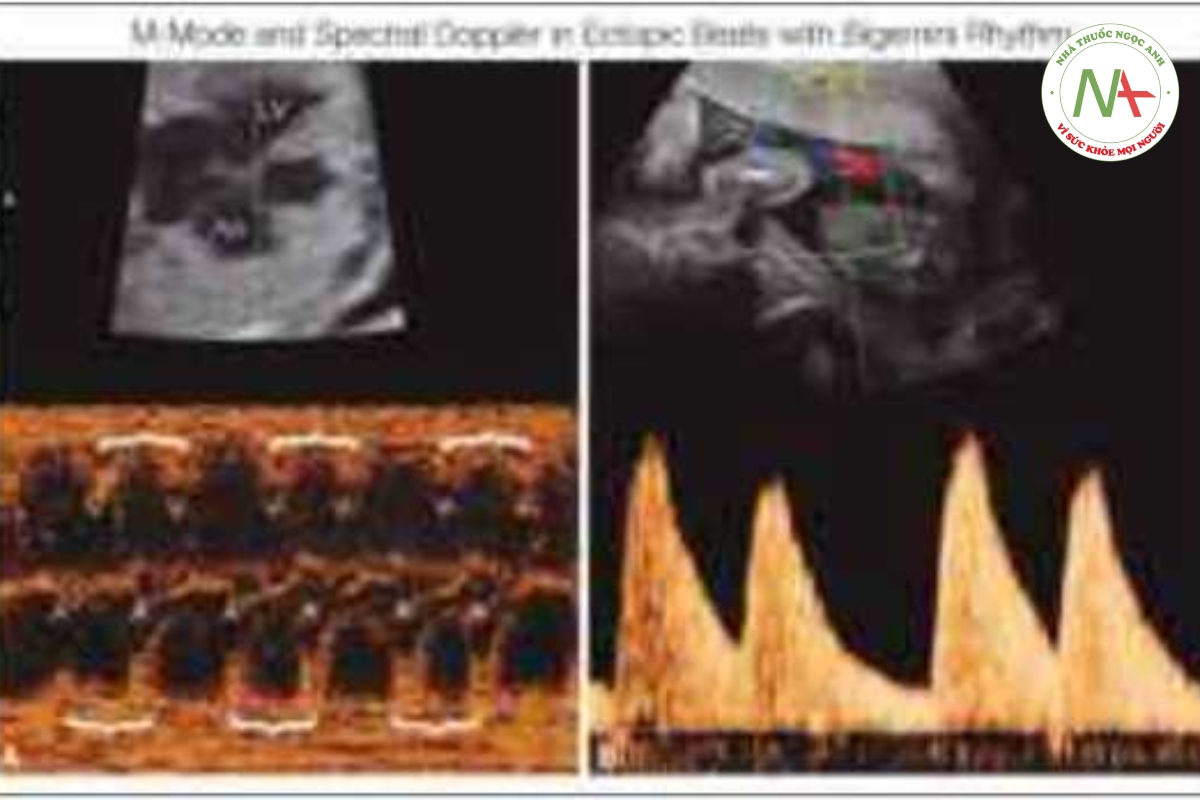
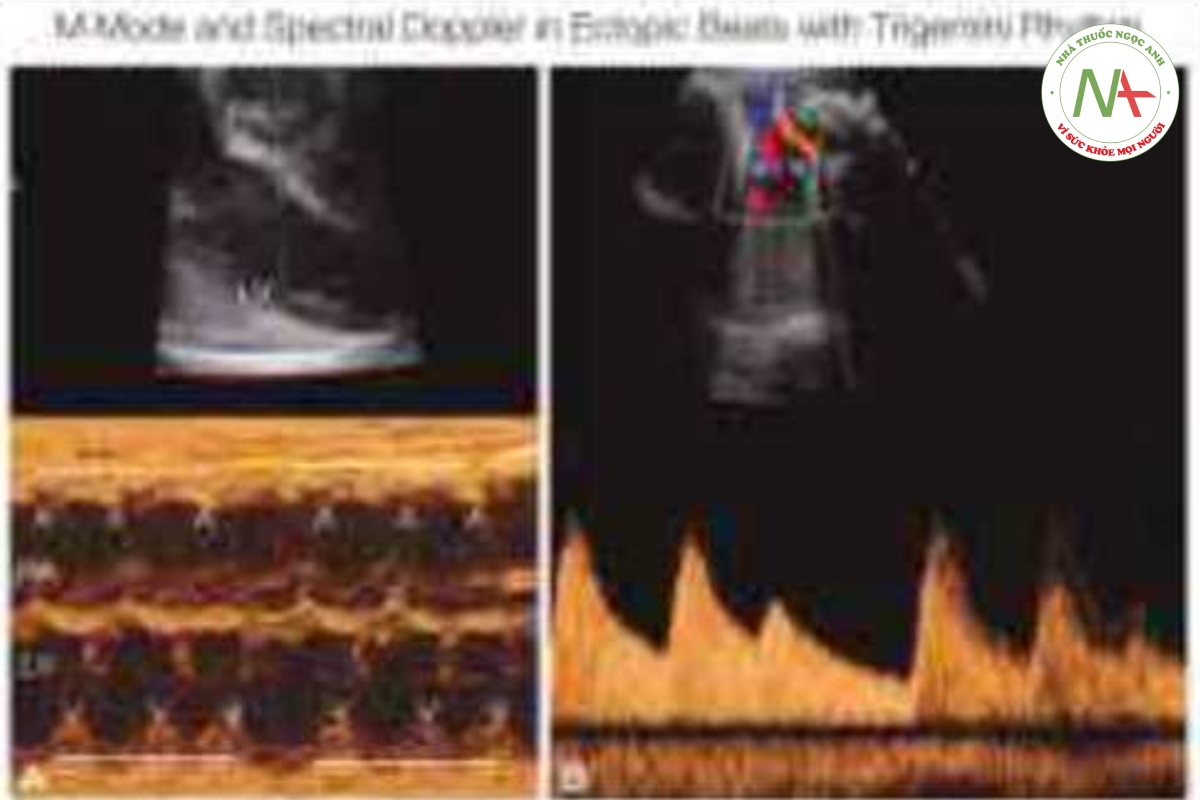
Đa số thai nhi có nhịp tim không đều được phát hiện là có các cơn ngoại tâm thu nhĩ (PAC) (Hình 46,8 và 46,9), hay gặp nhất vào cuối quý 2 của thai kỳ cho đến khi đủ tháng và thường là lành tính. Sinh lý bệnh của PAC vẫn chưa được hiểu rõ nhưng có tương quan với phình lỗ bầu dục (íoramen ovale aneurysm) hoặc nắp lỗ bầu dục dư thừa (flap redtindancy) (13). PAC có thể được dẫn truyền hoặc không dẫn truyền (block) (Hình 46.10), tương ứng dẫn đến nhịp tim không đều hoặc một khoảng nghỉ ngắn (short pausc). PAC có liên quan với bệnh tim bẩm sinh ở khoảng 1% đến 2% trường hợp và có thể tiến triển thành nhịp tim nhanh dai dẳng trong tử cung hoặc trong 3 đến 4 tuần đầu đời ở 1% đến 3% trường hợp (14). Các yếu tố nguy cơ làm PAC tiến triển thành nhịp tim nhanh bao gồm tần số thất thấp do nhiều nhịp ngoại tâm nhĩ không dẫn truyền và ngoại tâm thu nhĩ phức tạp bao gồm cả nhịp bộ đôi (bigeminy) (Hình 46.11) hoặc nhịp bộ ba (trigeminy) (Hình 46.12). Khi thấy PAC ứ thai nhi có bằng chứng rối loạn chức năng tim nên cảnh giác về khả năng xuất hiện nhịp nhanh trên thất (supraventricular tachycardia-SVT). Trong trường hợp có PAC thường xuyên hoặc phức tạp, cần phải đánh giá nhịp tim thai hàng tuần hoặc 2 tuần/lần bằng siêu âm hoặc thiết bị Doppler cầm tay (handheld Doppler device) nhằm tìm kiếm rối loạn nhịp nhanh cho đến khi PAC biến mất hoặc cho đến khi sinh thai.
Ngoại tâm thu thất
Ở một số ít trường hợp, các nhịp đến sớm có nguồn gốc lừ tâm thất chứ không phải tâm nhĩ và do đó được gọi là ngoại tâm thu thất (premature ventricular contraction- PVC). PVC cũng là tình trạng lành tính trong phần lớn các trường hợp. Tuy nhiên, khi thấy PVC, cần phải đánh giá tìm thấy vì PVC thường liên quan với các bất thường tim hơn PAC. Có thể khó phân biệt PAC với PVC ờ thai nhi, nhưng trong PVC Doppler xung hoặc bàn ghi M-mode sẽ cho thấy nhịp nhĩ co bóp đều còn nhịp thất co bóp không đều. Hở van ba lá trên Doppler màu hoặc sóng A nhỏ hơn trên Doppler xung tĩnh mạch chủ dưới kèm theo ngoại tâm thu có thể gợi ý ngoại tâm thu có nguồn gốc từ thất.
Quản lý nhịp tim thai không đều
Trong phần lớn các trường hợp, nhịp tim không đều do ngoại tâm thu nhĩ hoặc thắt thì không cần thiết phải điều trị vì hầu hết đều tự thoái tiền. Các tác giả khuyến cáo thai phụ nên ngừng các yếu tố khởi phát (inciting factors) đã biết hoặc nghi ngờ như hút thuốc, uống quá nhiều caffeine và các loại thuốc kích thích tim ((i-mimetics để điều trị dọa sinh non) khi có thể. Chúng tôi cũng hỏi thai phụ về việc sử dụng kem dưỡng da bơ ca cao (cocoa butter lotion) vì dữ liệu hồi cứu cho thấy có liên quan với PAC (15) và trong nhiều trường hợp, các tác giả nhận thấy PAC thường xuyên đã biến mất khi ngừng sử dụng bơ ca cao. Tần suất theo dõi được đề nghị là hàng tuần hoặc 2 lần/tuần, đặc biệt đối với ngoại tâm thu phức tạp, bao gồm theo dõi tần số và nhịp tim thai nhằm phát hiện sự tiến triển thành nhịp tim nhanh ở thai nhi, và có thể cần phải điều trị. Khi nhịp tim thai không đều dai dẳng cho đến khi sinh, các tác giả khuyến cáo thực hiện ECG ngay trong giai đoạn sơ sinh.
Rối loạn nhịp chậm
Nhịp tim thai chậm được định nghĩa là tần số tim thai < 110 nhịp/phút dai dẳng. Nhịp tim thai <110 nhịp/phút thoáng qua thường là lành tính và thường là do tăng kích thích thần kinh phế vị (vagal stimulation), ở thai nhi thường liên quan với tăng áp lực ổ bụng do ẩn đầu dò siêu âm. Các nguyên nhân gây nhịp tim thai chậm bao gồm nhịp chậm xoang, ngoại tâm thu nhĩ nhịp bộ đôi/bộ ba không dẫn truyền (blocked atrial bigeminy/trigeminy) và block AV độ cao (high-degree AV block) (16).
Nhịp chậm xoang
Nhịp chậm xoang rất hiếm gặp và có thể liên quan với rối loạn chức năng nút xoang, nhiễm toan máu thai nhi, hội chứng QT kéo dài bẩm sinh (congenital long QT syndromc-LQTS), hoặc các bất thường bẩm sinh, chẳng hạn như hội chứng đồng dạng (heterotaxy syndromcs) (17). Rối loạn chức năng nút xoang có thể do bất thường di truyền hoặc tổn thương nút xoang bình thường do nhiễm trùng hoặc kháng thể. Các đặc điểm của nhịp chậm xoang trên siêu âm tim bao gồm dẫn truyền AV 1:1 với tần số nhĩ chậm.
Hội chứng QT kéo dài
LQTS là bệnh lý kênh ion natri và kali di truyền mà kiểm soát sự tái cực (repolarization) của cơ tim, dẫn đến kéo dài khoảng QTc trên ECG (> 500 mili giây), ít nhất 17 gen có liên quan với LQTS, với 3 biến thể hay gặp nhất bao gồm KCNQ1 30%-35%, KCNQ2 20%- 30% và SCN5A 5%-10%, tương ứng gây ra LQTS typc 1,2 và 3, (18). KCNỌ1 và KCNQ2 kiểm soát các kênh ion kali tim, và SCN5A kiểm soát các kênh ion natri tim (18). LQTS di truyền trội trên NST thường với độ thấm gen không hoàn toàn (incomplete penetrance) và biểu hiện kiểu hình đa dạng (variable expressivíty) trong quần thể. LỌTS có tý lệ mắc khá cao trong dân số chung (112000- 2500 người) và là nguyên nhân phổ biến gây đột tử do rối loạn nhịp thất. Rối loạn nhịp tim cổ điển đặc trưng liên quan với LQTS là xoắn đính (tiếng Pháp: torsades de pointes – TdP) là một dạng nhịp nhanh thất đe dọa tính mạng, đặc trưng bởi sự thay đổi từ từ về biên độ và mức độ xoắn của phức bộ QRS xung quanh đường đẳng điện. TdP có thể tự kết thúc đột ngột hoặc có thể thoái triển thành rung thất, có khả năng dẫn đến tử vong. Sau khi được chẩn đoán, điều trị bằng thuốc chẹn p về CƯ bàn báo vệ khói các biến cố tim (19). LQTS có tác động đáng kể đối với mẹ và thai nhi; do đó, phát hiện trước sinh có thể làm giảm đáng kể các biến chứng và từ vong.
Ảnh hưởng đối với mẹ. Mang thai dường như có ảnh hưởng đến điện tiến, kết cục của phụ nữ bị LQTS và sự gia tăng nguy cơ cao nhất khi sinh và sau khi sinh (20). Trong các nghiên cứu cũ hơn, với một số ít phụ nữ dùng thuốc chẹn p, nguy cơ xảy ra biến cố tim lớn ở phụ nữ có nguy cơ cao được báo cáo là 3,8% trước khi mang thai, tăng lên 9% khi mang thai và 23,4% trong 9 tháng đầu sau sinh (21). Khi điều trị bằng thuốc chẹn p, nguy cơ TdP giảm đáng kể ờ phụ nữ mang thai. Tối ưu hóa nồng độ kali, magiê, canxi và vitamin D cũng đóng vai trò rất quan trọng làm giảm nguy cư bất thường nhịp. Điều quan trọng cũng cần lưu ý, đó là oxytocin thường được dùng trong chuyển dạ đã được chúng minh là kéo dài khoảng QTc và do đó về mặt lý thuyết, có thể làm tăng nguy cơ rối loạn nhịp thất ờ sân phụ bị LQTS (22,23). Tuy nhiên, oxytocin không bị chống chỉ định ở sản phụ bị LQTS và cách dùng có thể bao gồm ghi ECG nền và sau đó 1 đến 2 giờ sau khi bất đầu dùng oxytocin, ngừng sử dụng nếu khoảng QTc > 500 mili giây hoặc QTc tăng hơn 60 mili giây so với mức nên (22,23). Chỉ nên mổ lấy thai khi có chỉ định sản khoa ở những sản phụ bị LQTS được điều trị đầy đủ bằng thuốc chẹn p và không có tiền sử rối loạn nhịp tim gần đây.
Ảnh hưởng trên thai nhi. Biểu hiện bệnh LQTS có ý nghĩa nhất khi chẩn đoán trước sinh hoặc trong giai đoạn sơ sinh (24). LQTS chiếm tới 10% trường hợp thai chết lưu và hội chứng đột tử ở trẻ nhỏ (< 1 tuồi) (suddcn iníant dcath syndromc) và là nguyên nhân hay gặp nhất gây tử vong do rối loạn nhịp ờ trẻ em (25-28). Triệu chứng hay gặp nhất ở thai nhi mẳc LQTS là tần số tim thai cơ bản (baseline fetal heart rate) < bách phân vị thứ 3 so với tuổi thai (29,30). Điều quan trọng cần lưu ý là triệu chứng nhịp tim chậm này rất kín đáo và thường bị bỏ sót, trừ khi có chỉ số nghi ngờ cao với hội chứng này. LQTS thường sẽ không được chẩn đoán nếu dựa vào định nghĩa của Hiệp hội Sản phụ khoa Hoa Kỳ (ACOG) về nhịp tim chậm < 110 nhịp/phút, thay vì < bách phân vị thứ 3 theo tuổi thai (29-32). Khi thai nhi có nhịp nhanh thất và/hoặc block nhĩ thất 2:1 thì thai nhi có khả năng cao mắc LQTS, nhưng chỉ gặp ở < 25% các trường họp trước sinh (29,30,32). Khi nghi ngờ LQTS trên siêu âm trước sinh, cần phải hỏi tiền sử gia đình chi tiết đề đánh giá các cơn ngất, rối loạn nhịp ùm, hoặc các tình trạng khác có thể gợi ý LQTS có tính chất gia đình. Xét nghiệm di truyền thai nhi đối với LQTS được thực hiện thông qua thủ thuật xâm lấn và hiện chỉ giới hạn với các biến thể gia đình đã được xác định, và hiệu suất xét nghiệm đạt gần 90% các trường hợp (33).
Ngoại tâm thu nhĩ nhịp bộ đôi hoặc bộ ba dai dẳng (Persistent Atrial Bigeminy or Trigeminy)
Ngoại tâm thu nhĩ nhịp bộ đôi hoặc bộ ba dai dắng với nhịp đến sớm không dẫn truyền là một nguyên nhân khác gây nhịp tim thai chậm. Phân biệt loại nhịp tim chậm này với block nhĩ thất là cực kỳ quan trọng, bởi chúng có tiên lượng rất khác nhau. Trong cả hai trường hợp, tần số nhĩ cao hơn tần sổ thất. Trong block AV, khoảng thời gian giữa các xung nhĩ liên tiếp (consecutive atria) impulses) là khá hằng định, còn trong nhịp bộ đôi hoặc bộ ba với khoảng thời gian xung nhĩ ngắn hơn trên mỗi 2 hoặc 3 nhịp (Hình 46.11 và 46.12). Nhịp đến sớm không dẫn truyền thưởng là lành tính và có xu hướng tự thoái triển khi thai nhi tăng hoạt động.
Block nhĩ thất bẩm sinh (Congenital Atrioventricular Heart Block)
Có đến 40% các trường hợp block nhĩ thất bẩm sinh (CAVB) (Hình 46.13) xảy ra ở thai nhi bị dị tật tim bẩm sinh, đặc biệt là đồng dạng nhĩ trái (xem Chương 41) hoặc chuyển vị đại động mạch bẩm sinh có sửa chữa (congenitally corrected transposition of the great arteries) (xem Chương 38). Trong 60% còn lại, nếu không phát hiện bất thường tim cấu trúc thì block tim gần như chắc chắn là do bệnh mô liên kết (connective tissue disease) (qua trung gian miễn dịch) của người mẹ (Hình 46,14).
Trong hầu hết các trường hợp, tại thời điểm thai nhi được chẩn đoán người mẹ vẫn chưa biết là bị mắc bệnh nên cần phải tìm kiếm. CAVB gặp ờ khoảng 1/11.000 đến 1/22.000 ca sinh sống trong dân số chung và 1% đến 3% ca sinh sống ờ những thai kỳ có kháng thể kháng SSA/Ro, với nguy cư tái phát từ 14% đến 20% ở những thai kỳ này. (34-37). Đặc điểm của block tim độ 1, độ 2 hoặc độ 3 (hoàn toàn) được trình bày trong Băng 46.1.
Hầu hết các trường hợp nhịp chậm xoang và ngoại lâm thu nhĩ không dẫn truyền đều không cần phải điều trị. Thật không may, CAVB thai nhi có liên quan với bất thường tim mà không thề điều trị được trong từ cung, và khi tần số thất < 50 nhịp/phút làm gia tăng nguy cơ phù thai (xem Chương 41). CAVB có tỷ lệ tử vong cao > 70% khi kèm theo bất thường tim, trong khi tỳ lệ từ vong chi 19% ờ các trường hợp CAVB qua trung gian miễn dịch (38).
| Bảng 46.1 • Đặc điểm của Block nhĩ thất (AV) độ 1, độ 2 và độ 3 (hoàn toàn) | ||
| Block AV | Khoảng thời gian AV/dẫn truyền AV | Nhịp tim |
| Độ 1 | Kéo dài/ dẫn truyền AV 1:1 | Bình thường |
| Độ 2 – type 1 (Wenckebach) | Khoảng thời gian AV kéo dài tăng dần cho đến khi xung điện (impulse) không dẫn truyền | Thường không đều |
| Độ 2 – type 2 (Mobili) | Khoảng thời gian AV bình thường với xung điện không dẫn truyền, thường dẫn truyền 2:1 | Chậm, đều |
| Độ 3 – block AV hoàn toàn | Hoàn toàn không có sự dẫn truyền AV, phân ly nhĩ thất | Tần số thất chậm, đểu |
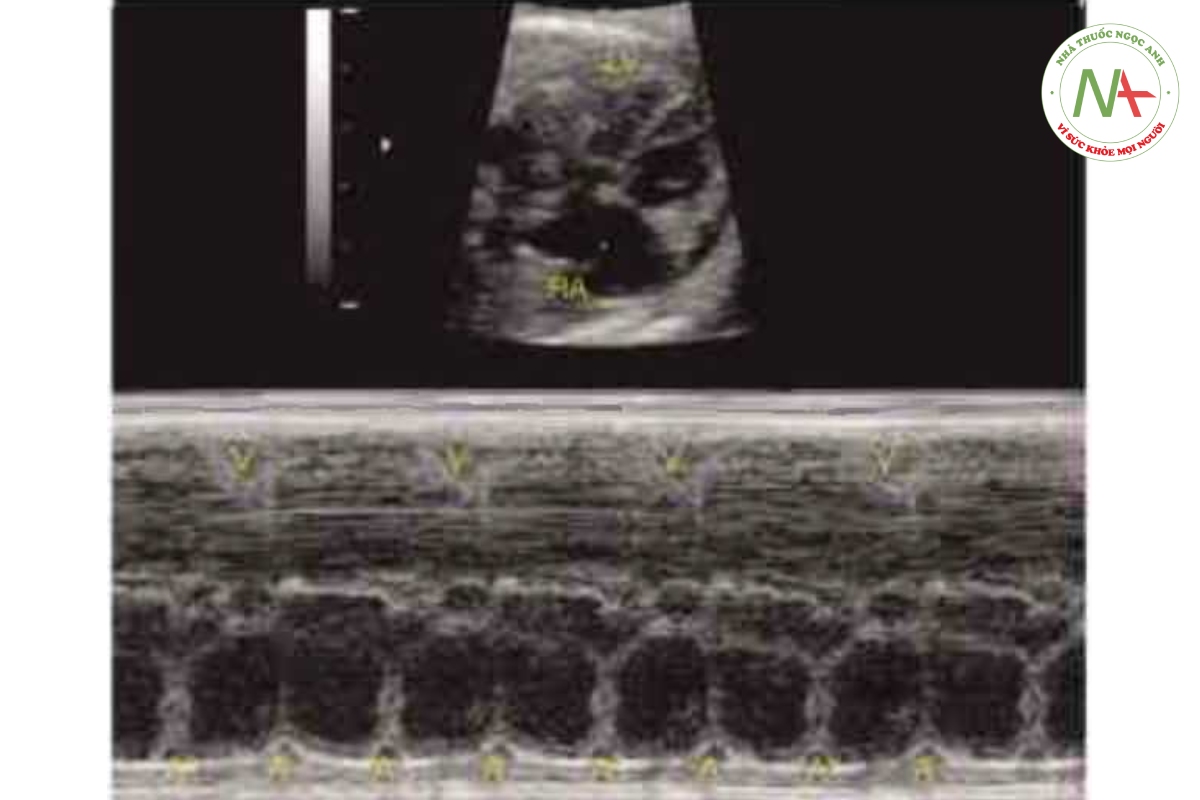
![TỔNG QUAN VỀ RỐI LOẠN NHỊP TIM THAI (FETAL ARRHYTHMIAS) 44 Hình 46.13: Bản ghi M-mode cùa một thai nhi bị block nhĩ thất hoàn toàn (CAVB). Thanh định hướng M mode cẳt qua tâm thất trái (LV) và tâm nhĩ phải (RA). Các nhát tâm nhĩ co bóp (mũi tên thẳng) có nhịp đều và tần số bình thường. Các nhát tâm thất co bóp (V) (mũi tên chếch) có tần số chậm hơn, phân ]y với các nhát tâm nhĩ co bóp. Thai nhi này có đồng dạng trái kèm bất thường tim.](https://nhathuocngocanh.com/wp-content/uploads/2024/01/TONG-QUAN-VE-ROI-LOAN-NHIP-TIM-THAI-FETAL-ARRHYTHMIAS-13.jpg)
Block tim nhĩ thất bẩm sinh qua trung gian miễn dịch (mmune-Mediated Congenital Atrioventricular Heart Block)
Cơ chế bệnh sinh. Cơ chế bệnh sinh của CAVB qua trung gian miễn dịch được cho là do đáp ứng viêm và tổn thương cơ tim và hệ thống dẫn truyền tim ờ những thai nhi nhạy cảm (susceptible fetuses), khởi đầu bằng việc các kháng thể lưu hành trong máu mẹ qua nhau thai bắt đầu từ 12 tuần tuổi. Hầu hết các trường hợp CAVB qua trung gian miễn dịch được phát hiện từ 18 đến 25 tuần tuổi thai (39). Tổn thương tim trong CAVB qua trung gian miễn dịch bao gồm rối loạn chức năng cơ tim, bệnh cơ tim, xơ chun nội tâm mạc (endocardial libroelastosis) và bất thường dẫn truyền (40). Hiệu giá kháng thể kháng SSA/Ro dường như đóng một vai trò đáng kể trong nguy cơ phát triển bệnh, với hiệu giá > 100 U/mL có liên quan với 85% nguy cơ CAVB (41). Bệnh cơ tim dãn muộn (Delayed dilated cardiomỵopathy) làm xấu đi đáng kể tiên lượng lâu dài, gặp ở 11 % trẻ mắc CAVB qua trung gian miễn dịch, mặc dù đã đặt máy tạo nhịp thành công (40,42).
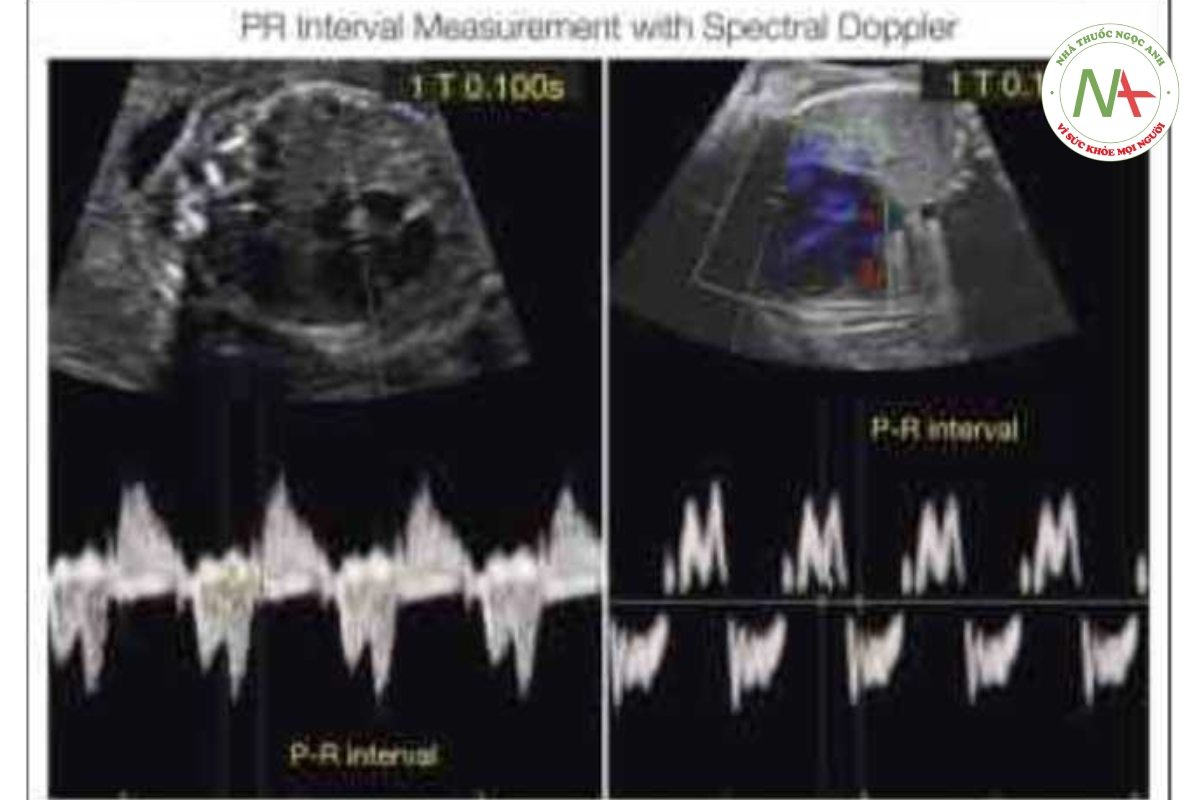
Sàng lọc trước sinh. Có thể sàng lọc CAVB trước sinh bằng cách đánh giá khoáng PR cơ học, được đo bằng Doppler xung với siêu âm tim thai nối tiếp từ 16 đến 24-28 tuần tuổi thai. Khoảng PR cơ học, bao gồm pha có đẳng tích (isovolumetric contraction phasc) cùa tâm thất, dài hơn khoảng PR điện (43) và giá trị bình thường ở thai nhi là 0,12 ± 0,02 giây khi đo từ vùng van hai lá / van động mạch chủ (Hình 46.15) (44). Block độ 1 được chẩn đoán khi khoảng PR van hai lá / van động mạch chủ của thai nhi > 150 mi li giây (45,46). Điều quan trọng cần lưu ý là chẩn đoán block độ 1 bằng khoáng PR cơ học là một tình trạng có thể thay đổi, vì hầu hết các thai nhi sẽ không tiến triển thành block tim độ 2 hoặc độ 3. Trong một nghiên cứu phát hiện các dấu hiệu block tim độ l ờ 8 thai nhi sử dụng khoảng PR, chỉ thai nhi tiến triển thành CAVB; 1 thai nhi khác đã chuyển từ block ở 2 sang độ 1 sau khi điều trị bằng betamethasone, nhưng 6 thai nhi còn lại đã tự phục hồi lại nhịp xoang bình thường trước hoặc sau khi sinh mà không cần điều trị gì (47). Hơn nữa, chẩn đoán block tim độ 3 thường không có block tim độ 1 hoặc độ 2 diễn ra trước đó, và có thể phát triển rất nhanh từ nhịp xoang bình thường trong vòng < 1 tuần (7,46-48). Gần đây, Cuneo và cộng sự đã đề xuất phương pháp theo dõi tim thai tại nhà 2 lần/ngày được thực hiện bởi bệnh nhân bằng thiết bị Doppler tại nhà như một cách giám sát khả thi đối với thai kỳ phơi nhiễm với kháng thể kháng Ro (49). Khi phát hiện có bất thường nhịp tim thai, cần phải siêu âm tim chẩn đoán trong vòng vài giờ sau đó. Chúng tôi tin rằng
theo dõi nhịp tim thai 2 lần/ngày là một cách tiếp cận đầy hứa hẹn giúp sàng lọc CAVB, và hiện đang được đánh giá trong các nghiên cứu tiền cứu lớn.
Hiện chưa có hướng dẫn dựa trên bằng chứng và đáng tin cậy để dự đoán thai nhi sẽ phát triển block tim trong trường hợp mẹ có kháng thể kháng SSA/Ro. Trong một cuộc khảo sát với một nhóm 49 bác sĩ và nhà nghiên cứu quốc tế có mối quan tâm đặc biệt đến thai kỳ và sức khỏe sinh sản ờ phụ nữ mắc bệnh thấp khớp, 80% đề nghị làm soát bằng siêu âm tim thai nối tiếp, với hầu hết bắt đầu từ 16 tuần tuổi thai (50). Đối với những thai phụ chưa từng có con bị lupus sơ sinh, 44% đề nghị siêu âm tim thai cách tuần và 28% đề nghị siêu âm tim thai hàng tuần. Đối với những thai phụ đã có con trước đó bị lupus sơ sinh, 80% đề nghị siêu âm tim thai hàng tuần (50). Do đó, với những dữ liệu hạn chế hiện có, chúng tôi tin rằng sàng lọc bằng siêu âm tim thai hàng tuần bắt đầu từ 16 cho đến 24-28 tuần tuổi thai ớ những thai phụ có kháng thể kháng SSA/Ro. Siêu âm tim thai bao gồm đo khoảng PR đồng thời đánh giá ,xem có hở van ba lá. bệnh cơ tim dãn, xơ chun nội lâm mạc (endocardial fibroelastosis) và giảm chức năng tim hay không. Theo dõi nhịp tim thai tại nhà là một công cụ đầy hứa hẹn và nên chờ kết quả của thử nghiệm đang diễn ra trước khi ứng dụng trên lâm sàng.
Quản lý
Hiện nay đã có bằng chứng xác thực ủng hộ việc sử dụng hydroxychloroquine (HCQ) nhằm làm giảm nguy cư tái phát CAVB và bệnh cơ tim dãn ở những thai kỳ có kháng thể kháng SSA/Ro. Dữ liệu tổng hợp từ một nỗ lực quốc tế cho thấy rằng những thai phụ có nguy cơ cao sinh con bị CAVB, sử dụng HCỌ có thể phòng ngừa bệnh tái phát ờ lần mang thai sau (51). Trong 257 thai phụ có SSA/Ro dương tính, trong đó 40 thai phụ phơi nhiễm với HCQ và 217 thai phụ không phơi nhiễm với HCQ (phơi nhiễm HCQ được định nghĩa là HCỌ được dùng liên tục trong suốt thai kỳ bắt đầu trước 10 tuần tuổi thai), tỷ lệ tái phát lupus sơ sinh với biểu hiện tại tim ờ thai nhi phơi nhiễm với HCQ là 7,5% so với 21,2% ờ nhóm không phơi nhiễm (51) không có trường hợp nào tử vong ở thai kỳ phơi nhiễm HCQ so với tỷ lệ tử vong 21,7% ờ nhóm không phơi nhiễm (51). Nhiều dữ liệu gần đây xác nhận lợi ích dự phòng của HCQ giúp làm giảm nguy cơ biểu hiện tại tim của kháng thể kháng SSA/Ro ở những thai kỳ nguy cơ cao với tiền sừ > 1 thai nhi / trẻ sơ sinh bị ánh hường (52).
Điều trị thai kỳ có CAVB qua trung gian miễn dịch đã được đề xuất bao gồm steroid chứa fluor như betamethasone hoặc dexamethasone, globulin miễn dịch tiêm tĩnh mạch (1VIG), và/hoặc p-mimeticus làm tăng cung lượng tim thai nhi. Cơ sở lý luận cho việc sử dụng các steroid chứa íluor bao gồm đặc tính chống viêm và đi qua nhau thai với số lượng đủ để có tác dụng trên thai nhi. Tuy nhiên, hiện đang thiếu dữ liệu chắc chắn về hiệu quả khách quan của các steroid chứa fluor từ các nghiên cứu tiến cứu lớn hoặc thử nghiệm lâm sàng. Một số nghiên cứu cho thấy hiệu quả của các steroid chứa fluor trong việc cải thiện các bất thường dẫn truyền, chức năng tim và đôi khi cả phù thai, và tăng tỷ lệ sống sót (53,54). Có một số đồng thuận giữa các chuyên gia cho rằng sử dụng steroid chứa flour trong quản lý CAVB độ 3 có lợi ích hạn chế nhất. Một tổng quan hệ thống và phân tích gộp gần đây về hiệu quả của steroid chứa flour trên sự tiến triển chung của CAVB độ 2 thành CAVB độ 3 liên tục hoặc ngắt quãng (intermittent) khi sinh phát hiện rằng tỷ lệ tiến triển ở thai nhi được điều trị bằng steroid là 52% so với 73% ở những người không được điều trị (55). Tuy nhiên, tỳ lệ thoái lui chung thành block độ 1, hoặc độ 1 / 2 ngắt quãng hoặc nhịp xoang ờ thai nhi được điều trị bằng steroid không có sự khác biệt so với nhóm chứng (55). Các tác giả kết luận rằng vẫn còn hạn chế bằng chứng về lợi ích của việc sử dụng steroid chứa fluor trong việc ảnh hưởng đến kết quả của thai nhi mắc CAVB qua trung gian miễn dịch độ hai (55). Trong cùng một cuộc khảo sát với một nhóm 49 bác sĩ và nhà nghiên cứu quốc tế được mô tả trước đó, khi được hỏi về các loại thuốc dùng để điều trị CAVB ở phụ nữ mang thai > 20 tuần tuổi có kháng thể kháng Ro, đối với CAVB độ 2, 88% những người trả lời đề nghị dùng dexamethasone, và đối với CAVB độ 3, những người trả lời đề nghị dùng dexamethasone (55%) hoặc IV1G (33%), mặc dù có 27% sẽ không điều trị gì (50). Hiện tại, khi không có bằng chứng chắc chắn đề hướng dẫn quản lý thì có lẽ là hợp lý khi tuân theo các khuyến cáo đã được công bố vào năm 2014 bởi Hiệp hội Tim mạch Hoa Kỳ (AHA) (56). AHA khuyến cáo như sau:
- Có thể xem xét thử nghiệm dexamethasone (trial of dexamethasone) (4-8 mg/ngày) đối với Block AV độ 2 hoặc Block AV độ 1 kèm theo ít nhất 1 dấu hiệu viêm ờ tim (thành tim tăng âm, hở van tim, rối loạn chức năng tim, tràn dịch màng ngoài tim, v.v.) để ngăn ngừa tiến triển thành CAVB, mặc dù lợi ích vẫn chưa được khẳng định chắc chắn.
- Cũng có thể xem xét điều trị bằng dexamethasone cho thai nhi có CAVB và không bị suy tim với mục tiêu cải thiện tỷ lệ sống sót hoặc giảm tỷ lệ bệnh cơ tim dãn, mặc dù lợi ích vẫn chưa được khẳng định chắc chắn vì các nghiên cứu cho đến nay đều mang tính hồi cứu, không phải ngẫu nhiên và quá trình theo dõi không đầy đủ.
- Có thể xem xét IVIG (1 g/kg cân nặng mẹ, liều toi đa 70 g mỗi 2-3 tuần), thường được dùng với dexamethasone vì nó giúp cải thiện tỷ lệ sống sót khi có xơ chun nội tâm mạc (cedocardial fibroelastosis) hoặc rối loạn chức năng tâm thu trong một nghiên cứu hồi cứu đa trung tâm.
- Sử dụng thuốc cường giao cảm p (terbutaline và salbutamol) được xem là hợp lý khi nhịp tim thai < 55 nhịp/phút hoặc với tần số tim thai cao hơn nếu có triệu chứng suy tim hoặc phù thai.
- Không khuyến cáo sử dụng dexamethasone như là điều trị dự phòng ờ các thai kỳ có nguy cơ.
- CAVB đơn độc, vô căn, huyết thanh âm tính được xem là có tiên lượng tốt hơn CAVB huyết thanh dương tính và có thể chỉ cần theo dõi mà không cần điều trị kháng viêm.
- Tác dụng phụ của dexamethasone có thể bao gồm thai giới hạn tăng trưởng (fetal growth restriction), thiếu ối, co thắt ống động mạch (ductal constriction), đái tháo đường ờ mẹ và tác dụng phụ trên hệ thần kinh trung ương.
- Vì có những rủi ro đáng kể và dữ liệu hạn chế về lợi ích nên cần tư vấn kĩ lưỡng cho thai phụ trước khi bắt đầu dùng dexamethasone. và nên ngừng thuốc nếu xuất hiện các tác dụng phụ đáng kế đối với mẹ hoặc thai nhi.
=> Đọc thêm: Xác định tỷ lệ mất đoạn AZF ở bệnh nhân nam vô tinh hoặc thiểu tinh bằng phương pháp QF – PCR.