Kỹ thuật y khoa
Tóc và da đầu. Nguyên nhân và các cách điều trị.
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
Nhà thuốc Ngọc Anh – Chương 29: Tóc và da đầu.
Tác gải: Margo Gkini, Mario Goisisvà Sara Izzo
Nguồn sách: Sách: Quy trình PRP và Tiêm cấy mỡ nâng cao -Tác giả: Dr: Mario Goisis
PRP và chứng rụng tóc nội tiết tố
Huyết tương giàu tiểu cầu (PRP) đã thu hút sự chú ý đáng kể trong các lĩnh vực kỹ thuật mô, chữa lành vết thương và tăng sinh mạch trong những thập kỷ qua [1–2]. Hiệu quả tái tạo của PRP phụ thuộc vào các yếu tố tăng trưởng (GFs) được giải phóng khi kích hoạt tiểu cầu, những yếu tố này dường như giúp tăng cường sự hình thành mạch, tái cấu trúc chất nền ngoại bào và các hiệu ứng tế bào như tăng sinh và biệt hóa tế bào [1, 3–5]. Năm 2006, Uebel và cộng sự đã sử dụng PRP trong quá trình cấy tóc ở bệnh nhân nam bị chứng rụng tóc nội tiết tố nam [3, 6–8]. Sau đó, các thử nghiệm tiếp theo được theo dõi, đánh giá hiệu quả của PRP trong chứng rụng tóc nội sinh tố ở cả nam và nữ.
Các yếu tố tăng trưởng
Các yếu tố tăng trưởng chính (GFs) liên quan đến chứng rụng tóc nội sinh là các yếu tố tăng trưởng có nguồn gốc từ tiểu cầu (PDGF), các yếu tố tăng trưởng biến đổi (TGF), các yếu tố tăng trưởng nội mô mạch máu (VEGF) và các yếu tố tăng trưởng giống insulin (IGF) cùng với các đồng dạng của chúng [9–12]. Sau khi liên kết với các thụ thể tương ứng của chúng trong vùng phình ra của nang lông, GFs kích hoạt sự tương tác giữa chúng và các loại tế bào khác nhau. Cụ thể, trong khu vực phình ra, các tế bào gốc nguyên thủy có nguồn gốc từ ngoại bì phân hóa thành biểu bì và tế bào tuyến bã nhờn được tìm thấy. Trong chất nền, các tế bào mầm có nguồn gốc trung mô được tìm thấy trong nhú bì. Hai loại tế bào này, cùng với các yếu tố tăng trưởng, tương tác và kích hoạt giai đoạn tăng sinh của sự phát triển của tóc, tạo ra đơn vị nang tóc trong tương lai [6].
Nhiều loại tế bào khác nhau, chẳng hạn như tế bào nội mô và tế bào sừng, tạo ra PDGF, là chất cơ bản cho sự phát triển và tăng sinh của tế bào. Trong ống nghiệm, các cytokine, được chứng minh là chất điều hòa tích cực và tiêu cực đối với hoạt động tăng trưởng của HF, sửa đổi sự biểu hiện của các đồng dạng PDGF trong HF [13]. Hơn nữa, PDGF gây ra và duy trì giai đoạn anagen trong chu kỳ lông chuột [14]. Tín hiệu PDGF tham gia vào cả tương tác giữa biểu bì – nang và trung bì cần thiết cho sự hình thành tóc [15].
TGF-b1 cảm ứng androgen từ các tế bào DP là một chất trung gian nội tiết ức chế trong chứng rụng tóc nội tiết tố. Do đó, người ta đã chứng minh rằng sự tiến triển của chứng rụng tóc nội tiết tố (AGA) có liên quan đến nồng độ androgen và TGF-b1. Các yếu tố tăng trưởng nội mô mạch máu dường như là nhân tố trung gian chính cho sự phát triển và chu kỳ của HF, cung cấp bằng chứng trực tiếp cho thấy sự tái tuần hoàn nang trứng được cải thiện thúc đẩy sự phát triển của tóc.
Yếu tố tăng trưởng giống insulin 1 (IGF-I) dường như cũng đóng một vai trò quan trọng trong việc thúc đẩy sự phát triển của tóc. IGF-I, được sản xuất bởi các tế bào DP, hoạt động trên thụ thể IGF-I của tế bào sừng, thúc đẩy sự phát triển của tóc thông qua việc kích thích sự gia tăng của tế bào sừng trong HFs. Trong một số báo cáo, IGF-I và IGF-II đã ngăn không cho HF có được trạng thái giống như catagen, Sheong và cộng sự cho thấy IGF-I có ảnh hưởng đáng kể đến tốc độ mọc tóc tuyến tính và kéo dài giai đoạn anagen tổng thể [5].
Rụng tóc nội tiết tố
Rụng tóc nội tiết tố là một chứng rụng tóc mãn tính phổ biến, ảnh hưởng đến cả hai giới. Mức độ phổ biến của nó tăng lên theo độ tuổi, mặc dù thực tế là nó có thể bắt đầu ở tuổi dậy thì. Không phân biệt tuổi tác và giới tính, rụng tóc dẫn đến suy giảm đáng kể chất lượng cuộc sống ở những bệnh nhân được chẩn đoán mắc chứng rụng tóc nội tiết tố, vì tóc là một đặc điểm quan trọng của hình ảnh, sự quyến rũ và sự tự tin. Mặc dù chứng rụng tóc nội tiết tố là gánh nặng cho cả nam và nữ, nhưng đối với phụ nữ thì điều đó lại khiến phụ nữ lo lắng hơn. Nhiều sản phẩm đã được đề xuất và sử dụng như các liệu pháp trị rụng tóc. Các liệu pháp điều trị bằng thuốc, được Cục Quản lý Thực phẩm và Dược phẩm (FDA) phê duyệt, để điều trị AGA bao gồm minoxi-dil và Finasteride. Cả hai đều có thể được sử dụng một mình hoặc kết hợp [16]. Mặc dù các lựa chọn điều trị có sẵn, mức độ hài lòng và tuân thủ điều trị của bệnh nhân thấp cũng như nhiều tác dụng phụ, đã làm cho nhu cầu nghiên cứu trong lĩnh vực điều trị mới AGA mới trở nên cấp thiết. [16, 17].
Điều trị với PRP
Vì PRP có thể đóng vai trò là một phương pháp điều trị tiềm năng cho AGA, nên một quy trình sử dụng tiêm PRP, với kết quả đáng khích lệ, được đề xuất ở đây.
Lựa chọn bệnh nhân và chẩn đoán
Những bệnh nhân mắc chứng rụng tóc giai đoạn đầu theo thang điểm Norwood-Ham-ilton cho nam giới và thang điểm Ludwig cho nữ giới là những ứng cử viên hoàn hảo để điều trị bằng phương pháp PRP. Cần loại trừ những bệnh nhân có hiện tại hoặc tiền sử tăng cường miễn dịch (bệnh ác tính, hóa trị liệu, liệu pháp steroid), bệnh lý liên quan đến da đầu, rối loạn tự miễn dịch, rối loạn huyết học và hội chứng rối loạn chức năng tiểu cầu. PRP, do thực tế là tự thân, có thể gây ra phản ứng tự miễn dịch ở bệnh nhân tự miễn dịch. Tuy nhiên, nó đã được sử dụng như một phương pháp điều trị chứng rụng tóc từng mảng với kết quả đáng khích lệ. Các tiêu chí loại trừ khác bao gồm xu hướng sẹo lồi và điều trị kháng đông. Nếu bệnh nhân đang sử dụng aspirin hoặc các thuốc chống viêm không steroid khác, họ nên tạm ngưng loại thuốc này trong 7 ngày trước khi điều trị. [17].Chẩn đoán rụng tóc nội tiết tố ở tất cả bệnh nhân phải dựa trên tiền sử bệnh chi tiết (bất kỳ loại thuốc nào gây rụng tóc), khám lâm sàng kỹ lưỡng, xét nghiệm và soi ba chiều. Các thử nghiệm trong phòng thí ng-hiệm nên bao gồm (a) CBC; (b) sắt huyết thanh, ferritin huyết thanh, và TIBC (tổng khả năng gắn kết với sắt); (c) axit folic; (d) T3, T4, TSH, fT3, fT4 và chất chống TPO; (e) VDRL; và (f), đối với phụ nữ, nên thực hiện cấu hình của nữ giới (DHEA, testosterone, androstene-dione, prolactin, kích thích nang trứng và hor-mone tạo hoàng thể) [18, 19]. Tiêu chuẩn nội soi để chẩn đoán chứng rụng tóc nội tiết tố bao gồm:
(a) Đa dạng về đường kính của lông, do sự thu nhỏ của các nang lông. Sự thay đổi hơn 20% của đường kính sợi tóc là một trong những dấu hiệu chẩn đoán tình trạng này.
(b) Các dấu hiệu xung quanh.
(c) Chấm vàng.
(d) Sự phát triển của các sợi lông đơn lẻ trong nang lông, thay vì 2–3 sợi lông [19].Trong trường hợp có vấn đề chẩn đoán phân biệt, sinh thiết có thể được tư vấn.
Chuẩn bị PRP
Theo thư viện quốc tế, huyết tương giàu tiểu cầu được sản xuất bằng các phương pháp khác nhau để cô đặc tiểu cầu thông qua ly tâm và tách tế bào. Có một số hệ thống có sẵn trên thị trường. Sự khác biệt cũng được quan sát thấy trong môi trường hoạt hóa của nó, với canxi clorua và canxi gluconat là những chất phổ biến nhất. Kết quả là, sự tập trung tiểu cầu và yếu tố tăng trưởng khác nhau xảy ra, do đó dẫn đến các kết quả khác nhau trong quá trình thử nghiệm [5]
Chúng tôi đặc biệt khuyến khích sử dụng các bộ dụng cụ đã được phê duyệt để chuẩn bị PRP. Chuẩn bị thủ công có thể không đạt được mức tiểu cầu mong muốn và có thể dẫn đến kết quả kém, không thể tái tạo và không thể so sánh được.
Để chuẩn bị PRP, có thể sử dụng Regen-Kit BCT-3 (RegenLab SA®, Le Mont-sur-Laus-anne, Thụy Sĩ). Ban đầu, máu toàn phần được thu thập từ tĩnh mạch trước ổ mắt của bệnh nhân (16 ml). Sau đó, máu được cho vào hai ống (Regen BCT) và được ly tâm trong 5 phút ở 1500 g bằng máy ly tâm phòng thí nghiệm RegenA-PRPCentri. Mỗi ống chứa một gel thixotropic bao gồm hỗn hợp các polyme để tách huyết tương (loại bỏ hồng cầu) và dung dịch natri xitrat, như một chất chống đông máu, nằm phía trên gel phân tách. Do đó, sau khi ly tâm, máu được phân đoạn, với các tế bào hồng cầu bị mắc kẹt dưới gel và các phần tử tế bào lắng trên bề mặt của gel. Nội dung được tiếp tục bằng một loạt các ngược nhẹ nhàng của ống. Tổng sản lượng PRP sau đó được nạp vào ống tiêm 1 ml, sẵn sàng để tiêm. Quá trình hoạt hóa bao gồm việc bổ sung canxi gluconat theo tỷ lệ 1: 9 (0,1 ml canxi gluconat trên 0,9 ml PRP) [17].
Ứng dụng PRP
Trước khi áp dụng PRP, da đầu được làm sạch bằng cách phun 0,1% octenidine-hydro-chloride. Gây tê tại chỗ có thể được áp dụng nếu bệnh nhân cảm thấy đau đớn mà họ không thể chịu được. Sau đó, PRP (0,05–0,1 ml / cm2) được tiêm, sử dụng kim 27-G hoặc 30,5-G, vào các khu vực liên quan đến andro-gen (trán, đỉnh, chẩm) của da đầu ở nam giới và vào các vùng có vấn đề ở phụ nữ, sử dụng ống tiêm BD-Luer-LokTM 1 ml. Kỹ thuật quấn tã có thể được thực hiện [17]. Trên cơ sở kinh nghiệm của các tác giả, súng mesotherapy cũng có thể được sử dụng để có độ chính xác cao hơn về độ sâu, ít đau hơn và ít chất thải sản phẩm hơn (ví dụ: U-225®). Phác đồ bao gồm ba đợt điều trị cách nhau 21–28 ngày. Sáu tháng khi bắt đầu điều trị, một phiên tăng cường cũng nên được thực hiện [17].
Kết quả
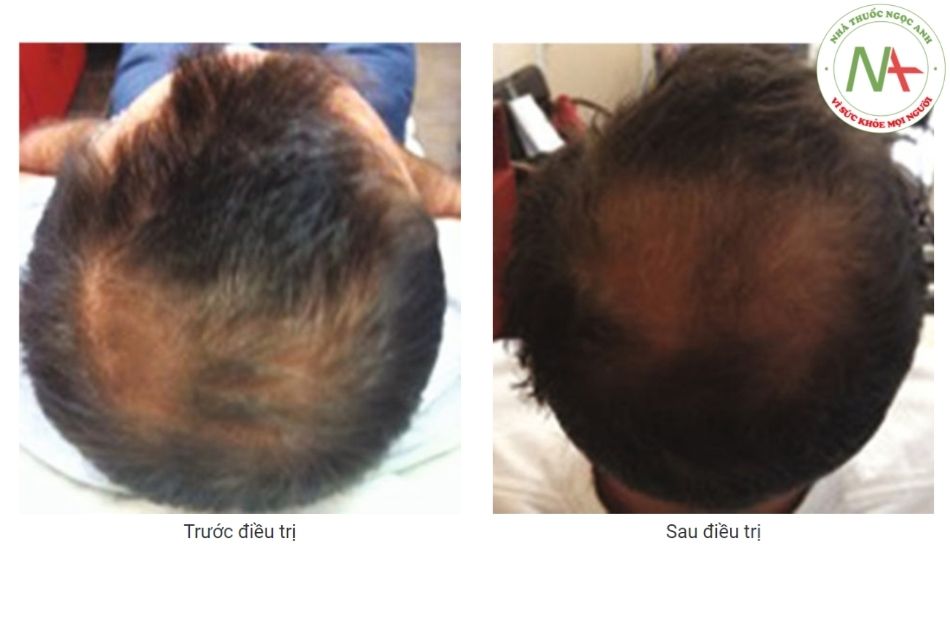
Sau khi áp dụng PRP, rụng tóc giảm. Sự gia tăng về số lượng tóc trung bình, về đường kính tóc trung bình và mật độ tóc cũng được nhận thấy. Sự cải thiện về số lượng và độ che phủ của tóc cũng có thể xảy ra cũng như tăng cường chất lượng tóc, theo đánh giá chủ quan của bệnh nhân [5].
Bệnh nhân rụng tóc nội tiết tố trước khi điều trị. Cùng một bệnh nhân lúc 3 tháng.
Nhiều chấm đen có thể được ghi nhận.
Tác dụng ngoại ý
Do bản chất tự thân của PRP và sự chuẩn bị thích hợp của nó, việc chuẩn bị cẩn thận không có tác dụng phụ đáng kể nào được ghi nhận, ngoại trừ đau nhẹ khi ứng dụng và nhạy cảm của da đầu. Không có trường hợp nhiễm trùng, nốt sần hoặc u nang [5, 17].
Điều trị kết hợp đơn trị liệu.
Theo các tác giả, mặc dù có những kết quả đáng khích lệ của điều trị PRP trong bệnh rụng tóc do di truyền nội tiết tố, nhưng liệu pháp đơn trị liệu vẫn được đưa ra trong giai đoạn đầu của chứng rụng tóc hoặc như một hình thức ngăn chặn. Trong trường hợp bệnh tiến triển, bác sĩ nên sử dụng PRP như một chất hỗ trợ điều trị hiệu quả với thuốc thông thường, chẳng hạn như minoxidil hoặc Fin-asteride. Bản chất tự thân của nó, khả năng phục hồi và không có tác dụng phụ, là một lựa chọn tuyệt vời cho những bệnh nhân có các tác dụng phụ do các bệnh rụng tóc khác hoặc phụ nữ trong độ tuổi sinh đẻ.
Kết luận
Mặc dù mối quan tâm ngày càng tăng đối với y học tái tạo, rất ít tài liệu về các thử nghiệm điều tra hiệu quả của PRP đối với sự phát triển của tóc đã được công bố. Hầu hết các nghiên cứu được xem xét đều đưa ra một số thiếu sót về phương pháp luận nghiêm trọng. Các sai sót chính bao gồm thiếu sự phê duyệt khoa học đối với các thiết bị được sử dụng để chuẩn bị PRP, thiếu giao thức tham chiếu về tần suất ứng dụng, cũng như các chỉ dẫn về lượng PRP được đưa vào, sự không đồng nhất trong mô tả các chế độ ứng dụng, thiếu kiểm soát, kích thước nhỏ các nhóm mẫu, thiếu các báo cáo chi tiết về đặc điểm của bệnh nhân và các phương pháp thống kê đã áp dụng. Hơn nữa, rất ít nghiên cứu đề cập đến các biện pháp an toàn để áp dụng cho PRP. Huyết tương giàu tiểu cầu có thể trở thành một tài sản hữu ích để điều trị chứng rụng tóc nội tiết tố nam. Tuy nhiên, nó vẫn là một hình thức trị liệu gây nhiều tranh cãi. Cần khẩn cấp các thử nghiệm mù ngẫu nhiên, lớn hơn, có đối chứng, với các thiết bị được phê duyệt để chuẩn bị PRP, cũng như dữ liệu dựa trên bằng chứng liên quan đến các thông số chỉ ra nồng độ, liều lượng và hiệu quả lâm sàng của chúng. Phương pháp mà chúng tôi trình bày ở đây rất dễ áp dụng và mang lại kết quả đáng khích lệ khi bệnh nhân có liên quan.
ADSC và tăng trưởng tóc
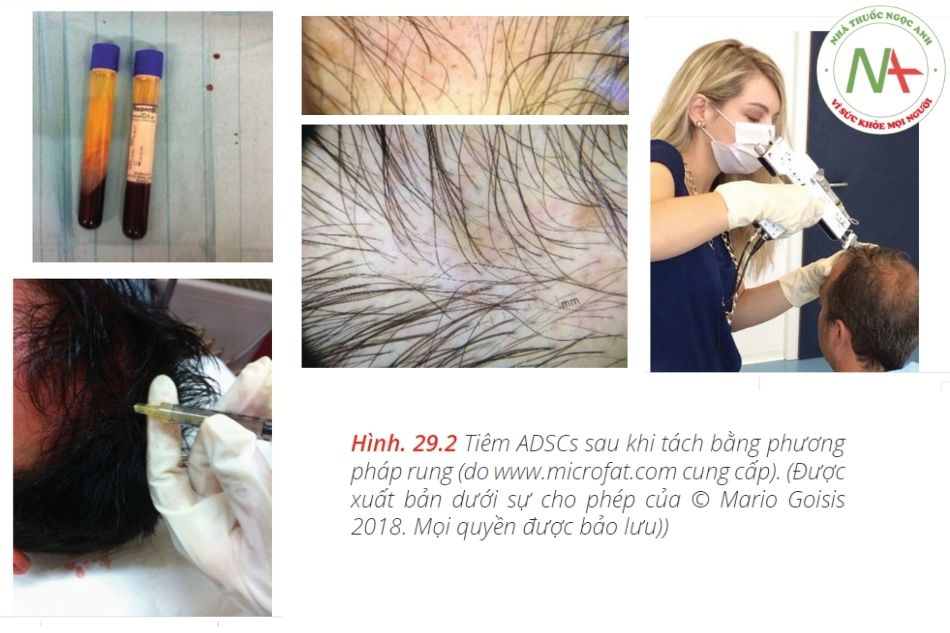
Một số báo cáo đã chỉ ra rằng các yếu tố tăng trưởng như PDGF, HGF, VEGF và fibronectin, làm tăng sự phát triển của lông ở các mô hình động vật và lâm sàng [20–24].Để hiểu liệu các tác động nội tiết của ADSC có thể thúc đẩy sự phát triển của tóc ở người hay không, Won và cộng sự đã nghiên cứu ảnh hưởng của ADSC đối với sự gia tăng của tế bào nhú da ở người được nuôi cấy (hDPCs) [20]. Điều trị bằng ADSCS cải thiện đáng kể sự tăng sinh của hDPC lên đến 130% sau 48 giờ. Nghiên cứu động vật trên chuột khỏa thân đã thiết lập những kết quả này. Đặc biệt, về mặt mô học, da trên lưng của những con chuột được điều trị bằng ADSC-CM cho thấy số lượng nang lông tăng lên. Nghiên cứu này gợi ý rằng ADSCs thúc đẩy sự phát triển của tóc (Hình 29.1 và 29.2).
Gần đây, có báo cáo rằng điều trị bằng phương tiện ADSCs (ADSC-CM) có hiệu quả đối với chứng rụng tóc kiểu phụ nữ (FPHL). Một nghiên cứu quan sát, hồi cứu về kết quả ở 27 bệnh nhân FPHL được điều trị bằng AD-SC-CM đã được hình thành. Các tác giả đã sử dụng microneedles để cho phép ASC-CM thâm nhập vào da người. Để đánh giá hiệu quả của phương pháp điều trị, bệnh án của bệnh nhân và hình ảnh đồ họa ba chiều đã được phân tích.
ASC-CM đã chứng minh hiệu quả của nó trong điều trị FPHL sau 12 tuần điều trị [25]. Ví dụ, độ dày của tóc và mật độ tóc được cải thiện đáng kể, và không có bệnh nhân nào báo cáo phản ứng phụ.Fukuoka và Suga cũng báo cáo tác dụng của một sản phẩm chứa dung dịch protein của môi trường điều hòa tế bào gốc có nguồn gốc từ mỡ trong việc tái tạo tóc. Sản phẩm được tiêm trong da trong 22 trường hợp rụng tóc [26]. Những bệnh nhân này được điều trị sáu lần sau mỗi 3-5 tuần, và tóc tăng lên đáng kể ở cả bệnh nhân nam và nữ.
Điều trị tóc bằng phuương pháp ghép da
Chỉ định
Rụng tóc. Vì các bác sĩ da liễu và bác sĩ chuyên khoa không được phép lấy mỡ ở một số quốc gia theo luật và quy định cụ thể, nên mô tả kỹ thuật ghép da xâm lấn tối thiểu (www.dermalgraft.com). Cả vùng cho, vùng nhận đều là lớp hạ bì. Liều lượng tối thiểu gây tê tại chỗ được tiêm: 32mg lidocain. Để so sánh, đó là một lượng lidocain tương tự lượng được tiêm với một liều Ceftriaxone (thông thường 1gram ceftriaxone được pha loãng trong 3,5 ml Dung dịch Lidocain 1%, là 35mg lidocain)
Thời gian phẫu thuật
Quy trình này thường mất 10 phút
Vật liệu
• Bộ ghép da (www.dermalgraft.com)
•Một kim dài 27-G, dài 3 cm
• 40 cc dung dịch Klein
• 100 cc dung dịch muối
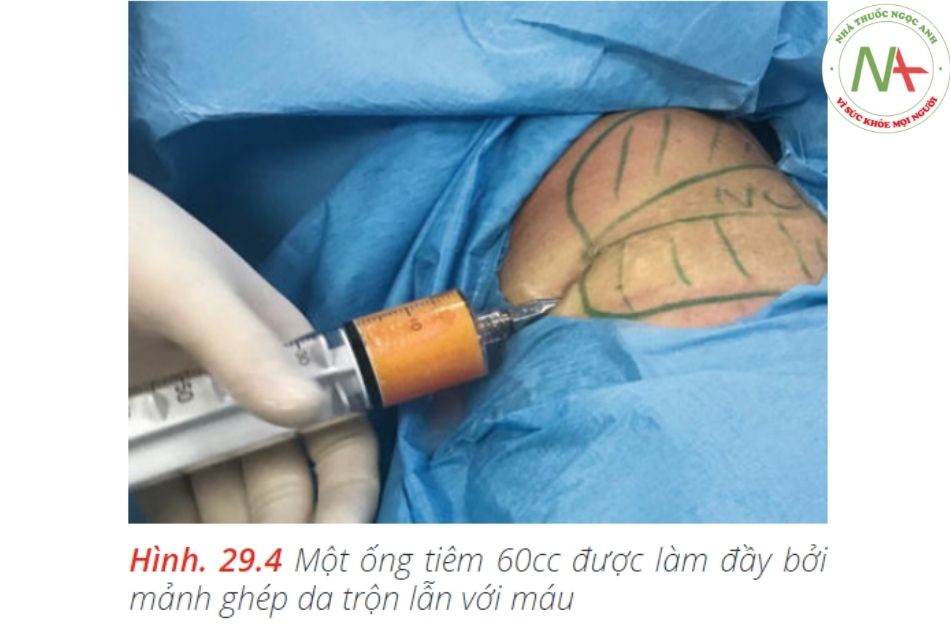
Quy trình
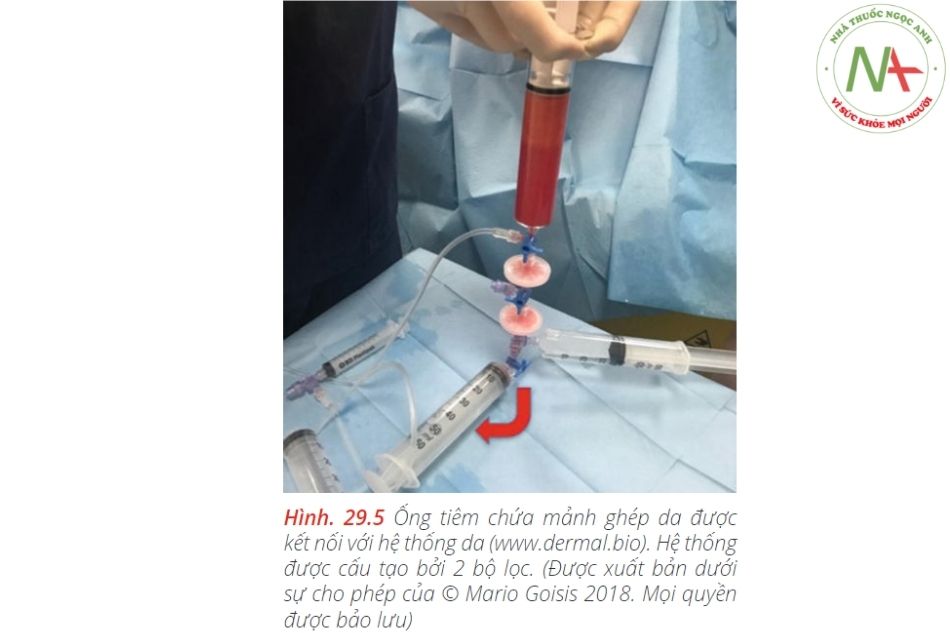
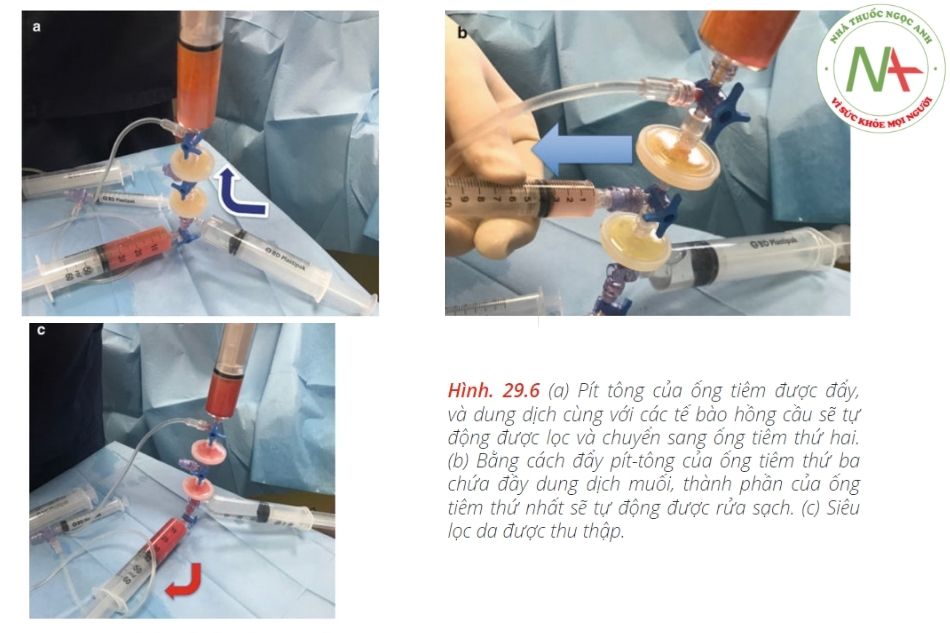
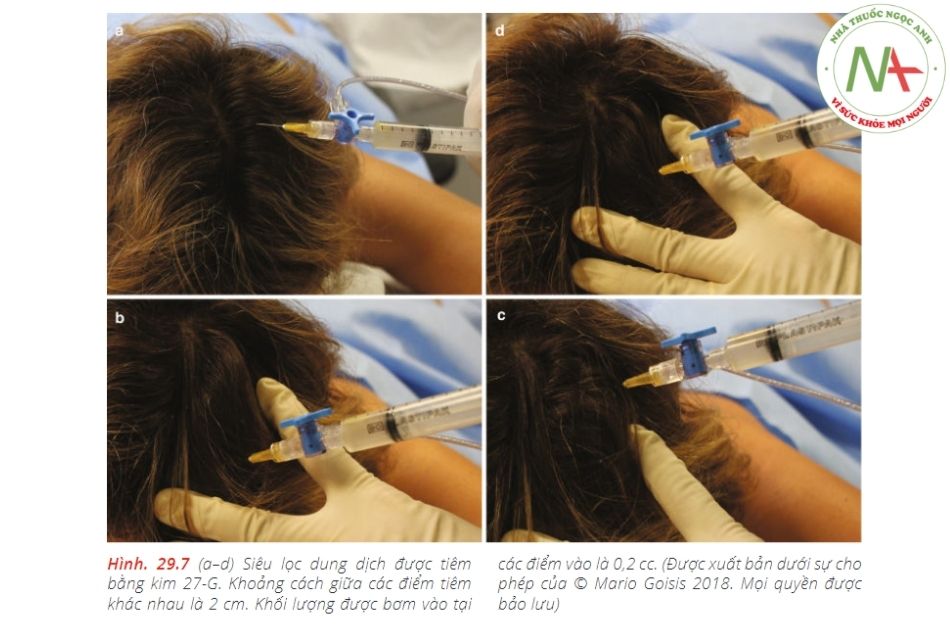
Quy trình được minh họa trong Hình. 29,3, 29,4, 29,5, 29,6a – c và 29,7a – d dưới đây.
Vật liệu
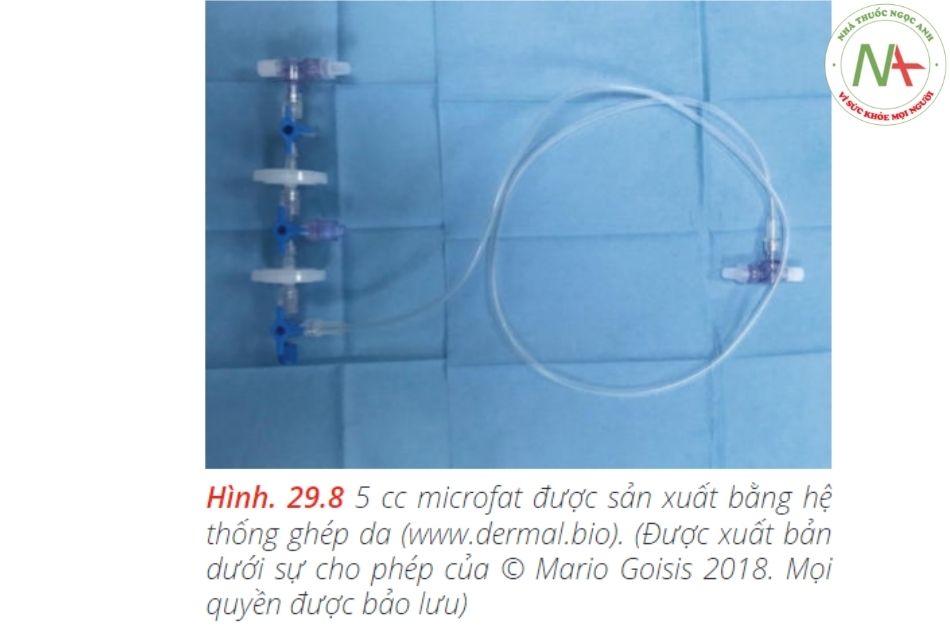
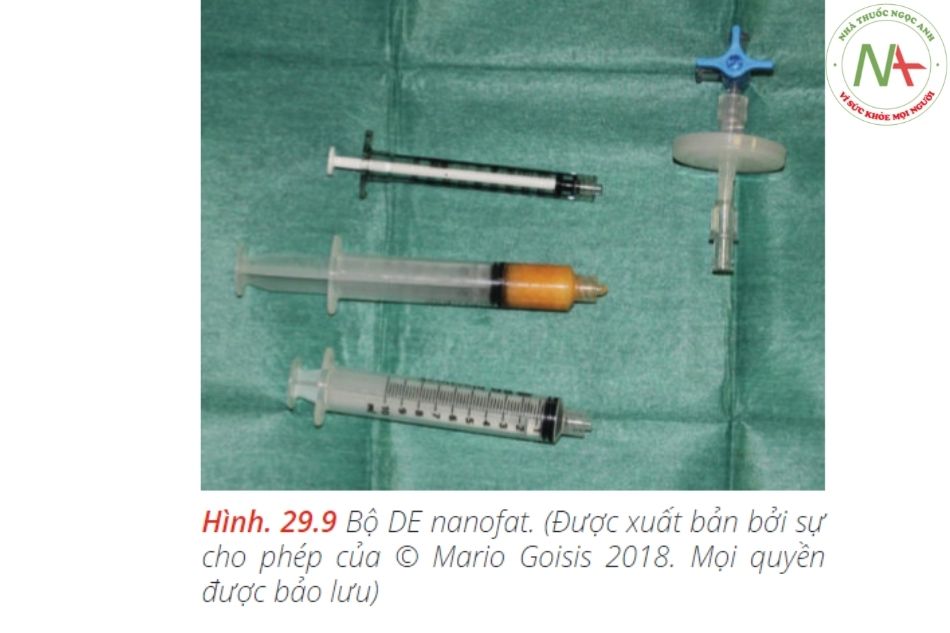
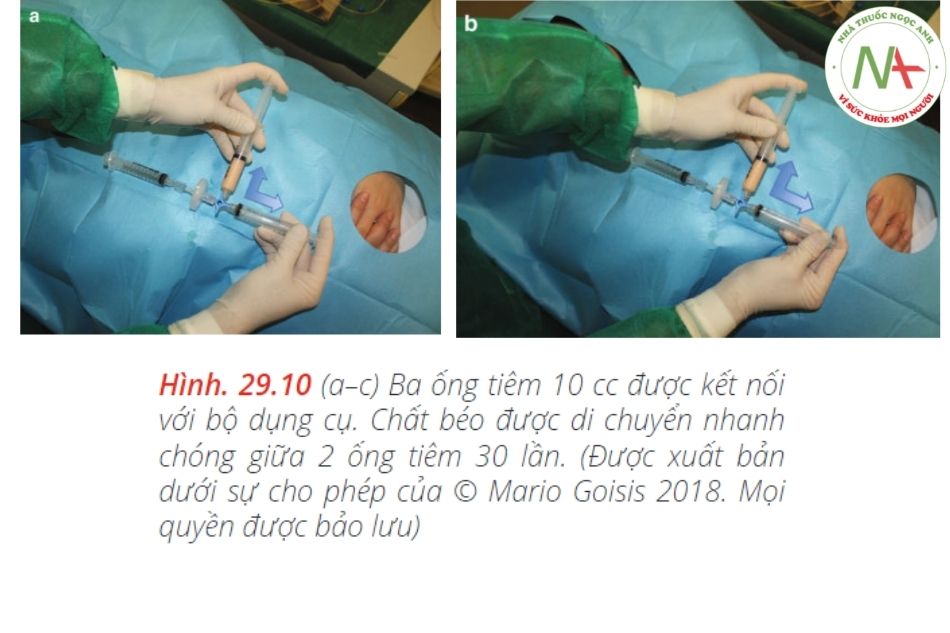
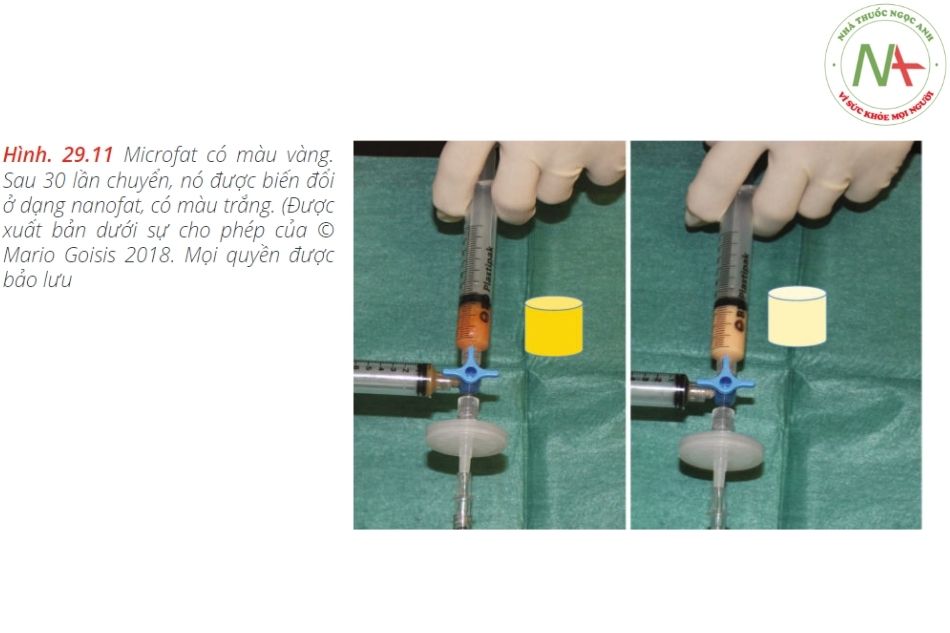
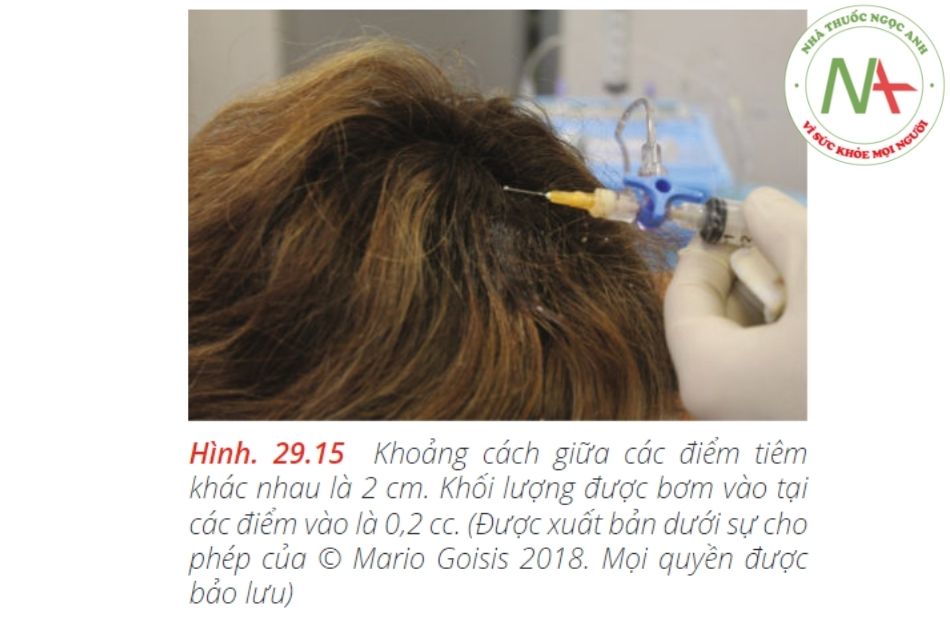
1–2 cc nanofat mỗi bên để tiêm chất béo nano: thay thế bằng1-2 cc nanofat để tiêm cho cả hai bên• Một kim 26G• Một ống cannula đầu tù 27G 3,7 cmMột hệ thống tiêu chuẩn để sản xuất chất béo nano được sử dụng, cụ thể là:• Hệ thống Nanofat (www.microfat.com), bao gồm một đầu nối với một hệ thống khép kín để nhũ tương microfat và lọc• 2 ống tiêm 10 cc• Để thu hoạch và xử lý : mảnh ghép da• Một hệ thống tiêu chuẩn để ghép da• Hệ thống ghép da khép kín.•3 ống tiêm 60cc• 2 ống tiêm 10 cc• 1 ống tiêm 1 cc• Kim 30 G• Kim 16 G• Một ống cannula Goisis đường kính 2 mm, dài 10 cm để lấy mỡThuốc bao gồm:• 100 cc dung dịch muối lạnh.• 40 cc dung dịch Klein lạnh.• Một lít dung dịch Klein bao gồm 800 mg lidocain, 1 mg epinephrine, 40 MEq natri bicarbonate và 1000 cc dung dịch muối.Vị trí: Việc thu hoạch mảnh ghép da có thể được thực hiện trong một phòng phẫu thuật nhỏ / phẫu thuật y tế. Cần có ôxy, đo SpO2 và một xe đẩy / hộp dụng cụ.Người hỗ trợ: Người hỗ trợ rất hữu ích để chuyển các vật dụng vào khu vực thủ thuật một cách vô trùng trong phần đầu tiên của quy trình. Mặc dù vậy, một bác sĩ có thể thực hiện toàn bộ quy trình một mình.Quy trình được mô tả trong các hình ảnh dưới đây (Hình 29.8, 29.9, 29.10a – c, 29.11, 29.12a, b, 29.13, 29.14, và 29.15)
1. Arora NS, Ramanayake T, Ren YF, Roma-nos GE. Platelet-rich plasma: a literature review. Implant Dent. 2009 Aug;18(4):303–10.2. Marx RE. Platelet-rich plasma: evidence to support its use. J Oral Maxillofac Surg. 2004;62:489–96.3. Eppley BL, Woodell JE, Higgins J. Platelet quantification and growth factor analysis from platelet-rich plasma: implications for wound healing. Plast Reconstr Surg. 2004;114:1502–8.4. Weibrich G, Kleis WK, Hafner G, Hitzler WE. Growth factor levels in platelet-rich plasma and correlations with donor age, sex, and platelet count. J Craniomaxillofac Surg. 2002;30:97–102.5. Gkini MA, Kouskoukis AE, Rigopoulos D, Kouskoukis K. Platelet- rich plasma as a poten-tial treatment for noncicatricial alopecias. Int J Trichology. 2015;7(2):54–63.6. Uebel CO, da Silva JB, Cantarelli D, Mar-tins P. The role of plate- let plasma growth factors in male pattern baldness surgery. Plast Reconstr Surg. 2006;118:1458–66.7. Marx RE. Platelet-rich plasma (PRP): what is PRP and what is not PRP? Implant Dent. 2001;10:225–8.8. Rodrigues SV, Acharya AB, Thakur SL. Platelet-rich plasma. A review. N Y State Dent J. 2012;78(1):26–30.9. Sánchez-González DJ, Méndez-Bo-laina E, Trejo-Bahena NI. Platelet-rich plas-ma peptides: key for regeneration. Int J Pept012;2012:532519.10. Su HY, Hickford JG, The PH, Hill AM, Frampton CM, BickerstaffeR. Increased vibrissa growth in transgenic mice expressing insulin- like growth factor 1. J Invest Dermatol. 1999;112:245–8.11. Tavakkol A, Elder JT, Griffiths CE, Cooper KD, Talwar H, Fisher GJ, Keane KM, Foltin SK, Voorhees JJ. Expression of growth hormone receptor, insulin-like growth factor 1 (IGF-1) and IGF-1 receptor mRNA and proteins in human skin. J Invest Dermatol. 1992;99(3):343–9.12. Arshdeep, Kumaran MS. Plate-let-rich plasma in dermatology: boon or a bane? Indian J Dermatol Venereol Leprol. 2014;80:5–14.13. Kamp H, Geilen CC, Sommer C, Blume-Peytavi U. Regulation of PDGF and PDGF receptor in cultured dermal papilla cells and fol-licular keratinocytes of the human hair follicle. Exp Dermatol. 2003;12:662–72.14. Tomita Y, Akiyama M, Shimizu H. PDGF isoforms induce and maintain anagen phase of murine hair follicles. J Dermatol Sci. 2006;43:105–15.15. Takakura N, Yoshida H, Kunisada T, Nishi-kawa S, Nishikawa SI. Involvement of platelet-de-rived growth factor receptor-alpha in hair canal formation. J Invest Dermatol. 1996;107:770–7.16. Blumeyer A, Tosti A, Messenger A, Rey-gagne P, Del Marmol V, Spuls PI, Trakatelli M, Fin-ner A, Kiesewetter F, Trüeb R, Rzany B, Blume-Pey-tavi U, European Dermatology Forum (EDF). Evidence- based (S3) guideline for the treatment of androgenetic alopecia in women and in men. J Dtsch Dermatol Ges. 2011;9(Suppl 6):S1–57.17. Gkini MA, Kouskoukis AE, Tripsianis G, Ri-gopoulos D, Kouskoukis K. Study of platelet-rich plasma injections in the treat- ment of andro-genetic alopecia through an one-year period. J Cutan Aesthet Surg. 2014;7(4):213–9.18. Mubki T, Rudnicka L, Olszewska M, Sha-piro J. Evaluation and diagnosis of the hair loss patient: part I. History and clinical exami- nation. J Am Acad Dermatol. 2014;71(3):415.e1–415.e15.19. Mubki T, Rudnicka L, Olszewska M, Sha-piro J. Evaluation and diagnosis of the hair loss patient: part II. Trichoscopic and laboratory evaral.
Xem thêm Mở rộng bắp chân (Nâng bắp chân)