Bệnh da liễu
Laser không xâm lấn – Bác sĩ Võ Dương Nguyên Sa
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
Nhà thuốc Ngọc Anh – Bài viết Laser không xâm lấn của Thạc sĩ – Bác sĩ Võ Dương Nguyên Sa, để tải file PDF của bài viết xin vui lòng click ở đây.
1. Trẻ hóa da
Trẻ hoá da là phương pháp điều trị nhắm đến sự rối loạn sắc tố liên quan đến tuổi tác và giãn mạch hoặc cải thiện những nếp nhăn và cấu trúc da (( Park SH, Yeo WC, Koh WS, Park JW, Noh NK, Yoon CS (2014) Laser dermatology plastic surgery, 2nd edn. (Korean). Koonja, Seoul)). Trẻ hoá da có thể được phân loại dựa vào phương pháp điều trị; trẻ hoá da xâm lấn (AR) bằng laser CO2 và laser Er:YAG (erbium-doped yttrium aluminium garnet) hoặc trẻ hoá da không xâm lấn (NAR), gây ra phản ứng nhiệt có chọn lọc đến lớp bì và mô mỡ dưới da không làm tổn thương lớp thượng bì. Trẻ hoá da cũng có thể được phân loại dựa trên mục tiêu điều trị; trẻ hoá da type I nhắm vào rối loạn sắc tố và rối loạn mạch máu trong khi trẻ hoá da type II tập trung vào việc cải thiện những nếp nhăn và cấu trúc da. Ví dụ, AR và NAR đều là phương pháp điều trị trẻ hoá da type II (Bảng 9.1). Nhìn chung, NAR đề cập đến điều trị trẻ hoá da sử dụng những phương pháp không xâm lấn để cải thiện những nếp nhăn và cấu trúc da (trẻ hoá da type II).
Trẻ hoá da bằng ánh sáng cũng được chia làm 4 loại dựa vào mục tiêu và phương pháp điều trị được nhắc đến trong một cuốn sách laser (Bảng 9.2) (( Raulin C, Karsai S (2011) Laser and IPL technology in dermatology and aesthetic medicine. Heidelberg: New York)).
Bảng 9.1 Các loại tái tạo da bằng phương pháp và mục tiêu điều trị
| Phương pháp điều trị | Mục tiêu điều trị |
| Trẻ hoá da xâm lấn | Trẻ hoá da type I |
| Trẻ hoá da không xâm lấn | Trẻ hoá da type II |
Bảng 9.2 Các loại trẻ hoá quang điều trị cho da tổn thương do ánh sáng
| Phân loại | Mục tiêu và phương pháp điều trị |
| Trẻ hoá quang type I | Điều trị rối loạn sắc tố
Điều trị giãn mạch Giảm đỏ da lan toả |
| Trẻ hoá quang không xâm lấn type II | Giảm nếp nhăn nhỏ (tác động lớp bì-thượng bì)
Giảm nếp nhăn và kích thước lỗ chân lông (tác động ở lớp bì) |
| Trẻ hoá quang xâm lấn type III | Xâm lấn tái tạo bề mặt: laser CO2 hoặc laser Er:YAG |
| Trẻ hoá quang – Hiệu ứng quang động type IV | Điều trị không xâm lấn kết hợp trẻ hoá quang type I với liệu pháp hiệu ứng quang động (PDT-trẻ hoá da bằng ánh sáng type II) |
Laser không xâm lấn đối với người da sẫm màu hơn
Sự biểu hiện lâm sàng của lão hoá da do ánh sáng giữa người Hàn Quốc và người da trắng khác nhau ở sự thay đổi sắc tố như là đồi mồi (liver spots) là đặc điểm chính trong lão hoá da do ánh sáng ở người Hàn Quốc, trong khi nếp nhăn là đặc điểm chính trong lão hoá da do ánh sáng ở người da trắng. Nếp nhăn ở mức độ trung bình đến nặng ở người Hàn Quốc chỉ trở nên rõ khoảng độ tuổi 50, muộn hơn 10 hoặc 20 năm so với người da trắng cùng độ tuổi (( Allemann IB, Goldberg DJ (2011) Basics in der- matological laser applications. Karger Medical and Scientific Publishers)). Mặc dù trẻ hoá da type II nhắm vào điều trị nếp nhăn ít được áp dụng đối với người Hàn Quốc, nhưng sự cải thiện về cấu trúc da, kích thước lỗ chân lông, và đỏ da vùng mặt vẫn chiếm nhu cầu cao, cho thấy rằng tầm quan trọng của trẻ hoá da type II ở người Hàn Quốc. Việc sử dụng laser không xâm lấn đặc biệt áp dụng cho người Hàn Quốc với lý do mức độ nếp nhăn ít hơn. Mặc khác, laser xâm lấn kém hiệu quả hơn và có nguy cơ tác dụng phụ như sự thay đổi về sắc tố ở người Hàn Quốc là rất cao. Do đó, laser không xâm lấn không cần thời gian nghỉ dưỡng và ít tác dụng phụ là phù hợp với người Hàn Quốc. Laser không xâm lấn có thể điều trị kết hợp với những thủ thuật khác hoặc laser khác.
2. Cơ chế của trẻ hoá quang học
Ba cơ chế hàng đầu của trẻ hoá quang học, không kể đến sự xâm lấn, như sau (( Goldman MP (2006) Cutaneous and cosmetic laser surgery. Mosby Elsevier, Philadelphia, PA)): Thứ nhất, trẻ hoá quang bằng cách tạo tổn thương nhiệt trên da để kích thích quá trình lành thương; Thứ hai, trẻ hoá quang bằng các cytokine gây viêm; Thứ ba, trẻ hoá quang bằng điều biến quang (Bảng 9.3). Chúng ta sẽ thảo luận ngắn gọn ba cơ chế này.
Đầu tiên, tạo tổn thương nhiệt trên da để kích thích quá trình lành thương được cho là cơ chế chính của trẻ hoá quang. Mặc dù cơ chế chính xác chưa được biết, người ta cho rằng tổn thương nhiệt đến da sẽ phá huỷ collagen, dẫn đến tăng sinh và kích hoạt các nguyên bào sợi để hình thành collagen mới. Cơ chế này đưa là một nghịch lý rằng để có collagen mới được hình thành thì sự phá huỷ collagen phải xảy ra trước. Có điều này là bởi vì sự biến tính một phần của collagen được cho là hoạt động như một tác nhân hoặc như một bộ khung cho sự tổng hợp collagen mới. Chúng ta sẽ đi vào chi tiết ở phần 9.2.5. Mục tiêu là để tăng nhiệt độ ở lớp bì lên đến 50-70 °C.
Bảng 9.3 Cơ chế của trẻ hoá quang học
| 1. Tạo tổn thương nhiệt trên da để kích thích quá trình lành thương |
| 2. Các cytokine gây viêm |
| 3. Điều biến quang |
Tổn thương nhiệt có thể được giới hạn ở các mức độ cụ thể ở lớp bì để các sẹo hay nếp nhăn sâu hơn có thể được điều trị bằng mức độ nhiệt sâu hơn, đồng thời với sự thâm nhập sâu hơn vào các dây chằng, cân mạc hoặc mỡ dưới da, toàn bộ các vùng của da có thể được săn chắc. Việc tạo ra năng lượng nhiệt này, dù là laser, nguồn ánh sáng như IPL, RF, sóng siêu âm, hoặc năng lượng sóng siêu vi có thể gây ra tổn thương và co thắt collagen. Có nhiều người cho rằng tổn thương nhiệt đến lớp bì không chỉ dẫn đến sự hình thành collagen sau đó bởi các nguyên bào sợi mà còn thay đổi glycosaminoglycans (GAG) và chất nền lớp bì dẫn đến tái cấu trúc da (( Hruza GJ, Tanzi EL (2018) Lasers and lights. Elsevier, Edinburgh)).
Thứ hai, các cytokine gây viêm có nguồn gốc khác nhau ảnh hưởng đến sự biểu hiện protein nền ngoại bào, như là collagen type I, fibronectin, và decorin trong nguyên bào sợi ở da người. Những yếu tố gây viêm này cũng phát sinh từ quá trình tổn thương tế bào và quá trình lành vết thương, do đó tham gia vào cơ chế đầu tiên của trẻ hoá quang (tạo tổn thương nhiệt trên da để kích thích quá trình lành thương). Một số người cho rằng những cytokine gây viêm có thể được giải phóng từ các tế bào của hệ miễn dịch, sau đó xâm nhập vào tổn thương bề mặt mao mạch (( Park SH, Yeo WC, Koh WS, Park JW, Noh NK, Yoon CS (2014) Laser dermatology plastic surgery, 2nd edn. (Korean). Koonja, Seoul)). Omi và cộng sự đã điều trị cho những bệnh nhân với laser xung màu (PDL, N-Lite, ICN Photonics, UK) và thu thập những mẫu bệnh phẩm sinh thiết. Thấy rằng không có sự thay đổi sợi collagen trong 3 giờ sau khi chiếu laser. Sự gia tăng collagen ở lớp bì được quan sát thấy vào tuần 2, 4, 5 sau chiếu laser. Điều này cho thấy rằng laser mạch máu có thể hữu ích trong trẻ hoá quang.
Các protein shock nhiệt (HSP) và protein chất nền (MMP) cũng tham gia vào cơ chế này. Desmettre, Souil và cộng sự đã quan sát thấy tiếp xúc ở 60ºC trong hơn 1 giây dẫn đến sự biến tính collagen, trong khi nhiệt độ thấp hơn 50ºC không đủ để thay đổi nhiệt nhưng đủ để kích hoạt protein shock nhiệt, do đó làm tăng sản xuất collagen. MMP ban đầu được cho là không hiệu quả đối với trẻ hoá da do đặc tính phân huỷ collagen của nó, nhưng điều ngược lại đã được chứng minh. Những nghiên cứu của Verani và cộng sự đã chỉ ra có sự tích tụ collagen bị phân huỷ một phần được tìm thấy trong tổn thương da do ánh sáng, có thể ức chế sự tổng hợp collagen qua nguyên bào sợi. Orringer và cộng sự cho rằng sự gia tăng MMP sau laser CO2,, laser xung màu, và laser không xâm lấn có thể loại bỏ collagen bị tổn thương do ánh sáng, dẫn đến sự kích hoạt nguyên bào sợi và sự hình thành collagen sau đó.
Thứ ba, điều biến quang còn được gọi là sự kích thích sinh học hoặc liệu pháp ánh sáng năng lượng thấp (LLLT). Hiệu ứng quang hoá có thể được phân loại theo cơ chế; điều biến quang, liệu pháp quang động (PDT), và laser Excimer. Thỉnh thoảng laser excimer được phân loại như hiệu ứng quang xâm lấn. Điều biến quang có thể được xem như một hiện tượng của hiệu ứng quang hoá. Điều biến quang được chứng minh là hiệu quả trong kiểm soát đau, sự lành thương, mụn viêm, và trẻ hoá da. Điều biến quang kích thích hoặc ức chế sự hoạt động tế bào bình thường qua cơ chế phi nhiệt. Nó xảy ra bằng cách kiểm soát việc sản xuất ATP ti thể hoặc bằng cách điều hoà hoặc điều chỉnh thụ thể. Trong vài năm nay, đã có nhiều tranh luận về hiệu quả và cơ chế của điều biến quang. Tuy nhiên, không có bất cứ câu hỏi nào về hiệu quả của điều biến quang và cơ chế cơ bản của nó. Ngoài ra, nó vẫn được xem là ít hiệu quả hơn so với những cơ chế khác. Chúng ta sẽ đi vào chi tiết của điều biến quang vào phần cuối của chương này.
Tiếp đến, chúng ta sẽ đi vào chi tiết trong cơ chế đầu tiên của trẻ hoá quang (tạo tổn thương nhiệt trên da để kích thích quá trình lành thương) và mối quan hệ của nó với NAR.
2.1 Tái tạo collagen
Mục tiêu của trẻ hoá type II là sợi collagen. Sợi collagen là thành phần chính của lớp bì, nó bao gồm khoảng 75% trọng lượng khô và 18-30% thể thích lớp bì, đồng thời tạo nên sự đàn hồi cho da. Collagen được tổng hợp trong nguyên bào sợi ở lớp bì, tế bào keratin ở lớp thượng bì, tế bào nội mô mạch máu, và tế bào cơ trơn (( Textbook Compilation Committee in Korean Dermatological Association (2014) Text book of der- matology 6th edition (Korean). Daehanuihak, Seoul)). Do đó, việc kích thích nguyên bào sợi ở lớp bì hoặc tế bào nội mô mạch máu là hữu ích.
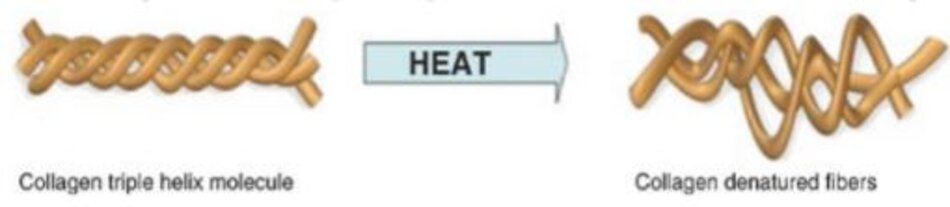
Một phân tử collagen bao gồm một chuỗi xoắn ba được tạo ra từ ba chuỗi polypeptide liên kết hydro với nhau. Mỗi chuỗi popeptide chứa khoảng 1000 amino acid. Các phân tử collagen tạo thành các sợi collagen, và các sợi này tạo thành các sợi collagen có kích thước lớn hơn.
Sự biến tính của chuỗi xoắn ba, mất độ đàn hồi và tăng độ dày của collagen đã được quan sát qua mẫu sinh thiết đối với da lão hoá. Nếu collagen được làm nóng, các liên kết cộng hoá trị của collagen bị phá vỡ dẫn đến sự co rút collagen. Đây được gọi là sự co rút do nhiệt (Hình 9.1). Điều này là tại sao sau NAR, như là hệ thống ThermaCool TCTM (Thermage Hayward, CA), sự co rút phân tử collagen ngay lập tức dẫn đến hiệu quả nâng cơ rõ rệt.
Sau khi collagen co, đại thực bào và MMP loại bỏ collagen bị hư tổn, và HSP được giải phóng sẽ kích hoạt quá trình lành thương, dẫn đến sự hình thành collagen mới từ các nguyên bào sợi. Trong suốt quá trình lành thương, sự tổng hợp collagen bắt đầu khoảng 3 ngày sau tổn thương và có thể tiếp tục khoảng 4 tuần. Sự trưởng thành collagen và tái tạo collagen bắt đầu vài tháng sau tổn thương và có thể tiếp tục khoảng 1 năm (Hình 9.2). Nó thường kéo dài khoảng 6 tháng.
Điều này ngụ ý rằng NAR không dẫn đến sự trẻ hoá da ngay lập tức. Về mặt lâm sàng, hiệu quả nâng cơ nổi bật rõ rệt sau NAR là do sự co rút (Bảng 9.4 quy trình 1), nhưng do hiệu quả co rút do nhiệt thoáng qua nên hiệu quả nâng cơ cũng chỉ là tạm thời. Cho đến 6 tháng sau NAR, làn da dần dần được trẻ hoá do sự tái tạo collagen (bảng 9.4 quy trình 2) (( Hruza GJ, Tanzi EL (2018) Lasers and lights. Elsevier, Edinburgh)). Mối liên quan giữa hiệu quả nâng cơ tức thì do co rút do nhiệt và hiệu quả nâng cơ sau đó do tái tạo collagen vẫn chưa được biết rõ (( Park SH, Yeo WC, Koh WS, Park JW, Noh NK, Yoon CS (2014) Laser dermatology plastic surgery, 2nd edn. (Korean). Koonja, Seoul)). Chúng tôi kết luận rằng hiệu quả nâng cơ tức thì bằng NAR tương quan với hiệu quả nâng cơ sau 6 tháng.
Bảng 9.4 Các quá trình thay đổi collagen bằng các thiết bị làm săn chắc da. (Chỉnh sửa từ (( Hruza GJ, Tanzi EL (2018) Lasers and lights. Elsevier, Edinburgh)))
| 1. Sự co collagen ngay lập tức bằng cách đốt nóng trực tiếp các sợi collagen |
| 2. Quá trình tái tạo và sản xuất collagen mới bị trì hoãn qua đáp ứng chữa lành vết thương |
Các nghiên cứu sâu hơn về thời gian NAR như sau (( Park SH, Yeo WC, Koh WS, Park JW, Noh NK, Yoon CS (2014) Laser dermatology plastic surgery, 2nd edn. (Korean). Koonja, Seoul)). Dainich và cộng sự đã quan sát được sự tái tạo collagen 1-2 tháng sau điều trị với laser erbium glass (Er:Glass) 1540 nm, nhưng hiệu quả này trở nên không rõ rệt sau 1 năm. Oritz và cộng sự đã thấy rằng laser CO2 fractional duy trì sự cải thiện 1-2 năm so với 3 tháng sau điều trị. Munskiatti và cộng sự đã thấy rằng laser CO2 tái tạo bề mặt cũng duy trì sự cải thiện 2 năm so với 3 tháng sau điều trị. Điều này ngụ ý rằng AR hiệu quả hơn và có thời gian kéo dài hơn so với NAR.

2.2 Phản ứng nhiệt của mô da
Phản ứng nhiệt đối với nhiệt độ da tăng cao được thể hiện trong bảng 9.5 (( Raulin C, Karsai S (2011) Laser and IPL technology in dermatology and aesthetic medicine. Heidelberg: New York)). Đối với laser không xâm lấn, mục tiêu chính của chúng ta là collagen. Phản ứng nhiệt của collagen đối với nhiệt độ da gia tăng như sau
Bảng 9.5 Phản ứng của mô da đến nhiệt
| Nhiệt độ (°C) | Phản ứng nhiệt |
| 42-45 | Bắt đầu tăng nhiệt độ, thay đổi cấu trúc và co rút collagen |
| 50 | Giảm hoạt động enzyme |
| 60 | Biến tính protein, đông tụ collagen, và thẩm thấu qua màng tế bào |
| 100 | Làm khô các mô và hình thành không bào |
| > 100 | Bắt đầu bay hơi và carbon hóa mô |
| 300-1000 | Mô bị cắt đốt, phá hủy bằng nhiệt năng và quang năng |
- 42 °C: sự co collagen
- 60 °C: sự đông tụ collagen
- >100 °C: bắt đầu bay hơi
Đối với quá trình tái tạo collagen, nhiệt độ phải vượt quá 60ºC để đông tụ collagen. Nhưng nhiệt độ không được quá 100ºC, vì tránh sự bay hơi trong NAR. Đối với NAR, nhiệt độ dao động giữa 60ºC đến 100ºC. Một số câu hỏi sau đây được phát sinh: (1) Nhiệt độ 60ºC có phải là điều kiện tiên quyết để tái tạo collagen không? Có bất kỳ yếu tố nào khác ảnh hưởng đến điều này không? (2) Có phải tiên lượng sẽ giống nhau ở bất kỳ nhiệt độ nào giữa 60ºC và 100ºC không, và có những tác dụng phụ nào không? (3) 100% collagen bị biến tính có tối ưu không? Đây là những câu hỏi về vấn đề này.
2.3 Phương trình Arrhenius
Trong bảng 9.5, sự biến tính collagen bắt đầu ở 42oC. Nhiệt độ thấp hơn 42ºC, không tính đến thời gian tiếp xúc, không dẫn đến bất kỳ sự thay đổi nào trong mô. Nhiệt độ cơ thể tăng lên 5ºC dẫn đến không có sự thay đổi đáng kể nào trong mô. Mặc khác, nhiệt độ giữa 42-50ºC gây ra sự thay đổi cấu trúc trong collagen. Sau vài phút, hoại tử mô có thể xảy ra theo phương trình Arrhenius.
Như đã đề cập ở “chương 3”; do phương trình Arrhenius, không chỉ nhiệt độ mà còn thời gian điều trị đã được xem xét kỹ là có liên quan đến sự biến tính collagen. Có 2 cách dẫn đến sự biến tính collagen trong NAR: thời gian điều trị ngắn và nhiệt độ cao (phương pháp A) hoặc thời gian điều trị dài và nhiệt độ thấp (phương pháp B). Sau đó, những điểm khác nhau giữa hai phương pháp này là gì? Chúng ta sẽ điểm qua sự khác nhau trong phần 9.2.6.
2.4 Tổn thương mô
Các phản ứng nhiệt đối với việc tăng nhiệt độ da rất đa dạng. Hình 9.3 giải thích các phản ứng nhiệt đối với nhiệt độ da tăng sau điều trị laser CO2 và được minh hoạ ở bảng 9.5. Theo phương trình Arrhenius, nhiệt độ không quan trọng. Sự thay đổi mô cụ thể không quan trọng về mặt lâm sàng. Điều quan trọng là liệu sự thay đổi mô cụ thể là những gì chúng ta muốn, hoặc những gì chúng ta không muốn. Đó là, liệu sự tổn thương có thể hồi phục hay không hồi phục. Ngoài ra, điều quan trọng cần chú ý là một vài tổn thương không hồi phục có thể gây ra sự hình thành sẹo sau một thời gian nhất định.
Mức năng lượng thích hợp của laser không xâm lấn sẽ mang lại hiệu quả mong muốn, trong khi mức năng lượng cao có thể gây ra bỏng, dẫn đến hình thành sẹo. Laser không xâm lấn hiếm khi gây ra hiện tượng bốc bay, do đó hầu hết sự hình thành sẹo xảy ra trong quá trình tổn thương không hồi phục dưới 100ºC. Một số tổn thương không hồi phục là mong muốn, nhưng sau một thời gian nhất định một số có thể gây ra hình thành sẹo không mong muốn.
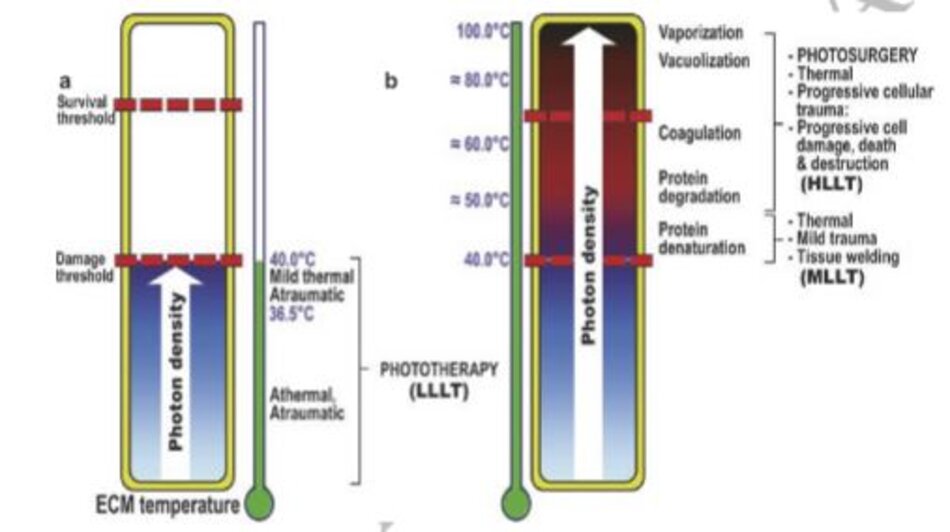
Calderhead đã đưa ra khái niệm về ngưỡng tổn thương và ngưỡng tồn tại bằng cách xem xét sự biến tính của mô và sự chết tế bào (Hình 9.4) (( Calderhead RG, Vasily DB (2016) Low level light therapy with light-emitting diodes for the aging face. Clin Plast Surg 43(3):541–550)). Điều trị được phân chia gồm liệu pháp ánh sáng năng lượng thấp (LLLT), liệu pháp ánh sáng năng lượng trung bình (MLLT), và liệu pháp ánh sáng năng lượng cao (HLLT). LLLT cũng được biết như một điều biến quang. Tái tạo bề mặt bằng laser CO2, điều trị đồi mồi bằng laser Q-switched hoặc IPL là những ví dụ của HLLT. Tổn thương không hồi phục đối với lớp thượng bì được gây ra bởi sự bóc tách hoặc đông máu không dẫn đến hình thành sẹo, nhưng nguy cơ tạo sẹo cao khi lớp bì đặc biệt lớp lưới có sự bóc tách hay đông máu. Điều này tại sao NAR bằng MLLT hoặc HLLT phải được điều trị dưới ngưỡng tồn tại để không phải tất cả mà chỉ một phần lớp bì bị tổn thương. Điều này sẽ được đề cập lại ở phần 9.4.

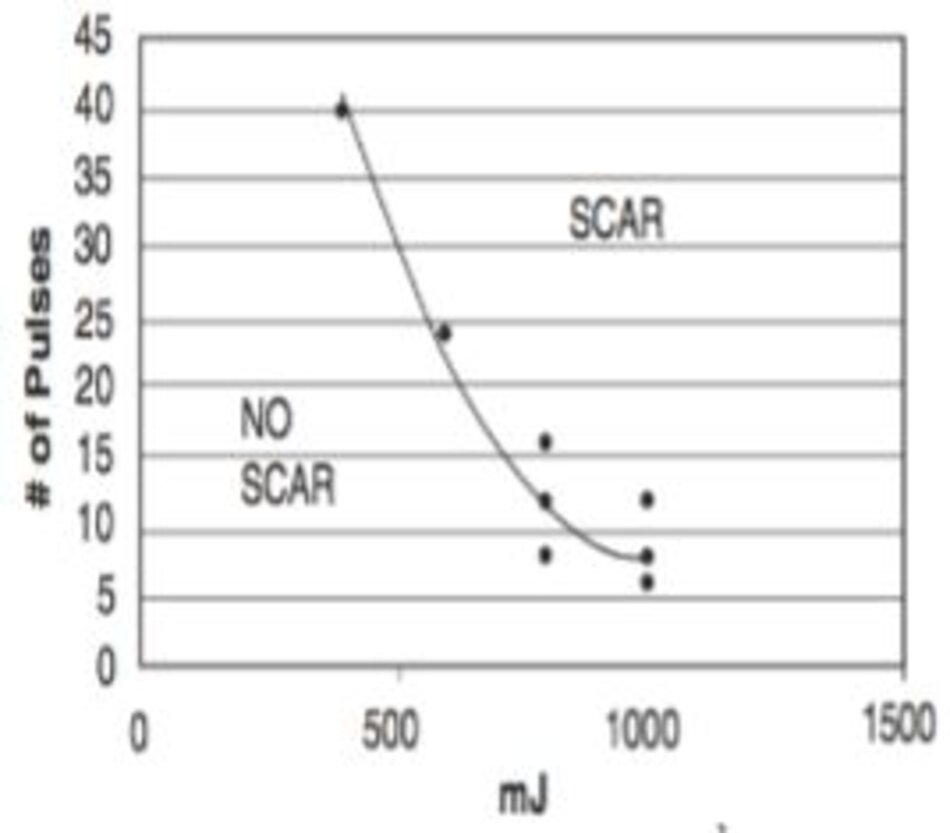
Ross và cộng sự đã sử dụng laser Er:Glass 1550 nm với tay cầm sapphire làm mát (( Ross EV, Sajben FP, Hsia J, Barnette D, Miller CH, McKinlay JR (2000) Nonablative skin remodeling: selective dermal heating with a mid-infrared laser and contact cooling combination. Lasers Surg Med 26(2):186–195))). Các vị trí sau tai nhận năng lượng xung dao động từ 400-1200 mJ và số lượng xung từ 4-40. Kết quả thu được bao gồm đỏ da, phù nề, và trắng vùng thượng tức thì. Trong sự kết hợp số lượng xung và năng lượng xung mà không làm trắng thượng bì ngay tức thì thì đỏ da và phù nề kéo dài ít nhất 2 tuần, với sự hồi phục sau đó. Nhưng kết hợp với việc làm trắng tức thì, vết trợt và loét dẫn đến sẹo teo sau 1 tháng.
Hình 9.5 Đường cong nối các chấm thể hiện sự hình thành sẹo. Năng lượng xung cao hơn và số lượng xung nhiều hơn thì nguy cơ sẹo xảy ra cao hơn. Điều quan trọng đáng chú ý là không chỉ năng lượng xung, mà còn số lượng xung cũng quan trọng trong hình thành sẹo.
Tức là, thậm chí nếu năng lượng xung thấp, số lượng xung cao có thể gây ra sẹo. Nói cách khác, cũng có thể giả định rằng sẹo cũng cũng có thể hình thành theo phương trình Arrhenius.
Bài báo gợi ý rằng thực sự có ngưỡng tồn tại cho việc hình thành sẹo và ngưỡng này tuân theo phương trình Arrehenius. Trong một cuốn sách, người ta cho rằng ở 80ºC, tính thấm màng tế bào bị tổn thương và trạng thái cân bằng hoá học của tế bào bị phá huỷ. Điều này ngụ ý rằng ở 80C có thể là ngưỡng tồn tại (( Niemz MH (2007) Laser-tissue interactions. Springer, New York)).
Đây là lý do tại sao NAR phải gây ra tổn thương giữa ngưỡng tổn thương và ngưỡng tồn tại. Cửa sổ điều trị của NAR rất hẹp. Tổn thương vượt qua ngưỡng tồn tại thì không liên quan đến điều trị đồi mồi bằng IPL bởi vì nó được loại bỏ ra khỏi da bằng chu trình tế bào. Nhưng trong NAR, tổn thương phải thấp hơn ngưỡng tồn tại. Điều này làm cho phạm vi điều trị hẹp hơn so với IPL và việc điều trị trở nên khó khăn hơn.
2.5 Sự biến tính collagen một phần hay toàn bộ
Alexiades-Armenakas và cộng sự đã điều trị cho 100 bệnh nhân có vùng da mặt và cổ nhăn, chảy xệ bằng fractional bipolar radiofrequency (FRF) (( Alexiades-Armenakas M, Newman J, Willey A, Kilmer S, Goldberg D, Garden J et al (2013) Prospective multicenter clinical trial of a minimally invasive temperature-controlled bipolar fractional radiofrequency system for rhytid and laxity treatment. Dermatol Surg 39(2):263–273)). Thiết bị này (e-Prime, Korean domestic name Profound; Syneron, Yokneam Illit, Israel) có thể đo được nhiệt độ bên trong da. Điều trị 1 pass duy nhất FRF (one single-pass FRF) được thực hiện với thời gian đã cài đặt sẵn, nhiệt độ cố định 62-78oC, thời gian năng lượng 3-5 giây. Nhiệt độ trung bình, thời gian năng lượng, và thể tích biến tính collagen của mỗi nhóm được tính toán và chia nhóm dựa vào sự cải thiện nếp nhăn ≤20% và ≥20% so với ban đầu (Bảng 9.6).
Trên mẫu sinh thiết, nhiệt độ càng cao (p = 0.08), thời gian năng lượng càng lớn (p = 0.03), và thể tích biến tính collagen càng dài (p = 0.05), về mặt thống kê cho thấy hiệu quả cải thiện nếp nhăn càng thấp (<20%, mean ± SD). Nhiệt độ mục tiêu trung bình là 69,5oC, thời gian năng lượng là 4,9 giây, và thể tích biến tính collagen là các nhóm 3 mm3 đã chỉ ra sự cải thiện nếp nhăn ít hơn 20%, trong khi nhiệt độ mục tiêu là 66,7oC, thời gian năng lượng là 4,2 giây, và thể tích biến tính collagen của các nhóm 2 mm3 cho thấy cải thiện nếp nhăn hơn 20%.
Bảng 9.6 Phân tích thống kê: Cài đặt thông số và thể tích tương ứng
| Cải thiện so với ban đầu | Nhiệt độ mục tiêu (°C) | Thời gian (s) | Thể tích (mm3) |
| ≤20%, mean ± SD | 69.5 ± 4.5 | 4.9 ± 0.3 | 3.02 ± 1.36 |
| >20%, mean ± SD | 66.7 ± 4.5 | 4.2 ± 1.0 | 2.00 ± 1.49 |
| p Value | 0.08 | 0.03 | 0.05 |
SD standard deviation. (Sao chép từ (( Alexiades-Armenakas M, Newman J, Willey A, Kilmer S, Goldberg D, Garden J et al (2013) Prospective multicenter clinical trial of a minimally invasive temperature-controlled bipolar fractional radiofrequency system for rhytid and laxity treatment. Dermatol Surg 39(2):263–273)))
Bài báo này không đưa ra ngưỡng tồn tại, nhưng nó chỉ ra nhiệt độ càng cao và thời gian năng lượng càng dài không đảm bảo hiệu quả tốt hơn, thay vào đó là ít hiệu quả hơn. Cũng cần lưu ý rằng thể tích biến tính collagen bằng sinh thiết càng lớn, nghĩa là hiệu quả ít hơn.
Tác giả của bài bào này đã xuất bản bài báo tiếp theo sau đó, Alexiades và cộng sự đã thực hiện FRF như miêu tả trước đó (( . Alexiades M, Berube D (2015) Randomized, blinded, 3-arm clinical trial assessing optimal temperature and duration for treatment with minimally invasive fractional radiofrequency. Dermatol Surg 41(5): 623–632)). 15 bệnh nhân được chia làm 3 nhóm và đánh giá mức độ cải thiện nếp nhăn và da chảy xệ (Bảng 9.7). Kết quả đã cho thấy sự cải thiện nếp nhăn ở nhóm 3 là tốt nhất với 25 %, 29% và 40 % tương ứng với nhóm 1, 2, 3. Cải thiện độ chảy xệ của da tương đối hiệu quả với nhóm 2 và nhóm 3, với 25%, 36%, 34% tương ứng nhóm 1, 2, 3. Về mặt hài lòng mang tính chủ quan, bệnh nhân nhóm 2 và nhóm 3 đạt độ hài lòng.
Sau 6 tháng, hệ số Pearson ngụ ý sự tương quan nhẹ với sự cải thiện nếp nhăn và da chảy xệ trong sự liên quan với sự thay đổi nhiệt độ 0,56 và 0,47, tương ứng. Nhiệt độ da mục tiêu tối ưu cho việc điều trị nếp nhăn và sư chảy xệ ở vùng mặt và cổ là 67oC và thời gian là 3-4 giây.
Bằng cách kết hợp những kết quả của hai bài báo này, có thể phân thành 4 nhóm điều trị. Đó là nhóm 52-57ºC, nhóm 62ºC, nhóm 67ºC, và nhóm 69ºC. Kết quả này chỉ ra rằng nhiệt độ càng cao (sự phá hủy collagen càng trầm trọng), thì tác động càng tốt lên vùng da chảy xệ và nếp nhăn da, trừ nhóm 69ºC. Nhóm 69ºC có thể tích biến tính collagne cao, nhưng hiệu quả thấp.
Mặc dù không hình thành sẹo, nhưng mức độ tổn thương collagen càng lớn thì hiệu quả càng kém. Các tác giả suy đoán rằng những lý do cơ bản cho điều này đầu tiên là sự tổn thương càng nhỏ thì cung cấp oxy càng tốt, dẫn đến tổn thương nhanh lành hơn và tái tạo collagen cao hơn. Thứ hai, người ta suy đoán rằng nhiệt độ càng thấp, collagen bị biến tính một phần được tạo ra nhiều hơn dẫn đến sự hình thành collagen càng nhiều. Collagen bị biến tính một phần có thể kích hoạt sự hình thành collagen mới. Ross và cộng sự miêu tả giả thuyết này như bộ khung thay vì sự kích hoạt (( . Alexiades M, Berube D (2015) Randomized, blinded, 3-arm clinical trial assessing optimal temperature and duration for treatment with minimally invasive fractional radiofrequency. Dermatol Surg 41(5): 623–632)). Người ta cho rằng collagen bị kết dính bởi nhiệt trở thành bộ khung cho collagen mới và cơ sở cho sự tái tạo collagen. Ngược lại, thí nghiệm in vivo và in vitro trên lợn, cho thấy sự biến tính hoàn toàn collagen và sự co rút rõ dẫn đến hình thành sẹo. Điều này ngụ ý rằng phải tránh sự biến tính collagen.
2.6 Hai phương pháp trẻ hóa không xâm lấn
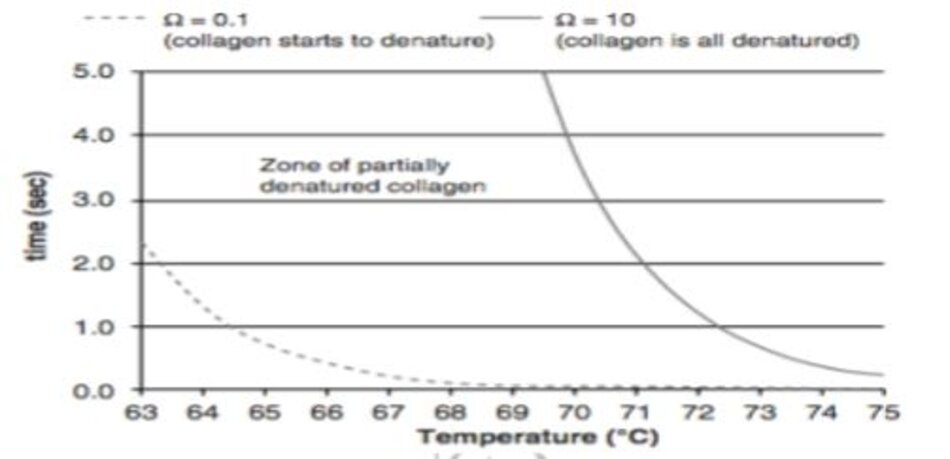
Dựa vào các kết quả trước đó, Alexiades-Armenakas và cộng sự đã trình bày bảng 9.6 trong bài báo này. Sự biến tính collagen được chia làm 3 vùng dựa vào nhiệt độ điều trị và thời gian tiếp xúc. Gồm có: vùng collagen không bị biến tính, vùng collagen bị biến tính một phần và vùng collagen bị biến tính hoàn toàn. Vùng collagen bị biến tính một phần cho thấy hiệu quả tốt nhất.
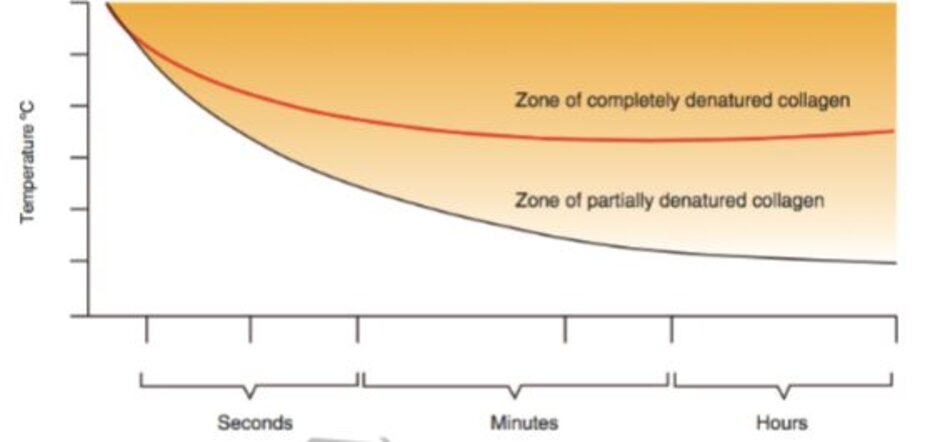
Đường cong giữa collagen bị biến tính một phần và hoàn toàn có thể tuân theo phương trình Arrhenius, vì vậy tôi (tác giả) đã vẽ lại hình 9.7 bằng cách áp dụng hình 3.12 từ phương trình Arrhenius.
Như đã xem xét trước đó, có 2 phương pháp NAR áp dụng phương trình Arrhenius: thời gian tiếp xúc ngắn và nhiệt độ cao (phương pháp A) hoặc thời gian tiếp xúc dài và nhiệt độ thấp (phương pháp B). Hình 9.7 chỉ ra đặc tính của mỗi phương pháp. Những điều này được tóm tắt trong bảng 9.8.
Collagen biến tính một phần sẽ tương tự một trong 2 phương pháp: thời gian tiếp xúc ngắn và nhiệt độ cao (phương pháp A) hoặc thời gian tiếp xúc dài và nhiệt độ thấp (phương pháp B). Tuy nhiên, phương pháp A có cửa sổ điều trị hẹp. Do đó, nó có thể không hiệu quả và dễ xảy ra tác dụng phụ như sẹo. Ngoài ra, cơn đau dữ dội cũng là vấn đề về mặt lâm sàng. Trái lại, phương pháp B có thể được thực hiện mà không phải lo lắng về tác dụng phụ bởi vì cửa sổ điều trị của nó rộng. Tuy nhiên, đòi hỏi thời gian thực hiện dài. Ví dụ, nếu nhiệt độ duy trì ở 45ºC, nó mất ít nhất 1 giờ để đạt hiệu quả.
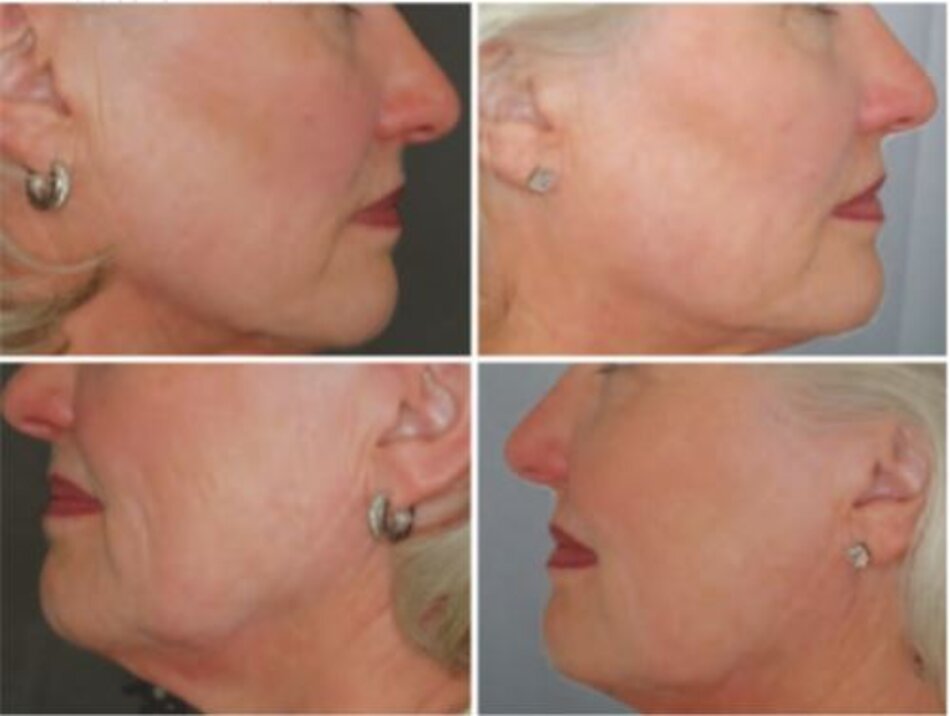
Bây giờ, chúng ta sẽ xem xét lại các bài báo quan trọng trong phương pháp A và B về NAR. Taylor và cộng sự đã thực hiện nghiên cứu so sánh hiệu quả điều trị vùng mặt trái và phải bằng 2 phương pháp khác nhau (( Taylor MB, Prokopenko I (2006) Split-face com- parison of radiofrequency versus long-pulse Nd-YAG treatment of facial laxity. J Cosmet Laser Ther 8(1):17–22)). Những bệnh nhân có làn da chảy xệ được điều trị như sau mặt bên trái: 1 lần với laser Nd: YAG 1064 nm xung dài, 3 pass, spot 10 mm, 50 ms, 50 J/cm2, và mặt bên phải: 1 lần với sóng siêu âm vô tuyến điện (RF, Thermage®). Có sự cải thiện hơn đối với nếp nhăn và da chảy xệ ở vùng mặt được điều trị với laser và về cơ bản giống nhau ở cả 2 phương pháp về cấu trúc, lỗ chân lông, và sắc tố. Sự cải thiện được duy trì ít nhất trong 2-6 tháng trên cả mặt trái và mặt phải (Hình 9.8 và 9.9).
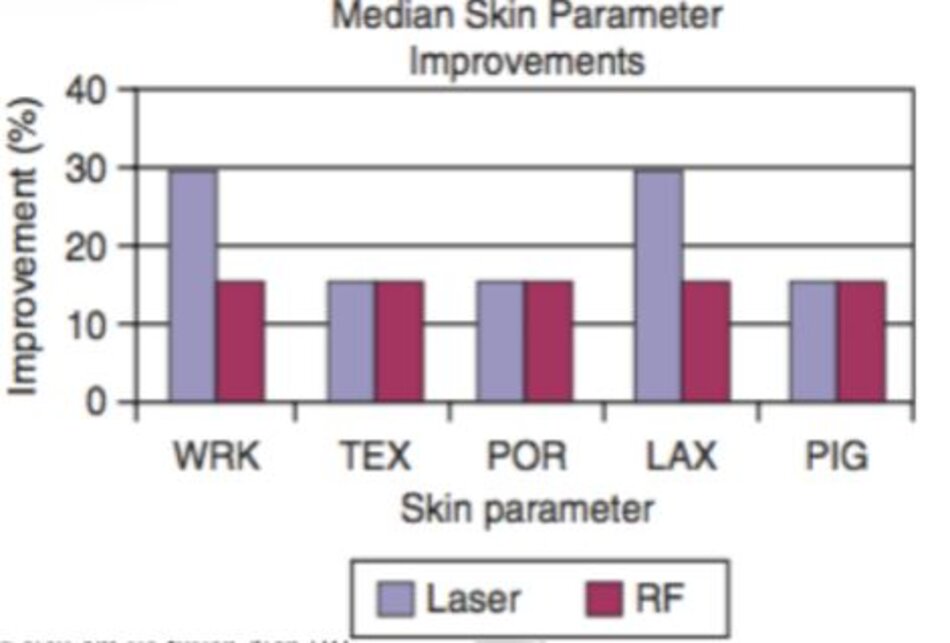
| Phương pháp | Nhiệt độ và thời gian | Cửa sổ điều trị và hạn chế | |
| A | Thời gian ngắn và nhiệt độ cao | Hẹp | Đau, tác dụng phụ |
| B | Thời gian dài và nhiệt độ thấp | Rộng | Thời gian thực hiện dài |
Bài báo này ngụ ý rằng hiệu quả của “ những kỹ thuật 5050” của laser Nd: YAG 1064 nm xung dài là tương đương hoặc tốt hơn Thermage®, một thiết bị đại diện cho NAR. Thermage® và những kỹ thuật 5050 đều là phương pháp A sử dụng năng lượng cao trong thời gian ngắn. Khi mà tôi không có Thermage®, tôi đã thử những kỹ thuật 5050 với Nd: YAG xung dài dựa vào bài báo này. Tuy nhiên, gần đây, tôi hiếm khi thực hiện quy trình này bởi vì quá đau nên bệnh nhân e dè. Cùng lúc, mụn nước được hình thành do biểu bì không được làm mát.
Schmults và cộng sự đã thực hiện laser Nd: YAG 1064 nm xung dài trên 9 bệnh nhân, 3 lần cách nhau 2 tuần (( Schmults CD, Phelps R, Goldberg DJ (2004) Nonablative facial remodeling: erythema reduction and histologic evidence of new collagen formation using a 300-microsecond 1064-nm Nd:YAG laser. Arch Dermatol 140(11):1373–1376)). Thông số spot 5 mm, 300 μs, và 13 J/cm2, nhưng bởi vì cách da 2-4 cm nên các thông số thực tế trên da là spot 6–7 mm, 7–9 J/cm2, shots 12,000– 14,700 và tổng thời gian thực hiện khoảng 30 phút. Đánh giá bằng hình ảnh cho thấy những bệnh nhân có đỏ da trước đó thì có sự cải thiện đỏ da đồng thời liên quan với sự cải hiện chất lượng da. Sự cải thiện bệnh thoái hóa sợi elastin do ánh nắng được nhìn thấy dưới kính hiển vi điện tử.
Bài báo này còn được gọi là “kỹ thuật Gen”, phương pháp B mà sử dụng năng lượng thấp trong thời gian dài. Đây là phương pháp tôi sử dụng hiện tại.
3. Kỹ thuật Gen
Vẫn còn nhiều tranh cãi về tác dụng và cơ chế của kỹ thuật Gen. Trong phần này sẽ tóm tắt tác dụng và cơ chế của kỹ thuật Gen. Chiba và cộng sự đã điều trị tổng cộng 19 bệnh nhân nữ người Nhật với da types III hoặc IV theo phân loại Fitzpatrick với laser Nd:YAG 1064nm xung dài (( Chiba C, Usui A, Hara H, Ishi Y (2009) Clinical expe- rience in skin rejuvenation treatment in Asians using a long-pulse Nd:YAG laser. J Cosmet Laser Ther 11(3):134–138)). Thông số là spot size 8 mm, thời gian xung 0.3 ms, và 13 J/cm2 , 7 Hz, không làm mát. Tay cầm được đặt cách da 2 cm với kỹ thuật di chuyển lặp lại. Cho vùng mặt, 4200 shot trong 10 phút, 2 đến 7 lần mỗi 3-4 tuần, và cho cánh tay phải, 1680 shot trong 4 phút và 5 lần mỗi 3 tuần.
Những kết quả đã cho thấy hơn 50% cải thiện về nếp nhăn, da chảy xệ, cấu trúc da được quan sát thấy 10 trong 19 bệnh nhân (53%). Thêm vào đó, về mô học đã chỉ ra có sự gia tăng về mật độ collagen trong lớp nhú bì.
Nghiên cứu này đã đo nhiệt độ bề mặt da trong khi thực hiện kỹ thuật Gen. Bằng kỹ thuật Gen, nhiệt độ da mặt đã tăng từ 33,5 đến 42°C, trong khi nhiệt độ da cánh tay phải tăng từ 32 lên 42,7°C. Bài báo trích dẫn rằng nhiệt độ da 55–65°C tại đó collagen bị biến tính tương quan với nhiệt độ bề mặt da 40–48°C (( Alam M, Dover JS (2003) Nonablative laser and light therapy: an approach to patient and device selection. Skin Therapy Lett 8(4):4–7)). Do đó, bài báo này gợi ý rằng điểm cuối lâm sàng cho kỹ thuật Gen là nhiệt độ bề mặt da từ 40-48°C. Khi một người bị sốt cao trong suốt đợt cảm lạnh thông thường, nhiệt độ cơ thể thường vào khoảng 40°C. Bằng cách chạm vào da của bệnh nhân bằng tay của người bác sĩ sau kỹ thuật Gen và cảm thấy hơi ấm tương tự, có thể giả định rằng đó là điểm cuối lâm sàng của kỹ thuật Gen. Tuy nhiên, không có bằng chứng nào cho thấy nhiệt độ bề mặt da dao động từ 40 đến 48°C khi nhiệt độ da là 55–65°C. Ngoài ra, vẫn chưa có sự thống nhất về điểm cuối lâm sàng của kỹ thuật Gen.
Badawi và cộng sự đã thực hiện laser Nd: YAG 1064-nm xung dài trên 22 bệnh nhân loại da III-VI theo phân loại Fitzpatrick (( Badawi A, Tome MA, Atteya A, Sami N, Morsy IA (2011) Retrospective analysis of non-ablative scar treatment in dark skin types using the sub- millisecond Nd:YAG 1,064 nm laser. Lasers Surg Med 43(2):130–136)). Các thông số là 14–16 J / cm2, thời gian xung 300– 500 μs và tốc độ lặp lại 5–7 Hz. Tay cầm cách bề mặt da 1–2 cm trở lên. Số lần bắn dao động từ 8000 đến 13,900 với trung bình là 11,700 shot. Trung bình 6 lần điều trị được thực hiện trên mỗi bệnh nhân cách nhau khoảng 3 tuần và thời gian theo dõi trung bình sau đợt điều trị cuối cùng là 9 tháng (khoảng 3–10 tháng). Sự cải thiện trung bình có ý nghĩa thống kê và đáng kể về mặt lâm sàng đã cho thấy sẹo: 2, cấu trúc da: 2.3 và sắc tố: 2. Bài báo ngụ ý rằng tác động của kỹ thuật Gen không chỉ cải thiện sẹo và cấu trúc da mà còn cải thiện sắc tố.
Trong bảng 9.9, tôi đã tóm tắt các tác động và các cytokine liên quan đến kỹ thuật Gen từ nhiều bài báo khác nhau.
Bảng 9.9 Tác động và các vấn đề liên quan đến kỹ thuật Gen (( Taylor MB, Prokopenko I (2006) Split-face com- parison of radiofrequency versus long-pulse Nd-YAG treatment of facial laxity. J Cosmet Laser Ther 8(1):17–22)), (( Schmults CD, Phelps R, Goldberg DJ (2004) Nonablative facial remodeling: erythema reduction and histologic evidence of new collagen formation using a 300-microsecond 1064-nm Nd:YAG laser. Arch Dermatol 140(11):1373–1376)), (( Lipper GM, Perez M (2006) Nonablative acne scar reduction after a series of treatments with a short- pulsed 1,064-nm neodymium:YAG laser. Dermatol Surg 32(8):998–1006)), (( Tanaka Y, Matsuo K, Yuzuriha S (2011) Objective assessment of skin rejuvenation using near-infrared 1064-nm neodymium: YAG laser in Asians. Clin Cosmet Investig Dermatol 4:123–130)).
| Tác động của kỹ thuật Gen | Các Cytokine liên quan |
|
|
Cho đến nay, chúng ta đã thảo luận rằng kỹ thuật Gen là một phương pháp NAR hiệu quả. Cơ chế của kỹ thuật Gen vẫn chưa được biết đầy đủ, nhưng cơ chế của tia laser đã từng đưa ra giả thuyết. Trước tiên, chúng ta hãy xem xét các chất màu hấp thu (chromophore) của kỹ thuật Gen là gì. Để biết được chất màu hấp thu, độ dài sóng và thời gian xung của các thông số laser phải được xem xét. Bước sóng của kỹ thuật Gen là 1064 nm. Hệ số hấp thụ của ba chromophore chính đều thấp, nhưng trong số ba tế bào này, hệ số hấp thụ đối với melanin là cao nhất, tiếp theo là máu và cuối cùng là nước. Tôi nghĩ rằng chromophore chính cho kỹ thuật Gen là lớp đáy. Lớp đáy có nhiều sắc tố nhất và đây là nơi tia laser chiếu tới trước khi tiếp xúc với máu. Ngoài ra, thời gian phục hồi nhiệt (TRT) của lớp đáy là khoảng 0,1–0,3 ms, phù hợp với thời gian xung của kỹ thuật Gen là 0,3 ms. Tuy nhiên, mật độ năng lượng khoảng 10 J / cm2, ngụ ý rằng thay vì điều trị trực tiếp lớp đáy, có thể truyền nhiệt đến lớp bì nhú, gần lớp đáy, thông qua sự khuếch tán nhiệt bằng cách chiếu chiếu lặp lại với năng lượng thấp. Chromophore thứ hai của công nghệ Gen là những mạch máu nhỏ, không nhìn thấy được. Nếu TRT của mạch máu nhỏ hơn 4,5 ms (độ dày của mạch máu 0,1 mm), đây là những mạch máu rất mỏng có thể gây đỏ da. Trong số này, có thể có một mạch máu tương ứng với 0,3 ms, và giống như lớp đáy, nếu được chiếu tia nhiều lần với năng lượng thấp, nó có thể truyền nhiệt đến các mạch máu, đặc biệt là lớp bì nhú. Tuy nhiên, đối với laser Nd: YAG 1064-nm xung dài, mật độ năng lượng 20–40 J/cm2 thường được dùng để triệt lông trong khi mật độ năng lượng 140– 160J /cm2 thường được dùng để điều trị tổn thương mạch máu. Có nghĩa là, mật độ năng lượng được sử dụng trong kỹ thuật Gen không đủ để tạo ra nhiệt qua các mạch máu. Tuy nhiên, nó có thể giúp kích thích các mạch máu của bì nhú và giải phóng các cytokine gây viêm, đây là cơ chế thứ hai của NAR.
Bước sóng 1064 nm có thể tạo ra nhiệt toàn bộ lớp bì, bao gồm cả lớp biểu bì, do hệ số hấp thụ của nước, nhưng vì hệ số hấp thụ thấp hơn so với melanin và máu, tôi tin rằng chromophore chính của kỹ thuật Gen là lớp đáy và các mạch của lớp bì nhú. Mô đích được cho là lớp đáy, màng đáy và lớp bì nhú.
Sự mất nhiệt bao gồm ba cơ chế: dẫn nhiệt, đối lưu và bức xạ. Đầu tiên, sự dẫn nhiệt (khuếch tán nhiệt) truyền nhiệt đến các mô xung quanh trong khi các chromophore là cách chính để xảy ra quá trình tản nhiệt. Thứ hai, đối lưu nhiệt là một phương pháp loại bỏ nhiệt của chromophore khi máu đi qua các mạch máu trong các mô. Thứ ba, có bức xạ (( Goldman MP (2006) Cutaneous and cosmetic laser surgery. Mosby Elsevier, Philadelphia, PA)). Trong kỹ thuật Gen, cơ học chính của sự mất nhiệt được cho là sự khuếch tán và đối lưu nhiệt. Trong khi sự mất nhiệt diễn ra hiệu quả và năng lượng tiếp tục được cung cấp bằng cách chiếu xạ liên tục nhiều lần với mức năng lượng thấp, kỹ thuật Gen cân bằng nhiệt của nó ở một nhiệt độ tương đối thấp. Tuy nhiên, năng lượng cao hoặc xếp chồng lên nhau cùng một chỗ có thể dẫn đến bỏng. Đó là lý do tại sao (1) khi bệnh nhân phàn nàn về cảm giác nóng, năng lượng phải được giảm bớt và (2) để tránh tiếp xúc lặp lại, tay cầm nên được di chuyển nhanh hơn hoặc phạm vi tiếp xúc phải được mở rộng ra một khu vực lớn hơn.
Các kỹ thuật Gen từ lâu đã được biết đến tại phòng khám tư, nhưng vẫn có những tranh luận liên quan đến hiệu quả của nó. Tại sao có những tranh cãi về hiệu quả của nó trong khi về mặt lý thuyết, nó có hiệu quả? Đầu tiên, vấn đề là quy trình không được thực hiện trong một thời gian đủ dài. Theo các bài báo, quy trình nên được thực hiện trong 30 phút. Nhưng ở phòng khám tư, rất khó để thực hiện quy trình laser trong 30 phút. Những gì nên được thực hiện? Tôi nghĩ là thay vì thực hiện trên toàn bộ khuôn mặt, giảm diện tích và chỉ thực hiện trên các vùng quan trọng như nám, vùng má và vùng cằm có thể giảm được thời gian. Thứ hai, NAR kém hiệu quả hơn đáng kể so với AR (( Park SH, Yeo WC, Koh WS, Park JW, Noh NK, Yoon CS (2014) Laser dermatology plastic surgery, 2nd edn. (Korean). Koonja, Seoul)). Ở một số bệnh nhân, nó có thể có hiệu quả, nhưng đối với một số người, nó có thể không có tác dụng gì. Thứ ba, không có điểm cuối lâm sàng trong NAR (( Wanner M, Sakamoto FH, Avram MM, Chan HH, Alam M, Tannous Z et al (2016) Immediate skin responses to laser and light treatments: therapeu- tic endpoints: how to obtain efficacy. J Am Acad Dermatol 74(5):821–833. quiz 34, 33)). Ví dụ, có những điểm cuối lâm sàng như sẫm màu, biến mất mạch máu và ban xuất huyết trong liệu pháp mạch máu, nhưng không có điểm cuối lâm sàng trong NAR. Có thể xảy ra các thay đổi lâm sàng như chuyển trắng, nhưng đây không phải là điểm cuối lâm sàng mà là điểm cuối cảnh báo nghĩa là hoại tử mô. Ở NAR không có điểm cuối lâm sàng đặc biệt nào ngoài ban đỏ. Nhưng ngay cả điều này cũng không rõ ràng vì chúng ta không biết ban đỏ sẽ có màu đỏ như thế nào hoặc nên duy trì nó trong bao lâu.
Trước đó, chúng ta đã xem xét điểm cuối lâm sàng cho kỹ thuật Gen là nhiệt độ bề mặt da và bằng cách chạm vào da của bệnh nhân bằng tay bác sĩ sau kỹ thuật Gen và cảm thấy hơi ấm tương tự như sốt cao khi cảm lạnh thông thường là điểm cuối lâm sàng. Nhưng đây vẫn chưa phải là một sự đồng thuận, và nó không chính xác. Tuy nhiên, khi bệnh nhân cảm thấy nóng, chúng ta nên coi đó là điểm cuối cảnh báo vì điều này có thể cho thấy khả năng bị bỏng. Trong trường hợp này, chúng ta nên dừng kỹ thuật Gen hoặc di chuyển tay cầm một cách nhanh chóng để nhiệt độ tăng lên từ từ.
4. Nguyên bào sợi trong lớp bì nhú và lớp bì lưới
Chúng ta đã biết rằng trong quá trình mài da cơ học hoặc sử dụng laser CO2 AR (tái tạo bề mặt da), có thể xảy ra sẹo nếu da bị loại bỏ vượt ra lớp bì nhú đến lớp bì lưới. Chúng ta biết rằng trong quá trình AR bằng laser CO2, chúng ta nên dừng lại khi thấy một lớp màu vàng. Sở dĩ nó có màu vàng là do tuyến bã nhờn. Đây là ranh giới giữa lớp bì nhú và lớp lưới. Đi sâu hơn ranh giới này và làm tổn thương lớp lưới, tương tự như vết thương bỏng toàn bộ, dẫn đến da trở nên cứng và hình thành sẹo và không có sự hiện diện của các phần phụ thượng bì như nang lông, tuyến bã nhờn và tuyến sinh dục (( Woodley DT (2017) Distinct fibroblasts in the pap- illary and reticular dermis: implications for wound healing. Dermatol Clin 35(1):95–100)). Tại sao có nguy cơ cao để lại sẹo khi lớp bì lưới bị tổn thương?
Nguyên bào sợi tổng hợp tất cả các thành phần của lớp bì. Nó điều chỉnh và thay thế quá trình tổng hợp collagen và các thành phần chất nền ngoại bào (ECM) của da (( Woodley DT (2017) Distinct fibroblasts in the pap- illary and reticular dermis: implications for wound healing. Dermatol Clin 35(1):95–100)). Nguyên bào sợi được biết là có vai trò đặc biệt quan trọng trong việc chữa lành vết thương. Khi mô bị tổn thương, các nguyên bào sợi sẽ di chuyển đến vùng bị tổn thương, tạo ra collagen mới và thúc đẩy quá trình chữa lành vết thương. Nguyên bào sợi khác nhau ở lớp bì nhú và lớp bì lưới, ở lớp bì nhú là nơi có nhiều nguyên bào sợi hơn và ở dạng hoạt động hơn. Chúng ta hãy xem xét kỹ hơn sự khác biệt giữa nguyên bào sợi ở lớp bì nhú và lớp bì lưới.
Qua nghiên cứu, Ryan R. Driskell và cộng sự đã chỉ ra các nguyên bào sợi trong lớp bì nhú và lớp bì lưới đến từ các dòng khác nhau. Nói cách khác, các nguyên bào sợi của lớp bì nhú đóng một vai trò quan trọng trong quá trình phát triển của tóc bằng cách hình thành lớp bì nhú và hình thành nang lông và cơ xương sống, trong khi các nguyên bào sợi của lớp bì lưới hình thành lớp bì lưới và lớp mỡ dưới da (hypodermis) (( Woodley DT (2017) Distinct fibroblasts in the pap- illary and reticular dermis: implications for wound healing. Dermatol Clin 35(1):95–100)).
Hãy xem lại thí nghiệm của Ryan R. Driskell và cộng sự. 19 kháng thể được xem là “ marker nguyên bào sợi” được tiêm vào những con chuột trước khi sinh và được kiểm tra vào ngày thứ hai sau khi sinh để xác nhận rằng các nguyên bào sợi của lớp bì nhú và lớp bì lưới có các marker nguyên bào khác nhau (Bảng 9.10).
Bảng 9.10 Nhuộm các marker nguyên bào sợi được chọn lọc ở lớp bì nhú và lớp bì lưới trong da ở gia đoạn cuối thai kỳ/sau sinh
| Marker tế bào | Lớp bì nhú | Lớp bì lưới |
| PDGFR alpha | Dương tính | Dương tính |
| CD34 | Dương tính | Dương tính |
| BLIMP 1 | Dương tính | Âm tính |
| CD26 | Dương tính | Âm tính |
| Lrig1 | Dương tính | Âm tính |
| Sca1 | Âm tính | Dương tính |
| DLK1 | Âm tính | Dương tính |
Protein trưởng thành do tế bào lympho B BLIMP gây ra, sự biệt hóa cụm CD, DLK1 Delta-like homolog 1, sự lặp lại giàu leucine Lrig1 và chuỗi domain protein giống immunoglobulin 1, thụ thể yếu tố tăng trưởng alpha có nguồn gốc từ tiểu cầu PDGFR alpha, Sca1 stem cells antigen 1 (Sao chép từ (( Woodley DT (2017) Distinct fibroblasts in the pap- illary and reticular dermis: implications for wound healing. Dermatol Clin 35(1):95–100))).
Kết quả cho thấy các marker nguyên bào sợi PDGFR-α và CD34 đều được tìm thấy trong các nguyên bào sợi của lớp bì nhú và lớp bì lưới, nhưng BLIMP-1, CD26 và Lrig1 chỉ được tìm thấy trong các nguyên bào sợi của lớp bì nhú trong khi Sca1 và DLK1 chỉ được tìm thấy trong nguyên bào sợi của lớp bì lưới.
Hai nguyên bào sợi với các marker sau đó được chiết xuất từ da và trộn nhau. Lần này, một buồng silicone được đưa vào lưng con chuột thí nghiệm và các nguyên bào sợi hỗn hợp được tiêm vào (Hình 9.10). Đáng ngạc nhiên, họ phát hiện ra rằng các nguyên bào sợi trong buồng tạo ra mô giống như da. Tương tự như lớp thượng bì và lớp bì, nó được cấu tạo bởi hai lớp được phân chia bởi màng đáy, bao gồm collagen type VII và sợi fibril.
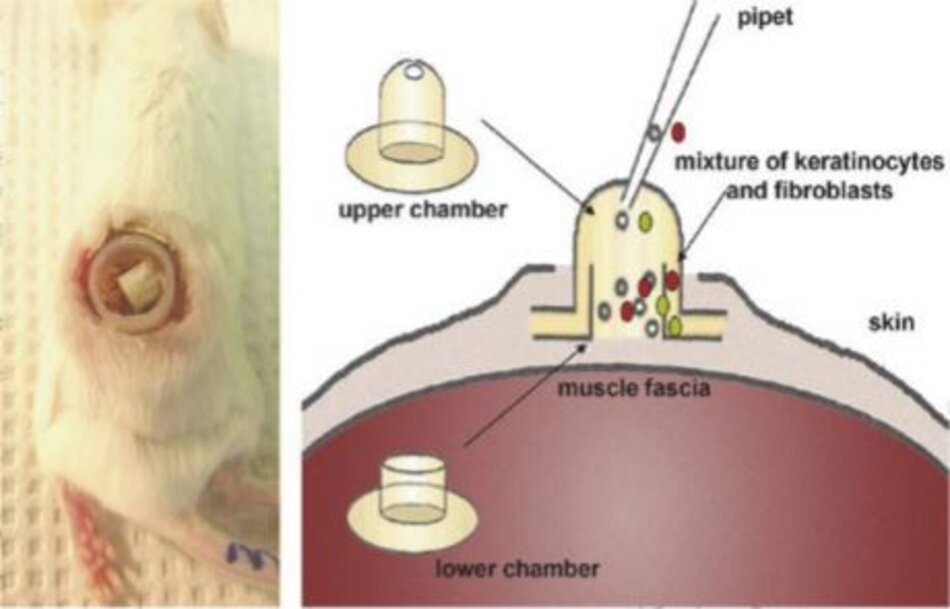
Khi các tế bào CD26+, BLIMP+, và Sca 1(các nguyên bào sợi từ lớp bì nhú) được chuyển vào buồng silicone, lớp bì nhú được sản xuất. Khi các tế bào với các marker khác (các nguyên bào sợi từ lớp bì lưới) được chuyển vào, lớp bì lưới và lớp mỡ dưới da được sản xuất. Các tế bào CD26+, BLIMP+, và Sca 1 (các nguyên bào sợi từ lớp bì nhú) đóng vai trò quan trọng trong hình thành nang lông, trong khi CD26+, BLIMP+, và DLK1+ (các nguyên bào sợi từ lớp bì lưới) đóng vai trò quan trọng trong hình thành lớp mỡ dưới da. Dựa vào những phát hiện này, chúng ta có thể kết luận rằng nguồn gốc của các nguyên bào sợi của 2 lớp bì là khác nhau và đóng vai trò khác nhau trong việc chữa lành vết thương.
Việc chữa lành vết thương có thể được chia thành hai loại. Lành thương thay thế và lành thương tăng sinh. Lành vết thương thay thế, chẳng hạn như sẹo bỏng, khi chúng lành lại, để lại sẹo và biến đổi thành các mô không có phần phụ thượng bì như nang lông, tuyến eccrine và tuyến bã nhờn (( Woodley DT (2017) Distinct fibroblasts in the pap- illary and reticular dermis: implications for wound healing. Dermatol Clin 35(1):95–100)). Ví dụ về lành vết thương tăng sinh là kỳ nhông và bào thai người. Kỳ nhông có thể tái tạo một chân mới đầy đủ chức năng sau khi chân ban đầu của chúng bị cắt bỏ. Trong ba tháng đầu của thai kỳ, ngay cả khi thai nhi bị thương trong tử cung thì chúng cũng không để lại sẹo.
Tóm lại, nếu tổn thương chỉ giới hạn ở lớp thượng bì và lớp bì nhú, quá trình lành thương tăng sinh sẽ diễn ra, đó là vai trò của các nguyên bào sợi của lớp bì nhú, và một lớp thượng bì hoàn toàn mới và lớp bì nhú được hình thành. Mặt khác, nếu lớp bì lưới bị tổn thương, quá trình lành thương thay thế sẽ diễn ra, đó là vai trò của các nguyên bào sợi của lớp bì lưới, do đó sẹo sẽ xảy ra.
Tại sao quá trình lành thương thay thế lại diễn ra, sau khi lớp bì lưới bị tổn thương? Tôi nghĩ lý do cho điều này là vì chức năng quan trọng nhất của da là chức năng hàng rào; để bảo vệ cơ thể của chúng ta khỏi thế giới bên ngoài. Khi tổn thương chỉ giới hạn ở lớp thượng bì và lớp bì nhú, lớp bì lưới đóng vai trò như một rào cản, vì vậy không có vấn đề gì lớn trong chức năng hàng rào ngay cả khi quá trình hồi phục tăng sinh diễn ra. Nhưng nếu lớp bì lưới bị tổn thương, chữa lành vết thương thay thế sẽ cần thiết để phục hồi nhanh chóng chức năng hàng rào mặc dù có sẹo (Bảng 9.11).
Bảng 9.11 So sánh nguyên bào sợi ở lớp bì nhú và lớp bì lưới
| Nguyên bào sợi ở lớp bì nhú | Nguyên bào sợi ở lớp bì lưới | |
| Sự lành thương | Tăng sinh | Thay thế |
| Tạo sẹo | Không | Có |
| Ví dụ | Kỳ nhông
Bào thai người(ba tháng đầu) |
Sẹo bỏng |
| Ý nghĩa | Về mặt thẩm mỹ | Sống còn |
| Laser xâm lấn | Tái tạo bề mặt bằng laser CO2 | Laser CO2 vi điểm |
| Laser không xâm lấn | Kỹ thuật Gen, laser mạch máu | Needle RF laser Er:Glass fractional |
Khi chọn lựa laser, chúng ta nên xem xét đến sự khác nhau của nguyên bào sợi ở lớp bì nhú và bì lưới, và sự khác nhau trong quá trình lành thương. Như vậy, laser nào sẽ hiệu quả nhất? Loại laser hiệu quả nhất để trẻ hóa lớp bì nhú là tái tạo bề mặt bằng laser CO2. Vậy thì loại laser nào hiệu quả nhất cho lớp bì lưới?
Nên hạn chế tổn thương đến lớp bì lưới càng nhiều càng tốt vì quá trình lành thương thay thế có thể gây sẹo. Tuy nhiên, tái tạo collagen trong lớp bì lưới có thể có hiệu quả đối với độ đàn hồi, nếp nhăn sâu và sẹo. Nói cách khác, lớp bì lưới cũng có thể là mục tiêu điều trị. Với thực tế là sự biến tính một phần của collagen hiệu quả và an toàn hơn so với sự biến tính toàn bộ của collagen, tôi tin rằng lý thuyết về quá trình quang nhiệt vi điểm là phương pháp thích hợp nhất. Laser CO2 vi điểm được biết đến là phương pháp điều trị sẹo hiệu quả. Phương pháp hiệu quả nhất đối với NAR của lớp bì lưới cũng phải tuân theo lý thuyết quang nhiệt vi điểm. Vì vậy, sử dụng kim RF lưỡng cực xâm lấn tần số cao hoặc laser Er: Glass 1550-nm vi điểm có vẻ phù hợp.
Lý tưởng nếu collagen được tái tạo trong cả lớp bì lưới và nhú. Điều trị kết hợp là cần thiết để điều này xảy ra. Nếu vậy, chúng ta nên sử dụng kết hợp những gì? Nếu chúng ta xem lại Bảng 9.11, chúng ta có thể thấy rằng một số liệu pháp kết hợp có thể thực hiện được. Phương pháp hiệu quả nhất sẽ là tái tạo bề mặt bằng laser CO2 với điều trị bằng laser CO2 vi điểm. Tuy nhiên, nếu các quy trình này được thực hiện trong cùng một ngày sẽ có nguy cơ dẫn đến các tác dụng phụ nghiêm trọng. Sẽ tốt hơn nếu thực hiện chúng vào những ngày khác nhau. Phương pháp NAR hiệu quả nhất sẽ là sự kết hợp của kỹ thuật Gen và kim RF. AR và NAR cũng có thể được sử dụng kết hợp. Ví dụ, có thể tiến hành tái tạo bề mặt bằng laser CO2 sau khi sử dụng kim RF.
Trước đó, chúng ta đã đưa ra ba câu hỏi trong Phần 9.2.2. Bây giờ, chúng ta sẽ giải quyết ba câu hỏi này. Đầu tiên, trong việc trẻ hóa da, thời gian cần được quan tâm. Theo phương trình Arrhenius, nhiệt độ là quan trọng nhưng thời gian cũng quan trọng. Thứ hai, tổn thương phải được tính đến. Ngoài ngưỡng tổn thương, còn có một ngưỡng tổn tại mà tại đó sẹo có thể xảy ra. Năng lượng cao không đảm bảo hiệu quả. Do đó, có hai phương pháp cho NAR và tôi khuyên nên dùng phương pháp B. Thứ ba, lớp điều trị nên được xem xét. Lớp bì lưới không nên điều trị quá mạnh. Điều trị vi điểm được khuyến khích vì nó hiệu quả và an toàn.
5. Laser không xâm lấn
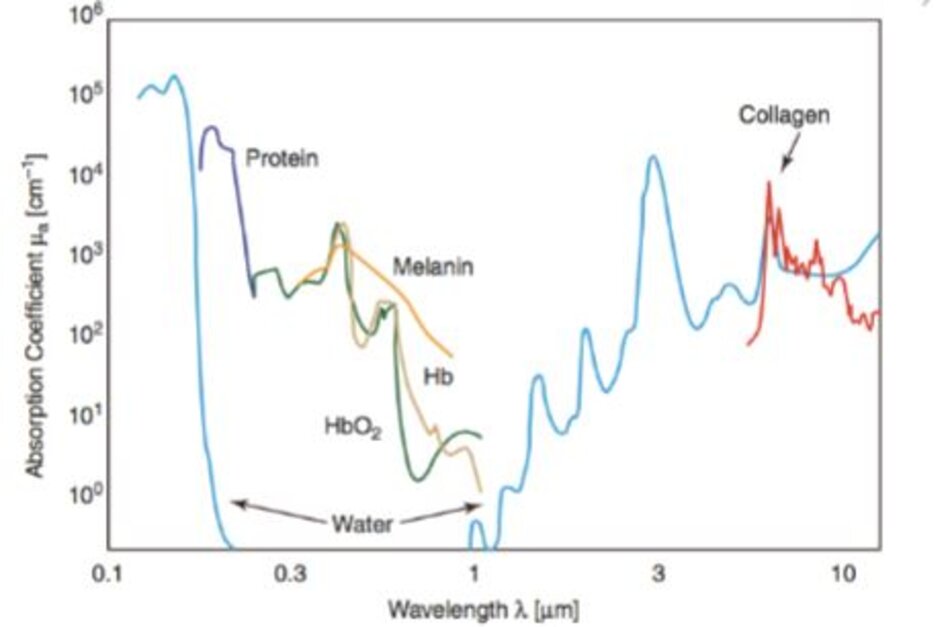
5.1 Đường cong hấp thụ collagen và nước
Đường cong hấp thụ collagen chỉ tồn tại ở vùng hồng ngoại xa (FIR,> 3 μm) và đạt đỉnh trong khoảng 6000 đến 7000 nm (Hình 9.11). Có một loại “laser điện tử tự do” sử dụng bước sóng này để đốt nóng trực tiếp collagen, nhưng nó vẫn chưa được thương mại hóa (( Goldman MP (2006) Cutaneous and cosmetic laser surgery. Mosby Elsevier, Philadelphia, PA)). Vì vậy, trẻ hóa da liên quan đến việc dẫn nhiệt gián tiếp từ nước bằng cách sử dụng các tia laser có hệ số hấp thụ đối với hầu hết nước, chẳng hạn như laser CO2 laser Er: YAG và tia hồng ngoại trung (MIR).
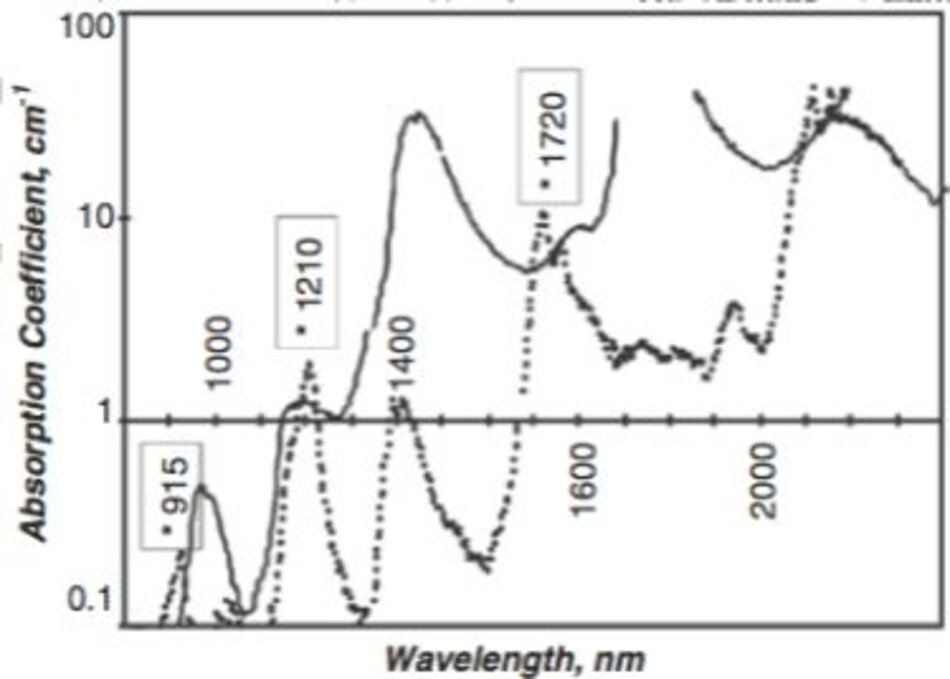
Các đường cong hấp thụ của nước cho thấy sự hấp thụ rất thấp trong dải tử ngoại và ánh sáng nhìn thấy, và tạo thành các đỉnh nhỏ ở 980 nm, các đỉnh lớn hơn ở 1060 và 1480 nm, và các đường cong hấp thụ tăng dần từ tia hồng ngoại trung (MIR) (Hình 9.12) (( Goldman MP (2006) Cutaneous and cosmetic laser surgery. Mosby Elsevier, Philadelphia, PA)).
5.2 Phân loại laser không xâm lấn theo cơ chế
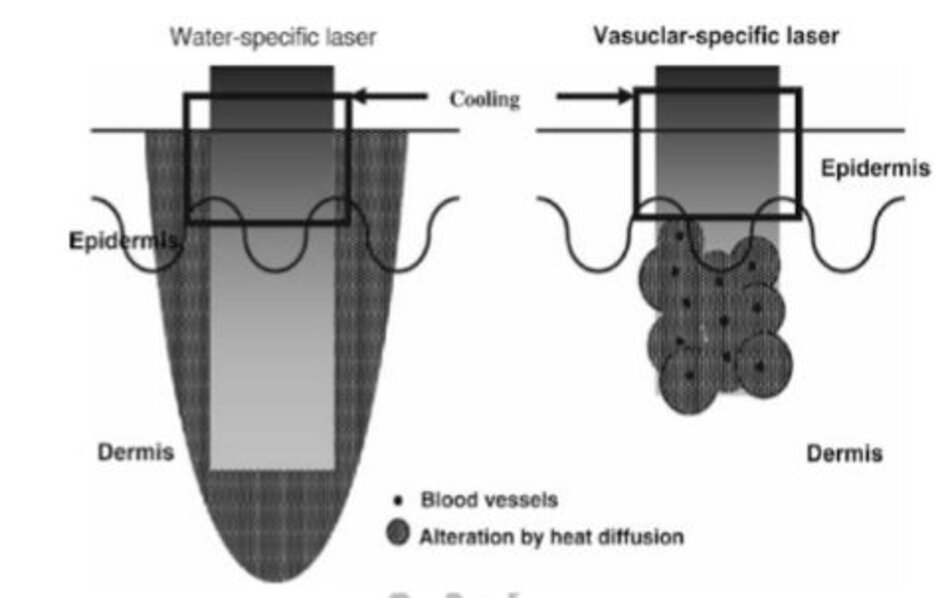
Mô đích cuối cùng của NAR là collagen, nhưng các phương pháp gián tiếp được sử dụng vì chúng ta không thể nhắm trực tiếp vào collagen bằng laser. Có hai mô đích gián tiếp của NAR: Thứ nhất, nước. Bằng cách tăng nhiệt độ của nước trong lớp bì qua cách sử dụng tia hồng ngoại trung, nhiệt độ của collagen cũng có thể được tăng lên. Thứ hai, mạch máu. Bằng cách tăng nhiệt độ của mạch máu qua cách sử dụng tia laser mạch máu, nhiệt độ của collagen cũng có thể được tăng lên. (Hình 9.13) (( Goldman MP (2006) Cutaneous and cosmetic laser surgery. Mosby Elsevier, Philadelphia, PA)).
Bảng 9.12 Cơ chế của NAR dựa vào mục tiêu
| Mục tiêu | Cơ chế |
| Nước | Làm nóng trực tiếp da → collagen mới |
| Hb và/hoặc melanin | Làm nóng gián tiếp da → collagen mới Mạch da và/hoặc cấu trúc phần phụ → chất trung gian tế bào và yếu tố tăng trưởng → phản ứng chữa lành vết thương → collagen mới |
| Điều biến quang | LLLT-LED, PDT |
Mô đích và cơ chế của NAR có thể được tóm tắt trong bảng 9.12. Đầu tiên, tái tạo collagen gián tiếp được thực hiện bằng cách làm nóng trực tiếp lớp da, …, tức là sử dụng nhiệt tác động vào nước của lớp bì bằng cách sử dụng bước sóng có hệ số hấp thụ cao đối với nước. Thứ hai, tái tạo collagen gián tiếp đạt được bằng
cách làm nóng da trực tiếp, tức là sử dụng nhiệt của laser mạch máu với hệ số hấp thụ cao đối với hemoglobin tác động vào mạch máu, và sau đó tác động nhiệt gián tiếp vào nước của mạch máu. Thứ ba, nhiệt được chiếu vào mạch máu dưới da và các mô xung quanh bằng laser mạch máu, từ đó giải phóng các chất trung gian tế bào và các yếu tố tăng trưởng, do đó tạo ra collagen thông qua quá trình chữa lành vết thương. Cuối cùng là điều chế quang.
5.3 Laser không xâm lấn dành cho người Hàn Quốc
Dựa trên những nghiên cứu trước đó, laser không xâm lấn có thể được phân loại gồm laser hồng ngoại trung và laser mạch máu. Ngoài ra, mặc dù không phải là laser, nhưng các phương pháp không xâm lấn có thể được thêm vào danh sách này (Bảng 9.13).
Vậy thiết bị NAR tốt nhất dành cho người Hàn Quốc là gì? Ngoại trừ laser mạch máu có bước sóng 500–600 nm, cả laser hồng ngoại trung và thiết bị không xâm lấn đều không liên quan đến màu da. Do đó, cả hai đều có thể được sử dụng một cách an toàn bất kể màu da. Nhưng phương pháp nào hiệu quả nhất? Về mặt lý thuyết, laser mạch máu có vẻ kém hiệu quả hơn, vì đầu tiên nó phải làm nóng các mạch máu, sau đó đến nước và cuối cùng tiếp cận collagen. Nhưng không có bài báo nào nêu ra điều này. Các laser hồng ngoại trung hầu hết không sử dụng ở phòng khám tư do đau nhiều và có tác dụng phụ.
Bảng 9.13 Các loại laser và thiết bị trong NAR
| Các loại laser và thiết bị trong NAR | Bước sóng | Tên hãng |
| Laser hồng ngoại trung | Er:Glass 1540 nm | Aramis |
| Diode 1450 nm | Smoothbeam | |
| Nd:YAG 1320 nm | CoolTouch | |
| Laser mạch máu | IPL, PDL, KTP xung dài 532 nm, và laser Nd:YAG xung dài 1064 nm | |
| Thiết bị không xâm lấn | RF, kim RF, Sóng siêu âm hội tụ | Thermage, LDM, and Ulthera |
Và như chúng ta đã thấy trong Bảng 9.11 trước (So sánh các nguyên bào sợi của lớp bì nhú và bì lưới), điều trị nên được chia thành điều trị lớp bì nhú và lớp bì lưới. Tôi tin rằng kỹ thuật Gen thích hợp nhất để điều trị ở lớp bì nhú. Trong điều trị lớp bì lưới, kim RF phù hợp với lý thuyết quang nhiệt vi điểm và được coi là phù hợp nhất về giá cả và độ chính xác.
6. Mặt hạn chế của laser không xâm lấn
NAR không cần thời gian nghỉ dưỡng và ít tác dụng phụ. Tuy nhiên, NAR có một số nhược điểm. Hãy xem lại các nhược điểm của NAR.
Đầu tiên, NAR kém hiệu quả hơn đáng kể so với trẻ hóa da xâm lấn (( Park SH, Yeo WC, Koh WS, Park JW, Noh NK, Yoon CS (2014) Laser dermatology plastic surgery, 2nd edn. (Korean). Koonja, Seoul)). Thứ hai, kết quả không nhất quán. Một số bệnh nhân thấy nó hiệu quả, trong khi những người khác thì không. Thứ ba, mặc dù gây tê tại chỗ, vẫn có sự khó chịu đáng kể. Đau có thể trầm trọng ở phương pháp A. Thứ tư, thời gian tiến hành rất dài (15–20 phút) đối với phương pháp B, vì vậy bác sĩ không muốn thực hiện tiến trình. Nhưng nếu chúng ta rút ngắn tiến trình thì nó kém hiệu quả hơn (( Goldman MP (2006) Cutaneous and cosmetic laser surgery. Mosby Elsevier, Philadelphia, PA)). Thứ năm, không có điểm cuối lâm sàng (( Wanner M, Sakamoto FH, Avram MM, Chan HH, Alam M, Tannous Z et al (2016) Immediate skin responses to laser and light treatments: therapeu- tic endpoints: how to obtain efficacy. J Am Acad Dermatol 74(5):821–833. quiz 34, 33)). Triệu chứng duy nhất có thể nhìn thấy là đỏ da, nhưng chúng ta không biết đỏ da sẽ kéo dài trong bao lâu và màu đỏ của nó như thế nào. Triệu chứng tiếp theo được quan sát thấy trên da là làm trắng thượng bì ngay lập tức, một điểm cuối cảnh báo cho thấy sự hình thành sẹo. Đây không phải là điểm cuối lâm sàng, mà là điểm cuối cảnh báo. Do đó, trong NAR năng lượng tối đa, số lần bắn tối đa và quy trình nên được cài đặt trước.
Vậy tại sao NAR lại kém hiệu quả hơn AR một cách đáng kể?
Đầu tiên, NAR có phạm vi điều trị rất hẹp so với AR. NAR phải điều chỉnh nhiệt độ giữa ngưỡng tổn thương và ngưỡng tồn tại, cái này rất hẹp. Mặt khác, trong AR, nếu nhiệt độ trên 100°C, mô da trên ngưỡng tồn tại ở bất kỳ nhiệt độ nào thường bị bay hơi hoặc bị tách ra khỏi da trong quá trình lành thương, chỉ còn lại mô giữa ngưỡng tổn thương và ngưỡng tồn tại. Thứ hai, sinh thiết sau AR bằng laser CO2 hoặc laser Er: YAG cho thấy một dải phân bố nhiệt mỏng. Mặt khác, NAR có sự phân bố nhiệt rộng trong da. Ở da lão hoá có đồi mồi, được quan sát thấy ở lớp nông (độ sâu từ 100–400 μm). Peel da cơ học, peel da hóa học hoặc tái tạo bề mặt bằng laser CO2 loại bỏ lớp này và khởi động cho việc tái tạo collagen. Nói cách khác, phạm vi của AR là hẹp, nhưng nó loại bỏ chính xác lớp nông mà chúng ta muốn nhắm đến và tạo ra sự tái tạo mô nhất định. Nhưng phạm vi của NAR rộng và sâu, và đôi khi nó có thể không hiệu quả hoặc hiệu quả không đủ đến lớp mà chúng ta muốn nhắm đến. Ngoài ra, hầu như chỉ có thể tạo ra nhiệt trong vùng dưới thượng bì bởi NAR. Làm mát thượng bì là cần thiết trong NAR, khó để làm mát thượng bì trong khi tạo ra nhiệt ngay dưới lớp thượng bì. Thay vào đó, có nhiều nguy cơ hình thành sẹo rỗ trong khi cố gắng tạo ra đủ nhiệt dưới thượng bì (( Goldman MP (2006) Cutaneous and cosmetic laser surgery. Mosby Elsevier, Philadelphia, PA)).
Thứ ba, là giả định của cá nhân tôi. AR, chẳng hạn như laser CO2, sẽ dẫn đến cả bóc tách và tổn thương nhiệt (Tổn thương nhiệt có thể được chia thành tổn thương nhiệt không hồi phục và tổn thương nhiệt hồi phục. Tổn thương nhiệt không hồi phục đôi khi được coi giống như thiệt hại nhiệt dư. Xem ” Chương 10 ”). Peel bằng hóa chất hoặc cơ học chỉ mang lại kết quả là bóc tách. NAR chỉ dẫn đến tổn thương do nhiệt (Bảng 9.14).
Bảng 9.4 Trẻ hóa da và tổn thương mô
| Phương pháp | Mô tổn thương |
| Trẻ hóa da xâm lấn | Bóc tách, tổn thươn nhiệt phục hồi và không phục hồi |
| Peel da hóa học, mài da | Bóc tách |
| Trẻ hóa da không xâm lấn | Tổn thương nhiệt hồi phục và không hồi phục |
Quy trình trẻ hóa da hiệu quả nhất theo thứ tự là AR, peel da hóa học, peel da cơ học và NAR.
Kết luận, chúng ta có thể cho rằng bóc tách là tổn thương mô hiệu quả nhất đến quá trình tổng hợp collagen. Bóc tách có thể hiệu quả nhất vì quá trình chữa lành vết thương được kích hoạt nhiều nhất. Đây có thể là lý do tại sao NAR có thể kém hiệu quả nhất vì không có sự bóc tách.
7 Kết luận về laser không xâm lấn
Ở Hàn Quốc, nhu cầu xóa nhăn không nhiều, và NAR kém hiệu quả hơn AR. Đây là những yếu tố đôi khi khiến chúng ta đánh giá thấp về NAR. Nhưng NAR là một tiến trình cần thiết. Lý do như sau: Thứ nhất, vẫn còn nhu cầu về cấu tạo da, kích thước lỗ chân lông và đỏ da mặt. Thứ hai, NAR không có thời gian nghỉ dưỡng và nhu cầu về việc này đang dần tăng lên. Thứ ba, và nguyên nhân quan trọng nhất là do nám. Trong điều trị nám, cách duy nhất để cải thiện lớp bì mà không làm ảnh hưởng đến lớp thượng bì (nơi chứa các tế bào hắc tố) là NAR. Vì vậy, NAR rất hữu ích ở người Hàn Quốc, vì tỷ lệ nám da và hoạt động của các tế bào melanocyte đều cao ở người Hàn Quốc.
8 Điều biến quang
8.1 Đường cong Arndt–Schultz
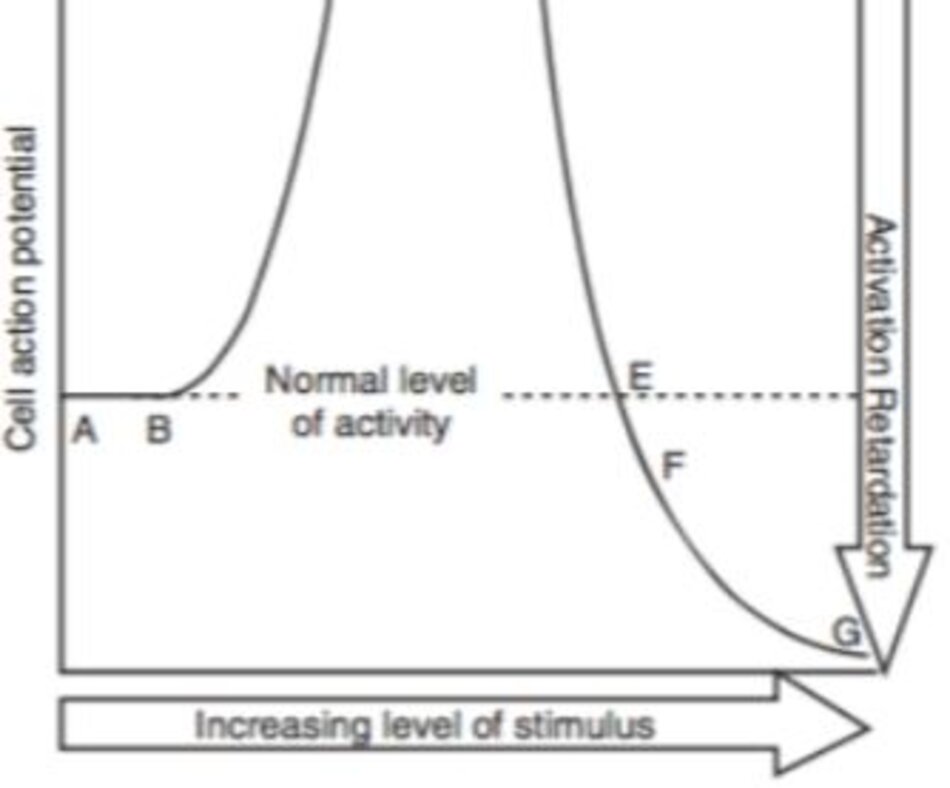
Bây giờ, chúng ta hãy thảo luận về cơ chế và hiệu quả của điều biến quang Đầu tiên chúng ta sẽ thảo luận về định luật Arndt – Schultz, được coi là nguyên tắc cơ bản của điều biến quang. Định luật Arndt – Schultz quy định rằng tất cả các loại thuốc và các loại độc tố đều kích thích hoạt động sống ở liều thấp nhưng lại ức chế và phá hủy hoạt động sống ở liều trung bình. Các chất gây kích ứng dưới mức có hại bao gồm kháng sinh, nọc rắn, nhiệt, bức xạ và từ trường. Hình 9.14 làm dễ hiểu hơn về điều này. Không có sự thay đổi trong các tế bào từ A – B, nhưng khi dùng nhiều hơn một lượng kích thích nhất định, hoạt động của tế bào sẽ tăng lên (B – C). Sau đó hoạt động tế bào tăng cao (C – D) và giảm (D – E), và cuối cùng hoạt động tế bào giảm xuống dưới mức bình thường và gây ra tổn thương tế bào (E – F), và chết tế bào (F – G) (( Calderhead RG, Vasily DB (2016) Low level light therapy with light-emitting diodes for the aging face. Clin Plast Surg 43(3):541–550)).
Về liệu pháp ánh sáng mức độ thấp (LLLT), liệu pháp ánh sáng mức độ trung bình (MLLT) và liệu pháp ánh sáng mức độ cao (HLLT), phần E-F và F-G có thể được xem là MLLT hoặc HLLT tương ứng. Phần tương ứng cho điều biến quang là phần B – E, ứng với LLLT. Nói cách khác, điều biến quang là một phương pháp điều trị kích thích tế bào sử dụng photon để tăng hoạt động của tế bào chứ không gây tổn thương tế bào hoặc làm chết tế bào.
Xem xét khái niệm của Calderhead về ngưỡng tổn thương và ngưỡng tồn tại, điều biến quang xảy ra dưới ngưỡng tổn thương. Điều biến quang được biết là không tạo ra nhiệt, và mặc dù nó được định nghĩa trên cơ sở là không có nhiệt được tạo ra, nhưng thực tế nó có thể tạo ra một số nhiệt.
Điều biến quang có ba tác động ở cấp độ tế bào. Đầu tiên, nếu các tế bào quang điện bị tổn thương và bị ức chế, điều biến quang sẽ xử lý các tế bào này. Thứ hai, điều biến quang giúp cho hoạt động của tế bào diễn ra tốt hơn và nhanh hơn. Ví dụ, nó thúc đẩy quá trình tổng hợp collagen của các nguyên bào sợi. Thứ ba, nếu không có đủ tế bào, điều biến quang sẽ triệu tập các tế bào khác tại đó và thúc đẩy các tế bào đang tồn tại tăng sinh (( Calderhead RG, Vasily DB (2016) Low level light therapy with light-emitting diodes for the aging face. Clin Plast Surg 43(3):541–550)).
8.2 Diode phát quang
Năm 1988, đèn LED mới (hay còn gọi là NASA LED) được phát triển bởi Giáo sư Harry Whelan từ Cơ quan Hàng không và Vũ trụ Quốc gia (NASA). Kể từ đó LED đã được sử dụng để điều biến quang do hiệu quả chữa lành vết thương và hiệu quả LLLT của nó.
Đèn LED có một chip bán dẫn nhỏ ở trung tâm tạo ra ánh sáng khi dòng điện chạy qua. Như vậy, đèn LED là ánh sáng, không phải là tia laser. Bốn đặc tính của ánh sáng, định nghĩa chúng từ laser là đa sắc, không liên kết, phân kỳ và cường độ thấp. Đèn LED của NASA có thể vượt qua hai trong số bốn đặc điểm ánh sáng. Thứ nhất, chất lượng của đèn LED càng cao thì độ rộng dải càng hẹp, do đó nó có thể tạo ra dải bước sóng chỉ hơi vượt ra ngoài bước sóng đặc trưng. Đây được gọi là chuẩn đơn sắc (quasimonochromaticity). Thứ hai, một tấm phản xạ hình parabol có thể được sử dụng để triệt tiêu sự phân tán từ 60 ° đến 110 °. Tuy nhiên, không giống như laser CO2, không có khả năng hội tụ vì nó không tạo ra sự chuẩn trực hoàn hảo. Tuy nhiên, đèn LED của NASA không thể xuất hiện quá mức và cường độ thấp, nhưng đây không phải là vấn đề trong điều biến quang (( Calderhead RG, Vasily DB (2016) Low level light therapy with light-emitting diodes for the aging face. Clin Plast Surg 43(3):541–550)).
Thay vào đó, có một số lợi thế đối với đèn LED. Đầu tiên, cần rất ít dòng điện để tạo ra ánh sáng. Thứ hai, vì đèn LED là chất bán dẫn rắn nên không cần đèn nháy như đèn dây tóc hoặc đèn huỳnh quang. Tức là không cần vật tư tiêu hao. Đây là lý do tại sao các bảng hiệu và đèn trong nhà được thay đổi thành đèn LED ngày nay. Thứ ba, do chuẩn đơn sắc (ánh sáng có dải bước sóng vài nanomet) nên đèn LED có mục tiêu đặc hiệu, giống như tia laser. Thứ tư, bác sĩ có thể không cần thao tác vì các đèn LED có thể được bố trí gần nhau trong một vùng rộng lớn để có thể chiếu xạ toàn bộ khuôn mặt cùng một lúc. Thứ năm, ưu điểm lớn nhất là giá rẻ. Một ưu điểm khác là không gây đau đớn và tác dụng phụ và có thể sử dụng ở mọi lứa tuổi từ trẻ sơ sinh đến người già, đây không hẳn là ưu điểm của đèn LED mà là ưu điểm của điều biến quang (( Calderhead RG, Vasily DB (2016) Low level light therapy with light-emitting diodes for the aging face. Clin Plast Surg 43(3):541–550)).
8.3 Dải điều biến sinh quang của Karu
Điều biến quang được xác định ba thông số của laser (bước sóng, độ rộng xung, và mật độ năng lượng). Bước sóng là thông số quan trọng nhất trong điều biến quang vì nếu không có hấp thụ thì không thể xảy ra phản ứng (( Calderhead RG (2007) The photobiological basics behind light-emitting diode (LED) phototherapy. Laser Ther 16(2):97–108)). Vậy bước sóng nào là bước sóng hiệu quả nhất của điều biến quang trong trẻ hóa da?
Tiina Karu, một nhà nghiên cứu quang học nổi tiếng của Nga, tuyên bố rằng dải điều biến sinh quang phù hợp cho điều biến quang là từ màu đỏ nhìn thấy được (khoảng 620 nm) đến hồng ngoại gần (khoảng 1000 nm) (( Calderhead RG, Vasily DB (2016) Low level light therapy with light-emitting diodes for the aging face. Clin Plast Surg 43(3):541–550)).
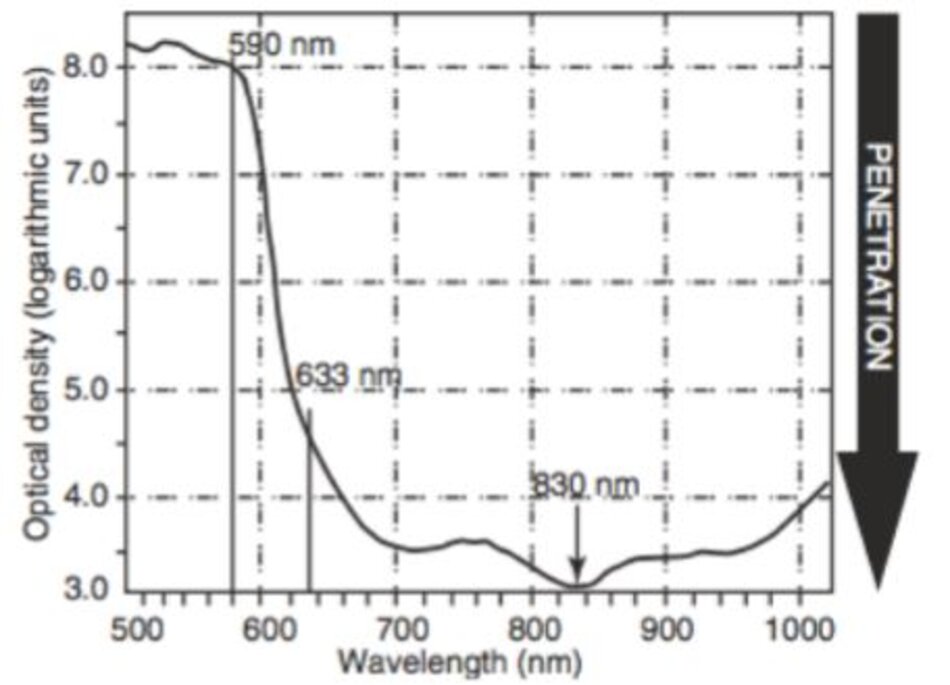
Bước sóng được hấp thụ càng tốt thì độ xuyên thấu càng nông. Ngược lại, độ hấp thụ càng kém thì độ xuyên thấu càng sâu. Trong hình 9.15, trục y là mật độ quang học (OD), biểu thị sự hấp thụ của toàn bộ da theo bước sóng không liên quan đến chromophore. Tỷ lệ hấp thụ càng thấp, độ sâu xuyên thấu càng sâu, vì vậy khi nó đi xuống trục z, độ sâu xuyên thấu càng sâu. Các bước sóng màu xanh lá cây và màu vàng (bước sóng 500–600 nm) được hấp thụ vào máu và melanin, làm cho chúng khó thâm nhập vào mô sống. Do đó, các bước sóng màu xanh lá cây và màu vàng không thích hợp để xuyên thấu sâu. Điều biến quang để trẻ hóa da đòi hỏi một bước sóng có thể tác động vào lớp bì để làm lành vết thương và trẻ hóa. Trong hình 9.15, chúng ta có thể thấy rằng bước sóng từ 620 đến 1000 nm là dải điều biến sinh quang thích hợp.
Trong khi 633 nm là bước sóng dài hơn 43nm so với 590 nm, mật độ quang học giảm 3 OD, từ 8 OD xuống 5 OD. Mặc dù chỉ giảm 3 OD nhưng trục y lại giảm đi 1000 lần vì nó được biểu thị bằng đơn vị logarit. Ngoài ra, 830 nm chênh lệch 5 OD so với 590 nm và có thể xuyên thấu sâu nhất. Đèn LED được sử dụng để trẻ hóa da chủ yếu sử dụng bước sóng 630 và 830 nm, thuộc dải điều biến sinh quang của Karu (( Calderhead RG, Vasily DB (2016) Low level light therapy with light-emitting diodes for the aging face. Clin Plast Surg 43(3):541–550)). Đèn LED không chỉ được sử dụng cho mục đích trẻ hóa da mà còn để điều trị mụn trứng cá (400 nm) và trẻ hóa lớp thượng bì và lớp bì nhú (590 nm) (( Opel DR, Hagstrom E, Pace AK, Sisto K, Hirano- Ali SA, Desai S et al (2015) Light-emitting diodes: a brief review and clinical experience. J Clin Aesthet Dermatol 8(6):36–44)).
8.4 Cơ chế liệu pháp ánh sáng cường độ thấp bằng đèn LED
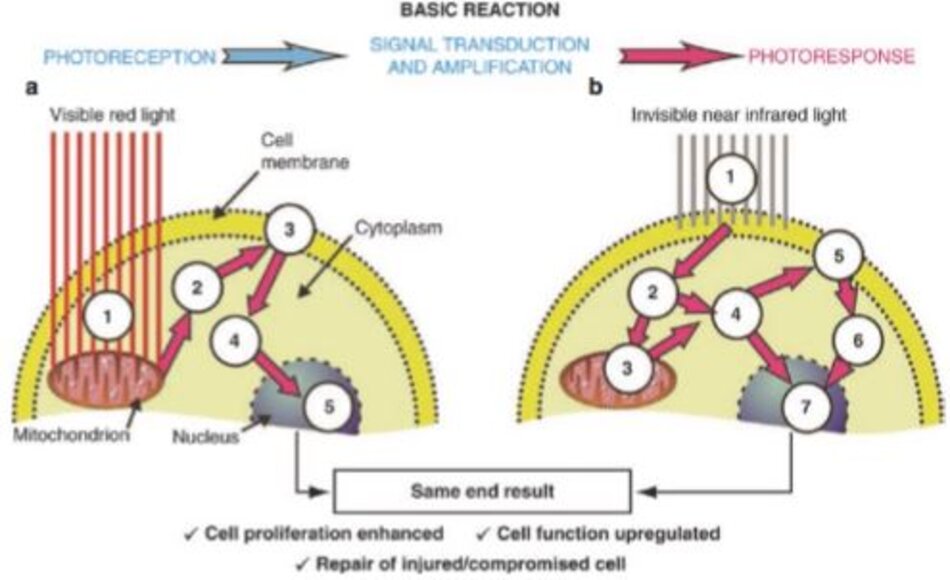
Cơ chế điều biến quang có thể được chia thành (1) ánh sáng nhìn thấy bao gồm 630 nm, dưới dải điều biến sinh quang của Karu, và (2) cận hồng ngoại bao gồm 830 nm (Hình 9.16). Ánh sáng nhìn thấy nhắm vào cytochrome C oxidase (CCO) của ty thể, và ánh sáng cận hồng ngoại nhắm vào màng tế bào. Cytochrome C oxidase hay phức hợp IV (CCO) là một loại enzyme tận cùng của ty thể và tham gia vào quá trình tổng hợp adenosine triphosphate (ATP). ATP được sử dụng làm nhiên liệu cho tế bào và toàn bộ sinh vật (( Calderhead RG (2007) The photobiological basics behind light-emitting diode (LED) phototherapy. Laser Ther 16(2):97–108)).
Đầu tiên, ánh sáng nhìn thấy được CCO hấp thụ để tạo ra ATP bằng cơ chế vận chuyển tầng quang hóa và thúc đẩy cơ chế vận chuyển thành tế bào như bơm natri-kali (Na1 / K1-ATPase). Sau đó, sự trao đổi nội bào/ngoại bào giữa các tế bào và chất nền ngoại bào làm tăng các ion canxi (Ca ++) và ion hydro (H +), cả hai đều là hợp chất truyền tín hiệu mạnh của tế bào. Cuối cùng, DNA và RNA của nhân được tạo ra dẫn đến sự tăng sinh của tế bào.
Thứ hai, các tia cận hồng ngoại được thành tế bào hấp thụ và thay đổi trạng thái điện tử của các phân tử thành tế bào thông qua các phản ứng quang-vật lý như trao đổi quay và dao động. Sau đó, nó thúc đẩy cơ chế vận chuyển tế bào, cho phép các ion canxi (Ca ++) tăng ion hydro (H +) và tạo ra nhiều ATP hơn trong ty thể. Ánh sáng cận hồng ngoại, không giống như ánh sáng nhìn thấy, gây ra phản ứng quang-vật lý gián tiếp chứ không phải là một tầng quang hóa. Cuối cùng, nó tạo ra sự điều biến sinh quang như tăng sinh tế bào.
8.5 Trẻ hoá da không xâm lấn bằng điều biến quang
Điều biến quang cũng đóng một vai trò trong việc trẻ hóa làn da. Tuy nhiên, hiệu quả không thấy ngay tức thì và cải thiện dần trong 12 tuần (( . Calderhead RG, Vasily DB (2016) Low level light therapy with light-emitting diodes for the aging face. Clin Plast Surg 43(3):541–550)).
Lee và cộng sự đã nghiên cứu sự hài lòng chủ quan của bệnh nhân bằng cách chia nhóm thành ba nhóm: 633, 830 và kết hợp giữa 633 & 830 nm. Kết quả cho thấy cả ba nhóm đều không “hài lòng lắm” trong 4 tuần đầu tiên. Nhưng 12 tuần sau, phản hồi “rất hài lòng” tăng lên. Đặc biệt, tổng số “rất hài lòng” và tăng cao nhất ở nhóm 830 nm. Lý do của sự gia tăng dần dần phản hồi hài long là vì sự điều biến quang bằng đèn LED cũng làm trẻ hóa da thông qua tái tạo collagen. Kết quả mô học cho thấy sự gia tăng collagen và elastin. Kết quả máy cắt mẫu cho thấy nhóm 830 nm có độ đàn hồi da cao hơn các nhóm còn lại. Ngoài ra, điều biến quang bằng đèn LED 830 nm không chỉ hiệu quả khi được sử dụng một mình mà còn khi được sử dụng như một phương thức bổ trợ.
Trelles và cộng sự đã nghiên cứu 60 bệnh nhân tiến hành tái tạo bề mặt bóc tách toàn bộ khuôn mặt, 30 người trong số họ được điều trị bằng LED-LLLT như một liệu pháp bổ trợ, và 30 người còn lại thì không [4]. Kết quả cho thấy rằng theo thống kê, đèn LED – LLLT ít đau hơn, ban đỏ, bầm tím và phù nề, đồng thời hồi phục vết thương nhanh hơn và ít biến chứng hơn so với nhóm không sử dụng đèn LED.
Liệu pháp bổ trợ bằng đèn LED hồi phục vết thương nhanh hơn 50%, giảm tác dụng phụ và thời gian nghỉ dưỡng. Quy trình điều trị bổ trợ bằng đèn LED như sau. Thực hiện đèn LED càng sớm càng tốt ngay sau khi làm thủ thuật. Năng lượng khoảng 60 J/cm2. Đối với chấn thương nặng hoặc các thủ thuật phẫu thuật rộng rãi, ít nhất sáu thủ thuật được đề nghị trong 3 tuần (hai lần một tuần). Khoảng thời gian tiến hành ít nhất phải là 2 ngày.
Đèn LED-LLLT 830 nm có thể được sử dụng như một liệu pháp bổ trợ sau bất kỳ thủ thuật nào, từ mài da nhẹ cho đến phẫu thuật cắt nếp nhăn da. Nó cũng mang lại hiệu quả cho bệnh nhân với đáp ứng nghỉ ngơi và thư giãn thần kinh phó giao cảm.
8.6 Sự đồng thuận đối với đèn LED
Không kể đến những nghiên cứu này, về mặt lâm sàng, chúng tôi hiếm khi tìm thấy những hiệu quả đáng chú ý của đèn LED. Đèn LED có thực sự hiệu quả?
Trước đây, nhiều người nghi ngờ điều biến quang (LLLT) bao gồm cả đèn LED. Có nhiều nghi ngờ về hiệu quả lâm sàng của nó vì hầu hết các nghiên cứu về điều biến quang sử dụng mô hình nuôi cấy tế bào, và chỉ một số ít là nghiên cứu lâm sàng (( Goldman MP (2006) Cutaneous and cosmetic laser surgery. Mosby Elsevier, Philadelphia, PA)). Nhưng gần đây, có nhiều nghiên cứu lâm sàng liên quan đến điều biến quang của đèn LED. Tuy nhiên, không có sự đồng thuận bởi nghiên cứu khách quan.
Jagdeo và cộng sự đã phân tích tác động của đèn LED trong 31 thử nghiệm ngẫu nhiên có đối chứng (RCT): mụn trứng cá (8 thử nghiệm), herpes simplex và zoster (HSV, HZV) (3 thử nghiệm), trẻ hóa da (6 thử nghiệm), lành vết thương cấp tính (5 thử nghiệm), vảy nến (3 thử nghiệm), viêm da cơ địa (1thử nghiệm), lành vết thương mãn tính (2 thử nghiệm), viêm niêm mạc miệng (1 thử nghiệm), viêm da bức xạ (1 thử nghiệm) và chữa viêm mô bào ở đùi (1 thử nghiệm). Việc đưa ra chỉ định dựa trên mức độ y học chứng cứ của Trung tâm Oxford. Các điểm được đề xuất là A, B, C và D, trong đó A là điểm cao nhất (( Jagdeo J, Austin E, Mamalis A, Wong C, Ho D, Siegel DM (2018) Light-emitting diodes in dermatology: a systematic review of randomized controlled trials. Lasers Surg Med 50:613)). Kết quả cho thấy mụn trứng cá, herpes simplex và zoster, và vết thương cấp tính lành là loại B, còn lại là C hoặc D.
Bài báo này chỉ phân tích RCTs, đây là một phương pháp nghiên cứu khách quan, nhưng số lượng bài báo quá ít để đưa ra kết luận rõ ràng về tác dụng của tất cả các đèn LED. Tuy nhiên, có thể nói đèn LED tương đối hiệu quả đối với mụn trứng cá, herpes simplex và zoster, và chữa lành vết thương cấp tính so với các bệnh khác. Nhưng mối quan tâm chính của chúng tôi – trẻ hóa da và chữa viêm mô bào ở đùi – tương ứng là cấp C và D, tức là, chúng tôi chưa thể nói rằng đèn LED có hiệu quả cho những chỉ định này.
Jagdeo và cộng sự đề xuất một quy trình cho từng loại bệnh dựa trên kết quả phân tích. (1) Đối với mụn trứng cá, nên sử dụng đèn LED ánh sáng xanh và đỏ trong 20 phút với năng lượng tương ứng là 6–40 và 8–100 mW/cm2. Khoảng cách điều trị nên là 4-8 tuần hai lần một tuần. (2) Đối với herpes sim- plex và herpes zoster, nên sử dụng đèn LED cận hồng ngoại. Thời gian hồi phục có
thể giảm ít nhất 2 ngày khi sử dụng đèn LED. Ngoài thuốc kháng vi rút đường uống, nên dùng đèn LED tại nhà 3 ngày. Thông số phải là 33 J/cm2 trong 10 phút ở 55 mW/cm2 ở bước sóng 830 nm (3). Đối với vết thương cấp tính, điều trị bằng ánh sáng vàng (590 nm) hoặc đèn LED cận hồng ngoại mỗi ngày cho đến khi vết thương lành có thể rút ngắn thời gian bệnh và đỏ da của vết thương cấp tính, bất kể nguyên nhân là gì. Đèn LED ánh sáng vàng được khuyến cáo là 50 mW/cm2 trong 1–2 phút và đèn LED cận hồng ngoại 5–40 J/cm2 trong 20 phút ở 50 mW/cm2 (( Jagdeo J, Austin E, Mamalis A, Wong C, Ho D, Siegel DM (2018) Light-emitting diodes in dermatology: a systematic review of randomized controlled trials. Lasers Surg Med 50:613)).
Để trẻ hóa da, sử dụng đèn LED cận hồng ngoại và đèn LED ánh sáng đỏ hàng ngày trong 8–10 tuần là hiệu quả nhất trong việc cải thiện nếp nhăn. Các thông số khác nhau giữa các tài liệu, gây khó khăn cho việc thực hiện một quy trình. Một số tài liệu nói rằng đèn LED ánh sáng vàng có hiệu quả trong việc trẻ hóa da, nhưng không tìm thấy RCTs.
Jagdeo và cộng sự đã khuyến cáo sử dụng đèn LED, mặc dù thực tế là chỉ có ba bệnh có mức Khuyến cáo B, vì đèn LED có ít tác dụng phụ hơn, giá cả phải chăng và ngày càng có nhiều kết quả lâm sàng đáng khích lệ hơn liên tục được công bố.
8.7 Nhận xét cá nhân về điều biến quang
Nhiều nghiên cứu gần đây về điều biến quang đã cho thấy nhiều sự thật liên quan đến hiệu quả của điều biến quang và cơ chế của nó. Tuy nhiên, cơ chế chính xác vẫn chưa được biết và có nhiều tranh luận về các thông số như năng lượng, hiệu quả và khoảng thời gian điều trị. Vấn đề chính là tính hiệu quả của nó. Theo kinh nghiệm cá nhân của tôi, tôi không thấy bất kỳ hiệu quả nào của điều biến quang thông qua đơn trị liệu với đèn LED, và do đó sử dụng nó như một liệu pháp bổ trợ. Như với các bài báo đã trình bày trước đó (( Jagdeo J, Austin E, Mamalis A, Wong C, Ho D, Siegel DM (2018) Light-emitting diodes in dermatology: a systematic review of randomized controlled trials. Lasers Surg Med 50:613)), tôi tin rằng đèn LED có hiệu quả đối với mụn trứng cá, herpes simplex và herpes zoster, và chữa lành vết thương cấp tính. Vì vậy, tôi sử dụng đèn LED để chữa lành vết thương cấp tính sau thủ thuật bóc tách chẳng hạn như laser CO2 vi điểm hoặc đỏ da nặng sau khi điều trị bằng laser và điều trị PDT cho mụn trứng cá.
9. Tài liệu tham khảo
Xem thêm: