Bệnh Nhi khoa, Bệnh tim mạch
Chăm sóc trẻ sau ngừng tim: Tuyên bố khoa học từ Hiệp hội Tim mạch Hoa Kỳ
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
Chăm sóc trẻ sau ngừng tim: Tuyên bố khoa học từ Hiệp hội Tim mạch Hoa Kỳ . Tải file PDF ở đây.
Dịch: BS. Đặng Thanh Tuấn – Khoa Hồi sức Ngoại – BV Nhi Đồng 1
Các định nghĩa
Sự trở lại của tuần hoàn tự phát/duy trì và tuần hoàn ngoài cơ thể
Trước đây, các hướng dẫn của AHA và các hướng dẫn cập nhật về hồi sức tim phổi (cardio- pulmonary resuscitation – CPR) và các tài liệu đào tạo về chăm sóc tim mạch khẩn cấp đã sử dụng chữ viết tắt ROSC (return of spontaneous circulation) để chỉ tuần hoàn tự nhiên trở lại, được định nghĩa là nhịp tim tưới máu trở lại kèm theo sự hiện diện của mạch trung tâm có thể sờ thấy được. Trong ấn phẩm này, chữ viết tắt ROSC đề cập đến sự trở lại của tuần hoàn bền vững, có thể bao gồm tuần hoàn do nhịp tim tự phát được tưới máu hoặc do thiết lập tuần hoàn ngoài cơ thể với quá trình oxygen hóa qua màng ngoài cơ thể (extracorporeal membrane oxygenation – ECMO). ECMO được thiết lập trong quá trình CPR tích cực được viết tắt là ECPR.
Xử trí nhiệt độ mục tiêu
Trong thập kỷ qua, đã có sự thay đổi trong danh pháp được sử dụng để mô tả việc xử trí thân nhiệt sau ngừng tim. Trong các nghiên cứu ban đầu, hạ thân nhiệt điều trị (32°C–34°C) được so sánh với liệu pháp điều trị nhiệt độ tiêu chuẩn (không kiểm soát) không bao gồm phòng ngừa sốt.1 Các nghiên cứu tiếp theo gần đây đã so sánh hạ thân nhiệt điều trị với điều trị nhiệt độ bình thường có kiểm soát (36°C– 37,5°C), với tình trạng sốt được ngăn ngừa tích cực.2,3 Hiện tại, xử trí nhiệt độ theo mục tiêu (targeted temperature management – TTM) là thuật ngữ được sử dụng để chỉ việc kiểm soát nhiệt độ mục tiêu được chỉ định đối với việc hạ thân nhiệt (32°C°–34°C) hoặc giữ nhiệt độ bình thường (36°C– 37,5°C). Trong tài liệu này, chúng tôi sử dụng thuật ngữ có trong các nghiên cứu được trích dẫn hoặc TTM cho cả tình trạng hạ thân nhiệt hoặc thân nhiệt bình thường, với (các) nhiệt độ mục tiêu được liệt kê.
Các giai đoạn và khoảng thời gian
PCAC khác nhau dựa trên cơ sở cả giai đoạn của hội chứng sau ngừng tim (post–cardiac arrest syndrome – PCAS) và bối cảnh chăm sóc được thực hiện sau ROSC. Các giai đoạn liên tiếp của PCAS và các khoảng thời gian chăm sóc được minh họa trong Hình 1.4 Khoảng thời gian sau 20 phút đầu tiên sau ROSC có thể khác nhau tùy theo từng bệnh nhân, tùy thuộc vào mức độ nghiêm trọng của PCAS, quỹ đạo hồi phục hoặc tốc độ xấu đi. Trong tất cả các giai đoạn, mục đích chăm sóc tập trung vào việc hạn chế tổn thương đang diễn ra và ngăn ngừa ngừng tim tái phát.
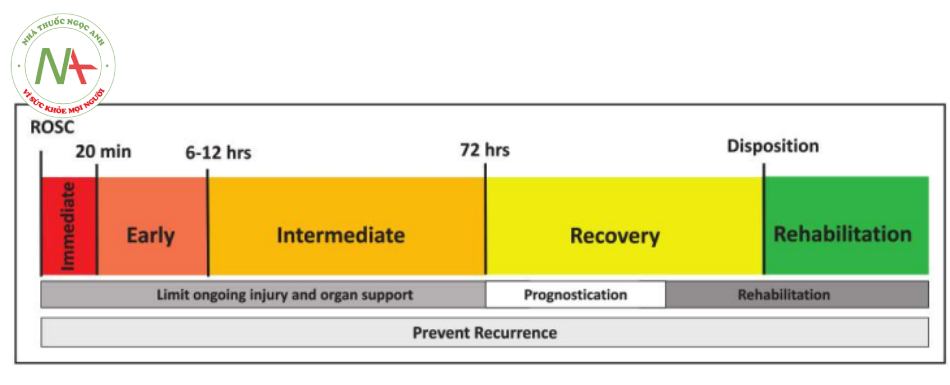
- Giai đoạn ngay lập tức (immediate): 0 đến 20 phút đầu tiên sau ROSC
- Giai đoạn sớm (early): khoảng thời gian sau ROSC từ 20 phút đến 6 đến 12 giờ
- Giai đoạn trung gian (intermediate): 12 đến 72 giờ
- Giai đoạn phục hồi (recovery): khoảng 72 giờ đến ngày thứ 7. Bắt đầu vào những thời điểm khác nhau đối với những bệnh nhân khác nhau; thời gian có thể bị ảnh hưởng bởi các yếu tố như chức năng tim mạch hoặc việc sử dụng TTM
- Giai đoạn phục hồi chức năng (rehabilitation): theo truyền thống bắt đầu bằng việc áp dụng dịch vụ chăm sóc sau khi xuất viện từ bệnh viện chăm sóc cấp tính, nhưng các dịch vụ phục hồi chức năng hiện nay thường được bắt đầu trong giai đoạn trung gian hoặc giai đoạn phục hồi
Bối cảnh
Tuyên bố khoa học này mô tả các bằng chứng được công bố đã được bình duyệt sẵn có về việc chăm sóc trẻ em được hồi sức sau ngừng tim, bao gồm PCAC ở trẻ em và tiên lượng, đồng thời cung cấp một danh sách các lỗ hổng kiến thức. Mục đích của tuyên bố này là cung cấp cho các bác sĩ lâm sàng các khuyến nghị để tối ưu hóa PCAC cho trẻ em, nêu bật những lỗ hổng kiến thức cần được các nhà nghiên cứu giải quyết để cải thiện kết quả và chăm sóc trong tương lai.
Năm 2008, PCAS được định nghĩa cho cộng đồng hồi sức quốc tế trong một tuyên bố khoa học của Ủy ban Liên lạc Quốc tế về Hồi sức.4 Tuyên bố này đề cập đến PCAC chủ yếu ở người lớn, nhấn mạnh sinh lý bệnh và nhu cầu tiếp tục hỗ trợ đa hệ thống sau ROSC.4 Tuyên bố mô tả những gì hiện được chấp nhận như 4 thành phần chính của PCAS: tổn thương não sau ngừng tim, rối loạn chức năng cơ tim sau ngừng tim, đáp ứng thiếu máu cục bộ/tái tưới máu hệ thống và sinh lý bệnh nền có sẳn.
Trước năm 2008, hướng dẫn hỗ trợ sự sống nâng cao cho trẻ em (pediatric advanced life support – PALS) của AHA tập trung chủ yếu vào việc ngăn ngừa ngừng tim, nhận biết ngay trường hợp ngừng tim và cung cấp CPR sớm vì kết quả của ngừng tim ở trẻ em rất kém.5,6 Trong Ủy ban Liên lạc Quốc tế năm 2008 trên tuyên bố khoa học về Hồi sức, PCAC ở trẻ em chỉ được giải quyết như một trường hợp đặc biệt.4 Phần này trích dẫn bằng chứng nhi khoa rất hạn chế hiện có, bao gồm các nghiên cứu đã công bố ở trẻ sơ sinh bị ngạt chứng minh tác dụng tích cực của hạ thân nhiệt điều trị so với không kiểm soát nhiệt độ,7,8 cũng như như một loạt trường hợp nhi khoa ghi nhận mối liên quan giữa sốt sau ngưng tim và kết cục xấu.9 Phần nhi khoa của Ủy ban Liên lạc Quốc tế về Hồi sức khoa học cho rằng chăm sóc tập trung sau ROSC có thể cải thiện khả năng sống sót đến khi xuất viện và nó nêu bật những lỗ hổng lớn trong bằng chứng cụ thể về PCAC của trẻ em.
Thập kỷ vừa qua đã dẫn đến những nỗ lực tập trung của các chuyên gia hồi sức nhằm giải quyết những lỗ hổng kiến thức cụ thể ở trẻ em sau ngừng tim. Ủy ban Liên lạc Quốc tế về Hồi sức Đồng thuận Quốc tế về CPR và Khoa học Chăm sóc Tim mạch Khẩn cấp với các Tuyên bố Khuyến nghị Điều trị đã xác định bằng chứng một cách có hệ thống và chặt chẽ, và các tuyên bố hướng dẫn của AHA dựa trên bằng chứng. Mặc dù vẫn cần nhiều nghiên cứu, nhưng tài liệu này cung cấp một cái nhìn tổng quan dựa trên đánh giá tài liệu và ý kiến đồng thuận của chuyên gia để hướng dẫn bác sĩ lâm sàng hiểu và xử trí trẻ sau ngừng tim. Dữ liệu được ngoại suy từ các nghiên cứu ở người lớn hỗ trợ cách tiếp cận tổng hợp chu đáo, dựa trên hệ thống và chủ động đối với PCAC, với mục tiêu tiếp tục là cải thiện khả năng sống sót lâu dài với kết quả thần kinh thuận lợi.
Dịch tễ học PCAS ở trẻ em
Thời gian và mức độ nghiêm trọng của các giai đoạn PCAS có thể khác nhau giữa những bệnh nhân bị ngừng tim ngoài bệnh viện (out-of- hospital cardiac arrest – OHCA) và những người bị ngừng tim trong bệnh viện (in-hospital cardiac arrest – IHCA) do tình trạng được chứng kiến, các tình trạng có sẵn, nguyên nhân ngừng tim, thời gian và chất lượng hành động của người ngoài cuộc (bystander), chẳng hạn như thực hiện ngay lập tức CPR chất lượng cao, có thể khác nhau giữa OHCA và IHCA. Do đó, chúng tôi mô tả dịch tễ học của OHCA và IHCA một cách riêng biệt.
Tài liệu của OHCA mô tả các kết quả dựa trên mẫu số của tất cả các biến cố ngừng tim xảy ra trong bối cảnh trước khi nhập viện, chẳng hạn như dữ liệu từ ROC (Resuscitation Outcomes Consortium),11–13 cơ quan đăng ký khu vực như CARES (Đăng ký ngừng tim để tăng cường khả năng sống sót)14,15 hoặc Cơ quan đăng ký Utstein toàn Nhật Bản,16 hoặc 2 nghiên cứu thuần tập về trẻ em bị ngừng tim sống sót sau khi nhập viện.17,18 Điều quan trọng cần lưu ý là mẫu số bệnh nhân khi so sánh tỷ lệ sống sót được báo cáo. Những khác biệt này cũng có liên quan vì thời điểm bắt đầu PCAC có thể khác nhau tùy theo nơi đạt được ROSC.
Người ta ước tính rằng >5000 trẻ em bị OHCA hàng năm ở Hoa Kỳ,11,19 với tỷ lệ mắc OHCA không do chấn thương ước tính là 8,04 trên 100 000 người-năm.11 Với tỷ lệ ROSC hiện tại là ≈36%,13 chúng tôi ước tính rằng >1800 trẻ sơ sinh và trẻ em có nguy cơ mắc PCAS hàng năm sau OHCA. Tỷ lệ sống sót đến khi xuất viện được báo cáo sau OHCA từ cơ quan đăng ký đa bang CARES của Hoa Kỳ và Cơ quan đăng ký ROC Bắc Mỹ đã không tăng đáng kể trong 10 năm qua, với tỷ lệ sống sót chung trong Cơ quan đăng ký ROC là 6,4% được báo cáo từ năm 2005 đến 200711 và 6,7% đến 10,2% được báo cáo trong năm 2007 đến 201213 và tỷ lệ sống sót trung bình là 8,2% trong sổ đăng ký CARES từ năm 2005 đến 2013.14 Kết quả thần kinh thuận lợi đã được báo cáo ở 77% trẻ em sống sót sau OHCA.14 Trong một nghiên cứu gần đây về TTM ở trẻ hôn mê sống sót sau OHCA đến được đưa vào đơn vị chăm sóc đặc biệt dành cho trẻ em (ICU), 38% sống sót khi xuất viện.
Việc xác định kết quả sau IHCA khó khăn hơn vì các báo cáo đã xuất bản thường sử dụng các mẫu số chỉ bao gồm những bệnh nhân được CPR. Theo thông tin từ cơ quan đăng ký IHCA Nhận hướng dẫn-Hồi sức của AHA20 và Cơ sở dữ liệu bệnh nhân nội trú dành cho trẻ em,21 ước tính có khoảng 6000 trẻ sơ sinh và trẻ em mắc IHCA hàng năm. Tỷ lệ ROSC được điều chỉnh theo nguy cơ đã tăng từ 42,9% năm 2000 lên 81,2% năm 2009 và tỷ lệ sống sót sau khi xuất viện được điều chỉnh theo nguy cơ đã cải thiện từ 14,3% năm 2000 lên 43,4% năm 2009 mà không làm gia tăng kết quả thần kinh bất lợi.22 Đáng chú ý, với nhấn mạnh vào việc phát hiện và điều trị các tình trạng trước khi ngừng điều trị kể từ năm 2003 đến năm 2004, IHCA diễn ra một cách thích hợp hơn đáng kể ở các ICU so với các khu điều trị thông thường.20 Trong một loạt bài gần đây hơn từ Get With The Guidelines–Hồi sức bệnh nhân đăng ký từ năm 2011 đến 2013, ROSC ICU không có nguy cơ được điều chỉnh (non–risk-adjusted) xảy ra ở 78%, với 45% sống sót để xuất viện; 89% những người sống sót có kết quả thần kinh thuận lợi.23 Trên cơ sở những dữ liệu này, chúng tôi ước tính rằng ≈4800 trẻ sơ sinh và trẻ em có nguy cơ phát triển PCAS hàng năm sau IHCA.
Mặc dù ROSC và tỷ lệ sống sót sau ngừng tim ở trẻ em đã được cải thiện, nhưng >6500 trẻ em mỗi năm ở Hoa Kỳ mắc PCAS.11,13,19–21 Mục tiêu của PCAC là tăng không chỉ tỷ lệ sống sót khi xuất viện mà còn tăng tỷ lệ sống sót với tình trạng kết cục thần kinh thuận lợi.
Sinh lý bệnh và biểu hiện lâm sàng của PCAS
Thuật ngữ bệnh sau hồi sức (postresuscitation disease) lần đầu tiên được đề xuất bởi Negovsky và Gurvitch24 vào năm 1995 để chỉ hệ thống thần kinh trung ương và các quá trình bệnh lý toàn thân do thiếu oxy-thiếu máu cục bộ và xảy ra trong quá trình hồi phục. Bệnh này bao gồm phản ứng viêm tế bào và sinh lý bệnh đã được mô tả rõ ràng bởi Neumar et al4 vào năm 2008.
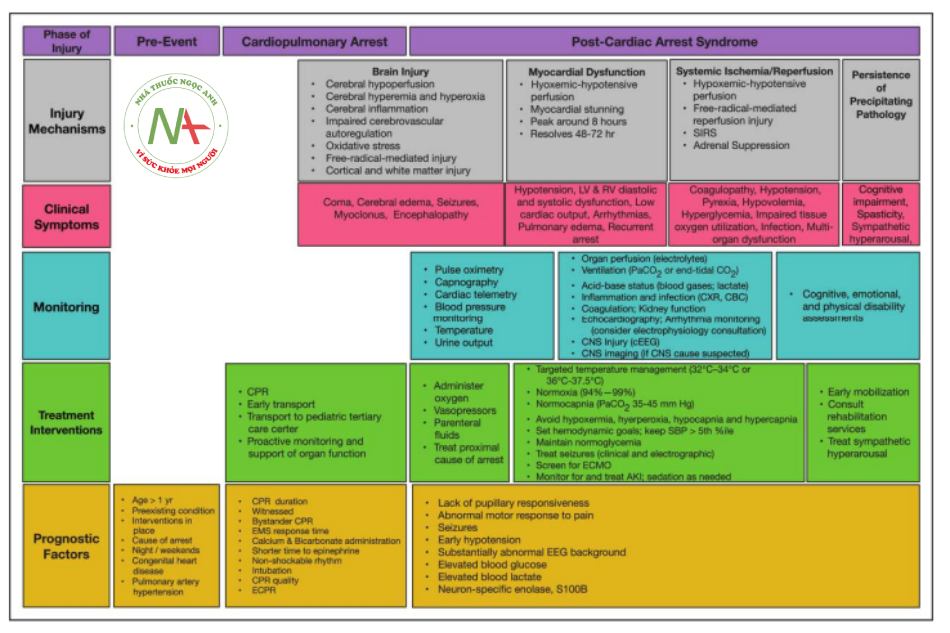
AKI, chấn thương thận cấp tính; CBC, công thức máu toàn bộ; CNS, hệ thống thần kinh trung ương; CPR, hồi sức tim phổi; CXR, chụp X-quang ngực; cEEG, điện não đồ liên tục; ECMO, oxygen hóa qua màng ngoài cơ thể; ECPR, hồi sức tim phổi ngoài cơ thể; EEG, điện não đồ; EMS, dịch vụ y tế khẩn cấp; LV, tâm thất trái; RV, tâm thất phải; SBP, huyết áp tâm thu; và SIRS, hội chứng phản ứng viêm toàn thân.
Các giai đoạn của PCAS được mô tả trong Hình 1. Các thành phần chính của hội chứng này là chấn thương não sau ngừng tim, rối loạn chức năng cơ tim sau ngừng tim, đáp ứng thiếu máu cục bộ/tái tưới máu hệ thống và sinh lý bệnh nền có sẳn; Xử trí PCAS yêu cầu hỗ trợ đa hệ thống trong từng giai đoạn (Hình 2). Các phần sau đây trình bày tổng quan về sinh lý bệnh của từng giai đoạn dựa trên dữ liệu từ các mô hình lâm sàng và tiền lâm sàng và các biểu hiện lâm sàng dự đoán ở trẻ em.
Tổn thương não sau ngừng tim
Tổn thương não sau ngừng tim vẫn là nguyên nhân hàng đầu gây bệnh tật và tử vong ở người lớn và trẻ em vì não có khả năng chịu đựng hạn chế đối với thiếu máu cục bộ, xung huyết hoặc phù nề. 3 giai đoạn đầu tiên của PCAS liên quan đến giảm tưới máu-hạ huyết áp với thiếu hụt năng lượng. Với ROSC, có sự bùng nổ của các gốc oxy hóa tự do (reactive oxygen species) và stress oxy hóa (oxidative stress) có thể xảy ra trong mô bị cạn kiệt chất chống oxy hóa (antioxidants).25 Kết quả là, tái tưới máu có liên quan đến độc tính kích thích, tích tụ canxi và tổn thương hoặc chết tế bào qua trung gian gốc tự do.26 Cả hoại tử tế bào (cellular necrosis) thần kinh và quá trình chết theo chương trình (apoptosis) đều do tổn thương xếp tầng này và có thể tiếp tục trong vài ngày đến vài tuần sau ROSC. Một loạt các tình trạng lâm sàng sau ngừng tim, bao gồm tăng oxy máu, thiếu oxy máu và hạ huyết áp, có thể làm trầm trọng thêm tổn thương tế bào thần kinh.
Các nghiên cứu tiền lâm sàng về tổn thương do thiếu oxy-thiếu máu cục bộ (hypoxic- ischemic injury) gợi ý rằng nồng độ oxy trong động mạch hệ thống quá mức bình thường trong quá trình tái tưới máu sau khi ngừng tim có thể làm trầm trọng thêm tổn thương thần kinh và gián đoạn protein qua trung gian gốc tự do và có thể làm trầm trọng thêm kết cục thần kinh, mặc dù sự liên quan của các mô hình động vật này với con người là không chắc chắn.27 Trong các nghiên cứu tiền lâm sàng, tái tưới máu do tăng oxy dẫn đến sự gia tăng quá trình chết tế bào thần kinh bị trì hoãn28–30 và làm giảm hoạt động của pyruvate dehydrogenase hồi hải mã.31 Do đó, tình trạng tăng oxy sau ROSC có thể làm trầm trọng thêm tổn thương tế bào thần kinh.
Dữ liệu lâm sàng về nhi khoa là không rõ ràng, với 3 nghiên cứu quan sát nhỏ về IHCA và OHCA ở trẻ em cho thấy không có mối liên hệ nào giữa tình trạng tăng oxy máu và kết cục,33–35 trong khi một nghiên cứu lớn đa trung tâm cho thấy sự hiện diện của oxy máu bình thường sau ROSC (được định nghĩa là PaO2 >60 và <300 mm Hg) so với tình trạng tăng oxy máu (PaO2 >300 mm Hg) có liên quan đến tỷ lệ sống sót đến khi xuất viện cao hơn.
Áp lực carbon dioxide động mạchảnh hưởng đến tưới máu não ở cả trẻ em và người lớn. Các nghiên cứu tiền lâm sàng cho thấy tăng thông khí làm giảm tưới máu mạch vành và khả năng sống sót sau khi ngừng tim.38 Tăng thông khí gây co mạch não và có thể làm giảm lưu lượng máu não (cerebral blood flow – CBF),39 do đó có khả năng làm trầm trọng thêm tình trạng thiếu máu não. Tăng CO2 máu gây giãn mạch não và tăng CBF.39 Phản ứng của mạch máu não với carbon dioxide có thể được bảo tồn ở một số bệnh nhân sau khi ngừng tim.
Các nghiên cứu lâm sàng về thông khí sau ngừng tim ở trẻ em còn hạn chế. Một nghiên cứu nhỏ về tình trạng giảm thông khí sau ngừng tim ở trẻ em đã chứng minh không có mối liên hệ nào với kết cục,33 trong khi một nghiên cứu khác cho thấy tăng CO2 máu (PaCO2 >50 mm Hg) và giảm CO2 máu (PaCO2 <30 mm Hg) có liên quan độc lập với tử vong.35 Dữ liệu dành cho người lớn chứng minh rằng có không có bằng chứng chất lượng cao nào chứng minh mối liên quan của tăng hoặc giảm CO2 máu với khả năng sống sót và kết cục thần kinh tồi tệ hơn.
Các biểu hiện lâm sàng của tổn thương não sau khi bị ngưng tim bao gồm hôn mê, phù não, co giật, rung giật cơ, hưng phấn giao cảm, và suy giảm chức năng và hành vi thần kinh trong thời gian dài.
Rối loạn chức năng cơ tim sau ngừng tim
Rối loạn chức năng cơ tim sau ngừng tim trong bối cảnh lâm sàng, bao gồm các báo cáo về choáng cơ tim, lần đầu tiên được mô tả trong y văn vào những năm 1990. Rối loạn chức năng cơ tim toàn bộ xảy ra ngay cả khi không có nguyên nhân ngừng tim và mức độ nghiêm trọng của rối loạn chức năng cơ tim có thể liên quan đến khoảng thời gian không có lưu lượng (no-flow time) trong khi ngừng tim.42 Rối loạn chức năng cơ tim có liên quan đến tử vong sớm mặc dù điều trị ban đầu thành công hồi sức ở trẻ em42,43 và người lớn.
Sự khởi đầu của rối loạn chức năng cơ tim sau ngừng tim bắt đầu trong vòng vài giờ sau khi ngừng tim, đạt đỉnh sau ≈ 8 giờ, bắt đầu cải thiện sau 24 giờ và thường hết trong vòng 48 đến 72 giờ.44 Sinh lý bệnh góp phần vào sự suy giảm chức năng tim thường xuyên có thể đảo ngược này sau khi ngừng tim vẫn chưa được hiểu đầy đủ nhưng có liên quan đến tổn thương do thiếu máu cục bộ/tái tưới máu tim mạch, rối loạn chức năng tim mạch qua trung gian cytokine và gây ra tổn thương cơ tim thứ phát do catecholamine hoặc sốc điện.44,48–51 Trẻ em ban đầu có thể biểu hiện trạng thái tăng động và sau đó phát triển rối loạn chức năng tim theo thời gian.52 Bởi vì rối loạn chức năng cơ tim có khả năng phát triển ở khoảng hai phần ba số bệnh nhân sau ROSC51 và sau đó được cải thiện, nó được cho là một yếu tố nguy cơ có thể thay đổi được.
Các nghiên cứu sau ngừng tim ở trẻ em đánh giá rối loạn chức năng cơ tim còn hạn chế. Trong các nghiên cứu hồi cứu nhỏ về OHCA ở trẻ em, tăng troponin I và giảm phân suất rút ngắn của tâm thất và phân suất tống máu có liên quan đến tỷ lệ tử vong tăng lên.43 Trong một nghiên cứu hồi cứu trên 58 trẻ em trong vòng 24 giờ sau khi nhập viện sau ROSC từ OHCA, siêu âm tim qua thành ngực cho thấy giảm chức năng tâm thu thất trái ở 41%, có liên quan đến tỷ lệ tử vong gia tăng.42 Rối loạn chức năng tâm trương thất trái xuất hiện ở 64% bệnh nhân. Huyết áp tâm thu hoặc tâm trương thấp và áp lực tĩnh mạch trung tâm thấp tại thời điểm siêu âm tim qua thành ngực không liên quan đến rối loạn chức năng tâm thu thất trái, do đó đặt ra câu hỏi liệu đánh giá định tính chức năng tâm thu thất trái bằng siêu âm tim có phải là thước đo chính xác cho rối loạn chức năng cơ tim hay không và liệu các dấu hiệu sinh tồn có là phương pháp đáng tin cậy để sàng lọc rối loạn chức năng cơ tim sau ngừng tim.
Mặc dù các nghiên cứu ban đầu về rối loạn chức năng cơ tim sau ngừng tim tập trung vào chức năng tâm thu thất trái, rối loạn chức năng tâm trương thất trái và rối loạn chức năng thất phải (right ventricular – RV) sau ngừng tim ở người lớn cũng đã được ghi nhận.46,47,53 Rối loạn nhịp tim thường gặp trong PCAC và có thể trầm trọng hơn khi sử dụng catecholamine, cần thiết để duy trì cung lượng tim đầy đủ.
Các biểu hiện lâm sàng của rối loạn chức năng cơ tim bao gồm hạ huyết áp, rối loạn chức năng tâm thu hoặc tâm trương thất trái và RV dẫn đến giảm cung lượng tim, rối loạn nhịp tim và phù phổi, có thể dẫn đến ngừng tim tái phát.
Thiếu máu cục bộ/tái tưới máu hệ thống
Sự kết hợp giữa thiếu máu cục bộ/tái tưới máu hệ thống (systemic ischemia/reperfusion) tạo ra một trạng thái tương tự như hội chứng nhiễm trùng huyết (sepsis syndrome), với các cytokine tăng cao, sự hiện diện của nội độc tố trong huyết tương, kích hoạt các con đường đông máu và ức chế các con đường chống đông máu.
Tăng đường huyết do bệnh nặng (critical illness hyperglycemia) thoáng qua xảy ra sau khi ngừng tim do tình trạng kháng insulin tương đối có liên quan đến nồng độ catecholamine nội sinh và tiết cortisol cao, dẫn đến tân tạo đường và phân giải glycogen. Ở trẻ em, glucose huyết thanh thường tăng trong 12 đến 18 giờ đầu tiên sau khi bị tổn thương và sau đó giảm xuống mức bình thường. Điều này có thể trầm trọng hơn do hạ thân nhiệt điều trị. Mặc dù tăng đường huyết do bệnh nặng có liên quan đến khả năng sống sót kém ở trẻ bị bệnh nặng,55,56 vẫn chưa rõ liệu tăng đường huyết là nguyên nhân hay dấu hiệu của các kết cục xấu.
Các biểu hiện lâm sàng của thiếu máu cục bộ/tái tưới máu hệ thống bao gồm rò rỉ mao mạch với giảm thể tích tuần hoàn trong lòng mạch, liệt mạch, rối loạn đông máu, tăng đường huyết, suy tuyến thượng thận, và suy giảm sử dụng và cung cấp oxy, góp phần gây rối loạn chức năng của nhiều cơ quan.
Sinh lý bệnh nền có sẵn (Persistent Precipitating Pathophysiology)
Xử trí trẻ sau ngừng tim bao gồm chẩn đoán và điều trị nguyên nhân gây ngừng tim. Việc không xác định và khắc phục nguyên nhân ban đầu của ngừng tim khiến bệnh nhân có nguy cơ bị tổn thương thứ cấp và thậm chí tái phát ngừng tim. Ví dụ về tình trạng bệnh có triệu chứng có thể làm phức tạp việc xử trí sau ngừng tim bao gồm sốt và sốc liên tục ở bệnh nhân nhiễm trùng, tăng CO2 dai dẳng hoặc giảm oxy máu ở trẻ bị suy hô hấp cấp tính, mất cân bằng điện giải (ví dụ, tăng kali máu), và trong ngừng tim do chấn thương, sốc giảm thể tích hoặc tắc nghẽn không được điều trị.
Chiến lược điều trị
PCAC phải bắt đầu ngay sau ROSC, tập trung vào việc hỗ trợ chức năng ban đầu của cơ quan nội tạng, dự đoán và điều trị PCAS, đồng thời giải quyết nguyên nhân cơ bản của việc ngừng tim. Một cách tiếp cận có hệ thống là cần thiết không chỉ để xử trí ngay lập tức bệnh nhân không ổn định mà còn để ngăn ngừa tình trạng mất bù ở bệnh nhân ổn định ban đầu. Những biện pháp can thiệp này nên được cung cấp càng sớm càng tốt và nhiều biện pháp có thể được thực hiện bất kể địa điểm ngưng tim. Chăm sóc ngay sau ROSC nên kết hợp các chiến lược điều trị để hỗ trợ tưới máu hệ thống và chức năng cơ quan. Một phản ứng phối hợp và tích hợp từ các nhân viên y tế chăm sóc trong các cơ sở tiền nhập viện, khoa cấp cứu và ICU có thể cải thiện kết quả cho những người sống sót ban đầu.
Giám sát chung
Trong giai đoạn sau ngừng tim, điều quan trọng là nhóm chăm sóc sức khỏe phải dự đoán và đánh giá sự tiến triển của rối loạn chức năng cơ quan và hệ thống cũng như chủ động hỗ trợ chức năng cơ quan. Điều này đòi hỏi phải theo dõi liên tục để hướng dẫn các liệu pháp chăm sóc tích cực (Bảng 1).
PCAC bắt đầu bằng việc thiết lập giám sát càng sớm càng tốt sau ROSC, đồng thời điều tra và điều trị bệnh tiềm ẩn cũng như nguyên nhân gần nhất của việc ngưng tim và xử trí các bất thường nghiêm trọng. Việc theo dõi tại hiện trường tiếp tục thông qua quá trình vận chuyển và bao gồm điện tâm đồ, đo độ bão hòa oxy, capnography, đo huyết áp không xâm lấn và xét nghiệm glucose tại điểm chăm sóc.
Theo dõi chăm sóc tích cực tổng quát
Theo dõi chăm sóc tích cực tổng quát bao gồm theo dõi tim liên tục từ xa, đo độ bão hòa oxy, theo dõi capnography liên tục, theo dõi nhiệt độ liên tục, đo huyết áp và lượng nước tiểu. Theo dõi bao gồm phân tích trong phòng thí nghiệm về khí máu tĩnh mạch hoặc động mạch, chất điện giải trong huyết thanh, nồng độ glucose và canxi. Lactate động mạch và độ bão hòa oxy tĩnh mạch trung tâm hỗ trợ đánh giá mức độ cung cấp oxy của mô. X- quang ngực hỗ trợ đánh giá vị trí ống nội khí quản, kích thước tim và tình trạng phổi.52 Theo dõi bổ sung bao gồm đánh giá chức năng thận, đo nồng độ huyết sắc tố, theo dõi chức năng đông máu và đánh giá các dấu hiệu viêm và nhiễm trùng.
Bảng 1. PCAS: Theo dõi
| Giám sát chung
· Độ bão hòa oxy, liên tục bằng phép đo oxy mạch nẩy · Capnography (định lượng) · Huyết áp động mạch (trong động mạch khi có thể hoặc không xâm lấn) · Đường huyết (điểm chăm sóc) · Theo dõi tim từ xa, liên tục · Điện tâm đồ · Nhiệt độ, lõi liên tục (thực quản, bàng quang hoặc trực tràng) · Lượng nước tiểu · Khí máu động mạch (pH, PaO2, PaCO2) · Lactate huyết thanh, động mạch · Đường huyết, chất điện giải, creatinine, công thức máu toàn bộ, xét nghiệm đông máu · Độ bão hòa oxy tĩnh mạch · Áp lực tĩnh mạch trung tâm · X quang ngực |
| Theo dõi huyết động bổ sung
· Siêu âm tim |
| Theo dõi thần kinh
· Khám lâm sàng thần kinh, nối tiếp · Điện não đồ, liên tục · Hình ảnh: CT não hoặc MRI não |
| CT, chụp cắt lớp vi tính; EEG, điện não đồ; MRI, chụp cộng hưởng từ; và PCAS, hội chứng sau ngừng tim. |
Theo dõi huyết động
Khoảng 95% IHCA ở trẻ em xảy ra trong ICU,20 và gần 50% những bệnh nhân này sẽ được đặt ống thông động mạch trước khi ngừng tim. Nếu có thể, nên đặt một ống thông động mạch để theo dõi liên tục áp lực trong động mạch nhằm tạo thuận lợi cho việc xác định và điều trị hạ huyết áp.58 Ngoài ra, ống thông tĩnh mạch trung tâm có thể hữu ích để theo dõi độ bão hòa oxy trong tĩnh mạch trung tâm và cung cấp một lộ trình cho việc truyền dịch truyền và thuốc. Catheter động mạch phổi hiện nay ít được sử dụng trong nhi khoa.
Mặc dù không có đủ bằng chứng để đề xuất thời gian hoặc tần suất tối ưu của siêu âm tim sau ngừng tim, nhưng nó là một công cụ hữu ích, không xâm lấn để xác định rối loạn chức năng cơ tim và các bất thường tim bẩm sinh và mắc phải.
Điện tâm đồ 12 chuyển đạo có thể hữu ích trong việc xác định nguyên nhân bị ngưng tim.
Theo dõi thần kinh
Theo dõi não rất hữu ích ở những bệnh nhân ngừng tim sau hôn mê để hướng dẫn điều trị nhằm ngăn ngừa tổn thương thần kinh thứ phát. Các cuộc kiểm tra thần kinh nối tiếp có thể giúp xác định tổn thương não do thiếu oxy-thiếu máu cục bộ đang tiến triển. Do tỷ lệ co giật điện não đồ cao sau ROSC,59 theo dõi bằng điện não đồ (EEG) đang gia tăng ở PCAC trẻ em.60 Hình ảnh thần kinh có thể hữu ích để xác định nguyên nhân não gây ngừng tim và sự hiện diện của tổn thương não nghiêm trọng.
Các thử nghiệm lâm sàng dành cho người lớn đang được tiến hành để đánh giá tính hữu ích của việc theo dõi quá trình oxygen hóa não và CBF. Một nghiên cứu nhỏ ở trẻ em (36 bệnh nhân)64 đã đánh giá vai trò của quá trình tự điều hòa não trong việc hướng dẫn xử trí huyết động và cung cấp oxy cũng như hỗ trợ tiên lượng thần kinh ở trẻ hôn mê sau ngừng tim, nhưng cần nhiều nghiên cứu hơn.
Tối ưu hóa huyết động sớm
Huyết áp
Huyết động không ổn định sau ROSC phổ biến ở cả trẻ em66,67 và người lớn.68,69 Tuy nhiên, người ta vẫn chưa hiểu đầy đủ liệu hạ huyết áp sau ngừng tim có phải là dấu hiệu báo trước về một kết cục xấu không thể tránh khỏi hay liệu nó có thể là một yếu tố nguy cơ có thể thay đổi được cần can thiệp sớm hay không.
Hạ huyết áp sớm sau khi ngừng timở trẻ em có liên quan đến khả năng sống sót sau khi xuất viện thấp hơn.66,67 Một nghiên cứu quan sát về IHCA ở trẻ em đã phát hiện ra rằng huyết áp tâm thu thấp hơn phân vị thứ năm theo độ tuổi và giới tính trong vòng 6 giờ đầu tiên sau khi ROSC phát triển ở 56% của 383 trẻ em và có liên quan độc lập với việc tăng tỷ lệ tử vong trong bệnh viện và kết cục thần kinh không thuận lợi.66 Hơn nữa, một nghiên cứu khác cho thấy trong số 80 trẻ em đạt được ROSC sau OHCA, nhịp tim bình thường và huyết áp bình thường trong giờ đầu tiên có liên quan độc lập với khả năng sống sót đến xuất viện.70 Gần đây nhất, một phân tích hậu kỳ về thử nghiệm THAPCA (Trị liệu hạ thân nhiệt sau khi ngừng tim ở trẻ em) của OHCA (THAPCA-OH) đã chứng minh rằng hạ huyết áp sớm xảy ra ở 26,7% bệnh nhân và có liên quan đến khả năng sống sót đến khi xuất viện thấp hơn.67 Bất chấp những dữ liệu này, trong một nghiên cứu thuần tập hồi cứu trẻ em <18 tuổi, chỉ có 41% bệnh nhân bị hạ huyết áp sớm sau ROSC được điều trị bằng thuốc vận mạch trong 6 giờ đầu tiên sau ROSC.
Khi xuất hiện hạ huyết áp sau ngừng tim, không rõ liệu việc tăng huyết áp thông qua truyền dịch và thuốc tăng co bóp/thuốc vận mạch có thể giảm thiểu tác hại hay không. Các nghiên cứu quan sát ở trẻ em71 và người lớn53,72–74 đã ghi nhận kết quả tồi tệ hơn ở những bệnh nhân cần thuốc vận mạch trong giai đoạn sau ngừng tim.
Cho đến nay, không có nghiên cứu can thiệp nào ở trẻ em hoặc người lớn đánh giá hiệu quả sống còn của việc điều chỉnh huyết áp sau ROSC. Một số thử nghiệm can thiệp theo phác đồ sau ngừng tim ở người lớn bao gồm các mục tiêu huyết áp đã chứng minh kết quả được cải thiện trong giai đoạn theo chỉ định của phác đồ.1,75,76 Tuy nhiên, không thể xác định mối quan hệ nhân quả hoặc có thể đảo ngược giữa hạ huyết áp và kết quả sau ROSC.
Hỗ trợ tuần hoàn
Hiện tại, không có bằng chứng chất lượng cao để hỗ trợ bất kỳ chiến lược cụ thể nào để tối ưu hóa huyết động sau ngừng tim ở trẻ em. Điều trị hạ huyết áp sau ngừng tim và rối loạn chức năng cơ tim có thể được hỗ trợ bằng cách theo dõi và đánh giá lactate động mạch và độ bão hòa oxy tĩnh mạch trung tâm.52 Dịch truyền tĩnh mạch, thuốc tăng co bóp cơ tim và thuốc vận mạch sẽ được sử dụng khi cần thiết để duy trì huyết áp tâm thu lớn hơn huyết áp phân vị thứ năm theo tuổi.
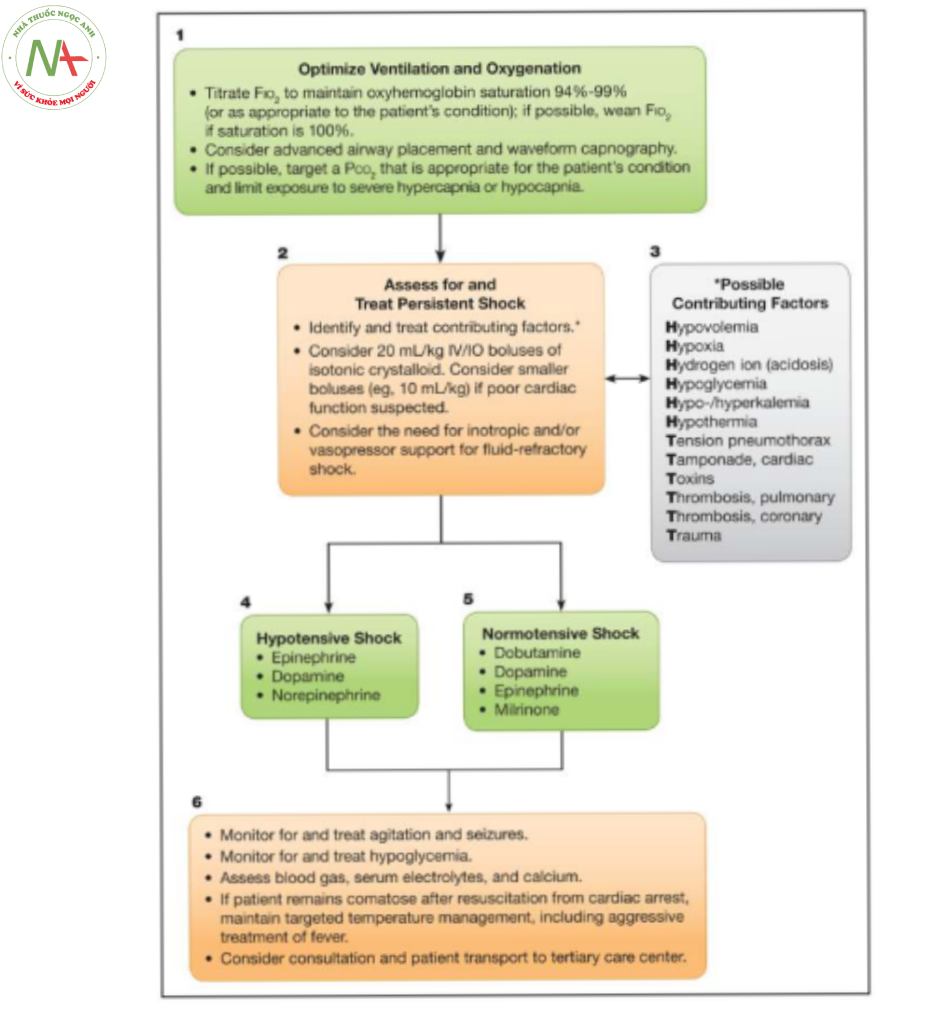
Không có dữ liệu được công bố để xác định liều lượng/thể tích tương đối tối ưu của dịch truyền so với thuốc tăng co bóp/thuốc vận mạch; tác nhân vận mạch ưa thích hoặc sự kết hợp của các tác nhân; các điểm cuối tưới máu tối ưu; khoảng thời gian tối ưu để đạt được tưới máu mục tiêu; hoặc liệu tác hại có thể xảy ra do truyền dịch hoặc dùng thuốc tăng co bóp/thuốc vận mạch hay không, đặc biệt là ở các phân nhóm như bệnh nhân tim và chấn thương. Các hướng dẫn trước đây đã khuyến nghị dùng thuốc vận mạch và thuốc tăng co bóp cơ tim với các khoảng liều lượng để điều trị hạ huyết áp và hỗ trợ cung lượng tim (Bảng 2). Các liệu pháp thuốc vận mạch thích hợp nên được điều chỉnh cho phù hợp với từng bệnh nhân và điều chỉnh khi cần thiết.52 Mức độ nghiêm trọng của PCAS của mỗi bệnh nhân, kết hợp với các đặc điểm trước và trong khi ngừng tim của bệnh nhân đó, đòi hỏi một cách tiếp cận riêng cho từng bệnh nhân nhằm tối ưu hóa tưới máu mà không tạo ra quá nhiều công cơ tim.
Bảng 2. Dịch truyền mạch có thể được sử dụng để tối ưu hóa huyết động trong PCAS
| Thuốc | Phạm vi liều | Loại thuốc | Các tác dụng phụ |
| Dobutamine | 2–20 μg/kg
mỗi 1 phút IV/IO |
Tăng co bóp; giãn mạch | Nhịp tim nhanh; tổn thương mạch máu ngoại biên |
| Dopamine | 2–20 μg/kg
mỗi 1 phút IV/IO |
Tăng co bóp; tăng nhịp tim; giãn mạch thận và tạng khi dùng liều thấp; co mạch khi dùng liều cao | Nhịp tim nhanh; tổn thương mạch máu ngoại biên |
| Epinephrine | 0.1–1 μg/kg
mỗi 1 phút IV/IO |
Tăng co bóp; tăng nhịp tim; giãn mạch khi dùng liều thấp; co mạch khi dùng liều cao | Nhịp tim nhanh; tổn thương mạch máu ngoại biên |
| Milrinone | 0.25–0.75
μg/kg mỗi 1 phút IV/IO |
Tăng co bóp; lusitrope; giãn mạch | Hạ huyết áp |
| Norepinephrine | 0.1–2 μg/kg
mỗi 1 phút |
Co mạch | Tổn thương mạch máu ngoại biên |
IO, trong xương; IV, tĩnh mạch; và PCAS, hội chứng sau ngừng tim.
Loạn nhịp tim
Các rối loạn nhịp quan sát thấy trong giai đoạn sau ngừng tim bao gồm ngoại tâm thu nhĩ và ngoại tâm thu thất, nhịp nhanh trên thất và nhịp nhanh thất. Blốc tim là bất thường nhưng có thể được quan sát như một biểu hiện của viêm cơ tim.79,80 Không có đủ bằng chứng ở người lớn và không có nghiên cứu được công bố ở trẻ em để hỗ trợ việc sử dụng thuốc chống loạn nhịp dự phòng thường quy sau ROSC,4,81 nhưng rối loạn nhịp trong giai đoạn này có thể cần điều trị. Điều trị phụ thuộc vào nguyên nhân và hậu quả huyết động của rối loạn nhịp tim. Khử cực sớm, cả tâm nhĩ và tâm thất, thường không cần điều trị ngoài việc duy trì tưới máu đầy đủ và cân bằng dịch truyền và điện giải bình thường. Loạn nhịp thất có thể biểu hiện rối loạn chức năng cơ tim nghiêm trọng hơn.
Đối với rối loạn nhịp tim đang diễn ra sau ROSC, việc lựa chọn liệu pháp điều trị bằng thuốc tối ưu phụ thuộc rất nhiều vào bệnh lý và chức năng cơ bản của tim, và việc tư vấn điện sinh lý tim ở trẻ em thường là cần thiết. Nhiều loại thuốc chống loạn nhịp bị chống chỉ định ở những bệnh nhân mắc hội chứng QT dài82 và hội chứng Brugada.83 Đặc biệt, nên tránh dùng bất kỳ loại thuốc nào kéo dài khoảng QT ở bất kỳ bệnh nhân nào nghi ngờ mắc hội chứng QT dài. Các ví dụ bao gồm amiodarone, procainamide và sotalol.
Nhiều thuốc vận mạch được sử dụng để hỗ trợ chức năng cơ tim có thể làm tăng tính dễ bị kích thích của cơ tim và nguy cơ loạn nhịp tim. Sự khử cực sớm của tâm nhĩ hoặc tâm thất thường được quan sát thấy và có thể được kiểm soát bằng cách tối ưu hóa liều lượng của thuốc vận mạch.
Loạn nhịp tim thường được báo cáo trong TTM.2,3,84,85 Nhịp tim chậm đặc biệt phổ biến với TTM nhưng thường không cần điều trị.
Oxygen hóa qua màng ngoài cơ thể
ECMO có thể được bắt đầu trong quá trình CPR hoặc sau ROSC khi bệnh nhân có tình trạng tim mạch bất ổn liên tục và có nguy cơ cao bị ngừng tim lặp lại. Khi ECMO được bắt đầu trong quá trình CPR (nghĩa là ECPR), nó sẽ được tiếp tục trong giai đoạn sau ngừng tim cho đến khi bệnh nhân có thể được tách ra khỏi hỗ trợ cơ học. Bản cập nhật hướng dẫn năm 2015 của AHA về CPR và chăm sóc tim mạch khẩn cấp và “Đồng thuận quốc tế năm 2015 về khoa học hồi sức tim phổi và chăm sóc tim mạch khẩn cấp với các khuyến nghị điều trị” đã khuyến nghị rằng ECPR có thể được xem xét cho trẻ em đã được chẩn đoán mắc bệnh tim mà trải qua IHCA, mặc dù cần cân nhắc đáng kể dựa trên sự sẵn có của nhân viên lành nghề và nhu cầu về các giao thức và thiết bị hiệu quả.
Hiệu quả lâm sàng của ECMO để hỗ trợ tim mạch sau ROSC chưa được nghiên cứu kỹ lưỡng. Trong một nghiên cứu trên quần thể PICU, việc sử dụng ECMO trong vòng 24 giờ sau ROSC có liên quan đến việc giảm tỷ lệ tử vong.87 Loạt trường hợp đã ghi nhận vai trò của ECMO88 và hỗ trợ thiết bị hỗ trợ tâm thất89,90 ở trẻ em bị sốc tim kháng trị hoặc viêm cơ tim tối cấp cấp tính.88,91 Trong PCAC, hỗ trợ tuần hoàn cơ học (ECMO) có thể được xem xét nếu tình trạng bất ổn tim mạch đáng kể vẫn tiếp diễn mặc dù đã tăng thể tích tuần hoàn thích hợp và sử dụng thuốc tăng co bóp, thuốc vận mạch và, nếu được chỉ định, thuốc chống loạn nhịp.
Oxygen hóa và thông khí
Việc cung cấp oxy và thông khí tối ưu cho trẻ em sau ROSC có thể bị cản trở bởi bệnh lý gây ra ngừng tim và bởi sinh lý bệnh sau ngừng tim sau đó. Những thách thức tiếp theo về xử trí có thể do hít sặc và tổn thương phổi xảy ra trong quá trình hồi sức,92 cũng như tổn thương phổi liên quan đến máy thở sau đó.93 Ngoài ra, các nhà cung cấp phải lưu ý đến thực tế là liệu pháp hạ thân nhiệt được sử dụng sau ROSC làm thay đổi mối quan hệ giữa độ bão hòa oxy động mạch và áp lực oxy động mạch sao cho, đối với độ bão hòa oxy động mạch nhất định, áp lực oxy động mạch (PaO2) thấp hơn mức quan sát được khi nhiệt độ bình thường. Hạ thân nhiệt cũng làm giảm tốc độ chuyển hóa; do đó, việc sản xuất carbon dioxide sẽ thấp hơn ở bất kỳ thông khí phút nào.94,95 Do đó, việc xử trí đứa trẻ được đặt nội khí quản sau khi tim ngừng đập đặt ra những thách thức đặc biệt đòi hỏi phải cân nhắc cẩn thận.
Oxygen hóa
Liệu pháp oxy là một phương pháp điều trị phản xạ ở những bệnh nhân bị bệnh nặng, bao gồm cả những người mắc bệnh ROSC sau khi tim ngừng đập. Mặc dù tình trạng thiếu oxy máu được chấp nhận rộng rãi là có hại, nhưng các kết luận của nghiên cứu không nhất quán về giá trị của tình trạng áp lực oxy động mạch cao, hoặc chứng tăng oxy máu, sau khi ngừng tim ở trẻ em.
Các bất thường về khí máu sau ngừng tim thường gặp ở trẻ em, đặc biệt là trong những giờ đầu tiên sau ROSC,33,34 và các bằng chứng được công bố đã không chứng minh được tác động nhất quán của tình trạng tăng oxy máu hoặc giảm oxy máu sau ngừng tim đối với kết cục. Trong một nghiên cứu hồi cứu trên 195 trẻ em, chỉ 13% có cả oxy máu bình thường và carbon dioxide bình thường (nghĩa là thông khí bình thường) trong 6 giờ đầu tiên sau ROSC và tình trạng tăng oxy máu động mạch không liên quan đến kết cục.33 Trong 1 nghiên cứu hồi cứu (n=74)34 và 1 nghiên cứu tiền cứu (n=223)35 ở trẻ em sau ngừng tim, không phải tình trạng tăng oxy máu (PaO2 >300 mm Hg) cũng như tình trạng thiếu oxy máu (PaO2 <60 mm Hg) trong 24 giờ đầu tiên sau khi ROSC không liên quan đến tỷ lệ tử vong trong 6 tháng. Ngược lại, một nghiên cứu hồi cứu đa trung tâm lớn trên 1875 trẻ em sau khi ngừng tim cho thấy tỷ lệ tử vong gia tăng với cả tình trạng tăng oxy máu (PaO2 ≥ 300 mm Hg; tỷ lệ chênh, 1,25 [95% CI, 1,17– 1,37]) và thiếu oxy máu (PaO2 <60 mm Hg; tỷ lệ chênh, 1,92 [95% CI, 1,8–2,21]), với tỷ lệ sống sót cao nhất ở trẻ em có PaO2 từ 60 đến 300 mm Hg.36 Để giải quyết tác động của việc tiếp xúc với oxy tích lũy theo thời gian, một nghiên cứu năm 2015 đã phân tích khí máu động mạch các mẫu ở 3 khoảng thời gian trong 24 giờ đầu tiên sau ROSC ở 200 trẻ em được điều trị có hoặc không có hạ thân nhiệt điều trị nhẹ. Những người sống sót tiếp xúc với oxy tích lũy cao hơn so với những người không sống sót, nhưng mối liên quan này chỉ thấy ở những bệnh nhân được điều trị bằng liệu pháp hạ thân nhiệt nhẹ.
Các nghiên cứu hiện tại đánh giá tác động của tình trạng thiếu oxy và tăng oxy máu tùy thuộc vào quyết định của bác sĩ lâm sàng về thời gian phân tích khí máu, với nhiều báo cáo dựa trên phân tích khí đầu tiên và các báo cáo khác ghi lại các giá trị khí máu tối đa hoặc tối thiểu trong khoảng thời gian 24 giờ.34– 36,97–102 Một hoặc 2 lần đo khí máu, có thể vài giờ sau ROSC, có thể không phản ánh tác động của việc cung cấp oxy quá mức trong vài phút đến đầu giờ sau ROSC.
Sau ROSC, điều hợp lý là nhắm đến PaO2 bình thường (hoặc giá trị phù hợp với tình trạng của trẻ nếu trẻ mắc bệnh tim tím tái) và sử dụng nồng độ oxy hít vào thấp nhất có thể, cai máy để duy trì độ bão hòa oxy ở mức 94% đến 99% theo hướng dẫn.52 Trong toàn bộ PCAC, phải tránh tình trạng thiếu oxy máu bất cứ khi nào có thể, đặc biệt là trong quá trình chuẩn độ oxy.58 Hướng dẫn AHA PALS năm 2010 khuyến nghị phân tích khí máu động mạch ngay lập tức càng sớm càng tốt sau ROSC và trong vòng 10 đến 15 phút kể từ khi thiết lập thông khí cơ học ban đầu để hướng dẫn xử trí và chuẩn độ oxy và để hỗ trợ thông khí cơ học.
Thông khí
Rối loạn sau ngừng tim ở PaCO2 là phổ biến.33,35,103,104 Sự thay đổi của PaCO2 có thể ảnh hưởng đến kết cục bằng cách làm trầm trọng thêm tình trạng thiếu máu cục bộ thông qua co mạch não do giảm CO2 máu gây ra38,105 hoặc thông qua giãn mạch não và phù não do tăng CO2.
Các nghiên cứu hồi cứu quy mô nhỏ sau ngừng tim ở trẻ em đã chứng minh rằng giảm CO2 máu và tăng CO2 máu là phổ biến, đặc biệt là trong những giờ đầu tiên sau ROSC. Trong một nghiên cứu tiền cứu, đa trung tâm, quan sát sau ngừng tim trên 223 trẻ em từ 1 tháng đến 18 tuổi, cả tình trạng giảm CO2 máu (PaCO2 <30 mm Hg) và tăng CO2 máu (PaCO2 >50 mm Hg) đều xuất hiện và có liên quan độc lập với tỷ lệ tử vong.35 Tuy nhiên, trong một phân tích hồi cứu quy mô nhỏ hơn sau đó về 195 trẻ em từ 24 giờ đến 18 tuổi, tình trạng oxygen hóa (tức là PaO2) cũng như tình trạng thông khí (tức là PaCO2) trong 6 giờ đầu tiên sau khi ROSC không liên quan đến kết cục.
Dữ liệu ngoại suy từ chăm sóc tích cực ở trẻ em cho thấy rằng trong PCAC, các chiến lược bảo vệ phổi, bao gồm thể tích hít vào thấp và áp lực dương cuối kỳ thở ra, được đảm bảo để giảm thiểu tổn thương phổi và ảnh hưởng đến huyết động.
Trên cơ sở bằng chứng sẵn có, sau ROSC, sẽ hợp lý khi nhắm mục tiêu CO2 bình thường (nghĩa là bình thường đối với trẻ, hoặc PaCO2 35– 45 mm Hg) hoặc PaCO2 cụ thể cho tình trạng của bệnh nhân, hạn chế tiếp xúc với tăng CO2 máu nghiêm trọng và giảm CO2 máu.58 Cần đánh giá sớm PaCO2 vì thông khí phút quy định ban đầu có thể chỉ có mối tương quan yếu với PaCO2 sau đó.108 Ngoài ra, mặc dù có thể hữu ích khi xác định mối tương quan của PaCO2 với CO2 cuối thì thở ra (PetCO2) để hỗ trợ theo dõi thông khí không xâm lấn,52 bác sĩ lâm sàng nên thận trọng khi sử dụng PetCO2 làm đại diện thay thế cho PaCO2 vì cung lượng tim và khoảng chết phế nang tăng lên sẽ ảnh hưởng đến mối tương quan của chúng.
Điều trị sinh lý bệnh nền có sẵn
Trong giai đoạn ngay sau ROSC, việc điều trị nguyên nhân gây ngừng tim có thể yêu cầucác biện pháp can thiệp có mục tiêu cụ thể (ví dụ: chạy thận nhân tạo khi ngộ độc, phẫu thuật sốc xuất huyết hoặc tổn thương khối nội sọ). Bởi vì những biện pháp can thiệp này mang lại nguy cơ cố hữu làm bệnh nhân mất ổn định, các nhân viên y tế phải xem xét tỷ lệ nguy cơ trên lợi ích của họ. Điều cần thiết là tất cả các thành viên của nhóm chăm sóc sức khỏe đa ngành, bao gồm các thành viên trong nhóm gây mê và phẫu thuật cũng như các nhóm tư vấn chăm sóc sức khỏe khác, phải hiểu rõ về các ưu tiên xử trí sau ngừng tim.
Xử trí nhiệt độ mục tiêu
Tăng thân nhiệt sau ngừng tim (nhiệt độ cơ thể tăng cao) là phổ biến và tình trạng tăng thân nhiệt kéo dài có liên quan đến kết cục thần kinh không thuận lợi ở trẻ em.
Hai thử nghiệm đối chứng ngẫu nhiên, đa quốc gia, đa trung tâm gần đây đã đánh giá tác động của TTM ở nhiệt độ từ 32°C đến 34°C so với TTM ở nhiệt độ từ 36°C đến 37,5°C đối với tỷ lệ sống sót sau 1 năm, với kết cục thần kinh thuận lợi ở trẻ em >2 ngày tuổi và <18 tuổi. Nghiên cứu THAPCA bao gồm cả thử nghiệm OHCA (THAPCA- OH)3 và thử nghiệm IHCA (THAPCA-IH).2 Đối với cả hai thử nghiệm, trẻ hôn mê trong vòng 6 giờ sau ROSC được chỉ định ngẫu nhiên vào TTM ở nhiệt độ từ 32°C đến 34°C hoặc TTM từ 36°C đến 37,5°C. Trẻ em được chọn ngẫu nhiên vào phạm vi nhiệt độ thấp hơn được làm mát đến 32°C đến 34°C trong 48 giờ, làm ấm lại trong 16 đến 24 giờ và duy trì ở nhiệt độ 36°C đến 37,5°C cho đến 120 giờ sau khi bắt đầu TTM. Trẻ được TTM đến ngưỡng nhiệt độ cao hơn được duy trì tích cực ở nhiệt độ 36°C đến 37,5°C trong 120 giờ (5 ngày).
Trong THAPCA-OH,3 tỷ lệ phần trăm những người sống sót có kết cục thần kinh thuận lợi sau 1 năm (được định nghĩa là Thang đo hành vi thích ứng Vineland, điểm phiên bản thứ hai ≥70) không khác biệt đáng kể giữa các nhóm TTM (TTM đến 32°C–34°C: 20% so với TTM ở nhiệt độ 36°C–37,5°C: 12%; nguy cơ tương đối, 1,54 [KTC 95%, 0,86–2,76]; P=0,14). Hạ kali máu và giảm tiểu cầu phổ biến hơn ở trẻ em được điều trị bằng TTM đến 32°C đến 34°C, và liệu pháp thay thế thận (renal replacement therapy – RRT) thường được sử dụng hơn ở nhóm TTM đến 36°C đến 37,5°C. Không có sự khác biệt về tỷ lệ nhiễm trùng, chảy máu, rối loạn nhịp tim nghiêm trọng hoặc tử vong sau 28 ngày.
Việc đăng ký tham gia THAPCA-IH đã bị dừng sớm do vô ích.2 Không có sự khác biệt nào được ghi nhận về tỷ lệ sống sót sau 1 năm với kết cục thần kinh thuận lợi (36% đối với TTM đến 32°C–34°C so với 39% đối với TTM đến 36°C– 37,5 °C: giảm nguy cơ, 0,92 [KTC 95%, 0,67–.27];
P=0,63), thay đổi đường cơ sở thần kinh thành 1 năm (P=0,70) hoặc tỷ lệ sống sót chung trong 1 năm (49% đối với TTM thành 32 °C–34°C so với 46% đối với TTM đến 36°C–37,5°C; nguy cơ tương đối, 1,07 [KTC 95%, 0,85–1,34]; P=0,56).
Trẻ em được điều trị bằng cả hai phác đồ TTM đều có tác dụng phụ tương tự nhau.
Có sự khác biệt quan trọng giữa các đối tượng trong THAPCA-OH và những đối tượng trong THAPCA-IH. 72% bệnh nhân trong THAPCA-OH có nguyên nhân ngừng tim là do hô hấp, trong khi 65% bệnh nhân trong THAPCA-IH có nguyên nhân ngừng tim là do tim. Đáng chú ý, >50% đối tượng THAPCA-IH được xử trí bằng ECMO. Ngoài ra, 37% bệnh nhân trong thử nghiệm THAPCA-IH so với 16% bệnh nhân trong thử nghiệm THAPCA-OH có kết cục thần kinh thuận lợi sau 1 năm theo dõi.
Thực hiện TTM
TTM đến 32°C đến 34°C có thể được chia thành 3 giai đoạn: bắt đầu, duy trì và làm ấm lại.
Có thể đạt được quá trình hạ thân nhiệt bằng nhiều phương thức, bao gồm chăn làm lạnh được điều khiển bằng servo bên dưới hoặc bên trên bệnh nhân; làm lạnh bề mặt bằng các túi nước đá, bể nước lạnh hoặc quạt; giảm nhiệt độ phòng; và thỉnh thoảng rửa dạ dày bằng nước muối lạnh. Cần đạt được nhiệt độ mục tiêu càng nhanh càng tốt để có hiệu quả, nhưng khoảng thời gian tối ưu để đạt được nhiệt độ mục tiêu vẫn chưa được biết. Việc sử dụng truyền liên tục để hạ nhiệt độ tương đối an toàn, trong khi truyền tĩnh mạch nước muối lạnh có thể làm tăng nguy cơ nhịp tim chậm sâu.111 Catheter làm mát nội mạch không được sử dụng trong nhi khoa vì chúng có đường kính lớn và có thể gây huyết khối; chúng có thể được xem xét cho trẻ lớn hơn.112 Nhiệt độ lõi (core temperature) của bệnh nhân nên được theo dõi liên tục.58 Các kỹ thuật hiện có bao gồm đầu dò nhiệt độ lõi trực tràng, thực quản hoặc bàng quang.
Việc tăng nhiệt độ TTM lên 32°C đến 34°C có liên quan đến những thay đổi về tốc độ chuyển hóa, nồng độ chất điện giải trong huyết thanh và huyết động học của bệnh nhân. Hạ kali máu, hạ photphat máu, hạ magie máu và hạ canxi máu phát triển trong quá trình hạ thân nhiệt và có thể dẫn đến rối loạn nhịp tim.3,4,112–114 Cần theo dõi chặt chẽ nồng độ chất điện giải và điều trị sự mất cân bằng, đặc biệt là trong quá trình hạ thân nhiệt. Hạ thân nhiệt cũng làm giảm độ nhạy insulin và bệnh nhân có nguy cơ bị tăng đường huyết.115 Nhịp tim chậm và hạ huyết áp đã được ghi nhận.112,113,116 Mặc dù giảm tiểu cầu đã được quan sát thấy trong quá trình hạ thân nhiệt,3,112 nhưng nó không liên quan đến việc tăng chảy máu hoặc nhu cầu sản phẩm máu. Hạ thân nhiệt có thể làm thay đổi chức năng hệ thống miễn dịch, nhưng không có sự khác biệt về tỷ lệ nhiễm trùng được ghi nhận trong các thử nghiệm THAPCA gần đây.
Giai đoạn duy trì TTM đến 32°C đến 34°C cần theo dõi cẩn thận để tránh biến động nhiệt độ. Topjian và cộng sự112 báo cáo chỉ tuân thủ 78% với phạm vi nhiệt độ khuyến nghị (nghĩa là hơn 1/5 bệnh nhân không được duy trì ở nhiệt độ khuyến nghị) mặc dù đã sử dụng phác đồ xử trí. Nhiệt độ <32°C đã được báo cáo ở ≈15% bệnh nhân trong các nghiên cứu về hạ thân nhiệt112,113 và có liên quan đến tỷ lệ tử vong gia tăng.113,116 Thời gian hạ thân nhiệt lý tưởng vẫn chưa rõ.
Các nghiên cứu đã công bố chưa xác định được phương pháp hoặc tốc độ làm ấm tối ưu sau khi TTM lên 32°C đến 34°C. Ở trẻ em, việc làm ấm thường được thực hiện với tốc độ không nhanh hơn 0,5°C cứ sau 2 giờ để giảm nguy cơ tăng tưới máu não, phù mạch và hạ huyết áp toàn thân cấp tính đã được ghi nhận trong quá trình làm ấm lại cho trẻ được điều trị hạ thân nhiệt sau chấn thương sọ não.117 Đối với trẻ hôn mê sau OHCA và IHCA, nhiệt độ TTM đến 32°C đến 34°C trong 24 đến 48 giờ là tương đối an toàn.2,3,116 Không rõ khoảng thời gian ngắn hơn để đạt được nhiệt độ mục tiêu, thời gian ngắn hơn hay dài hơn mục tiêu kiểm soát nhiệt độ, hoặc một mục tiêu nhiệt độ khác sẽ mang lại lợi ích.
Trong PCAC, sốt (≥38°C) nên được điều trị tích cực.58 Nên sử dụng các phương pháp tích cực và theo dõi nhiệt độ lõi liên tục kịp thời để đạt được TTM cho những bệnh nhân hôn mê sau ROSC. Để điều trị cho trẻ vẫn hôn mê sau OHCA, bản cập nhật hướng dẫn AHA PALS năm 2015 khuyến nghị rằng hợp lý là nên duy trì nhiệt độ bình thường liên tục (TTM đến 36°C–37,5°C) trong 5 ngày hoặc duy trì tình trạng hạ thân nhiệt liên tục trong 2 ngày (TTM đến 32C°–34°C) sau đó là 3 ngày thân nhiệt bình thường liên tục (TTM đến 36°C–37,5°C).2 Vì tỷ lệ tử vong tăng có liên quan đến nhiệt độ <32°C, nếu TTM đến 32°C đến 34°C được sử dụng, phải cẩn thận tỉ mỉ để tránh nhiệt độ <32°C.
Thuốc an thần và ức chế thần kinh cơ
Trẻ bị PCAS có thể cần điều trị bằng thuốc an thần hoặc thuốc giảm đau. Các bệnh nhân riêng lẻ có thể có các yêu cầu về thuốc khác nhau (lựa chọn cả thuốc và liều lượng) dựa trên bệnh đi kèm, tuổi bệnh nhân, tình trạng phát triển, mức độ tổn thương thần kinh và khoảng thời gian kể từ khi ngừng tim.119 Không có bằng chứng chất lượng cao nào để hướng dẫn các quyết định về an thần/giảm đau cho trẻ mắc PCAS.
Dữ liệu về cách tiếp cận bằng thuốcđể giảm đau và an thần ở người lớn còn hạn chế,120 và cách tiếp cận bằng thuốc thay đổi đáng kể trong thực tế. Sự kết hợp giữa opioid và benzodiazepin thường được sử dụng ở người lớn, mặc dù các thuốc an thần-gây mê như propofol và dexmedetomidine cũng là những lựa chọn.120 Việc sử dụng các loại thuốc này phải được cân bằng với nguy cơ biến chứng (ví dụ: nhiễm trùng và viêm phổi, hạ huyết áp và thở máy kéo dài) có thể phát sinh từ việc sử dụng chúng. Ở bệnh nhân người lớn mắc PCAS, tác dụng quá mức của thuốc dẫn đến việc kiểm tra thần kinh và tiên lượng gây nhầm lẫn.121 Không có đủ bằng chứng để xác định mức độ phổ biến của điều này xảy ra ở trẻ em hoặc thời gian ngừng sử dụng các thuốc này trước khi kiểm tra lâm sàng để tiên lượng.
Thuốc an thần và thuốc giảm đau rất quan trọng để kiểm soát chứng run thường xảy ra ở những bệnh nhân được điều trị bằng TTM.122 Run có thể làm tăng tốc độ chuyển hóa của não tại thời điểm mà việc cung cấp oxy cho não có thể đã bị tổn hại do cung lượng tim không đủ; điều này có thể tạo ra chấn thương não thứ cấp.123 Run rẩy cũng có thể làm sốt nặng hơn hoặc gây mất ổn định nhiệt độ, làm phức tạp TTM.124 Điều quan trọng cần lưu ý là run có thể xảy ra ở các nhiệt độ mục tiêu khác nhau trong quá trình TTM, bao gồm cả hạ thân nhiệt điều trị (32°C–34°C ) và điều trị nhiệt độ bình thường (36°C–37,5°C).
Opioid, được cung cấp bằng cách bolus hoặc tiêm truyền, thường được sử dụng là thuốc đầu tay để điều trị run. Tuy nhiên, việc sử dụng quá nhiều thuốc an thần/thuốc ngủ hoặc thuốc phiện có thể dẫn đến hạ huyết áp. Bằng chứng được công bố hạn chế về tác dụng và biến chứng của các phác đồ an thần và giảm đau trong quá trình hạ thân nhiệt bao gồm loạt nghiên cứu nhỏ dành cho người lớn.
Ức chế thần kinh cơ (neuromuscular blockade – NMB) có thể tạo điều kiện dễ dàng làm lạnh bệnh nhân PCAS. Chưa có nghiên cứu nhi khoa nào báo cáo về mối liên quan giữa việc sử dụng NMB để làm lạnh và kết cục của bệnh nhân. Dữ liệu dành cho người lớn về vấn đề này còn mâu thuẫn.128.129 Người lớn dùng NMB liều bolus có thời gian đạt được NMB nhanh hơn129, cần liều midazolam và fentanyl tích lũy thấp hơn, có số lượng liều rocuronium được sử dụng cao hơn, nhưng thức tỉnh sớm hơn và thời gian nằm ICU ngắn hơn.
Việc sử dụng NMB gây khó khăn cho quá trình kiểm tra thần kinh lâm sàng có khả năng dẫn đến tình trạng quá liều, dưới liều hoặc che giấu các kết cục kiểm tra thần kinh xấu đi. Ngoài ra, NMB sẽ che đậy các cơn co giật. Nghiên cứu sâu hơn là cần thiết để đánh giá vai trò của theo dõi sinh lý não để hướng dẫn an thần ở bệnh nhân mắc PCAS.
Nếu sử dụng TTM, người hành nghề phải biết rằng dược động học và dược lực học của thuốc an thần/thuốc ngủ và thuốc chẹn thần kinh cơ sẽ bị thay đổi, dẫn đến kéo dài thời gian thanh thải ở cả gan và thận.130 Giảm độ thanh thải các thuốc này sẽ làm chậm đi quá trình đánh giá bệnh nhân và tiên lượng kết cục của bệnh nhân một cách đáng tin cậy.131 Chuyển hóa thuốc có thể phức tạp hơn do rối loạn chức năng đa cơ quan thường liên quan đến PCAS.132 Theo dõi kích thích chuỗi bốn (train-of-four monitoring) có thể giúp định lượng mức độ NMB ở bệnh nhân PCAS nhưng đã được chứng minh là kém tin cậy hơn khi dùng cho bệnh nhân hạ thân nhiệt.
Hướng dẫn AHA PALS năm 201052 khuyến nghị kiểm soát cơn đau và sự khó chịu bằng thuốc giảm đau (ví dụ: morphine, fentanyl) và thuốc an thần (ví dụ: lorazepam hoặc midazolam). Các chất ức chế thần kinh cơ (ví dụ, vecuronium hoặc pancuronium) với tác dụng giảm đau hoặc an thần (hoặc cả hai) có thể cải thiện quá trình oxygen hóa và thông khí trong trường hợp mất đồng bộ bệnh nhân-máy thở hoặc chức năng phổi bị tổn thương nghiêm trọng. Tuy nhiên, các nhà cung cấp được cảnh báo rằng các tác nhân NMB có thể che giấu các cơn co giật và cản trở việc kiểm tra thần kinh.
Điều trị co giật
Co giật xảy ra ở 10%134 đến 50%135 trẻ em vẫn còn bệnh não sau khi đạt được ROSC. Gánh nặng cơn co giật thường rất lớn, với tình trạng co giật trên điện não đồ ở khoảng một nửa số trẻ bị co giật sau ROSC.135 Hơn nữa, khoảng một nửa số trẻ bị co giật sau ROSC chỉ trải qua các cơn co giật không co giật (cận lâm sàng, chỉ trên điện não đồ), không thể xác định được chỉ bằng quan sát lâm sàng.
Mặc dù hầu hết các nghiên cứu được sử dụng để dự đoán tỷ lệ co giật bao gồm các nhóm trẻ em không đồng nhất với các nhóm nhỏ bệnh nhân bị chấn thương não do thiếu oxy-thiếu máu cục bộ,136–148 một số nghiên cứu đơn trung tâm đã mô tả các nhóm trẻ em lớn hơn sau khi ngừng tim.134,149 Một nghiên cứu sớm, một nghiên cứu tiền cứu nhỏ về những đứa trẻ liên tiếp được điều trị hạ thân nhiệt sau khi ngừng tim đã báo cáo các cơn co giật trên điện não đồ ở 47%; hai phần ba có trạng thái co giật không co giật, và một phần ba chỉ có cơn co giật trên điện não đồ mà không có bất kỳ dấu hiệu lâm sàng nào.135 Các cơn co giật xảy ra thường xuyên hơn ở những đối tượng có mô hình nền điện não đồ bất thường hơn (ví dụ: gián đoạn quá mức – excessive discontinuity, ức chế bùng phát – burst suppression hoặc biểu đồ không có đặc tính sụt giảm cao – highly attenuated featureless tracings).135 Loạt ca nhi khoa gần đây đã chứng minh tỷ lệ co giật thấp hơn, điều này có thể phản ánh việc bao gồm những bệnh nhân bị tổn thương ít nghiêm trọng hơn với việc tăng cường sử dụng theo dõi điện não đồ theo thời gian. Hai nghiên cứu hồi cứu gần đây về trẻ em trong PCAC đã chứng minh các cơn co giật trên điện não đồ ở 10%149 đến 16%,134 và 71%149 đến 80%134 trong số này cấu thành trạng thái co giật trên điện não đồ. Các cơn co giật không thể dự đoán được từ bất kỳ biến số lâm sàng hoặc hồi sức nào. Co giật có liên quan đến kết cục thần kinh tổng thể không thuận lợi khi xuất viện nhưng không có tỷ lệ tử vong cao hơn.
Trong một cuộc khảo sát năm 2013 chủ yếu là các cơ sở giáo dục nhi khoa lớn ở Hoa Kỳ và Canada, 68% các cơ sở thực hiện theo dõi điện não đồ liên tục để xác định các cơn co giật bằng điện não đồ ở trẻ em sau khi ngừng tim.60 Một tuyên bố đồng thuận gần đây từ Hiệp hội sinh lý thần kinh lâm sàng Hoa Kỳ Điện não đồ liên tục chăm sóc tích cực Ủy ban Hướng dẫn khuyến nghị theo dõi điện não đồ liên tục đối với bệnh nhân người lớn và trẻ em vẫn còn bệnh não sau khi ngừng tim để xác định các cơn co giật bằng điện não.150,151 Tuyên bố khuyến nghị bắt đầu theo dõi điện não đồ càng sớm càng tốt, tiếp tục theo dõi trong 24 đến 48 giờ ở hầu hết bệnh nhân, nhưng tiếp tục cho đến sau 24 giờ thân nhiệt bình thường ở những bệnh nhân được điều trị bằng hạ thân nhiệt.
Vì co giật làm tăng nhu cầu chuyển hóa, có thể làm trầm trọng thêm rối loạn chức năng chuyển hóa và có thể làm tăng áp lực nội sọ, chúng có thể góp phần gây ra chấn thương não thứ phát. Vì những lý do này, nhiều bác sĩ lâm sàng hướng đến điều trị co giật, mặc dù cách tiếp cận này thường được hướng dẫn dựa trên tình trạng sức khỏe tổng thể của trẻ và các chỉ số tiên lượng khác. Tuy nhiên, chúng tôi thấy không đủ bằng chứng để xác định liệu điều trị cơn co giật lâm sàng hay điện tâm đồ có giúp cải thiện kết cục của bệnh nhân hay không và đâu là phương pháp tối ưu để kiểm soát cơn co giật sau khi ngừng tim.
Các cơn co giật cấp tính điển hình trên lâm sàng hoặc điện tâm đồ thường được điều trị ban đầu bằng benzodiazepin, levetiracetam hoặc phenytoin. Co giật rung giật cơ (Myoclonic seizures) có thể khó điều trị.149 Nhân viên y tế phải cảnh giác với các tác dụng phụ tiềm ẩn của thuốc chống co giật như rối loạn nhịp tim, hạ huyết áp và suy hô hấp. Ngoài ra, tác dụng an thần gây ra bởi thuốc chống co giật có thể làm phức tạp việc kiểm tra thần kinh.
Các nghiên cứu tiền cứu là cần thiết để xác định tác động của các cơn co giật đối với kết cục của bệnh nhân và liệu việc điều trị các cơn co giật trong giai đoạn sau ngừng tim có cải thiện kết cục của bệnh nhân hay không.
Kiểm soát đường huyết
Có rất ít bằng chứng được công bố về kiểm soát glucose sau ngừng tim. Trong một nghiên cứu thuần tập hồi cứu đa trung tâm lớn về trẻ em mắc IHCA trong khoảng thời gian 18 tháng vào năm 2003 và 2004 (n=353), nồng độ glucose cao nhất trong 12 giờ đầu tiên sau khi ngừng tim không liên quan đến tỷ lệ tử vong trong mô hình hồi quy logistic đa biến bao gồm các yếu tố lâm sàng và xét nghiệm trước ngừng tim, trong ngừng tim và sau ngừng tim.152 Cho đến nay, không có thử nghiệm lâm sàng can thiệp nào về kiểm soát glucose tập trung hoàn toàn vào trẻ em trong PCAC.
Cả hạ đường huyết và tăng đường huyết đều có liên quan đến kết cục không thuận lợi ở trẻ em bị bệnh nặng153–155 và người lớn.156–158 Các thử nghiệm ngẫu nhiên có kiểm soát sử dụng truyền insulin để duy trì kiểm soát chặt chẽ đường huyết ở trẻ em bị bệnh nặng159–161 và người lớn159,162 đã có nhiều kết cục khác nhau và tăng những lo ngại về tác động lâu dài của các đợt hạ đường huyết được quan sát thấy ở những bệnh nhân được chọn ngẫu nhiên để kiểm soát đường huyết chặt chẽ.160,161,163 Gần đây nhất, một thử nghiệm ngẫu nhiên có đối chứng gồm 35 trung tâm về kiểm soát đường huyết mục tiêu thấp hơn so với kiểm soát đường huyết mục tiêu cao hơn liên quan đến 713 trẻ sơ sinh và trẻ em (2 tuần –17 tuổi) đã bị ngừng sớm vì khả năng có lợi thấp và khả năng gây hại liên quan đến việc kiểm soát đường huyết mục tiêu thấp hơn. Thử nghiệm này chọn ngẫu nhiên trẻ em bị bệnh nặng đã được xác nhận tăng đường huyết (2 lần đo liên tiếp glucose huyết thanh ≥150 mg/dL hoặc ≥8,3 mmol/L) vào nhóm kiểm soát đường huyết mục tiêu thấp hơn (nồng độ glucose duy trì 80–100 mg/dL hoặc 4,4– 6,1 mmol/L) hoặc nhóm mục tiêu cao hơn (nồng độ glucose duy trì ở mức 150–180 mg/dL hoặc 8,3–10,0 mmol/L). Nồng độ glucose huyết thanh được đo liên tục và truyền insulin liên tục được chuẩn độ để duy trì glucose huyết thanh trong phạm vi mục tiêu. Không có sự khác biệt về kết cục chính của những ngày không nằm ICU giữa 2 nhóm, nhưng nhóm có mục tiêu glucose thấp hơn có tỷ lệ nhiễm trùng liên quan đến chăm sóc sức khỏe cao hơn và hạ đường huyết nghiêm trọng, được định nghĩa là mức đường huyết <40 mg/dL (2,2 mmol/L).
Trong PCAC, các bác sĩ lâm sàng nên tránh và điều trị kịp thời tình trạng hạ đường huyết. Trước đây, liệu trình PALS đã định nghĩa hạ đường huyết là nồng độ glucose ≤45 mg/dL ở trẻ mới sinh và ≤60 mg/dL ở trẻ nhỏ. Tăng đường huyết nặng cũng có thể là vấn đề vì nó có thể dẫn đến lợi tiểu thẩm thấu không kiểm soát được, điều này có thể làm trầm trọng thêm tình trạng giảm thể tích tuần hoàn sau ngừng tim và mất ổn định huyết động. Do đó, điều quan trọng là phải theo dõi nồng độ glucose huyết thanh, điều trị tăng đường huyết đáng kể và theo dõi lượng nước tiểu.
Hiện tại không có đủ bằng chứng được công bố để xác định nồng độ đường huyết tối ưu trong PCAC sẽ tối đa hóa kết cục thần kinh. Ngoài ra, không có đủ bằng chứng được công bố để xác định phương pháp lý tưởng để kiểm soát nồng độ glucose huyết thanh, thời gian lý tưởng của bất kỳ biện pháp kiểm soát glucose nào và tần suất theo dõi glucose lý tưởng cần thiết để giảm nguy cơ hạ đường huyết.
Nhận biết và điều trị rối loạn chức năng thượng thận
Chúng tôi không thể xác định bất kỳ dữ liệu đã công bố nào về phương pháp xác định, tỷ lệ mắc bệnh, kết cục hoặc hiệu quả điều trị suy thượng thận ở bệnh nhi sau khi ngừng tim. Suy thượng thận tương đối phổ biến sau khi ngừng tim ở người lớn và có liên quan đến khả năng sống sót đến khi xuất viện thấp.164,165 Trong một số loạt ca nhỏ ở người lớn, những người không sống sót (so với những người sống sót) có nồng độ hormone vỏ thượng thận và cortisol cao hơn và phản ứng kém hơn đối với kích thích hormone vỏ thượng thận trong quá trình 48 giờ đầu tiên sau ROSC.164,166–168 Trong một thử nghiệm ngẫu nhiên, mù đôi, đối chứng với giả dược dành cho người lớn, sử dụng hydrocortison liều stress trong trường hợp sốc sau ROSC không cải thiện kết cục sau ngừng tim, bao gồm thời gian đảo ngược sốc, kết cục thần kinh, và sống sót đến khi xuất viện.169 Thừa nhận chất lượng thấp của các bằng chứng đã công bố, các hướng dẫn gần đây của Hiệp hội Y học Chăm sóc Tích cực về tình trạng thiếu corticosteroid liên quan đến bệnh nặng ở người lớn đề xuất sử dụng corticosteroid sau khi ngừng tim ở người lớn. Khuyến cáo này phù hợp với khuyến nghị yếu hoặc có điều kiện.
Khoảng 30% trẻ em bị bệnh nặng có suy tuyến thượng thận tương đối, nhưng điều này chưa được đánh giá ở trẻ em được hồi sức sau khi ngừng tim.171 Mặc dù trẻ em bị bệnh nặng có suy tuyến thượng thận tương đối cần hỗ trợ thuốc vận mạch và truyền dịch nhiều hơn để duy trì huyết áp, một nghiên cứu tổng hợp gần đây -phân tích không chứng minh được sự khác biệt về kết cục giữa những người đã dùng và những người không dùng steroid ngoại sinh.172 Các hướng dẫn hiện tại về xử trí nhiễm trùng huyết ở trẻ em và trẻ sơ sinh khuyến cáo rằng nhân viên y tế nên cân nhắc sử dụng steroid nếu bệnh nhân có nguy cơ bị suy thượng thận với sốc kháng trị.
Không có đủ bằng chứng để hỗ trợ việc sử dụng corticosteroid thường xuyên sau khi ngừng tim. Bệnh nhân nên được điều trị theo khuyến nghị cho trẻ em bị bệnh nặng.
Xử trí suy thận
Dữ liệu mô tả tỷ lệ mắc và diễn biến lâm sàng của chấn thương thận cấp tính (acute kidney injury – AKI) sau ngừng tim ở trẻ em còn hạn chế. Trong một nghiên cứu hồi cứu gần đây trên 296 trẻ em trong PCAC, 37% mắc AKI, 11,5% mắc AKI nặng theo tiêu chí của Mạng lưới Tổ chức Chấn thương Thận Cấp tính và 6,4% cần RRT trong vòng 48 giờ sau ROSC.173 Các yếu tố nguy cơ đối với AKI nặng sau ngừng tim bao gồm bất thường creatinine ban đầu, không có tình trạng phổi mãn tính, vị trí ngừng tim trong bệnh viện, số liều epinephrine cao hơn trong khi ngừng tim và nhiễm toan nặng hơn sau ngừng tim.173 Trong thử nghiệm THAPCA-OH, 4,4% bệnh nhân cần RRT trong 5 ngày sau ROSC; RRT cần thiết thường xuyên hơn ở những bệnh nhân được điều trị bằng TTM ở nhiệt độ từ 36°C đến 37,5°C so với những bệnh nhân được điều trị bằng TTM ở nhiệt độ từ 32°C đến 34°C.3 Trong nghiên cứu THAPCA-IH, 24% bệnh nhân cần RRT, nhưng có không có sự khác biệt giữa các nhóm điều trị TTM.
AKI ở trẻ em bị bệnh nặng có liên quan đến tỷ lệ tử vong và bệnh tật gia tăng. Trẻ em bị AKI nặng được điều trị bằng RRT hoặc hỗ trợ vận mạch đã làm tăng đáng kể tỷ lệ tử vong.174 Đáng chú ý, các yếu tố nguy cơ đối với AKI sớm bao gồm ngừng tim trước khi nhập viện và pH huyết thanh <7,21, trong số các yếu tố dự đoán độc lập khác được xác định trong vòng 72 giờ sau khi nhập viện.
Trong suốt PCAC, điều quan trọng là theo dõi chức năng thận, bao gồm lượng nước tiểu và creatinine, vì bệnh nhân có nguy cơ phát triển AKI và RRT có thể được chỉ định. Nên thận trọng khi sử dụng thuốc gây độc cho thận và thuốc bài tiết qua thận, và có thể cần điều chỉnh liều. Nên theo dõi chặt chẽ nồng độ trong huyết thanh của các thuốc gây độc cho thận.
Tỷ lệ nhiễm trùng
Nhiễm trùng thường xảy ra sau khi ngừng tim ở trẻ em. Hầu hết các nghiên cứu báo cáo tỷ lệ nhiễm trùng trong thời gian trẻ tham gia PCAC được điều trị bằng liệu pháp hạ thân nhiệt với nhiệt độ <36°C hơn là những trẻ được điều trị bằng TTM từ 36°C đến 37,5°C.
Trong một tổng quan hệ thống về điều trị hạ thân nhiệt sau ngừng tim ở trẻ em (n=102), 27,5% trẻ em được điều trị bằng hạ thân nhiệt điều trị được chẩn đoán mắc viêm phổi sau ngừng tim và 9,8% được chẩn đoán nhiễm trùng huyết sau ngừng tim.
Trong các thử nghiệm THAPCA, nhiễm trùng trong vòng 7 ngày sau khi phân nhóm ngẫu nhiên được báo cáo là kết cục an toàn.2,3 Đối với IHCA, tỷ lệ nhiễm trùng được chứng minh bằng nuôi cấy không khác nhau giữa các bệnh nhân được điều trị bằng TTM ở nhiệt độ từ 32°C đến 34°C (tỷ lệ mắc bệnh, 27%) và những người được điều trị bằng TTM đến 36°C đến 37,5°C (tỷ lệ mắc bệnh, 29%). Tỷ lệ nhiễm trùng trong 100 ngày là 5,0 (KTC 95%, 3,7–6,5) trong nhóm TTM từ 32°C đến 34°C và 4,9 (KTC 95%, 3,7–6,4) trong nhóm TTM từ 36°C đến 37,5°C.2 Đối với OHCA, nhiễm trùng được chứng minh bằng nuôi cấy không khác nhau dựa trên phạm vi nhiệt độ TTM, xảy ra ở 46% bệnh nhân được điều trị bằng TTM đến 32° đến 34°C và 39% bệnh nhân được điều trị bằng TTM đến 36° C đến 37,5°. Tỷ lệ nhiễm trùng trong 100 ngày là 11,1 (KTC 95%, 9,2–13,4) ở nhóm được điều trị bằng TTM ở nhiệt độ từ 32°C đến 34°C và 9,9 (KTC 95%, 7,8–12,4) ở nhóm được điều trị bằng TTM để 36°C đến 37,5°C.
Trong một nghiên cứu hồi cứu tại một trung tâm về hạ thân nhiệt điều trị (33,5°C– 34,8°C) so với chăm sóc tiêu chuẩn sau khi ngừng tim ở trẻ em, 8,8% đối tượng có kết cục nuôi cấy dương tính vào ngày thứ 3 và 4 sau khi ngừng tim, được coi là đại diện cho nhiễm trùng bệnh viện mắc phải. Tuy nhiên, không có sự khác biệt về tỷ lệ nuôi cấy dương tính giữa bệnh nhân được điều trị hạ thân nhiệt và bệnh nhân được chăm sóc tiêu chuẩn.
Tỷ lệ nhiễm trùng sau ngừng tim tươngtự xảy ra ở trẻ em nhận ECPR.176 Dữ liệu từ cơ quan đăng ký ELSO (Tổ chức hỗ trợ sự sống ngoài cơ thể) từ năm 1998 đến 2008 đã ghi nhận tỷ lệ nhiễm trùng 10,8% trong khi điều trị bằng ECMO, tương đương với 22,8 ca nhiễm trùng trên 1000 ngày ECMO.
Theo dõi các dấu hiệu nhiễm trùng là rất quan trọng trong PCAC. Quyết định lấy mẫu cấy và bắt đầu sử dụng kháng sinh theo kinh nghiệm nên tuân theo các quy trình PICU tại địa phương.
Xử trí các bất thường về viêm và đông máu
Các con đường gây viêm được kích hoạt như một phần của PCAS, bao gồm các rối loạn của dòng thác đông máu. Tác động của việc ngăn chặn hoặc điều chỉnh các con đường này đã được nghiên cứu ở người lớn và trên mô hình động vật; chúng tôi xác định không có nghiên cứu nào cho đến nay liên quan đến trẻ sơ sinh hoặc trẻ em.
Các thử nghiệm ngẫu nhiên có đối chứng ở người lớn gần đây đã không chứng minh được bất kỳ tác dụng tích cực nào của hydrocortisone tiêm tĩnh mạch sau ngừng tim đúng lúc để đảo ngược sốc ở những bệnh nhân bị sốc phụ thuộc vào thuốc vận mạch,169 cyclosporine tiêm tĩnh mạch sau ngừng tim đối với suy đa cơ quan trong OHCA với nhịp không thể sốc điện,177 erythropoietin tiêm tĩnh mạch sau ngừng tim đối với kết cục thần kinh được cải thiện ở những người sống sót sau hôn mê của OHCA,178 hoặc sử dụng exenatide tương tự glucagon-like peptide-1 đối với nồng độ enolase đặc hiệu tế bào thần kinh trong huyết thanh (NSE; như một dấu hiệu của tổn thương thần kinh) ở bệnh nhân hôn mê trong 72 giờ đầu tiên sau khi nhập viện sau OHCA.
Một thử nghiệm ngẫu nhiên có kiểm soát mù đơn đa trung tâm gần đây ở người lớn sau IHCA đã so sánh tỷ lệ sống sót sau 28 ngày sau khi gói chăm sóc sau ngừng tim tiêu chuẩn có hoặc không có hoặc không có liệu trình Shenfu tiêm tĩnh mạch 14 ngày, một loại thuốc truyền thống của Trung Quốc có tác dụng chống viêm và chống chết tế bào tính chất.180 Thử nghiệm (n=978) đã chứng minh tỷ lệ sống sót sau 28 ngày tăng 12% (số cần điều trị, 8) vẫn tồn tại với phân tích đa biến. Mặc dù kết cục của nghiên cứu đơn lẻ này rất đáng khích lệ, nhưng cần phải xác nhận kết cục trong các nghiên cứu lớn hơn ở người lớn và trẻ em.
Nghiên cứu mở rộng trên động vật về việc ngăn chặn hoặc sửa đổi các con đường gây viêm đã mang lại kết cục đầy hứa hẹn. Tuy nhiên, cho đến nay, hầu hết các nỗ lực dịch tác phẩm này cho con người đều không thành công.
Bởi vì tình trạng viêm có thể làm thay đổi dòng chảy đông máu, các nhân viên y tế nên theo dõi các dấu hiệu chảy máu hoặc rối loạn đông máu; điều này đặc biệt quan trọng đối với những bệnh nhân được hỗ trợ ECMO. Tại thời điểm này, không có đủ bằng chứng để hỗ trợ các phương pháp điều trị cụ thể để điều chỉnh các quá trình gây viêm trong PCAC.
Phục hồi chức năng và hồi phục sau ngừng tim
Trẻ em sống sót sau ngừng tim có nguy cơ cao bị khuyết tật về thể chất, nhận thức và cảm xúc có thể ảnh hưởng đến chất lượng cuộc sống, chức năng gia đình, các hoạt động sinh hoạt hàng ngày, kết cục học tập và việc làm.181–184 Đánh giá bệnh nhân và gia đình theo chiều dọc và toàn diện không được thực hiện thường xuyên sau khi tim ngừng đập, mặc dù có nhiều bằng chứng cho thấy chúng là cần thiết.
Mặc dù một số đặc điểm của bệnh nhân, gia đình, sự kiện và chăm sóc tại bệnh viện liên quan đến kết cục sau OHCA ở trẻ em đã được hiểu rõ,13,18 có rất ít bằng chứng về các can thiệp cụ thể trong PCAC sẽ cải thiện kết cục chức năng của trẻ sau ngừng tim. Các nghiên cứu quan sát nhỏ về trẻ em sau khi bị bệnh hoặc chấn thương nghiêm trọng cho thấy rằng trẻ em bị chấn thương do thiếu oxy (anoxic injury) có khuyết tật nặng hơn và ít cải thiện hơn so với trẻ em bị chấn thương sọ não.
Không có đủ bằng chứng để hỗ trợ các biện pháp can thiệp phục hồi chức năng cụ thể hoặc thời điểm tối ưu để bắt đầu các biện pháp can thiệp đó. Tuy nhiên, trên cơ sở lợi ích của việc phục hồi chức năng cho bệnh nhân chấn thương sọ não và đột quỵ, các nhân viên y tế nên tham khảo ý kiến của các chuyên gia phục hồi chức năng trong vòng 72 giờ đầu tiên sau khi ngừng tim để điều chỉnh kế hoạch can thiệp phục hồi chức năng cho những người sống sót sau ngừng tim là điều hợp lý.
Có một nhu cầu quan trọng để xác định hiệu quả của các biện pháp can thiệp phục hồi chức năng cụ thể cho những bệnh nhi sống sót sau ngừng tim, thời điểm tốt nhất để bắt đầu điều trị phục hồi chức năng (nghĩa là sớm trong ICU so với sau khi xuất viện) và liều lượng của các biện pháp can thiệp cụ thể (ví dụ: vật lý trị liệu, liệu pháp nhận thức). Ngoài ra, cần có thêm thông tin để xác định thời điểm tối ưu cho việc đánh giá kết cục theo chiều dọc sau ngừng tim ở trẻ em và các công cụ tối ưu để sử dụng.
Tóm tắt
Nói chung, các dữ liệu này cho thấy rằng, tươngtự như nhiễm trùng huyết, một gói PCAC nhắm vào nhiều quá trình sinh lý, bao gồm hỗ trợ tuần hoàn và hỗ trợ oxygen hóa và thông khí, có thể hiệu quả hơn bất kỳ can thiệp đơn lẻ nào. PCAC có thể cần được điều chỉnh riêng cho từng bệnh nhân dựa trên độ tuổi của trẻ, nguyên nhân gây ngừng tim, bệnh đi kèm và giai đoạn của PCAS.187 Một cách tiếp cận tiêu chuẩn hóa như danh sách kiểm tra (Bảng 3) có thể giúp bác sĩ lâm sàng xác nhận rằng các lựa chọn điều trị quan trọng đã được giải quyết.
Bảng 3. Danh sách kiểm tra PCAC
| Oxygen hóa và thông khí | |
| · Đo oxygen hóa và mục tiêu oxy máu bình thường 94%–99% (hoặc độ bão hòa oxy bình | |
| thường/thích hợp của trẻ). | |
| · Tránh tình trạng thiếu oxy máu. | |
| · Đo PaCO2 và nhắm mục tiêu một giá trị phù hợp về mặt lâm sàng. | |
| · Tránh tình trạng giảm CO2 máu. | |
| Theo dõi huyết động | |
| · Đặt mục tiêu huyết động cụ thể trong PCAC và xem xét hàng ngày. | |
| · Sử dụng phương pháp đo tim từ xa. | |
| · Theo dõi huyết áp động mạch. | |
| · Theo dõi lactate huyết thanh, lượng nước tiểu và độ bão hòa oxy tĩnh mạch trungtâm | |
| để giúp hướng dẫn điều trị. | |
| · Sử dụng bolus dịch tiêm có hoặc không có thuốc tăng co bóp hoặc thuốc vận mạchđể | |
| duy trì huyết áp tâm thu lớn hơn phần trăm thứ năm theo tuổi và giới tính. | |
| TTM | |
| · Đo và theo dõi nhiệt độ lõi liên tục. | |
| · Phòng và điều trị sốt kịp thời. | |
| · Áp dụng TTM (32°C–34°C) trong 48 giờ và sau đó duy trì TTM (36°C–37,5°C) trong 3 | |
| ngày sau khi làm ấm lại hoặc áp dụng TTM (36°C–37,5°C) trong 5 ngày nếu bệnh nhân | |
| không phản hồi sau ROSC. | |
| · Ngăn chặn run rẩy. | |
| · Theo dõi huyết áp và điều trị hạ huyết áp trong quá trình sưởi ấm. | |
| · Phòng sốt sau khi ủ ấm. | |
| Giám sát thần kinh | |
| · Điều trị co giật lâm sàng. | |
| · Đảm bảo không sử dụng thường quy thuốc dự phòng co giật. | |
| · Xem xét hình ảnh não sớm để chẩn đoán các nguyên nhân gây ngừng tim có thể điều trị được. | |
| Kiểm soát đường huyết
· Đo đường huyết. · Tránh hạ đường huyết. |
|
| An thần
· Điều trị bằng thuốc an thần và giải lo âu. |
|
| Tiên lượng | |
| · Luôn xem xét nhiều phương thức (lâm sàng và khác) trên bất kỳ yếu tố tiên đoán nào. | |
| · Điện não đồ kết hợp với các yếu tố khác có thể hữu ích trong vòng 7 ngày đầu tiên của | |
| PCAS. | |
| · Hình ảnh thần kinh như MRI trong 7 ngày đầu tiên có thể có giá trị. | |
| · Hãy nhớ rằng các đánh giá có thể được sửa đổi bởi TTM hoặc hạ thân nhiệt gây ra. | |
| EEG chỉ điện não đồ; MRI, chụp cộng hưởng từ; PCAC, chăm sóc sau ngưng tim; PCAS, hội chứng sau ngừng tim; ROSC, sự trở lại của tuần hoàn bền vững; và TTM, xử trí nhiệt độ mục tiêu. | |
Tiên lượng sau ngưng tim
Các nghiên cứu quan sát về ngừng tim ở trẻ em đã xác định được nhiều yếu tố trước ngừng tim, trong ngừng tim và sau ngừng tim có liên quan đến kết cục thuận lợi hoặc không thuận lợi của bệnh nhân trong phân tích đơn biến. Tuy nhiên, danh sách các yếu tố liên quan đến sự khác biệt đáng kể trong kết cục trở nên ngắn hơn đáng kể khi các yếu tố này tiếp tục được phân tích hồi quy logistic đa biến. Ngay cả những biến số có liên quan chặt chẽ với kết cục cũng có khả năng tiên lượng hạn chế đối với từng bệnh nhân có khả năng mắc các yếu tố gây nhiễu không đo lường được. Các nhà cung cấp phải xem xét nhiều biến số khi cố gắng tiên lượng kết cục trong và sau khi ngừng tim. Mặc dù có những yếu tố liên quan đến kết cục tốt hơn hoặc tồi tệ hơn, nhưng không có yếu tố đơn lẻ nào được nghiên cứu dự đoán kết cục với độ chính xác đủ để khuyến nghị chấm dứt hoặc tiếp tục CPR hoặc để cho phép tiên lượng sau ROSC.58 Việc hiểu những yếu tố này có thể giúp các nhà cung cấp đánh giá và điều trị cho trẻ em trong PCAC và dự đoán một mức độ nghiêm trọng của bệnh tật và khả năng hồi phục của trẻ.
Các yếu tố trước khi bắt đầu liên quan đến kết cục
Một số điều kiện và phương pháp điều trị trước khi ngừng tim có liên quan độc lập với khả năng sống sót tồi tệ hơn khi xuất viện và kết cục thần kinh không thuận lợi sau khi ngừng tim ở trẻ em (Bảng 4). Kết cục tồi tệ hơn từ OHCA có liên quan đến việc giảm tuổi và một số nguyên nhân bị ngưng tim, bao gồm hội chứng đột tử ở trẻ sơ sinh194 và chấn thương do va chạm. Các yếu tố liên quan đến khả năng sống sót thấp hơn sau IHCA bao gồm tuổi lớn hơn21,189; sự hiện diện của các bệnh có sẵn từ trước các biện pháp can thiệp như đặt nội khí quản, thở máy, và sử dụng thuốc vận mạch tại thời điểm ngưng tim và các vụ ngưng tim xảy ra vào ca đêm và cuối tuần.
Bảng 4. Tóm tắt các yếu tố chính trước khi ngưng tim và trong khi ngưng tim có liên quan độc lập với kết cục
| Giai đoạn | Yếu tố | Loại kết cục | Sống sót | Nơi
ngưng tim |
| Trước ngưng tim | Tuổi nhỏ hơn: | |||
| Fink et al | Sống sót khi xuất viện | Giảm | OHCA | |
| Goto et al | Sống sót sau 1 tháng | |||
| Tuổi lớn hơn | Sống sót khi xuất viện | Giảm | IHCA | |
| Tình trạng bệnh nền:
Bệnh di truyền/chuyển hóa Nhiễm trùng huyết Suy gan Bệnh huyết học, ung thư, miễn dịch Bất thường thần kinh Bệnh tim bẩm sinh |
Sống sót khi xuất viện | Giảm | IHCA | |
| Bệnh phổi/đường thở có sẳn | Sống sót khi xuất viện | Tăng | OHCA | |
| Bệnh nhân hậu phẫu
Hậu phẫu tim |
Sống sót khi xuất viện | Tăng | IHCA | |
| Nơi can thiệp:
Đặt nội khí quản Truyền thuốc vận mạch |
Sống sót khi xuất viện | Giảm | IHCA | |
| Nguyên nhân ngưng tim: | ||||
| SIDS | Sống sót sau 1 năm | Giảm | OHCA | |
| Chấn thương | Sống sót khi xuất viện | Giảm | IHCA | |
| Chết đuối | Sống sót khi xuất viện | Tăng | OHCA | |
| Hen | Sống sót khi xuất viện | Tăng | IHCA | |
| Ngày và thời gian ngưng tim: | ||||
| Đêm | Sống sót khi xuất viện | Giảm | IHCA | |
| Đêm | Sống sót sau 1 tháng | Giảm | OHCA | |
| Cuối tuần: | ||||
| Meert et al | Sống sót sau 1 năm | Giảm | OHCA | |
| Kitamura et al | Sống sót sau 1 tháng | |||
| Phá rung nơi công cộng | Sống sót sau 1 tháng | Tăng | OHCA | |
| Thời gian đáp ứng EMS ngắn | Sống sót sau 1 tháng | Tăng | OHCA | |
| Trong lúc ngưng tim | Tình trạng chứng kiến: | |||
| Goto et al188 | Sống sót sau 1 tháng | Tăng | OHCA | |
| Fink et al13 | Sống sót khi xuất viện | |||
| Meert et al194 | Sống sót sau 1 năm | |||
| Andersen et al198 | Sống sót khi xuất viện | IHCA | ||
| Loại loạn nhịp VF/pVT: | ||||
| Tijssen et al12 | Sống sót khi xuất viện | Tăng | OHCA | |
| Kitamura et al199 | Sống sót sau 1 tháng | |||
| Goto et al200 | ||||
| Bắt đầu với VF/pVT vs không bắt đầu với VF/VT190,201:
PEA vs vô tâm thu198 Nhịp tim chậm190 |
Sống sót khi xuất viện | Tăng | IHCA | |
| PEA vs vô tâm thu188 | Sống sót khi xuất viện | Tăng | OHCA | |
| Vô tâm thu13
PEA12 |
Sống sót khi xuất viện | Giảm | OHCA | |
| VF/pVT tiếp theo vs VF/pVT nguyên phát191 VF/pVT tiếp theo vs không VF/pVT nguyên
phát 191 |
Sống sót khi xuất viện | Giảm | IHCA | |
| VF/pVT tiếp theo vs không VF/pVT duy trì188 | Sống sót thần kinh thuận
lợi sau 1 tháng |
Tăng | OHCA | |
| Thời gian ngắn bị sốc sau khi VF/VT188 | Sống sót thần kinh thuận
lợi sau 1 tháng |
Tăng | OHCA | |
| CPR với thông khí vs CPR chỉ ép ngực đơn thuần: | ||||
| Nhũ nhi202 | Sống sót khi xuất viện | Tăng | OHCA | |
| Trẻ >1 tuổi202,203 | Sống sót thần kinh thuận
lợi sau 1 tháng hoặc sống sót khi xuất viện |
Không khác biệt | ||
| CPR bởi người qua đường200 | Sống sót sau 1 tháng | Tăng | OHCA | |
| CPR được hỗ trợ bởi điều phối viên200 | Sống sót sau 1 tháng | Tăng | OHCA | |
| Dùng epinephrine ít lần hơn204 | Sống sót khi xuất viện | Tăng | IHCA | |
| Thời gian ngắn dùng epinephrine198 | Sống sót khi xuất viện | Tăng | IHCA | |
| Sử dụng ECPR190 | Sống sót khi xuất viện | Tăng | IHCA | |
| Thời gian EMS ngắn hơn12 | Sống sót khi xuất viện | Tăng | OHCA | |
| Huyết áp tâm trương ≥25 mm Hg ở nhũ nhi,
≥30 mm Hg ở trẻ em trong thời gian CPR205 |
Sống sót khi xuất viện | Tăng | IHCA | |
| AHA-compliant CPR depth (>1 y) ≥51 mm206 | Sống sót khi xuất viện | Tăng | IHCA | |
| Thuốc dùng khi CPR: Calcium87,152
Sodium bicarbonate152,190 Epinephrine190 Atropine18 Epinephrine18,188 |
Sống sót khi xuất viện | Giảm | IHCA | |
| Thời gian CPR dài hơn | ||||
| Goto188 | Sống sót sau 1 tháng | Giảm | OHCA | |
| López-Herce et al207 | Sống sót sau 1 năm | OHCA | ||
| Meert et al194 | ||||
| Del Castillo et al192 | Sống sót khi xuất viện | IHCA | ||
| Matos et al193 | ||||
| Đặt NKQ trong thời gian CPR208 | Sống sót khi xuất viện | Giảm | IHCA | |
AHA, Hiệp hội Tim mạch Hoa Kỳ; CPR, hồi sức tim phổi; ECPR, hồi sức ngoài cơ thể (sử dụng tuần hoàn ngoài cơ thể trong quá trình hồi sức); EMS, dịch vụ y tế khẩn cấp; IHCA, ngừng tim trong bệnh viện; OHCA, ngừng tim ngoài bệnh viện; PEA, hoạt động điện vô mạch; SIDS, hội chứng đột tử ở trẻ sơ sinh; VF/pVT, rung thất/nhịp nhanh thất vô mạch; và VF/VT, rung thất/nhịp nhanh thất.
*Khi một loạt các ấn phẩm nghiên cứu các yếu tố tiên lượng được lấy từ một cơ quan đăng ký duy nhất, ấn phẩm gần đây nhất từ cơ quan đăng ký đó được trích dẫn trong bảng này.
Nhịp ngưng tim ban đầu liên quan đến kết cục
Đối với cả OHCA và IHCA nhịp ngừng ban đầu của nhịp tim chậm190 và rung thất/nhịp nhanh thất vô mạch có liên quan đến khả năng sống sót cao hơn. Đối với IHCA và OHCA hoạt động điện vô mạch cũng liên quan đến khả năng sống sót cao hơn so với vô tâm thu.
Các yếu tố ngưng tim nội bộ liên quan đến kết cục
Nhiều yếu tố trong lúc ngưng tim có liên quan đến kết cục tốt hơn của bệnh nhân sau OHCA, bao gồm cả việc ngưng tim có người chứng kiến,13,188 CPR của người ngoài cuộc,200 và liều epinephrine ít thường xuyên hơn.204 Kết cục tốt hơn của bệnh nhân từ IHCA có liên quan đến thời gian sử dụng epinephrine ngắn hơn,198 sử dụng ECPR,190 tuân thủ độ sâu ép ngực khi CPR của AHA,206 và huyết áp tâm trương >25 mm Hg ở trẻ sơ sinh và >30 mm Hg ở trẻ em.
Đánh giá sau ngừng tim và các yếu tố liên quan đến kết cục
Các kết cục đánh giá sau ngừng tim và các yếu tố liên quan đến kết cục và vai trò của chúng trong tiên lượng thần kinh được mô tả trong các phần sau.
Khám thần kinh lâm sàng
Tiên lượng sau ngừng tim bằng khám thần kinh ở trẻ em phải xem xét giai đoạn phát triển của trẻ và có thể phức tạp do sử dụng thuốc (tức là thuốc an thần, thuốc giảm đau và thuốc NMB) và do các trạng thái sinh lý bệnh như hạ huyết áp và bất thường chuyển hóa nghiêm trọng. Có rất ít bằng chứng chất lượng cao để hỗ trợ việc sử dụng các phát hiện khám thần kinh bất thường để tiên lượng sau ngừng tim ở trẻ em. Trong một nghiên cứu đoàn hệ tương lai nhỏ gồm 57 trẻ liên tiếp bị tổn thương do thiếu máu cục bộ do thiếu oxy, trong đó có 44 trẻ bị ngừng tim, 3 đặc điểm có giá trị tiên đoán dương tính 100% về kết cục bất lợi: thang điểm Hôn mê Glasgow <5, không có hoạt động hô hấp tự phát và không có phản xạ đồng tử trong 24 giờ sau ROSC.209 Một nghiên cứu nhi khoa nhỏ về kết cục sau chấn thương hoặc chấn thương não cấp tính bao gồm 36 trẻ em sau khi ngừng tim. Độ nhạy và độ đặc hiệu đối với kết cục không thuận lợi (nghĩa là khuyết tật nghiêm trọng theo Thang điểm kết cục của Glasgow hoặc tử vong sau 5 năm kể từ khi bị thương) lần lượt là 93% và 50% đối với trường hợp không có đáp ứng vận động và 47% và 100% đối với trường hợp không có phản xạ đồng tử.
Trong một nghiên cứu nhỏ ở một trung tâm về IHCA và OHCA ở trẻ em được điều trị bằng phương pháp hạ thân nhiệt điều trị, việc không có đáp ứng vận động và đồng tử trong quá trình hạ thân nhiệt điều trị không dự đoán được kết cục bất lợi (Danh mục Hiệu suất Não ở Trẻ em [PCPC] 4–6) khi xuất viện, nhưng nếu không có vào giờ thứ 24 sau khi phục hồi nhiệt độ bình thường, họ dự đoán kết cục không thuận lợi khi xuất viện.211 Trong 2 nghiên cứu đoàn hệ đa trung tâm về OHCA và IHCA ở trẻ em, sự hiện diện của phản xạ đồng tử hai bên vào lúc 12 giờ sau khi hồi sức có liên quan độc lập với tỷ lệ tử vong thấp hơn khi xuất viện, mặc dù kết cục thần kinh không được đánh giá.
Đối với người lớn hôn mê sau khi ngừng tim, bản cập nhật hướng dẫn hỗ trợ sự sống tim nâng cao năm 2015 của AHA khuyến nghị rằng thời gian sớm nhất để tiên lượng kết cục thần kinh bất lợi bằng cách sử dụng khám lâm sàng ở bệnh nhân không được điều trị bằng TTM là 72 giờ sau khi ngừng tim. Các khuyến nghị lưu ý rằng thời gian cho đến khi tiên lượng có thể còn lâu hơn nếu tác dụng còn lại của thuốc an thần hoặc NMB gây khó khăn cho việc khám lâm sàng. Đối với bệnh nhân người lớn được điều trị bằng TTM, bản cập nhật hướng dẫn hỗ trợ sự sống cho tim nâng cao năm 2015 của AHA lưu ý rằng khi khám lâm sàng được sử dụng trong đó thuốc an thần hoặc liệt cơ có thể là yếu tố gây nhiễu, thời gian tiên lượng có thể là 72 giờ sau khi thân nhiệt trở lại bình thường. Bản cập nhật hướng dẫn hỗ trợ sự sống tim nâng cao năm 2015 của AHA lưu ý rằng thời gian hoạt động thường là 4,5 đến 5 ngày sau ROSC đối với bệnh nhân được điều trị bằng TTM.
Do không có dữ liệu triển vọng về độ tin cậy và thời điểm tối ưu của khám lâm sàng để tiên lượng thần kinh ở trẻ em sau ngừng tim, các nghiên cứu dành cho người lớn đã được xem xét. Phép ngoại suy từ dữ liệu người lớn và từ dữ liệu trẻ em tối thiểu hiện có cho thấy cần thận trọng khi diễn giải kết cục khám thần kinh lâm sàng sớm sau ngừng tim. Độ tin cậy của kiểm tra thần kinh lâm sàng trong việc dự đoán kết cục thần kinh được cải thiện khi sử dụng các kiểm tra nối tiếp và với thời gian trôi qua sau khi ngừng tim. Đối với trẻ em được điều trị bằng phương pháp hạ thân nhiệt, thời gian giữ nhiệt độ bình thường (sau khi làm ấm lại) cần thiết để cho phép diễn giải các kết cục lâm sàng một cách đáng tin cậy vẫn chưa được thiết lập.
Do những hạn chế của việc kiểm tra thần kinh ở trẻ em sau khi ngừng tim, hỗ trợ các xét nghiệm sinh lý thần kinh (ví dụ: điện não đồ, điện thế gợi lên [EPs], CBF và tự điều hòa,64,213–215 hình ảnh thần kinh,61,216 và dấu ấn sinh học huyết tương [nghĩa là protein đặc hiệu của não217–220]) đang được nghiên cứu tích cực trong nỗ lực cải thiện khả năng tiên lượng. Các bài kiểm tra thần kinh này được trình bày chi tiết trong các phần sau.
Xét nghiệm sinh lý thần kinh
Điện não đồ
Điện não đồ cung cấp dữ liệu khách quan về chức năng não và thường được sử dụng để đánh giá bệnh não và phân loại mức độ nghiêm trọng của chấn thương não ở trẻ em sau ngừng tim. Dữ liệu điện não đồ có thể được thu thập không xâm lấn tại giường bệnh và có thể được đánh giá liên tục hoặc theo các khoảng thời gian lặp đi lặp lại. Các đặc điểm cơ bản về điện não đồ chính ở trẻ em sau khi ngừng tim có sự đồng thuận đáng kể giữa các bên hoặc tốt hơn khi được giải thích bởi các nhà ghi điện não đồ nhi khoa được đào tạo.137,221 Tuy nhiên, cần có chuyên môn kỹ thuật để có được bản ghi điện não đồ chất lượng cao và kiến thức về tình trạng lâm sàng của bệnh nhân là điều cần thiết để đảm bảo rằng những thay đổi trên điện não đồ không phải do thuốc gây ra, liên quan đến hạ thân nhiệt đáng kể, hoặc do phù nề da đầu hoặc tích tụ dịch ngoài trục.150 Hơn nữa, không có đặc điểm điện não đồ nào có giá trị tiên đoán hoàn hảo cho các kết cục bất lợi và không có đặc điểm nào được đánh giá với thời gian lấy bệnh nhân làm trung tâm lâu hơn kết cục hành vi thần kinh, vì vậy điều quan trọng là phải xem xét các phát hiện điện não đồ trong bối cảnh lâm sàng tổng thể.
Trẻ em có nền điện não đồ bất thường nghiêm trọng hơn sau khi ngừng tim có xu hướng có kết cục tồi tệ hơn so với bệnh nhân chỉ có nền bất thường nhẹ hoặc trung bình. Một nghiên cứu đơn trung tâm đã đánh giá nền điện não đồ trong 24 giờ đầu sau khi tim ngừng đập ở 128 trẻ không được điều trị bằng liệu pháp hạ thân nhiệt.134 Nền điện não đồ được phân loại (từ bình thường đến xấu nhất) là bình thường, hoạt động sóng chậm không tổ chức (slow-disorganized), ức chế không liên tục hoặc bùng phát (discontinuous or burst- suppression), hoặc không có đặc tính sụt giảm (attenuated-featureless). Sau khi kiểm soát các biến đồng thời lâm sàng, đối với mỗi điểm số cơ bản tăng dần, tỷ lệ tử vong là 3,6 và tỷ lệ kết cục thần kinh không thuận lợi khi xuất viện là 4,4. Trong một nghiên cứu đơn trung tâm khác trên 73 trẻ em sau khi ngừng tim, bao gồm một số trẻ được điều trị bằng liệu pháp hạ thân nhiệt, hoạt động điện não đồ nền liên tục trong vòng 12 giờ sau ROSC có liên quan đến kết cục thần kinh thuận lợi khi xuất viện.149 Trong một nghiên cứu đơn trung tâm thứ ba về 34 trẻ sau khi ngừng tim, sự hiện diện của các trục ngủ (sleep spindles) trên điện não đồ ban đầu sau 24 giờ, dù bình thường hay bất thường về hình thái, có liên quan đến kết cục thuận lợi sau 6 tháng. Các trục ngủ không xuất hiện cho đến trung bình 12 giờ sau khi ngừng tim, cho thấy rằng có thể cần phải đánh giá một thời gian dài, thay vì điện não đồ ngắn, để đánh giá các trục ngủ.
Một nghiên cứu trên 35 trẻ em được điều trị bằng liệu pháp hạ thân nhiệt sau khi ngừng tim cho thấy rằng trong các giai đoạn hạ thân nhiệt và bình thường hóa thân nhiệt, các đường biểu diễn điện não đồ không phản ứng, ức chế không liên tục hoặc bùng phát hoặc thiếu hoạt động não rõ ràng có liên quan đến kết cục thần kinh tổng thể không thuận lợi khi xuất viện.223 Tương tự như vậy, một nghiên cứu đơn trung tâm trên 34 trẻ em sau khi ngừng tim có điện não đồ thu được trên lâm sàng vào các thời điểm khác nhau sau khi ROSC phát hiện ra rằng các mẫu điện não đồ không liên tục và đẳng điện có giá trị tiên đoán dương tính 90% đối với kết cục thần kinh không thuận lợi, trong khi giá trị tiên đoán âm tính của điện não đồ bình thường liên tục – Điện não đồ cho kết cục thần kinh không thuận lợi là 91%.
Ở nhiệt độ cực thấp được sử dụng trong trường hợp ngừng tuần hoàn do hạ thân nhiệt sâu, điện não đồ có thể phát triển dạng không liên tục và sau đó là đẳng điện.225–227 Mặc dù những bất thường nghiêm trọng này trên điện não đồ không được nhìn thấy khi hạ thân nhiệt điều trị xuống nhiệt độ thấp tới 33°C, nhưng các dạng điện não đồ đôi khi đã phát triển trong quá trình điều trị hạ thân nhiệt135,228 do hậu quả của chấn thương não tiến triển, điều chỉnh nhiệt độ hoặc điều chỉnh thuốc an thần. Các nghiên cứu gần đây đã chứng minh rằng các mẫu điện não đồ được thấy trong quá trình hạ thân nhiệt điều trị (32°C–34°C) có cùng ý nghĩa tiên lượng như những mẫu được thấy trong quá trình thân nhiệt bình thường.
Các nghiên cứu cũ hơn và nhỏ hơn đã báo cáo rằng ức chế bùng phát, gián đoạn quá mức, suy giảm nghiêm trọng, thiếu phản ứng và phóng điện dạng động kinh tổng quát209 có liên quan đến tiên lượng không thuận lợi. Ngược lại, cải thiện điện não đồ nhanh chóng, khả năng phản ứng và kiểu ngủ bình thường có liên quan đến tiên lượng thuận lợi.
Mặc dù hôn mê alpha thường được coi là có liên quan đến bệnh não thiếu oxy và tiên lượng không thuận lợi, nhưng đây là một dạng không đặc hiệu có thể xảy ra với nhiều bệnh sinh khác nhau và kết cục có lẽ chủ yếu phụ thuộc vào cơ chế bệnh sinh. Hôn mê alpha phản ứng với kích thích có thể cho thấy tiên lượng thuận lợi hơn.
Các nghiên cứu trong tương lai là cần thiết với đánh giá điện não đồ chuẩn hóa từ các nhóm trẻ em liên tiếp để xác định các mẫu điện não đồ hoặc sự kết hợp của các mẫu dự đoán không chỉ kết cục thần kinh tổng thể ngắn hạn mà còn cả kết cục hành vi thần kinh dài hạn lấy bệnh nhân làm trung tâm.
Bản cập nhật hướng dẫn AHA PALS năm 2015 khuyến nghị rằng điện não đồ được thực hiện trong vòng 7 ngày đầu tiên sau khi ngừng tim ở trẻ em có thể được xem xét để tiên lượng kết cục thần kinh tại thời điểm xuất viện nhưng không nên được sử dụng làm tiêu chí duy nhất.
Điện thế gợi lên (Evoked Potentials)
Việc sử dụng EP để tiên lượng thần kinh rất hấp dẫn vì chúng có thể được thực hiện ngay tại giường bệnh, không bị ảnh hưởng bởi thuốc an thần hoặc hạ thân nhiệt và có thể được đánh giá tại các thời điểm lặp lại. EP được sử dụng phổ biến nhất là EP somatosensory (SSEP). SSEP kiểm tra tính toàn vẹn của dây thần kinh ngoại vi (dây thần kinh giữa), tủy sống, thân não và vỏ não (sóng N20). Tuy nhiên, để tránh kết luận sai rằng không có sóng N20 là do chấn thương não nghiêm trọng, điều quan trọng là phải xem xét các tổn thương trước sóng N20 có thể làm giảm dẫn truyền SSEP và các tổn thương ngoài trục có thể làm giảm khả năng ghi lại sóng N20. Mặc dù sự vắng mặt hai bên của dạng sóng N20 ở những người lớn sống sót sau ngừng tim trong tình trạng hôn mê vào ngày thứ 3 thường dự đoán kết cục bất lợi,236 có rất ít thông tin ở trẻ em sau khi ngừng tim. Một nghiên cứu trên 42 trẻ em bị bệnh não do thiếu oxy-thiếu máu cục bộ hôn mê trong 24 giờ sau khi nhập viện PICU với tiên lượng không rõ ràng cho thấy rằng việc không có sóng N20 ở cả hai bên có giá trị tiên đoán dương tính 100% đối với kết cục bất lợi.209 Phát hiện này phù hợp với loạt trường hợp trẻ nhỏ hơn, lớn hơn. Các nghiên cứu bao gồm các quần thể có bệnh sinh không đồng nhất hơn (không chỉ trẻ em mắc bệnh não do thiếu oxy- thiếu máu cục bộ) cho thấy những phát hiện tương tự nhưng với độ nhạy và độ đặc hiệu thấp hơn một chút. Những nghiên cứu này mô tả một số trẻ em không có sóng N20 đã có kết cục thuận lợi, đặc biệt khi SSEP được dùng trong 24 giờ đầu sau khi ngừng tim, cho thấy rằng SSEP phải được xem xét trong bối cảnh lâm sàng tổng thể. Ngoài ra, các nghiên cứu chưa đánh giá SSEP ở trẻ em được điều trị bằng hạ thân nhiệt. Ở người lớn, 2 phân tích tổng hợp cho thấy độ tin cậy của SSEP là như nhau đối với những bệnh nhân được điều trị có hoặc không có hạ thân nhiệt, với tỷ lệ dương tính giả tương tự như báo cáo của Viện Hàn lâm Thần kinh Hoa Kỳ trước khi sử dụng hạ thân nhiệt. Thời điểm tối ưu để có được SSEP liên quan đến hạ thân nhiệt điều trị là không chắc chắn.
Vai trò của EP thính giác thân não (brainstem auditory EPs – BAEP) và EP thị giác thậm chí còn chưa rõ ràng. Vì BAEP sử dụng kích thích thính giác để đánh giá thân não nên chúng có thể thiếu tiện ích trong việc dự đoán kết cục nhận thức thần kinh, vốn chủ yếu dựa trên chức năng vỏ não. Các nghiên cứu nhỏ cũ hơn và loạt trường hợp đánh giá BAEP trong các nhóm không đồng nhất đã chứng minh rằng BAEP bất thường có liên quan không nhất quán với kết cục không thuận lợi, rằng BAEP bình thường không phải lúc nào cũng liên quan đến kết cục thuận lợi và đôi khi các phản ứng không có mặt ban đầu quay trở lại.238,241,242 Tương tự, các nghiên cứu nhỏ cũ hơn và loạt trường hợp đánh giá các EP thị giác trong các nhóm thuần tập không đồng nhất đã chứng minh rằng các EP thị giác bất thường liên quan một cách nhất quán với các kết cục bất lợi và các EP thị giác bình thường không phải lúc nào cũng liên quan đến các kết cục thuận lợi.
Không có đủ bằng chứng để hỗ trợ việc sử dụng EP thường xuyên để tiên lượng thần kinh sau khi ngừng tim ở trẻ em.
Hình ảnh thần kinh
Hình ảnh thần kinh sau khi ngừng tim có thể được thực hiện để làm sáng tỏ nguyên nhân ngừng tim và để hiểu rõ hơn tác động tiềm ẩn của nó đối với kết cục chức năng của trẻ. Cả chụp cắt lớp vi tính (computed tomography – CT) não và chụp cộng hưởng từ (magnetic resonance imaging – MRI) đều có thể đóng vai trò là công cụ chẩn đoán hoặc tiên lượng trong PCAC để đưa ra quyết định lâm sàng.
Chẩn đoán hình ảnh thần kinh
Chẩn đoán hình ảnh thần kinh thường được xem xét sau ROSC đối với trẻ chưa trở lại trạng thái thần kinh ban đầu, khi khám thần kinh bị nhầm lẫn bởi thuốc an thần hoặc NMB, khi nguyên nhân ngừng tim không rõ ràng hoặc khi trẻ có biểu hiện rối loạn thần kinh khu trú. Chụp CT não có thể được thực hiện nhanh chóng và trong một số ICU, máy di động đầu giường có thể được sử dụng cho những bệnh nhân không ổn định. Hình ảnh não thu được sớm sau ROSC (nghĩa là <24 giờ sau ROSC) có thể hỗ trợ xác định các yếu tố góp phần tiềm tàng dẫn đến ngừng tim—chẳng hạn như đột quỵ xuất huyết,246 chấn thương,247 khối u,248 hoặc não úng thủy—và do đó hướng dẫn các biện pháp can thiệp điều trị.249 Hình ảnh cổ hoặc cột sống có thể xác định tổn thương liên quan đến chấn thương (ví dụ: tổn thương hoặc chấn thương liên quan đến tác động hoặc bạo lực),250 đuối nước,251 và treo cổ.
Hình ảnh thần kinh để tiên lượng
Chụp cắt lớp vi tính
CT không cản quang không phải là một xét nghiệm nhạy cảm sớm (<12 giờ sau ROSC) sau thiếu máu cục bộ nhẹ nhưng thường có thể xác định phù não nặng hơn.250,253–255 Một mẫu thuận tiện hồi cứu gồm 78 trẻ mắc OHCA đã trải qua CT không cản quang trong vòng 24 giờ sau ROSC61 đã phát hiện ra rằng 40% mất biệt hóa chất xám – trắng, 27% xóa rãnh, 18% xóa bể đáy, 13% có dấu hiệu đảo ngược và không có bệnh nhân nào có lệch đường giữa. Những dấu hiệu này có nhiều khả năng xuất hiện ở những trẻ trải qua thời gian hồi sức tim phổi lâu hơn (≥20 phút). Trong nghiên cứu này, CT não bình thường (36%) có liên quan đến tỷ lệ sống sót (độ nhạy, 62%; độ đặc hiệu, 90%) và kết cục thần kinh thuận lợi. Sự hiện diện của ≥1 bất thường trên CT não có liên quan đến tỷ lệ tử vong cao hơn và kết cục thần kinh không thuận lợi.61 Tương tự, Rafaat và cộng sự62 phát hiện ra rằng sự hiện diện của các tổn thương không do chấn thương trên CT não (28 trong số 156 trẻ em) trong vòng 24 giờ sau ROSC sau khi chết đuối ở bệnh nhân nhi bị ngừng tim có liên quan đến thang điểm Hôn mê Glasgow là 3 và tử vong. Sau khi ngừng tim liên quan đến đuối nước, những đứa trẻ có CT não bình thường ban đầu và sau đó (sau hơn 24 giờ) có CT não bất thường có kết cục xấu.
Bằng chứng được công bố là không đủ để xác định thời điểm thích hợp nhất để chụp CT và liệu CT não trong 24 giờ đầu tiên sau khi ngừng tim có hữu ích để tiên lượng kết cục thần kinh thuận lợi hay không.
Chụp cộng hưởng từ
Chụp cộng hưởng từ não đang được sử dụng sau khi tim ngừng đập để thu thập dữ liệu bổ sung nhằm đưa vào tiên lượng bệnh nhân và lập kế hoạch cho các nhu cầu chăm sóc trong tương lai. MRI có độ chính xác vượt trội so với chụp CT trong việc đánh giá mức độ nghiêm trọng của tổn thương vùng do tổn thương do thiếu máu cục bộ do thiếu oxy. Các chuỗi hình ảnh thông thường (T1, T2) và hình ảnh khuếch tán (DWI) phần lớn là tiêu chuẩn tại các trung tâm y tế và là kỹ thuật hình ảnh được báo cáo thường xuyên nhất. Các trình tự DWI dựa vào sự hạn chế chuyển động của phân tử nước, do phù gây độc tế bào hoặc phù mạch.256 Khoảng thời gian giữa ngừng tim và chụp cộng hưởng từ ảnh hưởng đến việc giải thích vì các tổn thương có quỹ đạo thời gian điển hình để xuất hiện và giải quyết sau khi bị tổn thương.257 Các trình tự khác nhau cung cấp các thông số khác nhau thông tin tại các thời điểm cụ thể sau chấn thương.
Hai nghiên cứu đơn trung tâm đặc trưng cho MRI (1,5 T) sau khi ngừng tim ở trẻ em chứng minh tiềm năng ứng dụng của nó trong tiên lượng sau ngừng tim. Trong một báo cáo của Fink và cộng sự216 (n=28 trẻ em), những bất thường được phát hiện ở hạch nền trên hình ảnh thông thường và ở các thùy não với DWI trong 2 tuần đầu tiên sau khi ngừng tim có liên quan đến kết cục không thuận lợi. Tương tự như vậy, trong một loạt 23 trẻ em, tổn thương DWI ở vỏ não và hạch nền trong tuần đầu tiên sau khi ngừng tim có liên quan đến kết cục không thuận lợi.258 Vì MRI tăng độ nhạy so với CT trong việc phát hiện những bất thường do thiếu oxy-thiếu máu cục bộ gây ra, sự hiện diện của tổn thương trên MRI có liên quan đến kết cục không thuận lợi, nhưng một số trẻ em có tổn thương vùng lại có kết cục thuận lợi. Một nghiên cứu trên 14 trẻ em được đưa vào bệnh viện nhi cấp ba sau khi ngừng tim đã kiểm tra mối quan hệ giữa CBF và kết cục thần kinh bằng cách sử dụng MRI não bao gồm ghi nhãn vòng quay động mạch được thực hiện trong vòng 2 tuần sau khi ngừng tim. Trong nghiên cứu này, CBF và hệ số khuếch tán biểu kiến được tính toán trên toàn cục và ở 19 vùng não. Hệ số khuếch tán rõ ràng toàn cầu đã giảm đáng kể ở trẻ em có kết cục không thuận lợi. Sự kết hợp giữa tăng CBF và giảm hệ số khuếch tán rõ ràng trong cùng một vùng não có liên quan đến kết cục tồi tệ hơn, ngụ ý mối quan hệ giữa hạn chế khuếch tán nước và CBF.
Quang phổ cộng hưởng từ proton ([1]H) là một chuỗi MRI có thể định lượng một số chất chuyển hóa của tế bào ở cấp độ toàn cầu hoặc khu vực.259 Ashwal và cộng sự260 nhận thấy rằng việc tăng lactate não và giảm nồng độ N- acetylaspartate trong não có liên quan đến kết cục tồi tệ hơn sau khi chấn thương não trẻ em, bao gồm cả ngừng tim. Hiệu suất và giải thích kết cục quang phổ cộng hưởng từ yêu cầu chuyên môn và giao thức đặc biệt. Bằng chứng được công bố hiện có là không đủ để xác định các đặc điểm quang phổ cộng hưởng từ làm cơ sở tiên lượng và không có dữ liệu triển vọng nào được công bố để xác định tiện ích của nó trong tiên lượng sau khi ngừng tim ở trẻ em.
Có một số yếu tố hậu cần tiềm ẩn và nguy cơ cần xem xét khi xác định tiện ích lâm sàng của các kỹ thuật hình ảnh. CT liên quan đến việc tiếp xúc với bức xạ, mặc dù các phác đồ giảm liều ngày càng có sẵn. MRI thường liên quan đến việc tiếp xúc với các nguy cơ của thuốc an thần. Cả CT và MRI đều có thể liên quan đến nguy cơ vận chuyển trong bệnh viện. Các giao thức an toàn nên được sử dụng để đảm bảo rằng cấy ghép và các chống chỉ định khác được xem xét.
Các nghiên cứu được trình bày ở đây bị giới hạn bởi thiết kế của chúng (nghĩa là hồi cứu) và có thể bị sai lệch lựa chọn do các bác sĩ lâm sàng đưa ra, những người đã chỉ định xét nghiệm ở những bệnh nhân đáng lo ngại về mặt lâm sàng nhưng có lẽ là an toàn để xét nghiệm. Các nghiên cứu cũng bị hạn chế do thiếu mù trong giải thích hình ảnh và đánh giá kết cục. Cần nhiều công việc hơn để tối ưu hóa việc sử dụng các trình tự MRI khác nhau để tiên lượng sau khi ngừng tim, để xác định thời điểm chụp MRI lý tưởng sau ROSC, để xác thực dữ liệu nghiên cứu nhỏ trong các nhóm lớn hơn và để xác định liệu có tiện ích trong thử nghiệm lặp lại hay không.
CT não là một xét nghiệm chẩn đoán hữu ích sớm sau ROSC để xác định các nguyên nhân nội sọ có khả năng điều trị được của ngừng tim. Không có đủ dữ liệu để hỗ trợ việc sử dụng sớm CT để tiên lượng thần kinh. MRI não sử dụng hình ảnh thông thường và DWI trong 3 đến 7 ngày đầu tiên sau ROSC có thể hữu ích để bổ sung cho đánh giá lâm sàng, bao gồm khám thần kinh nhiều lần, điện não đồ và trong một số trường hợp, SSEP. Cùng với nhau, những phương thức này có thể được sử dụng để tiên lượng cho phổ phục hồi thần kinh.
Dấu ấn sinh học
Dấu ấn sinh học có thể được lấy mẫu từ máu sớm sau khi ngừng tim với mục tiêu tiên lượng tử vong và kết cục thần kinh. Nồng độ của các dấu ấn sinh học dựa trên não phản ánh tác động của tình trạng thiếu oxy và thiếu máu cục bộ đối với tế bào thần kinh, tế bào thần kinh đệm và tế bào hình sao. Nồng độ của chúng có thể được đo từ máu sau khi vận chuyển qua hàng rào máu não. Các dấu ấn sinh học khác được đo trong huyết thanh như lactate có thể phản ánh tổn thương toàn thân.261 Một số dấu ấn sinh học não (ví dụ: protein axit fibrillary thần kinh đệm, ubiquitin carboxy- terminal hydrolase L1) dành riêng cho não hơn các dấu ấn khác (ví dụ: S100B, NSE). NSE là một enzyme đường phân được giải phóng từ tế bào chất của tế bào thần kinh. Trong các nghiên cứu nhỏ về ngừng tim ở trẻ em, nồng độ NSE cao hơn từ 24 đến 96 giờ sau khi ngừng tim có liên quan đến tỷ lệ tử vong hoặc kết cục thần kinh không thuận lợi.218,220,262 Nồng độ NSE có thể vẫn tăng trong nhiều tuần đến nhiều tháng sau chấn thương não nghiêm trọng.263 S100B là một protein liên kết với canxi được tìm thấy trong các tế bào astroglia và Schwann. Các nghiên cứu ở trẻ em sau khi ngừng tim cho thấy kết cục không nhất quán. Trong một nghiên cứu đơn trung tâm, nồng độ cao hơn ở 48 và 72 giờ sau khi ngừng tim có liên quan đến kết cục thần kinh không thuận lợi sau 6 tháng,218 và nồng độ cao hơn ở 48, 72 và 96 giờ sau khi ngừng tim chỉ liên quan đến tử vong khi xuất viện trong một nghiên cứu khác.220 Giá trị NSE và S100B có thể bị ảnh hưởng bởi hạ thân nhiệt điều trị và nồng độ trong huyết thanh của chúng nên được giải thích một cách thận trọng.
Protein axit fibrillary thần kinh đệm là một sợi thần kinh được tìm thấy trong tế bào hình sao. Trong 1 nghiên cứu nhi khoa, nồng độ protein axit sợi thần kinh đệm sớm (tức là 10 giờ sau khi ngừng tim) không dự đoán được kết cục, trong khi nồng độ cao hơn sau đó (tức là 60 giờ sau khi ngừng tim) có liên quan đáng kể đến kết cục thần kinh bất lợi.217 Protein cơ bản của myelin hiện diện trong vỏ myelin bao quanh sợi trục. Nồng độ protein cơ bản myelin tăng cao có thể biểu hiện tổn thương sợi trục và có liên quan đến tỷ lệ tử vong và kết cục thần kinh không thuận lợi sau khi ngừng tim ở trẻ em.218 Ubiquitin carboxyterminal hydrolase L1 là enzyme khử phổ biến đặc hiệu cho tế bào chất của tế bào thần kinh. Trong một nghiên cứu nhỏ (n=43) ở trẻ em sau khi ngừng tim, nồng độ ubiquitin carboxy-terminal hydrolase L1 ở 60 giờ sau khi ngừng tim cao hơn ở những bệnh nhân có kết cục không thuận lợi.
Nhiều dấu ấn sinh học hứa hẹn khác về tổn thương thần kinh, viêm toàn thân và đa hình di truyền hiện đang được đánh giá. Một thử nghiệm đang diễn ra đang điều tra nồng độ của NSE, S100B, protein axit fibrillary thần kinh đệm và ubiquitin carboxy-terminal hydrolase L1 trong 72 giờ đầu tiên sau OHCA trẻ em và mối liên quan của chúng với kết cục thần kinh trong 1 năm.
Lactate được tạo ra trong quá trình chuyển hóa yếm khí, và nồng độ lactate trong huyết thanh được theo dõi như một chỉ báo gián tiếp về những bất thường trong tưới máu cơ quan đích và đáp ứng với điều trị. Sau khi ngừng tim, sự gia tăng nồng độ lactate có thể phản ánh không chỉ tình trạng giảm tưới máu hệ thống nghiêm trọng sau ngừng tim mà còn cả tình trạng giảm tưới máu não nghiêm trọng. Trong một số nghiên cứu về ngừng tim ở trẻ em, nồng độ lactate huyết thanh cao hơn trong 12 giờ đầu tiên sau khi ngừng tim có liên quan đến tỷ lệ tử vong gia tăng và nồng độ cao hơn trong vòng 12 giờ sau ROSC dự đoán một cách khiêm tốn về kết cục bất lợi (diện tích dưới đường cong: đối với IHCA, 0,76; đối với OHCA, 0,75).
Hiện tại, không có đủ bằng chứng để hỗ trợ việc sử dụng riêng nồng độ chất đánh dấu sinh học trong huyết thanh để dự đoán kết cục sau khi ngừng tim ở trẻ em. Mặc dù các dấu ấn sinh học cụ thể đã cho thấy nhiều hứa hẹn, nhưng chúng vẫn chưa được xác nhận trong các nghiên cứu nhi khoa trong tương lai sau khi tim ngừng đập.
Oxygen hóa não và CBF
CBF và khả năng tự điều hòa của não có thể được đánh giá liên tục không xâm lấn bằng Doppler xuyên sọ và quang phổ cận hồng ngoại. Doppler xuyên sọ đo vận tốc dòng máu chảy qua các động mạch não giữa và đã được sử dụng để xác định các mẫu CBF bất thường/sự tự điều hòa của não. Trong một nghiên cứu nhỏ (n=17) về Doppler xuyên sọ sau khi ngừng tim do ngạt ở trẻ em, sự đảo ngược hoặc không có lưu lượng máu động mạch não tâm trương trong khi sử dụng liệu pháp hạ thân nhiệt có liên quan đến tình trạng thực vật hoặc tử vong.267 Dữ liệu từ các nghiên cứu người lớn là không rõ ràng, không có mối tương quan rõ ràng giữa thiếu máu cục bộ hoặc tăng huyết áp được đo bằng Doppler xuyên sọ và các kết cục.
Quang phổ cận hồng ngoại có thể được sử dụng để đánh giá quá trình tự điều hòa của não bằng cách xác định mức độ tương quan giữa quang phổ cận hồng ngoại–chỉ số thể tích huyết sắc tố có nguồn gốc từ huyết sắc tố và áp suất động mạch trung bình (MAP).64 Phạm vi MAP duy trì CBF trong một vùng trong đó quá trình tự điều hòa được bảo tồn được coi là MAP tối ưu. Một nghiên cứu tiền cứu trên 36 trẻ em sau khi ngừng tim đã đánh giá quá trình tự điều hòa của não bằng cách sử dụng quang phổ cận hồng ngoại và MAP; những người có độ lệch lớn hơn so với MAP tối ưu trong 48 giờ đầu tiên sau ROSC có nhiều khả năng tử vong hơn, cần phải mở dạ dày hoặc mở khí quản hoặc giảm điểm PCPC.
Các nghiên cứu nhi khoa về các công cụ theo dõi thần kinh này bị giới hạn bởi quy mô, thiết kế hồi cứu, thời gian điều tra, sử dụng các định nghĩa không nhất quán và không có khả năng điều chỉnh các yếu tố gây nhiễu tiềm ẩn. Các cuộc điều tra trong tương lai có thể xác định cách sử dụng những công cụ này để tiên lượng kết cục sau khi ngừng tim.
Tác động của hạ thân nhiệt đối với tiên lượng thần kinh
Tác dụng của TTM đối với tiên lượng thầnkinh được đặc trưng kém sau khi ngưng tim ở trẻ em, nhưng thật hợp lý khi cho rằng cần có sự chậm trễ thận trọng trong việc đánh giá tiên lượng thần kinh. Ủng hộ khái niệm này, trong một nghiên cứu gần đây về tiên lượng sau ngừng tim ở trẻ em, sự đồng ý của bác sĩ thần kinh đã được cải thiện theo thời gian và chính xác hơn vào ngày thứ 5 đến ngày thứ 7 sau khi ngừng tim so với ngày thứ 1 hoặc ngày thứ 2 đến ngày thứ 4 sau khi ngừng tim.
Một số nghiên cứu gần đây cho thấy rằng các dấu hiệu hồi phục thần kinh ở những người sống sót sau ngừng tim ở người lớn có thể không xuất hiện trong 3 đến 4 ngày hoặc lâu hơn sau ROSC.131,271,272 Sự chậm trễ trong biểu hiện lâm sàng, kết hợp với khả năng dự đoán kém của chẩn đoán hình ảnh thần kinh, điều tra sinh lý thần kinh, và dấu ấn sinh học, đã tạo ra những thách thức cho việc tiên lượng ở người lớn sau khi ngừng tim.
Sự phức tạp của tiên lượng trở nên khó khăn hơn khi sử dụng TTM như một liệu pháp sau ngừng tim. TTM có thể kéo dài thời gian thanh thải thuốc an thần và giảm đau được sử dụng trong PCAC, dẫn đến chậm trễ trong biểu hiện lâm sàng (phần Thuốc an thần và phong tỏa thần kinh cơ). Hơn nữa, TTM có thể làm thay đổi chuyển hóa nãonvà hoạt động của tế bào thần kinh, do đó quá trình phục hồi sinh học có thể bị trì hoãn bất kể có sử dụng thuốc an thần hay không. Những hiện tượng này đã khiến bản cập nhật hướng dẫn hỗ trợ sự sống cho tim nâng cao năm 2015 của AHA đề xuất rằng thời điểm sớm nhất để tiên lượng bằng cách sử dụng lâm sàng kiểm tra ở những bệnh nhân người lớn được điều trị bằng TTM có thể là 72 giờ sau khi thân nhiệt trở lại bình thường so với 72 giờ sau khi ngừng tim đối với những người không được điều trị bằng TTM. Các hướng dẫn này lưu ý rằng đối với bệnh nhân người lớn được điều trị bằng TTM, thời gian tiên lượng thường là 4,5 đến 5 ngày sau ROSC.212 Thật vậy, trong một nghiên cứu lâm sàng về phục hồi sau ngừng tim ở người lớn bằng TTM, nhiều bệnh nhân đã thể hiện hoạt động vận động có chủ ý hoặc mở mắt chỉ sau 4 đến 5 ngày sau ROSC.131 Ảnh hưởng của TTM đối với khả năng dự đoán của CT hoặc MRI não chưa được nghiên cứu đầy đủ ở trẻ em trong PCAC để đưa ra hướng dẫn.
Tóm tắt tiên lượng
Không có biến đơn lẻ nào được tìm thấy là đủ chính xác và đáng tin cậy để tiên lượng ở trẻ em sau ngừng tim. Các bác sĩ nên xem xét nhiều yếu tố khi dự đoán kết cục ở trẻ sơ sinh và trẻ em đạt được ROSC sau ngừng tim.58
Cân nhắc đặc biệt
Bệnh tim bẩm sinh
Bệnh nhân mắc bệnh tim bẩm sinh, đặc biệt là những bệnh nhân có tổn thương tắc nghẽn tim trái, chuyển tâm nhĩ để chuyển vị các động mạch lớn, tăng áp động mạch phổi, sinh lý một tâm thất và các tổn thương cần phẫu thuật mở tâm thất trong quá trình sửa chữa, có nguy cơ ngừng tim cao hơn, đặc biệt là trong giai đoạn hậu phẫu.274 Các yếu tố nguy cơ bổ sung bao gồm rối loạn nhịp tim trước đó, giảm phân suất tống máu và tuần hoàn phổi và hệ thống không cân bằng.274 Trong giai đoạn sau ngừng tim, điều quan trọng là xác định bệnh lý và sinh lý tim cơ bản của trẻ vì thuốc và xử trí thở máy thường sẽ khác với yêu cầu của trẻ có tim bình thường. Điều này đặc biệt đúng đối với bệnh nhân có sinh lý đơn tâm thất. Để biết thêm chi tiết, độc giả có thể tham khảo báo cáo khoa học toàn diện của AHA về CPR ở trẻ sơ sinh và trẻ em mắc bệnh tim.
Ấn phẩm này tập trung vào PCAC của trẻ em có bất kỳ 3 tình trạng nào sau đây: sinh lý tâm thất đơn, tăng áp động mạch phổi hoặc bệnh tim bên phải.
Sinh lý tâm thất đơn
Bệnh nhân có sinh lý một tâm thất thường yêu cầu sửa chữa 3 giai đoạn để tách tuần hoàn phổi và tuần hoàn hệ thống.
Cho đến thời điểm giảm nhẹ ở giai đoạn 3, sự cân bằng giữa lưu lượng máu phổi và hệ thống được kiểm soát bởi kích thước của shunt phổi và bởi sức cản tương đối ở giường mạch máu phổi và hệ thống, có thể rất linh hoạt ở trẻ nhỏ. Trong giai đoạn sau ngừng tim, việc điều chỉnh sức cản mạch máu phổi và hệ thống sẽ giúp tối ưu hóa tưới máu và oxygen hóa hệ thống. Quá tải tuần hoàn phổi có thể do sức cản mạch máu phổi thấp hoặc sức cản mạch máu hệ thống cao và sẽ ảnh hưởng đến lưu lượng máu toàn thân. Ở những bệnh nhân bị quá tải tuần hoàn phổi, đặc biệt là trước khi giảm nhẹ giai đoạn 2, nồng độ oxy hít vào cao có thể làm giãn giường mạch máu phổi và giảm sức cản mạch máu phổi, làm tăng lưu lượng máu phổi bằng cách giảm lưu lượng máu hệ thống. Điều này gây ra hoặc góp phần gây ra hội chứng cung lượng tim thấp. Để tăng lưu lượng và tưới máu hệ thống và giảm quá tải tuần hoàn phổi, cần phải loại bỏ các yếu tố như nồng độ oxy hít vào cao gây giảm sức cản mạch máu phổi và giảm sức cản mạch máu hệ thống bằng thuốc ức chế phosphodiesterase (milrinone) hoặc thuốc chẹn α-adrenergic (phenoxybenzamin, phentolamin). Do đó, sử dụng oxy khi cần thiết và giảm sức cản mạch máu hệ thống sẽ là liệu pháp hữu ích nhất để tăng lưu lượng máu và cung cấp oxy cho hệ thống.
Sau phẫu thuật giảm nhẹ giai đoạn 2 (nối tĩnh mạch chủ trên-động mạch phổi), khi tĩnh mạch chủ trên hồi lưu trực tiếp vào động mạch phổi, giảm thông khí nhẹ kèm tăng CO2 sẽ cải thiện tưới máu hệ thống. Tăng CO2 nhẹ gây giãn mạch não, tăng CBF và hồi lưu tĩnh mạch não. Điều này làm tăng lưu lượng máu từ tĩnh mạch chủ trên đến động mạch phổi và hồi lưu tĩnh mạch phổi, dẫn đến tăng tiền tải tâm thất hệ thống và tưới máu hệ thống.
Sau khi hoàn thành giai đoạn điều chỉnh thứ ba (thủ thuật Fontan), tất cả máu tĩnh mạch hệ thống được chuyển trực tiếp vào tuần hoàn phổi, do đó lưu lượng máu phổi và tĩnh mạch phổi trở về tâm thất hệ thống phụ thuộc vào lưu lượng máu thụ động qua giường mạch máu phổi. Dòng máu thụ động này đòi hỏi một độ chênh áp suất trên giường mạch máu phổi. Phải tránh giảm thông khí (dẫn đến thiếu oxy phế nang) và nhiễm toan vì chúng có thể dẫn đến tăng sức cản mạch máu phổi, giảm lưu lượng máu phổi, giảm cung lượng tim và giảm tưới máu hệ thống. Thông khí áp lực dương có thể làm tăng áp lực trong lồng ngực và cản trở lưu lượng máu phổi,275 vì vậy thông khí cơ học phải được sử dụng một cách thận trọng, với việc ngừng thông khí tự phát ngay khi dung nạp được.
Tăng áp động mạch phổi
Tăng áp động mạch phổi thường xuất hiện ở trẻ sơ sinh và trẻ em mắc bệnh tim bẩm sinh, và nó làm tăng nguy cơ ngừng tim. Ngoài ra, tăng áp phổi được quan sát thấy ở 2% bệnh nhân sau phẫu thuật. Các cơn tăng áp phổi đi kèm với suy tim phải (nghĩa là tâm thất phổi), hạ huyết áp hệ thống và thiếu máu cục bộ cơ tim. Những cơn khủng hoảng này có thể được kích hoạt bởi các tác nhân kích thích như đau, lo lắng, hút khí quản, thiếu oxy và nhiễm toan, cũng như do ngừng điều trị đặc hiệu với tăng áp phổi. Sau khi có được ROSC sau ngừng tim ở trẻ bị tăng áp phổi, quan trọng là cung cấp đủ oxy; để giảm thiểu kích thích; cung cấp đầy đủ thuốc giảm đau, an thần và có thể là NMB; và cho dùng thuốc giãn mạch phổi. Cần điều trị tích cực tình trạng thiếu oxy phế nang và nhiễm toan để ngăn ngừa co thắt mạch phổi. Đối với liệu pháp ban đầu đa hướng đối với các cơn tăng áp phổi ở trẻ em, tuyên bố khoa học của AHA đề xuất sử dụng oxy, gây nhiễm kiềm thông qua tăng thông khí (chỉ trong thời gian ngắn khi cần thiết) hoặc sử dụng chất kiềm, và sử dụng thuốc giãn mạch phổi dạng hít hoặc toàn thân. Liệu pháp tăng co bóp/thuốc vận mạch được đề xuất để tránh thiếu máu cục bộ RV, có thể do hạ huyết áp toàn thân.
Tắc nghẽn và rối loạn chức năng tim bên phải
Rối loạn chức năng tâm thu và tâm trương bên phải xảy ra thường xuyên trong giai đoạn hậu phẫu ở những bệnh nhân cần tái tạo đường thoát RV bằng cách cắt bỏ cơ hoặc đặt ống dẫn hoặc miếng dán xuyên vòng. Nguy cơ ngừng tim tăng theo tuổi của bệnh nhân, mức độ nghiêm trọng của tắc nghẽn dòng chảy ra, quá tải thể tích và sự hiện diện của các dị tật còn sót lại như thông liên thất hoặc tắc nghẽn động mạch phổi đoạn xa. Sau khi ngừng tim, các mục tiêu điều trị nên bao gồm cẩn thận tránh siêu bơm phồng phổi hoặc giảm căng phồng phổi và duy trì đồng bộ nhĩ thất.
Xử trí bằng thuốc thường được yêu cầu để điều trị rối loạn chức năng RV với tắc nghẽn tim phải, nhưng những loại thuốc này, đặc biệt là catecholamine, phải được sử dụng thận trọng. Lưu lượng máu động mạch vành đến RV có thể giảm khi RV phì đại và áp lực cuối tâm trương RV tăng cao. Do đó, RV có thể bị thiếu máu cục bộ bất cứ khi nào nhu cầu oxy của cơ tim tăng lên chẳng hạn như nhịp tim nhanh và tăng áp lực cho thành mạch. Thuốc co mạch toàn thân như vasopressin và norepinephrine có thể hỗ trợ huyết áp và duy trì tưới máu mạch vành.
Tuyên bố khoa học của AHA về CPR ở trẻ sơ sinh và trẻ em mắc bệnh tim cung cấp thêm thông tin về những lưu ý đặc biệt khi chăm sóc trẻ mắc bệnh tim.
Ngừng tim loạn nhịp
Ở một đứa trẻ khỏe mạnh trước đó bị ngừng tim đột ngột với nhịp ban đầu là rung tâm thất/nhịp nhanh thất vô mạch, nguyên nhân rất có thể là do rối loạn nhịp tim. Bệnh lý này có thể bao gồm các bất thường về tim bẩm sinh hoặc di truyền như bệnh cơ tim phì đại hoặc giãn, bệnh lý kênh di truyền, hội chứng QT kéo dài, hội chứng Brugada, bệnh cơ tim RV hoặc nhịp nhanh thất đa hình do catecholamine, hội chứng Wolff-Parkinson-White hoặc bệnh tim bẩm sinh. Các tình trạng mắc phải có thể gây ngừng tim do loạn nhịp tim bao gồm viêm cơ tim, co thắt dây rốn và thuốc/độc tố như thuốc chống trầm cảm ba vòng, anthracycline và thuốc lạm dụng. Đối với nhiều bệnh nhân bị ngừng tim do nguyên nhân loạn nhịp đột ngột, CPR và khử rung tim nhanh chóng của người ngoài cuộc dẫn đến khả năng sống sót cao với kết cục chức năng tốt.
Trong giai đoạn ngay lập tức sau ngừng tim, đánh giá ban đầu nên bao gồm điều tracác nguyên nhân gây ngừng tim nguyên phát (loạn nhịp tim). Mặc dù không có xét nghiệm đơn lẻ nào có thể chẩn đoán, nhưng siêu âm tim rất hữu ích để đánh giá độ dày và chức năng của cơ tim, có khả năng là bất thường ở trẻ em mắc bệnh cơ tim và viêm cơ tim. Các tiêu chí điện tâm đồ có thể gợi ý sự hiện diện của bệnh lý kênh, nhưng cần phải thử nghiệm bổ sung và tư vấn điện sinh lý tim ở trẻ em. Thuốc chẹn beta và máy khử rung tim được cấy ghép là những liệu pháp chính để xử trí bệnh nhân mắc hội chứng QT kéo dài và thường nên tránh dùng thuốc chống loạn nhịp làm kéo dài khoảng QT (ví dụ: procainamide, sotalol và amiodarone).
Tư vấn điện sinh lý sẽ rất cần thiết để xác định sự phù hợp của liệu pháp bằng thuốc hoặc cấy máy tạo nhịp tim/máy khử rung tim cấy ghép. Nếu bệnh nhân được phát hiện mắc hội chứng di truyền, việc sàng lọc người thân cấp độ một đã được chứng minh là phát hiện thêm các thành viên gia đình có nguy cơ mắc bệnh.
Ngừng tim do chết đuối
Đuối nước gây ra 25% đến 31% trong tất cả các trường hợp OHCA ở trẻ em và tỷ lệ sống sót nằm trong khoảng từ 9% đến 46%. Thời gian ngâm nước lâu hơn và thời gian hô hấp nhân tạo lâu hơn có liên quan đến khả năng sống sót và kết cục thần kinh tồi tệ hơn. Phần lớn trẻ em được hô hấp nhân tạo trong hơn 30 phút và sống sót đến 1 năm với kết cục thần kinh không thuận lợi.
25% trẻ em trong thử nghiệm THAPCA-OH bị ngừng tim do đuối nước, với 46,4% sống sót sau 1 năm và 24,6% có kết cục thần kinh thuận lợi sau 1 năm.194 Trẻ em bị ngừng tim do đuối nước có kết cục tốt hơn so với trẻ em trong thử nghiệm THAPCA-OH, so với trẻ bị ngừng thở do các nguyên nhân hô hấp khác.194 Trẻ được điều trị bằng TTM ở nhiệt độ từ 32°C đến 34°C không có kết cục tốt hơn so với trẻ được điều trị bằng TTM ở nhiệt độ từ 36°C đến 37,5°C.
ECMO đã được sử dụng để làm ấm và hỗ trợ tim phổi ở trẻ em bị OHCA do đuối nước lạnh. Khi xem xét sổ đăng ký ELSO, trong số 198 trẻ em được điều trị bằng ECMO sau một vụ đuối nước từ năm 1986 đến 2015, tỷ lệ sống sót là 54%. Trong số này, 15,7% bị hạ thân nhiệt khi nhập viện, 35,4% bị ngừng tim trước khi được hỗ trợ sự sống ngoài cơ thể (ECLS) và 28,8% trải qua ECPR.295 Tỷ lệ sống sót cụ thể đối với trẻ em bị OHCA liên quan đến đuối nước không được báo cáo, nhưng tỷ lệ sống sót được báo cáo đối với nạn nhân đuối nước ở mọi lứa tuổi bị ngừng tim trước ECLS là 57% và tỷ lệ sống sót đối với những nạn nhân này ở mọi lứa tuổi đã trải qua ECPR là 23,4%.
Các nghiên cứu quan sát về ECLS ở trẻ em bị OHCA hạ thân nhiệt do đuối nước báo cáo các kết cục khác nhau. Mặc dù thời gian CPR dài hơn có liên quan đến tỷ lệ tử vong cao hơn, nhưng một số loạt trường hợp bao gồm một số nạn nhân đã được giải phóng thành công khỏi ECLS và sống sót với kết cục thần kinh thuận lợi.
Không có đủ dữ liệu được công bố để xác định cách xử trí tối ưu dành riêng cho trẻ em bị ngừng tim do đuối nước. Các bác sĩ lâm sàng được khuyến khích sử dụng PCAC chung được xác định trong tuyên bố này.
Cần có các nghiên cứu triển vọng đa trung tâm với thời gian theo dõi dài hạn để xác định rõ hơn vai trò của ECLS, TTM và các biện pháp can thiệp bảo vệ thần kinh khác trong nhóm bệnh nhân này. ECLS để làm ấm và hỗ trợ tuần hoàn cho nạn nhân chết đuối trong nước lạnh có thể ảnh hưởng đến sự sống còn. Các vấn đề chưa được giải quyết đối với TTM ở trẻ em bị OHCA liên quan đến đuối nước bao gồm tốc độ ủ ấm tối ưu cho trẻ bị hạ thân nhiệt, thời điểm bắt đầu TTM tối ưu, nhiệt độ mục tiêu tối ưu và tổng thời gian TTM tối ưu.
Vận chuyển sau ngưng tim
Nhóm viết đã xác định không có tài liệu đã xuất bản được đánh giá ngang hàng nào đề cập cụ thể đến việc chăm sóc vận chuyển trẻ em hoặc người lớn sau khi ngừng tim. Các nhận xét sau đây dựa trên các bằng chứng đã công bố đề cập đến việc chăm sóc trẻ em bị bệnh nặng trong môi trường vận chuyển.
Lý tưởng nhất là PCAC nên được cung cấp bởi một nhóm được đào tạo từ một cơ sở chăm sóc cấp ba cho trẻ em.52 Điều này thường đòi hỏi phải chuyển giao giữa các cơ sở tại thời điểm PCAS, bao gồm rối loạn chức năng tâm thu thất phụ thuộc vào cơ tim, đang tiến triển và khi những bệnh nhân này có nguy cơ đặc biệt bị chấn thương thứ phát.42 Những bệnh nhân bệnh nặng hơn (chẳng hạn như những người mắc PCAS) dễ bị mất ổn định hơn trong môi trường vận chuyển,304 và việc vận chuyển khoảng cách/thời gian dài hơn (chẳng hạn như chuyển bệnh nhân đến các PICU khu vực liên kết với nhau) có liên quan đến nguy cơ mất ổn định bệnh nhân cao hơn.305 Các nhà cung cấp tại trung tâm giới thiệu nên liên hệ với nhóm vận chuyển từ cơ sở chăm sóc cấp ba càng sớm càng tốt trong quá trình hồi sức và phối hợp vận chuyển với đơn vị tiếp nhận.52 Việc vận chuyển bệnh nhân được điều phối tốt nhất bởi một nhóm vận chuyển, với các thành viên được đào tạo và có kinh nghiệm trong việc chăm sóc trẻ em bị bệnh nặng và bị thương, và được giám sát bởi bác sĩ cấp cứu nhi khoa hoặc bác sĩ nhi khoa bác sĩ chăm sóc đặc biệt.52 Việc sử dụng các đội chuyên biệt này (trái ngược với các đội vận chuyển lấy người lớn làm trung tâm) có liên quan
đến việc giảm tỷ lệ mắc bệnh trong quá trình vận chuyển306 và giảm tỷ lệ mắc bệnh và tử vong của PICU.304,305
Các bác sĩ nên cố gắng ổn định bệnh nhân sau ROSC trước khi chuyển bệnh nhân thay vì chuyển bệnh nhân ra khỏi trung tâm giới thiệu càng nhanh càng tốt (“xúc và chạy”). Cần theo dõi hô hấp, huyết động, thần kinh và nhiệt độ thích hợp trong quá trình vận chuyển, cũng như thiết lập kiểm soát đường thở, tiếp cận mạch máu, thở máy và cung cấp hỗ trợ huyết động khi cần thiết. Điều quan trọng là phải theo dõi PetCO2 trong quá trình vận chuyển bệnh nhân đặt nội khí quản giữa các bệnh viện hoặc trong bệnh viện.52 Các nhân viên y tế tại bệnh viện giới thiệu nên xin lời khuyên từ các chuyên gia tại bệnh viện tuyến ba tiếp nhận vì bệnh nhân sẽ dễ bị rối loạn nhịp tim, hô hấp do PCAS, kết hợp với các loại thuốc được sử dụng để tạo điều kiện cho các can thiệp.
Trong quá trình vận chuyển, bệnh nhân sẽ được chăm sóc giống nhau với các mục tiêu điều trị giống như những mục tiêu được sử dụng trong môi trường bệnh viện. Theo dõi chặt chẽ và can thiệp kịp thời nên ngăn ngừa hoặc điều trị kịp thời cho bệnh nhân bị sốt hoặc hạ thân nhiệt ngoài ý muốn, hạ huyết áp, giảm oxy máu và giảm CO2 hoặc tăng CO2. Các nhà cung cấp nên lường trước những thay đổi về dấu hiệu sinh tồn của bệnh nhân do chính môi trường vận chuyển (ví dụ: ảnh hưởng của chuyển động của bệnh nhân đối với huyết áp, ảnh hưởng của nhiệt độ môi trường đối với bệnh nhân, ảnh hưởng của độ cao đối với quá trình oxygen hóa). Những thay đổi như vậy có thể đặc biệt khó phát hiện trong quá trình vận chuyển vì chất lượng giám sát và loại thiết bị được sử dụng thường kém phức tạp hơn so với những thiết bị sẵn có trong môi trường bệnh viện.
Bảng 5. Tóm tắt các công cụ hiện có để đánh giá theo dõi sau ngừng tim, bao gồm độ tuổi, thời gian và nguồn dữ liệu
| Lãnh vực | Ví dụ về thiết bị | Phạm vi tuổi | Thời gian, phút | Nguồn |
| Sức khỏe tổng thể và chức năng | PCPC/POPC307 | 0–21 tuổi | 5 | Chart/interview |
| GOS-E Peds308 | 1 tháng–18 năm | 3 | Chart/interview | |
| FSS | 0–18 tuổi | 5 | Chart/interview | |
| Khả năng nhận thức | Wechsler Intelligence Scales (WPPSI, WISC,309,310 WAIS) MSEL311 | 4 tuổi–người lớn | 60–90 | In person |
| 0–6 tuổi | 15–60 | In person | ||
| Chức năng thích ứng | VABS312 | 0–người lớn | 20–60 | Interview/survey |
| ABAS313 | 0–người lớn | 15–20 | Interview/survey | |
| Phát triển | BSID314 | 1–42 tháng | 30–90 | In person |
| Xúc động | CBCL | 2–21 tuổi | 20 | Interview/survey |
| BASC | 2–21 tuổi | 10–20 | Interview/survey | |
| Chức năng điều hành | BRIEF | 2 tuổi–người lớn | 10 | Survey |
| Chất lượng cuộc sống | CHQ315 | 5–18 tuổi | 5–15 | Interview/survey |
| ITQOL316 | 2 tháng–5 năm | 2–60 | Interview/survey | |
| PedsQL317 | 2–18 tuổi | 4 | Interview/survey |
ABAS, Hệ thống đánh giá hành vi thích ứng; BASC, Hệ thống Đánh giá Hành vi cho Trẻ em; BRIEF, Đánh giá Hành vi Kiểm kê Chức năng Điều hành; BSID, Bayley Scales of Infant and Toddler Development; CBCL, Bảng kiểm hành vi trẻ em; CHQ, Bảng câu hỏi sức khỏe trẻ em; FSS, Thang trạng thái chức năng; GOS-E Peds, Thang điểm kết cục của Glasgow–Sửa đổi nhi khoa mở rộng; ITQOL, Bảng câu hỏi về chất lượng cuộc sống của trẻ sơ sinh; MSEL, Mullen Scales of Early Learning; PCPC, Hạng mục Hiệu suất Não ở Trẻ em; PedsQL, Kiểm kê chất lượng cuộc sống ở trẻ em; POPC, Hạng mục hiệu suất tổng thể của trẻ em; VABS, Thang đo hành vi thích ứng của Vineland; WAIS, Thang đo trí thông minh dành cho người lớn của Wechsler; WISC, Thang điểm Trí tuệ Wechsler dành cho Trẻ em (6–16 tuổi); và WPPSI, Wechsler Preschool và Primary Scale of Intelligence (4– 6,5 tuổi).
Kết cục dài hạn
Các nghiên cứu về kết cục ngừng tim trước đây thường tập trung vào các kết cục ngắn hạn của ROSC, khả năng sống sót sau khi xuất viện và kết cục tổng thể về thần kinh khi xuất viện. Trong những thập kỷ gần đây, những cải thiện về kết cục xuất viện đã dẫn đến sự thay đổi trọng tâm từ kết cục xuất viện ngắn hạn sang tỷ lệ sống lâu dài (> 1 tháng sau khi nhập viện), cũng như các kết cục về chất lượng cuộc sống liên quan đến sức khỏe và hành vi thần kinh (neurobehavioral and health- related quality of life – HRQOL) (Bảng 5).
Kết cục thần kinh khi xuất viện dựa trên PCPC do Utstein khuyến nghị318, một thang đo toàn cầu về chức năng thần kinh.307 Thang đo này có thể được chấm điểm cả trong thời gian thực và từ đánh giá biểu đồ hồi cứu nhưng bị hạn chế do thiếu khả năng áp dụng cho nhóm trẻ sơ sinh. Các nghiên cứu về ngừng tim gần đây đã sử dụng các chỉ số chi tiết hơn để mô tả kết cục lâu dài.2,3,319
Sự sống sót lâu dài và kết cục thần kinh
Nhóm viết chỉ xác định một số nghiên cứu nhỏ về kết cục lâu dài sau khi ngừng tim ở trẻ em. Trong 2 loạt nhỏ nạn nhân trẻ em của OHCA sống sót sau khi xuất viện, 91%207 đến 92%320 sống sót sau 1 năm, 86%320 sống sót sau 5 năm và 77% sống sót sau 20 năm.320 Đáng chú ý là 84% đến 94% bệnh nhân những người được xuất viện với kết cục thuận lợi (PCPC 1 hoặc 2) có kết cục thần kinh thuận lợi sau 1 năm theo dõi,207.321 trong khi 40% đến 54% bệnh nhân có kết cục không thuận lợi khi xuất viện đã chết khi theo dõi.207 Trong thử nghiệm THAPCA-OH về TTM cho trẻ em hôn mê được nhập viện sau ROSC, một nửa số người sống sót xuất viện có thay đổi về chức năng thần kinh sau 1 năm theo dõi và một phần ba số đối tượng xuất viện với chức năng thần kinh nghiêm trọng được cải thiện từ bình thường đến chức năng trung bình.
Trong các nghiên cứu nhỏ về IHCA, 73% đến 86% những người sống sót sau khi xuất viện có thời gian sống lâu dài với kết cục thuận lợi (PCPC 1 hoặc 2),322–324 với hầu hết không có thay đổi nào trong năm đầu tiên.
Kết cục hành vi thần kinh
Các nghiên cứu triển vọng gần đây về kết cục hành vi thần kinh đã tập trung vào theo dõi qua điện thoại và trực tiếp; các phương pháp này thu được nhiều thông tin chi tiết hơn so với các đánh giá biểu đồ có thể thu được về kết cục hành vi thần kinh. Các nghiên cứu gần đây đã sử dụng Thang đo hành vi thích ứng của Vineland.2,3,326 Bảng 5 nêu bật các công cụ có thể được sử dụng để đánh giá kết cục ở trẻ em sau khi tim ngừng đập.
Nghiên cứu nhi khoa lớn nhất về kết cục hành vi thần kinh trong 1 năm sau OHCA là thử nghiệm THAPCA-OH về TTM cho trẻ hôn mê sau ROSC. Kết cục của thử nghiệm này không thể khái quát hóa cho tất cả bệnh nhi mắc OHCA vì nó chỉ theo dõi một nhóm nhỏ tất cả trẻ em mắc OHCA. Một phần ba số đối tượng đã đăng ký còn sống sau 1 năm; một phần ba trong số những người sống sót này có tình trạng chức năng tốt và chức năng trung bình,3,182 và một phần ba bị suy giảm chức năng nghiêm trọng.182 Mười phần trăm có sự thay đổi về chức năng trong năm đầu tiên, với hai phần ba (67%) cải thiện và một phần ba (33%) xấu đi.
Trong số trẻ em tham gia thử nghiệm lâm sàng THAPCA-IH, 47% còn sống sau 1 năm. Ba mươi phần trăm những người sống sót này có thay đổi <1-SD so với điểm Thang điểm Hành vi Thích ứng Vineland trước khi họ bị ngưng tim.
Xét nghiệm tâm thần kinh
Cho đến gần đây, các báo cáo về kết cục tâm thần kinh tập trung vào trí nhớ, ngôn ngữ và sự chú ý chỉ được giới hạn trong các nghiên cứu nhỏ chứng minh bệnh tật đáng kể.327 Trong nghiên cứu lớn nhất cho đến nay về 52 bệnh nhi sống sót sau ngừng tim, cha mẹ và giáo viên của họ đã hoàn thành bảng câu hỏi từ 2 đến 11 năm sau khi đứa trẻ xuất viện tại ICU (trung bình, 5,6 năm [khoảng, 1,8–11,9 năm]).328 Những đứa trẻ sống sót có điểm IQ, khả năng hiểu lời nói, chỉ số tổ chức nhận thức và tốc độ xử lý kém hơn so với một mẫu đại diện lớn gồm những đứa trẻ cùng độ tuổi từ dân số Hà Lan nói chung.319,328 Sau khi điều chỉnh điểm số IQ, những người sống sót có trí nhớ hình ảnh kém hơn, khả năng nhận biết tốt hơn, khả năng chú ý và chức năng điều hành tương đương. Mặc dù các gia đình báo cáo rằng những người sống sót có chức năng điều hành tốt hơn so với dân số nói chung, nhưng các giáo viên báo cáo rằng họ có kỹ năng tổ chức và lập kế hoạch kém hơn. Nhiều người trong số những người sống sót này cũng có vấn đề về sự chú ý và cơ thể328 và cần hỗ trợ chuyên nghiệp cho các vấn đề về cảm xúc/hành vi hoặc giáo dục đặc biệt.329 Các nghiên cứu nhỏ về thời gian theo dõi dài hạn (trung bình, 8 năm) đã chứng minh rối loạn chức năng thần kinh đáng kể (57% bệnh nhân) và chỉ số IQ thấp hơn (<80 [phạm vi, 20–78]; trung bình dân số, 100; SD, 15) ở những người sống sót sau ngừng tim do đuối nước.330,331
Kết cục HRQOL
HRQOL và gánh nặng gia đình là những lĩnh vực điều tra mới và quan trọng vì những người sống sót sau ngừng tim có thể bị rối loạn chức năng đáng kể và phụ thuộc vào người chăm sóc. HRQOL do cha mẹ báo cáo của những người sống sót sau ngừng tim cho thấy chức năng vai trò kém hơn, nhận thức về sức khỏe nói chung kém hơn và tác động của cha mẹ tồi tệ hơn so với các đối tượng kiểm soát khỏe mạnh nhưng sự gắn kết gia đình cao hơn. Các bệnh nhân báo cáo không có sự khác biệt về HRQOL so với các mẫu trẻ em đại diện người chưa bao giờ bị ngừng tim.
Cha mẹ của những trẻ sống sót sau ngừng tim báo cáo rằng bản thân họ cũng gặp những hạn chế trong các hoạt động hàng ngày, nhưng họ cũng cho biết họ thực hiện vai trò về thể chất, xã hội và cảm xúc tốt hơn so với nhóm dân số khỏe mạnh cùng độ tuổi.329 Trẻ em sống sót sau OHCA, so với những trẻ sống sót sau IHCA, báo cáo sự gắn kết gia đình tồi tệ hơn và chức năng thể chất của cha mẹ kém hơn.329 Gánh nặng gia đình ở những người sống sót sau thử nghiệm THAPCA-OH trở nên tồi tệ hơn vào thời điểm 3 và 12 tháng sau ngừng tim so với trước đây nhưng được cải thiện theo thời gian.
Sau khi ngừng tim, các kết cục lâu dài về hành vi thần kinh và tâm thần kinh và HRQOL thay đổi dựa trên nhiều yếu tố gây ngừng tim và một số bệnh nhân cải thiện theo thời gian. Trọng tâm trong tương lai vào việc đánh giá các kết cục lâu dài này và gánh nặng lâu dài đối với những người sống sót và gia đình là rất quan trọng để có thể xác định liệu các kết cục lâu dài có được cải thiện hay không khi chúng tôi cố gắng cải thiện chất lượng CPR và PCAC.
Định hướng tương lai tiềm năng
Việc xử trí bệnh nhi mắc ROSC sau khi ngừng tim là một thách thức và nhạy cảm về thời gian, đòi hỏi sự tham gia của nhiều nhà cung cấp chuyên gia từ chăm sóc tích cực đến thần kinh, tim mạch và thuốc phục hồi chức năng, điều dưỡng, dịch vụ xã hội và liệu pháp hô hấp. Do sự phức tạp này, người ta đã đề xuất rằng PCAC nên được tập trung tại các trung tâm có hiệu suất cao cụ thể (ví dụ: trung tâm ngừng tim hoặc trung tâm sau ngừng tim cấp 1, như được mô tả khác nhau trong tài liệu), giống như mô hình trung tâm chấn thương, để cho phép tập trung nhiều kinh nghiệm và nguồn lực địa phương hơn để cải thiện kết cục. Các nghiên cứu về OHCA dành cho người lớn gợi ý rằng việc chuyển bệnh nhân sau ngừng tim đến các trung tâm như vậy có thể cải thiện khả năng sống sót. Liệu các hệ thống chăm sóc tương tự có thể cải thiện khả năng sống sót và kết cục hành vi thần kinh sau khi ngừng tim ở trẻ em hay không vẫn còn không rõ ràng, mặc dù các nguyên tắc tương tự về thời gian nhạy cảm và độ phức tạp của việc chăm sóc áp dụng cho lĩnh vực nhi khoa sau ngưng tim.
Một cách tiếp cận khác để cải thiện việc chăm sóc sau ngừng tim liên quan đến nhu cầu giáo dục và đào tạo chuyên sâu hơn cho các chuyên gia về PCAC. Sau khi hoàn thành một chương trình giảng dạy cụ thể được thiết kế để cải thiện việc sử dụng TTM và các thành phần bổ sung của gói chăm sóc sau ngừng tim, các y tá và bác sĩ chăm sóc cấp cứu và quan trọng đã báo cáo việc sử dụng TTM và các thành phần khác của gói PCAC một cách nhất quán hơn.336 Công việc khác được yêu cầu xác định các phương pháp hiệu quả và phù hợp nhất để mở rộng kinh nghiệm đào tạo như vậy vào môi trường lâm sàng bận rộn.
Những lỗ hổng kiến thức quan trọng trong PCAC ở trẻ em
Trong quá trình xem xét tài liệu để giải quyết các phương pháp điều trị và tiên lượng liên quan đến PCAC ở trẻ em, nhiều lỗ hổng kiến thức quan trọng đã được xác định. Chúng tôi tóm tắt những lỗ hổng này trong Bảng 6 với mục tiêu kích thích nghiên cứu lâm sàng và tiền lâm sàng.
Một số cơ sở dữ liệu và bộ dữ liệu về ngừng tim hiện có và có thể giúp giải quyết một số khoảng trống quan trọng này: Đối với IHCA: AHA Get With The Guidelines– Resuscitation, THAPCA-IH,2 PC4 (Hiệp hội chăm sóc bệnh tim nghiêm trọng cho trẻ em),338 và ELSO339; và đối với OHCA, ROC Epistry,340 CARES,341 THAPCA-OH,3 và CanROC (Canadian Resuscitation Outcomes Consortium).
Bảng 6. Những lỗ hổng kiến thức nghiêm trọng liên quan đến PCAC và PCAS ở trẻ em
| Dịch tễ học
§ Dịch tễ học hiện đại của PCAC ở trẻ em là gì? § Làm cách nào chúng ta có thể theo dõi tác động của PCAC đối với các xu hướng trong kết cục? |
| Sinh lý bệnh
§ Các yếu tố ảnh hưởng đến sinh lý bệnh và sự tiến triển của PCAS ở trẻ em liên quan đến chức năng của tim và hệ thần kinh trung ương là gì? · Có cơ chế phụ thuộc vào tuổi? · Làm thế nào để những yếu tố này ảnh hưởng đến kết cục? |
| § Nguyên nhân gây ngừng tim có ảnh hưởng đến thời gian, cơ chế và tác động của PCAS không? |
| Mục tiêu và liệu pháp
§ Các mục tiêu và liệu pháp tối ưu sẽ ảnh hưởng đến kết cục là gì? Chúng có phụ thuộc vào tuổi tác không? Chúng thay đổi như thế nào theo từng giai đoạn của PCAS? · Thông khí o Áp lực oxy động mạch o PaCO2 · Huyết động o Huyết áp động mạch (tâm thu, tâm trương, trung bình) o Các phép đo rối loạn chức năng cơ tim và phục hồi · Não o Nền điện não đồ o Độ bão hòa oxy khu vực o Áp lực nội sọ và áp lực tưới máu não · Chuyển hóa o Nồng độ huyết sắc tố o Lactate huyết thanh · Lượng nước tiểu · Áp suất tĩnh mạch trung tâm · Có chỉ mục mới nào có thể được sử dụng để nhắm mục tiêu kết hợp các điểm cuối không? § Vai trò của TTM là gì? Có những quần thể đặc biệt nào có lợi hơn cho họ không? § Hỗ trợ vận mạch/bằng thuốc lý tưởng cần thiết để điều trị chức năng cơ tim sau ngừng tim và hạ huyết áp là gì? § Thời điểm và phương pháp tối ưu để bắt đầu ECMO (ECMO hoặc ECPR) là gì? § Hình ảnh thần kinh đóng vai trò gì trong các phương pháp chẩn đoán và tiên lượng? § Dự phòng chống loạn nhịp có vai trò gì trong PCAS không? § Có các yếu tố do điều trị làm thay đổi kết cục chẳng hạn như thuốc an thần và thuốc gây mê không? § Việc thực hiện một gói chăm sóc có làm thay đổi kết cục không? |
| § Khi nào là thời điểm tốt nhất để bắt đầu vật lý trị liệu tích cực, liệu pháp nghề nghiệp, liệu pháp âm nhạc và phục hồi chức năng toàn diện? Các can thiệp tối ưu cho trẻ em là gì? |
| Quần thể đặc biệt
§ PCAC nên được sửa đổi như thế nào đối với các nhóm đặc biệt (ví dụ: trẻ em mắc bệnh tim bẩm sinh, bị chấn thương, sau khi chết đuối)? |
| Hệ thống chăm sóc sức khỏe
§ Phương pháp tốt nhất (bao gồm cả nhóm và thời gian) để vận chuyển nhằm giảm tỷ lệ mắc bệnh và tử vong là gì? § Ai là thành viên chủ chốt của các nhóm đa ngành để tối ưu hóa PCAC? § Các trung tâm ngừng tim ở trẻ em có cải thiện kết cục không? § Giáo dục đa ngành, dựa trên mô phỏng có cải thiện việc thực hiện PCAC không? |
| Tiên lượng
§ Dấu ấn sinh học, đánh giá thần kinh và kỹ thuật hình ảnh nào dự đoán sớm và đáng tin cậy tổn thương thần kinh và kết cục? § Có quy tắc quyết định nào có thể dự đoán sự vô ích không? |
| Các biện pháp kết cục
§ Các biện pháp tốt nhất để theo dõi các biện pháp hành vi thần kinh và chất lượng cuộc sống dài hạn ở cả trẻ và gia đình là gì? |
| ECMO, quá trình oxygen hóa màng ngoài cơ thể; ECPR, hồi sức tim phổi ngoài cơ thể; EEG, điện não đồ; PCAC, chăm sóc sau ngưng tim; PCAS, hội chứng sau ngừng tim; và TTM, xử trí nhiệt độ mục tiêu. |