Bệnh thận - tiết niệu
Teo mật bẩm sinh (Biliary Atresia): Tổng quan, chẩn đoán và điều trị
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
Bài viết Teo mật bẩm sinh (Biliary Atresia): Tổng quan, chẩn đoán và điều trị tải pdf Tại đây.
Bản dịch của NTNH.
TỔNG QUAN
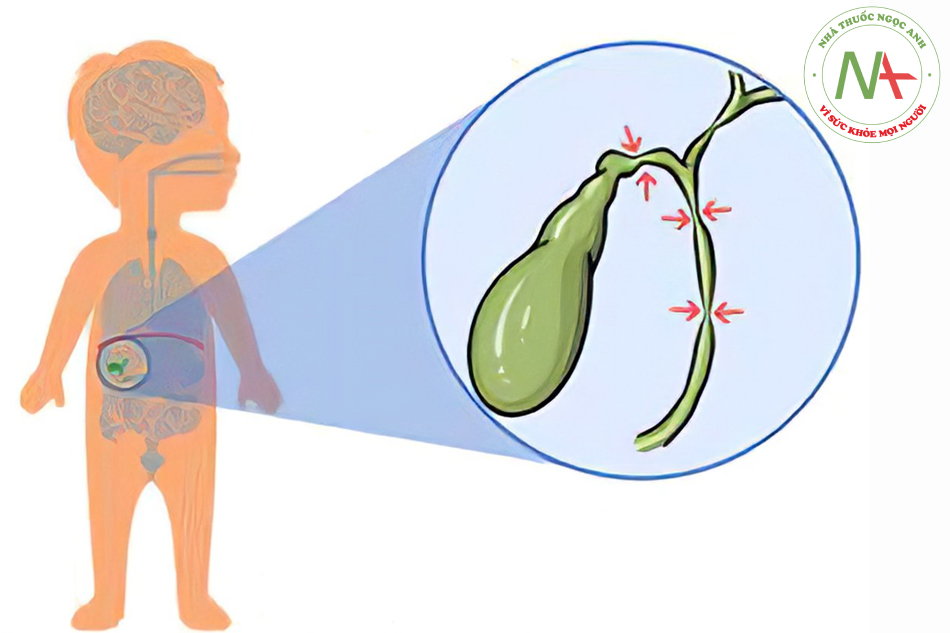
Teo mật bẩm sinh (BA) là bệnh lý tiến triển, không rõ nguyên nhân gây xơ hóa (fibro- obliterative) đường mật ngoài gan biểu hiện tắc nghẽn đường mật ở giai đoạn sơ sinh. Mặc dù tỉ lệ chung thấp (khoảng 1 trong 10,000 đến 20,000 ca sinh sống, nhưng BA là nguyên nhân thường gặp nhất gây vàng da sơ sinh căn chỉ định phẫu thuật và chỉ định thường gặp nhất trong ghép gan ờ trẻ em.
CÁC DẠNG TEO MẬT BẨM SINH
Ở trẻ nhũ nhi, BA có thể được chia thành 3 loại:
- BA không có bất kỳ dị dạng nào khác – Loại này thỉnh thoảng được gọi là BA chu sinh và xuất hiện với tì lệ 70 đến 85% trẻ BA. Những trẻ này đặc trưng không có vàng da sau sinh, nhưng xuất hiện tượng vòng hai tháng đầu đời, vàng da phát triển và phân dần trở nên bạc màu.
- BA liên quan đến laterality malformations – Loại này còn được gọi là BA có bất thường lách (BASM) và chiếm tỉ lệ 10 – 15% các trẻ BA. Laterality malformations bao gồm đảo ngược phủ tạng, vỏ lách hoặc đa lách, ruột xoay bất toàn, gián đoạn tĩnh mạch chủ dưới, và bất thường tim mạch. Dữ liệu cho thấy trẻ BASM có kết cục xấu hơn so với những trẻ BA chu sinh, khả năng do các bất thường tim mạch.
- BA liên quan đến các bất thường bấm sinh khác – Chiếm ti lệ 5-10% số ca BA: liên quan đến các bất thường bẩm sinh khác bao gồm thiếu sàn ruột, không hậu môn, bất thường thận, và/hoặc bất thường tim.
Bất kể BA loại này, trong mói trường hợp, mô học và chụp đường mật là đặc trưng. Mô bệnh học thường cho thấy viêm, xơ portal tract, ứ mật và tăng sinh đường mật: chụp đường mật cho thấy mất patency của đường mật ngoài gan.
BỆNH SINH
Nguyên nhân gây BA chưa rõ ràng, mặc dù nhiều cơ chế được chi ra. Ở một số bệnh nhân, nhiều cơ chế góp phần gây phát triển BA.
Nguyên nhân virus – Dữ liệu các virus đặc hiệu không được chi ra; các nghiên cứu không tìm ra dược mối tương quan giữa nhiễm tác nhân virus đặc hiệu với BA bao gồm CMV, và rotavirus. Tuy nhiên, một nghiên cứu cho thấy những trẻ dương tính với IgM CMV cho thấy giảm độ thanh thài vàng da sau phẫu thuật Kasai.
Toxic – Phân ứng viêm trung gian toxin.
Nguyên nhàn do gen – Các yếu tố do gen có thế đóng vai trò là nguyên nhân gây bệnh ờ một nhóm nhỏ các bệnh nhân BASM: các biến thế gen CFC1. PKD1L1. F0XA2
Nguyên nhân miễn dịch – Rối loạn miễn dịch, bệnh lý nguyên phát hoặc là kết quả của tình trạng nhiễm trùng hoặc kích hoạt gen, được chỉ ra trong vài nghiên cứu.
ĐẶC ĐIỂM LÂM SÀNG
Hầu hết trẻ BA sinh đủ tháng có cân nặng bình thường và giai đoạn đầu phát triển gần như giống với trẻ khỏe mạnh.
Biếu hiện chu sinh – Hầu hết trẻ BA có kết quả theo dõi sau sinh bình thường bao gôm cả siêu ám. Thinh thoảng siêu ám sau sinh phát hiện bất thường gợi ý BA, bao gôm nang ờ rốn gan hoặc hội chứng heterotaxy.
Nếu các dấu hiệu này hiện diện, đứa trẻ nên được đánh giá thêm qua siêu âm sau sinh và theo dõi các xét nghiệm sinh hóa cũng như lâm sàng trong vài tuần đầu và vài tháng đàu, đặc biệt là tăng bilirubin liên hợp.
Dấu hiệu và triệu chứng
- Vàng da là dấu hiệu đầu tiên cùa BA. Ban đầu, có thế chì xuất hiện vàng củng mạc. Khỏi phát vàng da theo thời gian từ lúc sinh đến 8 tuần tuổi.
- Một số trẻ có phân bạc màu. Phân bạc màu thường không được phát hiện vì phân nhạt nhưng không trắng và màu phân có thể biến đổi.
- Hầu hết trẻ tiểu sậm màu vì tiết quá nhiều bilirubin trong nước tiểu. Bố mẹ hoặc người chăm sóc có thể không phát hiện tiểu sậm màu là bất thường ở trẻ nhũ nhi.
- Nếu vàng da diễn tiến không phát hiện ra và bệnh lý đứa trẻ diễn biến, gan to, chắc và lách to.
Xét nghiệm
- Đứa trẻ có triệu chứng – Khi là xét nghiệm ở trẻ sau khi đến khám vì một trong những triệu chứng trên, ghi nhận tình trạng tăng bilirubin trực tiếp và/hoặc liên hợp và tăng men gan nhẹ hoặc trung bình, với tăng GGTP (gamma-glutamyl transpeptidase) không phù hợp, Nếu rối loạn đông máu biếu hiện tại thời điểm chấn đoán, khả năng là do thiếu vitamin K.
- Đứa trẻ chưa có triệu chứng – Các xét nghiệm được thực hiện ngay sau sinh (trước khi đứa trẻ phát triển triệu chứng do BA), tâng nhẹ bilirubin liên hợp được tìm thấy. Các nghiên cứu đề xuất những đứa trẻ có tăng bilirubin trực tiếp hoặc liên hợp trong giai đoạn chu sinh nên được theo dõi sát và đánh giá khả năng BA.
ĐÁNH GIÁ
Ờ đứa trẻ nghi ngờ BA nên được đánh giá càng sớm càng tót vì can thiệp phẫu thuật thành công tùy thuộc vào thời điểm phẫu thuật Kasai.
Đánh giá bao gồm các xét nghiệm huyết thanh, nước tiểu và hình ảnh học. Đề xuất xét nghiệm theo thứ tự ưu tiên dựa vào các test cho bệnh lý có thể điều trị trước, như tắc nghẽn đường mật, nhiễm trùng, và một số bệnh lý chuyển hóa. Bởi vì thời điểm phẫu thuật là quan trọng ở trẻ BA, đánh giá nên được hoàn thiện càng nhanh càng tốt, và thỉnh thoảng cần phẫu thuật thăm dò, kể cả nếu tất cả các xét nghiệm chưa về. Trong thực hành lâm sàng chúng tôi thường tiến hành từng bước nếu đứa trẻ dưới 6 tuần tuổi. Đối với những trẻ từ 6 tuần tuổi trở lên, chúng tôi cố gắng đánh giá đầy đủ càng nhanh càng tốt (eg 3-4 ngày). Một số bệnh như hội chứng Alagille hoặc thiếu alpha-1-antitrypsin có thể biểu hiện tương tự như BA.
Xét nghiệm – Đánh giá tình trạng ứ ở trẻ nhỏ bao gồm xét nghiệm máu để đánh giá chức năng gan và loại trừ bệnh lý chuyến hóa và các nguyên nhân khác.
Siêu âm bụng – Đánh giá giải phẫu đường mật bắt đầu với siêu âm. Công dụng của siêu âm để loại trừ các bất thường giải phẫu gây ứ mật (ie, nang đường mật, giãn đường mật trong gan, và sỏi mật). Ngoài ra, nhiều dấu hiệu (nếu biểu hiện) hỗ trợ chẩn đoán BA, bao gồm không có túi mật hình ảnh túi mật thành không đều, hoặc đa lách. Protocol siêu âm được áp dụng, ngoài các đặc điểm nêu trên, để hỗ trợ chẩn đoán BA còn bao gồm “triangular cord” sign, co bóp túi mật, không có ống mật chủ, và lớn hạch rốn gan.
Sinh thiết gan – Chúng tôi thực hiện sinh thiết gan ờ phần lớn trẻ nghi ngờ BA vì hai lý do. Thứ nhất vì mục đích xác định các thay đổi trên mô bệnh học phù hợp với tác nghẽn xem xét phẫu thuật thăm dò. Thứ hai là để phân biệt BA với các nguyên nhân khác gây ứ mật trong gan, không cần phẫu thuật thăm dò.
Chụp đường mật – Nếu các bước trên đánh giá hỗ trợ chẩn đoán BA, đứa trẻ nên được phẫu thuật Bước đầu tiên là chụp đường mật trong phẫu thuật – tiêu chuẩn vàng trong chẩn đoán BA.
CHẨN ĐOÁN
Nghi ngờ BA dựa vào biểu hiện tăng bilirubin liên hợp ở trẻ sơ sinh và/hoặc phân bạc màu. Nghi ngờ BA cần làm các xét nghiệm (thường là siêu âm, xạ hình gan mật, và sinh thiết gan). Chẩn đoán xác định dựa vào chụp đường mật trong mổ.
PHẪU THUẬT KASAI
Nếu xác định BA qua chụp đường mật, phẫu thuật Kasai (HPE) nên được thực hiện ngay. Phẫu thuật này nhằm nỗ lực tái lưu thông dịch mật từ gan xuống ruột non.
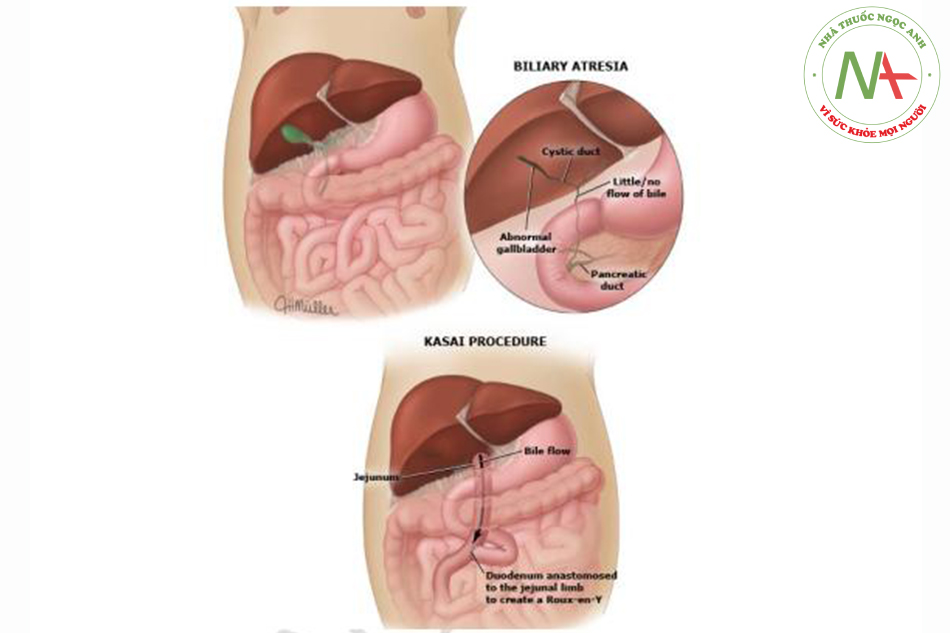
Trong thủ thuật này, quai ruột Roux-en-Y được bác sĩ phẫu thuật tạo ra và trực tiếp nối với rốn gan, sau đó cắt bỏ phần tàn dư đường mật và portal fibrous plate.
Nếu phẫu thuật HPE thành công, còn một phần lưu thông dịch mật chảy vào quai Roux và vàng da sẽ bắt đàu khỏi dan trong vài tuần sau phẫu thuật Ké cả nếu lưu thông dịch mật và cài thiện được tình trạng ứ mật, nhiều bệnh nhân bệnh lý gan tiến triển chậm dù đã phẫu thuật Kasai HPE và phần lớn bệnh nhân BA cuối cùng cân ghép gan. ít nhất 50% bệnh nhân trài qua HPE cần ghép gan lúc 2 tuổi vì suy HPE nguyên phát và/hoặc chậm lớn.
Nếu HPE không thành công, dịch mật không lưu thông và đứa trẻ vẫn vàng da, Nếu vàng da dai dẳng hoặc tăng bilirubin huyết thanh 3 tháng sau thủ thuật, bệnh nhân nên được đánh giá ghép gan.
=> Đọc thêm: COVID-19 đồng mắc với Toan ông Lượn Xa thoáng qua ở Trẻ nhũ nhi.
ĐIỀU TRỊ SAU PHẪU THUẬT
Điều trị nội khoa sau phẫu thuật Kasai HPE bao gồm các can thiệp sau:
- Lợi mật (choleretics)
- Cung cấp dinh dưỡng
- Bố sung vitamin tan trong dầu
- Phòng ngừa viêm đường mật
- Điều trị tăng áp cừa và hậu quà của nó
Bang chứng lâm sàng không hỗ trợ việc dùng glucocorticoids thường quy trong diều trị BA.
Lợi mật – Chúng tôi đề xuất điều trị bệnh nhân với ursodeoxycholic acid (ƯDCA) sau phẫu thuật Kasai HPE. ƯDCA là acid mật tan trong nước; dùng đường uống, nó làm thay đói cân bằng acid mật vè dạng tan trong nước. Điều này được cho là giúp ón định màng và giảm hình thành các free radicals, do đó bảo vệ ty thế khỏi sự phá hủy.
Khuyến cáo liều UDCA trong BA từ 15 đến 30 mg/kg/ngày và không nên quá 30 mg/kg/ngày. Đề tránh ngộ độc, điều trị UDCA nên ngưng nếu bilirubin toàn phần tăng trên 15 mg/dL (257 micromol/L).
Glucocorticoids (không chứng minh được lợi ích) – Bằng chứng lâm sàng không hỗ trợ việc dùng glucocorticoid thường quy trong điều trị BA. RCT nghiên cứu điều trị glucocorticoid ờ 140 trè BA. Glucocorticoids dược cho trong 13 tuàn (methylprednisolone 4 mg/kg/ngày TM trong 2 tuần, sau đó prednisolone 2 mg/kg/ngày đường uống trong 2 tuần, sau đó giâm liều dần), và kết quà được ghi nhận ờ thời điếm 6 tháng và 24 tháng sau HPE. Không có ý nghĩa thống kê về lợi ích cùa lưu thông mật ờ thời điếm 6 tháng sau HPE ờ nhóm trẻ được điều trị glucocorticoids so vói nhóm giả dược. Sau HPE, đứa trè được điều trị với glucocorticoid chậm phát trién các thòng số (chiều cao, cân nặng và vòng đầu) ờ thời điếm 6 tháng sau HPE.
Dinh dưỡng – Vấn đề dinh dưỡng trong BA là thường gặp và còn nhiều khó khăn. Dinh dưỡng kém là vấn đề lâm sàng đáng kể và là một trong những chì định thường gặp nhất của ghép gan.
Nhu cầu caloric – Nhiều yếu tố góp phần gây suy dinh dưỡng ở bệnh nhân BA, bao gồm chán ăn, kém hấp thu do thiếu muối mật đáng kế trong lòng ruột, và viêm gan mạn tính. Vì rối loạn hấp thu và thay đổi chuyển hóa, nên tăng năng lượng cần ờ trẻ nhũ nhi BA khoảng 130-150% nhu cầu năng lượng bình thường. Để bù trừ cho lượng mất và dị hóa, protein cần lên đến 3-4 g/kg/ngày ờ trẻ nhũ nhi và 2-3 g/kg/ngày ờ trẻ nhỏ.
Bố sung vitamin tan trong dầu – Tát cà trẻ vàng da có BA nên được bố sung các vitamins tan trong dầu. Khi hết vàng da, ngừng vitamin cung cấp, đứa trẻ có thể chuyển sang multivitamins. Theo dõi lượng vitamin thường quy. Lượng vitamin nên được theo dôi thường xuyên (ie, nhiều lần trong năm đầu tiên), bắt đầu trong tháng đàu tiên sau HPE, để điều chinh lượng bố sung phù họp và tránh ngộ độc.
Các biến chứng – Đứa trẻ lưu thông dịch mật sau HPE phải được theo dõi sát các biến chứng, đặc biệt là viêm đường mật lên và tăng áp cửa. Ngoài ra, tất cà các bệnh nhân nên được theo dõi thường quy lượng vitamin tan trong dầu, như được đề cập ờ trên.
Viêm đường mật – Viêm đường mật là biến chứng thường gập nhất ờ những bệnh nhân BA đã trài qua phẫu thuật Kasai HPE thành công. Tỉ lệ viêm đường mật ờ những bệnh nhân này từ 40 đến 90%, phần lớn bệnh nhàn trải qua ít nhất 1 đợt trước khi được 2 tuổi. Những bệnh nhân này tăng nguy cơ viêm đường mật vì bất thường giải phẫu và ứ đọng vi khuấn ờ vùng quai Roux. Bác sĩ lâm sàng nên đặt chỉ số nghi ngờ cao với viêm đường mật ờ những trẻ biểu hiện sốt mà không có ổ nhiễm trùng rõ ràng, đặc biệt nếu sốt kèm theo phân bạc màu, quấy khóc và xét nghiệm bất thường. Ngược lại, bệnh nhân phẫu thuật Kasai không thành công (ie, dịch mật không lưu thông) có nguy cơ thấp viêm đường mật nhưng vẫn có nguy cơ nhiễm trùng khác và sepsis.
Bởi vì viêm đường mật có thể đe dọa tính mạng và có thể ảnh hường đến kết cục ngán hạn và dài hạn, hầu hết các bác sĩ lâm sàng kê kháng sinh dự phòng trong ít nhất một năm sau phẫu thuật Kasai. Một thử nghiệm nhỏ không ngẫu nhiên cho thấy lợi ích kháng sinh dự phòng nhiều hơn nguy cơ đề kháng kháng sinh. Trimethoprim-sulfamethoxazole (4 mg/kg/ngày trimethoprim và 20 mg/kg/ngày sulfamethoxazole) hoặc neomycin (25 mg/kg/ngày chia 4 làn hàng ngày) cho thấy hiệu quả tương đương trong giảm ti lệ viêm đường mật.
Viêm đường mật tái phát có thể dự đoán nhu cầu ghép gan vì nó có thể gây xơ gan tiến triển: tuy nhiên, một đợt viêm đường mật không phải là yếu tố dự đoán ghép gan sớm.
Tăng áp cửa và xuất huyết do vỡ giãn tĩnh mạch thực quàn – Viêm gan mật mạn tính trong BA dẫn đến xơ gan tiến triển. Xơ gan gây tâng áp cửa. dẫn đến giãn tĩnh mạch thực quản và báng bụng.
- Biếu hiện lâm sàng – Phát triển lách to và/hoặc giảm tiểu cầu sau phẫu thuật Kasai HPE gợi ý tăng áp cửa. Ở một số bệnh nhân, tăng áp cửa lần đầu tiên được ghi nhận khi trẻ biểu hiện xuất huyết tiêu hóa trên do vỡ giãn tĩnh mạch thực quản.
- Theo dõi:
- Khám lâm sàng và xét nghiệm – Đánh giá sự phát triến lách to và theo dôi số lượng tiểu cầu là quan trọng để phát hiện tình trạng tăng áp cửa. Điều này sẽ không đáng tin cậy ờ những bệnh nhân vô lách hoặc đa lách.
- Nội soi – Một số trung tâm thực hiện nội soi để đánh giá kích thước và tình trạng giãn ờ những bệnh nhân có biểu hiện lâm sàng và siêu âm gợi ý tăng áp cửa sau phẫu thuật Kasai. Các trung tâm khác chi bắt đầu nội soi sau khi bệnh nhân bắt qua một đợt xuất huyết tiêu hóa do vỡ giãn. Không có bằng chứng beta blockers ngân ngừa hoặc làm chậm tiến triển giãn tĩnh mạch thực quản.
- Điều trị – Nội soi thắt (ablation) tĩnh mạch giãn nhìn chung được khuyến cáo sau lần xuất huyết đầu tiên (dự phòng thứ phát). Bệnh nhân biểu hiện xuất huyết cấp tính do vỡ giãn nên được bù dịch hồi sức để ổn định huyết động. Ngoài ra, điều trị các thuốc vasoactive (eg, octreotide) có thể bắt đầu trước khi nội soi. Tĩnh mạch giãn có thể được thắt hoặc chích xơ.
Dự phòng nguyên phát (nội soi thất TM thực quàn giãn trước khi có xuất huyết tiêu hóa do vỡ giãn tình mạch lần đàu) nhìn chung không được khuyến cáo, vi khỏng có lợi ích trong cài thiện ti lệ tử vong.
Báng bụng thường gặp ở trẻ BA đợi ghép gan và thường được điều trị với lợi tiểu. Chọc hút có thể cần trong những trường hợp kháng trị.
GHÉP GAN
Phần lớn trẻ BA cuối cùng cần ghép gan: BA là chỉ định thường gặp nhất trong ghép gan ở trẻ nhũ nhi và trẻ nhỏ. Trong các dữ liệu gần đây, ít nhất 60 đến 80% bệnh nhân BA cần ghép gan, kế cả điều trị tối ưu.
Chi định ghép gan ờ những bệnh nhân BA bao gồm:
- Primary failure (không lưu thông dịch mật) sau phẫu thuật Kasai:
- Đánh giá ghép gan ngay nếu bilirubin toàn phần > 6 mg/dL (100 micromol/L) trên 3 tháng sau HPE.
- Đánh giá ghép gan nên được xem xét nếu bilirubin toàn phần từ 2 đến 6 mg/dL (34 đến 100 micromol/L) dai dắng từ 3 tháng trỡ lên sau HPE.
- Chậm lớn dai dẳng – Ghép gan nên được xem xét ờ những trẻ chậm lớn vừa hoặc nặng không đáp ứng sau điều trị dinh dưỡng tích cực.
- Biến chứng tăng áp cửa (nếu không thể điều trị bằng các biện pháp khác):
- Xuất huyết tiêu hóa do giàn vỡ tình mạch thực quàn tái phát.
- Báng bụng kháng trị gây suy hô hấp, chèn lên ruột, hoặc chức năng thận.
- Hội chứng gan phổi.
- Tăng áp cửa-phổi.
- Rối loạn chức năng gan tiến triển:
- Intractable pruritus.
- Rối loạn đông máu dai dẳng.
- Nhiễm trùng đường mật tái phát cần điều trị kháng sinh tĩnh mạch kéo dài và cần đặt đường truyền tĩnh mạch trung tâm hoặc ngoại vi.
- HCC không di căn ngoài gan (rất hiếm)
=> Tham khảo thêm: Hướng dẫn điều trị Viêm Thận Lupus ở Trẻ em.