Bệnh hô hấp, COVID-19
Sử dụng huyết tương phục hồi điều trị COVID-19
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
Biên soạn: ThS. BS. Đào Thị Mỹ Vân.
1. TỔNG QUAN
Kể từ những năm 1890, liệu pháp kháng thể thụ động đã được sử dụng thành công để điều trị các bệnh truyền nhiễm. Trước khi có sẵn các kháng thể đơn dòng và các sản phẩm gamma globulin, liệu pháp miễn dịch thụ động dựa vào việc sử dụng các chế phẩm của máu được thu thập từ những người hiến tặng có bệnh đã hồi phục dùng điều trị dự phòng sau phơi nhiễm và điều trị bệnh. Việc đưa vào cơ thể người bệnh kháng thể thụ động của các tác nhân gây bệnh được hình thành từ trước là chiến lược hiệu quả duy nhất mang lại sự bảo vệ ngay lập tức. Do đó, cho đến khi vaccine được bao phủ rộng rãi, huyết tương hồi phục (HTHP) có khả năng khởi phát và tăng cường miễn dịch cho bệnh nhân nhiễm bệnh, ngăn chận tiến triển của bệnh, cải thiện lâm sàng đưa đến giảm gánh nặng bệnh tật trong các đại dịch.
Giải Nobel Sinh lý học và Y học đầu tiên năm 1901 được trao cho Emi Adolf von Behring cho công trình của ông về liệu pháp huyết thanh, đặc biệt là ứng dụng của nó chống lại bệnh bạch hầu. Việc sử dụng huyết thanh miễn dịch đã nhận được sự ủng hộ trên toàn thế giới và trở thành một phương pháp điều trị mang tính cách mạng.
Trong hơn một thế kỷ qua, huyết tương hồi phục đã được sử dụng tại nhiều quốc gia trong trận dịch cúm Tây Ban Nha 1918-1920, H1N1 2009-2010, Ebola 2013 ở Tây phi, SARS-CoV-1; H5N1 năm 2003 và MERS-CoV năm 2012. Đã có nhiều nghiên cứu báo cáo nêu rõ hiệu quả lâm sàng của liệu pháp huyết tương hồi phục liên quan đến các trận đại dịch nói trên.
Trong đại dịch COVID-19 này, ngày 23/08/2020 Cục Quản lý thực phẩm và dược phẩm Hoa Kỳ – FDA cũng đã cấp Giấy Phép Sử Dụng Khẩn Cấp cho huyết tương hồi phục để điều trị COVID-19. Theo đó, nhiều quốc gia trên thế giới đã sử dụng huyết tương hồi phục điều trị COVID-19. Các trung tâm thu thập máu từ khắp nơi trên thế giới đã thành lập các chương trình cho những người sống sót sau khi nhiễm bệnh COVID-19 để hiến huyết tương. Bên cạnh đó, các cơ quan quản lý của Hoa Kỳ, nhiều quốc gia châu Âu cũng đã cung cấp khả năng tiếp cận rộng rãi huyết tương hồi phục để sử dụng cho bệnh nhân nhập viện vì COVID-19.
Không phải chỉ tại Việt Nam hay các nước đang phát triển mà tại khắp nơi trên thế giới, khi vaccin chưa phủ đủ, các thuốc kháng vi rút, các immunoglobulin tiêm mạch (IVIG), các kháng thể đa dòng, kháng thể đơn dòng còn khan hiếm do quy trình sản xuất phức tạp, giá thành đắt đỏ, không phải lúc nào cũng sẵn có, trong các trận đại dịch bùng phát, huyết tương hồi phục là lựa chọn đầu tiên làm vũ khí mạnh mẽ chống lại không chỉ bệnh COVID-19 mà còn các bệnh truyền nhiễm khác.
2. TỔNG HỢP KẾT QUẢ CÁC NGHIÊN CỨU TRÊN THẾ GIỚI VỀ SỬ DỤNG HUYẾT TƯƠNG HỒI PHỤC TRONG ĐIỀU TRỊ COVID-19
2.1. Cơ chế xâm nhập và gây tổn thương tế bào vật chủ của virus SARS-CoV-2
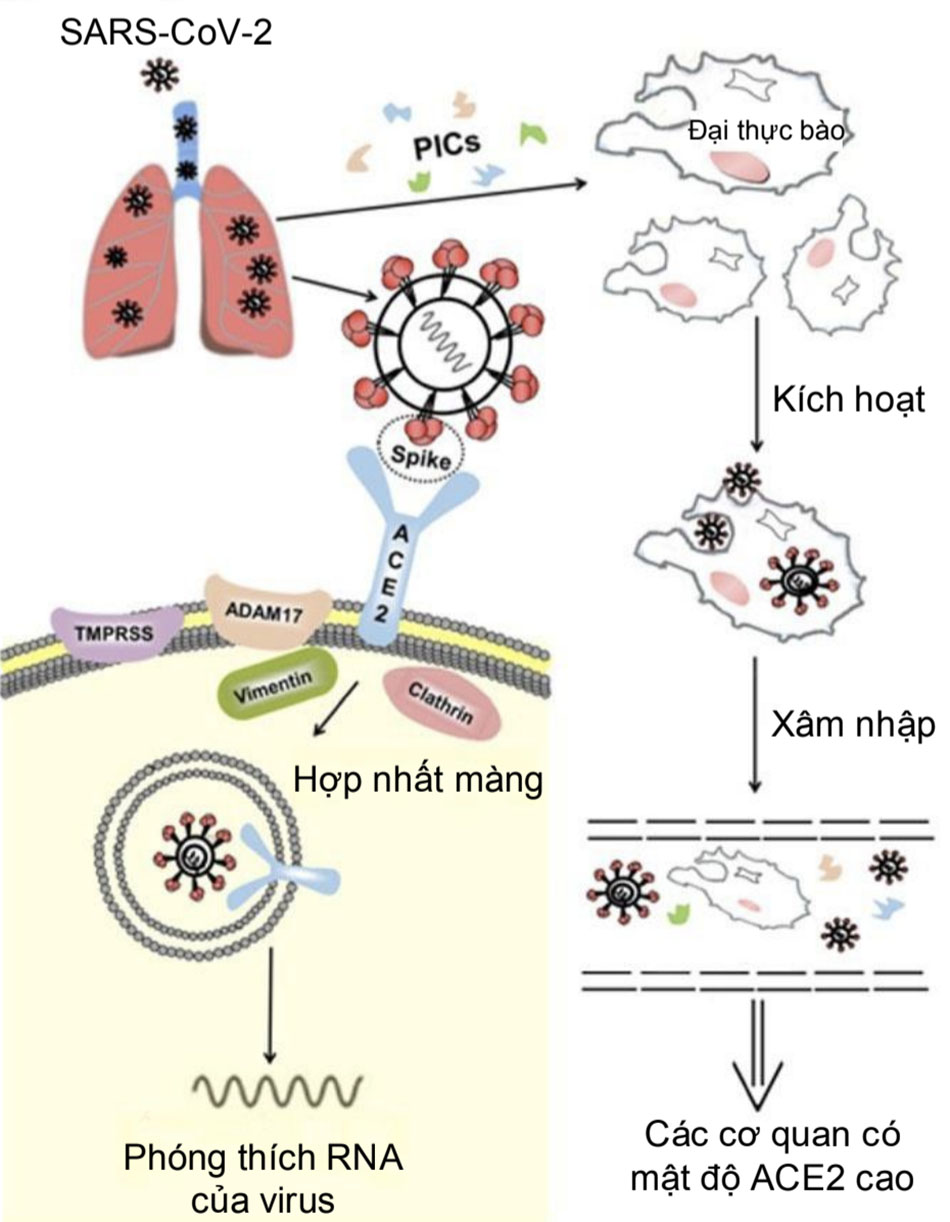
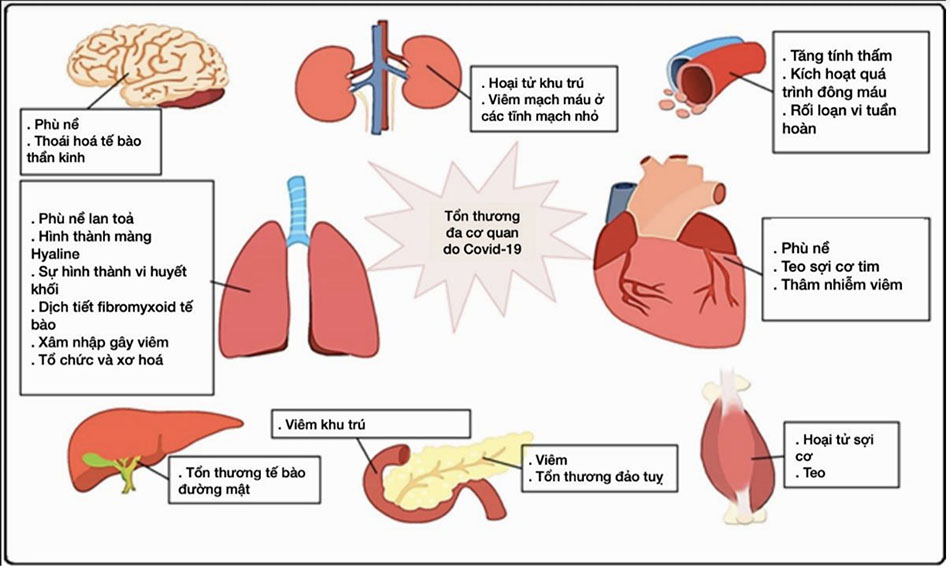
Trên các protein gai của virus SARS-CoV-2 có chứa một vùng được gọi là vùng gắn thụ thể (Receptor- Binding Domain-RBD), vùng này đặc biệt quan trọng để virus xâm nhập vào tế bào người. Tại đây, SARS-CoV-2 gắn với với thụ thể ACE2 (Angiotensin-converting enzyme 2) là enzym chuyển đổi Angiotensin 2 của tế bào vật chủ với ái lực cao để xâm nhập vào bên trong tế bào. SARS-CoV-2 có khả năng gắn với ACE2 cao hơn 10 đến 20 lần so với các chủng SARS-CoV khác. SARS-CoV-2 xâm nhập vào phổi, nơi glycoprotein đột biến của virus liên kết với ACE2 trên tế bào, cho phép virus xâm nhập vào tế bào. Một số proteinase xuyên màng, chẳng hạn như protease xuyên màng serine 2 (TMPRSS2) và vùng phân rã metallopeptidase 17 (ADAM17) cũng tham gia vào quá trình này. Ví dụ, SARS-CoV-2 có thể sử dụng TMPRSS2 để kích hoạt protein tăng đột biến trong các dòng tế bào. Các tế bào bị nhiễm và các tế bào viêm bị kích hoạt bởi các kháng nguyên virus có thể tạo ra các cytokine tiền viêm (pre-inflammatory cytokines-PICs) và chemokine để kích hoạt các phản ứng miễn dịch và phản ứng viêm để chống lại virus. Các không bào và và các đại thực bào đã nhiễm virus trong máu có thể di chuyển đến các cơ quan khác và lây nhiễm sang các tế bào của các cơ quan có mật độ thụ thể ACE2 cao. [Hình 1]
Tùy theo mức độ xâm nhập vào tế bào chủ và tốc độ tăng sinh trong cơ thể vật chủ sau khi xâm nhập, SARS-CoV-2 gây ra nhiều dạng của biểu hiện lâm sàng từ trạng thái mang mầm bệnh không triệu chứng đến suy đa cơ quan nghiêm trọng. [Hình 2].
2.2. Thành phần huyết tương hồi phục
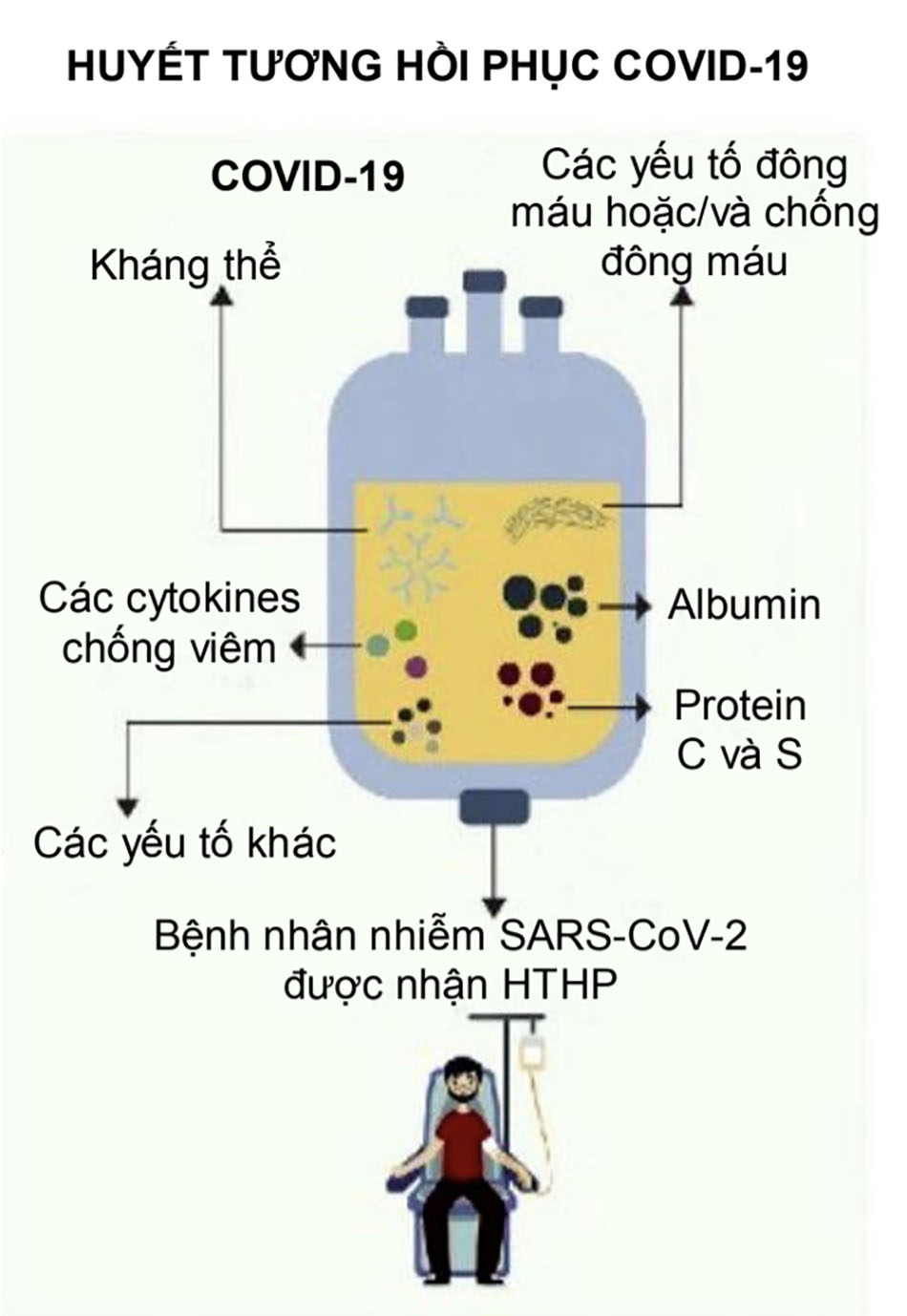
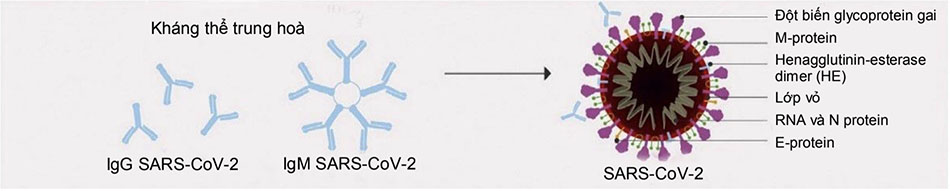
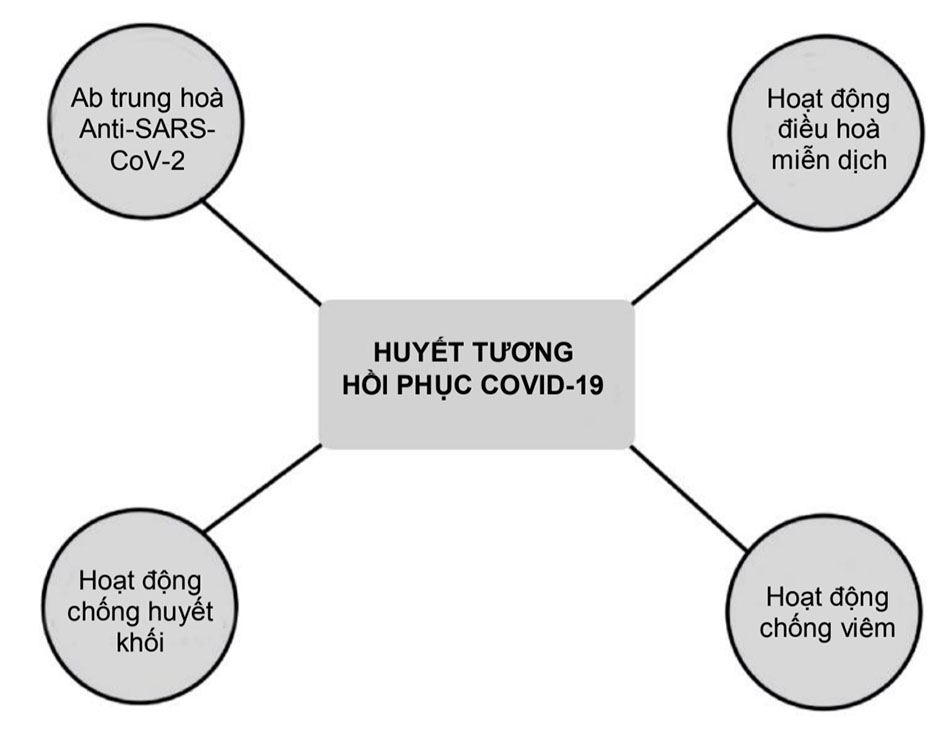
Thành phần của HTHP có thể thay đổi và bao gồm nhiều thành phần khác nhau có nguồn gốc từ máu, bao gồm hỗn hợp muối vô cơ, hợp chất hữu cơ, nước và hơn 1000 protein. Thành phần protein trong huyết tương bao gồm: albumin, kháng thể trung hòa là các immunoglobulin, bổ thể, yếu tố đông máu, các yếu tố chống huyết khối và nhiều yếu tố khác. Một số nghiên cứu ghi nhận huyết tương từ những người hiến tặng khỏe mạnh có tác dụng điều hòa miễn dịch nhờ vào các cytokines chống viêm và các kháng thể, là những chất có vai trò ngăn cản bổ thể, chống các cytokines gây viêm và kháng thể tự thân. [Hình. 3]
2.3. Cơ chế tác dụng chống viruscủa huyết tương hồi phục
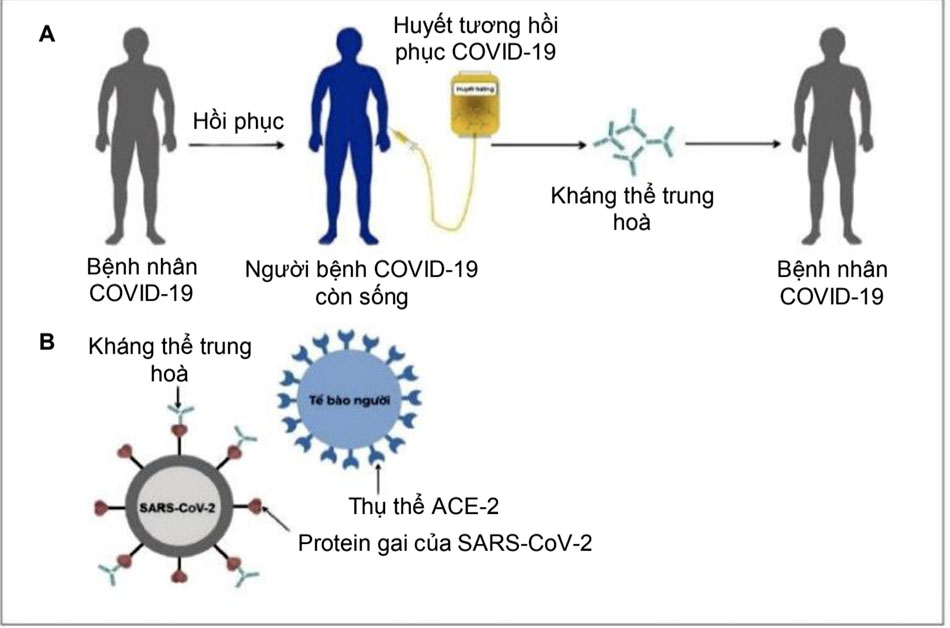
Trong huyết tương hồi phục hiến tặng từ người bệnh đã hồi phục có chứa các kháng thể trung hòa đặc hiệu đối với SARS-CoV-2 như là tác nhân hoạt động chính giúp người bệnh chống lại virus nhờ vào họat động của các kháng thể trung hòa qua cơ chế kháng thể trung hòa gắn vào virus, bất hoạt chúng, hạn chế virus xâm nhập vào tế bào vật chủ và tăng cường thanh thải virusra khỏi cơ thể thông qua quá trình thực bào và/hoặc hoạt hóa bổ thể. Qua cơ chế miễn dịch tế bào và dịch thể trực tiếp và gián tiếp, huyết tương hồi phục có tác dụng khởi phát và tăng cường đáp ứng miễn dịch, giảm thiểu cơn bão Cytokin, cải thiện diễn tiến bệnh, giảm tỷ lệ bệnh nặng và giảm tỷ lệ tử vong. [Hình 4]
2.3.1. Tác dụng chống viêm và điều hòa miễn dịch
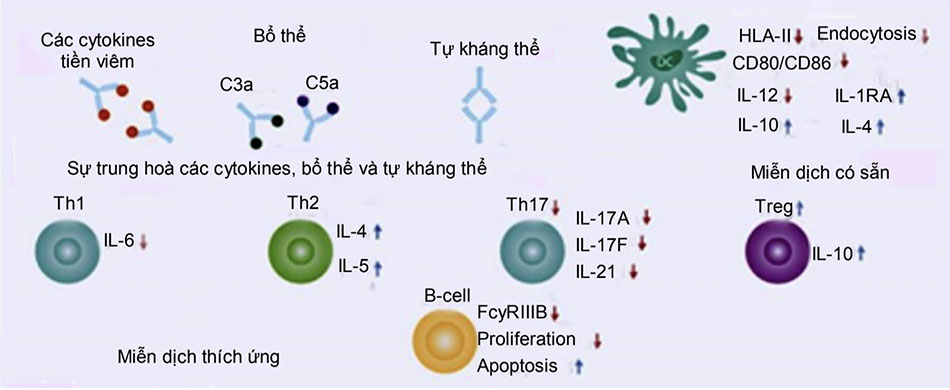
Tác dụng điều hòa miễn dịch: thông qua cơ chế gắn với vùng liên kết thụ thể protein gai (S1-RBD) của virus, các kháng thể trung hòa IgG ức chế sự xâm nhập của virus và ngăn cản sự tăng các đột biến protein gai, do đó có vai trò quan trọng trong việc loại bỏ virus và cần thiết trong việc bảo vệ cơ thể chống lại các bệnh do virus gây ra. Bên cạnh tác dụng trung hòa trực tiếp, các kháng thể không trung hòa IgG có trong HTHP cũng có thể đóng một vai trò trong việc tăng cường khả năng phục hồi ở bệnh nhân COVID-19, chủ yếu qua trung gian phân đoạn bất định (Fc) có vai trò diệt khuẩn, bao gồm gây độc tế bào phụ thuộc vào kháng thể (antibody-dependent cellular cytotoxicity-ADCC), thực bào tế bào phụ thuộc vào kháng thể (antibody-dependent cellular phagocytosis-ADCP) và gây độc tế bào phụ thuộc vào bổ thể (complement- dependent cytotoxicity- CDC) [Hình 5]
Tác dụng chống viêm: sử dụng HTHP làm giảm đáng kể các chỉ số CRP, TNF alpha và Interleukin-6 do đó làm giảm phản ứng siêu viêm bất lợi. Đây có thể là kết quả của việc trung hòa virus mà cũng có thể từ tác động chống viêm của một số yếu tố không phải globulin miễn dịch có trong HTHP theo ghi nhận từ một số nghiên cứu. Cụ thể, trong một số nghiên cứu cho thấy trong HTHP có chứa mức độ cao của các cytokines chống viêm mạnh là interleukin-10 và interleukin-21 có vai trò quan trọng trong tạo tế bào huyết tương và đáp ứng miễn dịch kháng vi rút.
2.3.2. Tác dụng chống huyết khối
Vai trò của antithrombin III: COVID-19 đã được công nhận gây ra rối loạn đông máu toàn thân. Các cơ chế phân tử cơ bản của tình trạng tăng đông được quan sát thấy ở bệnh nhân COVID-19 vẫn chưa được hiểu hoàn toàn, dường như có mối liên hệ chặt chẽ giữa hệ thống viêm và cầm máu. Nhiễm SARS-CoV-2 tạo ra rối loạn chức năng nội mô và phản ứng viêm toàn thân dẫn đến sự mất cân bằng nội mô giữa hai hệ thống đông máu và chống đông máu. Sự tăng cao của các cytokine tiền viêm trong bệnh COVID-19 hoạt hóa yếu tố VII, kích hoạt đường đông máu ngoại sinh, chuyển fibrinogen thành fibrin. Đồng thời với quá trình tăng đông là trạng thái giảm tiêu sợi huyết, gây ra do virus SARS-CoV-2 ức chế trực tiếp t-PA là chất hoạt hóa plasminogen mô và u–PA là chất hoạt hóa plasminogen urokinase. Cả hai tiến trình song song này tạo ra một vòng lẩn quẩn làm tăng tiến trình tạo huyết khối. HTHP được xem có thể cải thiện tình trạng tăng đông ở bệnh COVID-19 do chứa các yếu tố chống đông máu và đông máu bình thường trong một tỷ lệ sinh lý cân bằng. HTHP là nguồn có giá trị của một số protein huyết tương đóng vai trò chủ yếu trong quá trình cầm máu đó là antithrombin III và albumin. Antithrombin III hoạt động bằng cải thiện hiệu quả của heparin, một trong những nền tảng quan trọng trong điều trị COVID-19 hiện tại. Sự tụt giảm của antithrombin III trong bệnh COVID-19 thể nặng là yếu tố thúc đẩy thành lập huyết khối, một số nghiên cứu đã ghi nhận vai trò tích cực của antithrombin III hiện diện trong HTHP có vai trò ngăn chận biến chứng nguy hiểm này.
Vai trò của albumin: việc bổ sung albumin làm giảm tình trạng tăng đông máu ở bệnh nhân COVID-19. Một số nghiên cứu cho thấy nồng độ albumin cao hơn khi nhập viện có liên quan đến tỷ lệ thấp hơn các kết cục bất lợi bao gồm huyết khối tĩnh mạch, phát triển đến hội chứng suy hô hấp cấp tính (ARDS) và thời gan điều trị tại đơn vị chăm sóc đặc biệt (ICU) ở bệnh nhân COVID-19.
2.3.3. Tác dụng kháng virus trực tiếp
Vai trò của túi ngoại bào (EVs): Túi ngoại bào là một thành phần phổ biến có trong huyết tương người hiến tặng. EVs là các túi liên kết với lipid do tế bào tiết ra bên ngoài tế bào. Các EV tương hợp với ACE2 có thể hoạt động như các thụ thể mồi nhử vì các virion của virus SARS-CoV-2 gắn vào các EV này không thể hoàn thành một chu kỳ sao chép. Hơn nữa, EV từ huyết tương chứa một số phân tử sinh học khác như miRNA, protein/cytokine, lipid và glycan có thể làm thay đổi phản ứng miễn dịch đối với nhiễm SARS-CoV-2.
Vai trò của yếu tố đông máu Xa (FXa): FXa có trong thành phần của HTHP liên kết và phân cắt protein đột biến nhưng tạo ra kiểu phân cắt khác với kiểu phân cắt của furin và TMPRSS2 và ngăn chặn protein S liên kết với ACE2 vì vậy nó có vai trò kháng virus trực tiếp. Một ghi nhận là tác dụng kháng virus của FXa bị suy giảm bởi chất ức chế FXa trực tiếp rivaroxaban chứ không phải chất ức chế gián tiếp fondaparinux, cả in vivo và in vitro.
Vai trò kháng virus trực tiếp từ các kháng thể trung hòa phản ứng chéo: cơ sở cho các phản ứng miễn dịch dị hợp đối với SARS-CoV-2 có thể là do phản ứng chéo giữa các kháng nguyên bề mặt. Phản ứng chéo kháng nguyên có thể bắt nguồn từ việc tiếp xúc trước đó với nhiều loại mầm bệnh.
2.4. Những tiêu chí để tối ưu hiệu quả điều trị của huyết tương hồi phục
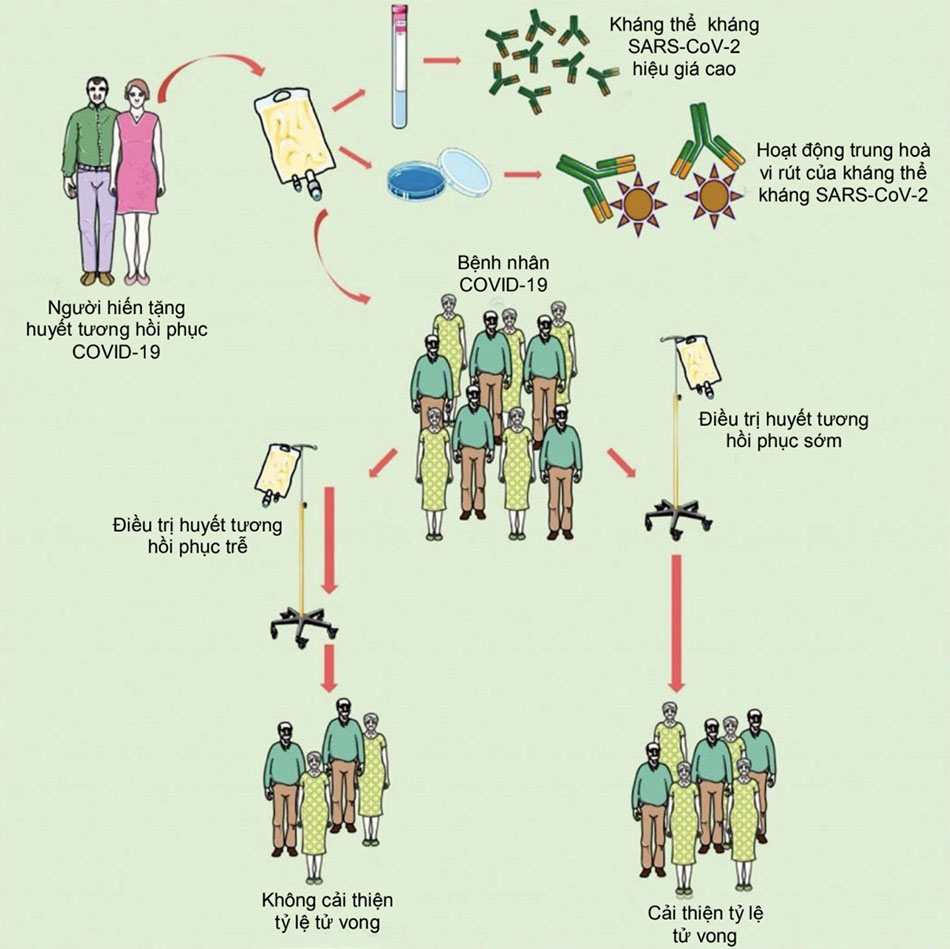
Sự tiến triển của bệnh COVID-19 qua 2 giai đoạn: giai đoạn đầu diễn ra sự sao chép cấp tính của virus, sau đó, trong trường hợp thanh thải virus không hiệu quả, giai đoạn thứ hai được biểu hiện bằng rối loạn phản ứng miễn dịch tiến triển đến siêu phản ứng viêm là nguyên nhân chính dẫn đến kết quả tồi tệ đưa đến rối loạn chức năng nhiều nội tạng và tử vong. Với mục tiêu ngăn cản sự xâm nhập vào tế bào vật chủ, hạn chế tăng sinh virus sau khi xâm nhập, thúc đẩy quá trình thanh thải virus, huyết tương hồi phục nên được cung cấp càng sớm càng tốt trong suốt quá trình lây nhiễm. Huyết tương hồi phục nên được truyền trong vòng 72 giờ từ khi có triệu chứng đầu tiên hay từ khi chẩn đoán xác định bệnh COVID-19. Đây được xem là tiêu chí quan trọng nhất để tối ưu hiệu quả điều trị. [Hình 8]
Hiệu giá kháng thể cao từ máu người hiến tặng có thể sẽ cho hiệu quả cao hơn so với máu người không được sàng lọc. Có thể phân biệt huyết tương hiệu giá kháng thể thấp hoặc cao dựa vào xét nghiệm định lượng kháng thể (bao gồm IgG) kháng miền liên kết thụ thể (RBD) trên protein s (S=Spike) của SARS-CoV2 trong huyết tương người.
2.5. Bằng chứng an toàn của huyết tương hồi phục
Ghi nhận từ hầu hết các báo cáo cho thấy trên tất cả bệnh nhân nhập viện được truyền huyết tương hồi phục an toàn không có biến chứng. Bằng chứng an toàn của truyền huyết tương hồi phục COVID-19 tương tự như bằng chứng an toàn đã biết của truyền huyết tương tươi đông lạnh.
Huyết tương hồi phục có thể sử dụng trên bệnh nhân suy thận, không tương tác với các thuốc khác, đặc biệt thích hợp với người cao tuổi.
2.6. Đối tượng bệnh nhân có chỉ định nhận huyết tương hồi phục
Bệnh nhân nhiễm COVID-19 từ 18-80 tuổi được chẩn đoán xác định bằng thử nghiệm phết mũi họng PCR real time dương tính, mức độ nhẹ đến trung bình có chỉ định truyền huyết tương hồi phục.
Bệnh nhân nhiễm COVID-19 không có triệu chứng cần cân nhắc trước khi quyết định truyền huyết tương hồi phục tùy theo bệnh lý đi kèm và khả năng tiến triển đến thể bệnh nặng của bệnh nhân.
Bệnh nhân nên được truyền huyết tương hồi phục trong vòng 72 giờ từ khi có chẩn đoán xác định hay có triệu chứng đầu tiên. Nếu không đủ điều kiện trên, bệnh nhân nên được truyền sớm nhất có thể. Bệnh nhân nhập viện trễ sau 72 giờ khởi phát bệnh, không có chống chỉ truyền huyết tương hồi phục nhưng hiệu quả điều trịsẽ thấp hơn.
Chống chỉ định: không có chống chỉ định tuyệt đối của huyết tương hồi phục. Người bệnh suy thận, suy tim cần hạn chế dịch truyền nên được bác sĩ lâm sàng cân nhắc trước truyền.
Bệnh nhân có bệnh lý nền đang điều trị bác sĩ lâm sàng nên tham khảo ý kiến bác sĩ chuyên khoa trước khi truyền huyết tương hồi phục.
Bệnh nhân COVID-19 thể nặng và thể nguy kịch có kèm hay không kèm theo biến chứng huyết khối giảm tiểu cầu cần cân nhắc kỹ lợi ích và rủi ro trước khi quyết đinh truyền huyết tương hồi phục
2.7. Những đối tượng có thể hiến tặng huyết tương hồi phục COVID-19
Bệnh COVID-19 người lớn được xác nhận khỏi bệnh khi có 2 lần xét nghiệm PCR real time âm tính cách nhau 24 giờ, không mắc các bệnh truyền nhiễm qua đường truyền máu, có thể hiến tặng huyết tương sau ít nhất 14 ngày kể từ ngày được xác định khỏi bệnh.
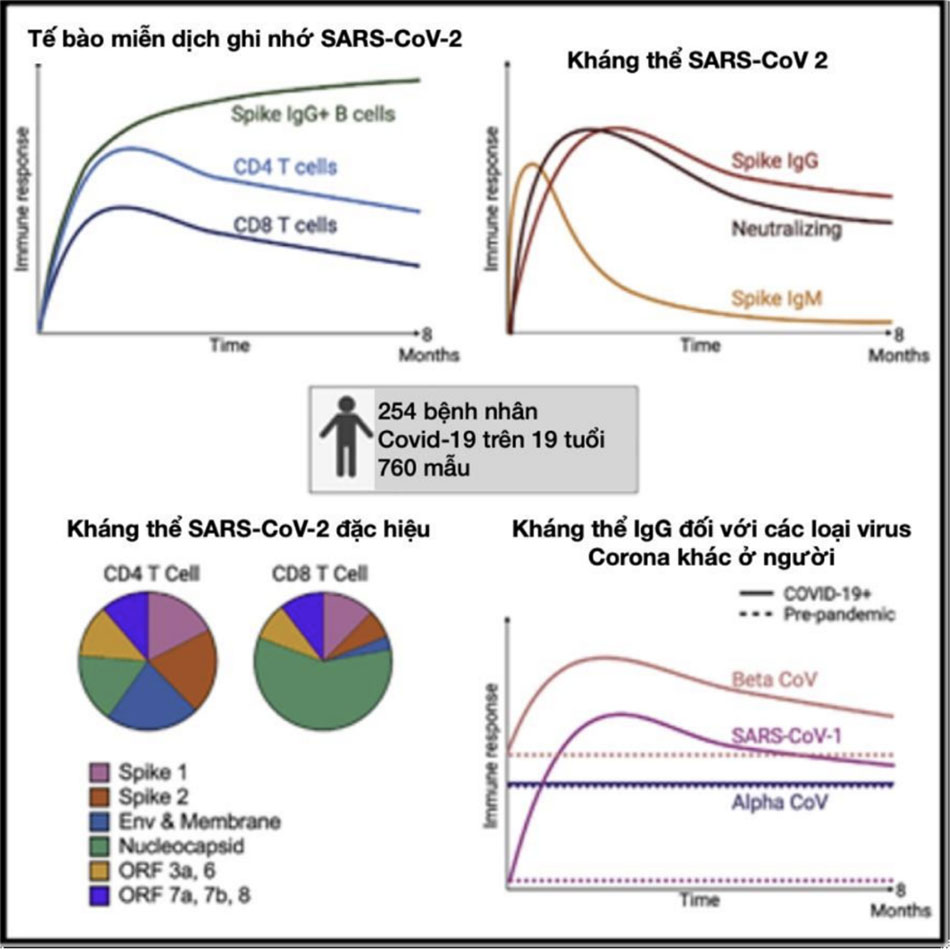
Kết quả từ các nghiên cứu cho thấy SARS-CoV-2 tạo ra một phản ứng miễn dịch mạnh mẽ với lượng kháng thể cao, bao gồm các globulin miễn dịch (IgM và IgG), tồn tại trong nhiều tháng sau khi khởi phát COVID-19. Mức độ kháng thể được phát hiện cao hơn sau bệnh nặng và giảm dần trong vòng 90 ngày sau khi khởi phát triệu chứng đối với thể bệnh nhẹ và tối đa lên đến 250 ngày theo một số nghiên cứu. Thời hạn tối đa cho phép người bệnh có thể tiếp tục hiến tặng huyết tương kể từ khi khỏi bệnh có thể kéo dài vài tháng sau khi khỏi bệnh. [Hình 9]
2.8. Hiệu quả kinh tế
Chi phí cho liệu trình điều trị với huyết tương hồi phục sẽ nhiều lần thấp hơn chi phí cho liệu pháp kháng virus với remdesivir và kháng thể đơn dòng (tocilizumab, casirivimab cộng với imdevimab…), tỷ lệ chi phí cho điều trị với huyết tương hồi phục trên chi phí cho liệu trình điều trị kháng virus cộng với kháng thể đơn dòng ước tính dưới 1/100, vì vậy huyết tương hồi phục được xem là giải pháp tiết kiệm.
Ngăn chặn diễn tiến đến thể bệnh nặng, nguy kịch, rút ngắn thời gian nằm viện, giảm đáng kể tỷ lệ nhập khoa ICU, huyết tương hồi phục có ý nghĩa lớn lao trong giảm gánh nặng tài chính quốc gia do đại dịch.
2.9. Xét nghiệm sàng lọc trước khi tiến hành hiến tặng huyết tương hồi phục
Người bệnh COVID-19 đã xác định khỏi bệnh ít nhất 14 ngày trước khi hiến tặng huyết tương bằng xét nghiệm PCR real tine COVID-19 âm tính 2 lần cách nhau 24 giờ.
Thực hiện các xét nghiệm thường quy trước khi hiến máu: nhóm máu ABO, Rh, xét nghiệm loại trừ bệnh lây nhiễm qua đường truyền máu: HIV, VGSV A B C và E, bệnh giang mai.
Định lượng kháng thể kháng SARS-CoV-2 để phân lập kháng thể hiệu giá cao hay thấp. Hiệu giá kháng thể đặc hiệu SARS-CoV-2 trong khoảng từ 1.800-16.200 và hiệu giá kháng thể trung hòa từ 80-480 là tiêu chuẩn chọn lọc được đề nghị.
2.10. Theo dõi các chỉ số huyết học và sinh hóa của người nhận huyết tương hồi phục
Trước và sau truyền huyết tương hồi phục người bệnh cần theo dõi các dấu hiệu lâm sàng, đánh giá nhu cầu oxy.
Cận lâm sàng trước truyền huyết tương hồi phục bao gồm: X-quang phổi, công thức máu toàn bộ, CRP, AST, ALT, creatinine, điện giải đồ máu, chức năng đông máu toàn bộ. Các xét nghiệm bổ sung tùy theo điều kiện tại cơ sở y tế và tình trạng lâm sàng của bệnh nhân bao gồm: tải lượng virus SARS-CoV-2, Ferritin, LDH, D.Dimer, Fibrinogen, Interleukin 6, yếu tố hoại tử khối u TNF α.
Đánh giá lại các xét nghiệm cận lâm sàng trên tại 3 thời điểm: (+1): ngày truyền HTHP; (+3): sau 3 ngày (72 giờ); (+7): sau 7 ngày và (+14): sau 14 ngày. Chỉ định thời điểm thực hiện và loại xét nghiệm có thể thay đổi tùy theo tình trạng lâm sàng và điều kiện của cơ sở y tế.
2.11. Liều lượng
Huyết tương tươi đông lạnh được hiến tặng từ người bệnh hồi phục sau nhiễm COVID-19 được khuyến cáo sử dụng mỗi lần từ 200-300ml, hoặc 3ml/kg cân nặng.
Quyết định truyền lập lại lần 2 hay lần 3 tùy thuộc vào diễn tiến lâm sàng và kết quả định lượng nồng độ các dấu ấn gây viêm, các chất tiền viêm cytokines sau truyền lần đầu tiên. Thông thường đáp ứng điều trị có được sau 72 giờ, biểu hiện qua cải thiện triệu chứng lâm sàng và giảm nồng độ của các chất chỉ điểm của phản ứng viêm.
3. KẾT LUẬN
Chẩn đoán COVID-19 nhanh chóng và sử dụng sớm huyết tương hồi phục được chuẩn độ kháng thể là át chủ bài chiến thắng COVID vì vô hiệu hóa virus, tăng cường đáp ứng miễn dịch, giảm tỷ lệ nhập viện, giảm tỷ lệ thể bệnh nặng – nguy kịch và giảm tỷ lệ tử vong.
Đại dịch COVID-19 thực sự là một trong sự kiện thảm khốc nhất trong lịch sử nhân loại. Các thuốc kháng virus đặc hiệu, các kháng thể đơn dòng và các thuốc điều trị hỗ trợ khác không thật sự mang lại kết quả lâm sàng tối ưu. Tại Việt Nam, trước tình trạng khan hiếm thuốc điều trị đặc hiệu, giá thành thuốc còn cao, huyết tương hồi phục là sản phẩm rẻ tiền, dễ có, sử dụng đơn giản, an toàn và hiệu quả cao. Vì thế triển khai sử dụng rộng rãi, kịp thời huyết tương hồi phục cho bệnh nhân COVID-19 giai đoạn này thực sự mang ý nghĩa CÁCH MẠNG và CỨU SINH.
TÀI LIỆU THAM KHẢO
1. Paola de Candia, Francesco Prattichizzo, Silvia Garavelli và cộng sự. Effect of time and titer in convalescent plasma therapy for COVID-19. [Truy cập trực tuyến] iScience; 2021. Đường dẫn: https://doi.org/10.1016/j.isci.2021.102898. [Truy cập ngày 18 tháng 9 năm 2021]
2. Romina Libster, M.D., Gonzalo Pérez Marc, M.D., Diego Wappner, M.D. và cộng sự. Early High-Titer Plasma Therapy to Prevent Severe Covid-19 in Older Adults. [Truy cập trực tuyến] N Engl J Med; 2021. Đường dẫn: https://www.nejm.org/doi/full/10.1056/NEJMoa2033700 [Truy cập ngày 19 tháng 9 năm 2021]
3. Massimo Franchini, MD; Claudia Glingani, BSc; Mario Morandi, PhD. và cộng sự. Safety and Efficacy of Convalescent Plasma in Elderly COVID-19 Patients: The RESCUE Trial. [Truy cập trực tuyến] Elsevier Inc.; 2021. Đường dẫn: https://doi.org/10.1016/j.mayocpiqo.2021.01.010 [Truy cập ngày 19 tháng 9 năm 2021]
4. Massimo Franchini, Giancarlo Maria Liumbruno. Convalescent Plasma for the Treatment of Severe COVID-19. [Truy cập trực tuyến] Dovepress; 2021. Đường dẫn: https://doi.org/10.2147/BTT.S272063 [Truy cập ngày 20 tháng 9 năm 2021]
5. Juan G. Ripoll, M.D., Noud van Helmond, M.D. Convalescent Plasma for Infectious Diseases: Historical Framework and Use in COVID-19. [Truy cập trực tuyến] Clinical Microbiology Newsletter; 2021. Đường dẫn: https://doi.org/10.1016/j.clinmicnews.2021.02.001 [Truy cập ngày 22 tháng 9 năm 2021]
6. Kristen W. Cohen, Susanne L. Linderman, Zoe Moodie và cộng sự. Longitudinal analysis shows durable and broad immune memory after SARS- CoV-2 infection with persisting antibody responses and memory B and T cells. [Truy cập trực tuyến] Cell Reports Medicine 2, 2021. Đường dẫn: https://doi.org/10.1016/j.xcrm.2021.100354 [Truy cập ngày 22 tháng 9 năm 2021]
7. Manuel Rojas, Yhojan Rodríguez, Diana M. Monsalve và cộng sự. Convalescent plasma in Covid-19: Possible mechanisms of action. [Truy cập trực tuyến] ScienceDirect, 2020. Đường dẫn: https://doi.org/10.1016/j.autrev.2020.102554 [Truy cập ngày 23 tháng 9 năm 2021]
8. Massimo Franchini, Giancarlo Maria Liumbruno, Giorgio Piacentini và cộng sự. The Three Pillars of COVID-19 Convalescent Plasma Therapy. [Truy cập trực tuyến] MDPI, 2021. Đường dẫn: https://doi.org/10.3390/life11040354 [Truy cập ngày 23 tháng 9 năm 2021]
9. Daniele Focosi, Massimo Franchini, Liise-anne Pirofski và cộng sự. COVID-19 Convalescent Plasma Is More than Neutralizing Antibodies: A Narrative Review of Potential Beneficial and Detrimental Co-Factors. [Truy cập trực tuyến] MDPI, 2021. Đường dẫn: https://doi.org/10.3390/v13081594 [Truy cập ngày 24 tháng 9 năm 2021]
10. Jun Yong Choi, MD, PhD. Convalescent Plasma Therapy for Coronavirus Disease 2019. [Truy cập trực tuyến] Infect Chemother, 2020. Đường dẫn: https://doi.org/10.3947/ic.2020.52.3.307 [Truy cập ngày 24 tháng 9 năm 2021]
11. Wentao Ni, Xiuwen Yang, Deqing Yang và cộng sự. Role of angiotensin- converting enzyme 2 (ACE2) in COVID-19. [Truy cập trực tuyến] Critical Care, 2020. Đường dẫn: https://doi.org/10.1186/s13054-020-03120-0 [Truy cập ngày 25 tháng 9 năm 2021]
12. Mireia Pelegrin, Mar Naranjo-Gomez, and Marc Piechaczyk1. Antiviral Monoclonal Antibodies: Can They Be More Than Simple Neutralizing Agents?. [Truy cập trực tuyến] Trends in Microbiology, 2015. Đường dẫn: https://doi.org/10.1016/j.tim.2015.07.005 [Truy cập ngày 25 tháng 9 năm 2021]