Bệnh huyết học
Liệu pháp vận mạch và Corticosteroid ở bệnh nhân sốc nhiễm trùng
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
Cách chúng tôi leo thang liệu pháp vân mạch và Corticosteroid ở bệnh nhân sốc nhiễm trùng – Tải file PDF Tại đây, tải bản gốc Tiếng Anh Tại đây.
Bijan Teja, MD; Nicholas A. Bosch, MD; and Allan J. Walkey, MD
Sốc nhiễm trùng được xác định bởi sự cần thiết của thuốc vận mạch để điều chỉnh hạ huyết áp và nhiễm toan do nhiễm trùng, với tỷ lệ tử vong 30% -40%. Việc chăm sóc bệnh nhân bị sốc nhiễm trùng nặng liên quan đến nhiều quyết định điều trị liên quan đến lựa chọn thuốc vận mạch và phương pháp điều trị hỗ trợ. . Trong ấn bản “Tôi làm như thế nào” này, chúng tôi cung cấp một cuộc thảo luận dựa trên trường hợp cụ thể về các quyết định lâm sàng phổ biến liên quan đến việc lựa chọn thuốc vận mạch đầu tay, mục tiêu huyết áp, đường phân phối thuốc vận mạch, sử dụng thuốc vận mạch thứ cấp và thuốc bổ trợ. Chúng tôi cũng xem xét các phương pháp chẩn đoán, điều trị và các chiến lược theo dõi cho bệnh nhân bị sốc nặng, cũng như các tiếp cận các trường hợp khó cai thuốc vận mạch.
Ca LS Ví dụ, phần 01
Một phụ nữ 65 tuổi bị rung nhĩ đến điều trị tại khoa cấp cứu vì sốt và tiểu khó. Huyết áp ban đầu là 75/40 mm Hg (MAP 52 mm Hg), nhịp tim là 95 nhịp/phút và độ bão hòa oxy là 92% khi thở không khí trong phòng. Các chi ấm áp và tưới máu tốt. Cô ấy đã nhận được Ringer’s lactate cho đến khi cô ấy không còn đáp ứng với truyền dịch bằng nhiều biện pháp và nhận được kháng sinh cho nhiễm trùng niệu mắc phải tại cộng đồng. Cô vẫn bị hạ huyết áp với HA là 82/45 mm Hg (MAP, 57 mm Hg). Lactate huyết thanh là 2,5 g/L. chức năng hai thất và rối loạn chức năng tâm trương độ 1 (không thay đổi so với đánh giá trước đó). Nhóm ICU đã được gọi để hỗ trợ, bao gồm cả việc bắt đầu điều trị bằng thuốc vận mạch. Sau khi thảo luận với bệnh nhân để xác định liệu liệu pháp vận mạch có phù hợp với mục tiêu của cô ấy hay không, norepinephrine được bắt đầu sử dụng đường truyền ngoại vi và bệnh nhân được chuyển đến ICU.
Có ngoại lệ nào đối với Norepinephrine được sử dụng đầu tiên không?
Chúng tôi hiếm khi bắt đầu sử dụng thuốc vận mạch khác thay thế cho norepinephrine như liệu pháp đầu tay trong sốc nhiễm trùng. Trong số những bệnh nhân có nguy cơ hoặc những người bị rung nhĩ hoặc các bệnh lý rối loạn nhịp trên thất khác và những người dự kiến sẽ chịu đựng kém với đáp ứng thất nhanh (ví dụ, những người có dự trữ tim kém), chúng tôi cân nhắc vasopressin hoặc phenylephrine thay vì norepinephrine làm thuốc vận mạch đầu tay.
Trong hơn một thập kỷ, các hướng dẫn đã khuyến cáo norepinephrine là thuốc vận mạch đầu tay trong sốc nhiễm trùng dựa trên các thử nghiệm lâm sàng ngẫu nhiên so sánh norepinephrine (chủ yếu là chất chủ vận a1 với chất chủ vận b1 bổ sung) với các thuốc vận mạch khác có cơ chế khác nhau như vasopressin, phenylephrine, dopamin, và epinephrine. Mặc dù một nghiên cứu ngẫu nhiên cho thấy norepinephrine có nguy cơ rối loạn nhịp tim thấp hơn so với dopamin, nhưng các nghiên cứu ngẫu nhiên khác không cho thấy sự khác biệt về tỷ lệ tử vong hoặc các kết quả khác lấy bệnh nhân làm trung tâm khi so sánh norepinephrine với các thuốc vận mạch thay thế ngoài dopamin. Do đó, các hướng dẫn xếp hạng cho tính ưu việt của norepinephrine chỉ cao khi so sánh với dopamine. Mặc dù nhìn chung chúng ta bắt đầu điều trị bằng norepinephrine đầu tay, đôi khi chúng tôi xem xét các thuốc không có chất chủ vận b1 (vasopressin hoặc phenylephrine) khi các tác dụng phụ liên quan đến adrenergic của norepinephrine được cho là—hoặc dường như—dẫn đến mất bù trên lâm sàng (ví dụ, nhịp thất nhanh do rung nhĩ), dựa trên bằng chứng quan sát gần như thực nghiệm thấy rằng việc bắt đầu sử dụng phenylephrine giúp kiểm soát nhịp tim được cải thiện một cách khiêm tốn so với norepinephrine ở những bệnh nhân bị nhiễm trùng huyết và rung nhĩ.
Sau khi Norepinephrine được bắt đầu, mục tiêu MAP là bao nhiêu?
Chúng tôi nhắm mục tiêu MAP từ 60 đến 65 mm Hg ở hầu hết bệnh nhân bị sốc nhiễm trùng. Lịch sử nhắm mục tiêu MAP là 65 mm Hg dựa trên bằng chứng cho thấy quá trình tự điều hòa của não thường bắt đầu giảm nhanh chóng khi MAP dưới 60 mm Hg. Các thử nghiệm gần đây đã làm rõ rằng các mục tiêu MAP > 65 mm Hg trong quá trình sốc có khả năng gây hại, làm tăng nguy cơ nhịp nhanh trên thất và có khả năng tử vong. “Thử nghiệm 65” chọn ngẫu nhiên các bệnh nhân từ 65 tuổi trở lên bị sốc giãn mạch với mục tiêu MAP từ 60 đến 65 mm Hg hoặc chăm sóc thông thường và không tìm thấy sự khác biệt nào về tỷ lệ tử vong do mọi nguyên nhân trong 90 ngày và một tín hiệu có thể giảm tỷ lệ tử vong với mục tiêu MAP thấp hơn sau khi điều chỉnh cho các biến cơ sở được xác định trước.
Khi nàO’ nên đặt đường truyền tĩnh mạch trung tâm để truyền thuốc vận mạch?
Đối với những bệnh nhân bắt đầu sử dụng norepinephrine liều thấp (ví dụ: < 15 ug/phút hoặc < 0,3 ug/kg/phút) , chúng tôi thường bắt đầu truyền norepinephrine qua đường truyền ngoại biên và sau đó đánh giá xem có cần loại đường truyền khác hay không. Ở những bệnh nhân dự kiến sẽ cần dùng norepinephrine trong > 24 đến 48 giờ, nhưng nếu huyết động ổn định và cần dùng liều thấp norepinephrine, chúng tôi thường chuyển sang truyền qua đường truyền TM cánh tay dựa trên chuyên môn và kinh nghiệm của bệnh viện địa phương. Ở những bệnh nhân huyết động không ổn định dai dẳng hoặc cần liều norepinephrine cao hơn, thêm thuốc vận mạch hoặc cổng bổ sung cho các dịch truyền khác, chúng tôi nhanh chóng chuyển sang truyền dịch qua tĩnh mạch trung tâm (CVC).
Trước đây việc lo ngại về sự thoát mạch của thuốc vận mạch gây tổn thương mô đã hạn chế việc truyền thuốc vận mạch vào TM ngoại biên. Tuy nhiên, bằng chứng gần đây cho thấy rằng việc truyền thuốc vận mạch qua các đường ngoại vi có < 5% nguy cơ thoát mạch khi sử dụng trong < 72 giờ, không có trường hợp hoại tử mô hoặc thiếu máu cục bộ chi được báo cáo trong một báo cáo hệ thống bao gồm bảy nghiên cứu với 1.382 bệnh nhân.Ngoài ra, sử dụng thuốc vận mạch qua tĩnh mạch ngoại biên có thể giảm thời gian điều trị bằng thuốc vận mạch so với truyền qua CVC. Những dữ liệu này đã dẫn đến một khuyến nghị yếu trong hướng dẫn của Chiến dịch Surviving Sepsis là bắt đầu dùng thuốc vận mạch ở ngoại vi để phục hồi MAP thay vì trì hoãn việc bắt đầu cho đến khi đặt CVC.
Khi nào chúng ta nên xem xét thêm thuốc vận mạch thứ hai?
Chúng tôi bắt đầu dùng thuốc vận mạch thứ hai cho bệnh nhân bị sốc nhiễm trùng và tăng nhu cầu sử dụng thuốc vận mạch, thường là liều norepinephrine đạt 15 ug/phút (hoặc 0,3 ug/kg/phút), một thực hành thường phù hợp với hướng dẫn của Chiến dịch sống sót sau nhiễm trùng huyết và bằng chứng hiện tại từ các thử nghiệm. Khi mục tiêu tưới máu không được đáp ứng với liều vừa phải của thuốc vận mạch ban đầu, quyết định thêm thuốc vận mạch khác hoặc tăng thuốc hiện tại phải cân nhắc lợi ích mong đợi (cải thiện cung lượng tim, huyết áp, tưới máu) và rủi ro (tăng nguy cơ rối loạn nhịp tim, thiếu máu cơ tim). ) của mỗi cách tiếp cận. Ít bằng chứng trực tiếp hướng dẫn việc ra quyết định liên quan đến việc bổ sung thuốc vận mạch thứ hai. Trong sốc nhiễm trùng, các hướng dẫn hiện tại đưa ra một khuyến cáo yếu là thêm vasopressin vào norepinephrine khi liều norepinephrine đạt tới 0,25 đến 0,5 mcg/kg/phút. Khuyến cáo yếu được thúc đẩy bởi các tác dụng tiết kiệm thuốc vận mạch catecholamine được quan sát thu được khi bổ sung vasopressin, với kết quả lâm sàng hỗn hợp qua các phân tích tổng hợp. Ví dụ, một phân tích tổng hợp trên 23 thử nghiệm cho thấy giảm rung nhĩ ở các nhóm bổ sung vasopressin với norepinephrine, với tác dụng không nhất quán trên tỷ lệ tử vong và liệu pháp thay thế thận. Một phân tích tổng hợp ở cấp độ bệnh nhân riêng lẻ của bốn thử nghiệm cho thấy không có mối liên hệ nào với tỷ lệ tử vong, nhưng giảm rối loạn nhịp tim, tăng thiếu máu cục bộ ở ngọn chi và tác dụng không nhất quán đối với nhu cầu lọc máu khi bổ sung vasopressin vào catecholamine. Trong trường hợp không có ngưỡng liều đáp ứng cho thấy những thay đổi về huyết áp và tỷ lệ biến chứng khi dùng liều norepinephrine, các quyết định về thời điểm bắt đầu thuốc vận mạch thứ hai tối ưu có thể được thông báo bằng những cân nhắc thực tế và bằng chứng gián tiếp từ các thử nghiệm. Các cân nhắc thực tế trên ls bao gồm tốc độ tăng liều thuốc vận mạch cần thiết và sự sẵn có của thuốc vận mạch thứ hai; không nên trì hoãn việc tăng liều thuốc vận mạch đầu tiên ở những bệnh nhân mất bù nhanh chóng để chờ thuốc vận mạch thứ hai. Tuy nhiên, các bác sĩ lâm sàng nên lập kế hoạch bổ sung sớm thuốc vận mạch thứ hai khi bị sốc cho những bệnh nhân có nhu cầu norepinephrine ngày càng tăng. Cơ sở lý luận cho việc sử dụng sớm thuốc vận mạch thứ cấp bao gồm các phân tích phân nhóm từ “Thử nghiệm Vasopressin trong Sốc nhiễm trùng” (VASST) so sánh việc bổ sung vasopressin vào norepinephrine với norepinephrine đơn độc, cho thấy tỷ lệ tử vong thấp hơn ở những bệnh nhân dùng liều norepinephrine thấp hơn (< 15 mcg/phút) trên đối tượng tham gia được chọn ngẫu nhiên để nhận vasopressin. Tương tự, thử nghiệm “Vasopressin với Norepinephrine là liệu pháp ban đầu trong sốc nhiễm trùng” (VANISH) về vasopressin so với norepinephrine ở bệnh nhân trong vòng 6 giờ kể từ khi bắt đầu sốc và cho thấy nhu cầu lọc máu giảm khi bổ sung vasopressin.
Thuốc vận mạch thứ hai nên là gì?
Vasopressin là lựa chọn hàng đầu của chúng tôi đối với thuốc vận mạch thứ hai. Các quyết định về lựa chọn thuốc vận mạch thứ hai nên được hướng dẫn bởi các mục tiêu của liệu pháp vận mạch. Nói chung, mục tiêu của điều trị thuốc vận mạch trong sốc phân bố là làm tăng khả năng co mạch bị suy giảm để đáp ứng mục tiêu huyết động mà không làm tăng biến chứng, đặc biệt khi không có bằng chứng cho thấy mục tiêu tưới máu không đạt được do cung lượng tim bị suy giảm. Các hướng dẫn hiện tại đề xuất vasopressin là thuốc vận mạch thứ cấp được ưu tiên, chủ yếu là do bằng chứng cho thấy vasopressin làm giảm nhu cầu lọc máu và rối loạn nhịp tim và đã được nghiên cứu kỹ lưỡng như một thuốc vận mạch thứ hai đạt được mục tiêu huyết động. Tuy nhiên, nếu rối loạn nhịp tim ít xảy ra hơn (ví dụ bệnh nhân trẻ tuổi), thiếu máu cục bộ ngón tay là mối quan tâm chính (ví dụ: tiền sử hội chứng Raynaud hoặc các dấu hiệu sớm của thiếu máu cơ tim), hoặc suy giảm cung lượng tim được cho là góp phần gây sốc (ví dụ: bệnh cơ tim do nhiễm trùng kết hợp và sốc phân bố), thì chúng tôi ưu tiên dùng epinephrine làm thuốc vận mạch thứ hai. Tuy nhiên, bằng chứng ủng hộ epinephrine như một thuốc vận mạch thứ cấp còn rất ít, và do epinephrine hoạt động thông qua hầu hết các thụ thể adrenergic giống như norepinephrine, các mục tiêu huyết động có thể không đạt được dễ dàng khi kết hợp norepinephrine và epinephrine như với các tác nhân hoạt động thông qua các cơ chế không phải catecholamine (ví dụ: , vasopressin hoặc angiotensin II). Mặc dù chúng tôi không sử dụng angiotensin II thường xuyên như một thuốc vận mạch thứ hai do cân nhắc về chi phí và không đủ bằng chứng về lợi ích kết quả lâm sàng, nhưng angiotensin II đẩy nhanh việc đạt được các mục tiêu MAP.
Những liệu pháp bổ sung nào nên được xem xét cho tình trạng sốc trở nên tồi tệ hơn?
Chúng tôi thêm corticosteroid (hydrocortisone 50 mg IV mỗi 6 giờ cộng với fludrocortisone 50 mg uống hàng ngày trong 7 ngày mà không giảm liều) cho những bệnh nhân có nhu cầu thuốc vận mạch tăng dần, thường là khi bắt đầu dùng thuốc vận mạch thứ hai. Nhiều phương pháp điều trị đã được đánh giá để cải thiện huyết động cho bệnh nhân bị sốc. Chúng bao gồm corticosteroid, xanh methylene, vitamin như axit ascorbic hoặc thiamine, hoặc sự kết hợp của các chất này.
Corticosteroid – thuốc hỗ trợ điều trị sốc được nghiên cứu kỹ lưỡng nhất – có nhiều cơ chế tác dụng bao gồm tác dụng miễn dịch và tác dụng trực tiếp lên các thụ thể glucocorticoid nội mô để giảm liệt mạch. Bằng chứng rõ ràng về tác dụng của corticosteroid liều thấp đến trung bình (< 400 mg hydrocortisone tương đương/ngày) trong việc tăng HA (tăng MAP trung bình, 5 mm Hg) và rút ngắn thời gian sốc (trung bình, ít hơn 1,5 ngày dùng thuốc vận mạch). Tuy nhiên, corticosteroid có thể làm tăng các tác dụng phụ như tăng đường huyết, tăng natri máu và yếu cơ. Một phân tích tổng hợp năm 2019 về 61 thử nghiệm nhiễm trùng huyết với > 12.000 bệnh nhân cho thấy lợi ích nhỏ của corticosteroid trong việc giảm tỷ lệ tử vong (nguy cơ tương đối, 0,91; 95% CI, 0,84-0,99). Do đó, các hướng dẫn đề xuất dùng corticosteroid cho bệnh nhân có sốc nhiễm trùng và “nhu cầu liên tục đối với thuốc vận mạch.” Cơ sở lý luận để bắt đầu dùng corticosteroid cho bệnh nhân có nhu cầu sử dụng thuốc vận mạch liều cao hơn (thay vì yêu cầu thấp hơn) bao gồm khái niệm cho rằng corticosteroid có khả năng hoạt động như một tác nhân giúp tiết kiệm thuốc vận mạch để giảm các tác dụng phụ liên quan đến thuốc vận mạch thường thấy ở liều cao, một giả thuyết được các thử nghiệm và nghiên cứu mô hình cho thấy lợi ích của corticosteroid trong sốc chỉ khi bệnh nhân có nhu cầu sử dụng thuốc vận mạch cao.
Cơ sở lý luận để sử dụng fludrocortison với hydrocortison có ba phần. Đầu tiên, hai thử nghiệm lớn nhất chứng minh lợi ích lâm sàng của steroid đã sử dụng hydrocortisone và fludrocortisone cùng nhau, trong khi các thử nghiệm đánh giá riêng hydrocortisone không cho thấy lợi ích về tỷ lệ tử vong; thứ hai, một thử nghiệm so sánh trực tiếp fludrocortisone cộng với hydrocortisone với hydrocortisone đơn độc cho thấy tỷ lệ tử vong tại bệnh viện giảm tuyệt đối 3% ở những bệnh nhân dùng fludrocortisone cộng với hydrocortisone, nhưng không đủ khả năng để phát hiện tác dụng khả thi về mặt lâm sàng. Thứ ba, lập luận chính để không sử dụng fludrocortisone là hydrocortisone—ở liều lượng được sử dụng trong lâm sàng—có hoạt tính giữ natri tương tự như fludrocortisone; tuy nhiên, mineralocorticoids có một số chức năng ngoài việc giữ natri, bao gồm vai trò chống chết tế bào thần kinh, thanh thải dịch phế nang bởi các tế bào biểu mô phổi và kích hoạt hệ thống miễn dịch bẩm sinh. Do đó, tác dụng đa năng ngoài khả năng giữ natri có thể mang lại lợi ích bổ sung từ việc kết hợp fludrocortisone với hydrocortisone.
Mặc dù chúng tôi sử dụng 7 ngày không giảm liều dựa trên thử nghiệm “Protein C hoạt tính và Corticosteroid đối với sốc nhiễm trùng ở người” (APROCCHSS), thời gian tối ưu là không chắc chắn và bằng chứng còn lẫn lộn về rủi ro và lợi ích của việc cai steroid để ngăn ngừa hạ huyết áp dội ngược. Nếu sốc tái diễn sau khi ngừng mà không giảm dần, chúng tôi xem xét việc khởi động lại steroid và bắt đầu đánh giá thêm về nguyên nhân gây sốc.
Các nghiên cứu điều tra xanh methylene như một thuốc hỗ trợ vận mạch còn rất ít. Các thử nghiệm thí điểm về xanh methylene bổ sung trong sốc nhiễm trùng cho thấy MAP và nhịp tim được cải thiện so với những người tham gia kiểm soát, có khả năng thông qua việc ức chế con đường oxit nitric. Với dữ liệu ít ỏi về lợi ích đối với kết cục điều trị của bệnh nhân, chúng tôi hạn chế sử dụng xanh methylene cho những bệnh nhân bị sốc kháng với nhiều thuốc vận mạch và corticosteroid, với mục tiêu tăng huyết áp tạm thời để cho phép bắt đầu các liệu pháp khác (ví dụ: các biện pháp kiểm soát nguồn lây nhiễm) mong cải thiện kết cục lâu dài.
Dựa trên các kết quả có khả năng hứa hẹn của một nghiên cứu nhỏ trước khi triển khai so với sau khi triển khai, nhiều thử nghiệm gần đây đã điều tra các lợi ích tiềm năng của axit ascorbic liều cao (có hoặc không có corticosteroid hoặc thiamine, thường được gọi là hồi sức trao đổi chất). Tuy nhiên, nhiều thử nghiệm ngẫu nhiên không cho thấy lợi ích—hoặc cho thấy tác hại— khi sử dụng axit ascorbic trong khi sốc. Chúng tôi không sử dụng phương pháp hồi sức chuyển hóa dựa trên axit ascorbic hoặc thiamine để điều trị sốc nhiễm trùng.
Ví dụ trường hợp, Phần 2
Sau 24 giờ, bệnh nhân cần tăng liều norepinephrine lên 0,5 mcg/kg/phút. Một CVC đã được đặt. Nhu cầu oxy và thuốc vận mạch được cải thiện. Các loại kháng sinh được thu hẹp để bao phủ Escherichia coli uropsis dựa trên kết quả nuôi cấy. Sau khi cải thiện dần dần, vào ngày nhập viện thứ 5, tình trạng của cô trở nên tồi tệ hơn. Cô ấy bị hạ huyết áp không liên tục mặc dù norepinephrine 0,5 mcg/kg/phút, bổ sung vasopressin 2,4 đơn vị/giờ (0,04 đơn vị/phút) và sau đó là epinephrine 0,3 mg/kg/phút. Huyết áp là 95/40 mm Hg (MAP, 57 mm Hg) và nhịp tim là 110 nhịp/phút. Hydrocortisone và fludrocortisone đã được bắt đầu. Các chi bị lốm đốm và đổ đầy mao mạch là 4 giây. Mức lactate huyết thanh là 4,5 g/L. Không tìm thấy bằng chứng về xuất huyết, hội chứng khoang bụng, hoặc tràn khí màng phổi, và kết quả siêu âm tim tại điểm chăm sóc không thay đổi mà không có bằng chứng chèn ép, rối loạn chức năng thất phải hoặc trái mới, hoặc tắc nghẽn đường ra.
Những đánh giá chẩn đoán nào nên được xem xét đối với sốc dai dẳng hoặc xấu đi?
Sốc xấu đi hoặc dai dẳng mặc dù đã kiểm soát nguồn và hồi sức ban đầu nên nhanh chóng xem xét đánh giá chẩn đoán bổ sung. Các nguyên nhân phổ biến và khuyến nghị đánh giá tình trạng sốc nặng hơn sau khi kiểm soát và ổn định nguồn ban đầu trong quá trình nhiễm trùng huyết được trình bày trong bảng 1. Các yếu tố góp phần làm nặng thêm tình trạng sốc thường bao gồm sốc phân bổ nặng hơn do nhiễm trùng bệnh viện, sốc tắc nghẽn do thuyên tắc phổi hoặc hội chứng khoang bụng, hoặc sốc tim do bệnh cơ tim nhiễm trùng hoặc rối loạn nhịp tim.
Ở liều thuốc vận mạch nào chúng ta ngừng tăng liều?
Chúng tôi không ngừng tăng liều lượng norepinephrine hoặc epinephrine ở bất kỳ liều lượng cụ thể nào. Không có bằng chứng về phản ứng tiệm cận của MAP đối với norepinephrine hoặc epinephrine ở liều cao hơn, chúng tôi không có giới hạn liều để tăng thêm các thuốc vận mạch này 1 cách tùy ý; tuy nhiên, chúng tôi thường không chuẩn độ liều vasopressin > 2,4 đơn vị/giờ (0,04 đơn vị/phút) vì lo ngại về cung lượng tim thấp hơn và tưới máu mạch vành hoặc nội tạng ở liều cao hơn. Các nghiên cứu đánh giá bệnh nhân dùng thuốc vận mạch liều cao để điều trị sốc nhiễm trùng (tương đương với norepinephrine > 1 mcg/kg/phút) đã cho thấy tỷ lệ sống sót dao động từ 10% đến 54%. Trong thử nghiệm APROCCHSS, liều norepinephrine trung bình khi đăng ký là 1,08 mcg/kg /phút đối với 1.086 bệnh nhân dùng norepinephrine và 2,01 mcg/kg/phút đối với 111 bệnh nhân dùng epinephrine. Tỷ lệ sống sót sau 90 ngày trong thử nghiệm này là 53,9%.
BẢNG 1 các vấn đề cần xem xét khi lâm sàng bệnh nhân bị sốc nặng hơn
<td”>Các vấn đề
| Diagnostic strategies | |
| Nguyên nhân mới gây sốc hoặc tồn tại đồng thời | • Sốc nhiễm trùng: Tìm kiếm nhiễm trùng chưa được chẩn đoán (ví dụ: lặp lại xét nghiệm nuôi cấy, chẩn đoán hình ảnh bổ sung), đánh giá mức độ phù hợp của điều trị (độ nhạy cảm với kháng sinh, kiểm soát nguồn bệnh)
• Sốc tim: làm lại siêu âm tim, độ bão hòa oxy tĩnh mạch trung tâm • Sốc mất máu: đánh giá khả năng đáp ứng với dịch (tái xuất hiện phản ứng đáp ứng với dịch truyền sau hồi sức có thể’ là dấu hiệu sớm của chảy máu ẩn), xét nghiệm CBC lặp lại, đánh giá nhịp tim tăng • Sốc tắc nghẽn: siêu âm tim tìm chèn ép tim, chụp CT để’ đánh giá thuyên tắc phổi, đánh giá_ lâm sàng hc chèn ép khoang bụng (ví dụ, ở bệnh nhân cổ trướng và sốc nhiễm trùng) • • Suy thượng thận: xem lại danh sách thuốc corticosteroid sử dụng tại nhà, xem xét các nguyên nhân tiềm ẩn gây suy thượng thận (ví dụ: sử dụng etomidate, bệnh tuyến yên) |
| Khả năng đánh giá thấp MAP bằng đường động mạch ngoại biên | • Bắt đầu bằng cách so sánh MAP không xâm lấn với MAP xâm lấn
• Ước tính huyết áp tâm thu bằng độ nảy của mạch • Đánh giá các biện pháp tưới máu khác (ví dụ: thay đổi trạng thái tinh thần, lactate, chức năng thận) • • Cân nhắc đặt catheter động mạch trung tâm (ví dụ: đùi hoặc nách) |
| Nhiễm toan góp phần làm giảm tác dụng vận mạch | • Đánh giá tình trạng toan, kiềm
• Cân nhắc truyền bicarbonate hoặc điều trị thay thế thận liên tục |
| Ức chế sự giãn mạch do nitric oxide gây ra | • Cân nhắc dùng thử xanh methylene theo kinh nghiệm như một biện pháp tạm thời |
Có nên đặt catheter động mạch trung tâm trong sốc kháng trị?
Bởi vì áp lực động mạch trung tâm mô tả tốt nhất áp lực tưới máu đến các cơ quan quan trọng, chúng tôi thường đặt catheter động mạch trung tâm (đùi hoặc nách) ở những bn bị sốc dường như kháng trị và tình trạng lâm sàng xấu đi mặc dù đã tăng liều thuốc vận mạch. Các hướng dẫn của Surviving Sepsis Campaign đưa ra một khuyến nghị yếu về việc theo dõi huyết áp động mạch xâm lấn hơn là theo dõi không xâm lấn, nhưng không chỉ rõ theo dõi huyết áp động mạch nên là trung tâm hay ngoại vi.1 Quản lý huyết động dựa trên áp lực động mạch quay ngược với áp lực động mạch trung tâm có thể dẫn đến sử dụng thuốc vận mạch quá mức.39 Một nghiên cứu cho thấy áp suất động mạch tâm thu và MAP cao hơn khi được đo từ vị trí đùi so với vị trí động mạch quay, với việc giảm liều thuốc vận mạch ngay lập tức được tạo điều kiện thuận lợi ở 11 trong số 14 bệnh nhân sau khi chuyển sang đặt ống thông động mạch trung tâm.
Nhiễm toan có nên được điều chỉnh?
Đối với những bệnh nhân bị nhiễm toan máu nặng, tổn thương thận cấp và sốc kháng trị có dự trữ thông khí tốt, chúng tôi truyền lý natri bicarbonate (HCO3-) nhắm mục tiêu PH trên > 7.3 và bắt đầu điều trị thay thế thận liên tục nếu toan máu vẫn không được kiểm soát. Phản ứng co mạch và liên kết với thụ thể b-adrenergic bị suy giảm do nhiễm toan.41,42 NaHCO3- và liệu pháp thay thế thận có thể điều chỉnh nhiễm toan tạm thời. Thử nghiệm “Natri bicacbonat để điều trị nhiễm toan nặng ở người bệnh nặng” (BICAR-ICU), thử nghiệm ngẫu nhiên những người trưởng thành bị bệnh nặng bị nhiễm toan máu nặng để truyền natri HCO3- (4,2% [500 mEq/L], tối đa 1 L) hoặc không truyền natri HCO3, nhận thấy rằng trong số những bệnh nhân bị tổn thương thận cấp tính, những người được truyền HCO3 có tỷ lệ tử vong thấp hơn và số ngày không dùng thuốc vận mạch nhiều hơn so với những người không dùng.40 Chúng tôi yêu cầu bệnh nhân có khả năng tăng thông khí phút một cách an toàn để bù đắp cho việc tăng sản xuất CO2 có thể xảy ra sau khi sử dụng HCO3-.
Ví dụ trường hợp, Phần 3
Các mẫu cấy máu của bệnh nhân cho kết quả dương tính với Staphylococcus aureus kháng methicillin. Kháng sinh thích hợp đã được bắt đầu và CVC đã được đặt. Lactate huyết thanh và tình trạng liệt mạch được cải thiện; tuy nhiên, cô tiếp tục nhận được norepinephrine với liều 0,3 mcg/kg/phút và vasopressin. HA là 90/50 mm Hg (MAP, 63 mm Hg) và nhịp tim là 95 nhịp/phút. Kết quả siêu âm tim tại giường không thay đổi và kết quả nuôi cấy lặp lại là âm tính.
Phương pháp tiếp cận cai thuốc vận mạch nên như thế nào?
Chúng tôi ngừng norepinephrine đầu tiên, sau đó là vasopressin cuối cùng, cho những bệnh nhân đang dùng cả hai thuốc vận mạch nhưng đang cải thiện lâm sàng. Có rất ít dữ liệu về cách tiếp cận cai thuốc vận mạch. Một số nghiên cứu quan sát nhỏ, đơn trung tâm ở những bệnh nhân bị sốc nhiễm trùng đang dùng norepinephrine và vasopressin đã phát hiện ra rằng việc ngừng sử dụng vasopressin trước tiên dẫn đến tăng tỷ lệ hạ huyết áp, cho thấy nên ngừng sử dụng norepinephrine trước.
Ví dụ trường hợp, Phần 4
Các chi của cô ấy ấm và được tưới máu tốt, tình trạng tâm thần và chức năng thận đang được cải thiện, nhưng những nỗ lực cai vasopressin liều thấp (2,4 đơn vị/giờ [0,04 đơn vị/phút]) đã dẫn đến MAP là 60 mm Hg.
Phương pháp tiếp cận điều trị chứng liệt mạch dai dẳng và không có khả năng cai thuốc vận mạch dạng truyền là gì?
Đối với những bệnh nhân cải thiện lâm sàng (đảo ngược rối loạn chức năng cơ quan), nhưng bị liệt vận mạch nhẹ, dai dẳng, chúng tôi giảm mục tiêu MAP xuống 60 mm Hg để giúp cai thuốc vận mạch. Hạ huyết áp liên tục phụ thuộc vào thuốc vận mạch mà không có bằng chứng giảm tưới máu cơ quan đích có thể hạn chế huy động, vật lý trị liệu và xuất viện khỏi ICU. Hạ mục tiêu MAP xuống 60 mm Hg dựa trên 65 thử nghiệm được thảo luận trong phần về mục tiêu MAP. Đôi khi, thuốc an thần cũng có thể góp phần gây hạ huyết áp và chúng tôi thường điều chỉnh thuốc an thần để giảm nhu cầu sử dụng thuốc vận mạch. Chúng tôi cũng xem xét chẩn đoán lặp lại (Bảng 1) để xác định các quá trình đang diễn ra có thể góp phần vào nhu cầu sử dụng thuốc vận mạch dai dẳng (ví dụ: áp xe trong ổ bụng).
Midodrine là một chất chủ vận a1-adrenergic đường uống đã được chấp thuận sử dụng ở Hoa Kỳ để điều trị hạ huyết áp thế đứng có triệu chứng. Nó đã được sử dụng ngoài nhãn hiệu để tạo điều kiện giải phóng khỏi thuốc vận mạch IV; tuy nhiên, thử nghiệm gần đây “Midodrine như hỗ trợ hỗ trợ điều trị hạ huyết áp kháng trị tại khoa chăm sóc đặc biệt” (MIDAS) cho thấy không có lợi ích nào của midodrine trong việc đẩy nhanh quá trình giải phóng khỏi vận mạch đường tĩnh mạch..47 Đáng chú ý, thử nghiệm này đã loại trừ những bệnh nhân bị suy gan và suy thận mãn tính, và một tác dụng có lợi đã được tìm thấy trong một phân tích sâu phân nhóm trên những bệnh nhân được gây tê ngoài màng cứng.
Ở những bệnh nhân hạ thấp mục tiêu MAP và giảm thiểu thuốc an thần không hiệu quả, đặc biệt nếu bệnh nhân bị suy gan, suy thận hoặc một thành phần thần kinh dẫn đến hạ huyết áp, chúng tôi thử dùng midodrine. Một bất lợi khi sử dụng midodrine là nó thường được tiếp tục ngay cả sau khi xuất viện. Chúng tôi thường kê toa midodrine 10 đến 20 mg uống mỗi 8 giờ với ngày giảm dần hoặc ngừng ngày cuối để tránh tiếp tục dùng sau khi xuất viện. Nếu không đạt được cải tiến nào trong việc đạt được các mục tiêu MAP, chúng tôi sẽ dừng sau 24 đến 48 giờ.
Kết luận
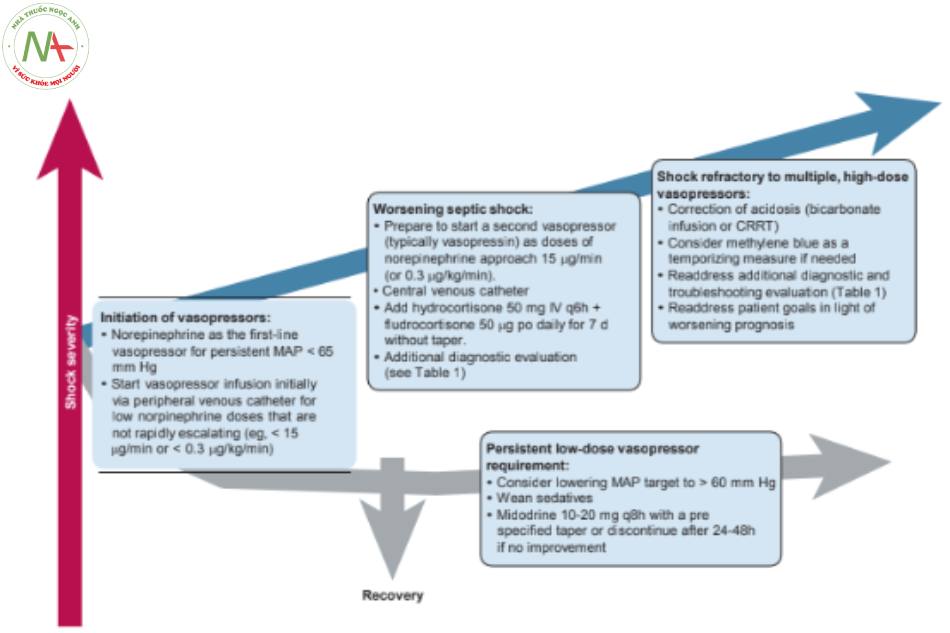
Việc chăm sóc bệnh nhân bị sốc nhiễm trùng có thể phức tạp. Cách tiếp cận được đề xuất của chúng tôi để điều trị hạ huyết áp trong sốc nhiễm trùng được tóm tắt trong Hình 1. Ở hầu hết bệnh nhân, chúng tôi bắt đầu sử dụng norepinephrine trước, thông qua đường truyền ngoại vi hoặc đường giữa, nhắm mục tiêu MAP từ 60 đến 65 mm Hg. Nếu liều norepinephrine đạt tới 15 mcg/phút (hoặc 0,3 mcg/kg/phút), chúng tôi bắt đầu dùng vasopressin cho hầu hết bệnh nhân, chuyển sang truyền qua CVC, và dùng hydrocortisone và fludrocortisone trong 7 ngày. Chúng tôi cũng đánh giá các nguyên nhân gây sốc đồng thời (Bảng 1). Đối với sốc kháng trị, chúng tôi xem xét theo dõi áp lực động mạch trung tâm và điều chỉnh nhiễm toan. Khi liệt mạch nhẹ kéo dài mà không có bằng chứng thiếu máu cơ quan đích, chúng tôi giảm mục tiêu MAP xuống 60 mm Hg, điều chỉnh hoặc ngừng thuốc an thần nếu có thể và thường thử dùng midodrine.
Tài liệu tham khảo
- Evans L, Rhodes A, Alhazzani W, et al. Surviving sepsis campaign: international guidelines for management of sepsis and septic shock 2021. Intensive Care Med. 2021;47(11):1181-1247.
- De Backer D, Biston P, Devriendt J, et al. Comparison of dopamine and norepinephrine in the treatment of shock. N Engl J Med. 2010;362(9):779-789.
- Law AC, Bosch NA, Peterson D, Walkey AJ. Comparison of heart rate after phenylephrine vs norepinephrine initiation in patients with septic shock and atrial fibrillation. Chest. 2022;162(4):796-803.
- Lamontagne F, Day AG, Meade MO, et al. Pooled analysis of higher versus lower blood pressure targets for vasopressor therapy septic and vasodilatory shock. Intensive Care Med. 2018;44(1):12-21.
- Hylands M, Moller MH, Asfar P, et al. A systematic review of vasopressor blood pressure targets in critically ill adults with hypotension. Can J Anaesth. 2017;64(7):703-715.
- Lamontagne F, Richards-Belle A, Thomas K, et al. Effect of reduced exposure to vasopressors on 90-day mortality in older critically ill patients with vasodilatory hypotension: a randomized clinical trial. JAMA. 2020;323(10):938-949.
- Tian DH, Smyth C, Keijzers G, et al. Safety of peripheral administration of vasopressor medications: a systematic review. Emerg Med Australas. 2020;32(2):220-227.
- Cardenas-Garcia J, Schaub KF, Belchikov YG, Narasimhan M, Koenig SJ, Mayo PH. Safety of peripheral intravenous administration of vasoactive medication. J Hosp Med. 2015;10(9):581-585.
- Delaney A, Finnis M, Bellomo R, et al. Initiation of vasopressor infusions via peripheral versus central access in patients with early septic shock: a retrospective cohort study. Emerg Med Australas. 2020;32(2):210-219.
- McIntyre WF, Um KJ, Alhazzani W, et al. Association of vasopressin plus catecholamine vasopressors vs catecholamines alone with atrial fibrillation in patients with distributive shock: a systematic review and meta-analysis. JAMA. 2018;319(18):1889-1900.
- Nagendran M, Russell JA, Walley KR, et al. Vasopressin in septic shock: an individual patient data meta-analysis of randomised controlled trials. Intensive Care Med. 2019;45(6):844-855.
- Gordon AC, Mason AJ, Thirunavukkarasu N, et al. Effect of early vasopressin vs norepinephrine on kidney failure in patients with septic shock: the VANISH randomized clinical trial. JAMA. 2016;316(5):509-518.
- Khanna A, English SW, Wang XS, et al. Angiotensin II for the treatment of vasodilatory shock. N Engl J Med. 2017;377(5):419-430.
- Annane D, Renault A, Brun-Buisson C, et al. Hydrocortisone plus fludrocortisone for adults with septic shock. N Engl J Med. 2018;378(9):809-818.
- Goodwin JE, Feng Y, Velazquez H, Sessa WC. Endothelial glucocorticoid receptor is required for protection against sepsis. Proc Natl Acad Sci U S A. 2013;110(1):306-311.
- Venkatesh B, Finfer S, Cohen J, et al. Adjunctive glucocorticoid therapy in patients with septic shock. N Engl J Med. 2018;378(9): 797-808.
- Rygẳrd SL, Butler E, Granholm A, et al. Low-dose corticosteroids for adult patients with septic shock: a systematic review with meta¬analysis and trial sequential analysis. Intensive Care Med. 2018;44(7): 1003-1016.
- Annane D, Bellissant E, Bollaert PE, et al. Corticosteroids for treating sepsis in children and adults. Cochrane Database Syst Rev. 2019;12(12):CD002243.
- Pirracchio R, Hubbard A, Sprung CL, Chevret S, Annane D. Rapid Recognition of Corticosteroid Resistant or Sensitive Sepsis (RECORDS) Collaborators. Assessment of machine learning to estimate the individual treatment effect of corticosteroids in septic shock. JAMA Network Open. 2020;3(12):e2029050-e2029050.
- Annane D, Sébille V, Charpentier C, et al. Effect of treatment with low doses of hydrocortisone and fludrocortisone on mortality in patients with septic shock. JAMA. 2002;288(7):862-871.
- Venkatesh B, Finfer S, Cohen J, et al. Adjunctive glucocorticoid therapy in patients with septic shock. N Engl J Med. 2018;378(9): 797-808.
- Sprung CL, Annane D, Keh D, et al. Hydrocortisone therapy for patients with septic shock. N Engl J Med. 2008;358(2):111-124.
- Annane D, Cariou A, Maxime V, et al. Corticosteroid treatment and intensive insulin therapy for septic shock in adults: a randomized controlled trial. JAMA. 2010;303(4):341-348.
- Louis S, Brunton L, Chabner B, Knollmann B. Goodman & Gilman’s Pharmacological Basis of Therapeutics. McGraw-Hill; 2011.
- Heming N, Sivanandamoorthy S, Meng P, Bounab R, Annane D. Immune effects of corticosteroids in sepsis. Front Immunol. 2018;9: 1736.
- Annane D. Why my steroid trials in septic shock were “positive.
Critical Care Med. 2o19;47(12):1789-1793. - Sobolewski KA, Brophy A, Opsha Y, Zaid A, Mistry N. Abrupt versus gradual cessation of steroids in patients with septic shock. J Crit Care. 2018;48:198-202.
- Keh D, Boehnke T, Weber-Cartens S, et al. Immunologic and hemodynamic effects of “low-dose” hydrocortisone in septic shock. Am J Respir Crit Care Med. 2003;167(4):512-520.
- Memis D, Karamanlioglu B, Yuksel M, Gemlik I, Pamukcu Z. The influence of methylene blue infusion on cytokine levels during severe sepsis. Anaesth ỉntensive Care. 2002;30(6):755-762.
- Kirov MY, Evgenov OV, Evgenov NV, et al. Infusion of methylene blue in human septic shock: a pilot, randomized, controlled study. Crit Care Med. 2001;29(10):1860-1867.
- Marik PE, Khangoora V, Rivera R, Hooper MH, Catravas J. Hydrocortisone, vitamin C, and thiamine for the treatment of severe sepsis and septic shock: a retrospective before-after study. Chest. 2017;151(6):1229-1238.
- Fujii T, Salanti G, Belletti A, et al. Effect of adjunctive vitamin C, glucocorticoids, and vitamin B1 on longer-term mortality in adults with sepsis or septic shock: a systematic review and a component network meta-analysis. ỉntensive Care Med. 2022;48(1):16-24.
- Lamontagne F, Masse MH, Menard J, et al. Intravenous vitamin C in adults with sepsis in the intensive care unit. N Engl J Med. 2022;386(25):2387-2398.
- Demiselle J, Fage N, Radermacher P, Asfar P. Vasopressin and its analogues in shock states: a review. Ann ỉntensive Care. 2020;10(1):9.
- Martin C, Medam S, Antonini F, et al. Norepinephrine: not too much, too long. Shock. 2015;44(4):305-309.
- Brown SM, Lanspa MJ, Jones JP, et al. Survival after shock requiring high-dose vasopressor therapy. Chest. 2013;143(3):664-671.
- Auchet T, Regnier MA, Girerd N, Levy B. Outcome of patients with septic shock and high-dose vasopressor therapy. Ann ỉntensive Care. 2017;7(1):43.
- Morelli A, Ertmer C, Lange M, et al. Effects of short-term simultaneous infusion of dobutamine and terlipressin in patients with septic shock: the DOBUPRESS study. Br JAnaesth. 2008;100(4): 494-503.
- Dorman T, Bresl ow MJ, Lipsett PA, et al. Radial artery pressure monitoring underestimates central arterial pressure during vasopressor therapy in critically ill surgical patients. Crit Care Med. 1998;26(10):1646-1649.
- Jaber S, Paugam C, Futier E, et al. Sodium bicarbonate therapy for patients with severe metabolic acidaemia in the intensive care unit (BICAR-ICU): a multicentre, open-label, randomised controlled, phase 3 trial. Lancet. 2018;392(10141):31-40.
- Page IH, Olmsted F. The influence of respiratory gas mixtures on arterial pressure and vascular reactivity in normal and hypertensive dogs. Circulation. 1951;3(6):801-819.
- Modest VE, JFt Butterworth. Effect of pH and lidocaine on beta- adrenergic receptor binding. Interaction during resuscitation? Chest. 1995;108(5):1373-1379.
- Hammond DA, McCain K, Painter JT, et al. Discontinuation of vasopressin before norepinephrine in the recovery phase of septic shock. J ỉntensive Care Med. 2019;34(10):805-810.
- Bissell BD, Magee C, Moran P, Bastin MLT, Flannery AH. Hemodynamic instability secondary to vasopressin withdrawal in septic shock. J ỉntensive Care Med. 2019;34(9):761-765.
- Bauer SR, Aloi JJ, Ahrens CL, Yeh JY, Culver DA, Reddy AJ. Discontinuation of vasopressin before norepinephrine increases the incidence of hypotension in patients recovering from septic shock: a retrospective cohort study. J Crit Care. 2010;25(2):362.e367. 362. e311.
- Musallam N, Altshuler D, Merchan C, Zakhary B, Aberle C, Papadopoulos J. Evaluating vasopressor discontinuation strategies in patients with septic shock on concomitant norepinephrine and vasopressin infusions. Ann Pharmacother. 2018;52(8):733-739.
- Santer P, Anstey MH, Patrocinio MD, et al. Effect of midodrine versus placebo on time to vasopressor discontinuation in patients with persistent hypotension in the intensive care unit (MIDAS): an international randomised clinical trial. ỉntensive Care Med. 2020;46(10):1884-1893.
- Rizvi MS, Nei AM, Gajic O, Mara KC, Barreto EF. Continuation of newly initiated midodrine therapy after intensive care and hospital discharge: a single-center retrospective study. Crit Care Med. 2019;47(8):e648-e653.