Metformin

Biên soạn và Hiệu đính
Dược sĩ Phan Hữu Xuân Hạo – Khoa Dược, Trường Y Dược – Đại học Duy Tân.
Danh pháp
Tên chung quốc tế
Metformin
Tên danh pháp theo IUPAC
3-(diaminomethylidene)-1,1-dimethylguanidine
Nhóm thuốc
Thuốc chống đái tháo đường nhóm biguanid
Mã ATC
A10BA02
A – Đường tiêu hóa và chuyển hóa
A10 – Thuốc chống đái tháo đường
A10B – Thuốc uống giảm Glucose máu
A10BA – Các Biguanides
A10BA02 – Metformin
Phân loại nguy cơ cho phụ nữ có thai
Nhóm B
Mã UNII
9100L32L2N
Mã CAS
657-24-9
Cấu trúc phân tử
Công thức phân tử
C4H11N5
Phân tử lượng
129.16g/mol
Cấu trúc phân tử
Metformin là một dẫn xuất của nhóm guanidine (biguanide), mang hai nhóm thế metyl ở vị trí 1
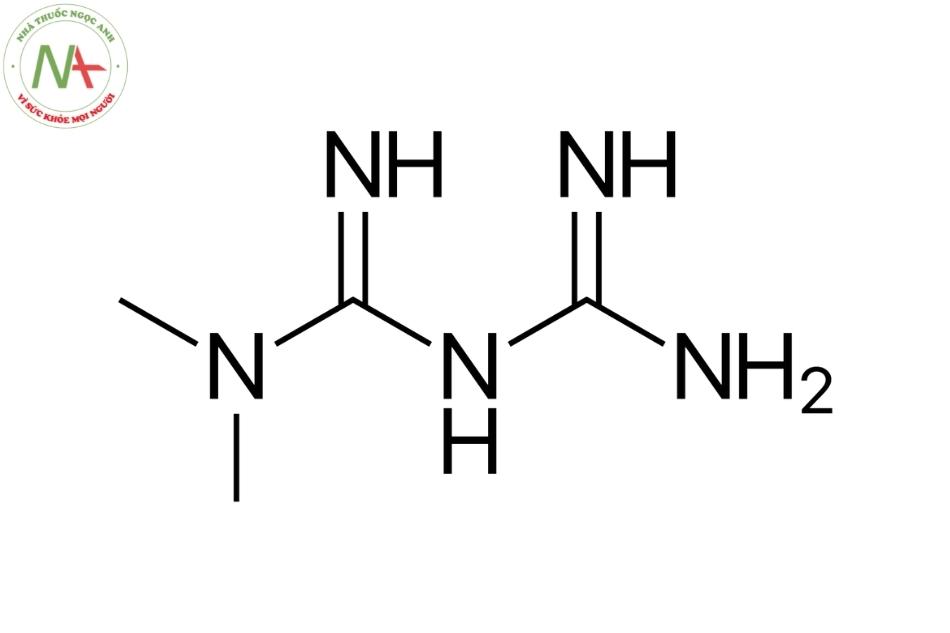
Các tính chất phân tử
Số liên kết hydro cho: 3
Số liên kết hydro nhận: 1
Số liên kết có thể xoay: 2
Diện tích bề mặt tôpô: 91.5 Ų
Số lượng nguyên tử nặng: 9
Các tính chất đặc trưng
Metformin có khả năng hòa tan tự do trong nước, tan ít trong rượu và thực tế không tan trong ete, cloroform, aceton, metylen clorua. Khi phân hủy bằng nhiệt, metformin giải phóng các khí độc hại như COx, NOx
Điểm nóng chảy: 223-226°C
Điểm sôi: 224,1ºC ở 760mmHg
Áp suất hơi: 7.58 x 10-5 mmHg ở 25 °C
Độ tan trong nước: 1,38mg/mL
Hằng số phân ly pKa: 12,4
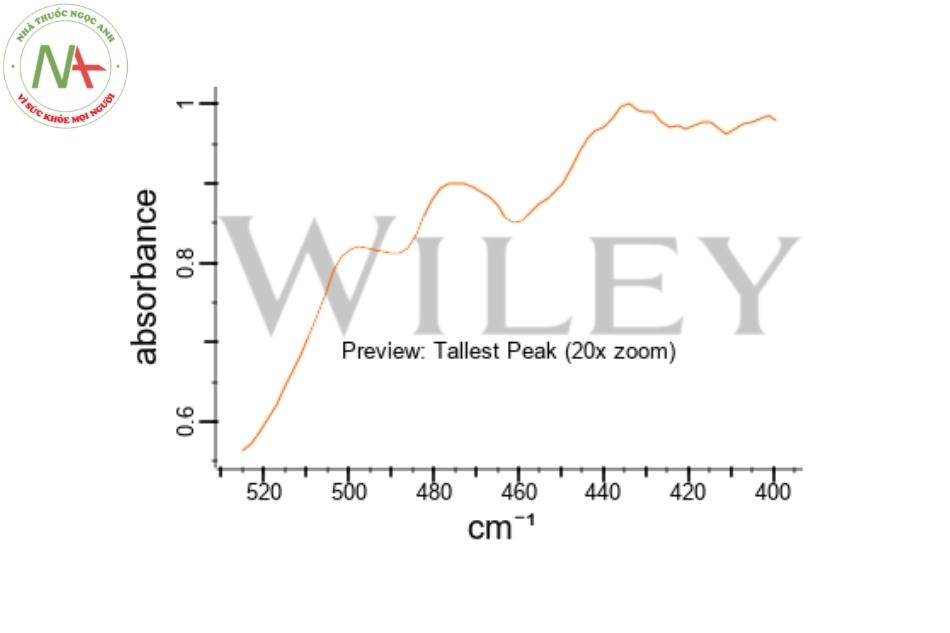
Phổ hồng ngoại: Đạt cực đại tại 434cm-1
Cảm quan
Metformin có dạng bột kết tinh màu trắng, tan vô hạn trong nước.

Dạng bào chế
Viên nén: 500mg; 850mg; 1000mg.
Độ ổn định và điều kiện bảo quản
Viên nén metformin hydroclorid cần bảo quản ở nhiệt độ 15-30°C.
Nguồn gốc
Nhóm biguanide điều trị đái tháo đường, cũng bao gồm các thuốc khác đã bị thu hồi như phenformin và buformin, đều có nguồn gốc từ hoa Tử Đinh Hương Pháp (Galega officinalis), một loại cây được sử dụng trong y học dân gian trong nhiều thế kỷ.
Metformin lần đầu tiên được mô tả trong các tài liệu khoa học vào năm 1922, bởi Emil Werner và James Bell, như một sản phẩm trong tổng hợp N, N-dimethylguanidine. Năm 1929, Slotta và Tschesche phát hiện ra tác động hạ đường của Metformin ở thỏ, cho thấy metformin là chất tương tự biguanide mạnh nhất mà họ từng nghiên cứu. Tuy nhiên kết quả này đã hoàn toàn bị lãng quên vì các chất tương tự biguanide khác như synthalins, đã bị thay thế và sớm bị lu mờ bởi insulin.
Sự quan tâm đến metformin được trở lại vào cuối những năm 1940. Đến năm 1950, metformin, không giống như một số hợp chất tương tự khác, đã được tìm thấy là không làm giảm huyết áp và nhịp tim ở động vật. Năm đó, bác sĩ người Philippines Eusebio Y. Garcia đã sử dụng metformin (ông đặt tên là Fluamine) để điều trị cúm.
Ông cũng lưu ý rằng thuốc “làm giảm lượng đường trong máu đến giới hạn sinh lý tối thiểu” và không độc hại. Garcia tin rằng metformin có các hành động diệt khuẩn, kháng virus, chống sốt rét, hạ sốt rét và giảm đau. Trong một loạt các bài báo vào năm 1954, nhà dược học người Ba Lan Janusz Supniewski đã không thể xác nhận hầu hết các tác dụng này, bao gồm cả việc giảm lượng đường trong máu. Thay vào đó, ông quan sát tác dụng kháng virus ở người.
Nhà đái tháo đường học người Pháp Jean Sterne đã nghiên cứu các đặc tính chống sốt đường huyết của galegine – một alkaloid được phân lập từ G. officinalis, có liên quan đến cấu trúc của metformin, và đã thấy nó được sử dụng ngắn hạn như một chất chống đái tháo đường trước khi synthalins được phát triển.
Sau đó, khi làm việc tại Laboratoires Aron ở Paris, ông được thúc đẩy bởi báo cáo của Garcia để điều tra lại hoạt động hạ đường huyết của metformin và một số chất tương tự biguanide. Sterne là người đầu tiên thử metformin trên người để điều trị bệnh tiểu đường, ông đã đặt tên “Glucophage” cho thuốc và công bố kết quả của mình vào năm 1957.
Sự quan tâm rộng rãi đối với metformin đã không được nhen nhóm cho đến khi các biguanides khác bị thu hồi trong những năm 1970. Mặc dù được phê duyệt ở Canada vào năm 1972, nhưng metformin không nhận được sự chấp thuận của Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) cho bệnh đái tháo đường loại 2 cho đến năm 1994.
Được sản xuất theo giấy phép của Bristol-Myers Squibb, Glucophage là công thức metformin có thương hiệu đầu tiên được bán trên thị trường Hoa Kỳ, bắt đầu từ ngày 3 tháng 3 năm 1995. Các công thức chung hiện có sẵn ở một số quốc gia và metformin được cho là đã trở thành loại thuốc chống đái tháo đường được kê đơn rộng rãi nhất thế giới.
Cơ chế hoạt động
Metformin có cơ chế tác dụng khác so với các nhóm thuốc điều trị đái tháo đường khác. Theo đó, metformin làm giảm nồng độ đường huyết bằng cách giảm sản xuất glucose ở gan, giảm hấp thu glucose ở ruột. Hơn nữa làm tăng độ nhạy của insulin bằng cách tăng hấp thu và sử dụng glucose ở ngoại vi.
Các quá trình này dẫn đến giảm lượng đường trong máu, kiểm soát bệnh tiểu đường loại 2 cũng như có tác dụng tích cực trong việc kiểm soát đường huyết.
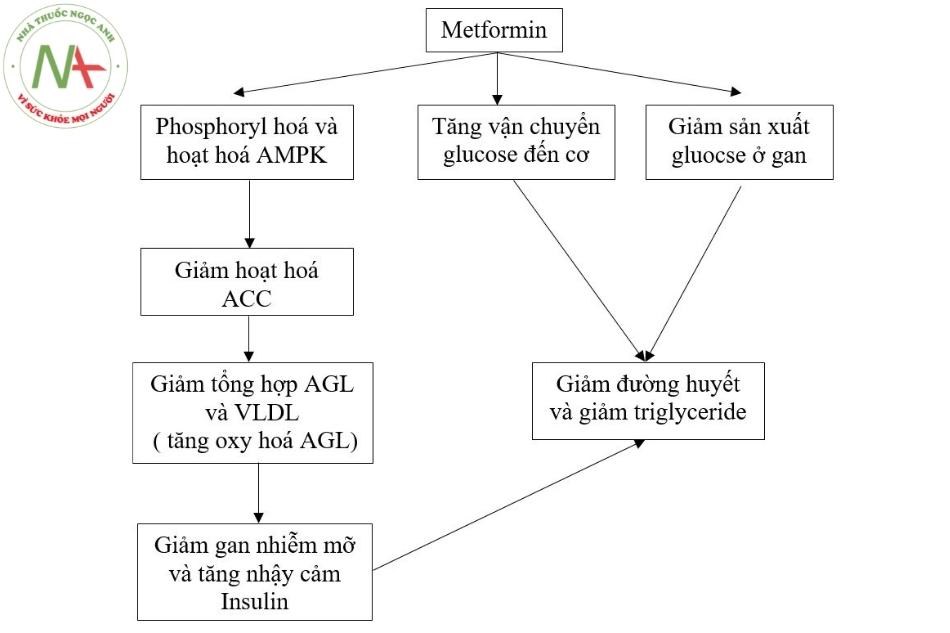
Ngoài ra, metformin còn có tác động tích cực trên chuyển hóa lipid, làm giảm cholesterol toàn phần, LDL-cholesterol và cả triglycerid. Trái với các sulfonylurea, trọng lượng cơ thể của người được điều trị bằng metformin có xu hướng ổn định hoặc giảm nhẹ.
Dùng metformin đơn trị liệu có thể có hiệu quả tốt đối với những người bệnh không đáp ứng hoặc chỉ đáp ứng một phần với sulfonylurea hoặc những người không còn đáp ứng với sulfonylurea. Ở những người bệnh này, nếu với metformin đơn trị liệu mà đường huyết vẫn không được khống chế theo yêu cầu thì phối hợp metformin với một sulfonylurea có thể có tác dụng hiệp đồng, vì cả hai thuốc cải thiện dung nạp glucose bằng những cơ chế khác nhau nhưng lại bổ sung cho nhau.
Ứng dụng trong y học
Metformin được sử dụng để giảm lượng đường trong máu ở những người mắc bệnh đái tháo đường loại 2. Ngoài ra, nó cũng được sử dụng như một liệu pháp thứ hai để điều trị vô sinh ở những người mắc hội chứng buồng trứng đa nang.
Đái tháo đường type 2
Hiệp hội Đái tháo đường Hoa Kỳ và Đại học Bác sĩ Hoa Kỳ đều khuyến nghị metformin như một liệu pháp đầu tay để điều trị bệnh đái tháo đường loại 2. Nó có tác dụng như repaglinide và hiệu quả hơn tất cả các loại thuốc đường uống trị đái tháo đường týp 2 khác.
Nghiên cứu tiền cứu ở Vương quốc Anh được thực hiện trong những năm 1980–90 đã cung cấp bằng chứng rằng metformin làm giảm tỷ lệ kết quả tim mạch bất lợi ở bệnh nhân thừa cân mắc bệnh đái tháo đường loại 2 so với các thuốc hạ đường huyết khác. Kết quả được cải thiện ngay cả ở những người bị bệnh thận, suy tim hoặc bệnh gan mãn tính ở một mức độ tương đối.
Hướng dẫn điều trị cho các hiệp hội chuyên môn lớn, bao gồm Hiệp hội Châu Âu về Nghiên cứu Bệnh Đái tháo đường, Hiệp hội Tim mạch Châu Âu và Hiệp hội Đái tháo đường Hoa Kỳ, hiện mô tả bằng chứng về lợi ích tim mạch của metformin là tương đương.
Một nghiên cứu đánh giá năm 2014 đã tìm thấy bằng chứng dự kiến rằng những người được điều trị bằng sulfonylurea có nguy cơ cao bị các biến cố hạ đường huyết nghiêm trọng, mặc dù nguy cơ mắc các biến cố tim mạch của họ thấp hơn nguy cơ của những người được điều trị bằng metformin nhưng vào thời điểm đó, không có đủ dữ liệu để xác định nguy cơ tử vong tương đối hoặc tử vong do bệnh tim.
Việc sử dụng metformin làm giảm trọng lượng cơ thể ở những người mắc bệnh đái tháo đường týp 2 trái ngược với sulfonylurea, có liên quan đến tăng cân. Một số bằng chứng cho thấy metformin có liên quan đến việc giảm cân ở bệnh nhân béo phì khi không mắc bệnh đái tháo đường. Ngoài ra metformin cũng làm giảm một cách khiêm tốn nồng độ lipoprotein và triglycerid mật độ thấp.
Hội chứng buồng trứng đa nang
Ở những người mắc hội chứng buồng trứng đa nang (PCOS), bằng chứng dự kiến cho thấy việc sử dụng metformin làm tăng tỷ lệ sống sót, bao gồm cả những người không thể mang thai với clomiphene.
Theo đó, metformin dường như không làm thay đổi nguy cơ sẩy thai và một số lợi ích khác cũng đã được tìm thấy cả trong thời kỳ mang thai và phụ nữ không mang thai bị PCOS.
Tuy nhiên, trong một đánh giá cập nhật của Cochrane (2020) về metformin so với giả dược/không điều trị trước hoặc trong khi thụ tinh ống nghiệm/ICSI ở phụ nữ bị PCOS, không tìm thấy bằng chứng thuyết phục nào về việc cải thiện tỷ lệ sinh sống.
Mặt khác, trong các phác đồ dài GnRH-agonist, các bằng chứng về cải thiện tỷ lệ sống sót không được chắc chắn nhưng có thể tăng tỷ lệ mang thai lâm sàng. Ngược lại trong các phác đồ ngắn GnRH-agonist, metformin có thể làm giảm tỷ lệ sống mà không chắc chắn về ảnh hưởng của nó đối với tỷ lệ mang thai lâm sàng.
Metformin có thể làm giảm OHSS nhưng có thể đi kèm với tần suất tác dụng phụ nhiều hơn. Hơn nữa, tác động của metformin đối với sảy thai là không chắc chắn. Do đó, các bằng chứng không ủng hộ việc sử dụng chung trong thời kỳ mang thai để cải thiện kết quả của bà mẹ và trẻ sơ sinh ở phụ nữ béo phì.
Vào năm 2004, Viện Y tế và Lâm sàng Quốc gia của Vương quốc Anh đã khuyến cáo rằng phụ nữ bị PCOS và có chỉ số khối cơ thể trên 25 nên được cung cấp metformin để điều trị rụng trứng và vô sinh khi các liệu pháp khác không mang lại kết quả.
Các hướng dẫn thực hành lâm sàng của Vương quốc Anh và quốc tế không khuyến cáo metformin như một phương pháp điều trị đầu tay hoặc hoàn toàn không khuyến cáo, ngoại trừ phụ nữ không dung nạp glucose. Các hướng dẫn đề xuất clomiphene là lựa chọn thuốc đầu tiên và nhấn mạnh việc thay đổi lối sống độc lập với điều trị y tế.
Điều trị bằng metformin làm giảm nguy cơ phát triển bệnh đái tháo đường týp 2 ở phụ nữ bị PCOS có biểu hiện rối loạn dung nạp glucose lúc ban đầu.
Đái tháo đường và thai nghén
Một đánh giá tổng thể về việc sử dụng metformin trong thời kỳ mang thai so với insulin đơn thuần cho thấy hiệu quả ngắn hạn tốt cho cả mẹ và con, nhưng không rõ ràng về độ an toàn lâu dài.
Một số nghiên cứu quan sát và thử nghiệm ngẫu nhiên có đối chứng cho thấy metformin có hiệu quả và an toàn như insulin trong việc kiểm soát bệnh đái tháo đường thai kỳ. Tuy nhiên, một số lo ngại đã được đưa ra và thiếu bằng chứng về tính an toàn lâu dài của metformin cho cả mẹ và con.
So với insulin, phụ nữ bị đái tháo đường thai kỳ được điều trị bằng metformin tăng nhẹ cân hơn và ít có khả năng bị tiền sản giật khi mang thai. Trẻ sinh ra từ những phụ nữ được điều trị bằng metformin có ít chất béo nội tạng hơn, và điều này có thể khiến chúng ít bị đề kháng insulin hơn trong cuộc sống sau này.
Việc sử dụng metformin cho bệnh đái tháo đường thai kỳ dẫn đến trẻ nhỏ hơn so với điều trị bằng insulin. Tuy nhiên, mặc dù ban đầu nhẹ cân hơn khi sinh, trẻ em tiếp xúc với metformin trong thời kỳ mang thai đã tăng trưởng nhanh hơn sau khi sinh và nặng hơn vào giữa thời thơ ấu so với những trẻ em tiếp xúc với insulin trong thai kỳ.
Hình thái trẻ sơ sinh nhẹ cân ban đầu nhưng tốc độ tăng trưởng bắt kịp vượt trội so với trẻ em so sánh có liên quan đến bệnh chuyển hóa tim lâu dài.
Thay đổi cân nặng
Sử dụng metformin thường liên quan đến giảm cân. Nó có vẻ an toàn và hiệu quả trong việc chống lại sự tăng cân do thuốc chống loạn thần olanzapine và clozapine. Mặc dù sự đảo ngược khiêm tốn của tăng cân liên quan đến clozapine được tìm thấy với metformin, việc ngăn ngừa tăng cân chính có giá trị hơn.
Sử dụng với insulin
Metformin có thể làm giảm nhu cầu insulin ở bệnh tiểu đường loại 1, mặc dù làm tăng nguy cơ hạ đường huyết.
Dược lực học
Sau khi uống, chất vận chuyển OCT1 chịu trách nhiệm hấp thu metformin vào tế bào gan. Khi loại thuốc này được tích điện dương, nó sẽ tích tụ trong tế bào và trong ty thể do các điện thế màng xuyên qua màng sinh chất cũng như màng trong của ty thể.
Metformin ức chế phức hợp I của ty thể, ngăn cản việc sản xuất ATP của ty thể dẫn đến tăng tỷ lệ ADP và AMP trong tế bào chất. Những thay đổi này kích hoạt protein kinase hoạt hóa AMP (AMPK-một loại enzyme đóng vai trò quan trọng trong việc điều hòa chuyển hóa glucose).
Ngoài cơ chế này, AMPK có thể được kích hoạt bằng cơ chế lysosome liên quan đến các chất hoạt hóa khác. Sau quá trình này, sự gia tăng tỷ lệ AMP:ATP cũng ức chế enzym fructose-1,6-bisphosphatase, dẫn đến việc ức chế quá trình tạo glucose, đồng thời ức chế adenylate cyclase và giảm sản xuất cyclic adenosine monophosphate (cAMP), một dẫn xuất của ATP được sử dụng cho tín hiệu tế bào.
Tiếp đó AMPK được hoạt hóa sẽ phosphoryl hóa hai đồng dạng của enzyme acetyl-CoA carboxylase, do đó ức chế tổng hợp chất béo và dẫn đến quá trình oxy hóa chất béo, giảm dự trữ ở gan và tăng độ nhạy cảm của gan với insulin. Ở ruột, metformin làm tăng chuyển hóa glucose kỵ khí trong các tế bào ruột, dẫn đến giảm hấp thu glucose và tăng vận chuyển lactate đến gan.
Dược động học
Hấp thu
Sau khi uống, metformin được hấp thu chậm và không hoàn toàn ở đường tiêu hóa, chủ yếu ở ruột non. Sinh khả dụng đường uống khoảng 50 – 60% khi đói, nồng độ đỉnh trong huyết tương đạt được trong vòng 1 – 3 giờ đối với dạng giải phóng tức thì và 4 – 8 giờ đối với dạng giải phóng kéo dài. Mức độ và tốc độ hấp thu của metformin giảm khi uống cùng thức ăn.
Phân bố
Metformin liên kết với protein huyết tương không đáng kể, có thể phân bố nhanh chóng vào các mô và dịch cơ thể với khối lượng phân phối trung bình sau khi uống liều 850mg ở mức 654 ± 358L.
Hơn nữa, thuốc cũng phân bố vào trong hồng cầu. Các nghiên cứu hiện tại vẫn chưa xác định liệu metformin có vượt qua hàng rào máu não, nhau thai hay vào sữa mẹ ở người hay không, tuy nhiên ở chuột cho con bú, metformin được phân phối vào sữa mẹ ở mức tương đương với huyết tương.
Chuyển hóa
Metformin hầu như không bị chuyển hóa.
Thải trừ
Sau khi uống, khoảng 90% lượng thuốc hấp thu được thải trừ qua nước tiểu trong vòng 24 giờ đầu ở dạng không chuyển hóa. Thời gian bán thải của thuốc trong huyết tương là 6,2 giờ. Độ thanh thải metformin qua thận giảm ở người suy thận và người cao tuổi, do đó có thể có nguy cơ tích lũy thuốc.
Chống chỉ định
Bệnh nhân suy thận nặng, (eGFR dưới 30mL/phút/1,73m2)
Bệnh nhân có tiền sử quá mẫn với metformin
Bệnh nhân toan chuyển hóa cấp tính hoặc mãn tính, bao gồm cả nhiễm toan ceton do đái tháo đường.
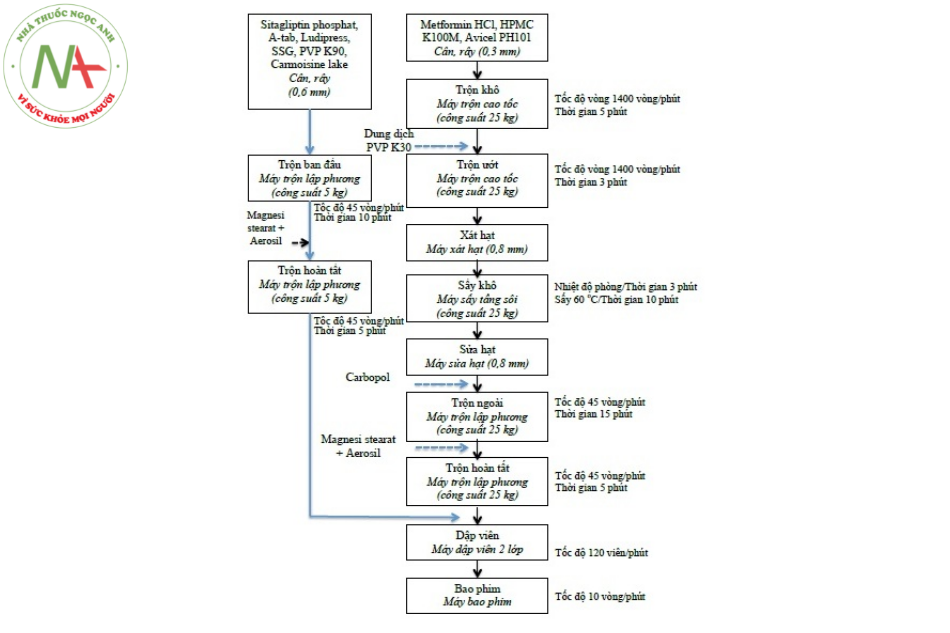
Phương pháp sản xuất
Trên thực tế, metformin được sản xuất dưới dạng metformin hydroclorid. Theo quy trình được mô tả trong bằng sáng chế Aron năm 1975 và Bách khoa toàn thư về sản xuất dược phẩm, lượng đồng cực của dimetylamin và 2-cyanoguanidine được hòa tan trong toluen bằng cách làm lạnh để tạo thành dung dịch đậm đặc.
Sau đó một lượng hiđro clorua được thêm vào từ từ bằng phương pháp phân cực. Hỗn hợp bắt đầu tự sôi và sau khi làm lạnh, metformin hydroclorid kết tủa với hiệu suất 96%.
Độc tính ở người
Biến chứng chuyển hóa hiếm gặp nhưng nghiêm trọng như nhiễm toan lactic có thể xảy ra do tích tụ metformin trong quá trình điều trị với tỷ lệ tử vong khoảng 50%. Sự khởi phát của nhiễm toan lactic thường rất nhẹ và chỉ kèm theo các triệu chứng không đặc hiệu như khó chịu, đau cơ, suy hô hấp, buồn ngủ ngày càng tăng và đau bụng dưới không đặc hiệu. Ngoài ra có thể có hạ thân nhiệt, hạ huyết áp và loạn nhịp tim kháng trị với tình trạng nhiễm toan rõ rệt hơn.
Nhiễm toan lactic cũng có thể xảy ra liên quan đến một số tình trạng sinh lý bệnh, bao gồm đái tháo đường, và bất cứ khi nào có sự giảm tưới máu đáng kể ở mô và giảm oxy máu. Nhiễm toan lactic được đặc trưng bởi nồng độ lactate trong máu tăng cao (>5mmol/L), giảm pH trong máu, rối loạn điện giải với tăng khoảng cách anion và tăng tỷ lệ lactate/pyruvate.
Khi metformin được coi là nguyên nhân gây nhiễm toan lactic, nồng độ metformin trong huyết tương >5ug/mL. Tỷ lệ nhiễm toan lactic được báo cáo ở những bệnh nhân dùng viên nén metformin hydrochloride, USP là rất thấp (khoảng 0,03 trường hợp/1000 bệnh nhân năm, với khoảng 0,015 trường hợp tử vong/1000 bệnh nhân năm).
Các trường hợp được ghi nhận chủ yếu ở những bệnh nhân đái tháo đường bị suy thận đáng kể, bao gồm cả bệnh thận nội tại và suy giảm tưới máu thận, thường do mắc nhiều bệnh nội khoa hoặc phẫu thuật đồng thời và dùng nhiều thuốc cùng lúc. Nguy cơ nhiễm toan lactic tăng lên theo mức độ rối loạn chức năng thận và tuổi của bệnh nhân.
Thận trọng khi sử dụng
Suy thận
Những ca nhiễm toan lactic liên quan đến metformin trong quá trình giám sát hậu mãi xảy ra chủ yếu trên những bệnh nhân suy thận nặng. Nguy cơ tích lũy metformin và nhiễm toan lactic liên quan đến metformin tăng lên theo mức độ nghiêm trọng của suy thận.
Vì metformin đào thải qua thận nên trước khi bắt đầu điều trị, người bệnh cần được kiểm tra creatinin huyết thanh. Sau đó, tiếp tục kiểm tra đều đặn tối thiểu 1 lần/năm ở người có chức năng thận bình thường, và ít nhất 2 – 4 lần/năm ở người có creatinin huyết thanh cao hơn giới hạn bình thường và cả ở người cao tuổi.
Các xét nghiệm chẩn đoán có sử dụng thuốc cản quang
Các thuốc cản quang chứa iod có thể gây suy giảm cấp tính chức năng thận và dẫn tới nhiễm toan lactic, do đó phải ngừng metformin trước hoặc vào thời điểm tiến hành X-quang và chỉ uống lại metformin trong 48 giờ sau khi kiểm tra chức năng thận đã trở lại bình thường.
Phẫu thuật hoặc các thủ thuật khác
Sự lưu giữ thức ăn và dịch trong quá trình phẫu thuật hoặc thực hiện các thủ thuật khác có thể làm tăng nguy cơ giảm thể tích, hạ huyết áp và suy thận. Do đó, phải ngừng metformin trong 48 giờ trước mọi can thiệp ngoại khoa như gây mê toàn thân, gây mê tủy sống hoặc quanh màng cứng. Chỉ dùng lại metformin 48 giờ sau can thiệp hoặc ăn uống trở lại bằng đường miệng và sau khi chắc chắn chức năng thận đã trở lại bình thường.
Tình trạng giảm oxy hít vào
Quá trình theo dõi hậu mãi đã ghi nhận một số ca nhiễm toan lactic liên quan đến metformin xảy ra trong bệnh cảnh suy tim sung huyết cấp, đặc biệt là khi có kèm theo giảm tưới máu và giảm oxy huyết. Trụy tim mạch (sốc), nhồi máu cơ tim cấp, nhiễm khuẩn huyết và các bệnh lý khác liên quan đến giảm oxy máu có mối liên quan với toan lactic và cũng có thể gây nitơ huyết trước thận.
Uống rượu
Rượu có khả năng ảnh hưởng đến tác động của metformin lên chuyển hóa lactate và từ đó có thể làm tăng nguy cơ nhiễm toan lactic liên quan đến metformin.
Suy gan
Bệnh nhân suy gan có thể tiến triển thành toan lactic liên quan đến metformin do suy giảm thải trừ lactat, dẫn đến tăng nồng độ lactate trong máu. Vì vậy, tránh sử dụng metformin trên những bệnh nhân đã được chẩn đoán bệnh gan thông qua bằng chứng xét nghiệm lâm sàng.
Tương tác với thuốc khác
Có tổng cộng 353 loại thuốc được biết là có tương tác với metformin, trong đó có 19 tương tác mức độ nghiêm trọng, 305 tương tác trung bình và 29 tương tác không đáng kể.
| Thuốc | Tương tác |
| Acetazolamide | Sử dụng metformin cùng với acetazolamide có thể làm tăng nguy cơ nhiễm toan lactic. Khả năng xảy ra cao hơn ở người bị bệnh thận hoặc gan, suy tim sung huyết cấp tính hoặc không ổn định, mất nước hoặc uống quá nhiều rượu. |
| Metrizamide | Sử dụng metformin cùng với các thuốc cản quang có chứa iod như metrizamide có thể gây suy thận và nhiễm toan lactic. |
| Gatifloxacin | Gatifloxacin có thể ảnh hưởng đến tác dụng điều trị của insulin cũng như các thuốc chống đái tháo đường khác. |
| Abemaciclib | Abemaciclib có thể làm tăng nồng độ và tác dụng trong máu của metformin, dẫn đến gia tăng các tác dụng phụ như buồn nôn, nôn mửa, tiêu chảy, đầy hơi và khó tiêu. |
| Aripiprazole | Aripiprazole có thể ảnh hưởng đến việc kiểm soát đường huyết và làm giảm hiệu quả của metformin cũng như các loại thuốc chống đái tháo đường khác. |
Một vài nghiên cứu của Metformin trong Y học
Sử dụng Metformin trong điều trị viêm gan nhiễm mỡ không do rượu
Cơ sở: Các chất làm nhạy cảm insulin có thể hữu ích trong điều trị bệnh gan nhiễm mỡ không do rượu.
Mục tiêu: Nghiên cứu thử nghiệm để đánh giá hiệu quả và độ an toàn của metformin trong bệnh gan nhiễm mỡ không do rượu.
Phương pháp: Trong một nghiên cứu mở, bệnh nhân bị bệnh gan nhiễm mỡ không do rượu đã được xác nhận về mặt mô học và được cho dùng metformin (20 mg/kg) trong 1 năm. Đề kháng insulin (phân tích mô hình đánh giá cân bằng nội mô bằng log cho đề kháng insulin và Chỉ số kiểm tra độ nhạy insulin định lượng) và mô học gan sau điều trị được so sánh với mô học trước điều trị.
Kết quả: Mười lăm bệnh nhân đã hoàn thành 1 năm điều trị. Trong 3 tháng đầu, có sự cải thiện về alanin aminotransferase và aspartate aminotransferase (P-value 0,01 và 0,02, tương ứng) cùng với sự cải thiện về độ nhạy insulin.
Tuy nhiên, sau 3 tháng, độ nhạy insulin không được cải thiện hơn nữa và có sự gia tăng dần dần của aspartate aminotransferase và alanine aminotransferase trở lại mức trước khi điều trị. Trong số 10 bệnh nhân được sinh thiết sau điều trị, ba bệnh nhân (33%) cho thấy cải thiện tình trạng nhiễm mỡ, hai bệnh nhân (20%) cho thấy cải thiện điểm viêm và một bệnh nhân(10%) cho thấy cải thiện xơ hóa.
Kết luận: Điều trị bằng metformin chỉ cải thiện thoáng qua các thông số ở gan. Sự giảm độ nhạy insulin tiến triển và bền vững không được ghi nhận trong quá trình điều trị.
Liệu pháp đầu tiên cho bệnh tiểu đường loại 2 với chất ức chế natri-glucose Cotransporter-2 và chất đồng vận thụ thể giống như Peptide-1 Glucagon
Cơ sở: Các hướng dẫn khuyến nghị chất ức chế natri-glucose cotransporter-2 (SGLT2) và chất chủ vận thụ thể glucagon-like peptide-1 (GLP1) như là liệu pháp điều trị bậc hai cho bệnh nhân tiểu đường loại 2. Việc mở rộng sử dụng chúng như là liệu pháp đầu tay đã được đề xuất nhưng lợi ích lâm sàng có thể không lớn hơn chi phí của chúng.
Mục tiêu: Để đánh giá hiệu quả chi phí suốt đời của chiến lược sử dụng thuốc ức chế SGLT2 hàng đầu hoặc thuốc chủ vận thụ thể GLP1.
Kết quả : Thuốc ức chế SGLT2 bậc 1 và chất chủ vận thụ thể GLP1 có tỷ lệ suy tim sung huyết, thiếu máu cục bộ, nhồi máu cơ tim và đột quỵ thấp hơn so với metformin. Thuốc ức chế SGLT2 dòng đầu tiên có giá cao hơn 43 000 đô la và thêm 1,8 tháng điều chỉnh chất lượng so với metformin dòng đầu tiên (478 000 đô la cho số năm sống điều chỉnh theo chất lượng cuộc sống [QALY]). Thuốc chủ vận thụ thể GLP1 dạng tiêm đầu tiên có giá cao hơn và giảm QALYs so với metformin.
Bằng cách loại bỏ tình trạng không thể tiêm, các chất chủ vận thụ thể GLP1 bậc một không còn bị chi phối nữa (ICER, $ 327 000 mỗi QALY). Thuốc chủ vận thụ thể GLP1 đường uống không hiệu quả về chi phí (ICER, $ 823 000 mỗi QALY). Để tiết kiệm chi phí dưới 150 000 đô la mỗi QALY, chi phí cho chất ức chế SGLT2 sẽ cần dưới 5 đô la mỗi ngày và dưới 6 đô la mỗi ngày cho chất chủ vận thụ thể GLP1 đường uống.
ICER: Tuổi thọ, chi phí trọn đời, tỷ lệ hiệu quả chi phí gia tăng
Kết quả: Là thuốc đầu tay, chất ức chế SGLT2 và chất chủ vận thụ thể GLP1 sẽ cải thiện kết quả bệnh tiểu đường loại 2, nhưng chi phí của chúng sẽ cần giảm ít nhất 70% để có hiệu quả hơn về chi phí trong điều trị.
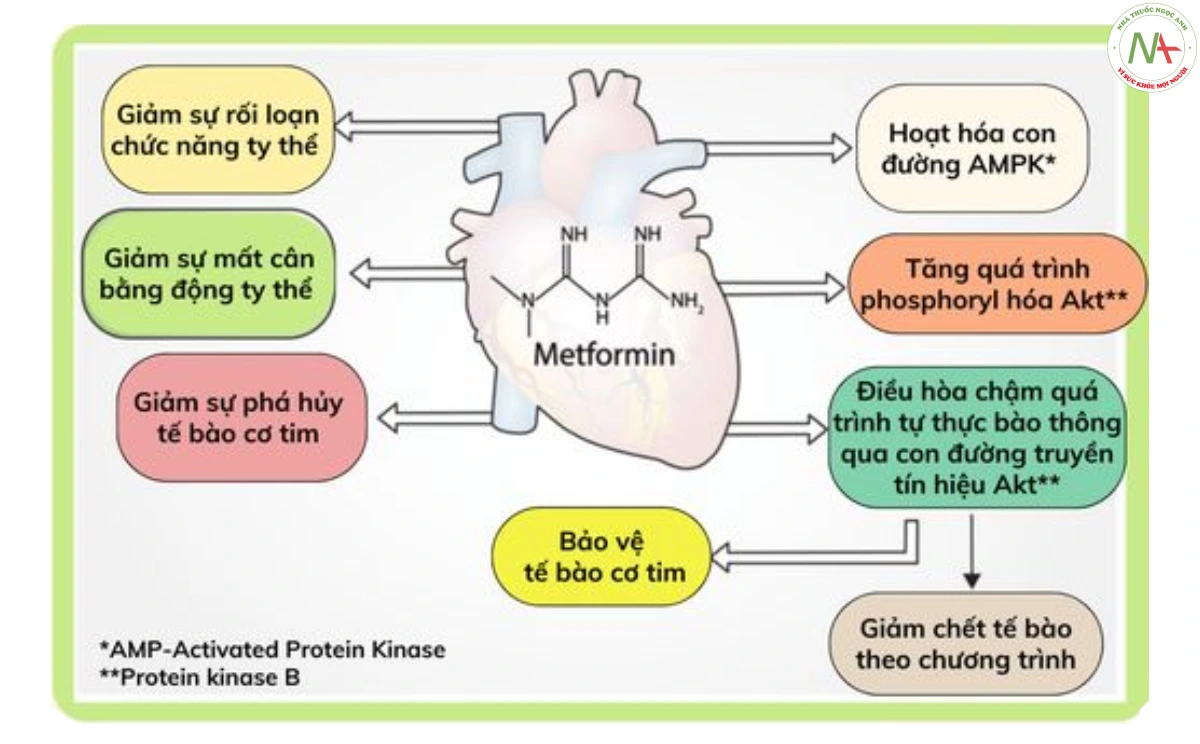
TÁC ĐỘNG CỦA METFORMIN ĐỐI VỚI TỔN THƯƠNG TÁI TƯỚI MÁU DO THIẾU MÁU CỤC BỘ: BẰNG CHỨNG VÀ CƠ CHẾ MỚI
Vào tháng 6 năm 2021, Tổ chức Y tế Thế giới đã liệt kê các bệnh tim mạch là một trong những nguyên nhân gây tử vong hàng đầu trên toàn thế giới (chiếm 32%) và phổ biến nhất là bệnh động mạch vành.
Metformin là một trong những thuốc được sử dụng nhiều nhất để kiểm soát bệnh đái tháo đường. Bên cạnh đó, thuốc này cũng đã cho thấy những tác dụng khác vượt xa khả năng kiểm soát đường huyết. Những tác dụng này được thực hiện qua trung gian điều hòa chuyển hóa năng lượng tế bào, ức chế quá trình chết tế bào theo chương trình, giảm sự chết của tế bào thông qua việc điều hòa quá trình tự thực bào, giảm rối loạn chức năng của ty thể và giảm stress oxy hóa. Điều này gợi ý rằng metformin có thể làm giảm rối loạn chức năng thất trái do thiếu máu cục bộ cơ tim.
Các thử nghiệm tiền lâm sàng và lâm sàng đã cho thấy những kết quả đầy hứa hẹn, đặc biệt trong bối cảnh nhồi máu cơ tim cấp tính.
METFORMIN VÀ NGUY CƠ THIẾU VITAMIN B12.
Tác giả: Bác sĩ Thành Minh Khánh.
Chú ý nhầm lẫn giữa triệu chứng thần kinh do thiếu Vitamin B12 và bệnh thần kinh đái tháo đường. Tại sao định lượng Homocystein trong chẩn đoán thiếu Vitamin B12?
I. Chuyển hóa Vitamin B 12 và sinh lý bệnh thiếu Vitamin B12.
Sinh lý hấp thu và vận chuyển (đánh giá bằng định lượng Vitamin B12 toàn phần):
- Vitamin B12 (còn được gọi là cobalamin) là một vitamin tan trong nước, chủ yếu thu được từ thực phẩm có nguồn gốc động vật như thịt đỏ, thịt gia cầm, động vật có vỏ, sữa, trứng và các sản phẩm có nguồn gốc từ sữa khác hoặc thực phẩm chức năng bổ sung vitamin B12. Sau khi được ăn vào, vitamin B12 được giải phóng khỏi các protein vận chuyển thức ăn bằng cách phân giải protein trong môi trường acid của dạ dày, tại đây vitamin B12 liên kết với một glycoprotein gọi là haptocorrin (còn được gọi là R-factor hoặc R-protein). Haptocorrin được sản xuất và tiết ra bởi các tuyến nước bọt.
- Phức hợp haptocorrin-vitamin B12 sẽ bảo vệ vitamin B12 khỏi việc bị thoái hóa trong môi trường acid của dạ dày. Một khi phức hợp haptocorrin-vitamin B12 đến tá tràng, sự thay đổi về pH và sự giáng hóa của haptocorrin bởi các protease của tuyến tụy sẽ tạo điều kiện cho vitamin B12 được phân cắt khỏi haptocorrin, dẫn đến việc giải phóng vitamin B12 ở dạng tự do. Tại tá tràng, vitamin B12 tự do liên kết với yếu tố nội tại (IF), một glycoprotein do tế bào thành dạ dày tiết ra, tạo ra phức hợp IF-vitamin B12.
- Phức hợp IF-vitamin B12 mới được hình thành sau đó liên kết với thụ thể cubilin qua cơ chế phụ thuộc calcium (thụ thể cubilin là một protein được mã hóa bởi gen CUBN) ở các tế bào ruột của hồi tràng đoạn xa, dẫn đến sự hấp thụ vitamin B12 qua cơ chế nhập bào nhờ thụ thể. Sau khi được nội hóa “internalization”, phức hợp IF-vitamin B12 được giải phóng khỏi thụ thể của nó và IF bị thoái hóa trong lysosome và vitamin B12 đi vào hệ tuần hoàn thông qua protein vận chuyển kháng đa thuốc 1 (multidrug resistance protein 1, MDR1).
- Trong máu tuần hoàn, khoảng 20% -25% vitamin B12 được liên kết với protein gắn kết của nó là transcobalamin. Phức hợp transcobalamin-vitamin B12 còn được gọi là holotranscobalamin (HoloTC), đại diện cho dạng cobalamin có hoạt tính sinh học và cho phép tế bào hấp thu vitamin B12 thông qua các thụ thể transcobalamin trên bề mặt các tế bào chuyên biệt. Khoảng 75% -80% vitamin B12 còn lại gắn kết với haptocorrin và được dự trữ ở gan. Một số vitamin B12 được bài tiết qua mật và trải qua tuần hoàn gan ruột.
Chuyển hóa cấp độ tê vào với vai trò Cofactor và sinh lý bệnh (đánh giá bằng định lượng homocysteine và Methylmaloic Acid)
- Ở cấp độ tế bào, vitamin B12 đóng vai trò như một cofactor cho enzyme methionine synthase, xúc tác chuyển homocysteine thành methionine. Phản ứng này diễn ra trong bào tương và chuyển 5-metyl-tetrahydrofolate (5-metyl-THF) thành THF trong khi đó chuyển một nhóm metyl thành homocysteine để tổng hợp methionin. THF sau đó được chuyển đổi thành các chất trung gian được sử dụng trong quá trình tổng hợp các bazơ pyrimidine của DNA. Do đó, thiếu hụt vitamin B12 dẫn đến TÍCH TỤ HOMOCYSTEIN, giảm tổng hợp DNA và các bất thường về huyết học như hình thành các bạch cầu trung tính tăng phân thùy và thiếu máu nguyên bào khổng lồ, hậu quả của quá trình tạo máu không hiệu quả. Thiếu máu có thể đi kèm với các triệu chứng khác nhau, bao gồm xanh xao, đánh trống ngực, nhịp tim nhanh và mệt, thường thấy ở những bệnh nhân thiếu vitamin B12. Mặc dù thiếu máu nguyên bào khổng lồ là bất thường huyết học phổ biến nhất, nhưng thiếu hụt vitamin B12 có thể ảnh hưởng đến tất cả các dòng tế bào tủy, dẫn đến giảm 3 dòng tế bào máu.
- Vitamin B12 cũng hoạt động như một cofactor cho enzyme methylmalonyl-CoA mutase, xúc tác chuyển đổi methylmalonyl-CoA thành succinyl-CoA, một phản ứng diễn ra trong ty thể . Do đó, sự thiếu hụt vitamin B12 dẫn đến TÍCH TỤ METHYLMALONYL-CoA sau đó được chuyển đổi thành METHYLMALONIC ACID (MMA), khiến nồng độ MMA trong huyết tương thường tăng cao ở những bệnh nhân thiếu vitamin B12.
=> Ở những đối tượng bị thiếu vitamin B12, nồng độ MMA và homocysteine tăng được cho là góp phần gây ra tổn thương myelin (bệnh lý tủy) và hậu quả là gây ra bệnh thần kinh ngoại vi và tự chủ. Các biểu hiện thần kinh của sự thiếu hụt vitamin B12 bao gồm quá trình thoái hóa sợi trục tiến triển, suy giảm chức năng thần kinh ngoại vi và cảm giác, thoái hóa tủy sống kết hợp bán cấp, chứng khó vận động và mất khả năng nhận biết và cảm nhận rung động. Các triệu chứng thần kinh nói trên có thể bị hiểu nhằm là các đặc điểm của bệnh thần kinh đái tháo đường ở bệnh nhân đái tháo đường được điều trị lâu dài bằng metformin. Không xác định được nguyên nhân của bệnh thần kinh có thể dẫn đến sự tiến triển của tổn thương thần kinh trung ương và / hoặc ngoại vi. Các biểu hiện về chức năng nhận thức của thần kinh như trí nhớ kém, suy giảm nhận thức, sa sút trí tuệ, mê sảng, trầm cảm và các đợt rối loạn tâm thần cũng có thể xảy ra khi thiếu vitamin B12 nghiêm trọng và mãn tính. Các triệu chứng khác đã được báo cáo ở bệnh nhân người lớn bị thiếu vitamin B12 bao gồm viêm lưỡi, tăng sắc tố da, vô sinh, giảm/ mất thính giác, bệnh xương và thoái hóa hoàng điểm.
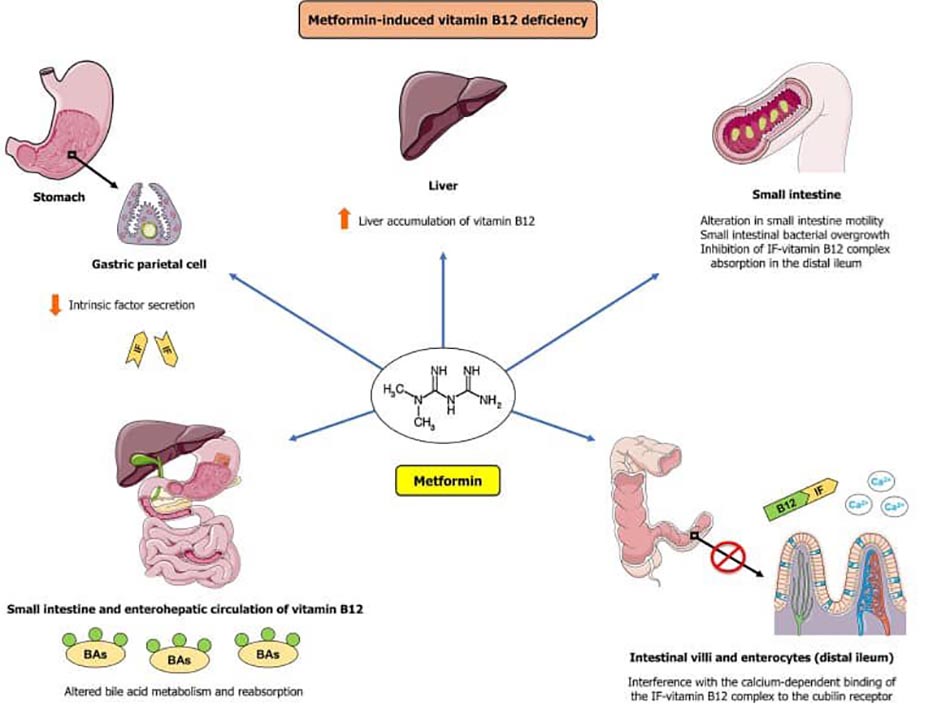
II. Các cơ chế cơ bản có thể dẫn đến sự thiếu hụt Vitamin B12 do Metformin
(1) Cản trở sự gắn kết phụ thuộc calcium của phức hợp IF (yếu tố nội tại)-vitamin B12 vào thụ thể cubilin trên tế bào ruột ở hồi tràng;
(2) Tương tác với thụ thể cubilin nhập bào;
(3) Thay đổi nhu động ruột non dẫn đến sự phát triển quá mức của vi khuẩn ruột non, dẫn đến ức chế sự hấp thu phức hợp IF-vitamin B12 ở đoạn xa hồi tràng;
(4) Thay đổi chuyển hóa và tái hấp thu acid mật;
(5) Tăng tích lũy vitamin B12 ở gan; và
(6) Giảm bài tiết IF bởi các tế bào thành dạ dày.
III. Các tiêu chế đề xuất để sàng lọc hiệu quả về chi phí và kiểm tra định kỳ về tình trạng Vitamin B12 ở bệnh nhân được điều trị bằng Metformin:
(1) Đánh giá toàn diện về tình trạng vitamin B12 nhằm phát hiện chính xác tình trạng thiếu vitamin B12 ở mô thực sự nên bao gồm:
(a) Ít nhất một dấu ấn sinh học về SỐ LƯỢNG vitamin B12 trong tuần hoàn (dạng vitamin B12 toàn phần hoặc dạng phức hợp transcobalamin-vitamin B12 hay còn gọi là holotranscobalamin).
Có thể tham khảo định nghĩa thiếu vitamin B12 “rõ ràng” khi vitamin B12 huyết thanh toàn phần <148 pmol / L và thiếu vitamin B12 “ở mức ranh giới” với ngưỡng 148 – 221 pmol / L. VÀ (b) Một dấu ấn sinh học CHỨC NĂNG (chuyển hóa) về tình trạng vitamin B12 (methylmalonic acid và / hoặc homocysteine toàn phần). Tổng phân tích tế bào máu máu gần đây cũng được khuyến nghị *Dựa vào kết quả của Diabetes Prevention Program/Diabetes Prevention Program Outcomes Study (2) Cần thực hiện tầm soát thiếu vitamin B12 khi có một hoặc nhiều yếu tố hoặc bệnh lý nguy cơ sau: (a) Nghi ngờ thiếu hụt vitamin B12 trên lâm sàng rõ rệt: bằng chứng lâm sàng về tình trạng thiếu vitamin B12, bao gồm thiếu máu hồng cầu lớn không rõ nguyên nhân, các triệu chứng thần kinh và bệnh thần kinh ngoại biên; (b) Bệnh thần kinh ngoại biên và / hoặc bệnh thần kinh tự chủ do đái tháo đường hiện đang mắc; (c) Thời gian điều trị metformin ≥ 5 năm; (d) Người lớn tuổi: ≥ 65 tuổi; (e) Tiếp xúc với metformin tích lũy cao được xác định bằng giá trị chỉ số sử dụng metformin (Metformin Usage Index, MUI) > 5 (tiêu chí này áp dụng cho bệnh nhân đái tháo đường type 2 được điều trị bằng metformin ít nhất 6 tháng);
*Chỉ số sử dụng metformin (MUI) được định nghĩa là tích số của liều metformin hàng ngày (mg) và thời gian điều trị cùng liều này (năm) chia cho 1000.
Ví dụ: Dùng metformin liều 1000 mg trong thời gian 1 năm tương đương với 1 MUI (1000 × 1/1000 = 1 MUI).
(f) Liều metformin ≥ 1500 mg / ngày trong thời gian ít nhất 6 tháng (nguy cơ thiếu vitamin B12 cao nhất đã được ghi nhận với liều metformin hàng ngày ≥ 2000 mg);
(g) Sử dụng đồng thời (≥ 12 tháng) trong thời gian dài với các loại thuốc ức chế acid như PPIs và H2RAs; và
(h) Hiện diện đồng thời các yếu tố nguy cơ hoặc bệnh đi kèm có liên quan đến tăng nguy cơ thiếu vitamin B12 cảnh báo việc tầm soát tình trạng thiếu hụt dựa trên đánh giá lâm sàng
IV. Các nguyên nhân gây thiếu Vitamin B12
– Suy dinh dưỡng, lạm dụng rượu mạn tính và chế độ ăn chay thuần chay hoặc ăn chay nghiêm ngặt.
– Lớn tuổi.
– Phẫu thuật nối tắt dạ dày, cắt một phần hoặc toàn bộ dạ dày, phẫu thuật cắt đoạn và viêm dạ dày mạn tính do nhiễm Helicobacter pylori.
– Viêm teo dạ dày.
– Sử dụng lâu dài (≥ 12 tháng) thuốc làm thay đổi bài tiết acid dạ dày hoặc pH dạ dày (ví dụ: PPIs, H2RA và antacids).
– Dùng metformin kéo dài.
– Sử dụng các loại thuốc ảnh hưởng đến sự hấp thu hoặc chuyển hóa vitamin B12 bao gồm nhựa resin gắn acid mật cholestyramine (được sử dụng để điều trị tăng cholesterol trong máu), colchicine (được sử dụng cho gout cấp) và nhiều loại kháng sinh như neomycin và thuốc chống lao para-aminosalicylic acid.
– Hội chứng phát triển quá mức vi khuẩn, cắt bỏ hồi tràng hoặc các bệnh đường tiêu hóa như viêm hồi tràng giai đoạn cuối, bệnh celiac, bệnh viêm ruột, bệnh Crohn và bệnh Sprue nhiệt đới.
– Nhiễm ký sinh trùng đường ruột (thường kèm theo tăng bạch cầu ái toan) do động vật đơn bào Giardia lamblia hoặc sán dây cá Diphyllobothrium latum.
– Rối loạn tụy ngoại tiết hoặc cắt bỏ túi mật.
– Nitrous oxide trong gây mê hoặc sử dụng nitrous oxide để giải trí.
– Các rối loạn di truyền ảnh hưởng đến các giai đoạn trong quá trình đồng hóa, vận chuyển và xử lý nội bào và chuyển hóa vitamin B12
Lược dịch từ: Infante M, Leoni M, Caprio M, Fabbri A. Long-term metformin therapy and vitamin B12 deficiency: An association to bear in mind. World J Diabetes. 2021 Jul 15;12(7):916-931. doi: 10.4239/wjd.v12.i7.916. PMID: 34326945; PMCID: PMC8311483.
Metformin không còn khuyến nghị là thuốc đầu tay mặc định cho mọi bệnh nhân đái tháo đường týp 2 – 24/09/2022
Lược dịch bởi Dược lâm sàng – Thông tin thuốc.
Ngày 24/9/2022, Đồng thuận của Hiệp hội Đái tháo đường Âu và Mỹ đã không còn khuyến nghị metformin là chỉ định đầu tay mặc định cho mọi bệnh nhân đái tháo đường týp 2. Các nguyên nhân chính bo gồm:
- . Lợi ích trên tim mạch và thận của GLP-1 RA và SGLT2i đã được chứng minh là không phụ thuộc metformin. Phối hợp điều trị từ sớm có thể giúp kéo dài thời gian trước khi thất bại với trị liệu.
- Metformin không khuyến cáo dùng trên eGFR <30 ml/phút/1,73m2 và cần giảm liều khi eGFR <45ml/phút/1,73m2.
- Dùng metformin có nguy cơ gây giảm vitamin B12, trầm trọng thêm triệu chứng bệnh thần kinh ngoại biên, cần theo dõi và kiểm soát thường xuyên nồng độ vitamin B12, đặc biệt ở BN thiếu máu hoặc mắc bệnh thần kinh ngoại biên.
Cập nhật về hiệu quả và an toàn của thuốc Metformin ở bệnh nhân đái tháo đường thai kỳ
Trong những thập kỷ qua, tỷ lệ mắc bệnh ĐTĐ TK ngày càng tăng. Cho đến nay insulin vẫn là thuốc điều trị duy nhất cho ĐTĐ TK. Tuy nhiên ngày càng có nhiều ý kiến và nghiên cứu về sử dụng metformin trong thai kỳ, dù vẫn còn gây tranh cãi. Mới đây một nhóm các thầy thuốc nội khoa, nội tiết, sản khoa ở Trường Đại học Athen, Hy Lạp đã tiến hành đánh giá toàn diện các dữ liệu hiện có về hiệu quả và độ an toàn của metformin trong thai kỳ, cho cả mẹ và con.
• Ưu điểm: Metformin đã được xác nhận về hiệu quả và độ an toàn trên mẹ, có khả năng kiểm soát đường huyết tương đương với insulin. Ngoài ra, nó làm giảm sự tăng cân của mẹ và có thể làm giảm sự xuất hiện của tăng huyết áp. Metformin không làm tăng nguy cơ dị tật bẩm sinh hoặc các tác dụng phụ nghiêm trọng khác, bao gồm điểm APGAR thấp. Một số nghiên cứu đã chứng minh giảm nguy cơ hạ đường huyết ở trẻ sơ sinh.
Tài liệu tham khảo
1. Drugbank, Metformin, truy cập ngày 18 tháng 4 năm 2022.
2. Nair, S., Diehl, A. M., Wiseman, M., Farr, G. H., Jr, & Perrillo, R. P. (2004). Metformin in the treatment of non-alcoholic steatohepatitis: a pilot open label trial. Alimentary pharmacology & therapeutics, 20(1), 23–28.
3. Pubchem, Metformin, truy cập ngày 18 tháng 4 năm 2022.
4. Bộ Y Tế (2012), Dược thư quốc gia Việt Nam, Nhà xuất bản Y học, Hà Nội.
5. Tác giả: Melanie J. Davies ORCID logo ; Vanita R. Aroda ORCID logo ; Billy S. Collins ORCID logo ; Robert A. Gabbay ORCID logo ; Jennifer Green ORCID logo ; Nisa M. Maruthur ORCID logo ; Sylvia E. Rosas ORCID logo ; Stefano Del Prato ORCID logo ; Chantal Mathieu ORCID logo ; Geltrude Mingrone ORCID logo ; Peter Rossing ORCID logo ; Tsvetalina Tankova ORCID logo ; Apostolos Tsapas ORCID logo ; John B. Buse. Ngày đăng: 23/09/2022. Management of Hyperglycemia in Type 2 Diabetes, 2022. A Consensus Report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). American Diabetes Association. Ngày truy cập: 25 tháng 09 năm 2022.
6. Hội đái tháo đường Hoa Kỳ, First-Line Therapy for Type 2 Diabetes With Sodium–Glucose Cotransporter-2 Inhibitors and Glucagon-Like Peptide-1 Receptor Agonists. Truy cập ngày 13 tháng 10 năm 2022.
Xuất xứ: Ấn Độ
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Tiêu chuẩn cơ sở
Xuất xứ: Việt Nam
Xuất xứ: Pháp
Xuất xứ: Pháp
Xuất xứ: Ấn Độ
Xuất xứ: Puerto Rico
Xuất xứ: USA
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Đức
Xuất xứ: Germany
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam