Sản xuất Dược phẩm
Hóa chất bảo vệ thực vật: khái niệm, phân loại, triệu chứng và cách xử lý khi bị ngộ độc
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
Tác giả: Giáo sư. Tiến sĩ Dược sĩ Thái Nguyễn Hùng Thu.
Bài viết Hóa chất bảo vệ thực vật trích trong chương 6 sách độc chất học – giáo trình đào tạo dược sĩ đại học bộ môn độc chất trường Đại học Dược Hà Nội.
Mục tiêu học tập
- Trình bày được khái niệm hóa chất bảo vệ thực vật, các cách phân loại và tên một số hóa chất bảo vệ thực vật thuộc các nhóm phân loại.
- Trình bày được cơ chế gây độc, triệu chứng và cách xử trí với nhiễm độc một số nhóm hóa chất bảo vệ thực vật chính.
- Trình bày được khái niệm mức tồn dư tối đa, nguyên tắc xử lý mẫu và phân tích các hóa chất bảo vệ thực vật.
Trong nông nghiệp, có rất nhiều mối nguy cơ có thể ảnh hưởng xấu đến năng suất và chất lượng của nông sản như sâu bệnh, cỏ dại, chuột, mối mọt, nấm,… Các nguồn thực vật như rau, hoa quả… và dược liệu là những sản phẩm nông nghiệp đặc biệt, do đó cũng có nguy cơ mắc phải các dịch bệnh nói trên. Hóa chất bảo vệ thực vật (HÓA CHẤT BẢO VỆ THỰC VẬT) đóng vai trò quan trọng để phòng trừ các loại dịch bệnh cho các sản phẩm nông nghiệp nói chung và dược liệu nói riêng. Hiện nay, khi trồng hầu hết các loại cây và dược liệu cần phải được sử dụng HÓA CHẤT BẢO VỆ THỰC VẬT nhằm chống lại sâu bệnh gây hại, tăng năng suất và chất lượng.
Khi được sử dụng, HÓA CHẤT BẢO VỆ THỰC VẬT có thể tồn dư lại trong sản phẩm. Nếu sử dụng đúng cách, mức tồn dư này có thể vẫn an toàn cho người sử dụng. Theo quy định, mỗi loại HÓA CHẤT BẢO VỆ THỰC VẬT đều có giá trị tồn dư tối đa (MRL: Maximum residue Tuy nhiên, việc lạm dụng hoặc sử dụng không đúng cách các loại HÓA CHẤT BẢO VỆ THỰC VẬT làm cho tồn dư HÓA CHẤT BẢO VỆ THỰC VẬT trong sản phẩm tăng lên vượt quá MRL. Khi đó, HÓA CHẤT BẢO VỆ THỰC VẬT sẽ gây ra các tác dụng không mong muốn cho người sử dụng.
1. Hóa chất bảo vệ thực vật
1.1. Định nghĩa hóa chất bảo vệ thực vật
Hóa chất bảo vệ thực vật (HCBVTV) được chuyển nghĩa từ thuật ngữ tiếng Anh “pesticide” có nghĩa là thuốc trừ côn trùng gây hại. Tuy nhiên hiện nay khái niệm này được mở rộng cho nhiều loại hóa chất được sử dụng trong trồng trọt cả với mục đích ngoài trừ sâu hại.
Tổ chức Nông nghiệp và Lương thực của Liên Hiệp Quốc (FAO) đã đưa ra định nghĩa về hóa chất bảo vệ thực vật như sau: “HÓA CHẤT BẢO VỆ THỰC VẬT là bất kỳ hợp chất hay hỗn hợp được dùng với mục đích ngăn ngừa, tiêu diệt hoặc kiểm soát các tác nhân gây hại, bao gồm vật chủ trung gian truyền bệnh của con người hoặc động vật, các bộ phận không mong muốn của thực vật hoặc động vật gây hại hoặc ảnh hưởng đến các quá trình sản xuất, chế biến, bảo quản, vận chuyển, mua bán thực phẩm, nông sản, gỗ và sản phẩm từ gỗ, thức ăn chăn nuôi hoặc hợp chất được phân tán lên động vật để kiểm soát côn trùng, nhện hay các đối tượng khác trong hoặc trên cơ thể chúng. HÓA CHẤT BẢO VỆ THỰC VẬT còn được dùng làm tác nhân điều hòa sinh trưởng thực vật, chất làm rụng lá, chất làm khô cây, tác nhân làm thưa quả hoặc ngăn chặn rụng quả sớm. Cũng có thể dùng HÓA CHẤT BẢO VỆ THỰC VẬT cho cây trong trước cũng như sau khi thu hoạch để bảo vệ sản phẩm không bị hỏng trong quá trình bảo quản và vận chuyển”.
1.2. Phân loại hóa chất bảo vệ thực vật
Có nhiều cách phân loại HÓA CHẤT BẢO VỆ THỰC VẬT khác nhau như: phân loại theo mối nguy, theo công dụng hay theo cấu tạo hóa học…
1.2.1. Phân loại theo mối nguy
Tổ chức Y tế Thế giới (WHO) phân loại HÓA CHẤT BẢO VỆ THỰC VẬT dựa vào các nghiên cứu về nguy cơ độc hại, chủ yếu là độ độc cấp tính đường uống và đường ngoài da khi thử nghiệm trên chuột.
Theo cách phân loại dựa trên LD50 , HÓA CHẤT BẢO VỆ THỰC VẬT được chia thành năm nhóm như ở bảng 1.1.
1.2.2. Phân loại theo công dụng
Dựa vào công dụng của HÓA CHẤT BẢO VỆ THỰC VẬT, người ta có thể phân loại như sau:
Hóa chất diệt trừ sinh vật gây hại: được gọi theo nhóm sinh vật gây hại như:
– Hóa chất trừ sâu (insecticides)
– Hóa chất trừ nấm (fungicides)
– Hóa chất trừ cỏ (herbicides)
– Hóa chất trừ chuột (rodenticides)
– Hóa chất trừ ốc sên (molluscicides)
– Hóa chất trừ nhện (acaricides)
– Hóa chất trừ vi khuẩn (bactericides)…
Hóa chất điều hòa sinh trưởng thực vật (PGR – plant growth regulators) là các hóa chất sử dụng để kích thích, làm chậm hoặc ức chế sự phát triển của thực vật.
Hóa chất dùng trong bảo quản, xử lý hay chế biển sau thu hái.
Trên cơ sở cách phân loại này, Alan Wood đã giới thiệu một trang điện tử trực tuyến giới thiệu bộ sưu tập đầy đủ các loại HÓA CHẤT BẢO VỆ THỰC VẬT được sử dụng.
1.2.3. Phân loại theo cấu tạo hóa học
Đây là cách phân loại được sử dụng phổ biến trong việc triển khai xây dựng các phương pháp phân tích, vì các HÓA CHẤT BẢO VỆ THỰC VẬT có cấu tạo tượng tự thường có tính chất giống nhau do đó phương pháp chiết và phân tích cũng giống nhau. Hơn nữa, từng nhóm HÓA CHẤT BẢO VỆ THỰC VẬT tác động đến vi sinh vật và cong người theo nguyên lý tương tự nhau. Theo cách phân loại này có một số nhóm HÓA CHẤT BẢO VỆ THỰC VẬT chính như sau:
– HÓA CHẤT BẢO VỆ THỰC VẬT nhóm clor hữu cơ (organochlorines)
– HÓA CHẤT BẢO VỆ THỰC VẬT nhóm phosphor hữu cơ (organophosphorus)
– HÓA CHẤT BẢO VỆ THỰC VẬT nhóm cúc tổng họp (synthetic pyrethroids)
– HÓA CHẤT BẢO VỆ THỰC VẬT nhóm carbamat
– HÓA CHẤT BẢO VỆ THỰC VẬT nhóm neonicotinoid
– HÓA CHẤT BẢO VỆ THỰC VẬT nhóm macrocyclic lacton
– HÓA CHẤT BẢO VỆ THỰC VẬT vô cơ
– HÓA CHẤT BẢO VỆ THỰC VẬT có nguồn gốc thực vật…
1.3. Một số nhóm hóa chất bảo vệ thực vật phổ biến
1.3.1. Nhóm clor hữu cơ
HÓA CHẤT BẢO VỆ THỰC VẬT nhóm clor hữu cơ (organnochlorines) là các hợp chất hữu cơ được hình thành khi thay thê các nguyên tử hydro của các hydrocarbon và dẫn xuất băng các nguyên tử clor. Trong phân tử các hợp chất này có thể tồn tại vòng benzen hoặc dị vòng (chứa dị tố O, N, hay S). Thường là các dẫn xuất clor của một số hợp chất hữu cơ như diphenylethan, cyclodien, benzen, hexan…
Về mặt cấu tạo, các HÓA CHẤT BẢO VỆ THỰC VẬT nhóm clor hữu cơ được xếp vào bốn nhóm nhỏ sau:
– Nhóm diphenyl aliphatic: DDT, dicofon, methoxyclor…
– Nhóm dẫn xuất của benzen: hexaclorocyclohexan (HCH, có nhiều đồng phân trong đó lindan là y-HCH), pentaclorophenol…
– Nhóm họp chất cyclodien: endrin, dieldrin, heptachlor, aldrin, endosulfan sulfat.
– Nhóm hợp chất polycloroterpen: toxaphen, polyclorocamphen.
Dưới đây là công thức cấu tạo của một số HÓA CHẤT BẢO VỆ THỰC VẬT nhóm clor hữu cơ:
DDT và các chất có cấu trúc tương tự:
DDT (dicloro diphenyl tricloroethan) là một nhóm các chất hữu cơ cao phân tử có chứa clor dạng bột màu trắng, mùi rất đặc trưng, không tan trong nước. DDT được sử dụng như là một loại thuốc trừ sâu có độ bền vững và độc tính cao.
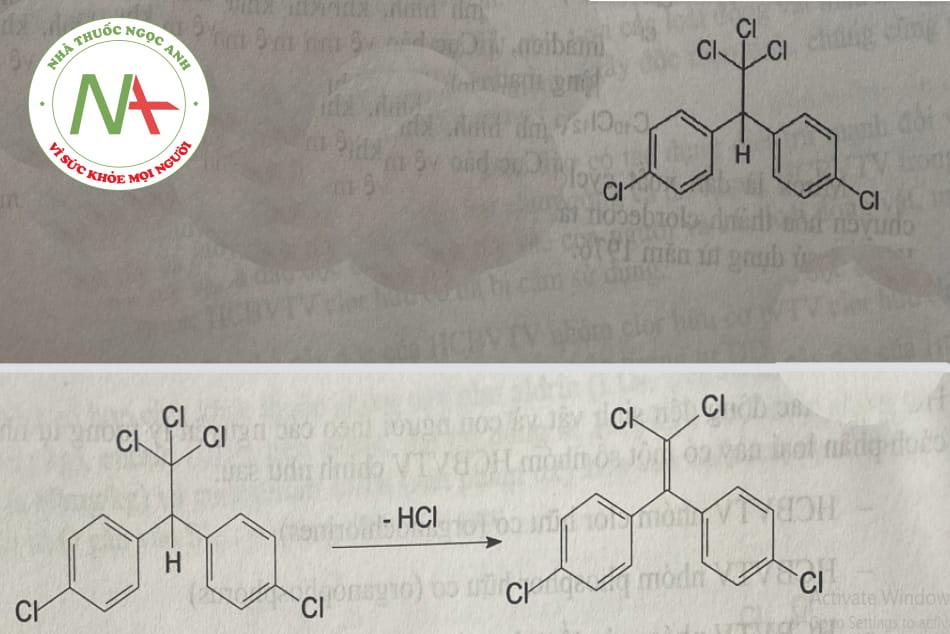
Trong cơ thể DDT dễ dàng bị phân hủy sinh học thành DDE (dicloro diphenyl tricloroethylen) là một hoạt chất có độc tính cao hơn cả DDT.
DDT có tác dụng lên hệ thần kinh của động vật: hệ thần kinh ngoại biên gây nên các sự rối loạn của hệ thống thần kinh dẫn đến tê liệt. LD50 trên chuột là 113mg/kg.
DDT bị cấm sử dụng trong nông nghiệp tại Hoa Kỳ từ năm 1973. Ở một số nước đang phát triển sau đó vẫn còn sử dụng. Tại Việt Nam, DDT vẫn được phép dùng trong phòng chống sốt rét cho đến năm 1995.
Ngoài ra còn có một số hợp chất tương tự như:
– DDD (dicloro diphenyl dicloroethan).
– Methoxychlor (Dimethoxy-DDT, C16H15Cl3O2; M= 345,7) ít đọc hơn DDT (LD50 trên chuột là 600mg/kg), không gây ung thư, không tích lũy lâu trong mô mỡ (thời gian mô mỡ của chuột là 2 tuần so với 6 tháng đối với DDT).
Một số dẫn xuất của benzen:
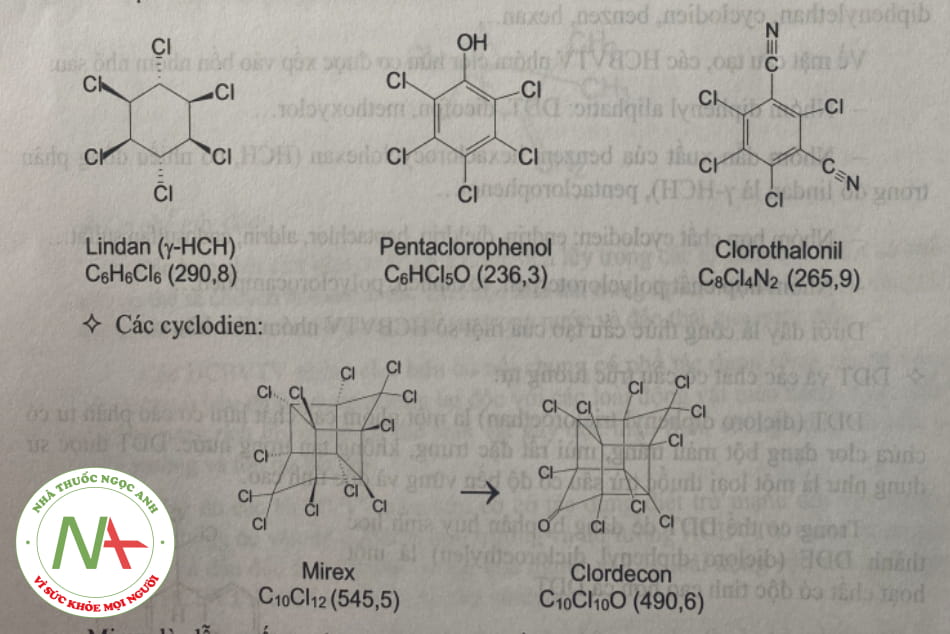
Các cyclodien:
Mirex là dẫn xuất cyclopantadien, bột trắng vô định hình, khi vào cơ thể sẽ chuyển hóa thành clordecon tác động mạnh hơn và đã bị Cục bảo vệ môi trường Hoa Kỳ cấm sử dụng từ năm 1976.
Một số hợp chất khác thuộc nhóm này như aldrin (LD50 trên chuột, đường uống là 39-60mg/kg), endrin (LD50 trên chuột, đường uống là 3mg/kg), endosulfan (LD50 trên chuột, đường uống là 80mg/kg) và endosulfan sulfat (sản phẩm oxy hóa của endosulfan có thêm một nguyên tư O gắn vào S)… có công thức như sau:
Các polycloroterpen:
Toxaphen là hỗn hợp của khoảng 200 polyclorocamphen được tạo ra qua quá trình clor hóa camphen (C10H16) với tổng khối lượng clor chiếm 67-69%. Các họp chất này có công thức phân tử từ C10H11CI5 đến C10H6CI12 (có khối lượng mol khoảng 308- 551), với công thức trung bình là C10H10Cl8 (nên còn có tên là octaclorocamphen, khối lượng mol là 414).
Các hợp chất polycloroterpen có cấu trúc tổng quát như sau:
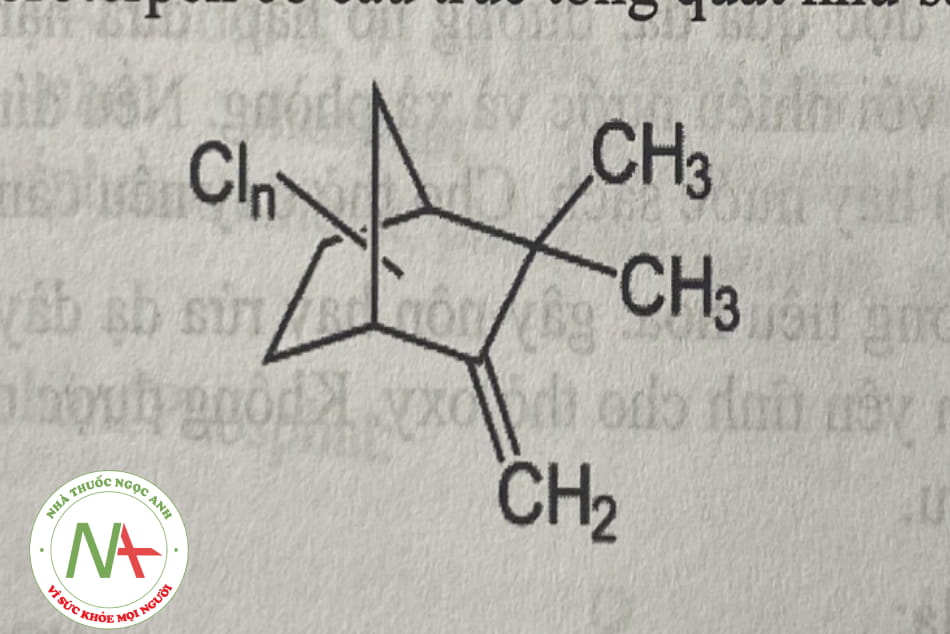
Cơ chế gây độc
Các hợp chất clor hữu cơ thường được tích lũy trong các tổ chức mỡ. Một số chất khi vào cơ thể sẽ chuyển hóa thành các chất độc hơn tan trong lipid, một số khác lại chuyển hóa thành các chất ít độc hơn ở dạng acid, tan trong nước và đào thải qua nước tiểu.
Các HÓA CHẤT BẢO VỆ THỰC VẬT nhóm clor hữu cơ nói chung có phổ tác dụng rộng, rất an toàn với cây trồng ở liều thông dụng nhưng lại độc với các loài động vật máu nóng. Các chất này
có khả năng tích lũy trong cơ thể sinh vật gây độc mạn tính, chứng cũng rất bền trong
môi trường và tồn dư lâu dài.
Mặc dù các HCBVTC clor hữu cơ có tác dụng diệt trừ mạnh đối với nhiều loại sâu hại nhưng do vấn đề ô nhiễm môi trường và dư lượng HCBVTC trong nông sản, sự tích lũy và đầu độc cao đối với cơ thể con người và các loài động vật, mà ngày nay đa số các HÓA CHẤT BẢO VỆ THỰC VẬT clor hữu cơ đã bị cấm sử dụng.
Cơ chế gây độc của HÓA CHẤT BẢO VỆ THỰC VẬT nhóm clor hữu cơ phụ thuộc vào dạng cấu tạo của chúng. DDT và các HÓA CHẤT BẢO VỆ THỰC VẬT có cấu trúc tương tự DDT là những chất rất độc trên hệ thần kinh. Chúng có tác dụng trên thần kinh ngoại biên thông qua ức chế các kênh vận chuyển Na+ qua màng tế bào thần kinh dẫn đến tê liệt và có thể dẫn đến tử vong. Còn một số loại HÓA CHẤT BẢO VỆ THỰC VẬT có cấu trúc dị vòng hoặc vòng chứa nhiều clor như aldrin, dieldrin, heptachlor, endrin… tác động thông qua việc gắn với các vùng picrotoxinin
của acid Ỵ-aminobutyric dẫn đến ức chế ion Cl– vào trong tế bào thần kinh. Hậu quả là gây nên trạng thái kích thích thần kinh. Các chất này cũng ức chế hoạt tính ATPase và một số enzym khác làm tế bào thần kinh bị nhiễm độc. Côn trùng khi bị nhiễm độc thần kinh lúc đầu có biểu hiện kích động, sau đó co giật và cuối cùng là tê liệt rồi chết.
Nguyên nhân nhiễm độc, triệu chứng và cách xử trí:
Nguyên nhân nhiễm độc:
Nguyên nhân nhiễm độc có thể do uống nhầm hay cố ý uống (tự tử) hay do tiếp xúc dài ngày với chất độc.
Triệu chứng:
– Khi bị ngộ độc cấp tính: Nôn mửa, tiêu chảy; nhức đầu, co giật, giãy dụa rồi tê liệt thần kinh trung ương; trụy tim mạch, chết sau vài giờ.
– Nhiễm độc mạn tính: mô mỡ tích lũy dần chất độc, làm tổn thương mô thần kinh gây co quắp, tê liệt, suy gan thận và rối loạn huyết học.
Xử trí:
Trường hợp nhiễm độc qua da, đường hô hấp: đưa nạn nhân ra khỏi nơi nhiễm độc, cởi bỏ quần áo, tắm với nhiều nước và xà phòng. Nếu dính vào mắt rửa bằng nước muối sinh lý (NaCl 0,9%) hay nước sạch. Cho thở oxy nếu cần.
Nhiễm độc qua đường tiêu hóa: gây nôn hay rửa dạ dày hoặc cho uống thuốc tẩy
muối, để người bệnh nằm yên tĩnh cho thở oxy. Không được dùng thuốc tẩy dầu không uống sữa, dầu ăn hay rượu.
Các xử trí chủ yếu là:
– Chống toan huyết bằng cách uống hay tiêm dung dịch kiềm.
– Hồi sức, hỗ trợ hô hấp, tuần hoàn, đặt nội khí quản (nêu cần)
– Chống co giật bằng các barbituric, diazepam, tiêm calci gluconat.
– Ăn ít chất béo, giàu protein và đường.
– Giữ ấm, tránh lạnh đột ngột, đề phòng phù phổi.
1.3.2. Nhóm phosphor hữu cơ
Các hợp chất phosphor hữu cơ (organophosphorus) được nghiên cứu sản xuất từ năm 1942, khởi đầu như các vũ khí hóa học. Một số chất được sử dụng làm vũ khí hóa học như: sarin, tabun.
Sarin ( 2-(Fluoro-methylphosphoryl) oxypropan hay isopropyl methyl fuorophosphat), còn được gọi là GB (theo NATO), là một chất độc cực mạnh. Việc sản xuất và tích trữ Sarin đã bị cấm theo Hiệp định vũ khí hóa học năm 1993.
HÓA CHẤT BẢO VỆ THỰC VẬT nhóm phosphor hữu cơ chủ yếu là các hợp chất của phosphor hóa trị 5, chúng là các ester hoặc amid của acid phosphoric (H3PO4) hoặc dân xuât. Công thức cấu tạo chung của các hợp chất phosphor hữu cơ như sau:
Trong đó R1, R2, R3 có thể là nhóm alkyl, aryl, amino hay các hợp chất thơm, dị vòng. Các nguyên tử O trong phân tử có thể được thay thế bằng S hay N để tạo ra các dẫn xuất thiophosphat, amidat và cũng được xếp vào nhóm này.
Một số HÓA CHẤT BẢO VỆ THỰC VẬT thuộc nhóm Phosphat:
Một số HÓA CHẤT BẢO VỆ THỰC VẬT thuộc nhóm Phosphorothionat:
Một số HÓA CHẤT BẢO VỆ THỰC VẬT thuộc nhóm Phosphorothiolat:
Một số HÓA CHẤT BẢO VỆ THỰC VẬT thuộc nhóm Phosphoronothiolat:
Một số HÓA CHẤT BẢO VỆ THỰC VẬT thuộc nhóm Phosphorodithiolat:
Một số HÓA CHẤT BẢO VỆ THỰC VẬT thuộc nhóm Phosphoroamidat:
Cơ chế gây độc:
Các HÓA CHẤT BẢO VỆ THỰC VẬT nhóm phosphor hữu cơ có đặc điểm chung là phổ tác dụng rộng, an toàn với cây trồng, diệt được nhiều sâu hại, tác dụng diệt côn trùng nhanh, có độc tính cao với động vật máu nóng, nhưng không tích lũy lâu dài thường được thải trừ nhanh qua nước tiểu và thời gian tồn dư trong môi trường không dài. Quá trình chuyển hóa của các HCBVTC nhóm phosphor hữu cơ rất khác nhau, sản phẩm chuyển hóa có thể là một HÓA CHẤT BẢO VỆ THỰC VẬT khác của nuoms phosphor hữu cơ:
HÓA CHẤT BẢO VỆ THỰC VẬT phosphor hữu cơ tác động vào thần kinh của côn trùng và người bằng cách ngăn cản sự tạo thành men cholinesterase (ChE) làm cho thần kinh hoạt động kém, làm yêu cơ, gây choáng váng và chết. Các chất nhóm phosphor hữu cơ gây phosphonn hóa enzym acetylcholinesterase. ChE có tác dụng phân giải acetylcholm trong cơ chế dẫn truyền xung động thần kinh qua synap. Khi ChE bị ức chế, làm ứ đọng acetylcholm, gây rối loạn dẫn truyền cholinergic, lam ức chế dẫn truyền các xung thần kinh tới các tế bào cơ, tuyến, não và hạch. Nhiễm độc xảy ra cấp tính có thể gây nôn, co thắt ruột, nhức đầu, mệt mỏi, chóng mặt, co giật, suy hô hấp, hôn mê và tử vong.
Tác dụng gây độc chủ yếu tại chỗ (tác dụng lên phổi do hít phải, tác dụng lên da, mắt do tiếp xúc…), thường hít phải tác dụng nhanh hơn uống.
Các HÓA CHẤT BẢO VỆ THỰC VẬT nhóm phosphor hữu cơ được sử dụng phổ biến từ những năm 80 của thế kỷ XX, nhưng do độc tính cao nên rất nhiều chất trong nhóm này đã bị cấm hoặc hạn chế sử dụng ở Việt Nam và nhiều quốc gia trên thế giới.
Nguyên nhân nhiễm độc, triệu chứng và cách xử trí:
Nguyên nhân nhiễm độc:
– Vô tình: có thể do hít phải (như trong các vụ cháy) hay đo tiếp xúc qua da (mang vác, đùa nghịch phim vào nhau, rửa tay không sạch sau khi phun) hoặc qua đường tiêu hóa (uống nhầm, ăn rau hoa quả xử lý bằng các HÓA CHẤT BẢO VỆ THỰC VẬT nhóm phosphor hữu cơ ngắn ngày trước khi thu hái…).
– Chủ ý: trong các vụ tự tử hay do được pha vào rượu để tăng độ rượu.
Triệu chứng:
– Mùi hơi thở, chất nôn hay chất thấm vào quần áo nạn nhân có mùi hắc như mùi tỏi.
– Mang tính phối hợp điển hình của hai hội chứng:
Cường phó giao cảm kiểu muscarin: tăng tiết dịch (nước bọt, mồ hôi…) co thắt
phế quản gây suy hô hấp cấp, nhịp tim chậm, có thể ngừng tim, đồng tử co thậm chí còn nhỏ như đầu kim.
Hội chứng thần kinh kiểu nicotin: co giật các thớ cơ (mi mắt, cơ mặt, rụt lưỡi co cơ cổ và lưng, có khi cơ toàn thân) nặng có thể dẫn đến hôn mê.
Xử trí:
– Rửa dạ dày với nhiều nước ấm.
– Tiệm atropin. Nếu nặng có thể dùng đến 20-60mg, tiêm tĩnh mạch 2,5,10mg cách 10 phút/lần cho đến khi da nóng, đồng tử giãn 5mm, sau đó tiêm dưới da và duy trì nếu cần thiết.
– Có thể dùng các oxim như PAM, obidoxim… để giải phóng cholinesterase.
– Nếu cần thiết đặt ống nội khí quản, hỗ trợ hô hấp, chú ý hút đờm dãi.
– Chăm sóc dinh dưỡng trong trường hợp hôn mê và thở máy kéo dài, dùng kháng sinh để tránh bội nhiễm.
Chú ý: Các oxim tạo phức hợp với các hợp chất hữu cơ có phosphor làm giải phóng cholinesterase khỏi liên kết với các HÓA CHẤT BẢO VỆ THỰC VẬT nhóm phosphor hữu cơ. Tuy nhiên việc sử dụng chỉ có hiệu lực khi sự phosphoryl hóa còn thuận nghịch (nên dùng trong vòng 36 giờ).
2-PAM hay Pralidoxim (2-pyridin aldoxim methyl clorid), thường dùng dưới dạng muối clorid hay methiodid.
1.3.3. Nhóm cúc tổng hợp (Pyrethroids)
HÓA CHẤT BẢO VỆ THỰC VẬT nhóm cúc tổng hợp là những chất hữu cơ có cấu trúc tương tự cá pyrethrin tự nhiên (Pyrethrum) có mặt trong một số loại hoa cúc (Chrysanthemum cinerariaefolium và Chrysanthemum coccineum):
Có hai thế hệ HÓA CHẤT BẢO VỆ THỰC VẬT nhóm cúc tổng hợp đã được sử dụng:
– Thế hệ thứ nhất được phát triển từ những năm 60 thế kỷ XX (như tetramethrin, resmethrin, bioallethrin..) với mục tiêu thay thế các hợp chất nhóm clor hữu cơ. Tuy nhiên, do đặc tính rất kém ổn định trong môi trường dưới dạng tác dụng của ánh sáng nên các HÓA CHẤT BẢO VỆ THỰC VẬT này hiện không còn được sử dụng rộng rãi.
– Thế hệ thứ hai được phát triển từ giữa những năm 70 thế kỷ XX (như permethrins gồm hai đồng phân, cypermethrins gồm bốn đồng phân, deltamethrins, cyfluthrin, λ-cyhalothrin…) có độ ổn định trong môi trường tốt hơn thế hệ thứ nhất do đó được sử dụng nhiều trong nông nghiệp. Tuy nhiên, các chất thế hệ thứ hai có độc tính cao với động vật có vú và co người. Dưới đây là công thức cấu tạo của một số HÓA CHẤT BẢO VỆ THỰC VẬT thuộc nhóm này:
Tác động của pyrethrum và các dẫn xuất tổng hợp hay bán tổng hợp nhanh và tương tự DDT.
Ngày nay, các hợp chất nhóm cúc tổng hợp thường được sử dụng phối hợp với một số HÓA CHẤT BẢO VỆ THỰC VẬT nhóm khác nhàm tăng tác dụng BVTV. Ngoài việc được sử dụng làm HÓA CHẤT BẢO VỆ THỰC VẬT trong nông nghiệp, các chất nhóm cúc tổng hợp còn được sử dụng nhiều để làm các thuốc diệt côn trùng (ruồi, muỗi, gián…) như: permethrin dùng tầm man diệt
muỗi…
Các chất nhóm cúc tổng hợp là các chất độc đối với dẫn truyền thần kinh do tác dugj luôn giữ kênh Na+ mở trong màng tế bào thần kinh gây ảnh hưởng đến sự dẫn truyền xung thần kinh làm mất cảm giác, tê liệt, ở liều cao có thể gây tử vong. Khi tiếp xúc trong thời gian dài có thể gây ngộ độc gan. Các chất này thường ít độc qua đường tiếp xúc và qua hô hấp. Liều độc của các chất nhóm cúc tổng hợp cũng thấp hơn nhiều loại HÓA CHẤT BẢO VỆ THỰC VẬT khác.
1.3.4. Nhóm carbamat
HÓA CHẤT BẢO VỆ THỰC VẬT nhóm carbamat là các ester xuất của acid carbamic (H2N-COOH) và dẫn xuất của acid carbamic. Đại diện cho nhóm fenobucarb, isoprocarb…
Một số HÓA CHẤT BẢO VỆ THỰC VẬT nhóm carbamat có công thức công tạo như sau:
Các HÓA CHẤT BẢO VỆ THỰC VẬT nhóm carbamat có đặc diêm chung là phổ tác dụng hẹp, hiệu lực thuốc ngăn, ít tan trong nước, tan nhiêu dung môi hữu cơ, bị kiềm phân hủy. Không tồn lưu lâu dài trong môi trường.
Các hợp chất carbamat cũng có khả năng tích lũy và đầu độc hệ thần kinh của vật nhưng độc tính kém các hợp chất phosphor hữu cơ. Khi sử dụng chúng tác động trực tiếp vào men cholinesterase của hệ thần kinh và có cơ chế gây độc giống như nhóm phosphor hữu cơ, tuy nhiên mức độ độc hại không bằng các hợp chất nhóm phosphor hữu cơ.
Nhiễm độc cấp các carbamat có triệu chứng lâm sàng như nhiễm độc cấp các HÓA CHẤT BẢO VỆ THỰC VẬT nhom phosphor hữu cơ vì đều ức chế cholinesterase nên cách xử trí cũng tương tự như với ngộ độc cấp các HÓA CHẤT BẢO VỆ THỰC VẬT nhóm phosphor hữu cơ.
1.3.5. Nhóm neonicotinoid
Nicotin là alcaloid có trong các cây họ Cà (Solanaceae), đặc biệt có hàm lượng khá cao trong cây thuốc lá. Các tính chất và độc tính của nicotin đã được nêu chi tiết trong Chương 4. Nicotin là một chất độc thần kinh rất mạnh với ảnh hưởng rõ rệt đến các loài côn trùng do vậy trước đây nicotin được sử dụng rộng rãi như là một loại thuốc trừ sâu. Hiện nay các dẫn xuất của nicotin như imidacloprid được sử dụng thay thế.
Neonicotinoid là nhóm HÓA CHẤT BẢO VỆ THỰC VẬT gây kích thích thần kinh có cấu trúc tương tự nicotin được sử dụng từ những năm 80 thế kỷ XX. Đại diện cho nhóm này gồm các chất như imidacloprid, acetamiprid, thiamethoxam, dinotefuran…
Gần đây, một số nước hạn chế sử dụng những chất của nhóm này vì có nhiều bằng chứng cho thấy nguy cơ gây rối loạn CDD (rối loạn sụt giảm bầy đàn) đối với ong mật. Nguyên nhân là do các chất này phá hủy hệ thống miễn dịch tự nhiên của ong mật nhạy cảm với nhiều trường hợp nhiễm trùng gây chết. Hiện nay, ở Việt Namcacs chất này vẫn được phép sử dụng làm HÓA CHẤT BẢO VỆ THỰC VẬT trong nông nghiệp.
Một số HÓA CHẤT BẢO VỆ THỰC VẬT neonicotinoid có công thức cấu tạo như sau:
Nhóm HÓA CHẤT BẢO VỆ THỰC VẬT này có độc tính thấp hơn các nhóm clor hữu cơ, phosphor hữu cơ và carbamat. Tuy nhiên, một số sản phẩm chuyển hóa của nhóm này lại cho thấy có độc tính cao đối với chim và cá. Cơ chế gây độc là do các sản phẩm này gắn với các receptor của acetylcholin, gây độc thần kinh trung ương. Đường tiếp xúc qua da có độc tính thấp, có thể gây đỏ và ngứa mắt nhẹ. Các nghiên cứu cũng cho thấy các chất này phân hủy nhanh trong đường tiêu hóa và loại trừ qua phân, nước tiểu trong vòng 48 giờ. Chưa thấy trường hợp bị ngộ độc cấp tính trên người.
1.3.6. Nhóm macrocyclic lacton
Các hợp chất nhóm macrocyclic lacton là các sản phẩm được lên men tự nhiên từ các loài Streptomyces. Một số họp chất đại diện của nhóm này gồm abamectin, ivermectin, emamectin, spinosad… có thành phần và công thức cấu tạo như sau:
Abamectin là hỗn hợp chứa trên 80% avermectin B1a (C48H72O14) và dưới 20% avermecti B1b (C48H72O14).
Ivermectin là hỗn hợp của 22,23 -dihydro avermectin B1a và 22,23-dihydro avermecitn B1b
Emamectin là dẫn xuất abamectin bằng cách thay thế một nhóm hydorxyl (-OH) ở vị trí 4″ bởi nhóm epi-amino-methyl (NHCH3). Emectin là hỗn hợp của 10% B1b và 90% B1a .
Spinosad gồm hai spinosad là spinosad A và spinosad D với tỷ lệ 17:3.
Trước đây, tác dụng chính của các chất thuộc nhóm này là diệt giun sán đối với gia súc. Hiện nay, các chất thuộc nhóm này được sử dụng để làm HÓA CHẤT BẢO VỆ THỰC VẬT trong nông nghiệp. Các HÓA CHẤT BẢO VỆ THỰC VẬT nhóm macrocyclic lacton thường được phối hợp với các HÓA CHẤT BẢO VỆ THỰC VẬT nhóm khác để tăng khả năng diệt trừ sâu hại.
Các chất này ngăn cản sự dẫn truyền tín hiệu của tế bào thân kinh và tế bào cơ
bằng cách tăng cường sự giải phóng và gắn acid Ỵ-aminobutỵnc vào đâu tê bào thần kinh dẫn đến làm tăng ion clor vào trong tế bào làm tê liệt hệ thần kinh. Các triệu chứng ngộ độc cấp có thể gặp phải bao gồm hôn mê, giảm huyết áp, suy hô hấp và tử vong.
1.4. Một số hóa chất bảo vệ thực vật khác
Ngoài các nhóm chính trên trong thực tế còn có nhiều HÓA CHẤT BẢO VỆ THỰC VẬT khác được sử dụng với các mục đích hay có nguồn gốc khác nhau như: thuốc diệt chuột, thuốc trừ cỏ… hay có nguồn gốc thực vật, có nguồn gốc vi sinh… Một số HÓA CHẤT BẢO VỆ THỰC VẬT có cấu tạo khác biệt do đó không được xếp vào các nhóm HÓA CHẤT BẢO VỆ THỰC VẬT chính nêu trên.
1.4.1. Một số HÓA CHẤT BẢO VỆ THỰC VẬT thuộc các nhóm khác
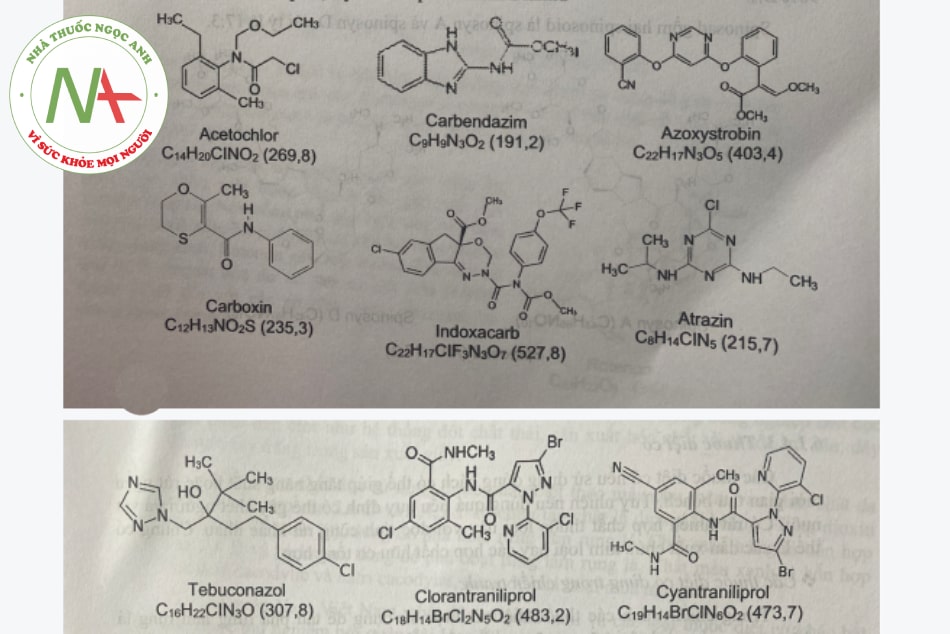
Một số HÓA CHẤT BẢO VỆ THỰC VẬT thuộc các nhóm khác nhưng cũng đang được sử dụng phổ biến có công thức cấu tạo như sau:
- Acetochlor: nhóm Cloroacetanilid
- Carbendazim: nhóm Benzimidazol
- Azoxystrobin: nhóm Strobin
- Carboxin: nhóm Carboxamid
- Indoxacarb: nhóm Oxadiazin
- Atrazin: nhóm Triazin
- Tebuconazol: nhóm Triazol
- Clorantraniliprol, Cyantraniliprol: nhóm Diamid
1.4.2. Một số HÓA CHẤT BẢO VỆ THỰC VẬT có nguồn gốc thực vật và vi sinh
Ngoài các HÓA CHẤT BẢO VỆ THỰC VẬT thuộc nhóm cúc tổng hợp (các pyrethrin) và nhóm neonicotinoid thì nhiều HCBỴTV có nguồn gốc từ thực vật hay vi sinh cũng được sử dụng để diệt côn trùng. Một số HÓA CHẤT BẢO VỆ THỰC VẬT có nguồn gốc từ thực vật như: Pyrethrum (lây từ hoa cây Chrysanthemum cinerariaefolium), nicotin từ cây thuốc lá… HÓA CHẤT BẢO VỆ THỰC VẬT nguồn gốc vi sinh như: bào tử Bacillus thurỉngỉens. Dưới đây là một số thuốc diệt côn trùng khác có nguồn gốc thực vật:
Allicin:
Allicin và tỏi có nhiều công dụng nên được sử dụng với nhiều mục đích khác nhau. Về góc độ HÓA CHẤT BẢO VỆ THỰC VẬT, tỏi có tác dụng:
Diệt giun sán như giun đũa, giun kim, giun móc và trứng của chúng.
Xua đuổi và diệt côn trùng: Nhiều loại côn trùng như gián, muỗi rất sợ mùi tỏi. Tỏi còn giết chết được các ấu trùng muỗi (loăng quăng) với liều lượng rất thấp 25ppm cho cá chất chiết hoặc 2ppm cho dầu tỏi. Vì vậy nếu để củ tỏi tươi trong tủ đựng thức ăn thì có thể sẽ không có gián chui vào.
Rotenon (C23H22O6-394,4) là một hợp chất không mùi được sử dụng để giết cá trước khi dùng nhiều làm thuốc trừ sâu. Rotenon có trong rễ và hạt của một số loài thực vật như derris, lonchocarpus, jicama… còn được gọi là nicoulin (phân lập từ Lonchocarpus cicou).
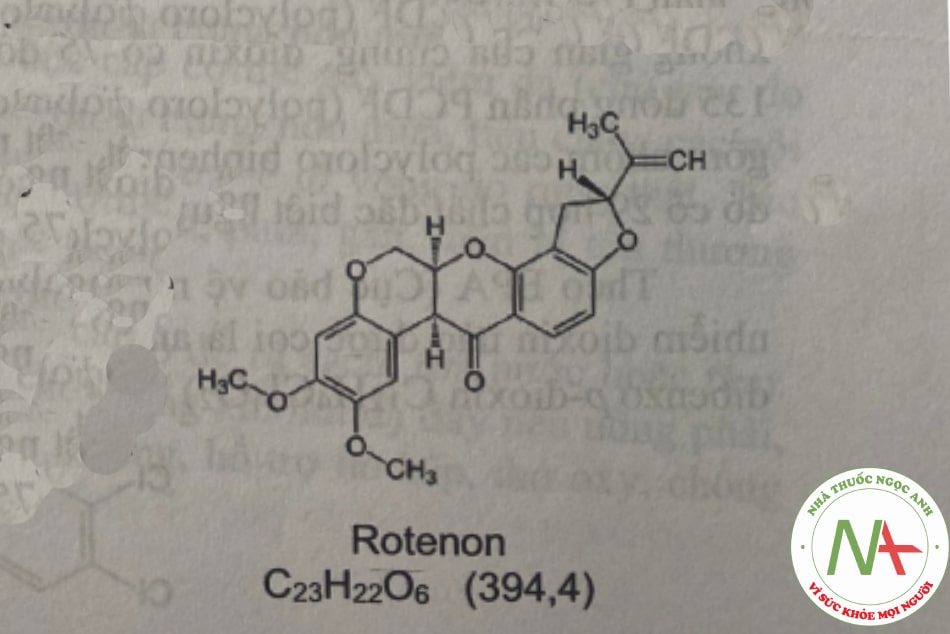
Rotenon chủ yếu tác dụng tại chỗ gây viêm da, giác mạc, viêm mũi họng. Rất ít khi gặp ngộ độc rotenon ở người. Nên uống phải gây kích ứng tiêu hóa, nôn hay buồn nôn, hít phải gây ức chế hô hấp, làm co quắp, động kinh. Rotenon gây ảnh hưởng đến một số quá trình chuyển do ức chế sự oxy hóa NADH thành NAD đối với các cơ chất như glutamat, α-cetoglutarat, pyruvat…
1.4.3. Thuốc diệt cỏ
Các thuốc diệt cỏ nếu sử dụng đúng cách có thể giúp tăng năng suất hoặc rút ngắn thời gian thu hoạch. Tuy nhiên nếu dùng quá liều quy định có thể gây chết người và vật nuôi. Có rất nhiều hợp chất thuộc loại này với độc tính cũng rất khác nhau. ung co
thể là các dẫn xuất chứa kim loại hay các hợp chất hữu cơ tổng hợp.
Các thuốc diệt cỏ dùng trong chiến tranh:
Trong chiến tranh các thuốc diệt cỏ được sử dụng để tàn phá rừng làm rụng lá nhằm tạo ra các vành đai trắng ngăn sự tân công của đối phương. Các chất thương được
sử dụng là:
2,4-D (acid 2,4-dicloro phenoxy acetic)
2,4,5-T (acid 2,4,5-triclorophenoxy acetic)
Picloram (acid 4-amino-3,5,6-tricloro-2-pyridin carboxylic)
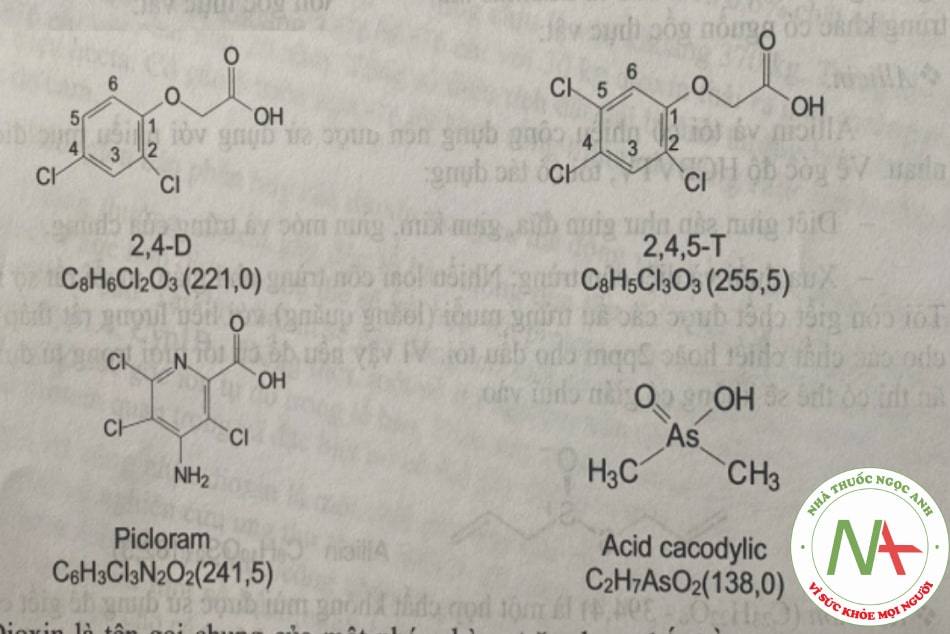
Dioxin là tên gọi chung của một nhóm hàng trăm hợp chất bền vững trong môi trường cũng như trong cơ thể người và các sinh vật. Tùy theo số nguyên tử clor và vị trí không gian của chúng, dioxin có 75 đồng phân PCDD (polycloro dibenzo dioxin) và 135 đồng phân PCDF (polycloro dibenzo furan) với độc tính khác nhau. Dioxin còn bao gồm nhóm các polucloro biphenyl (là các chất tương tự dioxin) gồm 429 hợp chất trong đó có 29 hợp chất đặc biệt nguy hiểm.
Theo EPA (Cục bảo vệ môi trường Hoa Kỳ) dường như không có mức độ phơi nhiễm dioxin nào được coi là an toàn. Trong số các hợp chất dioxin, TCĐ (tetracloro dibenzo p-dioxin C12H4Cl4O2) là nhóm độc chất.
Dioxin là sản phẩm phụ của nhiều quá trình sản xuất công nghiệp hóa học liên qua đến clor như hệ thống đốt chất thải, sản xuất hóa chất và thuốc trừ sâu, dây chuyền tẩy trắng trong sản xuất giấy.
Các dạng chất độc sử dụng được phân biệt theo màu cho thêm vào như: chất da cam là hỗn hợp của 2,4 D và 2,4,5 T có chứa tạp chất là dioxin (khoảng 370kg dioxin trong gần 77 triệu lít), dùng để phá hoại rừng làm rụng lá. Chất màu trắng là hỗn hợp của 2,4D và picloram, dùng để phá hoại rừng làm rụng lá: Chất màu xanh là hỗn hợp của các acid calodylic và natri cacodylat, dùng để phá hoại mùa màng….
Ở miền Nam Việt Nam, chất độc màu da cam và các loại thuốc diệt cỏ khác bắt đầu được thử nghiệm bởi quân đội Hoa Kỳ vào năm 1961 và được sử dụng rộng rãi với hàm lượng cao trong chiến tranh vào các năm 1967-2968, rồi giảm xuống và ngừng sử dụng năm 1971. Các loại hợp chất này được trộn vào dầu hỏa hoặc nhiên liệu diễn rồi rải bằng máy bay hoặc các phương tiện khác. Trong thời gian 10 năm đó, 76,9 triệu lít hóa chất đã được rải xuống rừng núi và đồng ruộng Việt Nam. Trong số này có 64% là chất độc màu da cam, 27% là chất màu trắng, 8,77% là chất màu xanh và 0,6% chất màu tím.
Tổng số lượng dioxin Việt Nam hứng chịu là vào khoảng 370kg. Trong khi đó vụ nhiễm dioxin ở Seveso (Italia) năm 1976 chỉ với 30kg dioxin thải ra môi trường mà tác hại của nó kéo dài hơn 20 năm. Tổng số diện tích đất đai bị ảnh hưởng chất độc da cam.
Thời gian bán phân hủy của dioxin trong cơ thể động vật là bảy năm hoặc lâu hơn.
Thông thường, dioxin gây độc tế bào thông qua thụ thể AhR (Aryl hydrocarbon receptor). Phức hợp dioxin- thụ thể sẽ kết hợp với protein vận chuyển để xâm nhập vào trong nhân tế bào. Tại đây dioxin sẽ gây đóng mở một số gen giải độc quan trọng của tế bào như Cyp1A, Cyp1B,.. Đồng thời, một số thí nghiệm trên chuột cho thấy dioxin làm tăng nồng độ các gốc ion tự do trong tế bào. Điều này có thể làm phá hủy các cấu trúc tế bào, các protein quan trọng và đặc biệt óc có thể gây đột biến trên phân tử ADN.
EPA đã công nhận dioxin là một chất gây ung thư cho con người. Năm 1977, Tổ chức quốc tế về nghiên cứu ung thư thuộc WHO đã công bố 2,3,7,8-TCDD là chất gây ung thư nhóm 1 (nhóm đã công nhận là gây ung thư). Ngoài ung thư, dioxin còn có thể liên quan đến một số bệnh gây nguy hiểm khác như bệnh rám da, đái tháo đường, thiểu năng sinh dục cho cả nam và nữ, gây quái thai, thiểu năng trí tuệ…
Các hợp chất 2,4D và 2,4,5T khi ngộ độc cấp có thể gây viêm da (chủ yếu do dioxin), uống phải có thể gây mệt mỏi, buồn ngủ, đau bụng, nôn mửa, tiêu chảy, các nội tạng có thể bị sung huyết, trương lực cơ bị co cứng có thể tử vong do rung thất. Tác dụng chậm có thể gây sút cân, chán ăn, viêm phế quản, phổi, gan, thận bị tổn thương (gan to, tăng protein niệu…)
Xử trí: Nếu bị tiếp xúc ngoài da: cởi bỏ quần áo để rũ sạch, rửa nước hoặc tắm. Rửa mắt, họng bằng dung dịch NaHCO3 2%. Thận trọng khi hút dạ dày nếu uống phải, dùng than hoạt, tẩy bằng MgSO4. Cho nằm chỗ thoáng, hỗ trợ hô hấp, thở oxy, chống co cứng trương lực cơ và loạn nhịp.
Một số thuốc diệt cỏ khác:
– Calci cyanamid (CaCN2) được sử dụng trong nông nghiệp làm thuốc rụng lá, phân bón. Có thể bị nhiễm độc qua đường hô hấp, da hay tiêu hóa. Cơ chế gây độc do hô hấp tế bào bị ngăn cản bởi ion CN– ức chế enzym cytochrom oxydase, oxy máu không được sử dụng nên da người nhiễm độc có màu hồng. Triệu chứng và cách xử trí tương tự như nhiễm độc cyanid.
– Dinitro orthocresol (DNOC, DOC) là hợp chất màu vàng, có mùi thuốc súng, không tan trong nước, dễ nổ, thường trộn với dầu hay than.
DOC được dùng để trừ sâu diệt cỏ trong nồng nghiệp dưới dạng bột hay dung dịch với liều lượng 10kg/ha. Nó có thể xâm nhập vào cơ thể thông qua đường hô hấp, tiêu hóa và qua da.
Nồng độ cho phép trong không khí là 0,001mg/l, với nồng độ 0,2mg/m3 có thể gây chết, liều gây tử vong khoảng 0,5g với người 50kg.
Triệu chứng nhiễm độc cấp tính: Trường hợp nhẹ: toát mồ hôi, mệt mỏi, khát nước, tim đập yếu, huyết áp giảm, nước tiểu vàng, nếu ngấm qua da thì da và tóc vàng. Trường hợp nặng: khó thở, mệt mỏi, vã mồ hôi, nôn mửa; chỗ da tiếp xúc bị phồng rộp, ngứa; sốt cao trên 40°c, rối loạn nhịp tim, ngất.
Xử trí: tránh xa nơi bị nhiễm độc, rửa dạ dày bằng NaHCO3 (nếu uống phải), hỗ trợ hô hấp nếu cần, hạ thân nhiệt bằng chườm đá, ủ lạnh, tránh dùng thuốc hạ nhiệt; giữ người bệnh yên tĩnh và điều trị triệu chứng.
2. Tình hình sử dụng hóa chất bảo vệ thực vật
2.1. Tình hình sử dụng hóa chất bảo vệ thực vật ở Việt Nam
Việc sử dụng HÓA CHẤT BẢO VỆ THỰC VẬT trong lịch sử có thể được chia làm bốn giai đoạn:
Giai đoạn 1 (trước năm 1940): Chủ yếu sử dụng các hợp chất vô cơ như đồng, lưu huỳnh, arsen, thủy ngân… Phần lớn các chất này đều rất độc và tồn tại lâu trong môi trường.
Giai đoạn 2 (từ 1940 đến 1960): Giai đoạn này bắt nguồn từ việc phát minh ra thuốc trừ sâu DDT (Paul Muller, giải Nobel háo học 1939) và sau đó là HÓA CHẤT BẢO VỆ THỰC VẬT nhóm clor hữu cơ. DDT từng được xem như là một loại thần dược cho nông nghiệp. Nhiều hóa chất được sử dụng trong giai đoạn này có chứa gốc clor đã để lại những hậu quả nghiêm trọng cho nhân loại trong đó đỉnh điểm là việc sử dụng các hợp chất clor hữu cơ (DDT; 2,4,5-T;2,3,7,8-TCDD) làm chất độc hóa học trong chiến tranh. Mặc dù ở giai đoạn này, một số HÓA CHẤT BẢO VỆ THỰC VẬT nhóm phosphor hữu cơ và carbamat đã ra đời nhưng vị trí của chúng còn kém xa các hợp chất nhóm clor hữu cơ.
Giai đoạn 3 (từ 1960 đến 1980): Năm 1962 Carson được xuất bản đã phát đi những cảnh báo về ảnh hưởng nghiêm trọng của các hợp chất clor hữu cơ đối với sức khỏe con người và môi trường. Từ 1973, cơ quan FDA Hoa Kỳ đã cấm sử dụng các hợp chất clor hữu cơ làm HÓA CHẤT BẢO VỆ THỰC VẬT. Thế giới đã phát minh ra các hợp chất thay thế như các chất nhóm phosphor hữu cơ, nhóm cúc tổng hợp là các hợp chất ít bền trong môi trường hơn. Các pyrethroid thế hệ II ra đời vào đâu những năm 70 thế kỷ XX mở ra khả năng áp dụng các loại HÓA CHẤT BẢO VỆ THỰC VẬT có độ chọn lọc cao và thân thiện với môi trường.
Giai đoạn 4 (từ 1980 đến nay): Đã phát minh ra nhiều loại HÓA CHẤT BẢO VỆ THỰC VẬT mới và nguồn gốc sinh học. Ngoài hiệu quả phòng trừ dịch bệnh cho nông nghiệp, tính an toàn của HÓA CHẤT BẢO VỆ THỰC VẬT ngày càng được chú ý nhiều hơn. Hầu như toàn bộ các HÓA CHẤT BẢO VỆ THỰC VẬT nhóm clor hữu cơ đã bị cấm sử dụng trên thế giới, các chất nhóm phosphor hữu cơ độc hại cũng đã bị cấm hoặc hạn chế sử dụng. Để đảm bảo hiệu quả trên mùa màng, người ta thường phối họp hai hoặc nhiều HÓA CHẤT BẢO VỆ THỰC VẬT có độc tính thấp hơn.
Ngày nay nhiều HÓA CHẤT BẢO VỆ THỰC VẬT mới đã được phát triển với ưu điểm là có tính chọn lọc hơn và ít độc hại hơn. Đặc biệt, các nhóm thuốc bảo vệ thực vật sinh học ngày càng được nghiên cứu phát triển vì ít độc hại. Tuy nhiên vai trò của những thuốc bảo vệ thực vật có bản chất hóa học vẫn chưa thể được thay thế. Theo thống kê của Cụ bảo vệ môi trường Hoa Kỳ (EPA), mỗi năm ở Mỹ sử dụng khoảng 1 tỷ tấn HÓA CHẤT BẢO VỆ THỰC VẬT, chiếm khoảng 22% lượng HÓA CHẤT BẢO VỆ THỰC VẬT được sử dụng trên toàn thế giời.
2.2. Tình hình sử dụng hóa chất bảo vệ thực vật tại Việt Nam
Hàng năm, Bộ NN&PTNT ban hành Thông tư về Danh mục thuốc BVTV. Thông tư 21/2013/TT-BNNPTNT ngày 17 tháng 4 năm 2013 ban hành các danh mục thuốc
BVTV được phép sử dụng, hạn chế sử dụng, cấm sử dụng ở Việt Nam. Bảng 6.2 tổng hợp số lượng các hoạt chất theo ba danh mục được phân loại dựa vào công dụng. Theo đó, có đến trên 1500 hoạt chất HÓA CHẤT BẢO VỆ THỰC VẬT được phép sử dụng ở Việt Nam trong đo nhiều nhất dùng để diệt trừ sâu hại và trừ nấm bệnh. Một số hoạt chất trừ sâu hạn chế sử dụng bao gồm carbofuran và methomyl (nhóm carbamat). Có 21 hoạt chất trừ sâu bị cấm sử dụng, bao gồm 14 chất nhóm clor hữu cơ (aldrin, BHC, lindan, chlordan, DDT dieldrin endosulfan, endrin, heptachlor, isodrin, natri pentachlorophenat, pentachlorophenol, polychlorocamphen, chlordimeform), năm chất nhóm phosphor hữu cơ (phosphamidon methamidophos, methyl parathion, monocrotophos, ethyl parathion) và hai chat VO cơ (Cd, Pb).
Hầu hết các thuốc BVTV sử dụng ở Việt Nam đều phải nhập khẩu từ nước ngoài. Hàng năm, Việt Nam nhập khẩu trên 70.000 tấn thành phẩm với trị giá 210 – 500 triệu USD. Trên 90% thuốc BVTV được nhập khâu từ Trung Quốc. Tuy nhiên, ngoài những thuốc BVTV nằm trong danh mục của Bộ Nông nghiệp và phát triển nông thôn còn có nhiêu loại thuốc BVTV được sử dụng trái phép trong nông nghiệp thông qua việc mua bán trao tay. Các sản phẩm này chủ yếu có nguồn gốc từ Trung Quốc và được nhập vào Việt Nam thông qua các con đường tiểu ngạch.
Bảng 6.1. số lượng hoạt chất HÓA CHẤT BẢO VỆ THỰC VẬT được phép sử dụng, hạn chế sử dụng và cấm sử dụng ở Việt Nam
| Danh mục | HÓA CHẤT BẢO VỆ THỰC VẬT được pháp sử dụng | HÓA CHẤT BẢO VỆ THỰC VẬT hạn chế sử dụng | HÓA CHẤT BẢO VỆ THỰC VẬT cấm sử dụng |
| Hóa chất diệt trừ sinh vật gây hại | |||
| Trừ sâu | 745 hoạt chất | 2 hoạt chất | 21 hoạt chất |
| Trừ nấm | 552 hoạt chất | – | 6 hoạt chất |
| Trừ cỏ | 217 hoạt chất | – | 1 hoạt chất |
| Trừ chuột | 10 hoạt chất | 1 hoạt chất | 1 hoạt chất |
| Trừ ốc sên | 25 hoạt chất | – | – |
| Trừ mối | 13 hoạt chất | 2 hoạt chất | – |
| Hóa chất điều hòa sinh trưởng thực vật | 52 hoạt chất | – | – |
| Hóa chất dùng trong bảo quản, xử lý hay chế biến sau thu hái | 10 hoạt chất | 8 hoạt chất | – |
Theo số liệu của Cục Bảo vệ thực vật, đến năm 2011, cả nước có 93 nhà máy, cơ sở sản xuất, gia công, sang chai, đóng gói thuốc BVTV và 28750 đại lý, cửa hàng kinh doanh buôn bán thuốc BVTV.
2.3. Sử dụng hóa chất bảo vệ thực vật an toàn và hiệu quả
Để đảm bảo an toàn và hiệu quả trong việc sử dụng HÓA CHẤT BẢO VỆ THỰC VẬT cho cây trồng nói chung và dược liệu nói riêng, cần phải thực hiện các biện pháp sau:
(1) Thực hiện biện pháp phòng trừ tổng hợp đối với mọi loại dịch hại và cây trồng, chỉ dùng biện pháp hóa học khi những biện pháp khác không hiệu quả.
(2) Đảm bảo sử dụng HÓA CHẤT BẢO VỆ THỰC VẬT theo nguyên tắc bốn đúng:
– Đúng thuốc: Mỗi loại HÓA CHẤT BẢO VỆ THỰC VẬT được sử dụng để diệt trừ một tác nhân gây hại cụ thể và không nên sử dụng cùng một loại thuốc trong nhiều vụ liên tiếp.
– Đúng liều lượng: Cần sử dụng theo đúng hướng dẫn của nhà sản xuất.
– Đúng lúc: Cần phun thuốc vào thời điểm mà dịch hại trên đồng ruộng dễ bị tiêu diệt nhất, đó là giai đoạn khi sâu còn non hay khi không có mưa lớn. Ngoài ra, cần ngưng sử dụng trước khi thu hoạch một thời gian nhất định tùy theo từng loại thuốc.
– Đúng cách: Cần pha thuốc đúng cách và phun thuốc làm sao cho HÓA CHẤT BẢO VỆ THỰC VẬT tiếp xúc được với dịch hại nhiều nhất. Không tự ý hỗn hợp nhiều loại HÓA CHẤT BẢO VỆ THỰC VẬT với nhau để phun trên đồng ruộng.
(3) Đảm bảo thời gian cách ly (PHI-Pre Harvesr Interval) của từng loại thuốc trên mỗi loại cây trồng.
(4) Đảm bảo an toàn cất giữ những HÓA CHẤT BẢO VỆ THỰC VẬT chưa sử dụng hết.
– Những HÓA CHẤT BẢO VỆ THỰC VẬT chưa sử dụng hoặc dùng chưa hết phải được cất giữ trong phòng riêng biệt, không dột, có khóa cửa chắc chắn, xa ơi ở và chuồng trại gia súc.
-Những dụng cụ đong thuốc, bình bơm thuốc, quần áo bảo hộ lao động phải được giặt giũ, rửa sạch sẽ sau mỗi đợt phun thuốc và phải cất giữa trong kho riêng.
-Không đổ thuốc dưa thừa, chưa dùng hết sang bất kỳ đồ đựng khác (vỏ chai bia, chai nước mắm …). Sau khi đã dùng hết thuốc không được dùng bao bì HÓA CHẤT BẢO VỆ THỰC VẬT (chai, túi) vào bất kỳ mục đích nào khác, phải huỷ và chôn.
(5) Đảm bảo an toàn trong lưu thông HÓA CHẤT BẢO VỆ THỰC VẬT.
3. Dư lượng hóa chất bảo vệ thực vật
3.1. Khái niệm về dư lượng và mức dư lượng tối đa
Dư lượng là phần còn lại của hoạt chất, các sản phẩm chuyển hóa và các thành phần khác có trong thuốc, tồn tại trên cây trồng, nông sản, đất, nước sau một thời gian dưới tác động của hệ sống và điều kiện ngoại cảnh.
Mức tồn dư tối đa (MRL) hay giới hạn tối đa dư lượng HÓA CHẤT BẢO VỆ THỰC VẬT (biểu thị bằng mg/kg), là nồng độ cao nhất của dư lượng thuốc có trong một đơn vị sản phẩm nông sản hay thực phẩm mà ở đó có thể được chấp nhận mà không gây hại cho người sử dụng. Dư lượng HÓA CHẤT BẢO VỆ THỰC VẬT được tính bằng miligam thuốc có trong 1 kilogam nông sản. Uy ban Codex (tổ chức tiêu chuẩn thuộc FAO và WHO) đã lập ra danh mục giới hạn tối đa của HÓA CHẤT BẢO VỆ THỰC VẬT trong thức ăn cho người và gia súc. Mỗi nước đều có các quy định mức tồn dư tối đa thường có trong thực phẩm.
Việc xác định MRL dựa trên các nghiên cứu về độc tính của HÓA CHẤT BẢO VỆ THỰC VẬT, các dữ liệu về tồn dư trong sản phẩm được sản xuất theo quy trình Thực hành nông nghiệp tốt (GAP) và lượng sản phẩm mà con người sử dụng.
3.2. Quy định về mức dư lượng tối đa
Mỗi loại HÓA CHẤT BẢO VỆ THỰC VẬT có một giá trị MRL khác nhau trên từng nền mẫu. Hơn nữa, MRL của mỗi nước lại khác nhau do sự khác nhau về số lượng sản phẩm và cách sử dụng của từng nước. WHO và FAO quy định MRL theo tiêu chuẩn Codex, trong đó quy định cụ thể cho mỗi HÓA CHẤT BẢO VỆ THỰC VẬT trong từng nền mẫu. Các giá trị này được xem là MRL quốc tế. Tại Việt Nam, theo Quyết định số 46-2007/QĐ-BYT ngày 19 tháng 12 năm 2007 của Bộ Y Tế đã quy định MRL của HÓA CHẤT BẢO VỆ THỰC VẬT trong các sản phẩm nông sản gồm hoa quả, rau củ, thịt cá… Các tiêu chuẩn này dựa trên tiêu chuẩn Codex do chưa có các nghiên cứu ở Việt Nam về đánh giá nguy cơ ô nhiễm HÓA CHẤT BẢO VỆ THỰC VẬT.
Bảng 6.2. Quy định của Dược điển Việt Nam IV về giới hạn HÓA CHẤT BẢO VỆ THỰC VẬT
| TT | Hợp chất | MRL (mg/kg) |
| 1 | Alaclor | 0,02 |
| 2 | Tổng aldrin và dieldrin | 0,05 |
| 3 | Azinphos-methyl | 1,0 |
| 4 | Bromopropylat | 3,0 |
| 5 | Tổng cis-Clordan, trans-Clordan và Oxyclordan | 0,05 |
| 6 | Clorfenvinphos | 0,5 |
| 7 | Cypermethrin và các đồng phân | 1,0 |
| 8 | Tổng o.p’-DDT, p.p’-DDE và p.p’-TDE | 0,5 |
| 9 | Deltametherin | 0,5 |
| 10 | Diazinon | 1,0 |
| 11 | Diclorvos | 2,0 |
| 12 | Dithiocarbamat (tính theo CS2) | 3,0 |
| 13 | Tổng α -Endosulfan, β-Endosulfan và Endosulfa sulfat | 0,05 |
| 14 | Endrin | 2,0 |
| 15 | Ethion | 0,5 |
| 16 | Fenitrothion | 1,5 |
| 17 | Fenvalerat | 0,05 |
| 18 | Fonofos | 0,05 |
| 19 | Tổng Heptaclor và Heptaclor epoxid | 0,1 |
| 20 | Hexaclorobenzen | 0,3 |
| 21 | Các đồng phân Hexaclorocyclohexan, trừ đồng phân γ | 0,6 |
| 22 | Lindan (γ-Hexachlorocyclohexan) | 0,2 |
| 23 | Malathion | 1,0 |
| 24 | Methidathion | 0,2 |
| 25 | Parathion | 0,5 |
| 26 | Parathon-methyl | 0,2 |
| 27 | Permethrin | 1,0 |
| 28 | Phosalon | 0,1 |
| 29 | Piperonyl butoxid | 3,0 |
| 30 | Pirimiphos-methyl | 4,0 |
| 31 | Tổng Pyrethrin | 3,0 |
| 32 | Tổng quintozen, pentacloroanalin, methylclorophenyl sulfid | 1,0 |
Dược điển Việt Nam IV có quy định về phương pháp phân tích HÓA CHẤT BẢO VỆ THỰC VẬT (phụ lục 17.12) trong đó giá trị giới hạn (mg/kg) được lấy quy định của Dược điển Mỹ. Theo quy định này, đối với các sản phẩm có nguồn gốc thực vật, giới hạn của từng HÓA CHẤT BẢO VỆ THỰC VẬT được đưa ra như ở bảng 6.2.
Còn các sản phẩm không có MRL thì giới hạn phải thấp hơn giới hạn phát hiện của phương pháp quy định bởi EPA. Cụ thể hơn, đối với các sản phẩm cuối cùng, giá trị
MRL được tính theo công thức sau:
MRL (mg/kg) = (AxM)/( 100x B)
Trong đó: A: là ADI – lượng ăn vào hàng ngày chấp nhận được (mg/kg cân nặng).
M: Khối lượng cơ thể người (60 kg)
B: Liều dùng dược liệu hàng ngày (kg)
Theo quy định này, mới chỉ có 32 HÓA CHẤT BẢO VỆ THỰC VẬT có giới hạn cho phép. Tuy nhiên, hiện nay vẫn còn rất nhiều HÓA CHẤT BẢO VỆ THỰC VẬT chưa có quy định về giới hạn này. Hầu như các sản phẩm dược liệu, chế phẩm từ dược liệu (như thuốc đông dược, trà thảo dược, thực phẩm chức năng có thành phần thảo dược…) đều chưa có MRL. Điều này gây ra những khó khăn khi đánh giá chất lượng của sản phẩm.
Để giải quyết vấn đề này, một số quốc gia phát triển và tổ chức trên thế giới như Nhật Bản, châu u… sử dụng giá trị MRL chung (default value) đối với các HÓA CHẤT BẢO VỆ THỰC VẬT chưa thiết lập được MRL. Giá trị MRL chung này không dựa trên các nghiên cứu về đánh giá nguy cơ mà dựa trên mức được coi là an toàn đối với người sử dụng. Hiện nay, tại Việt Nam chưa đưa ra giá trị MRL chung. Bảng 6.3 giới thiệu một số quy định về MRL chung của một số nước.
Bảng 6.3. Giá trị MRL chung của một số nước
| Quốc gia | MRL chung (mg/kg) |
| Châu u | 0,01 |
| Nhật Bản | 0,01 |
| Nam Phi | 0,01 |
| Argentina | 0,01 |
| Malaysia | 0,01 |
| New Zealand | 0,1 |
| Canada | 0,1 |
Mặc dù giá trị MRL chung có sự khác nhau giữa các nước nhưng xu hướng ngày càng có nhiều nước chấp nhận mức 0,01 mg/kg vì sự an toàn của sản phẩm đối với sức khỏe người sử dụng.
Cho đến nay, mức 0,01mg/kg là giá trị MRL thấp nhất của tất cả các HÓA CHẤT BẢO VỆ THỰC VẬT Giá trị MRL chung này được đa số các phòng thí nghiệm lựa chọn như là mức mà phương pháp phân tích phải đạt được để phân tích HÓA CHẤT BẢO VỆ THỰC VẬT.
3.3. Sử dụng hóa chất bảo vệ thực vật trong trồng cây thuốc
Cũng như nhiều loại cây trồng khác, trong quá trình phát triển cây thuốc cũng có nguy cơ mắc phải các bệnh dịch. Do đó, việc sử dụng HÓA CHẤT BẢO VỆ THỰC VẬT trong trồng cây thuốc là rất cần thiết. Tuy nhiên, lạm dụng hay sử dụng không đúng cách HÓA CHẤT BẢO VỆ THỰC VẬT có thể gây tồn dư trong dược liệu và các sản phẩm chế biến từ dược liệu.
Ngày 03 tháng 9 năm 2009, Bộ Y tế ban hành thông tư số 14/2009/TT-BYT về việc hướng dẫn triển khai, áp dụng các nguyên tắc tiêu chuẩn “Thực hành tốt trồng trọt và thu hái cây thuốc ” theo khuyến cáo của Tổ chức Y tê Thế giới. Theo đó, đối với việc sử dụng HÓA CHẤT BẢO VỆ THỰC VẬT, Tổ chức Y tế Thế giới quy định:
- Bất kỳ các hoá chất nông nghiệp nào dùng cho mục đích tăng trưởng hoặc diệt trừ dịch hại chỉ được sử dụng khi không có các phương pháp khác. Cân sử dụng biện pháp phòng trừ dịch hại tổng hợp.
- Chỉ được sử dụng các HÓA CHẤT BẢO VỆ THỰC VẬT có trong danh mục cho phép và cần phải được sử dụng với lượng nhỏ nhất có tác dụng.
- Việc sử dụng HÓA CHẤT BẢO VỆ THỰC VẬT cần được ghi lại về tên, lượng sử dụng, số lần sử dụng và thời gian sử dụng.
- Chỉ có các nhân viên được đào tạo mới được phép sử dụng HÓA CHẤT BẢO VỆ THỰC VẬT.
- Thời gian cách ly từ khi sử dụng HÓA CHẤT BẢO VỆ THỰC VẬT đến khi thu hoạch cần phải tuân theo đúng hướng dẫn của từng HÓA CHẤT BẢO VỆ THỰC VẬT và được sự đồng ý của bên mua.
- Dư lượng HÓA CHẤT BẢO VỆ THỰC VẬT trong các sản phẩm dược liệu phải đáp ứng được các yêu cầu của quốc gia trồng và tiêu thụ sản phẩm.
- Không trồng và thu hoạch dược liệu từ những khu vực gần với nơi có hàm lượng HÓA CHẤT BẢO VỆ THỰC VẬT cao như gần các nhà máy sản xuất, nước thải có chứa nhiều HÓA CHẤT BẢO VỆ THỰC VẬT.
- Thiết bị sử dụng để phun HÓA CHẤT BẢO VỆ THỰC VẬT cần được kiểm soát và hiệu chuẩn định kỳ.
- Trong quá trình bảo quản dược liệu, cần tránh xa các nguồn HÓA CHẤT BẢO VỆ THỰC VẬT.
Hiện nay ở Việt Nam, chỉ có một số ít các đơn vị trồng cây thuốc đạt chuẩn GACP-WHO.
3.4. Tồn dư hóa chất bảo vệ thực vật trong dược liệu
Tổ chức Y tế Thế giới đã ban hành hướng dẫn đánh giá chất lượng dược liệu trong đó HÓA CHẤT BẢO VỆ THỰC VẬT là một tiêu chí rất quan trọng. Mặc dù vậy, các nghiên cứu về tồn dư HÓA CHẤT BẢO VỆ THỰC VẬT trong dược liệu và sản phẩm từ dược liệu ở nước ta hiện nay còn rất hạn chế. Chất lượng các sản phẩm thuốc và thực phẩm chức năng từ thảo dược hiện nay vẫn còn thiếu những quy định về giới hạn kim loại nặng, quy định về tồn dư thuốc bảo vệ thực vật và hóa chất kích thích tăng trưởng. Hay gặp nhất là các mẫu dược liệu có các bộ phận thường dùng là lá và hoa như khổ sâm, ngải cứu, tía tô, húng quế, kinh giới, cúc hoa, mướp đắng, rau má… các mẫu dược liệu khô như đương quy, sâm, ngưu tất….
Một số HÓA CHẤT BẢO VỆ THỰC VẬT còn tồn dư như nhóm clor hữu cơ, nhóm cúc tổng hợp, nhóm phosphor hữu cơ… Hầu hết các nghiên cứu tại Việt Nam cho đến nay đều sử dụng phương pháp sắc ký khí hoặc sắc ký khí khối phổ để xác định dư lượng HÓA CHẤT BẢO VỆ THỰC VẬT. Các phương pháp này chỉ xác định được một số nhóm HÓA CHẤT BẢO VỆ THỰC VẬT như clor hữu cơ, phosphor hữu cơ và cúc tổng hợp mà không thể xác định được một số nhóm HÓA CHẤT BẢO VỆ THỰC VẬT mới đang được sử dụng phổ biến như nhóm carbamat, nhóm neonicotinoid… Do đó, cần phải có những phương pháp phân tích có thể ứng dụng để xác định các hợp chất này.
4. Phương pháp phân tích hóa chất bảo vệ thực vật
Việc xác định mức tồn dư HÓA CHẤT BẢO VỆ THỰC VẬT trong nông sản và dược liệu có ý nghĩa quan trọng để sàng lọc, loại bỏ các sản phẩm không đáp ứng được sự an toàn cho người sử dụng. Có nhiều phương pháp để xác định dư lượng HÓA CHẤT BẢO VỆ THỰC VẬT trong các sản phẩm nông nghiệp. Để đáp ưng nhu cầu phân tích hàng nghìn HÓA CHẤT BẢO VỆ THỰC VẬT, người ta phải áp dụng rất nhiều kỹ thuật phân tích khác nhau. Nhằm giảm thời gian và kinh phí, các phương pháp hiện nay hướng đến xác định đồng thời nhiều HÓA CHẤT BẢO VỆ THỰC VẬT cùng lúc. Các phương pháp này được gọi là phương pháp phân tích đa dư lượng. Nhiều phương pháp được công bố có thể xác định hàm trăm HÓA CHẤT BẢO VỆ THỰC VẬT trong cùng một lân phân tích.
Về nguyên tắc chính, quá trình phân tích HÓA CHẤT BẢO VỆ THỰC VẬT thường gồm hai giai đoạn: giai đoạn xử lý mẫu và giai đoạn phân tích trên thiết bị. Ở giai đoạn thứ nhất, các HÓA CHẤT BẢO VỆ THỰC VẬT được tách ra khỏi nền mẫu vào một dịch chiết thích hợp. Nền mẫu dược liệu rất đa dạng, do đó quá trình xử lý mẫu cần được tối ưu để chiết xuất được tối đa các HÓA CHẤT BẢO VỆ THỰC VẬT trên nhiều loại dược liệu khác nhau. Ở giai đoạn thứ hai một kỹ thuật phân tích phù hợp được chọn sử dụng để xác định hàm lượng HÓA CHẤT BẢO VỆ THỰC VẬT trong dịch chiết từ đó tính được hàm lượng trong mẫu ban đầu.
4.1. Các phương pháp xử lý mẫu
Phân tích dư lượng HÓA CHẤT BẢO VỆ THỰC VẬT trong các nền mẫu dược liệu và nông sản thường gặp phải khó khăn do sự khác nhau về thành phần của mẫu. Vì thế, mục tiêu của quá trình xử lý mẫu ngoài việc đạt được tối đa hiệu suất chiết HÓA CHẤT BẢO VỆ THỰC VẬT còn phải làm giảm được càng nhiều tạp chất càng tốt. Có rất nhiều kỹ thuật xử lý mẫu đã được sử dụng bao gồm chiết bằng dung môi, chiết siêu tới hạn, chiết pha lỏng dưới áp suất, chiết vi sóng chiết pha rắn, chiết phân tán pha rắn, vi chiết pha rắn và QuEChERS.
4.1.1. Chiết bằng dung môi (solvent extractionySE)
Các phương pháp được quy định trong Dược điển Việt Nam IV, Dược điển Mỹ XXXVII hay Dược diễn Trung Quốc 2010 đều sử dụng kỹ thuật chiết bằng dung môi và phối hợp thêm các kỹ thuật làm sạch khác để phân tích HÓA CHẤT BẢO VỆ THỰC VẬT. Theo Dược điển Việt IV và Dược điển Mỹ XXXVII, mẫu dược liệu được làm khô và chiết bằng aceton, sau đó được chuyển đổi về dung môi toluen trước khi cho qua các cột làm sạch phù hợp với từng nhóm HÓA CHẤT BẢO VỆ THỰC VẬT. Dược điển Trung Quốc sử dụng phương pháp chiết HÓA CHẤT BẢO VỆ THỰC VẬT clor hữu cơ bằng aceton và chiết lại bằng dichlormethan, sau đó dichlormethan được cô, cặn được hòa tan trong ehter dầu hỏa và làm sạch với acid sulfruric. Dịch chiết sau đó được phân tích bằng sắc ký khí. Các phuowgn pháp này có thể chiết được một số HÓA CHẤT BẢO VỆ THỰC VẬT thuộc ba nhóm clor hữu cơ, phosphor hữu cơ và pyrethriod, nhưng không chiết được các HÓA CHẤT BẢO VỆ THỰC VẬT thuộc các nhóm khác.
Người ta đã ứng dụng phương pháp chiết dung môi để phân tích HÓA CHẤT BẢO VỆ THỰC VẬT nhóm carbamat và các HÓA CHẤT BẢO VỆ THỰC VẬT phân cực trên nền mẫu bằng cách chiết với hỗn hợp dung môi methanol và đệm acetat có sử dụng siêu âm. Độ thu hồi đạt được từ 70-120% trong khoảng nồng độ từ 0,02 đến 0,2mg/kg.
So sánh khả năng chiết của các loại dung môi và hỗn hợp dung môi để chiết 15 HÓA CHẤT BẢO VỆ THỰC VẬT nhóm clor hữu cơ trong dược liệu bao gồm: hỗn hợp acetonitril và hexan (1:1), hỗn hợp nước và acetonitril (1:1) hay n-hexan, kết quả cho thấy sử dụng n-hexan cho hiệu suất chiết tốt nhất.
Trong các điều kiện chiết, pH là yếu tố khá quan trọng có thể ảnh hưởng đến hiệu suất chiết như: sử dụng pH 10 để chiết nhiều hợp chất có tính acid base khác nhau từ các loại quả họ cam hay điều chỉnh pH về 6 để làm tăng hiệu suất chiết của một số HÓA CHẤT BẢO VỆ THỰC VẬT thế hệ mới như benfuracarb và imidacloprid.
Phương pháp chiết soxhlet cũng được một số tác giả nghiên cứu để chiết HÓA CHẤT BẢO VỆ THỰC VẬT trong dược liệu. Tuy nhiên, các kết quả so sánh cho thấy hiệu quả của phương pháp này không cao, hiệu quả của soxhlet không tốt bằng chiết siêu tới hạn (SPE)…
Chiết bằng dung môi là phương pháp đơn giản, hiệu quả và khá ổn định. Tuy nhiên, phương pháp này có nhiều nhược điểm như rất mất thời gian và tốn công sức; sử dụng lượng lớn dung môi gây ảnh hưởng đến môi trường; một số dung môi độc hại có thể ảnh hưởng đến sức khỏe người làm. Phương pháp này cũng chỉ có thể ứng dụng để phân tích một vài nhóm HÓA CHẤT BẢO VỆ THỰC VẬT như nhóm clor hữu cơ, phosphor hữu cơ và pyrethroid.
4.1.2. Chiết siêu tới hạn (Supercritical-fluid extraction, SPE)
Nhiều tác giả đã phát triển phương pháp SFE để xác định HÓA CHẤT BẢO VỆ THỰC VẬT trong dược liệu. Do CO2 kém phân cực nên khi chiết các HÓA CHẤT BẢO VỆ THỰC VẬT có độ phân cực trung bình đến cao, cân phải sử dụng thêm các chất hỗ trợ hoặc chất tạo phức để thu được hiệu suất chiết cao hơn. SFE có thể được phối hợp với các kỹ thuật làm sạch khác khi phân tích mẫu dược liệu.
Người ta đã sử dụng SFE để chiết 13 HCBỴTV từ dược liệu. Dịch chiết CO2 lỏng được hấp thụ vào bẫy silica hoạt tính ờ -30°C. Chất phân tích được rửa giải với n-hexan ở 30°C sau khi đã cho bay hơi hết CO2. Hiệu suất thu hồi đạt được từ 78 đến 121%.
Tổng hợp các ứng dụng SFE trong phân tích các nền mẫu tự nhiên nếu dựa vào độ tan của các HÓA CHẤT BẢO VỆ THỰC VẬT thì người ta thấy phương pháp SFE rất phù hợp để có thể chiết hầu hết các HÓA CHẤT BẢO VỆ THỰC VẬT mà không phải sử dụng dung môi độc hại.
Ưu điểm nổi bật nhất của SPE là tính chọn lọc. Dịch chiết từ phương pháp này thường không cần phải trải qua quá trình làm sạch trước khi phân tích do đó phương pháp này rất phù hợp cho các nền mẫu phức tạp. Tuy nhiên, đến nay SPE không phải là một phương pháp phổ biến vì các chi phí đầu tư thiết bị khá tốn kém và việc mở rộng ứng dụng trên nền mẫu mới cần có những khảo sát riêng.
4.1.3. Chiết pha rắn (Solidphase extraction, SPE)
Chiết pha rắn là pháp làm sạch được sử dụng rất phổ biến phối hợp với các phương pháp chiết bằng dung môi. Theo Dược điển Mỹ XXXVII và Dược điển Việt Nam IV, pha rắn bản chất styren-divinylbenzen copolymer được dùng để làm sạch mẫu phân tích HÓA CHẤT BẢO VỆ THỰC VẬT nhóm clor hữu cơ, phosphor hữu cơ và nhóm pyrethroid. Trong khi đó, pha rắn silica gel có thể được dùng để làm sạch mẫu phân tích HÓA CHẤT BẢO VỆ THỰC VẬT nhóm clor hữu cơ và nhóm pyrethroid.
Ở Việt Nam, một số tác giả đã nghiên cứu phương pháp s p E với một Số loại pha rắn bao gồm cả pha thuận (florisil, silica gel) và pha đảo (C18) để chiết một số loại dược liệu như ngưu tất, bạch chỉ, tam thât, cúc hoa cho thay phương pháp SPE có ứng dụng tốt trong phân tích dược liệu.
Florisil là loại pha rắn được sử dụng rất phổ biến. Người ta đã sử dụng SPE VƠI pha rắn là florisil để làm sạch dịch chiết ether dầu hỏa của năm loại dược liệu khi chiết 26 loại HÓA CHẤT BẢO VỆ THỰC VẬT (21 hợp chất clor hữu cơ và 5 hợp chất pyrethroid). So sánh SPE với C18 và florisil để làm sạch dịch chiết HÓA CHẤT BẢO VỆ THỰC VẬT nhóm clor hữu cơ trong dược liệu cũng cho thấy florisil cho hiệu quả tốt hơn.
Nghiên cứu so sánh bốn loại cột SPE gồm florisil, silica, florisil-silica và than chì để phân tích 21 HÓA CHẤT BẢO VỆ THỰC VẬT nhóm clor hữu cơ trong dược liệu là lá cây. Phương pháp bao gồm quá trình chiết với hỗn hợp dung môi hexan:aceton (1:1) kết hợp với làm sạch băng SPE. Kết quả cho thấy nền than chì cho khả năng loại bỏ màu và các tạp chất tốt nhất.
Một số loại nền khác cũng được nghiên cứu sử dụng cho SPE như nền PS-DVB để chiết 90 HÓA CHẤT BẢO VỆ THỰC VẬT (đa số các HÓA CHẤT BẢO VỆ THỰC VẬT có độ thu hồi trên 80%, trừ một số chất rất phân cực) hay sử dụng tiểu phân nano của than để làm pha rắn hoặc sử dụng loại SPE ái lực để tách các thuốc trừ cỏ sulfonylurea.
4.1.4. Chiết với hệ phân tán pha rắn (matrix phase MSPD)
Trong số các pha rắn, C18 được sử dụng phổ biến hơn cả. Người ta đã sử dụng c 18 làm pha rắn để chiết 9 HÓA CHẤT BẢO VỆ THỰC VẬT từ mẫu quả. Hỗn hợp dicloromethan và methanol được dùng là dung môi rửa giải. Kỹ thuật MSPD được so sánh với kỹ thuật chiết với ethyl acetat. Kết quả cho thấy chiết bằng dung môi cho độ thu hồi tương tự nhưng đạt được giới hạn phát hiện tốt hơn kỹ thuật chiết với MSPD.
Ngoài C18 thì florisil và diatomit (diatomaceous earth) là hai pha rắn được sử dụng phổ biến trong MSPD. Kỹ thuật MSPD với chất hấp phụ là diatomit đã được sử dụng để phân tích 10 HÓA CHẤT BẢO VỆ THỰC VẬT trong nước quả ép. 1 g mẫu được trộn với 1 g chất hấp phụ và giải chiết bằng 10 mL ethyl acetat, dịch chiết sau đó được thổi khô, hòa cặn trong pha động và phân tích bằng LC-MS/MS. Phương pháp cho LOD tốt dưới 0,2μg/kg và độ thu hôi trong khoảng từ 77 đên 102%. Đặc biệt, có nghiên cứu đã sử dụng diatomit trong kỹ thuật macro-MSPD đê chiêt 266 HÓA CHẤT BẢO VỆ THỰC VẬT từ mẫu nước ép táo và phân tích bằng GC-MS. 10 g mâu được trộn với 20 g diatomit và chuyển vào cột thủy tinh. 160 mL hexamdichlormethan (1:1) được dùng làm dung môi rửa giải. Phương pháp cho thây có nhiều ưu điểm hơn phương pháp chiết lỏng lỏng.
Nói chung, dịch chiết của MSPD đủ sạch để có thể phân tích trên các thiết bị sắc ký. Tuy nhiên, đối với các mẫu phức tạp như mẫu nhiều béo cần thêm bước loại tạp của dich chiết thu được bằng cách cho qua cột florisil.
Giữa SPE và MSPD có sự tương đồng nhất định về bản chất. Tuy nhiên ở MSPD, quá trình chiết mẫu và làm sạch mẫu được thực hiện trong một bước với lượng chất hấp phụ nhỏ, lượng dung môi ít do đó giảm được chi phí và thời gian phân tích. Tuy nhiên, việc cô dung môi chiết vẫn còn là một vấn đề của MSPD, đông thời chưa có công bố về việc kết nối online giữa MSPD với các kỹ thuật sắc ký.
4.1.5. Vi chiết pha rắn (solid phase micro extraction, SPME)
Ứng dụng của SPME để phân tích HÓA CHẤT BẢO VỆ THỰC VẬT trong dược liệu chủ yếu trên các mẫu dạng lỏng như nước ép và thường bằng SPME nhúng. Đối với các mẫu dạng rắn, cân quá trình chiết sơ bộ để đưa về trạng thái lỏng trước khi chiết bằng SPME.
Nhiều ứng dụng của SPME đã được nghiên cứu để phân tích HÓA CHẤT BẢO VỆ THỰC VẬT chủ yếu trong giai đoạn từ những năm 1990 đến đầu những năm 2000. Ở Việt Nam, vào đầu những năm 2000, phương pháp SPME cũng đã được ứng dụng để phân tích HÓA CHẤT BẢO VỆ THỰC VẬT trong dược liệu và nhiều loại nền mẫu khác.
Phương pháp chiết SPME có độ ổn định và độ chính xác trong phân tích định lượng thường kém do đó không trở thành một phương pháp được ứng dụng rộng rãi.
4.1.6. Vi chiết pha lỏng (liquid phase microextraction, LPME)
Kỹ thuật LPME có thể được ứng dụng để phân tích nhiều loại HÓA CHẤT BẢO VỆ THỰC VẬT khác nhau gồm các chất nhóm clor hữu cơ, phosphor hữu cơ, carbamat, triazin… trong nước và các dịch chiết nước của mẫu rau quả, đất, dược liệu… Dung môi chiết thường được sử dụng là toluen, CCl4, n-hexan, iso-octan và cyclohexan. Độ thu hồi của kỹ thuật LPME khi ứng dụng phân tích HÓA CHẤT BẢO VỆ THỰC VẬT dao động từ 57% đến 108%. Khi so sánh với SPME, kỹ thuật LPME cho thấy có độ tin cậy tốt hơn.
4.1.7. Sắc ký thẩm thấu gel (gelpermeation chromatography, GPC)
Trong phân tích HÓA CHẤT BẢO VỆ THỰC VẬT, GPC được sử dụng để loại các tạp chất có khối lượng phân tử lớn. Dược điển Việt Nam quy định phương pháp làm sạch bằng GPC với pha tĩnh là PS-DVB và pha động là toluen để phân tích HÓA CHẤT BẢO VỆ THỰC VẬT trong thuốc có nguồn gốc thực vật. Ngoài ra, có nhiều tác giả đã ứng dụng kỹ thuật GPC để làm sạch mẫu trong phân tích HÓA CHẤT BẢO VỆ THỰC VẬT.
4.1.8. Phương pháp QuEChERS
Giới thiệu phương pháp:
Năm 2003, Anastasssiades và Lehotay giới thiệu một phương pháp mới để phân tích dư lượng HÓA CHẤT BẢO VỆ THỰC VẬT, sau này được gọi là QuEChERS (viết tắt của quick, easy, cheap, effective, rugged và safe), QuEChERS là một phương pháp phân tích đa dư lượng thuốc trừ sâu trong nhiều loại nền mẫu khác nhau, chỉ cần có khoảng 70-100% nước trong thành phần (mẫu khô được cho thêm nước). Như tên gọi của nó, chuẩn bị mẫu theo QuEChERS có nhiều thuận lợi so với các phương pháp truyền thống.
Phương pháp QuEChERS được báo cáo đầu tiên năm 2003 Anastasssiades và Lehotay. Năm 2005, Lehotay và các cộng sự đã nghiên cứu thẩm định và cho thấy rằng phương pháp này cho kết quả tốt với 207 chất trong số 235 thuốc trừ sâu trên các nền mẫu rau quả. Tuy nhiên những chất nhạy với pH bị ảnh hưởng rõ rệt. Sau đó Lehotay thay đổi phương pháp gốc bằng cách sử dụng đệm acetat pH4,8-5,0 để tăng độ thu hồi của thuốc trừ sâu. Phương pháp này sau đó đã được nghiên cứu trong 13 phòng thí nghiệm ở 7 quốc gia với 30 thuốc trừ sâu và trở thành phương pháp chính thức của AOAC 2007.01. Cùng thời gian đó, Anastasssiades và cộng sự phát triển một phương pháp QuEChERS khác sử dụng đệm citrat ở pH khoảng 5. Phương pháp này đã được thẩm định liên phòng tại nhiều phòng thí nghiệm ở Đức và trở thành phương pháp châu u CEN 15662.
Quy trình chiết theo QuEChERS được tóm tắt trong hình 6.1 Hiện nay có ba phiên bản chính của phương pháp vẫn còn được áp dụng. Đó là phiên bản đầu tiên do Anastasssiades và Lehotay phát triển, phiên bản dùng đệm acetat theo AOAC và phiên bản dùng đệm citrat theo tiêu chuẩn Châu Âu.
Theo kết quả so sánh ba phiên bản trên một số nền rau quả của Lehotay và cộng sự cho thấy phương pháp dùng đệm acetat cho hiệu suất chiết cao hơn đối với một số HÓA CHẤT BẢO VỆ THỰC VẬT bị ảnh hưởng bởi pH như pymetrozin và thiabendazol trên nền amaux có pH acid như chanh.
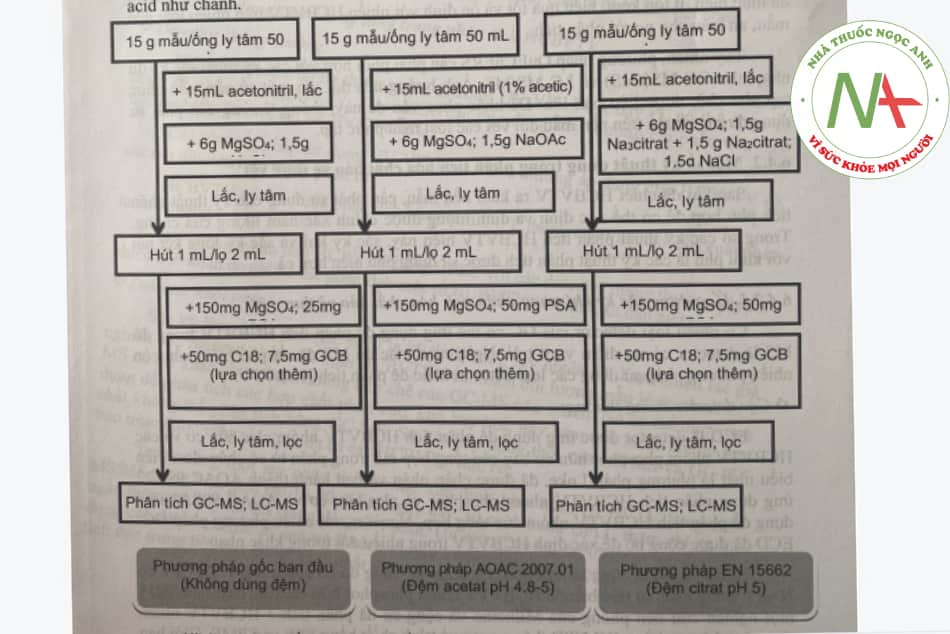
Ứng dụng của QuEChERS:
Có thể nói hiện nay, phương pháp QuEChER đã trở đầu trong phân tích HÓA CHẤT BẢO VỆ THỰC VẬT trong nhiều nền mẫu khác nhau như rau quả, ngũ cốc, các sản phẩm thực phẩm khác cũng như trên nhiều loại dược liệu hay sản phẩm chế biến từ dược liệu.
Nói chung, các tác giả đều ứng dụng phương pháp QuEChERS có thay đổi một số điểm trong dung môi chiết hay trong bước làm sạch. Acetonitril được ổn định pH bằng đệm acetat là dung môi được sử dụng phổ biến nhất. Trong bước làm sạch, MgSO4 và PSA luôn được sử dụng, ngoài ra một số tác giả phối hợp thêm GCB để tăng hiệu quả chiết.
Các kết quả trên cho thấy phương pháp QuEChERS có thể ứng dụng trên dược liệu và các sản phẩm từ dược liệu để xác định HÓA CHẤT BẢO VỆ THỰC VẬT. Phương pháp QuEChER nói chung có độ thu hồi đáp ứng được yêu cầu trên nhiều loại nền mẫu với nhiều HÓA CHẤT BẢO VỆ THỰC VẬT. Giống như tên gọi của nó, phương pháp QuEChERS có rất nhiều ưu điểm như: nhanh, dễ thực hiện, ít tốn kém, hiệu quả tốt và ổn định với nhiều HÓA CHẤT BẢO VỆ THỰC VẬT trên nhiều loại nền mẫu, an toàn cho người phân tích.
Tuy nhiên, phương pháp QuEChERS cần phải phối hợp với các kỹ thuật sắc ký đủ nhạy như GC-MS(/MS) và LC-MS/MS. Ảnh hưởng nền đối với một số nền mẫu phức tạp như chè, dược liệu còn lớn. Để khắc phục vấn đề này, thông thường cần phải sử dụng đường chuẩn trên nền mẫu đối với các loại mẫu phức tạp.
4.2. Một số kỹ thuật dùng trong phân tích hóa chất bảo vệ thực vật
Sau khi đã chiết HÓA CHẤT BẢO VỆ THỰC VẬT ra khỏi nền mẫu, cân phải sử dụng các kỹ thuật phân tích phù hợp để có thể xác định và định lượng được chính xác hàm lượng của chúng. Trong số các kỹ thuật phân tích HÓA CHẤT BẢO VỆ THỰC VẬT hiện nay, sắc ký khí và sắc ký lỏng kết nối với khối phổ là các kỹ thuật phân tích được sử dụng phổ biến hơn cả ứng dụng sắc ký khí trong phân tích hóa chất bảo vệ thực vật
4.2.1. Ứng dụng sắc ký khí trong phân tích hóa chất bảo vệ thực vật
Có nhiều loại loại detector của GC có thể ứng dụng để phân tích HÓA CHẤT BẢO VỆ THỰC VẬT trong đó S là detector có ưu điểm vượt trội. Ngày nay, mặc dù MS đã rất phổ biến, vẫn còn nhiều phương pháp sử dụng các loại detector khác để phân tích HÓA CHẤT BẢO VỆ THỰC VẬT.
Các detector thông thường:
ECD là detector được ứng dụng để phân tích HÓA CHẤT BẢO VỆ THỰC VẬT nhóm clor hữu cơ và cá HÓA CHẤT BẢO VỆ THỰC VẬT nhóm phosphor hữu cơ hay cúc tổng hợp mà trong phân tử có chứa clor. Tiêu biểu nhất là phương pháp Luke, được chấp nhận và ban hành thành AOAC 985.22 ứng dụng phân tích HÓA CHẤT BẢO VỆ THỰC VẬT nhóm phosphor và clor hữu cơ và AOAC 998.01 ứng dụng để phân tích HCBVYV nhóm cúc tổng hợp. Ngoài ra, rất nhiều phương pháp GC-ECD đã được công bố để xác định HÓA CHẤT BẢO VỆ THỰC VẬT trong nhiều đối tượng khác nhau.
Ngoài ra, NPD cũng là một detector được sử dụng do có nhiều loại HÓA CHẤT BẢO VỆ THỰC VẬT có N và P trong phân tử tiêu biểu là HÓA CHẤT BẢO VỆ THỰC VẬT nhóm phosphor hữu cơ. Gần đây, năm 2011 một số nghiên cứu liên phòng của Milhome và cộng sự đã phân tích 7 HÓA CHẤT BẢO VỆ THỰC VẬT nhóm phosphor hữu cơ bằng GC-NPD thông qua quá trình chiết bằng SPE và SPME. Giới hạn phát hiện của phương pháp dao động từ 0,01 đến 0,3 μg/L tùy từng chất. FPD cũng được sử dụng để phân tích HÓA CHẤT BẢO VỆ THỰC VẬT nhóm phosphor hữu cơ có chứa P va S.
Việc sử dụng các detector nhu ECD, NPD, FPD chỉ ứng dụng để phân tích một nhóm HÓA CHẤT BẢO VỆ THỰC VẬT có tính chất hóa học tương tự. Khi phân tích các HÓA CHẤT BẢO VỆ THỰC VẬT khác thường không đáp ứng được độ nhạy.
Detector khối phổ:
Khối phổ là một detector vạn năng, về nguyên tắc nó có thể ứng dụng để phân tích mọi loại hợp chất. Trong phân tích HÓA CHẤT BẢO VỆ THỰC VẬT, GC-MS đóng vai trò rất quan trọng. Ngày nay, sự ra đời của GC-MS/MS đã đáp ứng được các yêu cầu về phân tích hàm lượng rất nhỏ với độ chính xác rất cao. Khi phân tích HÓA CHẤT BẢO VỆ THỰC VẬT bằng GC-MS thường sử dụng nguồn ion hóa EI.
GC đã được ứng dụng rộng rãi để xác định đồng thời nhiều HÓA CHẤT BẢO VỆ THỰC VẬT, tuỵ nhiên có rất nhiều loại HÓA CHẤT BẢO VỆ THỰC VẬT không thể phân tích được bằng GC. GC chỉ phù hợp để phân tích các HÓA CHẤT BẢO VỆ THỰC VẬT không phân cực đến phân cực trung bình và các chất bay hơi mà không thể phân tích các hợp chất phân cực, chất không bay hoi hay chất bị phân hủy bởi nhiệt.
4.2.2. Ứng dụng của sắc ký lỏng trong phân tích HÓA CHẤT BẢO VỆ THỰC VẬT
Detector thông thường:
Một số detector thông thường như detector UV-VIS, PDA hay FL có thể được sử dụng để phân tích HÓA CHẤT BẢO VỆ THỰC VẬT. Tuy nhiên, các ứng dụng này thường chỉ phân tích một nhóm nhỏ hoặc một vài HÓA CHẤT BẢO VỆ THỰC VẬT đơn lẻ.
Các phương pháp sử dụng UV-VIS hoặc PDA thường áp dụng cho HÓA CHẤT BẢO VỆ THỰC VẬT có các nối đôi liên hợp trong phân tử.
Nói chung, phân tích HÓA CHẤT BẢO VỆ THỰC VẬT bằng HPLC với các detector thông thường gặp rất nhiều khó khăn do chỉ có thể phân tích một số HÓA CHẤT BẢO VỆ THỰC VẬT có tính chất đặc biệt.
Detector khối phổ:
Sắc ký lỏng khối phổ (LC-MS) là kỹ thuật mới, tuy nhiên đã được nhiều tác giả nghiên cứu phương pháp xác định HÓA CHẤT BẢO VỆ THỰC VẬT trên nhiều đối tượng mẫu khác nhau. LC-MS có thể khắc phục được những hạn chế của GC-MS nêu ở trên. Nó có thể được ứng dụng để phân tích các hợp chất phân cực, khó bay hơi, hay kém bền nhiệt những hợp chất không thể phân tích bằng GC-MS. Sự kết hợp đồng thời của LC-MS và GC-MS bao trùm được việc xác định tất cả các HÓA CHẤT BẢO VỆ THỰC VẬT hữu cơ.
Trong cùng một lần phân tích có thể xác định hàng trăm HÓA CHẤT BẢO VỆ THỰC VẬT bằng LC-MS/MS trong thời gian chỉ 10-20 phút. Ngày nay, sự ra đời của UPLC thậm chí đã rút ngăn thời gian này lại chỉ trong vòng 2-4 phút. Ưu điểm của LC-MS/MS so với việc sử dụng các detector khác là quá trình tách sắc ký không quá quan trọng. Mỗi chất phân tích đặc trưng bởi các giá trị m/z nhất định do đó nếu LC không tác được hoàn toàn vẫn có thể định lượng được nhờ vai trò của MS. Thông thường, mỗi chất phân tích cân xác định được 1 ion phân tử và 2 ion sản phẩm để cho kết quả tin cậy.
Khi so sánh khả năng ứng dụng của hai kỹ thuật GC-EI-MS và LC-ESI-MS, Alder và cộng sự kết luận rằng phương pháp LC-MS cho độ nhạy tốt hơn va kha nang ứng dụng rộng hơn. Trong số 500 loại HÓA CHẤT BẢO VỆ THỰC VẬT được quan tâm, chỉ có 49 HÓA CHẤT BẢO VỆ THỰC VẬT không phân tích được bang LC-MS, trong khi có 135 HÓA CHẤT BẢO VỆ THỰC VẬT không phân tích được bằng GC-MS. Giới hạn phát hiện của LC-MS/MS cũng thấp hơn khoảng 0,1-1 ng/mL trong khi của GC-MS/MS khoảng 10 ng/mL.
Như vậy, LC-MS/MS là một kỹ thuật đóng vai trò rất quan trọng trong phân tích HÓA CHẤT BẢO VỆ THỰC VẬT. Ngoài ra, để có thể bao trùm được toàn bộ HÓA CHẤT BẢO VỆ THỰC VẬT cần sử dụng thêm với GC-MS hay GC-MS/MS. Sự phối hợp giữa phương pháp xử lý mẫu theo QuEChERS và phương pháp phân tích theo GC-MS/MS và LC-MS/MS đem lại một phương pháp hoàn hảo để ứng dụng phân tích HÓA CHẤT BẢO VỆ THỰC VẬT.
Câu hỏi lượng giá
- Khái niệm hóa chất bảo vệ thực vật? Các cách phân loại, tên các nhóm hóa chất thực vật phổ biến và tên một số hóa chất bảo vệ thực vật thuộc các nhóm này.
- Kể tên một số HÓA CHẤT BẢO VỆ THỰC VẬT điển hình, cơ chế gây độc, triệu chứng và cách xử với nhiễm độc một số nhóm clor hữu cơ.
- Kể tên một số HÓA CHẤT BẢO VỆ THỰC VẬT điển hình, cơ chế gây độc, triệu chứng và cách xử trí với nhiễm độc một số nhóm phosphor hữu cơ.
- Tác động của dioxin và các thuốc diệt cỏ đối với con người và cách xử trí khi bị nhiễm độc?
- Trình bày cách sử dụng hóa chất bảo vệ thực vật an toàn và hiệu quả.
- Trình bày được khái niệm mức tồn dư tối đa, nguyên tắc xử lý mẫu và phân tích các hóa chất bảo vệ thực vật.
- Nguyên tắc và ứng dụng của phương pháp QuEChERS trong phân tích dư lượng HÓA CHẤT BẢO VỆ THỰC VẬT?
