Bệnh hô hấp, COVID-19, Thông Tin Thuốc
Dexamethasone và Methylprednisolone liều cao trong điều trị bệnh viêm phổi do Covid-19
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
PLOS ONE 16(5): e0252057. Published: May 25, 2021. https://doi.org/10.1371/journal.pone.0252057.
Dịch bởi: Thạc sĩ Bác sĩ Đào Thị Mỹ Vân.
Để tải bài viết Dexamethasone và Methylprednisolone liều cao trong điều trị bệnh viêm phổi do Covid-19 pdf mời các bạn click vào link ở đây.
Tóm tắt
Giới thiệu
Cho đến nay, chưa có liệu pháp hiệu quả trong điều trị hội chứng hô hấp cấp tính do Coronavirus 2 (SARS-CoV2) gây ra bệnh Coronavirus 2019 (Covid-19). Hiện tại, dexamethasone đã cho thấy hiệu quả trong việc làm giảm tỷ lệ tử vong ở những bệnh nhân cần thở oxy, đặc biệt là những bệnh nhân thở máy xâm lấn. Tuy nhiên, có chăng một loại corticosteroid khác với liều lượng và thời gian sử dụng phù hợp có thể đạt được kết quả lâm sàng tốt hơn? Mục tiêu của nghiên cứu này là so sánh sự khác biệt về kết quả lâm sàng và kết quả xét nghiệm ở những bệnh nhân nặng do Viêm phổi SARS-CoV2 được điều trị bằng dexamethasone ở liều 6mg so với những bệnh nhân được điều trị bằng methylprednisolone liều cao.
Phương pháp
Một nghiên cứu đoàn hệ có liên quan với việc phân tích tỷ lệ sống sót của 216 bệnh nhân được chẩn đoán viêm phổi nặng do Covid-19, được xác nhận bằng phản ứng chuỗi polymerase đối với SARS-CoV2 theo phác đồ Berlin, những bệnh nhân này nằm tại một phòng khám đa khoa ở Medellín, Colombia. Họ được bổ sung oxy và xác nhận viêm phổi bằng phương pháp chụp X-quang và CT lồng ngực. Kích thước mẫu không được tính toán vì tổng số đáp ứng được các tiêu chí đã được đánh giá. 111 bệnh nhân được điều trị theo phác đồ tại cơ sở với dexamethasone 6 mg mỗi ngày tiêm tĩnh mạch trong 7 đến 10 ngày nếu họ cần thở oxy. Từ ngày 15 tháng 9 năm 2020, quy trình của phòng khám đã được sửa đổi bởi dịch vụ Bệnh truyền nhiễm và Hô hấp, với việc khuyến nghị dùng liều cao methylprednisolone từ 250 đến 500 mg mỗi ngày trong ba ngày và tiếp sau đó uống prednisone 50 mg mỗi ngày trong 14 ngày. Phác đồ này không được áp dụng trong phòng chăm sóc đặc biệt và tiếp tục được sử dụng dexamethasone. Kết quả lâm sàng và sự khác biệt trong kết quả xét nghiệm của những bệnh nhân được sử dụng dexamethasone so với nhóm nghiên cứu sau đó nhận được methylprednisolone từ ngày 15 tháng 9 đến ngày 31 tháng 10 năm 2020 đã được đánh giá. Việc theo dõi tình trạng tái phát hoặc tình trạng sống của bệnh nhân được thực hiện thông qua việc tái khám hoặc qua điện thoại sau khi xuất viện một tháng.
Kết quả
216 bệnh nhân bị viêm phổi do Covid-19 được ghi lại bằng hình ảnh kính mờ và áp suất phế nang/ phân suất oxy hít vào (PaFi) dưới 300. 111 bệnh nhân dùng dexamethasone (DXM) và 105 bệnh nhân được dùng methylprednisolone (MTP). Bệnh nhân trong nhóm DXM tiến triển thành ARDS nặng với tỷ lệ cao hơn (26,1% so với 17,1% so với nhóm MTP). Sau khi hoàn thành 4 ngày điều trị bằng corticosteroid đường tiêm, các chỉ số xét nghiệm về mức độ nghiêm trọng được giảm đáng kể ở nhóm được dùng MTP, CRP 2,85 (2,3–3,8) so với 7,2 (5,4–9,8), (p-value <0,0001), D-dimer 691 (612–847) so với 1083 (740–1565) (p-value = 0,04) và DHL 273 (244–289) so với 355 (270,6–422) (pvalue = 0,01). Sau khi bắt đầu điều trị bằng corticosteroid, tỷ lệ bệnh nhân được chuyển đến đơn vị chăm sóc đặc biệt (4,8% so với 14,4%) và tỷ lệ tử vong (9,5% so với 17,1%) ở nhóm được dùng MTP thấp hơn. Thời gian hồi phục ở những bệnh nhân được điều trị bằng MTP cũng rút ngắn hơn, còn 3 ngày (3– 4) so với DXM 6 ngày (5–8) (p-value <0,0001). Trong thời gian 30 ngày theo dõi, 88 bệnh nhân còn sống ở nhóm dùng MTP (chiếm 92,6%) so với những người được dùng dexamethasone là 58 (chiếm 63,1%).
Kết luận
Trong nghiên cứu này, việc điều trị bệnh nhân nặng bị viêm phổi do Covid-19 bằng methylprednisolone liều cao trong 3 ngày, sau đó là prednisone đường uống trong 14 ngày, so với việc sử dụng 6mg dexamethasone trong 7 đến 10 ngày, đã làm giảm đáng kể thời gian hồi phục cũng như nhu cầu chuyển đến phòng chăm sóc đặc biệt và đánh dấu mức độ nghiêm trọng Protein phản ứng C (CRP), D-dimer và LDH. Các nghiên cứu đối chứng ngẫu nhiên với methylprednisolone được yêu cầu để xác thực tác dụng, và các nghiên cứu trên tổng số bệnh nhân nhập viện tại các khu chăm sóc đặc biệt.
Giới thiệu
Coronavirus 2019 (Covid-19) là căn bệnh có tên là Hội chứng hô hấp cấp tính nặng SARSCoV-2 do vi rút Coronavirus 2 gây ra, đây là một mầm bệnh mới được xác định ban đầu ở Vũ Hán, Trung Quốc vào tháng 12 năm 2019 [1]. Tính đến ngày 11 tháng 11 năm 2020, toàn cầu có 52.024.841 người bị nhiễm bệnh, trong đó có 1.282.944 trường hợp tử vong, chiếm tỷ lệ là 2,5% [2] với mức độ lây lan cao hơn so với các dịch bệnh trước đây như SARS-CoV và MERS [3]. Để đối mặt với đại dịch này, những loại thuốc đã từng được sử dụng trong các đợt dịch SARS-COV và MERS trước đây, bao gồm chloroquine và hydroxychloroquine [4], lopinavir/ ritonavir [5], azithromycin [6], và ivermectin [7], khi so sánh với những loại khác, cho thấy một số phản ứng tích cực trong việc chống lại SARS-CoV2 trong ống nghiệm. Tại một trung tâm nghiên cứu ở Michigan, Hoa Kỳ, việc sử dụng hydroxychloroquine một mình hoặc kết hợp với azithromycin có liên quan đến việc giảm tỷ lệ tử vong [8]. Tuy nhiên, trong các thử nghiệm lâm sàng ngẫu nhiên, không có tác dụng thuận lợi nào được chứng minh.
Vào ngày 16 tháng 6 năm 2020, báo cáo sơ bộ của nghiên cứu Phục hồi [9] đã được công bố, trong đó báo cáo đã so sánh những bệnh nhân bị viêm phổi do Covid-19 được dùng dexamethasone 6mg mỗi ngày trong tối đa 10 ngày (hoặc cho đến khi xuất viện) so với những bệnh nhân không dùng corticosteroid. Trong nghiên cứu này, tỷ lệ tử vong ở nhóm bệnh nhân được dùng dexamethasone thấp hơn so với nhóm không dùng. Mặc dù tỷ lệ tử vong giảm 11% ở bệnh nhân thở máy có xâm lấn (29% so với 40%), sự khác biệt về tỷ lệ tử vong toàn cầu là rất nhỏ (22,9% so với 25,7%), dựa trên nghiên cứu Phục hồi này, hầu hết các hướng dẫn trong các bệnh viện trên toàn thế giới đã bổ sung thông tin này vào. Tuy nhiên, cho đến nay vẫn chưa rõ việc điều trị những biến chứng của Covid-19, Hội chứng suy hô hấp cấp tiến triển (ARDS) [10] hoặc Hội chứng phóng thích Cytokine (CRS) [11], là tác dụng cụ thể của dexamethasone hay là một loại tác dụng mà các corticosteroid khác có thể gây ra, hoặc ngay cả khi corticosteroid liều thấp hoặc cao đều có tác dụng tương tự. Mục tiêu của nghiên cứu là so sánh kết quả lâm sàng của bệnh nhân được điều trị bằng dexamethasone so với methylprednisolone liều cao ở cấp bệnh viện tại một phòng khám đa khoa ở Medellín, Colombia.
Phương pháp
Nghiên cứu đoàn hệ không phân biệt với phân tích tỷ lệ sống sót được thực hiện tại một phòng khám đa khoa ở Medellín, Colombia.
Nghiên cứu được tiến hành ở các bệnh nhân trên 18 tuổi, nhập viện vì viêm phổi do Covid-19 được xác nhận bằng kết quả dương tính với SARS-CoV2 bằng phương pháp RTPCR SARS-CoV2 theo phác đồ Berlin. Bệnh nhân cũng được bổ sung oxy và xác nhận viêm phổi thông qua chụp X-quang và CT lồng ngực. Kích thước mẫu không được tính toán vì tổng số trên đã đáp ứng các tiêu chí và đã được đánh giá. Sau khi được sự đồng ý, bệnh nhân được điều trị theo phác đồ của hội đồng (từ ngày 11 tháng 6 đến ngày 14 tháng 9 năm 2020) với dexamethasone 6mg tiêm tĩnh mạch hàng ngày trong tối đa 10 ngày (hoặc cho đến khi xuất viện) nếu bệnh nhân cần được bổ sung oxy (nghiên cứu đoàn hệ hồi cứu). Từ ngày 15 tháng 9 năm 2020, phác đồ đã được thay đổi từ dexamethasone thành methylprednisolone 250-500mg mỗi ngày trong ba ngày, tiếp theo là prednisone 50mg uống mỗi ngày trong 14 ngày (nghiên cứu đoàn hệ tiền cứu). Liều trung bình của methylprednisolone là 500mg tiêm tĩnh mạch mỗi ngày trong ba ngày. Liều lượng dựa trên các báo cáo về SARS-CoV và kinh nghiệm về viêm phổi cấp và viêm phổi chẩn đoán tại trung tâm. Tất cả bệnh nhân được dùng ivermectin – một giọt/ kg trong 3 ngày để ngăn ngừa hội chứng Loeffler do corticosteroid (một giọt tương đương với 200 microgam ivermectin). Tất cả bệnh nhân bắt đầu được điều trị từ ngày đầu tiên nhập viện và không được chọn ngẫu nhiên.
Được xem là tiêu chí loại trừ để tham gia bất kỳ nhóm thuần tập nào của nghiên cứu, các chống chỉ định liên quan đến corticosteroid đã được xem xét, bất đồng đối với hệ thống y tế, tử vong trong 24 giờ đầu, bệnh nhân được chăm sóc giảm nhẹ hoặc có thời gian sống sót dưới sáu tháng. Nếu bệnh nhân yêu cầu nhập viện vào ICU và không nhận được ít nhất hai liều corticosteroid, thì được rút khỏi nhóm thuần tập để theo dõi (Trong phác đồ tại ICU, chỉ dexamethasone 6mg được tiêm tĩnh mạch là được thực hiện). Nếu bệnh nhân nhận được ít nhất hai liều methylprednisolone nhưng không tiếp tục với prednisone, họ sẽ không được đưa vào nhóm, nhưng kết quả của họ vẫn tiếp tục được theo dõi. Những bệnh nhân được điều trị dexamethasone ít hơn hai ngày cũng được rút khỏi theo dõi nghiên cứu. Colchicine được sử dụng theo phác đồ tại phòng khám kể từ ngày 1 tháng 7; giá trị này được bao gồm trong các đánh giá của bệnh nhân.
Sau khi nhập viện, các xét nghiệm trong phòng thí nghiệm sẽ được thực hiện, chẳng hạn như xét nghiệm huyết đồ, thận, chức năng gan, khí máu động mạch, lactate dehydrogenase, D-dimer, ferritin huyết thanh và protein phản ứng C. Heparin trọng lượng phân tử thấp được kê đơn cho tất cả bệnh nhân để ngăn ngừa tắc mạch huyết khối trong thời gian nằm viện. Viêm phổi được phân loại là nặng khi thiếu oxy máu hoặc nhu cầu bổ sung oxy, và trong một số trường hợp, phức tạp với hội chứng sốc nhiễm trùng, hoặc tổn thương đa cơ quan. Hội chứng suy hô hấp cấp tiến triển (ARDS) được xác định khi có thâm nhiễm phổi hai bên không được giải thích được căn nguyên khác ngoài Covid-19 và PaFi nhỏ hơn 300. Kết quả khí máu động mạch trong mỗi lần bệnh nhân nhập viện được đánh giá để xác định sự tiến triển của ARDS. Kết quả ưu tiên chính là thời gian phục hồi, được định nghĩa là sự cải thiện lâm sàng đáng kể trong diễn biến của bệnh nhân để xem xét xuất viện. Do đó, cần cải thiện tình trạng khó thở, giảm việc hỗ trợ oxy ít nhất cho đến oxy qua ống thông mũi (nếu trước đó cho thở oxy qua mặt nạ Ventury, mặt nạ không hít lại, thở máy không xâm lấn hoặc thở máy xâm lấn) hoặc không cần oxy bổ sung. Kết quả thứ hai là phải chuyển đến đơn vị chăm sóc đặc biệt (ICU), tử vong và tái nhập viện sau 30 ngày xuất viện, vào viện vì nhiễm khuẩn. Việc theo dõi được thực hiện bằng tư vấn ngoại trú một tháng sau khi xuất viện hoặc qua điện thoại, hỏi về tình trạng tái phát hoặc tình trạng sống. Sự tiêu chuẩn hóa được thực hiện dưới sự quan sát của nhà nghiên cứu, do đó cần đảm bảo kỹ thuật thích hợp trong việc thu thập thông tin. Với những dữ liệu này, một cơ sở dữ liệu được xây dựng trong Microsoft Excel và trước khi phân tích, nó đã được kiểm soát chất lượng. Khi tất cả các biến đã được thu thập, các biến định lượng được biểu thị dưới dạng trung vị mẫu của chúng (cùng với khoảng tin cậy 95% bootstrap tương ứng của chúng) và được so sánh bằng cách sử dụng kiểm định giả thuyết Mann & Whitney hai mặt. Các biến định tính được biểu thị bằng giá trị tuyệt đối, cùng với giá trị phần trăm tương ứng của chúng (%) và được so sánh bằng cách sử dụng kiểm định z hai mẫu để kiểm tra giả thuyết tỷ lệ. Việc so sánh hiệu suất điều trị của methylprednisolone (MTP) với dexamethasone (DXM) được thực hiện thông qua biến phản ứng ‗Thời gian phục hồi‘, được đo bằng ngày, biểu thị thời gian hồi phục cho đến khi xuất viện nếu đã nhận được ít nhất hai liều điều trị tương ứng. Phân tích này được thực hiện thông qua mô hình phân tích tỷ lệ sống sót với hồi quy Cox [12], và nó đã được chứng minh rằng các rủi ro là tỷ lệ thuận, từ hai giai đoạn: đầu tiên, một hồi quy Cox mạnh mẽ [13] được thực hiện để xác định các biến dự báo giải thích tỷ lệ rủi ro (HR), tránh sự can thiệp có thể xảy ra đối với các quan sát ngoại lai trong ước tính khả năng xảy ra một phần. Trong giai đoạn thứ hai, với các biến quan trọng (‗Điều trị‘ và ‗Colchicine‘), một mô hình mới đã được ước tính cho các ước tính điểm và khoảng tin cậy 95% của chúng. Các phân tích thống kê này được thực hiện trong phần mềm thống kê R [14] thông qua gói coxrobust [15] để thực hiện hồi quy Cox mạnh mẽ và gói tồn tại [16] cho hồi quy Cox truyền thống.
Đạo đức
Nghiên cứu này đã được Ủy ban đạo đức Clinica Medellin phê duyệt. Những người tham gia nghiên cứu đã cam kết đồng ý thực hiện. Số đăng ký dùng thử ISRCTN33037282.
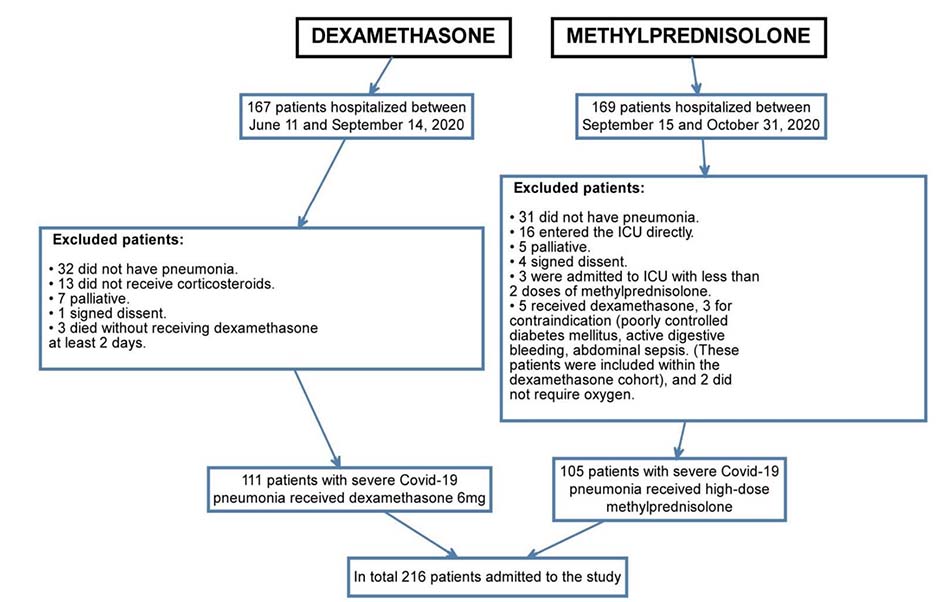
Kết quả
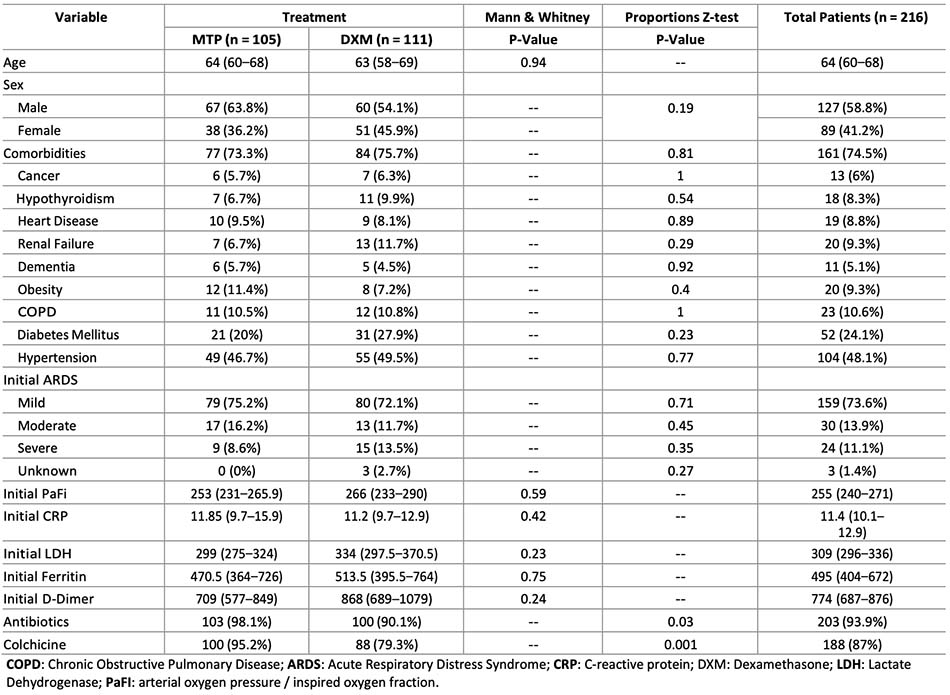
Tổng cộng có 216 bệnh nhân, trong đó có111 bệnh nhân đã nhận dexamethasone (nhóm DXM hồi cứu), và 105 bệnh nhân nhận được methylprednisolone (nhóm MTP tiền cứu) (Hình 1). Không có sự khác biệt có ý nghĩa thống kê giữa hai nhóm bệnh nhân, làm giảm khả năng so sánh về các biến số về tuổi, giới tính, bệnh đi kèm, ban đầu: PaFi, CRP, DHL, Ferritin, D-dimer, hoặc sử dụng kháng sinh. Colchicine được kê cho 100 bệnh nhân (95,2%) của nhóm MTP so với 88 (79,3%) của nhóm DXM (Bảng 1).
Kết quả lâm sàng
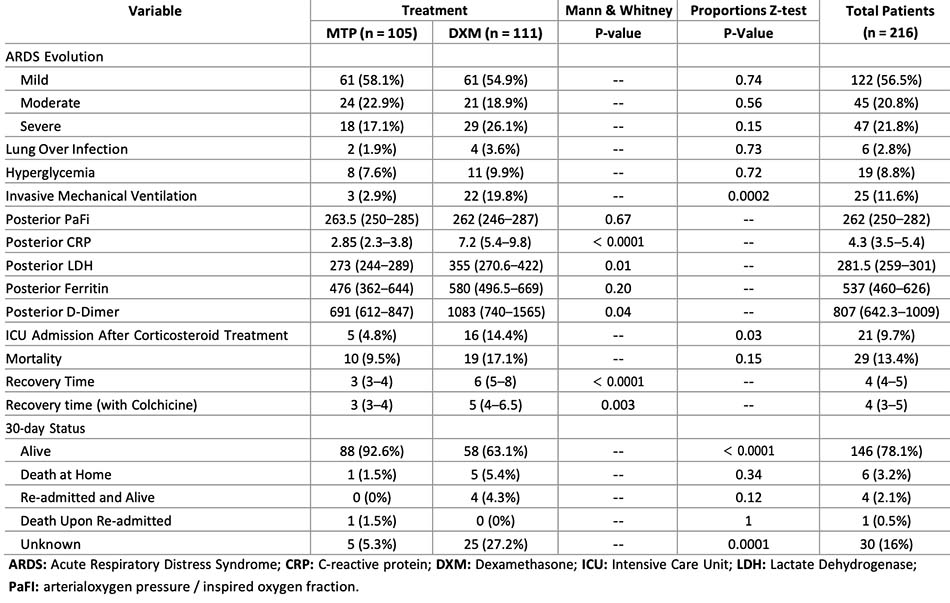
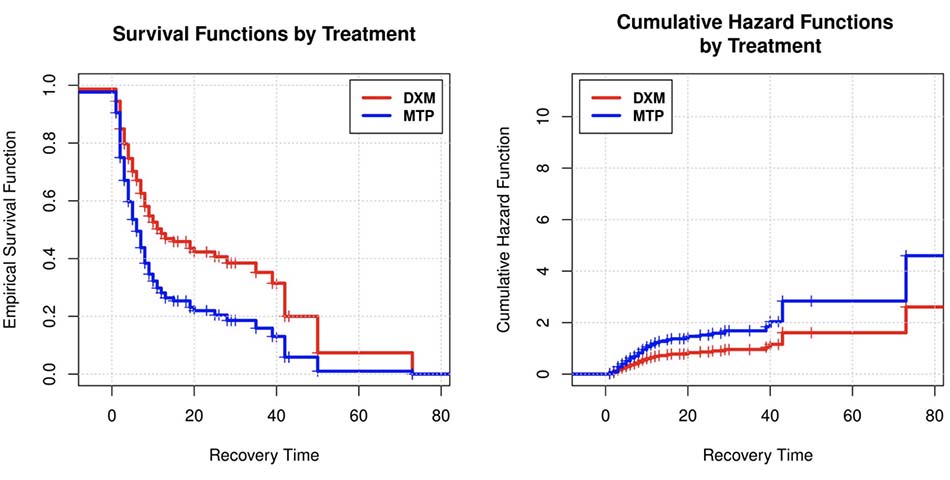
Bệnh nhân trong nhóm DXM tiến triển thành ARDS nặng chiếm tỷ lệ cao hơn (26,1% so với 17,1% ở nhóm MTP). Sau khi hoàn thành 4 ngày điều trị bằng corticosteroid đường tiêm, các dấu hiệu cận lâm sàng về mức độ nghiêm trọng giảm đáng kể ở nhóm được dùng MTP, với CRP 2,85 (KTC 95%: 2,3– 3,8) so với 7,2 (5,4–9,8), (giá trị p <0,0001 ), D-dimer 691 (KTC 95%: 612–847) so với 1083 (KTC 95%: 740–1565) (p-value = 0,04) và DHL 273 (KTC 95%: 244–289) so với 355 (95% CI: 270,6–422; p-value = 0,01). Chuyển đến phòng chăm sóc đặc biệt và tỷ lệ tử vong sau khi bắt đầu dùng corticosteroid thấp hơn ở nhóm được dùng MTP (4,8% so với 14,4%) và (9,5% so với 17,1%), tương ứng. (Bảng 2). Thời gian hồi phục ngắn hơn ở những bệnh nhân được điều trị bằng MTP, 3 ngày (3–4) so với DXM 6 ngày (5–8) (pvalue <0,0001) (Hình 2). Tại thời điểm theo dõi 30 ngày, 88 bệnh nhân (tỷ lệ 92,6%) còn sống ở nhóm dùng MTP so với 58 bệnh nhân (tỷ lệ 63,1%) ở những người được dùng dexamethasone.
Phân tích hiệu suất thời gian hồi phục
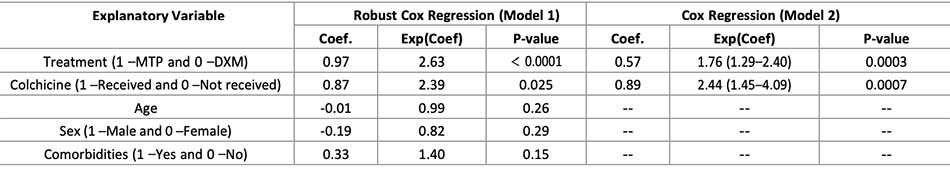
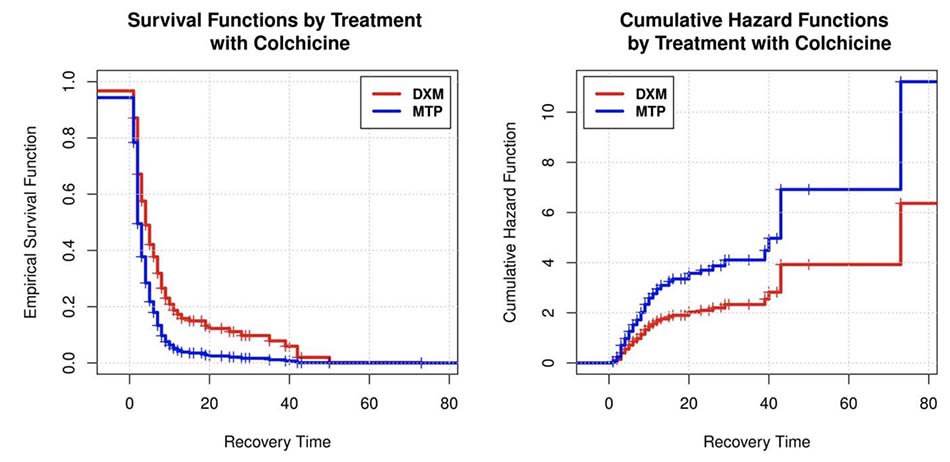
Thông qua mô hình nguy cơ tỷ lệ, tác động của các biến lên hàm tỷ lệ rủi ro của biến phản ứng ‘Thời gian phục hồi’. Từ mô hình Cox mạnh mẽ đã được chứng minh, chỉ có các biến ‘Điều trị’ và ‘Colchicine’ là có ý nghĩa trong việc lập mô hình tỷ lệ nguy hiểm hàm số. Hồi quy Cox thứ hai được thực hiện với các biến có ý nghĩa của mô hình đầu tiên để mô hình hóa tỷ lệ rủi ro, cũng quan sát mức độ ý nghĩa của nó (Bảng 3). Trong nghiên cứu này, hàm sống sót Ŝ cho biết xác suất ước tính mà một bệnh nhân cần thêm ngày để hồi phục và hàm tỷ lệ rủi ro ̂ ( ) cường độ xác suất mà một bệnh nhân đang hồi phục tại thời điểm t + Δ, tại thời điểm t nó vẫn chưa phục hồi, với Δ> 0. Đối với biến ‘Điều trị’, hệ số hồi quy ước tính là +0,57 chỉ ra rằng việc điều trị bằng methylprednisolone có tác động tích cực với giá trị 1,76 (1,29–2,40) trong hàm tỷ lệ rủi ro ̂ ( ), nghĩa là, bệnh nhân dùng methylprednisolone có cơ hội phục hồi tức thì từ Covid-19 cao hơn so với những bệnh nhân được dùng DXM (Bảng 3A). Những bệnh nhân được sử dụng MTP có nguy cơ tích lũy cao hơn về việc hồi phục trong thời gian t + Δ vì tại thời điểm t vẫn chưa hồi phục (Bảng 3B). Điều tương tự cũng xảy ra với biến ‗Colchicine‘; đối với điều này, hệ số hồi quy ước tính là +0,89 đã thu được, cho thấy rằng việc áp dụng Colchicine có tác động tích cực với giá trị 2,44 (1,45–4,09) trong hàm tỷ lệ nguy cơ ̂ ( ), tức là những bệnh nhân được dùng Colchicine có cơ hội phục hồi tức thì từ Covid-19 cao hơn so với những người không dùng (Bảng 4A).
Những bệnh nhân được bổ sung Colchicine vào corticosteroid có nguy cơ hồi phục tích lũy cao hơn trong thời gian t + Δ cho rằng tại thời điểm t họ vẫn chưa hồi phục (Bảng 4B).
Bảng 1: Đặc điểm lâm sàng và xã hội học của bệnh nhân nhập viện vì viêm phổi do Covid-19, phân theo nhóm điều trị https://doi.org/10.1371/journal.pone.0252057.t001.
Thảo luận
Cho đến nay, không có loại thuốc nào cho thấy hiệu quả chống lại SARS-COV2. Remdesivir, mặc dù đã được Cơ quan Quản lý Thực phẩm và Dược phẩm (FDA) ở Hoa Kỳ chấp thuận như một chất kháng vi-rút đối với SARS-COV2, đã bị nghi ngờ do tác dụng lâm sàng hạn chế của nó [17], trọng tâm hiện tại là hướng đến các biến chứng liên quan đến Covid-19: ARDS và Hội chứng giải phóng Cytokine, cả hai đều có đặc trưng ở sự gia tăng yếu tố hoại tử khối u-alpha (TNF alpha), interleukin (IL) 1B, IL-2 IL-6, IL-8, IL-10 và interferon y (IFN y) [18] tạo ra phản ứng rối loạn điều hòa đáp ứng viêm tự thân, tổn thương mô đích nặng nề và hiện tượng viêm toàn thân, và thậm chí là tử vong. Do đó, corticosteroid đã được sử dụng, đây là loại thuốc có tác dụng kháng viêm mạnh [19]. Theo bối cảnh lịch sử, trong trận dịch SARS ở Quảng Châu, Trung Quốc, xảy ra vào năm 2003, bệnh nhiễm khuẩn có liên quan đến hình ảnh lâm sàng tương tự như dịch bệnh Covid-19, Zhao và cộng sự. [20], Khi so sánh bốn phương pháp điều trị cho bệnh nhân viêm phổi do SARS-CoV, bao gồm các loại thuốc kháng sinh, thuốc kháng vi-rút khác nhau, và trong một số trường hợp, corticosteroid được sử dụng với các liều lượng khác nhau. Chỉ những bệnh nhân dùng methylprednisolon liều cao 160-1000mg mỗi ngày trong vòng 5-14 ngày thì không cần thở máy, không gây tử vong.
Bảng 2: Kết quả lâm sàng của bệnh nhân viêm phổi do Covid-19 nhập viện, theo nhóm điều trị. https://doi.org/10.1371/journal.pone.0252057.t002
Thời gian bắt đầu đại dịch Covid-19, việc sử dụng corticosteroid còn gây tranh cãi [21]. Tuy nhiên, các bằng chứng gần đây đã thay đổi việc quản lý ARDS thứ phát do nguyên nhân khác tại ICU. Villar và cộng sự. [22], trong một nghiên cứu kiểm soát giả dược, ngẫu nhiên và đa trung tâm, người ta đã phát hiện ra rằng bệnh nhân ARDS được điều trị bằng dexamethasone có tỷ lệ tử vong thấp hơn (21% so với 36%, giá trị p <0,0047). Wu và cộng sự [23], đã mô tả một nhóm bệnh nhân mắc ARDS thứ phát do Covid-19, được điều trị bằng methylprednisolone, có nguy cơ tử vong thấp hơn (HR, 0,38; KTC 95%, 0,20–0,72).
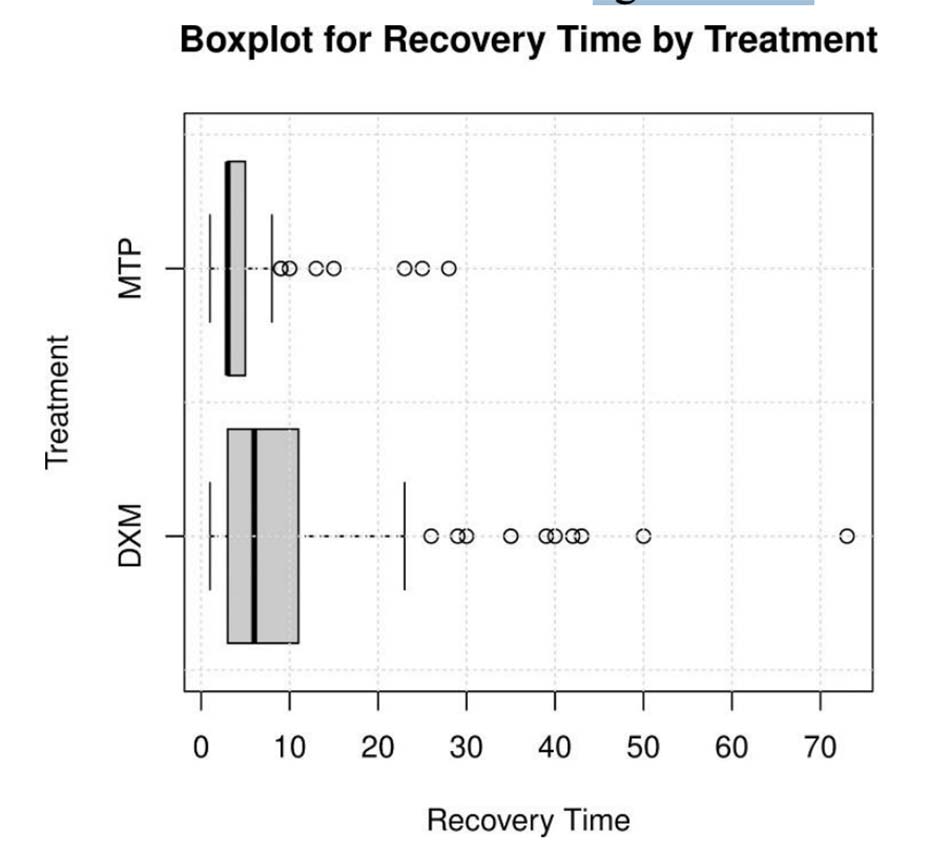
https://doi.org/10.1371/journal.pone.0252057.g002
Gần đây, kết quả PHỤC HỒI đã sửa đổi hướng dẫn điều trị [9]. Trong nghiên cứu này, những bệnh nhân được sử dụng dexamethasone đã giảm tỷ lệ tử vong ở một phần ba bệnh nhân thở máy và một phần năm ở những bệnh nhân khác chỉ được thở oxy. Tuy nhiên, sự khác biệt về tỷ lệ tử vong của tất cả bệnh nhân là 22,9% ở những người dùng dexamethasone 6mg so với 25,7% ở những người không dùng. Ở bệnh nhân Covid-19, tỷ lệ tử vong cao có thể được giải thích là do sự phát triển nhanh chóng của viêm phổi thứ phát sau SARSCoV2, vì sự xuất hiện của nó ngay cả trong tuần đầu tiên lây nhiễm đã được ghi nhận trong khám nghiệm tử thi. Bệnh lý này thường cần điều trị bằng corticosteroid liều cao, được một số người gọi là liều “xung” với thời gian dài hơn. Do đó, liều được đề xuất bởi PHỤC HỒI có thể không đủ cho một tỷ lệ cao bệnh nhân [24] Yang và cộng sự. [25], đánh giá 175 bệnh nhân bị Covid-19 nghiêm trọng, ghi nhận trong phân tích đa biến số như một yếu tố bảo vệ chống lại sự tiến triển thành bệnh hiểm nghèo khi sử dụng methylprednisolone (giá trị p <0,001; OR: 0,054 KTC 95%: 0,017 – 0.173.
Bảng 3: Phân tích hiệu suất thời gian khôi phục — Mô hình Cox. https://doi.org/10.1371/journal.pone.0252057.t003
Edalatifard và cộng sự. [26], Trong một thử nghiệm lâm sàng nhỏ, chọn ngẫu nhiên 34 bệnh nhân bị viêm phổi do Covid-19 nhận methylprednisolone 250 mg mỗi ngày trong ba ngày so với 34 bệnh nhân được chăm sóc tiêu chuẩn. Bệnh nhân có cải thiện lâm sàng cao hơn trong nhóm được sử dụng methylprednisolone so với nhóm chăm sóc tiêu chuẩn (94,1% so với 57,1%), và tỷ lệ tử vong thấp hơn ở nhóm có dùng methylprednisolone (5,9% so với 42,9%; p value <0,001). Ruiz-Irastorza và cộng sự. [27], Trong một nghiên cứu quan sát so sánh về bệnh nhân mắc viêm phổi do Covid -19, so với những bệnh nhân được dùng MTP vào tuần thứ 2 (125–250 mg/ ngày trong ba ngày) với những người không được sử dụng. Sự điều chỉnh tỷ số rủi ro liên quan đến tử vong hoặc đặt nội khí quản cho bệnh nhân trong nhóm được cho thuốc MTP vào tuần thứ 2 lần lượt là 0,35 (95% CI 0,11 đến 1,06, p-value = 0,064) tương ứng với 0,33 (95% CI 0,13-084, pvalue = 0,020).
Nghiên cứu này đánh giá sự khác biệt giữa kết quả lâm sàng và xét nghiệm ở bệnh nhân được điều trị bằng dexamethasone hoặc methylprednisolone liều cao. Chúng tôi cho thấy tỷ lệ tử vong thấp hơn ở nhóm methylprednisolone và thời gian phục hồi của bệnh nhân ngắn hơn, một phát hiện đã không được báo cáo cho đến nay. Lời giải thích dường như tương ứng với hiệu ứng phụ thuộc vào liều lượng của corticosteroid, quan sát thấy sự giảm đáng kể hơn trong phản ứng viêm ở nhóm bệnh nhân này hơn dexamethasone, giảm CRP, LDH và Ddimer. Các phòng thí nghiệm này, đã được đề xuất như là điểm đánh dấu mức độ nghiêm trọng trong Covid-19, không có sẵn tại thời điểm ban đầu hoặc theo dõi như một phản ứng sau khi điều trị trong nghiên cứu PHỤC HỒI. Mặc dù dùng corticosteroid liều cao, không có nguy cơ bội nhiễm tăng lên, có thể do thời gian dùng thuốc ngắn. Hai trường hợp nhiễm trùng trên (1,9%) so với DXM 4 (3,7%) xảy ra ở nhóm MTP, tương ứng trong tất cả các trường hợp là viêm phổi liên quan đến máy thở. Tăng đường huyết được quan sát thấy ở một số bệnh nhân đái tháo đường trong cả hai nhóm điều trị. Tỷ lệ bệnh nhân trong nhóm dung MTP liều cao tiến triển thành ARDS nặng và chuyển đến đơn vị chăm sóc đặc biệt sau khi bắt đầu dùng corticosteroid thấp hơn hơn nhóm nhận được DXM, điều liên quan đến tình trạng diễn tiến lâm sàng nặng hơn hoặc tiến triển đến nguy kịch. Tương tự như vậy, thời gian phục hồi ngắn hơn ở những bệnh nhân được điều trị bằng MTP, có ý nghĩa quan trọng hơn trong đại dịch Covid-19 hiện tại, là nó có thể giúp xuất viện sớm hơn và do đó tránh được sự quá tải của hệ thống bệnh viện. Quy trình y tế được trình bày bao gồm việc sử dụng colchicine 0,5mg mỗi 12 giờ, cho đến 14 ngày kể từ ngày 1 tháng 7 năm 2020. Để tránh sai lệch trong kết quả hoạt động của corticosteroid, mục tiêu chính của chúng tôi, chúng tôi đánh giá việc sử dụng colchicine như một phát hiện phụ trong nghiên cứu. Việc sử dụng colchicine được hỗ trợ bởi các nghiên cứu khác gần đây. Trong nghiên cứu lâm sàng ngẫu nhiên GRECCO [28], việc sử dụng colchicine làm giảm thời gian kết thúc ưu tiên dẫn đến tình trạng xấu đi trên lâm sàng ở 1,8% (1 trong số 55 bệnh nhân) so với 14,0% ở nhóm đối chứng (7 trên 50 bệnh nhân), với giá trị tỷ lệ chênh lệch 0,11, KTC 95% (0,01–0,96) và giá trị p có ý nghĩa = 0,02. Hơn nữa, với Scarsi và cộng sự, [29], colchicine được thử nghiệm trên bệnh nhân viêm phổi do Covid-19 và ARDS, nơi nó cho thấy tỷ lệ sống sót tốt hơn so với chăm sóc tiêu chuẩn ở 21 ngày theo dõi (84,2% so với 63,6 %, giá trị p = 0,001). Là điểm mạnh chính trong nghiên cứu của chúng tôi, tất cả bệnh nhân nhập viện trong thời kỳ thành lập được điều trị như nhau, không có lựa chọn hoặc quản lý bệnh nhân theo tiêu chí của bác sĩ điều trị, điều này cho phép so sánh giữa các nhóm bệnh nhân một cách hiệu quả. Một điểm mạnh khác là tập trung vào việc xử trí bệnh nhân nhập viện tại các khu bệnh viện đa khoa, nơi các nghiên cứu khác không cho thấy bất kỳ tác dụng nào của thuốc. Tuy nhiên, đây cũng là hạn chế chính của nó vì tác dụng của nó trong phòng chăm sóc đặc biệt không được đánh giá. Mặc dù một trung tâm duy nhất là một hạn chế, nhưng sẽ rất hữu ích khi so sánh trực tiếp giữa các nhóm bằng cách không sửa đổi các điều kiện về nguồn lực bệnh viện hoặc nhân viên bệnh viện. Thiết kế quan sát, quy mô dân số nhỏ và tính chất trung tâm đơn lẻ của nghiên cứu hạn chế khả năng khái quát của các phát hiện.
Kết luận
Trong nghiên cứu này, việc điều trị Viêm phổi do Covid-19 nặng bằng methylprednisolone liều cao trong ba ngày, sau đó là prednisone đường uống trong 14 ngày giảm đáng kể, so với dexamethasone 6 mg trong 7 đến 10 ngày, thời gian hồi phục, nhu cầu chuyển đến chăm sóc đặc biệt, và đánh dấu mức độ nghiêm trọng Protein phản ứng C (CRP), D-dimer và LDH. Các nghiên cứu ngẫu nhiên có đối chứng với dexamethasone được yêu cầu để chứng thực tác dụng của nó, và các nghiên cứu trên quần thể nhập viện tại các khu chăm sóc đặc biệt.
Thông tin hỗ trợ
S1 Dataset (XLSX)
Lời cám ơn
Các tác giả xin cám ơn hai vị tư vấn ẩn danh vì những ý kiến đóng góp quan trọng giúp cải thiện phiên bản cuối cùng của bản thảo này.
Sự đóng góp của tác giả
Khái niệm hóa: Miguel Alejandro Pinzón, Santiago Ortiz, Héctor Holguín, Juan Felipe Betancur, Doris Cardona Arango, Henry Laniado, Carolina Arias Arias, Bernardo Muñoz, Julián Quiceno, Daniel Jaramillo, Zoraida Ramirez. Quản lý dữ liệu: Miguel Alejandro Pinzón, Santiago Ortiz, Juan Felipe Betancur, Doris Cardona Arango, Henry Laniado, Carolina Arias Arias, Daniel Jaramillo.
Phân tích: Miguel Alejandro Pinzón, Santiago Ortiz, Héctor Holguín, Doris Cardona Arango, Henry Laniado, Carolina Arias Arias, Daniel Jaramillo.
Điều tra: Miguel Alejandro Pinzón, Santiago Ortiz, Héctor Holguín, Juan Felipe Betancur, Doris Cardona Arango, Henry Laniado, Carolina Arias Arias, Bernardo Muñoz, Julián Quiceno.
Phương pháp luận: Miguel Alejandro Pinzón, Santiago Ortiz, Héctor Holguín, Juan Felipe Betancur, Doris Cardona Arango, Henry Laniado, Carolina Arias Arias, Bernardo Muñoz, Daniel Jaramillo, Zoraida Ramirez.
Quản lý dự án: Miguel Alejandro Pinzón, Santiago Ortiz, Héctor Holguín, Carolina Arias Arias, Bernardo Muñoz.
Phần mềm: Santiago Ortiz. Giám sát: Miguel Alejandro Pinzón, Santiago Ortiz, Juan Felipe Betancur, Doris Cardona Arango, Henry Laniado, Carolina Arias Arias, Bernardo Muñoz, Julia´n Quiceno, Daniel Jaramillo.
Thẩm định: Miguel Alejandro Pinzón, Santiago Ortiz. Trình bày: Santiago Ortiz. Lên bản nháp: Miguel Alejandro Pinzón, Héctor Holguín, Juan Felipe Betancur, Doris Cardona Arango, Bernardo Muñoz, Julia´n Quiceno, Daniel Jaramillo, Zoraida Ramirez.
Viết – đánh giá & biên tập: Miguel Alejandro Pinzón, Santiago Ortiz, Héctor Holguín, Juan Felipe Betancur, Doris Cardona Arango, Henry Laniado, Carolina Arias Arias, Julián Qui ceno, Zoraida Ramirez.
Tài liệu tham khảo
1. Zhu Na, Zhang Dingyu, Wang Wenling, Li Xingwang, Yang Bo, Song Jingdong, et al. A Novel Coronavi- rus from Patients with Pneumonia in China, 2019. N Engl J Med. 2020 Feb 20; 382(8):727–733. Epub2020 Jan 24. https://doi.org/10.1056/NEJMoa2001017 PMID: 31978945.
2. Coronavirus Update (Live): 30,157,437 Cases and 947,034 Deaths from COVID-19 Virus Pandemic—Worldometer [Internet]. Worldometers.info. 2020 [cited 10 november 2020]. Available from: https:// www.worldometers.info/coronavirus/?zarsrc=130.
3. Mahase E. Coronavirus COVID-19 has killed more people than SARS and MERS combined, despite lower case fatality rate. BMJ. 2020 Feb 18; 368:m641. https://doi.org/10.1136/bmj.m641 PMID: 32071063
4. Yao X, Ye F, Zhang M, et al. In Vitro Antiviral Activity and Projection of Optimized Dosing Design of Hydroxychloroquine for the Treatment of Severe Acute Respiratory Syndrome Coronavirus 2 (SARS- CoV-2). Clin Infect Dis. 2020 Mar 9. pii: ciaa237. https://doi.org/10.1093/cid/ciaa237
5. Yao TT, Qian JD, Zhu WY, Wang Y, Wang GQ. A systematic review of lopinavir therapy for SARS coro-navirus and MERS coronavirus-A possible reference for coronavirus disease-19 treatment option. J Med Virol. 2020 Feb 27. https://doi.org/10.1002/jmv.25729 PMID: 32104907
6. Gautret Philippe, Lagier Jean-Christophe, Parola Philippe et al. Hydroxychloroquine and azithromycin as a treatment of COVID-19: results of an open-label non-randomized clinical trial. Int J Antimicrob Agents. 2020 Jul; 56(1):105949. https://doi.org/10.1016/j.ijantimicag.2020.105949 PMID: 32205204
7. Caly Leon, Druce Julian D, Catton Mike G, Jans David A, Wagstaff Kylie M. The FDA-approved drug ivermectin inhibits the replication of SARS-CoV-2 in vitro. Antiviral Res. 2020 Jun; 178:104787. Epub 2020 Apr 3. https://doi.org/10.1016/j.antiviral.2020.104787 PMID: 32251768
8. Arshad S., Kilgore P., Chaudhry Z.S., Jacobsen G., Wang D.D. & Huitsing K. (2020). ―Treatment withhydroxychloroquine, azithromycin, and combination in patients hospitalized with COVID-19‖. Interna-tional Journal of Infect Dis. 97, 396–403
9. RECOVERY Collaborative Group, Horby P, Lim WS, Emberson JR, Mafham M, Bell JL, et al Dexa- methasone in Hospitalized Patients with Covid-19—Preliminary Report. N Engl J Med. 2020 Jul 17:NEJMoa2021436. https://doi.org/10.1056/NEJMoa2021436
10. Fan Eddy, Beitler Jeremy R, Brochard Laurent, Calfee Carolyn S, Ferguson Niall D, Slutsky Arthur S, et al. COVID-19-associated acute respiratory distress syndrome: is a different approach to management warranted?. Lancet Respir Med. 2020 Aug; 8(8):816–821. Epub 2020 Jul 6. https://doi.org/10. 1016/S2213-2600(20)30304-0 PMID: 32645311
11. Mehta Puja, McAuley Daniel F, Brown Michael, Sanchez Emilie, Tattersall Rachel S, et al. COVID19: consider cytokine storm syndromes and immunosuppression Lancet. 2020 28 March-3 April; 395 (10229): 1033–1034. Published online 2020 Mar 16. https://doi.org/10.1016/S0140-6736(20)30628- 0 PMID: 32192578
12. Cox D. R. (1972), Regression Models and Life-Tables. Journal of the Royal Statistical Society: Series B (Methodological), 34, 187–202.
13. Minder C. E. and Bednarski T. (1996). A Robust Method for Proportional Hazards. Regression. Statis- tics in Medicine, 15, 1033–1047. https://doi.org/10.1002/(SICI)1097- 0258(19960530)15:10<1033:: AID-SIM215>3.0.CO;2-Y PMID: 8783440
14. R Core Team (2020), R: A Language and Environment for Statistical Computing. R Foundation for Statistical Computing, Vienna, Austria.
15. Bednarski, T. and Borowicz, F. (2006), coxrobust: Robust Estimation in Cox Model.
16. Therneau, T. (2020), A Package for Survival Analysis in R.
17. Wang Y, Zhang D, Du G, Du R, Zhao J, Jin Y, et al. Remdesivir in adults with severe COVID-19: a ran- domised, double-blind, placebo-controlled, multicentre trial. Lancet. 2020 May 16; 395(10236):1569–1578. Epub 2020 Apr 29. https://doi.org/10.1016/S0140-6736(20)31022-9 PMID: 32423584
18. Ragab Dina, Eldin Haitham Salah, Taeimah Mohamed, Khattab Rasha, Salem Ramy. The COVID-19 Cytokine Storm; What We Know So Far. Front. Immunol., 16 June 2020 | https://doi.org/10.3389/ fimmu.2020.01446
19. The WHO Rapid Evidence Appraisal for COVID-19 Therapies (REACT) Working Group. Association Between Administration of Systemic Corticosteroids and Mortality Among Critically Ill Patients With COVID-19 A Meta-analysis JAMA. 2020; 324(13):1330–1341. Published online September 2, 2020. https://doi.org/10.1001/jama.2020.17023 PMID: 32876694
20. Zhao F. Zhang M. Xu K. Huang W. Zhong W. Cai Z. et al. Description and clinical treatment of an early outbreak of severe acute respiratory syndrome (SARS) in Guangzhou, PR China Z. Journal of Medical Microbiology (2003), 52, 715–720 https://doi.org/10.1099/jmm.0.05320-0 PMID: 12867568
21. Russell CD, Millar JE, Baillie JK. Clinical evidence does not support corticosteroid treatment for 2019- nCoV lung injury. Lancet. 2020 Feb 15; 395(10223):473–475. https://doi.org/10.1016/S0140- 6736(20)30317-2 PMID: 32043983
22. Jesu´s Villar, Carlos Ferrando, Domingo Mart´ınez, et al. Dexamethasone Treatment for the Acute Respi- ratory Distress Syndrome: A Multicentre, Randomised Controlled Trial. Lancet Respir Med. 2020 Mar; 8(3):267–276. https://doi.org/10.1016/S2213-2600(19)30417-5 PMID: 32043986
23. Chaomin Wu, Xiaoyan Chen, Yanping Cai, et al. Risk Factors Associated With Acute Respiratory Dis- tress Syndrome and Death in Patients With Coronavirus Disease 2019 Pneumonia in Wuhan, China. JAMA Intern Med. 2020 Jul 1; 180(7):934–943. https://doi.org/10.1001/jamainternmed.2020.0994 PMID: 32167524
24. Kory Pierre, Kanne Jeffrey P. SARS-CoV-2 organising pneumonia: ‗Has there been a widespread fail- ure to identify and treat this prevalent condition in COVID-19?. BMJ Open Respir Res. 2020; 7(1): e000724. Published online 2020 Sep 22. https://doi.org/10.1136/bmjresp-2020-000724 PMID: 32963028
25. Yang R, Xiong Y, Ke H, Chen T, Gao S. The role of methylprednisolone on preventing disease progres-sion for hospitalized patients with severe COVID-19. Eur J Clin Invest. 2020 Nov; 50(11): e13412. Epub 2020 Oct 2. https://doi.org/10.1111/eci.13412 PMID: 32954492
26. Edalatifard M, Akhtari M, Salehi M, Naderi Z, Jamshidi A, Mostafaei S, et al. Intravenous methylprednis- olone pulse as treatment for hospitalized severe COVID-19 patients: results from a randomised con- trolled clinical trial. Eur Respir J. 2020 Sep 17:2002808. Online ahead of print. https://doi.org/10.1183/ 13993003.02808-2020 PMID: 32943404
27. Guillermo Ruiz-Irastorza Jose-Ignacio Pijoan, Bereciartua Elena, Dunder Susanna, Dominguez Jokin, et al. Second week methyl-prednisolone pulses improve prognosis in patients with severe coronavirus disease 2019 pneumonia: An observational comparative study using routine care data. PLoS One. 2020; 15(9): e0239401. Published online 2020 Sep 22. https://doi.org/10.1371/journal.pone.0239401PMID: 32960899
28. Deftereos S, Giannopoulos G, Vrachatis D, Gerasimos Siasos, Giotaki S, Gargalianos P. Effect of Col- chicine vs Standard Care on Cardiac and Inflammatory Biomarkers and Clinical Outcomes in Patients Hospitalized With Coronavirus Disease 2019: The GRECCO-19 Randomized Clinical Trial. JAMA NetwOpen. 2020 Jun 1; 3(6):e2013136. https://doi.org/10.1001/jamanetworkopen.2020.13136 PMID: 32579195
29. Scarsi M, Piantoni S, Colombo E, Airo´ P, Richini D, Miclini M, et al. Association between treatment with colchicine and improved survival in a single-centre cohort of adult hospitalised patients with COVID-19 pneumonia and acute respiratory distress syndrome. Ann Rheum Dis. 2020 Oct; 79(10):1286–1289. Epub 2020 Jul 30. https://doi.org/10.1136/annrheumdis-2020-217712 PMID: 32732245; PMCID: PMC7509521.