Thẩm mỹ - Làm đẹp
Chất làm đầy nâng da mặt gồm những loại nào? Quy trình sản xuất?
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
Tác giả: Kyle K. Seo
nhathuocngocanh.com – Bài viết Chất làm đầy nâng da mặt gồm những loại nào? Quy trình sản xuất? được trích trong chương 2 trong sách Căng Da Mặt Với Chất Làm Đầy.
Các loại chất làm đầy dạng tiêm
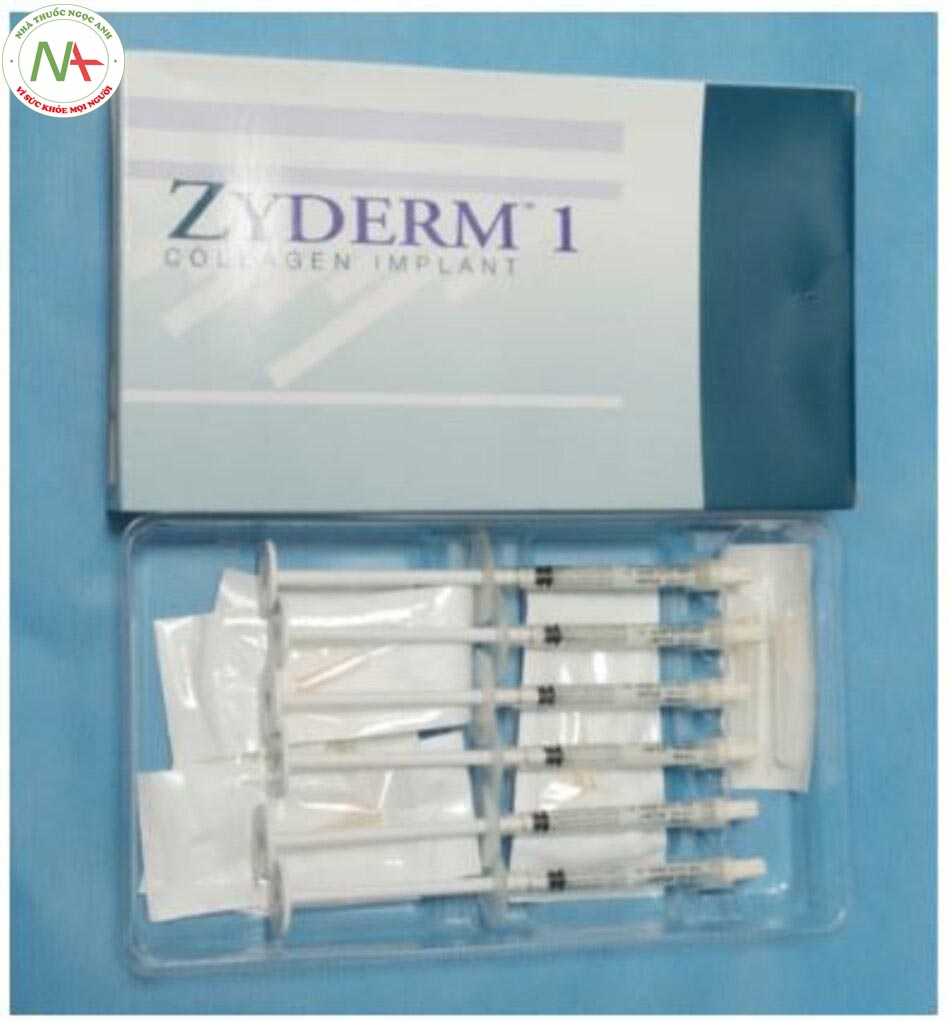
Theo định nghĩa, chất làm đầy dùng để chỉ tất cả các chất được tiêm vào để mang lại hiệu quả lấp đầy ở những khu vực thiếu hụt thể tích. Trong các quy trình thẩm mỹ khuôn mặt, chúng bao gồm các chất được đặt vào mặt để làm căng các nếp nhăn sâu hoặc để phục hồi các khu vực lõm trên khuôn mặt. Theo nghĩa này, chất làm đầy có thể hiểu rộng hơn là bao gồm mỡ tự thân được sử dụng trong các quy trình ghép mỡ hoặc, bao gồm cả parafin hoặc silicon trước đây được sử dụng rộng rãi trong các phương pháp điều trị thẩm mỹ bất hợp pháp. Điều đó cho thấy, chất làm đầy đầu tiên được công nhận là một thiết bị y tế hợp pháp dựa trên collagen – một thành phần cấu trúc của da. Vào đầu những năm 1980, ZYDERM® có nguồn gốc từ bò (Allergan. Hoa Kỳ) được giới thiệu trên thị trường, được coi là chất làm đầy tiêm hiện đại đầu tiên được FDA Hoa Kỳ chấp thuận (Hình 2.1). Tuy nhiên, do nguồn gốc động vật của chúng, việc sử dụng chất làm đầy collagen bò bị hạn chế bởi nguy cơ phản ứng sinh miễn dịch vốn có và thời gian tác dụng ngắn của chúng. Theo đó, với sự ra đời sau đó và sự thống trị của chất làm đầy HA, chất làm đầy collagen bò nhanh chóng không còn được ưa chuộng trên toàn cầu.
Ngày nay, chất làm đầy dạng tiêm vẫn thường được gọi là “chất làm đầy qua da”, có thể do chất làm đầy đầu tiên được sử dụng là dựa trên collagen. Hiển nhiên là, collagen là một phần thiết yếu của cấu trúc da và thực sự chất làm đầy collagen ban đầu được tiêm trực tiếp vào lớp hạ bì để cải thiện độ đàn hồi và nếp nhăn của da. Tuy nhiên, việc sử dụng chất làm đầy dạng tiêm kể từ đó đã phát triển đáng kể và ngày nay chúng được sử dụng không chỉ đơn giản để tinh chỉnh các nếp nhăn mà còn được sử dụng trong một loạt các quy trình thẩm mỹ mới và xâm lấn tối thiểu để tận dụng tối đa hiệu quả của chất làm đầy dạng tiêm (Hình 2.2) [1]. Ví dụ như nâng cao chiếc mũi tẹt hoặc làm đầy đôi môi mỏng, hoặc thậm chí định hình lại đường nét trên khuôn mặt. Hơn nữa, trong khi thuật ngữ “chất làm đầy da” ngụ ý chúng được tiêm vào lớp hạ bì, độ sâu tiêm cần thiết cho các quy trình nâng da này sâu hơn nhiều, nghĩa là ở sâu dưới da hoặc thậm chí xuống mặt phẳng trên xương. Theo cơ sở này, có thể công bằng khi cho rằng thuật ngữ “chất làm đầy da” đã trở thành một từ nhầm lẫn, và đã đến lúc từ “da” nên được loại bỏ.
Sau chất làm đầy collagen, HA đã chiếm lĩnh thị trường tiêm chất làm đầy trên thế giới. Các ưu điểm chính dẫn đến thành công của nó là tính an toàn tuyệt vời của nó bao gồm các thành phần giống nhau tạo nên lớp hạ bì, gây ra các phản ứng sinh miễn dịch tối thiểu trong cơ thể và khả năng phục hồi độc nhất của nó, theo đó kết quả không mong muốn có thể bị loại bỏ bằng cách sử dụng cách thức loại bỏ chất làm đầy trở lại trạng thái ban đầu. Ngoài độ an toàn đặc biệt, chất làm đầy HA cũng đã được chứng minh là có thời gian tác dụng tuyệt vời. Mặc dù ban đầu các chất làm đầy HA được cho là tồn tại trong khoảng từ 6 tháng đến 1 năm trong mô khi lần đầu tiên được giới thiệu vào đầu những năm 2000, nhưng hiện nay người ta đã chấp nhận rộng rãi rằng thời gian tác dụng của chúng có thể kéo dài đến vài năm nếu được tiêm nhanh hoặc duy trì liên tục. Điều này là do khi tiêm chất làm đầy HA dưới dạng tiêm nhanh, nó tối thiểu diện tích bề mặt của chất làm đầy HA tiếp xúc với hyaluro-nidase của cơ thể, ức chế sự phân hủy của enzym. Đáng chú ý, chất làm đầy HA được tiêm ở trán, sống mũi và vùng bọng mắt có thời gian tác dụng kéo dài từ 5–10 năm.
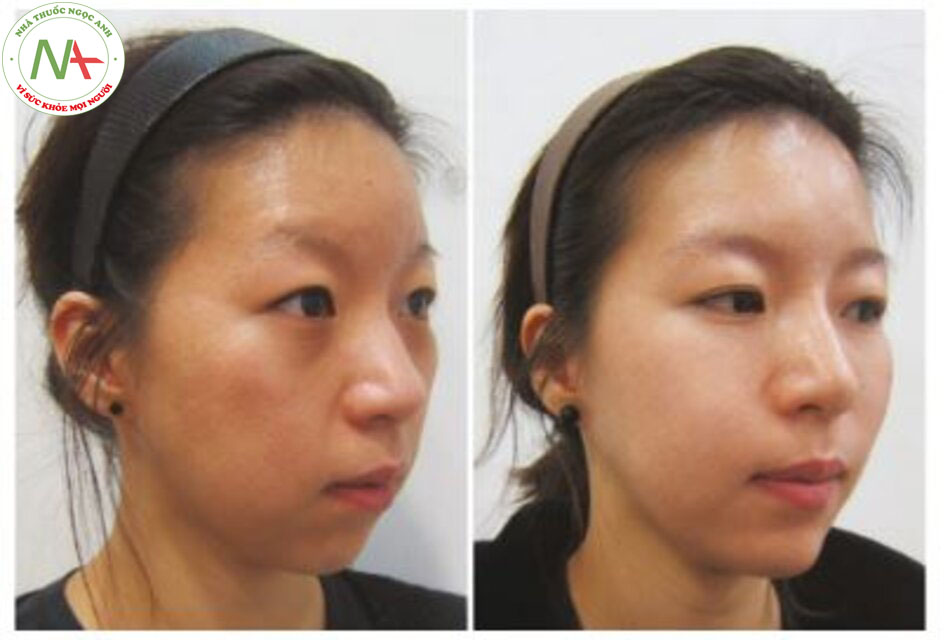

Chất làm đầy HA đầu tiên được tung ra thị trường là Hylaform® (gel Hylan B) (Genzyme Biosurgery) chiết xuất từ mào gà trống, sản phẩm này đã bị ngừng sử dụng do các vấn đề liên quan đến tạp chất protein từ nguồn gia cầm. Sau đó, chất làm đầy HA đã được được sản xuất bằng cách sử dụng HA tinh chế từ các nguồn vi khu-ẩn như liên cầu khuẩn, cho đến ngày nay vẫn là sản phẩm chiếm ưu thế nhất trên thị trường.
Trong khi chất làm đầy dựa trên colla-gen hoặc HA được thiết kế chủ yếu để thay thế và phục hồi thể tích bị mất (“chất làm đầy thay thế”), chất làm đầy kích thích col-lagen, còn được gọi là chất làm đầy kích thích sinh học, bao gồm các polyme phân hủy sinh học tạo ra sự kích thích sinh học collagen trong vùng được tiêm trong khi chúng tự từ từ suy thoái trong cơ thể. Ví dụ điển hình về các chất làm đầy kích thích collagen này bao gồm Radiesse® cho canxi hydroxylapatite (CaHA) và Sculptra® cho axit poly-l-lactic (PLLA) (xem Phần 2.4.3). Nhìn chung, những chất làm đầy kích thích collagen này được biết là có thời gian tác dụng dài hơn so với chất làm đầy HA. Tuy nhiên, hạn chế đối với các chất làm đầy này là chúng không cho phép tùy chỉnh thể tích theo yêu cầu, vì kết quả có thể tùy thuộc vào sự thay đổi của từng cá nhân trong quá trình sản xuất collagen; và phải mất 4-12 tuần để collagen mới hình thành trong khi lượng bổ sung ban đầu từ chất mang, có thể là CMC (carboxymethylcellulose) hoặc nước muối, sẽ tiêu biến ngay sau khi điều trị. Hơn nữa, kết quả của chất làm đầy kích thích collagen khó có thể đảo ngược trong trường hợp có bất kỳ nốt sần hoặc bất thường nào phát sinh do vị trí sản phẩm không đồng đều.
Trong khi đó, các sản phẩm như PAAG (polyacrylamide gel) dựa trên Aquamid® hoặc PMMA (polymethyl methacrylate) dựa trên Bellafill® được phát triển để cung cấp tuổi thọ kéo dài dựa trên việc sử dụng các chất tổng hợp vĩnh viễn (xem Phần 2.4.2). Tuy nhiên, liệu những chất làm đầy vĩnh viễn này có là một lựa chọn tốt hay không vẫn còn là câu hỏi được đặt ra, vì cấu trúc cơ mặt không phải là vĩnh viễn. Với quá trình lão hóa, khuôn mặt mất đi nét trẻ trung do sự chảy xệ và kết khối mô ngày càng tăng trên khuôn mặt, tình trạng này vẫn tiếp tục diễn ra mạnh mẽ sau khi tiêm các chất làm đầy vĩnh viễn này. Do đó, điều này có thể dẫn đến vẻ ngoài không hài hòa giữa vùng được tiêm và phần còn lại của khuôn mặt lão hóa. Hơn nữa, tính lâu dài của chất làm đầy cũng ngụ ý rằng dù áp dụng các giải pháp vĩnh viễn hoặc bán vĩnh viễn, các biến chứng tiềm ẩn phát sinh là vĩnh viễn, mà phẫu thuật cắt bỏ vẫn là lựa chọn duy nhất.
Chất làm đầy axit hyaluronic
Axit hyaluronic (“HA”) là loại chất làm đầy tiêm được sử dụng rộng rãi nhất trên thế giới, với khả năng tương thích sinh học tuyệt vời, tính sinh miễn dịch thấp và khả năng có thể loại bỏ giúp nó chiếm ưu thế hơn các loại chất làm đầy tiêm khác (Hình 2.3). Mặc dù các sản phẩm chất làm đầy HA được bán trên thị trường ít nhiều giống nhau về hình thức bên ngoài, nhưng vẫn có sự khác biệt nhỏ về nồng độ HA, kỹ thuật liên kết chéo, mức độ liên kết chéo, độ dẻo, độ cứng của gel, độ kết dính, v.v. giữa các sản phẩm trong cùng một nhãn hiệu chất làm đầy HA. Cần có kiến thức về các đặc tính đó để có thể tùy chỉnh việc sử dụng từng sản phẩm cho từng mục đích sử dụng.
Đặc tính của HA
Axit hyaluronic là một polymer trọng lượng phân tử cao bao gồm các disaccha-ride lặp lại lần đầu tiên được phát hiện vào năm 1934 bởi Karl Meyer và John Palmer trong dịch thủy tinh của mắt bò [2]. Axit hyaluronic được cho là có nguồn gốc từ hyaloid (có nghĩa là thủy tinh thể) và axit uronic, một thành phần của các đơn vị dis-sacharide lặp lại. Ở trạng thái tự nhiên, axit hyaluronic tồn tại ở dạng muối, chủ yếu là natri hyaluronat liên kết với natri (Na), một cation được tìm thấy rộng rãi nhất trong cơ thể con người. Năm 1986, thuật ngữ “hyaluronan” được thông qua theo danh pháp quốc tế của polysacchar-id [3]. Tương ứng, các thuật ngữ axit hyal-uronic, sodium hyaluronate và hyaluronan đều được sử dụng thay thế cho nhau để chỉ cùng một HA.
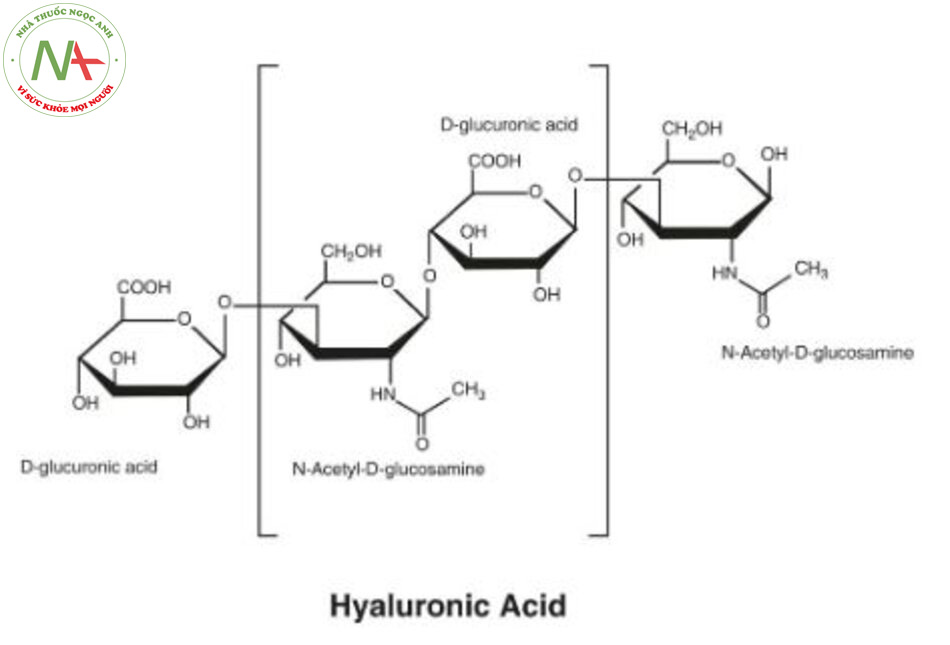
Axit hyaluronic tạo thành phân tử gly-cosaminoglycan (GAGs) bao gồm các chuỗi polysaccharide được tạo thành từ axit d-glucuronic xen kẽ và các đơn vị N-ace-tyl-d-glucosamine kết hợp với nhau theo cách lặp đi lặp lại (Hình 2.4) [2]. GAG được gọi chung là nhóm các polysaccharide dài, không phân nhánh chứa các axit amin được tạo thành từ các đơn vị disaccha-ride lặp lại. Đại diện cho một thành phần quan trọng của chất nền ngoại bào, GAGs được phân loại thành sáu lớp dựa trên cấu trúc mono-saccharide cơ bản, cụ thể là HA, chondroitin sulfate, keratin sulfate, der-matan sulfate, heparin, và heparin sulfate. Trong số các GAG, HA được tìm thấy nhiều nhất ở da [2]. Tuy nhiên, không giống như các lớp khác của GAG, nó không bị biến đổi với các nhóm sulfat và không liên kết cộng hóa trị với lõi protein.
Hơn nữa, nó là lớp GAG duy nhất có trong cả nguồn động vật và vi khuẩn. Là một phân tử rất ưa nước, HA cũng có khả năng giữ nước gấp 1000 lần trọng lượng phân tử của nó [2]. Trong dung dịch nước, sự phong phú của các điện tích âm trong cấu trúc hóa học của HA nói chung khiến các điện tích âm đẩy nhau. Điều này cho phép HA chiếm một không gian lớn hơn, vì toàn bộ mạng lưới phân tử mở rộng và được bao quanh bởi các phân tử nước. Ngoài ra, trong khi các phân tử HA giảm thể tích khi chịu sự gia tăng áp suất bên ngoài, chúng chủ yếu phục hồi thể tích ban đầu khi tác dụng ngoại lực, do lực đẩy lẫn nhau giữa các điện tích âm. Những đặc điểm này cho phép HA tồn tại ở dạng gel khi trộn với nước, thể hiện các đặc tính của cả độ nhớt và độ đàn hồi. Trong môi trường pH sinh lý bình thường, các nhóm cacboxyl (–COOH) bao gồm axit d-glucuronic của HA được chuyển thành muối natri. HA sở hữu bốn nhóm hydroxyl (–OH) và một nhóm muối natri trong mỗi đơn vị disaccharide [2]. Các nhóm hydroxyl của HA hình thành liên kết hydro với các phân tử nước và do đó dễ dàng hòa tan trong nước.
Mỗi đơn vị disaccharide của HA bao gồm axit d-glucuronic và N-acetyl-d-glu-cosamine đại diện cho một đơn phân có trọng lượng phân tử 400 Da, với mỗi đơn phân liên kết với nhau thông qua liên kết β-1,4 glycosidic để tạo thành polyme HA. Các polyme HA có trong dịch khớp của con người được biết là bao gồm 20.000 đơn phân hoặc khối lượng phân tử là bảy triệu Da. Là một thành phần chính của chất nền ngoại bào của cơ thể, HA có vai trò hấp thụ độ ẩm và giữ cho các mô được bôi trơn và ngậm nước trong khi cung cấp hỗ trợ cấu trúc cần thiết. Hơn nữa, nó cũng có vai trò điều chỉnh sự di chuyển và tăng sinh của tế bào, cũng như điều chỉnh việc kiểm soát viêm nhiễm và sửa chữa / tái tạo vết thương. Tổng hàm lượng HA ở một người trưởng thành nặng 70 kg được ước tính là khoảng 15 g [4], với khoảng một nửa lượng này được biết là nằm trong da. Axit hyal-uronic cũng được tìm thấy với nồng độ cao trong dịch khớp, sụn và thể thủy tinh của mắt. Cơ thể luôn duy trì cân bằng nội môi HA tối ưu, theo đó một phần ba HA của cơ thể được chuyển hóa, tức là bị phân hủy và được tổng hợp mỗi ngày [4]. Trong khi HA liên tục được bổ sung trong cơ thể con người, quá trình lão hóa làm giảm dần quá trình sản xuất HA tự nhiên, dẫn đến da mất độ ẩm và độ đàn hồi theo thời gian.
Không giống như collagen, cấu trúc phân tử của HA vẫn giống hệt nhau trên tất cả các loài động vật, với sự khác biệt duy nhất là chiều dài polyme. Các polyme HA có nguồn gốc từ các chủng vi khuẩn thường có chiều dài 4000–6000 đơn phân, ngắn hơn so với 10.000–15.000 được tìm thấy trong HA nguồn gốc động vật, và do đó có trọng lượng phân tử thấp hơn, 1,5–2,5 triệu Da [2].
Quy trình sản xuất chất làm đầy axit hyaluronic
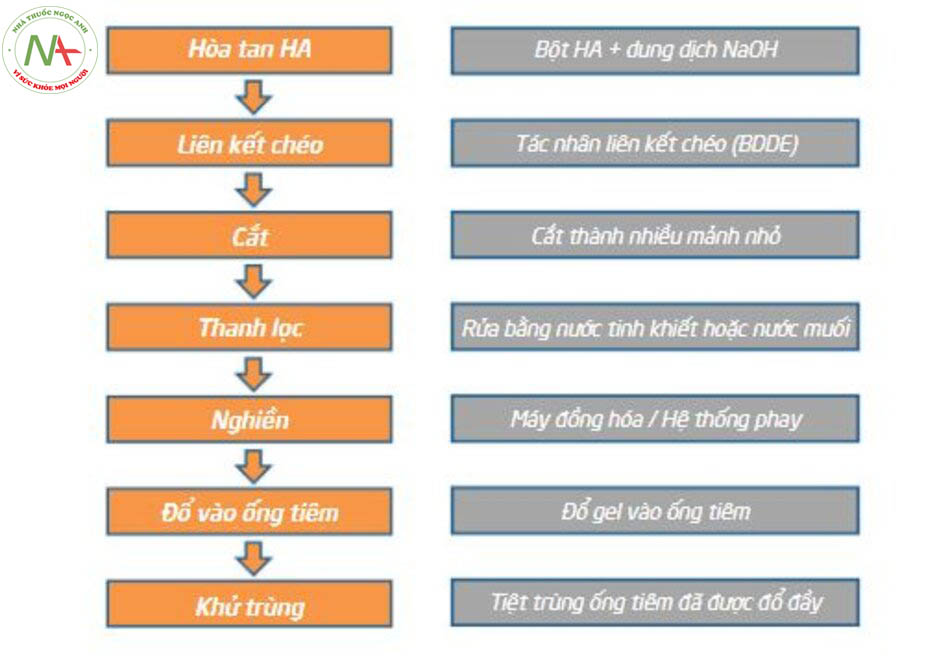
Nhìn chung, quy trình sản xuất chất làm đầy HA bao gồm các bước sau: hòa tan bột HA (nguyên liệu thô) trong dung dịch NaOH, bổ sung chất liên kết chéo, sau đó là phản ứng liên kết chéo, cắt, làm sạch, ng-hiền vụn, đổ Gel HA vào ống tiêm, và khử trùng (Hình 2.5).
Trong số các bước quy trình này, liên kết chéo của chuỗi polyme HA là giai đoạn sản xuất quan trọng nhất, vì nó cuối cùng xác định các đặc tính lưu biến của chất làm đầy HA đồng thời ổn định các phân tử HA để kéo dài tuổi thọ trong cơ thể sống. Sau khi trải qua phản ứng liên kết chéo, số lượng lớn gel HA sau đó được phân tách thành nhiều mảnh nhỏ (“cắt”) để tạo điều kiện làm sạch. Tiếp theo, các phần HA được phân tách được rửa sạch bằng nước tinh khiết hoặc nước muối để loại bỏ mọi tạp chất không mong muốn. Trong bước tiếp theo, gel được xử lý để giảm kích thước hạt gel. Điều này được thực hiện bằng cách nghiền gel, sau đó chúng được đưa qua bằng dao quay hoặc máy đồng hóa hoặc bằng cách đưa gel qua lưới có kích thước xác định của máy đồng hóa. Trong cả hai trường hợp này, việc giảm kích thước hạt gel cho phép tiêm gel vào da thông qua một kim cỡ nhỏ. Tuy nhiên, vì phương pháp lưới tạo ra các hạt có kích thước được kiểm soát, nó cũng cho phép các hạt gel điều chỉnh để phù hợp với chỉ định lâm sàng mong muốn. Điều này sẽ không xảy ra nếu sử dụng thiết bị đồng hóa, vì kích thước hạt thu được là không đồng nhất. Sau khi nghiền, gel HA được đổ đầy vào các ống tiêm riêng lẻ, sau đó được chuyển vào lò hấp để khử trùng [5].
Một cân nhắc chính trong quá trình sản xuất chất làm đầy HA là cần kiểm soát quá trình sản xuất đối với các protein không mong muốn, nội độc tố và các tác nhân liên kết chéo còn sót lại. Protein là nguyên nhân chính gây ra nhiễm trùng và dị ứng; do đó, điều quan trọng là phải đảm bảo nguyên liệu thô HA đáp ứng các yêu cầu của Dược điển Châu Âu (EP) về hàm lượng protein (<0,1% nguyên liệu thô). Đối với hầu hết các sản phẩm chất làm đầy HA được bán trên thị trường, các nhà sản xuất cố gắng giữ mức protein còn lại ở mức 10μg / mL hoặc thấp hơn để giảm thiểu nguy cơ phản ứng dị ứng. Trong khi đó, mức độ nội độc tố được kiểm soát ở mức 0,5 EU / mL (đơn vị nội độc tố) hoặc thấp hơn theo quy định trong EP để tránh các phản ứng gây sốt và / hoặc viêm nhiễm có thể xảy ra [5]. Mặc dù mức BDDE cũng được quy định ở mức dưới 2 ppm, nhưng trên thực tế, BDDE hiếm khi được phát hiện trong sản phẩm bổ sung HA cuối cùng.
Sản xuất nguyên liệu thô HA
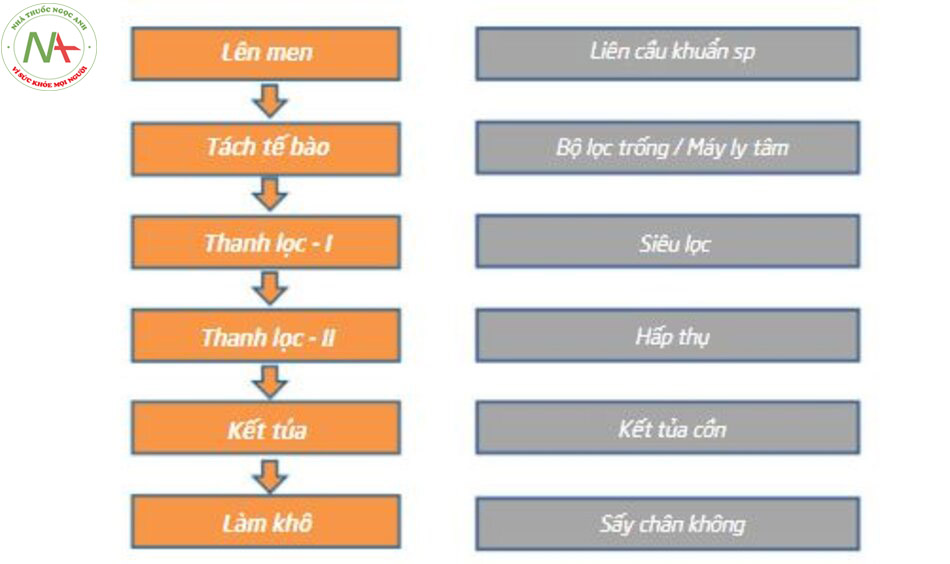
Sản xuất công nghiệp nguyên liệu thô HA (với số lượng lớn) dựa trên việc chiết xuất từ mào gà trống hoặc lên men vi sinh bằng cách sử dụng các chủng vi khuẩn. Trong giai đoạn phát triển sơ khai của chất làm đầy HA, HA sinh học chiết xuất từ mào gà trống đã được sử dụng cho hầu hết các sản phẩm, vì quá trình tạo ra HA có trọng lượng phân tử cao tự nhiên. Ví dụ, Hyla-form® (Genzyme Biosurgery), được FDA Hoa Kỳ phê duyệt vào năm 2004, được sản xuất bằng cách sử dụng HA có nguồn gốc từ mào gà trống, có trọng lượng phân tử khoảng 3000 kDa. Tuy nhiên, việc sản xuất thương mại HA từ mào gà trống tốn nhiều thời gian và tốn kém, bao gồm nhiều bước quy trình và thời gian hoàn thành đáng kể. Hơn nữa, có những khó khăn kỹ thuật đáng kể trong việc loại bỏ các vi rút có thể có (trong gia cầm) hoặc các protein và axit nucleic có khả năng tồn tại trong mô động vật. Ngoài ra, tỷ lệ mắc bệnh nghiêm trọng với Bệnh não dạng xoắn ở bò cho thấy những căn bệnh chết người có thể lây truyền giữa các loài (từ động vật đến người) theo những cách mà trước đây chưa được biết đến. Ở khía cạnh đó, việc sử dụng các vật liệu có nguồn gốc từ vi khuẩn được coi là có rủi ro thấp hơn nhiều so với nguồn gốc từ động vật vì vi khuẩn rất khác với tế bào động vật. Do những lo ngại về sản xuất và an toàn này, việc chiết xuất HA từ mào gà trống cuối cùng không còn được ưa chuộng, và thay vào đó, quá trình lên men vi khuẩn đã trở thành phương pháp sản xuất HA được ưa chuộng hơn [6]. Quá trình lên men vi khuẩn có khả năng tạo ra HA với chi phí thấp hơn đáng kể, với số lượng lớn và dễ dàng hơn trong việc loại bỏ các protein và nội độc tố ngoại lai còn sót lại trong quá trình so với chiết xuất HA từ mào gà trống. Streptococcus là vi khuẩn được sử dụng rộng rãi nhất để sản xuất HA từ vi khuẩn, trong đó Streptococ-cus Zooepidemicus là chủng được sử dụng nhiều nhất [6]. Restylane® là chất làm đầy tiêm từ HA đầu tiên được FDA Hoa Kỳ chấp thuận vào năm 2003. Nó cũng dựa trên HA được chiết xuất từ quá trình lên men vi sinh vật, có trọng lượng phân tử khoảng 1000 kDa. Được thúc đẩy bởi những tiến bộ trong công nghệ lên men, trọng lượng phân tử HA thu được từ quá trình sản xuất HA của vi sinh vật đã tăng dần từ dưới 2000 kDa trong những ngày đầu lên trên 3000 kDa hiện nay [6]. Trong khi quá trình lên men vi sinh vật có thể tạo ra HA với độ tinh khiết cao hơn, không có mầm bệnh còn sót lại như vi rút gia cầm so với HA có nguồn gốc từ gia cầm, nguy cơ ô nhiễm nội độc tố vi khuẩn, bào quan nội bào và các protein không mong muốn vẫn còn, do đó cần phải tinh chế phức tạp và sâu rộng. Để đạt được mục đích này, các tế bào vi khuẩn trước tiên phải được ly tâm để tách tế bào, và sau đó được phân giải trong dung dịch natri hydroxit (NaOH). Sau đó, dung dịch không có tế bào thu được sẽ trải qua các quy trình tiếp theo là siêu lọc, hấp phụ vào than hoạt tính hoặc alumin, và kết tủa bằng cồn để loại bỏ bất kỳ tạp chất hoặc mảnh vụn tế bào nào (Hình 2.6) có thể còn lại trong sản phẩm. Quá trình thanh lọc này có thể khác nhau giữa các nhà sản xuất. Trọng lượng phân tử trung bình của HA có thể được kiểm soát thông qua điều kiện lên men và xử lý trong quá trình tinh chế.
Như đã giải thích, độ tinh khiết của nguyên liệu thô HA được xác định phần lớn bởi phương pháp cụ thể và mức độ tinh chế được áp dụng trong quá trình sản xuất. Những cân nhắc chính trong việc lựa chọn nguyên liệu thô HA là nội độc tố của vi khuẩn và protein có nguồn gốc tế bào còn lại trong sản phẩm và liệu lượng của chúng có nằm trong quy cách yêu cầu hay không. Mức độ tương ứng mà các tạp chất này còn sót lại xác định mức độ an toàn sinh học của HA, và cấp độ lâm sàng của nó. Nguyên liệu thô HA để sử dụng trong công nghiệp được phân loại là cấp thực phẩm, cấp mỹ phẩm hoặc cấp y tế, với cấp độ y tế được chia nhỏ thành các loại để sử dụng làm công thức nhãn khoa (cấp thuốc nhỏ mắt) hoặc chế phẩm tiêm (cấp độ tiêm) tùy thuộc vào yêu cầu nghiêm ngặt của việc thanh lọc. HA cấp độ thuốc nhỏ mắt được sử dụng trong sản xuất thuốc nhỏ mắt, chất bảo quản kính áp tròng, và các chế phẩm bôi ngoài da cho các tổn thương niêm mạc miệng, trong khi HA cấp độ tiêm được sử dụng để sản xuất cấy ghép thấu kính nội nhãn, thuốc tiêm nội nhãn, chất chống dính sau phẫu thuật (để ngăn ngừa sự kết dính của mô sau phẫu thuật), và chất làm đầy tiêm, v.v.
HA cấp độ tiêm thường đắt hơn 3–4 lần so với HA cấp độ thuốc nhỏ mắt được sử dụng cho các công thức nhãn khoa, với bột HA để tiêm có độ tinh khiết cao nhất trong số tất cả các công thức nguyên liệu thô HA [7].
Vì sự an toàn của các sản phẩm chất làm đầy HA dạng tiêm không chỉ phụ thuộc vào chất lượng của các bước tinh chế được thực hiện trong quá trình sản xuất mà còn phụ thuộc vào bản thân nguyên liệu HA thô. Chất lượng và độ tinh khiết của nguồn nguyên liệu HA thô là điều quan trọng để xác định độ an toàn của sản phẩm chất làm đầy HA cuối cùng. Do đó, ít nhất, các sản phẩm chất làm đầy HA đáp ứng tiêu chuẩn tối thiểu về chất lượng nếu chúng được sản xuất bằng nguyên liệu HA có nguồn gốc từ các nhà cung cấp có trong danh sách Hồ sơ Thạc sĩ Dược phẩm của FDA Hoa Kỳ và được Cục Quản lý Chất lượng Thuốc & Chăm sóc Sức khỏe Châu Âu phê duyệt. (EDQM) [7]. Tính đến năm 2020, các nhà sản xuất nguyên liệu HA có trong danh sách DMF của FDA như sau: LG Chem LTD (công ty Hàn Quốc); Kewpie Corp, Kikkoman Biochemifa Co, Kibun Food Chemifa Co. LTD, Kyowa Hakko Kogyo Co LTD, Seikagaku Corp, Shiseido Co LTD (Các đơn vị Nhật Bản); Bloomage Biotechnol-ogy Corp LTD, Shandong Freda Biochem Co LTD, Shandong Awa Biopharm Co LTD (các đơn vị Trung Quốc); Bioiberica SA, Contipro AS, Fidia Farmaceutici SPA, No-vozymes AS (các đơn vị thuộc Liên minh Châu Âu); Phòng thí nghiệm nghiên cứu da liễu INC, Lifecore Biomedical LLC, Maruha Nichiro Corp (các đơn vị Hoa Kỳ). Về vấn đề này, LG Chem.’sYVOIRE® dựa trên công thức HA của riêng mình và Neuramis® của Medytox Inc. được bào chế với HA thô do Shiseido Co LTD (Nhật Bản) cung cấp trong khi hầu hết các nhà sản xuất chất làm đầy HA không tiết lộ nguồn gốc cung cấp nguyên liệu HA của họ.
Bàn luận: Cơ hội và sự cần thiết
Một người thợ lợp mái tôn sửa chữa mái trên một tòa nhà cao tầng đã vô tình làm rơi chiếc búa của mình khiến người đi bộ qua đường tử vong. Mặc dù việc người thợ làm mái làm rơi chiếc búa hoàn toàn là do ngẫu nhiên, nhưng nó chắc chắn dẫn đến sự kiện xác định là cái chết của người đi bộ. Đó là lý do được trình bày trong cuốn sách Cơ hội và Sự cần thiết của người đoạt giải Nobel Jaques Monod để giải thích quá trình tiến hóa. Về bản chất, ông cho rằng đó là sự trùng hợp ngẫu nhiên khi một tế bào thể hiện dạng sống thô sơ nhất được tạo ra thông qua một số chuỗi phản ứng sinh hóa khó giải thích và rất khó xảy ra giữa các vật chất vô cơ; và rằng các động vật thấp hơn hoặc cao hơn ngày nay là sản phẩm cần thiết của quá trình tiến hóa hỗn độn và phức tạp mà các tế bào sau đó đã trải qua. Lần đầu tiên đọc cuốn sách này ở trường đại học, tôi chỉ đơn giản coi nó là một tập hợp các lập luận thông minh, nếu đúng hơn là nghịch lý, ủng hộ thuyết tiến hóa. Tuy nhiên, thời gian dần trôi, tôi đã đánh giá cao cách những ý tưởng được tán thành trong Cơ hội và Sự cần thiết có liên quan đặc biệt đến cuộc sống của chúng ta như thế nào.
Năm 1998, khi đang làm nghiên cứu viên tại Bệnh viện Đại học Quốc gia Seoul (SNUH), Khoa Da liễu, tôi tình cờ đọc được một nghiên cứu hấp dẫn của Tiến sĩ Shelley được công bố trên Tạp chí Học viện Da liễu Hoa Kỳ liên quan đến việc tiêm độc tố botulinum vào lòng bàn tay của bệnh nhân để điều trị chứng tăng tiết mồ hôi lòng bàn tay. Thực tế là hiệu quả được tìm thấy kéo dài đến 5-6 tháng khiến tôi bị thu hút. Mặc dù rõ ràng không phải là một tình trạng nguy hiểm đến tính mạng hay một bệnh truyền nhiễm, nhưng chứng tăng tiết mồ hôi khu trú, đặc biệt là tăng tiết mồ hôi lòng bàn tay, có thể khiến bản thân bệnh nhân rất buồn bã, do nó cản trở các hoạt động hàng ngày của họ theo một số cách gây phiền toái. Bàn tay đẫm mồ hôi có nguy cơ bị tê cóng nhiều hơn vào mùa đông; Ngoài ra, khi viết, ghi chú hoặc hoàn thành các bài kiểm tra viết, cần phải đặt một chiếc khăn tay bên dưới bàn tay để không làm ướt giấy. Bàn tay ướt át không lý tưởng để cầm tay hay bắt tay và có thể khiến người đó gặp bất lợi không đáng có trong các tương tác xã hội khác nhau. Mức độ đau khổ của bệnh nhân như vậy theo một nghiên cứu cho thấy tình trạng đau khổ về tinh thần và tâm lý do chứng tăng tiết mồ hôi gây ra còn lớn hơn so với bệnh viêm khớp dạng thấp mãn tính hoặc suy thận mãn tính. Mặc dù đã có sẵn một số biện pháp điều trị chứng tăng tăng tiết mồ hôi lòng bàn tay, bao gồm cả thuốc bôi ngoài da và thuốc uống, nhưng chỉ có tác dụng tạm thời và tối thiểu. Trong hầu hết các trường hợp, bệnh nhân chỉ được chuyển đến khoa phẫu thuật lồng ngực để tiến hành phẫu thuật nội soi xâm lấn nhiều hơn. Tuy nhiên, dù có điều trị bằng phương pháp vĩnh viễn này, phẫu thuật cắt dây giao cảm cũng có những vấn đề riêng của nó. Nói một cách đơn giản, bệnh tăng tiết mồ hôi lòng bàn tay là một vấn đề vô cùng thú vị đối với một bác sĩ da liễu bình thường.
Trong năm đầu tiên tôi thực tập nội trú tại SNUH, một trong những trách nhiệm của tôi là đo lượng mồ hôi tiết ra của bệnh nhân tăng tiết mồ hôi ở lòng bàn tay theo hướng dẫn của giáo sư tại Khoa Da liễu. Đó là một công việc rất tốn thời gian. Hơn thế nữa, vì thang đo chính xác được sử dụng cho các phép đo được lưu giữ tại một văn phòng riêng biệt trên tầng mười hai của tòa nhà, mỗi chuyến đi lại giữa văn phòng và bệnh nhân mất tới 30 phút. Tuy nhiên, chẳng có gì có ích từ những chuyến đi và bài kiểm tra mệt mỏi hàng ngày đó ngoài một bài luận văn được xuất bản dưới danh nghĩa giáo sư phụ trách. Tôi không thể thấy nó có thể mang lại lợi ích gì cho bệnh nhân khi cuối cùng họ phải chuyển đến khoa phẫu thuật lồng ngực để điều trị thực sự.
Với ký ức mệt mỏi đó vẫn còn in đậm trong tâm trí tôi, thật tuyệt vời khi biết rằng một mũi tiêm duy nhất có thể giúp bệnh nhân giảm chứng tăng tiết mồ hôi lòng bàn tay trong nhiều tháng. Loại thuốc cơ bản cũng có giá cả phải chăng, chỉ khoảng 60 USD cho mỗi lọ Botox®. Sau khi xem xét thêm tài liệu, tôi phát hiện ra rằng những tài liệu nghiên cứu ít ỏi vẫn chỉ ở giai đoạn sơ khai và ngay lúc đó tôi đã tìm thấy thị trường thích hợp của mình. Rất nhanh chóng, tôi đưa ra một đề xuất nghiên cứu trong vòng 3 ngày và chuẩn bị thực hiện.
Khó khăn duy nhất là có một lỗi đánh máy về giá niêm yết trong dược phẩm SNUH – khoảng 60 USD! Theo tôi, hóa ra chữ số 0 cuối cùng đã bị bỏ sót do nhầm lẫn, có nghĩa là giá thực tế là một con số khổng lồ 600 USD. Hai chai để tiêm cho cả hai tay sẽ có giá 1.200 USD cho mỗi lần điều trị và tôi phải nghiêm túc suy nghĩ xem từ quan điểm của bệnh nhân, 5–6 tháng tạm thời khỏi mồ hôi có phù hợp với loại chi phí đó hay không. Tuy nhiên, cuối cùng, tôi quyết định phương pháp điều trị vẫn có sức hấp dẫn như một phương pháp điều trị không xâm lấn mới liên quan đến việc sử dụng thuốc tiêm và được đẩy nhanh hơn so với kế hoạch. Đó là cách lần đầu tiên tôi bắt đầu luyện tập với botulinum toxin.
Chắc chắn, cuộc sống hoạt động theo những cách bí ẩn. Nếu không phải vì sự vất vả của những phép đo mồ hôi đó, hoặc sự ngẫu nhiên của bài báo JAAD về bệnh tăng da ở lòng bàn tay, hoặc giá Botox® được niêm yết không chính xác trong dược phẩm SNUH, tôi tự hỏi liệu tôi có thực hiện các thủ tục botox hay không. Chúng ta là sản phẩm cuối cùng của vô số sự kiện ngẫu nhiên đã xảy ra trong quá khứ của chúng ta. Sự khác biệt duy nhất giữa cuộc sống của chúng ta và quá trình tiến hóa là cuộc sống của con người không kéo dài hàng tỷ năm, và do đó, chúng ta cần một số hình thức nỗ lực để thu hẹp khoảng cách giữa cơ hội và kết quả cần thiết mà chúng ta mong muốn. Tương tự như cách chúng ta chắc chắn phát hiện ra người bạn đời của mình từ nhiều cuộc gặp gỡ ngẫu nhiên trong cuộc sống, tôi cho rằng chính niềm đam mê, sự tận tâm và mồ hôi đã biến những cuộc ngẫu nhiên đơn thuần của ngày hôm qua thành thành quả xứng đáng của ngày mai (tháng 6 năm 2019).
Kết hợp Tác nhân liên kết chéo / Phản ứng liên kết chéo
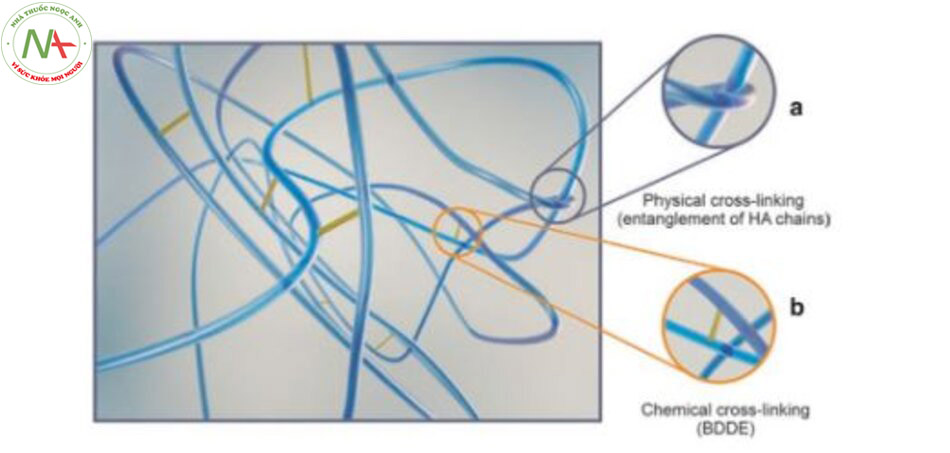
Hòa tan trong nước, bột HA chuyển thành một chất lỏng đặc như keo với kết cấu nhớt tương tự như nước sốt chua ngọt, một trạng thái được gọi là HA tự do. HA tự do hầu như không có bất kỳ cấu trúc hoặc độ đàn hồi nào và do đó không có khả năng cung cấp hỗ trợ trong mô. Nếu HA tự do được tiêm như là chất làm đầy, nó sẽ phân hủy trong vòng một tuần do hoạt động của hyaluronidase nội sinh hoặc các gốc tự do trong mô người. Do đó, để tạo độ đàn hồi cho HA tự do và tăng thời gian tồn tại của nó trong cơ thể, liên kết chéo được đưa vào giữa các polyme HA để ổn định HA thành dạng gel. Liên kết chéo có thể đạt được bằng các phương pháp vật lý hoặc hóa học. Mỗi quy trình liên kết chéo cụ thể hoặc công nghệ gel dẫn đến các loại gel có đặc tính phụ thuộc vào cả yếu tố vật lý và hóa học. Yếu tố vật lý làm tăng tác dụng của các chất liên kết chéo hóa học do các polyme HA vướng mắc với nhau. Điều này tạo ra một mạng lưới liên kết chặt chẽ của các chuỗi polyme HA (Hình 2.7) được liên kết với nhau chỉ bởi một số liên kết chéo hóa học. Đối với các yếu tố hóa học, nhiệt độ mà HA lỏng (tức là HA pha loãng trong nước) phản ứng với chất liên kết chéo và thời gian HA phản ứng với chất liên kết chéo là các thông số quan trọng nhất để liên kết các phân tử HA với nhau. Restyl-ane® là ví dụ sản phẩm điển hình có đặc tính là kết quả của các yếu tố vật lý. Công nghệ NASHA™ được sử dụng để tạo gel dẫn đến gel đặc với G’ (độ đàn hồi) cao nhưng với mức độ biến đổi (MoD) dưới 1%, đó là điều quan trọng để đảm bảo khả năng tương thích sinh học tốt.
Trong khi liên kết chéo vật lý có vai trò quan trọng, các đặc tính của gel phụ thuộc nhiều vào việc đưa vào các tác nhân liên kết chéo để liên kết với nhau giữa các phân tử HA. Ở đây, tác nhân liên kết chéo đóng một vai trò tương đương với gluten trong lúa mì. Không giống như các loại ngũ cốc khác, bột mì trộn với nước sẽ tạo ra cục bột đàn hồi, co giãn và dai, nguyên nhân chủ yếu là do sự hiện diện của gluten trong protein lúa mì. Trong quá trình nhào bột, gluten trong bột mì kết hợp với tinh bột để tạo thành một màng gluten lưới, giúp bột có độ đàn hồi và cho phép nó giữ hình dạng ở trạng thái nghỉ và dễ dàng được kéo dài ra. Tương tự như vậy, các chất liên kết chéo liên kết với các chuỗi polyme HA riêng lẻ và liên kết chúng với nhau để xây dựng một mạng lưới HA liên kết chéo chặt chẽ, chuyển đổi các polyme HA từ dạng lỏng sang dạng gel (Hình 2.8). Do đó, khối lượng gel HA được sản xuất hiệu quả tạo thành một thể thống nhất chống lại sự phân hủy bởi các gốc tự do. Cuối cùng, tương tự như cách bột mì được chia thành các loại rắn, trung bình và mềm tùy thuộc vào hàm lượng gluten của nó, các sản phẩm chất làm đầy HA có thể được phân loại là cứng (tức là có độ nhớt cao) hoặc mềm (tức là có độ nhớt thấp) như đã được xác định bằng các phép đo lưu biến.
Trong các chất khác nhau để sử dụng làm chất liên kết chéo như 1,4-butanedi-ol diglycidyl ether (BDDE), divinyl sulfone (DVS) và bişcarbodiimidie (BCDI), BDDE là chất liên kết chéo được sử dụng rộng rãi nhất cho đến nay trong sản xuất thương mại chất làm đầy HA do tính chất độc hại thấp chưa từng có của nó [5]. Liều gây chết trung bình (LD50) của BDDE qua đường uống cho chuột chỉ là 1134 mg / kg, ít hơn nhiều so với 32 mg / kg đối với DVS.
Lượng BDDE còn sót lại trong sản phẩm có các tiêu chuẩn áp dụng nghiêm ngặt vì tàn dư của BDDE chưa phản ứng có thể gây hại cho cơ thể con người.

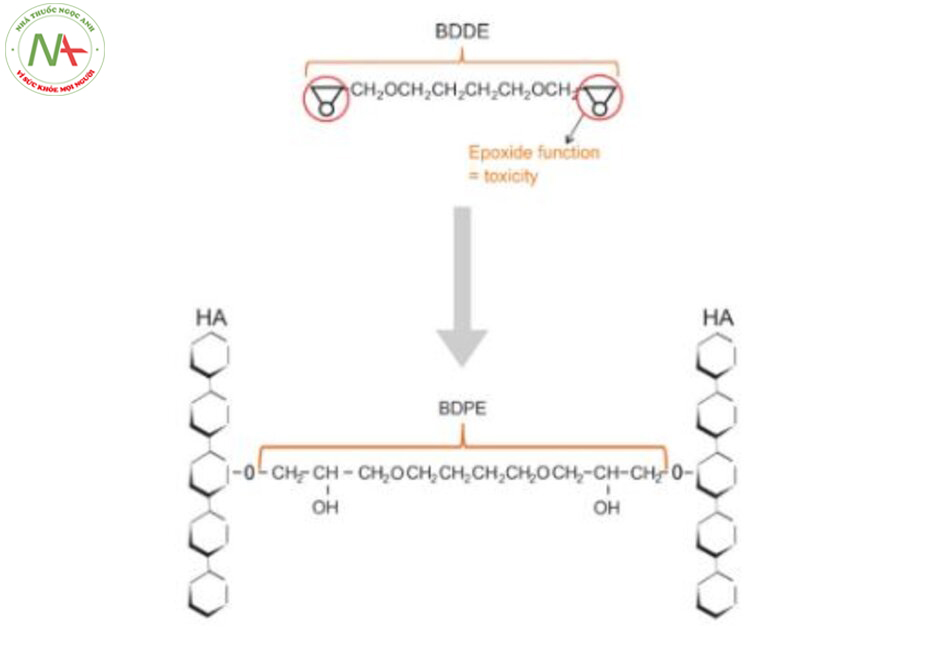
Tuy nhiên, ở giới hạn hiện tại là <2 μg, BDDE còn lại trong các sản phẩm chất làm đầy HA chỉ bằng 1/25 triệu liều gây tử vong ở người lớn 50 kg [5]. Dù vậy, ngành công nghiệp vẫn cam kết giảm thiểu hơn nữa BDDE còn sót lại bằng cách tăng thời gian phản ứng hoặc tốc độ phản ứng trong phản ứng liên kết chéo và bằng cách loại bỏ tối đa các mảnh vỡ BDDE trong quá trình làm sạch và tinh chế gel HA liên kết chéo. Trong khi đó, trong quá trình liên kết chéo, các nhóm epoxit của BDDE phản ứng với các nhóm hydroxyl của HA trong điều kiện kiềm, tạo thành các dẫn xuất 1,4-butanedi-ol di- (propan-2,3-diolyl) ete (BDPE) như trong Hình 2.9[8]. Tuy nhiên, khi làm như vậy, một số phân tử BDDE liên kết với HA ở cả hai đầu (“BDPE liên kết đôi”) trong khi những phân tử khác liên kết với HA ở một đầu chỉ ở dây móc (“BDPE liên kết đơn”) (Hình 2.10).
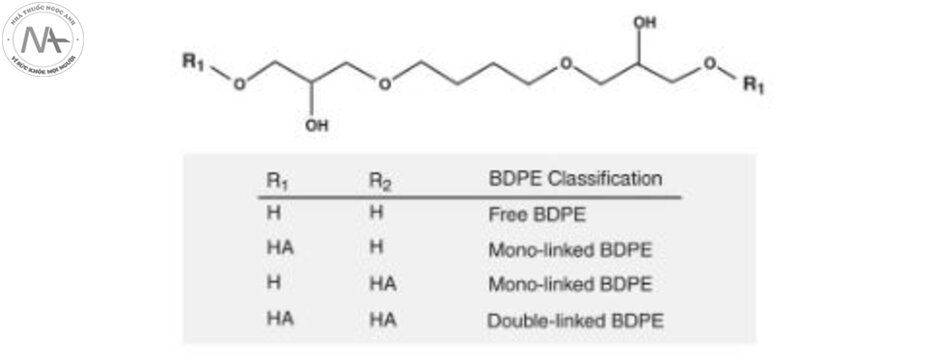
Mức độ liên kết chéo cao hơn với BDDE có liên quan đến thời gian HA trong mô cũng được kéo dài, cũng như độ đàn hồi và độ kết dính cao hơn của gel HA. Do đó, mức độ liên kết chéo là yếu tố chính trong việc so sánh các đặc tính lưu biến của các sản phẩm HA khác nhau. Các thông số chính để mô tả mức độ liên kết chéo bao gồm mức độ biến đổi (MoD), mức độ thay thế (DS), tỷ lệ liên kết chéo (CrD), mức độ liên kết chéo (DC) và tỷ lệ liên kết chéo hiệu quả (CrR), được định nghĩa tương ứng như sau (Bảng 2.1) [8]:
(a) Mức độ biến đổi (MoD): tỷ lệ giữa tổng số liên kết đơn (kiểu dây móc) và liên kết đôi BDPE và tổng số đơn phân HA (đơn vị disaccharide).
(b) Mức độ thay thế (DS): tỷ lệ giữa các disaccharide HA liên kết với BDPE và tổng số đơn phân HA (đơn vị disaccharide).
(c) Tỷ lệ liên kết chéo được biểu thị bằng từ viết tắt CrD: tỷ lệ giữa các gốc BDPE có liên kết đôi và tổng số đơn phân HA (đơn vị disaccharide).
(d) Mức độ liên kết chéo được ký hiệu bởi từ viết tắt DC: số lượng các disaccharid HA thực sự liên kết chéo so với tổng số các disaccharid HA.
(e) Tỷ lệ liên kết chéo hiệu quả (CrR): tỷ lệ giữa BDDE liên kết đôi so với tổng BDPE.
Trong tất cả các thuật ngữ trên, mẫu số được biểu thị bằng tổng số đơn vị đơn phân HA (đơn vị disaccharide), trong khi tử số thay đổi đối với mỗi tham số. Nói một cách đơn giản, MoD và CrD biểu thị tỷ lệ BDPE liên kết chéo với HA, trong khi DS và DC biểu thị tỷ lệ các đơn vị disaccharide HA liên kết chéo so với tổng số HA. Trong khi đó, CrD là tỷ lệ BDDE được liên kết đôi với HA (BDPE liên kết đôi), trong khi MoD bao gồm tỷ lệ của cả BDPE liên kết đơn (hình dây móc) và liên kết đôi.
Bằng cách minh họa, CrD là 20% tương đương với DC là 40%, vì DC đại diện cho gấp đôi giá trị của CrD. Trong mỗi trường hợp, điều này ngụ ý rằng đối với mỗi 10 đơn phân HA (hoặc đơn vị disaccharide) trong gel, hai phân tử BDDE (CrD là 20%) hoặc bốn đơn vị disaccharide HA (DC là 40%) đã được liên kết chéo. Trong khi đó, MoD là 50% và CrR là 40% dẫn đến DS là 70%, vì điều này ngụ ý rằng đối với mỗi 10 đơn phân HA (hoặc đơn vị disaccharide), các liên kết đã được hình thành với trung bình 5 phân tử BDDE (MoD là 50 %), trong đó chỉ có 2 phân tử là BDDE liên kết đôi (CrR là 40%), và do đó bảy trong số mười đơn vị disaccharide HA được kết nối với BDDE (DS là 70%) (Hình 2.11).
Mức độ liên kết chéo cao giúp gel có độ cứng cao hơn và kéo dài tuổi thọ. Tuy nhiên, quá nhiều nội dung liên kết chéo cản trở việc tiêm thuốc dễ dàng do sự kết hợp của sản phẩm, làm giảm tính ưa nước của HA và chỉ góp phần gây ra các phản ứng sinh miễn dịch. Do đó, sự cân bằng đầy đủ của các liên kết chéo là một trong những yếu tố cần thiết của một chất làm đầy HA lý tưởng. Về vấn đề này, một sản phẩm có CrR thấp, bao gồm chủ yếu là BDPE liên kết đơn thay vì BDPE liên kết đôi, có xu hướng thể hiện đặc tính lưu biến mềm hơn và linh hoạt hơn.
Bảng 2.1 Định nghĩa MoD, CrD, DS và DC đối với chất làm đầy HA đã được điều chỉnh
| Định nghĩa dựa trên số lượng… | ||
| .. Đơn vị liên kết chéo / đơn vị HA | … Đơn vị HA thay thế / HA | |
| Tham số | Mức độ biến đổi (MoD) | Mức độ thay thế (DS) |
| Định nghĩa | nliên kết chéo được liên kết / nHA disaccharides | nDisaccharides HA được thay thế / nHA disaccharides |
| Xác định | Từ NMR | DS = MoD + CrD = MoDx(1 + CrR) |
| Tham số | Tỷ lệ liên kết chéo (CrD) | Mức độ liên kết chéo (DC) |
| Định nghĩa | nliên kết chéo được liên kết đôi / nHA disaccharides | nCác disaccharides HA liên kết chéo / nHA disaccharides |
| Xác định | CrD = CrR – MoD | DC = 2 x CrD = 2 x CrR x MoD |
CrR: Tỷ lệ liên kết chéo hiệu quả. Được sửa đổi từ tài liệu tham khảo [8].
![Chất làm đầy nâng da mặt gồm những loại nào? Quy trình sản xuất? 114 Hình 2.11 Một cấu trúc giả định về liên kết chéo giữa HA và BDDE bao gồm “BDPE liên kết đôi” và “BDPE liên kết đơn” (Hình được điều chỉnh từ Tham khảo [8]).](https://nhathuocngocanh.com/wp-content/uploads/2022/07/chat-lam-day-nang-da-mat-gom-nhung-loai-nao-quy-trinh-san-xuat-anh-11.jpg)
Nồng độ axit hyaluronic
Là kết quả của việc tiếp xúc với nhiệt trong quá trình khử trùng, tất cả gel HA bao gồm cả gel liên kết chéo và một phần có thể chiết xuất, thường được ký hiệu là HA tự do. HA tự do hoạt động như một chất bôi trơn để tạo điều kiện thuận lợi cho việc đưa các phần tử HA vào mô và không cung cấp hỗ trợ cấu trúc trong nó và của chính nó. Ví dụ, cả Restylane® (Galderma) và Juvéderm® Voluma® (Allergan) có cùng nồng độ HA là 20 mg / mL và chứa nồng độ HA tự do tương tự từ 20 đến 30%.
Hầu hết các sản phẩm làm đầy HA thương mại hiện nay trên thị trường có nồng độ HA trong khoảng 20–24 mg / mL. Quy tắc chung được chấp nhận là nồng độ HA cao hơn tương đương với độ đàn hồi cao hơn và thời gian tác dụng lâu hơn. Trong số các thương hiệu nội địa của Hàn Quốc, Cleviel® (Pharmaresearch Prod-ucts, Korea), có nồng độ HA cao đáng chú ý là 50 mg / mL để có độ đàn hồi và tuổi thọ tối đa. Tuy nhiên, nhược điểm của việc sử dụng một sản phẩm có nồng độ HA cao như vậy là nó đòi hỏi lực đẩy ra lớn hơn trong quá trình tiêm do kết cấu chắc, cứng của nó; không dễ dàng tạo khuôn sau khi tiêm; và khó hòa tan hơn với hyaluroni-dase ngoại sinh. Hơn nữa, nồng độ HA cao hơn trong chất làm đầy HA được cho là có liên quan đến sự gia tăng thể tích tiêm sau 2–4 tuần sau điều trị do sự hydrat hóa của các phân tử HA liên kết chéo [9]. Về mặt này, Juvéderm® Ultra™, với nồng độ HA là 24 mg / mL và được sản xuất bằng công nghệ HYLACROSS™, đặc biệt dễ gây ra tác dụng phụ không mong muốn như sưng tấy hoặc không đều sau điều trị do sự bão hòa của các phân tử HA. Do đó, các phiên bản tiếp theo của chất làm đầy Juvéderm®, bao gồm công nghệ VYCROSS™, đã làm giảm đáng kể nồng độ HA của chúng để tránh các vấn đề như vậy. Ví dụ, Juvéderm® Voluma™ được chỉ định để phục hồi thể tích sâu (dưới da) chứa 20 mg / mL HA, Juvéderm ® Volift™ để điều chỉnh nếp nhăn sâu chứa 17,5 mg / m HA, trong khi Juvéderm® Volbella™ cho các đường rãnh sâu và nếp nhăn bao gồm cả nếp nhăn quanh mắt với 15 mg / mL HA trong sản phẩm.
HA đơn pha và hai pha
Thông thường chất làm đầy HA được phân loại là HA một pha và hai pha, dựa trên quy trình sản xuất cụ thể của chúng. Trong sản xuất chất làm đầy HA, khi phản ứng liên kết chéo hoàn tất, gel HA sau đó được chuyển vào máy đồng hóa hoặc máy xay để nghiền thành các hạt mịn có thể dễ dàng đi qua kim. HA hai pha thu được ở giai đoạn này bằng cách ‘sàng lọc’ gel HA thông qua các sàng phân loại có đường kính xác định, tạo ra các hạt HA có kích thước mong muốn. Khi so sánh, HA đơn pha không trải qua quá trình sàng phân loại hạt và do đó, nó là một gel đồng nhất chứa các hạt có hình dạng và kích thước hỗn hợp. Do đó, HA hai pha rắn chắc hơn, đàn hồi hơn và đặc biệt có cảm giác các hạt đặc hơn, trong khi HA đơn pha có kết cấu mềm hơn, cấu trúc lỏng hơn với các hạt kết dính yếu hơn. Về mặt này, Restylane® SubQ™, có kích thước hạt lớn nhất trong số các sản phẩm Restylane®, bao gồm các hạt lớn đến mức chúng thực sự có thể nhìn thấy bằng mắt thường, có đường kính gần 1 mm [10].
Tuy nhiên, về mặt khoa học, việc phân loại chất làm đầy HA một pha hoặc hai pha là không phù hợp, vì tất cả các gel HA đều bao gồm các hạt gel khi được kiểm tra dưới kính hiển vi (Hình 2.12). Thuật ngữ ‘chất làm đầy HA một pha’ ban đầu được Juvéderm® đề xuất với mục đích phân biệt chất làm đầy HA mềm của họ với chất làm đầy gel rắn là NASHA™ originial, Restylane®. Tuy nhiên, thuật ngữ gel HA một pha thực sự là một oxymoron vì theo định nghĩa, gel tồn tại như một hỗn hợp của pha lỏng trong một pha rắn, nói cách khác, theo tính chất vật lý, gel là một hỗn hợp hai pha. Theo logic này, người ta có thể tranh luận rằng chất làm đầy HA hai pha nên được mô tả thích hợp hơn như một loại gel ba pha [11]. Hơn nữa, một số chất làm đầy HA thường được phân loại là chất làm đầy HA đơn pha như Restylane® Volyme và Restylane® Refyne sử dụng công nghệ OBT™ cũng chứng minh kích thước hạt gần như đồng nhất do quá trình ‘sàng lọc’ trong quá trình sản xuất để có độ đồng nhất tối ưu. Mặc dù vậy, những thuật ngữ này thường được sử dụng trong thực hành lâm sàng như một cách viết tắt để mô tả các chất làm đầy HA khác nhau nhằm hỗ trợ sự hiểu biết của các bác sĩ điều trị. Do đó, cần lưu ý rằng các thuật ngữ ‘một pha’ và ‘hai pha’ như được đề cập trong cuốn sách này chỉ được sử dụng cho mục đích thuận tiện. Tuy nhiên, để mô tả tốt nhất chất làm đầy HA theo cách tạo thuận lợi cho việc lựa chọn chất làm đầy nhất định cho một chỉ định lâm sàng nhất định, nên sử dụng các xét nghiệm lưu biến khoa học như đo lưu biến.
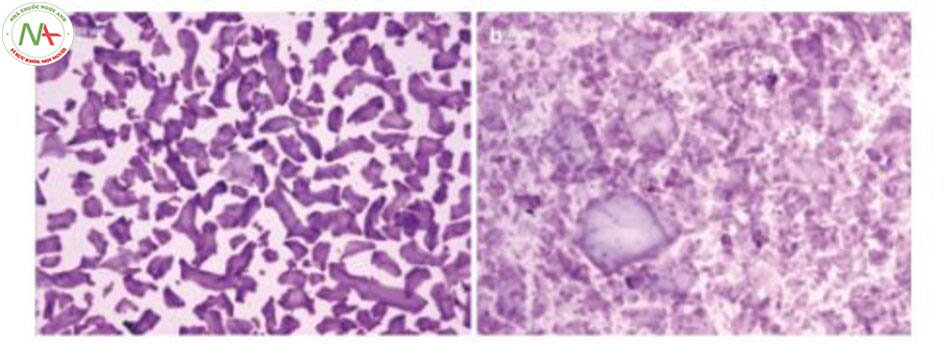
Về đặc tính lưu biến của chúng, chất làm đầy HA hai pha rắn có độ đàn hồi và độ nhớt cao hơn HA đơn pha mềm (Bảng 2.2), giúp giữ hình dạng tốt hơn chống lại biến dạng bên ngoài và khả năng nâng đỡ mạnh hơn [11]. Do đó, HA hai pha phù hợp đặt ở các mặt phẳng sâu hơn, nơi chúng có thể nâng cao mô sâu hoặc hỗ trợ cho việc suy giảm thể tích trên khuôn mặt nhưng nó ít phù hợp hơn khi tiêm nông vào lớp hạ bì và không dễ tạo khuôn sau khi tiêm.
Ngược lại, HA đơn pha có độ đàn hồi và độ nhớt thấp hơn nhưng thể hiện mức độ liên kết cao hơn so với HA hai pha tồn tại dưới dạng các hạt gel riêng lẻ tập hợp lại với nhau như cát. Tính liên kết là một yếu tố quan trọng khác quyết định lưu biến cho biết khả năng của một sản phẩm để chống lại sự biến dạng bên ngoài. Đáng chú ý, trong nghiên cứu của Sundaram và cộng sự, hai chất làm đầy HA mềm một pha Belotero® Balance™ và Juvéderm® Ultra Plus™ có mức độ liên kết cao nhất, chất làm đầy HA hai pha Restylane® có mức độ liên kết thấp nhất (Bảng 2.2). [13] Chất làm đầy HA mềm hơn với chỉ số G thấp hơn và độ kết dính cao hơn phù hợp để tiêm vào những vùng da mặt cử động nhiều như trán, nếp gấp mũi và má hơn là chất làm đầy rắn, vì chất làm đầy HA một pha có thể phục hồi hiệu quả hình dạng ban đầu mà không phân tách ra hay bị biến dạng khi các cơ mặt chuyển động. Ngoài ra, do có độ nhớt thấp hơn, chất làm đầy HA một pha có thể tạo ra kết quả mềm mượt ngay cả khi được đặt ở bề mặt lớp hạ bì vì chúng dễ dàng tản ra trên mặt phẳng mô và có thể tạo ra khuôn dễ dàng [14].
Do tính chất ưa nước, chất làm đầy HA có thể giãn nở thể tích trong vòng 2-4 tuần sau khi tiêm và do đó, có thể gây vón cục và không đều không mong muốn, đặc biệt là ở những vùng có mô mỏng bao phủ như vùng quanh hốc mắt (Hình 2.13). Sự trương nở sau tiêm do quá trình hydrat hóa các phân tử HA dường như xảy ra nhiều hơn ở chất làm đầy HA mềm một pha so với chất làm đầy HA hai pha dạng rắn trong khi các điều kiện khác như nồng độ HA cũng cần được xem xét (Hình 2.14) [15]. Độ nở ra sau khi tiêm của chất làm đầy HA có thể được đo bằng phép đo ‘hệ số trương nở’, biểu thị trạng thái hydrat hóa (bão hòa) của gel HA [17]. Khi gần bão hòa (gần trạng thái cân bằng), gel sẽ không bị nở lên đáng kể sau khi tiêm. Dưới mức cân bằng (không bão hòa), gel sẽ dễ dàng hút nước từ chất lỏng xung quanh cho đến khi nó đạt đến trạng thái cân bằng hydrat hóa. Đặc điểm hấp thụ chất lỏng của gel khác nhau giữa các sản phẩm và phụ thuộc vào nồng độ axit hyaluronic và bị giới hạn bởi mức độ liên kết chéo. Nói chung, khi mức độ liên kết chéo tăng lên trong chất làm đầy HA rắn có chỉ số G’ cao, hệ số trương nở sẽ giảm. reversible, các sản phẩm gel mềm hơn với mức độ liên kết chéo thấp hơn và có chỉ số G’ thấp hơn sẽ có hệ số trương nở cao hơn. Cũng có thể giả thiết rằng điều này xảy ra một phần là do HA một pha mềm có xu hướng tản ra trong mô, khiến diện tích bề mặt gel tiếp xúc với nước trong mô lớn hơn. Điều này trái ngược với các chất làm đầy HA hai pha ít tản ra hơn, hợp nhất vào mô theo cách có mục đích hơn và do đó có diện tích bề mặt hạn chế hơn trên mỗi thể tích trong mô. Đáng chú ý, Juver-derm® Ultra Plus™, dựa trên công nghệ HYLACROSS™ với nồng độ HA 24 mg / m và Belotero® Volume™ kết hợp công nghệ CPM™ với nồng độ HA 26 mg / m là các sản phẩm HA đơn pha được lưu ý vì tính giãn nở đáng kể sau tiêm (Bảng 2.2).
Vì vậy, chúng không thích hợp để tiêm ở những vùng da mỏng trên khuôn mặt; ngay cả khi được sử dụng để tạo đường viền và tạo nét khuôn mặt, nên pha loãng sản phẩm với nước muối theo tỷ lệ 6: 4 với sáu phần HA và bốn phần nước muối tương ứng (xem Phần 3.1.3).
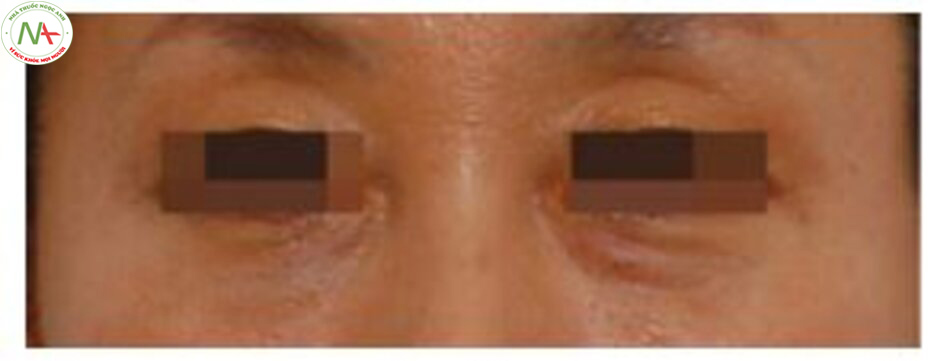
![Chất làm đầy nâng da mặt gồm những loại nào? Quy trình sản xuất? 118 Hình 2.14 Xu hướng thời gian trong phép đo hình ảnh 3D theo loại chất làm đầy. Không có sự khác biệt đáng kể nào giữa chất làm đầy B và J. Phép đo 3D với chất làm đầy B lớn hơn với chất làm đầy R tại các khoảng thời gian ngoại trừ 30 phút. Hơn nữa, các phép đo 3D với chất làm đầy B tốt hơn với chất làm đầy Y ở 2, 4 và 24 tuần. (B: Belotero® J: Juvéderm® R: Restylane® Y: YVOIRE®) (Trích dẫn từ Tham khảo [15]).](https://nhathuocngocanh.com/wp-content/uploads/2022/07/chat-lam-day-nang-da-mat-gom-nhung-loai-nao-quy-trinh-san-xuat-anh-14.jpg)
Lựa chọn chất làm đầy HA
Ba yếu tố chính cần xem xét trong việc lựa chọn một sản phẩm chất làm đầy là độ an toàn, tuổi thọ và giá cả như tôi đã nhấn mạnh trong các bài giảng từ đầu những năm 2000 (Hình 2.15). Trong số đó, an toàn được ưu tiên hàng đầu, vì chất làm đầy tiêm về cơ bản là các chất bên ngoài được đưa vào cơ thể con người. Về điểm này, HA vượt trội hơn tất cả các loại chất làm đầy mô mềm khác hiện có trên thị trường. Nó không chỉ giảm thiểu rủi ro phản ứng có hại, mà chất làm đầy HA tiêm còn có thể hủy bỏ dễ dàng bằng cách tiêm hyaluroni-dase nếu có bất kỳ vấn đề nào xảy ra, giúp bệnh nhân trở lại tình trạng trước khi điều trị một cách hiệu quả. Trước những lo ngại gần đây về các trường hợp viêm nhiễm do phản ứng quá mẫn loại chậm với chất làm đầy HA, tỷ lệ quá mẫn loại chậm cũng trở thành một tiêu chí an toàn đáng kể để lựa chọn sản phẩm chất làm đầy HA.
Trong khi chất làm đầy HA trước đây kéo dài từ 6 tháng đến 1 năm sau khi tiêm, theo quan sát của tôi, thời gian tác dụng thường kéo dài ngoài khung thời gian được đề xuất này, thậm chí kéo dài hơn tới 5–10 năm với điều trị duy trì lặp lại 2 –3 lần. Trong khi chất làm đầy HA đơn pha Juvéderm® Voluma và BELOTERO® Volume có xu hướng tồn tại lâu hơn HA hai pha. Khi được điều trị, giữa các bệnh nhân và các vùng mặt khác nhau có các biến đổi khác nhau, nhưng dường như không có sự khác biệt đáng kể về tuổi thọ của chất làm đầy giữa các nhãn hiệu chất làm đầy HA khác nhau miễn là chúng có khả năng tăng thể tích tương tự nhau. Nếu có bất cứ điều gì, các sản phẩm có chứa quá nhiều hàm lượng liên kết chéo để tăng tuổi thọ cần được xử lý cẩn thận hơn vì chúng thường có khả năng chống hòa tan với hyaluroni-dase cao hơn.
Giá cả chắc chắn là một yếu tố quan trọng cần cân nhắc đối với bất kỳ người hành nghề nào quan tâm đến lợi nhuận kinh doanh của mình. Tuy nhiên, vì giá mỗi mL chất làm đầy HA giảm xuống hơn một nửa so với đầu những năm 2000, nên giá chất làm đầy HA đã trở nên ít đáng lo ngại hơn đối với bác sĩ. Mặc dù vậy, giá của chất làm đầy HA cho mỗi ống tiêm vẫn rất quan trọng trong trường hợp làm đầy da mặt cần ít nhất 6–10 ml được sử dụng trong một lần. Về mặt này, nó giúp tạo ra sự cạnh tranh gay gắt trên thị trường nội địa vì giá của chúng đã giảm xuống còn 1/5–1/10 giá chất làm đầy HA nhập khẩu vào đầu những năm 2000. Nhiều nhãn hiệu chất làm đầy HA của Hàn Quốc thậm chí có giá 20–40 USD cho mỗi ống tiêm 1 mL nhưng vẫn đảm bảo cung cấp chất lượng tương đương. Điều này đã giúp phương pháp chất làm đầy HA có nhiều ưu điểm như phương pháp ghép mỡ tự thân ở Hàn Quốc và cuối cùng chất làm đầy HA có thể thay thế mỡ để làm căng da mặt.
Quá khó để quyết định lựa chọn chất làm đầy phù hợp giữa vô số các sản phẩm chất làm đầy HA trên thị trường. Tuy nhiên, việc lựa chọn chất làm đầy HA phù hợp cho một quy trình xét về nhiều mặt cũng tương tự như việc chọn đúng gậy đánh gôn trong một trận đấu. Tương tự như một gậy đánh bóng tốt chưa chắc đã là gậy gạt bóng tốt, nó là cả một nghệ thuật để chọn chất làm đầy HA hoàn hảo với đặc tính lưu biến phù hợp để có chỉ định phù hợp. Ngoài ra, giống như trong chiếc túi của người chơi gôn điển hình có chứa nhiều loại gậy chơi gôn của mỗi thương hiệu khác nhau, chẳng hạn như gậy sắt XXIO, gậy đánh bóng PING và gậy gạt bóng Scotty Cameron, người thực hành có thể cân nhắc sử dụng kết hợp các sản phẩm HA khác nhau từ các nhà sản xuất khác nhau miễn là cảm thấy thoải mái nhất khi sử dụng. Cá nhân tôi, thương hiệu chất làm đầy yêu thích mà tôi hầu như chỉ sử dụng trong hơn 10 năm đầu tiên thực hành các phương pháp điều trị bằng chất làm đầy mô mềm là Restylane®. Trong 5–6 năm qua, chất làm đầy Belotero® HA cũng là một sự lựa ưa chuộng. Về cơ bản, để chọn một chất làm đầy HA tốt nhất để sử dụng là sự đánh giá của mỗi học viên dựa trên nhiều yếu tố như mức độ thoải mái của họ với sản phẩm, vùng mục tiêu, mặt phẳng tiêm và đặc tính lưu biến của sản phẩm, tức là độ đàn hồi và tính liên kết của HA, mức độ nồng độ HA và mức độ liên kết chéo (Hình 2.16), v.v. Do đó, thường có nhiều trường hợp kết hợp các nhãn hiệu chất làm đầy HA khác nhau để điều trị các vùng mặt khác nhau của một bệnh nhân nhất định, ví dụ, bằng cách sử dụng Restyl-ane® cho mũi hoặc rãnh lệ kết hợp với Be-lotero® Volume cho vùng má trước hoặc má hóp. Ngoài ra, các sản phẩm HA khác nhau trong cùng dòng chất làm đầy HA có thể được áp dụng ở các tiểu vùng khác nhau của một vùng da mặt nhất định. Một ví dụ điển hình là việc sử dụng Belotero® Volume để làm phồng phần thân môi và Belotero® Balance để làm phồng viền môi.
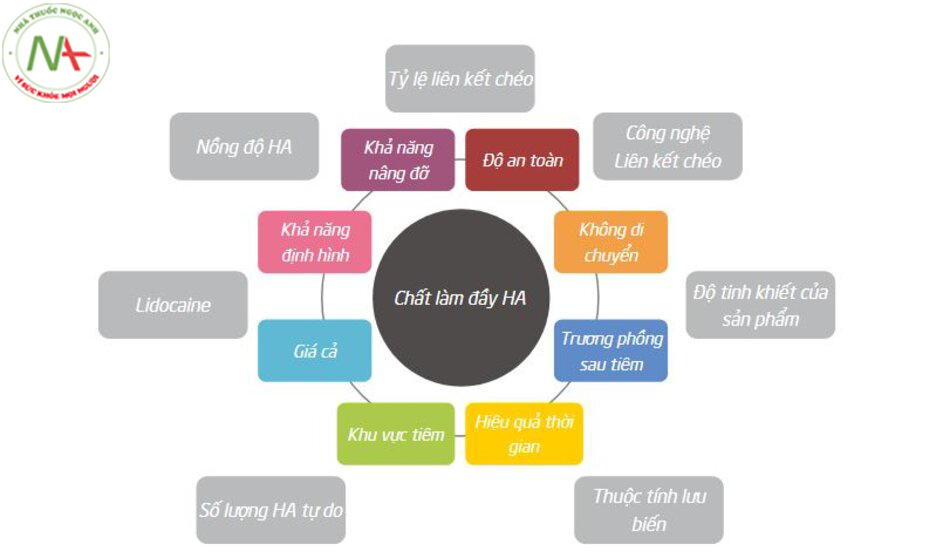
Lựa chọn chất làm đầy HA dựa trên vùng da mặt; Theo nguyên tắc chung, việc sử dụng chất làm đầy HA hai pha rắn với chỉ số G’ cao hơn, chẳng hạn như Restylane® được khuyên dùng để điều trị các vùng da mỏng bên trong như vùng quanh mắt, bao gồm bọng mắt dưới, rãnh lệ và mí mắt trên, để tránh hiện tượng trương phồng sau tiêm không thuận lợi do các phân tử HA hút nước. Vì lý do này, chất làm đầy HA hai pha rắn với G’ cao hơn cũng thích hợp để nâng sống mũi (nasal dorsum) nơi da cũng mỏng. Nói chung, các sản phẩm có G’ cao hơn, kích thước hạt lớn hoặc nồng độ HA cao hơn thích hợp cho các chỉ định yêu cầu tăng thể tích vì chúng cung cấp hỗ trợ cấu trúc tốt hơn dù nó là chất làm đầy HA đơn pha mềm hay chất làm đầy HA hai pha rắn. Mặt khác, các chất làm đầy HA một pha mềm với G ‘tương đối cao và độ kết dính cao như Belotero® Volume, Juvéderm® Voluma và Restylane® Volyme thường thích hợp để nâng các vùng có tính di động cao như vùng má hóp, rãnh mũi môi, trán và thái dương nơi chuyển động đáng kể bởi các chuyển động cơ bên dưới. Việc điều trị đôi môi nơi có kết cấu mềm mại, mượt mà khi chạm vào chỉ nên được thực hiện riêng với các sản phẩm HA một pha mềm có G ’thấp hơn như Belotero® Intense, Restylane® Kysse và Juverderm® Ultra XC. Ngược lại, chất làm đầy HA hai pha rắn được ưa chuộng ở những vùng như cằm và cầu mũi (nasal bridge), nơi mong muốn có kết cấu săn chắc, sắc nét.
Lựa chọn chất làm đầy HA dựa trên chất lượng da; Đối với những bệnh nhân có làn da mỏng, cần cân nhắc đến khả năng sờ / nhìn thấy sản phẩm, các sản phẩm có chỉ số G’ thấp hơn là thích hợp nhất. Các sản phẩm G’ thấp như BELOTERO® Intense, Restylane® Defyne, Juvéderm® Volift và Juvéderm® Ultra Plus XC mềm hơn và dễ dàng phân bố trong mô.
Lựa chọn chất làm đầy HA dựa trên mặt phẳng tiêm; Nói chung, các sản phẩm rắn hơn với chỉ số G’ cao hơn được chỉ định cho các mặt phẳng tiêm sâu hơn và mức độ hiệu chỉnh lớn hơn, trong khi các sản phẩm (mềm hơn) có G’ thấp hơn được chỉ định cho các mặt phẳng tiêm nông hơn và hiệu chỉnh ít nghiêm trọng hơn. Các sản phẩm có G’ cao thích hợp cho các chỉ định cần tăng thể tích vì chúng cung cấp hỗ trợ cấu trúc tốt hơn trong mô sâu. Đối với các khu vực như má, cằm và đường viền hàm, nơi để tiêm sản phẩm vào xương để nâng lên, các sản phẩm có G ‘cao hơn như BE-LOTERO® Volume, Restylane® Lyft và Ju-véderm® Voluma sẽ mang lại lợi thế lớn hơn so với sản phẩm G ‘thấp hơn vì nó sẽ có khả năng chống lại các lực nén vốn có trong mặt phẳng tiêm sâu hơn. Trong khi đó, các sản phẩm HA mềm hơn với G’ thấp hơn như BELOTERO Soft, Restylane® Skinbooster Vital, Restylane® Fynesse và Juvéderm® Volbella phù hợp để thực hiện các hiệu chỉnh trong da tốt hơn. Xem Lựa chọn chất làm đầy theo từng chỉ định để biết thêm chi tiết.
Tính chất lưu biến của chất làm đầy HA
Người ta thường nói một người thợ thủ công kém cỏi đổ lỗi cho các công cụ của mình; tuy nhiên, để trở thành một nghệ nhân bậc thầy cũng phụ thuộc vào sự hiểu biết về các công cụ của mình. Trong các phương pháp điều trị bằng chất làm đầy, việc lựa chọn HA phù hợp cho một chỉ định lâm sàng nhất định là bước khởi đầu để tạo ra kết quả thẩm mỹ tuyệt vời. Lựa chọn HA lý tưởng, theo nhiều khía cạnh, tương tự như việc chọn gậy đánh gôn phù hợp cho một cú đánh. Tương tự như một gậy đánh bóng tốt không nhất thiết là gậy gạt bóng tốt, nó là cả một nghệ thuật khi chọn chất làm đầy HA hoàn hảo với các đặc tính lưu biến phù hợp cho một chỉ định nhất định. Các vùng khác nhau trên khuôn mặt có độ dày, độ căng của da, hoạt động của cơ và mật độ mô khác nhau, nên mỗi chất làm đầy có vị trí tiêm khác nhau. Về mặt này, hiểu biết về các thuộc tính lưu biến của từng chất làm đầy là chìa khóa để quyết định sử dụng sản phẩm nào và ở đâu.
Lưu biến học, liên quan đến dòng chảy của vật chất, đặc biệt thích hợp với các quy trình chất làm đầy như gel HA vì vật liệu hai pha thể hiện các đặc tính của cả chất lỏng và chất rắn cùng một lúc. Lưu biến học nghiên cứu về các đặc tính liên quan đến nhau, sự hiểu biết về các đặc tính đó rất quan trọng đối với việc sản xuất và xử lý vật liệu trong nhiều ngành công nghiệp khác nhau, từ sơn, mực in, thuốc mỡ đến chất kết dính, thể hiện cả tính chất nhớt của chất lỏng và tính đàn hồi của chất rắn. Chất làm đầy gel HA cũng là một vật liệu hai pha bao gồm cả thành phần lỏng và rắn. Do đó, nhiều nghiên cứu đã tìm hiểu tính lưu biến của các chất làm đầy HA khác nhau để thiết lập đặc điểm lâm sàng của chúng và so sánh điểm mạnh và điểm yếu tương đối của chúng trong việc đạt được kết quả thẩm mỹ mong muốn. Hiểu được các đặc tính lưu biến này có thể giúp dự đoán trạng thái của các chất làm đầy HA khác nhau trong và sau khi cấy vào mô, do đó có thể lựa chọn tối ưu chất làm đầy HA cho một ứng dụng lâm sàng nhất định, dẫn đến việc hình thành thuật ngữ “điều chỉnh lưu biến” [11].
Cả trong và sau khi được cấy vào mô, HA phải chịu một loạt các lực biến dạng phức tạp, trong đó các sản phẩm khác nhau hoạt động khác nhau tùy theo các đặc tính lưu biến nội tại của chúng. Trong quá trình tiêm, chất làm đầy HA có thể bị biến dạng đứt gãy khi nó được tiêm ra từ ống tiêm qua mũi kim hoặc ống thông nhỏ. Sau khi được cấy vào mô, sản phẩm sau đó sẽ tiếp xúc với các ứng suất cơ học và cường độ khác nhau như trọng lực, lực kéo trượt do chuyển động của cơ mặt và lực nén do mô da bên dưới tác động. Trong số này, lực kéo bên có thể phát sinh trong hai trường hợp. Đầu tiên là khi chất làm đầy HA được đặt vào giữa hai lớp mô giải phẫu khác nhau, ví dụ giữa lớp mỡ sâu và mặt phẳng cơ như trường hợp tiêm sâu cho hõm má. Trong trường hợp này, mỗi lớp ngang tiếp xúc với HA lại có một mức độ ứng suất kéo trượt khác nhau tác dụng lên chất làm đầy HA được tiêm vào. Thứ hai là khi chất làm đầy HA được tiêm trong cùng một lớp mô giải phẫu, nhưng phần HA nằm gần bề mặt cơ hơn sẽ bị kéo và cắt thành nhiều phần. Trong khi đó, lực nén là một lực biến dạng dọc tác dụng lên chất làm đầy HA, được tạo ra do các mô bên dưới da khi khuôn mặt trạng thái tĩnh và do cơ mặt khi khuôn mặt ở trạng thái động. Đa số lực nén tác động lên HA được truyền vào các mặt phẳng sâu như lớp thượng bì hoặc lớp dưới da nhiều hơn so với lớp thượng bì. Khả năng chống lại các lực biến dạng khác nhau và giữ được hình dạng ban đầu mà không bị dịch chuyển khỏi vị trí được cấy ghép là yếu tố thiết yếu của chất làm đầy HA tăng thể tích.
Độ đàn hồi
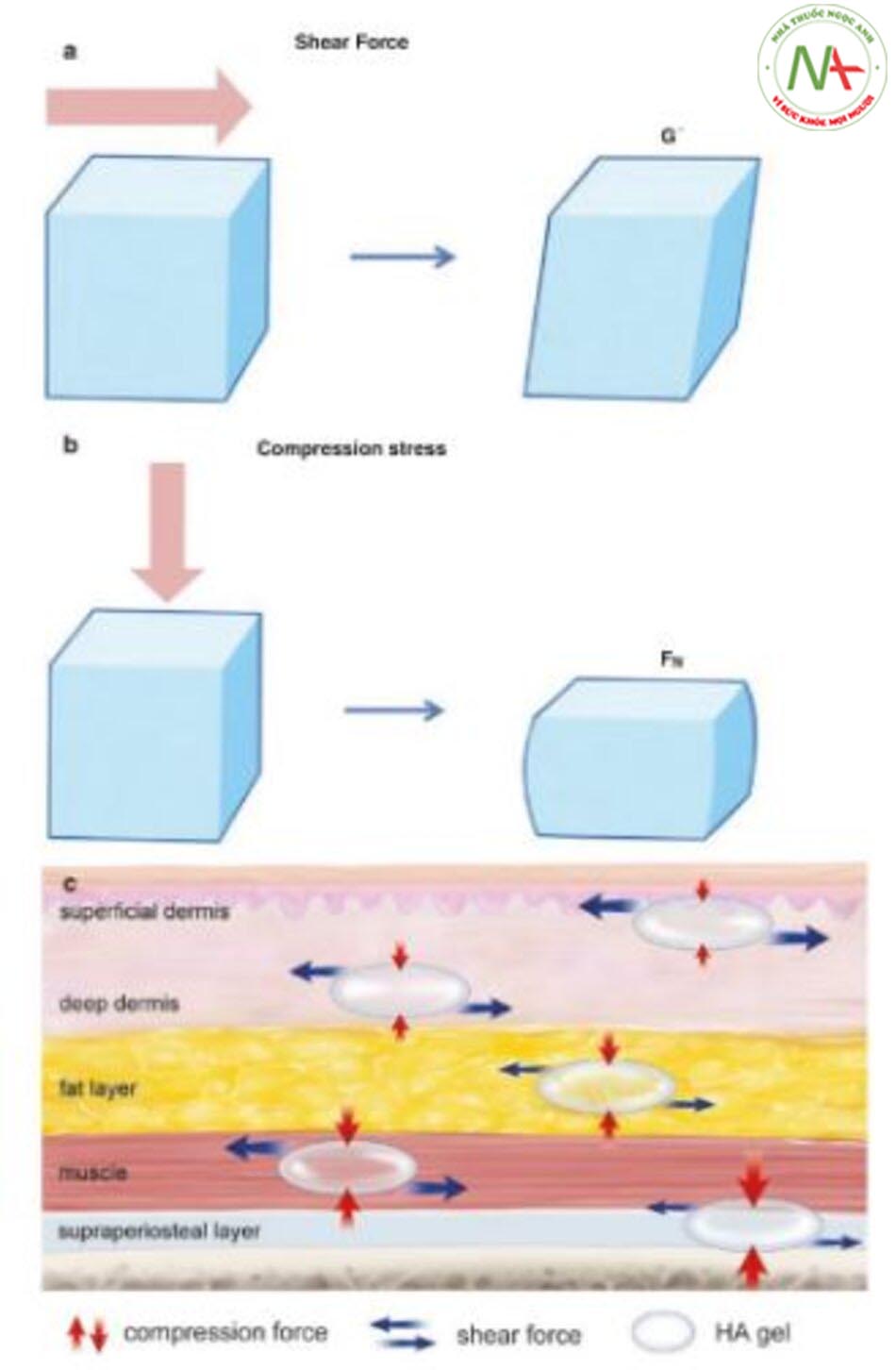
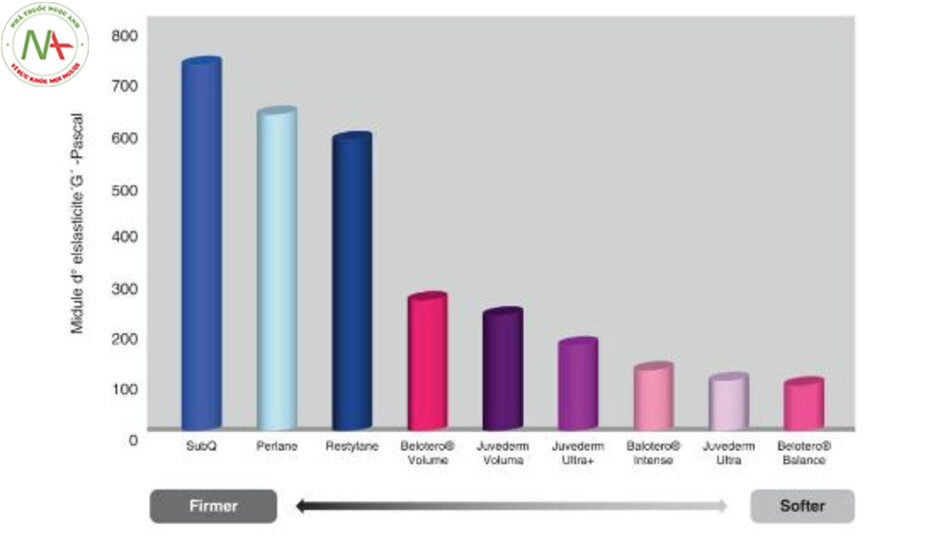
Tính đàn hồi thể hiện khả năng khôi phục lại hình dạng ban đầu của gel sau khi bị biến dạng, là đặc tính lưu biến quan trọng nhất đối với chất làm đầy. Ví dụ, nút tai dùng một lần làm bằng polyurethane có đặc điểm là có độ đàn hồi cao trong khi mật ong thì không. Ngoài ra, trong khi cả hai đều là gel, bánh gelatin có độ đàn hồi cao hơn so với bánh pudding sô cô la (Hình 2.17). Độ đàn hồi của chất làm đầy HA có thể được biểu thị bằng cách sử dụng các thông số lưu biến khác nhau tùy theo loại lực biến dạng được áp dụng. Tính đàn hồi của gel khi chịu lực ép (tức là ứng suất ngang) được biểu thị bằng chỉ số đàn hồi (G ‘), đo độ cứng hoặc độ rắn của gel và do đó nó có khả năng chống lại sự biến dạng khi có sự tác dụng của lực kéo trượt (Hình 2.18a). Mặt khác, độ đàn hồi của gel khi bị nén (tức là ứng suất thẳng đứng) được đo bằng phản lực (FN) ở chế độ tĩnh và bằng chỉ số đàn hồi (E ′) trong quá trình chuyển động của cơ mặt, nghĩa là ở chế độ động [12] (Hình 2.18b). Mức độ mạnh của các lực động khiến sự biến dạng của các chất làm đầy axit hyaluronic khác nhau tùy thuộc vào mặt phẳng tiêm. Trong khi lực kéo trượt mạnh hơn ở mặt phẳng bề ngoài (hạ bì) và lớp cơ, lực nén mạnh hơn ở các mặt phẳng sâu hơn (lớp mỡ dưới da sâu và lớp thượng bì) (Hình 2.18c). Các yếu tố khác nhau có thể ảnh hưởng đến G ‘và E ′ của chất làm đầy HA, bao gồm nồng độ HA, mức độ liên kết chéo, tỷ lệ BDPE liên kết đôi / kiểu dây móc (liên kết đơn) trong gel, tỷ lệ HA dạng tự do trong gel và quy trình sản xuất được sử dụng. Nói chung, gel HA có nồng độ HA và mức độ liên kết chéo cao hơn thì có G’ cao hơn, trong khi những loại gel có thành phần BDPE liên kết đơn hoặc HA dạng tự do cao hơn thì có G ’thấp hơn. Ngoài ra, với kích thước hạt bằng nhau, gel HA hai pha thường có G ’cao hơn so với HA đơn pha (Hình 2.19). Về mặt ý nghĩa lâm sàng, các sản phẩm có chỉ số đàn hồi G ’cao không thích hợp cho những vùng cần cảm giác mịn, đều như môi vì bạn không mong muốn có thể sờ thấy kết cấu gel cứng, chắc. Ngược lại, các sản phẩm có G ’cao hơn có thể nâng đỡ hiệu quả hơn do có xu hướng không lan rộng và giữ nguyên hình dạng ban đầu trong khu vực được cấy ghép (Hình 2.20). Do đó, chúng thường xuyên được sử dụng trong thực hành lâm sàng để nâng thể tích trong các mặt phẳng mô sâu. Nói tóm lại, G’ cao hơn tức là vật liệu có khả năng nâng đỡ lớn hơn như đã được chứng minh lâm sàng trong nghiên cứu về mặt phân chia có kiểm soát của Monheit et al. thực hiện trên 140 bệnh nhân [17]. Các quan sát tương tự cũng thu được đối với các thông số nén FN và E ′, với các chỉ số FN và E ′ cao hơn tương quan với khả nang tăng thể tích cao hơn [12]. Điều đó cho thấy rằng, các sản phẩm cứng hơn, có độ đàn hồi cao hơn đòi hỏi lực tiêm lớn hơn trong quá trình tiêm, cũng như việc sử dụng kim hoặc ống tiêm lớn hơn, dày hơn. Ngoài ra, vì những sản phẩm này không có khả năng tạo khuôn và trải rộng dễ dàng, nên chúng được tiêm vào các mặt phẳng mô sâu hơn là ở các lớp bề mặt.
Độ nhớt
Độ nhớt được định nghĩa là khả năng của chất lỏng chống lại sự biến dạng hoặc xu hướng kết dính lại với nhau mà không bị phân mảnh khi bị tác động. Ví dụ, bơ để trong tủ lạnh hoặc bơ đậu phộng có độ nhớt cao và do đó không dễ dàng phết lên bánh mì nướng, trong khi bơ ở nhiệt độ phòng có độ nhớt thấp và do đó dễ dàng miết theo bề mặt khi phết (Hình 2.21). Độ nhớt được đo bằng mô đun nhớt (G ′′) hoặc độ nhớt phức hợp (η *) về khả năng biến dạng kéo trượt và bằng mô đun nhớt (E ′′) về biến dạng nén. Độ nhớt phức hợp (η *) mô tả khả năng gel chống lại biến dạng trượt bên ngoài; hay nói cách khác là khả năng chống lại việc bị lan trải. Khi lực trượt nằm trong một phạm vi nhất định (trong phạm vi đàn hồi tuyến tính), η * giảm tương ứng với sự gia tăng của ứng suất trượt[11]. Chỉ số nhớt (G ′′) ’là thước đo khả năng tiêu hao năng lượng của gel dưới tác động của lực kéo trượt (Hình 2.22). Trong phạm vi nhớt đàn hồi tuyến tính, G ′′ tương đối giống, nếu không muốn nói là hoàn toàn giống với độ nhớt phức (η *). Tuy nhiên, đối với chất làm đầy HA hai pha, η * được coi là chỉ số chính xác hơn G ′′ để dự đoán trạng thái lâm sàng của chúng và do đó được sử dụng rộng rãi hơn [11].



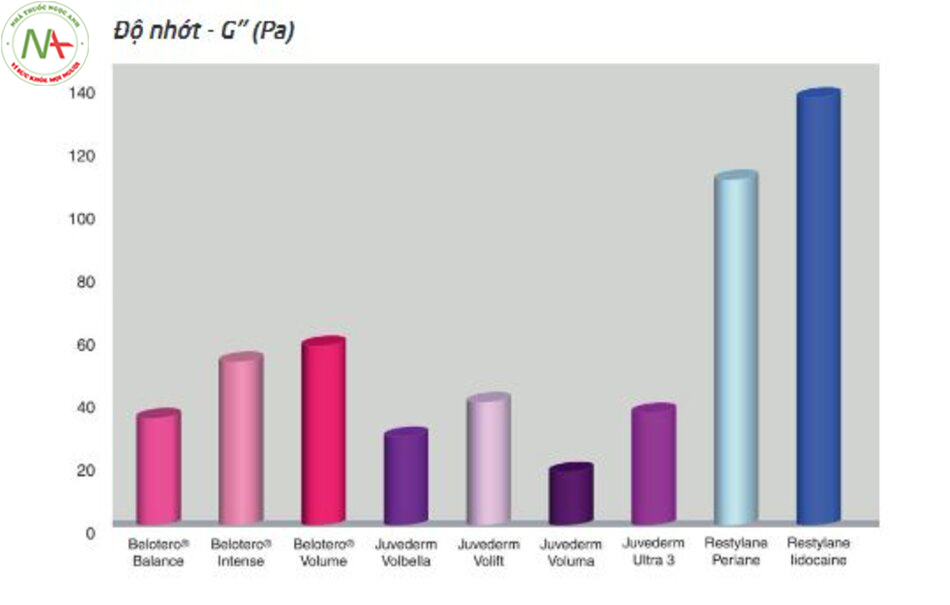
Trong khi chất làm đầy HA có độ nhớt cao hơn cần lực tiêm lớn hơn vì chúng không bơm trơn tru, khi được cấy vào mô, chúng có thể chống lại một lượng lớn ứng suất trượt mà không bị lan trải, do đó đảm bảo duy trì hình dạng và tính toàn vẹn của cấu trúc.
Điều này chứng tỏ chúng rất phù hợp để tiêm vào những vùng cơ mặt vận động nhiều hoặc trong các mặt phẳng mô sâu nơi chúng có thể cung cấp khả năng tăng thể tích sâu. Ngược lại, chất làm đầy HA dạng lỏng hơn với độ nhớt ít hơn sẽ dễ dàng tiêm và chảy đều hơn qua mô và do đó thích hợp để tiêm vào lớp hạ bì nông. Trong nghiên cứu của Rosamilia et al. [18]dựa trên dòng sản phẩm chất làm đầy HA của Belotero®, Belotero® soft, một sản phẩm mềm hơn với độ nhớt thấp hơn, được chứng minh là dễ lan trải vào mô hơn so với Belotero® Volume™, một sản phẩm ít lỏng hơn nhưng có độ nhớt cao hơn. Trong khi đó, chất làm đầy HA hai pha, với dạng hạt trong vật chất, thường được biết là có độ nhớt cao hơn HA đơn pha [19]. Dựa trên sự khác biệt về lưu biến như vậy, khi được tiêm trong da trong lớp hạ bì, Belo-tero® Balance™ dưới dạng HA đơn pha đã được chứng minh là có sự tích hợp đồng nhất hơn trong mô so với Restylane® hai pha với độ nhớt cao hơn [14].
Tan Delta (δ)
Vì chất làm đầy là vật liệu nhớt đàn hồi có các đặc tính của cả độ nhớt và độ đàn hồi, trạng thái của chúng không thể được xác định một cách thích hợp dựa trên một thông số đặc tính của chất rắn hoặc chất lỏng. Sự hiểu biết này đã dẫn đến việc đề xuất các tính toán lưu biến thứ cấp khác nhau xuất phát từ các thông số lưu biến chính. Trong số này, tan delta (δ) là một chỉ số được sử dụng tương đối phổ biến, đo tỷ số giữa độ nhớt G” trên độ đàn hồi G’ (G ”/ G’) trong một vật liệu nhất định [11]. Nói cách khác, tan δ là một mô đun phức tạp xem xét sự cân bằng tổng thể của độ đàn hồi và độ nhớt của gel HA nhất định. Giá trị tan δ nhỏ hơn 1 biểu thị rằng sản phẩm có tính đàn hồi hơn tính nhớt, trong khi tan δ lớn hơn 1 biểu thị độ nhớt lớn hơn độ đàn hồi. Vì hầu hết các chất làm đầy HA có tính đàn hồi hơn là tính chất lỏng, giá trị tan của chúng thường nhỏ hơn 1, với một số chất làm đầy cứng hơn, đàn hồi hơn cho thấy giá trị tan thậm chí còn thấp hơn 0,2. Ngay cả trong cùng một dòng chất làm đầy HA, các sản phẩm được chỉ định để nâng thể tích sâu có giá trị tan δ thấp hơn. Trong khi đó, tan δC (E ′′ / E ′) là mô đun đàn hồi nhớt tương ứng để mô tả đặc tính của gel khi chịu lực nén tác dụng [12]. Tuy nhiên, giá trị tan δC (E ′′ / E ′) thường khác giá trị tan δ (G ”/ G ‘) ở chỗ giá trị tan δC nhỏ hơn 1 đối với dòng sản phẩm Belotero® và Ju-véderm® của dòng Hylacross™ Ultra™, tức là các sản phẩm có giá trị tan cao; 1–2 cho các sản phẩm của dòng VYCROSS™; và lớn hơn 3 đối với dòng sản phẩm Restylane® có giá trị tan thấp nhất trong số các sản phẩm được thử nghiệm (nghĩa là nhỏ hơn 0,2). Từ đó, HA hoạt động khác nhau dưới ứng suất kéo trượt so với khi nén [11]. Cũng cần lưu ý rằng HA đặt trong mô sâu không chỉ tiếp xúc với ứng suất trượt mà còn chịu lực nén, với lượng lực nén ở mặt phẳng sâu lớn hơn ở lớp bề mặt.
Tính liên kết
Tính liên kết mô tả xu hướng không phân ly của vật liệu do lực hút bên trong của các phân tử với nhau. Ví dụ, mật ong là một vật liệu có tính kết dính cao, trong khi các hạt cát kém kết dính hơn nhiều (Hình 2.23). Tính liên kết của chất làm đầy HA thể hiện mức độ nguyên vẹn của nó trong mô mà không bị phân tách sau khi cấy ghép.
Để có một quy trình đánh giá khách quan, độ gắn kết của chất làm đầy HA được đo bằng thang điểm trực quan tiêu chuẩn hóa 5 điểm được gọi là Thang đo liên kết Ga-vard-Sundaram (“Thang đo liên kết GS”). [13]Thang đo độ liên kết GS dao động giữa giá trị 1 (phân tán hoàn toàn) và 5 (liên kết hoàn toàn) (Hình 2.24). Nhìn chung, với kích thước hạt giống hệt nhau, chất làm đầy HA hai pha có xu hướng kém kết dính hơn chất làm đầy HA đơn pha. Chất làm đầy HA hai pha Restylane® có độ gắn kết là 1 trên Thang đo độ liên kết GS, trong khi chất làm đầy HA đơn pha Belotero® Bal-ance™ có độ gắn kết cao nhất là 5 [12, 13]. Ngay cả trong số các chất làm đầy HA một pha, vẫn có sự khác biệt đáng kể về mức độ gắn kết của chúng, phản ánh sự khác biệt trong quy trình sản xuất. Ví dụ: trong cùng dòng chất làm đầy HA của Juvéderm, uvé-derm® Ultra Plus™ (Juvéderm® Ultra 3™) với công nghệ HYLACROSS™ có độ gắn kết là 4, trong khi Juvéderm® Voluma™ với công nghệ VYCROSS™ có độ liên kết thấp hơn đáng kể là 1 [12].
Ý nghĩa lâm sàng đáng chú ý nhất của tính liên kết nằm là hỗ trợ khả năng nâng của chất làm đầy HA, cũng như tính đàn hồi. Điều này đã được chứng minh trong nghiên cứu so sánh hiệu quả điều trị rãnh mũi môi bằng Belotero® Intense và Restyl-ane® Lyft ở 20 đối tượng [20]. Hiển nhiên, độ đàn hồi là yếu tố quan trọng quyết định khả năng nâng của chất làm đầy axit hy-aluronic. Vì vậy, nghiên cứu trên rất đáng chú ý ở chỗ nó đã chứng minh rằng Belo-tero® Intense với G ‘ là 111 Pa (o,7 Hz) có thể mang lại hiệu quả nâng đỡ tương đương với Restylane® Lyft có G’ là 549 Pa. Do đó, có thể thừa nhận rằng, mặc dù có chỉ số G’ thấp hơn, Belotero® Intense vẫn có thể sánh vai với Restylane® Lyft một cách hiệu quả nhờ độ gắn kết là 4, cao hơn đáng kể so với độ gắn kết của Restyl-ane® Lyft là 1. Tính liên kết về khả năng nâng thể tích của chất làm đầy đặc biệt có ảnh hưởng đến việc điều trị các khu vực có tính di động cao như rãnh mũi môi, rãnh môi hàm và trán. Theo kinh nghiệm của tôi, các sản phẩm có độ kết dính thấp như Restylane® SubQ thường dễ bị vón cục hoặc tách lớp khi bị kéo trượt bởi cơ hoạt động mạnh ở những khu vực này, trong khi Belotero® Volume có xu hướng giữ nguyên hình dạng và vị trí ban đầu hiệu quả hơn. Để dễ hình dung, những khác biệt như vậy cũng tương đương về sức nâng giữa Belo-tero® Intense và Restylane® Lyft, mặc dù chỉ số đàn hồi kéo trượt (G’) của dòng sản phẩm Belotero® thấp hơn nhiều.

![Chất làm đầy nâng da mặt gồm những loại nào? Quy trình sản xuất? 128 Hình 2.24 Thang đo liên kết GS *. (a) Restylane®; Độ liên kết 1 ở giây thứ 90 (phân tán hoàn toàn). (b) Belotero® Balance; Độ liên kết 5 ở giây thứ 90 (hoàn toàn liên kết). * Thang đo liên kết Gavard-Sundaram (Tham khảo [13])](https://nhathuocngocanh.com/wp-content/uploads/2022/07/chat-lam-day-nang-da-mat-gom-nhung-loai-nao-quy-trinh-san-xuat-anh-24.jpg)
Ý nghĩa lâm sàng (Bảng 2.3)
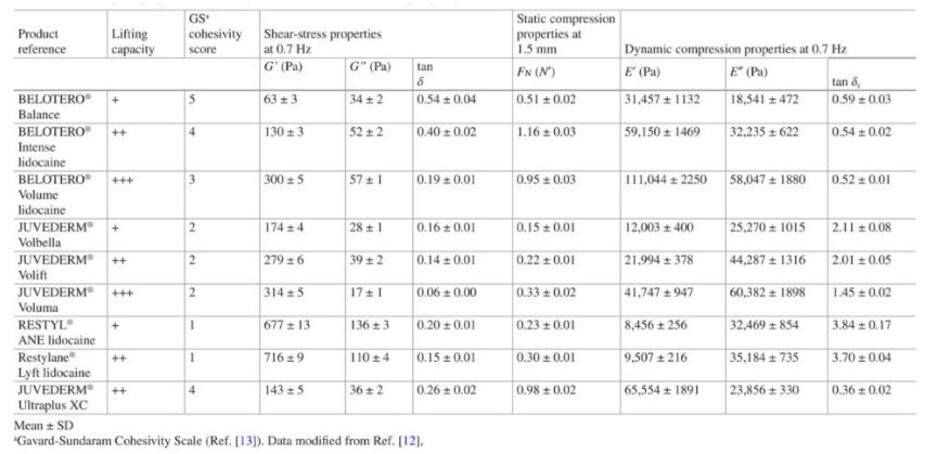
Có thể rất khó để so sánh lưu biến trực tiếp giữa các sản phẩm với các quy trình sản xuất khác nhau. Thật vậy, người ta thường thấy cùng một sản phẩm hiển thị các giá trị lưu biến khác nhau trong các nghiên cứu khác nhau tùy thuộc vào các thông số thử nghiệm cơ bản được áp dụng. Do đó, khi đánh giá tính lưu biến của các gel HA khác nhau, việc so sánh các sản phẩm trong cùng một dòng thương hiệu sẽ phù hợp hơn là giữa các dòng khác nhau. Giá trị đo lường của các sản phẩm thuộc các nhãn hiệu khác nhau chỉ hữu ích chỉ khi chúng có xu hướng hoặc kiểu mẫu chung.
Chất làm đầy dày hơn, rắn hơn với độ nhớt cao thường khó tiêm hơn và do đó yêu cầu sử dụng kim hoặc ống tiêm dày hơn. Ví dụ: mặc dù Belotero® Volume dưới dạng gel một pha vẫn có thể đi qua kim 30-G vì việc tiêm đẩy HA một pha không bị hạn chế bởi kích thước của dụng cụ tiêm, nhưng Belotero® Volume dường như cứng hơn nhiều khi đẩy qua ống tiêm 25-G so với ống tiêm 23-G dày hơn.
Các sản phẩm lỏng mềm có độ nhớt thấp như Restylane® Vital, Belotero® Soft và Juvéderm® Volbella thích hợp để tiêm bề mặt trong lớp hạ bì vì chúng sẽ dễ dàng lan truyền qua mặt phẳng mô. Nói chung, chất làm đầy HA một pha mềm có G ’thấp hơn như Belotero® Soft và Juvéderm® Volbella chảy đều hơn và tích hợp đồng nhất vào mô, do đó tạo ra ít bất thường hoặc rối loạn hơn HA hai pha có kết cấu dày hơn và cứng hơn. Mặt khác, khả năng lan trải cao hơn có nghĩa là chất làm đầy HA đơn pha mềm có diện tích bề mặt tiếp xúc với các gốc tự do và enzym hyaluroni-dase nội sinh nhiều hơn đáng kể so với HA hai pha rắn, dẫn đến sự thoái biến nhanh hơn. Thật vậy, theo kinh nghiệm của tôi, khi Restylane® và Belotero® được sử dụng để tiêm trong da ở các rãnh mũi môi (thông qua kỹ thuật tiêm kiểu lá dương xỉ) hoặc trên da mặt (thông qua kỹ thuật tiêm cấp ẩm nâng cơ), Restylane® dường như có thời gian tác dụng dài hơn, kéo dài hơn 1 năm trong khi Belotero® Balance dường như tồn tại trong thời gian ngắn hơn. Quan sát này tương đồng với những phát hiện từ nghiên cứu của Tran và cộng sự, so sánh sự tích hợp sinh học của các chất làm đầy HA khác nhau trong lớp hạ bì dựa trên đặc tính đàn hồi nhớt của chúng. Theo nghiên cứu, dù Belotero® Balance được chứng minh là cung cấp sự tích hợp đồng nhất hơn trong mô, nó dường như có ít sản phẩm còn lại sau 118 ngày so với Restylane® [14].
Do đó, cách tiếp cận ưa thích của tôi khi thực hiện phương pháp điều trị tiêm cấp ẩm (hydrolifting) là sử dụng Belote-ro® Balance ở những bệnh nhân có làn da mỏng hoặc lão hóa do ánh sáng hoặc ở những vùng da mặt có mô mỏng bao phủ như vùng quanh mắt; và sử dụng Restyl-ane® hoặc Restylane® Vital ở những bệnh nhân có da dày bình thường.
Trong khi đó, với mục đích là nâng da và tăng thể tích, bạn nên chọn chất làm đầy HA dày hơn, chắc hơn như Restyl-ane® Lyft, Belotero® Volume và Juvé-derm® Voluma có giá trị G ’cao nhất trong các sản phẩm. Restylane® Lyft là chất làm đầy HA hai pha có độ đàn hồi cao và do đó có kết cấu gel khá cứng, phù hợp hơn để đặt ở những vùng xương nằm ngay dưới da, vì nó sẽ không có vấn đề gì khi sờ thấy sản phẩm cứng này. Một lưu ý thêm khi sử dụng Restylane® Lyft là do độ gắn kết tương đối thấp của dòng chất làm đầy HA Restylane®, nên nó thường được tiêm ở những khu vực ít di động như sống mũi, đường viền hàm và má bên, nơi mà sản phẩm không chịu lực co mạnh mẽ của các cơ xung quanh. Đáng chú ý, vùng thái dương có thể được điều trị bằng cách sử dụng HA hai pha hoặc một pha, dù cơ thái dương có co giãn liên tục, vì băng cơ thái dương dày đè lên trên chất làm đầy ngăn cản việc tạo ra các bất thường có thể nhìn thấy được. Trong khi đó, HA đơn pha đặc với độ kết dính cao như Belotero® Volume thường thích hợp cho các vùng siêu động ở trán, má, cằm, rãnh mũi môi, rãnh môi hàm và má trước.
Chất làm đầy HA đơn pha là chất làm đầy mềm với độ nhớt ít hơn, rất lý tưởng để đặt vào những vùng như môi và má nơi cần mềm và mịn. Mặt khác, chất làm đầy HA hai pha rắn hơn và đàn hồi hơn phù hợp để tiêm vào những vùng mà có xương ở bên dưới có thể sờ thấy trực tiếp, chẳng hạn như sống mũi, đường viền hàm và má. Trong khi xét về độ giãn rộng, trán cũng có thể được coi là một khu vực thích hợp để điều trị bằng HA hai pha, nhưng trên thực tế, điều đó lại không đúng. Thay vào đó, do khu vực này có hoạt động của cơ và không gian hạn chế để có thể tiêm chất làm đầy, HA đơn pha mềm hơn với độ gắn kết cao hơn và tích hợp mô đồng nhất hơn là một lựa chọn tốt để nâng da trán. Mặt khác, chất làm đầy HA hai pha phù hợp để tiêm ở những vùng da mỏng như vùng quanh mắt, bao gồm bọng mắt dưới và rãnh lệ, do tính chất của chất làm đầy HA đơn pha có G’ thấp hơn để giữ nước khi được tiêm vào các vùng này.
Trong khi đó, khi chất làm đầy HA được tiêm nhanh vào lớp hạ bì hoặc lớp dưới da, nó có thể tạo ra hiệu ứng Tyndall (Hình 2.25), một sự đổi màu hơi xanh có thể nhìn thấy bằng mắt do sự tán xạ ánh sáng ưu tiên bởi chất làm đầy HA được tiêm vào nông. Hiện tượng này, được gọi chính xác hơn là “tán xạ Rayleigh”, xảy ra khi ánh sáng truyền qua không khí hoặc chất lỏng bị phân tán bởi không khí hoặc các hạt nước có kích thước nhỏ hơn bước sóng ánh sáng [21]. Khi nó xảy ra, ánh sáng có bước sóng ngắn hơn bị tán xạ mạnh hơn nhiều; do đó, ánh sáng xanh lam, có bước sóng ngắn, được ưu tiên phản xạ trở lại mắt.
Bảng 2.3 Ý nghĩa lâm sàng của các đặc tính lưu biến (xem từng chỉ định)
| Chỉ định | Khu vực | Các đặc tính lưu biến thích hợp | Khuyến nghị |
| Nâng dưới vùng da mỏng | Rãnh lệ
Rãnh mí mắt – má |
Hai pha, độ nhớt thấp đến trung bình | Restylane®,Restylane® Skinbooster Vital |
| Tiêm Nội bì
Tiêm cấp ẩm Kỹ thuật tiêm kiểu lá dương xỉ |
Vùng da dày | Đơn pha hoặc hai pha với độ nhớt thấp | Belotero® Balance,Restylane® Skinbooster Vital, Juvéderm® Volbella |
| Vùng da mỏng (vùng quanh mắt và cổ) | Đơn pha với độ nhớt thấp | Belotero® Soft | |
| Tăng thể tích và nâng da | Vùng thái dương | Giá trị G ’cao nhất trongtừng phạm vi sản phẩm | Restylane® Lyft,Restylane® Volym, Belotero® Volume, Juvéderm® VolumaJuvéderm® Volux |
| Khu vực siêu động Trán, Rãnh mũi môi,Rãnh môi hàm Cằm | Đơn pha với độ đàn hồi và tính liên kết cao | Belotero® VolumeJuvéderm® VolumaJuvéderm® Volux | |
| Sống mũi | Hai pha với độ đàn hồi cao | Restylane® Lyft | |
| Đường viền hàm và má bên | Đơn pha hoặc hai pha với độ đàn hồi cao | Restylane® Lyft,Restylane® Volume,Belotero® Volume, Juvéderm® Voluma | |
| Phân lớp kép | Lớp sâu | Hai pha với độ đàn hồi cao | Restylane® Lyft |
| Lớp bề mặt | Đơn pha với độ đàn hồi cao | Belotero® Volume |
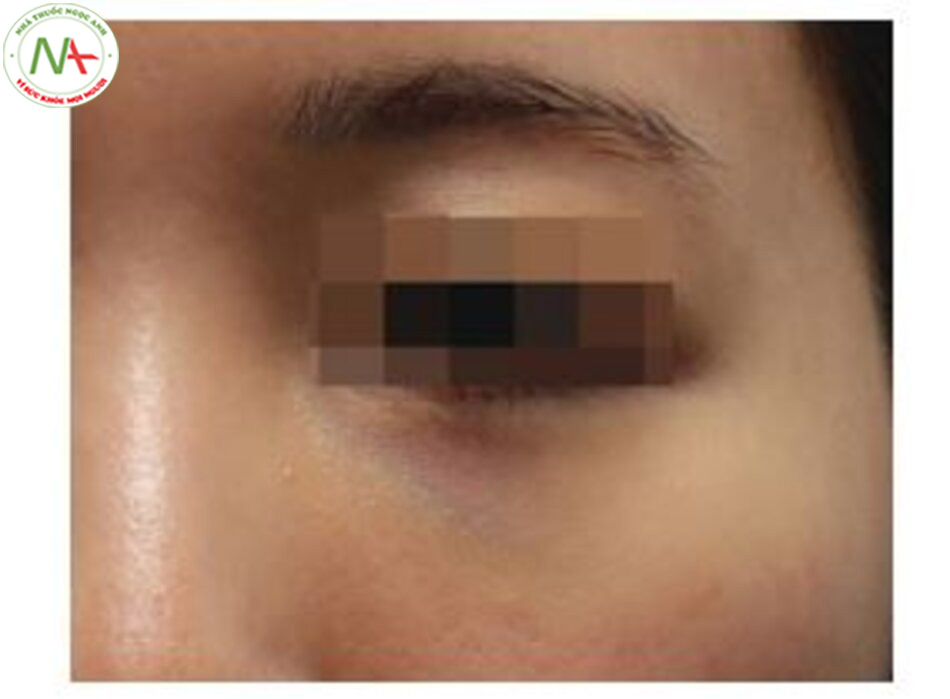
Điều này giải thích tại sao bầu trời có màu xanh lam, cũng như nước trong một cái ao trong vắt. Để so sánh, hiệu ứng Tyndall được nhìn thấy khi ánh sáng tạo ra chùm sáng có thể nhìn thấy được khi truyền qua chất kết dính có đường kính hạt từ 1 đến 1000 nm [22]. Chính vì lý do đó mà đèn pha ô tô khi gặp sương mù sẽ tạo ra chùm sáng. Do đó, mặc dù tán xạ Rayleigh nên là thuật ngữ thích hợp, nhưng thuật ngữ hiệu ứng Tyndall được sử dụng thường xuyên hơn để mô tả màu hơi xanh khó coi xuất hiện khi tiêm chất làm đầy HA, chúng tôi vẫn sẽ gọi hiện tượng này là hiệu ứng Tyndall để tiện cho việc thảo luận. Hiệu ứng Tyndall xảy ra thường xuyên nhất nếu chất làm đầy HA được đặt quá nông ở lớp hạ bì hoặc với số lượng lớn dưới da ở những vùng da mỏng manh trên khuôn mặt như bọng mắt hoặc rãnh lệ. Mặc dù có đề xuất rằng Belo-tero® có xu hướng tạo ra ít Tyndalling hơn khi được tiêm vào vùng quanh ổ mắt có da mỏng như ở bọng mắt và rãnh lệ, chúng ta cần chú ý khi giải thích những phát hiện này. Giả thuyết cơ bản của phát hiện này là không giống như HA hai pha đã có khuôn mẫu phân bố siêu hạt khi được tiêm vào mô da, Belotero® có độ nhớt thấp và tính liên kết yếu cho phép nó lan ra qua lớp hạ bì theo mô hình đồng nhất, mượt mà hơn, mà không có các hạt chất làm đầy riêng rẽ gây ra khả năng tán xạ ánh sáng xanh [11].
Tuy nhiên, nó chỉ ra rằng, trong thực hành lâm sàng, việc chỉnh sửa rãnh lệ được thực hiện bằng cách đặt một lớp thể tích nhỏ xuống dưới da bằng kỹ thuật rút ngược chỉ tuyến tính, trái ngược với tiêm da ở lớp hạ bì bề mặt. Theo cơ sở này, thật khó để kết luận Belotero® có lợi hơn so với các sản phẩm khác khi chỉnh sửa rãnh lệ. Điều tương tự cũng áp dụng cho trường hợp nó được sử dụng để nâng bọng mắt, trong đó chất làm đầy được tiêm vào mức dưới da trong quá trình rút kim.
Thay vào đó, theo kinh nghiệm của riêng tôi, tôi đã quan sát các trường hợp Tyndalling sau khi tiêm Belotero® Vol-ume™ với thể tích lớn (> 1 mL) vào dái tai. Dựa trên kinh nghiệm lâm sàng này, tôi cho rằng không có sản phẩm nào mà hoàn toàn không có nguy cơ bị Tyndalling khi được tiêm vào những vùng có mô mỏng hoặc với khối lượng lớn ở mô dưới da. Đúng như vậy, Belotero® đã được chứng minh là tạo ra ít Tyndalling hơn ở lớp hạ bì bề ngoài. Tuy nhiên, khi nói đến nâng thể tích rãnh lệ hoặc bọng mắt, lớp hạ bì nông không phải là độ sâu mục tiêu của mũi tiêm. Nếu không, tính ưa nước của HA một pha sẽ tạo ra nguy cơ Tyndalling ở những khu vực này; và như vậy, thay vào đó, chất làm đầy HA hai pha có thể là một lựa chọn tốt hơn, mặc dù đây vẫn còn là một chủ đề một nghiên cứu trong tương lai.
Restylane®, một HA hai pha, có kết cấu gel chắc, khá cứng, cho thấy độ nhớt và G’ cao và có khả năng nâng mô tốt, ít lan rộng hơn. Mặc dù độ nhớt đàn hồi cao khiến cho dòng chảy không được trơn tru trong quá trình tiêm và độ lan tỏa gel thấp làm cho nó khó định hình hơn, nhưng với khả năng nâng mô cao, nó vẫn là sản phẩm lý tưởng để tiêm trong mặt phẳng mô sâu, nơi nó có thể nâng cấu trúc tốt.
Khi được sử dụng cho kỹ thuật phân lớp kép, HA hai pha như Restylane® có thể được kết hợp với việc tiêm HA đơn pha trong lớp bề mặt để có kết quả tối ưu. Chất làm đầy HA đơn pha có tính dễ dát mỏng và do đó nó rất phù hợp cho lớp bề mặt. Ví dụ, khi nâng má trước dưới hốc mắt, trước tiên có thể tiêm HA hai pha vào mặt phẳng mô sâu để có thể tích và lực nâng tổng thể và sau đó, tinh chỉnh lại bất kỳ chỗ lõm nào còn lại trên bề mặt bằng HA một pha trong mặt phẳng bề mặt (Bảng 2.4).
Bảng 2.4 Chất làm đầy HA với khả năng tăng thể tích cao hơn
| Tên thương mại | Restylane® Lyft™ | Restylane® Volyme™ | Juvéderm® VOLUMA™ | Juvéderm® VOLUMA™ | Belotero® Volume™ |
| Nhà sản xuất | Galderma(Sweden) |
Galderma(Sweden)
|
Allergan(France) | Allergan(France) | Merz(Switzerland) |
| Công nghệ sản xuất | NASHA™ | OBT™ | Vycross™ | Vycross™ | CPM™ |
| Đơn pha hay hai pha | Hai pha | Đơn pha | Đơn pha | Đơn pha | Đơn pha |
| Nồng độ HA | 20 mg/mL | 20 mg/mL | 20 mg/mL | 25 mg/mL | 26 mg/mL |
| MoD(%) | nhỏ hơn 1%a | 6-8% | 4% | 6-7% | 5.1%a |
| Kim tiêm | 29G ½” | 29G ½” | 29G ½” | 29G ½” | 27G ½”
30G ½” |
| Mức độ tiêm | Dưới da / Trên xương/ Lớp hạ bì sâu | Dưới da / Trên xương | Dưới da / Trên xương/ Lớp hạ bì sâu | Dưới da / Trên xương | Lớp hạ bì sâu/ Dưới da / Trên xương/ |
| Tên thương mại | YVOIRE ® Y-Solu-tion™ 720 | YVOIRE ® Contour™ | YVOIRE® Contour™ | e.p.t.q.®S500™ |
| Nhà sản xuất | LG Chem (Korea) | LG Chem (Korea) | Medytox (Korea) | JETEMA (Korea) |
| Công nghệ sản xuất | S-HICE™ | HICE™ | SHAPE™ | 2CM™ |
| Đơn pha hay hai pha | Hai pha | Hai pha | Đơn pha | Đơn pha |
| Nồng độ HA | 20 mg/mL | 22 mg/mL | 20 mg/mL | 24mg/mL |
| MoD(%) | 3.3% | 2.0% | Chưa rõ | 1.89% |
| Kim tiêm | 27G ½” | 23G ½” | 27G ½” | 27G ½” |
| Mức độ tiêm | Dưới da / Trên xương | Dưới da / Trên xương | Lớp hạ bì sâu /Dưới da | Dưới da / Trên xương |
Các sản phẩm chất làm đầy HA chính
Restylane®: Tiêu chuẩn vàng của chất làm đầy HA
Restylane® (Galderma, Thụy Điển) là chất làm đầy HA đầu tiên được FDA Hoa Kỳ chấp thuận vào năm 2003, sau chứng nhận CE ở Châu Âu vào năm 1996. Ngày nay, Re-stylane® được coi là tiêu chuẩn vàng của chất làm đầy HA dựa trên độ an toàn được chứng nhận trên toàn cầu và tỷ lệ hiệu quả. Tính đến năm 2020, hơn 40 triệu ca điều trị bằng Restylane®đã được thực hiện trên toàn thế giới. Đáng chú ý, Restylane® là chất làm đầy HA đầu tiên ứng dụng công nghệ axit hyaluronic ổn định không từ động vật (NASHA™). Mặc dù việc sử dụng HA không từ động vật không còn là đặc điểm phân loại giữa các chất làm đầy HA thương mại hiện có ngày nay, vì hầu hết HA không từ động vật đều có nguồn gốc từ quá trình lên men vi khuẩn, nhưng khi Restyl-ane® lần đầu tiên được ra mắt, NASHA™ thực sự là một đặc điểm vượt trội, nên nó được thêm vào tên sản phẩm, vì các loại gel HA lúc ấy đều dựa trên chiết xuất từ mào gà trống. Trong khi đó, thuật ngữ “ổn định” trong NASHA biểu thị các đặc điểm của Restylane® là gel HA đặc với mức độ biến đổi thấp chỉ bao gồm các hạt gel có cùng kích thước.
Sử dụng công nghệ NASHA™ để ổn định gel HA thay vì sử dụng liên kết chéo hóa học với BDDE dẫn đến có ít hơn 1% MoD (mức độ thay đổi) trong sản phẩm Re-stylane® cuối cùng (Hình 2.7). Do đó, nó có thể giảm thiểu các biến chứng tiềm ẩn phát sinh từ việc thay đổi HA bởi tác nhân liên kết chéo và do đó đảm bảo tính tương thích sinh học tối ưu. Trong khi đó, mỗi sản phẩm trong dòng Restylane® là một chất làm đầy HA hai pha đàn hồi có chứa các hạt gel có kích thước được chỉ định riêng (Hình 2.27). Theo thứ tự tăng dần của kích thước hạt gel, các dòng sản phẩm lần lượt là Restylane® Skinbooster Vital Light, Re-stylane® Skinbooster Vital, Restylane® và Restylane® Lyft (trước đây là Restylane® Perlane) (Bảng 2.5). Mặc dù Restylane® SubQ cũng đã được đưa vào danh mục, có kích thước hạt lớn nhất, nhưng sau đó nó đã bị ngừng sản xuất vào năm 2018. Trong khi đó, cũng cần lưu ý rằng Restylane® đã bao gồm ‘khái niệm phù hợp với mô’, nhờ đó các sản phẩm được điều chỉnh cho phù hợp với các chỉ định lâm sàng và độ sâu tiêm khác nhau ngay từ đầu những năm 2000, từ đó trở thành đặc điểm tiêu chuẩn của hầu hết các thương hiệu chất làm đầy HA ngày nay.
Theo đó, chẳng hạn như Restylane® Skinbooster Vital bao gồm các hạt gel nhỏ hơn, được chỉ định để tiêm lớp hạ bì bề mặt để điều trị các nếp nhăn nhỏ và mất độ đàn hồi; Restylane® Lyft với kích thước hạt gel lớn hơn thường được sử dụng để tiêm sâu ngay trên màng xương hoặc trong mô dưới da để phục hồi tình trạng thiếu hụt thể tích; Restylane® Skinbooster Vital Light có kích thước hạt nhỏ nhất được sử dụng cho các vùng da mỏng, mịn, bao gồm cả vùng quanh mắt và cổ. Trong khi đó, Restylane® nguyên bản có kích thước hạt trung bình, phù hợp để tiêm vào lớp hạ bì sâu để chỉnh sửa các nếp nhăn trung bình.
Vào năm 2009, các sản phẩm Restyl-ane® bổ sung 0,3% lidocain đã được tung ra thị trường, đảm bảo sự thoải mái hơn cho bệnh nhân. Vào năm 2010, dòng chất làm đầy HA của Emervel kết hợp công nghệ OBT™ (công nghệ cân bằng tối ưu) đã được phê duyệt tại EU, công nghệ này vào năm 2016 đã được đổi tên và hợp thành thương hiệu Restylane®, do đó mở rộng phạm vi và tính linh hoạt của dòng sản phẩm Re-stylane® (Hình 2.8). Các sản phẩm OBT™ là chất làm đầy HA mềm (đơn pha) có cùng nồng độ HA là 20 mg / mL, nhưng có sự khác biệt về mức độ và loại liên kết chéo, cũng như kích thước hạt. MoD của chất làm đầy OBT™ nằm trong khoảng 6–8% và thay đổi tùy theo sản phẩm. Trong khi các sản phẩm sử dụng công nghệ OBT™ thường được phân loại là HA đơn pha mềm, nhưng chúng cũng có kích thước hạt gần như không đổi nhờ quy trình ‘sàng lọc’ trong quá trình sản xuất để có độ đồng nhất tối ưu. Các sản phẩm có kích thước hạt nhỏ và có liên kết chéo thấp được dùng để tiêm bề mặt (ví dụ: Restylane® Fyness), trong khi các sản phẩm có kích thước hạt lớn hơn và có liên kết chéo cao được dùng để tiêm sâu hơn và tiêm tăng thể tích (ví dụ, Restylane ® Volyme™). Chúng có đặc điểm là có kết cấu gel mềm hơn và linh hoạt hơn các sản phẩm NASHA™. Các sản phẩm tích hợp công nghệ OBT™ bao gồm Restylane® Fyness, Restylane® Kysse, Restylane® Re-fyne, Restylane® Defyne và Restylane® Volyme™. Restylane® Refyne, Restylane® Defyne, and Restylane® Volyme™.
Từ chất làm đầy HA cực mềm đến cực rắn, dòng sản phẩm Restylane® cực kỳ linh hoạt và được sử dụng trong hầu hết các chỉ định. Sản phẩm NASHA™ của công ty Restylane® Lyft™ có khả năng nâng đỡ mô cao hơn, nên phù hợp để sử dụng cho việc phục hồi thể tích. Nhờ khả năng giãn nở sau tiêm tương đối thấp, sản phẩm NA-SHA™ Restylane® cũng là chất làm đầy được lựa chọn để điều trị rãnh mũi má, rãnh lệ và các vùng da mỏng khác trên khuôn mặt. Mặt khác, sản phẩm OBT™ mềm Restylane® Refyne được tối ưu hóa để sử dụng ở lớp hạ bì bề mặt để tránh những bất thường tiềm ẩn do tính dễ trải mỏng và khả năng lan tỏa của nó. Ngoài ra, các sản phẩm OBT™ Restylane® mềm được khuyên dùng để sử dụng trong các khu vực điều trị động như rãnh môi hàm và trán thay vì NASHA™ Restylane® Lyft™ của hãng.

Bảng 2.5 Các sản phẩm Restylane®
| Tên thương mại | Restylane®Lyft | Restylane®Lidocaine | Restylane®SkinboosterVital | Restylane®SkinboosterVital Light |
| Công nghệ sản xuất | NASHA™ | NASHA™ | NASHA™ | NASHA™ |
| Đơn pha hay hai pha | Hai pha | Hai pha | Hai pha | Hai pha |
| Nồng độ HA | 20 mg/mL | 20 mg/mL | 20 mg/mL | 20 mg/mL |
| Khả năng nâng đỡ | +++ | ++ | + | + |
| Kích cỡ mũi kim | 29G ½ | 29G ½ | 29G ½ | 29G ½ |
| Mức độ tiêm | Dưới da/ Trên xương/ Lớp hạ bì sâu | Lớp hạ bì từ trung bình đến sâu | Lớp hạ bì từ nông đến trung bình | Lớp hạ bì từ nông đến trung bình |
| Kích thước hạt | 650 μm | 300 μm |
| Tên thương mại | Restylane®Fynesse™ | Restylane®Refyne™ | Restylane®Defyne™ | Restylane®Volyme™ | Restylane®Kysse™ |
| Công nghệ sản xuất | OBT™ | OBT™ | OBT™ | OBT™ | OBT™ |
| Đơn pha hay hai pha | Đơn pha | Đơn pha | Đơn pha | Đơn pha | Đơn pha |
| Nồng độ HA | 20 mg/mL | 20 mg/mL | 20 mg/mL | 25 mg/mL | 26 mg/mL |
| Khả năng nâng đỡ | + | ++ | +++ | ++++ | +++ |
| Kích cỡ mũi kim | 30G ½ | 30G ½ | 30G ½ | 27G ½ | 30G ½ |
| Mức độ tiêm | Hạ bì trên | Lớp hạ bì từ trung bình đến sâu | Lớp hạ bì sâu/ Dưới da | Dưới da / Trên xương | Hạ bì trên |

Juvéderm®: Chất làm đầy
HA mềm đầu tiên (Hình 2.28) Juvéderm® (Allergan, Pháp) đã được CE phê duyệt tại Châu Âu vào năm 2004 và được FDA Hoa Kỳ phê duyệt vào năm 2006. Juverderm® là chất làm đầy HA mềm (một pha) đầu tiên được áp dụng công nghệ HYLACROSS™ để cạnh tranh với chất làm đầy HA rắn, Dòng sản phẩm NASHA™ (Bảng 2.6). Trong khi chất làm đầy HA rắn (hai pha) Restylane® là một loại gel có độ đặc của hạt, thì Juvéderm® mang đặc trưng của HA đơn pha có kết cấu gel mịn và đồng nhất. Là một chất làm đầy mịn, trải đều với độ nhớt đàn hồi thấp, Ju-verderm® có khả năng dễ tiêm và dễ dựng khuôn hơn, đặc biệt thích hợp để tiêm vào mặt phẳng bề mặt. Mặc dù độ nhớt đàn hồi thấp nhưng Juverderm® cũng rất phù hợp để nâng thể tích và tạo đường nét nhờ tính kết dính cao. Trong dòng sản phẩm Juvé-derm®, Juvéderm® Ultra™ và Juvéderm® Ultra Plus™ được bào chế bằng công nghệ HYLACROSS™ với cùng nồng độ HA là 24 mg / mL, mặc dù có tỷ lệ phần trăm liên kết chéo khác nhau, Juvéderm ® Ultra™ là 6% và Juvéderm® Ultra Plus™ là 8%. Do tỷ lệ liên kết chéo cao hơn, Juvéderm® Ultra Plus™ có khả năng gắn kết và nâng mô cao hơn, do đó thường được sử dụng để tăng thể tích trong mặt phẳng sâu [9].
Tuy nhiên, do nồng độ HA cao (24 mg / mL) và sử dụng HA trọng lượng phân tử cao, các sản phẩm HYLACROSS™ dễ bị hydrat hóa hơn (tức là gel trương nở) và có thể hút nước nhiều gấp đôi so với sản phẩm dựa trên công nghệ VYCROSS™ [9]. Do đó, vón cục và không đều đã được ghi nhận là tác dụng phụ thường gặp của các sản phẩm HYLACROSS™ do giãn nở sau khi tiêm. Để giải quyết nhược điểm này, VYCROSS™ đã được giới thiệu như một sự cải tiến có thể giảm độ trương nở và tăng cường độ ổn định. Để đạt được điều này, VYCROSS™ kết hợp cả HA trọng lượng phân tử cao và thấp để tạo ra ma trận gel HA tích hợp vào mô hiệu quả hơn với nồng độ HA thấp hơn (Hình 2.29). Kết hợp HA trọng lượng phân tử thấp (chuỗi ngắn) và HA trọng lượng phân tử cao (chuỗi dài) trong quá trình liên kết chéo có thể tạo ra một liên kết chặt chẽ hơn và hiệu quả hơn giữa các phân tử HA so với chỉ sử dụng HA trọng lượng phân tử cao.
Để dễ hình dung hơn, công nghệ liên kết chéo VYCROSS™ có thể được so sánh như việc trộn một bát mì trộn cay (cơm trộn Hàn Quốc trộn với mì lạnh) sau khi rưới nước sốt lên trên. Lúc này, việc cắt các phần mì bằng kéo sẽ giúp nước sốt và các sợi mì hòa quyện vào nhau một cách kỹ lưỡng và đồng đều hơn. Tương tự như vậy, VYCROSS™ là một phương pháp hiệu quả để tạo ra các phân tử HA liên kết chéo và dày đặc hơn, mang lại sự ổn định cao hơn với lượng hydrat hóa tối thiểu. Cũng như các dòng chất làm đầy HA chính khác, dòng sản phẩm VYCROSS™ cũng bao gồm một chuỗi các sản phẩm phù hợp với từng chỉ định lâm sàng khác nhau dựa trên các đặc tính khác nhau của gel.
Juvéderm® Voluma™, 20 mg / mL, là sản phẩm đầu tiên được bào chế bằng công nghệ VYCROSS™, có nồng độ HA cao nhất (20 mg / mL) và độ đàn hồi trong phạm vi VYCROSS™, nên nó có khả năng nâng mô tối đa khi được đặt trong các mặt phẳng mô sâu như một chất làm đầy HA tăng thể tích. Năm 2013, Juvéderm® Voluma™ đã được FDA phê duyệt để điều chỉnh tình trạng thâm hụt thể tích vùng giữa mặt. Được chú ý vì khả năng tạo ra kết quả lâu dài, Juvéderm® Voluma™ cũng là chất làm đầy HA đầu tiên nhận được sự chấp thuận của FDA với thời gian hiệu chỉnh 24 tháng. Juvéderm® Volift™, chứa nồng độ HA thấp hơn 17,5 mg / mL, có các đặc tính lưu biến trung gian giữa các đặc tính của Juvéderm® Voluma™ và Juvéderm® Vol-bella™ và cho thấy khả năng ngậm nước ít hơn 30% so với Juvéderm® Voluma™ [9] .
Juvéderm® Volift™ thích hợp để tiêm vào lớp hạ bì sâu hoặc mặt phẳng dưới da, không chỉ để làm đầy các nếp nhăn và rãnh sâu như rãnh mũi miệng và các rãnh quanh miệng mà còn để tăng thể tích ở các vùng như trán. Trong khi đó, Juvéderm® Volbel-la™ là chất làm đầy mềm có nồng độ HA là 15 mg / mL, do đó có độ nhớt và độ kết dính thấp nhất trong dòng sản phẩm. Ju-véderm® Volbella™ thích hợp để tiêm vào lớp hạ bì để xóa bỏ các nếp nhăn nông và biến dạng rãnh lệ cũng như để tăng thêm độ căng mọng cho môi.
Tất cả các sản phẩm trong họ Juvé-derm®, không chỉ bao gồm Juvéderm® Ultra™ và Juvéderm® Ultra Plus™ mà còn toàn bộ dòng sản phẩm VYCROSS™, đều có 0,3% lidocain, mang lại sự thoải mái trong quá trình điều trị, với mỗi công thức sản phẩm đều được USFDA phê duyệt. Juvé-derm® Ultra là Juvéderm® Ultra XC không có lidocain và Juvéderm® Ultra Plus là Ju-véderm® Ultra Plus XC không có lidocain.
Bảng 2.6 Các sản phẩm của Juvéderm®
| Tên thương mại | Juvéderm®VOLITE™ | Juvéderm®VOLBELLA™ | Juvéderm®VOLIFT™ | Juvéderm®VOLUMA™ | Juvéderm®VOLUX™ |
| Công nghệ sản xuất | Vycross™ | Vycross™ | Vycross™ | Vycross™ | Vycross™ |
| Đơn pha hay hai pha | Đơn pha | Đơn pha | Đơn pha | Đơn pha | Đơn pha |
| Nồng độ HA | 12 mg/mL | 15 mg/mL | 17.5 mg/mL | 20 mg/mL | 25 mg/mL |
| Khả năng nâng đỡ | + | ++ | +++ | ++++ | ++++ |
| Kích cỡ mũi kim | 32G ½ ‘ | 30G ½ ‘ | 30G ½ ‘ | 27G ½ ‘ | 27G ½ ‘ |
| Mức độ tiêm | Nội bì | Bề mặt/ Nội bì/ Niêm mạc môi | Lớp hạ bì sâu/ Niêm mạc môi | Dưới da / Trên xương | Dưới da / Trên xương |
| Tên thương mại | Juvéderm® Ultra XC | Juvéderm® Ultra XC |
| Công nghệ sản xuất | Hylacross™ | Hylacross™ |
| Đơn pha hay hai pha | Đơn pha | Đơn pha |
| Nồng độ HA | 24 mg/mL | 24 mg/mL |
| Mức độ liên kết chéo | 6% | 8% |
| Kích cỡ mũi kim | 30G ½ ‘ | 27G ½ ‘ |
| Mức độ tiêm | Lớp hạ bì giữa | Lớp hạ bì giữa và/hoặc sâu |
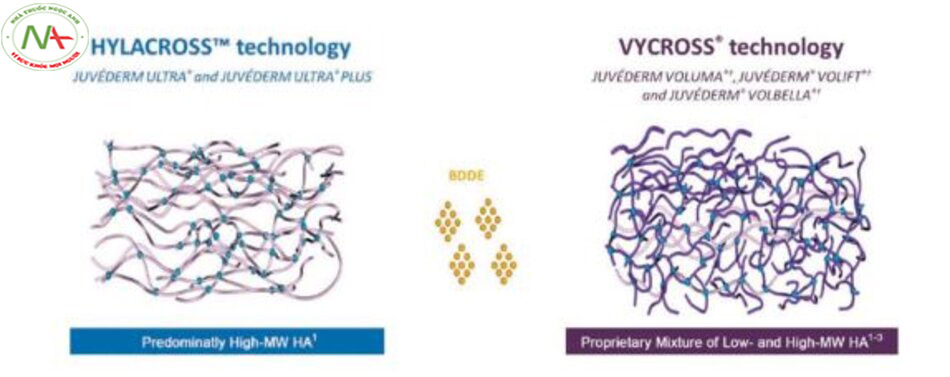
Belotero®: HA Filler nổi tiếng về độ an toàn
Dòng sản phẩm Belotero® được sản xuất và bán bởi Merz Pharmaceuticals GmbH (Đức) và ban đầu được phát triển bởi Anteis S.A., Thụy Sĩ, với tên thương mại là Esthélis® (Bảng 2.7). Belotero® đạt chứng nhận CE vào năm 2005 và được FDA Hoa Kỳ phê duyệt vào năm 2011. Mặc dù xuất hiện trên thị trường khá muộn, Belotero® vẫn được công nhận rộng rãi trong những năm qua nhờ tính an toàn và kết quả thuận lợi như một chất làm đầy HA một pha. Dòng sản phẩm Belotero® được xây dựng trên công nghệ Cohesive Polydensified Matrix (CPM™) các phân tử HA liên kết chéo với BDDE còn dư sau liên kết chéo ban đầu. Điều này khiến Belote-ro® có một kết cấu gel lỏng nhưng có độ kết dính cao, với các mức độ liên kết chéo khác nhau cùng tồn tại trong cùng một chất gel (Hình 2.31). Các vùng mật độ cao trong gel giúp gel tăng khả năng tăng thể tích và tuổi thọ cho sản phẩm, trong khi các vùng mật độ thấp ít nhớt hơn giúp gel dễ tiêm hơn và phân phối / tích hợp vào mô đồng nhất hơn. Việc chứa nhiều lớp mật độ trong cùng một sản phẩm cũng cho phép nó duy trì khả năng đàn hồi và tính toàn vẹn của cấu trúc tốt hơn chống lại các lực biến dạng bên ngoài của cơ mặt sau khi tiêm. Các nghiên cứu cho thấy rằng các sản phẩm dựa trên công nghệ CPM™ có tính kết dính cao hơn đáng kể so với các sản phẩm dựa trên công nghệ VYCROSS™ hoặc NASHA [13].
Các sản phẩm CPM™ cũng được chứng minh là có chỉ số đàn hồi E ′ và phản lực FN cao hơn so với các sản phẩm VYCROSS™ hoặc NASHA dưới tác dụng của áp suất nén [15]. Chính vì những lý do này mà Belo-tero® được chứng minh có khả năng tăng thể tích tương đương với các sản phẩm NA-SHA, mặc dù có G ’thấp hơn đáng kể. Đáng chú ý, tính liên kết đóng một vai trò quan trọng trong công dụng làm tăng thể tích của chất làm đầy HA vì nó cho phép sản phẩm duy trì thể tích và hình dạng ngay cả ở những vùng điều trị động như rãnh mũi miệng, rãnh môi hàm và trán.
Ngoài hiệu quả đã được chứng minh, một ưu điểm khác của Belotero® nằm ở tính an toàn và khả năng dung nạp tuyệt vời. Nhờ có độ nhớt thấp hơn, Belotero® thâm nhập vào lớp hạ bì một cách phân bố và khuếch tán hơn, tạo ra kết quả mịn, đều với ít Tyndalling hơn. Đáng chú ý nhất, không có trường hợp u hạt nào được báo cáo do tiêm Belotero® kể từ khi nó được tung ra thị trường vào năm 2005. Nó cũng có tỷ lệ biến chứng chậm liên quan đến miễn dịch thấp nhất trong số các chất làm đầy HA hiện nay.
Dòng sản phẩm Belotero® cũng bao gồm một loạt các sản phẩm phù hợp với các chỉ định và độ sâu tiêm khác nhau. Be-lotero® Volume™ có nồng độ HA cao nhất (26 mg / mL) và mức độ liên kết chéo cao nhất trong số các sản phẩm CPM™, do đó, chỉ số đàn hồi kéo trượt G ’và chỉ số đàn hồi E ′ cao nhất. Do đó, nó thích hợp để tiêm trong mặt phẳng mô sâu để phục hồi thể tích trên khuôn mặt. Belotero® Intense™ có nồng độ HA là 25,5 mg / mL và độ nhớt trung bình giữa Belotero® Volume™ và Belotero® Balance™. Tuy nhiên, nó vẫn phù hợp cho việc phục hồi thể tích khuôn mặt vì FN (phản lực) và độ gắn kết của nó cao hơn so với Belotero® Volume™. Do đó, nó được chỉ định để tiêm vào lớp hạ bì sâu hoặc mô dưới da để điều chỉnh các nếp nhăn sâu hơn (ví dụ, rãnh mũi miệng) hoặc để tăng thêm thể tích ở môi hoặc trán. Be-lotero® Balance có nồng độ HA là 22,5 mg / mL, độ nhớt và độ đàn hồi thấp nhưng có độ kết dính cao nhất trong số các sản phẩm CPM™. Là một chất làm đầy mềm, lan rộng, Belotero® Balance™ có khả năng tích hợp lan tỏa và đồng đều vào mô, và nó thích hợp để tiêm nông vào mặt phẳng da. Nó không chỉ thích hợp để điều chỉnh các rãnh sâu trung bình mà còn để tiêm cấp ẩm nâng hạ bì để cải thiện độ đàn hồi của da, cũng như làm nổi bật đường viền môi. Cuối cùng, Belotero® Soft™ có nồng độ HA thấp nhất (20 mg / mL) và mức độ liên kết chéo thuộc khoảng dòng sản phẩm CPM™ và do đó có độ nhớt thấp nhất. Ngược lại, chính những đặc điểm này lại mang đến một kết cấu mềm, dễ lan tỏa, khiến nó trở nên lý tưởng để sử dụng ở lớp hạ bì bề mặt hoặc ở những vùng có mô mỏng bao phủ như vùng quanh mắt và cổ.

Bảng 2.7 Các sản phẩm Belotero® (kích thước hạt và MoD không được công ty tiết lộ)
| Tên thương mại | Belotero®Soft™ | Belotero® Balance™ | Belotero® Intense™ | Belotero® Volume™ |
| Đơn pha hay hai pha | Đơn pha | Đơn pha | Đơn pha | Đơn pha |
| Nồng độ HA | 20 mg/mL | 22.5 mg/mL | 22.5 mg/mL | 26 mg/mL |
| Khả năng nâng đỡ | + | ++ | +++ | ++++ |
| Kích cỡ mũi kim | 30G ½ ‘ | 30G ½ ‘ | 27G ½ ‘ | 27G ½ ‘ |
| Mức độ tiêm | Lớp hạ bì từ nông đến trung bình | Lớp hạ bì từ trung bình đến sâu | Lớp hạ bì sâu/ Dưới da | Lớp hạ bì sâu/ Dưới da/ Trên màng xương |
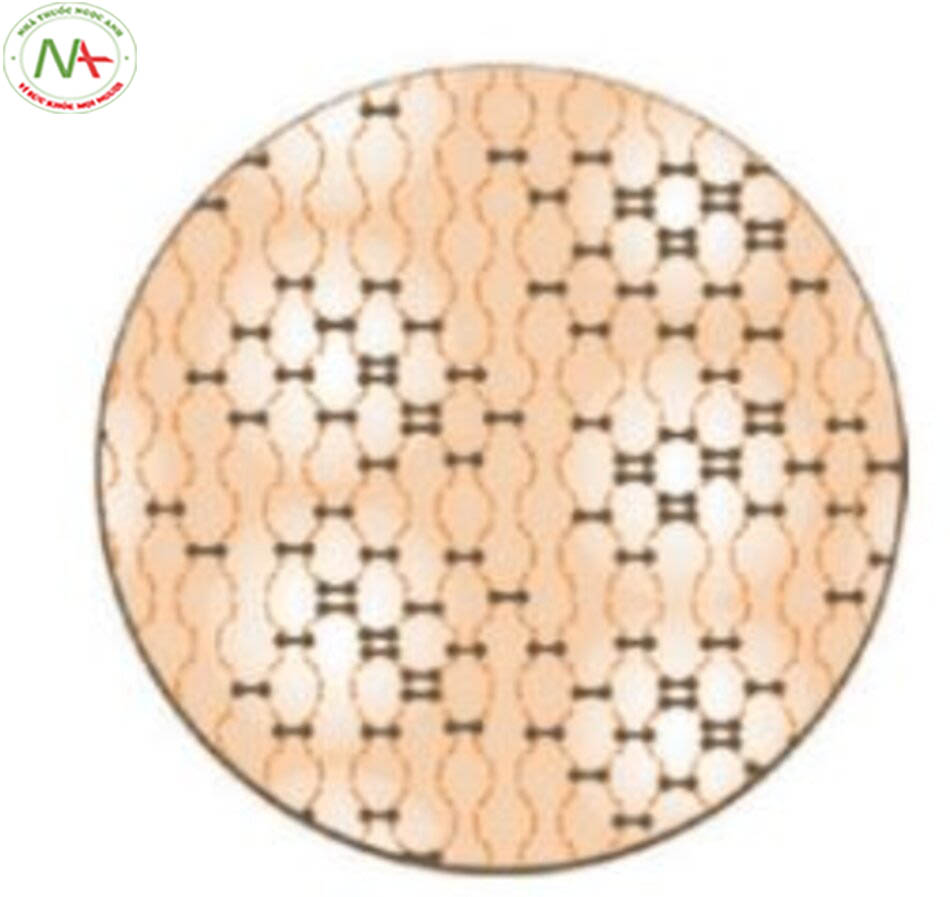
YVOIRE®: Chất làm đầy HA đầu tiên của Hàn Quốc
YVOIRE® là chất làm đầy HA đầu tiên của Hàn Quốc được phát triển vào năm 2011 với công nghệ liên kết chéo HICE™ (High Concentration Equalized) (Bảng 2.8). Sản phẩm YVOIRE® của LG Chem (Hàn Quốc) là chất làm đầy HA hai pha, được phân loại theo kích thước hạt axit hy-aluronic để phù hợp với mục đích và cách sử dụng. Công nghệ liên kết chéo HICE™ là công nghệ sản xuất độc nhất của LG Chem, có thể thu được hiệu quả liên kết chéo cao dù chỉ thêm vào một lượng nhỏ chất liên kết chéo bằng cách phân tán đồng đều các chất liên kết chéo và HA trọng lượng phân tử cao có nồng độ cao.
Là kết quả của công nghệ liên kết chéo, YVOIRE® là sản phẩm chất làm đầy được sử dụng thường xuyên trong hơn 10 năm và được công nhận về độ đàn hồi và độ an toàn cao nhờ sử dụng ít chất liên kết chéo nhất. Từ nguyên liệu thô axit hyaluronic đến sản phẩm cuối cùng, LG Chem trực tiếp tiến hành nghiên cứu và quản lý quy trình sản xuất. Nguyên liệu thô axit hyal-uronic được sử dụng trong YVOIRE® đã được liệt kê trong Hồ sơ tổng thể về dược phẩm (DMF) của FDA Hoa Kỳ và được chứng nhận bởi EDQM Châu Âu (Cục Quản lý Chất lượng Thuốc & Chăm sóc Sức khỏe Châu Âu) đảm bảo sự công nhận quốc tế về sự an toàn và công nghệ.
YVOIRE® Classic™ / Classic plus™ có kích thước hạt nhỏ nhất (350–400μm) và độ đàn hồi thấp, thích hợp để cải thiện nếp nhăn. YVOIRE® Volume™ / Volume plus™ có các hạt lớn hơn (800–900μm) có độ đàn hồi cao hơn so với loại Classic, phổ biến cho hầu hết các nhu cầu tăng thể tích. Trong các nghiên cứu đánh giá ngẫu nhiên với 58 bệnh nhân có mức độ NLF từ trung bình đến nặng để so sánh hiệu quả của YVOIRE® Classic™ với Restylane® hoặc YVOIRE® Volume™ so với Lyft™, kết quả so sánh cho thấy hiệu quả phục hồi rãnh mũi miệng và độ an toàn của chúng là tương đương nhau (p <0,05) [23]. YVOIRE® Contour™ / Contour plus™ thích hợp cho những vùng cần nâng cơ có độ đàn hồi cao nhất. Vì YVOIRE® Contour / Contour plus có thành phần hạt kép nên các khoảng trống giữa các hạt lớn (1400μm) được lấp đầy bằng các hạt nhỏ hơn (350μm), nó giúp lực tiêm được liên tục, trôi chảy, dẫn đến vẻ ngoài mịn màng và tự nhiên cho khuôn mặt. Trong các nghiên cứu lâm sàng đánh giá ngẫu nhiên với 83 bệnh nhân về nâng thể tích vùng má trước giữa, kết quả cho thấy không có sự khác biệt về hiệu quả và độ an toàn (p <0,05) của YVOIRE® Con-tour khi so sánh với Restylane® Sub-Q ở 26 và 52 tuần sau khi điều trị [23]. Các sản phẩm Plus có chứa lidocain để giảm đau do tiêm.
Nồng độ HA của các sản phẩm không chứa lidocain là 22 mg và nồng độ HA của các sản phẩm Plus chứa lidocain là 20 mg. Ngay sau khi điều trị, hơn 90% bệnh nhân được điều trị bằng YVOIRE® Clas-sic plus hoặc YVOIRE® Volume™ plus được báo cáo là đỡ đau hơn so với những người được điều trị bằng YVOIRE® Clas-sic hoặc YVOIRE® Volume™. Điều đó nói lên rằng, hiệu quả lâm sàng và độ an toàn của YVOIRE® Classic plus™ hoặc Volume plus™ tương đương với YVOIRE® Classics hoặc Volume™ s [27].
YVOIRE® Y-solution™ được nghiên cứu để tăng tính kết dính vì chất làm đầy hai pha thường có tính kết dính thấp hơn. Để đáp ứng cả độ đàn hồi và độ kết dính cao, YVOIRE® Y-solution™ áp dụng công nghệ liên kết chéo S-HICE™ (Superior, Sta-ble High Concentration Equalized) tiên tiến hơn HICE™ để đạt được độ gắn kết cao hơn. S-HICE™ là một công nghệ được nâng cấp nhằm tăng tính ổn định và gắn kết giữa các hạt ở dạng hạt nhỏ thông qua các quá trình phân tán hạt khác nhau. Dựa trên công nghệ liên kết chéo S-HICE™, YVOIRE® Y-solution™ là chất làm đầy Y-phasic™ với khả năng nâng cơ cao bằng cách kết hợp các ưu điểm của chất làm đầy một pha có độ kết dính cao và chất làm đầy hai pha có độ đàn hồi cao. YVOIRE® Y-solution™ được ra mắt lần đầu tiên tại Hàn Quốc vào năm 2018 với ba sản phẩm bao gồm Y-solution 360™, Y-solution 540™ và Y-solution 720™. Tất cả các sản phẩm YVOIRE® Y-solution™ đều chứa lidocain và nồng độ HA của nó tương ứng là 12 mg, 20 mg và 20 mg với MoD lần lượt là 2,4%, 3,5% và 3,3%.

| Tên thương mại | YVOIRE® Volume S™ | YVOIRE® Volume Plus™ | YVOIRE® Con-tour™ | YVOIRE® Contour Plus C™ |
| Công nghệ sản xuất | HICE™ | HICE™ | HICE™ | HICE™ |
| Đơn pha hay hai pha | Hai pha | Hai pha | Hai pha | Hai pha |
| Nồng độ HA | 22 mg/mL | 20 mg/mL | 22 mg/mL | 20 mg/mL |
| Khả năng nâng đỡ | +++ | +++ | ++++ | ++++ |
| Kích cỡ mũi kim | 32G ½ “ | 30G ½ “ | 30G ½ “ | 27G ½ “ |
| Mức độ tiêm | Hạ bì trên | Hạ bì sâu | Dưới da/ Trên xương | Hạ bì sâu |
| Kích thước hạt | 900 μm | 900 μm | 1300 μm/ 350 μm | 1300 μm/ 350 μm |
Neuramis®: Chất làm đầy mềm HA mềm tiêu biểu của Hàn Quốc
Neuramis® là một dòng chất làm đầy axit hyaluronic một pha được phát triển bởi Medytox Inc. (Hàn Quốc) (Bảng 2.9). Kể từ khi sản phẩm đầu tiên Neuramis® Deep đạt chứng nhận CE vào năm 2011, một loạt các sản phẩm có chứa lidocain đã được phát triển, cụ thể là Neuramis® Light Lidocain, Neuramis® Lidocaine, Neuramis® Deep Lidocaine™ và Neura-mis® Volume Lidocain™. Hiện tại, Neur-amis® Deep™ và Neuramis® Deep Lido-cain™, và Neuramis® Volume Lidocaine™ đã đạt được chứng chỉ CE. Thông qua một quy trình sản xuất độc đáo được gọi là công nghệ “SHAPE™ (Stabilized Hyal-uronic Acid & Purification Enhancement)”, liên kết chéo của axit hyaluronic phù hợp được hình thành, tạo ra gel axit hyaluron-ic có độ kết dính cao. Axit hyaluronic nào cũng được liên kết chéo và các sản phẩm cuối cùng chứa axit hyaluronic ở nồng độ 20 mg / mL. Để đảm bảo an toàn và chất lượng của các sản phẩm, chỉ sử dụng axit hyaluronic chất lượng cao được đăng ký trong FDA Dược phẩm Master và Cục Quản lý Chất lượng Thuốc và Chăm sóc Sức khỏe Châu Âu. Nồng độ axit hyaluronic của tất cả các sản phẩm là 20 mg / mL.
Neuramis® lidocaine cung cấp bốn sản phẩm với các mức độ liên kết chéo khác nhau để phù hợp với mọi nhu cầu (Bảng 2.9). Neuramis® Light Lidocaine™ là một axit hyaluronic liên kết chéo nhẹ phù hợp tiêm vào lớp hạ bì để cải thiện các nếp nhăn sâu. Neuramis® Lidocaine™ và Neur-amis® Deep Lidocaine™ được sử dụng để phục hồi mô ở lớp hạ bì trung bình đến sâu. Trong một thử nghiệm lâm sàng ngẫu nhiên, Neurmis® Deep Lidocaine™ đã cho thấy khả năng chỉnh sửa rãnh mũi môi tốt hơn đáng kể so với Restylane® Lyft™ trong tối đa 24 tuần (p <0,05) [29]. Neur-amis® Volume Lidocaine™ là sản phẩm axit hyaluronic liên kết chéo mạnh nhất phù hợp tiêm vào lớp dưới da và / hoặc lớp trên xương. Trong một nghiên cứu so sánh ngẫu nhiên, Neuramis® Volume Li-docaine™ cho kết quả tương tự so với Ju-vederm® voluma™ về hiệu quả và độ an toàn trong việc phục hồi tình trạng thâm hụt khối lượng vùng giữa khuôn mặt ở 88 bệnh nhân [30].

Bảng 2.9 Đặc điểm sản phẩm dòng Neuramis® lidocain
| Tên thương mại | Neuramis®Light Lidocaine™ | Neuramis®Lidocaine™ | Neuramis®Deep Lidocaine™ | Neuramis®Volume Lido-caine™ |
| Công nghệ sản xuất | SHAPE™ | SHAPE™ | SHAPE™ | SHAPE™ |
| Đơn pha hay hai pha | Đơn pha | Đơn pha | Đơn pha | Đơn pha |
| Nồng độ HA | 20 mg/mL | 20 mg/mL | 20 mg/mL | 20 mg/mL |
| Khả năng nâng đỡ | + | ++ | +++ | ++++ |
| Kích cỡ mũi kim | 30G x 3/16 ′′ | 30G x 1/2 ′′ | 27G x 1/2 ′′ | 27G x 1/2 ′′ |
| Mức độ tiêm | Lớp hạ bì từ nông đến trung bình | Lớp hạ bì từ trung bình đến sâu | Lớp hạ bì từ trung bình đến sâu | Dưới da/ Trên xương |
e.p.t.q.®: Chất làm đầy HA với độ An toàn hàng đầu (Hình 2.34)
e.p.t.q.® (epitique) (JETEMA, Hàn Quốc), một chất làm đầy axit hyaluronic một pha được phát triển vào năm 2017 áp dụng công nghệ 2CM™ (2 Crosslink-ing Method) và được CE phê chuẩn cho e.p.t.q.® lidocaine vào năm 2020. Công nghệ 2CM™ không chỉ sử dụng liên kết chéo hóa học mà còn cả liên kết chéo vật lý để đạt được hiệu quả liên kết chéo tối đa với lượng BDDE tối thiểu để tạo ra một cấu trúc tổ ong cứng và chắc. e.p.t.q.® có mức độ điều chỉnh (MoD) trong phạm vi 1% với sử dụng tối thiểu các liên kết chéo để đảm bảo an toàn tuyệt vời, nhưng vẫn giữ được tính liên kết cao. Sử dụng công nghệ nghiền được gọi là Downing Process, e.p.t.q.® có các hạt mịn và đồng nhất. Nhờ có các hạt mịn này, e.p.t.q.® có thể được tiêm bằng kim mỏng (30G). Thông thường, các sản phẩm có chứa các hạt gel có kích thước lớn không nên sử dụng với kim mỏng do có thể ảnh hưởng đến kích thước hạt và trạng thái cân bằng lưu biến [31].
e.p.t.q.® được phân loại theo độ nhớt đàn hồi: S100, S300, S500 (Bảng 2.10) [29]. Cả ba đều có nồng độ axit hyaluronic là 24 mg / mL và chứa lidocain để giảm đau. Dù e.p.t.q.® là chất làm đầy một pha với công thức gel mềm, nhưng nó vẫn có kích thước hạt đồng nhất với khả năng dựng khuôn tuyệt vời. Ngoài ra, do quá trình sản xuất tập trung vào vấn đề an toàn như hàm lượng chất liên kết chéo tối thiểu (MoD khoảng 1%), nên tỷ lệ phản ứng viêm do quá mẫn loại chậm thường thấp hơn 0,1% dựa trên kinh nghiệm sử dụng 2.000 ống tiêm của tôi trong 2 năm qua.

| Tên thương mại | e.p.t.q.®LidocaineS100™ | e.p.t.q.®LidocaineS300™ | e.p.t.q.®LidocaineS500™ |
| Công nghệ sản xuất | 2CM™ | 2CM™ | 2CM™ |
| Đơn pha hay hai pha | Đơn pha | Đơn pha | Đơn pha |
| Nồng độ HA | 24 mg/mL | 24 mg/mL | 24 mg/mL |
| Khả năng nâng đỡ | + | ++ | +++ |
| Kích cỡ mũi kim | 27G 1/2 ′′ | 27G 1/2 ′′ | 27G 1/2 ′′ |
| Mức độ tiêm | Lớp hạ bì | Lớp hạ bì sâu | Dưới da |
| Kích thước hạt | 310 μm | 310 μm | 310 μm |
| MoD(%) | 1.18 | 1.53 | 1.89 |
Các loại chất làm đầy dạng tiêm khác
Chất làm đầy collagen
Là một thành phần quan trọng của hạ bì có vai trò là sức mạnh và khả năng phục hồi của da, collagen là vật liệu đầu tiên được sử dụng làm chất làm đầy mô mềm. Các chất làm đầy dựa trên collagen đầu tiên được USFDA chấp thuận sử dụng vào đầu những năm 1980 là ZYDERM®1 từ bò (collagen bò 35 mg / mL), ZYDERM® 2 (collagen từ bò 65 mg / mL) và ZYPLAST® (collagen từ bò 35 mg / mL, liên kết chéo với glutaraldehyde) (Allergan. CA, US) [3]. Phiên bản của Nhật Bản, tức là Koken Atelocollagen® (Koken Co. Japan), cũng có nguồn gốc từ bò. Tuy nhiên, do nguồn gốc động vật, những chất làm đầy collagen từ bò này cần phải xét nghiệm dị ứng da 4 tuần trước khi điều trị, mặc dù kết quả xét nghiệm âm tính cũng không loại trừ nguy cơ phản ứng dị ứng. Tuy nhiên, sau đó, với sự ra đời và thống trị của chất làm đầy HA, chất làm đầy collagen bò sớm không còn được sử dụng trên toàn cầu, điều này khiến Allergan cuối cùng phải chấm dứt việc sản xuất ZYDERM® và ZYPLAST® vào năm 2010. Trong khi đó, EVOLENCE® (John-son & Johnson.New Jersey , US) là chất làm đầy collagen từ lợn (collagen từ lợn 30 mg / mL), đã được USFDA phê duyệt vào năm 2008 [3]. Lợi ích của EVOLENCE® là chúng được liên kết chéo, do đó mang lại kết quả lâu dài hơn so với các chất làm đầy colla-gen trước đó và không yêu cầu thử nghiệm dị ứng. Tuy nhiên, dù có những ưu điểm này, Johnson & Johnson cũng bị buộc phải ngừng sản xuất EVOLENCE® vào năm 2009 do nhu cầu thị trường đối với chất làm đầy collagen giảm mạnh. Trong khi đó, COSMODERM® và COSMOPLAST® (Aller-gan, CA) là chất làm đầy collagen có nguồn gốc từ mô người được USFDA phê duyệt vào năm 2003 nhưng sau đó đã bị ngừng sản xuất vào năm 2010.
Nhận xét: Trong khi chất làm đầy col-lagen đã tạo ra bước đột phá mới bằng cách đi tiên phong tr ong thị trường chất làm đầy dạng tiêm, nhưng chúng đã bị lỗi thời bởi nguy cơ phản ứng sinh miễn dịch và thời gian tác dụng ngắn chỉ kéo dài từ 3–6 tháng. Điều đó cho thấy, cần phải chấp nhận rằng chất làm đầy collagen cung cấp khả năng tạo khuôn tốt và dễ dàng lan truyền vào các mô mà không xảy ra Tyn-dalling, điều này làm cho chúng trở nên lý tưởng để điều trị nếp nhăn ở những vùng da mỏng manh như vùng quanh mắt.
Thuốc tiêm vĩnh viễn
PMMA (Polymethyl Methacry-late)
Polymethyl Methacrylate (PMMA) là một chất thường được sử dụng trong thực hành phẫu thuật chỉnh hình gắn phục hình xương cho cơ thể con người (Hình 2.35). BellaFill® là (Suneva Medical Inc., US) là chất làm đầy vĩnh viễn dựa trên PMMA chứa các vi cầu PMMA bề mặt nhẵn có kích thước 30–50μm được dùng để tránh hiện tượng thực bào của đại thực bào [31, 31] (Hình 2.36). Năm 2006, PMMA dạng tiêm đã được USFDA phê duyệt với tên thương mại ArteFill® (Artes Medical, US), theo đó ArteFill® trở thành chất làm đầy mô mềm vĩnh viễn đầu tiên được USFDA phê duyệt. ArteFill® được đổi tên thành BellaFill® vào năm 2014. BellaFill® bao gồm các vi cầu PMMA trong 3,5% collagen bò với tỷ lệ 1: 4 [30]. Theo thời gian, collagen được tái hấp thu và các vi cầu PMMA hoạt động như một giá đỡ để kích thích sinh học tổng hợp collagen.
Đối với sản phẩm có chứa collagen bò làm chất vận chuyển, cần phải thực hiện kiểm tra dị ứng da trước khi điều trị bằng BellaFill®. Các tác dụng phụ, mặc dù hiếm gặp, bao gồm phản ứng dị vật, u hạt, biến dạng đường viền và nhiễm trùng [30]. Cần thận trọng khi sử dụng vì PMMA là một hợp chất tổng hợp không thể loại bỏ ngược nếu có vấn đề xảy ra.
Nhận xét: Tính vĩnh viễn của chất làm đầy cho thấy rằng bất kỳ biến chứng tiềm ẩn nào phát sinh do chất làm đầy đó cũng là vĩnh viễn. Để tránh những hậu quả khó lường trong cuộc sống, các học viên nên tránh xa những giải pháp vĩnh viễn này.
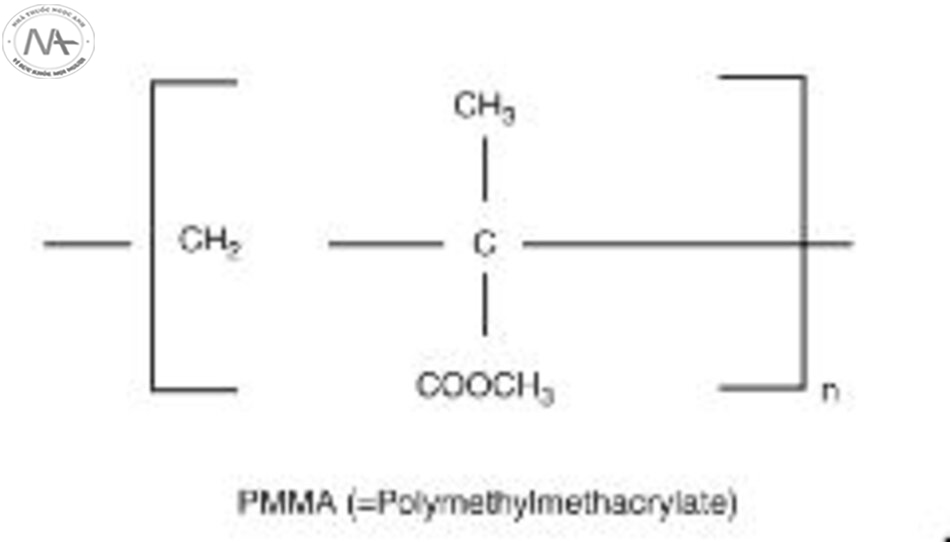
PAAG (Gel Polyacrylamide)
Polyacrylamide gel (PAAG) là một loại polymer cao được sử dụng như một thành phần trong sản xuất kính áp tròng mềm (Hình 2.37). Chất làm đầy mô mềm vĩnh viễn có chứa PAAG được phát triển lần đầu tiên vào năm 1980 tại Ukraine với tên thương mại là Interfall® và được cấp chứng nhận CE vào năm 2001 tại Đan Mạch với tên thương mại là Aquamid® (Contura InternationalA / S, Đan Mạch).
Aquamid® là một sản phẩm hydro-gel kết hợp 2,5% polyacrylamide liên kết chéo và 97,5% nước và được cho là có kết cấu tự nhiên và khả năng tương thích sinh học thuận lợi [31]. Tuy nhiên, u hạt, biến dạng đường viền và sản phẩm bị dịch chuyển thường được quan sát thấy sau khi sử dụng của nó [33]. May mắn thay, sản phẩm có thể được loại bỏ thậm chí vài năm sau điều trị bằng cách sử dụng dung dịch muối gấp 2–3 lần thể tích PAAG đã tiêm, tiếp theo là 3–5 phút xoa bóp mạnh và chọc thủng bằng kim hoặc dao rạch 18-G, sau đó sản phẩm sẽ được ép kiệt ra (Hình 2.38) [32, 33]. Trước những dư luận tiêu cực xung quanh những biến chứng từ việc tiêm Amazing gel® (sản phẩm của công ty FuHua High Molecular, Trung Quốc) cho việc nâng ngực, PAAG phần lớn đã không còn được ưa chuộng và thực tế không còn được sử dụng nữa. Trong khi Aquafilling® (Séc), bao gồm PAAG (2%) và nước (98%) đã được ra mắt thị trường vài năm trước, tuyên bố rằng có thể loại bỏ ngược bằng nước muối thông thường, nhưng việc tiêm Aquafilling®, cũng như Aquamid®, không thể bị loại bỏ hoàn toàn chỉ với một tác nhân loại bỏ ngược nào đó (Hình 2.39).
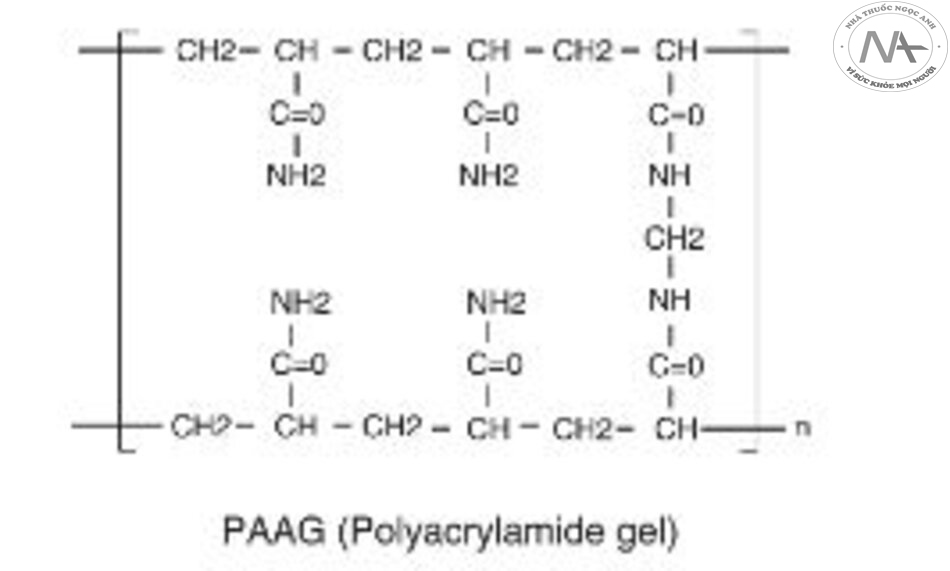
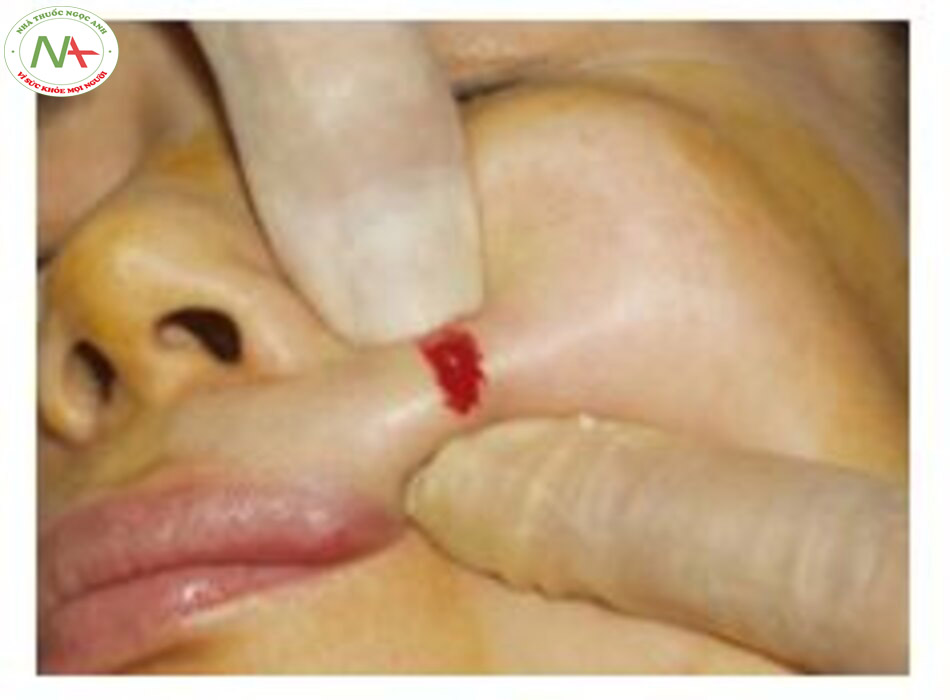
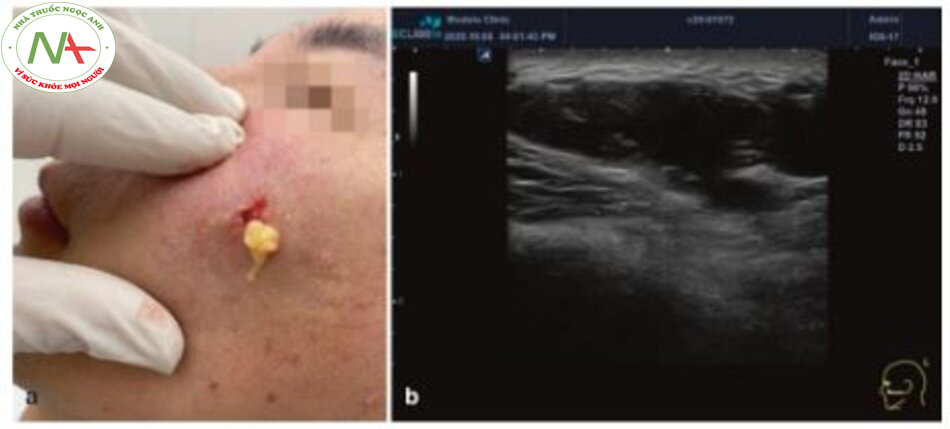
Chất làm đầy kích thích collagen
Trước năm 2000, chất làm đầy mô mềm được phát triển chủ yếu để sử dụng như tác nhân làm tăng thể tích hoặc làm đầy, với chất làm đầy dựa trên collagen hoặc HA được tiêm vào để cung cấp thể tích thay thế cho tình trạng xẹp da mặt. Tuy nhiên, từ năm 2000 trở đi, xu hướng phổ biến trong phát triển chất làm đầy mô mềm đã chuyển từ chất làm đầy thay thế sang các polyme cao có thể phân hủy sinh học, chúng có khả năng kích thích sinh học collagen trong vùng được tiêm trong khi bản thân chúng bị phân hủy từ từ trong cơ thể. Những chất làm đầy kích thích colla-gen này, còn được gọi là chất làm đầy kích thích sinh học, được cho là có thời gian tác dụng dài hơn so với chất làm đầy HA. Các sản phẩm chính bao gồm canxi hy-droxylapatite (CaHA), PLLA, PDLLA, PCA và chất làm đầy dựa trên PDO. Tuy nhiên, việc sử dụng chất làm đầy kích thích sinh học cũng có những rủi ro và thách thức của riêng nó, bao gồm sự thay đổi riêng lẻ trong quá trình tổng hợp collagen, hình thành nốt sần do sản xuất quá mức colla-gen và bề mặt da không đều do các nốt sần nổi lên. Đáng chú ý nhất, kết quả của chất làm đầy kích thích collagen vẫn không thể đảo ngược lại trong trường hợp tiêm nhầm vị trí hoặc biến chứng. Do đó, nên tránh sử dụng chúng ở những vùng da mặt mỏng, chẳng hạn như vùng quanh mắt hoặc niêm mạc môi.
Chất làm đầy Canxi Hydroxylap-atite (CaHA)
Canxi Hydroxylapatite (Ca10(PO4)6(OH)2) hoặc CaHA là khoáng chất chính cấu tạo nên răng và xương. Có thành phần tương tự như sỏi mật hoặc sỏi tiết niệu, nó từ lâu đã được sử dụng trong các thủ thuật phẫu thuật chỉnh hình hoặc các ứng dụng nha khoa như vật liệu hàn răng hoặc vật liệu tái tạo nha khoa. Chất làm đầy canxi hydrox-ylapatite bao gồm 30% CaHA và 70% natri cacboxy-metylcellulose (CMC), glycerine và nước vô trùng. CaHA bao gồm các vi cầu mịn có đường kính từ 25–45μm được dùng để tránh hiện tượng thực bào của đại thực bào (Hình 2.40). Sau khi được đặt trong mô mềm, các vi cầu CaHA tạo ra tân sinh collagen tại vị trí tiêm trong khi bản thân chúng từ từ phân hủy thành các ion canxi và photphat, và bị loại bỏ hoàn toàn [34] (Hình 2.41). Trong khi đó, chất mang gel, natri carboxymethylcellulose (CMC), cung cấp thể tích ban đầu trong vài tuần hoặc tháng đầu khi tiêm, sau đó nó dần dần tiêu biến đi, để lại collagen mới lấp đầy khoảng trống của nó [35].
Radiesse® (Merz, Đức) là chất làm đầy CaHA đầu tiên được USFDA phê duyệt vào năm 2001 để sử dụng trong điều trị suy dây thanh đới và hàn xương (Hình 2.42). Vào năm 2006, nó đã nhận được FDA Hoa Kỳ phê duyệt về việc điều chỉnh các nếp nhăn nghiêm trọng trên khuôn mặt và / hoặc chứng loạn dưỡng mỡ (lipoatrophy) trên khuôn mặt ở những người nhiễm vi rút gây suy giảm miễn dịch ở người (HIV). Mặc dù có thành phần chủ yếu là canxi, Radiesse® không hóa lỏng hoặc canxi hóa trong mô mềm hoặc màng xương khi được tiêm vào [36]. Không có báo cáo nào về trường hợp tạo xương xảy ra do tiêm Radiesse® vào mô mềm [34]. Về mặt lý thuyết, điều này là do sự phát triển của tế bào mới thành CaHA là phù hợp với mô xung quanh và các tế bào mới không tách biệt thành các loại tế bào khác [34].
Mặc dù Radiesse® được biết là có thời gian tác dụng kéo dài trong vài năm, bệnh nhân ban đầu có thể cảm nhận chỉ có hiệu quả tạm thời và tồn tại trong thời gian ngắn do chất mang gel xẹp xuống sau vài tuần hoặc vài tháng đầu tiên khi tiêm. Trong trường hợp như vậy, tốt nhất là nên tiêm cải thiện dần dần sau điều trị 1–2 tháng [36]. Cũng cần lưu ý rằng việc tiêm Radiesse® có thể gây đau đớn nhiều vì nồng độ pH của sản phẩm (6,8–8,0) nằm ngoài phạm vi pH của cơ thể con người. Điều chế lại 1,3 mL Radiesse® với 0,2 mL lidocain trước khi tiêm có thể giúp giảm đau đáng kể [36]. Radiesse® cũng có xu hướng gây sưng phồng ban đầu lớn hơn chất làm đầy HA, có lẽ do chất mang gel của nó. Do đó, tốt nhất là tránh tiêm lượng lớn Radiesse® vào cùng một vị trí trong một lần điều trị duy nhất. Thay vào đó, tốt hơn là sử dụng phương pháp tiếp cận từng bước với các lần điều trị cách nhau 2-4 tuần cho đến khi đạt được kết quả mong muốn. Một biến chứng đáng chú ý của Radiesse® là hình thành các nốt sần cứng khi được tiêm bo-lus (tiêm truyền hóa chất nhanh) ở những vị trí có da mỏng như vùng quanh hốc mắt hoặc niêm mạc môi. Cần phải phẫu thuật cắt bỏ hoặc điều trị bằng cách tiêm triam-cinolone trong trường hợp hình thành các nốt sần [37]. Ngược lại, sự hình thành u hạt do phản ứng của cơ thể với chất lạ ít khi xảy ra ở Radiesse® so với các chất làm đầy vĩnh viễn khác, PLLA hoặc thậm chí là chất làm đầy HA [37–39]. Có thể giải quyết các tình trạng không đều hoặc chỉnh sửa quá mức trong vòng 2 tuần đầu điều trị bằng cách dùng kim 18-G chọc thủng vết tiêm và lấy sản phẩm ra ngoài theo cách thủ công. Tuy nhiên, trong trường hợp thời gian đã trôi qua đáng kể từ lần điều trị ban đầu, phẫu thuật cắt bỏ hoặc tiêm triamcinolone trở thành lựa chọn khả dụng duy nhất.
Nhận xét: Radiesse® đã được đánh giá là một cột mốc mới trong quá trình nâng da mặt khi lần đầu tiên được tung ra thị trường. Tuy nhiên, sự phổ biến và tính linh hoạt ban đầu của nó sớm bị hạn chế bởi những nhược điểm như sưng phồng ban đầu đáng kể, hình thành nốt sần khi tiêm bolus và nguy cơ phát triển quá mức của các sợi collagen có thể cản trở ống tiêm trong lần điều trị thứ hai hoặc thứ ba. Hơn nữa, vì sản phẩm không thể bị hòa tan với tác nhân đảo ngược, nên thực hiện nâng da mặt với Radiesse® không được có bất kì sai sót nào. Những yếu tố này đã hạn chế việc sử dụng rộng rãi Radiesse® trong các ứng dụng tăng thể tích da mặt. Tuy nhiên, tác dụng kích thích sinh học collagen của Radiesse® đã được sử dụng phổ biến cho mục đích làm săn chắc da bằng cách pha loãng sản phẩm từ hai đến ba lần với nước muối và lidocain và tiêm nông vào lớp dưới da [40]. Ví dụ như trẻ hóa da nhăn ở cổ và mu bàn tay.
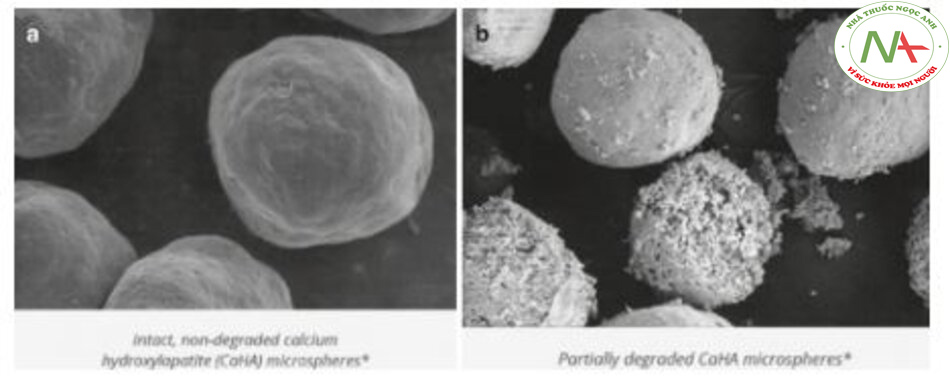
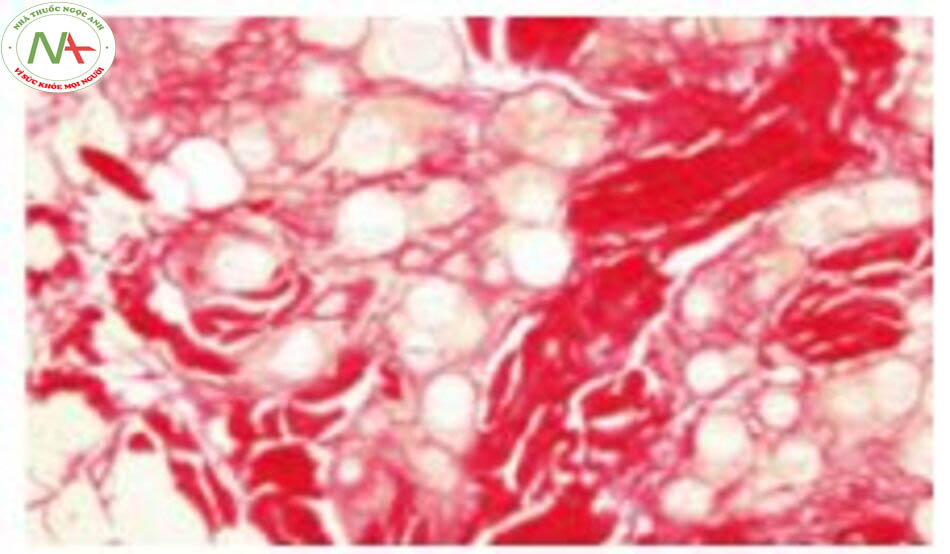

Chất làm đầy PCL (Hình 2.43)
Polycaprolactone (PCL) là một loại polyme có thể tái hấp thụ sinh học đã được sử dụng từ lâu trong y tế như là chỉ phẫu thuật tự tiêu (Hình 2.44). Chất làm đầy mô mềm dựa trên Polycaprolactone (PCL) được bán trên thị trường với tên El-lansé™ (AQTIS Medical, Hà Lan). Ellansé™ là chất làm đầy polyme cao có thể phân hủy sinh học bao gồm 30% PCL trong 70% carboxymethylcellulose (CMC) làm chất mang gel. Tương tự như Radiesse®, El-lansé™ dựa trên PCL bao gồm các vi cầu mịn với kích thước hạt nằm trong khoảng 25–50μm để tránh hiện tượng thực bào của đại thực bào. Khi được tiêm vào, các vi cầu PCL thúc đẩy sự hình thành collagen mới trong mô xung quanh và dần dần phân hủy thành nước và CO2, sau đó chúng bị đào thải khỏi cơ thể. Chất mang gel, natri cacboxymethylcellulose (CMC), cung cấp khả năng điều chỉnh thể tích ngay lập tức trong những tuần hoặc tháng đầu tiên và tiêu biến trong 3 tháng, và được thay thế bằng collagen mới. Tóm lại, ngoài sự khác biệt về thành phần hoạt chất, Ellansé™ có nhiều điểm tương đồng với Radiesse® về thành phần, cơ chế tác dụng, chỉ định và biến chứng.

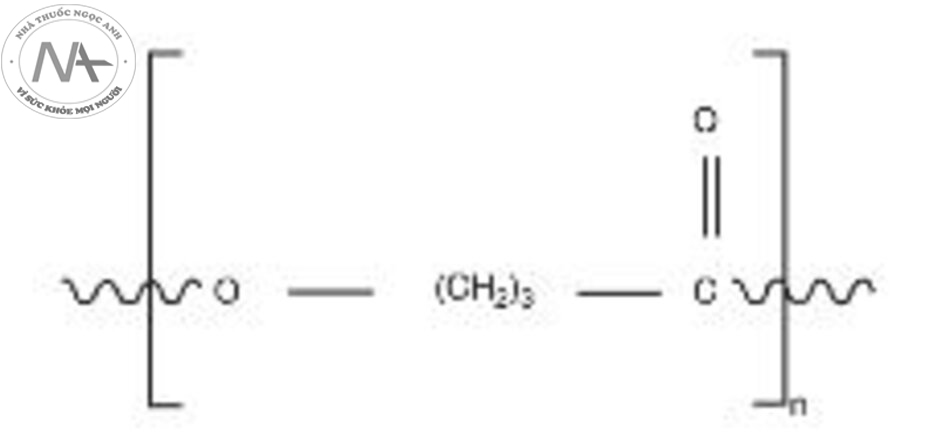
PLLA (Poly-l-Lactic Acid) (Hình 2.45)
Axit Poly-l-lactic (PLLA) là một polyme tương thích sinh học có thể tái hấp thụ sinh học đã được sử dụng rộng rãi trong y tế từ những năm 1970 như là chỉ khâu phẫu thuật có thể hấp thụ hoặc làm vật liệu cấy ghép xương, kẹp trong phẫu thuật chỉnh hình hoặc nha khoa (Hình 2.46). Sculp-tra® (Galderma, Thụy Sĩ) là một công thức bao gồm bột đông khô của axit Poly-l-lactic (PLLA). Nó đã nhận được chứng nhận CE vào năm 1999 và được USFDA phê duyệt để điều trị chứng loạn dưỡng mỡ mặt ở bệnh nhân nhiễm HIV vào năm 2003 [41]. Sau đó vào năm 2009, nó đã được FDA chấp thuận cho việc điều chỉnh các nếp nhăn và đường rãnh trên mặt tại thị trường Hoa Kỳ. Sau khi được đặt trong mô, PLLA dần dần bị phá vỡ thành các đơn phân axit lactic trong vòng 24 tháng thông qua quá trình thủy phân không có enzym [42]. Trong quá trình này, nó tạo ra tình trạng viêm nhiễm có kiểm soát tại khu vực được tiêm để kích thích sản xuất collagen [43]. Sau đó, axit lactic được chuyển hóa thành carbon diox-ide và nước và được bài tiết ra khỏi cơ thể một cách tự nhiên [44]. Các vi hạt PLLA có trong sản phẩm ở dạng tinh thể không đều thay vì các vi cầu mịn. Sculptra® chỉ chứa các hạt PLLA có đường kính 40–60μm để tránh hiện tượng thực bào của đại thực bào [44]. Các thành phần khác có trong bột ngoại trừ PLLA còn có Mannitol và Natri. Sculptra® có dạng lọ với liều lượng 367,5 mg, với mỗi lọ chứa PLLA 150 mg, natri carboxymethylcellulose (CMC) 90 mg và mannitol 127,5 mg. CMC được thêm vào để đảm bảo sự phân bố đồng đều của các hạt PLLA [45] trong khi mannitol được thêm vào để tạo ra một thể đồng nhất, rắn ở quá trình đông khô cuối cùng[46].
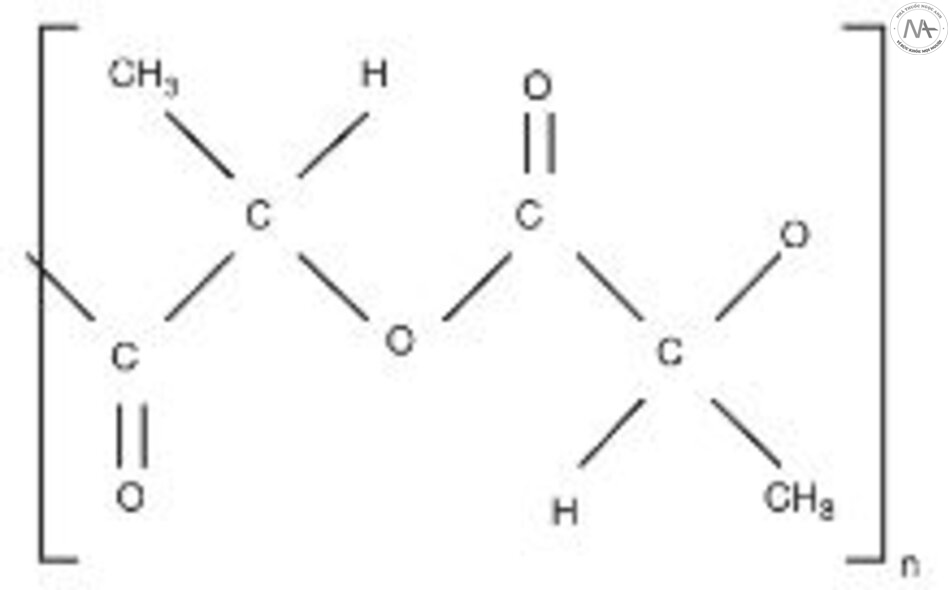
Không giống như Radiesse® hoặc El-lanséTM, kết hợp chất mang gel, Sculp-tra® ở dạng bột đông khô và do đó cần được hòa ra bằng nước cất vô trùng (sau đây gọi là “nước cất”) từ 2-72 giờ trước khi sử dụng [47, 48]. Do có Mannitol trong bột, nên sử dụng nước cất thay vì nước muối để đảm bảo độ thẩm thấu thích hợp. Mặc dù thể tích hòa tan được khuyến nghị là 5 mL mỗi lọ [48, 49], nhưng người tiêm thường sử dụng thể tích hòa tan cao hơn là 10 mL để giảm thiểu nguy cơ hình thành nốt sần [50]. Thay vì chỉ hòa tan với nước cất, tốt hơn là nên thêm 1–2 mL lidocain 1% vào 8–9 mL nước cất để pha loãng sản phẩm nhằm giảm thiểu cảm giác khó chịu khi tiêm [50]. Về thời gian pha, nên pha sản phẩm trước khi sử dụng ít nhất 1 ngày. Việc hòa tan sản phẩm trước bằng nước cất và để nguyên liệu đã hòa tan ở trạng thái đủ hydrat hóa là để đảm bảo sự phân tán đồng đều của các vi hạt PLLA tổng hợp trong hỗn hợp và ngăn chặn sản phẩm vón cục gây ra các nốt sần. Trong dược lý, thời gian bảo quản lên đến 3 ngày sau khi hydrat hóa, nhưng Sculptra® đã hòa tan có thể được bảo quản đến 3–4 tuần trong tủ lạnh, miễn là có các biện pháp bảo vệ cần thiết để ngăn ngừa nhiễm bẩn [50]. Bản thân PLLA không hòa tan trong nước và do đó nó di chuyển lơ lửng khi hòa tan bằng nước cất. Mặt khác, CMC và mannitol có thể hòa tan và sau khi hòa với nước cất, sẽ được hydrat hóa. Do đó, chúng tôi khuyến cáo rằng lọ Sculptra®, một khi đã được hydrat hóa bằng nước cất, nên được khuấy nhẹ ngay trước khi tiêm để đảm bảo PLLA phân tán đồng đều và đồng nhất. Sau đó, hỗn dịch này được chuyển từ lọ vào ống tiêm 1 mL để tiêm vào mô. Để tránh gây bầm tím và vô tình tiêm Sculptra® vào nội mạch, bạn nên sử dụng ống truyền 23-G để phân phối sản phẩm đồng đều vào mặt phẳng sâu dưới da hoặc trên màng xương. Một khu vực dành riêng cho việc sử dụng kim 21-G là vùng thái dương được bao phủ bởi cân mạc dày, không thể dễ dàng xuyên thủng bằng ống thông.
Thể tích tiêm cần thiết để bao phủ toàn bộ khuôn mặt, bao gồm cả gò má trước, hõm má và hõm thái dương, dao động từ 1 lọ đến 2 lọ mỗi buổi tùy thuộc vào mức độ thâm hụt thể tích trên khuôn mặt [48]. Theo các vùng trên khuôn mặt, thể tích sản phẩm được tiêm là 1–2 mL đối với vùng gò má trước , 2–4 mL đối với vùng hõm má và 1–3 mL đối với hõm thái dương mỗi bên. Theo nguyên tắc chung, chỉ nên dùng một lọ mỗi lần trong trường hợp thái dương không cần điều trị. Ở những nơi cần điều trị như ở thái dương hoặc vùng thâm hụt thể tích nghiêm trọng, có thể cần đến hai lọ trong một lần điều trị. Để tránh sự xuất hiện của các nốt sần, điều quan trọng là hạn chế tiêm bề mặt hoặc tiêm ở những vùng da mỏng như vùng quanh mắt. Do đó, trán và mũi có lớp da mỏng không thích hợp để điều trị bằng Sculptra®. PLLA cũng nên tránh sử dụng ở các vùng động như vùng quanh miệng và môi (Hình 2.47). Ngay sau khi tiêm xong, nên xoa bóp kỹ các khu vực được điều trị để phân phối PLLA đồng đều khắp mô để tránh hình thành nốt sần. Ngoài ra, bệnh nhân nên được hướng dẫn xoa bóp các khu vực điều trị trong 5 phút, 5 lần một ngày, trong 5 ngày sau khi điều trị (quy tắc 5-5-5) [51].
Thể tích có được ngay lập tức sau tiêm Sculptra® sẽ biến mất trong vòng 2-3 ngày sau do sự thay thế thể tích trực tiếp được cung cấp bởi vật liệu hòa tan bao gồm nước cất. Quá trình sản sinh collagen mới từ việc tiêm PLLA bắt đầu sau 4 tuần kể từ khi điều trị và đạt đến đỉnh điểm sau tháng thứ ba, với quá trình kích thích sinh học collagen từ việc tiêm kéo dài hơn 25 tháng. Điều trị bằng Sculptra® thường cần khoảng ba lần tiêm cách nhau 3–4 tuần để có hiệu quả tốt nhất [51].
Tuy nhiên, không giống như các chất làm đầy khác như HA, cho phép bác sĩ hoặc bệnh nhân tùy chỉnh thể tích mong muốn, kết quả của Sculptra® phụ thuộc vào sự thay đổi của từng cá nhân trong quá trình hình thành collagen mới ở vùng được điều trị. Do đó, rủi ro là có thể không nhìn thấy kết quả ngay cả sau khi hoàn thành đủ ba lần điều trị. Do đó, điều trị bằng Sculptra® đòi hỏi nỗ lực của bệnh nhân để tối đa hóa sự hình thành collagen, ví dụ, bằng cách tránh giảm cân, chế độ ăn uống lành mạnh giàu protein và duy trì giấc ngủ đều đặn, chất lượng. Liên quan đến các phản ứng có hại, một biến chứng thường gặp của Sculptra® là hình thành nốt sần do vị trí không đồng đều của sản phẩm trong mô hoặc sự kết tụ của các vi hạt PLLA trong sản phẩm được tiêm. Chiến lược phòng ngừa tốt nhất là sử dụng hỗn dịch loãng và đồng nhất được pha loãng đến 10 mL và đảm bảo rằng nó được tiêm đều trong mô. Bệnh nhân cũng nên xoa bóp định kỳ các khu vực được điều trị trong tuần đầu tiên. Cần lưu ý rằng các nốt sần dễ xuất hiện hơn ở các vùng da mỏng, bao gồm cả vùng quanh mắt và trán. Chúng thường xuất hiện với kích thước bằng hạt đỗ hoặc hạt đậu 1–2 tháng sau khi tiêm và sẽ biến mất trong vòng chưa đầy một năm. Trong lúc đó, có thể cố gắng xoa bóp sâu một cách mạnh mẽ để nghiền nát các nốt sần một cách cơ học [52, 53]. Nếu không có cải thiện, có thể nên cân nhắc dùng kim chọc hút các hạt PLLA đã kết tụ thành cục sau khi tiêm nước muối sinh lý vào vùng được điều trị. Trong khi đó, u hạt là một biến chứng khác của Sculptra®, cần được phân biệt với các nốt sần (Hình 2.48). U hạt thường xảy ra sau khi tiêm 3–6 tháng do phản ứng quá mức của cơ thể với chất ngoại lai [51, 53]. Mặc dù chúng xuất hiện dưới dạng nốt sần hoặc sẩn nhưng về mặt mô học, chúng là u hạt ngoại lai. U hạt có thể kèm theo đổi màu da, phù nề và ban đỏ. Các phương pháp điều trị đối với u hạt bao gồm tiêm triamcinolone hoặc tiêm 5-FU [54]. Nếu u hạt không tiêu biến với phương pháp tiêm, nên tiếp tục phẫu thuật cắt bỏ. Cần chú ý vì u hạt không được điều trị có thể tồn tại hơn 10 năm.
Nhận xét: Là một chất kích thích sinh học giúp kích thích sản sinh collagen của cơ thể, Sculptra® có thể là một lựa chọn thay thế hấp dẫn cho những bệnh nhân muốn trẻ hóa nhưng không muốn sử dụng chất làm đầy dạng tiêm do không thích cấy chất lạ vào mặt. Tuy nhiên, nhược điểm là kết quả của Sculptra® phụ thuộc nhiều vào phản ứng của cơ thể để sản sinh col-lagen tự nhiên, có thể khác nhau đáng kể giữa các cá nhân; do đó, kết quả có thể bị hạn chế nếu không muốn nói là gần như không đáng kể ở một số bệnh nhân. Đúng vậy, theo quảng cáo, điểm yếu này có thể được hiểu là một lợi thế của Sculptra® trong việc tăng khối lượng tinh vi mà tự nhiên theo thời gian. Gần đây, PLLA cũng đã được sử dụng như một chất kích thích sinh học, không chỉ tăng cường độ đàn hồi của da mà còn thu nhỏ lỗ chân lông, làm mờ vết sẹo, làm đều màu da thông qua việc tiêm nông vào lớp dưới hạ bì [42].
P-d,l-LA (Poly-d,l-Lactic Acid)
PDLLA (Poly-d,l-Lactic Acid) là một đồng phân lập thể của axit polylactic bao gồm các axit d-và l-lactic được sắp xếp xen kẽ nhau để tạo thành một cấu trúc chuỗi Hình 2.48 U hạt ở vùng dưới ổ mắt do tiêm Sculptra® không phù hợp.không đều. Không giống như PLLA (axit polyl- l-lactic) chỉ bao gồm các axit l-lac-tic liên kết chặt chẽ, các đồng phân d – và l- bao gồm PDLLA được đặt cách xa nhau hơn, dẫn đến liên kết giữa các phân tử yếu hơn. Điều này tạo thành PDLLA với một đặc tính mềm, dễ vỡ với độ cứng giảm và hình dạng vô định hình, không giống như các hạt PLLA có hình dạng tinh thể [55].
Lenisna® (VAIM, Hàn Quốc) và Juve-look® (VAIM, Hàn Quốc) là các sản phẩm có chứa các vi cầu xốp dạng lưới của PDL-LA thu được bằng cách hòa tan các hạt PDLLA vô định hình trong hỗn hợp DMSO (dimethylsulfoxide) và EC (ethylene car-bonate) và phun phân chia hàm lượng (microspraying) (Hình. 2.49). Lenisna® và Juvelook® đã nhận được chứng nhận CE vào năm 2020 và được chấp thuận sử dụng ở Châu Âu. Một ưu điểm đáng chú ý của Lenisna® và Juvelook® là chúng chứa HA thay cho CMC, mặc dù ở dạng không liên kết chéo, giúp các sản phẩm này điều chỉnh thể tích ngay lập tức trong thời gian đầu điều trị.
Một lọ Lenisna® chứa 200 mg PDL-LA đông lạnh khô (PDLLA 170 mg, HA 30 mg), trong khi Juvelook® có trong lọ liều lượng 50 mg (PDLLA 42,5 mg, HA 7,5 mg.) Điều đó cho thấy rằng, Juvelook® có đơn vị liều lượng đóng gói nhỏ hơn của Lenis-na®, vì nó được pha chế đặc biệt để chỉ chứa các vi cầu PDLLA có kích thước 50μm hoặc nhỏ hơn. Do đó, kích thước hạt trung bình của Juvelook® có đường kính 24μm (20–50μm), còn của Lenisna® là 51μm (50–80μm). Điều này cho phép Juvelook® được tiêm trực tiếp vào lớp hạ bì để tái tạo da mà không lo hình thành nốt sần. Đây cũng là đặc điểm phân biệt nó với Sculp-tra®, mặc dù nó có thời gian tác dụng và khả năng nâng đỡ kém hơn Lenisna® [55]. Các vi cầu có trong Lenisna® và Juvelook® bao gồm cấu trúc xốp đa lỗ, khiến chúng thủy phân nhanh hơn từ bên trong (Hình 2.50). Kết quả là, khi bị thủy phân, các sản phẩm này dần dần bị phân hủy thành các đơn phân axit lactic trong khoảng thời gian từ 1–1,5 năm. Như với PLLA, PDLLA cũng tạo ra tình trạng viêm ở vùng được tiêm trong quá trình thoái biến, kích thích sản xuất collagen, mặc dù thời gian và số lượng giảm so với PLLA. Tuy nhiên, điểm này có thể là điểm mạnh, vì nó sẽ giảm nguy cơ hình thành nốt sần và u hạt. Lenis-na® thích hợp để bổ sung thể tích, tương tự như Sculptra®, bằng cách tiêm ở mặt phẳng sâu dưới da; để so sánh, Juvelook®, bao gồm các hạt mịn hơn, chủ yếu để tái tạo da thông qua tiêm vào da.

Cũng như Sculptra®, Lenisna® và Ju-velook® ở dạng bột đông khô không bị hòa tan trong chất mang gel mà thay vào đó, cần phải hòa tan bằng nước cất vô trùng trước khi tiêm. Bột có chứa man-nitol, nên sử dụng nước cất thay vì nước muối để đảm bảo độ thẩm thấu thích hợp. Về thể tích pha loãng, Lenisna® được pha với 6 mL nước cất, trong đó 1 mL lidocain được thêm vào; trong khi Juvelook® được hòa với 4 mL nước cất, thêm vào 1 mL lido-cain [56]. Với Lenisna® và Juvelook® bao gồm nhiều vi cầu xốp và bão hòa dễ dàng hơn so với Sculptra®, chúng có thể được sử dụng ngay sau 30–60 phút hydrat hóa. Tuy nhiên, tốt hơn nếu sử dụng máy khu-ấy trộn lọ trong khoảng 20 phút trước khi tiêm hoặc để sản phẩm pha loãng 1 ngày hoặc tốt nhất là 1 tuần trước khi sử dụng. Các sản phẩm đã hòa tan có thể được bảo quản đến 3–4 tuần trong tủ lạnh, với điều kiện là phải cẩn thận để tránh bị nhiễm bẩn.
Ngay trước khi sử dụng, nên lắc nhẹ lọ Lenisna® hoặc Juvelook® đã thủy hóa để có được hỗn dịch đều và đồng nhất. Sau đó, hỗn dịch này được chuyển từ lọ vào ống tiêm 1 mL để tiêm vào mô. Để tránh bị bầm tím và vô tình tiêm vào nội mạch, bạn nên sử dụng ống truyền 23-G để phân phối sản phẩm đồng đều vào mặt phẳng sâu dưới da hoặc trên màng xương. Khu vực duy nhất được sử dụng kim 21-G là vùng thái dương, được bao phủ bởi căn cơ dày khó có thể xuyên thủng bằng ống thông. Khi sử dụng sản phẩm để thay thế thể tích, nên sử dụng 0,7 mL Lenisna® đã hòa tan được pha thêm với 0,3 mL nước muối [56]. Điều này tạo ra kết quả tương đương với việc sử dụng Sculptra® được pha thành 10 mL. Thể tích sản phẩm được tiêm trên mỗi vùng điều trị (mỗi bên) là 1–2 mL đối với gò má trước, 2–4 mL đối với hõm má trước và 1–3 mL đối với hõm thái dương. Một lọ mỗi phiên là đủ nếu các vùng thái dương không cần điều trị. Nơi có tình trạng thâm hụt thể tích mặt nghiêm trọng, có thể cần đến hai lọ cho một lần điều trị. Kết hợp với HA liên kết chéo có thể được xem xét ở những bệnh nhân muốn bổ sung thể tích tức thì hoặc muốn tránh điều trị lặp lại. Trong trường hợp đó, khuyến cáo sử dụng 0,7 mL Lenisna® đã hòa tan pha loãng thêm với 0,3 mL HA liên kết chéo [56].
Thể tích tiêm phải tương đương với 1,5–2 lần lượng tiêm nếu chỉ sử dụng HA liên kết chéo. Mặc dù kết quả ban đầu có thể không rõ, nhưng thể tích sẽ dần dần tăng rõ ràng sau tuần thứ tư, khi việc tiêm PDLLA bắt đầu sản xuất collagen. Điều này giúp sản phẩm có tính linh hoạt cao hơn, không chỉ được sử dụng để bổ sung thể tích da mặt mà còn để làm săn chắc da. Khi được sử dụng để trẻ hóa da, nên thêm 0,5 mL nước muối vào 0,5 mL Lenisna® đã pha để tiêm vào lớp dưới da. Ngay sau khi hoàn thành việc tiêm, nên xoa bóp các khu vực được điều trị để phân phối PDLLA đồng đều khắp mô, nên xoa bóp nhẹ nhàng hơn so với trường hợp tiêm Sculptra®. Bệnh nhân nên được hướng dẫn xoa vùng điều trị trong 3 phút, 3 lần một ngày, trong 3 ngày sau khi điều trị (quy tắc 3-3-3) [56].
Ưu điểm lớn nhất của Juvelook® là khả năng được tiêm trực tiếp vào lớp hạ bì để làm săn chắc da, vì nó giảm thiểu nguy cơ nổi nốt sần ngay cả khi được đặt rất nông trên da. PDLLA được tiêm vào lớp hạ bì có thể hoạt động như một chất kích thích sinh học, không chỉ tăng cường độ đàn hồi của da mà còn hạn chế lỗ chân lông, vết sẹo, làm đẹp màu da như trường hợp của PLLA [57]. Juvelook® có thể được sử dụng một mình hoặc kết hợp với HA liên kết chéo hoặc các thành phần thúc đẩy da khác như PDRN, chiết xuất nhau thai và exosome. Cần thận trọng ở những vùng da mỏng, chẳng hạn như vùng quanh mắt. Các nốt sần do Juvelook® hình thành được cho là sẽ biến mất trong vòng một tháng sau khi xoa bóp lặp đi lặp lại bằng thiết bị tần số vô tuyến, vì việc áp dụng nhiệt kết hợp với áp suất mạnh có thể có hiệu quả trong việc loại bỏ các vi cầu PDLLA có cấu trúc nhiều xốp và nhiệt độ tan chảy từ 55–60 ° C, thấp hơn 10 ° C so với PLLA.
Tham khảo
- Glogau RG. Fillers: paradigm shifts produce new challenges. In: Carruthers J, Carruthers A, editors. Soft tissue augmen-tation. Philadelphia: Elsevier; 2018. p. 3–6.
- Fraser JR, Laurent TC, Laurent UB. Hyaluronan: its nature, distribution, functions and turnover. J Intern Med. 1997;242(1):27–33.
- Soo-Keun L. Textbook of botulinum toxin and filler. 2nd ed. Seoul: Hanbibook Co; 2018. p. 233–42.
- Stern R. Hyaluronan catabolism: a new metabolic pathway. Eur J Cell Biol. 2004;83(7):317–25.
- Lim CY. Are the hyaluronic acid fillers safe? Filler Toxin. 2014;1(2):6–9.
- Choi S, Choi W, Kim S, Lee SY, Noh I, Kim CW, Choi S. Purification and biocom-patibility of fermented hyaluronic acid for its applications to biomaterials. Biomater Res. 2014;18:6–16.
- Roh NK. The truth nobody tells about fillers. Filler Toxin. 2017;4(2):45–9.
- Kenne L, Gohil S, Nilsson EM, Karls-son A, Ericsson D, Helander Kenne A, Nord LI. Modification and cross-linking param-eters in hyaluronic acid hydrogels—defi-nitions and analytical methods. Carbohydr Polym. 2013;91(1):410–8.
- Humphrey S, Fotzgeral R. Juvederm family. In: Carruthers J, Carruthers A, ed-itors. Soft tissue augmentation. Philadel-phia: Elsevier; 2018. p. 67–70.
- Narins RS, Mariwalla K. NASHA Family. In: Carruthers J, Carruthers A, ed-itors. Soft tissue augmentation. Philadel-phia: Elsevier; 2018. p. 17–24.
- Sundaram H, Cassuto D. Biophysical characteristics of hyaluronic acid soft-tis-sue fillers and their relevance to aes-thetic applications. Plast Reconstr Surg. 2013;132(4 Suppl 2):5S–21S.
- Molliard GS, Albert S, Mondon K. Key importance of compression proper-ties in the biophysical characteristics of hyaluronic acid soft-tissue fillers. J Mech Behav Biomed Mater. 2016;61:290–8.
- Sundaram H, Rohrich RJ, Liew S, Sattler G, Talarico S, Trévidic P, Molliard SG. Cohesivity of hyaluronic acid fillers: development and clinical implications of a novel assay, pilot validation with a five-point grading scale, and evaluation of six U.S. Food and Drug Administra-tion-approved fillers. Plast Reconstr Surg. 2015;136(4):678–86.
- Tran C, Carraux P, Micheels P, Kaya G, Salomon D. In vivo bio-integration of three hyaluronic acid fillers in human skin: a histological study. Dermatology. 2014;228(1):47–54.
- Park KY, Kim JM, Seok J, Seo SJ, Kim MN, Youn CS. Comparative split-face study of durational changes in hyaluronic acid fillers for mid-face volume augmentation. Dermatol Ther. 2019;32(4):e12950.
- Fagien S, Bertucci V, von Grote E, Mashburn JH.Rheologic and Physicochem-ical Properties Used to Differentiate Inject-able Hyaluronic Acid Filler Products. Plast Reconstr Surg. 2019;143(4):707e−720e.
- Monheit GD, Baumann LS, Gold MH, Goldberg DJ, Goldman MP, Narins RS, Bachtell N, Garcia E, Kablik J, Gershkovich J, Burkholder D. Novel hyaluronic acid der-mal filler: dermal gel extra physical prop-erties and clinical outcomes. Dermatol Surg. 2010;36(Suppl 3):1833–41.
- Rosamilia G, Hamade H, Freytag DL, Frank K, Green JB, Devineni A, Gavril DL, Hernandez CA, Pavicic T, Cotofana S. Soft tissue distribution pattern of fa-cial soft tissue fillers with different vis-coelastic properties. J Cosmet Dermatol. 2020;19(2):312–20.
- Monheit G, Kestemont P, Sundaram H. Hyaluronic acid fillers on the horizon: roundtable discussion. J Drugs Dermatol. 2012;11(8):s26–8; discussion s28.
- Buntrock H, Reuther T, Prager W, Kerscher M. Efficacy, safety, and patient satisfaction of a monophasic cohesive polydensified matrix versus a biphasic nonanimal stabilized hyaluronic acid fill-er after single injection in nasolabial folds. Dermatol Surg. 2013;39(7):1097–105.
- Mandelson B. Rayleigh scatter-ing. https:// en.m.wikipedia.org/wiki/Rayleigh_scattering.
- Rootman DB, Lin JL, Goldberg R, Rootman DB. Does the Tyndall effect describe the blue hue periodically ob-served in subdermal hyaluronic acid gel placement? Ophthal Plast Reconstr Surg. 2014;30(6):524–7.
- Yang SD, Shin S, Lee J, Yang SD. Two randomized controlled trials of hyaluron-ic acid fillers for the correction of nasola-bial folds. Plast Reconstr Surg Glob Open. 2020;8(7):e2975.
- Huh CH, Eom Y, Yang SD, Shin JW, Seo KK. A randomized, active-controlled, 52-week study of hyaluronic acid fillers for anteromedial malar region augmen-tation. Plast Reconstr Surg Glob Open. 2020;8(2):e2648.
- Choi SY, Han HS, Yoo KH, Lee JS, Kim BJ, Lee YW. Reduced pain with injection of hyaluronic acid with pre-incorporated lidocaine for nasolabial fold correction: a multicenter, double-blind, randomized, ac-tive-controlled, split-face designed, clinical study. J Cosmet Dermatol. 2020;19:3229–33. https://doi. org/10.1111/jocd.13421.
- Joo HJ, Woo YJ, Kim JE, Kim BJ, Kang H. A randomized clinical trial to evaluate the efficacy and safety of lidocaine-con-taining monophasic hyaluronic acid filler for nasolabial folds. Plast Reconstr Surg. 2016;137(3):799–808.
- Jung JM, Lee WS, Kim HT, Moon YS, Paik SH, Lee WJ, Chang SE, Lee MW, Won CH, Kim BJ. A multi-center, randomized, double blinded, comparative study of two hyaluronic acid fillers for temporary resto-ration of mid-face volume in Asians. J Cos-met Dermatol. 2020;19(7):1619–26.
- Won L, et al. Soft tissue filler prop-erties can be altered by a small-diameter needle. Dermatol Surg. 2020;46(9):1155–62.
- LEE W, et al. Clinical application of a new hyaluronic acid filler based on its rhe-ological properties and the anatomical site of injection. Biomed Dermatol. 2018;2:22.
- Khetarpal S, Dover JS. Introduction to permanent fillers: pors and cons. In: Carruthers J, Carruthers A, editors. Soft tissue augmentation. Philadelphia: Elsevi-er; 2018. p. 67–70.
- Sadick NS. Bellafill. In: Carruthers J, Carruthers A, editors. Soft tissue aug-mentation. Philadelphia: Elsevier; 2018. p. 79–84.
- Ono S, Ogawa R, Hyakusoku H. Com-plications after polyacrylamide hydrogel injection for soft-tissue augmentation. Plast Reconstr Surg. 2010;126(4):1349–57.
- Kavoussi H, Ebrahimi A. Delayed gel indurations as an adverse effect of poly-acrylamide filler and its easy treatment. Dermatol Res Pract. 2012;2012:539153.
- Radmanesh M, Radmanesh R, Baha-doram M. Successful removal of polyacryl-amide hydrogel by pulsed fiberoptic 1444-nm Nd-YAG laser. J Cosmet Laser Ther. 2013;15(6):342–4.
- Drobeck HP, et al. Histologic ob-servation of soft tissue responses to im-planted, multifaceted particles and discs of hydroxylapatite. J Oral Maxillofac Surg. 1984;42:143–9.
- Sheinin RC, Mahmould BH, Ozog DM. Radiesse and radiesse with lidocaine. In: Carruthers J, Carruthers A, editors. Soft tissue augmentation. Philadelphia: Elsevi-er; 2018. p. 41–8.
- Voigts R, Devore DP, Grazer JM. Dispersion of calcium hydroxylapatite accumulations in the skin: animal stud-ies and clinical practices. Dermatol Surg. 2010;36(Supplement s1):798–803.
- Pavicic T. Calcium hydroxylapatite filler: an overview of safety and tolera-bility. J Drugs Dermatol. 2013;12(9):996–1002.
- Tzikas TL. A 52-month summary of results using calcium hydroxylapatite for facial soft tissue augmentation. Dermatol Surg. 2008;34(Suppl 1):9–15.
- Sadick NS, Katz BE, Roy D. A mul-ticenter, 47-month study of safety and ef-ficacy of calcium hydroxylapatite for soft tissue augmentation of nasolabial folds and other areas of the face. Dermatol Surg. 2007;33(Suppl 2):S122–6; discussion S126–7.
- Goldie K, Peeters W, Alghoul M, But-terwick K, Casabona G, Chao YYY, Costa J, Eviatar J, Fabi SG, Lupo M, Sattler G, Wal-dorf H, Yutskovskaya Y, Lorenc P, Goldie K. Global consensus guidelines for the injec-tion of diluted and hyperdiluted calcium hydroxylapatite for skin tightening. Der-matol Surg. 2018;44(Suppl 1):S32–41.
- Beleznay K, Fitzgerald R, Humphrey S. Poly-L-lactic acid. In: Carruthers J, Car-ruthers A, editors. Soft tissue augmenta-tion. Philadelphia: Elsevier; 2018. p. 49–56.
- Brown SA, Rohrich RJ, Baumann L, Brandt FS, Fagien S, Glazer S, Kenkel JM, Lowe NJ, Monheit GD, Narins RS, Ren-don MI, Werschler WP. l. Subject global evaluation and subject satisfaction using injectable poly-L-lactic acid versus hu-man collagen for the correction of naso-labial fold wrinkles. Plast Reconstr Surg. 2011;127(4):1684–92.
- Fitzgerald R, Bass LM, Goldberg DJ, Graivier MH, Lorenc ZP, Lin MJ, Dubin DP, Goldberg DJ, Khorasani H. Practices in the usage and reconstitution of poly-Llactic acid. J Drugs Dermatol. 2019;18(9):880–6.
- Stein P, Vitavska O, Kind P, Hoppe W, Wieczorek H, Schürer NY. The biologi-cal basis for poly-Llactic acid-induced aug-mentation. J Dermatol Sci. 2015;78(1):26–33.
- Drugs.com. Sodium Carboxymethyl-cellulose. https:// www.drugs.com/inac-tive/carboxymethylcellulosesodium-452.html. Accessed 16 Apr 2019.
- Schierle CF, Casas L. Nonsurgical rejuvenation of the aging face with in-jectable poly-L-lactic acid for restoration of soft tissue volume. Aesthet Surg J. 2011;31(1):95–109.
- Sculptra®Aesthetic. Product Label-ing. Instructions for Use. L.P. Fort Worth, TX: Galderma Laboratories; September 2014.
- Palm M, Chayavichitsilp P. The “skinny” on Sculptra: a practical primer to volumization with poly-L-lactic acid. J Drugs Dermatol. 2012;11(9):1046–52.
- Lowe NJ, Maxwell CA, Lowe P, Shah A, Patnaik R. Injectable poly-l-lactic acid: 3 years of aesthetic experience. Dermatol Surg. 2009;35(Suppl 1):344–9.
- Lin MJ, Dubin DP, Goldberg DJ, Kho-rasani H. Practices in the usage and recon-stitution of polyL-lactic acid. J Drugs Der-matol. 2019;18(9):880–6.
- Redaelli A, Forte R. Cosmetic use of polylactic acid: report of 568 patients. J Cosmet Dermatol. 2009;8(4):239–48.
- Lee JM, Kim YJ. Foreign body gran-ulomas after the use of dermal fillers: pathophysiology, clinical appearance, his-tologic features, and treatment. Arch Plast Surg. 2015;42(2):232–9.
- Graivier MH, Bass LM, Lorenc ZP, Fitzgerald R, Goldberg DJ, Lemperle G. Differentiating nonpermanent inject-able fillers: prevention and treatment of filler complications. Aesthet Surg J. 2018;38(suppl_1):S29–40.
- Blanco MD, Sastre RL, Teijón C, Olmo R, Teijón JM. Degradation behaviour of microspheres prepared by spray-dry-ing poly(D,L-lactide) and poly(D,Llac-tide-co-glycolide) polymers. Int J Pharm. 2006;326(1–2):139–47.
- Jung WK. Sculptra vs. Esthephil vs. Etreville vs. Lenisa vs. Juvelook. Filler Tox-in. 2020;6(1):35–9.
- Bohnert K, Dorizas A, Lorenc P, Sadick NS. Randomized, controlled, mul-ticentered, double-blind investigation of injectable poly-L-lactic acid for im-proving skin quality. Dermatol Surg. 2019;45(5):718–24.