COVID-19, Bệnh hô hấp
Yếu tố tiên lượng cho bệnh nhân ARDS COVID-19 được thở máy là gì?
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
nhathuocngocanh.com – Bài viết Sự phát triển của tỷ lệ thông khí là một yếu tố tiên lượng trong Bệnh nhân ARDS COVID-19 được thở máy được biên dịch bởi bác sĩ Đặng Thanh Tuấn – Bệnh viện Nhi Đồng 1. Để tải link PDF của bài viết, xin vui lòng click vào link ở đây
Tóm tắt
Bối cảnh
Tỷ lệ tử vong do COVID-19 cao, đặc biệt ở những bệnh nhân cần thở máy. Mục đích của nghiên cứu là khảo sát mối liên quan giữa tỷ lệ tử vong và các biến số đo được trong ba ngày đầu thở máy ở bệnh nhân được đặt nội khí quản COVID-19 lúc nhập viện ICU.
Phương pháp
Nghiên cứu thuần tập đa trung tâm, quan sát, bao gồm các bệnh nhân liên tiếp mắc COVID-19 nhập viện 44 ICU Tây Ban Nha từ ngày 25 tháng 2 đến ngày 31 tháng 7 năm 2020, những người này yêu cầu đặt nội khí quản khi nhập viện ICU và thở máy trong hơn ba ngày. Chúng tôi đã thu thập dữ liệu nhân khẩu học và lâm sàng trước khi nhập viện; thông tin về diễn biến lâm sàng ở ngày 1 và ngày 3 thở máy; và kết quả.
Các kết quả
Trong số 2.095 bệnh nhân COVID-19 nhập viện ICU, 1.118 (53,3%) được đặt nội khí quản vào ngày thứ nhất và vẫn thở máy ở ngày thứ ba. Từ ngày 1 đến ngày 3, PaO 2/FiO2 tăng từ 115,6 [80,0–171,2] lên 180,0 [135,4–227,9] mmHg và tỷ số thông khí từ 1,73 [1,33–2,25] lên 1,96 [1,61–2,40]. Tỷ lệ tử vong khi nhập viện là 38,7%. Tỷ lệ thông khí (OR 1,04 [CI 1,01–1,07], p= 0,030) và creatinine tăng cao hơn (OR 1,05 [CI1,01–1,09], p = 0,005) và số lượng tiểu cầu tăng thấp hơn (OR 0,96 [CI 0,93–1,00], p = 0,037) có liên quan độc lập với nguy cơ tử vong cao hơn. Không quan sát thấy mối liên quan giữa tỷ lệ tử vong và sự thay đổi PaO2/FiO2 (OR 0,99 [CI 0,95 đến 1,02], p = 0,47).
Kết luận
Tỷ lệ thông khí cao hơn và sự gia tăng của nó ở ngày thứ 3 có liên quan đến tỷ lệ tử vong ở bệnh nhân COVID-19 được thở máy khi nhập viện ICU. Không tìm thấy mối liên quan nào trong sự biến đổi PaO2/FiO2.
Bối cảnh
Tỷ lệ tử vong được ghi nhận trong đại dịch COVID-19, mặc dù có thể thay đổi, là rất cao, đặc biệt là ở những bệnh nhân nhập viện ICU, và thậm chí cao hơn ở những bệnh nhân cần thở máy xâm nhập (MV, mechanical ventilation) cho ARDS [1]. Trong một phân tích tổng hợp gần đây bao gồm 69 nghiên cứu, tỷ lệ tử vong theo trường hợp chung là 45% [2]. Khi các trường hợp được phân tầng theo độ tuổi, tỷ lệ tử vong tăng lên 84,4% ở những bệnh nhân trên 80 tuổi. Tuy nhiên, sự không đồng nhất quan sát được là cao (I> 90%) nhưng với kiểm định hồi quy Egger không có ý nghĩa cho thấy không có sai lệch về công bố. 15 nghiên cứu bao gồm từ châu Âu cho kết quả tương tự so với các châu lục khác [2].
Cơ quan đăng ký giám sát Euro ở Tây Ban Nha [3] đã báo cáo dữ liệu dịch tễ học từ đợt đại dịch đầu tiên ở Tây Ban Nha đến ngày 17 tháng 4 năm 2020. Họ báo cáo 8.289 bệnh nhân nhập viện ICU (4,6% tổng số), 4.085 trong số đó yêu cầu MV (78% của những người được nhận vào ICU). Tỷ lệ tử vong chung của bệnh nhân thở máy là 42%. Trong số các yếu tố khác nhau liên quan đến tử vong, tuổi tác, bệnh thận mãn tính và thời gian ngắn hơn từ khi khởi phát triệu chứng đến khi khám Cấp cứu là quan trọng nhất. Nghiên cứu mạng REVA [4] gần đây đã mô tả 4.643 bệnh nhân nhập viện ICU ở Pháp. Vào ngày đầu tiên nhập viện, 63% bệnh nhân được đặt nội khí quản và về tổng thể, 80% được MV. Tỷ lệ tử vong trong 90 ngày liên quan đến tuổi tác, tiểu đường, béo phì và ARDS nặng.
Phần lớn các cuộc điều tra đối với bệnh nhân COVID nhập viện ICU đã cố gắng xác định các yếu tố tiên lượng bằng cách sử dụng dữ liệu từ ngày đầu tiên nhập viện hoặc dữ liệu thu được vào ngày đầu tiên nhập viện ICU. Ở bệnh nhân ICU, những dữ liệu này có thể bị hiểu sai, hoặc vì bệnh nhân không “ổn định về mặt lâm sàng” hoặc vì chúng không liên quan vì chúng không thể sửa đổi (ví dụ: tuổi, béo phì, v.v.). Mặt khác, trong nhiều bệnh cấp tính đường hô hấp có suy hô hấp cấp, tình trạng bệnh nhân 72 giờ sau khi nhập viện ICU cung cấp các manh mối quan trọng về tiên lượng, có tính đến những gì đã xảy ra kể từ khi nhập viện, bao gồm cả xử trí đầy đủ hoặc không đầy đủ [5, 6]. Loại nghiên cứu quan sát này có thể cung cấp bằng chứng về các can thiệp y tế có lợi.
CIBERESUCICOVID nghiên cứu các bệnh nhân nhập viện ICU do nhiễm SARS-CoV-2 [7]. Những bệnh nhân yêu cầu thở máy xâm nhập trong ngày đầu tiên nhập viện ICU và những người vẫn thở máy 3 ngày sau đó được chọn để nắm bắt những gì đã xảy ra kể từ khi nhập viện đến 72 giờ sau khi nhập viện ICU. Giả thuyết của chúng tôi là sự khác biệt giữa ngày 1 và ngày 3 về các biến số liên quan và có liên quan độc lập với tỷ lệ tử vong tại bệnh viện có thể giúp bác sĩ lâm sàng thiết lập các biện pháp điều chỉnh và hiểu rõ hơn về tiên lượng.
Phương pháp
Thiết kế nghiên cứu
CIBERESUCICOVID là một nghiên cứu thuần tập đa trung tâm, quan sát, tiền cứu/hồi cứu, thu nhận bệnh nhân nhiễm COVID-19 được nhận vào ICU Tây Ban Nha (các trung tâm tham gia được liệt kê trong Hồ sơ bổ sung 1: Bảng 1). Nghiên cứu đã được phê duyệt bởi Hội đồng Đánh giá Nội bộ của Viện và đã nhận được sự đồng ý của bệnh nhân hoặc người thân của họ. Các nhà nghiên cứu địa phương đã được một thành viên của nhóm nghiên cứu liên hệ và các bệnh viện tham gia đã được sự chấp thuận của ủy ban đạo đức địa phương. Việc thu thập dữ liệu được bắt đầu vào tháng 5 năm 2020. Các bệnh nhân liên tiếp nhập viện trước khi bắt đầu nghiên cứu được đưa vào hồi cứu. Bệnh nhân nhập viện sau khi bắt đầu nghiên cứu được bao gồm tiền cứu. Dữ liệu bệnh nhân được xác định danh tính được thu thập và lưu trữ thông qua công cụ thu thập dữ liệu điện tử REDCap, được lưu trữ tại CIBER, Tây Ban Nha. Dữ liệu từ hồ sơ y tế của bệnh nhân đã được các nhà nghiên cứu địa phương được đào tạo đưa vào cơ sở dữ liệu riêng biệt. Trước khi phân tích thống kê, dữ liệu đã được kiểm tra bởi ba người thu thập dữ liệu có kinh nghiệm độc lập được đào tạo về chăm sóc quan trọng (PC, AM, CS) và các nhà điều tra địa điểm đã được liên hệ với bất kỳ câu hỏi nào. Các phân tích còn thiếu đã được thực hiện và các nhà điều tra hiện trường đã được liên hệ để có được dữ liệu đáng tin cậy và đầy đủ nhất có thể (Tệp bổ sung 1: Hình 1). Kết quả được báo cáo theo hướng dẫn Tăng cường báo cáo các nghiên cứu quan sát trong dịch tễ học (STROBE) [8].
Bảng 1 Đặc điểm nhân khẩu học và lâm sàng của những bệnh nhân được thở máy xâm nhập (MV) trong 24 giờ đầu tiên nhập viện ICU
| No All | patients
(n = 1118) |
Survivors (n = 685) | Non-survivors (n = 433) | p–value
|
|
| Age, years | 1118 | 65.0 [57.0–72.0] | 62.0 [53.0–69.0] | 69.0 [63.0–74.0] < 0.001 | |
| Age, categories | 1118 | ||||
| < 50 | 144 (12.9%) | 125 (18.3%) | 19 (4.4%) < 0.001 | ||
| 50–69 | 612 (54.7%) | 407 (59.4%) | 205 (47.3%) < 0.001 | ||
| 70–79 | 345 (31.0%) | 149 (21.8%) | 197 (45.5%) < 0.001 | ||
| ≥ 80 | 16 (1.4%) | 4 (0.6%) | 12 (2.8%) 0.004 | ||
| Sex, female | 1118 | 322 (28.8%) | 211 (30.8%) | 111 (25.6%) | 0.07 |
| BMI, kg/m2 | 1019 | 28.1 [25.6–31.5] | 28.3 [25.7–31.6] | 27.8 [25.5–31.3] | 0.27 |
| Comorbidities | |||||
| Active smoker | 741 | 61 (8.2%) | 33 (7.1%) | 28 (10.4%) | 0.17 |
| Hypertension | 1117 | 555 (49.7%) | 308 (45.0%) | 247 (57.2%) < 0.001 | |
| Diabetes mellitus | 1117 | 258 (23.1%) | 153 (22.3%) | 105 (24.3%) | 0.47 |
| Dyslipidemia | 1117 | 275 (24.6%) | 165 (24.1%) | 110 (25.4%) | 0.62 |
| Chronic cardiac failure | 1117 | 138 (12.4%) | 60 (8.8%) | 78 (18.1%) < 0.001 | |
| Chronic kidney disease | 1117 | 58 (5.1%) | 25 (3.6%) | 33 (7.4%) 0.003 | |
| Chronic respiratory disease | 1117 | 119 (10.7%) | 52 (7.6%) | 67 (15.5%) < 0.001 | |
| Days since first symptoms | 1098 | 7.0 [5.0–9.0] | 7.0 [5.0–9.0] | 7.0 [4.0–9.0] 0.047 | |
| Days from hospital admission to intubation | 1116 | 1.0 [0.0–4.0] | 1.0 [0.0–3.0] | 1.0 [0.0–4.0] | 0.38 |
| APACHE score | 615 | 12.0 [9.5–16.0] | 11.0 [8.8–15.0] | 14.0 [11.0–18.0] < 0.001 | |
| SOFA score | 779 | 7.0 [5.0–8.0] | 7.0 [4.0–8.0] | 7.0 [5.0–9.0] < 0.001 | |
| SOFA hemodynamic component | 1041 | 3.0 [0.0–4.0] | 3.0 [0.0–4.0] | 3.0 [0.0–4.0] | 0.09 |
| SOFA renal component | 1108 | 0.0 [0.0–0.0] | 0.0 [0.0–0.0] | 0.0 [0.0–1.0] < 0.001 | |
| Temperature, ºC | 995 | 36.9 [36.0–37.8] | 37.0 [36.0–37.9] | 36.8 [36.0–37.8] | 0.08 |
| Respiratory rate, bpm | 942 | 25.0 [20.0–30.0] | 24.0 [20.0–30.0] | 25.0 [20.0–30.0] | 0.63 |
| Arterial blood gases at ICU admission | |||||
| PaO2/FiO2 ratio, mmHg | 1067 | 115.6 [80.0–171.2] | 117.5 [82.2–176.7] | 111.27 [74.1–157.9] 0.01 | 7 |
| PaO2/FIO2 ratio categories | 1067 | ||||
| PaO2/FiO2 ratio < 100 mmHg | 424 (39.7%) | 249 (37.4%) | 175 (43.5%) 0.05 | ||
| PaO2/FiO2 ratio ≥ 100 and < 200 mmHg | 462 (43.3%) | 295 (44.4%) | 167 (41.5%) | 0.37 | |
| PaO2/FiO2 ratio ≥ 200 and < 300 mmHg | 132 (12.4%) | 88 (13.2%) | 44 (11.0%) | 0.29 | |
| PaO2/FiO2 ratio ≥ 300 mmHg | 49 (4.6%) | 33 (5.0%) | 16 (4.0%) | 0.55 | |
| pH | 1076 | 7.36 [7.29–7.43] | 7.38 [7.31–7.44] | 7.33 [7.26–7.41] < 0.001 | |
| PaCO2, mmHg | 1084 | 43.9 [36.0–52.0] | 43.0 [36.0–50.5] | 45.1 [37.0–55.0] 0.001 | |
| Lactate, mg/dL | 753 | 13.0 [9.9–17.1] | 12.6 [9.0–16.2] | 14.4 [10.8–18.9] < 0.001 | |
| Laboratory findings at ICU admission | |||||
| Lymphocyte count, 109/L | 1095 | 0.63 [0.43–0.90] | 0.67 [0.47–0.95] | 0.60 [0.40–0.84] 0.001 | |
| Neutrophil count, 109/L | 472 | 7.66 [5.57–11.32] | 7.32 [5.30–10.84] | 7.97 [5.81–12.00] | 0.10 |
| Platelet count, 109/L | 1106 | 226.0 [173.0–299.0] | 236.0 [182.0–
308.8] |
212.0 [163.8–277.3] < | 0.001 |
| D-dimers, mg/L | 877 | 1.12 [0.59–3.52] | 0.98 [0.53–2.30] | 1.71 [0.70–5.51] < 0.001 | |
| Ferritin, ng/mL | 379 | 1398 [821–2250] | 1330 [766–2172] | 1500 [890–2400] | 0.11 |
| IL6, pg/mL | 215 | 114.0 [47.5–181.4] | 103.1 [45.1–
186.8] |
125.9 [60.2–153.2] | 0.66 |
| CRP, mg/dL | 987 | 17.5 [9.4–26.6] | 17.0 [9.1–26.0] | 18.4 [10.0–27.7] | 0.068 |
| Bilirubin, mg/dL | 1018 | 0.62 [0.42–1.00] | 0.64 [0.43–1.00] | 0.60 [0.40–1.00] | 0.76 |
| Serum creatinine, mg/dL | 1108 | 0.87 [0.67–1.15] | 0.82 [0.64–1.07] | 0.95 [0.75–1.28] < 0.001 | |
| Ventilatory setting and pulmonary mechanics at MV start | |||||
| Tidal volume/PBW (mL/kg) | 908 | 7.1 [6.4–8.0] | 7.1 [6.4–7.9] | 7.1 [6.4–8.0] | 0.80 |
| Respiratory rate, bpm | 999 | 20.0 [18.0–24.0] | 20.0 [18.0–24.0] | 20.0 [18.0–24.0] | 0.63 |
| PEEP, cmH2O | 1045 | 12.0 [10.0–14.0] | 12.0 [10.0–14.0] | 12.0 [10.0–14.0] | 0.52 |
| FiO2, % | 1064 | 75.0 [60.0–100.0] | 70.0 [60.0–100.0] | 80.0 [60.0–100.0] < 0.0 | 01 |
| Peak inspiratory pressure, cmH2O | 509 | 31.0 [27.0–35.0] | 30.0 [27.0–34.0] | 31.0 [27.5–35.5] | 0.08 |
| End-inspiratory plateau pressure, cmH2O | 440 | 25.0 [22.0–28.0] | 25.0 [21.0–28.0] | 25.0 [22.0–28.0] | 0.10 |
| Driving pressure, cmH2Oa | 432 | 12.0 [9.6–15.0] | 12.0 [9.0–14.0] | 12.0 [9.8–15.0] | 0.25 |
| Compliance, mL/cmH2Ob | 413 | 37.1 [29.3–50.0] | 37.1 [30.0–50.0] | 35.8 [28.2–50.0] | 0.33 |
| Ventilatory ratioc | 889 | 1.73 [1.33–2.25] | 1.68 [1.32–2.15] | 1.87 [1.41–2.36] 0.001 | |
| Position | 960 | ||||
| Supine | 591 (61.6%) | 394 (65.5%) | 197 (55.0%) < 0.001 | ||
| Prone | 346 (36.0%) | 192 (31.9%) | 154 (43.0%) 0.008 | ||
| Other | 23 (2.4%) | 16 (2.6%) | 7 (2.0%) | 0.46 |

Nghiên cứu dân số và thu thập dữ liệu
Tất cả các bệnh nhân liên tiếp được nhận vào ICU tại một trung tâm tham gia từ ngày 25 tháng 2 đến ngày 31 tháng 7 năm 2020, được ghi danh nếu họ đáp ứng các tiêu chí sau: ≥ 18 tuổi, nhập viện ICU và phòng thí nghiệm xác nhận nhiễm SARS-CoV-2. Đối với nghiên cứu này, chúng tôi chọn những bệnh nhân cần thở máy xâm nhập trong ngày đầu tiên nhập viện ICU và những người này vẫn được thở máy 3 ngày sau đó. Sự lựa chọn này phản hồi để nắm bắt những gì đã xảy ra trong những ngày đầu tiên đưa vào ICU trong một quần thể đồng nhất. Bệnh nhân bị loại trừ nếu họ bị nhiễm SARS-CoV-2 chưa được xác nhận, không có dữ liệu tại thời điểm ban đầu hoặc khi xuất viện, hoặc được nhập viện ICU vì các lý do khác. Những bệnh nhân yêu cầu sự hỗ trợ của ECMO trong giai đoạn này (tức là nhập viện ICU – Ngày thứ 3) đã được loại trừ khỏi phân tích để tránh sai lệch tiềm ẩn trong phân tích khí máu và cơ học phổi [9].
Sau khi đưa vào, dữ liệu dịch tễ học trước đó bao gồm nhân khẩu học, bệnh đi kèm, triệu chứng lâm sàng, trình tự bệnh và phương pháp điều trị được thực hiện khi nhập viện đã được thu thập. Các nhà nghiên cứu địa điểm sau đó đã thu thập dữ liệu có được khi nhập viện, nhập viện ICU, bắt đầu MV, 72–96 giờ sau khi nhập viện ICU, cai máy, xuất viện ICU và xuất viện, bao gồm các dấu hiệu sinh tồn, thiết bị hỗ trợ hô hấp (ví dụ: oxy mặt nạ, oxy lưu lượng cao qua mũi, và thông khí không xâm lấn và xâm lấn), sử dụng các liệu pháp bổ trợ (ví dụ: phong tỏa thần kinh cơ, nằm sấp và thủ thuật huy động), các phát hiện trong phòng thí nghiệm, khí máu động mạch và cài đặt thở máy nếu thích hợp. Các thông số huyết động và rối loạn chức năng cơ quan được nghiên cứu với Điểm đánh giá thất bại cơ quan tuần tự (SOFA) khi nhập viện ICU. Các phương pháp điều trị dược lý được thực hiện khi và trong quá trình nhập viện ICU cho đến khi xuất viện khỏi ICU hoặc bệnh viện, hoặc tử vong, cũng được thu thập.
Dữ liệu cụ thể về MV kể từ khi bắt đầu đặt nội khí quản, cũng như ở ngày thứ 3 đã được phân tích. Các thông số MV liên quan đến tổn thương phổi do thông khí (VILI) như thể tích khí lưu thông, tần số thở, áp lực bình nguyên cuối thì hít vào và áp lực đỉnh hít vào, áp lực dương cuối kỳ thở ra (PEEP), áp lực đẩy và độ giãn nở tĩnh của hệ thống hô hấp (Crs) đã được thu thập. Suy giảm oxy được phân tích bằng cách sử dụng tỷ lệ PaO2/FiO2 và các bất thường của chuyển hóa CO2 được nghiên cứu bằng cách sử dụng tỷ lệ thông khí (VR, ventilatory ratio), một thông số thay thế của Vd/Vt. Các giá trị sự kiện tồi tệ nhất được ưu tiên ghi lại.
Các định nghĩa
Chẩn đoán ARDS dựa trên định nghĩa của Berlin [10]. Bệnh hô hấp mãn tính được định nghĩa là bất kỳ bệnh phổi tắc nghẽn mãn tính nào, bệnh xơ nang, giãn phế quản và các bệnh phổi mô kẽ, ngoại trừ bệnh hen suyễn [11]. Thể tích khí lưu thông được báo cáo bằng mL/kg trọng lượng cơ thể dự đoán (PBW). Áp lực đẩy được định nghĩa là áp lực bình nguyên trừ PEEP. Crs được tính bằng thể tích khí lưu thông/(áp lực cao nguyên – PEEP). Tỷ lệ thông khí được xác định là (thông khí phút x PaCO2)/(PBW × 100 × 37,5) (giá trị bình thường: 1). Các phép đo delta được tính là sự khác biệt giữa giá trị tại ngày thứ 3 của đưa vào ICU và ngày đầu tiên của đưa vào ICU. Các định nghĩa khác đã được báo cáo trong Dữ liệu Bổ sung Trực tuyến.
Kết quả
Kết cục chính là tử vong trong bệnh viện. Tử vong ICU, tử vong 28 ngày, thời gian thở máy, thời gian ICU, và thời gian nằm viện cũng được thu thập và báo cáo. Các biến chứng phổi (tức là viêm phổi bệnh viện, viêm khí quản, ARDS, tràn khí màng phổi, tràn dịch màng phổi, thuyên tắc phổi) và các biến chứng ngoài phổi (bao gồm các biến chứng ảnh hưởng đến hệ thống huyết học, tim mạch, thận, tiêu hóa, gan, nội tiết và thần kinh) trong quá trình nhập viện ICU cũng được thu thập và bao gồm khi xuất viện.
Phân tích thống kê
Chúng tôi báo cáo số lượng và tỷ lệ phần trăm bệnh nhân cho các biến phân loại và trung vị [phần tư thứ nhất – phần tư thứ ba] cho các biến liên tục. Phần trăm đã được tính trừ dữ liệu bị thiếu. Các biến phân loại được so sánh bằng kiểm định Chi bình phương hoặc kiểm định chính xác của Fisher, trong khi các biến liên tục được so sánh bằng kiểm định Mann – Whitney U phi tham số.
Để khám phá các yếu tố nguy cơ liên quan đến tử vong trong bệnh viện, các mô hình đa biến tác động hỗn hợp [12, 13] đã được sử dụng, được xác định bằng phân bố xác suất nhị thức và hàm liên kết logit, với các trung tâm là hiệu ứng ngẫu nhiên. Các biến sau đây được đưa vào mô hình đa biến đầu tiên chỉ dựa trên mức độ liên quan lâm sàng: tuổi, giới tính, tăng huyết áp, bệnh hô hấp mãn tính, thành phần huyết động SOFA và lúc nhập viện ICU: tỷ lệ PaO2/FiO2, creatinin huyết thanh, số lượng tế bào lympho, số lượng tiểu cầu, D -dimer, bilirubin toàn phần, và tỷ lệ thông khí. Các biến sau đây được đưa vào mô hình đa biến thứ hai dựa trên những phát hiện trước đó và các hạn chế lâm sàng: tuổi, delta tỷ lệ PaO2/FiO2, delta creatinine huyết thanh, delta số lượng tế bào lympho, delta số lượng tiểu cầu, delta bilirubin toàn phần và delta tỷ lệ thông khí. Cả hai mô hình đều bao gồm các biến số thông khí và oxygen hóa liên quan, các xét nghiệm trong phòng thí nghiệm, hỗ trợ các cơ quan và các đặc điểm nhân khẩu học. Tỷ lệ cược (OR) và khoảng tin cậy 95% của chúng đã được tính toán. Tính cộng tuyến đơn được đánh giá bằng cách sử dụng hệ số tương quan Pearson (r). SOFA bị loại trừ vì tính thẳng hàng (r> | ± 0,30 |) với creatinine, trong khi PaCO2 và pH bị bỏ qua vì tính thẳng hàng của tỷ lệ thông khí. Đa cộng tuyến được kiểm tra bằng phương sai yếu tố lạm phát (VIF). Một nguyên tắc chung là nếu VIF> 10, thì đa cộng tuyến là cao [14]. Mức độ tuyến tính của các biến liên tục được đánh giá bằng cách sử dụng kiểm định Box – Tidwell (Tệp bổ sung 1: Bảng 2). Giả định về độ tuyến tính đối với các phép đo delta đã được xác nhận trong một biểu đồ phân tán của công cụ dự đoán so với logit vì thử nghiệm Box – Tidwell không chấp nhận các giá trị âm (Tập tin bổ sung 1: Hình 2). Các biến không thỏa mãn tiêu chí này đã được nhập dưới dạng các đường khối hình khối hạn chế trong mô hình. Đường đặc tính hoạt động của máy thu được sử dụng để đánh giá khả năng phân biệt của mô hình để phân biệt bệnh nhân chết với bệnh nhân sống và được biểu thị bằng diện tích dưới đường đặc tính hoạt động của máy thu (AUC), nằm trong khoảng từ 0,5 (không có khả năng phân biệt) đến 1,0 (hoàn hảo khả năng phân biệt). Hiệu chuẩn được đánh giá bằng cách sử dụng điểm Brier, nằm trong khoảng từ 0,0 đến 1,0, trong đó mô hình có kỹ năng hoàn hảo có điểm là 0,0 và người kém nhất có điểm là 1,0. Mức ý nghĩa được đặt ở mức 0,05 (hai mặt) và tất cả các phân tích được thực hiện bằng R phiên bản 4.0.3.
Bảng 2 Các phát hiện trong phòng thí nghiệm và xử trí thông khí của bệnh nhân thở máy sớm ở ngày thứ 3 theo tỷ lệ tử vong khi nhập viện
| No All | patients
(n = 1118) |
Survivors (n = 685) | Non-survivors (n = 433) | p–value | |
| Arterial blood gases | |||||
| PaO2/FiO2 ratio, mmHg | 1054 | 180.0 [135.4–227.9] | 190.0 [148.6–
237.5] |
158.0 [114.0–208.7] < 0. | 001 |
| PaO2/FiO2 ratio categories | 1054 | ||||
| PaO2/FiO2 ratio < 100 mmHg | 98 (9.3%) | 36 (5.6%) | 63 (15.2%) < 0.001 | ||
| PaO2/FiO2 ratio ≥ 100 and < 200 mmHg | 550 (52.2%) | 317 (49.4%) | 233 (56.6%) 0.023 | ||
| PaO2/FiO2 ratio ≥ 200 and < 300 mmHg | 313 (29.7%) | 232 (36.1%) | 81(19.7%) < 0.001 | ||
| PaO2/FiO2 ratio ≥ 300 mmHg | 91 (8.6%) | 56 (8.7%) | 35 (8.5%) | 1.00 | |
| pH | 1082 | 7.39 [7.33–7.44] | 7.40 [7.35–7.45] | 7.37 [7.30–7.41] < 0.001 | |
| PaCO2, mmHg | 1090 | 47.0 [41.8–54.0] | 46.0 [40.0–51.0] | 50.3 [44.0–58.0] < 0.001 | |
| Lactate, mg/dL | 756 | 15.3 [11.7–20.1] | 15.3 [11.1–19.8] | 16.6 [12.6–20.7] 0.001 | |
| Laboratory findings | |||||
| Lymphocyte count, 109/L | 1090 | 0.64 [0.41–1.00] | 0.70 [0.48–1.00] | 0.60 [0.38–0.90] < 0.001 | |
| Neutrophil count, 109/L | 472 | 7.58 [5.60–10.50] | 7.40 [5.24–10.29] | 8.10 [6.10–10.5] 0.030 | |
| Platelet count, 109/L | 1095 | 255.0 [189.0–325.0] | 274.0 [206.5–
340.0] |
222.5 [168.8–293.0] < 0. | 001 |
| D-dimers, mg/L | 754 | 2.31 [1.05–6.52] | 1.97 [0.96–4.76] | 3.27 [1.39–8.92] < 0.001 | |
| Ferritin, ng/mL | 345 | 1326 [835–2200] | 1308 [790–2144] | 1361 [839–2244] | 0.50 |
| IL6, pg/mL | 115 | 98.0 [43.1–196.6] | 81.0 [44.4–191.0] | 125.9 [41.7–196.9] | 0.51 |
| CRP, mg/dL | 925 | 10.0 [3.4–22.6] | 9.3 [3.1–20.7] | 10.8 [3.8–23.5] | 0.09 |
| Bilirubin, mg/dL | 957 | 0.75 [0.42–1.30] | 0.75 [0.42–1.26] | 0.76 [0.42–1.35] | 0.71 |
| Serum creatinine, mg/dL | 1101 | 0.92 [0.67–1.39] | 0.81 [0.62–1.17] | 1.10 [0.78–1.88] < 0.001 | |
| Ventilatory setting and pulmonary mechanics | |||||
| Tidal volume/PBW (ml/kg) | 926 | 7.3 [6.5–8.1] | 7.3 [6.5–8.1] | 7.3 [6.5–8.1] | 0.81 |
| Respiratory rate, rpm | 1006 | 22.0 [18.0–24.0] | 21.0 [18.0–24.0] | 22.0 [20.0–25.0] 0.003 | |
| PEEP, cmH2O | 1051 | 12.0 [10.0–14.0] | 12.0 [10.0–14.0] | 12.0 [10.0–14.0] | 0.46 |
| FiO2, % | 1065 | 50.0 [40.0–60.0] | 50.0 [40.0–60.0] | 60.0 [50.0–70.0] < 0.001 | |
| Peak inspiratory pressure, cmH2O | 537 | 30.0 [27.0–35.0] | 30.0 [27.8–34.6] | 33.0 [27.0–36.0] | 0.11 |
| End-inspiratory plateau pressure, cmH2O | 413 | 24.0 [21.0–28.0] | 24.0 [21.0–27.0] | 25.0 [22.0–29.0] 0.001 | |
| Driving pressure, cmH2Oa | 401 | 12.0 [10.0–15.0] | 12.0 [9.5–14.0] | 12.2 [10.0–16.0]0.022 | |
| Compliance, mL/cmH2Ob | 399 | 37.5 [28.8–48.0] | 38.4 [30.0–48.3] | 34.6 [25.1–46.6] 0.032 | |
| Ventilatory ratioc | 905 | 1.96 [1.61–2.40] | 1.86 [1.53–2.24] | 2.11 [1.77–2.68] < 0.001 | |
| Position | 967 | ||||
| Supine | 658 (68.0%) | 451 (74.0%) | 219 (58.6%) < 0.001 | ||
| Prone | 285 (29.5%) | 138 (23.3%) | 145 (38.8%) < 0.001 | ||
| Other | 24(2.5%) | 16 (2.7%) | 9 (2.4%) | 0.84 |
Bảng 3 Mô hình đa biến đánh giá các yếu tố dự báo tử vong khi nhập viện (N = 619 bệnh nhân)
| Variable | Odds ratio (95% CI) p value | |
| Age, years | 1.01 (1.01 to 1.02) < 0.001 | |
| Sex, male | 1.04 (0.96 to 1.12) | 0.34 |
| Hypertension | 1.01 (0.94 to 1.09) | 0.83 |
| Chronic respiratory disease | 1.16 (1.03 to 1.29) 0.013 | |
| SOFA hemodynamic component | 1.01 (0.99 to 1.03) | 0.53 |
| PaO2/FiO2 ratio at ICU admission, mmHg | 1.00 (0.99 to 1.00) | 0.14 |
| Serum creatinine at ICU admission, mg/dL | 1.09 (1.03 to 1.15) 0.003 | |
| Lymphocyte count at ICU admission, × 109/L | 1.00 (0.98 to 1.03) | 0.89 |
| Platelet count at ICU admission, × 109/L | 1.00 (1.00 to 1.00) | 0.12 |
| Total bilirubin at ICU admission, mg/dL | 0.97 (0.91 to 1.03) | 0.27 |
| D-dimers at ICU admission, μg/L | 1.00 (1.00 to 1.00) | 0.29 |
| Ventilatory ratio at ICU admission | 1.07 (1.01 to 1.14) 0.016 |
Bảng 4 Mô hình đa biến đánh giá các yếu tố dự báo tử vong khi nhập viện (N = 660)
| Variable | Odds ratio (95% CI) | p value |
| Age | 1.01 (1.01 to 1.02) | < 0.001 |
| Delta PaO2/FiO2 ratio, mmHg | 1.00 (1.00 to 1.00) | 0.47 |
| Delta serum creatinine, mg/dL | 1.06 (1.02 to 1.11) | 0.005 |
| Delta lymphocyte count, × 109/L | 1.01 (0.98 to 1.04) | 0.40 |
| Delta platelet count, × 109/L | 0.99 (0.98 to 1.00) | 0.037 |
| Delta total bilirubin, mg/dL | 0.99 (0.97 to 1.02) | 0.79 |
| Delta ventilatory ratio | 1.05 (1.01 to 1.10) | 0.030 |
Kết quả
Nhân khẩu học và đặc điểm lâm sàng khi đưa vào ICU
Từ ngày 25 tháng 2 đến ngày 31 tháng 7 năm 2020, 2.095 bệnh nhân mắc COVID-19 đã (1,8%) có thể được rút nội khí quản trong ba ngày đầu tiên này. Mười bệnh nhân (0,8%) yêu cầu hỗ trợ ECMO trong ba ngày đầu tiên đã bị loại trừ.
Đặc điểm của dân số nghiên cứu bệnh nhân cần đặt nội khí quản vào ngày đầu tiên và vẫn cần MV vào ngày thứ ba được trình bày chi tiết trong Bảng 1. Tóm lại, tuổi trung bình là 65,0 [57,0–72,0] tuổi, chiếm đa số (54,7%) từ 50 đến 69 tuổi. Bảy mươi mốt phần trăm (n = 786) là nam giới, bệnh đi kèm thường xuyên nhất là tăng huyết áp, tỷ lệ này có ở555 (49,7%), và chỉ 61 (8,2%) là người hút thuốc chủ động. Vào ngày đầu tiên của MV, bệnh nhân cho thấy độ giãn nở của hệ thống hô hấp là 37,1 [29,3–50,0] mL/cmH2O, với áp lực đẩy là 12,0 [9,6–15,0] cmH2O, thể tích khí lưu thông là 7,1 [6,4–8,0] mL/Kg và tỷ lệ thông khí là 1,7 [1,4–2,3]. Tỷ lệ PaO2/FiO2 là 115,6 [80,0–171,2] mmHg, và tỷ số này dưới 200 mmHg ở 886 (83,0%) bệnh nhân
và dưới 100 mmHg ở 424 (39,7%); 346 (36,0%) bệnh nhân cần nằm sấp trong ngày MV đầu tiên. Tần số thở đo được là 20,0 [18,0–24,0] bpm, với PaCO2 là 43,9 [36,0–52,0] mmHg và pH là 7,36 [7,29–7,43]. Mức độ lactate là 13,0 [9,9–17,1] mg/dL với 704 (67,6%) bệnh nhân cần thuốc vận mạch tại thời điểm này. Điểm SOFA là 7,0 [5,0– 8,0], mức trung bình của creatinin là 0,87 [0,67– 1,15] mg/dL và số lượng tiểu cầu là 226,0 [173,0–299,0] × 109/L. Về dấu ấn sinh học COVID-19 trong phòng thí nghiệm, số lượng tế bào lympho trung bình thấp (0,63 [0,43–0,90] × 109/L) và nồng độ D-dimer, ferritin và IL-6 trong huyết tương tăng đáng kể với giá trị trung bình là 1,12 [ 0,59–3,52] mg/L, 1389,0 [821,0–2250,0] ng/mL và 114,0 [47,5–181,4] pg/mL, tương ứng. được nhận vào 44 ICU (Tệp bổ sung 1: Bảng 3), 1.645 (78,5%) MV yêu cầu (Tệp bổ sung 1: Bảng 4) và 1.188 (72,2%) cần đặt nội khí quản vào ngày đầu tiên nhập viện ICU (Hình 1). Phần lớn nhóm thuần tập cuối cùng này vẫn nhận được hỗ trợ MV vào ngày thứ ba khi nhập viện ICU [1.118 (94,1%)], trong khi 38 (3,1%) tử vong và 22
Diễn biến lâm sàng ở ngày thứ 3 khi nhập viện ICU
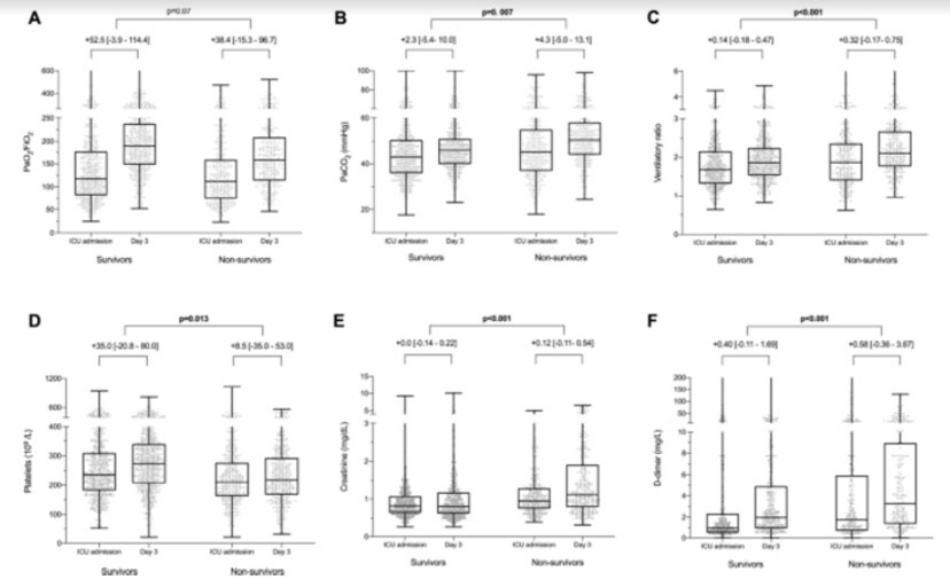
Những phát hiện chính ở ngày MV thứ ba được hiển thị trong Bảng 2. Sự khác biệt delta giữa ngày thứ 3 và nhập viện ICU cho thấy sự gia tăng chung về tỷ lệ PaO2/FiO2 (+ 46,7 [–9,3 đến 108,3]), nhưng mức tăng này không cao hơn đáng kể ở những bệnh nhân sống sót đến khi xuất viện (p = 0,07). Ngược lại, chúng tôi nhận thấy sự khác biệt về sự thay đổi mức độ PaCO2 (+ 2,3 [–5,4 đến + 10,0] so với + 4,3 [–5,0 đến + 13,1] mmHg, p = 0,007) và độlớn của tỷ lệ thông khí ( + 0,14 [–0,18 đến + 0,47] so với + 0,32 [–0,17 đến + 0,75], p <0,001) giữa những người sống sót và không sống sót. Về vấn đề này, delta của D-dimer là dấu ấn sinh học COVID-19 duy nhất có sự khác biệt đáng kể giữa những người sống sót và không sống sót (+ 0,40 [–0,11 đến + 1,69] so với + 0,58 [–0,36 đến + 3,67] mg/L , p = 0,001). Về các dấu hiệu sinh học ngoài phổi khác của rối loạn chức năng cơ quan, mức độ creatinin delta cao hơn ở những người không sống sót (+ 0,0 [–0,14 đến + 0,22] so với + 0,12 [–0,11 đến +0,54] mg/dL, p <0,001), và sự gia tăng số lượng tiểu cầu cao hơn ở những người sống sót (+ 35,0 [–20,8 đến + 80,0] so với + 8,5 [–35,0 đến + 53,0]× 109/L, p = 0,013). Ngoài ra, chúng tôi nhận thấy sự biến đổi của bilirubin cao hơn đáng kể ở những người không sống sót (+ 0,04 [–0,16 đến + 0,4] so với + 0,05 [–0,16 đến + 0,56] mg/dL, p = 0,023). Tất cả các biến thể này được trình bày chi tiết trong Hình 2 và tệp bổ sung 1: Bảng 5. Không có mối tương quan giữa tỷ lệ thông khí và các dấu ấn sinh học tiên lượng, cơ học phổi hoặc dữ liệu trao đổi khí ngoại trừ các mối tương quan yếu nhưng có ý nghĩa được tìm thấy giữa tỷ số thông khí và PEEP (r = 0,11, p <0,001), PaO2/FiO2 (r = – 0,19, p <0,001) và áp lực đẩy (r= 0,15, p = 0,004) ở ngày thứ 3 (Hình bổ sung 1:Hình 3 và Bảng 6).
Điều trị và các biến chứng trong quá trình nhập viện ICU
Trong số 1.118 bệnh nhân, 986 (88,8%) bệnh nhân được dùng Hydroxychloroquine và 892 (80,4%) Lopinavir/Ritonavir trong quá trình nhập viện ICU của họ. Dexamethasone và methylprednisolone được sử dụng lần lượt ở 233 (21,4%) và 572 (52,4%) bệnh nhân, trong khi 499 (45,0%) được điều trị bằng Tocilizumab. Điều trị chống đông máu bằng heparin được sử dụng ở 1065 (96,0%) bệnh nhân. Những người sống sót sau khi xuất viện được điều trị này thường xuyên hơn [662 (97,1% người sống sót) so với 403 (94,4% người không sống sót); p = 0,04]. Rối loạn đông máu gặp ở290 (26,0%) dân số, và biến chứng xuất huyết được xác định ở 103 (9,2%) bệnh nhân. Thuốc vận mạch là cần thiết tại bất kỳ thời điểm nào khi nhập viện ICU ở 1028 bệnh nhân (92,6%). Suy thận cấp được xác định ở 493 (44,1%) bệnh nhân, và 157 (14,1%) bệnh nhân cần điều trị thay thế thận. Thuốc chẹn thần kinh cơ đã được sửdụng tại một số thời điểm ở 950 (85,9%) bệnh nhân, và 482 (43,2%) bệnh nhân cần mở khí quản. Các thủ thuật huy động phế nang được sử dụng ở 653 (61,8%) bệnh nhân, nằm sấp ở 874 (79,0%), và 20 (1,8%) trường hợp cần hỗ trợ hô hấp ngoài cơ thể. Theo định nghĩa của Berlin, 76 (6,8%) có ARDS nhẹ, 467 (41,8%) có ARDS trung bình và 575 (51,4%) bị ARDS nặng.
Mặc dù phần lớn nhóm thuần tập được điều trị kháng sinh (1102 bệnh nhân, 99,2%), viêm phổi do vi khuẩn được chẩn đoán ở 368 (33,1%) bệnh nhân thở máy và nhiễm khuẩn huyết ở 446 (40,0%). Ba mươi ba phần trăm bệnh nhân bị rối loạn chức năng gan. Tràn khí màng phổi [53 (7,7%) so với 55 (12,7%), p =0,007)] và xuất huyết [49 (7,2%) so với 54 (12,7%), p = 0,004)] thường xuyên hơn ở những bệnh nhân không sống sót. Tệp bổ sung 1: Bảng 7 liệt kê các liệu pháp COVID-19 và các phương pháp điều trị khác, và Tệp bổ sung 1: Bảng 8 trình bày các biến chứng chính trong dân số 1.118 bệnh nhân này.
Kết quả và các yếu tố dự báo tử vong khi nhập viện
Tỷ lệ tử vong khi nhập viện của tất cả bệnh nhân COVID-19 nhập viện ICU trong thời gian nghiên cứu là 32,6% và tỷ lệ bệnh nhân cần đặt nội khí quản trong 24 giờ đầu tiên là 40,2%.
Đặc biệt, trong nhóm thuần tập bệnh nhân vẫn cần MV ở ngày thứ 3, chúng tôi nhận thấy tỷ lệ tử vong nhập viện chung là 38,7%. Cụthể ở nhóm dân số này, tỷ lệ tử vong do ICU là 37,5%, trong khi tỷ lệ tử vong trong 28 ngày là 31,9%. Nguyên nhân tử vong chính là suy đa cơ quan (n= 179; 41,7%) và suy hô hấp (n = 178; 41,5%). Thời gian MV, ICU và thời gian nằm viện lần lượt là 16,0 [9,0–27,0], 20,0 [11,0–32,0] và 30,0[19,0–48,0] ngày (Tệp bổ sung 1: Bảng 9).
Sau khi điều chỉnh đa biến bao gồm các biến ở ngày đầu tiên nhập viện ICU, tuổi lớn hơn, sựhiện diện của bệnh hô hấp mãn tính, nồng độ creatinin cao hơn và tỷ lệ thông khí cao hơn có liên quan đáng kể đến việc tăng nguy cơ tử vong khi nhập viện (Bảng 3). Kết quả tương đương thu được khi bệnh nhân tử vong hoặc rút ống nội khí quản trong ba ngày đầu tiên này được đưa vào phân tích (Tệp bổ sung 1: Bảng 10).
Tương tự như vậy, khi chúng tôi đưa vào mô hình sự thay đổi của các biến giữa ngày 1 và ngày 3 khi nhập viện ICU, chúng tôi nhận thấy rằng sự gia tăng cao hơn trong tỷ lệ thông khí (OR 1,04 [CI 1,01–1,07]) và mức creatinine (OR 1,05 [CI 1,01–1,09]) và số lượng tiểu cầu tăng thấp hơn (OR 0,96 [CI 0,93–1,00]) có liên quan đáng kể với nguy cơ tử vong cao hơn. (Bảng 4). Điều thú vị là chúng tôi nhận thấy rằng cả tỷ lệ PaO2/FiO2 ban đầu (0,97 [CI 0,94 đến 1,01]) cũng như sự biến đổi của nó (OR 0,99 [CI 0,95 đến 1,02]) đều không liên quan đến tử vong khi nhập viện.
Thảo luận
Nghiên cứu hiện tại tập trung vào một quần thể bệnh nhân COVID-19 rất đồng nhất cần đặt nội khí quản và thở máy ở ngày đầu tiên nhập viện ICU và tiếp tục được thở máy vào ngày thứ 3. Tỷ lệ tử vong tại bệnh viện của những bệnh nhân này trong đợt đầu tiên của đại dịch là 38,7%. Chúng tôi đã điều tra các yếu tố liên quan đến tỷ lệ tử vong ở ngày thứ nhất và quan trọng hơn, bất kỳ thayđổi nào giữa ngày thứ nhất và ngày thứ 3. Mô hình ngày thứ nhất cho thấy tuổi tác, bệnh hô hấp mãn tính, tăng creatinine huyết thanh và tăng tỷ lệ thông khí là những yếu tố độc lập liên quan đến tỷ lệ tử vong tại bệnh viện trong khi mô hình ngày 1 so với ngày 3 xác định được tuổi, tăng creatinin huyết thanh cao hơn từ ngày 1 đến ngày 3, số lượng tiểu cầu tăng thấp hơn từ ngày 1 đến ngày 3 và tỷ lệ thông khí tăng cao hơn từ ngày 1 đến ngày thứ 3 là yếu tố dự báo tỷ lệ tử vong.
Tỷ lệ phần trăm tử vong được báo cáo của bệnh nhân COVID nhập viện ICU rất không đồng nhất, dao động từ 30 đến 60%, và chủ yếu là do quần thể được thởmáy không xâm lấn và xâm lấn hỗn hợp, các giai đoạn hỗn hợp của đại dịch và các điểm cuối khác nhau. Nghiên cứu đa trung tâm của chúng tôi cho thấy tỷ lệ tử vong khi nhập viện của một nhóm dân số được xác định rõ là cần MV và vẫn được thở máy 3 ngày sau khi bắt đầu thở máy (38,7%).
Vào ngày đầu tiên, chúng tôi đã tìm thấy một số biến nhân khẩu học liên quan đến tỷ lệ tử vong cao hơn như tuổi tác và các bệnh hô hấp mãn tính. Những yếu tốnày không thể được sửa đổi và chỉ đơn giản là phản ánh một nhóm dân số dễ bị tổn thương hơn trong đó COVID-19 có sự diễn tiến tồi tệ hơn. Các nghiên cứu khác xác nhận rằng tuổi và các bệnh hô hấp mãn tính là những yếu tố tiên lượng xấu cả ở bệnh nhân thở máy, thở máy hỗn hợp và không thở máy [15, 16]. Trong số các xét nghiệm trong phòng thí nghiệm, chỉ có creatinine huyết thanh cao hơn lúc nhập viện ICU có liên quan đến tử vong khi nhập viện. Đáng chú ý, oxygen hóa ở ngày đầu tiên của MV không phải là một yếu tố liên quan đến tỷ lệ tử vong cao hơn. Nghiên cứu có thể so sánh tốt nhất với nghiên cứu của chúng tôi là của Botta và cộng sự, người đã nghiên cứu 533 bệnh nhân COVID Hà Lan được thở máy [17]. Giống như chúng tôi, họ phát hiện ra rằng tuổi tác có liên quan đến tỷ lệ tử vong trong 28 ngày, trong khi PaO2/FiO2 thì không. Trong nghiên cứu của chúng tôi, tỷ lệ thông khí ở ngày đầu tiên có liên quan đến tỷ lệ tử vong khi nhập viện. Botta và cộng sự. [17] đã không đo điểm đánh dấu thay thế này của khoảng chết. Tuy nhiên, họ chỉ ra rằng thể tích khí lưu thông cao hơn và mức độ độ giãn nở thấp hơn có liên quan đến việc tăng tỷ lệ tử vong trong 28 ngày.
Trong bối cảnh này, việc xác định các yếu tố tiên lượng là rất quan trọng để phát hiện những yếu tố có thể chấp nhận được để can thiệp y tế. Trong nhiều bệnh hô hấp cấp tính cần MV, diễn biến ngày thứ 3 là rất quan trọng. Trong cả viêm phổi nặng mắc phải tại cộng đồng [18] và viêm phổi do thở máy [5], sự khác biệt giữa ngày 1 và ngày 3 về các thông số sinh lý chính là những yếu tố tiên lượng đáng tin cậy về diễn biến và tiên lượng. Do đó, chúng tôi đã thực hiện mô hình đa biến thứ hai so sánh ngày 1 và ngày 3 của MV. Nhìn chung, chúng tôi nhận thấy rằng sự chênh lệch (chênh lệch ngày 3 so với ngày 1) về số lượng tiểu cầu (tăng thấp hơn), nồng độ creatinin (tăng cao hơn) và tỷ lệ thông khí (tăng cao hơn) có liên quan đáng kể đến tỷ lệ tử vong khi nhập viện. Những thay đổi trong quá trình oxygen hóa không liên quan đến tỷ lệ tử vong thấp hơn.
Tỷ lệ thông khí là một chỉ số được xác nhận gần đây rất hấp dẫn vì nó đơn giản để tính toán bằng cách sử dụng thông khí phút và PaCO2. Nó so sánh hai tham số này với các giá trị lý tưởng và giá trị dự đoán tương ứng như một giá trị đứng cho Vd/Vt. Chỉ số này đã được xác nhận trong các chế độ được kiểm soát của MV. Tỷ lệ thông khí phụ thuộc vào sản xuất CO2, và bất kỳ sự gia tăng sản xuất CO2 nào cũng có thể làm thay đổi giá trị của nó. Giá trị xấp xỉ 1 sẽ đại diện cho phổi thông khí bình thường [21]. Ở những bệnh nhân ARDS không dùng COVID, tỷ lệ thông khí cao có liên quan đến tử vong [22, 23].
Trước đây chúng tôi đã báo cáo rằng tỷ lệ thông khí tăng ở bệnh nhân COVID ARDS [24]. Trong một loạt 267 bệnh nhân COVID-ARDS, Schenck et al. [25] cũng tìm thấy giá trị cao hơn ở những bệnh nhân vẫn đặt nội khí quản ở ngày thứ 3 và 7. Họ cũng nhận thấy giá trị cao hơn đáng kể ở 47 bệnh nhân đã chết (tỷ lệ thông khí trung bình là 2,26 [1,53–2,50]). Trong một mẫu chỉ có 8 bệnh nhân, Liu et al. [26] nhận thấy tỷ lệ thông khí thấp hơn ở những bệnh nhân được điều trị bằng thể tích khí lưu thông thấp hơn. Không có nghiên cứu nào trong số ba nghiên cứu này thực hiện các phân tích đa biến về tỷ lệ tử vong. Cuối cùng, dữ liệu Provent COVID [27] bao gồm 927 bệnh nhân được thở máy liên tiếp cho thấy việc đánh giá mức độ suy giảm khả năng thông khí bằng cách sử dụng ước tính khoảng chết (tỷ lệ khoảng chết, tỷ lệ thông khí và tỷ lệ PCO2 cuối triều trên động mạch), không phải ở cơ sở cũng như trong những ngày tiếp theo, không liên quan đáng kể đến tỷ lệ tử vong trong 28 ngày. Việc loại trừ hay không loại trừ bệnh nhân dùng ECMO không được báo cáo cụ thể [27]. Ngoài ra, sự khác biệt quan trọng khác giữa nghiên cứu này và của chúng tôi là mức độ nghiêm trọng của ARDS cao hơn trong nghiên cứu của chúng tôi (51% so với 10%) và chúng tôi đã bao gồm sự khác biệt đồng bằng giữa ngày 3 và ngày 1 mà dường như không phải là trường hợp Nghiên cứu của Morales Quintero [27].
Mô hình hồi quy đa biến của chúng tôi cho thấy sự gia tăng tỷ lệ thông khí khi nhập viện ICU có liên quan đến tỷ lệ tử vong khi nhập viện, với mỗi đơn vị làm tăng 7% nguy cơ tử vong ([1–14], p = 0,015). Tỷ lệ thông khí delta ở ngày thứ 3 cũng có liên quan đến tử vong, với mỗi đơn vị- tăng nguy cơ tử vong là 5% ([1–10], p = 0,030). So với các nghiên cứu trước đây ở bệnh nhân ARDS không dùng COVID, Sinha et al. nhận thấy rằng tỷ lệ thông khí có liên quan độc lập với tử vong khi nhập viện sau khi điều chỉnh tỷ lệ PaO2/FiO2 và áp lực đẩy (OR 1,51 [CI 1,09–2,12), p = 0,015) [22]. Có thể lập luận rằng những phát hiện của chúng tôi về tỷ lệ thông khí có thể được mong đợi sau kết quả Sinha của et al. trên ARDS không COVID [22]. Tuy nhiên, chúng tôi nghĩ rằng chúng là cần thiết sau tất cả những tranh cãi về kiểu hình ARDS COVID. Một sự khác biệt quan trọng khác so với Sinha et al. [22] là chúng tôi đã chứng minh không chỉ giá trị tiên lượng của tỷ lệ thông khí ở ngày thứ nhất mà còn giá trị tiên lượng ở ngày thứ 3, điều này mang lại nhiều tính nhất quán cho dữ liệu của chúng tôi.
Việc giải thích tỷ lệ thông khí rất phức tạp, nhưng nó có thể được coi là một dấu hiệu đại diện cho khoảng chết sinh lý [22]. Tăng khoảng chết trong COVID 19 có thể là do sự kết hợp của các phế nang giảm tưới máu do vi huyết khối của phế nang mao mạch cộng với phù mô kẽ làm suy giảm tuần hoàn phổi [28]. Liên quan đến cơ chế đầu tiên (microthrombosis), cả chúng tôi và Barbeta et al. [24] tìm thấy mối tương quan giữa nồng độ D-dimer trong máu và tỷ lệ thông khí. Ngoài ra, chúng tôi không tìm thấy mối tương quan đáng kể của VR với tiểu cầu hoặc độ giãn nở. Chúng tôi tìm thấy mối tương quan yếu với PaO2/FiO2. Sinha và cộng sự. cũng tìm thấy mối tương quan nghịch giữa PaO2/FiO2 và tỷ số thông khí, cho thấy rằng sự không phù hợp thông khí- tưới máu dẫn đến tăng CO2 máu và giảm oxy máu [22]. Tuy nhiên, trong nghiên cứu của chúng tôi tỷ lệ thông khí vượt quá PaO2/FiO2 trong dự đoán tử vong tại bệnh viện. Trên thực tế, đối với mối liên hệ của nó với mức độ mô phổi kém thông khí [29], khoảng chết sinh lý được đề xuất như một yếu tố dự báo mạnh hơn sự oxy hóa các kết quả ARDS không COVID [30]. Không giống như ARDS điển hình, tình trạng giảm oxy máu nghiêm trọng được quan sát thấy trong COVID- 19 có thể được tìm thấy ở những bệnh nhân có thể tích phổi và hô hấp tương đối được bảo tồn [1], do đó có thể không phản ánh gánh nặng của bệnh nhu mô [31, 32].
Hơn nữa, những bệnh nhân có khoảng chết cao hơn thường cần thông khí phút cao hơn để tránh tăng CO2 máu, dẫn đến tăng tổn thương phổi do năng lượng cơ học động cao hơn [33]. Thật vậy, không thể phủ nhận vai trò tiềm tàng của căng phồng phổi và tổn thương phổi do máy thở vì mối tương quan yếu giữa áp lực đẩy và tỷ số thông khí ở ngày thứ 3 có thể cho thấy. Có thể tỷ số thông khí ngày càng tăng là hậu quả của sự tiến triển của bệnh, nhưng mặt khác nó cũng có thể là một thông số mà chúng ta có thể đo lường để theo dõi diễn biến của bệnh nhân khi áp dụng các phương pháp điều trị và chiến lược thông khí cụ thể.
Có một số hạn chế của nghiên cứu này. Đầu tiên, các phép đo của chúng tôi vào ngày 1 và ngày 3 chỉ là ảnh chụp nhanh về bản chất động lực học của suy hô hấp COVID 19 (chúng tôi đã chọn giá trị xấu nhất). Thứ hai, chúng tôi đã không đo capnography thể tích, và do đó, chúng tôi không thể đánh giá tác động của tốc độ trao đổi chất đối với sự trao đổi khí. Tốc độ trao đổi chất có thể thay đổi khi sốt và phong tỏa thần kinh cơ. Thứ ba, và do tính chất quan sát của nghiên cứu, các quy trình thông khí không được tiêu chuẩn hóa, nhưng phần lớn các trung tâm đã sử dụng các chiến lược thông khí bảo vệ. Thứ tư, nó đã được chứng minh rằng tỷ lệ thông khí được tăng lên khi sử dụng bộ lọc HME so với việc sử dụng máy tạo ẩm có hệ thống sưởi. Bộ lọc HME đã được sử dụng cho hầu hết các bệnh nhân của chúng tôi. Cuối cùng, việc thiếu nhóm kiểm soát bệnh nhân ARDS không COVID-19 là một hạn chế tiềm năng khác. Tuy nhiên, để thu thập dữ liệu chắc chắn hiện tại về quần thể này là hoàn toàn không thể do số lượng bệnh nhân không COVID được nhận vào trong thời gian nghiên cứu ở các ICU khác nhau rất thấp, điều này có thể khiến cho bệnh nhân ARDS không thể khớp với COVID-19.
Điểm mạnh của nghiên cứu này là tính chất đa trung tâm, bao gồm một số lượng lớn bệnh nhân có đặc điểm rất đồng nhất và hiệu suất của phân tích đa biến vào ngày 1 của MV và vào ngày 3, cho phép chúng tôi xem xét mức độ của những thay đổi đã xảy ra đặt giữa ngày 1 và ngày 3.
Kết luận
Kết luận, trong một quần thể bệnh nhân COVID 19 ARDS được đặt nội khí quản ở ngày đầu tiên nhập viện ICU vẫn còn thở máy sau 3 ngày, chúng tôi nhận thấy các yếu tố liên quan độc lập với tử vong trong bệnh viện cả ở ngày thứ nhất và quan trọng nhất là những thay đổi xảy ra giữa ngày thứ nhất và ngày thứ 3 là yếu tố dự đoán kết quả. Mức độ cao hơn của creatinine và tỷ lệ thông khí ở ngày thứ nhất và sự gia tăng tỷ lệ thông khí và nồng độ creatinin cao hơn và mức tăng tiểu cầu thấp hơn ở ngày thứ 3 có liên quan độc lập với tửvong trong bệnh viện. Chúng tôi nhận thấy rằng tuổi tác và các bệnh hô hấp mãn tính cũng có liên quan độc lập với tỷ lệ tử vong khi nhập viện. Tỷ lệ PaO2/FiO2 lúc nhập viện ICU và tình trạng xấu đi hoặc cải thiện ở ngày thứ 3 không liên quan đến tiên lượng. Cần có các nghiên cứu tiền cứu và can thiệp sâu hơn để xác định các phương pháp điều trị và chiến lược có thể làm giảm tỷ lệ thông khí.