Tóm tắt
ĐẶT VẤN ĐỀ
Nhiễm trùng và tăng viêm toàn thân gây rối loạn chức năng cơ quan và tử vong ở bệnh nhân xơ gan mất bù. Các nghiên cứu tiền lâm sàng cung cấp hỗ trợ cho vai trò chống viêm của albumin, nhưng các thử nghiệm lâm sàng quy mô lớn đã được khẳng định còn thiếu. Cho dù nhắm mục tiêu mức albumin huyết thanh là 30 g mỗi lít hoặc cao hơn ở những bệnh nhân này với việc truyền lặp lại hàng ngày dung dịch albumin người 20%, so với chăm sóc tiêu chuẩn, có làm giảm tỷ lệ nhiễm trùng, rối loạn chức năng thận và tử vong hay không vẫn chưa được biết.
PHƯƠNG PHÁP
Chúng tôi đã tiến hành một thử nghiệm ngẫu nhiên, đa trung tâm, nhãn mở, nhóm song song liên quan đến những bệnh nhân nhập viện mắc bệnh xơ gan mất bù có mức albumin huyết thanh dưới 30 g mỗi lít khi nhập viện. Bệnh nhân được chỉ định ngẫu nhiên để nhận dung dịch albumin người 20% nhắm mục tiêu trong tối đa 14 ngày hoặc cho đến khi xuất viện, tùy điều kiện nào đến trước hoặc chăm sóc tiêu chuẩn. Điều trị bắt đầu trong vòng 3 ngày sau khi nhập viện. Điểm kết thúc chính tổng hợp là nhiễm trùng mới, rối loạn chức năng thận, hoặc tử vong trong khoảng thời gian từ ngày 3 đến ngày 15 sau khi bắt đầu điều trị.
KẾT QUẢ
Có tổng cộng 777 bệnh nhân được phân nhóm ngẫu nhiên, và rượu được báo cáo là nguyên nhân gây xơ gan ở hầu hết những bệnh nhân này. Tổng lượng albumin truyền trung bình là 200 g (khoảng giữa các phân vị, 140 đến 280) cho mỗi bệnh nhân được sử dụng cho nhóm albumin mục tiêu (tăng mức albumin lên ≥30 g mỗi lít), so với mức trung bình là 20 g (phạm vi giữa các phân vị , 0 đến 120) cho mỗi bệnh nhân được quản lý trong nhóm chăm sóc tiêu chuẩn (sự khác biệt trung bình đã điều chỉnh, 143 g; khoảng tin cậy 95% [CI], 127 đến 158,2). Tỷ lệ bệnh nhân có biến cố kết thúc chính không có sự khác biệt đáng kể giữa nhóm albumin mục tiêu (113 trong số 380 bệnh nhân [29,7%]) và nhóm chăm sóc tiêu chuẩn (120 trên 397 bệnh nhân [30,2%]) (tỷ lệ chênh lệch đã điều chỉnh , 0,98; KTC 95%, 0,71-1,33; P = 0,87).Một phân tích theo thời gian – sự kiện, trong đó dữ liệu được kiểm duyệt tại thời điểm xuất viện hoặc vào ngày thứ 15 cũng không cho thấy sự khác biệt đáng kể giữa các nhóm (tỷ lệ nguy cơ, 1,04; KTC 95%, 0,81-1,35). Các tác dụng ngoại ý nghiêm trọng đe dọa tính mạng hoặc nghiêm trọng hơn xảy ra ở nhóm dùng albumin so với nhóm chăm sóc tiêu chuẩn.
KẾT LUẬN
Ở những bệnh nhân nhập viện vì xơ gan mất bù, truyền albumin để tăng mức albumin lên mục tiêu 30 g mỗi lít hoặc hơn không có lợi hơn so với chăm sóc tiêu chuẩn hiện tại ở Vương quốc Anh.
Bệnh gan gây ra 2 triệu ca tử vong mỗi năm trên toàn thế giới và là nguyên nhân tử vong hàng đầu ở người lớn từ 35 đến 49 tuổi ở Anh, nơi chiếm hơn 10% số ca tử vong ở nhóm tuổi này. Bệnh nhân xơ gan mất bù rất dễ bị nhiễm trùng dẫn đến suy thận và tử vong, và nguy cơ tử vong do nhiễm trùng đang gia tăng ở những bệnh nhân nội trú bị xơ gan ở Hoa Kỳ. Hơn nữa, tình trạng viêm toàn thân tăng lên ở bệnh nhân xơ gan góp phần gây suy thận và tử vong.
Truyền albumin lần đầu tiên được sử dụng ở những bệnh nhân xơ gan hơn 70 năm trước, và chúng vẫn được kê đơn phổ biến để phục hồi normovolemia ở những bệnh nhân bị giãn mạch ngoại vi. Hướng dẫn quốc tế khuyến cáo sử dụng dung dịch albumin người sau khi chọc dò khối lượng lớn ở bệnh nhân viêm phúc mạc do vi khuẩn tự phát và hội chứng gan thận. Dịch truyền đã được nghiên cứu đối với bệnh não gan, nhiễm trùng viêm phúc mạc không qua da do vi khuẩn, hạ natri máu và cổ trướng.
Các nghiên cứu tiền lâm sàng cho thấy tác dụng chống viêm của albumin ở bệnh nhân xơ gan; Phát hiện này cho thấy truyền albumin có thể hạn chế tình trạng viêm toàn thân, ngăn ngừa nhiễm trùng, giảm nguy cơ rối loạn chức năng thận và tăng khả năng sống sót. Nồng độ albumin huyết thanh thấp có liên quan đến tăng nguy cơ tử vong ở những bệnh nhân bị xơ gan và nhiễm trùng nhập viện, truyền albumin và truyền albumin làm tăng nồng độ huyết thanh lên hơn 30 g mỗi lít đã làm giảm tình trạng viêm toàn thân ở những bệnh nhân xơ gan mất bù và đã giảm tỷ lệ nhiễm trùng bệnh viện ở những bệnh nhân xơ gan nhập viện do nhiễm trùng phúc mạc do vi khuẩn không qua da.
Tuy nhiên, các thử nghiệm lâm sàng về albumin đã cho thấy những kết quả trái ngược nhau. Một thử nghiệm với albumin ở những bệnh nhân bị viêm phúc mạc do vi khuẩn tự phát cho thấy lợi ích, nhưng thử nghiệm trên những bệnh nhân bị nhiễm trùng khác thì không, và thử nghiệm sau đó đã bị chấm dứt vì phù phổi gây chết người liên quan đến albumin. Không có chất lỏng nào được sử dụng như dịch vụ chăm sóc tiêu chuẩn trong những thử nghiệm này. Một phân tích tổng hợp gần đây không cho thấy bất kỳ can thiệp nào ở bệnh nhân hội chứng gan thận làm giảm tỷ lệ tử vong do bất kỳ nguyên nhân nào, và một phân tích tổng hợp khác gần đây không cho thấy sự khác biệt giữa albumin và các thuốc giãn nở huyết tương khác về tỷ lệ tử vong. sau khi nội soi khối lượng lớn.
Trong một thử nghiệm ngẫu nhiên bao gồm bệnh nhân ngoại trú bị cổ trướng, truyền albumin hàng tuần làm giảm tỷ lệ nhiễm trùng và rối loạn chức năng thận và có liên quan đến xác suất tử vong thấp hơn so với chăm sóc tiêu chuẩn. Ngược lại, không có tác dụng trong một thử nghiệm nhỏ hơn, trong đó albumin được sử dụng ít thường xuyên hơn so với hàng tuần. Các thử nghiệm lớn để đề cập đến tính hữu ích của albumin trong việc ngăn ngừa nhiễm trùng, rối loạn chức năng thận và tử vong ở bệnh nhân nhập viện còn thiếu. Chúng tôi đã tiến hành thử nghiệm ATTIRE (Albumin để ngăn ngừa nhiễm trùng trong suy gan mãn tính) để đánh giá xem có nên nhắm mục tiêu tăng mức albumin huyết thanh lên 30 g mỗi lít hoặc hơn hay không khi sử dụng lặp lại truyền hàng ngày dung dịch albumin 20% cho người, so với chăm sóc tiêu chuẩn, sẽ làm giảm tỷ lệ nhiễm trùng, rối loạn chức năng thận và tử vong ở bệnh nhân xơ gan mất bù nhập viện.
Phương pháp
THIẾT KẾ THỬ NGHIỆM
Thử nghiệm ATTIRE là một thử nghiệm tiền cứu, can thiệp, đa trung tâm, ngẫu nhiên, nhãn mở, liên quan đến những bệnh nhân nhập viện bị xơ gan mất bù, biến chứng cấp tính và mức albumin dưới 30 g mỗi lít. Nhóm quản lý thử nghiệm của chúng tôi đã thiết kế thử nghiệm, thử nghiệm đã được Ủy ban Đạo đức Nghiên cứu London – Brent và Cơ quan Quản lý Thuốc và Sản phẩm Chăm sóc sức khỏe chấp thuận.
Sự đồng ý bằng văn bản đã được thông báo từ các bệnh nhân. Đối với những bệnh nhân mất khả năng vận động, một đại diện hợp pháp đã cung cấp sự đồng ý bằng văn bản được thông báo cho đến khi bệnh nhân phục hồi khả năng. Thử nghiệm được tiến hành và báo cáo theo quy trình. Một ủy ban giám sát an toàn và dữ liệu độc lập, có các thành viên biết về nhiệm vụ của nhóm thử nghiệm, giám sát việc tiến hành thử nghiệm.
Các nhà thống kê đã phân tích dữ liệu là các tác giả thử nghiệm. Tác giả cuối cùng đã viết bản thảo đầu tiên của bản thảo, với sự đóng góp của các tác giả khác; tất cả các tác giả đảm bảo về tính đầy đủ và chính xác của dữ liệu và phân tích cũng như tính trung thực của thử nghiệm đối với giao thức.
NGƯỜI BỆNH
Bệnh nhân được đánh giá từ 18 tuổi trở lên, nhập viện với chẩn đoán lâm sàng là biến chứng cấp tính của xơ gan mất bù, có mức albumin huyết thanh dưới 30 g / lít trong vòng 72 giờ sau khi nhập viện (vì điều trị sớm có nhiều khả năng bị có lợi hơn so với liệu pháp điều trị muộn hơn), và có thời gian nằm viện dự đoán là 5 ngày hoặc lâu hơn một cách ngẫu nhiên. Các nhà điều tra đã sử dụng đánh giá lâm sàng để tránh tuyển dụng những bệnh nhân chỉ được bảo đảm nhập viện trong thời gian ngắn và những người mong đợi thời gian sống sót trong thời gian ngắn là tốt. Bệnh nhân nhập viện do nhiễm trùng khởi phát tại cộng đồng đủ tiêu chuẩn vì họ có tỷ lệ nhiễm trùng bệnh viện cao. Việc tuyển dụng diễn ra từ ngày 15 tháng 1 năm 2016 đến ngày 28 tháng 6 năm 2019, tại 35 bệnh viện trên khắp nước Anh, Scotland và xứ Wales.
Tiêu chí loại trừ chính là ung thư biểu mô tế bào gan tiến triển liên quan đến tuổi thọ dưới 8 tuần và được chăm sóc giảm nhẹ.
NGẪU NHIÊN HÓA
Các bệnh nhân được ghi danh và được phân công ngẫu nhiên vào các nhóm thử nghiệm với việc sử dụng hệ thống dựa trên Web (Phong bì kín). Việc lấy ngẫu nhiên được thực hiện với thuật toán xu thiên lệch giảm thiểu giúp cân bằng các chỉ định điều trị theo điểm trung tâm, Mô hình cho bệnh gan giai đoạn cuối (MELD), số rối loạn chức năng cơ quan, sử dụng hoặc không sử dụng thuốc kháng sinh và mức albumin huyết thanh (tất cả các bệnh nhân có mức albumin <30 g mỗi lít khi bắt đầu thử nghiệm).
Trong quy trình ban đầu, các phép ngẫu nhiên tiếp theo được cho phép hơn 30 ngày sau khi hoàn thành điều trị thử nghiệm, để tính đến thời gian bán hủy 21 ngày của albumin. Tuy nhiên, vì thử nghiệm không bị che khuất nên có thể có sự thiên vị tiềm ẩn vì kiến thức về phương pháp điều trị ban đầu có thể ảnh hưởng đến quyết định tham gia lại của bệnh nhân và chỉ những người sống sót mới có thể làm như vậy. Do đó, dữ liệu về những bệnh nhân trải qua phân tích ngẫu nhiên ban đầu được trình bày ở đây, và các phân tích bao gồm dữ liệu về những bệnh nhân trải qua một phân tích ngẫu nhiên hoặc ngẫu nhiên tiếp theo được báo cáo trong phần Phân tích Thống kê Bổ sung của Phụ lục Bổ sung .
SỰ CAN THIỆP
Trước đây, chúng tôi đã phát hiện ra rằng mức albumin dưới 30 g mỗi lít là dự đoán của rối loạn chức năng miễn dịch ở bệnh nhân xơ gan, 15 tuổi và chúng tôi đã chọn ngưỡng này cho thử nghiệm của mình. Trong một thử nghiệm trước đây về truyền albumin ở bệnh nhân nhiễm trùng huyết, mức albumin mục tiêu là 30 g mỗi lít trở lên đã không đạt được, vì vậy chúng tôi đã nhắm mục tiêu 35 g mỗi lít trở lên để đảm bảo rằng sẽ đạt được 30 g mỗi lít hoặc hơn. Bệnh nhân có mức albumin huyết thanh dưới 30 g mỗi lít được chỉ định nhận dung dịch albumin người 20% hàng ngày (truyền với tốc độ 100 ml mỗi giờ) kể từ ngày đầu tiên tuyển dụng, với mục đích duy trì mức albumin ở 35 g mỗi lít trở lên, hoặc chăm sóc y tế tiêu chuẩn. Truyền trong nhóm albumin được tiếp tục trong tối đa 14 ngày sau khi phân nhóm ngẫu nhiên hoặc cho đến khi xuất viện (nếu xuất viện trước 14 ngày) hoặc cho đến khi bệnh nhân được coi là đủ sức khỏe để xuất viện nếu việc tiếp tục nhập viện được bảo đảm vì các lý do phi y tế như sắp xếp hỗ trợ tại nhà (nếu quyết định này được thực hiện trước 14 ngày). Truyền albumin kết thúc vào thời điểm xuất viện hoặc khi bệnh nhân được coi là đủ sức khỏe để xuất viện (nếu điều này xảy ra trước 14 ngày). Dữ liệu được thu thập cho đến ngày 15 sau khi phân loại ngẫu nhiên, khi xuất viện, hoặc khi bệnh nhân được coi là đủ sức khỏe để xuất viện (nếu điều này xảy ra trước 15 ngày) (Hình S1).
Thể tích dung dịch albumin người được xác định theo mức albumin huyết thanh của bệnh nhân (hoặc lần đo gần nhất) vào ngày dùng thuốc (xem Bảng S2), và hiệu quả của phác đồ đã được xác minh trong nghiên cứu khả thi của chúng tôi. Việc truyền nhóm albumin được tiếp tục trong suốt thời gian điều trị thử nghiệm, ngay cả khi bệnh nhân có biến cố sơ cấp không béo đủ điều kiện. Các bác sĩ lâm sàng có thể kê toa các phác đồ khác nhau cho những bệnh nhân bị nội soi khối lượng lớn, viêm phúc mạc do vi khuẩn tự phát hoặc hội chứng gan thận, theo hướng dẫn; tuy nhiên, trong nhóm albumin, dung dịch albumin người 20% phải được truyền nếu mức albumin huyết thanh của bệnh nhân dưới 35 g mỗi lít, trừ khi có những lo ngại về an toàn. Những sai lệch so với kế hoạch này đã được ghi lại trong các biểu mẫu báo cáo tình huống.
Vì dung dịch albumin người 20% được khuyến cáo cho những bệnh nhân được đặt nội khí quản khối lượng lớn, viêm phúc mạc do vi khuẩn tự phát, hoặc hội chứng gan thận, sẽ là phi đạo đức nếu từ chối sử dụng nó cho những bệnh nhân trong nhóm chăm sóc tiêu chuẩn có những tình trạng này. Do đó, những bệnh nhân này được phép sử dụng albumin, và các bác sĩ lâm sàng chịu trách nhiệm về liều lượng. Việc sử dụng truyền albumin cho các chỉ định khác trong nhóm chăm sóc tiêu chuẩn được coi là sai lệch trong quy trình và được theo dõi bởi ủy ban giám sát an toàn và dữ liệu độc lập. Tham gia các bác sĩ lâm sàng đưa ra tất cả các quyết định điều trị khác.
ĐIỂM KẾT THÚC
Điểm cuối chính là tổng hợp nhiễm trùng do bất kỳ nguyên nhân nào, rối loạn chức năng thận hoặc tử vong ở bệnh nhân nhập viện từ ngày thử nghiệm thứ 3 đến ngày thứ 15, ngày xuất viện (nếu trước ngày thứ 15), hoặc ngày bệnh nhân được đánh giá là đủ sức khỏe để xuất viện (nếu trước ngày 15). Bệnh nhân được đánh giá hàng ngày cho đến khi xuất viện, tử vong, hoặc xác định rằng họ đủ sức khỏe để xuất viện. Dữ liệu về nhiễm trùng hoặc rối loạn chức năng thận không được thu thập sau khi xuất viện hoặc khi bệnh nhân được coi là đủ sức khỏe để xuất viện. Dữ liệu tử vong được thu thập sau khi xuất viện, nhưng chỉ những trường hợp tử vong xảy ra trước ngày xuất viện hoặc ngày 15 (tùy theo ngày nào trước đó) mới được đưa vào đánh giá điểm kết thúc chính. Tử vong từ ngày thứ 3 đến ngày 15 ở bệnh nhân xuất viện được đưa vào phân tích tử vong ở 28 ngày đến 6 tháng.
Nghiên cứu khả thi của chúng tôi cho thấy rằng ở hầu hết bệnh nhân được dùng albumin, mức albumin huyết thanh từ 30 g / lít trở lên đạt được trong vòng 3 ngày, và chúng tôi lý luận rằng việc đánh giá kết quả bắt đầu từ ngày thứ 3 sẽ cho phép thiết lập bất kỳ tác dụng sinh học nào của anbumin. Hơn nữa, mặc dù tất cả các bệnh nhân trải qua phân nhóm ngẫu nhiên đều được nhận albumin hoặc chăm sóc tiêu chuẩn vào ngày phân nhóm ngẫu nhiên, một số tử vong rất nhanh sau khi nhập viện và được coi là không có khả năng hưởng lợi từ albumin nếu họ còn sống. Chúng tôi đã xem các sự kiện xảy ra vào ngày 1 hoặc ngày 2 là không có khả năng liên quan đến albumin và chúng tôi đã loại trừ các sự kiện này khỏi việc đánh giá điểm cuối chính để tránh khả năng sự khác biệt giữa các nhóm sẽ ảnh hưởng đến kết quả thử nghiệm .
Việc chẩn đoán nhiễm trùng ở bệnh nhân xơ gan có thể gặp nhiều khó khăn, với tỷ lệ nhiễm trùng âm tính cao. Do đó, chúng tôi xác định nhiễm trùng theo chẩn đoán của bác sĩ lâm sàng; một chẩn đoán như vậy đã kích hoạt việc ghi lại thông tin hỗ trợ để hội đồng bác sĩ xác nhận một cách mù quáng.
Theo định nghĩa của điểm cuối chính, rối loạn chức năng cơ quan đã được thay đổi thành chỉ rối loạn chức năng thận vào năm 2018, sau nghiên cứu khả thi của chúng tôi. mức creatinine từ 0,3 mg mỗi decilit trở lên trong vòng 48 giờ, hoặc khi bắt đầu điều trị thay thế thận. Những bệnh nhân được điều trị thay thế thận ở thời điểm ban đầu không thể có biến cố ở điểm cuối này.
Điểm cuối phụ là chết ở 28 ngày, 3 tháng và 6 tháng; các thành phần điểm cuối chính tổng hợp; tổng lượng albumin được sử dụng trong quá trình thử nghiệm; thời gian nằm viện; số ngày trong phòng chăm sóc đặc biệt; tỷ lệ mắc các rối loạn chức năng cơ quan khác (định nghĩa được cung cấp trong Bảng S3); tỷ lệ ghép gan trong vòng 6 tháng sau khi bắt đầu thử nghiệm; điểm MELD khi kết thúc thử nghiệm; sử dụng terlipressin để điều trị rối loạn chức năng thận, hạ huyết áp, hoặc chảy máu tĩnh mạch; và các sự kiện bất lợi nghiêm trọng. Phân tích chất lượng cuộc sống và phân tích kinh tế sức khỏe đang được tiến hành.
PHÂN TÍCH THỐNG KÊ
Chúng tôi ước tính tỷ lệ xuất hiện biến cố kết thúc chính tổng hợp là 30%, trong đó tỷ lệ nhiễm trùng bệnh viện ở bệnh nhân xơ gan là 20 đến 30% và thực tế là 30% các trường hợp nhiễm trùng này gây ra rối loạn chức năng cơ quan. Chúng tôi giả định rằng mức albumin mục tiêu sẽ làm giảm tỷ lệ nhiễm trùng xuống 30%, như trong các nghiên cứu trước đây, và chúng tôi tính toán rằng 389 bệnh nhân mỗi nhóm sẽ cung cấp 80% sức mạnh để phát hiện ra điều này giữa- khác biệt nhóm ở mức ý nghĩa 0,05. Giả sử mất 10% để theo dõi hoặc cắt cơn, chúng tôi ước tính một mẫu mục tiêu là 433 bệnh nhân cho mỗi nhóm; tuy nhiên, do số lượng bệnh nhân bỏ theo dõi hoặc rút lui thấp hơn dự kiến, chúng tôi đã hoàn thành việc đăng ký sau khi 828 bệnh nhân được phân loại ngẫu nhiên.
Việc phân tích điểm cuối chính được thực hiện với mô hình hồi quy logistic-hiệu ứng hỗn hợp bao gồm chỉ báo xử lý nhị phân, các biến phân tầng là các hiệu ứng cố định và một điểm chặn ngẫu nhiên cho mỗi vị trí. Chúng tôi cũng thực hiện phân tích theo thời gian sự kiện, với dữ liệu bệnh nhân được kiểm duyệt khi xuất viện, ngày bệnh nhân được coi là đủ sức khỏe để xuất viện, hoặc ngày xét xử 15, tùy theo ngày nào sớm hơn. Tất cả các bệnh nhân trải qua phân tích ngẫu nhiên đều được đưa vào phân tích ý định điều trị, nhưng các biến cố xảy ra vào ngày 1 hoặc ngày 2 (75 biến cố ở nhóm albumin và 94 ở nhóm chăm sóc tiêu chuẩn) không được phân loại là điểm kết thúc chính. các sự kiện, được xác định trước từ ngày 3 đến ngày 15. Bệnh nhân bị nhiễm trùng, rối loạn chức năng thận, hoặc cả hai vào ngày 1 hoặc ngày 2 và những người cũng có bất kỳ thành phần nào của điểm cuối chính giữa ngày 3 và ngày 15 được phân loại là có sự kiện điểm cuối chính. Các phân tích hỗ trợ bao gồm việc mở rộng cửa sổ điểm cuối đến các ngày từ 1 đến 15 và các ngày từ 2 đến 15.
Các điểm cuối thứ cấp là tác động của việc điều trị đối với các thành phần riêng lẻ của điểm cuối chính. Đối với điểm cuối phụ, ước tính điểm và khoảng tin cậy 95% được báo cáo; những khoảng tin cậy này không được điều chỉnh cho nhiều lần so sánh và không nên được sử dụng để suy ra hiệu quả điều trị dứt điểm. Các phân tích được thực hiện với việc sử dụng phần mềm SAS, phiên bản 9.4 (Viện SAS).
Kết quả
NGƯỜI BỆNH
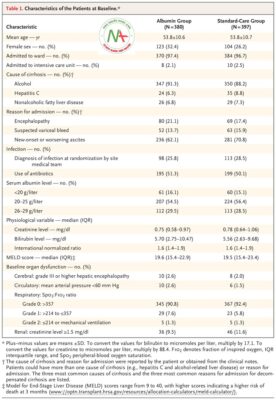
Trong 3 năm, 9273 bệnh nhân đã được sàng lọc và 1563 người được coi là đủ điều kiện tham gia thử nghiệm. Tổng cộng có 829 bệnh nhân được phân nhóm ngẫu nhiên (mặc dù 1 trong số những bệnh nhân này đã rút lại sự đồng ý rất sớm trong thử nghiệm), trong đó 51 bệnh nhân đã trải qua một lần ngẫu nhiên hoặc ngẫu nhiên tiếp theo, để lại 777 bệnh nhân duy nhất đã trải qua ngẫu nhiên ít nhất một lần và những người có dữ liệu có thể được đánh giá (xem Hình S2). Hầu hết các bệnh nhân bị bệnh gan liên quan đến rượu, và các nhóm được kết hợp với nhau ở thời điểm ban đầu ( Bảng 1); 203 trong số 770 bệnh nhân (26,4%) đã được điều trị để cai rượu, và 191 trong số 768 bệnh nhân (24,9%) được coi là bị viêm gan do rượu. Trung bình, các bệnh nhân được thu nhận vào ngày sau khi nhập viện và có mức albumin trung bình (± SD) là 23,2 ± 3,7 g mỗi lít. Số ngày nhập viện trung bình trong thời gian điều trị thử nghiệm (dự kiến cho ≤14 ngày) là 8 ngày (phạm vi liên phần, 6 đến 15) ở nhóm albumin và 9 (phạm vi liên phân vị, 6 đến 15) trong nhóm chăm sóc tiêu chuẩn , không có sự khác biệt đáng kể giữa hai nhóm thử nghiệm (Bảng S8). Tổng cộng 40 bệnh nhân trong nhóm albumin và 47 bệnh nhân trong nhóm chăm sóc tiêu chuẩn được xuất viện trong vòng 5 ngày sau khi phân loại ngẫu nhiên. Thời gian theo dõi tử vong tối thiểu là 3 tháng và thời gian tối đa là 6 tháng sau khi phân nhóm ngẫu nhiên.
Đối với điểm kết thúc chính tổng hợp, dữ liệu còn thiếu duy nhất là của 54 bệnh nhân đã ngừng điều trị (35 bệnh nhân ở nhóm dùng albumin và 19 ở nhóm chăm sóc tiêu chuẩn). Một phân tích ngưỡng bao gồm những dữ liệu bị thiếu này đã loại trừ lợi ích của liệu pháp albumin (xem phần Phân tích thống kê bổ sung trong Phụ lục bổ sung ).
LIỆU PHÁP ALBUMIN
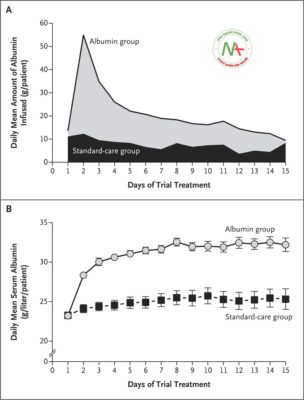
Trong suốt thử nghiệm, trung bình 200 g (phạm vi liên phân vị, 140 đến 280) của albumin trên mỗi bệnh nhân được sử dụng trong nhóm albumin, so với 20 g (phạm vi liên phân vị, 0 đến 120) được sử dụng trong nhóm chăm sóc tiêu chuẩn (đã điều chỉnh chênh lệch trung bình, 143 g; khoảng tin cậy 95% [CI], 127 đến 158,2). Tổng cộng có 196 trong số 397 bệnh nhân (49,4%) trong nhóm chăm sóc tiêu chuẩn không nhận được bất kỳ albumin nào. Lượng albumin trung bình hàng ngày được truyền về cơ bản có sự khác biệt đáng kể giữa nhóm albumin và nhóm chăm sóc tiêu chuẩn trong suốt thời gian điều trị thử nghiệm ( Hình 1A ), và mức albumin trung bình là 30 g mỗi lít trở lên trong khoảng thời gian từ ngày 3 đến ngày 15 ở nhóm dùng albumin ( Hình 1B ).
ĐIỂM CUỐI CHÍNH
Trong phân tích ý định điều trị, tổng số 113 trong số 380 bệnh nhân (29,7%) trong nhóm albumin và 120 trong số 397 bệnh nhân (30,2%) trong nhóm chăm sóc tiêu chuẩn có một sự kiện kết thúc chính kết hợp được xác định theo giao thức. (tỷ lệ chênh lệch đã điều chỉnh, 0,98; KTC 95%, 0,71-1,33; P = 0,87). Khi tất cả các trường hợp tử vong được báo cáo được bao gồm cả ngày chết được xác nhận, 116 trong số 380 bệnh nhân (30,5%) trong nhóm albumin và 119 trong số 397 (30,0%) trong nhóm chăm sóc tiêu chuẩn có biến cố kết thúc chính (tỷ lệ chênh lệch, 1,02; KTC 95%, 0,75 đến 1,40). Ba sự kiện bổ sung trong nhóm albumin tương ứng với những bệnh nhân chết trong thời gian điều trị (từ ngày 3 đến ngày 15 trong bệnh viện); những cái chết này đã được xác định bằng cách xác minh kết quả. Một sự kiện cuối cùng chính ít hơn trong nhóm chăm sóc tiêu chuẩn là một ca tử vong đã được xác minh là nằm ngoài cửa sổ sự kiện chính. Một phân tích thời gian-sự kiện cũng không cho thấy sự khác biệt đáng kể giữa các nhóm (tỷ lệ nguy cơ nhiễm trùng, rối loạn chức năng thận hoặc tử vong, 1,04; KTC 95%, 0,81-1,35). Bốn bệnh nhân trong nhóm dùng albumin và 6 bệnh nhân trong nhóm chăm sóc tiêu chuẩn tử vong từ khi xuất viện đến ngày 15, và những trường hợp tử vong này không được coi là biến cố kết thúc tổng hợp chính nhưng được đưa vào phân tích tử vong ở 28 ngày và 6 tháng.
Các phân tích hỗ trợ trong đó cửa sổ báo cáo được mở rộng sang ngày 1 hoặc ngày 2 cho thấy không có sự khác biệt đáng kể giữa các nhóm trong các sự kiện điểm cuối chính (xem Bảng S5). Các phân tích phân nhóm được chỉ định trước không cho thấy bằng chứng về sự khác biệt đáng kể trong các biến cố điểm cuối chính theo điểm MELD cơ bản, mức albumin huyết thanh, việc sử dụng hoặc không sử dụng kháng sinh, số rối loạn chức năng cơ quan, lý do nhập viện, tình trạng bệnh cùng tồn tại và tuổi tác (xem Hình . S4 và Bảng S6). Hình S4 cho thấy sự khác biệt có thể có theo giới tính, nhưng khoảng tin cậy vượt qua 1 đối với cả nam và nữ.
Các phân tích bao gồm những bệnh nhân trải qua một lần phân nhóm ngẫu nhiên hoặc ngẫu nhiên tiếp theo cho thấy không có sự khác biệt đáng kể giữa các nhóm (xem Bảng S7). Trong một phân tích trong đó các thành phần của điểm cuối chính được kiểm tra riêng biệt, không có bằng chứng về sự khác biệt đáng kể giữa các nhóm. Nhiễm trùng mới xảy ra ở 79 trong số 380 bệnh nhân (20,8%) trong nhóm albumin và 71 trong số 397 (17,9%) trong nhóm chăm sóc tiêu chuẩn (tỷ lệ chênh lệch đã điều chỉnh, 1,22; KTC 95%, 0,85-1,75). Các biểu mẫu báo cáo trường hợp nhiễm trùng không cho thấy sự sai lệch trong việc báo cáo các trường hợp nhiễm trùng ở hai nhóm.
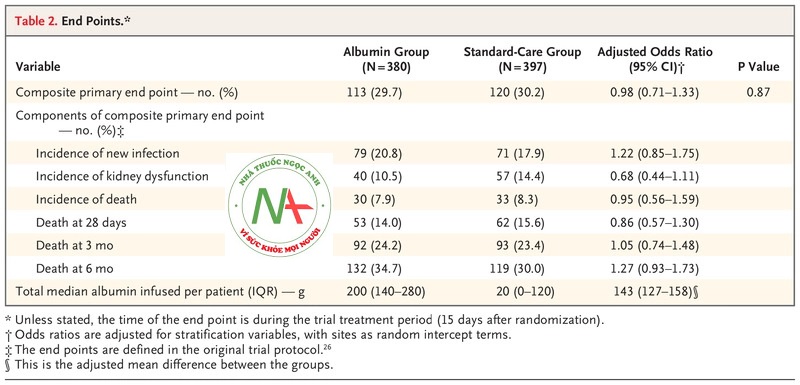
Rối loạn chức năng thận xảy ra ở 40 trong số 380 bệnh nhân (10,5%) nhóm albumin và 57 trên 397 bệnh nhân (14,4%) ở nhóm chăm sóc tiêu chuẩn (tỷ lệ chênh lệch đã điều chỉnh, 0,68; KTC 95%, 0,44-1,11). Tử vong xảy ra ở 30 trong số 380 bệnh nhân (7,9%) ở nhóm dùng albumin và 33 trong số 397 (8,3%) ở nhóm chăm sóc tiêu chuẩn (tỷ lệ chênh lệch, 0,95; KTC 95%, 0,56 đến 1,59) ( Bảng 2 ).
ĐIỂM CUỐI PHỤ
Không có sự khác biệt đáng kể giữa các nhóm về thời gian chết và thời gian chết (xem Hình S3). Tại 28 ngày, 53 trong số 380 bệnh nhân (14,0%) trong nhóm albumin và 62 trong số 397 bệnh nhân (15,6%) trong nhóm chăm sóc tiêu chuẩn đã tử vong (tỷ lệ chênh lệch đã điều chỉnh, 0,86; KTC 95%, 0,57 đến 1,30); tại thời điểm 3 tháng, lần lượt 92 bệnh nhân (24,2%) và 93 bệnh nhân (23,4%) tử vong (tỷ lệ chênh lệch đã điều chỉnh, 1,05; KTC 95%, 0,74-1,48); và sau 6 tháng, lần lượt 132 bệnh nhân (34,7%) và 119 bệnh nhân (30,0%) tử vong (tỷ số chênh lệch đã điều chỉnh, 1,27; KTC 95%, 0,93-1,73).
Không có bằng chứng về sự khác biệt đáng kể giữa các nhóm trong quá trình điều trị liên quan đến sự phát triển của rối loạn chức năng hô hấp, tim mạch hoặc não mới hoặc việc sử dụng terlipressin. Ngoài ra, không có sự khác biệt đáng kể giữa các nhóm về thời gian nhập viện. Theo phạm vi giữa các nhóm, có thể có nhiều ngày trong phòng chăm sóc đặc biệt ở nhóm albumin hơn so với nhóm chăm sóc tiêu chuẩn, nhưng số ngày này nói chung là rất nhỏ.
CÁC BIẾN CỐ BẤT LỢI
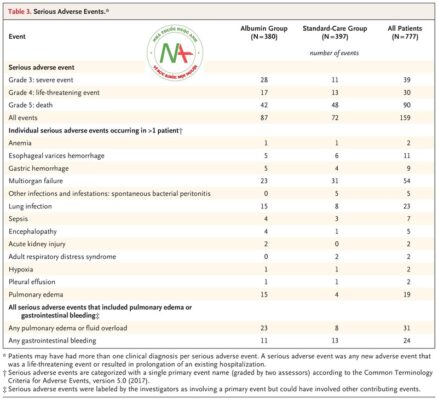
Có nhiều tác dụng phụ nghiêm trọng đe dọa tính mạng hoặc nghiêm trọng hơn, đặc biệt là phù phổi hoặc quá tải chất lỏng, ở nhóm albumin hơn so với nhóm chăm sóc tiêu chuẩn ( Bảng 3 ). Các chi tiết bổ sung được cung cấp trong Bảng S9 và S10.
Thảo luận
ATTIRE, một thử nghiệm đa trung tâm để đánh giá hiệu quả của albumin trong việc ngăn ngừa nhiễm trùng, rối loạn chức năng thận hoặc tử vong ở bệnh nhân xơ gan mất bù, không cho thấy lợi ích của liệu pháp albumin mục tiêu so với chăm sóc tiêu chuẩn hiện tại ở Vương quốc Anh. Không có ảnh hưởng đến tỷ lệ nhiễm trùng, được thể hiện bởi không có sự khác biệt đáng kể giữa các nhóm về tỷ lệ nhiễm trùng mới hoặc các biến cố ở giai đoạn cuối ở những bệnh nhân nhập viện nhiễm trùng hoặc đang dùng kháng sinh khi nhập viện. Mặc dù phác đồ nhắm mục tiêu để tăng mức albumin huyết thanh lên 30 mỗi lít hoặc hơn, không có lợi ích rõ ràng của can thiệp đối với điểm kết thúc chính ở bất kỳ phân nhóm nào được phân tích.Cuối cùng, không có sự khác biệt đáng kể giữa các nhóm về tỷ lệ tử vong ở 28 ngày, 3 tháng và 6 tháng.
Một hạn chế của thử nghiệm này là nó không bị mù. Chúng tôi đã chọn không sử dụng phương pháp làm mù vì bệnh nhân trong nhóm chăm sóc tiêu chuẩn được truyền chất lỏng “nonalbumin” có thể không tăng mức albumin huyết thanh đến mức mục tiêu đã đặt và có thể đã nhận được lượng chất lỏng có hại trong một nỗ lực tăng vô ích. mức albumin, và thử nghiệm albumin thường quy sẽ không làm cho thử nghiệm bị cản trở. Tuy nhiên, các bệnh nhân nhận được lượng dung dịch albumin người 20% khác nhau về cơ bản, đặc biệt là trong thời gian đầu của thử nghiệm khi nồng độ albumin tăng lên có thể mang lại lợi ích. Lượng albumin trung bình được truyền trong nhóm chăm sóc tiêu chuẩn thấp hơn dự đoán, do đó sự khác biệt giữa các nhóm về lượng albumin được truyền lớn hơn dự kiến; tuy nhiên, truyền albumin mục tiêu không ảnh hưởng đến kết quả.
Chúng tôi kết luận rằng liệu pháp albumin nhắm mục tiêu không có tác dụng quan trọng về mặt lâm sàng trong việc ngăn ngừa nhiễm trùng hoặc giảm sự phát triển của rối loạn chức năng thận ở bệnh nhân xơ gan mất bù nhập viện. Phát hiện này trái ngược với những nghiên cứu trong phòng thí nghiệm của chúng tôi, và sự khác biệt này nhấn mạnh tầm quan trọng của các thử nghiệm lâm sàng xác nhận được cung cấp phù hợp. Việc truyền một lượng lớn albumin hơn có lẽ sẽ không an toàn và có thể dẫn đến các tác dụng phụ nghiêm trọng hơn hoặc đe dọa tính mạng ở nhóm dùng albumin.
Mặc dù các thành phần của điểm cuối tổng hợp không tương đương về mức độ nghiêm trọng, nhưng chúng đại diện cho một quỹ đạo bệnh chung và di chuyển phù hợp với nhau. Việc sử dụng điểm cuối tổng hợp đã cải thiện hiệu quả thống kê, và hiệu ứng rỗng nhất quán đã được quan sát thấy trong tất cả các thành phần. Chúng tôi đã xác nhận ảnh hưởng nghiêm trọng của xơ gan do rượu ở Vương quốc Anh, như đã được trình bày trước đây trong thử nghiệm Steroid hoặc Pentoxifylline đối với bệnh viêm gan do rượu (STOPAH), và kết quả có thể khác nhau đối với các nguyên nhân khác gây xơ gan.
Thử nghiệm của chúng tôi không cho thấy lợi ích của liệu pháp albumin khi được sử dụng để tăng và duy trì mức albumin huyết thanh đến 30 g mỗi lít hoặc hơn ở bệnh nhân xơ gan nhập viện. Với sự khác biệt gần gấp ba lần về lượng albumin được truyền giữa các nhóm và không có lợi ích trên tất cả các phân nhóm và điểm kết thúc được kiểm tra, những dữ liệu này hỗ trợ nhu cầu đánh giá lại việc sử dụng albumin ở bệnh nhân xơ gan.
Nhóm tác giả
- Louise China, Ph.D.,
- Nick Freemantle, Ph.D.,
- Ewan Forrest, M.D.,
- Yiannis Kallis, Ph.D.,
- Stephen D. Ryder, D.M.,
- Gavin Wright, Ph.D.,
- Andrew J. Portal, M.D.,
- Natalia Becares Salles, Ph.D.,
- Derek W. Gilroy, Ph.D.,
- and Alastair O’Brien, Ph. D
Nguồn: A Randomized Trial of Albumin Infusions in Hospitalized Patients with Cirrhosis
https://www.nejm.org/doi/full/10.1056/NEJMoa2022166
