Thông Tin Thuốc
Rối loạn chức năng đông máu của kháng sinh Cefoperazon, Cefoperazon – Sulbactam
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
Biên soạn:
DS Đinh Thu Hương, Khoa Dược, Bệnh viện Phổi Trung Ương
Hiệu đính:
ThS. Trần Thị Thu Trang – Bộ môn Dược lâm sàng Trường ĐH Dược Hà Nội
Nguồn:
Khoa Dược, Bệnh viện Phổi Trung Ương.
Sử dụng kháng sinh hợp lý, an toàn, hiệu quả là một phần quan trọng trong Chương trình quản lý kháng sinh. Bên cạnh hiệu quả điều trị, việc sử dụng kháng sinh cần quan tâm đến các tác dụng không mong muốn, đặc biệt trên những bệnh nhân nặng, có nhiều yếu tố nguy cơ gặp tác dụng phụ. Theo tổng kết từ Trung tâm Quốc gia về thuốc và phản ứng có hại của thuốc, kháng sinh là nhóm được báo cáo nhiều nhất, đặc biệt tần suất các báo cáo tác dụng không mong muốn (ADR) về cefoperazon; cefoperazon-sulbactam được xếp hạng trong 8 thuốc nghi ngờ được báo cáo nhiều nhất [8]. Bên cạnh các tác dụng phụ thường gặp như rối loạn tiêu hóa, dị ứng thuốc, độc tính trên gan, trên thận… thì các tác dụng trên hệ thống đông máu, cụ thể là giảm thời gian prothrombin máu, giảm số lượng tiểu cầu và tăng nguy cơ chảy máu được báo cáo ngày càng nhiều. Đây thật sự là một ADR thầm lặng, hiện chưa thật sự được chú ý trong thực hành lâm sàng, đã làm gia tăng lo ngại về tính an toàn liên quan tới cefoperazon và cefoperazon-sulbactam [2, 4, 7, 8].
Cefoperazon là kháng sinh cephalosporin thế hệ 3. Các dữ liệu in vitro cho thấy cefoperazon có tác dụng hiệp đồng khi phối hợp với chất ức chế beta-lactamase là sulbactam. Việc kết hợp sulbactam với cefoperazon giúp mở rộng phổ kháng khuẩn của cefoperazon trên Acinetobacter baumanii và một số vi khuẩn Gram âm tiết ra beta-lactamase phổ rộng (extended spectrum beta-lactamase – ESBL). Ngoài ra, cefoperazon/sulbactam còn có hoạt tính chống lại các chủng vi khuẩn kỵ khí Bacteroides. Với phổ kháng khuẩn này, cefoperazon/sulbactam đã được chứng minh được hiệu quả trong việc điều trị các loại nhiễm khuẩn như: nhiễm khuẩn ổ bụng; sốt liên quan đến nhiễm khuẩn ở bệnh nhân giảm bạch cầu trung tính; nhiễm khuẩn mắc phải ở bệnh viện, trong đó chủ yếu là viêm phổi mắc phải ở bệnh viện; nhiễm khuẩn vết mổ sau phẫu thuật; nhiễm khuẩn đường tiết niệu và nhiễm khuẩn gây ra bởi các vi khuẩn tiết ra beta-lactamase [1].
Tại Bệnh viện Phổi Trung ương, cefoperazon và cefoperazon/sulbactam thuộc nhóm kháng sinh sử dụng nhiều nhất với tỉ lệ khoảng 20% về số lượng và 25-30% về giá trị tiền trong các kháng sinh.
1. Cơ chế gây chảy máu của kháng sinh cephalosporin dưới góc nhìn liên quan cấu trúc-tác dụng
Nhiều dữ liệu đã cho thấy bệnh nhân bị thiếu hụt nhiều yếu tố đông máu sau khi sử dụng cefoperazon, cefoperazon/sulbactam. Mặc dù xét nghiệm mức vitamin K không được thực hiện nhưng việc giảm chọn lọc các yếu tố II, IX và X, cùng phản ứng tích cực với việc bổ sung vitamin K, cho thấy rõ ràng là thiếu hụt vitamin K trên các đối tượng trên [2, 3, 5].
Trước đây nguyên nhân chủ yếu gây rối loạn yếu tố đông máu liên quan đến vitamin K gây ra bởi kháng sinh cephalosporin là do giảm hệ vi khuẩn có lợi sống tại đường ruột (những vi khuẩn này cung cấp một phần vitamin K (K2) cho cơ thể). Tuy nhiên giả thuyết này hiện nay ít được ủng hộ do một số kháng sinh phổ rộng khác cephalosporin thế hệ mới có hoạt tính tương tự trên hệ khuẩn đường ruột nhưng không ghi nhận làm thay đổi các yếu tố đông máu. Kèm theo đó, khi dùng các kháng sinh đường tiêm, phản ứng này vẫn xảy ra như khi dùng đường uống.
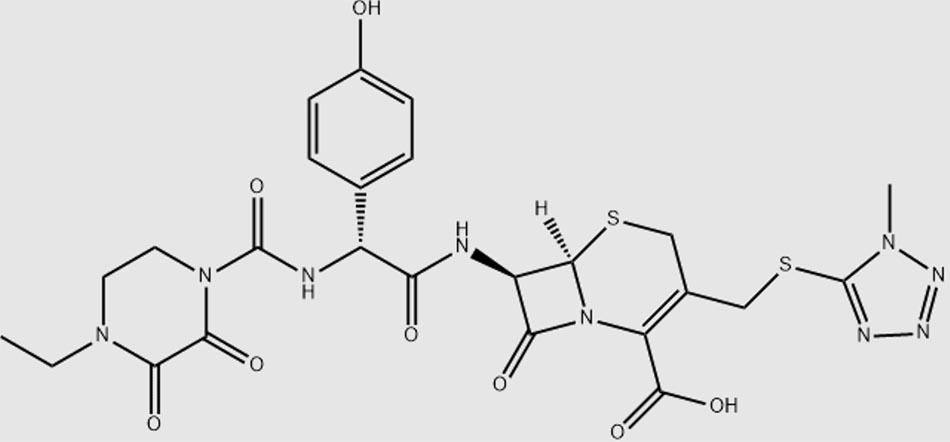
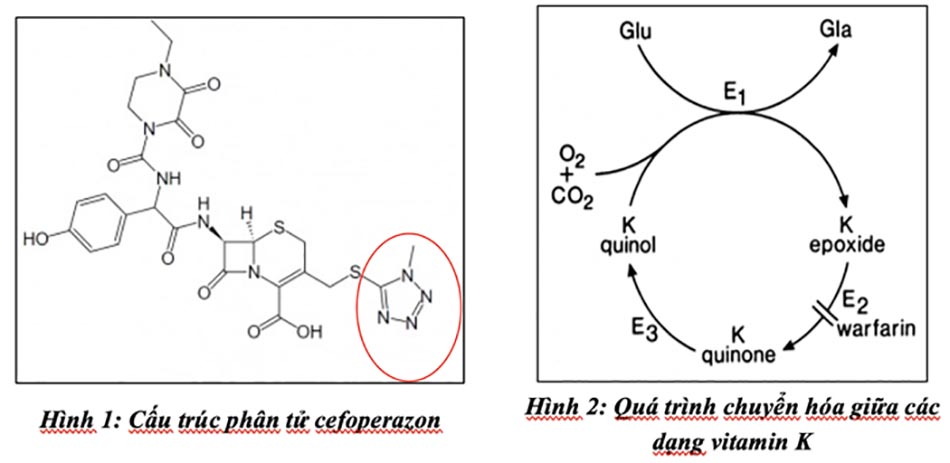
Kết quả từ nhiều nghiên cứu invitro cho thấy, các kháng sinh cephalosporin có chuỗi bên là N-methylthiotetrazol (NMTT-cephalosporin) (gồm 5 kháng sinh cephalosporin thế hệ 2 là cefamandol, cefbuperazon, cefmetazol, cefminox, cefotetan; 3 kháng sinh thế hệ 3 là cefmenoxim, cefoperazon, moxalactam) và một cephalosporin có chuỗi bên là methylthiadiazol (MTD) (cefazolin) gây tăng nồng độ vitamin K1 2,3-epoxid trong huyết tương. Cơ chế giả định của hiện tượn này là do các thuốc ức chế phản ứng g-carboxyl hóa chuyển từ vitamin K dạng epoxide thành dạng quinone tại gan (ức chế enzyme E2 tương tự như warfarin và nhóm dicoumarol), từ đó làm giảm chuyển hóa về dạng hoạt tính của vitamin K trong cơ thể, làm tăng nồng độ vitamin K1 2,3 epoxid ở tế bào gan [3, 5, 7] (Hình 1, 2).
2. Báo cáo rối loạn đông máu, xuất huyết liên quan đến cefoperazon/cefoperazon-sulbactam trên thực hành lâm sàng
Một tổng quan hệ thống (systematic review) và phân tích tổng hợp (meta-analysis) của Park và cộng sự (2019) đánh giá về hồ sơ an toàn của nhóm cephalosporin trên giảm prothrombin và chảy máu ghi nhận: NMTT-cephalosporin làm tăng nguy cơ gây giảm prothrombin huyết và kéo dài thời gian prothrombin so với nhóm không có nhánh NMTT (tương ứng OR 1,676; 95%CI 1,275-2,203 và OR 2,050; 95%CI 1,398-3,005). Phân tích dưới nhóm cho thấy cefoperazon làm tăng nguy cơ giảm prothrombin với nhóm đối chứng (OR 2,506; 95%CI 1,293-4,860) [7]. Nhóm NMTT-cephalosporin cũng làm tăng biến cố xuất huyết, tuy nhiên không có ý nghĩa thống kê (OR 1.359, 95% CI 0,920–2,009) [4].
Nghiên cứu thuần tập hồi cứu của Wang và cộng sự (2020) trên 23.242 bệnh nhân cho thấy tỉ lệ kéo dài PT, rối loạn đông máu, giảm tiểu cầu, chảy máu ở nhóm bệnh nhân sử dụng cefoperazon/sulbactam lần lượt là 5,3%; 9,2%; 15,7% và 4.2,%. Các phân tích so sánh điểm xu hướng cho thấy cefoperazon-sulbactam làm tăng nguy cơ kéo dài PT (aOR 2,26, 95% CI 1,61-3,18), rối loạn đông máu (aOR 1,81, 95% CI 1,43-2,30) và giảm tiểu cầu (aOR 1,46, 95 % CI 1,25-1,72), nhưng không làm tăng chảy máu (aOR 1,05, 95% CI 0,79-1,40) so với ceftazidim. Phân tích cũng cho thấy, biến cố xảy ra ở cefoperazon/sulbactam cao hơn cefoperazon/tazobactam, trong đó: kéo dài PT (OR: 1,92, 95% CI: 1,43–2,57; aOR: 1,65, 95% CI: 1,21–2,25), rối loạn đông máu (OR: 1,84, 95% CI: 1,48–2,30; aOR: 1,63, 95% CI: 1,30–2,06). Kết quả này có thể mở ra thêm một giả thuyết về hiệp đồng tác dụng của sulbactam và cefoperazon trên prothrombin huyết tương [7].
3. Một số yếu tố nguy cơ ảnh hưởng làm tăng nguy cơ rối loạn đông máu
3.1. Tình trạng suy giảm chức năng gan, thận
Cefoperazon thải trừ chủ yếu qua gan, sulbactam thải trừ chủ yếu qua thận; do vậy sự suy giảm chức năng gan/thận có thể dẫn đến tăng nồng độ thuốc trong máu. Bên cạnh đó, tình trạng giảm albumin máu (có thể do suy gan, hoặc suy thận) làm tăng nồng độ dạng tự do của các cephalosporin trong huyết tương (vì các thuốc này có tỉ lệ gắn kết cao với albumin) dẫn đến tăng độc tính của thuốc. Bệnh nhân người cao tuổi có chức năng gan-thận giảm theo sinh lý cũng là đối tượng nguy cơ cao [6, 7].
3.2. Tình trạng suy dinh dưỡng
Tình trạng suy dinh dưỡng có thể làm tăng nguy cơ chảy máu khi điều trị với kháng sinh cephalosporin, trong đó nguyên nhân chủ yếu có thể do thiếu hụt dữ trữ vitamin K. Ngoài ra trên những bệnh nhân suy dinh dưỡng, albumin huyết tương cũng có thể giảm và dẫn đến hệ quả tương tự như suy giảm chức năng gan, thận [6, 7].
3.3. Trẻ sơ sinh và trẻ nhỏ
Trẻ sơ sinh, đặc biệt là sơ sinh thiếu tháng có nguy cơ thiếu vitamin K do hệ vi khuẩn đường ruột phát triển chưa hoàn chỉnh [6, 7].
4. Hướng can thiệp giảm thiểu nguy cơ chảy máu trên đối tượng nguy cơ khi sử dụng kháng sinh cefoperazon, cefoperazon/sulbactam
4.1. Đánh giá đối tượng nguy cơ và theo dõi qua các cận lâm sàng
Người bệnh có nguy cơ cao (tiền sử xuất huyết, giảm prothrombin…) khi sử dụng các kháng sinh mới, đặc biệt là kháng sinh cephalosporin có nhánh bên NMTT, nguy cơ chảy máu có thể thấp nếu dùng thuốc trong thời gian ngắn. Tuy nhiên trên những bệnh nhân nặng, có tổn thương dạ dày và chức năng thận suy giảm, dùng thuốc kéo dài nguy cơ có thể cao hơn (chưa bao gồm nguy cơ do tương tác thuốc).
Với đặc thù bệnh tật tại Bệnh viện Phổi Trung ương với tỉ lệ người bệnh mắc bệnh mạn tính, dùng nhiều thuốc kéo dài và nguy cơ cao như thuốc điều trị lao (rifampicin, linezolid…), hóa chất điều trị ung thư (nhóm platin, bleomycin…) cũng làm tăng các biến cố bất lợi trên huyết học. Do đó bác sĩ điều trị cần cân nhắc giữa lợi ích (điều trị nhiễm khuẩn) và nguy cơ (xuất huyết, rối loạn huyết động) khi sử dụng cefoperazon, cefoperazon/sulbactam trên các đối tượng này.
4.2. Dự phòng xuất huyết bằng vitamin K trên bệnh nhân nguy cơ cao
Dự phòng bằng vitamin K có thể được cân nhắc trên những bệnh nhân có nguy cơ chảy máu cao [2]. Vitamin K1 trong dự phòng xuất huyết do thuốc nói chung có thể được dùng theo đường uống, tiêm bắp, tiêm tĩnh mạch; trong đó đường uống được ưu tiên với liều 2,5-25mg [9].
4.3 Xử trí trong trường hợp xuất huyết
Ngưng thuốc có nguy cơ gây xuất huyết như cefoperazon, cefoperazon/sulbactam và giải quyết các yếu tố nguy cơ là quan trọng nhất. Trong trường hợp đã có xuất huyết xảy ra, bổ sung vitamin K1 đường uống hoặc tiêm, phức hợp prothromin và huyết tương tươi là hướng giải quyết có thể được cân nhắc [3].
KẾT LUẬN
Xuất huyết do rối loạn cơ chế đông máu liên quan đến vitamin K là một trong những nguy cơ cần thận trọng khi sử dụng kháng sinh, nhất là kháng sinh phổ rộng như cefoperazon; cefoperazon/sulbactam. Đánh giá đối tượng nguy cơ, theo dõi chặt chẽ các chỉ số đông máu (PT, APTT, INR) cùng với đánh giá lâm sàng là rất quan trọng để có cân nhắc phù hợp trong lựa chọn kháng sinh, liều dùng và thời gian dùng nhằm tối ưu hóa điều trị cho bệnh nhân.
TÀI LIỆU THAM KHẢO:
1. Bộ Y Tế (2015), Hướng Dẫn Sử Dụng Kháng Sinh.
2. Hu H Fatal Vitamin K-Dependent Coagulopathy Associated With Cefoperazone/Sulbactam: A Case Report, Drug Saf – Case Rep 6, 6. 2019.
3. M. J. Shearer HB (1988), Mechanism Of Cephalosporin-Induced Hypoprothrombinemia: Relation To Cephalosporin Side Chain, Vitamin K Metabolism, And Vitamin K Status, J Clin Pharmacol, Số 28(1), Tr. 88-95.
4. Gi Hyue Park SK (2019), The Association Between Cephalosporin Andhypoprothrombinemia: A Systematic Reviewand Meta-Analysis, International Journal Ofenvironmental Researchand Public Health.
5. Mc Tique J Suttie JW EJ (1986), Efffect Of N-Methylthiotetrazol On Rat Liver Microsomal Vitamin K-Dependent Carboxylation, Biochem Pharmacol, Số 35, Tr. 2429-33.
6. Wang W SX (2018), RISK OF Bleeding And Coagulation Disorders Associated With Cefoperazone/Sulbactam: A Real World Study Based On Electronic Medical Records, Value In Health, Số 21, Tr. Supplement 2, S62.
7. Wen Wang YL (2020), Cefoperazone-Sulbactam And Risk Of Coagulation Disorders Or Bleeding: A Retrospective Cohort Study, Expert Opin Drug Saf, Số 19(3), Tr. 339-47.
8. Tổng Kết Công Tác Báo Cáo ADR Năm 2020, Trung Tâm DI&ADR Quốc Gia.
9. Bộ Y Tế (2018), Dược Thư Quốc Gia Việt Nam, Tr. 1147-1148.