Bệnh Nhi khoa
Khí máu động mạch ở trẻ: Các khía cạnh kỹ thuật và diễn giải
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
Tác giả: Colm Travers và Namasivayam Ambalavanan
Biên dịch: Bác sĩ Đặng Thanh Tuấn
nhathuocngocanh.com – Bài viết Khí máu: Các khía cạnh kỹ thuật và diễn giải được trích từ chương 10 sách Thông Khí Hỗ Trợ Cho Trẻ Sơ Sinh Tập 1.
Nội dung chính
Đo khí máu động mạch ngắt quãng (intermittent arterial blood gas measurement) la tiêu chuẩn vang để đánh giá mức độ đầy đủ của oxygen hoa và thông khí có trẻ sơ sinh bị bệnh.
Các thiết bị theo dõi liên tục không xâm lân tại giường (bedside continuous noninvasive monitoring device), chàng han như máy đo độ bão hòa oxy mạch máy (pulse oximeter), quang phổ cận hồng ngoại (near-infrared spectroscopy) va may theo dõi carbon dioxide qua da (transcutaneous carbon dioxide monitor), thường được SỬ dụng đế cung cấp các giá trị khi máu gần đúng theo thời gian thực.
Kiến thức về các phương pháp lấy máu khí máu (blood gas), các khía cạnh kỹ thuật của máy phân tích khí máu và các giá trị khi máu là nên tàng đế cung cáp dịch vu chăm sóc bệnh nhân tối ưu.
Trẻ sơ sinh có sinh lý và các bệnh lý riêng biệt ảnh hưởng đến việc giải thích lâm sàng dữ liệu xét nghiệm khí máu và các máy theo dõi không xâm lấn.
Giới thiệu
Các trị số đo khí máu ước tính mức độ nghiêm trọng của bệnh hô hấp, chẩn ‘ đoán suy hô hấp, đổng thời cũng cho biết các điệu chinh hỗ trợ hô hấp. Trong chương này, trước tiên chúng tôi muốn thảo luận về sinh lý học của quá trình vận chuyển khí trong máu, sau đó sẻ mô tả các kỹ thuật đo khí máu thường được sử dụng ở đơn vị chăm sóc đặc biệt dành cho trẻ sơ sinh (neonatal intensive care unit – NICU). Tiếp theo, chúng tôi tập trung mô tả các khía cạnh kỹ thuật của việc ước lượng khí máu bằng các thiết bị có sẵn trên thị trường. Cuối cùng, chúng tôi sẽ thảo luận về việc giải thích kết quả khí máu, cũng như một số nguy hiểm và cạm bẫy của phép đo khí máu trong thực hành lâm sàng.
Sinh lý khí máu
Trao đổi khí chủ yếu xảy ra tại các túi phổi (lung saccule) ở trẻ sinh non tháng trong phế nang ở trẻ sinh non trưởng thành hơn vị trí dù tháng, mặc dù đói khí mức độ nhỏ cũng xảy ra qua da non từ giai đoạn sớm ngay sau khi sinh. Sau khi sinh, mau da duoc khứ oxy cua tinh mach hè thòng trở lại tâm nhĩ và sau đó là tâm thất phải. Máu này được bơm qua hệ mạch máu động phối đến các mao mạch tiếp giáp với các túi phế nang/phế nang. Khi máu đi qua các phế nang được thông khí, oxy được thêm vào máu và carbon dioxide được lấy ra. Noi chung, nóng độ oxy của máu động mạch ra khỏi tâm thất til phan anh su phu lơp của thông khí và tưới máu. Hàm lượng oxy sê giảm |fl su tưới mau hạt tương hợp với sự thông khí (các phế nang được sục khí) 51 hát tương hợp thông khí-tưới máu (ventilation-percussion mismatch) xày máu đi từ hên phải của tim sang bên trái của tim mà không đi qua tuan h phoi – gọi là shunt ngoài phổi (extrapulmonary shunt), hoặc khi máu đi qua các bộ phận của phổi bị xẹp phổi và/hoặc được thông khí không đủ – tức shunt trong phổi (intrapuImonarỵ shunt).
Sự thải carbon dioxide (CO.) chủ yếu phụ thuộc vào mức độ thông khí phế nang. Khi thông khí phế nang tăng, áp lực riêng phần của co. trong khi phế nang (partial pressure of co, in alveolar gas – PACO.) giảm. Sự chênh lệch nồng độ giữa áp lực riêng phần của CO, trong máu động mạch (partial pressure of CO2 in arterial blood – PCO2) và PACO, tàng lên để có nhiều cơ, khuếch tán từ máu vào phế nang hơn và được loại bò khỏi máu qua phổi. Đo đo, áp lực riêng phần của CO, trong máu (PaCO,) giảm. Ngược lại, giảm thông khí phế nang sẽ làm tăng PaO2 trong máu động mạch hệ thống đo sự chênh lệch nóng độ giảm.
Sự chuyển hóa hiếu khí (aerobic metabolism) của glucose để sản xuất adenosine triphosphate (ATP) đóng vai trò tiêu thụ oxy và sản xuất co,. Quá trình chuyển hóa hiếu khí tạo ra khoảng 38 phần tử ATP cho mỗi phần tử glucose được chuyển hóa, mặc dù một số ATP được tiêu thụ trong quá trình này, tạo ra 30 ATP. Trong điều kiện cung cấp không đủ oxy cho tế bào, quá trình chuyển hóa kỵ khí (anaerobic metabolism) sẽ xảy ra cùng với việc chuyển đổi glucose thành pyruvate. Quá trình này kém hiệu quả hơn quá trình chuyển hóa hiếu khí và tạo ra hai phân tử ATP cho mỗi phân tử glucose được tiêu thụ. Pyruvate được chuyển hóa thành lactic acid, làm tăng kiêm thiếu (base debit) cua máu động mạch. Sự thiếu hụt kiểm được định nghĩa là sự khác biệt giữa dung tích bộ đệm thực tế (actual buyer capacity) và dung tích bộ đệm lý tưởng (ideal buffer capacity).
Một khái niệm quan trọng cần nắm rõ là: Mặc dù PaO2 và PaCO2 động mạch cung cấp thông tin quan trọng về sự tương hợp thông khí-tưới máu và sự đầy đủ của thông khí phế nang, song chúng không cung cấp thông tin trực tiếp về sự cung cấp đấy đủ oxy đến giường mạch máu hệ thống và các mô ngoại vi. Để ước tính xem lượng oxi đã được cung cấp đầy đủ đến các mô hay chưa, có thể đánh giá lượng máu trở lại từ hệ thống tuần hoàn về tim (máu tĩnh mạch trộn). Lấy mẫu máu từ tâm nhĩ phải bằng cách sử dụng một ống thông tĩnh mạch rốn với đầu của nó trong phần thấp của tâm nhĩ phải, gần giống với máu tĩnh mạch trộn. Theo dõi tình trạng oxygen hóa trong máu tĩnh mạch trộn rất hữu ích cho việc đánh giá mức độ đầy đủ của việc cung cấp và tiêu thụ oxy ở mô, đặc biệt trong oxygen hóa qua màng ngoài cơ thể (extracorporeal membrane oxygenation – ECMO) ở trẻ sơ sinh.
Vận chuyển oxy
Việc cung cấp oxy (oxygen delivery) đến các mô phụ thuộc vào hàm lượng oxy (oxygen content) trong máu cũng như cung lượng tim. Ở hầu hết trẻ sơ sinh, cung lượng tim dao động từ 120 đến 150 mL/kg/phút. Đánh giá khách quan tại giường về cung lượng tim không dễ dàng và cũng không chính xác. Phương pháp siêu âm tim chức năng (functional echocardiography) và phương pháp Doppler thường được sử dụng. Ngoài ra còn có các phương pháp thay thế khác như phân tích biểu đồ sóng mạch (pulse contour analysis), trở kháng sinh học (bioimpedance) hoặc kỹ thuật pha loãng chất chỉ thị (indicator dilution technique) (thường ở trẻ lớn hơn). Hàm lượng oxy trong máu động mạch (CO2) bao gồm oxi liên kết với hemoglobin (huyết sắc tổ) và oxy hòa tan tự do* Do đó, co2 = (HbO2) + (O2 hòa tan); trong đó, CO2 là hàm lượng oxy, HbO2 là oxy liên kết với hemoglobin và O2 hòa tan là oxy trong dung dịch.
Thông thường, chỉ có một lượng nhỏ oxy được hòa tan trong huyết tương, trừ phi PaO2 quá cao (ví dụ như tiếp xúc với FiO2 cao hoặc liệu pháp oxy cao áp). Ở 38°c, 0,3 mL oxy được hòa tan trong 100 mL huyết tương (0,003 mL/ dL/mmHg PaO2, và PaO2 giả định là 100 mmHg). Mối quan hệ này là tuyến tính trên toàn bộ phạm vi của PaO2 (xem Hình 10.1, đường cong B). Do lượng oxy hòa tan trong máu là tối thiểu, nên hàm lượng oxy trong máu thường xấp xỉ lượng oxy liên kết với hemoglobin (tức CaO2 ~ HbO2).
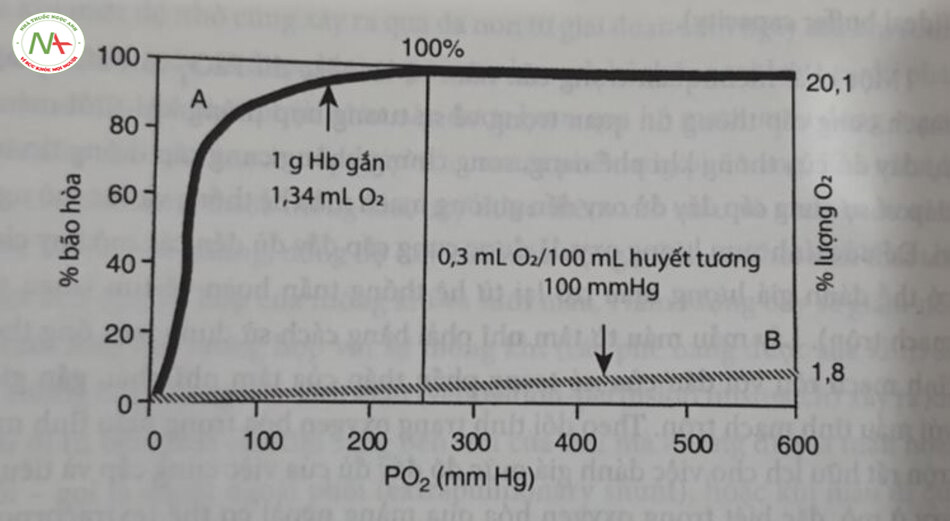
Do đó, lượng oxy liên kết với hemoglobin phụ thuộc vào nồng độ hemoglobin, khả năng vận chuyển oxy của hemoglobin và phần trăm độ bão hòa oxy của hemoglobin, được biểu thị bằng toán học la: CaO2 ~ (Hop = (Gam Hh) X (Dung tích O2) X (% bão hòa). Dung tích O2 biểu thị lượng oxy tối đa có thể được vận chuyển bởi một gam hemoglobin đã bão hòa hoàn toàn. Giá trị này là 1,34 mL 0, trên mỏi gam hemoglobin bão hòa 100%.
Giả sử mức hemoglobin là 15 g/100 mL máu và độ bão hòa của máu động mạch là 100%, đóng thời bỏ qua lượng nhỏ oxy hòa tan trong máu, thì hàm lượng oxy trong máu động mạch bình thường rơi vào khoảng cp = 15 X 1,34 X 1,0 = 20 mL O2 trên 100 mL máu động mạch hoặc 0,2 mL o, trên mồi mL máu. Sử dụng các già định tương tự, kèm thêm giả định rằng cung lượng tim bình thường ở trẻ sơ sinh nằm trong khoảng 120 mL/kg/phút, chúng ta sẽ tính được lượng o2 cỏ thế được cung cấp cho hệ tuần hoàn như sau:
Lượng O2 được cung cấp = (Cung lượng tim) X (CaO2) = (120 mL máu/kg/phút) X (0,2 mL O2/mL máu) = 24 mL 0,/kg/phút
Mức tiêu thụ oxy (oxygen consumption) ở trẻ sơ sinh rơi vào khoảng 6mL/ kg/phút trong những trường hợp bình thường. Do đó, cơ thể trích xuất 6 mL/ kg/phút oxy từ khoảng 24 mL/kg/phút, nhờ vậy mà có thể được cung cấp qua tuần hoàn hệ thống. Vậy nên, lượng oxy được cung cấp thường cao hơn lượng yêu cầu của các mò. Khi quá trình cung cấp oxy giảm xuống dưới ngưỡng mà tại đó, lượng oxy được cung cấp ít hơn lượng cần thiết, tình trạng thiếu oxy ở mỏ và quá trình chuyển hóa kị khí sẽ xảy ra. Thông thường, khoảng 25% lượng oxy được láy khỏi máu vào thời điểm nó trở về tim. Nhìn chung, độ bão hòa tĩnh mạch trộn (mixed venous saturation) từ 70% đến 75% thể hiện việc cung cấp oxy cho mô đầy đủ. Do vậy, độ bão hòa tĩnh mạch trộn từ 70% đến 75% được nhắm mục tiêu ở những bệnh nhân có thể theo dõi trực tiếp độ bão hòa oxy máu tĩnh mạch trộn (ví dụ như bệnh nhân đang điều trị ECMO).
Tìm hiểu về đường cong phân ly oxyhemoglobin
Mặc dù PaO2, đóng góp rất ít vào trong hàm lượng oxy của máu, song không thè’ không kể đến tám quan trọng sinh lý học của nó, vì chỉ có oxy hòa tan trong huyết tương mới đi vào tế bào. Oxy liên kết với hemoglobin không có sẵn cho các mỏ cho đến khi được giải phóng khỏi heme và hòa tan trong huyết tương. Đường cong phân ly oxyhemoglobin (oxyhemoglobin dissociation curve – ODC) dạng hình sigma mó tả phán trám hemoglobin bão hòa với oxy ở một PaO nhát đinh. Hemoglobin gần như bảo hòa hoàn toàn ở PaO2, nằm trong khoảng từ 80 đến 100 mmHg (Hình 10.1, đường cong A).
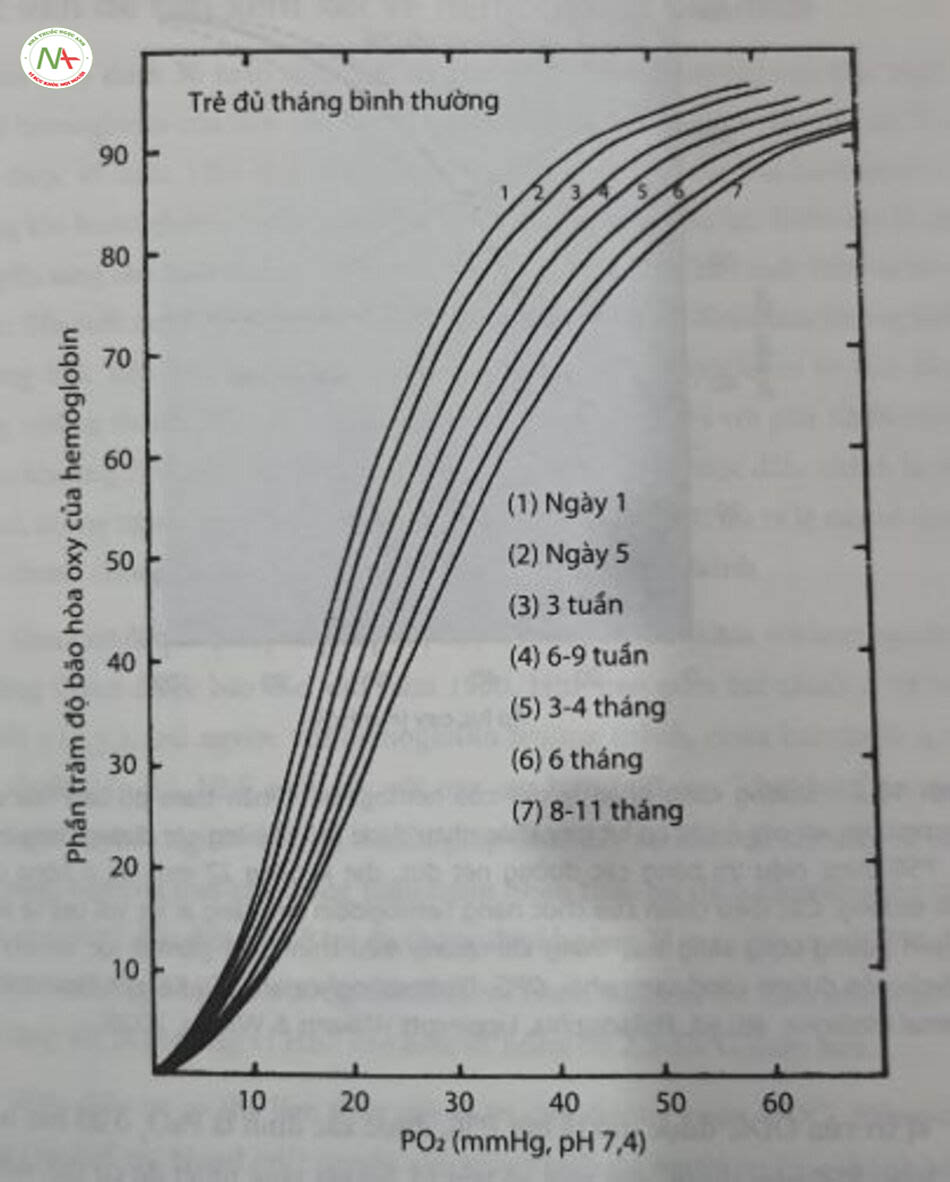
Tuy Nhiên,nóng độ diphosphoglycerate trong hồng cầu(diphosphoglycerate – DPG), tỷ lệ hemoglobin trưởng thành (adult hemoglobin – HbA) với hemoglobin bào thai (fetal hemoglobin – HbF), nhiệt độ, PaCO2, và nồng độ ion hydro (nhiễm toan) làm dịch chuyển vị trí của đường cong phân ly. Khi tuổi sau sinh tảng, nóng độ DPG và tỷ lệ hemoglobin A (HbA) tăng lên, làm
dịch chuyển đường cong sang phải (Hình 10.2). DPG ảnh hưởng nhiều đến liên kết oxy đối với hemoglobin trưởng thành hơn so với hemoglobin bào thai (HbF). Nhiệt độ, PaCO2, tảng và nồng độ ion hydro (nhiễm toan) củng dịch chuyển đường cong sang phải. Khi đường cong dịch chuyển sang phải, hemoglobin liên kết ít oxy hơn tại một PaO2, nhất định, nhờ đó giải phóng oxy dễ dàng hơn đến các mô (Hình 10.3). Thai nhi có nóng độ DPG trong hồng cái thấp hơn và nhiều HbF hơn nền đường cong phân ly bị dịch chuyển sang trái. Điều này giúp duy trì độ bão hòa oxy cao hơn ở mức PaO2 thấp hơn. Các tình trạng như nhiễm kiếm hoặc hạ thân nhiệt cũng sẽ làm dịch chuyển đường cong phân ly sang trái, dẫn đến độ bão hòa oxy của hemoglobin cao hơn đối với một PaO2, nhất định.
Hemoglobin liên kết với oxy trong phổi và vận chuyển oxy đến các mô. Sau đó, oxi được giải phóng khỏi hemoglobin và đi vào giai đoạn hòa tan trong huyết tương, được biểu thị bằng áp lực riêng phần của oxy (PaO2). Như đã lưu ý, hemoglobin làm tăng khả năng cung cấp oxy lên rất nhiều vì lượng oxy hòa tan trong máu là tối thiểu. Mối quan hệ giữa độ bão hòa oxy và PaO, được mô tả bằng ODC. Phấn dốc của đường cong chứng tỏ rằng độ bão hòa oxy thay đói nhanh chóng trong quá trình tải (loading) và dỡ tải (unloading) hemoglobin cùng với oxy. Điếu này phản ánh sự giãn ra của cấu trúc hemoglobin xảy ra với sự gắn kết với oxy. Khi oxy liên kết với heme, phân tử hemoglobin giãn ra, do đó làm lộ ra các phân từ heme xa hơn, tạo điều kiện cho quá trình liền két oxy tiếp theo. Quá trình giàn ra này được gọi là quá trình biến đổi dị lập thể (allosteric modification) và được điều chỉnh bởi hiệu ứng Haldane. Quá trình ngược lại xảy ra với quá trình dỡ tải oxy. Khi các vị trí liên kết oxy trèn phàn tù hemoglobin tiếp cận bảo hòa hoàn toàn với oxi, thì đường cong ODC phẲng. Do đó, ở độ bão hòa oxy cao hơn, rát khó dự đoán PaO,. Độ bão hòa oxy 100% có thế tương ứng với PaO2 nằm trong khoảng từ 80 đến hơn 300 mmHg.
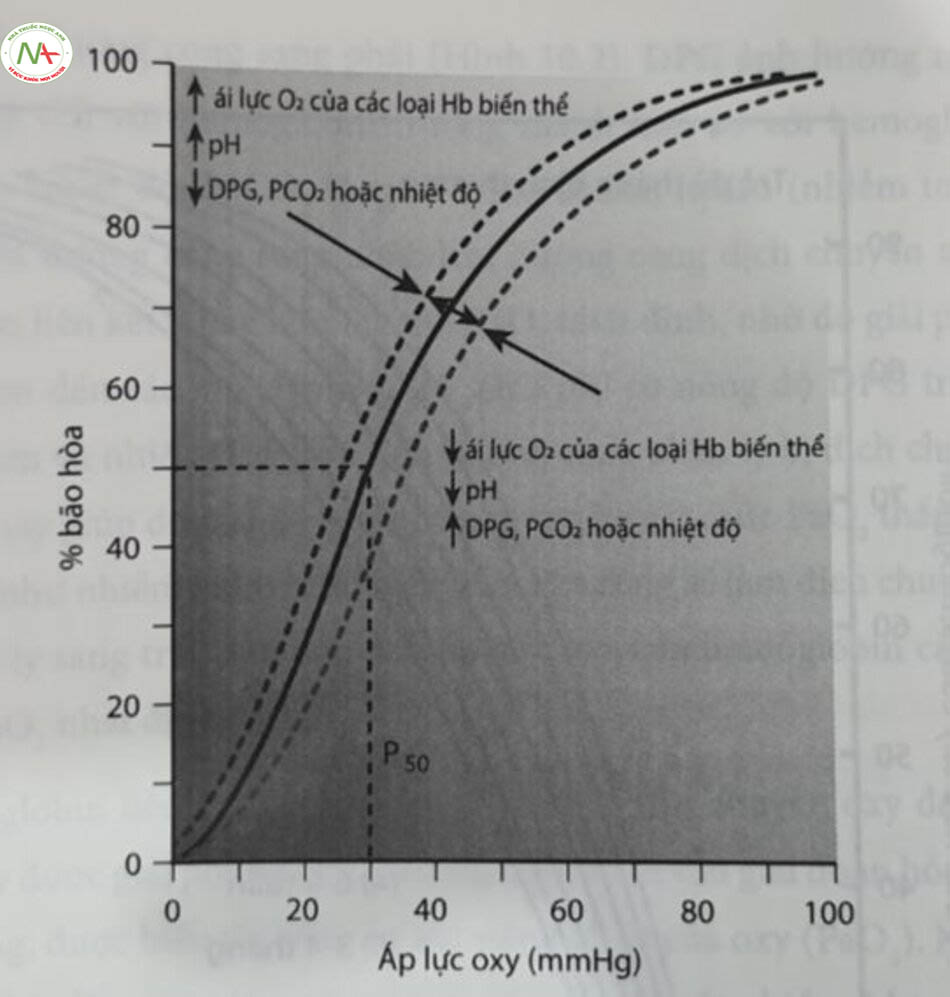
Vị trí của ODC được mô tả bởi P50, được xác định là PaO2 ở độ bão hòa oxy 50%. P50 phụ thuộc vào một số yếu tố. Sự gia tăng nhiệt độ cơ thể, nóng độ ion hydro (giảm pH), PaCO2,2,3-DPG, hoặc nồng độ hemoglobin ở người trưởng thành làm dịch chuyển DOC sang bên phải một cách độc lập. Ngược lại, sự giảm xuống của bất kỳ yếu tổ nào trong số này sẽ làm dịch chuyển đường cong sang trái. Do đó, PaO2 đối với bất kỳ độ bão hòa oxy nhất định nào sẽ thay đổi trong mỗi cá nhân khi các yếu tố này thay đổi. Ví dụ, khi bị sót, sự dịch chuyển sang phải của đường cong dẫn đến PaO2 cao hơn cho giá trị P50. Cà nồng độ hemoglobin ở người trưởng thành và nồng độ 2,3-DPG đấu tăng trong thời kỳ sơ sinh, khiến ODC bị dịch chuyển sang phải.
Các vấn đề cần xem xét về hemoglobin bào thai
Trẻ sơ sinh dưới 30 tuần tuổi thai có gần 100% HbF (hemoglobin bào thai). Tỷ lệ hemoglobin của thai nhi so với người trưởng thành giảm dần; do đó, khi thai được 40 tấn, HbF chiếm khoảng 70% trong tổng số các loại hemoglobin, trong khi hemoglobin trưởng thành (HbA) chiếm 30% còn lại. Điểu này là do chuyển sang sản xuất hemoglobin trưởng thành và không sản xuất HF có liên quan đến tuổi sau kỳ kinh cuối thay vì tuổi theo thời gian. Sinh non không ảnh hưởng trực tiếp đến quá trình chuyển đổi sản xuất hemoglobin từ bào thai sang trưởng thành. Một đứa trẻ được sinh ra ở tuần thứ 24 với gần 100% HbF sẽ có khoảng 70% HbF khi được 16 tuần tuổi (tuổi thai được điều chỉnh là 40 tuần), tương tự với trẻ được sinh ra ở tuổi thai 40 tuần, mặc dù tỷ lệ này sẽ thay đổi nhanh chóng hơn sau khi truyền máu người trưởng thành.
Quan sát đấu tiên cho thấy HbF có đặc tính liên kết oxy khác với hemoglobin trưởng thành được báo cáo vào năm 1930. HbF bao gồm hai chuỗi a và hai chuỗi Ya^yp, trái ngược với hemoglobin trưởng thành, chứa hai chuỗi a và hai chuỗi p (a2p2). HbF có ái lực với oxy cao hơn (giữ oxy “chặt hơn”) so với hemoglobin của người trưởng thành, giúp thúc đẩy sự khuếch tán oxy từ bên mẹ sang bên của thai nhi trong tuần hoàn nhau thai. Sự dịch chuyển sang trái này của ODC dẫn đến P50 ở trẻ đủ tháng đạt khoảng 21 mmHg so với P50 đạt mức 27mmHg ở người trưởng thành (xem Hình 10.2). Ở trẻ sinh non, P50 có thể thấp tới 18 mm Hg vì HbF cao hơn và nóng độ 2,3-DPG thấp hơn.
Việc điều trị có thể làm thay đổi vị trí của đường cong ODC. Hổng cáu lắng (packed red blood cell) truyền cho trẻ sơ sinh do người trưởng thành hiến tặng và vẽ cơ bản chứa 100% hemoglobin người trưởng thành. Do đó, việc truyền máu sẽ dịch chuyển DOC sang phải. Trẻ sinh non có nồng độ Hb cao hơn và cũng có nhiều khả năng phải truyền máu hơn. Truyền máu ở trẻ sinh non gây ra sự thay đổi ODC lớn hơn so với trẻ đủ tháng. Khi đánh giá ảnh hưởng của việc truyền máu đối với ODC, cần xem xét các yếu tố quan trọng khác như nống độ 2,3-DPG, nhiệt độ và loại chất bảo quản được sử dụng.
Dựa trên vị trí của ODC, độ bão hòa oxy đối với một PaO, nhất định có thể khá khác nhau. Trong thực tế, các bác sĩ lâm sàng nhắm mục tiêu vào phạm vi bão hòa oxy cụ thể để tránh nguy cơ tăng oxy máu và giảm oxy máu. Mục tiêu bão hòa oxy thường không bị thay đổi khi vị trí của ODC thay đổi sau truyền máu, dẫn đến PaO2 cao hơn đối với một độ bão hòa oxy nhất định. Điểu này là phù hợp, bởi vì độ bão hòa oxy hemoglobin chứ không phải PaO2 gây ảnh hưởng trực tiếp đến hàm lượng oxy trong máu và phân phối cho mô.
Máy phân tích khí máu hiện đại có hai cài đặt trước cho HbF: 0% và 80%. Mặc dù không chính xác, xong việc sử dụng giá trị đặt trước HbF 80% sẽ phù hợp hơn cho xét nghiệm khí máu ở trẻ sơ sinh. Các lỗi khi báo cáo các giá trị khí máu chưa điều chỉnh có thể không phải lúc nào cũng rõ ràng đối với bác sĩ lâm sàng. Kết quả khí máu có độ bão hòa oxy 100% được hiệu chỉnh cho HbF tương ứng với độ bão hòa oxy chưa điều chỉnh 105%. Tuy nhiên, do máy khí máu không báo độ bão hòa oxy lớn hơn 100% nên bác sĩ lâm sàng sẽ không thấy rõ điều này.
Giảm oxy máu và thiếu oxy mô
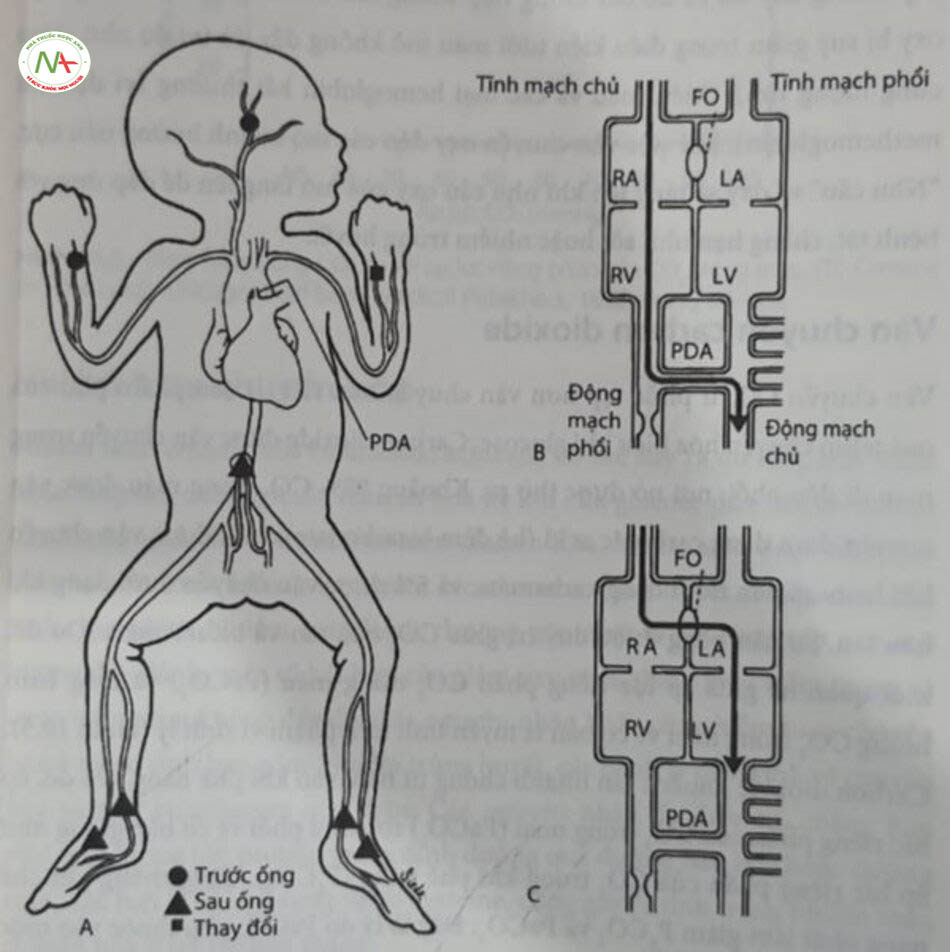
Mặc dù giảm oxy máu (hypoxia) và thiếu oxy mô (hypoxia) thường xảy ra cùng nhau, nhưng chúng không đồng nghĩa với nhau. Giảm oxy máu thường được định nghĩa là hàm lượng oxy trong máu động mạch thấp, trong khi tình trạng thiếu oxy mô liên quan đến việc cung cấp oxy đến mô không đầy đủ. Giảm oxy máu xảy ra trong mọi tình huống mà tại đó, máu đi vào tuần hoàn hệ thống nhưng lại không tưới máu cho các phế nang được thông khí đầy đủ (giảm sự tương hợp thông khí-tưới máu). Máu có thể nối tắt (bypass) qua các phế nang được thông khí đầy đủ bằng shunt ngoài phối và/hoặc trong phổi. Với tầng áp phổi dai dẳng ở trẻ sơ sinh (persistent pulmonary hypertension of the newborn – PPHN) hoặc bệnh tim bẩm sinh tím (cyanotic congenital heart disease), máu đi vào động mạch chủ mà không đi qua tuấn hoàn phổi (shunt ngoài phổi). Trong PPHN, một shunt từ phải sang trái qua ống động mạch (ductus arteriosus) thường có thể được phát hiện bằng cách so sánh PaO, hoặc độ bão hòa oxy của máu trước và sau ống động mạch (Hình 10.4). Nếu độ bão hòa của máu trước ống động mạch cao hơn đáng kể’ so với độ bão hòa của máu sau ống động mạch (chênh lệch > 5%-10%) sẻ cho thấy một shunt từ phải sang trái đáng kể vé mặt lâm sàng. Tuy nhiên, độ bão hòa trước và sau ống động mạch bằng nhau không loại trừ tăng áp động mạch phổi. Shunt từ phải sang
trái có thể xảy ra qua lỗ bầu dục (foramen ovale) mà không có bất kỳ sự khác biệt nào trước và sau ống động mạch. Tình trạng giảm oxy máu liên quan đến các bệnh phổi đặc trưng bởi xẹp phổi (ví dụ như hội chứng suy hô hấp, viêm phổi) chủ yếu là do shunt trong phổi. Bất cứ khi nào phế nang được thông kty không đầy đủ, máu đến các phế nang đó có thể không được bão hòa hoàn toàn. Khi tình trạng xẹp phổi ngày càng nặng hơn, tình trạng shunt trong phổi và giảm oxy máu sau đó sẽ tăng lên.
Tình trạng thiếu oxy ở mô xảy ra khi lượng oxy cung cấp đến các mô giảm xuống dưới ngưỡng tiêu thụ oxy tới hạn (critical threshold of oxygen consumption). Tình trạng thiếu oxy có thể xảy ra mặc dù có đủ PaO2. Sẽ rất hữu ích khi khái niệm hóa tình trạng thiếu oxy dưới dạng mất cân bằng trong cung cấp, phân phối và nhu cầu oxy. Giảm “nguồn cung cấp” được thấy ở độ cao lớn do áp lực riêng phần của oxy trong khí quyển thấp hơn, với nỗ lực hô hấp không đầy đủ và do bất tương hợp thông khí-tưới máu. Việc “cung cấp” oxy bị suy giảm trong điều kiện tưới máu mô không đầy đủ (ví dụ như giảm cung lượng tim), thiếu máu và các loại hemoglobin bất thường (ví dụ như methemoglobin), khi việc vận chuyển oxy đến các mô bị ảnh hưởng tiêu cực. “Nhu cầu” về oxy sẽ tăng lên khi nhu cầu oxy của mô tăng lên để đáp ứng với bệnh tật, chẳng hạn như sốt hoặc nhiễm trùng huyết.
Vận chuyển carbon dioxide
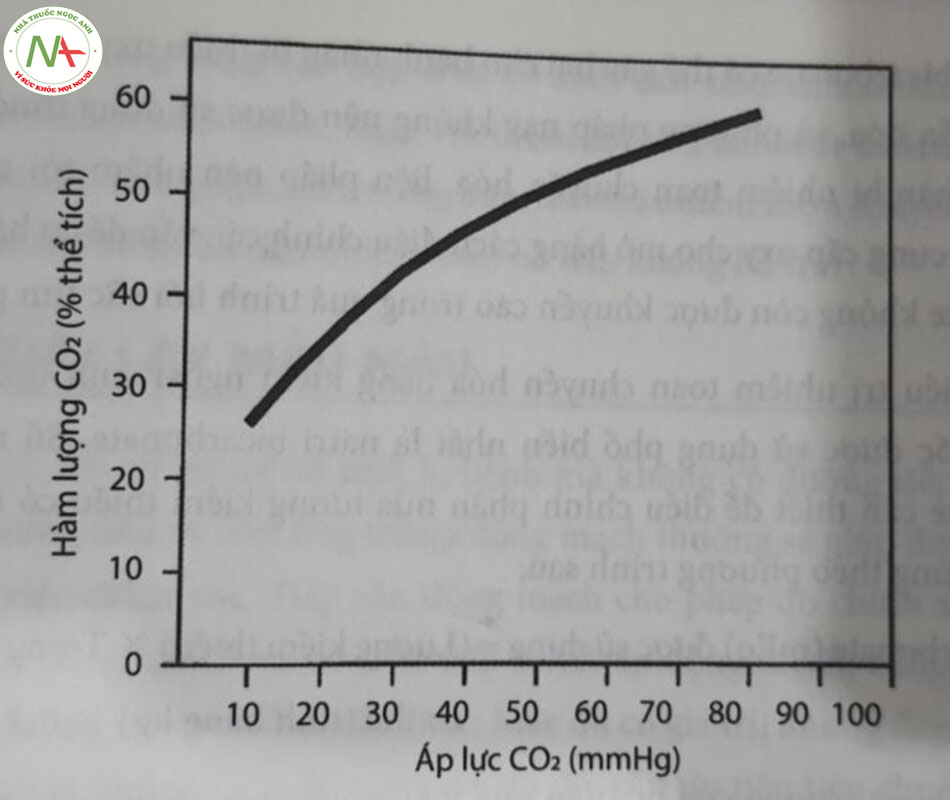
Vận chuyển CO2 ít phức tạp hơn vận chuyển oxy. CO2 là sản phẩm phụ của quá trình chuyển hóa hiếu khí glucose. Carbon dioxide được vận chuyển trong máu đi đến phổi, nơi nó được thở ra. Khoảng 85% CO2 trong máu được vận chuyển dưới dạng carbonic acid (hệ đệm bicarbonat), 10% được vận chuyển bởi hemoglobin dưới dạng carbamate, và 5% được vận chuyển dưới dạng khí hòa tan. Sự cân bằng được duy trì giữa CO2 hòa tan và bicarbonate. Do đó, mối quan hệ giữa áp lực riêng phần CO2 trong máu (PaCO,) và tổng hàm lượng co2 trong máu vê’ cơ bản là tuyến tính trên phạm vi sinh lý (Hình 10.5). Carbon dioxide khuếch tán nhanh chóng từ máu vào khí phế nang. Do đó, áp lực riêng phần của CO2 trong máu (PaC CỌ rời khỏi phổi về cơ bản giống như áp lực riêng phần của CO2 trong khí phế nang (PACO2). Tăng thông khí phế nang phút làm giảm PAO2 và PaCO2. Đây là lý do PaCO2 phụ thuộc vào mức độ thông khí phế nang.
Nhiễm toan chuyển hóa
Nhiễm toan chuyển hóa (metabolic acidosis) có thế xảy ra do tăng mất kiếm hoặc tàng sản xuất axit. Sự chuyên hóa kỵ khí cùa glucose dẫn đến sự tích tụ của lactic acid, dân đến nhiễm toan chuyển hóa. Lactic acid được đệm bởi bicarbonate (một kiếm), làm giảm bicarbonate trong huyết thanh, dẫn đến thiếu hụt kiếm. Nhiễm toan lactic thường gặp nhất là do cung cấp oxy mò không dãy đủ do một số kết hợp của giảm oxy máu, thiếu máu trầm trọng và cung lượng tim không đấy đù. Các nguyên nhân khác của nhiễm toan chuyển hóa ở trẻ sơ sinh bao gom: Nhiễm trùng huyết, các bệnh lý bẩm sinh vé chuyển hóa và mất bicarbonate qua thận. Các nguyên nhân do điều trị, chẳng hạn như một lượng lớn protein trong dinh dưỡng qua đường tiêu hóa hoặc đường ruột, đặc biệt là khi bổ sung thêm cysteine, cũng gây ra tình trạng nhiễm toan chuyển hóa ở trẻ rất non tháng.
Ở hầu hết trẻ sơ sinh khỏe mạnh, lượng kiếm thiếu (base debit) thường từ +3 đến -1. Mặc dù việc cung cấp kiếm cho trẻ bị nhiễm toan chuyển hóa do mất bicarbonat ở thận có thể hợp lý, nhưng có bằng chứng cho thấy rằng việc dùng bicarbonate có thể gây hại cho bệnh nhân bị thiếu oxy mô và nhiễm toan chuyển hóa, và phương pháp này không nên được SỬ dụng thường quy. Ờ bệnh nhân bị nhiễm toan chuyển hóa, liệu pháp nén nhắm tới mục tiêu khôi phục cung cấp oxy cho mô bằng cách điều chỉnh các vấn đề cơ bản. Natri bicarbonate không còn được khuyến cáo trong quá trình hồi sức tim phổi.
Khi điều trị nhiễm toan chuyển hóa bằng kiềm ngoại sinh (exogenous base), thuốc được sử dụng phổ biến nhất là natri bicarbonate. Số mEq của bicarbonate cần thiết để điều chỉnh phân nửa lượng kiếm thiếu có thể được tính gần đúng theo phương trình sau:
Bicarbonate (mEq) được sử dụng = (Lượng kiềm thiếu) X Trọng lượng cơ thể (tính bằng kg) X 0,3
Do tính ưu trương của nó, nên pha loãng natri bicarbonate (1 mEq/mL) với nước vô trùng theo tỉ lệ 1:1 và dùng từ từ, tốt nhất là trong 30 đến 60 phút. Acetate có thế được bổ sung vào đường tiêm thay cho chloride để điều trị nhiễm toan chuyển hóa. Nên cẩn thận khi sử dụng bicarbonate và acetate ở trẻ sơ sinh bị nhiễm toan chuyển hóa và hô hấp kết hợp, vì CO2 là sản phầm phụ của quá trình chuyển hóa bicarbonate và acetate. Do đó, PaCO2 sẽ tăng, trừ phi thông khí phút cũng tăng. Vì vậy, nên hạn chế sử dụng kiềm ngoại sinh trong một số trường hợp mất bicarbonate ở ống thận hoặc một số nguyên nhân hiếm gặp của nhiễm toan lactic bẩm sinh.
Nhiễm kiềm chuyển hóa
Nguyên nhân phổ biến nhất của nhiễm kiềm chuyển hóa (metabolic alkalosis) tương đối ở trẻ sơ sinh là do nhiễm toan hô hấp được bù trừ mãn tính. Nếu tình trạng nhiễm toan hô hấp có bù trừ được điều chỉnh bằng cách giảm nhanh PaCO, sẽ dẫn đến tình trạng nhiễm kiềm chuyển hóa tuyệt đối. Các nguyên nhân khác gây nhiễm kiềm chuyển hóa ở trẻ sơ sinh bao gồm: Giảm clo máu do điều trị lợi tiểu mãn tính, hoặc mất bài tiết dịch vị (tiêu chảy hoặc nôn thường xuyên) và sử dụng quá nhiều acetate trong dinh dưỡng qua đường tĩnh mạch. Nhiễm kiềm chuyển hóa nhẹ cũng có thể xảy ra sau truyền máu khi chuyển hóa citrat trong thuốc chống đông máu. Hiếm khi cần điều chỉnh nhiễm kiềm chuyển hóa bằng các hợp chất có tính axit như ammonium chloride hay arginine hydrochloride, hoặc với thuốc lợi tiểu làm mất bicarbonate như acetazolamid. Trong hầu hết trường hợp, điều trị nhiễm kiềm chuyển hóa bằng các thuốc này đều dẫn đến nhiễm toan hô hấp không bù trừ.
Kỹ thuật lấy mẫu máu
Mặc dù có thể xử trí trẻ sơ sinh bị bệnh mà không có đường tiếp cận động mạch, nhưng nếu có một ống thông động mạch thường sẽ giúp đơn giản hóa đáng kể việc chăm sóc. Tiếp cận động mạch cho phép đo chính xác các khí trong máu động mạch và đo trực tiếp huyết áp động mạch, cũng như cung cấp một đường lấy các mẫu máu khác. Mặc dù có giá trị, nhưng ống thông rốn không phải là không tiềm ẩn nguy cơ; do đó, cần ưu tiên tiêu chuẩn hóa việc sử dụng chúng.
Ống thông động mạch rốn
Ống thông động mạch rốn (umbilical artery catheter – ỨC) là con đường ưu tiên để tiếp cận động mạch trong hầu hết các NICK. WAC thường có thể được đặt nhanh chóng và dễ dàng ngay sau khi sinh, với nguy cơ biến chứng không lớn. Các động mạch rốn có thể tiếp cận dễ dàng trong những ngày đầu tiên của cuộc đời. Mặc dù khả năng đặt thành công ít hơn đáng kể sau một vài ngày, nhưng vẫn có thể đặt thông động mạch rốn cho đến 2 tuần tuổi. Các trị số khí máu thực hiện trên máu được lấy từ ống thông động mạch rốn phản ánh kết quả máu sau ống động mạch (postductal blood).
Ống thông rốn phải đảm bảo độ mềm dẻo, không bị gập, cản quang, trong suốt, không gây thuyên tắc và phải có lỗ cuối nhưng không có lỗ bên. Có hai kích thước ống thông phổ biến là 3,5 F và 5,0 F. Hiện không có sẵn nhiêu dữ liệu đề cập đến giá trị tương đối của hai loại kích thước ống thông này. Một số bác sĩ lâm sàng cảm thấy nên sử dụng ống thông lớn hơn đế giảm thiểu sự hình thành huyết khối, làm cho nó ít bị “đông máu” hơn. Những người khác lại cảm thấy óng thông nhỏ hơn sẽ tốt hơn, vì nó giúp giảm thiểu các thay đổi của lưu lượng máu động mạch chủ. Quyết định về kích thước ống thông nên sử dụng
thường dựa trên sở thích cá nhân và kích thước bệnh nhân. Cách tiếp cận thông thường của chúng tôi là sử dụng ống thông 3,5 F ở trẻ sơ sinh nặng dưới 1.500 g hoặc 2.000 g và ống thông 5,0 F ờ trẻ nặng hơn 1.500 g hoặc 2.000 g. Chúng tôi chỉ sử dụng ổng thống một lòng khi thông động mạch rốn.
Quy trình đặt ống thông mạch máu rốn có trong video của Anderson và cộng sự trên New England Journal of Medicine (tạm dịch: Tạp chí Y học New England Các video bổ sung mô tả phương pháp này cũng được đăng tải thông qua Media Link, the American Academy of Pediatrics Online Learning Center (https://vimeo.com/57453941).
Trước khi đặt, ống thông được gắn vào một khóa ba chia và ống tiêm có chứa dung dịch nước muối sinh lý đã được heparin hóa, sau đó được dùng để loại bỏ bọt khí. Khi ống thông đã được đưa vào và hoạt động bình thường, phải gắn khóa ba chia vào dụng cụ truyền liên tục dịch truyền đã được heparin hóa và vào đầu dò áp lực. Cẩn cẩn thận khi siết chặt các kết nối khóa ba chia để giảm thiểu khả năng ngắt kết nối ngẫu nhiên.
Ống thông được đưa vào trong khi trẻ sơ sinh được duy trì trong môi trường nhiệt độ trung tính với các dấu hiệu sinh tồn được theo dõi. Chan cua trẻ sơ sinh phải được cố định một cách lỏng lẻo và nếu bạn nới lỏng cánh tay thì cũng có thể hữu ích. UAC được đưa vào trong điếu kiện vô trùng sau khi cuống rốn được làm sạch bằng povidone-iodine hoặc chlorhexidine. Nên loại bỏ thuốc sát trùng ngay sau khi đặt để giảm tổn thương da. Ngoài ra, có thể dẫn đến suy giáp do điều trị nếu iodine vẫn còn trên da. Một sợi chỉ vô trùng buộc cuống rốn được vòng xung quanh phần dưới của cuống rốn và cột chờ bằng một nút duy nhất. Sợi chỉ này có thể thắt chặt lại nếu chảy máu khi cắt cuống rốn, hoặc nới lỏng nếu nó ngăn cản ống thông luồn vào. Tiếp theo, cắt cuống rốn cách da khoảng 0.5 đến 1,0 cm. Gốc rốn dài hơn làm cho việc đặt ống thông khó khăn hơn. Cần cắt cuống rốn bằng dao mổ trong một lần cắt, chứ không nên cửa đi cửa lại. Điều này cho phép các động mạch rốn nhô ra từ mặt cắt cuống rốn. Có thể dễ dàng xác định được hai động mạch có thành dày và tĩnh mạch đơn, lớn hơn, có thành mỏng (thường ở vị trí cao hơn 12 giờ).
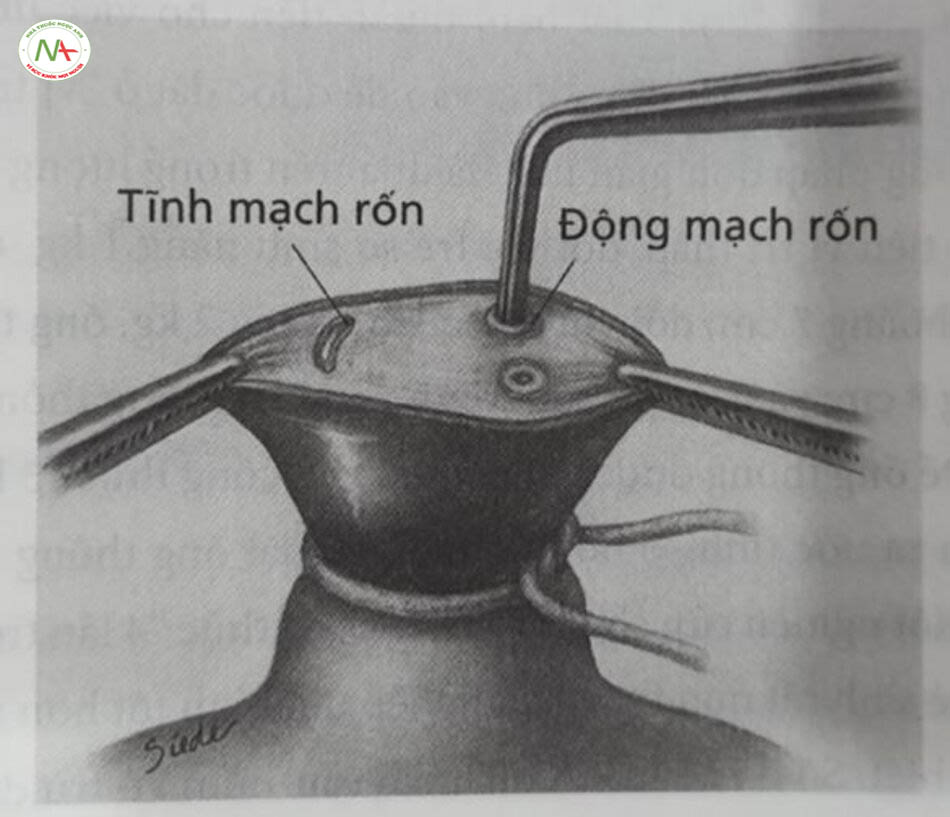
Một trong những bước quan trọng hơn khi đặt WAP là làm giãn lòng động mạch. Mục tiêu của việc làm giãn là mờ lòng ổng đủ để cho phép ống thông đi qua trơn tru mà không làm rách nội mạc và tạo ra “lòng ổng giả”. Một khi đã tạo ra một lòng ống giả, ỨC sẽ hiếm khi đưa được vào lại lòng ống thật, dẫn đến việc đặt không thành công. Có thể bắt đầu làm giãn mạch máu bằng việc đặt một đẩu của một chiếc kẹp nhỏ vào lòng mạch. Nên tránh loại đầu kẹp có răng. Xoay nhẹ nhàng sẽ giúp mạch giãn ra cho đến khi có thể đặt cả hai đẩu của kẹp vào lòng mạch (Hình 10.6). Sau khi đặt cả hai đầu kẹp, có thể xoay chúng từ từ và dang rộng trong khi rút ra để làm giãn dẩn mạch máu đến cờ ổng thông. Khi lòng mạch giãn ra, đưa kẹp vào sâu thêm với mục tiêu giần ra ít nhất từ 5 đến 8 mm. Khi mạch máu đã được giãn ra đầy đủ, có thể đưa ống thông vào. Ống thông sẽ dễ dàng luôn vào hơn nếu động mạch rốn được giữ ổn định bằng một hoặc hai chiếc kẹp nhỏ, cong. Thông thường, ống thông đi qua với ít lực cản. Nếu ống thông gặp sức cản đáng kể, điều đó thường có nghĩa là ống thông đã bị bóc tách quả lớp nội mạc và đa tạo ra một lòng ống già. Khi xảy ra tình trạng này, nên rút ống thông ra. Đẩy mạnh ổng thông có thể’ dẫn đến tổn thương mạch và/hoặc thủng phúc mạc hoặc bàng quang.
Hiếm khi ống thông đi xuống dưới đến động mạch chậu ngoài, động mạch này trở thành động mạch đùi tưới máu cho chi dưới thay vì đi vào động mạch chủ. Nếu điều này xảy ra, một ống thông thứ hai đôi khi có thể được đưa vào cùng một động mạch rốn mà không cần rút ống thông thứ nhất. Với ống thông thứ nhất được đặt trong động mạch chậu ngoài, ống thông thứ hai thường được dẫn vào động mạch chủ xuống.
Một khi ổng thông đi vào động mạch chủ, nó phải được đưa vào “vị trí cao” hoặc “vị trí thấp”. Những vị trí này tránh đặt đầu ống thông tiếp giáp với góc của động mạch thận, mạc treo ruột hoặc động mạch thân tạng. Nếu chọn “vị trí thấp”, đẩu ống thòng phải nằm giữa mức của đốt sống thắt lưng thứ ba và thứ tư (L3-L4) trên phim chụp X-quang, an toàn bên dưới động mạch thận và động mạch mạc treo. Nếu “vị trí cao” được chọn, đầu ổng thông phải nằm giữa đốt sống ngực thứ sáu và thứ mười (T6-T10, tối ưu là T8), phía trên điểm xuất phát của động mạch thân tạng. Mặc dù cả hai vị trí đều được sử dụng phổ biến, sống một phân tích tổng hợp các thử nghiệm ngẫu nhiên so sánh vị trí đặt ống thông thấp và cao cho thấy tỷ lệ biến chứng mạch máu ngoại vi cao hơn ở trẻ được đặt ống thông ở “vị trí thấp”. Tuy nhiên, hầu hết các biến chứng này đểu nhẹ.
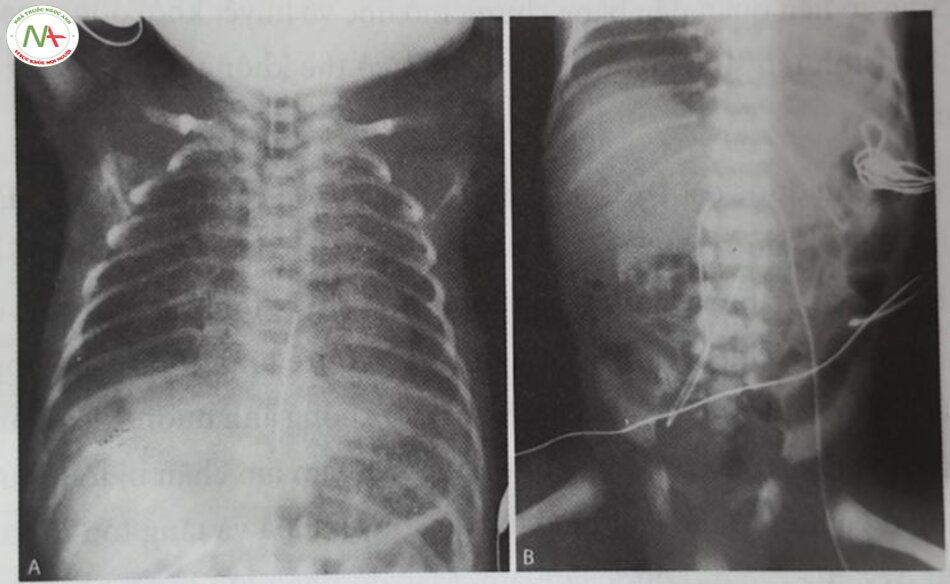
Một số biểu đồ đã được xuất bản, thuận tiện cho việc ước tính khoảng cách mà một ống thông phải được đưa vào để được đặt ở vị trí thấp sao cho chính xác. Phương pháp đơn giản nhất là dựa trên trọng lượng của trẻ sơ sinh. Khi nhắm mục tiêu vị trí thấp, đối với trẻ sơ sinh nặng 1kg, ống thông phải được đưa vào khoảng 7cm; đối với trẻ sơ sinh nặng 2 kg, ống thông nên được đưa vào khoảng 8cm; và đối với trẻ sơ sinh nặng 3kg, ống thông nên được đặt khoảng 9 cm. Để ống thông được đặt ở vị trí cao, công thức “3 lần trọng lượng cộng với 9” đưa ra ước tính sơ bộ về’ chiều dài đặt ống thông cần thiết, được tính bằng cm. Một nghiên cứu cho thấy rằng công thức “4 lần trọng lượng cộng với 7” đối với trẻ sinh rất non tháng cho phép ước tính tốt hơn về chiều dài đặt ống thông cần thiết. Số đo bể mặt (chiều dài rốn-núm vú trừ đi 1 cm cộng với hai lần khoảng cách từ rốn đến khớp mu), hoặc đồ thị dựa trên chiếu dài đến rốn có thể’ được sử dụng để ước tính chiều dài đặt ống chính xác. Tuy nhiên, các thử nghiệm lâm sàng ngẫu nhiên cho thấy việc sử dụng cân nặng của trẻ lúc sinh để ước tính độ sâu của chiều dài đặt ống thông là giải pháp ưu việt hơn. Bất kể dùng phương pháp nào để tính độ sâu của chiều dài đặt ống thông, thì chiều dài của gốc rốn đểu phải được thêm vào độ sâu ước tính của chiều dài đặt ống thông. Sau khi đặt, nên xác định vị trí của ống thông bằng X-quang (Hình 10.7), vì các phương pháp này không phải lúc nào cũng chính xác. Cũng có tỉ£ nẵng siêu âm để kiểm tra vị trí đầu ống thông. Khi đã định vị chính xác, phải giữ chặt ống thông bằng chỉ khâu và băng. Nói chung, một chỉ khâu lụa 3-0 được buộc vào cuống rốn, tạo thành một “mỏ neo”, và sau đó được buộc vào ống thông. Đặc biệt phải chú ý không làm thủng ống thông bằng kim khâu. Sau đó, ống thông có thể được giữ chặt hơn nữa bằng một cầu băng.
Bộc lộ dưới cuống rốn
Nếu các nỗ lực thông cả động mạch rốn lẫn động mạch ngoại vi không thành công và bệnh nhân không thể được xử trí đầy đủ nếu thiếu ống thông động Ỉ lạch, thì đôi khi có thể đặt lại các động mạch rốn bằng phương pháp bộc lộ với cuống rốn (subumbilical countdown). Đây là một thủ thuật phẫu thuật và chỉ nên được thực hiện bởi một bác sĩ đã có kinh nghiệm về’ kỹ thuật này trước đó, vì một số biến chứng có thể xảy ra, bao gồm xâm nhập vào khoang phúc mạc và thoát vị dưới ổ bụng.
Các biến chứng của đặt ống thông động mạch rốn
Mặc dù đặt ống thông động mạch rốn là biện pháp an toàn và được dung nạp tốt ở hầu hết bệnh nhân, sống cũng cần nhớ rằng không phải là không có nguy cơ. Các biến chứng liên quan đến ống thông động mạch rốn bao gồm: Tổn thương mạch máu, các biến chứng liên quan đến sai vị trí, nhiễm trùng, chảy máu và các tai nạn liên quan đến ống thông (vô tình tuột, đứt, v.v…). Hiếm khi việc đặt ống thông có liên quan đến các biến chứng huyết khối nghiêm trọng, bao gồm hoại thư và hoại tử mông hoặc chân. Các nghiên cứu cho thấy ỨC trong 5 ngày đầu tiên không liên quan đến nguy cơ huyết khối cao. Tuy nhiên, bằng chứng trên động vật cho thầy rằng: Ngay cả việc sử dụng trong thời gian ngắn cũng có liên quan đến bằng chứng mô học về huyết khối động mạch chủ và sự tăng sinh tân sinh của thành mạch và có thể không phải là bằng chứng lâm sàng.
Trẻ sơ sinh được đặt ƯƠC đôi khi sẽ có các ngón chân bị chuyên mau sam hoặc tím, có lẽ là do vi thuyên tắc hoặc co thắt mạch. Làm ấm chân đời bên có thể khiến mạch giãn trở lại và tăng tưới máu ở chi bị tổn thương. Mặc dù đây là một thực tế phổ biến, sống một nghiên cứu ở trẻ bình thường không bị co thắt mạch cho thấy rằng sự làm ấm lên tại chỗ không ảnh hưởng đến lưu lượng máu ngoại vi đến gót chân đối bên. Không nên làm ấm chân bị tổn thương vì khả năng điếu này có thể làm tăng tốc độ chuyển hóa và tăng tổn thương mô do thiếu oxy của các mô được làm ấm. Mặc dù phần lớn bệnh nhân có ngón chân đen được tưới máu đầy đủ và không bị ảnh hưởng nặng nề, nhưng vẫn có nguy cơ bị tổn thương mạch máu nghiêm trọng đi kèm với hoại từ và mất mô. Nếu ngón chân vẫn còn đen, hoặc trầm trọng hơn với đồ đẩy mao mạch kém, hoặc lan rộng ra bàn chân hay cẳng chân nhiều hơn, thì nên rút ổng thông. Trong một số trường hợp hiếm hoi, trẻ sơ sinh bị ỨC sẽ bị trắng bệch ở bàn chân hoặc một phần của chân, thể hiện lượng máu động mạch bị tổn thương nghiêm trọng, do đó cần phải rút ống thông ngay lập tức.
Nêu sự tưới máu đến chi không được cải thiện ngay sau khi rút ống thông, điếu này có thể cho thấy biến chứng huyết khối nghiêm trọng. Đánh giá thường bao gồm một số kết hợp của siêu âm hoặc đánh giá Doppler, hoặc có thể’ chụp mạch máu. Cả thuốc giãn mạch toàn thân lẳn thuốc giãn mạch tại chỗ đã được mở tài là có một số hiệu quả trong tình huống này, nhưng thiếu bằng chứng xác thực về hiệu quả. Khi xác định một cục máu đông đáng ké, thuốc tiêu huyết khối với chất kích hoạt plasminogen mô, được truyền trực tiếp vào mạch bị ảnh hưởng hoặc hệ thống, đã được thử nghiệm. Phải cân nhắc những lợi ích tiềm năng của liệu pháp làm tan huyết khối so với các nguy cơ mà liệu pháp này đem lại, đặc biệt là ở trẻ sơ sinh bị xuất huyết nội sọ có khả năng xảy ra lan rộng thêm. Không may là có rất ít tài liệu bàn về cách tiếp cận tối ưu cho trẻ sơ sinh bị tắc nghẽn mạch máu nặng.
Tỷ lệ nhiễm trùng liên quan đến WACC có vẻ như thấp hơn tỷ lệ nhiễm trùng liên quan đến ống thông tĩnh mạch trung tâm. Tuy nhiên, như với tất cả các ống thông trung tâm, phải cẩn thận tỉ mỉ để duy trì tình trạng vô trùng trong quá trình đặt ống thông và trong quá trình tiếp cận các ống thông trung tâm sau đó. Chúng tôi khuyến cáo hạn chế tối đa việc “ngắt kết nối” đường truyền
Tỷ lệ nhiễm trùng liên quan đến UAC có vẻ như thấp hơn tỷ lệ nhiễm trùng liên quan đến ống thông tĩnh mạch trung tâm. Tuy nhiên, như với tất cả các ống thông trung tâm, phải cẩn thận tỉ mỉ để duy trì tình trạng vô trùng trong quá trình đặt ống thông và trong quá trình tiếp cận các ổng thông trung tàm sau đó. Chúng tôi khuyến cáo hạn chế tối đa việc “ngắt kết nối” đường truyền để giảm nguy cơ nhiễm trùng đường truyến trung tâm. Một bản đánh giá của Cochrane cho thấy rằng: Không có đủ bằng chứng đề khuyến cáo sử dụng hoặc chống lại việc sử dụng kháng sinh thường quy ở trẻ sơ sinh có đặt ống thông rốn, dõng thời khuyến nghị không nên áp dụng liệu pháp kháng sinh theo kinh nghiệm kéo dài với nuôi cấy âm tính ở trẻ sơ sinh. Tuy nhiên, việc sử dụng “khóa kháng sinh” (“antibiotic lock”) có thể làm giảm nhiễm trùng huyết liên quan đến ống thòng ở trẻ sơ sinh.
Một vấn đề đáng quan ngại của UAC là tác động của việc lấy mẫu máu lén lưu lượng máu não. Các nghiên cứu siêu âm và quang phổ cận hồng ngoại (near-infrared spectroscopy – NIRS) đã chỉ ra rằng, việc lấy máu thường quy từ ống thông rốn sê làm thay đổi huyết động học và oxygen hóa não. Mặc dù việc giảm thế tích máu rút ra có thể làm giảm những thay đổi này, nhưng vẫn chưa rõ liệu việc rút máu chậm hơn có mang lại lợi ích hay không. Mặc dù chưa biết liệu những thay đổi huyết động não như vậy có làm tăng nguy cơ biến chứng như xuất huyết não thất hay không, nhưng việc giảm thiểu thể tích máu rút và tránh rút nhanh hoặc chuyển nhanh vào ống thông rốn là điếu hợp lý.
Dinh dưỡng qua đường ruột đồng thời với UAC tại chỗ được coi là an toàn, với hầu hết các bác sĩ lâm sàng tiếp tục cho ăn khi đang đặt ong thong rốn. Động mạch mạc treo tràng trên không bị ảnh hưởng bởi sự có mặt của ống thông rốn trong quá trình nuôi dưỡng dinh dưỡng.
Có rất ít tài liệu được xuất bản đưa ra quyết định về thời gian mà một UAC có thể duy trì an toàn. Ở hầu hết các cơ sở, chúng thường được rút bỏ trong vòng vài ngày, khi trẻ sơ sinh không còn yêu cầu hỗ trợ hô hấp quan trọng hoặc lấy mẫu máu thường xuyên. Tương tự như tất cả các liệu pháp khác, nguy cơ tiềm ẩn của ỨC phải được cân bằng với những lợi ích tiềm tàng đối với mỗi trẻ sơ sinh.
Các vị trí đặt ống thông khác
Ở một sổ trẻ sơ sinh, việc đặt ống thông động mạch rốn không thành công. Trong những trường hợp như vậy, phương pháp đặt ống thông động mạch ngoại vi qua da được ưu tiên thay thế. Phương pháp can thiệp động mạch qua da cũng là lựa chọn tốt nhất cho trẻ không còn NỮA nhưng vẫn cần tiếp cận động mạch. Các kỹ thuật khác, chẳng hạn như phẫu thuật bộc lộ động mạch rốn hoặc động mạch ngoại vi, khó thực hiện hơn và tiềm ẩn nhiều nguy cơ hơn. Mặc dù kỹ thuật đặt ống thông động mạch ngoại vi qua da là một thách thức, đặc biệt là ở trẻ sơ sinh cân nặng dưới 1kg, nhưng thường có thể áp dụng biện pháp đặt ống thông qua động mạch quay, động mạch mu bàn chân hoặc động mạch chày sau. Nên tránh đặt ống thông động mạch thái dương, bởi đã có báo cáo cho thấy rằng kỹ thuật này có thể gây tắc mạch não và đột quỵ.
Nêu động mạch quay được đặt ống thông, có thể thực hiện thử nghiệm Allen để’ đảm bảo tính thông thoáng của động mạch trụ. Tuy nhiên, độ tin cậy của thử nghiệm này vẫn còn bị hoài nghi. Ngược lại, nếu muốn đặt ống thông động mạch trụ, thì nên đánh giá mức độ thông thoáng của động mạch quay. Bát đấu thử nghiệm Allen bằng cách bóp nhẹ bàn tay cho hết máu. Tạo áp lực lên cả động mạch quay lẫn động mạch trụ, sau đó loại bỏ áp lực từ bàn tay và động mạch sẽ đặt ống thông. Nếu toàn bộ bàn tay hồng lên và được tưới máu, có thể tiến hành an toàn. Đánh giá Doppler cũng có thể được sử dụng ghi lại tuần hoàn bàng hệ.
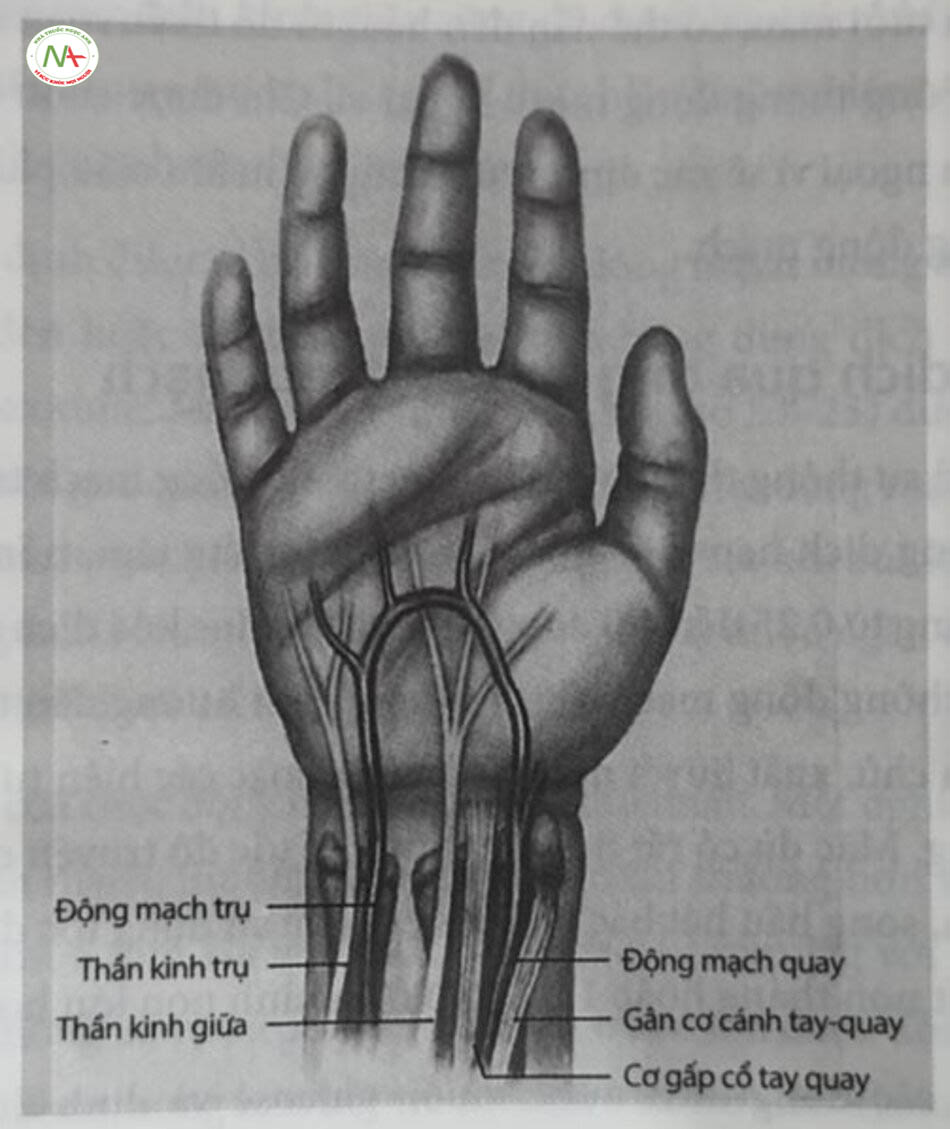
Có thế xác định vị trí của động mạch bằng cách sờ hoặc soi đèn. Nếu muốn chích động mạch quay hoặc động mạch trụ, thì phải giữ bàn tay ở tư thế duỗi nhẹ. Có thể giảm đau toàn thân trước khi đặt ống thông. Đôi khi, có thể’ dùng biện pháp gây tê cục bộ bằng lidocain, và cục sấn tạo thành có thể yêu cáu phải xoa bóp nhẹ nhàng và đợi trong vài phút. Vị trí đặt phải được sát khuẩn trước khi tiến hành bằng dung dịch povidone-iodine hoặc chlorhexidine. Động mạch quay thường dễ dàng đặt ổng thống nhất ở điểm mạch đập cực đại trên phần xa của xương quay, gần với thánh lòng bàn tay nòng của động mạch. Ở vị trí này, động mạch nằm giữa hai gân, gân nông và gân bên của dây thần kinh giữa (Hình 10.8).
Có thể sử dụng ống thông (catheter) trong tình trạng khô hoặc được tráng đầy bằng dung dịch nước muối sinh lý đã được heparin hóa, nhằm tạo điều cần thuận lợi cho máu dội ngược trở lại. Ống thông và kim được nâng lên mắt góc khoảng 30 độ cho đến khi được đưa vào mạch máu và thấy dòng máu phụt trở lại. Kim được giữ cố định và ống thông được luôn vào động mạ kim được rút ra. Một kỹ thuật thay thế là chọc thủng động mạch qua ca thanh trước lẫn thành sau rói rút kim. Sau đó, ống thông được rút ra cho đen khi đau của nó đi vào lòng mạch và thấy được máu phụt trở lại; lúc này, nó được luôn vào mạch máu. Tuy nhiên, theo kinh nghiệm của chúng tôi, phương pháp này ít thành công hơn ở trẻ sơ sinh.
Khi vào đúng vị trí, ổng thông phải được cố định chặt bằng băng dán trong suốt, đóng thời được kết nối với dịch truyền là dung dịch nước muối đã được heparin hóa bằng đầu nối chữ T và khóa ba chia. Băng cố định ống thông phải cho phép nhìn rõ toàn bộ tất cả các ngón tay mà không bị che khuất bởi tình trạng giảm tưới máu, có thể dẫn đến hoại tử do thiếu máu cục bộ, là một biến chứng của ống thông động mạch ngoại vi. Chỉ được chọn để luồn ống thông động mạch ngoại vi sẽ xác định xem xét nghiệm khí máu phản ánh giá trị trước hay sau ống động mạch.
Truyền dịch qua ống thông động mạch
Nên duy trì sự thông thoáng của cả ống thông động mạch trung tâm lẫn ngoại vi bằng dung dịch heparin hóa. ơ hấu hét trung tâm, nồng độ heparin nam trong khoảng từ 0,25 đến 1,0 đơn vị/mL. Heparin hóa dịch truyền làm giảm tỷ lệ tắc ống thông động mạch nhưng không ảnh hưởng đến tấn xuất huyết khối động mạch chủ, xuất huyết nội sọ, tử vong hoặc các hiện tượng thiếu máu cục bộ lâm sàng. Mặc dù có rất ít bằng chứng về tốc độ truyền dịch cho ống thông động mạch, sống hầu hết bác sĩ lâm sàng đều sử dụng tốc độ tối thiểu 0.5 mL/ giờ ở trẻ rát non tháng hoặc 1 mL/giờ ở trẻ sinh non lớn hơn hoặc dù tháng.
Tất cả các dung dịch nước muỗi, glucose và dinh dưỡng nóng độ cao (hyperalimentation solution) đều có thể được truyền vào ỨC, và người ta đã chứng minh rằng việc truyền dung dịch chứa axit amin có độ thẩm thấu bình thường ít gây tán huyết hơn so với dung dịch một phần tư muối, đồng thời giúp cải thiện dinh dưỡng. Ngược lại với động mạch rốn mà qua đó, người ta có thể truyền được nhiều loại dung dịch, không nên dùng bất cứ loại nào khác ngoài dung dịch nước muối sinh lý để truyền vào động mạch ngoại vi vón toán tại mối lo ngại ve lat dụng kích thích của chúng. Ở những trẻ rất non tháng mà dung dịch nước muối sinh lý 1 mL/giờ cung cấp một lượng natri quá mức, các bác sĩ lâm sàng thường truyền nước muối 0,45%. Trong trường hợp cần thêm kiềm, natri acetate sẽ được truyền thay cho natri chloride. Thuốc hoặc các sản phẩm máu không được sử dụng thông qua ống thông động mạch ngoại vi.
Chọc động mạch
Các mẫu khí máu có thể được lấy từ việc chọc ngắt quãng các động mạch quay, trụ, thái dương, chày sau, hoặc động mạch mu bàn chân. Nhìn chung, không nên dùng động mạch đùi và động mạch cánh tay để’ chọc động mạch (arterial puncture) vì sự hình thành huyết khối nghiêm trọng có thể dẫn đến mất chi; ngoài ra, tổn thương dây thần kinh giữa cũng đã được báo cáo khi chọc động mạch cánh tay. Như đã lưu ý trước đó, có thể thực hiện thử nghiệm Allen trước khi chọc động mạch quay hoặc động mạch trụ.
Sau khi đã xác định được vị trí chính xác của động mạch mong muốn bằng phương pháp soi đèn hoặc sờ, nên sát khuẩn da bằng dung dịch povidone- iodine hoặc chlorhexidine. Một kim cỡ nhỏ (ví dụ như cởi 23-25) dược dưa vào vị trí vát nghiêng một góc qua da, ngược lại với hướng của động mạch. Máu sẽ chảy vào ống một cách tự nhiên hoặc hút nhẹ nhàng. Sau khi rút kim ra, nên án liên tục trong 5 phút. Nếu sự hình thành khối máu tụ được ngăn chặn, cùng một động mạch có thể được tái sử dụng nhiều lần.
Hạn chế chính của chọc động mạch là đau do thủ thuật. Một nghiên cứu cho thấy rằng: Chọc tĩnh mạch, thường được coi là ít chấn thương hơn so với chọc động mạch, làm giảm 6 mmHg với PaCO, và giảm 17mmHg với PaO,. Mặc dù tiêm lidocain (không có epinephrine) dưới da trước khi chọc động mạch sẽ giúp giảm đau một phần, sống hầu hết trẻ sơ sinh vẫn trở nên kích động trong khi chọc. Vì lý do này, việc chọc động mạch để’ lấy khí máu không được sử dụng thường xuyên.
Máu mao mạch được động mạch hóa
Máu mao mạch được động mạch hóa (arterialized capillary blood) cung cấp một ước tính thó của các giá trị máu động mạch. Vé lý thuyết, máu đi qua giường mao mạch ngoại vi giãn ra bị hạn chế thời gian xảy ra trao đổi O2 và CO2, do đó giá trị khí máu mao mạch xấp xỉ với giá trị khí máu động mạch. Tuy nhiên, máu thu được đóng thời từ ỨC và gót chân được làm ấm của trẻ sơ sinh đã chứng minh rằng: Máu mao mạch động mạch hóa dự đoán kém vé các giá trị trong máu động mạch, bao gồm pH, PaCO, và PaO2. Các mẫu máu mao mạch động mạch hóa có lẽ hữu ích nhất ở trẻ sơ sinh thở máy móc tính, vì chúng có mức độ hữu ích vừa phải trong việc theo dõi những thay đổi lớn về pH và PaCO2.
Để tạo động mạch hóa cho máu ở mao mạch, nên làm ấm đấu chỉ trong vài phút. Cấn thực hiện việc làm ắm với các hóa chất tỏa nhiệt được thiết kế đặc biệt để’ làm động mạch hóa máu mao mạch thay vì chườm ấm. Nên cẩn thận làm sạch vị trí và dùng một lancet nhỏ để’ chọc thủng da ở mặt giữa hoặc mặt bên của gót chân. Không nên sử dụng phần phía sau gót chân (Hình 10.9).
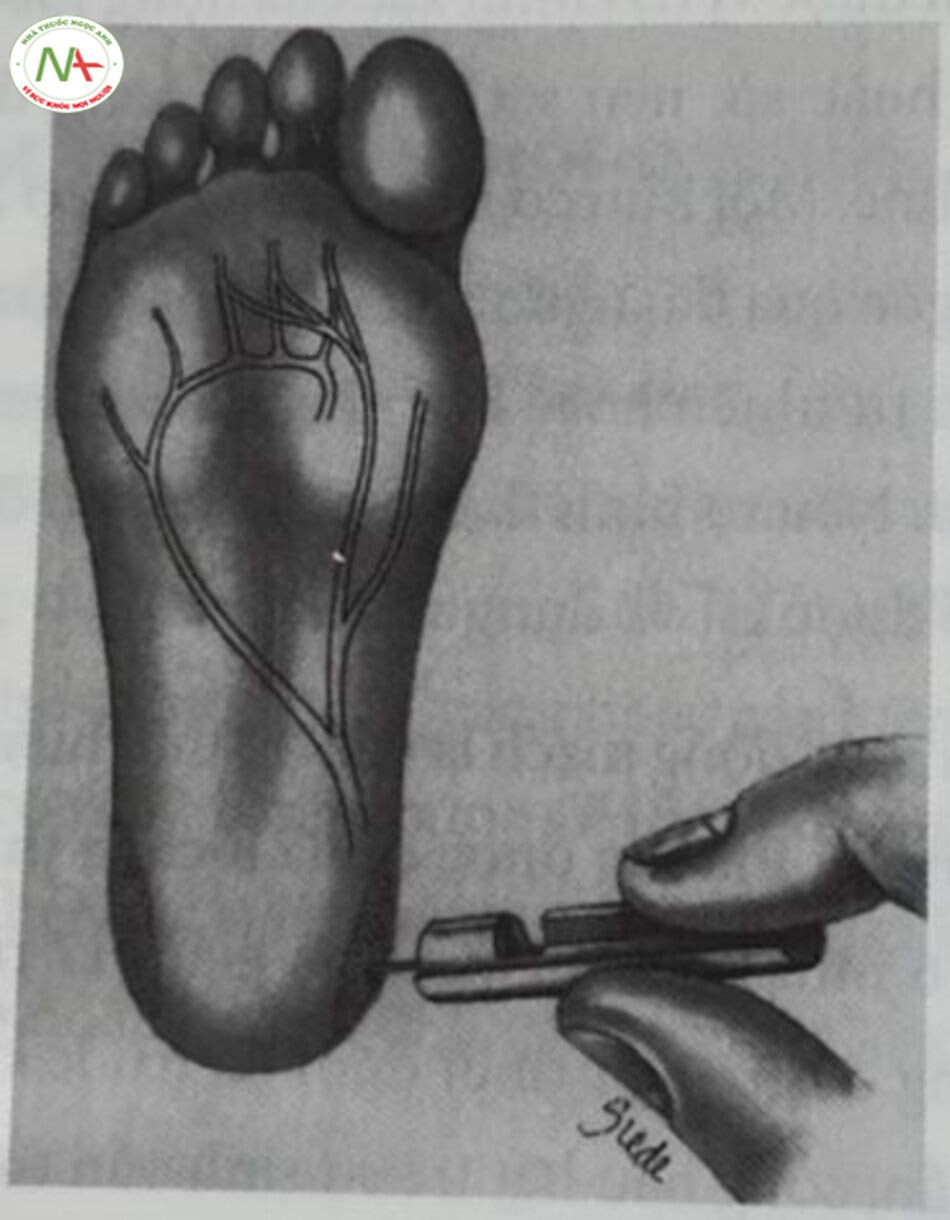
Có nhiều thách thức kỹ thuật để lấy được các mẫu máu mao mạch tối ưu. Làm ấm không đủ dẫn đến máu không được động mạch hóa đầy đủ. Việc bóp ^quá nhiều sẽ làm nhiễm máu “động mạch” với máu tĩnh mạch và/hoặc mô kẽ. Sự tiếp xúc của máu với không khí trong quá trình thu thập sẽ làm tăng giả PO2 và giảm giá các giá trị PCO2. Tình trạng tưới máu ngoại vi thấp dẳng đến tình trạng ứ trệ và tăng giả PCO2. Vì lý do này mà hiếm khi một mẫu mao mạch ở trẻ 2 giờ tuổi với biểu hiện tím đầu chi (acrocyanosis) rõ rệt có thể đem lại thông tin hữu ích và có nguy cơ đặt nội khí quản không cần thiết đo tình trạng nhiễm toan hô hấp rõ ràng vì ứ máu. Các vấn đề lâu dài liên quan đến các mẫu mao mạch thường xuyên bao gồm viêm xương sụn và nốt vôi hóa gót chân. Các nốt vôi hóa này có thể tồn tại trong vài tháng đến vài năm nhưng dường như không gây ra các vấn đề vĩnh viễn cho trẻ sơ sinh.
Theo dõi xâm lấn liên tục
Một số thiết bị đã được phát triển để đo độ bão hòa hemoglobin, PaO, và PaCO2, trực tiếp nội mạch hoặc “nội tuyển” (“inline”). Tuy nhiên, bất chấp những ưu điểm rộn ràng của chúng, những thiết bị này vẫn chưa được dùng phổ biến ở hầu hết các NICK ở Bắc Mỹ, cả vì giá thành lẫn độ phức tạp của chúng cũng như bời tính dễ sử dụng của công nghệ không xâm lấn. Một nghiên cứu đã chứng minh rằng có sự giảm nhu cầu truyền máu ở trẻ sinh non sử dụng máy phân tích khí máu nội tuyến.
Ước tính khí trong máu không xâm lấn
Sự phát triển của các kỹ thuật đơn giản, an toàn và không xâm lấn để có được các ước tính liên tục của khí máu là một trong những tiến bộ quan trọng nhất trong chăm sóc trẻ sơ sinh. Máy đo độ bão hòa oxy có mặt ở khắp nơi trong NICU và bão hòa oxy hiện được coi là một dấu hiệu sinh tốn. Mặc dù ít được sử dụng rộng rãi hơn so với máy đo độ bão hòa oxy mạch nảy (pulse oximeter), cả máy theo dõi CO2 qua da lận máy theo doi co, cuối thì thở ra đều đóng vai trò quan trọng trong việc xử trí trẻ sơ sinh. NIRS là một công nghệ khác đang dán chuyển từ nghiên cứu sang sử dụng lâm sàng thường quy ở một số trẻ sơ sinh được chọn.
Đo độ bão hòa oxy
Theo dõi độ bão hòa oxy thông qua máy đo độ bão hòa oxy mạch nảy (pulse oximeter) (SpO2) là phương pháp thực hành tiêu chuẩn trong NICU. Máy đo độ bão hòa oxy mạch nảy hoạt động dựa trên nguyên tắc: Oxyhemoglobin (hemoglobin bão hòa) có màu khác với deoxyhemoglobin (hemog o in không bão hòa), do đó hấp thụ ánh sáng ở tâm số khác. Oxyhemoglobin chứng tô khả năng hấp thụ ánh sáng hồng ngoại ở bước sóng 940nm cạo hơn SO với deoxyhemoglobin, cho thấy ánh sáng đỏ ở bước sóng 660nm có độ hấp thụ cao hơn. Một đấu dò (probe) bao gồm nguồn sáng và cảm biến quang (photo sensor) được đặt sao cho nguồn sáng và cảm biến quang nằm ở hai phía đối diện nhau và có mô ở giữa. Khi ánh sáng đi qua các mô, hemoglobin bão hòa và hemoglobin không bão hòa sẽ hấp thụ các tần số ánh sáng khác nhau. Bằng cách đo độ chênh tỷ lệ của các tấn số khác nhau của ánh sáng được hấp thụ trong thời kỳ tâm thu và tâm trương, có thể tính được lượng ánh sáng được hấp thụ do động mạch. Sau đó, bằng cách so sánh sự hấp thụ ánh sáng ở hai tán số thích hợp, có thể tính được phần trăm oxyhemoglobin bão hòa. Các cải tiến của hệ thống này bao gồm các thuật toán phức tạp giúp tính toán độ bão hòa chính xác hơn và để’ tách các xung động mạch khỏi nhiễu động của chuyển động. Độ bão hòa oxy chức năng (functional oxygen saturation) đo bằng máy đo độ bão hòa oxy mạch nảy được biểu diễn bằng phương trình 100 X OxyHb/x Hb + Deoxy Hb); trong đó, Oxi Hb là oxyhemoglobin và Deoxy Hb là deoxyhemoglobin.
Nhìn chung, máy đo độ bão hòa oxy mạch nảy cung cấp dữ liệu tuyệt vời vê oxygen hóa trong phạm vi sinh lý học nhưng lại tổn tại những hạn chế quan trọng cắn được xem xét. Việc tính toán độ bão hòa phụ thuộc vào ánh sáng cảm biến, do đó nếu đế ánh sáng môi trường chiếu vào cảm biến có thể dẫn đến trị số sai. Chuyển động và tưới máu kém có thể cản trở tín hiệu. Bằng cách chỉ tập trung vào oxyhemoglobin and deoxyhemoglobin, phép đo độ bão hòa oxy mạch nảy truyền thống có thể cung cấp các giá trị sai lệch trong bối cảnh nóng độ cao của các loại hemoglobin khác.
Trong bói cảnh nóng độ carboxyhemoglobin tăng cao, phép đo độ bão hòa oxy mạch nảy sẽ đánh giá quá mức độ bão hòa oxy 1% cho mỗi lần tăng 1% carboxyhemoglobin. Có điếu này là vì carboxyhemoglobin hấp thụ ánh sáng tương tự như oxyhemoglobin (Hình 10.10). Ngược lại, methemoglobin hấp thụ lượng anh sáng đỏ và hồng ngoại bằng nhau (xem Hình 10.10). Khi lượng methemoglobin tảng lèn, tỷ lệ hấp thụ ánh sáng ở cả hai bước sóng tiến gán đến 1, tương ứng với độ bảo hòa oxy là 85%. Với công nghệ tiên tiến, có bước sóng ánh sáng được một số nhà sản xuất máy đo độ bão hòa oxy sử dụng đàn tàng lên, cho phép máy đo độ bão hòa oxy do tồng lượng hemoglobin và các loại hemoglobin khác như methemoglobin và carboxyhemoglobin. Tuy nhiên, công nghệ này không được sử dụng thường xuyên ở trẻ sơ sinh.
Phép đo co-oximeter được sử dụng trong các máy phân tích khí máu hiện đại và khác với phép đo độ bão hòa oxy mạch nảy ở chỗ nó sử dụng phép đo quang phổ để xác định nồng độ tương đối của các dẫn xuất hemoglobin. Máy đo co-oximeter hiện đại sử dụng hơn 100 bước sóng ánh sáng khác nhau. Bằng cách này, chúng đo trực tiếp một sổ loại hemoglobin như: Oxyhemoglobin, deoxyhemoglobin, carboxyhemoglobin, methemoglobin và sulíhemoglobin. Do đó, những loại máy đo co-oximetry này ít gặp lỗi báo cáo độ bão hòa oxy hơn so với phép đo độ bão hòa oxy mạch nảy. Độ bão hòa oxy “phân đoạn” (“fractional” oxygen saturation) đo bảng máy phân tích khí máu được biểu thị bằng phương trình 100 X OxyH/(Oxy + Deoxy Hb + COHb + MetHb); trong đó, Oxi Hóa là oxyhemoglobin, Deoxy Hb là deoxyhemoglobin, COHb là carboxyhemoglobin và MetHb là methemoglobin. Trong bối cảnh nóng độ các loại hemoglobin bất thường tăng cao, nên hướng dản liệu pháp điều trị bằng xét nghiệm khí máu thay vì đo độ bão hòa oxy mạch nẩy.
Các nhà sản xuất khác nhau sử dụng các thuật toán khác nhau có thể cho kết quả hơi khác nhau một chút. Các nhà sản xuất liên tục cập nhật phần mềm cho thiết bị của họ, đổng thời xuất bản nhiều bài báo bàn về những hạn chế của các thiết bị lỗi thời. Cần lưu ý rằng, sự hiện diện của HbF, thiếu máu, hoặc tăng bilirubin máu có ảnh hưởng không đáng kể’ đến độ chính xác của phép đo độ bão hòa oxy mạch nảy. Máy đo độ bão hòa oxy mạch nảy phụ thuộc vào lưu Lượng máu mạch nẩy. Trong các tình huống như sốc, hoặc nếu phù nề nghiêm trọng che khuất nhịp nảy của mạch, máy đo độ bão hòa oxy mạch nảy có thể hoạt động không đáng tin cậy. Tương tự, ở các bệnh nhân được hỗ trợ toàn bộ từ ECMO tĩnh mạch-động mạch, vốn là những người có nhịp nảy của mạch tối thiểu, nhiều máy đo oxy mạch nảy hoạt động kém hiệu quả nếu áp lực mạch (pulse pressure) nhỏ hơn 10mm Hg.
Máy đo độ bão hòa oxy mạch nảy không phân biệt được mực độ tăng oxy máu ở phần phẳng phía trên của đường cong ODC (xem hình 10.1). Ví dụ, PaO2 là 80 và PaO2 là 180 mm Hg, cả hai đều thể hiện về cơ bản là 100% bão hòa oxy (SpO2). Một số bác sĩ lâm sàng cho rằng đây là một hạn chế đáng kể của phương pháp đo độ bão hòa oxy mạch nảy so với phương pháp theo dõi oxy qua da. Các khuyến cáo hiện tại nhắm mục tiêu SpO2 từ 91% đến 95% ở trẻ sinh non để tránh tăng oxy máu, từ đó làm giảm nguy cơ mắc bệnh võng mạc ở trẻ sinh non. Máy đo độ bão hòa oxy mạch nảy cũng kém chính xác hơn ở mức SpO2 thấp (ví dụ như độ bão hòa < 70%). Bên ngoài phòng sinh, điều này thường không đặt ra vấn đề quan trọng về mặt lâm sàng, bởi mức độ chính xác của độ bão hòa thấp có thể không thay đổi việc đưa ra quyết định lâm sàng.
Một ưu điểm chính của phép đo độ bão hòa oxy mạch nảy nằm ở chỗ: Độ bão hòa oxi là chỉ số hàm lượng tốt hơn so với PaO2, vì độ bão hòa được sử dụng để tính lượng oxy được mang bởi hemoglobin (yếu tố góp phần chính vào hàm lượng oxy trong máu); trong khi đó, PaO2 đại diện cho oxy hòa tan, là một thành phần phụ của quá trình vận chuyển oxy.
Quang phổ cận hồng ngoại
Các đặc tính hấp thụ ánh sáng của hemoglobin được oxygen hóa và khử oxy có thể áp dụng cho các kỹ thuật khác ngoài phép đo độ bão hòa oxy mạch nảy. Quang phổ cận hồng ngoại (near-infrared spectroscopy – NIRS) là một kỹ thuật dựa trên sự hấp thụ khác biệt của ánh sáng và tính chất tương đối trong suốt của mô đối với ánh sáng hồng ngoại để ước tính oxygen hóa mô. NIRS có thể được sử dụng như trị số đo thay thế cho oxygen hóa tĩnh mạch trộn của mô. Kỹ thuật này đã được chấp thuận trong khoa sơ sinh nhưng giá trị thực của nó vẫn chưa được biết đến nhiều, bởi kết quả từ biện pháp theo dõi NIRS vẫn chưa được chứng minh là có sự cải thiện. Trong một thử nghiệm lâm sàng ngẫu nhiên, mục tiêu oxygen hóa não được cải thiện nhờ sử dụng NIRS, những mục tiêu giảm nguy cơ xuất huyết não thất nặng hoặc nguy cơ tử vong không đạt được mức độ quan trọng trong thống kê, và không có sự khác biệt về kết quả phát triển thần kinh ở trẻ 2 tuổi đã điều chỉnh. Theo dõi NIRS khác với đo độ bão hòa oxy mạch nảy ở nhiều khía cạnh, vì độ bão hòa mô được đo bằng NIRS đại diện cho số bình quân gia quyền (weighted average) của độ bão hòa động mạch và tĩnh mạch, trong đó hệ số gia trọng (weighting factor) không thể được xác định chính xác và thay đổi theo từng mô cũng như theo thời gian.
Lựa chọn phương pháp theo dõi
Theo dõi qua da
Điện cực oxy và CO2 qua da cho phép ước tính gián tiếp liên tục PaO2 và PaCOr Mặc dù phương pháp đo độ bão hòa oxy mạch nảy đã thay thế phấn lớn vai trò của phương pháp theo dõi oxy qua da trong việc ước tính tình trạng oxygen hóa, song nhiều trung tâm vẫn hay sử dụng phương pháp theo dõi CO2 qua da. Các thiết bị theo dõi CO2 qua da (transcutaneous CO2 monitor) hiện tại có thể được chạy ở nhiệt độ thấp hơn so với các thế hệ máy theo dõi trước đó, nhằm giảm nguy cơ tổn thương nhiệt đối với da non.
PO, qua da (transcutaneous PO2 -TcO2) về’ cơ bản là đo PH, của da. Mặc dù PO, của da thường thấp hơn PaO2, song việc đốt nóng da trực tiếp dưới điện cực TcPO, gây giãn mạch cục bộ trên da, dẫn đến PO2 của da gần bằng với PaO,. Mặc dù việc làm nóng da còn để lại một số tác động khac ngoai gian mạch, song ảnh hưởng lẻn ODC, tiêu thụ oxy mô và tiêu thụ oxy điện cực lại bị triệt tiêu đối với hầu hết bệnh nhân. Các nghiên cứu đã chỉ ra rằng, TcPO2 sáp xì PaO2 ngay cả ở bệnh nhân bị tưới máu kém; tuy nhiên, ở trẻ lớn hơn bị bệnh phổi mãn tính, TcPO2 đánh giá thấp hơn PaO,.
Mối quan hệ giữa PaO2 và PCO2 qua da (TpcCO,) phức tạp hơn mối quan hệ giữa PaO, và TcPO2. TcPCO2 phải luôn lớn hơn PaCO2 vì các lý do sau: (1) Gia nhiệt làm tăng sản xuất CO2 cục bộ; (2) có một sự chênh lệch cơ, động mạch-tế bào quan trọng; và (3) da có tác dụng làm mát điện cực. Các hiệu ứng này khá đồng đều ở một nhiệt độ nhất định và kết hợp với nhau để tạo ra mối quan hệ tuyến tính giữa TcP, và PaCO,. Các kết quả sai có thể xảy ra với máy theo doi TcP CO2. Mặc dù các chỉ số TcP, cho kết quả cực thấp có thể do tiếp xúc với không khí, sóng các chỉ số TcP CO, cao giả thường yêu cầu đối chiếu với khí máu để đảm bảo PaCO, không thực sự tăng cao.
Bất chấp những hạn chế của nó, phép đo CO2 qua da vẫn rất hữu ích cho các giá trị xu hướng của PaCO2, đặc biệt trong những trường hợp không có các chỉ số lâm sàng đáng tin cậy về mức độ thông khí đầy đủ. Nó có thể đặc biệt hữu ích trong việc xử trí trẻ sơ sinh khó đánh giá thể tích khí lưu thông. Nhiều bác sĩ lâm sàng coi việc theo dõi TcPCO2 là biện pháp hữu ích khi bắt đầu thông khí tần số cao, với cả hai chế độ thông khí phản lực (jet ventilation) lân tông 1 dao động (oscillatory ventilation) đều có thể làm thay đổi PaCO2 nhanh chóng khi mới chuyển từ chế độ thông khí thông thường (conventional ventilation) sang.
Capnography
Capnography, còn được gọi là phương pháp theo dõi CO2 cuối thì thở ra (end-tidal CO2 monitoring), là phép đo lượng cơ, khí thở ra. Bởi vì PCO, phế nang xấp xì với PaCO2> nên một mẫu khí phế nang tinh khiết sẽ giúp ước tính PaCO,. Capnography đo nóng độ CO2 trong khí thở ra và hiển thị nóng độ này dưới dạng hàm số’ theo thời gian. Nếu PCO, thỏ ra có mức cao nguyên cuối thì thở ra (end-tidal plateau) tót. thi điều này thường đại diện cho PCO2 phế nang. Theo dõi CO2 cuoi thi thở ra có thể được thực hiện bằng kỹ thuật dòng chính (mainstream), dòng phụ (sidestream) hoặc dòng vi mô (microstream). Kỹ thuật này đã được sử dụng rộng rãi ở các đơn vị chăm sóc đặc biệt dành cho người lớn và trẻ em, nơi bệnh nhân nhận được thể tích khí lưu thông tương đối lớn và tần số hô hấp thấp nên dẻ đo lường cao nguyên phế nang (alveolar plateau). Tuy nhiên, kỹ thuật này đã không còn được chấp nhận rộng rãi trong CƯ, chủ yếu vì nó chỉ cung cấp một ước tính sơ bộ về PaCO, ở trẻ sơ sinh bị bệnh phổi nặng.
Ở trẻ sơ sinh bị bệnh, rất khó để lấy mẫu khí phế nang không lẫn với khí từ đường thở. Trẻ sơ sinh thường sử dụng tần số hô hấp cao hơn và thể’ tích khí lưu thông thấp hơn, quá nhỏ để có được mẫu cao nguyên phế nang cuối thì thở ra đầy đủ. Ngoài ra, bệnh lý phế nang tương tác độc lập với mối quan hệ của CO2 cuối thì thở ra so với PaCO,. Capnography có thể là một phương pháp ước tính chính xác PaCO2 ở trẻ khỏe mạnh hoặc ở trẻ sau phẫu thuật thở máy với phổi bình thường, nhưng lại chỉ cung cấp ước tính sơ bộ về PaCO2, thường bị đánh giá tháp ở trẻ mắc bệnh phổi nặng. Một nghiên cứu về capnography trong quá trình vận chuyển trẻ sơ sinh cho thấy PCO, cuối thì thở ra đánh giá thấp đáng kể PaCO2, nhưng mức độ đánh giá thấp không phụ thuộc vào PaCO2 hay mức độ nghiêm trọng của bệnh phổi. Phân tích định lượng các đường cong capnography có thể chỉ ra biên độ của nhịp thở tự phát so với nhịp thở có hỗ trợ bởi máy thở.
Capnography có một số ưu điểm như: Tương đối rẻ, di động, không xâm lấn và dễ sử dụng. Một trong những ứng dụng hữu ích nhất của việc theo dõi CÓ, thở ra là xác định nhanh vị trí đặt ống nội khí quản (endotracheal tube – ETT) thích hợp. Các thiết bị so màu (colorimetric device) nhỏ, dùng một lần được gắn vào đầu nối trung tâm của ống nội khí quản ngay sau khi đặt nội khí quản để đảm bảo CO2 thở ra được phát hiện, cho thấy đặt nội khí quản Thành công. Ngoài ra, Chương trình Hồi sức Sơ sinh (Neonatal Resuscitation Program) khuyến cáo nên sử dụng máy dò CO2 so màu để xác minh vị trí đặt ống nội khí quản. Trẻ sơ sinh có cung lượng tim rất thấp có thể không thở ra đủ CÓ, để được máy dò CO2 phát hiện một cách đáng tin cậy. Mặc dù phát hiện định tính (so màu) rất hữu ích đối với việc xác định vị trí đặt ống nội khí quản, song không có bằng chứng chắc chắn ủng hộ cho việc theo dõi tại giường có tích hợp theo doi co, cuối thì thở ra như một lựa chọn, kiến việc theo dõi liên tục có, thờ ra trở thành một lựa chọn thực tế cho trẻ sơ sinh thở máy, với lưu ý rằng một số máy theo dõi CO2 cuối thì thở ra làm tăng đáng kế khoảng chết (dead space) ở trẻ rất non tháng.
Sự phụ thuộc vào các mẫu khí máu động mạch đã giảm dần. Các nỗ lực giảm số lượng xét nghiệm máu, bao gồm cả khí máu, đã được thúc đẩy để giảm thể’ tích máu mất đi do điều trị. “Tăng CO2 máu cho phép” (“permissive hypercarbia”) đã dẫn đến một phạm vi rộng hơn của các giá trị PaCO2 được chấp nhận và do đó, các trị số đo khí máu ít thường xuyên hơn. Việc tăng cường sử dụng các chế độ thông khí mục tiêu thể tích do bệnh nhân kích hoạt có thể’ làm giảm thêm tần suất lấy mẫu khí máu. Bất chấp những xu hướng này, việc lấy mẫu khí máu động mạch đáng tin cậy ở trẻ sơ sinh không ổn định vẫn đóng vai trò quan trọng. Chúng tôi thường xuyên đặt UAC cho trẻ sơ sinh cần đặt nội khí quản, hoặc thở áp lực đường thở dương liên tục (continuous positive airway pressure – CPAP) qua mũi với nhu cầu oxy đáng kể và ở hầu hết trẻ sơ sinh có cân nặng dưới 1 kg. chúng tôi thường loại bỏ UAC sau một vài ngày khi không cần đo khí máu thường xuyên hoặc đo huyết áp liên tục nữa. Ở những trẻ lớn hơn bị bệnh nặng, có thế đặt ống thông động mạch ngoại vi.
Chúng tôi theo dõi tất cả trẻ sơ sinh bằng phương phap đo độ bao ho sy mạch nẩy liên tục cho đến khi xuất viện, mặc dù một số đơn VỊ chuyển sang theo dõi ngừng thở đơn thuần trước khi xuất viện. Trẻ sơ sinh cần hỗ trợ hô hấp đáng kể được theo dõi bằng phương pháp theo dõi CO2 qua da, bên cạnh việc đo độ bão hòa oxy mạch nảy. Capnography không được sử dụng rộng rãi trong NICK của chúng tôi, nhưng đã được dùng cho trẻ sơ sinh lớn hơn bị bệnh phổi nhẹ. Chúng tôi sử dụng phương pháp theo dõi NIRS thường quy ở trẻ rất non tháng cẩn hỗ trợ hô hấp trong tuần đầu tiên sau khi sinh.
Việc theo dõi liên tục trẻ thở máy được bổ sung bằng các trị số đo khí máu ngắt quang. Tại NICU cua chúng tôi, trẻ thở máy ổn định mà không có đường ong thong động mạch thương co khi mau mao mạch được thực hiện sau mỗi 24 đến 48 giờ; trong khi đó, trẻ sơ sinh kém ổn định hơn thì được thực hiện thường xuyên từ hai đến bốn lần mỗi ngày. Ở những trẻ bị bệnh nặng không có đường ống thông động mạch, chúng tôi hiếm khi sử dụng mẫu lấy từ ống nông tĩnh mạch rốn, vì PCO2 tĩnh mạch có thể cao hơn đáng kể so với PCO2 động mạch. Đôi khi, áp dụng biện pháp thô sơ này có thể thích hợp hơn so với việc thực hiện lặp đi lặp lại các mẫu khí máu mao mạch động mạch hóa hoặc chọc động mạch ngắt quãng.
Phân tích khí máu
Máy phân tích khí máu (blood gas analyzer) tiếp tục được cách tân, cung cấp nhiều trị số khí máu hơn mức cơ bản như pH, PCO2 và PaO2. Các máy phân tích khí máu hiện đại có khả năng đo các dạng hemoglobin, chất điện giải trong huyết thanh và các chất chuyển hóa khác nhau. Máy phân tích khí máu tại điểm chăm sóc (point-of-care) tạo điều kiện phân tích mẫu máu tại giường và trong phòng sinh, có thể thúc đẩy nhanh quá trình đưa ra quyết định lâm sàng. Khí máu động mạch, tĩnh mạch và mao mạch được phân tích trong NICU có thể làm giảm sai số thu thập mẫu – trước và sau, đồng thời giảm thời gian cho ra kết quả. Máy phân tích có nhiều kích cỡ khác nhau, từ loại cầm tay cho đến hệ thống máy tính đề bàn di động.
Nguyên tắc đo của máy phân tích khí máu
Điện cực khí máu truyền thống đối với pH, PCO2 và PaO2 có chức năng đo sự thay đổi của dòng điện hoặc điện áp. Các điện cực được cấu tạo bằng màng thẩm thấu và được ngâm trong dung dịch cho phép H’, CO2 hoặc O2 đi qua màng, phản ứng với dung dịch và gây ra sự thay đổi dòng điện hoặc điện áp tương đương với phép đo pH, PaCO2 hoặc PaO,. Hiện tại, các máy phân tích sử dụng các công nghệ như đo điện thế (potentiometric), đo cường độ dòng điện (amperometric), huỳnh quang (fluorescence) và điện cực chọn lọc ion (ion- selective electrode) đê’ đo khí máu, chất điện giải và chất chuyền hóa. Máy phân tích trích xuất các biến số khác như kiếm dư (base excess – BE)/kiếm thiếu (base debit – BD), bicarbonate, độ bão hòa oxy của hemoglobin từ các giá trị pH, PCO2 và PaO2 đo được thông qua các thuật toán và biểu đồ. Các giá trị trích xuất được tính toán và do đó có thể không chính xác so với các giá trị đo được.
Độ bão hòa oxy của hemoglobin không tính toán được các dyshemoglobin (hemoglobin mất chức năng). Trong trường hợp này, máy đo co-oximeter sẽ thích hợp hơn vì có thể đo trực tiếp các loại hemoglobin khác nhau. Vì lý do này, một số máy phân tích khí máu hiện đại cũng tích hợp máy đo co-oximeter. Thể tích mẫu cần thiết để đo khí máu mao mạch và động mạch phụ thuộc vào máy phân tích, có thể nằm trong khoảng từ 65 đến 150 pL. Thể tích mẫu nhỏ hơn có thể cung cấp ít chất phân tích hơn hoặc không có các trị số của co-oximeter. Hiệu lực của kết quả khí máu phụ thuộc vào chức năng của máy phân tích, cách thu thập mẫu và kỹ thuật xử lý mẫu (các yêu tổ trước và sau phan tích). Mau mau được đưa vào máy phân tích phải được thu thập trong một ống tiêm hoặc ống mao dẫn thích hợp có chứa đúng chất chống đông máu.
Đảm bảo chất lượng máy phân tích khí máu
Đế đảm bảo kết quả đáng tin cậy và nhất quán, máy phân tích khí máu phải là một phần của chương trình đảm bảo chất lượng nhằm theo dõi, lập tài liệu và điều chỉnh độ chính xác của máy phân tích. Các biện pháp kiểm soát chất lượng nội bộ có thế bao gồm: Lịch trình hiệu chuẩn, kiểm soát chất lượng và bảo trì, so sánh mẫu với thiết bị phòng thí nghiệm và kiểm tra chuyên s ngoài. Thế hệ mới nhất của máy phân tích tại điểm chăm soc co chua cac goi kín dùng một lần, bao gồm: Cảm biến, điện cực, dung dịch kiểm soát chất lượng, giải pháp làm sạch và ngăn chặn chất thải. Ưu điểm của các hệ thống này là ít phải bảo trì hơn, phát hiện lỗi tốt hơn và kiểm soát chất lượng nhất quán. Ngày nay, các máy phân tích truyền thống vẫn được sử dụng, đi kèm với các yêu cầu như: Cần bảo trì nhiều hơn, chăm sóc bằng tay các điện cực, giải pháp kiểm soát chất lượng và xử trí chất thải. So sánh các phương pháp phân tích khác nhau đế đo độ bão hòa oxy được trình bày trong Bảng 10.1.
| BẢNG 10.1 Các phương pháp phân tích đế đo độ bão hòa oxy | |||||
| Thiẽt bị | Mẫu | Đo lường | Dữ liệu được báo cáo | Ưu điểm | Nhước điểm |
| Mây phán tích khí máu động mạch (ABG) | Máu | Áp lực riêng phàn cùa oxy hòa tan trong máu toán phàn tại mọt điện | PaO2, SO2 (đỏ bảo hòa oxy). Mổt só loai máy có sẳn khả nâng đo CO-oximatry | Đồng thời đo pH và PaCO2 | Xâm lấn, SaO2 có thé không chính xác néu có các loại hemoglobin bất thường |
| Máy đo CO-oximeter | Máu | Sự hấp thụ của các dân xuát Hb sử dụng nhiẽu bưóc sóng ánh sáng | SaO2, FO2Hb\ FHHba, FMetHba, FCOHba, FSHba, tổng nồng độ | Đo nồng đô của các loại Hb | Xâm lấn, thực hiện trong phòng thí nghiệm |
| Máy đo độ bão hóa oxy mạch náy | Qua da | Hấp thụ ở hai bưóc sóng (660 nm vã 940 nm) trong máu | SpO2 | Theo dõi tại giường liên tục, khổng xầm lán | Không chính xac khi có mật các chát gáy nhiều: MetHb, một só loai thuốc |
- Chữ “F” đứng trước mổi từ viết tắt đề cập đến “phân đoạn” (“íractional”), ý chỉ nồng độ phân đoạn của mỗi loại hemoglobin.
Được sao chép vá có hiệu chình tư Haymond S: Oxygen Saturation, A Guide to Laboratory Assessment (tạm dịch: Độ bão hòa oxy, hưong dản đánh giá phòng thi nghiệm). Clinical Laboratory News, ngày 10-12 tháng 2 năm 2006.
Giải thích lâm sàng về khí máu
Hiểu rõ về sinh lý học của quá trình trao đổi khí khiến việc giải thích khí trong máu trở nên tương đối đơn giản. Giảm oxy máu thường là kết quả của sự bất tương hợp thông khí-tưới máu hoặc shunt. Trong nhiều trường hợp, giảm oxy máu có thể được điều trị bằng cách đảo ngược tình trạng xẹp phổi và/hoặc giảm sức cản mạch máu phổi, hoặc ở trẻ sơ sinh bị bệnh tim bẩm sinh tím, cải thiện lưu lượng máu phổi. Mục tiêu của chúng tôi khi điều trị cho tất cả các trẻ sơ sinh là đảm bảo cung cấp oxy tối ưu đến các mô bằng cách nhắm mục tiêu độ bão hòa oxy thích hợp, mức hemoglobin và cung lượng tim đầy đủ. Tăng CO2 máu được điều trị bằng cách tăng thông khí phút, áp dụng biện pháp tăng tần số hô hấp và/hoặc thể tích khí lưu thông. Tuy nhiên, không thể chắc chắn khoảng “bình thường” và “chấp nhận được” của PaCO2 là bao nhiêu, đặc biệt
Trong phần này, chúng tôi xét đến khía cạnh sinh lý học liên quan tới việc giải thích các yếu tố cốt lõi của phân tích khí máu – pH, PCO2, BaO , bicarbonate và kiểm dư/kiêm thiếu. Máy phân tích khí máu đo trực tiếp độ pH, PCO2 và PaO2. Thông thường, các kết quả này được thu thập trong máu động mạch hoặc mẫu mao mạch động mạch hóa.
Các thành phần của xét nghiệm khí máu được đo trực tiếp
pH
Độ pH cung cấp một đánh giá tổng thể về’ toan kiềm. Độ pH của khí máu phản ánh nồng độ ion hydro ngoại bào: pH = -log[H+]. Chính xác hơn, độ pH bằng log ảm của ion hydronium (H3O+), mặc dù chúng tôi quy chiếu đến các ion hydro theo quy ước. Nồng độ ion hydro cao hơn dẫn đến độ pH thấp, và ngược lại. Bời vì pH bằng log âm của nồng độ ion hydro, nên các thay đổi lớn về nồng độ hydro dẫn đến những thay đổi nhỏ của pH.
Nồng độ các ion hydro trong máu thấp một cách đáng ngạc nhiên so với các ion thông thường khác. Ví dụ, nồng độ natri huyết thanh lớn hơn 3 triệu lần so với nóng độ của các ion hydro. Duy trì độ pH trong phạm vi bình thường đóng vai trò quan trọng đối với chức năng tế bào bình thường trong toàn cơ thể, bởi pH ảnh hưởng đến chức năng của protein và màng tế bào. Vì lý do này, cơ thể duy trì kiểm soát rất chặt chẽ nóng độ ion hydro. Hóa cảm thụ quan trong động mạch và tủy sống của chúng ta điều chỉnh thông khí dựa trên độ pH (và cả PaO2 lân PaC CỌ.
Trên toàn bộ phạm vi pH tương thích với sự sống (6,9-7,6), sự khác biệt quan sát được về nồng độ ion hydro nhỏ hơn 0,13 mmol/L. Sự kiểm soát chặt chẽ này đạt được thông qua một loạt hệ thống đệm và cơ chế bù trừ trong cơ thể. Hệ đệm quan trọng nhất là đệm carbonic acid-bicarbonate, trong đó H* và HCO3’ kết hợp để tạo thành H2COV ở trạng thái cân bằng với nước và CO2. Tỷ lệ thông thường của bicarbonate trong CO2 hòa tan là 20:1. Hemoglobin, protein bao gồm albumin và globulin, và phosphate cũng có chức năng đệm axit quan trọng. Sự xáo trộn kết quả cân bằng axit là nhiễm toan (pH thấp) hoặc nhiễm kiềm (pH cao). Phạm vi pH bình thường nằm trong khoảng 7,35 đến 7,45. Ngay cả trong các trạng thái “nhiễm toan” nghiêm trọng (ví dụ như pH 7,10), máu sẽ tương đối kiếm, vì tính trung tính toán kiếm được xác định bằng độ pH 7,0.
Ngoài chức năng đệm, hoặc trung hòa axit, axit dễ bay hơi có thể được loại bỏ khỏi cơ thể qua phổi, trong khi thận có thể’ bài tiết axit cố định và điều chỉnh nồng độ bicarbonate. Hasselbalch giới thiệu việc sử dụng thuật ngữ “bù trừ” (“compensation”) để mô tả các phương pháp điều chỉnh rối loạn toan kiềm vào năm 1915. Các cơ chế bù trừ khôi phục độ pH vẽ mức bình thường nhưng thường không dẫn đến hiệu chỉnh hoàn toàn hoặc sửa chữa quá mức độ pH. Điếu này xảy ra nếu kích thích thúc đầy sự bù trừ bị mất đi khi độ pH đạt đến mức bình thường. Ví dụ, một em bé bị nhiễm toan chuyển hóa và độ pH là 7,30 có thể làm tăng thông khí phút để loại bỏ CO2 ra khỏi cơ thể, dẫn đến độ pH tăng lên 7,35 nhưng không cao hơn. Tuy nhiên, nhiều bằng chứng gán đây cho thấy việc điều chỉnh độ pH lên hơn 7,40 ở bệnh nhân người lớn bị nhiễm toan hô hấp mãn tính đặt ra câu hỏi về hiểu biết của chúng tôi liên quan đến chủ đề này.
Một số bác sĩ lâm sàng cho rằng thuật ngữ “bù trừ” gây hiểu nhầm và khuyến cáo nên coi quá trình này như một “phản ứng thứ cấp”. Phản ứng thứ cấp của hệ hô hấp đối với sự rối loạn toan kiềm bắt đầu gần như ngay lập tức và ảnh hưởng đến độ pH trong vòng vài phút, trong khi phản ứng của thận bắt đẩu trong vòng 6 đến 12 giờ và mất 3 đến 5 ngày. Nếu độ pH bất thường, bước tiếp theo là xác định xem sự rối loạn đó là hô hấp hay chuyển hóa.
Carbon dioxide
PaCO2 thường là biến tiếp theo được kiểm tra sau khi đánh giá pH. Carbon dioxide là một sản phẩm phụ bình thường của quá trình chuyển hóa hiếu khí. PaCO2 đại diện cho áp lực riêng phần của CO2 được hòa tan trong máu. Carbon dioxide có độ hòa tan hơn 20 lần so với oxy trong máu. PaCO2 là chỉ số tốt nhất cho thấy sự đóng góp của hô hấp trong viec kiểm soát. Phạm vi bình thường của PaCO2 là 35 đến 45 mm Hg.
Phần lớn CO2 trong máu được vận chuyển đến phổi dưới dạng bicarbonate, trước khi chuyển hóa trở lại thành CO2, được thở ra và loại bỏ. Do đó, bất kỳ thao tác nào làm tăng thông khí phế nang cũng sẽ làm giảm PaCO2. Thông khí phế nang được biểu diễn bằng phương trình sau: Tần số hô hấp X (Thể tích khí lưu thông – Thể tích khoảng chết). Tăng tần số máy thở, tăng thể tích khí lưu thông và/hoặc giảm thể tích khoảng chết sẽ dẫn đến giảm PaCO,. Khoảng chết có thể chiếm tới 20% thể tích khí lưu thông ở trẻ sơ sinh cực kỳ nhẹ cân được đặt nội khí quản. Duy trì PaCO2 trong phạm vi sinh lý phụ thuộc cả vào thông khí phế nang lẫn tốc độ sản xuất CO2.
Áp lực riêng phần của oxy
PaO2 đại diện cho lượng oxy hòa tan trong huyết tương của máu và được dùng để đánh giá tình trạng oxygen hóa của bệnh nhân. Bằng cách xem xét phương trình hàm lượng oxy trong máu (Hàm lượng oxy =1,34 X Nóng độ hemoglobin X Độ bão hòa oxy/100 + 0,003 X PaO2), rõ ràng là oxy hòa tan đóng góp rất ít vào tồng lượng oxy trong cơ thể. Tuy nhiên, điếu cực kỳ quan trọng là dạng oxy hòa tan này sẽ đi vào tế bào.
Chỉ có thể đo chính xác PaO, từ máu động mạch. Vị trí xét nghiệm máu động mạch là yếu tố quan trọng cẩn xem xét ở trẻ sơ sinh còn ống động mạch, đặc biệt là trong bệnh cảnh tăng áp động mạch phổi với shunt từ phải sang trái, trong đó máu trước ống động mạch (preductal blood) sẽ có PaO2 cao hơn máu sau ống động mạch (postductal blood). Máu động mạch ở tay phải có nguồn gốc từ trước ống, trong khí máu được lấy từ chi dưới hoặc từ ỨC là máu sau ống động mạch. Mặc dù nguồn gốc của động mạch dưới đòn trái có nhiều khả năng là trước ống động mạch hơn là sau ống động mạch, nhưng siêu âm tim sẽ được yêu cầu để’ xác định điếu này. Do đó, không nên sử dụng máu lấy từ động mạch quay hoặc động mạch trụ bên trái, nếu có thể.
Thiếu oxy mô (hypoxia) là một thuật ngữ định tính dùng để’ chỉ tình trạng oxygen hóa mô không đầy đủ. Không nên nhẩm với giảm oxy máu (hypoxia), tức là chỉ số PaO2 dưới bình thường” trong máu. Các định nghĩa của oxy máu bình thường, giảm oxy máu và tăng oxy máu sẽ phụ thuộc vào điều kiện được coi là “bình thường” đối với PaO,. Thay đổi liệu pháp đề đáp ứng với tình trạng giảm oxy máu đòi hỏi bệnh nhân phải được đánh giá cẩn thận, vì có nhiều nguyên nhân gây ra tình trạng giảm oxy máu. Đánh giá tình trạng thiếu oxy mỏ bao gồm đánh giá các dấu hiệu lâm sàng của bệnh lý, gốm có sự tưới máu đẩy đù và sự nâng lóng ngực, sự hiện diện và loại nhiễm toan bao gom lactate, cũng như xét nghiệm và điều trị bệnh cơ bản. Điếu quan trọng là hướng liệu pháp đến việc điều chỉnh nguyên nhân cơ bản trước khi hiệu chỉnh nồng độ oxy một cách đơn giản.
Các thành phần của xét nghiệm khí máu không được đo trực tiếp
Các giá trị sau đây thường được báo cáo trong kết quả khí máu được lấy từ các giá trị đo khác, hoặc được tính toán bằng cách sử dụng toán đố hoặc thuật toán.
Bicarbonate
Bicarbonate là một kiếm, có nghĩa rằng đây là chất nhận hydro (HCO3‾ + H+ ↔ H2O + CO2). Do đó, nó được “tiêu thụ” khi trung hòa axit, dẫn đến nồng độ bicarbonat trong huyết thanh thấp hơn trong tình trạng nhiễm toan chuyển hóa. Nồng độ bình thường của bicarbonate trong máu là từ 22 đến 24 mEq/L. Thận đóng vai trò quan trọng trong việc cân bằng nội môi toàn kiếm thông qua tái hấp thu HCO3‾, bài tiết ammonium qua nước tiểu và tạo thành axit có thế chuẩn độ. Ngưỡng bicarbonate trong thận thường là 15 mEq/L. Trẻ sinh cực non thường bị nhiễm toan chuyển hóa do mất bicarbonat ở thận xuống đến ngưỡng này trong những tuần đầu tiên sau sinh. Sự gia tăng mãn tính PaCO2, như đã thấy ở trẻ bị loạn sản phế quản phối, cuối cùng sẽ dẫn đến tăng Học khi cơ thể có gắng duy trì tỷ lệ 20:1 giữa bicarbonate và CO2 hòa tan. Nóng độ CHO, tàng có thể trám trọng hơn do sử dụng thuốc lợi tiểu mãn tính, vì thận của trẻ sơ sinh có anion chloride thấp giữ lại anion bicarbonate. Cho bệnh nhân uống natri bicarbonat có thể làm tăng nồng độ PaCO, tạm thời tới khi phổi có thế điều chỉnh được chúng. Natri bicarbonat đã từng là phương pháp điều trị nhiễm toan lactic phổ biến. Tuy nhiên, phương pháp này đã được coi là một vấn đề nghiêm trọng và không còn được khuyến khích sử dụng. Thay vào đó, giải pháp nên chú trọng là điều chỉnh nguyên nhân cơ bản.
Nồng độ HCG được báo cáo trên kết quả khí máu không được đo trực tiếp mà được tính từ pH và PaCO2. Nó phản ánh tình trạng chuyển hóa được suy ra từ cân bằng toan kiềm. Nhiều phương pháp khác nhau đã được báo cáo trong nhiều năm để tính toán mức HCO3’ trong mẫu khí máu với một mức độ pH và PaCO, nhất định. Bicarbonate tiêu chuẩn được tính toán với máu được cân bằng với PaCO2 tại mức 40mmHg ở 37°c. Các giá trị HCO . được tính toán có thể không tạo ra chỉ số chuyển hóa đơn thuần trong quá trình giảm cũng như tăng CO2 máu và các bác sĩ lâm sàng nên tìm hiểu phương pháp mà cơ sở của họ cần sử dụng để tính toán các giá trị HCO/. Chúng tôi khuyến khích độc giả tìm hiểu các ấn phẩm mô tả chi tiết hơn về mối quan hệ giữa PaCO2, và HCO3‾.
Kiềm dư
Kiếm dư (base excess – BÊ) đê cập đến sự khác biệt giữa nồng độ đệm kiếm quan sát được và bình thường, hoặc nói theo cách khác là lượng axit hoặc bazơ cần thiết để’ đưa pH về 7,4 trong bối cảnh của PaO2 bình thường. BE thường được lấy từ toán đồ. Vì các mẫu máy phân tích khí máu khác nhau sử dụng các phương pháp tính BÉ không giống nhau, nên kết quả nhận được có thể khác nhau giữa các nhà sản xuất.
Mặc dù tên gọi có nghĩa là thừa bazơ, nhưng hiện tượng thiếu hụt có thể xảy ra khi nồng độ bazơ quan sát được ở dưới mức bình thường. Một số bác sĩ lâm sàng thích sử dụng thuật ngữ “base device” (“kiềm thiếu”) để chỉ các mức kiềm có giá trị âm và để dành thuật ngữ “BE” cho trường hợp ngược lại. BE/ basc debit là một chi số khác vé tình trạng toan kiềm chuyển hóa. Một số trung tâm có thế đo BE hoặc BE tiéu chuẩn của dịch ngoại bào. BE tiêu chuẩn được tính toán khác với BE và được phát triên như một chi sỗ độc lập với PaCO3
Giá trị BÉ bình thường ở trẻ sơ sinh nằm trong khoảng từ -3 đến + 1. Một HBE âm tính, hoặc một kiếm thiếu, được quan sát thấy trong tình trạng nhiễm toan chuyển hóa, trong khi BE dương tính xảy ra trong nhiễm kiềm chuyển hóa. BÉ được giải thích cùng với nồng độ bicarbonate.
Độ bão hòa oxy
Gác nội dung thảo luận rộng hơn vé độ bão hòa oxy đã được đề cập trước đó trong chương này. Độ bão hòa oxy động mạch (arterial oxygen saturation – SaO.) đo máy khí máu tiêu chuẩn báo cáo là một giá trị được tính toán. Vì quá trình tính toán không xem xét các loại hemoglobin không tiêu chuẩn (ví dụ như carboxyhemoglobin, methemoglobin), nên có thể đưa ra ước tính không chính xác.
Máy khí máu sử dụng phương pháp đo co-oximeter do trực tiếp nhiều loại hemoglobin và do đó cung cáp SaO, chính xác hơn.
- Phép do co-oximetry trực tiếp đo các loại hemoglobin sau:
- Oxyhemoglobin: Hemoglobin liên kết với oxy.
- Deoxyhemoglobin: Hemoglobin không liên kết với oxy.
- Carboxyhemoglobin: Hemoglobin hên két với carbon monoxide.
- Methemoglobin: Một dạng hemoglobin bị oxy hóa.
- Sulfhemoglobin: Một dạng hemoglobin bất thường không thể hèn két oxy.
Lactate
Lactate không phải là một giá trị khí máu truyền thống. Tuy nhiên, lactate thường được đo bằng nhiều máy phân tích khí máu, vì vậy cần có một cuộc thảo luận cơ bản ngắn gọn về giá trị của nó. Máy phân tích được trang bị đế đo lactate sẽ đo trực tiếp máu bằng cảm biến sinh học sử dụng các nguyên tắc đo cường độ dòng điện. Lactate là kết quả của quá trình chuyển hóa glucose
trong quá trình thiếu oxy mô, theo đó lactate, ATP và nước được tạo ra. Thiếu oxy mô và/hoặc tưới máu mô kém có thế dân đen tăng lactate máu, cũng có thể do các cơ chế khác. Nồng độ lactate trong máu là sự điều chỉnh lại độ chênh giữa sản xuất và thanh thải, trong đó gang chịu trách nhiệm về phần lớn thanh thải lactate. Nồng độ lactate trong máu bình thường đối với trẻ đủ tháng phụ thuộc vào các giá trị đã được thiết lập cục bộ và đã được báo cáo ở mức nhỏ hơn 2,0 mmol/L.
Giá trị động mạch, tĩnh mạch và mao mạch đổi với nồng độ lactate đều đã được sử dụng trên lâm sàng, với hầu hết các báo cáo đều cho thay moi tuong quan tõt giữa các loại mẫu. Nên chạy màu trong vòng 15 phút để tránh tăng nồng độ lactate trước khi xét nghiệm. Giá trị lactate đóng vai trò hữu ích trong việc đánh giá trẻ sơ sinh. Lactate đo được trong máu cuống rốn được chứng minh là phù hợp với pH và BE, đóng thời có giá trị tiên đoán tương tự đối với bệnh tật ngắn hạn so với pH và BE. Một nghiên cứu hồi cứu vẽ trẻ đủ tháng bị ngạt sau sinh so sánh giá trị dự đoán của pH, kiếm thiếu và lactate đối với tỷ lệ mắc bệnh não thiếu oxy (hypoxic encephalopathy – HIE) từ trung bình đến nặng cho thấy rằng: Nóng độ lactate cao nhất trong những giờ đầu tiên của cuộc đời là yếu tố dự báo quan trọng của HIE từ trung bình đến nặng. Đo lactate huyết thanh rất hữu ích trong việc phân biệt tăng sản xuất axit (ví dụ như do cung cấp oxy mô không đầy đủ) vì mất bicarbonate, chẳng hạn như xảy ra trong nhiễm toan ống thận.
Các lỗi trong đo khí máu
Ngay cả những bọt khí nhỏ trong mẫu khí máu cũng có thể gây ra những sai sót đáng kể. Bọt khí chứa không khí phòng, gồm bốn thành phần chính: Nitơ (78%), oxy (21%), argon (1%) và CO2 (0,04%). Không khí phòng có PACO2 gần bằng 0 và PAO2 xấp xỉ 150 mm Hg. Do đó, bọt khí làm giảm PaCO2 và có thể tăng hoặc giảm PaO2, tùy thuộc vào việc PaO2 thấp hơn hay lớn hơn 150 mm Hg. Lượng khí tiếp xúc với máu động mạch được hút qua đường truyền kim cánh bướm (tĩnh mạch da đầu) là đủ để thay đổi trị số đo PaO2. Vì vậy, điểu quan trọng là phải loại bỏ bọt khí khỏi mẫu máu trước khi đặt nó vào máy phân tích khí máu.
Pha loãng mẫu máu với dịch truyền tĩnh mạch thường sẽ làm giảm PaCO2 và tăng kiếm thiếu mà không ảnh hưởng đến độ pH. Điếu này có thể là do sự khuếch tán CO2 từ máu vào dịch truyền tĩnh mạch, nơi không chứa co,. Do khả năng đệm của máu, độ pH thay đói ít, mặc dù PaCO, giảm, làm xuất hiện nhiễm toan chuyển hóa kết hợp nhiễm kiềm hô hấp. Việc pha loãng mẫu khí máu với nhũ tương lipid dường như không ảnh hưởng gì đến các trị số đo khí máu. Heparin khô cũng không ảnh hưởng đến kết quả khí máu.
Kết quả khí máu có thế không chính xác nếu bệnh phẩm không được xử lý kịp thời, vì tế bào tiếp tục tiêu thụ oxy và tạo ra CO2 sau khi lấy mẫu. Do đó, mâu thường được đặt trên nước đá để làm chậm quá trình chuyển hóa của các tế bào trong máu. Tuy nhiên, một nghiên cứu thực nghiệm cho thấy rằng: Các mẫu ổn định đối với PaO2 và SaO2 trong tối đa 30 phút ở nhiệt độ phòng hoặc khi được giữ trong nước đá; bên cạnh đó, những thay đổi sau 60 phút là nhỏ và không có ý nghĩa lâm sàng. PaCO2 cho thấy tăng đáng kể sau 20 phút ở nhiệt độ phòng trong một thống kê, nhưng những thay đổi vé mật lâm sàng lại không đáng ké.
Hầu hết các máy phân tích khí máu đo PaO, và sau đó tính độ bão hòa với giả định rằng máu máu là của người lớn. Tuy nhiên, nếu mẫu chứa một lượng đáng ké HbF, độ bão hòa được tính toán sẽ thấp một cách bất hợp lý (do sự dịch chuyển sang trái của ODA với HbF). Nếu việc quan trọng cần làm là phải chính xác độ bão hòa của bệnh nhãn thì nên thực hiện bằng phương pháp co-oximeter.
Đánh giá độ chính xác của kết quả khí máu
Việc xác định xem kết quả khí máu có hợp lệ hay không đòi hỏi bác sĩ phải có tư^duy phản biện. Chỉ cần tồn tại một số sai sót tiềm ẩn cũng có thể ảnh hưởng xấu đến độ chính xác của kết quả khí máu. Nhìn chung, thời gian của những sai sót này có thể được chia thành các giai đoạn trước phân tích và giai đoạn phân tích.
Lỗi trước phân tích (preanalytical errors) đế cập đến các lỗi xảy ra trong khoảng thời gian trước khi xét nghiệm mẫu trong máy phân tích khí máu. Chúng bao gồm các lõi trong việc thu thập và xử lý mẫu. Phấn thảo luận dưới đây tập trung vào các lỏi trước phân tích vì đây là những lỗi mà bác sĩ lâm sàng dễ gặp nhất.
Lưu ý vé nhiệt độ: Các máy phân tích khí máu hiện đại hiệu chinh mau đến 37°c. Mặc dù đây là tiêu chuẩn trong các NICK hiện đại, nhưng có thể có những trường hợp bác sĩ lâm sàng muốn kiểm tra một mẫu không được hiệu chỉnh nhiệt độ. Ví dụ, trẻ sơ sinh bị bệnh não thiếu oxy-thiếu máu cục bộ được điều trị bằng liệu pháp hạ thân nhiệt trong thời gian 72 giờ. Nhiệt độ trung tâm cơ thể mục tiêu thường nằm trong khoảng 33,5°c đến 34,5°c. Có nên điều chỉnh mẫu này thành 37°c không? Làm như vậy có thể không tạo ra tình trạng toan kiềm thực sự của bệnh nhân vì nó sẽ thay đổi PaO2, (cao hơn ~ 15mm Hg) và PaCO2 (thấp hơn ~ 6mm Hg) được báo cáo. Có sự nhầm lẫn về cách tiếp cận tốt nhất là để hiệu chỉnh nhiệt độ trong những tình huống này. Nhiều bác sĩ lâm sàng trong các đơn vị chăm sóc đặc biệt dành cho người lớn không điều chỉnh máu về 37°C vì lý do như vậy. Bằng chứng trong dân số trẻ em ít rõ ràng hơn, khiến một số trung tâm ửng hộ việc cung cấp cả kết quả khí máu đã điều chỉnh nhiệt độ lẫn không điều chỉnh nhiệt độ cho bệnh nhân có thân nhiệt đáng kể nằm ngoài giới hạn bình thường.
Các bác sĩ lâm sàng được khuyến khích đánh giá kết quả khí máu một cách nghiêm túc để xác định độ chính xác của nó đối với bệnh nhân. Có một số cách tiếp cận được chấp nhận. Dưới đây là một cuộc thảo luận ngắn gọn về một số cách tiếp cận như vậy:
- Xem lại mối quan hệ giữa pH và sự thay đổi cấp tính của PaCO2. Giả sử tốc độ chuyển hóa bình thường và không đổi, sự gia tăng cấp tính của PaCO, là 1 mmHg gây ra sự giảm tương ứng của pH là 0,006; trong khi đó, sự giảm cấp tính của PaCO2 là 1 mmHg dẫn đến sự tăng lên 0,01 của pH. Hiểu được mối quan hệ này cho phép bác sĩ lâm sàng so sánh độ pH dự kiến và đo được. Ví dụ, sau khi PaCO, tăng cấp tính 15mmHg, pH sẽ giảm 0,09 (15 X 0,006 = 0,09), dẫn đến pH dự kiến là 7,31 (7,40 – 0,09 = 7,31). Nếu độ pH đo được khác với độ pH dự kiến ± 0,03 đơn vị thi phải có rối loạn không do hô hấp hoặc chuyển hóa.
- Trong giảm CO2 máu, pH dự kiến = 7,40 + (40 mm Hg – PaCO2) X 0,01
- Trong tăng CO2 máu, pH dự kiến = 7,40 – (PaO2 – 40mmHg) X 0,006 Kiểm tra độ chính xác độc lập này hỗ trợ bác sĩ lâm sàng đánh giá tình trạng chuyển hóa của bệnh nhân mà không cần tham khảo các giá trị HCO3‾ hoặc BE.
- Sử dụng công thức, toán đó hoặc bản đó khí máu để tính toán hoặc vẽ biểu đồ của các biến toán kiểm.
- So sánh bicarbonat huyết tương tính được với CO2 tổng.
- CO2 tổng (total CO2) là thước đo CO2 ở tất cả các trạng thái, được đo bằng máu tĩnh mạch trong quá trình kiểm tra điện giải trong phòng thí nghiệm, và là một chỉ số của bicarbonate huyết tương.
- Tổng giá trị CO2 sẽ cao hơn một chút so với bicarbonat huyết tương vì là máu tĩnh mạch; tuy nhiên, nó có thể là một cách khác để kiểm tra độ chính xác của khí máu.
- Bất kể sử dụng phương pháp nào, vấn đề quan trọng là phải xem xét tình trạng lâm sàng của bệnh nhân khi giải thích kết quả khí máu.
Kết luận
Mặc dù các giá trị khí máu động mạch thường là vô giá trong việc xử trí bệnh nhân suy hô hấp, song không nên giải thích những giá trị này khi không có dữ liệu lâm sàng. Kết quả khí máu khác biệt đáng kể so với các kết quả trước đó cả thế cho thấy tình trạng của bệnh nhân xuất hiện sự thay đổi lớn, hoặc có thể thể hiện một sai số trong phép đo khí máu. Xét nghiệm khí máu từ phòng thí nghiệm hay máy theo dõi không xâm lấn tinh vi đếu không thế thay thế việc quan sát lâm sàng cẩn thận.
Có một số công cụ trực tuyến hữu ích và thân thiện với thiết bị di động giúp giải thích khí máu ở ấn bản gốc của cuốn sách này (Goldsmiths Assisted Ventilation of the Neonate, 7th Edition) để tìm hiểu một số ứng dụng liên quan đến đánh giá khí máu ở trẻ sơ sinh do bác sĩ Satish Deo Pujari người Ấn Độ phát triển.