Bệnh tim mạch
Hướng dẫn sử dụng thuốc trong một số bệnh lý cấp cứu tim mạch
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
Nguồn: Sách Thuốc tim mạch trong thực hành lâm sàng (PGS.TS.BS. Phạm Mạnh Hùng – Ths. BSNT. Phạm Trần Linh)
Chủ đề: Hướng dẫn sử dụng thuốc trong một số bệnh lý cấp cứu tim mạch
Tác giả
Phạm Mạnh Hùng
Văn Đức Hạnh
Nhà thuốc Ngọc Anh xin giới thiệu đến bạn đọc về chủ đề Sử dụng thuốc trong một số bệnh lý cấp cứu tim mạch qua bài viết sau đây.
SỬ DỤNG THUỐC TRONG CẤP CỨU NGỪNG TUẦN HOÀN
Khái niệm ngừng tuần hoàn
Ngừng tuần hoàn là tình trạng đột ngột ngừng hoạt động của tim hoặc tim hoạt động không hiệu quả kèm theo suy sụp huyết động nhanh chóng. Trong trường hợp điển hình, tình trạng này xảy ra do nhịp nhanh thất hoặc rung thất ở bệnh nhân có tiền sử mắc bệnh lý tim cấu trúc đặc biệt là bệnh lý động mạch vành.
Dây chuyền cấp cứu ngừng tuần hoàn
Với mục đích tăng cường khả năng sống sót cho người bệnh, dây chuyền cấp cứu ngừng tuần hoàn được xây dựng trong hai tình huống: Ngừng tuần hoàn trong bệnh viện và ngừng tuần hoàn ngoài bệnh viện.
Dây chuyền cấp cứu ngừng tuần hoàn trong bệnh viện gồm năm bước:
(1) Xây dựng hệ thống giám sát và phòng tránh ngừng tuần hoàn.
(2) Nhận biết tình trạng ngừng tuần hoàn và kích hoạt hệ thống phản ứng khẩn cấp.
(3) Tiến hành hồi sinh tim phổi ngay lập tức.
(4) Khử rung (sốc điện) kịp thời.
(5) Duy trì sự sống và chăm sóc sau ngừng tuần hoàn.
Trình tự của dây chuyền cấp cứu ngừng tuần hoàn ngoài bệnh viện như sau:
(1) Nhận biết ngừng tuần hoàn và kích hoạt hệ thống phản ứng khẩn cấp.
(2) Tiến hành hồi sinh tim phổi ngay lập tức.
(3) Khử rung kịp thời.
(4) Tiến hành cấp cứu cơ bản và nâng cao.
(5) Duy trì sự sống và chăm sóc sau ngừng tuần hoàn.
Yêu cầu của hồi sinh tim phổi: đúng quy trình và đạt chất lượng cao đặc biệt chú trọng vào quá trình ép tim
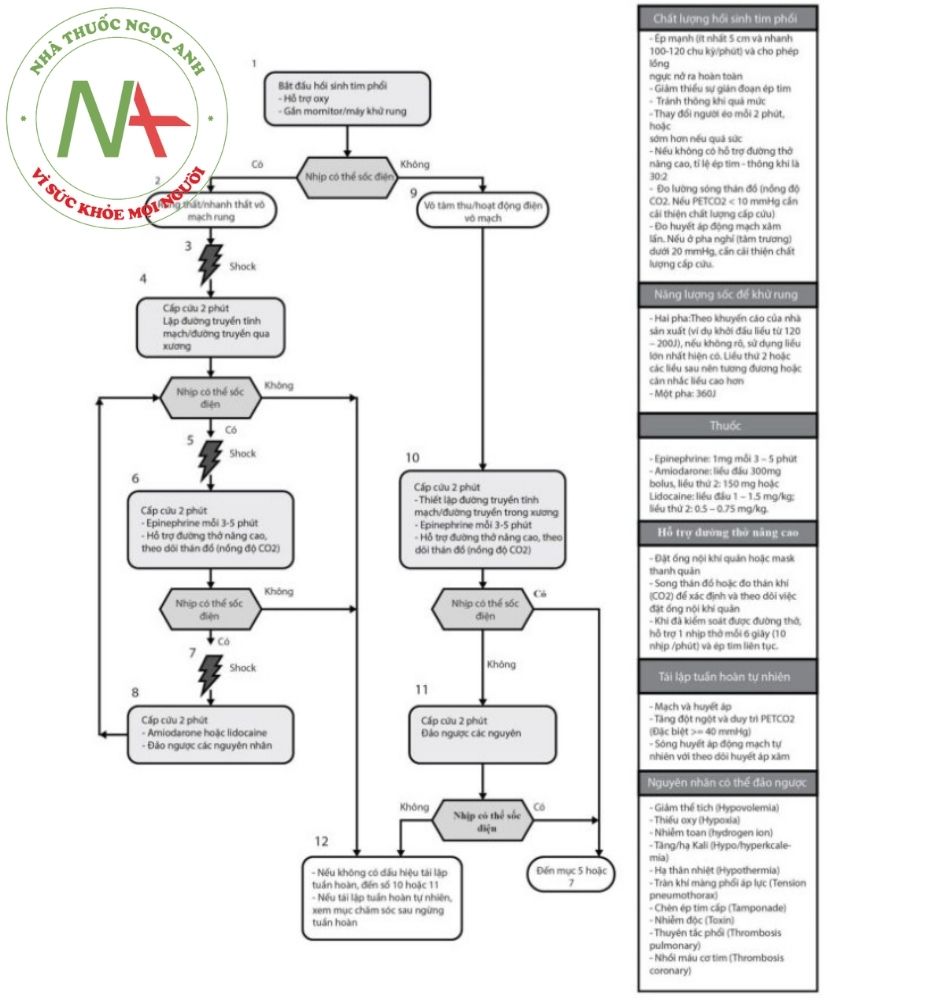
Đối với cấp cứu ngừng tuần hoàn, các khuyến cáo hiện tại đều chú trọng vào quá trình hồi sinh tim phổi (Cardiopulmonary Resuscitation – CPR), cần đảm bảo việc hồi sinh tim phổi phải đúng quy trình và đạt chất lượng cao.
Quy trình cấp cứu ngừng tuần hoàn cho một người cứu hộ được khuyến cáo như sau: người cứu hộ duy nhất sẽ bắt đầu ép tim trước khi tiến hành hô hấp nhân tạo (quy trình C-A-B).
Hồi sinh tim phổi chất lượng cao được các khuyến cáo hiện tại nhấn mạnh đặc biệt bao gồm:
Ép tim với tốc độ và biên độ vừa đủ cho phép ngực nảy lên hoàn toàn sau mỗi lần ép, giảm thiểu gián đoạn trong khi ép tim và tránh thông khí quá mức.
100 đến 120 lần/phút, biên độ ép tim ở người lớn ít nhất là 5cm nhưng không quá 6cm. Để thành ngực nảy lên hoàn toàn sau mỗi lần ép tim, người cứu hộ phải tránh đè lên ngực giữa các lần ép tim. Giảm thiểu gián đoạn trong khi ép tim nhấn mạnh tránh hiện tượng ép tim bị gián đoạn bởi các công việc khác như đặt đường truyền tĩnh mạch, đặt nội khí quản hoặc giảm thiểu thời gian từ khi ngừng ép tim tới khi bệnh nhân được sốc điện.
Để tránh thông khí quá mức, khuyến nghị tỷ lệ thông khí đơn giản là (6 giây/lần thông khí).
Vai trò của sốc điện
Các khuyến cáo hiện hành nhấn mạnh vai trò của sốc điện trong hồi sinh tim phổi trong các trường hợp ngừng tuần hoàn do nhịp nhanh thất hoặc rung thất. Nên sử dụng máy khử rung càng sớm càng tốt. Tuy nhiên, trước khi lấy được máy khử rung, người cứu hộ cần khẩn trương hồi sinh tim phổi đúng quy trình và đạt chất lượng như đề cập ở phần trên.
Vai trò của các biện pháp khác sau cấp cứu ngừng tuần hoàn
Các biện pháp điều trị sau cấp cứu ngừng tuần hoàn như hồi sức tuần hoàn, hô hấp, lọc máu… được đề cập tới ở các cuốn sách khác. Xem thêm Chương II. Cấp cứu tim mạch, Lâm sàng tim mạch học, 2019).
Sử dụng thuốc trong hồi sinh tim phổi
Trong chương sách này, chúng tôi tập trung vào phân tích việc sử dụng thuốc trong cấp cứu ngừng tuần hoàn. Các khía cạnh khác của cấp cứu ngừng tuần hoàn được đề cập trong các cuốn sách khác.
a. Adrenalin
Cập nhật cấp cứu ngừng tuần hoàn của Hội Tim Mạch Hoa Kỳ 2019 nhấn mạnh vai trò của adrenalin trong cấp cứu ngừng tuần hoàn. Adrenalin được cho rằng có lợi ích trong cấp cứu ngừng tuần hoàn do tác động kích thích alpha adrenergic (gây co mạch). Các tác động này có thể dẫn đến tăng áp lực trong động mạch vành và động mạch não trong quá trình hồi sinh tim phổi. Vai trò và an toàn của các tác động trên beta adrenergic hiện tại vẫn đang tranh cãi do các tác động này có thể tăng tiêu thụ oxy cơ tim, giảm tưới máu dưới nội tâm mạc và nguy cơ dẫn đến các rối loạn nhịp tim. Mặt khác, các tác động trên alpha adrenergic của thuốc cũng có thể gây co mạch ở mức độ vi mạch và gây hậu quả thiếu máu mô nhiều hơn.
Nhiều thử nghiệm ngẫu nhiên và không ngẫu nhiên đã được tiến hành để đánh giá vai trò của adrenalin trong cấp cứu ngừng tuần hoàn. Có thể kết luận như sau: adrenalin giúp tăng sống sót tại thời điểm ra viện, tăng khả năng sống sót tại thời điểm 30 ngày, tuy nhiên adrenalin không cải thiện biến cố thần kinh giữa các nhóm so sánh.
Đối với việc sử dụng adrenalin liều cao (0,1 – 0,2 mg/kg), giả thuyết cho rằng sử dụng adrenalin liều cao sẽ làm tăng tưới máu động mạch vành từ đó làm tăng tái lập tuần hoàn tự nhiên và tăng khả năng sống sót sau hồi sinh tim phổi. Tuy nhiên, tác dụng phụ của adrenalin liều cao ở giai đoạn sau cấp cứu ngừng tuần hoàn có thể làm mất lợi ích tiềm tàng của thuốc trong giai đoạn đang ngừng tim. Các thử nghiệm cũng chứng minh adrenalin liều cao thất bại trong việc cải thiện sống còn tại thời điểm ra viện.
Khuyến cáo của Hội Tim Mạch Hoa Kỳ năm 2019 về việc sử dụng adrenalin như sau:
- Adrenalin được chỉ định sử dụng cho các bệnh nhân ngừng tuần hoàn (khuyến cáo I, mức độ bằng chứng B-R).
- Nên sử dụng 1mg adrenalin mỗi 3 – 5 phút tiêm tĩnh mạch (khuyến cáo IIa, mức độ bằng chứng C-LD).
- Không khuyến cáo sử dụng adrenalin liều cao trong cấp cứu ngừng tuần hoàn (khuyến cáo III: không có lợi ích, mức độ bằng chứng B-R).
Về thời điểm sử dụng adrenalin trong cấp cứu ngừng tuần hoàn. Hiện chưa có thử nghiệm ngẫu nhiên có đối chứng tập trung vào việc xác định thời điểm tối ưu sử dụng adrenalin. Các nghiên cứu quan sát mặc dù có nhiều sai số nhưng phần lớn chứng minh việc sử dụng adrenalin sớm giúp tăng tỷ lệ tái lập tuần hoàn tự nhiên. Khuyến cáo của Hội Tim Mạch Hoa Kỳ năm 2019 nhấn mạnh:
Nên sử dụng adrenalin sớm trong cấp cứu ngừng tuần hoàn có nguyên nhân không phải các rối loạn nhịp cần sốc điện (khuyến cáo IIa, mức độ bằng chứng C-LD).
Nên sử dụng adrenalin sớm sau khi không tái lập được tuần hoàn do sốc điện ở những bệnh nhân ngừng tuần hoàn do rối loạn nhịp cần sốc điện.
b. Vasopressin
Vasopressin là một chất co mạch ngoại vi không phải adrenergic, thuốc này có khả năng gây co mạch vành và mạch thận. Các thử nghiệm lâm sàng ngẫu nhiên có đối chứng đến thời điểm năm 2020 cho thấy việc sử dụng vasopressin từ đầu không chứng minh mang lại bất kỳ lợi ích nào so với adrenalin và việc kết hợp vasopressin với adrenalin cũng không mang lại lợi ích khác biệt so với sử dụng adrenalin đơn thuần. Do không cung cấp được các bằng chứng có lợi của vasopressin, đồng thuận của Hội Tim Mạch Hoa Kỳ 2020 nhấn mạnh việc duy trì chỉ sử dụng adrenalin đơn độc như một chất co mạch trong cấp cứu ngừng tuần hoàn.
c. Amiodarone và lidocaine
Trong 2 thử nghiệm ngẫu nhiên mù đôi tiến hành trên đối tượng có rung thất/nhịp nhanh thất vô mạch phục hồi bằng sốc điện ngoài bệnh viện, các bệnh nhân đã nhận được ít nhất 3 lần sốc điện và tiêm adrenaline.
Thống kê cho thấy những bệnh nhân được truyền amiodarone có khả năng cải thiện sống còn tại thời điểm nhập viện cao hơn so với nhóm không được truyền amiodarone.
Tương tự, nhiều thử nghiệm sau đó chứng minh amiodarone 300mg có khả năng cải thiện sống còn tại thời điểm nhập viện tốt hơn so với nhóm đối chứng. Các thử nghiệm này không khảo sát thời điểm hoặc cách thức phối hợp giữa amiodarone với adrenaline. Không có thử nghiệm nào được tiến hành đánh giá vai trò của amiodarone ở bệnh nhân ngừng tuần hoàn trong bệnh viện.
Truyền tĩnh mạch lidocaine – một thuốc chống rối loạn nhịp tim phổ biến đã được tiến hành trong nhiều thử nghiệm ở những bệnh nhân ngừng tuần hoàn ngoài bệnh viện. Các thử nghiệm so sánh giữa nhóm bệnh nhân được truyền amiodarone hoặc lidocaine với nhóm placebo cho thấy không có sự khác biệt có ý nghĩa thống kê về mặt sống còn giữa nhóm bệnh nhân được truyền amiodarone và lidocaine nhưng những bệnh nhân ở hai nhóm này có tỷ lệ sống còn cao hơn có ý nghĩa so với nhóm placebo. Hiện không có thử nghiệm nào đánh giá hiệu quả của lidocaine trong các trường hợp ngừng tuần hoàn trong bệnh viện.
Khuyến cáo của Hội Tim Mạch Hoa Kỳ năm 2018 đối với việc sử dụng amiodarone và lidocaine như sau:
Amiodarone hoặc lidocaine có thể được cân nhắc sử dụng trong trường hợp rung thất hoặc nhịp nhanh thất vô mạch không đáp ứng với sốc điện. Các thuốc này có thể đặc biệt hiệu quả ở bệnh nhân ngừng tuần hoàn có người chứng kiến và được sử dụng thuốc sớm (khuyến cáo IIb, mức độ bằng chứng B-R).
Trong lược đồ cấp cứu ngừng tuần hoàn năm 2018, Hội Tim Mạch Hoa Kỳ khuyến cáo phác đồ sử dụng amiodarone và lidocaine như sau:
Tiêm tĩnh mạch amiodarone liều đầu tiên 300 mg, liều thứ hai 150 mg hoặc
Tiêm tĩnh mạch lidocaine liều đầu tiên 1–1,5 mg/kg, liều thứ hai 0,5–0,75 mg/kg.
Sau khi tái lập tuần hoàn tự nhiên, vai trò của lidocain vẫn còn nhiều tranh cãi do thiếu các bằng chứng về lợi ích. Hội Tim Mạch Hoa Kỳ khuyến cáo về sử dụng lidocaine sau khi tái lập tuần hoàn tự nhiên như sau:
Hiện tại thiếu các bằng chứng về việc sử dụng lidocain ở giai đoạn sớm (trong vòng 1h) sau khi tái lập tuần hoàn tự nhiên.
Nếu không có chống chỉ định, cân nhắc sử dụng lidocain để dự phòng trong một số tình huống đặc biệt khi điều kiện điều trị rung thất hoặc nhịp nhanh thất vô mạch bị hạn chế (ví dụ trong quá trình vận chuyển cấp cứu) (khuyến cáo IIb, mức độ bằng chứng C-LD).
d. Magie
Magie hoạt động giống như một chất giãn mạch và là một co-factor quan trọng trong điều chỉnh nồng độ natri, kali và canxi qua màng tế bào. Một số thử nghiệm đánh giá vai trò của magie cho thấy magie không cải thiện tái lập tuần hoàn tự nhiên hoặc sống còn khi ra viện. Magie thường được chỉ định trong điều trị xoắn đỉnh nhưng vai trò thực sự là dự phòng tái phát xoắn đỉnh hơn là tác động điều trị. Mặt khác các thử nghiệm về vai trò của magie ở người bệnh xoắn đỉnh chỉ dừng lại ở một số nghiên cứu quan sát với cỡ mẫu nhỏ mà chưa có thử nghiệm ngẫu nhiên có đối chứng nào được công bố.
Hội Tim Mạch Hoa Kỳ năm 2018 khuyến cáo sử dụng magie như sau:
Không khuyến cáo sử dụng thường quy magie trong cấp cứu ngừng tuần hoàn ở người lớn (khuyến cáo III: không có lợi, mức độ khuyến cáo C-LD).
Cân nhắc sử dụng magie ở bệnh nhân xoắn đỉnh (khuyến cáo IIb, mức độ khuyến cáo C-LD).
e. Chẹn beta giao cảm
Năm 2015 Hội Tim Mạch Hoa Kỳ đưa ra khuyến cáo về sử dụng chẹn beta trong cấp cứu ngừng tuần hoàn: hiện thiếu các bằng chứng về việc sử dụng thường quy thuốc chẹn beta giao cảm sau cấp cứu ngừng tuần hoàn.
Tuy nhiên, có thể cân nhắc khởi đầu hoặc tiếp tục sử dụng thuốc chẹn beta giao cảm đường uống hoặc đường tĩnh mạch sau khi nhập viện ở bệnh nhân ngừng tuần hoàn do rung thất hoặc nhịp nhanh thất vô mạch (khuyến cáo IIb, mức độ khuyến cáo C-LD).
Năm 2018, sau khi xem xét lại các dữ liệu cũng như các nghiên cứu, Hội Tim Mạch Hoa Kỳ năm 2018 không đưa ra khuyến cáo về việc sử dụng chẹn beta giao cảm sau cấp cứu ngừng tuần hoàn do thiếu các bằng chứng về lợi ích trong sử dụng thường quy thuốc chẹn beta giao cảm ở giai đoạn sớm (trong vòng 1h) sau khi tái lập tuần hoàn tự nhiên. Vai trò của thuốc này vẫn là một dấu hỏi và cần thời gian cũng như các thử nghiệm để khẳng định vai trò của thuốc ở bệnh nhân sau cấp cứu ngừng tuần hoàn.
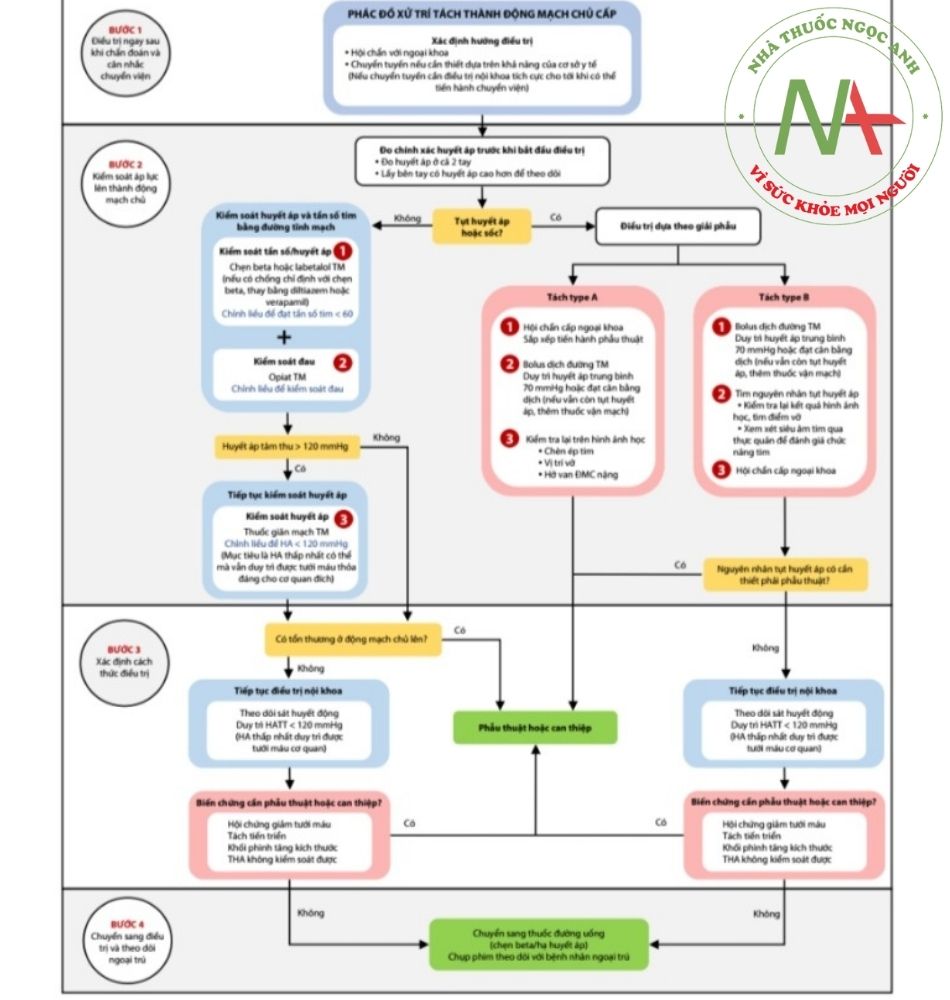
SỬ DỤNG THUỐC TRONG BỆNH LÝ TÁCH THÀNH ĐỘNG MẠCH CHỦ CẤP
Tách thành động mạch chủ (ĐM chủ) là một trong những bệnh lý tim mạch có tiên lượng tử vong ngắn hạn nặng nề nhất. Trong giai đoạn cấp tính, bệnh có diễn biến phức tạp đòi hỏi cần có chiến lược xử trí cấp cứu kịp thời và nhanh chóng.
Phân loại
Được áp dụng rộng rãi trên lâm sàng, gồm tách thành động mạch chủ Stanford type A (vị trí tách ở động mạch chủ lên) hoặc tách thành động mạch chủ Stanford type B (vị trí tách ở dưới chỗ xuất phát của động mạch dưới đòn trái).
Tách thành động mạch chủ cấp (<14 ngày) và tách thành động mạch chủ mạn tính ≥14 ngày).
Ngoài ra còn có phân loại khác như Debakey nhưng ít áp dụng hơn trên lâm sàng.
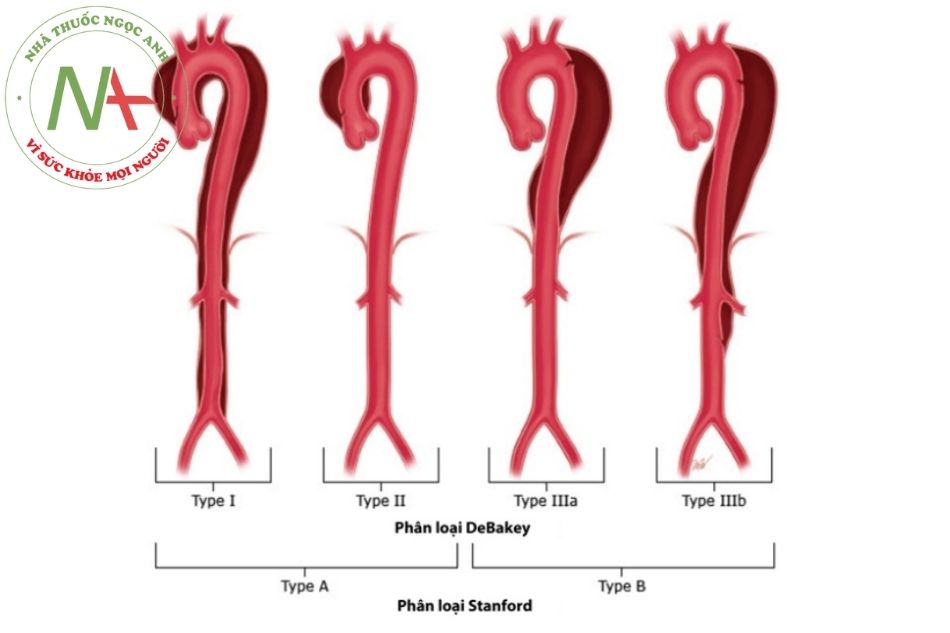
Stanford A: tổn thương liên quan tới ĐM chủ lên
Stanford B: tổn thương không bao gồm ĐM chủ lên
Nguyên tắc điều trị
Tách thành động mạch chủ Stanford type A: Phẫu thuật.
Tách thành động mạch chủ Stanford type B có biến chứng: Phẫu thuật hoặc can thiệp đặt stent graft động mạch chủ.
Tách thành động mạch chủ Stanford type B không có biến chứng: Điều trị nội khoa.
Điều trị nội khoa trước phẫu thuật, trước can thiệp stent graft cần được tiến hành ngay tại thời điểm chẩn đoán và cần nhanh chóng đạt được mục tiêu về kiểm soát nhịp tim, huyết áp và giảm đau nhưng tuyệt đối không được gây trì hoãn phẫu thuật và can thiệp stent graft.
Khuyến cáo điều trị tách thành động mạch chủ cấp của ESC 2014
Ở tất cả các bệnh nhân tách thành động mạch chủ, điều trị nội khoa bao gồm giảm đau và kiểm soát huyết áp: khuyến cáo I, mức độ chứng cứ C.
Khuyến cáo phẫu thuật cấp cứu cho các bệnh nhân tách thành động mạch chủ type A: khuyến cáo I, mức độ chứng cứ B.
Tách thành động mạch chủ type A kèm tổn thương tưới máu cơ quan, chiến lược hybrid (thay động mạch chủ lên và/hoặc quai động mạch chủ kèm can thiệp động mạch chủ hoặc can thiệp động mạch nhánh) cần được cân nhắc: khuyến cáo IIa, mức độ chứng cứ B.
Tách thành động mạch chủ type B không kèm biến chứng, khuyến cáo điều trị nội khoa: khuyến cáo I, mức độ C.
Tách thành động mạch chủ type B, TEVAR nên cân nhắc chỉ định: khuyến cáo IIa, mức độ chứng cứ B.
Ở những bệnh nhân tách thành động mạch chủ type B có biến chứng, TEVAR được khuyến cáo sử dụng: khuyến cáo I, mức độ chứng cứ C.
Ở những bệnh nhân tách thành động mạch chủ type B có biến chứng, phẫu thuật nên được cân nhắc sử dụng: khuyến cáo IIb mức độ chứng cứ C.
Mục đích chính của điều trị nội khoa trong bệnh lý tách thành động mạch chủ: Giảm tiến triển xé thêm của đoạn động mạch chủ tổn thương bằng cách giảm nhịp tim, giảm huyết áp và giảm co bóp cơ tim.
Yếu tố tác động lên quá trình tiến triển xé thêm của đoạn động mạch chủ tổn thương
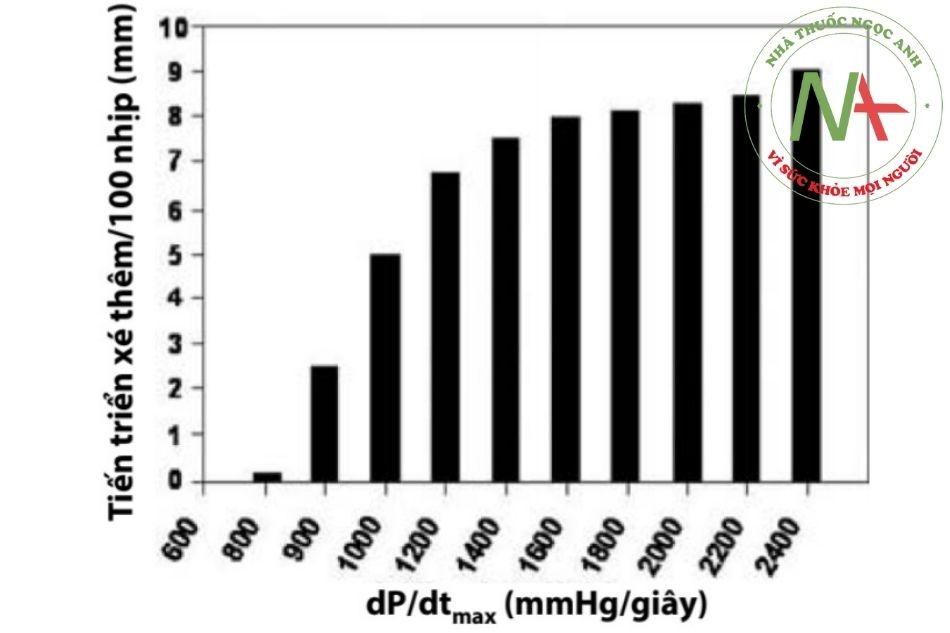
Chú thích: dP/dt : vận tốc co bóp của tâm thất. (Nguồn: Marina Feldman, et al. Medical Management of Acute Type A Aortic Dissection. Ann Thorac Cardiovasc Surg 2009;15(5):286-93)
Áp lực tác động lên thành động mạch chủ (aortic wall stress) là yếu tố gây xé thêm đoạn động mạch chủ tổn thương. Yếu tố chính ảnh hưởng tới áp lực tác động lên thành động mạch chủ là vận tốc co bóp của tâm thất (velocity of ventricular contraction – dP/dt), tốc độ co bóp tâm thất (the rate of ventricular contraction) và huyết áp.
Cần sử dụng đầu tiên các thuốc chẹn beta giao cảm để kiểm soát các yếu tố trên bằng cách giảm nhịp tim và huyết áp thấp nhất mà vẫn duy trì tưới máu tạng trong cơ thể. Mục tiêu ban đầu trong điều trị nội khoa là nhịp tim nhỏ hơn 60 chu kì/phút và huyết áp tâm thu từ 100 – 120 mmHg.
Điều trị nội khoa
a. Kiểm soát nhịp tim và kiểm soát huyết áp bằng thuốc chẹn beta giao cảm truyền tĩnh mạch:
Truyền tĩnh mạch ngay từ ban đầu thuốc chẹn beta giao cảm như propranolol, metoprolol, labetalol hoặc esmolol là lựa chọn tối ưu.
Những bệnh nhân có chống chỉ định với chẹn beta giao cảm như hen phế quản nặng, suy tim sung huyết hoặc bệnh phổi tắc nghẽn mạn tính có thể cân nhắc sử dụng esmolol vì thời gian bán thải ngắn.
Labetalol là thuốc chẹn cả alpha và beta receptor nên có ưu điểm kiểm soát tốt cả nhịp tim và huyết áp mà có thể không cần thêm các thuốc giãn mạch.
Những bệnh nhân không dung nạp với thuốc chẹn beta giao cảm, có thể thay thế bằng thuốc chẹn kênh canxi loại nondihydropyridine (verapamil hoặc diltiazem).
Chưa rõ vai trò của thuốc chẹn beta giao cảm, verapamil hoặc diltiazem trong việc kiểm soát tần số tim ở người bệnh hở van động mạch chủ mức độ có ý nghĩa vì tác động tăng nhịp tim phản xạ.
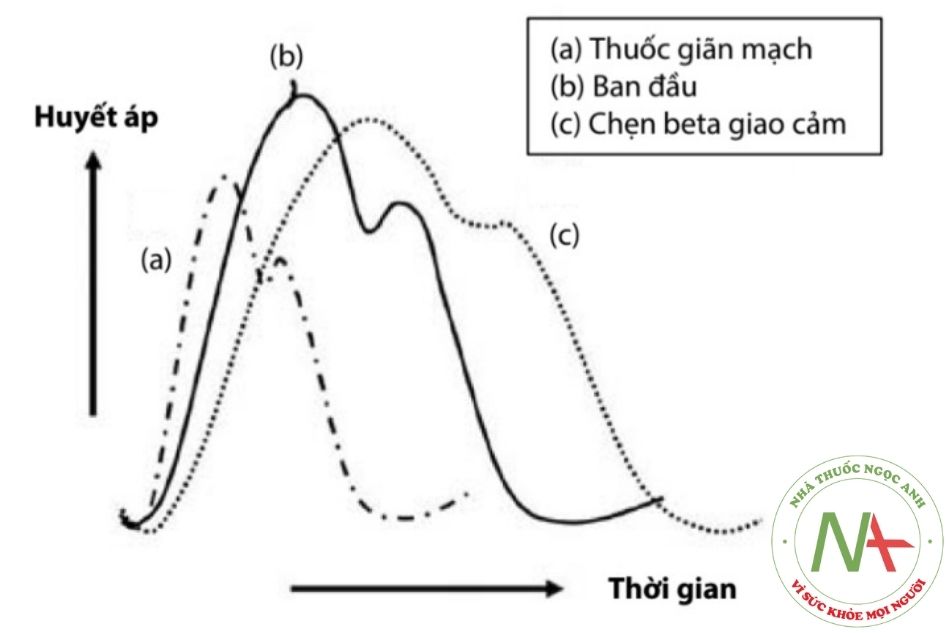
Đường (a) dưới tác động của thuốc giãn mạch sẽ gây hạ huyết áp nhưng gây tăng nhịp tim phản xạ, đường (b) là tình trạng ban đầu, lưu ý cả tình huống (a) và (b) đều làm tăng dP/dt, đường (c) dưới tác động của thuốc chẹn beta giao cảm sẽ gây giảm hạ huyết áp mức độ vừa phải nhưng gây giảm nhịp tim từ đó giảm dP/dt. (Nguồn: Marina Feldman, et al. Medical Management of Acute Type A Aortic Dissection. Ann Thorac Cardiovasc Surg 2009;15(5):286-93)
b. Phối hợp truyền tĩnh mạch chẹn beta giao cảm với truyền tĩnh mạch thuốc hạ huyết áp khác:
Kiểm soát huyết áp ở bệnh nhân tách thành động mạch chủ cấp thực sự là một thách thức trong thực hành lâm sàng. Nhiều trường hợp cần sử dụng phối hợp nhiều loại thuốc huyết áp khác nhau để kiểm soát huyết áp. Sau khi khởi đầu bằng thuốc chẹn beta giao cảm, thuốc giãn mạch có thể được chỉ định để kiểm soát huyết áp.
Truyền tĩnh mạch nitroprusside sodium là lựa chọn tốt vì dễ dàng tăng liều thuốc. Ngoài ra, nicardipine, nitroglycerin, fenoldopam và các thuốc giãn mạch truyền tĩnh mạch khác có thể chỉ định trong trường hợp này.
Thuốc giãn mạch nếu không có sự khởi đầu của thuốc chẹn beta giao cảm có thể gây tăng nhịp tim phản xạ và tăng lực co bóp tâm thất từ đó làm tiến triển nặng thêm bệnh lý tách thành động mạch chủ.
Sau khi ổn định huyết áp bằng các thuốc truyền tĩnh mạch, hầu hết bệnh nhân cần các thuốc hạ huyết áp tác dụng kéo dài để điều trị bao gồm thuốc chẹn beta giao cảm kèm các nhóm thuốc khác. Thuốc ức chế men chuyển hoặc ức chế thụ thể có thể làm chậm lại quá trình giãn động mạch chủ và có thể được chỉ định.
c. Kiểm soát đau bằng truyền opiate tĩnh mạch:
Kiểm soát đau đóng vai trò quan trọng trong giảm các kích thích giao cảm từ đó giúp giảm nhịp tim và giảm huyết áp và giảm tiến triển tách thành động mạch chủ. Cần kiểm soát đau ngay tại thời điểm vào viện bằng các thuốc giảm đau opiate truyền tĩnh mạch do các thuốc giảm đau thông thường không đáp ứng giảm cảm giác đau ở bệnh nhân tách thành động mạch chủ.
d. Xử trí khi bệnh nhân bị tụt huyết áp
Tụt huyết áp ở bệnh nhân tách thành động mạch chủ là một triệu chứng nặng, cảnh báo bệnh nhân có thể mắc biến chứng của tách thành động mạch chủ với tiên lượng tử vong rất cao.
Các nguyên nhân gây tụt huyết áp ở bệnh nhân tách thành động mạch chủ bao gồm: tràn máu màng ngoài tim do vỡ động mạch chủ vào khoang màng ngoài tim, hở van động mạch chủ nhiều, tắc nghẽn lòng thật do lòng giả quá to đè ép hoặc nhồi máu cơ tim cấp. Tất cả các trường hợp này cần phẫu thuật cấp cứu, riêng tràn máu màng ngoài tim gây ép tim cần được dẫn lưu màng ngoài tim trước mổ để tránh ép tim cấp.
Tụt huyết áp hoặc sốc tại thời điểm nhập viện có thể do vỡ lòng giả vào các cấu trúc lân cận (màng phổi hoặc trung thất) và cũng cần phẫu thuật cấp cứu ngay lập tức.
Điều trị nội khoa ban đầu với mục đích nâng huyết áp để đảm bảo tưới máu mô bao gồm truyền dịch, truyền các thuốc tăng co mạch và/hoặc các thuốc tăng co bóp cơ tim. Lưu ý, các thuốc tăng co mạch có khả năng gây tiến triển thêm lòng giả, các thuốc tăng co bóp cơ tim có thể liên quan tới việc làm tăng lực và vận tốc co bóp tâm thất và có thể làm tăng mức độ xé động mạch chủ.
VIÊM CƠ TIM CẤP
Viêm cơ tim là tình trạng bệnh lý được đặc trưng bởi các biểu hiện lâm sàng phức tạp từ không có triệu chứng cho đến các dấu hiệu suy tim, rối loạn nhịp tim… rầm rộ nặng nề với tiên lượng tử vong rất cao. Chẩn đoán nghi ngờ viêm cơ tim dựa vào các biểu hiện lâm sàng và các phương pháp thăm dò không xâm nhập. Chẩn đoán xác định dựa vào các tiêu chuẩn giải phẫu bệnh trên mô bệnh sinh thiết cơ tim.
Điều trị viêm cơ tim bao gồm các biện pháp điều trị thông thường như điều trị suy tim, điều trị rối loạn nhịp tim và hồi sức cũng như các biện pháp điều trị bằng các thuốc ức chế miễn dịch. Tuy nhiên, vai trò và tác dụng của các thuốc điều trị ức chế miễn dịch vẫn đang còn tranh cãi và chưa được đưa vào trong các khuyến cáo thực hành với mức độ bằng chứng cao.
Điều trị suy tim
Điều trị các bệnh nhân suy tim có phân số tống máu giảm và huyết động ổn định bằng các thuốc như lợi tiểu, sử dụng sớm ức chế men chuyển hoặc ức chế thụ thể angiotensin và chẹn beta giao cảm. Trong trường hợp bệnh nhân sử dụng các thuốc trên còn triệu chứng suy tim, có thể kết hợp thêm với thuốc kháng aldosteron để tăng hiệu quả tác dụng.
Ức chế men chuyển và chẹn beta giao cảm có thể có lợi ích đặc biệt ở những bệnh nhân viêm cơ tim có phân số tống máu giảm. Các thuốc sẽ giúp cải thiện tử vong và các biến cố tim mạch khác. Một nghiên cứu trên chuột cho thấy sử dụng captopril vào ngày thứ 3 ở chuột viêm cơ tim do coxsackie virus sẽ giúp giảm hoại tử cơ tim. Mặt khác, sử dụng chẹn beta giao cảm sẽ cải thiện các biến cố tim mạch ở chuột viêm cơ tim do coxsackie virus.
Mặc dù digoxin có tác dụng cải thiện triệu chứng ở bệnh nhân suy tim có phân số tống máu giảm nhưng hiệu quả trên biến cố tim mạch và an toàn vẫn chưa được chứng minh thậm chí digoxin làm tăng nguy cơ tử vong ở chuột viêm cơ tim.
Những bệnh nhân có huyết động không ổn định có thể cần hỗ trợ tuần hoàn ngoài cơ thể bằng thiết bị hỗ trợ thất hoặc ECMO (extracorporeal membrane oxygenation).
Hỗ trợ thất trái
Hỗ trợ thất trái được chỉ định khi suy tim cấp mức độ nặng hoặc trường hợp sốc tim không đáp ứng điều trị nội khoa. Trong một số trường hợp, các thiết bị này như cầu nối giúp bệnh nhân hồi phục sau giai đoạn viêm cơ tim cấp mức độ nặng.
Điều trị rối loạn nhịp tim
Bệnh nhân viêm cơ tim có thể gặp các rối loạn nhịp nhanh hoặc rối loạn nhịp chậm.
a. Các rối loạn nhịp nhanh bao gồm: Nhịp nhanh trên thất và nhịp nhanh thất.
Cơn nhịp nhanh trên thất: có thể là khởi đầu của tình trạng suy tim hoặc là tác nhân gây suy tim nặng thêm:
Chuyển nhịp xoang là ưu tiên hàng đầu trong điều trị các cơn tim nhanh trên thất này.
Chiến lược chuyển nhịp xoang, kiểm soát tần số thất tương tự như chiến lược xử trí cơn tim nhanh trên thất.
Đối với cơn tim nhanh thất:
- Các cơn nhịp nhanh thất không bền bỉ có triệu chứng có thể sử dụng các thuốc điều trị rối loạn nhịp.
- Đối với nhịp nhanh thất có triệu chứng cần xử trí bằng sốc điện, đối với rối loạn nhịp tái phát nên được điều trị ngay bằng thuốc chống rối loạn nhịp.
b. Đối với các rối loạn nhịp chậm có triệu chứng hoặc block nhĩ thất hoàn toàn cần đặt máy tạo nhịp tạm thời và theo dõi tình trạng nhịp tim, các rối loạn nhịp này thường chỉ tạm thời và có thể hồi phục.
Sử dụng thuốc chống đông
Chỉ định dùng thuốc chống đông ở bệnh nhân viêm cơ tim bao gồm:
- Các chỉ định thường quy như có bằng chứng của tắc mạch hệ thống hoặc huyết khối trong thất trái.
- Đối với các bệnh nhân rung nhĩ cần đánh giá nguy cơ tắc mạch để chỉ định dùng chống đông.
- Cần đánh giá lại việc dùng chống đông nếu hồi phục hoàn toàn tình trạng rung nhĩ và suy tim.
Lưu ý: Bệnh nhân suy tim nhịp xoang có hoặc không có tình trạng giảm phân số tống máu không có chỉ định dùng thuốc chống đông.
Xem thêm:
Thuốc điều trị rối loạn nhịp tim: Phân loại và lưu ý khi sửa dụng
TÀI LIỆU THAM KHẢO
- European Heart Rhythm Association, Heart Rhythm Society, Zipes DP, et al. ACC/AHA/ESC 2006 guidelines for management of patients with ventricular arrhythmias and the prevention of sudden cardiac death: a report of the American College of Cardiology/American Heart Association Task Force and the European Society of Cardiology Committee for Practice Guidelines (Writing Committee to Develop Guidelines for Management of Patients With Ventricular Arrhythmias and the Prevention of Sudden Cardiac Death). J Am Coll Cardiol 2006;48:e247.
- Kleinman M.E, Brennan E.E, Goldberger Z.D, et al. 2015 American Heart Association Guidelines Update for Cardiopulmonary Resuscitation and Emergency Cardiovascular Care. Part 5: Adult Basic Life Support and Cardiopulmonary Resuscitation Quality. Circulation. 2015;132[suppl 2]:S414–S435.
- Panchal A.R, Berg K.M, Kudenchuk P.J, et al. 2018 American Heart Association Focused Update on Advanced Cardiovascular Life Support Use of Antiarrhythmic Drugs During and Immediately After Cardiac Arrest. An Update to the American Heart Association Guidelines for Cardiopulmonary Resuscitation and Emergency Cardiovascular Care. Circulation. 2018;138:e740–e749.
- Panchal A.R, Berg K.M, Hirsch K.G, et al. 2019 American Heart Association Focused Update on Advanced Cardiovascular Life Support: Use of Advanced Airways, Vasopressors, and Extracorporeal Cardiopulmonary Resuscitation During Cardiac Arrest An Update to the American Heart Association Guidelines for Cardiopulmonary Resuscitation and Emergency Cardiovascular Care. Circulation. 2019;140:e881–e894.
- Tsai TT, Nienaber CA, Eagle KA. Acute aortic syndromes. Circulation. 2005;112:3802–13.
- Schwab CW, Lawson RB, Lind JF, et al. Aortic injury: comparison of supine and upright portable chest films to evaluate the widened mediastinum. Ann Emerg Med. 1984;13:896 –Panchal A.R, Berg K.M, Hirsch K.G, et al. 2019 American Heart Association Focused Update on Advanced Cardiovascular Life Support: Use of Advanced Airways, Vasopressors, and Extracorporeal Cardiopulmonary Resuscitation During Cardiac Arrest An Update to the American Heart Association Guidelines for Cardiopulmonary Resuscitation and Emergency Cardiovascular Care. Circulation. 2019;140:e881–e894.
- Tsai TT, Nienaber CA, Eagle KA. Acute aortic syndromes. Circulation. 2005;112:3802–13.
- Schwab CW, Lawson RB, Lind JF, et al. Aortic injury: comparison of supine and upright portable chest films to evaluate the widened mediastinum. Ann Emerg Med. 1984;13:896 –9.9.
- Eggebrecht H, Schmermund A, von Birgelen C, et al. Resistant hypertension in patients with chronic aortic dissection. J Hum Hypertens. 2005;19:227–31.
- Kim KH, Moon IS, Park JS, et al. Nicardipine hydrochloride injectable phase IV open-label clinical trial: study on the anti-hypertensive effect and safety of nicardipine for acute aortic dissection. J Int Med Res. 2002;30:337– 45.
- Hiratzka LF, Bakris GL, Beckman JA, et al. 2010 ACCF/AHA/AATS/ACR/ASA/SCA/SCAI/SIR/STS/SVM Guidelines for the Diagnosis and Management of Patients With Thoracic Aortic Disease. J Am Coll Cardiol 2010;55:e27–129.
- Erbel R, Aboyans V, Boileau C, et al. 2014 ESC guidelines on the diagnosis and treatment of aortic diseases. European Heart Journal (2014) 35, 2873–2926.
- Isselbacher EM, Cigarroa JE, Eagle KA. Cardiac tamponade complicating proximal aortic dissection. Is pericardiocentesis harmful? Circulation. 1994;90:2375– 8.
- Kaji S, Nishigami K, Akasaka T, et al. Prediction of progression or regression of type A aortic intramural hematoma by computed tomography. Circulation. 1999;100:II281– 6.
- Motoyoshi N, Moizumi Y, Komatsu T, et al. Intramural hematoma and dissection involving ascending aorta: the clinical features and prognosis. Eur J Cardiothorac Surg. 2003;24:237– 42.
- Moizumi Y, Komatsu T, Motoyoshi N, et al. Management of patients with intramural hematoma involving the ascending aorta. J Thorac Cardiovasc Surg. 2002;124:918 –24.
- Sanz J, Einstein AJ, Fuster V. Acute aortic dissection: anti-impulse therapy. In: Elefteriades J ed.; Acute Aortic Disease. New York: Informa Healthcare, 2007; pp 229–50.
- Rezkalla S, Kloner RA, Khatib G, Khatib R. Effect of delayed captopril therapy on left ventricular mass and myonecrosis during acute coxsackievirus murine myocarditis. Am Heart J 1990; 120:1377.
- Tominaga M, Matsumori A, Okada I, et al. Beta Blocker treatment of dilated cardiomyopathy. Beneficial effect of carteolol in mice. Circulation 1991; 83:2021.
- Matsumori A, Igata H, Ono K, et al. High doses of digitalis increase the myocardial production of proinflammatory cytokines and worsen myocardial injury in viral myocarditis: a possible mechanism of digitalis toxicity. Jpn Circ J 1999; 63:934.
- Rockman HA, Adamson RM, Dembitsky WP, et al. Acute fulminant myocarditis: long term followup after circulatory support with left ventricular assist device. Am Heart J 1991; 121:922.
- Chen JM, Spanier TB, Gonzalez JJ, et al. Improved survival in patients with acute myocarditis using external pulsatile mechanical ventricular assistance. J Heart Lung Transplant 1999;18:351.

