Valsartan
Biên soạn và Hiệu đính
Dược sĩ Xuân Hạo
Danh pháp
Tên chung quốc tế
Tên danh pháp theo IUPAC
(2S)-3-methyl-2-[pentanoyl-[[4-[2-(2H-tetrazol-5-yl)phenyl]phenyl]methyl]amino]butanoic acid
Nhóm thuốc
Đối kháng thụ thể angiotensin II
Mã ATC
C – Hệ tim mạch
C09 – Thuốc có tác dụng trên hệ Renin – Angiotensin
C09C – Các chất đối kháng Angiotesin II, đơn chất
C09CA – Các chất đối kháng Angiotesin II, đơn chất
C09CA03 – Valsartan
Phân loại nguy cơ cho phụ nữ có thai
D
Mã UNII
80M03YXJ7I
Mã CAS
137862-53-4
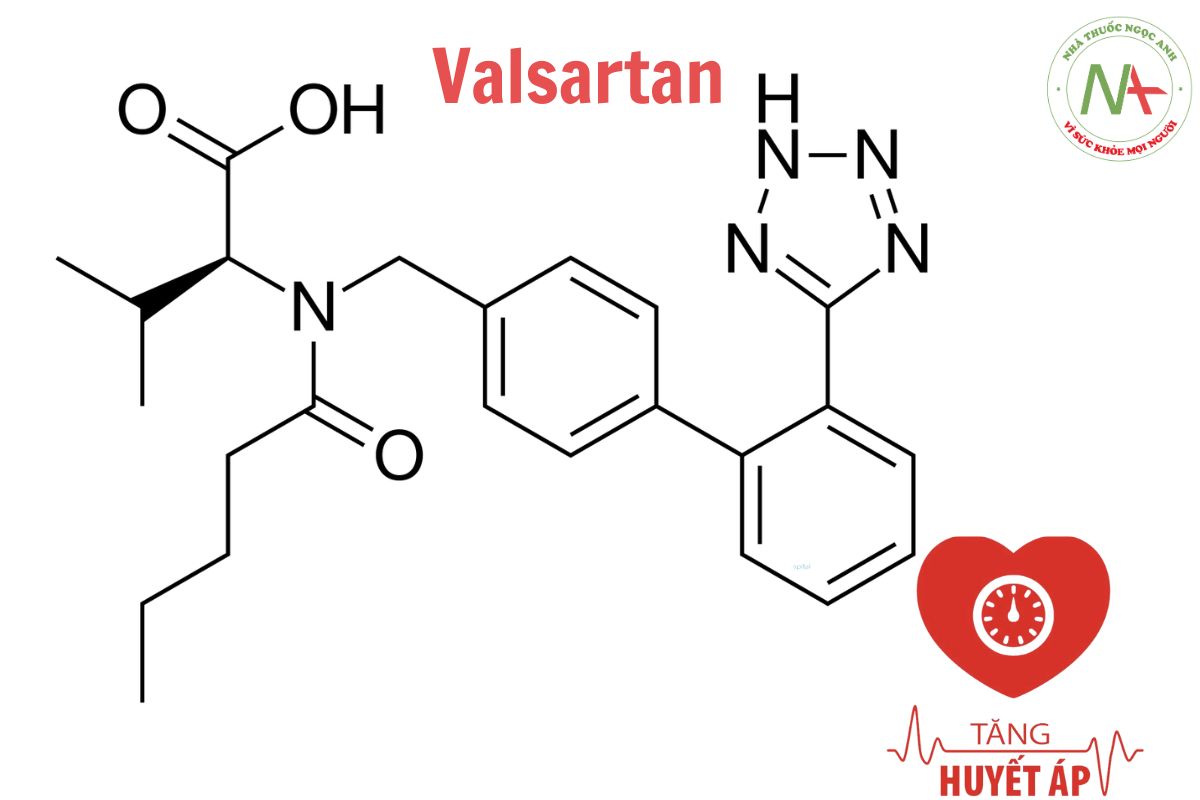
Cấu trúc phân tử
Công thức phân tử
C24H29N5O3
Phân tử lượng
435.5
Cấu trúc phân tử
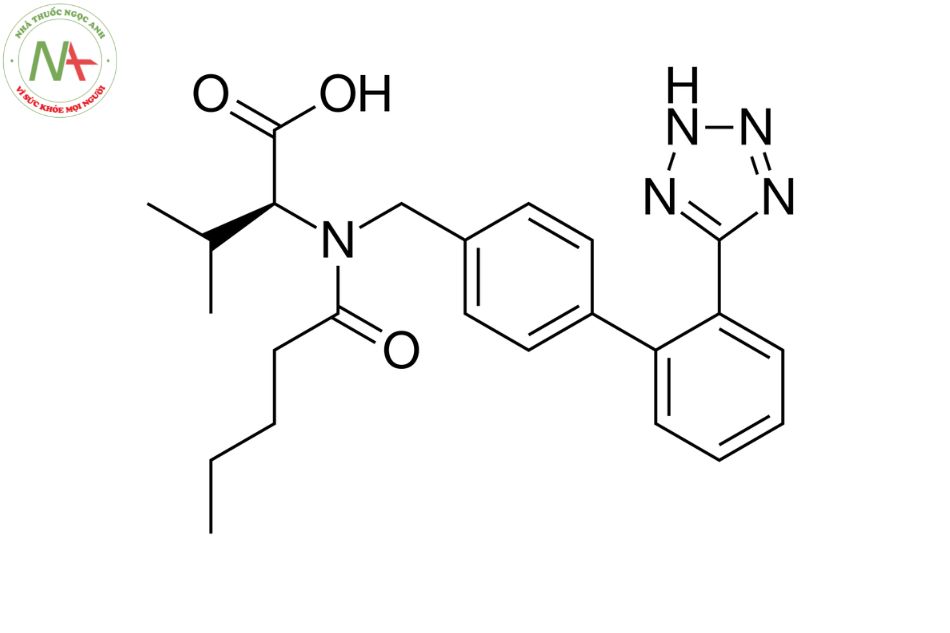
Các tính chất phân tử
Số liên kết hydro cho: 2
Số liên kết hydro nhận: 6
Số liên kết có thể xoay: 10
Diện tích bề mặt tôpô: 112 Ų
Số lượng nguyên tử nặng: 32
Các tính chất đặc trưng
Điểm nóng chảy: 116-117 °C
Điểm sôi: 83-88 °C
Tỷ trọng riêng: 1.2 ± 0.1 g/cm3
Phổ hồng ngoại: Đạt cực đại tại 1605 cm-1
Độ tan trong nước: 1.406 mg/L ở 25 °C
Hằng số phân ly pKa: 4.73
Chu kì bán hủy: 6 giờ
Khả năng liên kết với Protein huyết tương: 94 – 97%
Cảm quan
Valsartan có dạng bột mịn màu trắng đến gần như trắng, hòa tan được trong nước, ethanol, DMSO và dimethyl formamid.
Dạng bào chế
Viên nén bao phim: 40 mg, 80 mg, 160 mg và 320 mg.
Độ ổn định và điều kiện bảo quản
Viên nén valsartan nên được bảo quản trong bao bì kín, tránh ẩm và nhiệt độ không quá 30 độ C.
Nguồn gốc
Valsartan được cấp bằng sáng chế vào năm 1990, sau đó được đưa vào sử dụng trong y tế vào năm 1996 và có sẵn dưới dạng thuốc generic. Vào năm 2020, valsartan là loại thuốc được kê đơn nhiều thứ 123 ở Hoa Kỳ, với hơn 5 triệu đơn thuốc.
Dược lý và cơ chế hoạt động
Valsartan là thuốc đối kháng thụ thể của angiotensin II typ 1 (AT1), có tác dụng dược lý tương tự losartan. Tuy nhiên, valsartan không phải tiền thuốc (khác với losartan) nên tác dụng dược lý của thuốc không phụ thuộc vào phản ứng thủy phân ở gan.
Trong hệ renin-angiotensin-aldosteron, angiotensin I không có hoạt tính nhưng khi chuyển thành angiotensin II có hoạt tính co mạch mạnh, làm tăng huyết áp, đồng thời kích thích tuyến thượng thận tiết aldosteron. Ái lực gắn của angiotensin II trên thụ thể AT1 và AT2 là tương tự nhau, trong khi đó, ái lực của valsartan đối với AT1 mạnh gấp khoảng 20.000 lần so với AT2.
Vì AT1 tham gia vào hầu hết hoặc tất cả các hoạt động trên tim mạch, thận và TKTW. Do đó, khi ức chế chọn lọc angiotensin II gắn vào thụ thể AT1 ở nhiều mô khác nhau, trong đó có cơ trơn mạch máu và tuyến thượng thận, valsartan làm hạ huyết áp thông qua đối kháng các tác dụng được gây ra bởi angiotensin II (co mạch, giải phóng arginin vasopressin, tăng bài tiết aldosteron, tăng bài tiết catecholamin ở tuyến thượng thận và trước synap, tái hấp thu nước và gây phì đại cơ tim).
So với các thuốc đối kháng thụ thể AT1, các thuốc ức chế enzym chuyển angiotensin I thành angiotensin II không hoàn toàn vì angiotensin II còn có thể được tạo ra nhờ các enzym khác mà không bị các thuốc ức chế ACE chẹn lại. Hơn nữa, valsartan không ức chế giáng hóa bradykinin, do đó không gây các phản ứng bất lợi như ho dai dẳng liên quan đến quá trình này và thường xảy ra ở các thuốc ức chế enzym chuyển angiotensin.
Tác dụng hạ huyết áp xuất hiện trong khoảng 2 giờ sau khi uống valsartan, đạt cực đại sau 4 – 6 giờ và duy trì trong 24 giờ. Khi dùng liều lặp lại, tác dụng chống tăng huyết áp của valsartan thể hiện rõ rệt sau 2 tuần, đạt tối đa sau 4 tuần và được duy trì khi điều trị lâu dài. Tỷ lệ đáy/đỉnh của hiệu quả giảm huyết áp tâm thu và tâm trương tương ứng là 78% và 74% cho thấy valsartan có thể được sử dụng 1 lần/ngày trong kiểm soát huyết áp.
Ứng dụng trong y học
Valsartan là một loại thuốc dùng để điều trị bệnh tăng huyết áp, bệnh thận do đái tháo đường, suy tim và giảm tử vong cho người bị rối loạn chức năng tâm thất trái sau khi bị nhồi máu cơ tim. Ngoài việc sử dụng đơn lẻ, các dạng kết hợp của valsartan thường được sử dụng bao gồm: valsartan/hydrochlorothiazide, valsartan/amlodipine, valsartan/amlodipine/hydrochlorothiazide và valsartan/sacubitril.
Tăng huyết áp
Valsartan (và các ARB khác) là một lựa chọn điều trị ban đầu thích hợp cho hầu hết những người bị huyết áp cao và không có các bệnh kèm theo khác, cũng như thuốc ức chế men chuyển, thuốc lợi tiểu thiazide và thuốc chẹn kênh canxi. Nếu bệnh nhân mắc bệnh đái tháo đường hoặc bệnh thận đồng thời, ARB hoặc thuốc ức chế men chuyển có thể được xem xét thay vì các nhóm thuốc huyết áp khác.
Suy tim
Valsartan đã làm giảm tỷ lệ tử vong và nhập viện do suy tim khi sử dụng đơn lẻ hoặc kết hợp với thuốc chẹn beta trong điều trị suy tim. Điều quan trọng là sự kết hợp giữa valsartan và thuốc ức chế men chuyển không cho thấy lợi ích về tỷ lệ mắc bệnh hoặc tử vong mà ngược lại làm tăng nguy cơ tử vong khi được thêm vào liệu pháp kết hợp thuốc chẹn beta và thuốc ức chế men chuyển, đồng thời làm tăng nguy cơ mắc các tác dụng phụ như tăng kali máu, hạ huyết áp và suy thận.
Theo nghiên cứu PARADIGM-HF, valsartan kết hợp với sacubitril trong điều trị suy tim làm giảm đáng kể tỷ lệ tử vong và nhập viện do mọi nguyên nhân và tim mạch do suy tim.
Bệnh thận do đái tháo đường
Ở những người mắc bệnh đái tháo đường týp 2, liệu pháp hạ huyết áp bằng valsartan làm giảm tốc độ tiến triển của albumin niệu (albumin trong nước tiểu), thúc đẩy quá trình hồi phục thành albumin niệu bình thường và có thể làm giảm tốc độ tiến triển thành bệnh thận giai đoạn cuối.
Dược động học
Hấp thu
Valsartan được hấp thu nhanh sau khi uống với sinh khả dụng đạt khoảng 25%. Thời gian đạt nồng độ đỉnh trong huyết tương là khoảng 2 đến 4 giờ sau khi dùng thuốc.
Thức ăn ảnh hưởng bất lợi đến sự hấp thu của valsartan, làm giảm diện tích dưới đường cong (AUC) khoảng 40% và giảm nồng độ cực đại trong huyết tương khoảng 50%. Tuy nhiên, nồng độ trong huyết tương sau khi uống 8 giờ là tương tự nhau dù người bệnh đói hay không. Do đó, việc giảm AUC không có ý nghĩa về mặt lâm sàng nên valsartan có thể được uống trong hoặc ngoài bữa ăn.
Ngoài ra, AUC và nồng độ đỉnh trong huyết tương của valsartan tăng tỷ lệ tuyến tính với liều trong khoảng liều được khuyến cáo trên lâm sàng.
Phân bố
Valsartan liên kết mạnh với protein huyết tương (khoảng 94 – 97%), chủ yếu liên kết với albumin. Thể tích phân bố của thuốc ở trạng thái ổn định sau khi tiêm tĩnh mạch là khoảng 17 lít, chứng tỏ valsartan không phân bố đáng kể vào các mô.
Chuyển hóa
Valsartan không được chuyển hóa đáng kể, chỉ có 20% liều được tìm thấy dưới dạng chất chuyển hóa là valeryl 4-hydroxy valsartan không có hoạt tính. Các nghiên cứu hiện tại chưa xác định được chính xác các enzym tham gia chuyển hóa valsartan nhưng có thể thuốc không được chuyển hóa qua hệ enzym cytochrom P450.
Thải trừ
Valsartan được thải trừ theo nhiều pha với T1/2 alpha < 1 giờ và T1/2 beta khoảng 9 giờ. Thuốc được thải trừ chủ yếu qua đường mật vào phân (khoảng 83%) nhưng cũng qua thận vào nước tiểu (khoảng 13% liều), chủ yếu dưới dạng không chuyển hóa.
Sau khi tiêm tĩnh mạch, độ thanh thải valsartan huyết tương khoảng 2 lít/giờ và độ thanh thải thận 0,62 lít/giờ (khoảng 30% độ thanh thải toàn bộ). Thời gian bán thải của valsartan là khoảng 6 giờ.
Độc tính ở người
Các tác dụng phụ thường gặp khi sử dụng valsartan bao gồm mệt mỏi, chóng mặt, lượng kali trong máu cao, tiêu chảy và đau khớp. Các tác dụng phụ nghiêm trọng khác có thể xảy ra bao gồm các vấn đề về thận, huyết áp thấp và phù mạch.
Quá liều valsartan có thể gây hạ huyết áp nặng, nhịp tim nhanh, suy tuần hoàn có thể kèm theo sốc, giảm ý thức. Ngoài ra, chậm nhịp tim cũng có thể xảy ra do kích thích thần kinh phó giao cảm.
Tính an toàn
Ở bệnh nhân suy tim
Thời gian trung bình để đạt được nồng độ đỉnh trong huyết tương (Cmax) và nửa đời thải trừ của valsartan tương tự như người khỏe mạnh. Trị số AUC và Cmax của valsartan tăng tuyến tính và hầu như tỷ lệ với liều trong phạm vi liều khuyến cáo (40 – 160 mg, ngày 2 lần). Tỷ lệ tích lũy thuốc trung bình là khoảng 1,7. Độ thanh thải biểu kiến của valsartan sau khi uống là khoảng 4,5 lít/giờ và không bị ảnh hưởng bởi tuổi tác.
Người cao tuổi
Ở một số người, nồng độ valsartan trong máu hơi cao hơn so với người trẻ, nhưng điều này không có ý nghĩa về mặt lâm sàng.
Suy thận
Không có mối liên hệ nào giữa chức năng thận và nồng độ valsartan trong huyết tương. Do đó không cần hiệu chỉnh liều đối với người bị suy thận (Clcr> 10 ml/phút). Mặt khác, các nghiên cứu hiện nay vẫn chưa có kinh nghiệm điều trị đối với người bệnh có Clcr < 10 ml/phút.
Suy gan
Khoảng 70% liều valsartan hấp thu được thải trừ qua mật, chủ yếu dưới dạng không chuyển hóa. Ở những người bị suy gan nhẹ tới vừa, AUC tăng gấp đôi so với người khỏe mạnh. Tuy nhiên, không có mối tương quan nào giữa nồng độ huyết tương của valsartan và mức độ nặng của bệnh gan. Mặt khác, valsartan chưa được nghiên cứu ở những người bị suy gan nặng.
Thời kỳ mang thai
Valsartan cũng như các thuốc tác dụng trực tiếp lên hệ renin-angiotensin-aldosteron nói chung khi sử dụng trong ba tháng giữa và ba tháng cuối của thai kỳ có thể gây tổn hại cho thai nhi (suy giảm chức năng thận, chậm cốt hóa xương sọ, ít nước ối) và trẻ sơ sinh (suy thận, tăng kali huyết, hạ huyết áp), thậm chí có thể gây chết thai.
Vì vậy, valsartan được chống chỉ định sử dụng cho phụ nữ có thai trong giai đoạn ba tháng giữa và ba tháng cuối của thai kỳ. Hơn nữa, thuốc cũng không khuyến cáo trong ba tháng đầu của thai kỳ. Mặc dù các nghiên cứu dịch tễ học hiện chưa chứng minh được nguy cơ gây quái thai khi sử dụng valsartan trong giai đoạn này, nhưng cũng không thể loại trừ được hoàn toàn nguy cơ.
Khi phát hiện có thai, người bệnh đang sử dụng valsartan cần ngừng ngay thuốc và điều trị thay thế bằng thuốc khác. Nếu đã sử dụng valsartan trong một thời gian dài kể từ ba tháng giữa thai kỳ, người bệnh cần siêu âm để kiểm tra chức năng thận và chụp sọ của thai nhi. Hơn nữa, trẻ sơ sinh có mẹ sử dụng valsartan trong thời kỳ mang thai cần được theo dõi chặt chẽ nguy cơ hạ huyết áp.
Thời kỳ cho con bú
Dữ liệu thực nghiệm trên chuột cho thấy valsartan có thể được bài tiết vào sữa mẹ. Tuy nhiên, các nghiên cứu hiện nay vẫn chưa rõ liệu valsartan có được bài tiết vào sữa mẹ ở người hay không. Do đó, nên ngừng cho con bú trong thời gian sử dụng valsartan hoặc ngừng thuốc và điều trị thay thế bằng thuốc khác để giảm thiểu các nguy cơ có thể xảy ra cho trẻ.
Tương tác với thuốc khác
| Thuốc | Tương tác |
| Lithi | Tăng nồng độ lithi trong máu, gây ngộ độc lithi |
| Aliskiren | Nguy cơ làm tăng nồng độ kali huyết thanh và tụt huyết áp |
| Thuốc ức chế enzym chuyển angiotensin | Nguy cơ tụt huyết áp, tăng nồng độ kali huyết thanh và suy thận |
| Thuốc chống tăng huyết áp nhóm chẹn beta và chẹn kênh canxi | Tăng tác dụng hạ huyết áp |
| Thuốc lợi tiểu quai, thuốc lợi tiểu nhóm thiazid | Tăng nguy cơ hạ huyết áp, tăng hoặc giảm nồng độ kali huyết thanh |
| Thuốc lợi tiểu giữ kali, các chế phẩm bổ sung kali | Nguy cơ tăng nồng độ kali và tăng nồng độ creatinin huyết thanh ở người bệnh suy tim |
| Thuốc chống viêm không có cấu trúc steroid (NSAIDs) | Giảm tác dụng hạ huyết áp, tăng nồng độ kali huyết thanh và tăng nguy cơ suy thận |
Lưu ý khi sử dụng Valsartan
Hạ huyết áp nặng hiếm gặp ở người bệnh tăng huyết áp không biến chứng, thường xảy ra ở người bệnh có giảm khối lượng tuần hoàn do sử dụng thuốc lợi tiểu liều cao, chế độ ăn ít muối, đang thẩm tách máu, đang bị tiêu chảy hoặc nôn. Ở những người bệnh này, nên bù natri và/hoặc bù nước hoặc giảm liều thuốc lợi tiểu trước khi bắt đầu sử dụng valsartan.
Cần giám sát chặt chẽ người bệnh có nguy cơ hạ huyết áp trong giai đoạn bắt đầu điều trị. Nếu xảy ra hạ huyết áp có biểu hiện triệu chứng, nên đặt bệnh nhân ở tư thế nằm ngửa, đầu thấp. Trong trường hợp hạ huyết áp nặng, cần bù dịch bằng cách truyền tĩnh mạch dung dịch natri clorid 0,9%.
Hạ huyết áp thoáng qua không bắt buộc chống chỉ định nhưng cần hiệu chỉnh lại liều valsartan thận trọng sau khi huyết áp của người bệnh đã ổn định.
Thận trọng đối với người bệnh suy tim hoặc có dấu hiệu lâm sàng rối loạn chức năng tâm thu thất trái sau nhồi máu cơ tim vì những người bệnh này thường xảy ra hạ huyết áp. Tuy nhiên, không cần ngừng thuốc nếu liều của thuốc vẫn đang nằm trong khoảng khuyến cáo. Đồng thời, cần theo dõi chặt chẽ chức năng thận trong thời gian điều trị.
Nguy cơ tăng kali máu, đặc biệt đối với các bệnh nhân bị suy tim hoặc những người bệnh có suy thận kèm theo. Không nên sử dụng đồng thời valsartan với các thuốc lợi tiểu giữ kali, các chế phẩm bổ sung kali hoặc các thuốc khác có khả năng làm tăng nồng độ kali huyết thanh (heparin). Đồng thời, cần theo dõi định kỳ nồng độ kali huyết thanh.
Thận trọng ở những người bệnh chỉ còn một thận và hẹp động mạch thận hai bên hoặc hẹp động mạch thận một bên do độ an toàn của valsartan chưa được nghiên cứu ở những đối tượng này.
Thuốc có thể làm tăng nồng độ creatinin huyết thanh hoặc tăng nitrogen urê máu (BUN) ở bệnh nhân bị hẹp động mạch thận. Do đó, cần theo dõi chặt chẽ chức năng thận ở những người bệnh này khi điều trị bằng valsartan.
Thận trọng ở người bệnh suy thận có Clcr < 10 ml/phút hoặc đang thẩm tách máu.
Suy giảm chức năng thận liên quan đến việc sử dụng valsartan hoặc các thuốc ức chế hệ renin-angiotensin-aldosteron nói chung chủ yếu xảy ra ở người bệnh suy tim nặng hoặc có các yếu tố nguy cơ như tiền sử suy thận, hẹp động mạch thận hoặc sử dụng đồng thời với các thuốc lợi tiểu.
Thận trọng ở người bệnh suy gan nhẹ đến trung bình không mắc kèm ứ mật.
Thận trọng ở người bệnh cường aldosteron nguyên phát do hệ renin-angiotensin-aldosteron không được hoạt hóa ở những bệnh nhân này.
Thận trọng với người bệnh bị hẹp van động mạch chủ hoặc hẹp van hai lá hoặc bệnh lý phì đại cơ tim.
Một vài nghiên cứu của Valsartan trong Y học
Tác dụng của valsartan đối với kết quả thận ở những người bị rối loạn dung nạp glucose
Mục đích: Kiểm tra ảnh hưởng của valsartan đối với kết quả thận ở bệnh nhân bị rối loạn dung nạp glucose (IGT).
Phương pháp: Trong một thử nghiệm ngẫu nhiên mù đôi, 9306 bệnh nhân mắc IGT được chỉ định dùng valsartan (160 mg mỗi ngày) hoặc giả dược. Các tiêu chí phụ chính là sự phát triển của bệnh đái tháo đường và hai kết cục tim mạch tổng hợp.
Các điểm cuối về thận được xác định trước bao gồm: tổng hợp tử vong do thận, bệnh thận giai đoạn cuối (ESRD) hoặc tăng gấp đôi creatinine huyết thanh; mức lọc cầu thận ước tính (eGFR) ≤30 mL/phút/1,73 m2 ; nhập viện vì suy thận; và tiến triển từ albumin niệu bình thường thành albumin niệu vi lượng, albumin niệu vi lượng thành albumin niệu đại thể, và albumin niệu bình thường thành albumin niệu đại thể. Thời gian theo dõi trung bình là 6,2 năm.
Kết quả: Valsartan làm giảm tỷ lệ mắc bệnh đái tháo đường nhưng không làm giảm các biến cố tim mạch. Trong nhóm valsartan, 25/4631 bệnh nhân (0,5%), so với 26/4675 (0,6%) bệnh nhân trong nhóm giả dược, phát triển ESRD hoặc tăng gấp đôi creatinine huyết thanh (tỷ số nguy hiểm [HR] 0,96, khoảng tin cậy 95% [CI ] 0,55-1,66; P = 0,87).
Rất ít bệnh nhân trong cả hai nhóm có eGFR ≤30 mL/phút/1,73 m2 hoặc phải nhập viện điều trị thận. Ít bệnh nhân dùng valsartan hơn (237/4084 [5,8%]) so với nhóm dùng giả dược (342/4092 [8,4%]) phát triển albumin niệu vi lượng (HR 0,68, KTC 95% 0,57-0,80; P < 0,0001) và ít bệnh nhân điều trị bằng valsartan hơn phát triển macroalbumin niệu.
Nhìn chung, tỷ lệ albumin-to-creatinine trong nước tiểu (UACR) thấp hơn 11% với valsartan (95% CI 8-13; P <0,0001) và thấp hơn 9% (95% CI 6-11; P <0,0001) sau khi điều chỉnh cho cả glucose và huyết áp.
Kết luận: Tác dụng của valsartan trên UACR không hoàn toàn được giải thích bằng sự thay đổi huyết áp hoặc glucose. Valsartan làm giảm tỷ lệ albumin niệu vi lượng trong IGT mà không làm tăng tỷ lệ tăng kali máu hoặc rối loạn chức năng thận so với giả dược.
Tài liệu tham khảo
- Currie, G., Bethel, M. A., Holzhauer, B., Haffner, S. M., Holman, R. R., & McMurray, J. J. V. (2017). Effect of valsartan on kidney outcomes in people with impaired glucose tolerance. Diabetes, obesity & metabolism, 19(6), 791–799.
- Drugbank, Valsartan, truy cập ngày 14 tháng 2 năm 2023.
- Pubchem, Valsartan, truy cập ngày 14 tháng 2 năm 2023.
- Bộ Y Tế (2012), Dược thư quốc gia Việt Nam, Nhà xuất bản Y học, Hà Nội
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Ấn Độ
Xuất xứ: Hàn Quốc
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Ba Lan
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Ấn Độ
Xuất xứ: Singapore
Xuất xứ: Ý
Xuất xứ: Tây Ba Nha
Xuất xứ: Việt Nam
Xuất xứ: Tây Ban Nha