Cilostazol
Biên soạn và Hiệu đính
Dược sĩ Xuân Hạo
Danh pháp
Tên chung quốc tế
Tên danh pháp theo IUPAC
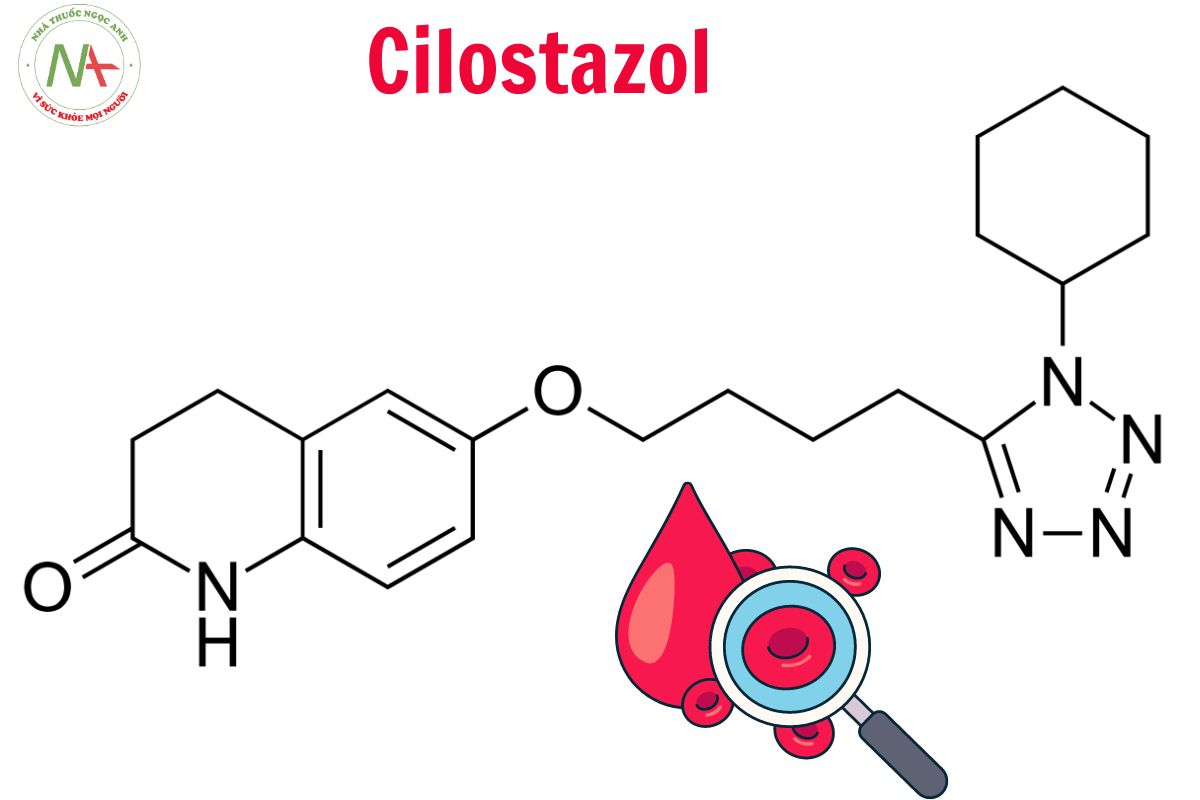
6-[4-(1-cyclohexyltetrazol-5-yl)butoxy]-3,4-dihydro-1H-quinolin-2-one
Nhóm thuốc
Thuốc ức chế kết tập tiểu cầu và có hiệu quả giãn mạch, ức chế có chọn lọc phosphodiesterase tế bào.
Mã ATC
B — Máu và cơ quan tạo máu
B01 — Thuốc chống nhiễm mạch
B01A — Tác nhân chống nhiễm mạch
B01AC — Loại trừ chất ức chế kết tập tiểu cầu. heparin
B01AC23 — Cilostazol
Mã UNII
N7Z035406B
Mã CAS
73963-72-1
Cấu trúc phân tử
Công thức phân tử
C20H27N5O2
Phân tử lượng
369.5 g/mol
Cấu trúc phân tử
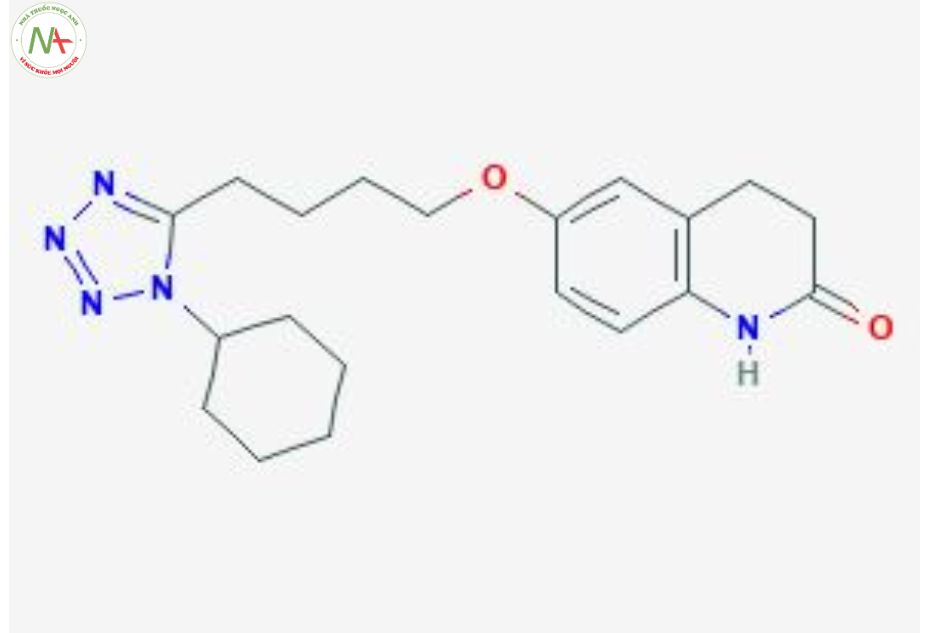
Cilostazol là một lactam là 3,4-dihydroquinolin-2(1H)-one trong đó hydro ở vị trí 6 được thế bởi nhóm butoxy 4-(1-cyclohexyl-1H-tetrazol-5-yl). Nó là một thành viên của tetrazoles và một lactam.
Các tính chất phân tử
Số liên kết hydro cho: 1
Số liên kết hydro nhận: 5
Số liên kết có thể xoay: 7
Diện tích bề mặt tôpô: 81,9 Ų
Số lượng nguyên tử nặng: 27
Các tính chất đặc trưng
Điểm nóng chảy: 159,4-160,3°C
Độ hòa tan trong nước: Trong nước , 1,678 mg/L ở 25 °C (est)
Áp suất hơi: 4,14X10-11 mm Hg ở 25 °C (est)
LogP: 2.3
Hằng số Định luật Henry: 1,48X10-13 atm-cu m/mol ở 25 °C (est)
Cảm quan
Tinh thể hình kim không màu từ metanol. Thực tế không hòa tan trong nước. Tự do hòa tan trong axit axetic , cloroform , n-metyl-2-pyrrolidon , DMSO ; ít tan trong metanol , etanol . Thực tế không hòa tan trong ether.
Dạng bào chế
Viên nén hàm lượng lần lượt là 50 mg và 100 mg.
Độ ổn định và điều kiện bảo quản của Cilostazol
Đối với dạng viên nén cần được bảo quản ở nhiệt độ phòng dưới 30oC. Tránh ánh sáng ẩm ướt và tầm tay trẻ em.
Nguồn gốc
Cilostazol , được bán dưới tên thương mại là Pletal và các thương hiệu khác, là một loại thuốc được sử dụng để điều trị các triệu chứng đau cách hồi trong bệnh mạch máu ngoại biên .
Cilostazol đã được chấp thuận sử dụng trong y tế tại Hoa Kỳ vào năm 1999.
Vào năm 2019, đây là loại thuốc được kê đơn nhiều thứ 347 tại Hoa Kỳ, với hơn 800 nghìn đơn thuốc.
Dược lý và cơ chế hoạt động
Cilostazol và một số chất chuyển hóa của nó là chất ức chế AMP vòng (cAMP) phosphodiesterase III (chất ức chế PDE III), ức chế hoạt động của phosphodiesterase và ngăn chặn sự thoái biến của cAMP dẫn đến tăng cAMP trong tiểu cầu và mạch máu, dẫn đến ức chế kết tập tiểu cầu và giãn mạch.
Cilostazol làm giảm các triệu chứng đau cách hồi, thể hiện qua việc tăng khoảng cách đi bộ. Đau cách hồi là cơn đau ở chân xảy ra khi đi bộ và biến mất khi nghỉ ngơi. Cơn đau xảy ra do giảm lưu lượng máu đến chân.
Ứng dụng trong y học của Cilostazol
Cilostazol được phê duyệt để điều trị chứng đau cách hồi ở Hoa Kỳ và Vương quốc Anh.
Cilostazol cũng được sử dụng để phòng ngừa đột quỵ thứ phát, mặc dù cho đến nay chưa có cơ quan quản lý nào phê duyệt cụ thể cho chỉ định đó.
Suy tim
Cilostazol nguy hiểm đối với những người bị suy tim nặng. Cilostazol đã được nghiên cứu ở những người không bị suy tim, không có bằng chứng về tác hại, nhưng sẽ cần nhiều dữ liệu hơn để xác định không có rủi ro. Mặc dù cilostazol sẽ không được chấp thuận cho một tình trạng tầm thường, Ủy ban Tư vấn Tim-Thận và FDA đã kết luận rằng các bệnh nhân và bác sĩ được thông báo đầy đủ sẽ có thể chọn sử dụng nó để điều trị chứng đau cách hồi.
Dược động học
Hấp thu
Sự hấp thu của Cilostazol xảy ra thông qua uống. Tuy nhiên, sinh khả dụng tuyệt đối của Cilostazol hiện chưa được biết.
Phân phối
Cilostazol liên kết cao với protein huyết thanh, với tỷ lệ liên kết 95-98%, chủ yếu với albumin. Tỷ lệ liên kết protein trung bình của các chất chuyển hóa 3,4-dehydro-cilostazol và 4′-trans-hydroxy-cilostazol lần lượt là 97,4% và 66%. Ở những bệnh nhân suy thận, phần tự do của Cilostazol trong huyết thanh cao hơn 27% so với những người bình thường.
Chuyển hóa
Cilostazol được chuyển hóa rộng rãi ở gan bởi các enzyme cytochrome P450, chủ yếu là CYP3A4, và ở mức độ thấp hơn bởi CYP2C19, thành các chất chuyển hóa chủ yếu được loại bỏ qua nước tiểu. Hai chất chuyển hóa hoạt động chính, 3,4-dehydrocilostazol và 4′-trans-hydroxy-cilostazol, chiếm ít nhất 50% hoạt tính dược lý.
Bài tiết
Cilostazol chủ yếu được bài tiết dưới dạng chất chuyển hóa hoạt động và không hoạt động qua nước tiểu (74%) và phân (20%). Lượng Cilostazol không chuyển hóa trong nước tiểu không thể định lượng được, và ít hơn 2% liều được bài tiết qua nước tiểu dưới dạng 3,4-dehydro-cilostazol, trong khi 30% liều được bài tiết qua nước tiểu dưới dạng 4′-trans-hydroxy-cilostazol.
Độc tính của Cilostazol
Thông tin về quá liều cấp tính cilostazol ở người còn hạn chế. Các dấu hiệu và triệu chứng của quá liều cấp tính có thể được dự đoán là do tác dụng dược lý quá mức: nhức đầu dữ dội, tiêu chảy, hạ huyết áp, nhịp tim nhanh và có thể rối loạn nhịp tim. LD 50 đường uống của cilostazol là >5,0 g/kg ở chuột nhắt và chuột cống và >2,0 g/kg ở chó.
Tương tác của Cilostazol với thuốc khác
Tương tác thuốc động: Dùng Cilostazol đồng thời với các chất ức chế CYP3A4 (ví dụ clarithromycin, diltiazem, erythromycin, itraconazole, ketoconazole) hoặc thuốc ức chế CYP2C19 (omeprazole) có thể làm thay đổi nồng độ thuốc trong máu hoặc gây ra tác dụng không mong muốn. Kết hợp Lovastatin với Cilostazol có thể dẫn đến tương tác thuốc động (tăng nồng độ lovastatin và giảm nồng độ Cilostazol). Dùng đồng thời Diltiazem với Cilostazol có thể làm giảm độ thanh thải của Cilostazol lên đến 30%, tăng nồng độ tối đa lên 30% và tăng diện tích dưới đường cong thời gian nồng độ lên 40%.
Tương tác dược lực học: Cilostazol có thể tăng cường tác dụng / độc tính của các chất ức chế chức năng tiểu cầu khác.
Tăng tác dụng / độc tính: Cilostazol có thể làm tăng tác dụng của thuốc chống đông máu, thuốc chống tiểu cầu, drotrecogin alfa, ibritumomab, salicylat, tan huyết khối, tositumomab và tositumomab có nhãn I131.
Tác dụng của Cilostazol có thể được tăng cường bằng cách sử dụng đồng thời với thuốc chống nấm azole toàn thân, thuốc ức chế CYP12C19 hoặc CYP3A4, dasatinib, thảo dược bổ sung (có đặc tính kháng tiểu cầu), kháng sinh macrolid, thuốc chống viêm không steroid, este ethyl axit béo omega-3, omeprazole, pentosan polysulfate natri, pentoxifylline và các chất tương tự prostacyclin.
Thận trọng khi sử dụng Cilostazol với bất kỳ loại thuốc nào khác có thể làm giảm huyết áp, vì nó có thể làm tăng nguy cơ hạ huyết áp với nhịp tim nhanh phản xạ.
Giảm tác dụng: Hiệu quả của cilostazol có thể bị giảm bởi các chất gây cảm ứng CYP3A4, bổ sung thảo dược có tác dụng gây CYP3A4, deferasirox, thuốc chống viêm không steroid và peginterferon alfa-2b.
Lưu ý khi dùng Cilostazol
Lưu ý và thận trọng chung
Cilostazol là một loại thuốc được sử dụng để giảm claudication không liên tục ở những người bị bệnh động mạch ngoại biên không đau và không hoại tử mô ngoại biên sau thời gian dài đi bộ.
Cần thận trọng khi sử dụng Cilostazol ở những người có nhịp đập ngoài tử cung nhĩ hoặc thất, rung nhĩ, rung (chống chỉ định nếu nặng), đau thắt ngực ổn định, tiểu đường (nguy cơ chảy máu nội nhãn cao), phẫu thuật và kết hợp với các thuốc làm tăng nguy cơ chảy máu.
Bệnh nhân nên được cảnh báo về bất kỳ chảy máu hoặc dễ bị bầm tím trong quá trình điều trị. Trong trường hợp chảy máu thủy tinh thể, Cilostazol nên ngưng ngay lập tức.
Bệnh nhân nên được tư vấn để báo cáo bất kỳ dấu hiệu nào khác có thể gợi ý sự phát triển sớm của rối loạn lưu lượng máu, chẳng hạn như sốt và đau họng. Cần thực hiện công thức máu toàn bộ nếu nghi ngờ nhiễm trùng hoặc có bất kỳ bằng chứng lâm sàng nào khác về rối loạn máu.
Cilostazol nên ngưng ngay lập tức nếu có bằng chứng lâm sàng hoặc bất thường về huyết học.
Lưu ý đối với phụ nữ mang thai
Cho đến nay, không có nghiên cứu về tác dụng của Cilostazol đối với phụ nữ mang thai. Trong các thí nghiệm trên động vật, Cilostazol làm giảm trọng lượng của thai nhi, tăng tỷ lệ mắc các bất thường về tim mạch, thận và xương (khiếm khuyết thông liên nhĩ, ống động mạch, động mạch dưới đòn, hóa thạch chậm). Do đó, Cilostazol nên tránh ở phụ nữ mang thai.
Lưu ý đối với phụ nữ cho con bú
Cilostazol được bài tiết qua sữa của động vật thí nghiệm, vì vậy nên ngừng cho con bú khi sử dụng thuốc hoặc ngừng do nguy cơ cho trẻ bú.
Lưu ý khi lái xe hoặc vận hành máy móc
Cilostazol có thể gây chóng mặt và bệnh nhân nên được thận trọng trước khi lái xe hoặc vận hành máy móc.
Một vài nghiên cứu về Cilostazol trong Y học
Cilostazol dùng để đau cách hồi
Bối cảnh: Bệnh động mạch ngoại vi (PAD) ảnh hưởng từ 4% đến 12% người từ 55 đến 70 tuổi và 20% người trên 70 tuổi. Một khiếu nại phổ biến là đau cách hồi (đau chi dưới do tập thể dục giảm khi nghỉ ngơi). Những bệnh nhân này có tỷ lệ tử vong do tim mạch tăng từ ba đến sáu lần. Cilostazol là một loại thuốc được cấp phép sử dụng để cải thiện khoảng cách đi cách hồi và, nếu được chứng minh là làm giảm nguy cơ tim mạch, có thể mang lại các lợi ích lâm sàng bổ sung. Đây là bản cập nhật của bài đánh giá được xuất bản lần đầu vào năm 2007.
Mục tiêu: Xác định tác dụng của cilostazol đối với khoảng cách đi cách hồi ban đầu và tuyệt đối, tỷ lệ tử vong và các biến cố mạch máu ở những bệnh nhân bị đau cách hồi ổn định.
Phương pháp tìm kiếm: Chuyên gia Thông tin về Mạch máu Cochrane đã tìm kiếm Cơ sở dữ liệu Đăng ký Chuyên ngành Mạch máu Cochrane, CENTRAL, MEDLINE, Embase, CINAHL và AMED cũng như Nền tảng Đăng ký Thử nghiệm Lâm sàng Quốc tế của Tổ chức Y tế Thế giới và các cơ quan đăng ký thử nghiệm ClinicalTrials.gov, vào ngày 9 tháng 11 năm 2020.
Tiêu chí lựa chọn: Chúng tôi đã xem xét các thử nghiệm mù đôi, ngẫu nhiên có đối chứng (RCT) của cilostazol so với giả dược hoặc so với các loại thuốc khác được sử dụng để cải thiện khoảng cách đi cách hồi ở những bệnh nhân bị đau cách hồi ổn định.
Thu thập và phân tích dữ liệu: Hai tác giả đánh giá độc lập các thử nghiệm để lựa chọn và trích xuất dữ liệu độc lập. Những bất đồng đã được giải quyết bằng cách thảo luận. Chúng tôi đã đánh giá rủi ro sai lệch bằng công cụ rủi ro sai lệch Cochrane. Độ chắc chắn của bằng chứng được đánh giá bằng GRADE. Đối với các kết quả phân đôi, chúng tôi đã sử dụng tỷ lệ chênh lệch (OR) với khoảng tin cậy (CI) tương ứng là 95% và đối với các kết quả liên tục, chúng tôi sử dụng chênh lệch trung bình (MD) và 95% CI. Chúng tôi đã tổng hợp dữ liệu bằng mô hình hiệu ứng cố định hoặc mô hình hiệu ứng ngẫu nhiên khi xác định được tính không đồng nhất. Kết quả chính là khoảng cách đi lại ban đầu (ICD) và chất lượng cuộc sống (QoL). Các kết quả phụ là khoảng cách đi cách hồi tuyệt đối (ACD), tái thông mạch máu, cắt cụt chi, biến cố bất lợi và biến cố tim mạch.
Kêt quả chung cuộc: Chúng tôi bao gồm 16 RCT mù đôi (3972 người tham gia) so sánh cilostazol với giả dược, trong đó có 5 nghiên cứu cũng so sánh cilostazol với pentoxifylline. Thời gian điều trị dao động từ sáu đến 26 tuần. Tất cả những người tham gia đều bị đau cách hồi thứ phát do PAD. Liều cilostazol dao động từ 100 mg đến 300 mg; liều pentoxifylline dao động từ 800 mg đến 1200 mg. Mức độ chắc chắn của bằng chứng đã bị hạ xuống một cấp đối với tất cả các nghiên cứu vì xu hướng xuất bản bị nghi ngờ mạnh mẽ. Các lý do khác để hạ cấp là báo cáo không chính xác, không nhất quán và chọn lọc. Cilostazol so với giả dược Những người tham gia dùng cilostazol có ICD cao hơn so với những người dùng giả dược (MD 26,49 mét; 95% CI 18,93 đến 34,05; 1722 người tham gia; sáu nghiên cứu; bằng chứng có độ chắc chắn thấp). Chúng tôi đã báo cáo các biện pháp QoL một cách mô tả do không đủ chi tiết thống kê trong các nghiên cứu để kết hợp các kết quả; có thể có dấu hiệu cải thiện chất lượng cuộc sống ở các nhóm điều trị bằng cilostazol (bằng chứng có độ chắc chắn thấp). Những người tham gia dùng cilostazol có ACD cao hơn so với những người dùng giả dược (39,57 mét; 95% CI 21,80 đến 57,33; 2360 người tham gia; tám nghiên cứu; bằng chứng chắc chắn rất thấp). Các tác dụng phụ được báo cáo phổ biến nhất là nhức đầu, tiêu chảy, phân bất thường, chóng mặt, đau và đánh trống ngực. Những người tham gia dùng cilostazol có tỷ lệ bị đau đầu cao hơn so với những người tham gia dùng giả dược (OR 2,83; 95% CI 2,26 đến 3,55; 2584 người tham gia; 8 nghiên cứu; bằng chứng chắc chắn vừa phải). Rất ít nghiên cứu báo cáo về các kết quả khác nên kết luận về tái thông mạch máu, cắt cụt chi, hoặc các sự kiện tim mạch không thể được thực hiện. Cilostazol so với pentoxifylline Không có sự khác biệt nào được phát hiện giữa cilostazol và pentoxifylline để cải thiện khoảng cách đi bộ, cả về ICD (MD 20,0 mét, 95% CI -2,57 đến 42,57; 417 người tham gia; một nghiên cứu; bằng chứng có độ chắc chắn thấp); và ACD (MD 13,4 mét, KTC 95% -43,50 đến 70,36; 866 người tham gia; hai nghiên cứu; bằng chứng có độ chắc chắn rất thấp). Một nghiên cứu báo cáo về QoL; các tác giả nghiên cứu đã báo cáo không có sự khác biệt về chất lượng cuộc sống giữa các nhóm điều trị (bằng chứng có độ chắc chắn rất thấp). Không có nghiên cứu báo cáo về tái thông mạch máu, cắt cụt chi hoặc biến cố tim mạch. Những người tham gia dùng cilostazol có tỷ lệ bị đau đầu cao hơn so với những người tham gia dùng pentoxifylline ở tuần thứ 24 (OR 2,20, KTC 95% 1,16 đến 4,17; 982 người tham gia; hai nghiên cứu; bằng chứng có độ chắc chắn thấp). Cilostazol so với pentoxifylline Không có sự khác biệt nào được phát hiện giữa cilostazol và pentoxifylline để cải thiện khoảng cách đi bộ, cả về ICD (MD 20,0 mét, 95% CI -2,57 đến 42,57; 417 người tham gia; một nghiên cứu; bằng chứng có độ chắc chắn thấp); và ACD (MD 13,4 mét, KTC 95% -43,50 đến 70,36; 866 người tham gia; hai nghiên cứu; bằng chứng có độ chắc chắn rất thấp). Một nghiên cứu báo cáo về QoL; các tác giả nghiên cứu đã báo cáo không có sự khác biệt về chất lượng cuộc sống giữa các nhóm điều trị (bằng chứng có độ chắc chắn rất thấp). Không có nghiên cứu báo cáo về tái thông mạch máu, cắt cụt chi hoặc biến cố tim mạch. Những người tham gia dùng cilostazol có tỷ lệ bị đau đầu cao hơn so với những người tham gia dùng pentoxifylline ở tuần thứ 24 (OR 2,20, KTC 95% 1,16 đến 4,17; 982 người tham gia; hai nghiên cứu; bằng chứng có độ chắc chắn thấp). Cilostazol so với pentoxifylline Không có sự khác biệt nào được phát hiện giữa cilostazol và pentoxifylline để cải thiện khoảng cách đi bộ, cả về ICD (MD 20,0 mét, 95% CI -2,57 đến 42,57; 417 người tham gia; một nghiên cứu; bằng chứng có độ chắc chắn thấp); và ACD (MD 13,4 mét, KTC 95% -43,50 đến 70,36; 866 người tham gia; hai nghiên cứu; bằng chứng có độ chắc chắn rất thấp). Một nghiên cứu báo cáo về QoL; các tác giả nghiên cứu đã báo cáo không có sự khác biệt về chất lượng cuộc sống giữa các nhóm điều trị (bằng chứng có độ chắc chắn rất thấp). Không có nghiên cứu báo cáo về tái thông mạch máu, cắt cụt chi hoặc biến cố tim mạch. Những người tham gia dùng cilostazol có tỷ lệ bị đau đầu cao hơn so với những người tham gia dùng pentoxifylline ở tuần thứ 24 (OR 2,20, KTC 95% 1,16 đến 4,17; 982 người tham gia; hai nghiên cứu; bằng chứng có độ chắc chắn thấp). cả về ICD (MD 20,0 mét, 95% CI -2,57 đến 42,57; 417 người tham gia; một nghiên cứu; bằng chứng có độ chắc chắn thấp); và ACD (MD 13,4 mét, KTC 95% -43,50 đến 70,36; 866 người tham gia; hai nghiên cứu; bằng chứng có độ chắc chắn rất thấp). Một nghiên cứu báo cáo về QoL; các tác giả nghiên cứu đã báo cáo không có sự khác biệt về chất lượng cuộc sống giữa các nhóm điều trị (bằng chứng có độ chắc chắn rất thấp). Không có nghiên cứu báo cáo về tái thông mạch máu, cắt cụt chi hoặc biến cố tim mạch. Những người tham gia dùng cilostazol có tỷ lệ bị đau đầu cao hơn so với những người tham gia dùng pentoxifylline ở tuần thứ 24 (OR 2,20, KTC 95% 1,16 đến 4,17; 982 người tham gia; hai nghiên cứu; bằng chứng có độ chắc chắn thấp). cả về ICD (MD 20,0 mét, 95% CI -2,57 đến 42,57; 417 người tham gia; một nghiên cứu; bằng chứng có độ chắc chắn thấp); và ACD (MD 13,4 mét, KTC 95% -43,50 đến 70,36; 866 người tham gia; hai nghiên cứu; bằng chứng có độ chắc chắn rất thấp). Một nghiên cứu báo cáo về QoL; các tác giả nghiên cứu đã báo cáo không có sự khác biệt về chất lượng cuộc sống giữa các nhóm điều trị (bằng chứng có độ chắc chắn rất thấp). Không có nghiên cứu báo cáo về tái thông mạch máu, cắt cụt chi hoặc biến cố tim mạch. Những người tham gia dùng cilostazol có tỷ lệ bị đau đầu cao hơn so với những người tham gia dùng pentoxifylline ở tuần thứ 24 (OR 2,20, KTC 95% 1,16 đến 4,17; 982 người tham gia; hai nghiên cứu; bằng chứng có độ chắc chắn thấp). bằng chứng có độ chắc chắn rất thấp). Một nghiên cứu báo cáo về QoL; các tác giả nghiên cứu đã báo cáo không có sự khác biệt về chất lượng cuộc sống giữa các nhóm điều trị (bằng chứng có độ chắc chắn rất thấp). Không có nghiên cứu báo cáo về tái thông mạch máu, cắt cụt chi hoặc biến cố tim mạch. Những người tham gia dùng cilostazol có tỷ lệ bị đau đầu cao hơn so với những người tham gia dùng pentoxifylline ở tuần thứ 24 (OR 2,20, KTC 95% 1,16 đến 4,17; 982 người tham gia; hai nghiên cứu; bằng chứng có độ chắc chắn thấp). bằng chứng có độ chắc chắn rất thấp). Một nghiên cứu báo cáo về QoL; các tác giả nghiên cứu đã báo cáo không có sự khác biệt về chất lượng cuộc sống giữa các nhóm điều trị (bằng chứng có độ chắc chắn rất thấp). Không có nghiên cứu báo cáo về tái thông mạch máu, cắt cụt chi hoặc biến cố tim mạch. Những người tham gia dùng cilostazol có tỷ lệ bị đau đầu cao hơn so với những người tham gia dùng pentoxifylline ở tuần thứ 24 (OR 2,20, KTC 95% 1,16 đến 4,17; 982 người tham gia; hai nghiên cứu; bằng chứng có độ chắc chắn thấp). 982 người tham gia; hai nghiên cứu; bằng chứng có độ chắc chắn thấp). 982 người tham gia; hai nghiên cứu; bằng chứng có độ chắc chắn thấp).
Kết luận của các tác giả: Cilostazol đã được chứng minh là cải thiện khoảng cách đi bộ ở những người bị đau cách hồi. Tuy nhiên, những người tham gia dùng cilostazol có tỷ lệ bị đau đầu cao hơn. Không có đủ bằng chứng về hiệu quả của cilostazol đối với các biến cố nghiêm trọng như cắt cụt chi, tái thông mạch máu và các biến cố tim mạch. Mặc dù tầm quan trọng của QoL đối với bệnh nhân, phân tích tổng hợp không thể được thực hiện do sự khác biệt trong các biện pháp được sử dụng và báo cáo. Dữ liệu rất hạn chế cho thấy không có sự khác biệt giữa cilostazol và pentoxifylline để cải thiện khoảng cách đi bộ và dữ liệu quá hạn chế để đưa ra bất kỳ kết luận nào về các kết quả khác.
Tài liệu tham khảo
- Drugbank, Cilostazol , truy cập ngày 02/04/2023.
- Pubchem, Cilostazol, truy cập ngày 02/04/2023.
- Brown, T., Forster, R. B., Cleanthis, M., Mikhailidis, D. P., Stansby, G., & Stewart, M. (2021). Cilostazol for intermittent claudication. Cochrane Database of Systematic Reviews, (6).
Xuất xứ: Việt Nam
Xuất xứ: Ba Lan
Xuất xứ: Hungary
Xuất xứ: Việt Nam
Xuất xứ: Ấn Độ
Xuất xứ: Ấn Độ
Xuất xứ: Việt Nam
Xuất xứ: Tây Ban Nha
Xuất xứ: Hàn Quốc
Xuất xứ: Việt Nam
Xuất xứ: Hungary
Xuất xứ: Việt Nam
Xuất xứ: Hàn Quốc