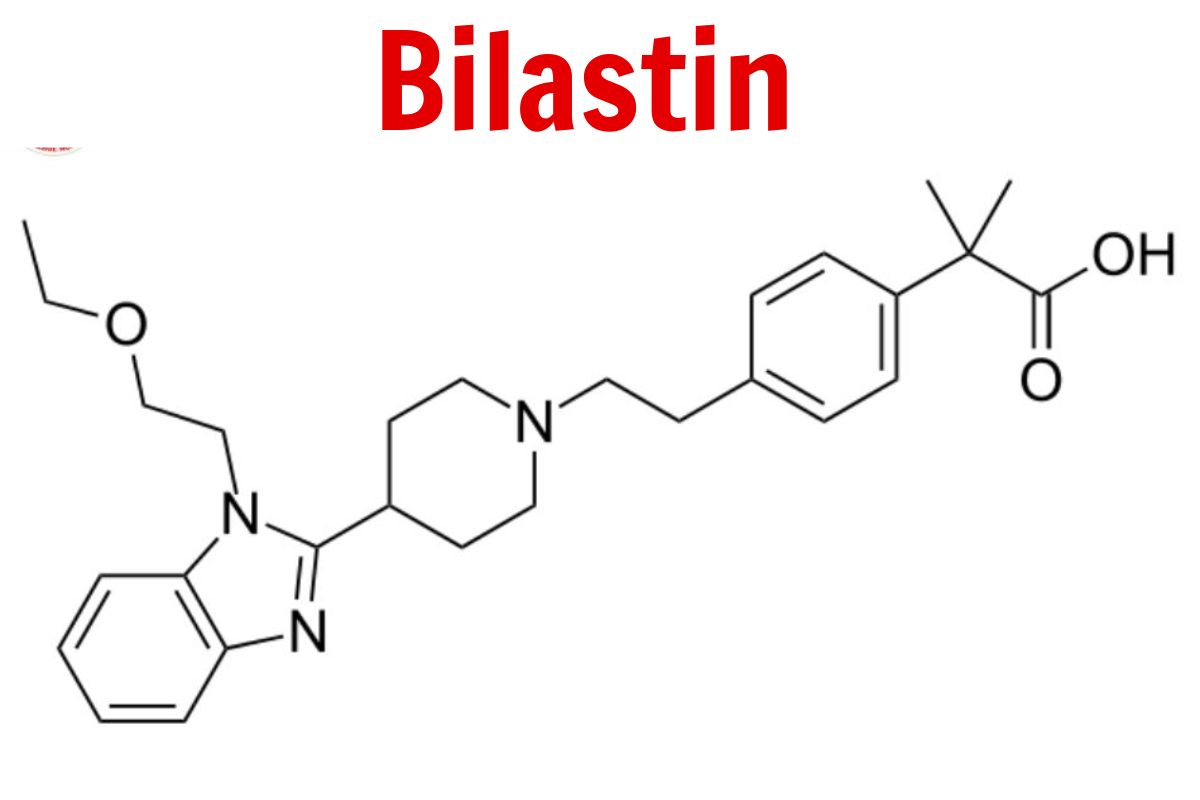
Bilastin
Danh pháp
Tên chung quốc tế
Tên danh pháp theo IUPAC
2-[4-[2-[4-[1-(2-ethoxyethyl)benzimidazol-2-yl]piperidin-1-yl]ethyl]phenyl]-2-methylpropanoic acid
Nhóm thuốc
Thuốc chống dị ứng, kháng histamin H1
Mã ATC
S — Thuốc tác động lên các cơ quan cảm giác
S01 — Thuốc tác động lên nhãn khoa
S01G — Thuốc chống dị ứng
S01GX — Thuốc chống dị ứng khác
S01GX13 — Bilastin
R —Thuốc trên hệ hô hấp
R06 — Thuốc kháng Histamin có hệ thống
R06A — Thuốc kháng Histamin có hệ thống
R06AX — Các thuốc kháng histamin khác dùng toàn thân
R06AX29 — Bilastin
Mã UNII
PA1123N395
Mã CAS
202189-78-4
Cấu trúc phân tử
Công thức phân tử
C 28 H 37 N 3 O 3
Phân tử lượng
463,6 g/mol
Cấu trúc phân tử
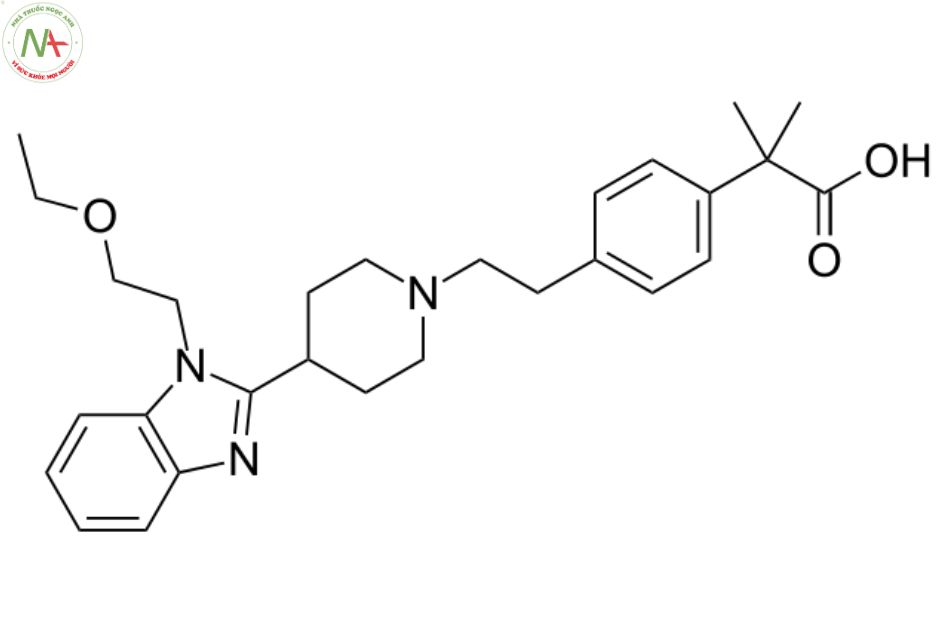
Là 1 thành viên của nhóm thuốc benzimidazoles
Các tính chất phân tử
Số liên kết hydro cho: 1
Số liên kết hydro nhận: 5
Số liên kết có thể xoay: 10
Diện tích bề mặt tôpô: 67,6 Ų
Số lượng nguyên tử nặng: 34
Các tính chất đặc trưng
Sinh khả dụng: 61%
Khả năng liên kết protein: 84-90%
Thời gian bán hủy: 14,5 giờ
Cảm quan
Không có thông tin
Dạng bào chế
Viên nén hàm lượng 10mg, 20mg.
Độ ổn định và điều kiện bảo quản của Bilastin
Bảo quản Bilastin trong điều kiện nhiệt độ < 30oC ở nơi cao ráo thoáng mát tránh ẩm ướt. Để Bilastin xa tầm với của trẻ.
Nguồn gốc
Bilastin là thuốc kháng histamin thế hệ thứ hai và có hiệu lực bằng cách ức chế chọn lọc thụ thể histamin H1
Bilastine 20mg ra đời năm nào? Ban đầu Bilastin được nghienen cứu và phát triển ở Tây Ban Nha bởi FAES Farma vào năm 2008. Bilastin có hiệu quả tương tự như cetirizine , fexofenadine và desloratadine.
Bilastin được chấp thuận ở Liên minh Châu Âu để điều trị triệu chứng viêm kết mạc dị ứng và mày đay vào năm 2010. Tuy nhiên, thuốc này không được chấp thuận cho bất kỳ mục đích sử dụng nào ở Hoa Kỳ.
Dược lý và cơ chế hoạt động
Bilastin là một chất chống histamin có tác dụng kéo dài, không gây buồn ngủ. Nó đối kháng chọn lọc trên thụ thể H1 ngoại vi và không ảnh hưởng đến thụ thể Muscarinic.
Ứng dụng trong y học của Bilastin
Bilastin ức chế các phản ứng mẩn ngứa và ban đỏ do histamin trong vòng 24 giờ.
Trong các thử nghiệm lâm sàng trên người lớn và trẻ vị thành niên mắc viêm mũi dị ứng (theo mùa hoặc quanh năm), việc sử dụng Bilastin 20 mg một lần mỗi ngày trong 14 – 28 ngày đã giảm hiệu quả các triệu chứng như hắt hơi, chảy nước mũi, ngứa mũi, ngạt mũi, chảy nước mắt và đỏ mắt.
Bilastin kiểm soát triệu chứng hiệu quả trong vòng 24 giờ.
Trong các thử nghiệm lâm sàng, không ghi nhận trường hợp kéo dài khoảng QT hoặc tác dụng không mong muốn trên tim mạch của Bilastin, ngay cả khi sử dụng liều 200 mg mỗi ngày (gấp 10 lần liều điều trị) trong vòng 7 ngày trên 9 bệnh nhân hoặc kết hợp với các thuốc ức chế P-gp như ketoconazole (24 bệnh nhân) và erythromycin (1 bệnh nhân). Nghiên cứu theo dõi khoảng QT cũng không ghi nhận vấn đề với 30 người tình nguyện.
Trong các thử nghiệm lâm sàng kiểm soát, khi sử dụng liều khuyến cáo là 20 mg một lần mỗi ngày, Bilastin không gây ảnh hưởng đáng kể đến hệ thần kinh trung ương và không có tình trạng buồn ngủ khác biệt so với giả dược.
Đối với trẻ em, các nghiên cứu phát triển lâm sàng trên đối tượng thanh thiếu niên (từ 12 đến 17 tuổi) cho thấy không có sự khác biệt về hiệu quả và tính an toàn so với người trưởng thành. Trong các nghiên cứu lâm sàng, 128 thanh thiếu niên sử dụng Bilastin trong điều trị viêm mũi dị ứng và 116 thanh thiếu niên sử dụng giả dược, không có sự khác biệt đáng kể về hiệu quả và tính an toàn.
Tuy vậy, cơ quan quản lý dược phẩm châu Âu đã trì hoãn yêu cầu nộp kết quả nghiên cứu lâm sàng của Bilastin trên một nhóm đối tượng trẻ em trong điều trị viêm mũi dị ứng và mày đay.
Viêm mũi dị ứng
Trong hơn 4.600 bệnh nhân tham gia vào 10 thử nghiệm lâm sàng, hiệu quả của Bilastin trong điều trị viêm mũi dị ứng (AR) và mày đay đã được đánh giá. Tất cả các thử nghiệm so sánh Bilastin với giả dược và một loại thuốc kháng histamine thế hệ thứ hai khác có hiệu quả đã được chứng minh.
Trong các nghiên cứu về viêm mũi dị ứng (SAR), các nghiên cứu được tiến hành song song, mù đôi và kiểm soát giả dược trên nam và nữ bệnh nhân từ 12 tuổi trở lên có triệu chứng khi bắt đầu nghiên cứu. Các triệu chứng mũi (hắt hơi, chảy nước mũi, ngứa mũi và nghẹt mũi) được đánh giá hàng ngày trước và trong quá trình điều trị. Các triệu chứng không liên quan đến mũi (ngứa mắt, chảy nước mắt, ngứa tai và vòm miệng) cũng được đánh giá bằng một thang điểm từ 0-3, giúp phản ánh sự biến đổi hàng ngày của SAR ở từng bệnh nhân và nhóm điều trị. Đánh giá cũng được thực hiện về chất lượng cuộc sống và sự khó chịu, cũng như các tác dụng phụ và sự an toàn chung của liệu pháp.
Đối với mày đay, một bài báo tổng quan đã xem xét dữ liệu từ các thử nghiệm trên mô hình da và mề đay để đánh giá khả năng của Bilastin trong việc điều trị mày đay và cập nhật liều dùng.
Các tác giả kết luận rằng Bilastin có hiệu quả và an toàn tốt, tuy nhiên cần có thêm các thử nghiệm lâm sàng có kiểm soát để so sánh hiệu quả của Bilastin trong một nghiên cứu tăng liều thực tế ở bệnh nhân mày đay, đặc biệt là trong việc kiểm soát triệu chứng ngứa.
Dược động học
Hấp thu
Sau khi uống, Bilastin được hấp thu nhanh và đạt nồng độ tối đa trong huyết thanh sau khoảng 1,3 giờ. Thuốc không tích lũy trong cơ thể. Giá trị sinh khả dụng trung bình của Bilastin khi dùng đường uống là 61%.
Phân bố
Các nghiên cứu in vitro và in vivo cho thấy Bilastin là chất cơ chế của P-gp và CATP. Bilastin không tương tác với các chất vận chuyển BCRP hoặc các chất vận chuyển tại thận như OCT2, OAT1 và OAT3. Dựa trên các nghiên cứu in vitro, Bilastin không được dự đoán là gây ức chế cho các chất vận chuyển trong toàn hệ thống, bao gồm P-gp, MRP2, BCRP, BSEP, OATP1B1, CATP1B3, OATP2B1, OAT1, CAT3, OCT1, OCT2 và NTCP. Chỉ có mức độ ức chế thấp được ghi nhận với P-gp, OATP2B1 và OCT1, với giá trị ICso ước tính >300 MM, cao hơn nhiều so với nồng độ tối đa ước tính trong huyết thanh (Cmax). Vì vậy, các tương tác này không có ảnh hưởng lớn đến tác dụng lâm sàng của Bilastin.
Tuy nhiên, nghiên cứu cũng cho thấy Bilastin có thể có tác dụng ức chế lên các chất vận chuyển trên niêm mạc ruột.
Trong điều trị, Bilastin gắn kết với protein huyết tương ở tỷ lệ 84-90%.
Chuyển hóa
Các nghiên cứu in vitro cho thấy Bilastin không gây tác động hoặc ức chế hoạt động của các enzym CYP450.
Thải trừ
Trong một nghiên cứu cân bằng khối trên người tình nguyện khỏe mạnh, sau khi uống một liều duy nhất 20 mg 14C-Bilastin, gần như 95% liều dùng được tìm thấy trong nước tiểu (28,3%) và phân (66,5%) dưới dạng Bilastin không biến đổi.
Điều này cho thấy Bilastin không trải qua quá trình chuyển hóa quan trọng trong cơ thể người. Thời gian bán thải trung bình tính trên người tình nguyện khỏe mạnh là 14,5 giờ.
Độc tính của Bilastin
Độc tính của Bilastin đã được nghiên cứu trong các thử nghiệm tiền lâm sàng trên chuột nhắt, chuột cống và chó. Kết quả cho thấy không có trường hợp tử vong nào xảy ra sau khi uống liều lượng lớn Bilastin.
Đối với tiêm tĩnh mạch, giá trị LD50 (liều gây chết cho 50% động vật) là 33 mg/kg đối với chuột nhắt và 45-75 mg/kg đối với chuột cống.
Không có dấu hiệu nhiễm độc nào được quan sát ở bất kỳ cơ quan nào sau khi sử dụng liều lượng lớn Bilastin qua đường uống (ở chuột nhắt, chuột cống và chó) hoặc tiêm tĩnh mạch (ở chuột cống và chó) trong vòng 4 tuần.
Không có ảnh hưởng đến khả năng sinh sản, không có tác dụng gây quái thai hoặc gây đột biến, và không có dấu hiệu gây ung thư rõ ràng trong các nghiên cứu trên chuột cống, chuột nhắt và thỏ.
Tương tác của Bilastin với thuốc khác
Tương tác với nước bưởi chùm: Uống Bilastine 20 mg cùng nước bưởi chùm có thể giảm sinh khả dụng của thuốc khoảng 30%. Hiện tượng này cũng có thể xảy ra với các loại nước quả khác. Mức độ giảm sinh khả dụng có thể khác nhau tùy thuộc vào từng loại chế phẩm và loại hoa quả. Cơ chế tương tác này liên quan đến ức chế ATP 1A2, chất vận chuyển Bilastine từ đường tiêu hóa vào máu. Thuốc có tính cơ chất hoặc ức chế OATP1A2 như ritonavir hoặc rifampicin cũng có thể làm giảm nồng độ Bilastine trong huyết tương.
Tương tác với Ketoconazol hoặc Erythromycin: Uống Bilastine cùng lúc với Ketoconazol hoặc Erythromycin có thể làm tăng AUC (diện dưới đường cong nồng độ thời gian) của Bilastine lên gấp đôi và tăng Cmax (nồng độ tối đa) lên 2-3 lần. Điều này có thể được giải thích bởi tương tác với các chất vận chuyển đưa thuốc trở lại ruột, vì Bilastine là cơ chất của P-gp và không trải qua quá trình chuyển hóa. Tuy nhưng, những thay đổi này không ảnh hưởng đến mức độ an toàn của Bilastine cũng như Ketoconazol hoặc Erythromycin. Các thuốc khác có tính cơ chất hoặc ức chế P-gp, như Cyclosporine, cũng có khả năng tăng nồng độ Bilastine trong huyết tương.
Tương tác với Diltiazem: Uống Bilastine 20 mg và Diltiazem 60 mg cùng lúc có thể làm tăng nồng độ C (nồng độ tối đa) của Bilastine lên 50%. Hiện tượng này cũng liên quan đến tương tác với các chất vận chuyển đưa thuốc trở lại ruột và không ảnh hưởng đến mức độ an toàn của Bilastine.
Tương tác với Lorazepam: Uống Bilastine 20 mg và Lorazepam 3 mg cùng lúc trong vòng 8 ngày không gây tăng hiệu ứng trên hệ thần kinh trung ương của Lorazepam.
Tương tác với thức ăn: Có thể thức ăn ảnh hưởng đến sinh khả dụng của Bilastine qua đường uống, làm giảm khoảng 30%. Ngoài ra, thuốc này còn có tương tác với rượu.
Lưu ý khi dùng Bilastin
Lưu ý và thận trọng chung
Đối với trẻ em
Thông tin về độ hiệu quả và an toàn của Bilastin đối với trẻ em dưới 12 tuổi vẫn chưa được nghiên cứu đầy đủ.
Trên bệnh nhân suy thận nặng hoặc trung bình, việc sử dụng Bilastin cùng với các chất ức chế glycoprotein P như ketoconazole, erythromycin, cyclosporine, ritonavir hoặc diltiazem có thể làm tăng nồng độ Bilastin trong huyết thanh, gây tăng nguy cơ phản ứng phụ. Do đó, cần tránh sử dụng Bilastin cùng với các chất ức chế glycoprotein P trên bệnh nhân suy thận nặng hoặc trung bình.
Lưu ý trong hời kỳ mang thai
Hiện chưa có đủ dữ liệu hoặc chỉ có rất ít dữ liệu về việc sử dụng Bilastin trong thai kỳ.
Các nghiên cứu trên động vật không cho thấy tác động có hại trực tiếp hoặc gián tiếp đến khả năng sinh sản, phát triển của thai nhi và sau khi sinh. Tuy nhiên, để đảm bảo an toàn, nên tránh sử dụng Bilastin trong thời kỳ mang thai.
Lưu ý trong thời kỳ cho con bú
Hiện chưa có nghiên cứu trên con người để xác định liệu Bilastin có bài tiết vào sữa mẹ hay không. Dữ liệu dược động học trên động vật cho thấy Bilastin được bài tiết qua sữa. Do đó, cần quyết định tiếp tục cho con bú hoặc ngừng sử dụng Bilastin dựa trên sự cân nhắc giữa lợi ích của việc cho con bú và lợi ích của mẹ khi sử dụng Bilastin.
Lưu ý cho người lái xe và vận hành máy móc
Không ảnh hưởng. Tuy nhiên, cần thông báo cho bệnh nhân biết rằng có một số trường hợp hiếm gặp có thể gây buồn ngủ và ảnh hưởng đến khả năng vận hành máy móc hoặc lái xe.
Một vài nghiên cứu về Bilastine trong Y học
Hiệu quả và độ an toàn của bilastine ở bệnh nhân Nhật Bản bị viêm mũi dị ứng lâu năm: Một nghiên cứu giai đoạn III nhóm song song, ngẫu nhiên, mù đôi, có đối chứng với giả dược
Bối cảnh: Bilastine, một loại thuốc kháng histamine H1 thế hệ thứ hai không có tác dụng an thần , đã được phê duyệt ở hầu hết các nước châu Âu kể từ năm 2010. Nghiên cứu này nhằm đánh giá tính ưu việt của bilastine so với giả dược ở bệnh nhân Nhật Bản bị viêm mũi dị ứng lâu năm (PAR).
Phương pháp: Nghiên cứu giai đoạn III, ngẫu nhiên, mù đôi, có đối chứng với giả dược, nhóm song song (số đăng ký thử nghiệm JapicCTI-142600) đánh giá hiệu quả của thời gian điều trị 2 tuần bằng bilastine (20 mg một lần mỗi ngày), fexofenadine (60 mg hai lần mỗi ngày) hoặc giả dược phù hợp (hình nộm kép) ở bệnh nhân mắc bệnh PAR. Tất cả các bệnh nhân được hướng dẫn ghi lại các triệu chứng ở mũi và mắt trong nhật ký hàng ngày. Tiêu chí đánh giá chính là sự thay đổi trung bình về tổng số điểm triệu chứng ở mũi (TNSS) từ đường cơ sở đến Tuần 2 (Ngày 10-13).
Kết quả: Tổng số 765 bệnh nhân được phân bổ ngẫu nhiên để nhận bilastine, fexofenadine hoặc giả dược (lần lượt là 256, 254 và 255 bệnh nhân). Sự thay đổi trung bình về TNSS so với ban đầu ở Tuần 2 đã giảm đáng kể khi dùng bilastine (-0,98) so với giả dược (-0,63, P = 0,023). Bilastine và fexofenadine cho thấy không có sự khác biệt đáng kể về tiêu chí đánh giá chính. Tuy nhiên, sự thay đổi trung bình về TNSS so với ban đầu vào Ngày 1 đã giảm đáng kể khi dùng bilastine (-0,99) so với dùng giả dược (-0,28, P < 0,001) hoặc fexofenadine (-0,62, P = 0,032). Các loại thuốc tích cực cũng cải thiện TNSS tức thời 1 giờ sau lần dùng thuốc đầu tiên và trước lần dùng thuốc thứ hai vào Ngày 1 (P <0,05). Các loại thuốc nghiên cứu được dung nạp tốt.
Kết luận: Sau thời gian điều trị 2 tuần, bilastine 20 mg một lần mỗi ngày có hiệu quả và dung nạp được ở bệnh nhân Nhật Bản mắc bệnh PAR, và cho thấy tác dụng nhanh chóng.
Tài liệu tham khảo
- Drugbank, Bilastin, truy cập ngày 30/05/2023.
- Pubchem, Bilastin, truy cập ngày 30/05/2023.
- Okubo, K., Gotoh, M., Asako, M., Nomura, Y., Togawa, M., Saito, A., … & Ohashi, Y. (2017). Efficacy and safety of bilastine in Japanese patients with perennial allergic rhinitis: a multicenter, randomized, double-blind, placebo-controlled, parallel-group phase III study. Allergology International, 66(1), 97-105.
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Ý