Bệnh hô hấp, Ung thư
Chẩn đoán U phổi qua các đặc điểm và biểu hiện lâm sàng
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
Bài viết Chẩn đoán U phổi qua các đặc điểm và biểu hiện lâm sàng tải bản pdf Tại đây.
Tác giả TS.BS. NGUYỄN VĂN THÀNH.
ĐẶT VẤN ĐỀ
U phổi (lung tumor) là các tổn thương dạng u phát triển trong phổi. U phổi là thuật ngữ mang tính mô tả, không phản ánh bản chất bệnh học. U phổi có thể là lành tính, có thể là ác tính (cancer). U phổi có nguồn gốc từ nhiều dạng tế bào, có thể phổ biến, hiếm, thậm chí rất hiếm gặp.
Một số dạng u nguyên phát phổi
- U cơ trơn phế quản (bronchial leiomyoma): Là dạng u lành tính hiếm gặp. U hình thành từ cơ trơn phế quản, khí quản hoặc từ cấu trúc nhu mô phổi, thậm chí có thể từ cơ trơn mạch máu. Điển hình, u phát triển từ lớp cơ trơn phế quản, hình thành u đơn độc bám bên cạnh thành phế quản.
- Ung thư phổi (lung cancer): Là thuật ngữ thông thường chỉ ung thư liên bào phổi (carcinoma).
- U carcinoid phổi: Là u tế bào thần kinh – nội tiết phổi (lung neuroendocrine tumor). Có hai dạng điển hình và không điển hình. Dạng điển hình hiếm gặp, thường phát triển từ phế quản trung tâm thành dạng khối (mass) với tính chất ác tính thấp. Dạng không điển hình cũng hiếm gặp, với tính chất u tương tự như dạng điển hình nhưng có tính xâm lấn hơn, thường phát triển từ phế quản nhỏ.
- U phôi bào phổi – màng phổi (pleuropulmonary blastoma): Là ung thư hiếm gặp, xuất phát từ phổi hoặc màng phổi. Thường gặp trên trẻ em và người trẻ.
- U tế bào thần kinh – nội tiết của phổi: U phát triển từ các tế bào thần kinh – nội tiết, các tế bào có nhiệm vụ kiểm soát và sửa chữa cấu trúc biểu mô (tế bào có thể gặp ở đường tiêu hóa, tuyến giáp, buồng trứng). Các tế bào này có chức năng vừa giống tế bào thần kinh vừa có khả năng tạo ra nội tiết (nội tiết tế bào). U thần kinh nội tiết là rất đa dạng tế bào và cũng rất khác nhau về mức độ xâm lấn, đáp ứng điều trị và tiên lượng. Theo mức độ biệt hóa, nhóm này được chia thành 3 dạng biệt hóa rõ có tính xâm lấn thấp (trong đó gồm cả u carcinoid phổi điển hình), biệt hóa rõ có tính xâm lấn trung bình (trong đó gồm cả u carcinoid phổi không điển hình) và biệt hóa kém có tính xâm lấn cao (gồm cả ung thư tế bào lớn, tế bào nhỏ phổi).
- U lymphoma phổi: U xuất phát từ tế bào lymphocyte. Hầu hết lymphoma phổi là thứ phát sau các ung thư từ hạch bạch huyết, cấu trúc mô bạch huyết lan tới hạch bạch huyết phổi.
- Sarcoma phổi: Là dạng ung thư mô liên kết phổi rất hiếm gặp. Xuất phát từ rất nhiều loại tế bào mô liên kết (mô kẽ gian phế nang hay thành phế quản) và tính ác tính cao.
Các loại u phổi không thuộc u nguyên phát ở phổi:
- U trung thất: U trung thất là u ở khoang trung thất. Phổ biến nhất trong u trung thất là u nguồn gốc thần kinh (neurinoma), chiếm khoảng 20% u trung thất, thường ở khoang trung thất sau. Tiếp theo là u tuyến ức (thymoma), chiếm khoảng 15 – 20% u trung thất, thường ở khoang trung thất trước. Ung thư phổi cũng thường lan tới hạch ở trung thất.
- U màng phổi: U màng phổi thông thường là ung thư, hầu hết là do di căn. Ung thư tế bào nguồn gốc màng phổi nguyên phát, u trung biểu mô (mesothelioma) được cho là do phơi nhiễm với asbestos.
- U di căn phổi: Là ung thư từ cơ quan khác di căn tới phổi, còn gọi là ung thư phổi thứ phát. Ung thư di căn tới phổi thường từ bàng quang, vú, đại tràng, thận, tuyến tiền liệt.
Như vậy, một cách khái quát, chúng ta hiểu u phổi là một thuật ngữ mô tả tổn thương phổi thông thường dạng u, gồm cả ác tính và lành tính, nguyên phát hoặc thứ phát. Trong thuật ngữ này, y học cũng thường ghép vào các bệnh lý ác tính mà hình ảnh tổn thương không phải dạng u và những bệnh lý ác tính không thuộc phổi (trung thất, màng phổi).
U LÀNH TÍNH PHỔI
Đặc điểm bệnh học
Tổn thương phổi dạng nốt đơn độc (solitary pulmonary nodules) thấy trên khoảng 1-2/1.000 lần kiểm tra X-quang ngực. Khảng 30% trong số này là ác tính. Số còn lại là u lành tính, chiếm khoảng 2 – 5% các tổn thương u nguyên phát ở phổi.
U lành tính phổi có đa dạng nguồn gốc từ các cấu trúc phổi. Các dạng u lành tính bao gồm u tuyến phế quản (bronchial adenomas), loạn sản phổi (hamartomas) và các dạng loạn sản không phổ biến khác (như u sụn, u xơ, u mỡ, u cơ, u mạch máu, u quái…). Mặc dù u lành tính phổi không ảnh hưởng quan trọng tới sức khỏe nhưng có thể biến chứng làm bít tắc phế quản và gây ra viêm phổi, xẹp phổi, ho máu. U lành tính phổi thường không gây ra triệu chứng lâm sàng, hay gặp ở người lớn, tuổi trung bình là 65,2 cho tất cả các dạng.
Căn nguyên và sinh bệnh học của u lành tính phổi còn chưa được biết. Thuật ngữ u lành tính dựa trên đặc tính mô học. Trong khi một số dạng u thực sự có hình ảnh lành tính thì số khác lại mang đặc tính loạn sản như hamartomas. Các tổn thương u dạng tân sinh (neoplastic) tăng sản tự động, thoát cơ chế kiểm soát. Các khối u lành tính có thể phát triển lớn và xâm lấn ra bên ngoài cấu trúc tại chỗ. Cách phân loại u lành tính dựa theo bản chất giải phẫu bệnh học và trong thực hành thường kết hợp với vị trí để tiện sử dụng (thí dụ nội lòng phế quản, ngoại vi nhu mô phổi) và thêm thông tin tổn thương là đơn độc hay đa dạng. U lành tính phổi cũng được phân loại theo nguồn gốc của u, tuy nhiên trong đó cũng có những dạng u không xác định được nguồn gốc (hamartoma, tế bào sáng, u quái). Phân loại theo tế bào biểu mô như u nhú (papiloma), polyp. Phân loại theo tế bào nguồn gốc lá phôi giữa (mesodermal) như u sợi (fibroma), u mỡ (lipoma), u cơ trơn (leiomyoma), u sụn, u tế bào hạt (granular cell tumor), u mạch máu (hemangioma), và các dạng tế bào khác như u nguyên bào cơ (myofibroblastic tumor), u tế bào sắc tố vàng (xanthoma), u tế bào dạng tinh bột (amyloid), u nang lympho dọc theo niêm mạc (mucosa-associated lymphoid tumor).
Hai dạng chiếm tỷ lệ nhiều nhất trong u lành tính phổi là u loạn sản phổi (hamartomas) và u tế bào tuyến phế quản (adenomas).
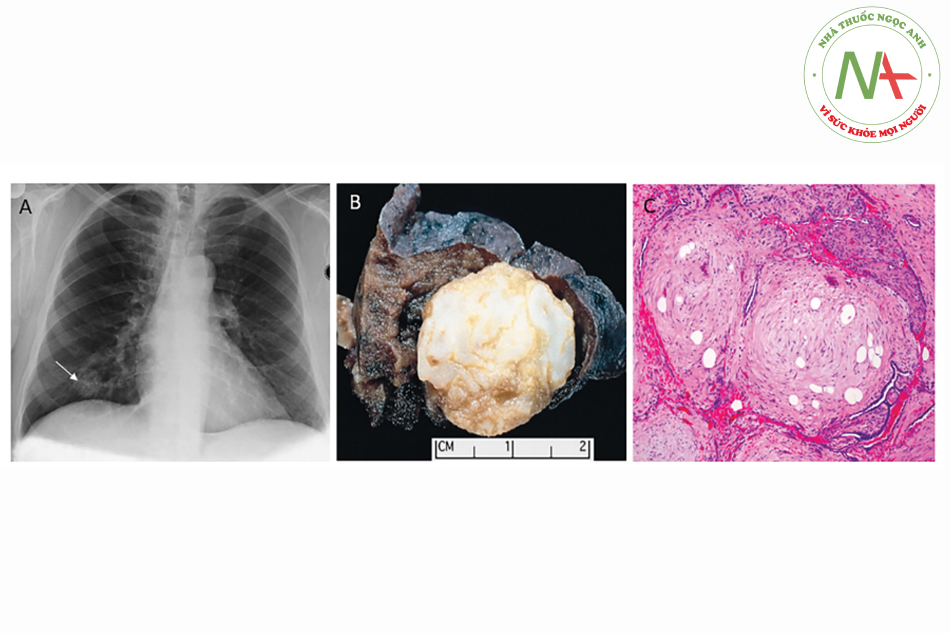
- U loạn sản phổi (hamartomas): Là phát triển u gồm các tế bào trưởng thành và mô cấu trúc lộn xộn. Cấu trúc u chủ yếu gồm các khối sụn trong (hyalin) kết hợp với mô liên kết, niêm dịch, tế bào mỡ, tế bào trơn và các khe nứt của biểu mô hô hấp. Hamartomas dạng sụn – tuyến (chondroadenomas) là dạng hay gặp nhất. U thường xuất hiện trên người lớn, khu trú ở ngoại vi phổi. Hình ảnh đại thể chắc đặc giống như đá cẩm thạch (hình 13.1). Về vi thể, u thường chứa các cấu trúc biểu mô, mô mỡ, sụn. Do đặc điểm cấu trúc như trên, cắt bỏ u thường dễ thực hiện, ngay cả khi thực hiện khoét hình chêm.
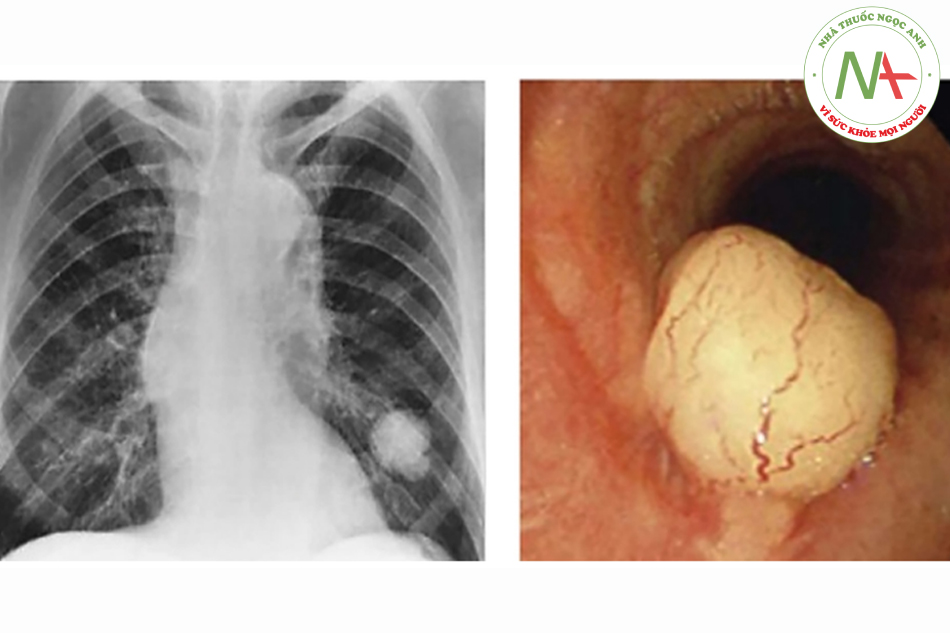
- U tuyến phế quản (bronchial adenomas): U tuyến phế quản chiếm tới 50% các trường hợp u lành tính phổi. Thuật ngữ u tuyến phế quản, nếu sử dụng theo cách không chặt chẽ, gồm u carcinoid, u nang tuyến (adenocystic carcinomas), u biểu bì nhầy (mucoepidermoid carcinomas). Đây là các dạng u với tính ác tính thấp. Thuật ngữ u tuyến phế quản có thể dễ làm lẫn lộn giữa u lành tính và u ác tính (adenocarcinoma). Trong u tuyến phế quản, u tuyến nhầy (mucous gland adenomas), phát triển từ các phế quản lớn, thực sự là u lành tính.
Chẩn đoán
Chẩn đoán ban đầu cần đánh giá đặc điểm của u. Biểu hiện lâm sàng phụ thuộc vào vị trí u (khí quản, đường thở hay nhu mô), kích thước u. Các tình huống chẩn đoán có thể là khối u phổi thấy được trên X-quang ngực, hình thâm nhiễm phổi điều trị như viêm phổi không giải quyết được, khò khè dai dẳng kiểu hen, ho dai dẳng, khó thở, ho máu, viêm phổi tái diễn, xẹp phổi. Đôi khi, u phổi lành tính chỉ phát hiện được tình cờ trên bệnh nhân hoàn toàn không có triệu chứng.
Chẩn đoán trước phẫu thuật có thể dựa trên kết hợp phân tích hình ảnh với sinh thiết qua nội soi hay sinh thiết xuyên thành ngực. Hầu hết các trường hợp chỉ được chẩn đoán mô học sau phẫu thuật cắt bỏ tổn thương. Chỉ định phẫu thuật cắt bỏ u trên một trường hợp u phổi không xác định là một quyết định phức tạp cần được phân tích cẩn thận trên nhiều yếu tố nguy cơ khác nhau và trên từng người bệnh. Hướng dẫn theo dõi và chẩn đoán bằng CT ngực của Hội Fleischner trên các khối u chưa xác định là rất khả dụng. Đây là hướng dẫn dựa trên các đánh giá của bản thân khối u và các yếu tố nguy cơ (bảng 13.1).
Bảng 13.1. Hướng dẫn xử trí khối u phát hiện tình cờ (không triệu chứng) bằng CT ngực (Fleischner Society 2017).
| U đặc (solide tumor) | |||
| Dạng u | Kích thước | ||
| Đơn độc | < 6mm
(< 100mm3) |
6 – 8mm
(100 – 250mm3) |
> 8mm
(> 250 mm3) |
| Nguy cơ thấp | Không theo dõi thường xuyên | CT 6 – 12 tháng sau đó xem xét 18-24 tháng | Xem xét CT sau 3 tháng, PET/CT hoặc sinh thiết |
| Nguy cơ cao | Theo dõi CT 12 tháng không bắt buộc | CT 6 – 12 tháng sau đó
18 – 24 tháng |
Xem xét CT sau 3 tháng, PET/CT hoặc sinh thiết |
| Đa dạng | |||
| Nguy cơ thấp | Không theo dõi thường xuyên | CT 3 – 6 tháng sau đó xem xét 18 – 24 tháng | CT 3 – 6 tháng sau đó xem xét 18 – 24 tháng |
| Nguy cơ cao | Theo dõi CT 12 tháng không bắt buộc | CT 3 – 6 tháng sau đó
18 – 24 tháng |
CT 3 – 6 tháng sau đó
18 – 24 tháng |
| U bán đặc (subsolide tumor) | |||
| Dạng u | < 6mm (< 100mm3) | > 6 – 8mm (> 100mm3) | |
| Kính mờ | Không theo dõi thường xuyên | CT sau 6 – 12 tháng để xác định có còn hiện diện. Nếu còn, CT lại mỗi 2 năm cho đến 5 năm. | |
| Đặc một phần | Không theo dõi thường xuyên | CT sau 6 – 12 tháng để xác định có còn hiện diện. Nếu không thay đổi và phần đặc < 6mm, CT lại mỗi năm cho đến 5 năm | |
| Đa dạng | CT 3 – 6 tháng, nếu ổn định, xem xét CT 2 – 4 năm | CT lại sau 3 – 6 tháng. Xử trí tiếp theo dựa trên nốt nghi ngờ nhất. | |
Chú ý: Không áp dụng cho tầm soát ung thư phổi, bệnh ung thư phổi nguyên phát, bệnh nhân suy giảm miễn dịch, bệnh nhân trẻ < 35 tuổi. Kích thước u là trung bình của trục dài và ngắn, làm tròn chính xác đến milimet.
Các tài liệu hướng dẫn khuyến cáo hạn chế các xử trí can thiệp cho những khối u chỉ phát hiện được tình cờ. Một trong các tổn thương thông thường phát hiện được tình cờ là dạng tổn thương nốt đơn độc. Chỉ định kỹ thuật xâm lấn để chẩn đoán và điều trị nhìn chung là rất quan trọng, chỉ thực hiện được ở tuyến chuyên khoa sâu. Kỹ thuật sinh thiết xuyên thành ngực có thể áp dụng dễ dàng nhất nhưng phụ thuộc nhiều vào kinh nghiệm thực hiện và hạn chế hiệu quả chẩn đoán khi khối u nhỏ, tổn thương dạng kính mờ. Các kỹ thuật sinh thiết phổi qua nội soi dưới hướng dẫn của siêu âm hay điện từ dẫn đường (E-BUS, ENB) giúp cải thiện nhiều hiệu quả sinh thiết qua nội soi. Kỹ thuật phẫu thuật và cắt tối thiểu cho phép chẩn đoán và điều trị trên một số chọn lọc bệnh nhân.
Theo dõi và chỉ định các biện pháp chẩn đoán cần dựa trên đánh giá nguy cơ. Nhóm nguy cơ thấp bao gồm trẻ tuổi, không hoặc ít hút thuốc lá, kích thước u nhỏ, bờ u rõ và đều, vị trí không ở thùy trên. Nhóm nguy cơ thấp có khả năng ung thư < 5%. Nhóm nguy cơ cao bao gồm cao tuổi, hút thuốc lá nhiều, kích thước u lớn, bờ u không đều hoặc có gai, ở thùy trên. Nhóm nguy cơ trung bình là nhóm chia cả các yếu tố nguy cơ cao và nguy cơ thấp.
UNG THƯ PHỔI NGUYÊN PHÁT
Lâm sàng
Bệnh nhân có triệu chứng lâm sàng nghi ngờ ung thư phổi cần được đánh giá lâm sàng chi tiết bằng các biện pháp không can thiệp hoặc can thiệp để xác định bản chất tế bào và định giai đoạn. Về mặt mô học, quan trọng nhất là chẩn đoán phân biệt được ung thư tế bào nhỏ hay không tế bào nhỏ. Khi đánh giá lâm sàng trên bệnh nhân nghi ngờ ung thư phổi cần đánh giá khả năng di căn, bệnh đồng mắc, tình trạng chức năng, hội chứng cận u và khả năng trị liệu ưu tiên.
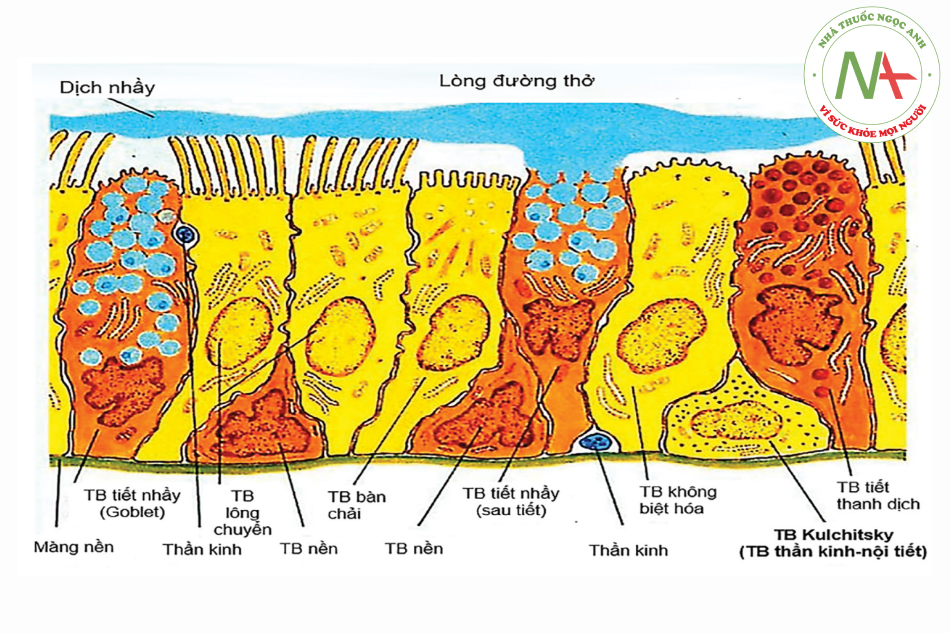
Về phân loại tế bào học, ung thư phổi được chia thành bốn nhóm chính, gồm ung thư dạng tế bào tuyến (adenocarcinoma), ung thư dạng tế bào gai (hay còn gọi là tế bào dạng biểu bì, tế bào vảy – squamous hoặc epidermoid), ung thư tế bào nhỏ và ung thư tế bào lớn không xếp loại. Các loại ung thư khác như ung thư tế bào nền (basaloid carcinomas) hoặc ung thư tế bào thần kinh – nội tiết (neuro-endocrine carcinoma) (hình 13.3) hiếm gặp. Về lâm sàng, điều trị và tiên lượng, các dạng ung thư theo tế bào học là khác nhau. Ung thư dạng tế bào nhỏ là loại ung thư xâm lấn nhất và là loại nhạy cảm nhất với hóa trị liệu, hơn hẳn so ba loại ung thư còn lại. Các loại ung thư dạng không tế bào nhỏ thường có cùng bệnh cảnh lâm sàng và phương pháp trị liệu. Do vậy thực chất ung thư phổi cần thiết phải phân biệt thành hai nhóm, đó là ung thư dạng tế bào nhỏ (small cell lung cancer, SCLC) và ung thư dạng không tế bào nhỏ (non-small cell lung cancer, NSCLC).
Khi có chẩn đoán ung thư phổi, thông thường bệnh nhân đã có triệu chứng. Tỷ lệ có triệu chứng thay đổi từ 40 – 98% các trường hợp tùy theo nhóm chẩn đoán thụ động hay nhóm chẩn đoán chủ động bằng tầm soát ung thư. Chỉ có dưới 10% các trường hợp là không triệu chứng khi có chẩn đoán ung thư phổi. Các triệu chứng phổ biến nhất là mệt mỏi (81%), ho (71%), khó thở (59%), sụt cân (54%), đau ngực (48%), và ho máu (25%).
Các triệu chứng ung thư phổi có thể chia thành ba nhóm.
- Nhóm các triệu chứng có liên quan đến sự phát triển của khối u trong lồng ngực.
- Nhóm các triệu chứng có liên quan đến di căn.
- Nhóm các triệu chứng toàn thân và triệu chứng có liên quan đến hội chứng cận u (paraneoplastic syndromes).
Thời gian từ khi xuất hiện triệu chứng tới khi đi khám bệnh trung bình là 103 ngày. Đây là điều cần lưu ý trong vấn đề giáo dục cộng đồng, nhất là với những người hút thuốc lá để có khả năng chẩn đoán sớm.
Khai thác tiền sử, khám lâm sàng và X-quang ngực là các bước đầu tiên và quan trọng trong chẩn đoán. Các bước tiếp theo là cần xác định bản chất ác tính của tổn thương, phân loại dạng tế bào ung thư và định giai đoạn phát triển của ung thư (staging). Bảng 13.2 trình bày dấu hiệu và triệu chứng ban đầu của ung thư phổi.
Bảng 13.2. Dấu hiệu và triệu chứng ban đầu ung thư phổi.
| Dấu hiệu và triệu chứng | Tỷ lệ (%) |
| Ho | 8 – 75 |
| Sụt cân | 0 – 68 |
| Khó thở | 3 – 60 |
| Đau ngực | 20 – 49 |
| Ho máu | 6 – 25 |
| Đau xương | 6 – 25 |
| Sốt | 0 – 20 |
| Mệt mỏi | 0 – 10 |
| Chèn ép tĩnh mạch chủ trên | 0 – 4 |
| Khó nuốt | 0 – 2 |
| Thở khò khè | 0 – 2 |
(Nguồn: Andersen HA và cs. Diagnosis of symptomatic lung cancer. Semin Respir Med. 1982;3:165-175; Grippi MA. Clinical aspects of lung cancer, Semin Roentgenol. 1990:25:12-24; Hyde L và cs. Clinical manifestations of lung cancer. Chest. 1974;65:299-306; Cromartie RS III và cs. Carcinoma of the lung. Ann Thorac Surg. 1980;30:30-35; Karsell PR và cs. Diagnostic tests for lung cancer. Mayo Clin Proc. 1993;68:288-296; American Thoracic Society, European Respiratory Society. Pretreatment evaluation of non-small-cell lung cancer. Am J Respir Crit Care Med. 1997;156:320-332).
Các triệu chứng liên quan sự phát triển của khối u trong lồng ngực
- Ho là triệu chứng hay gặp nhất trong ung thư. Ho có thể xuất hiện trong một thời gian dài trước khi có chẩn đoán. Ho máu là triệu chứng có thể thấy trên khoảng 25% các trường hợp mà điển hình là dạng lẫn máu trong đờm.
- Ho máu ở người hút thuốc lá là lý do thông thường khiến bệnh nhân đi khám, được chỉ định chụp X-quang ngực và nội soi phế quản.
- Đau ngực có thể do xẹp phổi, do u xâm lấn vào thành ngực, tràn dịch màng phổi hoặc tràn dịch màng ngoài tim ác tính.
- Khó thở thường xuất hiện ở giai đoạn muộn. Khó thở có thể do ung thư lan vào tổ chức bạch huyết, vào khí quản, vào phế quản lớn và hiếm khi vào dây thần kinh hoành.
- Khàn tiếng là triệu chứng xâm lấn của khối u hay hạch vào dây thần kinh quặt ngược thanh quản (thường là dây thanh trái). Triệu chứng này báo hiệu khả năng phẫu thuật không còn và tiên lượng rất xấu. Nội soi thanh quản dễ dàng nhận thấy di động hai dây thanh bất thường.
- Hội chứng chèn ép tĩnh mạch chủ trên thể hiện trên lâm sàng và X-quang do làm tắc nghẽn tĩnh mạch chủ trên hoặc hai nhánh tĩnh mạch vô danh. Bệnh biểu hiện bằng sưng phồng vùng cổ và mặt (phù áo khoác). Các tĩnh mạch bàng hệ ngực – bụng có thể nhìn thấy trên các vùng cao của cơ thể. Bệnh nhân có thể than phiền về các triệu chứng hô hấp, thần kinh trung ương do phù. Các triệu chứng như khó thở, nuốt khó hoặc các triệu chứng thần kinh trung ương cũng có thể do chính bản thân khối u gây ra mà không phải do phù.
- Hội chứng Pancoast: Các triệu chứng của hội chứng Pancoast được tạo ra do khối u vùng đỉnh phổi xâm lấn vào các tổ chức lân cận (đám rối thần kinh cánh tay, thân giao cảm, thành ngực, các xương sườn, các đốt sống ngực trên) và đè ép vào động – tĩnh mạch dưới đòn. Bệnh nhân có triệu chứng đau ngực do các phát triển ung thư vào xương sườn, thần kinh, cột sống. Tổn thương phát triển vào các thân dây thần kinh giao cảm gây ra hội chứng Horner (co đồng tử, sụp mi và thụt nhãn cầu vào trong) với các biểu hiện khô da hoặc quá tiết mồ hôi. Sự phá hủy các thân trên của đám rối thần kinh cánh tay (C8 và D1) tạo ra cảm giác đau ở xương trụ cánh tay và phá các cơ nhỏ của cánh tay. Có thể thấy hiện tượng hủy xương sườn trên X-quang ngực.
Hội chứng có liên quan đến khối u di căn
Gần một nửa số trường hợp ung thư loại không tế bào nhỏ và hơn hai phần ba các trường hợp ung thư tế bào nhỏ khi chẩn đoán đã có các biểu hiện di căn. Điều này giải thích lý do tại sao triệu chứng di căn thường là triệu chứng được phát hiện trong lần khám đầu tiên. Các triệu chứng thần kinh như cơn động kinh, triệu chứng liệt tăng dần có thể là các triệu chứng đầu tiên của di căn não. Đau xương hay gãy xương thông thường là triệu chứng di căn xương. Hiếm khi gặp các triệu chứng vàng da hoặc đau bụng do di căn gan.
Các triệu chứng của hội chứng cận u
Bao gồm các triệu chứng về lâm sàng, sinh học, X-quang kết hợp với khối u nhưng không phải do khối u xâm lấn hay đè ép. Sự hay gặp của các triệu chứng cận u thay đổi theo dạng tế bào ung thư. Các khối u như ung thư loại tế bào nhỏ thể hiện khả năng tiết ra các nội tiết thần kinh khác nhau và thể hiện các kháng nguyên bề mặt tế bào. Hầu hết các triệu chứng của hội chứng này trong ung thư phổi là phì đại xương khớp trong bệnh lý phổi, sự chế tiết không phù hợp của các hormon chống bài niệu, triệu chứng tăng năng vỏ thượng thận. Hội chứng thần kinh – cơ và hội chứng cận u khác là hiếm gặp. Hội chứng cận u bao gồm.
- Hội chứng phì đại xương – khớp trong bệnh lý phổi.
- Hội chứng chế tiết không phù hợp các hormon chống bài niệu.
- Hội chứng tăng năng nội tiết vỏ thượng thận.
- Hội chứng cận u làm tăng calci máu.
- Hội chứng thần kinh – cơ.
Cận lâm sàng
Tiếp theo các đánh giá lâm sàng, việc triển khai các kỹ thuật chẩn đoán không xâm lấn hoặc xâm lấn nhằm đạt được 2 yêu cầu: i) Thiết lập chẩn đoán tế bào học, ii) Xác định giai đoạn bệnh. Trừ khi bệnh nhân đang trong tình trạng không còn có thể đề xuất một phương pháp trị liệu nào, tất cả bệnh nhân đều cần được CT scan ngực. CT scan ngực cần khảo sát được cả phần bụng trên và tuyến thượng thận. CT scan cản quang giúp khảo sát tổn thương hạch ở rốn phổi và trung thất tốt hơn do tạo phản quang khác với cấu trúc mạch máu và cũng giúp nhìn rõ hơn tổn thương gan và thượng thận.
Hình ảnh học đóng vai trò cơ bản trong phân loại giai đoạn ung thư phổi. Các tiến bộ quan trọng về hình ảnh học như CT scan có độ phân giải cao, PET-CT (positron emission tomography/computed tomography) đã được áp dụng trong thực hành thường quy giúp tăng khả năng đánh giá và phân loại giai đoạn ung thư phổi (hình 13.4). Phân loại giai đoạn mới dựa trên các tiến bộ hình ảnh học này đã giúp cải thiện sự lựa chọn phương pháp điều trị và tiên lượng bệnh. Phân loại giai đoạn (staging) ung thư phổi có thể là lâm sàng (dựa trên X-quang và CT) và phân loại bệnh học (hay phân loại dựa trên phẫu thuật). PET-CT thông thường giúp tăng khả đánh giá giai đoạn lâm sàng (so với CT scan) do xác định được thêm các ổ tổn thương mới mà các phương pháp khảo sát khác không xác định được. Mức độ đồng thuận giữa phân loại lâm sàng và phân loại bệnh học chỉ đạt được khoảng từ 35 – 55%.
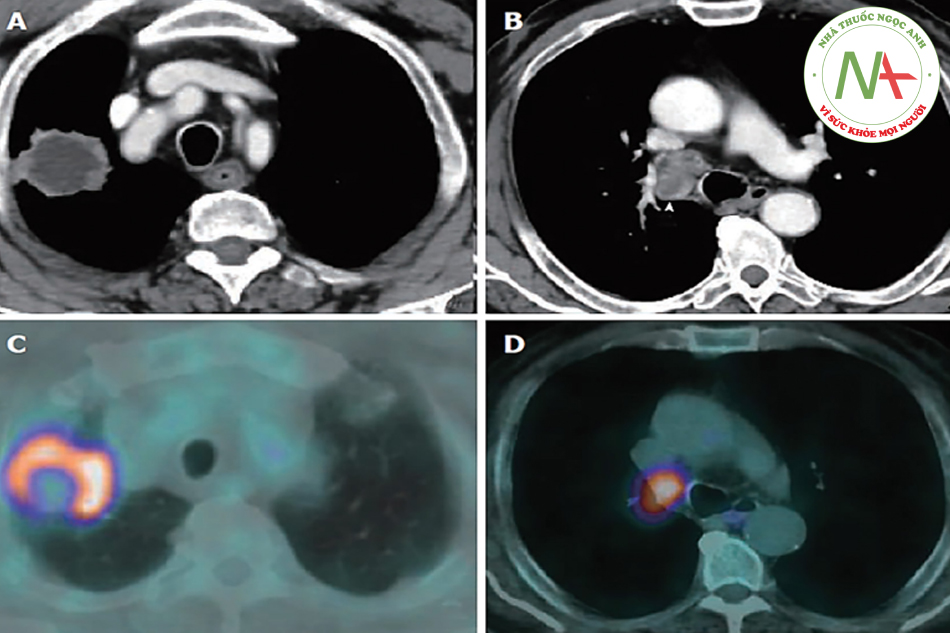
Hình ảnh CT scan giúp phác họa những nét chính của tổn thương như kích thước u, sự hiện diện của nốt u vệ tinh, hình ảnh xẹp phổi, nhiễm trùng hay xâm lấn vào cấu trúc lân cận. Đây là các yếu tố để xác định giai đoạn u (T). Hạch vùng cũng có thể xác định được trên CT scan. Hạch được xem là to khi có kích thước > 10mm đo ở chỗ đường kính nhỏ nhất. Hạch trung thất to rất nhiều khả năng do bị di căn. 62% hạch 10 – 15mm là ác tính và 90% hạch > 15mm là ác tính. Nếu hình ảnh rất gợi ý khối u di căn trung thất thấy được trên CT scan thì việc định giai đoạn tiếp theo là không cần thiết. CT scan còn giúp xác định có hay không bất thường màng phổi, thành ngực, màng tim, bất thường phổi đối bên.
PET (bằng 18-fluoro-2-deoxyglucose, FDG) đang đóng vai trò ưu thế trong đánh giá ban đầu ung thu phổi. Dương tính giả hay âm tính giả cũng có thể xảy ra do tăng hay giảm chuyển hóa FDG. Kết hợp PET-CT làm tăng khả năng phân tích chi tiết cấu trúc mô bất thường cũng như cấu trúc mô xung quanh. PET-CT có độ nhạy và độ đặc hiệu cao hơn CT scan trong việc đánh giá di căn hạch và có khả năng chẩn đoán di căn xa (gan, thượng thận, xương) rất tốt.
MRI scan là kỹ thuật hình ảnh được lựa chọn khi đánh giá di căn não. MRI có độ nhạy cao hơn CT scan khi khảo sát não. Nên chỉ định MRI scan khi có biểu hiện di căn (trên CT hoặc PET scan) và có các triệu chứng thần kinh hoặc các triệu chứng không đặc hiệu như sốt, sụt cân, mệt mỏi hay chán ăn. MRI scan cũng là lựa chọn trong trường hợp đánh giá tập trung các xâm lấn thành ngực, cơ hoành, u rãnh trên (superior sulcus tumors), đám rối cánh tay, cột sống.
Bất kỳ một tổn thương ngoài lồng ngực nào được phát hiện bằng hình ảnh học cũng nên sinh thiết nếu có thể để chẩn đoán mô học. Điều này không chỉ giúp cho chẩn đoán mô học ung thư phổi chính xác hơn mà còn góp phẩn chẩn đoán di căn ở cả SCLC và NSCLC.
=> Tham khảo: Xử trí hội chứng suy hô hấp cấp nặng: bước đầu.
Chẩn đoán
Đối với ung thư tế bào nhỏ
Đặc tính hình ảnh đặc biệt trên CT scan có thể gợi ý tổn thương do SCLC. Đặc biệt khi thấy các tổn thương dạng phì đại hạch lớn, xâm lấn vào trung thất trực tiếp hoặc khối lớn cạnh rốn phổi. Gợi ý này sẽ tăng lên nếu có hội chứng tiết hormone chống bài niệu không thích hợp với giảm natri máu, tiết ACTH lạc chỗ, hội chứng thần kinh cận u. Khi có chẩn đoán tế bào học SCLC, chẩn đoán giai đoạn cần tập trung để xác định tổn thương còn khu trú ở một bên phổi (khối u, hạch) hay đã lan tràn (tràn dịch màng phổi, màng tim, xâm lấn hạch thượng đòn, rốn phổi đối bên hay di căn xa). Việc xác định này giúp xác định đủ an toàn cho một cổng xạ trị. Nếu nghi ngờ bệnh ở giai đoạn lan tràn, bệnh nhân nên được đánh giá giai đoạn đầy đủ bằng CT scan tăng cản quang ngực, bụng, xương, và MRI hay CT scan tăng cản quang não. MRI là kỹ thuật hình ảnh được ưu tiên chọn trong trường hợp khảo sát di căn não. Do tế bào ung thư SCLC có tính chuyển hóa ác tính cao nên PET scan có độ nhạy 100% để phát hiện các khối u nguyên phát. Trong SCLC chẩn đoán giai đoạn cũng cần được xác định mô bệnh học bằng các kỹ thuật sinh thiết nếu có thể.
Đối với ung thư không tế bào nhỏ
Mục tiêu chẩn đoán trong trường hợp nghi ngờ NSCLC là thu được bệnh phẩm đủ để chẩn đoán mô bệnh học, gen và xác định giai đoạn bằng các kỹ thuật ít can thiệp nhất có thể. Nếu có chẩn đoán hình ảnh gợi ý tổn thương di căn xa thì vị trí này nên được lấy bệnh phẩm chẩn đoán trước.
Tế bào học đờm là cách chẩn đoán ít can thiệp nhất. Tuy nhiên hiệu quả chẩn đoán tùy thuộc rất nhiều vào kỹ thuật xử lý bệnh phẩm và năng lực phân tích tế bào học. Sự lập lại kết quả nhiều lần giống nhau làm tăng giá trị chẩn đoán. Hiệu quả chẩn đoán tế bào học đờm sẽ tăng nếu khối u ở trung tâm, khối u lớn, ung thư tế bào gai, có triệu chứng ho máu.
Chọc dò và phân tích tế bào dịch màng phổi khi có tràn dịch. Chẩn đoán tế bào học dịch màng phổi dương tính không chỉ giúp xác định ung thư mà còn giúp chẩn đoán giai đoạn IV trong NSCLC và giai đoạn lan tràn trong SCLC. Kết hợp siêu âm tại giường với thủ thuật chọc dò màng phổi làm tăng tính an toàn và hiệu quả của thủ thuật này. Hình ảnh siêu âm cũng có thể giúp phát hiện các bất thường trên màng phổi (dày, nốt). Nên có 50ml dịch để xét nghiệm tế bào học. Nhiều dịch hơn cũng không làm tăng khả năng chẩn đoán. Có thể làm lặp lại nhiều lần xét nghiệm dịch màng phổi. Khi có tràn dịch, sinh thiết màng phổi mù hay có hướng dẫn hình ảnh qua da làm tăng hiệu quả chẩn đoán. Sinh thiết màng phổi qua nội soi lồng ngực (thoracoscopy) trong tràn dịch màng phổi ác tính có độ nhạy cao. Tuy nhiên khi trên CT scan đã nhìn thấy dày màng phổi, nốt màng phổi thì hiệu quả sinh thiết qua da có kết quả với tỷ lệ tương đương. Như vậy sinh thiết qua nội soi lồng ngực nội hay ngoại khoa chỉ nên dành cho những trường hợp tràn dịch màng phổi không có điểm đích để sinh thiết màng phổi qua da.
Cách lấy bệnh phẩm chẩn đoán mô học
Có nhiều kỹ thuật lấy bệnh phẩm chẩn đoán mô học u tiên phát. Hiệu quả chẩn đoán tùy thuộc nhiều vào đặc tính u và các kỹ thuật kết hợp (bảng 13.3).
Bảng 13.3. Phương pháp lấy bệnh phẩm chẩn đoán mô, tế bào học ung thư.
| Phương pháp | Phân tích |
| Sinh thiết hoặc FNA tổn thương di căn hoặc hạch có thể tiếp cận được | Thực hiện khi có thể sờ thấy hạch |
| Chọc hút hoặc sinh thiết bằng kim xuyên thành ngực (qua da) dưới hướng dẫn của CT scan | Độ nhạy cao với tổn thương sát thành ngực, thấp với tổn thương nhỏ. Biến chứng tràn khí màng phổi. |
| Nội soi kết hợp chải, rửa phế quản | Độ nhạy cao với tổn thương trung tâm nhưng thấp với tổn thương ngoại vi. |
| Sinh thiết phế quản qua nội soi | Cho tổn thương trung tâm. |
| Nội soi sinh thiết dưới hướng dẫn điện-từ trường cho tổn thương ngoại vi | Cần có trang thiết bị và người nội soi được đào tạo kỹ thuật. |
| Sinh thiết xuyên thành dưới hướng dẫn của siêu âm nội lòng phế quản | Độ nhạy cao với tổn thương trung tâm nhưng thấp với tổn thương ngoại vi. Cần có người nội soi được đào tạo kỹ thuật. |
| Sinh thiết màng phổi | Nếu có tràn dịch màng phổi và tế bào học dịch màng phổi (-). |
| Phân tích tế bào học đờm | Áp dụng cho tổn thương trung tâm. Không xâm lấn. Có thể làm nhiều lần. |
| Phân tích tế bào học dịch màng phổi | Nếu có tràn dịch màng phổi. Nên chọc dưới hướng dẫn siêu âm để tránh tràn khí màng phổi. Có thể làm nhiều lần xét nghiệm. |
| Nội soi lồng ngực (VATS) | Chỉ định cho nốt phổi đơn độc nguy cơ cao. |
FNA: Chọc hút bằng kim nhỏ (fine needle aspiration), VATS: Thủ thuật nội soi lồng ngực ngoại khoa có video trợ giúp (video-assisted thoracoscopic surgery).
Nội soi phế quản có chỉ định để lấy bệnh phẩm khối u phổi cũng như hạch trung thất. Hiệu quả chẩn đoán cao khi sinh thiết được trực tiếp trên khối u và thực hiện sinh thiết nhiều lần. Tối thiểu một lần soi cũng nên thực hiện để có 3 mẫu sinh thiết. Hiệu quả của chải và rửa phế quản thấp hơn sinh thiết. Kết hợp các kỹ thuật trên sẽ làm tăng hiệu quả chẩn đoán. Hình ảnh nội soi và kết quả sinh thiết cũng giúp chẩn đoán giai đoạn ung thư khi kết luận tổn thương ung thư ở khu vực phế quản nào (phế quản thùy, phế quản gốc hay carina). Các kỹ thuật lấy bệnh phẩm từ khối u ngoại vi qua nội soi phế quản bằng kỹ thuật thông thường có hiệu quả rất thấp. Độ nhạy của bệnh phẩm chẩn đoán ung thư nếu áp dụng tất cả các kỹ thuật (chải, rửa, sinh thiết xuyên thành, hút xuyên thành) là 78%. Các kỹ thuật mới được áp dụng như nội soi có hướng dẫn điện – từ (electromagnetic navigational bronchoscopy, ENB) và nội soi kết hợp siêu âm nội lòng phế quản (radial probe endobronchial ultrasound, R-EBUS) có thể làm tăng hiệu quả chẩn đoán của kỹ thuật sinh thiết xuyên thành các tổn thương ngoại vi. Kỹ thuật nội soi ENB giúp cho người nội soi xác định được đường đi tới tổn thương ngoại vi dựa trên một sơ đồ ảo hình ảnh phân chia các phế quản. Kết hợp cả R-EBUS với ENB khả năng chẩn đoán lên tới 93%.
Các kỹ thuật lấy bệnh phẩm qua thành ngực dưới hướng dẫn của hình ảnh học cho kết quả tốt đối với các tổn thương ngoại vi. Sinh thiết kim có nòng (core) mặc dù không làm tăng độ nhạy nhưng giúp lấy được bệnh phẩm chất lượng cao cho nhuộm hóa mô và chẩn đoán phân tử. Trên cơ sở này giúp chẩn đoán tổn thương lành tính rất tốt.
Sinh thiết qua nội soi lồng ngực có hỗ trợ video (video-assisted thoracoscopic surgery, VATS) có hiệu quả chẩn đoán cao nhất nhưng cần thực hiện với điều kiện chuyên môn cao.
Nhìn chung, kỹ thuật lấy bệnh phẩm qua nội soi phế quản vẫn là ưu tiên lựa chọn hiện nay, nhất là khi có khả năng kết hợp EBUS hay ENB. Hơn nữa nội soi phế quản cũng có thể giúp cho đánh giá tổn thương trung thất.
Phân loại giai đoạn
Phân loại giai đoạn (staging) ung thư phổi theo khối u, hạch và di căn (tumor, lympho node, metastasis, TNM) trước đây chỉ để sử dụng cho ung thư không tế bào nhỏ. Đối với ung thư tế bào nhỏ chỉ phân loại “khu trú” (local) hay “lan tràn” (extensive). Phân giai đoạn hữu dụng nhất là phân giai đoạn lâm sàng. Phân giai đoạn bệnh học sẽ được thực hiện chỉ sau khi thực hiện phẫu thuật cắt phổi. Dưới đây là bảng phân loại giai đoạn theo TNM của Hội nghiên cứu Ung thư phổi quốc tế (International Association for the Study of Lung Cancer – IASLAC) lần thứ 7, năm 2007 có thể áp dụng để tham khảo phân loại cho ung thư phổi cả hai dạng ung thư tế bào nhỏ và không tế bào nhỏ (bảng 13.4a, 13.4b).
Bảng 13.4a. Phân loại giai đoạn TNM (IASLAC).
| Phân loại | Mô tả | |
| Khối u tiên phát (T) | T1 | Khối u < 3cm không xâm lấn vào phế quản thùy và màng phổi tạng |
| T1a
T1b |
Khối u < 3cm
Khối u > 2cm – < 3cm |
|
| T2 | Khối u > 3cm – < 7cm hoặc đã xâm lấn vào phế quản gốc hoặc đã xâm lấn vào màng phổi tạng hoặc kết hợp xẹp phổi, viêm phổi tắc nghẽn mở rộng đến rốn phổi. | |
| T2a
T2b |
Khối u > 3cm – < 5cm
Khối u > 5cm – < 7cm |
|
| T3 | Khối u > 7cm hoặc đã xâm lấn trực tiếp vào cơ hoành, thành ngực, thần kinh hoành, trung thất, màng phổi thành, màng ngoài tim hoặc xẹp hoặc viêm phổi tắc nghẽn toàn bộ phổi hoặc có nốt u vệ tinh trong cùng 1 thùy. | |
| T4 | Khối u đã xâm lấn vào trung thất hoặc khí quản hoặc thần kinh quặt ngược hoặc carina hoặc thân đốt sống hoặc có nốt u vệ tinh ở thùy phổi khác của phổi cùng bên | |
| Hạch vùng (N) | N0
N1 N2 N3 |
Không di căn hạch vùng
Di căn hoặc mở rộng trực tiếp hạch quanh phế quản cùng bên, hạch trong phổi hoặc hạch rốn phổi. Di căn vào hạch trung thất cùng bên hoặc hạch dưới carina. Di căn vào cơ thang hoặc hạch thượng đòn hoặc hạch, trung thất đối bên. |
| Di căn xa (M) |
M0 M1 M1a M1b |
Không di căn xa
Có di căn xa Có nốt u phổi vệ tinh ở phổi đối bên, nốt màng phổi hoặc tràn dịch màng phổi, màng tim. Di căn ngoài lồng ngực |
Nguồn: The IASLC Lung Cancer Staging Project: proposals for the revision of the TNM stage groupings in the forthcoming (seventh) edition of the TNM Classification of malignant tumours. Journal of Thoracic Oncology. 2007;2(8):706-714
Dưới đây là phân loại giai đoạn ung thư theo phiên bản lần thứ 6 và 7 (bảng 13.4b).
Bảng 13.4b. Phân giai đoạn ung thư phổi (IASLAC).
| Giai đoạn | Phân loại lần thứ 6 | Phân loại lần thứ 7 |
| IA | T1, N0, M0 | T1a-T1b, N0, M0 |
| IB | T2, N0, M0 | T2a, N0, M0 |
| IIA | T1, N1, M0 | T1a-T1b, N1, M0
T2a, N1, M0 T2b, N0, M0 |
| IIB | T2, N1, M0
T3, N0, M0 |
T2b, N1, M0
T3, N0, M0 |
| IIIA | T3, N1, M0
T1-3, N2, M0 |
T1-T2, N2, M0
T3, N1-N2, M0 T4, N0-N1, M0 |
| IIIB | T4, N0-N2, M0
T1-4, N3, M0 |
T4, N2, M0
T1-T4, N3, M0 |
| IV | T1-4, N0-N3, M1 | T1-T4, N0-N3, M1a-M1b |
Chẩn đoán di căn hạch trung thất
Khoảng 1/3 số bệnh nhân ung thư phổi có tổn thương trung thất khi chẩn đoán (tức là N2, N3). Chẩn đoán giai đoạn trung thất là yếu tố cốt lõi cho đánh giá giai đoạn ung thư và làm cơ sở cho quyết định phẫu thuật. Chẩn đoán giai đoạn trung thất chỉ không còn giá trị khi đã xác định được có tổn thương di căn xa hoặc khi bệnh nhân không còn bất kỳ một chỉ định điều trị nào. Bảng 13.5 phân loại tổn thương trung thất dựa trên các đặc tính
CT ung thư phổi NSCLC. Như vậy khảo sát trung thất bằng CT ung thư NSCLC có thể được xếp vào 1 trong 4 dạng.
- Dạng A: Với hình ảnh xâm nhiễm ác tính vào trung thất làm cho trung thất thay đổi với các ranh giới giải phẫu bình thường không còn. Với nhóm này mục tiêu là làm sao để có bệnh phẩm chẩn đoán mô học bằng kỹ thuật ít can thiệp nhất.
- Dạng B: Hình ảnh hạch riêng biệt, to ra nhưng không đủ bằng chứng nói rằng đó là ác tính.
- Dạng C: Gồm những trường hợp tổn thương trung tâm hoặc N2 nhưng hình ảnh hạch trung thất bình thường.
- Dạng D: Gồm những trường hợp có tổn thương phổi ngoại vi nhưng hạch trung thất và rốn phổi bình thường.
Bệnh nhân nhóm B, C cần có khảo sát đánh giá giai đoạn trung thất. Các kỹ thuật đánh giá trung thất bao gồm chọc xuyên thành ngực bằng kim hút (transthoracic needle aspiration, TTNA), chọc xuyên phế quản bằng kim hút (transbronchial needle aspiration, TBNA) kết hợp hay không EBUS, siêu âm qua nội soi (endoscopic ultrasound, EUS), nội soi trung thất.
Bảng 13.5. Phân dạng tổn thương trung thất dựa trên đặc tính CT scan.
Dạng A: Xâm nhiễm trung thất: Xâm lấn u với ranh giới giải phẫu bình thường không thể phân biệt được.
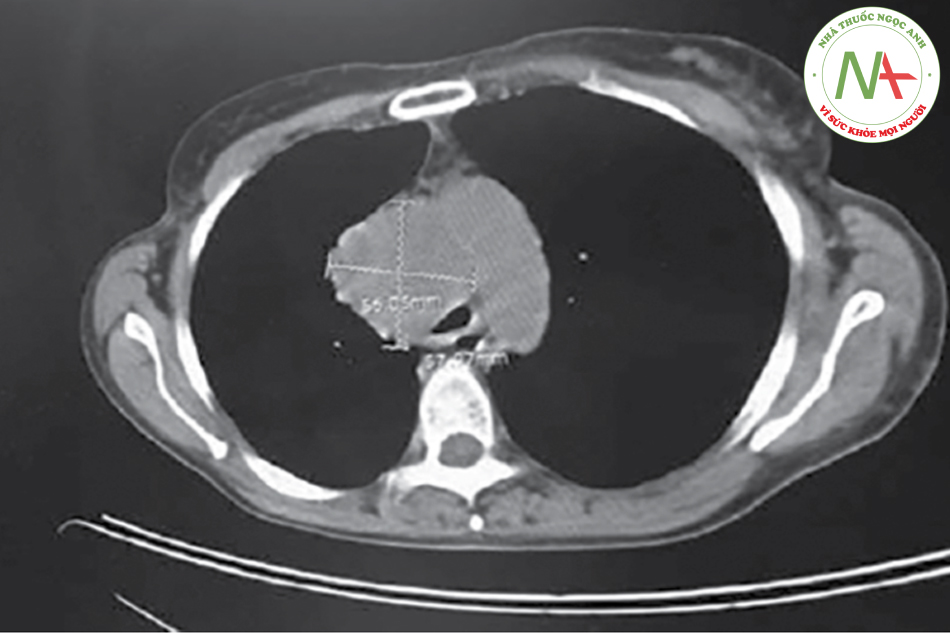
Dạng B: Hạch trung thất riêng biệt to ra, đường kính nhỏ nhất đo được trên CT scan > 10mm (hình bên là hạch cạnh phải khí quản).
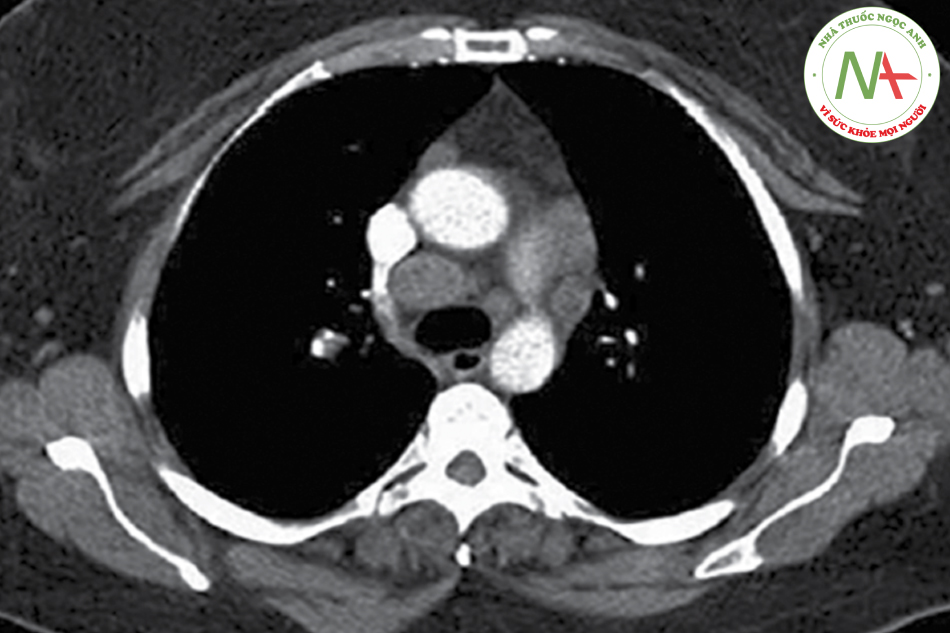
Dạng C: Khối u trung tâm giai đoạn I: Hạch N1 nhưng hạch trung thất không to.
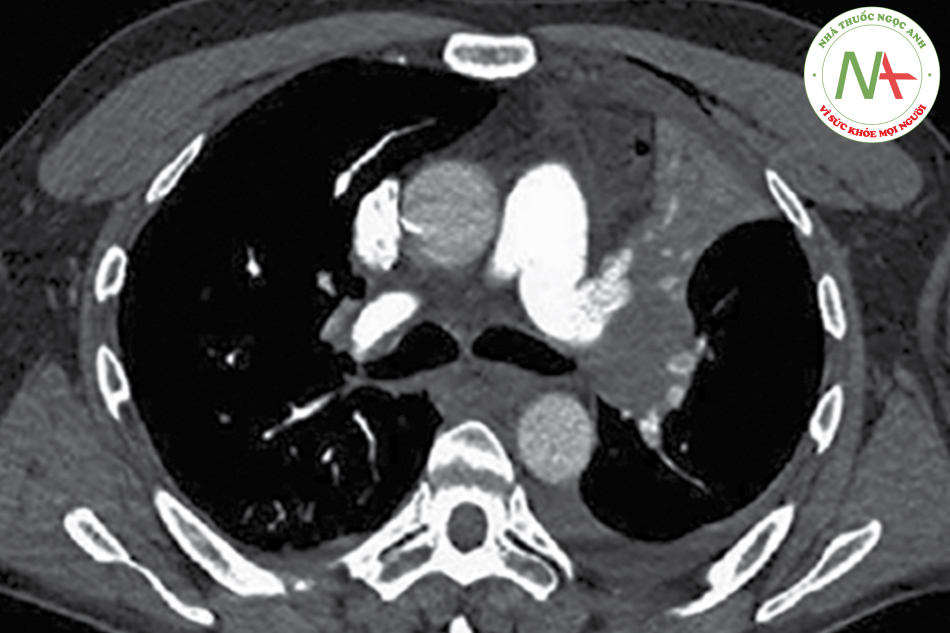
Dạng D: Khối u ngoại vi giai đoạn I: Hạch trung thất và rốn phổi bình thường.
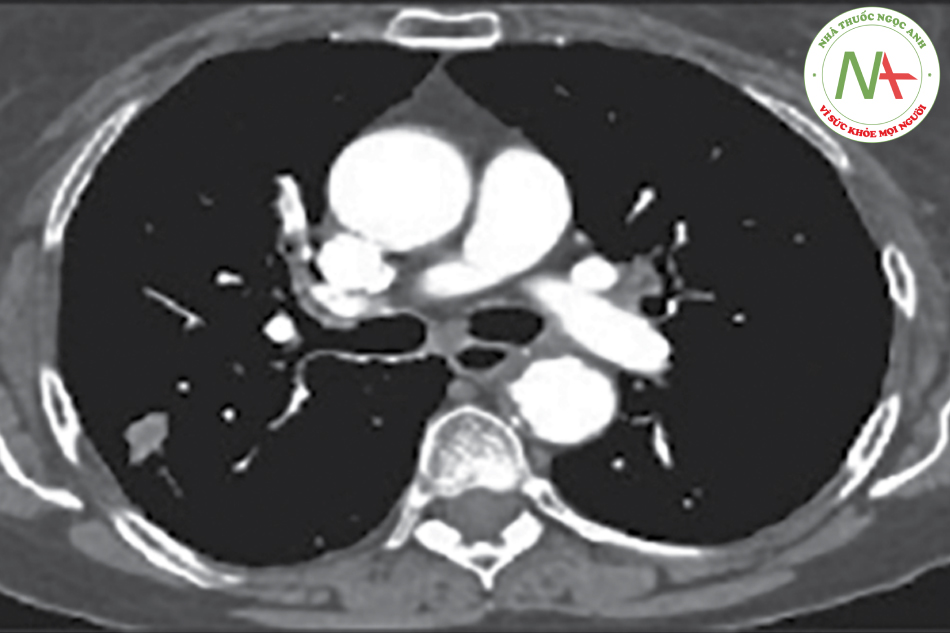
Phân loại dạng tổn thương trung thất trên không bao gồm u liên tục trung thất hoặc thành ngực. Nguồn: Detterbeck F Invasive mediastinal staging of lung cancer. Chest. 2007;132(3 Suppl) :202S-220S.
Tài liệu tham khảo
- Dale K Mueller. Benign Lung Tumors. img.medscape.com/pi/iphone/medscapeapp/html/A426952-business.html (online).
- Jeffrey I. Myers, Douglas A. Arenberg. Chapter 56. Benign lung tumors. in Murray & Nadel’s Textbook of Respiratory. Medicine 6th edition 2016.
- Heber MacMahon et al. Guidelines for Management of incidental Pulmonary nodules Detected on CT images: From the Fleischner Society 20171. rsna.org. Radiology: Volume 284: Number 1, July 2017.
- Ross H. Albert et al. Evaluation of the Solitary Pulmonary Nodule. Am Fam Physician. 2009;80(8):827-831, 834.

Bị đau ngực, khó thở, ro ra máu thì có phải bị ung thư phổi không a
Dạ các dấu hiệu này có khả năng mắc ung thư phổi. Tuy nhiên, bạn cần đến bệnh viện thăm khám để được chấn đoán kết quả chính xác nhất ạ