Bệnh hô hấp
Theo dõi Carbon Dioxide thở ra ở bệnh nhân đặt và không đặt nội khí quản
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
Bài viết Theo dõi Carbon Dioxide thở ra ở bệnh nhân đặt và không đặt nội khí quản – tải về file pdf ở đây.
Bản dịch của BS. Đặng Thanh Tuấn – BV Nhi Đồng 1.
Tóm tắt
Trong vài thập kỷ qua, việc đánh giá CO2 thở ra ở cả bệnh nhân đặt nội khí quản và không đặt nội khí quản đã phát triển thành một thành phần thiết yếu trong nhiều khía cạnh theo dõi bệnh nhân. Bên cạnh việc đánh giá cơ bản về thông khí, theo dõi CO2 thở ra có thể cung cấp thông tin có giá trị về an toàn cho bệnh nhân và dữ liệu sinh lý quan trọng liên quan đến thông khí và tưới máu phù hợp trong phổi, cung lượng tim và tốc độ chuyển hóa. Mặc dù có những lợi ích theo dõi lâm sàng quan trọng và tính sẵn có rộng rãi, nhưng việc theo dõi CO2 thở ra thường không được sử dụng đúng mức. Mục đích của bài viết này là xem xét tầm quan trọng và trình bày kiến thức sâu rộng để hỗ trợ việc sử dụng CO2 thở ra giám sát trong các lĩnh vực khác nhau của thực hành lâm sàng. Các khái niệm ứng dụng nâng cao và sự phát triển trong tương lai của việc theo dõi CO2 thở ra cũng sẽ được thảo luận.
Giới thiệu
Phép đo CO2 trong không khí lần đầu tiên được phát triển vào khoảng năm 1918 và được thực hiện để phân tích nồng độ khí trong các mỏ.1 Quá trình phân tích này hết sức tẻ nhạt, sử dụng một thiết bị phức tạp liên quan đến việc đo lượng CO2 và các loại khí khác được hấp thụ hóa học từ một thể tích khí đã biết. Thể tích CO2 hấp thụ sau đó được so sánh với tổng thể tích khí, cho ra phần trăm CO2 hiện có. Một thập kỷ sau, một kỹ thuật đã được phát triển để phân tích CO2 thở ra từ một hơi thở trong khi tập thể dục.2 Quá trình này đòi hỏi phải thu giữ khí thở ra bằng cách sử dụng một hệ thống có kích thước bằng buồng điện thoại bao gồm một loạt van được điều khiển bằng cơ điện, dẫn các phần khí thở ra tuần tự vào 6 túi cao su nhỏ. CO2 thu được trong mỗi túi sau đó được phân tích nhiều lần để thu được CO2 trung bình, được vẽ biểu đồ theo thời gian, từ đó tạo ra biểu đồ khí thở ra đầu tiên. Đến những năm 1970, CO2 thở ra đã được theo dõi trong các ICU sử dụng hệ thống khối phổ hút khí thở ra qua các ống mao dẫn dài đến vị trí giám sát trung tâm.3,4 Đo định kỳ áp suất riêng phần của CO2 cuối triều (PETCO2) xảy ra theo lịch trình đã định thời gian hoặc theo vòng tuần tự khi chu kỳ lấy mẫu luân phiên giữa một số giường được giám sát.4 Với sự ra đời của cảm biến hồng ngoại nhỏ hơn, thiết bị theo dõi CO2 thở ra di động đã xuất hiện trên giường bệnh vào những năm 1980. Hiện đã có 5 máy theo dõi CO2 thu nhỏ có thể nằm gọn trong lòng bàn tay và có khả năng hiển thị biểu đồ CO2 thở ra.6,7
Sự tiến bộ về công nghệ theo dõi CO2 thở ra trùng hợp với sự phát triển của việc sử dụng và tầm quan trọng trong thực hành lâm sàng. Tầm quan trọng của việc theo dõi CO2 thở ra còn vượt xa việc sử dụng cơ bản việc theo dõi mức độ thông khí đầy đủ. Phát hiện khí CO2 thở ra đã được chứng minh là một cơ chế vô giá để xác nhận việc đặt nội khí quản, nhận biết tình cờ đặt nội khí quản vào thực quản và các lợi ích quan trọng khác về an toàn cho bệnh nhân. Những cải tiến bảo vệ bệnh nhân được cung cấp bởi việc theo dõi CO2 cũng bao gồm: phát hiện tình trạng ngắt kết nối, tắc nghẽn đường thở xâm lấn và theo dõi tình trạng suy hô hấp sau phẫu thuật, trong khi gây mê trong thủ thuật và trong quá trình giảm đau do bệnh nhân kiểm soát. Điều quan trọng nhất là việc sử dụng PETCO2 để đánh giá hiệu quả của hồi sức tim phổi (cardiopulmonary resuscitation, CPR), dự đoán kết quả và hướng dẫn việc tiếp tục nỗ lực hồi sức.8 CO2 thở ra cũng có thể được mô tả là dấu hiệu sinh tồn của thông khí và tưới máu vì thể tích CO2 được bài tiết bởi hệ thống tim mạch là một chỉ số nhạy cảm không chỉ về hiệu quả thông khí mà còn về tưới máu phổi và cung lượng tim. Thể tích CO2 thở ra mỗi phút ( CO2) cũng có thể được sử dụng để ước tính tốc độ chuyển hóa và nhu cầu dinh dưỡng của bệnh nhân nguy kịch.9
Sự công nhận và tầm quan trọng của việc theo dõi CO2 thở ra trong nhiều lĩnh vực chăm sóc bệnh nhân đã dẫn đến khuyến nghị mở rộng việc sử dụng nó bởi các cơ quan quản lý và đưa vào các tiêu chuẩn và hướng dẫn thực hành của nhiều tổ chức chuyên môn, chẳng hạn như Hiệp hội Gây mê Hoa Kỳ (ASA), Hiệp hội Tim mạch Hoa Kỳ, Hiệp hội Chăm sóc Hô hấp Hoa Kỳ, Ủy ban Hỗn hợp và Trung tâm Dịch vụ Medicare và Medicaid. Bất chấp mức độ nhận thức cao cũng như hướng dẫn về quy định và tổ chức, việc theo dõi CO2 thở ra thường không được sử dụng đúng mức.8,10–16
Nguyên nhân của sự chênh lệch giữa kiến thức và thực hành có thể một phần là do gánh nặng chi phí để có được công nghệ; thời gian bác sĩ cần thiết để thiết lập, bảo trì và xử lý sự cố; và thiếu nhận thức về các phương pháp hay nhất để sử dụng tối ưu. Các tiêu chuẩn chăm sóc được chấp nhận rộng rãi bắt buộc sử dụng theo dõi CO2 trong các trường hợp cụ thể hoặc các loại bệnh nhân mang lại khả năng tác động cao nhất đến sự an toàn của bệnh nhân và ảnh hưởng đến kết quả cũng đang thiếu.
Mục đích của đánh giá này là nâng cao nhận thức và hiểu biết của các nhà cung cấp dịch vụ chăm sóc sức khỏe về tầm quan trọng của việc theo dõi CO2 thở ra và ứng dụng của nó trong thực hành lâm sàng. Tiếp theo việc đánh giá các công nghệ khác nhau sẽ là việc xem xét các chỉ dẫn đã được công nhận để theo dõi và đánh giá tiềm năng tiến bộ hơn nữa trong việc theo dõi CO2 thở ra.
=> Tham khảo: Hướng dẫn ESICM về hội chứng nguy kịch hô hấp cấp tính: định nghĩa, kiểu hình và chiến lược hỗ trợ hô hấp.
Phân loại và các loại theo dõi CO2 thở ra
Hiểu các công nghệ hiện có và cách chúng hoạt động có thể cung cấp những hiểu biết quan trọng về ứng dụng thích hợp, những hạn chế tiềm ẩn và các vấn đề liên quan đến việc sử dụng. Sau đây là phần đánh giá ngắn gọn về phân loại và các loại theo dõi CO2 thở ra thường được sử dụng.
Máy dò màu CO2 (Colorimetric CO2 detectors)
Máy dò CO2 so màu cung cấp khả năng theo dõi CO2 thở ra định tính và bán định lượng liên tục. Máy dò CO2 so màu là dạng máy theo dõi CO2 đơn giản nhất. Chúng là những thiết bị di động, rẻ tiền, sử dụng một lần, có thể nhanh chóng phát hiện và xác nhận đặt nội khí quản và ước tính lượng CO2 trong khí thở ra. Máy dò so màu chứa vật liệu được xử lý hóa học nhạy cảm với độ pH và phản ánh nồng độ CO2 trong khí thở ra bằng so màu.17 Hạn chế của máy dò so màu CO2 bao gồm các kết quả dương tính giả khi môi trường phát hiện bị nhiễm axit dạ dày hoặc dung dịch axit được truyền qua ống nội khí quản.17,18
Theo dõi CO2 dòng chính (Mainstream CO2 monitoring)
Các thiết bị theo dõi CO2 dòng chính sử dụng một cảm biến hồng ngoại nhỏ bao gồm một cuvet mẫu hoặc cuvet và một băng quang học hồng ngoại được đặt trong đường dẫn khí ở đường thở. Vị trí đo này mang lại các giá trị CO2 theo thời gian thực trong đường thở và biểu diễn đồ họa theo thời gian thực của dạng sóng CO2 được vẽ theo thời gian hoặc theo thể tích thở ra. Nhược điểm của theo dõi CO2 dòng chính bao gồm: chi phí của cảm biến; khả năng làm hỏng cảm biến và cáp kết nối trong quá trình xử lý và theo dõi bệnh nhân; tăng khoảng chết cơ học bộ dây; khả năng bị ô nhiễm do chất tiết ho ra và chất ngưng tụ trong bộ dây; và trọng lượng bổ sung của cảm biến, bộ chuyển đổi đường thở và cáp ở đầu nối đường thở của bệnh nhân. Ngoài ra, nhiều thiết bị dòng chính chỉ được sử dụng cho bệnh nhân được đặt nội khí quản.19
Theo dõi CO2 dòng bên (Sidestream CO2 monitoring)
Các thiết bị theo dõi CO2 dòng bên hút mẫu khí từ dây thở của máy thở hoặc thiết bị tương tác với bệnh nhân khác thông qua chiều dài ống có lỗ nhỏ. Các thiết kế giao diện khác nhau để sử dụng cho bệnh nhân không đặt nội khí quản kết hợp các điểm lấy mẫu ở mũi và miệng để cải thiện độ chính xác của phép đo. Một số thiết kế giao diện bao gồm khả năng quản lý đồng thời oxy thông qua thiết bị kênh phân chia. Thiết bị lấy mẫu dòng bên sử dụng cảm biến CO2 hồng ngoại trong máy theo dõi đặt cách xa bệnh nhân và chỉ có thể hiển thị ở dạng sóng dựa trên thời gian. Theo dõi CO2 dòng phụ dựa trên thời gian là loại được sử dụng phổ biến hơn trong bối cảnh phòng mổ, trong quá trình theo dõi bệnh nhân không đặt nội khí quản và trong quá trình CPR.
Phương pháp lấy mẫu dòng phụ thường yêu cầu sử dụng bẫy nước hoặc ống chuyên dụng để loại bỏ hơi nước trước khi phân tích nhằm tránh tắc nghẽn và nhiễm bẩn ống mẫu. Phân tích mẫu cách xa bệnh nhân dẫn đến thời gian trễ thường là vài giây trước khi kết quả đo được hiển thị. Do việc lấy mẫu dòng bên yêu cầu tốc độ dòng mẫu được hút liên tục từ bộ dây máy thở, nên có thể xảy ra nhiễu với việc đo các thông số thông khí và cơ chế kích hoạt. Ngoài ra, khi hệ thống dòng phụ được sử dụng trong khi phẫu thuật với thuốc gây mê dạng hít, cần có hệ thống thu gom để ngăn ngừa ô nhiễm môi trường xung quanh và phơi nhiễm với nhà cung cấp dịch vụ chăm sóc sức khỏe.19
Capnometry so với Capnography
Capnometry được thực hiện bởi một capnometer. Capnometer là máy theo dõi đo nồng độ CO2 trong khí thở theo thời gian và hiển thị các giá trị số cho PETCO2, tần số hô hấp và đôi khi là nồng độ CO2 được hít vào hoặc áp suất riêng phần. Capnometer có thể là dòng chính hoặc dòng phụ trong thiết kế.20,21
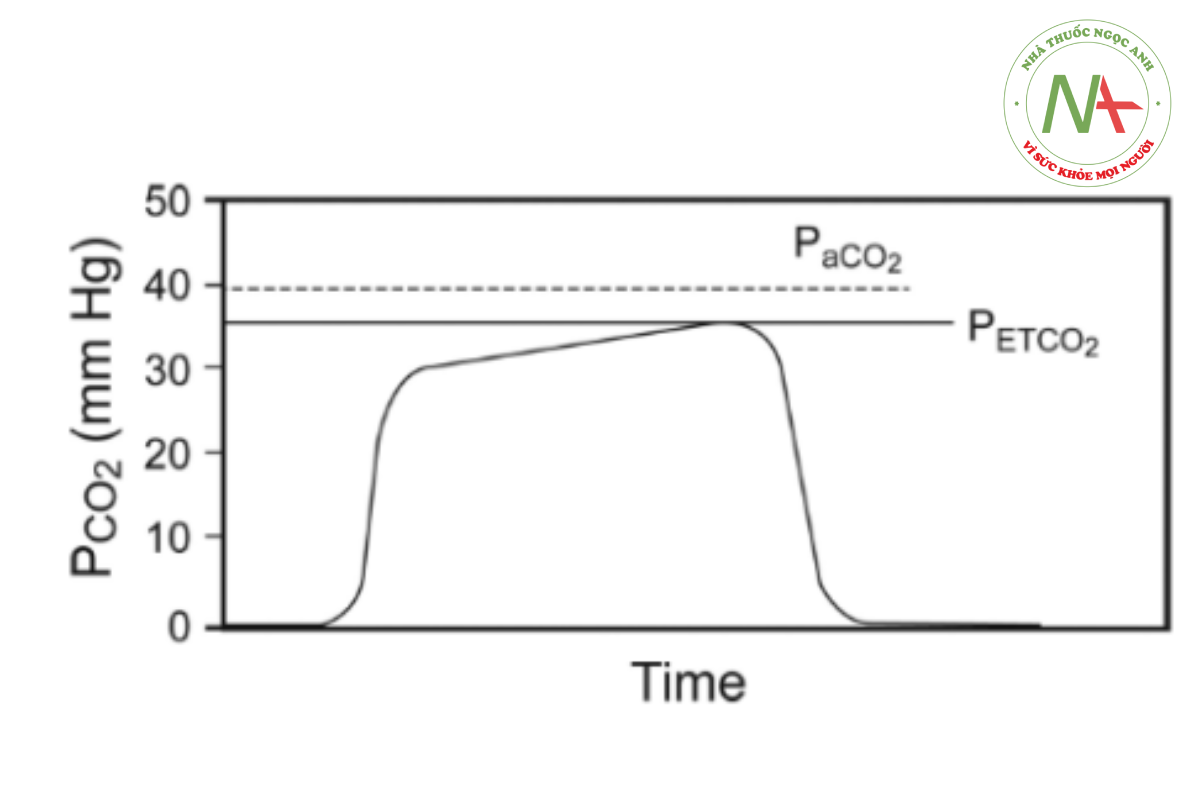
Các thuật ngữ capnometry và capnography thường được sử dụng đồng nghĩa, nhưng trái ngược với capnometry, capnography được thực hiện bởi một capnograph, một máy theo dõi có chức năng giống như capnometer nhưng kết hợp tính năng bổ sung để hiển thị dạng sóng CO2 được gọi là capnogram (Hình 1). Capnograph cũng có thể là dòng chính hoặc dòng phụ trong thiết kế. Giá trị theo dõi lâm sàng bổ sung của capnography là khả năng giải thích trực quan dạng sóng và hình thái học của capnogram. Giá trị của việc xem capnogram đồng nghĩa với việc biết được nhịp tim và xem điện tâm đồ. Giải thích các giai đoạn khác nhau; hình dạng, diện tích và độ dốc của các phân đoạn capnogram; và sự tích hợp của capnogram thở ra với thể tích khí lưu thông thở ra tiết lộ thông tin có giá trị lâm sàng liên quan đến thông khí và tưới máu cũng như sinh lý tim phổi.20,21
Các chỉ định theo dõi CO2 thở ra
Theo dõi CO2 thở ra là cần thiết và hữu ích trong thực hành lâm sàng đối với một loạt các chỉ định theo dõi, bao gồm thông khí, tuần hoàn, chuyển hóa, cải thiện sự an toàn của bệnh nhân, ảnh hưởng và dự đoán kết quả chăm sóc. Sau đây là đánh giá về các chỉ định theo dõi CO2 thở ra để theo dõi trong và ngoài bệnh viện đối với bệnh nhân người lớn và trẻ em được đặt nội khí quản và không đặt nội khí quản.
Theo dõi mức độ đầy đủ của thông khí
Theo dõi liên tục CO2 thở ra từ khi bắt đầu đặt nội khí quản đến khi rút ống, dù bằng phương pháp đo capnometry hay capnography, là một phương pháp được chấp nhận để đảm bảo thông khí đầy đủ trong quá trình thở máy ở cả bệnh nhân người lớn và trẻ em.14,22 Theo dõi CO2 ở người lớn không đặt nội khí quản,13,23,24 trẻ sơ sinh và bệnh nhi25–27 cũng có thể có hiệu quả. Để phản ánh lợi ích tiềm năng này, ASA đã xác định theo dõi CO2 là tiêu chuẩn chăm sóc trong theo dõi gây mê từ năm 1986.28 Ở những bệnh nhân khỏe mạnh được thở máy, PETCO2 gần giống với PaCO2 và thường thấp hơn 2–5 mm Hg29– 31 và do đó có thể là một chỉ số hiệu quả về mức độ thông khí đầy đủ (xem Hình 1).
Tuy nhiên, tất cả các bác sĩ lâm sàng cần hiểu rõ rằng trong các tình trạng bệnh, chẳng hạn như ARDS, COPD và hen suyễn, sự không phù hợp giữa thông khí/tưới máu ( / ) trong phổi có thể khiến chênh lệch PaCO2 − PETCO2 tăng lên. Sự chênh lệch PaCO2 − PETCO2 tăng có thể xảy ra ở các mức độ khác nhau với sự gia tăng khoảng chết sinh lý, tưới máu ống dẫn lưu, cung lượng tim thấp và tình trạng / thấp.
Có ý kiến cho rằng việc thiếu sự đồng thuận với PaCO2 ở phổi bị bệnh đã tác động tiêu cực đến nhận thức về giá trị và việc sử dụng theo dõi CO2.8 Ngược lại với cách giải thích sai lầm này, khi tồn tại sự chênh lệch lớn về PaCO2 − PETCO2, PETCO2 có thể là một phương tiện hiệu quả để xác định xu hướng thay đổi PaCO2 và hiệu quả thông khí cũng như những thay đổi trong phần khoảng chết sinh lý (VD/VT).32 Do đó, điều quan trọng là phải nhận ra rằng sự khác biệt PaCO2 − PETCO2 có thể là dấu hiệu của mức độ tổn thương phổi và tương quan với việc tăng VD/VT.5,32,33
Hơn nữa, việc theo dõi sự khác biệt PaCO2 – PETCO2 trong khi phẫu thuật đã được chứng minh là có thể dự đoán tỷ lệ tử vong ở bệnh nhân chấn thương. Bệnh nhân có chênh lệch PaCO2 − PETCO2 > 8–10 mm Hg có tỷ lệ tử vong cao hơn cả trong khi phẫu thuật34–37 và sau phẫu thuật cấp cứu.34,37
Các lợi ích đôi khi bị bỏ qua khác của việc theo dõi chênh lệch PaCO2 − PETCO2 để đánh giá mức độ thông khí đầy đủ bao gồm: giảm sử dụng khí máu động mạch,38 ảnh hưởng đến chi phí và mất máu không cần thiết; xác định và ngăn ngừa tình trạng thông khí quá mức và tăng thông khí ở bệnh nhân chấn thương thần kinh39–43; và ảnh hưởng của việc giải thích trực quan capnogram đến việc tăng cường theo dõi trong quá trình thở máy và quản lý đường thở.44
Xác nhận đặt nội khí quản
Có lẽ một trong những tác động đáng kể nhất của việc theo dõi CO2 thở ra là việc sử dụng nó như một phương pháp dứt khoát để xác nhận việc đặt nội khí quản và giảm tác hại liên quan đến việc xác định hậu quả nghiêm trọng của việc vô tình đặt nội khí quản vào thực quản, tử vong và tổn thương não do thiếu oxy. Việc sử dụng máy theo dõi CO2 ngoài việc hiển thị trực tiếp ống nội khí quản đi qua dây thanh âm là tiêu chuẩn được chấp nhận trong thực hành lâm sàng để xác nhận đặt nội khí quản ở bệnh nhân người lớn, trẻ em và trẻ sơ sinh.45–49
Capnography và capnometry so với nghe bằng ống nghe đã được chứng minh là phương pháp đáng tin cậy nhất để xác nhận vị trí đặt ống nội khí quản trong trường hợp cấp cứu trước khi nhập viện.50 Một số nghiên cứu đã chứng minh rằng khi sử dụng theo dõi PETCO2 liên tục, độ nhạy (tỷ lệ dương tính thực sự) và độ đặc hiệu (tỷ lệ âm tính thực sự) để xác nhận đặt nội khí quản đều là 100%.50–52 Máy dò so màu cũng được cho là có độ nhạy cao (88–98%) và đặc hiệu 100% trong việc xác nhận đặt nội khí quản thích hợp17,18 và hữu ích trong việc hướng dẫn và dự đoán hồi sức thành công ở những bệnh nhân không ngừng tim.17,18,53 Tỷ lệ ống nội khí quản bị đặt sai vị trí không được phát hiện trong các trường hợp ngừng thở ngoài bệnh viện cao tới 23% đã được báo cáo khi không sử dụng theo dõi PETCO2 liên tục.52
Sự công nhận những sự thật quan trọng này bởi ASA,28,54 Hiệp hội Chăm sóc Hô hấp Hoa Kỳ,55 Hiệp hội Tim mạch Hoa Kỳ,56,57 hệ thống Dịch vụ Y tế Khẩn cấp,42,58 Hiệp hội Chăm sóc Đặc biệt ở Vương quốc Anh,42 Đại học Hoàng gia Các bác sĩ gây mê và Hiệp hội các bác sĩ gây mê của Vương quốc Anh và Ireland,16 đã dẫn đến việc đưa việc sử dụng theo dõi CO2 trong quá trình đặt nội khí quản vào các tiêu chuẩn thực hành, hướng dẫn thực hành lâm sàng và khuyến nghị thực hành tương ứng của họ. Bằng chứng thuyết phục này yêu cầu sử dụng theo dõi CO2 trong quá trình đặt nội khí quản như một tiêu chuẩn chăm sóc chung để xác nhận đặt nội khí quản.11 Tuy nhiên, cần hiểu rõ rằng trong quá trình ngừng tim, độ chính xác để xác nhận đặt nội khí quản thích hợp bằng cách sử dụng theo dõi CO2 sẽ giảm đi do không có cung lượng tim, lưu lượng máu phổi và do đó không có CO2 thở ra.17,18,50 Trong tình huống này, việc không có CO2 thở ra khi sử dụng bất kỳ thiết bị theo dõi CO2 nào có thể bị hiểu nhầm là đặt nội khí quản vào thực quản.
Theo dõi tình trạng hô hấp
Việc sử dụng CO2 thở ra để theo dõi tình trạng hô hấp là một lĩnh vực khác ngày càng có ý nghĩa và được quan tâm. CO2 thở ra cung cấp một phương tiện đo tần số hô hấp chính xác và đáng tin cậy. Tần số hô hấp tăng cao là dấu hiệu nhạy cảm và đặc hiệu hợp lý của rối loạn chức năng hô hấp.59 Tần số hô hấp thấp là một dấu hiệu của suy hô hấp do thuốc giảm đau opioid và có thể được phát hiện sớm bằng cách theo dõi CO2 thở ra.60
Ức chế hô hấp do opioid gây ra trong giai đoạn chăm sóc sau gây mê là mối quan tâm chính được nhấn mạnh bởi các tiêu chuẩn bắt buộc của ASA,28 Cảnh báo Sự kiện Sentinel của Ủy ban Hỗn hợp,61 và Quy định và Hướng dẫn Diễn giải cho các Bệnh viện của Trung tâm về Dịch vụ Medicare và Medicaid.62 Bởi vì quá trình oxygen hóa và thông khí là các quá trình sinh lý riêng biệt, chỉ riêng việc theo dõi oxygen hóa mạch nẩy không nên được coi là một biện pháp theo dõi chức năng thông khí phù hợp.61–64 Độ bão hòa oxy thường xuyên được duy trì, ngay cả ở tần số thở thấp và chỉ đo độ bão hòa oxy mạch nẩy thường không phát hiện được tình trạng suy hô hấp, giảm thông khí và các đợt ngưng thở chủ yếu khi bệnh nhân được bổ sung oxy.65 Do đó, việc áp dụng theo dõi CO2 thở ra trong môi trường sau gây mê, trong quá trình an thần theo thủ thuật và khi sử dụng thuốc giảm đau dạng thuốc phiện có thể đưa ra cảnh báo sớm quan trọng về sự suy giảm thông khí ở bệnh nhân người lớn và trẻ em.65-69
Một hạn chế đáng kể cần cân nhắc khi sử dụng theo dõi PETCO2 để phát hiện tình trạng suy hô hấp là có 2 loại giảm thông khí do thuốc khác nhau (Bảng 1). Giảm thông khí loại 1 hoặc thở chậm được đặc trưng bởi tần số hô hấp giảm, thể tích khí lưu thông giảm nhẹ và PETCO2 và PaCO2 tăng. Mặt khác, giảm thông khí loại 2 hoặc giảm thở được đặc trưng bởi sự giảm đáng kể về thể tích khí lưu thông, tần số hô hấp giảm nhẹ và PETCO2 giảm hoặc bình thường, trong khi PaCO2 có thể tăng cao.70
Bảng 1. Đặc điểm của giảm thông khí thở chậm (Loại 1) và giảm thở (Loại 2)70
| Hypoventilation Classification | Respiratory Frequency | Tidal Volume | Anatomic Dead Space | VD/VT | PETCO2 | PaCO2 |
| Type 1 (bradypncic) | — | – | No change | Minimal change | + | + |
| Type 2 (hypopncic) | – | — | No change | +++ | – or no change | + |
| VD = dead space volume
VT = tidal volume PETCO2 = end-tidal CO2 – = decrease + = increase |
Trong quá trình giảm thông khí do giảm hô hấp, nhịp thở nông và thể tích khí lưu thông nhỏ hơn tương ứng với khoảng chết giải phẫu gây ra giảm thông khí phế nang, tăng thông khí khoảng chết, tăng PaCO2 và tăng chênh lệch PaCO2 – PETCO2. Sự khác biệt đáng kể này giữa giảm thông khí do thở chậm và giảm thông khí do giảm thở là rất quan trọng để các bác sĩ lâm sàng thừa nhận và hiểu rõ. PETCO2 thấp hoặc bình thường trong quá trình giảm thông khí do giảm hô hấp có thể đi kèm với suy hô hấp đáng kể và PaCO2 tăng rõ rệt, có thể không được nhận biết nếu việc theo dõi bệnh nhân tập trung vào giá trị của PETCO2.
Một lĩnh vực đáng quan tâm khác là ngày càng có nhiều bằng chứng cho thấy việc sử dụng thuốc giảm đau do bệnh nhân kiểm soát (PCA) gây ra rủi ro đáng kể cho bệnh nhân và khả năng gây ra trách nhiệm pháp lý đối với các nhà cung cấp dịch vụ chăm sóc sức khỏe và bệnh viện. Điều này một lần nữa được phản ánh trong các tuyên bố lập trường và hướng dẫn từ ASA,71,72 Trung tâm Dịch vụ Medicare và Medicaid,62 Ủy ban Hỗn hợp,73 Tổ chức An toàn Bệnh nhân Gây mê,74,75 và Viện Thực hành Thuốc An toàn,64 khuyến nghị theo dõi PETCO2 liên tục để bảo vệ chống suy hô hấp do opioid gây ra trong quá trình sử dụng PCA. Mối quan tâm đặc biệt thúc đẩy các khuyến nghị này là các trường hợp được ghi chép đầy đủ về “PCA theo ủy quyền”, trong đó một thành viên gia đình hoặc nhà cung cấp dịch vụ chăm sóc sức khỏe, chứ không phải bệnh nhân, sử dụng các liều PCA. Điều này đã dẫn đến những hậu quả nghiêm trọng và tử vong được coi là có thể phòng ngừa được nếu sử dụng phương pháp theo dõi PETCO2.73,76–78 Hơn nữa, giá trị của việc theo dõi CO2 trong quá trình an thần theo thủ thuật8,26,28,71,79,80 và trong khoa cấp cứu như một dấu hiệu sớm của suy hô hấp, đặc biệt khi bệnh nhân đang thở oxy,65,81,82 để hỗ trợ việc xác định mức độ nghiêm trọng của bệnh và để cải thiện sự an toàn của bệnh nhân13,70,83–85 cũng ngày càng trở nên bắt buộc đối với bệnh nhân người lớn và trẻ em.
Theo dõi trong quá trình CPR
Người ta đã chứng minh rõ ràng rằng việc theo dõi CO2 thở ra trong quá trình CPR cung cấp thông tin vô giá về vị trí chính xác của đường thở nâng cao,28,50,52,56,57,86 hiệu quả của ép tim,56,86–88 sự hồi phục tự nhiên tuần hoàn,56,86,87,89,90 và dự đoán kết quả và sự sống sót sau khi ngừng tim.86,87,91
Giá trị của việc theo dõi CO2 thở ra như một hướng dẫn về hiệu quả của việc ép tim lần đầu tiên được chứng minh vào năm 1978 từ một loạt 3 bệnh nhân trong quá trình CPR.91 Các nghiên cứu trên động vật sau đó đã chứng minh rằng PETCO2 tương quan với cung lượng tim và mức độ đầy đủ của CPR và rất hữu ích như một hướng dẫn để CPR thành công và dự đoán sự quay trở lại của tuần hoàn tự phát.92–95 Những phát hiện này đã được xác nhận trong 4 nghiên cứu trên đối tượng là con người, chỉ ra rằng khi PETCO2 <10 mm Hg trong CPR, bệnh nhân không sống được96–99 (Hình 2).
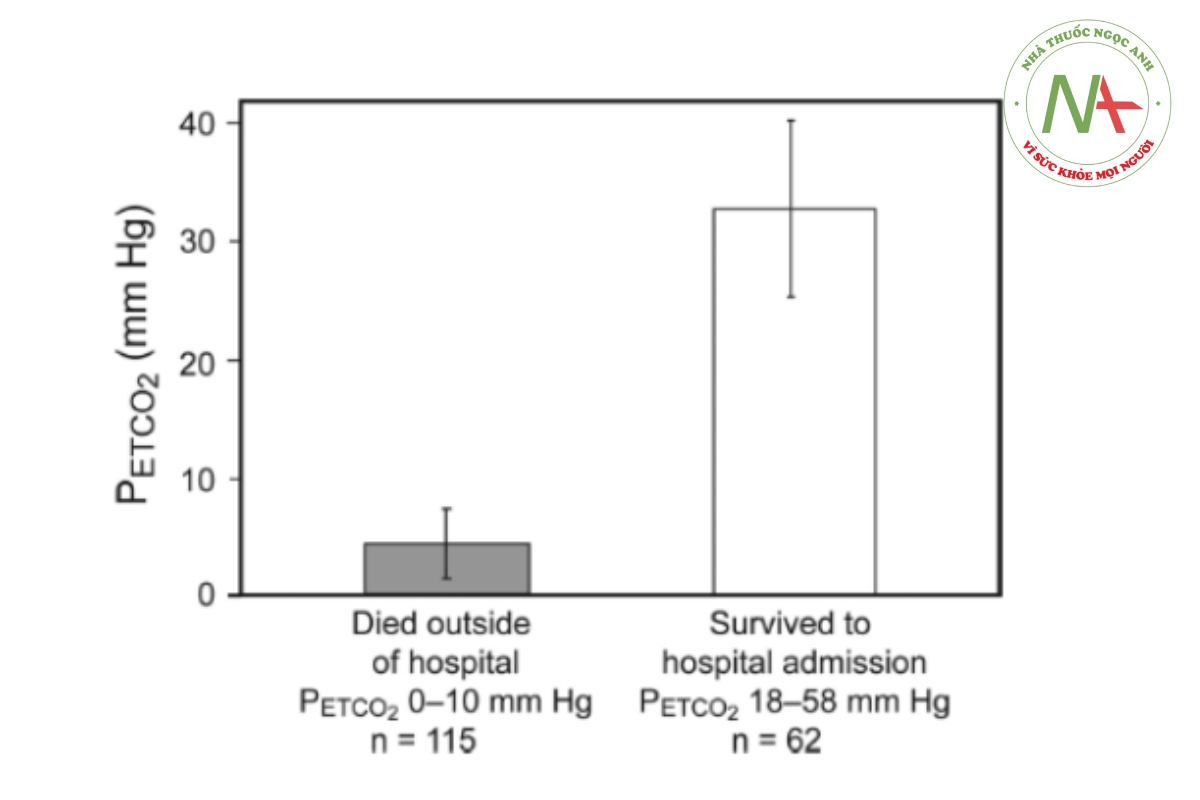
Những dữ liệu này cung cấp bằng chứng để hỗ trợ giá trị mục tiêu ngưỡng PETCO2 >10 mmHg trong CPR. Các nghiên cứu bổ sung cũng chứng minh rằng những thay đổi về PETCO2 trong các nỗ lực hồi sức đã dự đoán kết quả và sự quay trở lại của tuần hoàn tự phát,89,100 cho thấy rằng PETCO2 có thể hữu ích trong việc quyết định thời điểm chấm dứt nỗ lực hồi sức ở bệnh nhân người lớn và trẻ em.101 Khi giá trị của PETCO2 vào lúc 20 phút sau khi bắt đầu CPR được sử dụng làm xét nghiệm sàng lọc để dự đoán sự quay trở lại của tuần hoàn tự phát, giá trị ngưỡng từ 14 mm Hg trở xuống có độ nhạy, độ đặc hiệu, giá trị tiên đoán dương (độ chính xác của kết quả dương tính) và giá trị tiên đoán âm (độ chính xác của kết quả âm tính) là 100%.100
Theo dõi PETCO2 trong quá trình CPR có thể là một công cụ hiệu quả để phát hiện hiệu quả của việc ép tim từ bên ngoài và sự phát triển của tình trạng mệt mỏi của người cứu hộ. Ngoài ra, sự gia tăng đột ngột của PETCO2 được theo dõi liên tục trong quá trình CPR chất lượng cao có liên quan đến sự quay trở lại của tuần hoàn tự phát89 (Hình 3).
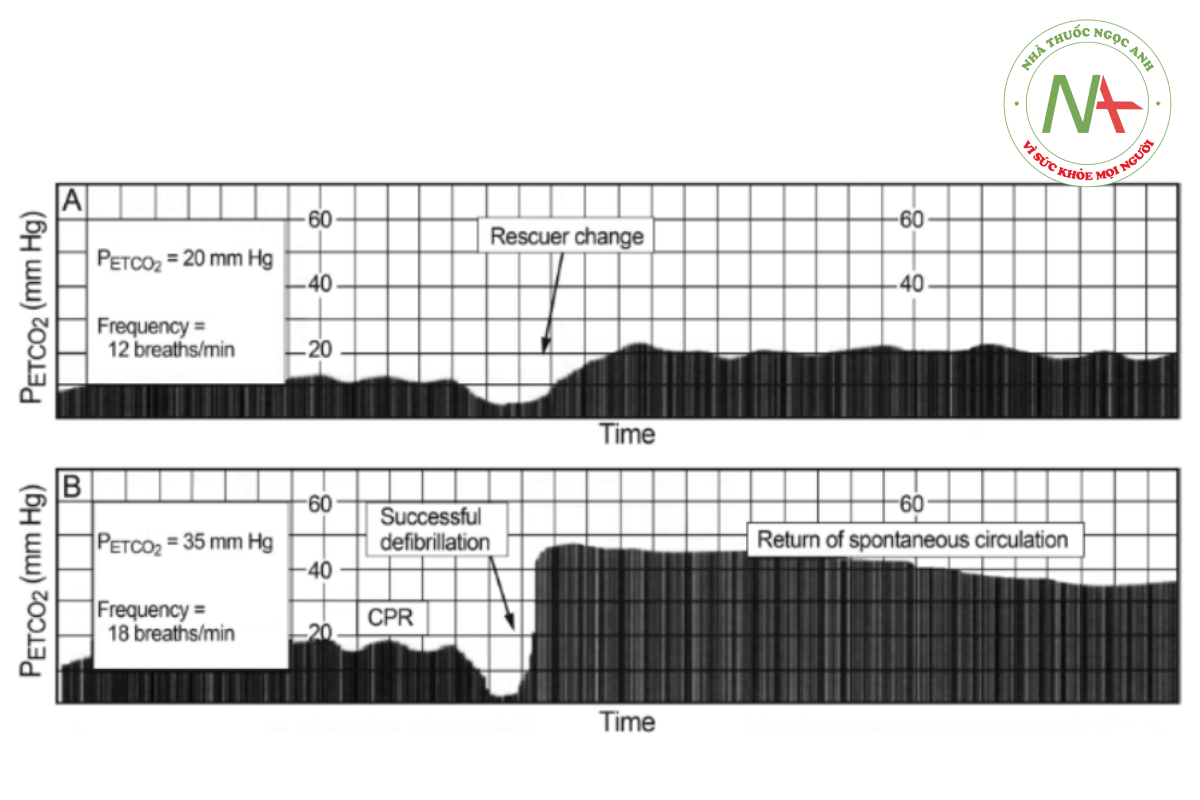
Bằng chứng này hỗ trợ việc sử dụng theo dõi PETCO2 trong quá trình CPR ở cả hồi sức trong và ngoài bệnh viện. Việc sử dụng giải thích capnography dạng sóng định lượng đã được đưa vào đào tạo hỗ trợ sự sống tim nâng cao để xác nhận vị trí đường thở trước và để theo dõi hiệu quả hồi sức kể từ năm 2010.56 Sự kết hợp giữa bằng chứng thực hành lâm sàng và công nghệ đã dẫn đến sự sẵn có của việc theo dõi CO2 thở ra như một tính năng được tích hợp vào máy khử rung tim và máy theo dõi vận chuyển hiện đại mới.
Capnography thể tích
Capnography thể tích khác với capnography tiêu chuẩn ở chỗ CO2 thở ra được vẽ dựa trên thể tích khí lưu thông thở ra. Phân tích các giai đoạn của biểu đồ thể tích, hình dạng và đường cong, cũng như các phép đo dựa trên tính toán từ biểu đồ thể tích có thể tiết lộ thông tin quan trọng liên quan đến hiệu quả thông khí và tưới máu, tỷ lệ khoảng chết sinh lý và tốc độ chuyển hóa của cơ thể.102
Các giai đoạn của Capnogram thể tích
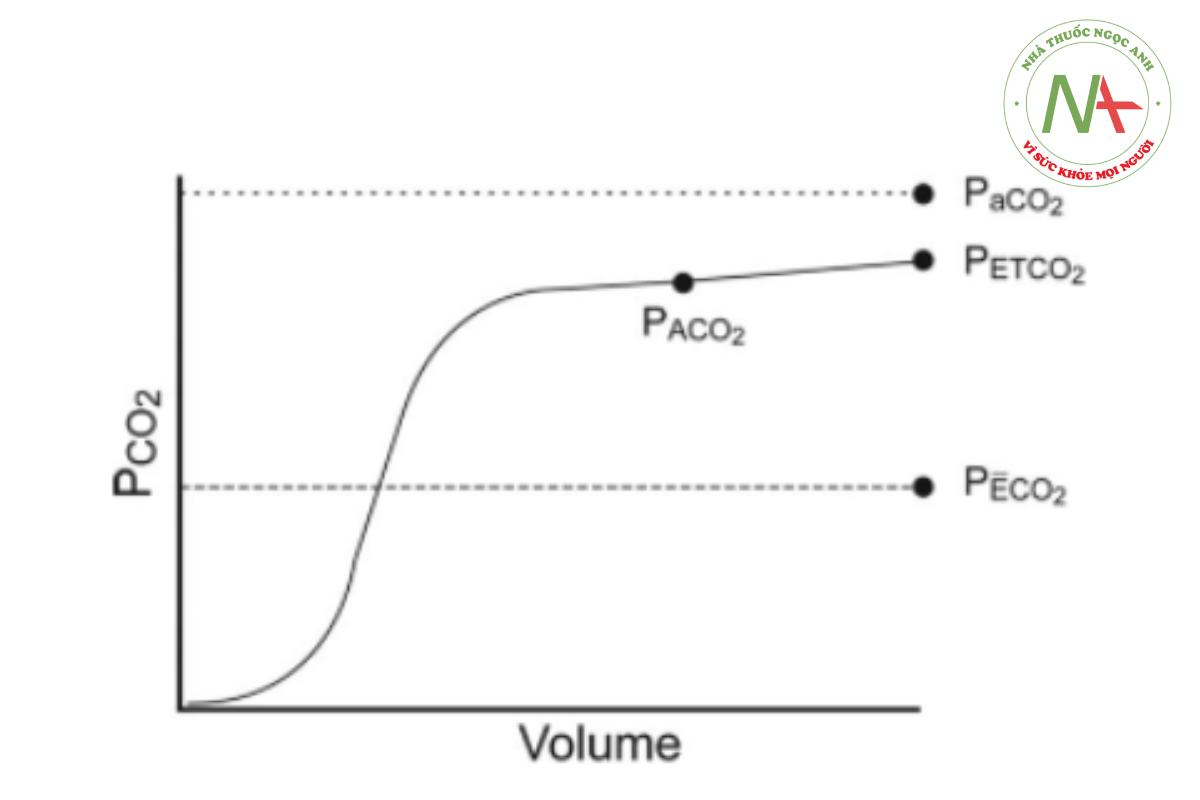
3 giai đoạn của biểu đồ thể tích đồng nghĩa với các giai đoạn của biểu đồ dựa trên thời gian. Giai đoạn 1 đặc trưng cho việc làm trống khoảng chết giải phẫu (đường dẫn khí), nơi CO2 thở ra gần bằng không. Giai đoạn 2 đại diện cho hỗn hợp khí từ khoảng chết giải phẫu và khí phế nang chứa CO2. Giai đoạn 3 biểu thị sự làm trống của các khoang khí phế nang (còn được gọi là cao nguyên phế nang), điểm cuối của giai đoạn này bằng CO2 cuối thì thở ra (Hình 4). Sự gia tăng độ dốc của giai đoạn 3 biểu thị sự gia tăng số lượng đơn vị trao đổi khí phế nang với mức độ không phù hợp V/Q khác nhau, chẳng hạn như trong quá trình tắc nghẽn đường thở và khoảng chết phế nang tăng cao.102
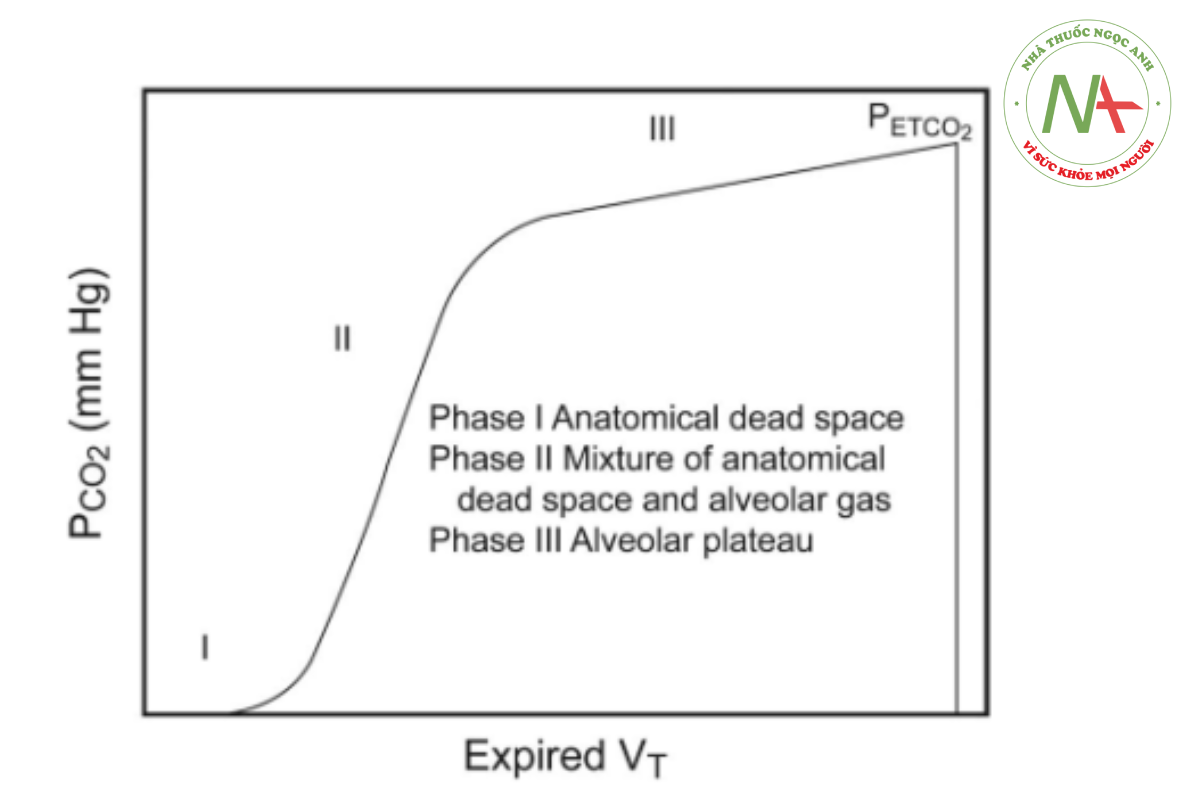
Khoảng chết Fowler
Sử dụng các nguyên tắc được mô tả bởi Fowler,103 thể tích khoảng chết giải phẫu có thể được xác định và đo lường bằng phân tích máy tính của biểu đồ thể tích.104 Điểm giữa của giai đoạn 2 của biểu đồ thể tích biểu thị ranh giới giữa đường dẫn khí và đường thở trao đổi khí (tiểu phế quản hô hấp). Khi pha 2 bị cắt bởi một đường thẳng đứng xuất phát từ một đường chồng lên mặt phẳng nghiêng của pha 3 thì có thể tạo ra giao điểm tại trục x sao cho có thể tạo ra 2 vùng ở hai bên đường thẳng đứng có diện tích bằng nhau. Điểm giao nhau này và các diện tích tương đương bằng với thể tích khoảng chết giải phẫu trên biểu đồ thể tích (Hình 5).
Khoảng chết giải phẫu ở tình nguyện viên nam và nữ khi nghỉ ngơi ban đầu được ước tính lần lượt là 156 và 104 mL.103 Vì các đường dẫn khí có thể giãn nở, nên thể tích khoảng chết giải phẫu có thể tăng lên khi thể tích phổi hít vào chủ động tối đa103 và bằng cách áp dụng áp lực dương.105 Việc áp dụng PEEP lên tới 18 cm H2O đã được chứng minh là làm tăng thể tích khoảng chết giải phẫu lên trung bình 5%.105 Sự gia tăng thể tích khoảng chết giải phẫu này làm tăng dần tổng khoảng chết sinh lý. Khả năng đo khoảng chết giải phẫu bằng capnography thể tích cho phép các thành phần của khoảng chết sinh lý được phân vùng bằng phân tích một hơi thở.
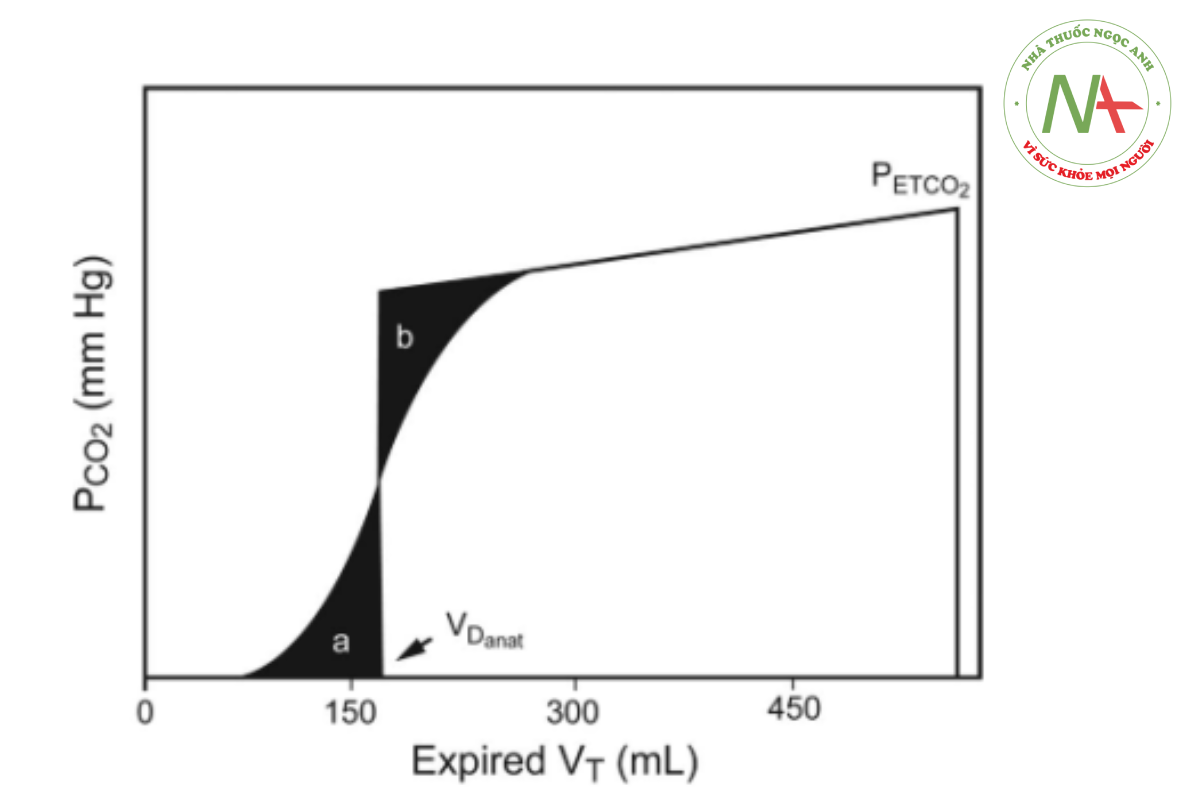
Phân tích CO2 trong một hơi thở
Phân tích dạng sóng CO2 của một hơi thở được xây dựng dựa trên việc xác định khoảng chết giải phẫu Fowler và cho phép trích xuất thông tin bổ sung về hiệu quả thông khí cũng như phân tích và nghiên cứu sâu hơn về khoảng chết sinh lý.
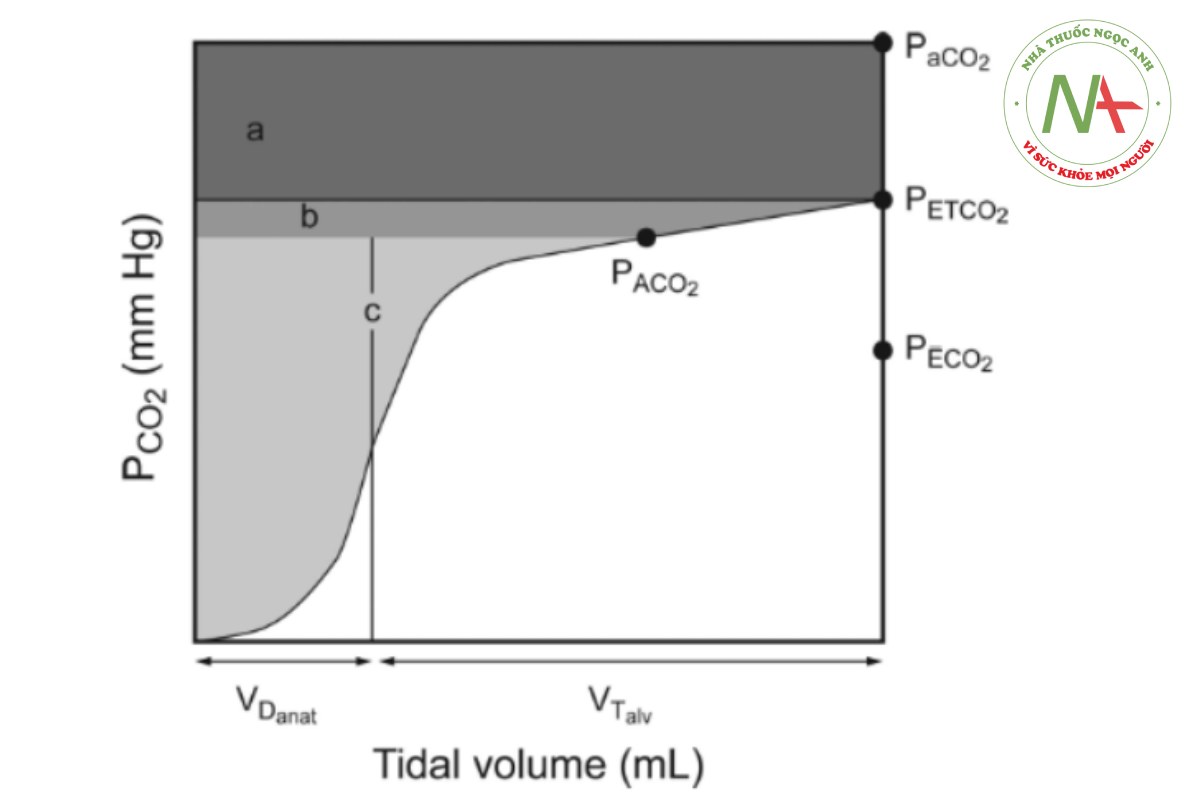
Khi đường vuông góc xác định khoảng chết giải phẫu được vẽ qua biểu đồ thể tích đến trục x, điểm giao nhau với đường này từ một đường bổ sung được đặt chồng lên giai đoạn 3 của biểu đồ thể tích cho phép các thể tích thành phần trong hơi thở khí lưu thông thở ra là được phân chia thành VD giải phẫu, VD phế nang và VT phế nang106,107 (Hình 6).
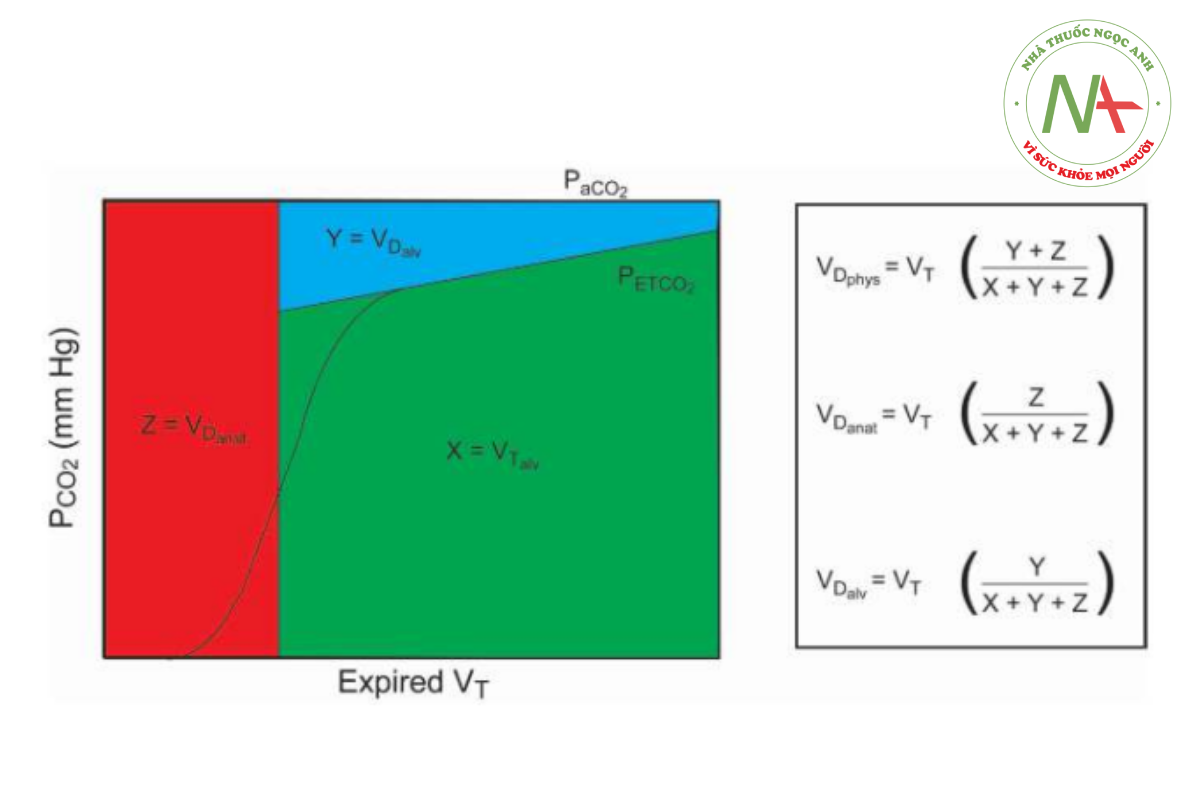
Việc phân tích vùng capnogram thể tích này cho phép nghiên cứu sâu hơn về các thành phần khác nhau và mối quan hệ của chúng. Ví dụ, VD phế nang và VD giải phẫu đều được phát hiện là các chỉ số huy động và quá căng phổi,105 và tỷ lệ VD phế nang/VT phế nang giảm hoặc tăng song song với phản ứng dương tính hoặc tiêu cực với PEEP liên quan đến quá trình oxygen hóa và shunt.108
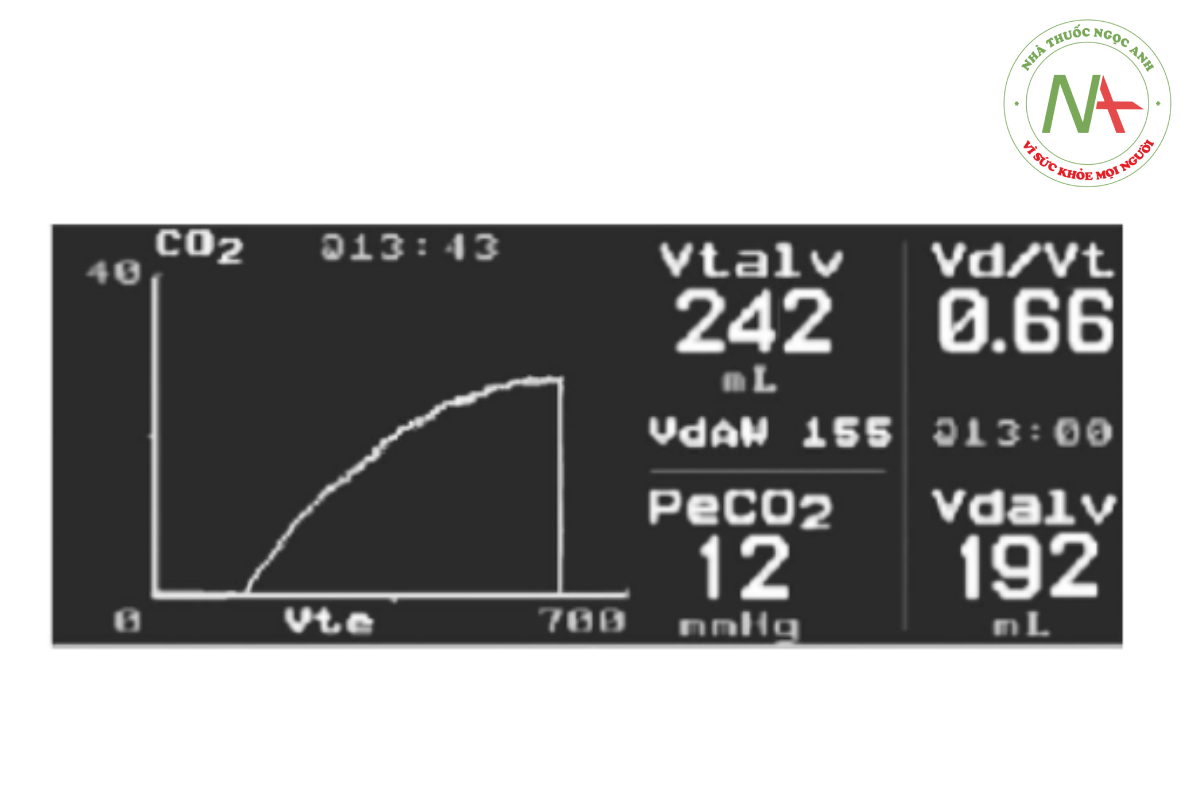
Ngoài ra, hình dạng và hình thái “vây cá mập” dốc cổ điển của biểu đồ thể tích dựa trên thời gian hoặc thể tích có thể là dấu hiệu trực quan của bất tương xứng V/Q do co thắt phế quản và tắc nghẽn đường thở14,109,110 (Hình 7) và tăng VD/VT ở bệnh nhân mắc ARDS (Hình 8).
Đo khoảng chết sinh lý
Kỹ thuật truyền thống để đo VD/VT tại giường sử dụng phương pháp thu thập và phân tích khí thở ra để đo áp suất riêng phần của CO2 thở ra trung bình (PĒCO2).111,112 Những tiến bộ trong công nghệ đã giới thiệu việc sử dụng máy phân tích chuyển hóa113,114 và capnography thể tích để đo
PĒCO2.115,116
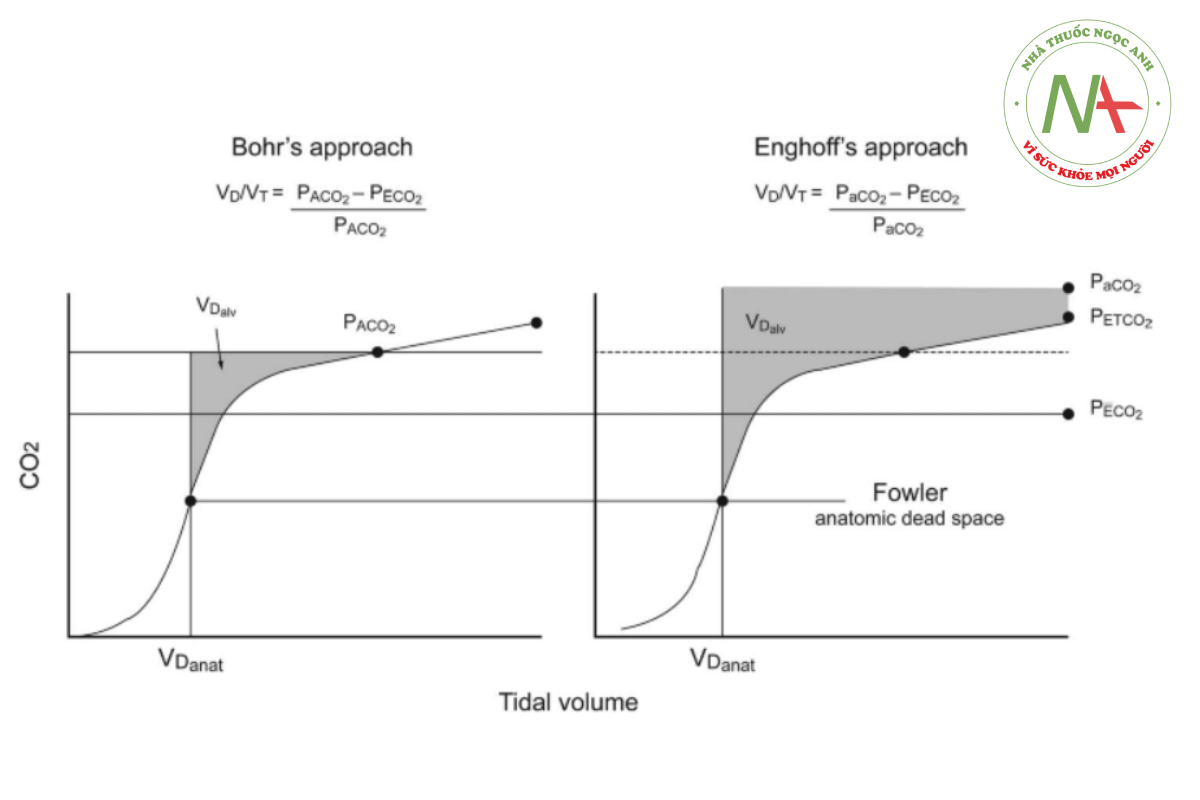
Phép tính đơn giản tại đầu giường của VD/VT sử dụng phép biến đổi Enghoff của phương trình Bohr.117 Phương trình Enghoff khác với phương trình Bohr ban đầu ở chỗ thay thế PaCO2 bằng áp suất riêng phần của hỗn hợp CO2 phế nang (PACO2).118 Vì PACO2 khó đo hoặc ước tính chính xác tại giường bệnh nên phương trình Enghoff đã trở thành phương pháp tiêu chuẩn trong nhiều năm trong thực hành lâm sàng tại giường bệnh để tính
VD/VT, trong đó phương trình Enghoff-Bohr là
VD/VTEngh = (PaCO2 − P CO2)/PaCO2 (1)
và phương trình Bohr ban đầu là
VD/VTBohr = (PACO2 − P CO2)/PACO2 (2)
Trước đây, các phép đo PĒCO2 sử dụng phương pháp túi thu khí111,112 rất cồng kềnh, tốn thời gian và dễ xảy ra lỗi và đòi hỏi phải thu tới 30– 60L khí thở ra để đo mẫu CO2 trung bình. Ngoài ra, phương pháp túi thu khí không còn khả thi do sự xuất hiện phổ biến của dòng lệch (bias flow) trên các máy thở hiện tại. Việc giới thiệu máy phân tích chuyển hóa để đo PĒCO2 yêu cầu sử dụng hiệu chỉnh thể tích nén bộ dây máy thở116 và dựa vào phép đo chính xác tỷ lệ CO2 thở ra trung bình (FĒCO2), theo đó
PĒCO2 = FĒCO2 × (PB − 47) (3)
(PB biểu thị áp suất khí quyển, 47 là áp suất hơi nước ở 37°C)
Sự ra đời của máy theo dõi CO2 theo thể tích đã đơn giản hóa phép đo tại giường bằng cách đo liên tục PĒCO2 và cho phép nhập PaCO2 không liên tục để tính VD/VT.115
P CO2 cũng có thể được lấy từ phép đo capnography theo thể tích của máy thở sử dụng VCO2 và thông khí phút thở ra (VE), theo đó116
F CO2 = VCO2/VE (4)
Bằng cách sử dụng Công thức 3 để tính PĒCO2, Công thức 1 sau đó có thể được sử dụng để tính VD/VT.116
Tính hữu ích lâm sàng của các phép đo khoảng chết sinh lý
Đo VD/VT ở bệnh nhân nguy kịch trong khi thở máy là rất quan trọng vì nhiều lý do. Giá trị tiên lượng của VD/VT có liên quan đến mức độ nghiêm trọng của tổn thương phổi và nguy cơ tử vong ở bệnh nhân mắc ARDS. Hơn nữa, VD/VT có thể hữu ích như một chỉ báo về huy động phổi so với căng quá mức ở bệnh nhân mắc ARDS, có thể hữu ích như một yếu tố dự báo thành công rút nội khí quản ở bệnh nhân người lớn và trẻ em, đồng thời có thể hữu ích trong việc đánh giá mức độ nghiêm trọng và xác nhận sự nghi ngờ của thuyên tắc phổi.
Đánh giá mức độ nghiêm trọng của tổn thương phổi
VD/VT được biết đến là một dấu hiệu của loại119 và mức độ nghiêm trọng của tổn thương phổi trong ARDS liên quan đến mức độ thiếu oxy máu,120 thay đổi mô bệnh học,120,121 khiếm khuyết V/Q,122,123 shunt trong phổi,119,123,124 và sự cần thiết của các liệu pháp hỗ trợ cấp cứu.119,124 Việc theo dõi các thay đổi nối tiếp trong VD/VT trong suốt quá trình bệnh hiểm nghèo bên cạnh các dấu hiệu khác về mức độ nghiêm trọng của bệnh là cần thiết.
Dự đoán khả năng sống sót ở bệnh nhân ARDS
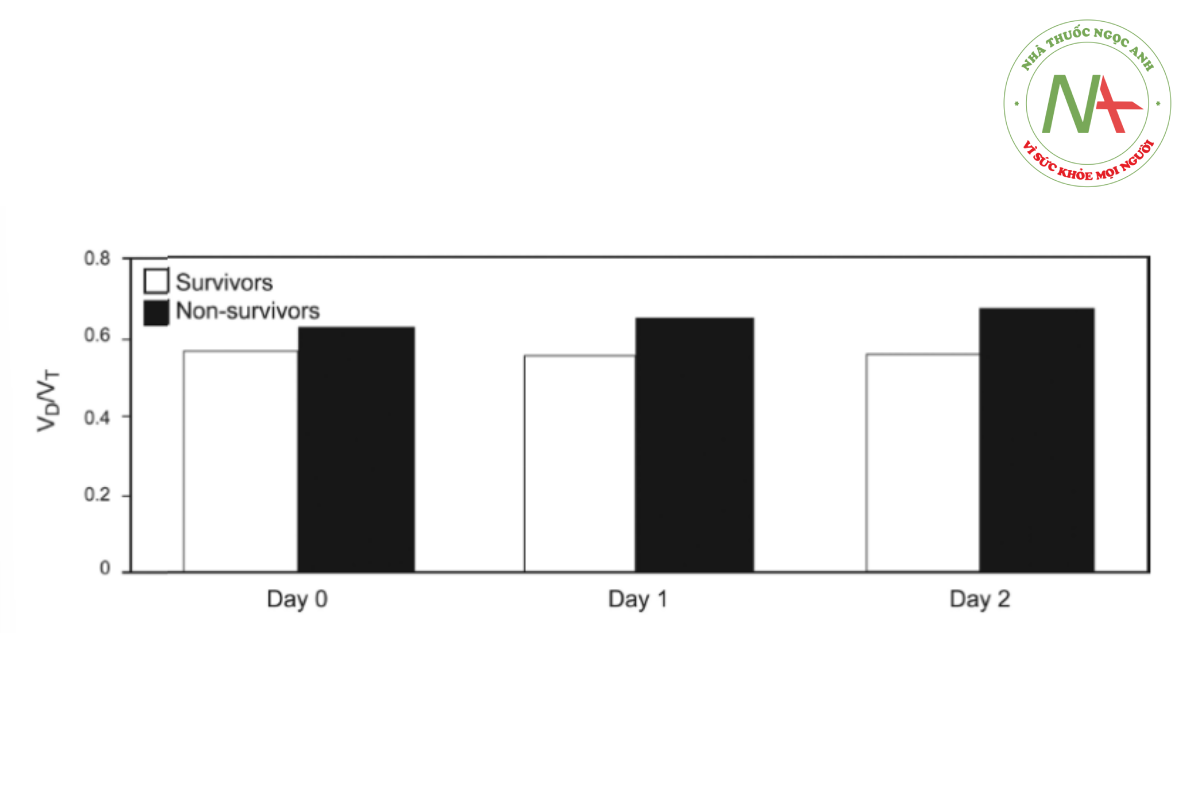
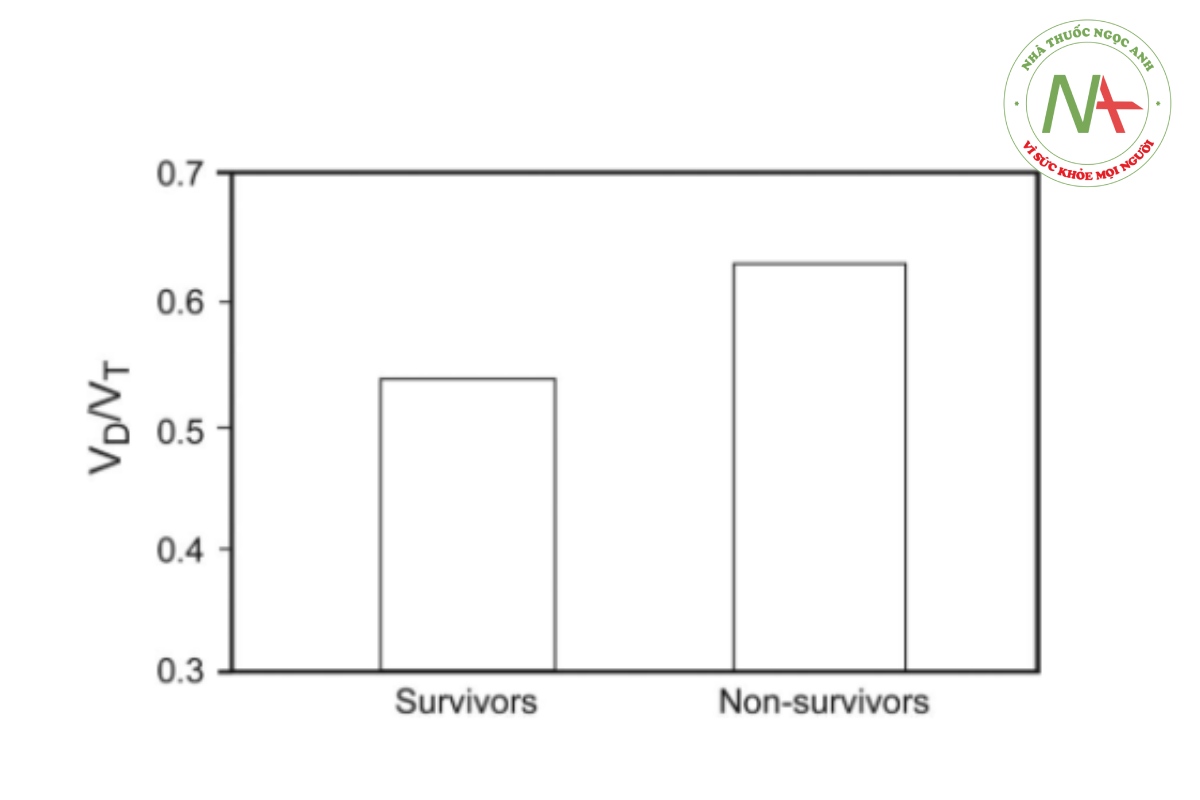
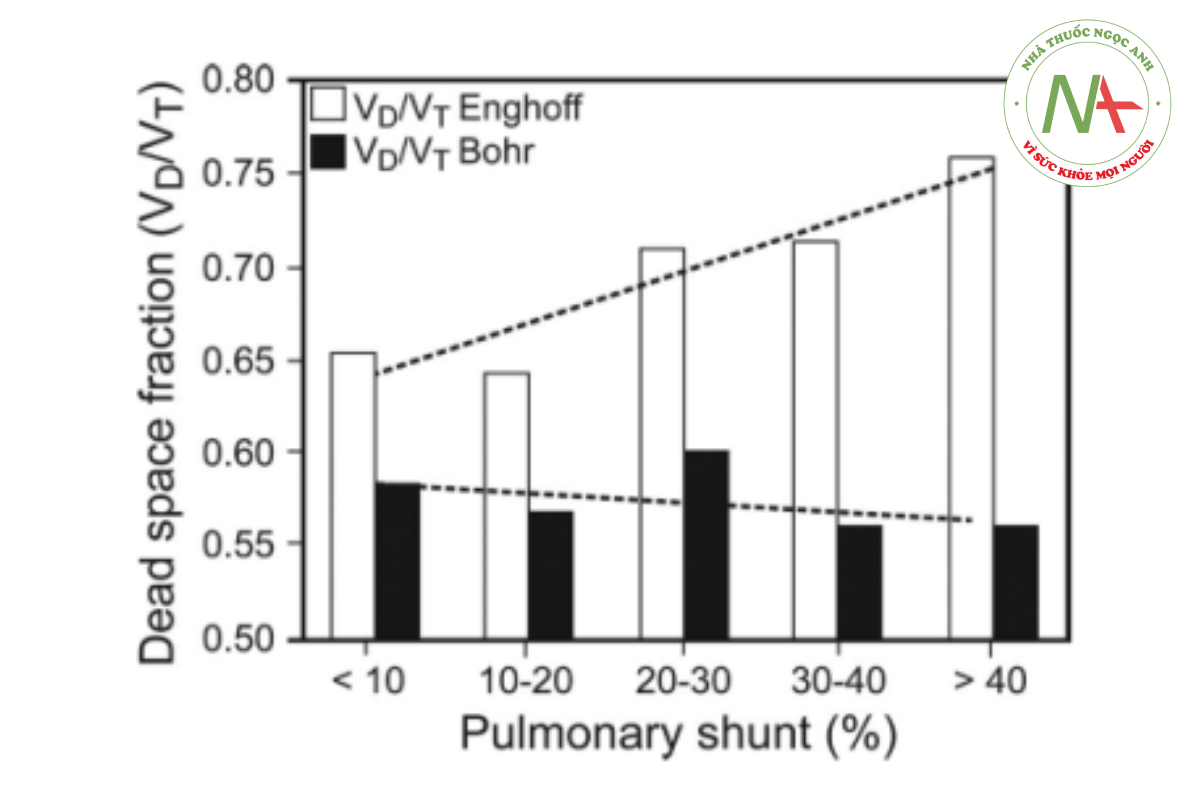
VD/VT đã được chứng minh là có khả năng dự đoán nguy cơ tử vong ở bệnh nhân mắc ARDS ở cả giai đoạn đầu và giai đoạn giữa của bệnh.125 – 131 Trong 2 ngày đầu tiên sau chẩn đoán ARDS, VD/VT cao hơn đáng kể ở những người không sống sót131 (Hình 9). Bệnh nhân có VD/VT = 0,57 được phát hiện có tỷ lệ tử vong cao hơn, với tỷ lệ tử vong tăng 45% cho mỗi 0,05 lần tăng tỷ lệ khoảng chết.127 Tỷ lệ khoảng chết trung bình cũng cao hơn đáng kể ở những bệnh nhân tử vong so với những người sống sót (Hình 10). Do đó, khi VD/VT liên tục tăng trong suốt quá trình ARDS như một dấu hiệu của sự vô ích có thể xảy ra, có thể sử dụng thông tin này để giúp hướng dẫn các quyết định về kế hoạch chăm sóc trong thời gian bệnh nặng.
Dấu hiệu huy động phổi và phổi quá căng
Các phép đo VD/VT ở bệnh nhân mắc ARDS đã được chứng minh là hữu ích trong việc chuẩn độ PEEP và tối ưu hóa chức năng tim phổi105,108,132 và có thể hữu ích như một công cụ để theo dõi việc huy động phổi so với tình trạng phổi căng quá mức.133 – 135
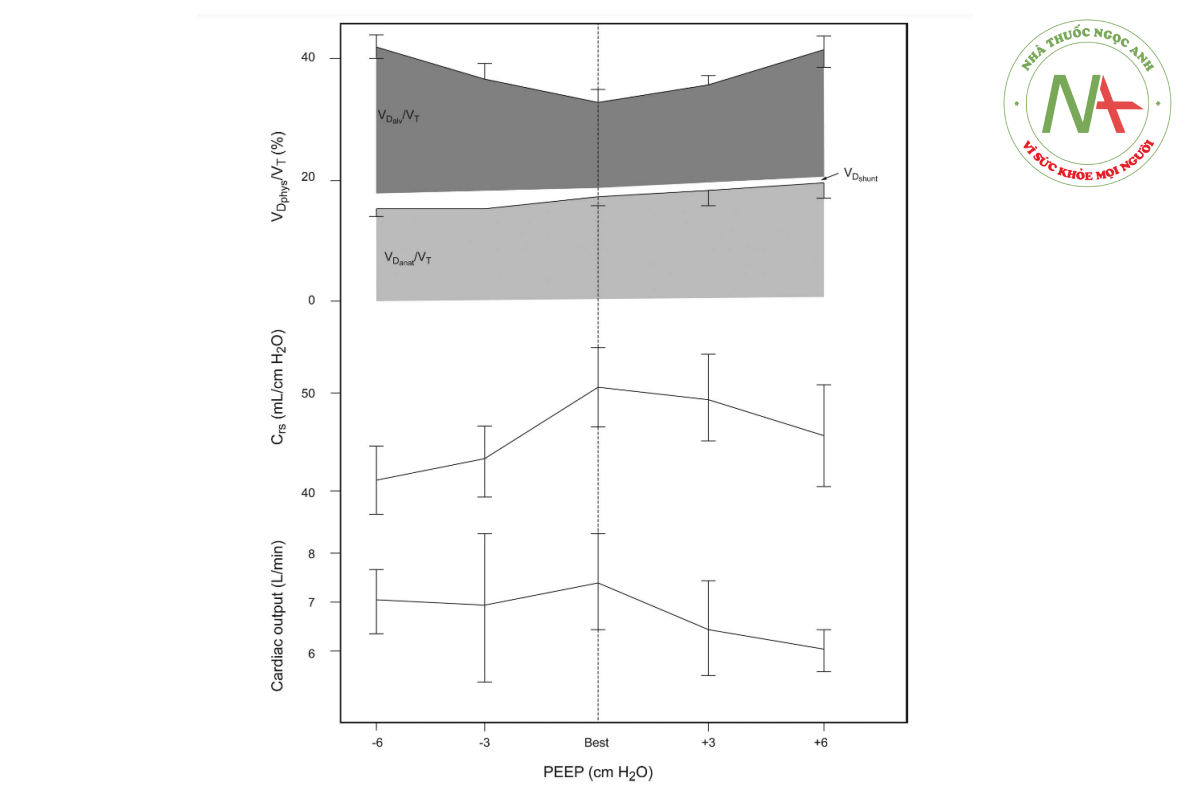
Trong một trong những bài báo kinh điển về y học chăm sóc tích cực xuất bản năm 1975, Suter và cộng sự105 đã chứng minh giá trị của việc đo VD/VT như một hướng dẫn để tối ưu hóa trao đổi khí và cơ học phổi ở bệnh nhân chấn thương phổi (Hình 11). Công việc ban đầu này đã được xác nhận nhiều lần và do đó hỗ trợ đánh giá và theo dõi VD/VT để hỗ trợ đưa ra quyết định quản lý ở bệnh nhân mắc ARDS.108,132,134,135
Dự đoán giải phóng thành công từ thông khí cơ học
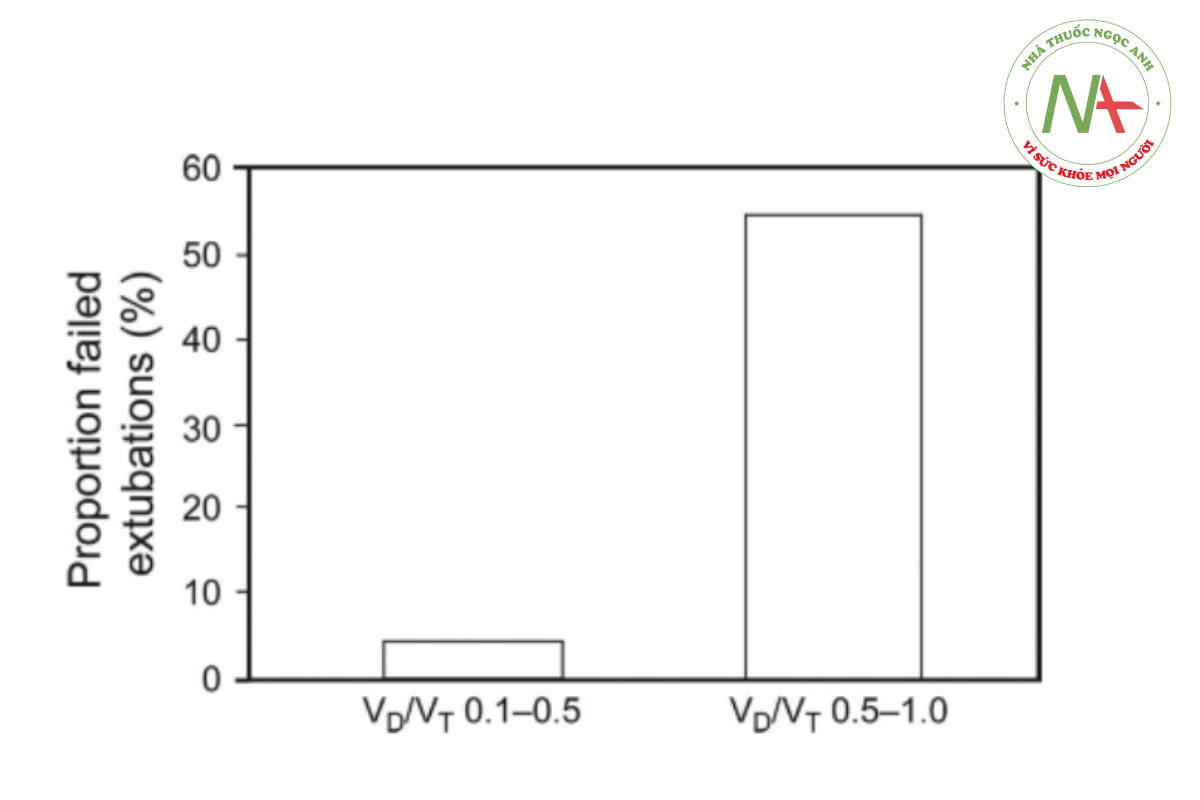
Đánh giá VD/VT cũng có thể được sử dụng để dự đoán thành công rút ống nội khí quản ở bệnh nhân nhi và người lớn.137,138 Giá trị VD/VT ≤ 0,50 và ≥ 0,65 ở trẻ sơ sinh và trẻ em được cho là dự đoán thành công hay thất bại rút nội khí quản136 (Hình 12), trong khi ở bệnh nhân người lớn, giá trị ngưỡng cho VD/VT = 0,58 cung cấp độ nhạy và độ đặc hiệu tốt nhất để dự đoán thất bại rút ống nội khí quản.137 Người ta cũng đề xuất rằng tăng VD/VT có thể hữu ích để dự đoán nhu cầu thở máy không xâm lấn sau rút ống nội khí quản138 và do đó có khả năng ngăn chặn nhu cầu đặt lại nội khí quản.
Chẩn đoán thuyên tắc phổi
VD/VT, ngoài các xét nghiệm chẩn đoán và đánh giá lâm sàng khác, có thể hữu ích trong việc loại trừ hoặc chẩn đoán thuyên tắc phổi. VD/VT > 40% được phát hiện là rất gợi ý thuyên tắc phổi và có thể so sánh về độ nhạy và độ đặc hiệu với xạ hình tưới máu phổi.139 Đánh giá kích thước của vùng dạng sóng capnogram được xác định là một phương pháp sàng lọc hữu ích đối với thuyên tắc phổi. Khi diện tích capnogram thấp, biểu thị sự khác biệt giữa PaCO2 và PETCO2 lớn hơn, thì có nhiều khả năng xảy ra thuyên tắc phổi.140 Ngược lại, khi PETCO2 bình thường (>36 mm Hg), chênh lệch PaCO2 − PETCO2 hẹp giúp loại trừ thuyên tắc phổi một cách đáng tin cậy so với chụp cắt lớp vi tính xoắn ốc có cản quang hoặc chụp cắt lớp thông khí/tưới máu.141
Tỷ lệ khoảng chết phế nang cuối kỳ thở ra ([PaCO2 − PETCO2]/PaCO2) là 15% cũng đã được chứng minh là giúp loại trừ hoặc xác nhận tắc mạch phổi.141 Khi tỷ lệ VD phế nang/VT phế nang < 20%, xác suất tắc mạch phổi thấp142–146 và được phát hiện là làm giảm nhu cầu xét nghiệm chẩn đoán thêm. Mặt khác, VD/VT phế nang tăng cao cũng dự đoán thuyên tắc phổi, mức độ nghiêm trọng của khiếm khuyết tưới máu và mức độ tắc mạch máu.148
Phương pháp tiếp cận của Bohr so với Enghoff đối với các phép đo khoảng chết sinh lý
Phương trình khoảng chết Bohr dựa trên tính toán hoặc ước lượng PACO2 từ hỗn hợp khí phế nang và P CO2, biểu thị tác động kết hợp của thể tích VD giải phẫu, VD phế nang và VT phế nang. PACO2 bị ảnh hưởng bởi sự pha loãng CO2 từ phía phế nang của màng phế nang-mao mạch từ các đơn vị trao đổi khí với lượng tưới máu thấp hoặc không có. P CO2 được xác định bằng thể tích CO2 bài tiết ra khỏi phổi (VCO2) so với tổng VE (Công thức 3 và 4). Khoảng chết Bohr bị ảnh hưởng bởi các khu vực thông khí đến bất bình đẳng tưới máu, chẳng hạn như trong quá trình giãn phế nang do PEEP và/hoặc VT quá mức, tắc mạch máu phổi và tưới máu phổi thấp thứ phát do giảm thể tích tuần hoàn hoặc sốc. Khoảng chết Bohr được công nhận là khoảng chết thực sự, hay sự cân bằng giữa thông khí hiệu quả và không hiệu quả xảy ra trong phổi149 (Hình 13).
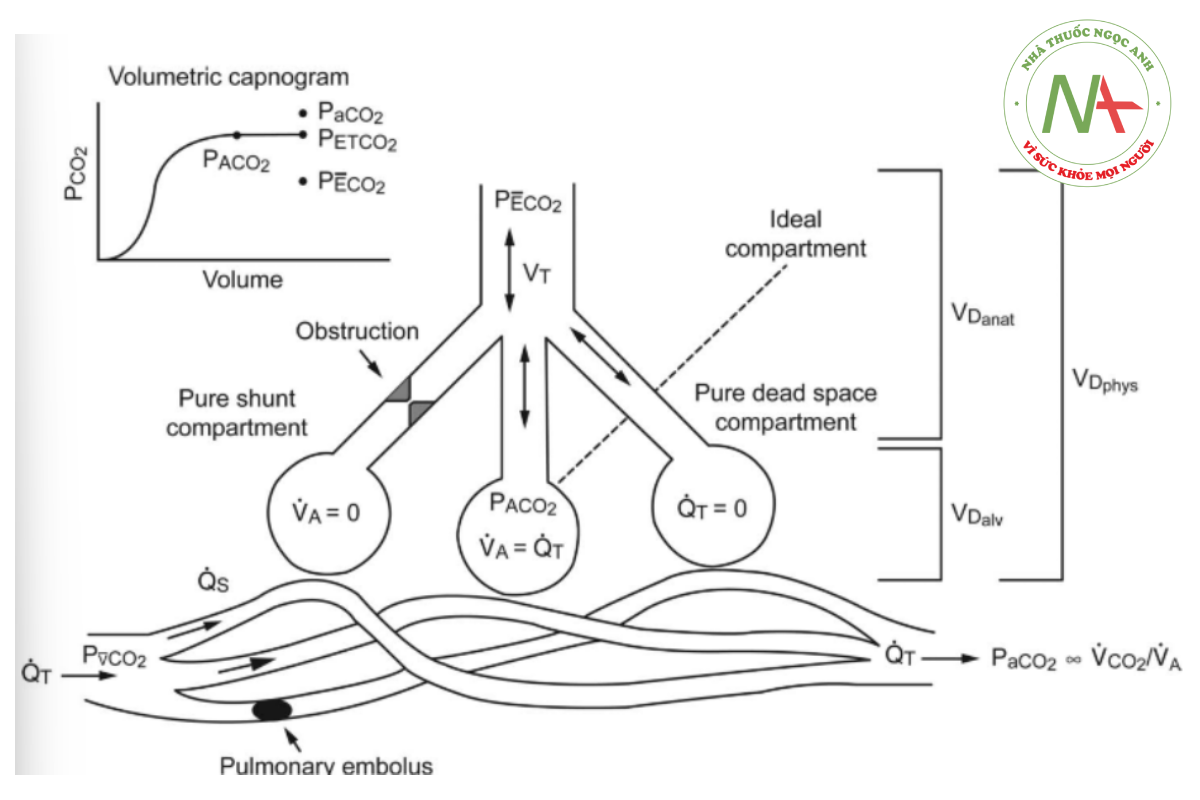
Mặt khác, phương trình khoảng chết Enghoff dựa vào PaCO2 của máu động mạch và do đó bị ảnh hưởng bởi sự kém hiệu quả trao đổi khí toàn cục và ảnh hưởng của sự kết hợp giữa shunt và trộn lẫn tĩnh mạch (Hình 14). PaCO2 có thể tăng từ tất cả các nguồn phù hợp thông khí và tưới máu thấp đến shunt, chẳng hạn như xẹp phổi, viêm phổi, COPD và hen suyễn. PaCO2 cũng có thể tăng khi sự gia tăng chuyển hóa và sản xuất CO2 không đi kèm với sự gia tăng bài tiết CO2. Khi VCO2 tăng mà không tăng thông khí phế nang theo tỷ lệ, việc sản xuất CO2 vượt quá tốc độ bài tiết và PaCO2 tăng lên. Do đó, điều quan trọng là phải hiểu rằng phương trình Enghoff đánh giá quá cao VD/VT khi có shunt và V/Q thấp.
Việc xác định PACO2 bằng phương pháp capnography theo thể tích để tính khoảng chết Bohr đã được chứng minh bằng mô hình toán học,152 và được đo bằng mô hình tổn thương phổi ở động vật.153 PACO2 được tính toán từ điểm giữa pha 3 của biểu đồ tỷ trọng thể tích được so sánh với PACO2 được suy ra về mặt toán học bằng cách sử dụng kỹ thuật loại bỏ nhiều khí trơ. Điều này chứng tỏ mối tương quan tuyến tính chặt chẽ giữa 2 phương pháp tính PACO2 (r = 0,99, P < 0,001) và khoảng chết Bohr (r = 0,96, P < 0,001). Khoảng chết Bohr và giá trị trung bình PACO2 từ phương pháp capnography theo thể tích tương tự như các tính toán kỹ thuật loại bỏ khí trơ đa năng, với độ lệch trung bình lần lượt là 10 mL (CI 95% −44 đến 64 mL) và −0,10 mm Hg (CI 95% −2,18 đến 1,98 mm Hg)..
Khả năng đo PACO2 từ biểu đồ thể tích và do đó cho phép tính toán khoảng chết Bohr có một số ý nghĩa quan trọng. Đo khoảng chết Bohr cho kết quả phản ánh chính xác hơn về thông khí và tưới máu hiệu quả và không hiệu quả trong phổi không bị ảnh hưởng bởi tác động của shunt và V/Q thấp đối với PaCO2 (Hình 15).
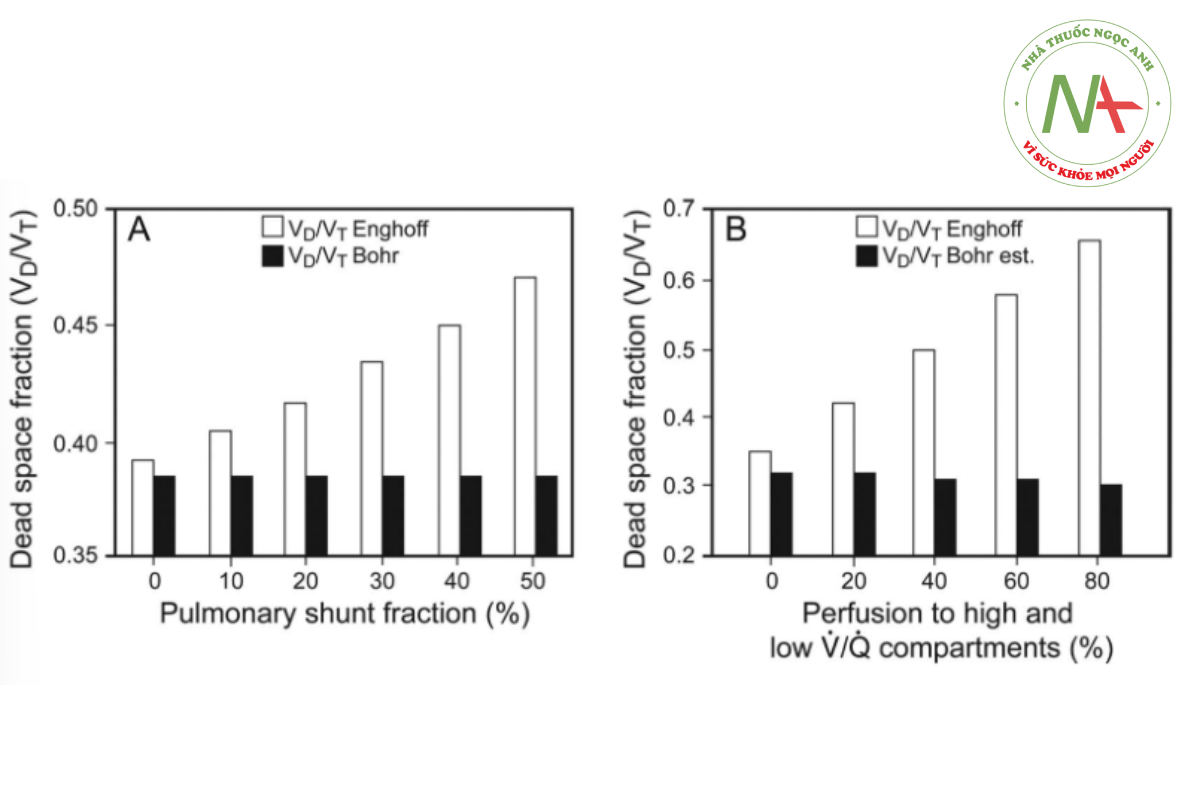
Tác động của shunt đối với phép đo VD/VT đã được nghiên cứu bằng cách sử dụng mô phỏng mô hình máy tính kiểm soát các biến thể của PACO2, VD phế nang, VD giải phẫu, shunt phổi và phân bổ tỷ lệ V/Q154 (Hình 16) và trong mô hình động vật rửa phổi sử dụng điểm giữa của giai đoạn 3 để xác định PACO2155 (Hình 17). Cả hai thí nghiệm đều xác nhận rằng việc tăng mức shunt và V/Q thấp ảnh hưởng rõ rệt đến các giá trị khoảng chết được tính toán bởi Enghoff’s (Phương trình 1) chứ không phải phương trình Bohr (Phương trình 2).
Ước tính khoảng chết Bohr cũng có thể được tính bằng cách thay thế PETCO2 cho PACO2, theo đó phương trình ước tính Bohr là:
VD/VTBohr Est = (PETCO2 − PĒCO2)/PETCO2 (5)
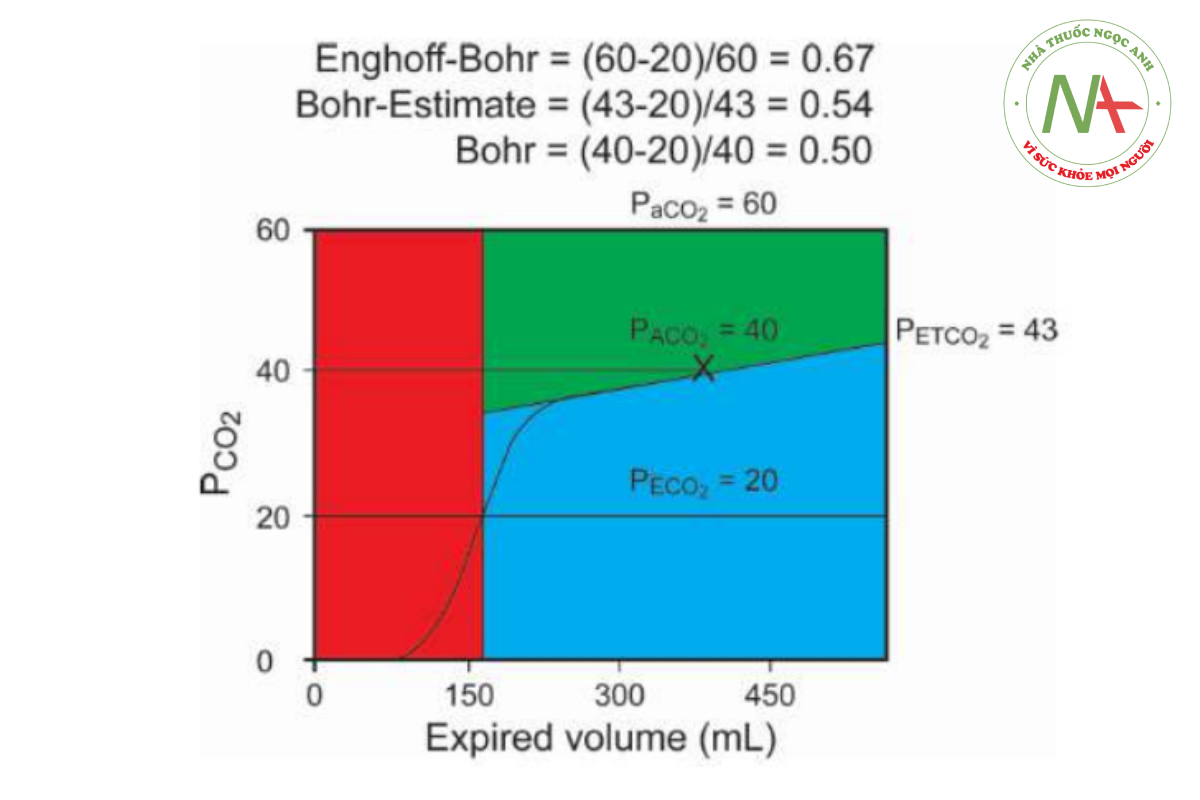
Việc so sánh VD/VTEngh, VD/VTBohr và VD/VTBohr Est liên quan đến khu vực đại diện cho VD giải phẫu và VD phế nang trên biểu đồ thể tích được mô tả trong Hình 18. Các tính toán ví dụ dựa trên các phương trình khác nhau liên quan đến biểu đồ thể tích được thể hiện trong Hình 19.
Hình 18 và 19 chứng minh rằng phương trình Enghoff đánh giá quá cao VD/VT thực. Sử dụng phương trình ước tính Bohr cũng đánh giá cao VD/VT, nhưng sự khác biệt này sẽ luôn gần với khoảng chết Bohr thực sự hơn phương trình Enghoff, cho dù VD/VT là bình thường hay cao.
Mặc dù việc xác định PACO2 từ điểm giữa của pha 3 của biểu đồ thể tích là có thể thực hiện được về mặt kỹ thuật, nhưng sử dụng phương trình ước tính Bohr và thay thế PETCO2 cho PACO2 sẽ đơn giản hóa việc tính toán, đặc biệt là khi điểm giữa của giai đoạn 3 không thể xác định rõ ràng.
Vì PĒCO2 có thể được tính bằng Công thức 4 và PETCO2 có sẵn trong quá trình theo dõi thể tích CO2, nên việc đo liên tục VD/VTBohr Est là khả thi về mặt kỹ thuật và sẽ loại bỏ yêu cầu lấy mẫu khí máu động mạch định kỳ để đo PaCO2 để tính VD/VT. Giá trị lâm sàng của việc theo dõi liên tục và xu hướng của VD/VTBohr Est trong quá trình thở máy cho bệnh nhân nguy kịch cần được nghiên cứu thêm.
Người ta cũng đề xuất rằng việc đánh giá đồng thời khoảng chết Enghoff và Bohr bằng phương pháp capnography theo thể tích có thể hữu ích trong việc nhận biết tác động của shunt và sự bất tương xứng V/Q so với khoảng chết thực sự hoặc thông khí lãng phí ở những bệnh nhân nguy kịch có VD/VT tăng cao.149 Do nhiều nghiên cứu xác định VD/VT là yếu tố dự báo kết quả, chẩn đoán bệnh và mức độ nghiêm trọng của bệnh đã sử dụng phương trình Enghoff,125–131,136–138,141–148 nên kết luận của những nghiên cứu này có thể cần được xem xét lại bằng cách sử dụng cách tiếp cận mới này.
Ước tính tỷ lệ chuyển hóa và chi tiêu năng lượng khi nghỉ ngơi
Việc ước tính tốc độ chuyển hóa có thể được thực hiện bằng phép đo VCO2 từ phương pháp capnography theo thể tích. Phương trình Weir là tiêu chuẩn được chấp nhận sử dụng trong quá trình thử nghiệm chuyển hóa để tính toán nhu cầu hỗ trợ dinh dưỡng ở những bệnh nhân bị bệnh nặng. Các sửa đổi đối với phương trình Weir có thể được sử dụng để tính mức tiêu hao năng lượng khi nghỉ ngơi (resting energy expenditure, REE) bằng cách lấy giá trị VO2 được điều chỉnh cho chỉ số hô hấp bình thường (RQ) dựa trên phép đo VCO2. REE theo phương trình Weir và REE dựa trên VCO2 (REECO2) có thể được tính toán, trong đó
REE = (3,9 × VO2) + (1,1 × VCO2) × 1,44 (6) và
REE-CO2 = (3,9 × VCO2/0,85) + (1,1 × VCO2) × 1,44 (7)
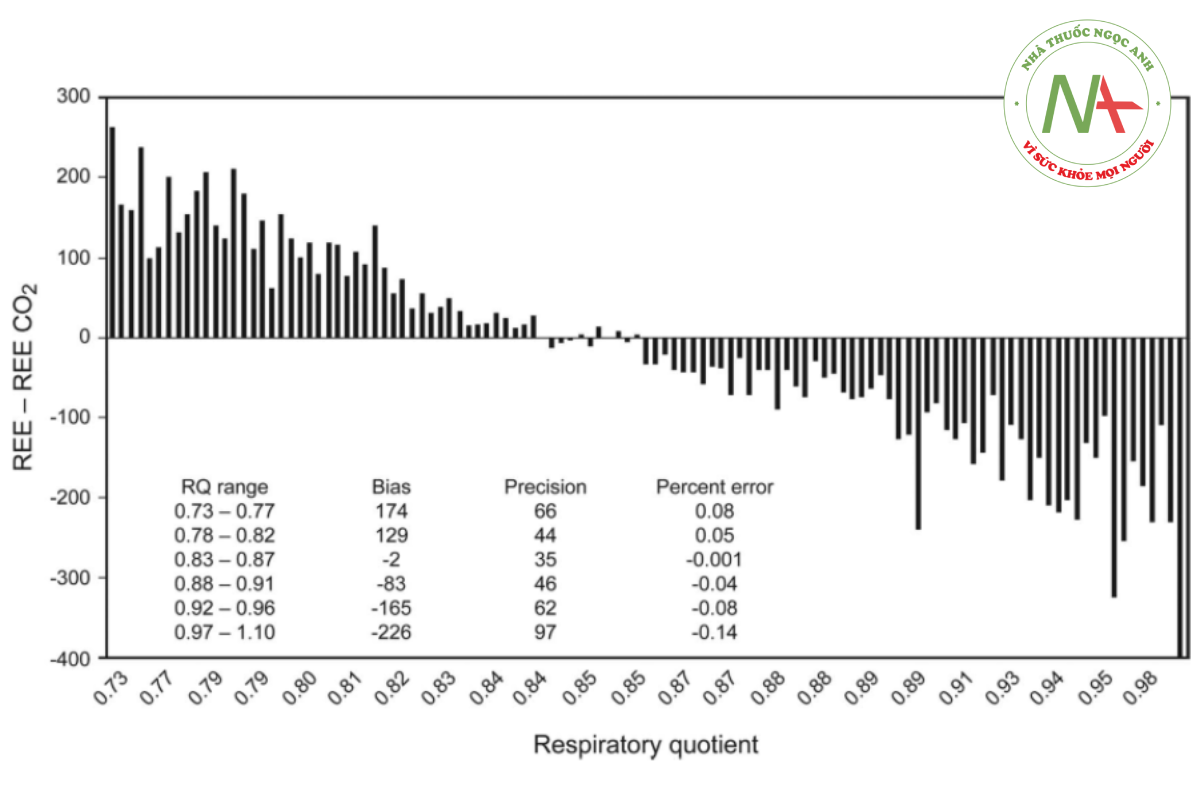
Khi RQ thực tế bằng 0,85, phép tính REECO2 cho kết quả giá trị REE tương đương với giá trị được tính theo phương trình Weir tiêu chuẩn. Máy phân tích chuyển hóa CCM Express (Medical Graphics Corporation, St Paul, Minnesota) sử dụng Công thức 7 để tính toán REE-CO2 với độ chính xác xấp xỉ ±10% so với REE.156 REE được đo bằng CCM Express sử dụng phương pháp Weir tiêu chuẩn được so sánh hồi cứu với tính toán REE-CO2 ở 67 bệnh nhân ICU trưởng thành.157 Hệ số tương quan r = 0,99 và hệ số xác định r2= 0,98, với độ lệch và độ chính xác giữa các phép đo −15 ± 126 cal/d. Khi sự khác biệt giữa REE và REE-CO2 được so sánh với RQ đo được, khi giá trị của RQ tiến tới 0,70, sai số phần trăm (độ chệch trung bình/trung bình REE đối với phạm vi RQ) trở nên dương hơn và khi RQ tiến tới 1.0, phần trăm lỗi trở nên âm hơn. Hơn nữa, khi RQ bình thường trong khoảng từ 0,80 đến 0,90, sai số trung bình là khoảng ±5% (Hình 20).157
Cần lưu ý rằng khi sử dụng phương pháp này, nếu thiết bị đo VCO2 có sai lệch và độ chính xác đáng kể so với phép đo bằng máy phân tích chuyển hóa thì sẽ dẫn đến phương sai bổ sung giữa REE và REE-CO2. Sự khác biệt về độ chính xác của phép đo này có thể được bù bằng cách sử dụng hiệu chỉnh độ chệch của phép đo.
Phương trình REE-CO2 có thể được đơn giản hóa hơn nữa bằng cách giải phương trình với bất kỳ sự kết hợp nào của VCO2 và VO2 bằng RQ là 0,85 và chia REE tính toán cho VCO2 đo được, có thể rút ra một hệ số duy nhất để tính REE-CO2, theo đó
REE-CO2 = 8,19 × VCO2 (8)
Ví dụ: khi VCO2 = 221 mL/phút và VO2 = 260 mL/phút, RQ = 221/260 = 0,85 và phương trình Weir trả về REE được tính toán là 1.810 kcal/d, theo đó:
REE = (3,9 × 260) + (1,1 ×221) × 1,44 = 1.810 kcal/ngày (9)
Bảng 2. Lượng calo tương đương của oxy và carbon dioxide liên quan đến chỉ số hô hấp và chất dinh dưỡng9,158
| Substrate | Respiratory Quotient | Oxygen Caloric Equivalent (kcal/L) | Carbon Dioxide Caloric Equivalent (kcal/L) |
| Carbohydrate | 1.0 | 5.05 | 5.05 |
| Mixed | 0.90 | 4.83 | 5.52 |
| Protein | 0.80 | 4.46 | 5.57 |
| Fat | 0.71 | 4.74 | 6.67 |
Bảng 3. So sánh 4 phương pháp xác định mức tiêu hao năng lượng cơ bản hoặc mức tiêu hao năng lượng khi nghỉ ngơi158
| Method | Mean | SD |
| BEE by Harris-Benedict equation, kcal/d | 1,716 | 225 |
| REE by Weir equation, kcal/d | 2,755 | 969 |
| REE by o2 caloric equivalent, kcal/d | 2,712 | 971 |
| REE by co2 caloric equivalent, kcal/d | 2,677 | 854 |
BEE = basal energy expenditure
REE = resting energy expenditure
REE-CO2 có thể được tính như sau:
REE = (3,9 × 221/0,85) + (1,1 ×221) × 1,44 = 1.810 kcal/ngày (10)
REE-CO2 factor = 1.810/221 = 8,19 (11) và
REE-CO2 = 8,19 × 221 = 1.810 kcal/ngày (12)
Nhiệt lượng tương đương và carbon dioxide và oxy cũng có thể được sử dụng để tính toán gián tiếp REE từ các phép đo VCO2 (Bảng 2).158–160 Khi RQ = 0,90, hệ số calo tương đương CO2 bằng 5,52 kcal/L, trong đó
REE-CO2 equivalent = 5,52 × VCO2 × 1,44 (13)
Kỹ thuật này được so sánh với phép tính Harris-Benedict và phương trình Weir. Phương trình Harris-Benedict đã đánh giá thấp đáng kể REE, nhưng không có sự khác biệt đáng kể giữa phép tính tương đương Weir và REE-CO2158 (Bảng 3). Do khó khăn về mặt kỹ thuật khi đo VO2 nên cách tính tương đương REE-CO2 đơn giản hơn và nên là phương pháp được ưa chuộng hơn, đặc biệt khi FIO2 > 0,60.159
Khả năng thực hiện các phép đo chuyển hóa bằng cách sử dụng VCO2 từ capnography theo thể tích có một số ý nghĩa quan trọng. Khả năng đo VCO2 ngày càng có sẵn trên máy theo dõi và máy thở độc lập. Điều này làm cho việc ước tính REE dễ dàng tiếp cận hơn khi không có máy phân tích chuyển hóa. Khi VCO2 được theo dõi liên tục hoặc không liên tục trong quá trình thở máy, nếu tính toán REE-CO2 được tích hợp vào máy thở, các ước tính về tốc độ chuyển hóa và nhu cầu dinh dưỡng có thể có sẵn trong thời gian thực và có xu hướng trong quá trình bệnh hiểm nghèo.9
Ngoài ra, do FIO2 không ảnh hưởng đến độ chính xác của phép tính REE-CO2 nên FIO2 > 0,60 có thể không còn là hạn chế trong việc đo lường ước tính hợp lý về REE. Ý nghĩa của việc sử dụng tính toán REE-CO2 là rất quan trọng vì ngay cả những bệnh nhân nguy kịch nhất được thở máy nhận 100% oxy và mức PEEP cao cũng có thể thực hiện ước tính REE để quản lý nhu cầu dinh dưỡng phức tạp của họ.
Do phương pháp đo capnography thể tích và theo dõi VCO2 ngày càng trở nên sẵn có hơn và ít tốn kém hơn so với xét nghiệm chuyển hóa truyền thống, nên việc sử dụng chúng nên được xem xét để kết hợp vào quy trình điều trị và đánh giá dinh dưỡng tiêu chuẩn. Cần có các nghiên cứu xác nhận và đo lường kết quả sâu hơn để xác minh tác động của các phương pháp đo nhiệt lượng gián tiếp thay thế này.
Tóm tắt
Theo dõi CO2 thở ra vượt ra ngoài mục đích sử dụng cơ bản là đánh giá thông khí. Việc sử dụng theo dõi CO2 thở ra bao gồm cải thiện sự an toàn của bệnh nhân, sử dụng trong việc đánh giá việc chăm sóc và đánh giá các biện pháp can thiệp, xác định sinh lý bất thường, định lượng mức độ nghiêm trọng của bệnh và dự đoán kết quả. Để ghi nhận những lợi ích đáng kể này, tầm quan trọng của việc theo dõi CO2 thở ra ngày càng được nhấn mạnh bởi các tiêu chuẩn thực hành, hướng dẫn và tuyên bố tư vấn từ các tổ chức chuyên môn và cơ quan quản lý.
Những tiến bộ trong tương lai về capnography thể tích sẽ bao gồm khả năng ước tính liên tục khoảng chết Bohr và tốc độ chuyển hóa trong quá trình thở máy. Những tiến bộ này hiện đang ở ngưỡng khả thi về mặt kỹ thuật và các nhà sản xuất thiết bị sẽ sớm đưa những cải tiến quan trọng này trong việc theo dõi bệnh nhân vào thực hành lâm sàng tại giường bệnh. Tác động và ý nghĩa quan trọng của các phương pháp theo dõi có giá trị sử dụng CO2 thở ra này sẽ rất quan trọng đối với tất cả các nhà cung cấp dịch vụ chăm sóc sức khỏe để hiểu và sử dụng.
=> Đọc thêm: Trao đổi khí trong hội chứng nguy kịch hô hấp cấp tính.

