Nguồn: Sách Lâm sàng tim bẩm sinh
Chủ biên
PGS.TS.BS. Nguyễn Lân Hiếu
Tham gia biên soạn
Nguyễn Lân Hiếu
Nguyễn Văn Hiếu
Đỗ Quốc Hiển
Nhà thuốc Ngọc Anh xin gửi đến quý bạn đọc chủ đề: Thay van động mạch phổi qua đường ống thông trong thực hành lâm sàng tim bẩm sinh.
GIỚI THIỆU CHUNG
Thay van động mạch phổi qua đường ống thông (transcatheter pulmonary valve implantation – TPVI) là thủ thuật ít xâm lấn, có thể thay thế phẫu thuật trong điều trị hẹp đường ra thất phải (ĐRTP) hoặc hở van động mạch phổi nặng gây rối loạn chức năng thất phải.
Ở bệnh nhân đã phẫu thuật conduit (ống nối có van) giữa thất phải – động mạch phổi, TPVI nhằm kéo dài thời gian của đoạn mạch nối thất phải – động mạch phổi trong trường hợp suy chức năng conduit (do hẹp hoặc hở) và do đó làm giảm tổng số lần cần phẫu thuật tim hở trong suốt cuộc đời của bệnh nhân.
Một số trung tâm đã phát triển mở rộng việc ứng dụng TPVI để điều trị bệnh nhân tứ chứng Fallot (tetralogy of Fallot) không có conduit và điều trị bệnh nhân tứ chứng Fallot bị thoái hóa van động mạch phổi sinh học.
Can thiệp thay van động mạch phổi qua đường ống thông được tiến hành đầu tiên trên thế giới vào năm 2000 bởi Philipp Bonhoeffer, trên bệnh nhân nam 12 tuổi có hẹp hở van động mạch phổi nhiều sau phẫu thuật tim bẩm sinh. Kết quả can thiệp thành công đã mở ra một hướng điều trị mới trong can thiệp tim mạch.
Hiện nay, thay van ĐMP qua đường ống thông được thực hiện ngày càng nhiều với ưu điểm so với phẫu thuật như: giảm tỷ lệ tử vong, ít xâm lấn, tránh được các biến chứng về tim phổi nhân tạo, giảm các biến chứng chảy máu, nhiễm khuẩn và giảm thời gian hậu phẫu. Tuy nhiên, do hệ thống delivery sheath (ống chuyển dụng cụ) kích thước lớn nên không thực hiện được ở các bệnh nhân nhỏ tuổi. Bên cạnh đó, khung stent có kích thước từ 18 – 29 mm, do đó ở những bệnh nhân có đường kính đường ra thất phải quá lớn hoặc quá nhỏ đều không thực hiện được.
Hiện tại phổ biến trên thị trường có hai van loại stent-van động mạch phổi là van Melody (Medtronic Inc) và van Edwards SAPIEN XT (Edwards Lifescatics LLC). Van Harmony (Medtronic Inc) hiện mới được Cục quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) phê duyệt sử dụng trên lâm sàng gần đây và chưa có tại Việt Nam.
CHẨN ĐOÁN HÌNH ẢNH
Siêu âm tim
Là cận lâm sàng đầu tay để đánh giá ở bệnh nhân can thiệp thay van động mạch phổi qua đường ống thông. Giúp đánh giá chức năng tâm thất phải và trái của bệnh nhân (Hình 1d), phát hiện tình trạng hở van động mạch phổi bằng cách sử dụng siêu âm Doppler màu (Hình 1b) và siêu âm Doppler liên tục (Hình 1c). Bên cạnh đó siêu âm tim có thể đánh giá sơ bộ đường ra thất phải (Hình 1a).
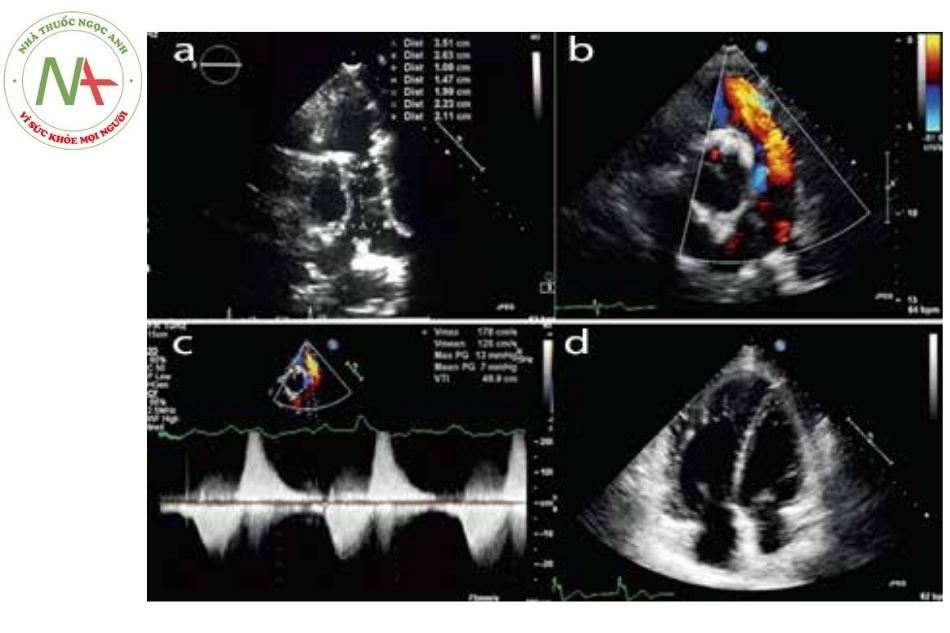
- Siêu âm trục ngắn cho phép đo đạc các thông số.
- Doppler màu ở trục ngắn thể hiện tình trạng hở van động mạch phổi nặng.
- Siêu âm Doppler liên tục vùng đường ra thất phải cho thấy tình trạng hở van ĐMP nặng.
- Hình ảnh siêu âm 4 buồng cho thấy hình ảnh thất phải giãn.
Chụp cộng hưởng từ (MRI)
- MRI tim có thể giúp đánh giá mức độ rối loạn chức năng van động mạch phổi thông qua tính toán tỷ lệ dòng hở van, phân suất tống máu thất phải, thể tích cuối tâm trương thất phải.
- Đánh giá giải phẫu buồng tim của bệnh nhân: như kích thước ĐRTP, mức độ hẹp conduit, cấu trúc 3D của ĐRTP và khoảng cách của các động mạch vành đến đường ra thất phải hoặc conduit.
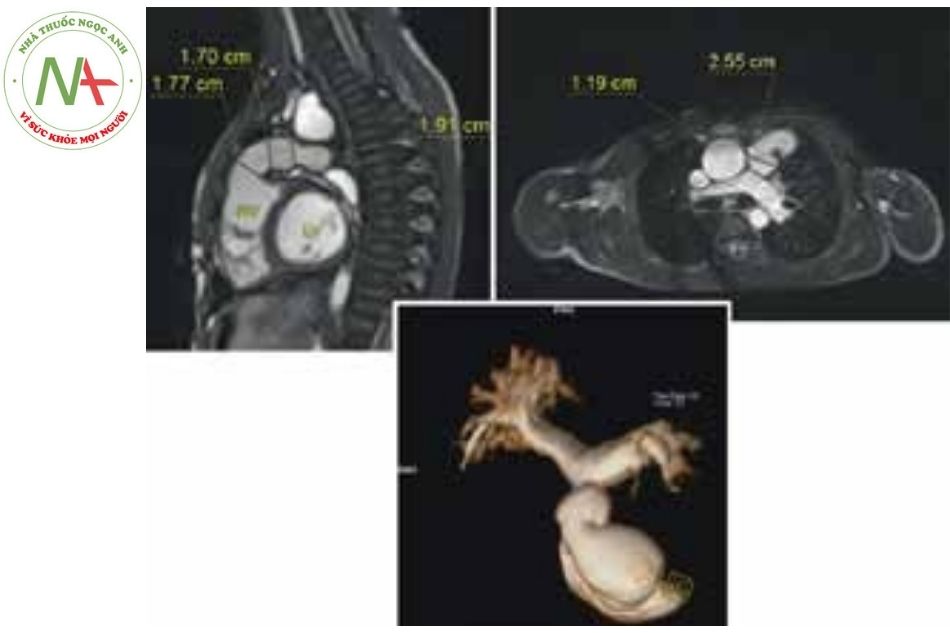
(Nguồn: Gianfranco Butera. Atlas of Cardiac Catheterization for Congenital Heart Disease, 2019)
Chụp cắt lớp vi tính đa dãy (MSCT)
- Rất có giá trị trong đánh giá giải phẫu buồng tim: đường ra thất phải (cấu trúc 2D, 3D), mức độ hẹp conduit, giãn sau hẹp, landing zone. Các thông tin nói trên quan trọng trong quyết định lựa chọn stent-van.
- Đặc biệt có giá trị trong đánh giá là khoảng cách của các động mạch vành đến đường ra thất phải hoặc conduit.
CHỈ ĐỊNH CAN THIỆP VÀ LỰA CHỌN BỆNH NH N
Chỉ định can thiệp
Hai chỉ định can thiệp thay van động mạch phổi qua da (TPVI) là: tắc nghẽn đường ra thất phải nặng (severe right ventricular outflow tract obstruction) hoặc hở van ĐMP nặng (severe pulmonic regurgi- tation). Trên các nhóm bệnh nhân: có conduit thất phải – động mạch phổi, hoặc đường ra thất phải tự nhiên, hoặc thoái hóa van động mạch phổi (ĐMP) sinh học.
Tắc nghẽn đường ra thất phải nặng kèm theo có hoặc không có hở van ĐMP nhẹ:
- Với chức năng tâm thu thất phải bình thường:
- Có triệu chứng (giảm khả năng gắng sức, với VO2 max < 65% khả năng dự kiến dung nạp với gắng sức) liên quan đến tắc nghẽn đường ra thất phải kèm theo vận tốc đỉnh sóng Doppler liên tục > 3,5 m/s.
- hoặc
- Không triệu chứng kèm theo tắc nghẽn đường ra thất phải với vận tốc đỉnh Doppler sóng liên tục > 4,0 m/s hoặc tắc nghẽn đường ra thất phải với áp lực tâm thu thất phải lớn hơn 2/3 áp lực tâm thu hệ thống.
- Với rối loạn chức năng tâm thu thất phải:
- Các ngưỡng tương tự được sử dụng như với chức năng tâm thu thất phải bình thường.
- Bệnh nhân suy chức năng tâm thu thất phải nặng có tắc nghẽn đường ra thất phải nặng với chênh áp (gradient) không đạt ngưỡng tiêu chuẩn để can thiệp, do cung lượng tim thấp: một số bệnh nhân có thể được hưởng lợi từ TPVI, tuy nhiên vẫn còn thiếu dữ liệu để ủng hộ hướng tiếp cận này.
Hở van ĐMP nặng kèm theo ít hoặc không có tắc nghẽn đường ra thất phải, có triệu chứng, rối loạn nhịp tim hoặc chỉ số thể tích cuối tâm trương thất phải > 150 cm/m² qua chụp cộng hưởng từ tim.
Khuyến cáo của ESC/AEPC
Khuyến cáo của Hiệp hội Tim mạch Châu u (ESC) và Hội Tim mạch Nhi khoa Châu u (AEPC) năm 2010 về quản lý bệnh tim bẩm sinh ở tuổi đang trưởng thành, gồm các chỉ định phẫu thuật hoặc TPVI ở bệnh nhân có conduit nối thất phải – động mạch phổi:
- Can thiệp được khuyến cáo ở những bệnh nhân có triệu chứng với áp lực tâm thu thất phải > 60 mmHg (vận tốc dòng hở van ba lá > 3,5 m/s; có thể thấp hơn trong trường hợp giảm lưu lượng) và/hoặc hở van ĐMP từ trung bình đến nặng.
- Can thiệp được gợi ý ở những bệnh nhân tắc nghẽn đường ra thất phải nặng và/hoặc hở van ĐMP nặng không có triệu chứng khi có ít nhất một trong các tiêu chuẩn sau:
- Giảm khả năng gắng sức khi kiểm tra gắng sức tim phổi.
- Giãn thất phải tiến triển.
- Giảm chức năng tâm thu thất phải tiến triển.
- Hở van ba lá tiến triển (ít nhất mức độ trung bình).
- Áp lực tâm thu thất phải > 80 mmHg (vận tốc dòng hở van ba lá > 4,3 m/s).
- Rối loạn nhịp nhĩ hoặc nhịp thất dai dẳng.
Tiêu chuẩn lựa chọn và loại trừ bệnh nhân
Bệnh nhân được thay van ĐMP cần đáp ứng hai tiêu chuẩn sau:
- Đường kính động mạch phổi/conduit phù hợp để đặt stent-van: Giới hạn kích thước trên thường là < 29 mm theo đường kính. Không có giới hạn dưới, tuy nhiên kích thước động mạch phổi/ conduit nhỏ quá (< 14 mm) cũng không phù hợp đặt stent-van.
- Kích thước cơ thể phù hợp: Không có giới hạn dưới tuyệt đối về độ tuổi nhưng cần có kích thước cơ thể thích hợp (ví dụ: cân nặng > 20 kg) để phù hợp với việc đặt đường vào dụng cụ tại đùi.
Các tiêu chí loại trừ: theo hướng dẫn của Hiệp hội Tim mạch Châu u (ESC) năm 2010 về quản lý bệnh tim bẩm sinh ở tuổi đang trưởng thành và Hội Tim mạch Nhi khoa Châu u (AEPC):
- Bằng chứng về nguy cơ chèn ép mạch vành do xác định thông qua bơm bóng thử.
- Tắc tĩnh mạch trung tâm hoặc tắc nghẽn đáng kể.
- Nhiễm trùng đang hoạt động (như viêm nội tâm mạc) hoặc nguy cơ nhiễm trùng cao (như lạm dụng thuốc tiêm tĩnh mạch).
- Phẫu thuật được ưu tiên khi cần tiến hành các sửa chữa khác như phẫu thuật thắt vòng ba lá, bắc cầu chủ – vành hoặc phẫu thuật điều trị rối loạn nhịp tim.
HỆ THỐNG VAN MELODY VÀ EWARDS SAPIEN XT
Van MELODY
Thay van động mạch phổi qua catheter bằng van Melody đã được chứng minh là phương pháp điều trị an toàn và hiệu quả cho bệnh nhân sau phẫu thuật conduit thất phải – động mạch phổi. Các nghiên cứu đã cho thấy hiệu quả làm giảm tắc nghẽn conduit, phục hồi chức năng van, trì hoãn can thiệp phẫu thuật tiếp theo và cải thiện đáng kể chức năng thất phải, cũng như nâng cao chất lượng cuộc sống bệnh nhân.
Hệ thống van Melody
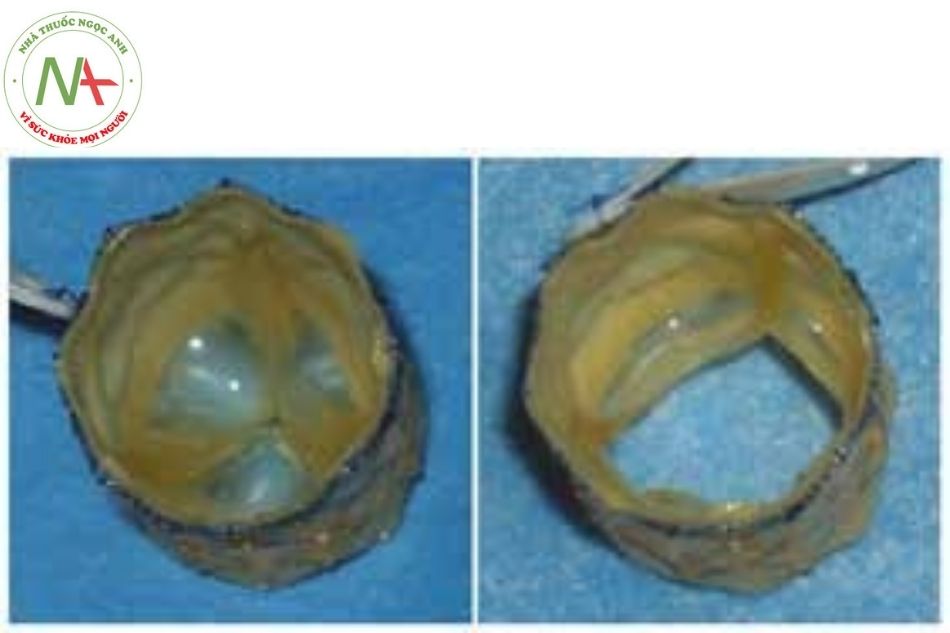
(TPV: transcatheter pulmonary valve)
Van Melody được cấu tạo gồm 2 thành phần: một đoạn tĩnh mạch cảnh của bò (BJV) có van ở trung tâm và một stent bạch kim-iridium dài 28 mm. Đoạn tĩnh mạch được khâu trong stent bằng chỉ polypropylene 5.0. Dụng cụ được đảm bảo vô trùng và bảo quản trong dung dịch có chứa glutaraldehyde và isopropyl alcohol. Do cấu trúc như trên nên còn được gọi là stent-van.
Stent-van Melody có hai kích thước:
- Melody TPV 20: Van làm từ tĩnh mạch cảnh bò, kích thước 16 mm và có thể giãn tới 20 mm. Sử dụng bóng 18 hoặc 20 mm và introducer sheath 22 Fr.
- Melody TPV 22: Van làm từ tĩnh mạch cảnh bò, kích thước 18 mm và có thể giãn tới 22 mm. Sử dụng bóng 18, 20 hoặc 22 mm và introducer sheath (ống mở đường vào) 22 Fr.
Lưu ý: Trước khi sử dụng, cần rửa 2 phút trong dung dịch NaCL 09% 500 ml để loại bỏ hết glutaraldehyde.
Van EDWARDS SAPIEN XT
Mục đích sử dụng ban đầu của van SAPIEN là can thiệp thay van động mạch chủ qua da, về sau được cải tiến trở thành một lựa chọn thay thế cho van Melody trong thay van động mạch phổi và đã được sử dụng thành công từ năm 2005.
Từ tháng ba năm 2016, van SAPIEN XT (thế hệ ĐMP thứ hai của van Edwards SAPIEN) đã được FDA phê duyệt để sử dụng cho động mạch phổi ở những bệnh nhân có suy chức năng thất phải.
Van SAPIEN được sử dụng với kích thước ĐRTP từ 21-29 mm, khi so sánh với Van Melody (Medtronic, Inc.) được sử dụng với ĐRTP khoảng 16-22 mm.

Cấu tạo Stent-van SAPIEN XT:
- Được làm từ màng ngoài tim của bò tạo thành hình ba lá, được khâu bằng tay vào một stent nở bằng bóng có chất liệu coban-crom. Một vòng vải bít bao phủ phần dưới của stent để tạo ra một vòng thắt giúp ngăn ngừa sự rò rỉ qua chân
- Van có có 3 kích thước:
- 23 mm (cho ĐRTP 21-23 mm), cao 14,3 Sử dụng introducer sheath 14 Fr.
- 26 mm (cho ĐRTP 24-26 mm), cao 17,2 Introducer sheath 14 Fr.
- 29 mm (cho ĐRTP > 26mm), cao 19,1 Introducer sheath 16 Fr.
- Có thể sử dụng trong các trường hợp thay van qua đường ống thông với conduit bị vôi hóa.
DỤNG CỤ CAN THIỆP
Hệ thống bóng nong và delivery sheath
Hệ thống bóng nong và delivery sheath tương tự giữa van MELODY và Edwards SAPIEN XT. Tuy nhiên có khác nhau về kích thước tương ứng với kích thước van.
Dưới đây chúng tôi chỉ trình bày hệ thống tương ứng với van MELODY.
- 1 hệ thống bóng trong bóng (balloon in balloon):
- Có 3 kích cỡ bóng (18; 20 và 22 mm) với van Thân bóng được bao phủ bởi sheath bên ngoài.
- Phần đầu gần của catheter bóng có 3 đường vào: lỗ màu xanh lá cây cho dây dẫn (guidewire), lỗ màu chàm để cho bóng bên trong và màu cam cho bóng bên ngoài.
- Trên thân catheter của bóng có 2 maker: Marker đánh dấu vị trí stent-van được che phủ bởi sheath, và khi rút sheath về đến maker tiếp theo (marker van không che bởi sheath) sẽ bộc lộ hoàn toàn bóng và stent-van.
- Stent-van Melody: được gấp và phủ lên trên bóng.
- Một đầu trục vót nhọn hình nón: có màu xanh để đối xứng và cân đối trục dụng cụ.
- Delivery sheath Teflon: có nòng được bện từ các sợi dây đàn hồi, giúp giảm nguy cơ bị xoắn cũng như tăng tính linh hoạt và khả năng đẩy dụng cụ. Đầu gần sheath có van cầm máu. Phần đầu xa của sheath che phủ bóng và stent-van, khi rút về sẽ bộc lộ bóng và stent-van.
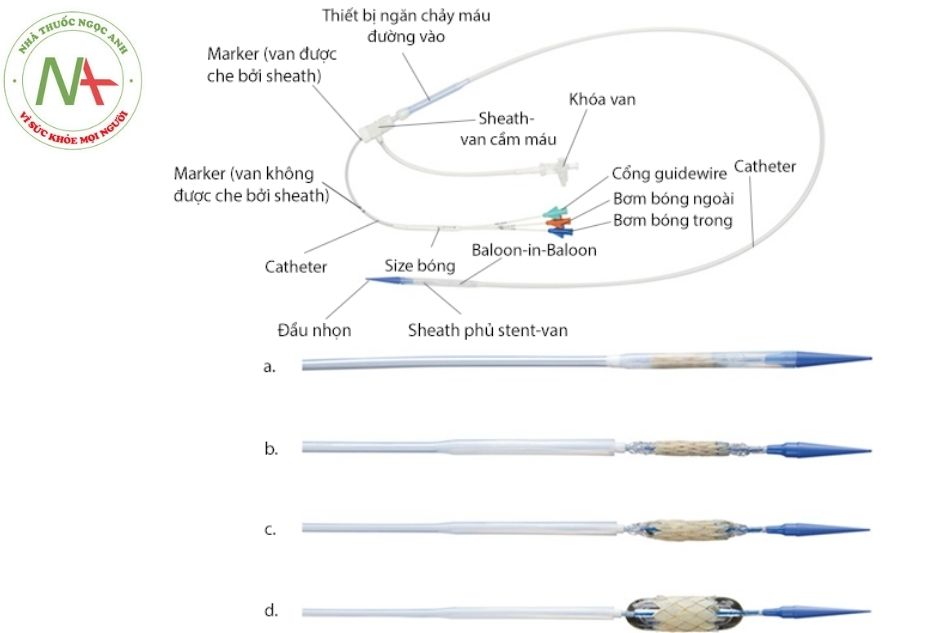
- Sheath phủ lên van
- Rút lại sheath, bộc lộ van
- Lên bóng
- Lên bóng để van nở tối đa
Các bước can thiệp và dụng cụ tương ứng
Bảng 1. Các bước can thiệp và dụng cụ tương ứng
| Đánh giá huyết động, chụp buồng thất phải và động mạch phổi | Ống thông pigtail, JR, multipurpose (MP). |
| Chụp gốc động mạch chủ hoặc ĐMV chọn lọc | Ống thông pigtail, Juskin vành phải/vành trái (JR/JL), EBU. |
| Lên bóng đo kích thước (balloon sizing), nong van động mạch phổi và loại trừ đè ép động mạch vành | – Trường hợp hẹp van động mạch phổi, có thể sử dụng dây dẫn cứng hơn (ví dụ: Amplatz super stiff wire) và bóng áp suất trung bình (ví dụ: Mull- ins-X, Z-med, Zmed II – NuMED Inc., VACS III – Osypka GmbH) để nong.– Trường hợp có vôi hóa nặng, thường cần nong áp lực cao, như bóng Atlas (BARD).
– Trường hợp đường ra có kích thước lớn, nên sử dụng bóng nong có áp lực vừa phải (ví dụ: bóng định cỡ PTS, PTS-X – NuMED Inc..). |
| Đặt pre-stent vào đường ra thất phải | – Thông thường, sử dụng Introducer Check-Flo Performer 14-16 Fr và bóng áp suất trung bình để triển khai stent (ví dụ: Mullins-X, Z-med, Z-med II-NuMED, Inc., VACS III-Osypka GmbH hoặc bóng BiB).– Covered-CP stent (NuMED, Inc.) làm giảm nguy cơ thoát mạch của dòng máu; Non-covered stent (Ví dụ stent CP, stent Andra) phù hợp trong một số trường hợp nhất định.
– Tường hợp ĐRTP rộng, không vôi hóa, các stent Andra (Andramed, Inc.) được nhiều bác sĩ can thiệp lựa chọn vì chúng có thể cải thiện “độ bám” trên thành mạch. – Việc chuẩn bị landing zone cho đặt stent-van là rất quan trọng và có thể được kiểm tra ở góc chụp “barrel view”. |
| Đặt van | – Van 23, 26, 29 mm SAPIEN (Edwards Lifesciences, LLC); kích thước ĐRTP: 21-29 mm.– Van Melody (Medtronic, Inc.); kích thước ĐRTP: 16-22 mm. |
Chú thích: ĐMV: Động mạch vành; ĐMP: Động mạch phổi; ĐRTP: Đường ra thất phải.
QUY TRÌNH KỸ THUẬT CAN THIỆP
Kỹ thuật can thiệp hai van Melody và Edward Sapien XT là tương tự nhau. Trong quá trình can thiệp, bệnh nhân thường được gây mê (toàn thân hoặc gây tê tủy sống).
Tạo đường vào mạch máu
- Tĩnh mạch đùi: là đường vào mạch máu thường dùng, nên chuẩn bị sát trùng ở cả 2 bên đùi. Đường vào tĩnh mạch cảnh trong có thể dùng nếu đường tĩnh mạch đùi không khả thi hoặc khó vào thất phải từ tĩnh mạch chủ dưới (ít dùng).
- Đường vào động mạch đùi hoặc động mạch quay (5 hoặc 6 Fr): Để chụp gốc động mạch chủ hoặc động mạch vành chọn lọc.
- Sau khi tạo đường vào mạch máu, tiêm heparin tĩnh mạch 100 IU/kg để duy trì thời gian ACT > 250 giây.
- Một số phác đồ nghiên cứu dùng aspirin 81 mg (liều cho người trưởng thành) vào buổi tối ngay trước ngày can thiệp. Tuy nhiên trong thực hành lâm sàng, việc sử dụng aspirin còn chưa được thống nhất.
- Tất cả các bệnh nhân nên được sử dụng kháng sinh dự phòng (liều đầu tiên vào thời điểm bắt đầu thủ thuật, 2 liều tiếp theo cách nhau 8 giờ).
Thông tim phải và trái
Được thực hiện bằng các kỹ thuật căn bản nhằm khảo sát giải phẫu động mạch phổi, động mạch vành, cũng như áp lực và sức cản hệ động mạch phổi.
==>> Xem thêm: Thông tim thăm dò huyết động, chụp buồng tim và mạch máu
Chụp buồng thất phải và động mạch phổi
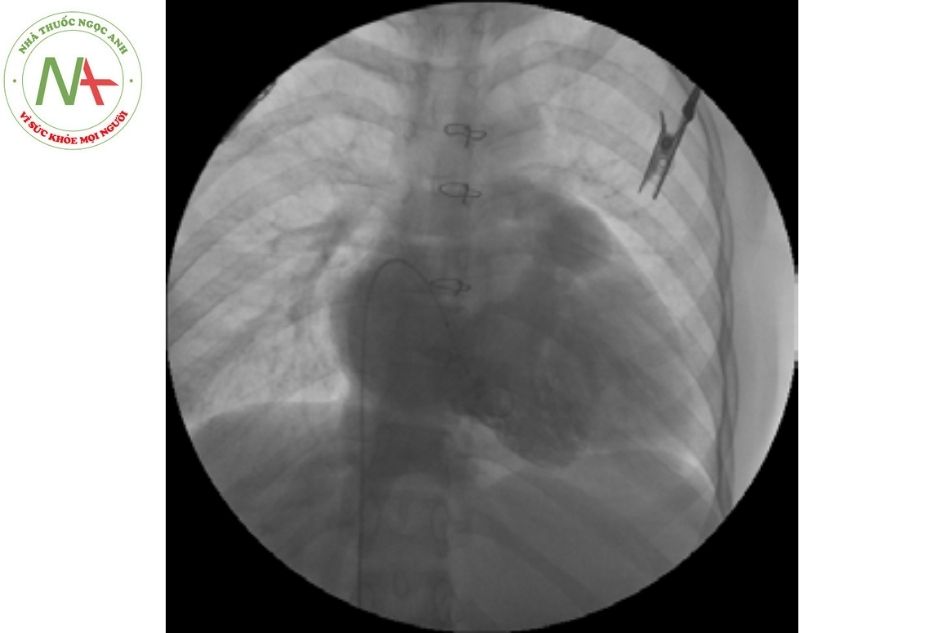
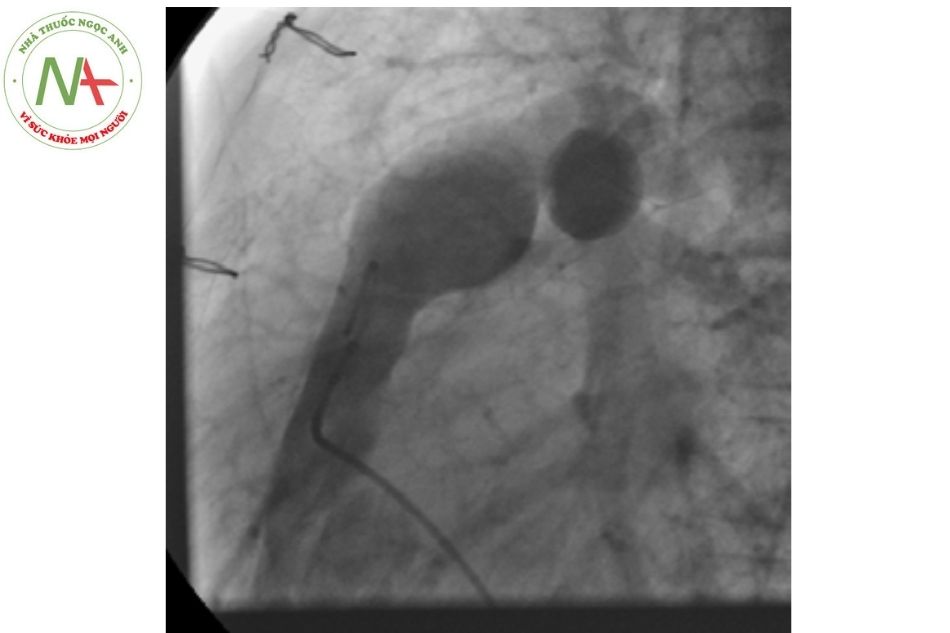
Đánh giá hình ảnh chụp ống conduit nối thất phải
– ĐMP (tốt nhất là bằng 2 bình diện) thông qua một ống thông có lỗ bên, để đánh giá mức độ hở van động mạch phổi và hình dạng của conduit, tình trạng vôi hóa và để xác định/loại trừ bất kỳ tình trạng hẹp nhánh xa động mạch phổi nào.
Đo áp lực động mạch phổi và chênh áp qua ĐRTP.
Sử dụng bóng đo để khảo sát đường ra thất phải
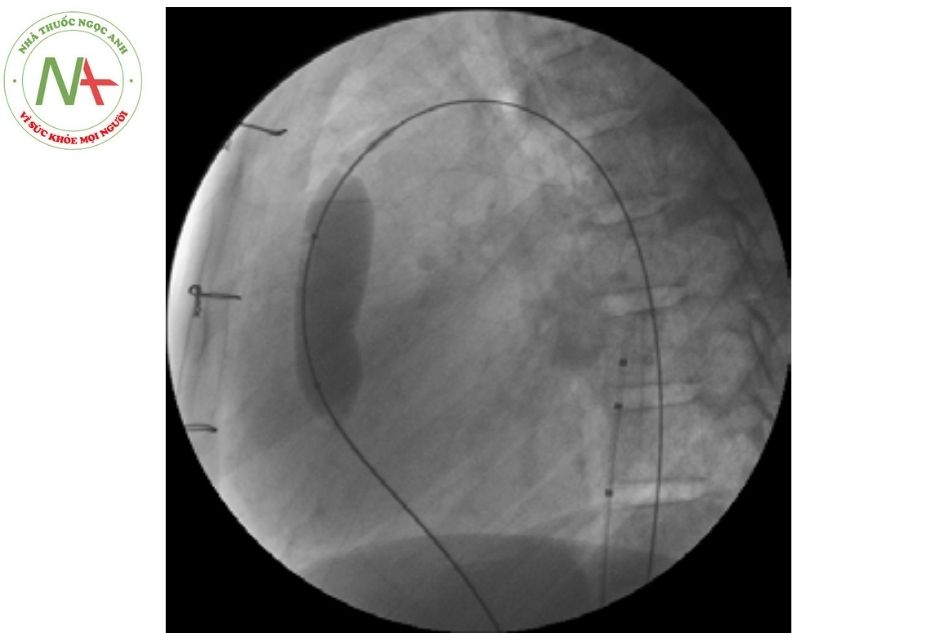
- Sử dụng bóng đo (sizing balloon) để khảo sát ĐRTP:
- Sử dụng bóng sizing balloon Amplatzer II: cho thấy hình ảnh đường ra thất phải (ĐRTP) và landing zone (vùng đặt van).
- Bóng nong áp lực thấp như Z-Med X (NuMED) hoặc bóng Crystal (Balt): đánh giá độ căng của động mạch phổi.
- Bóng áp lực cao như Mullins X (NuMED) hoặc bóng Atlas Gold PTA(Bard): được sử dụng nếu ĐRTP kém giãn nở khi dùng với bóng áp lực thấp.
- Lưu ý: Đường kính của conduit được đánh giá bằng cách bơm bóng ngang qua van động mạch phổi. Việc lựa chọn bóng đo phù hợp có vai trò rất quan trọng.
- Nếu trên phim chụp mạch, khoảng cách giữa đường ra thất phải (ĐRTP) và gốc động mạch chủ xa nhau, thì có thể sử dụng bóng giãn nở được (chẳng hạn như một bóng đo kích thước lỗ thông liên nhĩ).
- Nếu khoảng cách nói trên nhỏ hơn 10 mm: cần sử dụng một bóng áp lực cao để làm giãn conduit một cách từ từ đến khi đạt được đường kính cuối cùng, trước khi tiến hành đặt stent trong conduit.
- Lưu ý quan trọng: là chắc chắn rằng đường kính cuối cùng của conduit sau khi nong bóng sẽ không ảnh hưởng đến lưu lượng máu mạch vành.
Đánh giá động mạch vành trước can thiệp thay van động mạch phổi
- Bệnh nhân có nguy cơ cao mắc bệnh động mạch vành (ĐMV) thường được chụp chụp cắt lớp vi tính đa dãy (MSCT) hoặc cộng hưởng từ (MRI) để khảo sát hệ mạch vành trước can thiệp.
- Chụp gốc động mạch chủ đánh giá động mạch vành hoặc chụp động mạch vành chọn lọc đồng thời với bơm bóng vùng ĐRTP là bắt buộc ở tất cả các bệnh nhân thay van động mạch phổi qua da. Bước này là rất quan trọng do tỷ lệ bất thường gốc động mạch vành ở bệnh nhân mắc bệnh tim bẩm sinh cao hơn bình thường. Nếu động mạch vành ở gần vị trí đặt stent có nguy cơ bị chèn ép cao, cần đánh giá lại kỹ hơn trước khi quyết định thay van ĐMP qua da.
- Lưu ý: Chống chỉ định thay van ĐMP qua da nếu có chèn ép động mạch vành khi bơm bóng ĐRTP.
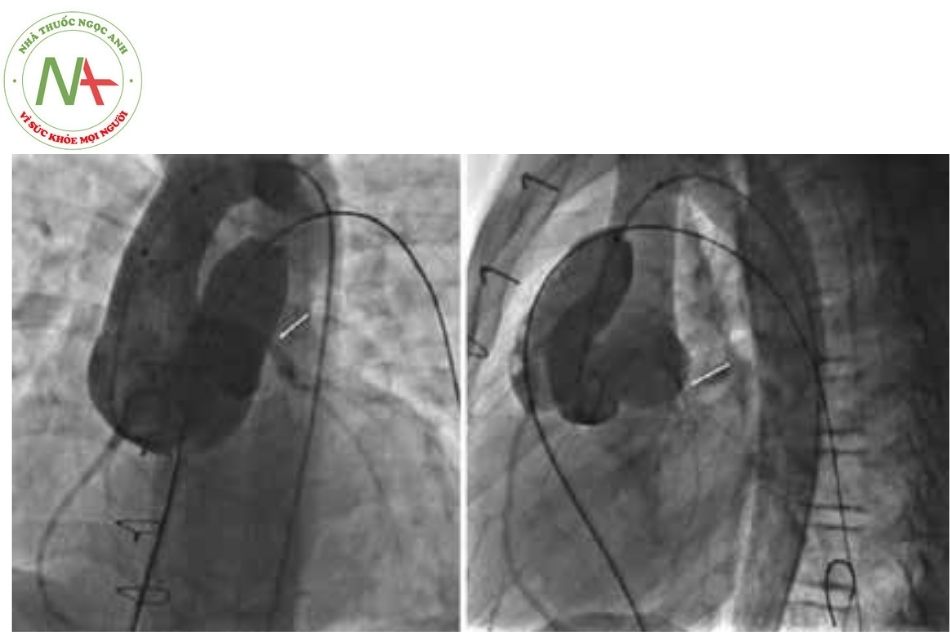
Đặt trước stent (pre-stent) vào đường ra thất phải
- Các nghiên cứu quan sát đã thấy rằng việc đặt trước stent (pre-stenting) vào ống conduit, sau đó mới tiến hành thay van ĐMP (TPVI) sẽ giúp giảm nguy cơ tiến triển gãy stent-van với van Do đó, việc đặt trước stent vào ống conduit trước TPVI hiện nay là thông lệ tiêu chuẩn ở hầu hết các trung tâm tim mạch.
- Thông thường, covered stent được ưu tiên hơn để tránh nguy cơ chảy máu nếu rách ống conduit trong quá trình triển khai đặt stent, do khi đó cần phải sử dụng bóng áp lực cao để nong ống conduit đến đường kính đã được kiểm tra từ trước.
- Non-covered stent được dùng nếu dự kiến đặt covered stent sẽ gây bít tắc gốc của một trong 2 nhánh động mạch phổi.
- Trong một số trường hợp (như: hẹp đoạn dài hoặc có dấu hiệu ĐRTP co lại (recoil) đáng kể khi xuống bóng): Có thể cần đặt thêm stent cho stent đặt trước đó (pre-stent) để hỗ trợ vùng landing zone.
Triển khai đặt pre-stent
Covered stent được triển khai trên hệ thống bóng nong BiB (bóng trong bóng) (NuMED Inc) hoặc một bóng trên super stiff wire (dây dẫn siêu cứng), trong đó wire được đặt trong các động mạch phổi, tốt nhất là trong động mạch phổi trái.
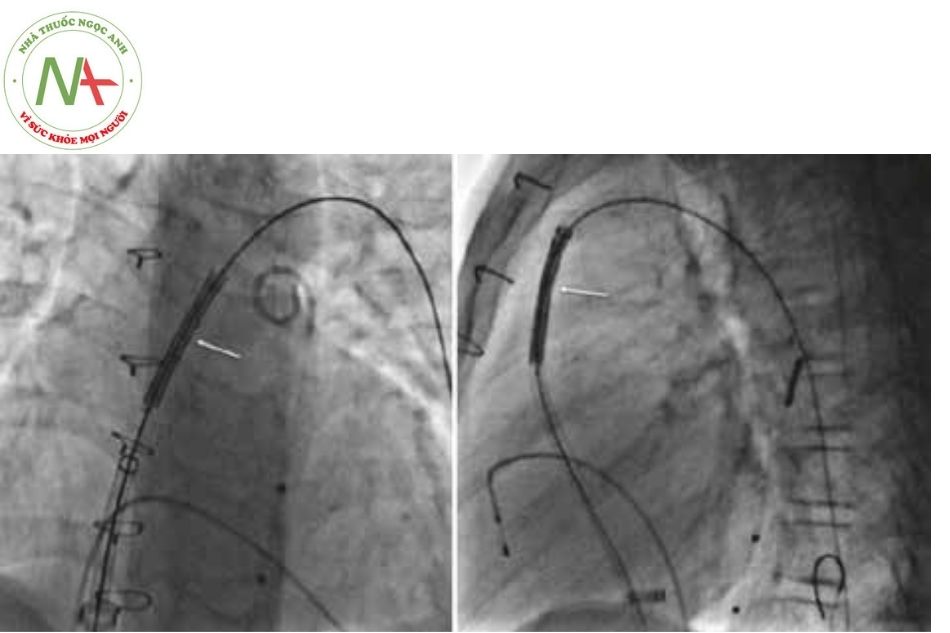
Lên bóng đặt stent: Nhìn chung, nên bơm bóng đến đường kính nhỏ hơn kích thước ban đầu của conduit khoảng 2 mm hoặc lớn hơn một chút trong trường hợp conduit có luồng chảy ngược không kèm theo hẹp.
Chụp kiểm tra sau đặt pre-stent
Luôn chụp mạch lại sau khi đặt stent để kiểm tra các biến chứng có khả năng xảy ra (như rách hoặc thoát thuốc cản quang từ ống conduit).
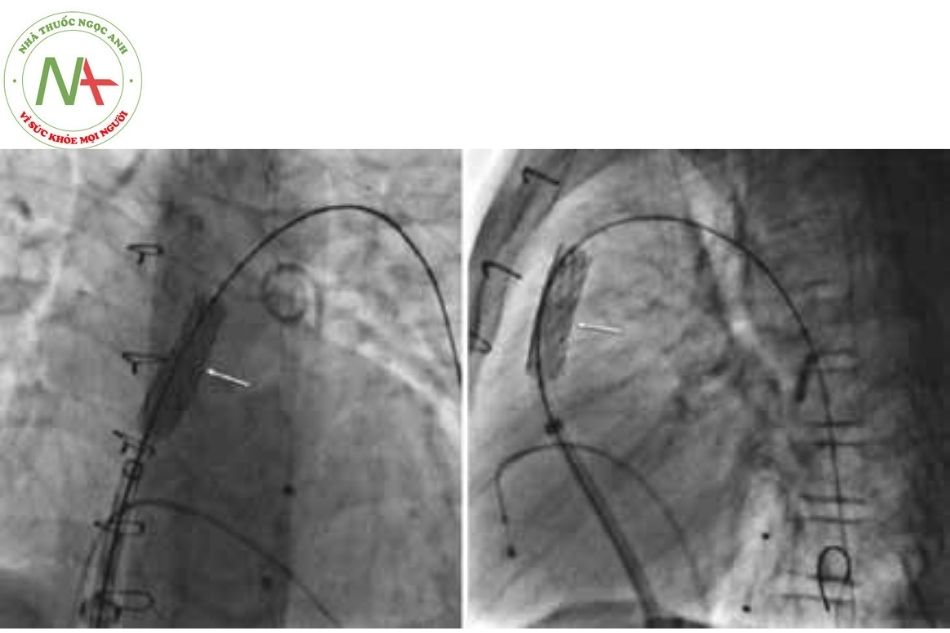
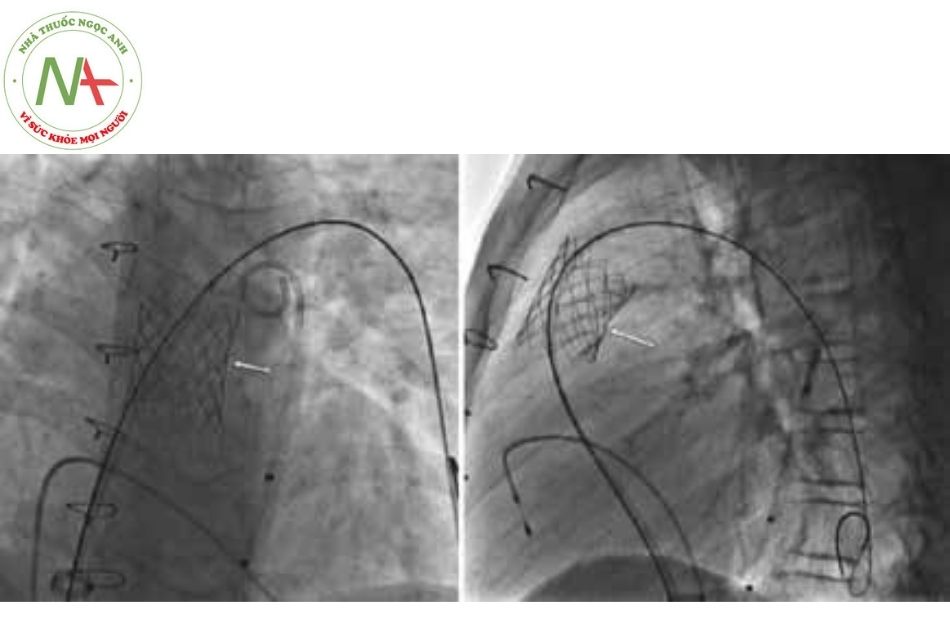
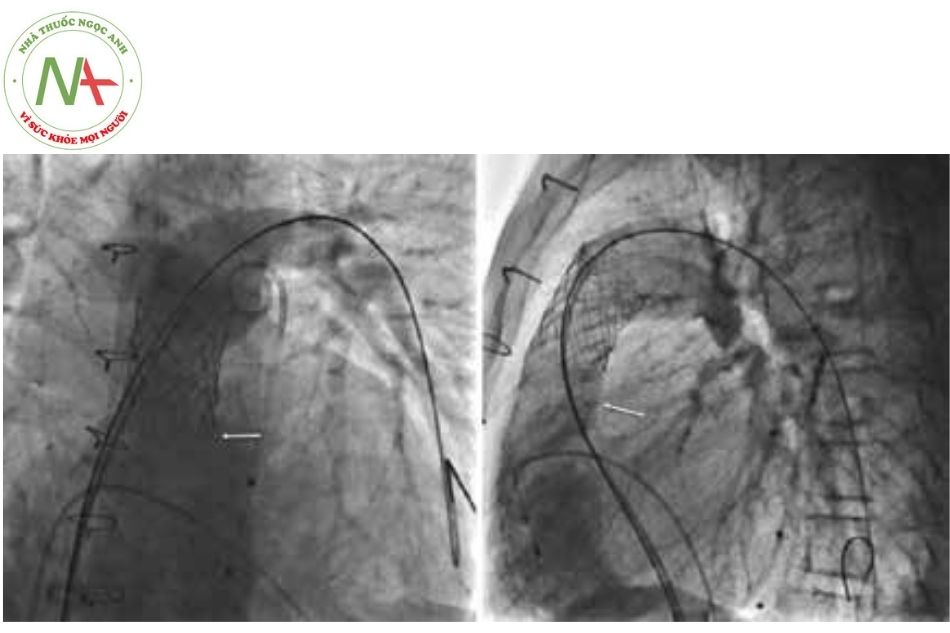
Lưu ý
Trong trường hợp stent bị co lại sau khi bóng xẹp, có thể cần nong lại với bóng áp lực cao, hoặc trong một số trường hợp cụ thể, có thể đặt nhiều stent để tạo vùng landing zone ổn định nhằm tránh cho van bị co lại sau này.
Sau khi đặt stent, điều quan trọng là đánh giá chênh áp qua stent. Thường không chấp nhận bất kỳ chênh áp nào lớn hơn 15 mmHg; nếu lớn hơn 15 mmHg, stent cần được nong rộng hơn nữa với một bóng có áp lực cao hơn (ví dụ bóng Atlas) cho đến khi chênh tồn dư nhỏ hơn 15 mmHg.
Đặt stent-van động mạch phổi
- Stent-van được uốn đối xứng bằng cách sử dụng một dụng cụ uốn chuyên dụng gần với bóng trên trục của bóng.

Chú thích: Hệ thống đưa van vào cơ thể được sử dụng là NovaFlex+ (Edwards
Lifesciences). Trong hệ thống delivery, van được gắn vào phần gần của bóng (mũi tên màu trắng)
- Introducer sheath tĩnh mạch đùi được dùng có kích thước phù hợp với cỡ stent-van:
- Van Melody TPV 20 và 22mm sử dụng introducer sheath Trong khi đó van Edwards SAPIEN XT 23 và 26 mm sử dụng sheath 14 Fr, van 29 mm sử dụng sheath 16 Fr.
- Đầu của sheath thường ở gần tĩnh mạch chủ dưới.
- Với van Edwards SAPIEN XT: Hệ thống NovaFlex được đưa qua introducer sheath thông qua loader cho đến khi van thoát ra khỏi sheath. Loader được rút vào đầu gần của hệ thống delivery. Van Melody cũng đưa qua sheath tương tự.
- Tại tĩnh mạch chủ dưới, việc căn chỉnh van được bắt đầu bằng cách nhấn nút nhả và kéo trở lại ống thông bóng cho đến khi hệ thống đưa dụng cụ khóa vào vị trí căn chỉnh van, sau đó sử dụng bánh xe căn chỉnh van (Hình 14) để đặt van giữa các điểm đánh dấu.
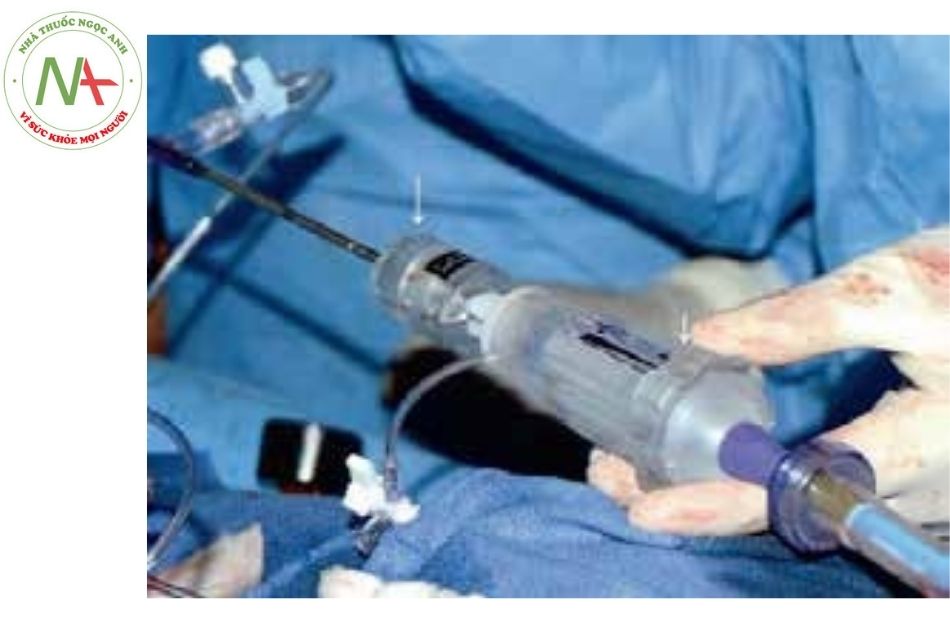
Chú thích: Hai hệ thống bánh xe: bánh xe uốn cong (mũi tên ngắn) được sử dụng để điều khiển van đi qua đường ra thất phải và bánh xe căn chỉnh van (mũi tên dài) được sử dụng để định vị van chính xác hơn giữa các điểm đánh dấu.
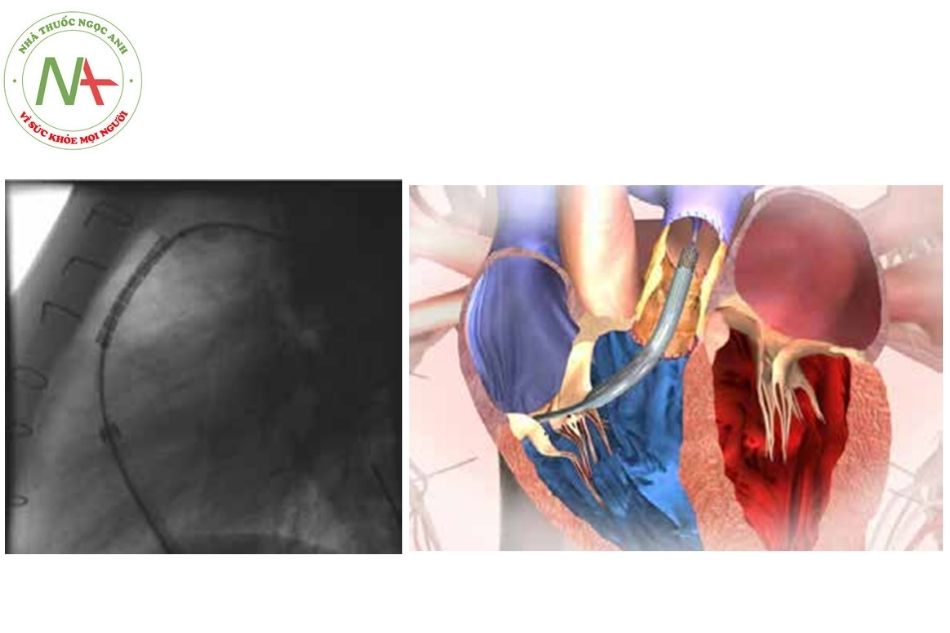
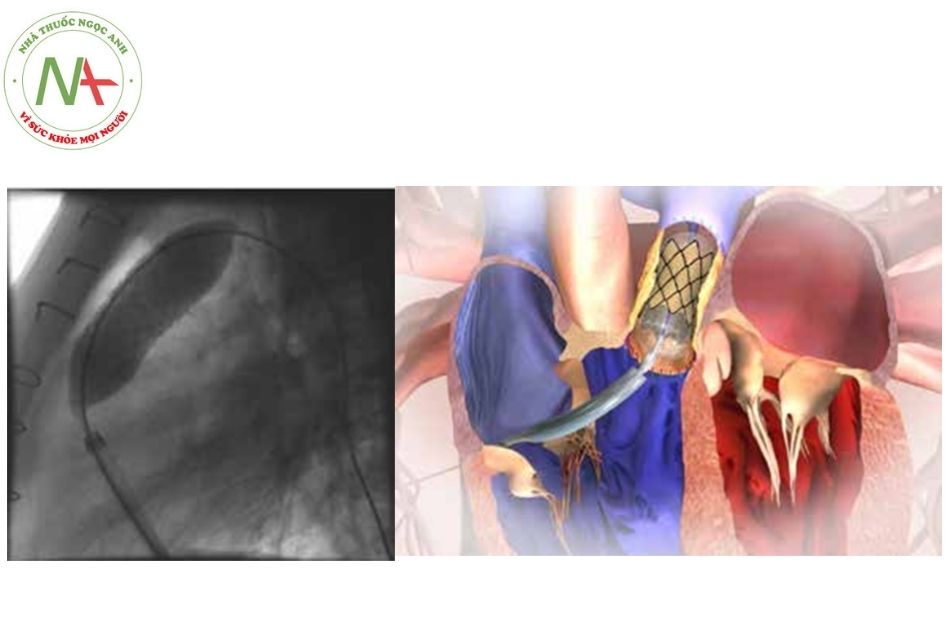
- Đặt stent-van:
- Van được đưa qua vùng ĐRTP đã được đặt pre-stent, trên dây dẫn cứng (Meier hoặc Lunderquist);
- Bánh xe uốn cong (Hình 14) được sử dụng để thao tác giúp van ở đúng vị trí.
- Khi thả nút đặt stent, ống thông Flex rút lại điểm đánh dấu đôi để hoàn toàn ra ngoài bóng.
- Chụp mạch để chắc chắn van ở chính giữa stent (landing zone). Đặt stent ra xa hoặc gần đều có thể khiến van bị rơi.
- Trong quá trình đặt van, điều quan trọng cần lưu ý là cần lên hết toàn bộ thể tích của bóng (phụ thuộc thể tích, không phải phụ thuộc áp lực). Bơm được giữ trong một vài giây (< 10 giây) và sau đó bóng được xuống nhanh chóng.
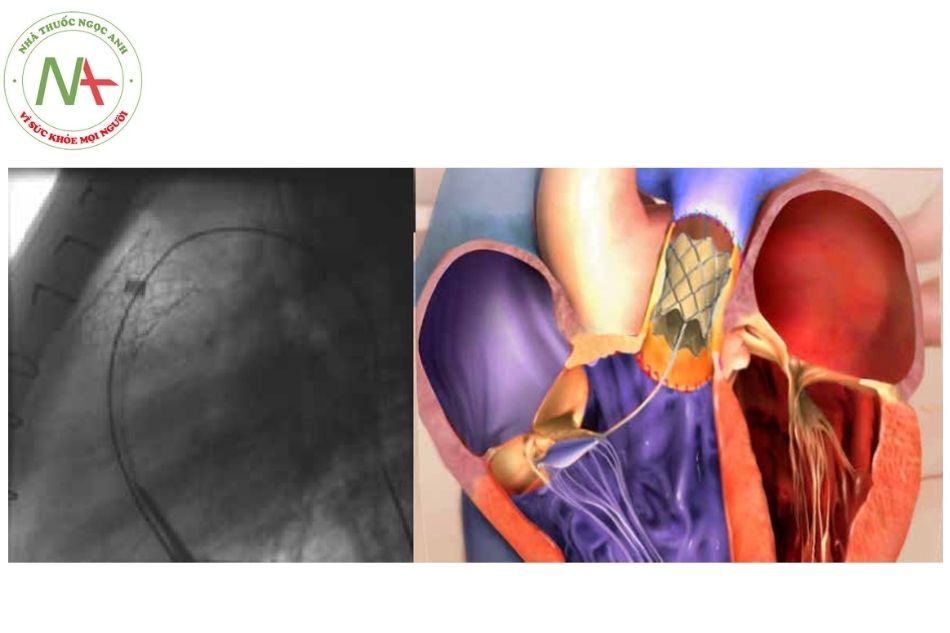
Kiểm tra lại sau đặt stent-van
- Cần chụp đánh giá để loại trừ tình trạng tổn thương ĐMP gây thoát mạch, sau mỗi lần nong bóng ở ĐRTP hoặc ngay khi xảy ra mất ổn định huyết động trong quá trình can thiệp.
- Đánh giá hoạt động của van thông qua chỉ số huyết động và chụp mạch để phát hiện bất kỳ dấu hiệu nào của hở van.
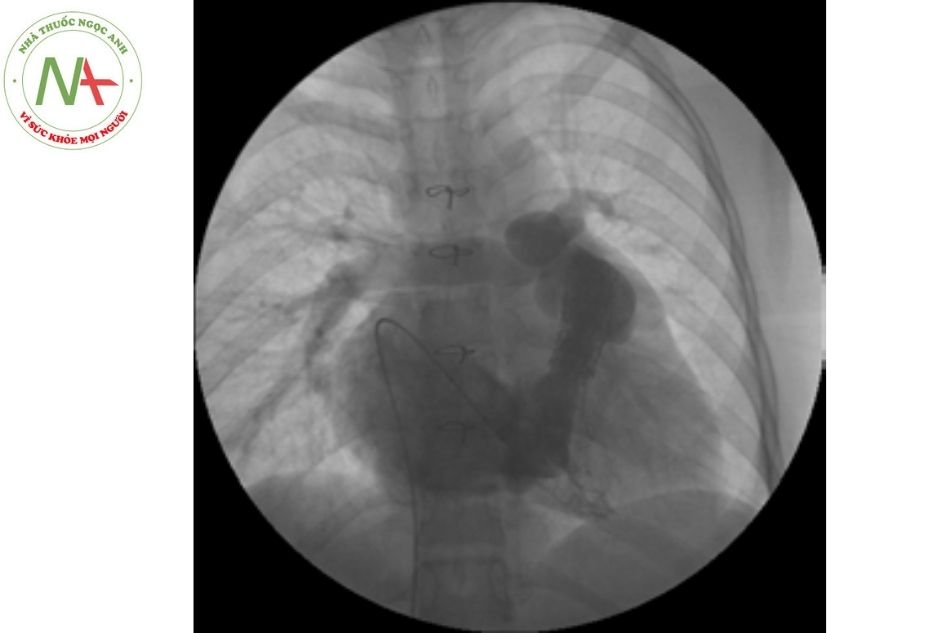
- Chụp lại động mạch chủ lên hoặc chụp động mạch vành chọn lọc để đánh giá dòng máu trong động mạch vành trái.
- Ngoài ra, siêu âm tim đánh giá chức năng đường ra thất phải trước và sau khi đặt van giúp đánh giá chính xác mức độ hở van động mạch phổi sau khi rút dây dẫn.
6.6. Đóng đường vào mạch máu
Khi sử dụng introducer sheath có kích thước lớn, thiết bị đóng mạch như hai chỉ khâu Perclose (Abbott Vascular, Abbott Park, IL) được khuyến cáo sử dụng ở giai đoạn đầu của can thiệp giúp cầm máu tối ưu.
Tuy vậy, thông thường khâu chỉ “hình số 8” cũng đạt được hiệu quả. Chỉ Vicryl 0 khâu vào vùng phần mềm xung quanh vị trí chọc mạch để tạo ra áp lực ép trên vị trí chọc mạch. Mũi chỉ khâu được tháo vào ngày hôm sau.
BIẾN CHỨNG VÀ XỬ TRÍ
Rách conduit
Trường hợp xảy ra thoát mạch do rách conduit, cần dùng covered stent (stent CP, NuMED Inc) đặt để xử trí vết rách:
- Mục tiêu là áp stent vào thành ĐRTP và xòe các đầu vào thành tim để bịt kín vết rách. Khi đó có thể không cần bơm bóng để covered stent nở hết cỡ, đặc biệt trường hợp có thể gây chèn ép động mạch vành.
- Chiều dài của covered stent nên vượt quá chiều dài ĐRTP từ 1 đến 2 mắt stent (zigs) ở cả đầu gần và đầu xa.
Gãy trong stent
- Xảy ra với tỷ lệ 20 đến 21% trong các ca không đặt stent từ trước và 5 đến 16% trong các ca có đặt stent trước. Việc xử trí có thể cần đặt covered stent nếu có biến chứng thoát mạch.
- Trường hợp không có chảy máu, có thể xử trí bằng cách đặt thêm 1 van vào vị trí van ban đầu (van trong van).
Đè ép động mạch vành
- Biến chứng hiếm xảy ra nhưng có tỷ lệ tử vong rất cao.
- Biện pháp dự phòng là quan trọng: việc kiểm tra bóng để loại trừ khả năng chèn ép động mạch vành phải trước khi đặt van là bắt buộc. Đồng thời cần chụp lại động mạch vành trước khi nong rộng hơn trong trường hợp có nghi ngờ.
==>> Xem thêm: Can thiệp nong và đặt stent trong một số bệnh tim bẩm sinh
Viêm nội tâm mạc nhiễm khuẩn
Bệnh nhân có nguy cơ mắc viêm nội tâm mạc nhiễm khuẩn. Do đó cần lưu ý dùng kháng sinh dự phòng trước và trong can thiệp. Đồng thời dự phòng viêm nội tâm mạc nhiễm khuẩn sau can thiệp thay van.
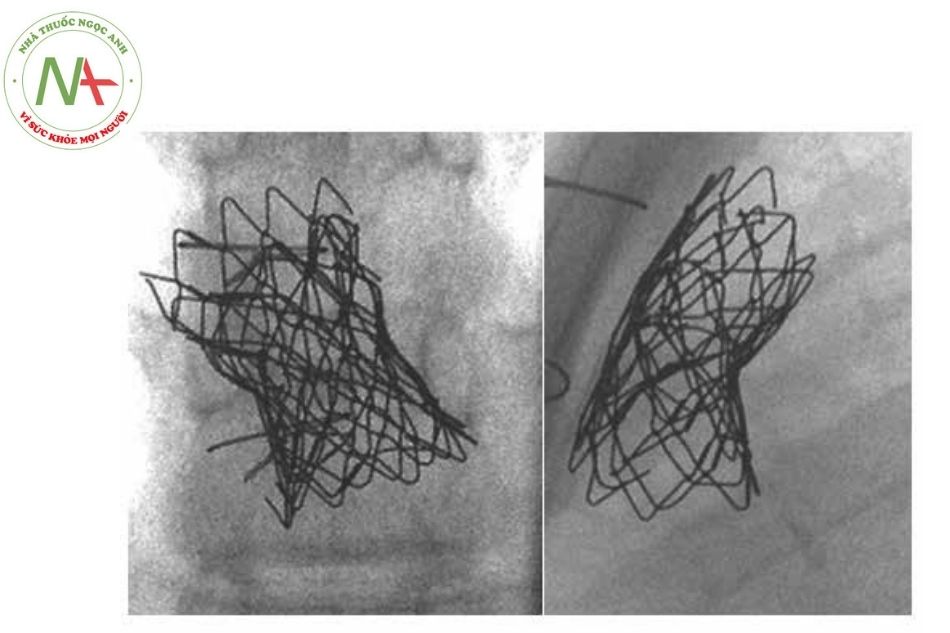
(Nguồn: Gianfranco Butera. Atlas of Cardiac Catheterization for Congenital Heart Disease, 2019)
KẾT QUẢ CAN THIỆP
Kết quả ngắn hạn và trung hạn của thay van ĐMP qua đường ống thông (TPVI) với van Melody và SAPIEN là tương tự nhau, tuy nhiên van Melody có nhiều dữ liệu nghiên cứu lâu dài hơn.
Van Melody
Dữ liệu có nhiều nghiên cứu ngắn hạn, trung hạn và dài hạn. Các nghiên cứu đã loại trừ 4 đến 8% bệnh nhân được lên kế hoạch điều trị TPVI do kích thước đường ra thất phải (ĐRTP) không thuận lợi hoặc do đè ép động mạch vành.
Sau khi can thiệp TPVI thành công, các nghiên cứu ghi nhận:
- Tỷ lệ tử vong chung là 0-5 %.
- Dụng cụ không ổn định chiếm 1%, rách conduit cần phẫu thuật 0,8 đến 2%, đè ép động mạch vành (LAD) sau khi đặt dụng cụ từ 0 đến 1% và tắc gốc của một trong các nhánh chính động mạch phổi (“jailing “) chiếm 0,6%.
- Chênh áp qua tổn thương hẹp đường ra thất phải giảm đáng kể từ giá trị trung bình 35-40 xuống 10-20 Tỉ lệ hở van ĐMP giảm từ giá trị trung bình 16-27% xuống 1-2%.
- Tỉ lệ van Melody không bị rối loạn chức năng hoặc tái can thiệp là 94-95% trong một năm. Những bệnh nhân không cần can thiệp lại có hở van ĐMP nhẹ hoặc ít hơn khi theo dõi một năm. Nhìn chung, phẫu thuật cần tiến hành chiếm 3% trong thời gian theo dõi với 86% không phải tái phẫu thuật sau 30 tháng.
- Viêm nội tâm mạc được chẩn đoán chiếm 1-3% các ca bệnh theo dõi trong năm năm sau TPVI với van Melody.
Sau sáu tháng, phân độ NYHA được cải thiện ở 77% bệnh nhân và chỉ xấu đi 0,8% trường hợp.
Các nghiên cứu lâu dài cho thấy kết quả tốt (tỷ lệ sống sót sau khi không có biến cố ước tính là 88% sau 10 năm) ở những bệnh nhân có chênh áp đỉnh tồn dư tại vị trí tắc nghẽn đường ra thất phải < 15 mmHg (đo trên thông tim sau can thiệp).
Một nghiên cứu đã so sánh kết quả lâu dài của TPVI (van Melody) với thay van động mạch phổi sinh học, sau 10 năm theo dõi, không có sự khác biệt về tỷ lệ không thay lại van giữa các nhóm.
Van Edwards SAPIEN
Hiện còn thiếu dữ liệu các nghiên cứu so sánh với phẫu thuật. Nghiên cứu của Kenny D và cộng sự cho thấy chênh áp đỉnh – đỉnh tâm thu qua conduit giảm từ 27 xuống 12 mmHg. Tại thời điểm theo dõi sáu tháng, số bệnh nhân trong nhóm NYHA I tăng từ 5 lúc ban đầu lên 27. Hở van ĐMP trung bình hoặc nhẹ chiếm 97% bệnh nhân.
Trong nghiên cứu COMPASSION cũng của tác giả Kenny D và cộng sự trong thời gian 3 năm, tổng số 69 bệnh nhân đã được điều trị thành công. Tại thời điểm theo sau ba năm, 90% bệnh nhân có hở van ĐMP nhẹ hoặc trung bình. Tỷ lệ không phải tái can thiệp là 94% và không bị viêm nội tâm mạc nhiễm khuẩn là 97%.
CHĂM SÓC VÀ THEO DÕI
Bệnh nhân thường được theo dõi sát sau can thiệp, duy trì uống aspirin 81 mg trong ít nhất 6 tháng, tuân thủ điều trị dự phòng viêm nội tâm mạc lâu dài.
- Có thể ra viện 24 giờ sau can thiệp nếu tình trạng ổn định.
- Cần chú ý cẩn thận đến vị trí chọc mạch trước khi xuất viện để đảm bảo không có khối máu tụ hoặc chảy máu chưa cầm.
Khám theo dõi và siêu âm tim được thực hiện vào các thời điểm 1, 6 và 12 tháng và hàng năm sau đó. Xquang tim phổi được chụp trước khi xuất viện và sau 6 tháng để xác định vị trí van/stent và phát hiện bất kỳ biến chứng gãy stent có thể xảy ra.
Cần tư vấn cho bệnh nhân về mức độ quan trọng của dự phòng viêm nội tâm mạc nhiễm khuẩn.
TÀI LIỆU THAM KHẢO
1.Baumgartner H, Bonhoeffer P, De Groot NM, et al. ESC Guidelines for the management of grown-up con- genital heart disease (new version 2010). Eur Heart J 2010; 31:2915.
2. Gianfranco Butera, Massimo Chessa, Andreas Eicken, John Thomson. Atlas of Cardiac Catheterization for Congenital Heart Disease. Springer International Publishing AG, 2019.
3. EickenA, Ewert P, Hager Aetal (2011). Percutaneous pulmonary valve implantation: two-centre experience with more than 100 patients. Eur Heart J 32:1260–1265.
4. Butera G, Milanesi O, Spadoni I et al (2013). Melody transcatheter pulmonary valve implantation. Results from the registry of the Italian society of pediatric cardiology. Catheter Cardiovasc Interv 81:310–316.
5. Holoshitz N, Hijazi ZM (2013). Transcatheter pulmonary valve replacement: valves, techniques of implanta- tion and outcomes. Intervent Cardiol 4:465–477.
6. Oechslin L, Corti R, Greutmann M, Kretschmar O, Gaemperli O (2018). Percutaneous pulmonary valve im- plantation in grown-up congenital heart disease patients: Insights from the Zurich experience. J Interv Car- diol 31(2):251-260.
7. Boudjemline Y, Brugada G, Van-Aerschot I, et al. Outcomes and safety of transcatheter pulmonary valve re- placement in patients with large patched right ventricular outflow Arch Cardiovasc Dis 2012; 105:404.
8. Gillespie MJ, Rome JJ, Levi DS, et Melody valve implant within failed bioprosthetic valves in the pulmo- nary position: a multicenter experience. Circ Cardiovasc Interv 2012; 5:862.
9. Cheatham JP, Hellenbrand WE, Zahn EM, et al. Clinical and hemodynamic outcomes up to 7 years after transcatheter pulmonary valve replacement in the US melody valve investigational device exemption Circulation 2015; 131:1960.
10. Cools B, Brown S, Budts W, et al. Up to 11 years of experience with the Melody valved stent in the right ventricular outflow tract. EuroIntervention 2018; 14:e988.
11. Nordmeyer J, Ewert P, Gewillig M, et al. Acute and midterm outcomes of the post-approval MELODY Regis- try: a multicentre registry of transcatheter pulmonary valve implantation. Eur Heart J 2019; 40:2255.
12. Georgiev S, Ewert P, Tanase D, et al. A Low Residual Pressure Gradient Yields Excellent Long-Term Outcome After Percutaneous Pulmonary Valve Implantation. JACC Cardiovasc Interv 2019; 12:1594.
13. Kenny D, Hijazi ZM, Kar S, et al. Percutaneous implantation of the Edwards SAPIEN transcatheter heart valve for conduit failure in the pulmonary position: early phase 1 results from an international multicenter clinical trial. J Am Coll Cardiol 2011; 58:2248.
14. Kenny D, Rhodes JF, Fleming GA, et al. 3-Year Outcomes of the Edwards SAPIEN Transcatheter Heart Valve for Conduit Failure in the Pulmonary Position From the COMPASSION Multicenter Clinical Trial. JACC Cardio- vasc Interv 2018; 11:1920.
