Bệnh truyền nhiễm
Nhiễm virus hợp bào hô hấp: Nguyên nhân, chẩn đoán và hướng dẫn điều trị theo BMJ
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
Nhà thuốc Ngọc Anh – Để tải bài viết Nhiễm virus hợp bào hô hấp: Nguyên nhân, chẩn đoán và hướng dẫn điều trị theo BMJ file PDF xin vui lòng click vào link ở đây.
Tóm tắt
◊ Virus hợp bào hô hấp (RSV) là nguyên nhân phổ biến nhất gây bệnh viêm tiểu phế quản; gần như mọi trẻ em đều đã từng bị nhiễm virus này trước 2 tuổi.
◊ Các đợt bùng phát theo mùa xảy ra trên toàn thế giới vào các tháng mùa đông.
◊ Có các đặc điểm là ho, thở khò khè, suy hô hấp, và giảm oxy máu.
◊ Hầu hết các đợt phát bệnh đều ở thể nhẹ và tự khỏi.
◊ Điều trị chủ yếu là hỗ trợ: bổ sung oxy, làm sạch mũi và phổi, hỗ trợ hô hấp, hỗ trợ dinh dưỡng.
◊ Các nhóm nguy cơ cao bị bệnh nặng bao gồm trẻ nhũ nhi có tiền sử sinh non, bệnh phổi mạn tính, bệnh tim bẩm sinh phức tạp, và suy giảm miễn dịch.
◊ Miễn dịch dự phòng với palivizumab sẵn có dành cho các nhóm nguy cơ cao.
Thông tin cơ bản
Định nghĩa
RSV trước đây được xếp vào họ Paramyxovirus. Sau đó loại virus này được xếp lại vào bộ Mononegavirales là một thành viên của họ Pneumoviridae. Virus là nguyên nhân gây bệnh viêm tiểu phế quản phổ biến nhất. Các triệu chứng bao gồm sổ mũi, ho, thở khò khè, suy hô hấp, và giảm oxy máu[1] RSV cũng có thể gây viêm phổi ở trẻ em và, trong trường hợp hiếm gặp, ở cả người lớn có sức đề kháng bình thường.[Fig-1]
Dịch tễ học
RSV là một trong những mầm bệnh quan trọng nhất ở tuổi mầm non và là nguyên nhân phổ biến nhất gây bệnh viêm tiểu phế quản và viêm phổi ở trẻ sơ sinh trên toàn thế giới.[1] Một đánh giá tổng hợp 98 nghiên cứu nhận thấy không có thay đổi đáng kể nào về số ca nhập viện do RSV trong 20 năm qua.[4]
RSV gây ra tỷ lệ mắc bệnh và tỷ lệ tử vong đáng kể, đặc biệt là trong số trẻ nhũ nhi có nguy cơ cao và trẻ sinh non, bị bệnh phổi mạn tính, bệnh tim bẩm sinh phức tạp, hoặc suy giảm miễn dịch.[5] Nam giới, tuổi < 6 tháng, sinh ra vào nửa đầu mùa RSV, tình trạng đông đúc/nhiều anh chị em, và được gửi ở trung tâm giữ trẻ đều có liên quan đến nguy cơ gia tăng phải nhập viện vì RSV.[4]
Tại Scotland, trung bình 1976 trẻ em nhập viện mỗi năm trong giai đoạn 2001 đến 2003, với chẩn đoán chính là viêm tiểu phế quản.[6] Tại Hoa Kỳ, bệnh chiếm 18% số ca ở phòng cấp cứu và 20% số ca nhập viện do nhiễm trùng đường hô hấp cấp ở trẻ em dưới 5 tuổi.[7] Trong số các bệnh nhân bị nhiễm trùng đường hô hấp cấp trong năm 2015 ở Trung Quốc, RSV chiếm 18,7% (95%CI (Khoảng tin cậy 95%) 17,1% đến 20,5%).[8] Trong cùng năm đó, trên toàn cầu, ước tính có 33,1 triệu (độ dao động không chắc chắn (uncertainty range) [UR] 21,6-50,3) các đợt nhiễm trùng đường hô hấp dưới cấp tính do RSV dẫn đến khoảng 3,2 triệu (UR 2,7-3,8) ca nhập viện và 59.600 (UR 48.000-74.500) ca tử vong tại bệnh viện ở trẻ em dưới 5 tuổi. Ở trẻ em dưới 6 tháng tuổi, 1,4 triệu (UR 1,2-1,7) ca nhập viện và 27.300 (UR 20.700-36.200) ca tử vong tại bệnh viện có nguyên nhân từ nhiễm trùng đường hô hấp dưới cấp tính do RSV.[9]
Các đợt bùng phát theo mùa xảy ra trên toàn thế giới vào các tháng mùa đông. Tại Hoa Kỳ và trên khắp bắc bán cầu, dịch bệnh thường bắt đầu vào tháng Mười Một, với đỉnh điểm vào tháng Một hoặc tháng Hai. Số ca bệnh giảm trong 2 tháng sau đó với các ca bệnh xuất hiện rải rác trong phần còn lại của năm. Sự dao động theo vùng cũng xảy ra nhưng khả năng dự đoán được thấp hơn.[10] Ở nam bán cầu, các đợt bùng phát theo mùa xảy ra từ tháng Năm đến tháng Chín. Các vùng nhiệt đới thường lưu hành bệnh kéo dài lâu hơn liên quan đến mùa mưa. Đến 2 tuổi, gần như tất cả trẻ em đều đã bị nhiễm RSV, và một nửa trong số đó đã bị nhiễm hai lần. Không xảy ra sinh miễn dịch kéo dài và hay gặp tình trạng tái nhiễm, thường thì mức độ nặng sẽ thấp hơn.
Gánh nặng của việc nhiễm RSV ngày càng tăng hơn ở người lớn và người cao tuổi. Ước tính số người lớn và người trên 65 tuổi có nguy cơ cao nhập viện vì RSV ở Hoa Kỳ nhiều gấp 3 lần so với số trẻ em dưới 5 tuổi.[11] Ngày càng có nhiều nghiên cứu báo cáo về tác động của virus này và các bệnh do virus khác gây nên trong môi trường chăm sóc dài hạn, các trung tâm chăm sóc người lớn, và nhà dưỡng lão.[12] [13] Nhiều bác sĩ chăm sóc cho người lớn hiếm khi coi RSV là một nguyên nhân gây bệnh đường hô hấp, và việc này thường dẫn đến việc lạm dụng thuốc kháng sinh.[14]
Bệnh căn học
RSV trước đây được xếp vào họ Paramyxovirus. Sau đó loại virus này được xếp lại vào bộ Mononegavirales là một thành viên của họ Pneumoviridae. Màng plasma của virus có nguồn gốc từ tế bào vật chủ và bao quanh một nucleocapsid. Hệ di truyền của virus trong nucleocapsid bao gồm một sợi RNA với 10 gen mã hóa cho tổng cộng 11 protein. Hai trong số các protein này tái bản virus trực tiếp, và 9 protein còn lại hoạt động như các protein cấu trúc và glycoprotein bề mặt.[15]
RSV có 3 glycoprotein bề mặt: protein dung hợp (F), protein nhỏ kỵ nước (SH), và protein gắn glycosyl hóa (G). Các protein F và G là những mục tiêu chính của các kháng thể của vật chủ và do đó đóng vai trò quan trọng trong sinh lý bệnh học của RSV. Protein G làm trung gian cho việc gắn vào tế bào vật chủ, và protein F giúp dung hợp màng plasma của virus và vật chủ, cho phép chuyển RNA của virus vào tế bào vật chủ. Protein F cũng đẩy mạnh sự tập hợp các tế bào đa nhân bằng việc dung hợp các màng của chúng, dẫn đến sự hợp bào, hình thành nên tên của loại virus này.[15] Vai trò của Protein SH kém rõ ràng hơn.[Fig-1]
Sinh lý bệnh học
Virus lây truyền qua đường tiếp xúc với các giọt nước bọt từ đường hô hấp trong không khí, nhiễm vào lớp niêm mạc liên kết hoặc niêm mạc mũi họng.[16] [17] RSV có thể sống sót trên các bề mặt cứng sau khoảng thời gian lên tới 6 giờ.[18] Giai đoạn ủ bệnh của virus từ 3 đến 5 ngày. Các bệnh nhân có sức đề kháng bình thường thải bỏ virus bình quân trong 8 ngày, dù việc thải loại này có thể lên tới 4 tuần.[16] [19] [20] Các bệnh nhân suy giảm miễn dịch có thể thải bỏ virus trong 4 đến 6 tuần.
Quá trình tái bản virus bắt đầu ở biểu mô mũi và sau đó tiến triển xuống dưới qua biểu mô tiểu phế quản và tế bào phế nang típ 1 và 2.[21] [22] Nhiễm virus thường chỉ giới hạn ở đường hô hấp và hiếm khi ghi nhận gây bệnh ngoài phổi.[23] Sự tái bản virus dẫn đến hoại tử biểu mô ở tiểu phế quản, sau đó là sự thâm nhiễm tế bào lympho T quanh tiểu phế quản và phù nề dưới niêm mạc.[24] Các xét nghiệm nhận thấy có thể có xu hướng di truyền của bệnh RSV thể nặng liên quan đến đột biến F của các gen IL4, TLR4, và CD14.[25] [26] Sự bài tiết các chất niêm mạc nhày tăng về số lượng và hòa lẫn với các mảnh vỡ tế bào. Việc bị mất biểu mô có lông rung khiến cho sự thanh thải các chất bài tiết này trở nên khó khăn. Kết quả cuối cùng là niêm mạc dày đặc làm hẹp đường thở, gây ra thở khò khè, ho, bẫy khí, và tỷ lệ thông khí tưới máu (V/Q) không tương xứng.
Đồng nhiễm các virus hô hấp thường được ghi nhận, với tỷ lệ lên tới 60%. Đồng nhiễm các loại rhinovirus và bocavirus ở người hay gặp nhất. Tác động của đồng nhiễm RSV lên mức độ nặng của bệnh hiện vẫn còn gây tranh cãi. Các đánh giá gợi ý rằng đồng nhiễm RSV, xét về tổng thể, không có liên quan đến việc gia tăng mức độ nặng của bệnh, nhưng hiệu ứng của đồng nhiễm theo các cặp cụ thể lên mức độ nặng của bệnh là chưa rõ.[4] [27] [28] [29]
Phân loại
Phân loại virus
RSV trước đây được xếp vào họ Paramyxovirus. Sau đó loại virus này được xếp lại vào bộ Mononegavirales là một thành viên của họ Pneumoviridae.[1] [2] [3] Họ này bao gồm một số mầm bệnh hô hấp của động vật ngoài metapneumovirus ở người.
Phòng ngừa
Ngăn ngừa sơ cấp
Không có vắc-xin để phòng nhiễm RSV; tuy nhiên, một loại vắc-xin tiềm năng hạt nano RSV F điều chế từ tế bào côn trùng đang được nghiên cứu phát triển và đã chứng tỏ được tiềm năng.[41] [42] Các thử nghiệm lâm sàng giai đoạn 2 đang diễn ra và Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ đã công nhận chỉ định của vắc-xin tiềm năng này trong việc bảo vệ người từ 60 tuổi trở lên.[43] Vắc-xin tiểu phần RSV F hiện cũng đang được thử nghiệm để sử dụng ở phụ nữ có thai với kỳ vọng truyền miễn dịch cho bào thai.[44] Nhiều loại vắc-xin tiểu phần, axit nucleic, và vắc-xin sống giảm động lực hiện đang ở các giai đoạn đầu của quá trình phát triển.[45] [46] Một báo cáo của Tổ chức Y tế Thế giới cung cấp phần tóm tắt toàn diện về việc phát triển vắc-xin RSV.[45]
Globulin miễn dịch RSV (RSV-IGIV) truyền miễn dịch cho trẻ nhũ nhi có nguy cơ; tuy nhiên nó có một số nhược điểm hạn chế. Các bất lợi chính của RSV-IGIV là yêu cầu dùng qua tĩnh mạch, thời gian tiêm truyền lâu (4-6 giờ), và lượng tiêm truyền lớn.[47]
Miễn dịch dự phòng với palivizumab sẵn có cho trẻ nhũ nhi có nguy cơ cao (ví dụ như tiền sử sinh non [<29 tuần thai], bệnh phổi mạn tính do sinh non, bệnh tim bẩm sinh phức tạp do sinh non, hay suy giảm miễn dịch).[20] [48] [49] Việc sử dụng biện pháp này trong các nhóm nguy cơ cao có thể giảm mức nhập viện 45% đến 55%.[50] [51] [52] [53] [54] [55] [56] 1[B]Evidence Biện pháp dự phòng với Palivizumab ở các nhóm bệnh nhân này cũng có liên quan đến việc giảm tỷ lệ tử vong do mọi nguyên nhân trong mùa RSV.[54] Tỷ lệ nhập viện cao do RSV cũng thấy ở trẻ nhũ nhi sinh non từ 33 đến 35 tuần, giới tính nam, sinh ra trong nửa đầu của mùa RSV, có nhiều anh chị em, hoặc tới nhà trẻ.[4] [57] [58] [59] Palivizumab được chỉ định tiêm bắp hàng tháng trong mùa RSV.[48]
Ngăn ngừa thứ cấp
Một số chiến lược tập trung vào việc hạn chế lây lan RSV. Rửa tay trong môi trường lâm sàng và ngoài lâm sàng là rất quan trọng.[61] 5[C]Evidence Rửa tay và rửa các đồ chơi dùng chung là quan trọng đối với tất cả các thành viên gia đình và những người tiếp xúc gần gũi để hạn chế sự lây lan của RSV. Bệnh nhân cần nhập viện phải được cách ly với những cẩn thận khi tiếp xúc.[20] Việc sử dụng đúng cách các biện pháp bảo hộ như áo choàng, găng tay, và khẩu trang là hiệu quả nếu có những giọt nước bọt từ hệ hô hấp trong không khí và nên sử dụng chúng khi chăm sóc các bệnh nhân này.[132] [133] [134] [135] Không cần thiết sử dụng khẩu trang hô hấp N95, và khẩu trang này không hiệu quả hơn loại khẩu trang phẫu thuật đơn giản.[19] [70] [136] Việc sàng lọc RSV ở những bệnh nhân nghi ngờ cho phép lập đoàn hệ và cách ly bệnh nhân đã xác định bị nhiễm, qua đó làm hạn chế sự lan tỏa rộng hơn của virus.[70]
Chẩn đoán
Tiền sử ca bệnh
Tiền sử ca bệnh #1
Một bé gái 6 tháng tuổi, tiền sử khỏe mạnh, tới khám vào giữa mùa đông với diễn biến bệnh 3 ngày bị sổ mũi, ho, và khó chịu. Một số trẻ em khác trong độ tuổi đi học trong gia đình cũng có các triệu chứng hô hấp. Đứa trẻ nhũ nhi có thân nhiệt 38,5°C (101,2°F), nhịp thở 70 lần/phút và mức bão hòa oxy 85% thở khí trời. Cháu bé có biểu hiện cánh mũi phập phồng, đầu gật gù, co rút hõm ức và cơ liên sườn. Sau khi nghe, nhận thấy tiếng khò khè ở hai bên và thở ra kéo dài. Trẻ đỡ khó thở hơn một chút sau khi hút nhầy mũi, và mức oxy hóa của cháu bé cải thiện với oxy ấm và ẩm thông qua gọng mũi, nhưng không có sự cải thiện nào bằng salbutamol khí dung.
Các bài trình bày khác
Bệnh viêm tiểu phế quản do RSV có thể gây suy hô hấp nặng. Trẻ nhũ nhi có nguy cơ cao, ví dụ như trẻ sinh non, bệnh phổi mạn tính, bệnh tim bẩm sinh phức tạp, hay suy giảm miễn dịch, dễ bị bệnh nặng hơn. Khó thở là một biến chứng thường gặp, đặc biệt là ở trẻ nhũ nhi nhỏ tuổi, và có thể là dấu hiệu của bệnh. Viêm phổi do RSV thường có biểu hiện sốt nhẹ, ho dai dẳng, và khó chịu.
Cách tiếp cận chẩn đoán từng bước
Nhìn chung, có thể xác định nghi ngờ nhiễm RSV dựa vào mùa, tiền sử, và qua khám lâm sàng. Tuy nhiên, có nhiều virus cũng gây ra các triệu chứng tương tự và cũng có liên quan đến viêm tiểu phế quản.[60] Mặc dù chẩn đoán xác định bệnh chỉ có thể khẳng định dựa vào các xét nghiệm, điều này lại thường không được khuyến cáo.[61]
Đặc điểm lâm sàng
Nhiễm RSV gần như luôn có triệu chứng. Mức độ nặng biến thiên tùy vào tuổi, tiền sử nhiễm trùng trước đó, và các bệnh đồng nhiễm của bệnh nhân.[30] [62] [63]
Các bác sĩ lâm sàng cần xác định liệu bệnh nhân có nguy cơ cao hình thành bệnh nặng hay không, bao gồm các yếu tố sau: tiền sử sinh non, < 6 tháng tuổi vào thời điểm bắt đầu mùa RSV, bệnh phổi mạn tính, bệnh tim bẩm sinh phức tạp, hoặc suy giảm miễn dịch. Những bệnh nhân này cần được theo dõi sát và nhập viện thường xuyên.[61]
Trẻ nhũ nhi thường có biểu hiện bệnh ở đường hô hấp trên, như sổ mũi và nghẹt mũi. Bác sĩ có thể chẩn đoán nghi nhiễm RSV khi, trong 2 đến 4 ngày sau đó, đường hô hấp dưới cũng bị bệnh và bệnh có biểu hiện thở nhanh, ho, thở khò khè, thở ra kéo dài, và thở gắng sức. Các triệu chứng thực thể của bệnh ở thể trung bình bao gồm thiếu oxy máu (bão hòa oxy <90%), thở nhanh, thở gắng sức (cánh mũi phập phồng, cơ liên sườn, đầu gật gù), kém ăn, và mất nước. Có nhiều hơn các ca bệnh nặng liên quan đến giảm oxy máu và suy hô hấp.[30] [64] [65] Bác sĩ cần hỏi về khó khăn khi ăn uống, tình trạng khó chịu, và các triệu chứng thực thể của viêm tai giữa, do cũng có thể có những tình trạng này. Ngừng thở có thể là biểu hiện duy nhất ở trẻ nhũ nhi nhỏ tuổi (<1 tháng tuổi) và có thể đủ mức độ nặng để dẫn đến tử vong.[66] Trẻ nhũ nhi nhỏ tuổi cũng có thể bị nhiễm khuẩn huyết.
Bệnh RSV ở trẻ lớn hơn và người lớn khỏe mạnh thường giới hạn ở đường hô hấp trên nhưng có thể tiến triển thành viêm khí-phế quản.[67] Các triệu chứng cơ năng bao gồm ngạt mũi, biểu hiện ở tai và các xoang, ho có đờm, và thở khò khè.[67]
Những người cao tuổi và bị suy giảm miễn dịch có nguy cơ mắc bệnh đường hô hấp dưới mức độ nặng.[68]
Xét nghiệm chẩn đoán
Học viện Nhi khoa Hoa Kỳ (AAP) khuyến cáo rằng chẩn đoán viêm tiểu phế quản nên được thiết lập dựa trên các dấu hiệu khi khai thác tiền sử và khám lâm sàng.[61] AAP cũng khuyến cáo rằng các bác sĩ lâm sàng không nên làm xét nghiệm thường quy hoặc chụp x-quang để chẩn đoán.[61] Tương tự như vậy, các xét nghiệm này ở người lớn cũng không được chứng tỏ là đem lại lợi ích.[20] [69] Tuy nhiên, việc xác nhận sự hiện diện của RSV có thể có ích trong việc phân lập và lập đoàn hệ các bệnh nhân với tình trạng nhiễm trùng đã biết.[70] Xét nghiệm virus nhanh đã được chứng tỏ là làm giảm số lần chụp x-quang ngực ở khoa tai nạn và cấp cứu, và các kết quả gợi ý rằng điều này có lợi đối với việc giảm sử dụng thuốc kháng sinh, mặc dù kết quả này không có ý nghĩa thống kê và cần phải có các thử nghiệm quy mô lớn tiếp theo trong lĩnh vực này.[71] Xét nghiệm nhanh dịch hút từ mũi họng để tìm RSV sẵn có thông qua phản ứng miễn dịch huỳnh quang (nhuộm kháng thể huỳnh quang trực tiếp), phản ứng chuỗi polymerase (PCR), và xét nghiệm hấp thụ miễn dịch liên kết enzym ELISA. Miễn dịch huỳnh quang có mức độ khả dụng cao hơn, và thường là lựa chọn đầu tiên để phát hiện RSV.[20] [72] Kết quả của một phân tích tổng hợp cho thấy rằng độ nhạy kém của các xét nghiệm phát hiện kháng nguyên nhanh đối với RSV ở người lớn có thể ngăn việc sử dụng các xét nghiệm này trong nhóm dân số này.[73]
Máy đo độ bão hòa oxy qua da
Máy đo độ bão hòa oxy qua da có sẵn ở hầu hết các cơ sở lâm sàng. Đó là một phương pháp nhanh và chính xác để đánh giá chứng thiếu oxy máu. Cần cân nhắc sử dụng phương pháp này ở bất kỳ trẻ nhũ nhi nào có các triệu chứng từ trung bình đến nặng.[61] Mức độ nặng của bệnh có các đặc điểm sau.
- Bệnh ở mức độ nhẹ: không bị thiếu oxy máu.
- Bệnh ở mức độ trung bình: thiếu oxy máu (bão hòa oxy <90%), thở nhanh, thở gắng sức (cánh mũi phập phồng, co rút cơ liên sườn, đầu gật gù), kém ăn, và mất nước.
- Bệnh ở mức độ nặng: thiếu oxy máu dai dẳng, suy hô hấp tiến triển, hay suy hô hấp mức độ nặng.
Các xét nghiệm khác
X-quang phổi có thể cho thấy xẹp phổi, phổi căng phồng quá mức, và dày thành phế quản.[74] [75] [76] Thâm nhiễm mô kẽ ít gặp hơn. Cần chụp x-quang ngực cho các bệnh nhân bị bệnh nặng, và những người không cải thiện so với kỳ vọng.[61] Tổng phân tích tế bào máu và xét nghiệm sinh hóa thường không hữu ích nhưng có thể cân nhắc nếu bị bệnh ở mức độ nặng. Chỉ định cấy máu nếu nghi ngờ nhiễm vi khuẩn.[Fig-2][Fig-3]
Các yếu tố nguy cơ
Thường gặp
Phơi nhiễm với RSV
- RSV có tỷ lệ tấn công là 98% đối với nhiễm lần đầu và 75% đối với các lần nhiễm sau đó.[30] Sự lan truyền virus cần phải có sự tiếp xúc gần gũi.
- Việc tới trung tâm giữ trẻ (nhà trẻ) và có nhiều anh chị em là các yếu tố nguy cơ làm bệnh RSV nặng hơn.[31]
Bệnh tim bẩm sinh phức tạp
- Trẻ nhũ nhi bị tổn thương tim bẩm sinh phức tạp có nguy cơ bị bệnh nặng tăng cao đáng kể. Tỷ lệ tử vong ở những trẻ nhũ nhi này từng lên tới 37%, nhưng với sự tiến bộ của các trị liệu hỗ trợ, tỷ lệ này đã giảm xuống còn từ 2,5% đến 3,5%[32] [33] [34]
Tiền sử sinh non
- Trẻ nhũ nhi sinh ra khi được <35 tuần có nguy cơ bị bệnh nặng tăng cao đáng kể. Điều này đặc biệt đúng với những người bị bệnh phổi mạn tính như loạn sản phế quản phổi.[35] [36]
Suy giảm miễn dịch
- Sự suy giảm miễn dịch có thể là do hóa trị liệu trị bệnh leukemia, dùng thuốc ức chế miễn dịch sau ghép tạng, virus gây suy giảm miễn dịch ở người HIV, hay hội chứng suy giảm miễn dịch kết hợp. Những bệnh nhân này có nguy cơ tăng cao bị bệnh nặng, bệnh kéo dài, và đào thải virus kéo dài.[37]
Bệnh phổi mạn tính
- Bệnh loạn sản phế quản phổi làm gia tăng nguy cơ bị bệnh nặng.[35] [36]
Trẻ nhũ nhi có nguy cơ cao và không có miễn dịch dự phòng gần đây chống lại RSV
- Trẻ nhũ nhi có nguy cơ cao bao gồm các cháu bé có tiền sử sinh non, bệnh phổi mạn tính, bệnh tim bẩm sinh phức tạp, và suy giảm miễn dịch.
Trẻ nhũ nhi <6 tháng tuổi
- Trẻ nhũ nhi < 6 tháng tuổi ở đầu mùa dịch RSV có nguy cơ gia tăng bị bệnh nặng và phải nhập viện.[36] [38]
Mùa đông
- Các đợt bùng phát theo mùa xảy ra trên toàn thế giới trong các tháng mùa đông. Tại Hoa Kỳ và trên khắp bắc bán cầu, dịch bệnh thường bắt đầu vào tháng Mười Một, với đỉnh điểm vào tháng Một hoặc tháng Hai. Số ca bệnh sau đó giảm và kết thúc vào Tháng Năm. Sự dao động theo vùng cũng xảy ra nhưng khả năng dự đoán được thấp hơn.[10] Ở nam bán cầu, các đợt bùng phát theo mùa xảy ra từ tháng Năm đến tháng Chín.
Người cao tuổi
- Nguy cơ mắc bệnh RSV nặng gia tăng ở bệnh nhân cao tuổi.[39]
Không thường gặp
Phơi nhiễm khói thuốc lá
- Phơi nhiễm khói thuốc lá là một yếu tố nguy cơ mắc bệnh RSV nặng hơn.[31]
Tiền sử gia đình bị hen suyễn
- Số liệu không nhất quán. Tiền sử gia đình bị hen suyễn có thể là một yếu tố nguy cơ với bệnh RSV nặng.[40]
Các yếu tố về tiền sử và thăm khám
Các yếu tố chẩn đoán chủ yếu
Có các yếu tố nguy cơ (thường gặp)
- Các yếu tố nguy cơ chính bao gồm phơi nhiễm RSV với, không có miễn dịch dự phòng chống RSV gần đây, tiền sử sinh non, trẻ nhũ nhi < 6 tháng, bệnh phổi mạn tính, bệnh tim bẩm sinh phức tạp, suy giảm miễn dịch, mùa đông, và tuổi cao.
Sổ mũi/nghẹt mũi (thường gặp)
- Các triệu chứng cơ năng của bệnh đường hô hấp trên thường gặp trong nhiễm RSV giai đoạn đầu.[61] [77]
Thở nhanh (thường gặp)
- Hay gặp ở trường hợp nhiễm trùng mức độ trung bình đến nặng.
Thở gắng sức (thường gặp)
- Đầu gật gù, khò khè (autopeep), cánh mũi phập phồng, và co rút cơ liên sườn phổ biến ở trường hợp nhiễm trùng mức độ trung bình đến nặng.[20] [61] [77]
Ho (thường gặp)
- Có thể khô hoặc ướt.[61]
Khò khè (thường gặp)
- Kết quả từ sự kết hợp giữa nút nhầy và hẹp đường thở do tình trạng viêm. Mức độ bệnh có thể biến thiên từ nhẹ đến nặng.
Ăn uống kém (thường gặp)
- Thường biểu hiện triệu chứng ở trẻ nhũ nhi.[20]
Chứng xanh tím (thường gặp)
- Thường gặp ở ca bệnh nặng.[20]
Ran (thường gặp)
- Bằng chứng nhiễm trùng đường hô hấp dưới có thể thấy ở 20% đến 30% trẻ nhũ nhi.[20]
Ngưng thở (không thường gặp)
- Một biến chứng đã được biết rõ ở trẻ nhũ nhi và có liên quan đến tử vong ở trẻ nhũ nhi.[66] Tỷ lệ mắc mới có thể lên tới 20% ở trẻ nhũ nhi < 6 tháng tuổi nhưng thường gặp nhất ở trẻ nhũ nhi < 1 tháng tuổi.[78] [79] [80] [66] [81] [82] Ngưng thở liên quan đến RSV thường tự khỏi và không tái phát ở các lần nhiễm sau đó.
Các yếu tố chẩn đoán khác
Sốt (thường gặp)
- Nhiễm RSV thường gây sốt, mặc dù hiếm khi sốt > 40°C (>103,9°F).[77]
Xét nghiệm chẩn đoán
Xét nghiệm thứ nhất cần yêu cầu
| Xét nghiệm | Kết quả |
| Đầu đo bão hòa oxy qua da
• Có sẵn ở hầu hết các cơ sở lâm sàng. Đó là một phương pháp nhanh và chính xác để đánh giá chứng thiếu oxy máu. Cần cân nhắc sử dụng phương pháp này ở bất kỳ trẻ nhũ nhi nào có các triệu chứng từ trung bình đến nặng.[61] Sử dụng đầu đo bão hòa oxy qua da thường quy không cho thấy cải thiện kết quả. |
Thiếu ô xy máu |
Các xét nghiệm khác cần cân nhắc
| Xét nghiệm | Kết quả |
| X quang ngực
• Cho thấy xẹp phổi, căng phồng phổi quá mức, dày thành phế quản, thâm nhiễm.[Fig-2][Fig-3] • Cần thực hiện ở các bệnh nhân bị bệnh nặng, và những người không cải thiện so với kì vọng.[61] [83] |
Xẹp phổi, căng phồng phổi quá mức, dày thành phế quản, thâm nhiễm |
| Nhuộm kháng thể huỳnh quang trực tiếp đối với các mẫu bệnh phẩm hô hấp (ví dụ dịch hút mũi họng)
• Miễn dịch huỳnh quang có mức độ khả dụng cao hơn và được sử dụng chủ yếu ở các bệnh viện công có quy mô nhỏ.[20] [72] • Có sẵn trên thị trường và tương đối dễ sử dụng. Độ nhạy > 90%.[84] |
Phát hiện kháng nguyên virus |
| Phản ứng chuỗi sao chép ngược (PCR) đối với mẫu bệnh phẩm từ đường hô hấp (ví dụ dịch hút từ mũi họng)
• Một phương pháp nhanh và nhạy để phát hiện RSV • Mức độ sẵn có ngày càng cao và hiện là phương pháp ưu tiên để xét nghiệm virus ở hầu hết các trung tâm y tế lớn.[83] [85] • Độ nhạy lâm sàng vượt trội so với các phương pháp chẩn đoán khác. |
Phát hiện axit ribonucleic của virus |
| Xét nghiệm hấp thụ miễn dịch liên kết với enzyme (ELISA) đối với bệnh phẩm đường hô hấp (ví dụ như dịch hút từ mũi họng)
• Sẵn có dành cho việc phát hiện RSV. Có độ nhạy lên đến 95%.[1] |
Phát hiện kháng nguyên virus |
| Nuôi cấy virus đối với mẫu bệnh phẩm hô hấp (ví dụ dịch hút mũi họng)
• Được coi là tiêu chuẩn vàng chẩn đoán RSV. • Thời gian quay vòng kéo dài từ 3 đến 7 ngày đối với cấy virus tiêu chuẩn, hay 1 đến 2 ngày đối với nuôi cấy vỏ. |
Sự phát triển của virus |
Chẩn đoán khác biệt
| Tình trạng | Các dấu hiệu/triệu chứng khác biệt | Các xét nghiệm khác biệt |
| Metapneumovirus ở người | • Gây ra hội chứng lâm sàng tương tự RSV Có thể không phân biệt được về mặt lâm sàng.[86] | • Phản ứng khuếch đại chuỗi gien (PCR ) dương tính với metapneumovirus. |
| Virus cúm | • Chiếm 1% đến 24% số ca viêm tiểu phế quản.[84] [87] [88] Có các biểu hiện gần giống với RSV. Thường sốt > 38,9°C (>101,9°F). Thường có biểu hiện viêm mũi. Tần suất viêm phổi và bội nhiễm vi khuẩn cao hơn so với RSV. | • Chụp x quang ngực (XQ ngực) có thể cho thấy thâm nhiễm.
• PCR: dương tính với virus cúm. • Test nhanh bằng xét nghiệm miễn dịch hoặc phát hiện neuraminidase của virus: dương tính với virus cúm. • Xét nghiệm hấp thụ miễn dịch liên kết với enzyme (ELISA) và nuôi cấy virus: dương tính với virus cúm. |
| Virus á cúm | • Chiếm 10% đến 30% số ca viêm tiểu phế quản. Á cúm loại III có biểu hiện gần giống với RSV. Sự hiện diện của viêm mũi có liên quan với nhiễm á cúm. Á cúm loại III thường xuất hiện vào cuối mùa xuân sau đỉnh lưu hành của RSV. | • Xét nghiệm ELISA và PCR: dương tính với virus á cúm.
• Nuôi cấy virus: dương tính với virus á cúm (xét nghiệm tiêu chuẩn). |
| Viêm phổi do vi khuẩn | • Nhiễm vi khuẩn không liên quan đến thở khò khè và nói chung gây ra sốt cao hơn so với RSV.[77]
• Sốt >40°C (>103,9°F). |
• XQ ngực: thâm nhiễm thùy
• Số lượng bạch cầu: tăng cao và có bạch cầu non gợi ý vi khuẩn đang hoạt động. |
| Nhiễm khuẩn huyết sơ sinh | • Thường có tiền sử ăn uống kém và thở gắng sức (tương tự như nhiễm RSV ở trẻ nhũ nhi), giảm ý thức, giảm lượng nước tiểu, ngưng thở, nhiệt độ không ổn định, sốc. | • Cấy bệnh phẩm: máu, nước tiểu và dịch não tủy có thể phát hiện vi sinh vật gây bệnh hoặc có thể bình thường.
• Khí máu động mạch có thể cho thấy nhiễm toan chuyển hoá và/ hoặc toan hô hấp, thiếu ô xy máu. |
| Enterovirus-D68 (EV-D68) | • Gây ra một hội chứng lâm sàng tương tự như cảm lạnh thông thường. Có thể gây bệnh hô hấp nặng với các triệu chứng thực thể và triệu chứng cơ năng của viêm phổi. Mặc dù EV-D68 chủ yếu gây ra bệnh hô hấp, bệnh toàn thân cũng xảy ra, đặc biệt là liên quan đến thần kinh. | • Nhiều phòng thí nghiệm lâm sàng sử dụng real-time RCR được thiết kế để phát hiện cả rhinovirus và enterovirus, nhưng các xét nghiệm này không phân biệt được hai loại virus này. Hầu hết các phòng thí nghiệm lâm sàng không thực hiện thường quy giải trình tự virus để xác định EV-D68. |
Các tiêu chí chẩn đoán
Mức độ nặng của bệnh[61]
Bệnh ở mức độ nhẹ
- Không bị thiếu oxy máu.
Bệnh ở mức độ trung bình
- Thiếu oxy máu (bão hòa oxy <90%), thở nhanh, thở gắng sức (cánh mũi phập phồng, co rút cơ liên sườn, đầu gật gù), kém ăn, và mất nước.
Bệnh ở mức độ nặng
- Thiếu oxy máu dai dẳng, suy hô hấp tiến triển, hay suy hô hấp nặng.
Điều trị
Cách tiếp cận điều trị từng bước
Các chiến lược điều trị chủ yếu là hỗ trợ, tập trung vào việc đảm bảo đủ oxy, thở máy, dinh dưỡng, và bù nước.
Trẻ nhũ nhi có nguy cơ cao bao gồm các cháu bé có tiền sử sinh non, < 6 tháng tuổi ở thời điểm bắt đầu mùa RSV, bệnh phổi mạn tính, bệnh tim bẩm sinh phức tạp, hoặc suy giảm miễn dịch. Những bệnh nhân này cần được theo dõi sát và thường xuyên phải nhập viện.
Các chiến lược điều trị tùy thuộc vào mức độ nặng của bệnh.
Nhập viện và chăm sóc hỗ trợ
Bệnh ở mức độ nhẹ
- Bệnh nhân không bị thiếu oxy máu.
- Đối với hầu hết trẻ nhũ nhi, bệnh RSV thường nhẹ và tự khỏi và do đó có thể được điều trị ngoại trú. Chăm sóc ngoại trú cần theo dõi thường xuyên để đảm bảo rằng tình trạng bệnh nhân không bị xấu đi. Trẻ nhũ nhi có nguy cơ cao (ví dụ tiền sử sinh non, < 6 tháng tuổi ở thời điểm bắt đầu mùa RSB, bệnh phổi mạn tính, bệnh tim bẩm sinh phức tạp, hoặc suy giảm miễn dịch) có thể cần được nhập viện.
- Điều trị chủ yếu là hỗ trợ và cung cấp đủ dinh dưỡng. Trẻ nhũ nhi cần phải thở bằng mũi, và tắc nghẽn mũi là một vấn đề thường gặp. Làm sạch mũi đơn giản với nhỏ nước muối và bầu hút có thể cải thiện đáng kể việc thở gắng sức.
- Liệu pháp điều trị triệu chứng thường là đủ đối với người lớn khỏe mạnh, do bệnh thường giới hạn ở đường hô hấp trên và tự khỏi.
Bệnh ở mức độ trung bình
- Các triệu chứng thực thể của bệnh ở mức độ trung bình ở trẻ nhũ nhi bao gồm thiếu oxy máu (bão hòa oxy <90%), thở nhanh, thở gắng sức (cánh mũi phập phồng, co rút cơ liên sườn, đầu gật gù), kém ăn, và mất nước.
- Những bệnh nhân này cần được nhập viện để chăm sóc và theo dõi thêm.[61] Nên điều trị thiếu oxy máu bằng oxy ấm, ẩm thông qua canuyl đặt vào mũi hoặc mặt nạ.
- Cần chú ý đặc biệt đến việc luôn cung cấp đủ nước và tái bổ sung dinh dưỡng đầy đủ. Trẻ nhũ nhi ăn kém hoặc thở khó khăn hay nhịp thở tăng cần được cho ăn qua ống thông mũi dạ dày hoặc ống thông mũi ruột non. Những người không thể dung nạp thức ăn qua ruột cần được điều trị dịch truyền tĩnh mạch.[61]
- Người cao tuổi, suy giảm miễn dịch, hay mắc đồng thời các bệnh khác có thể bị bệnh ở mức độ trung bình và cần được điều trị với chăm sóc hỗ trợ đồng thời giải quyết đợt cấp của các bệnh lý nền.
Bệnh ở mức độ nặng
- Trẻ nhũ nhi bị thiếu oxy máu dai dẳng, suy hô hấp tiến triển, hay suy hô hấp nặng cần được chuyển sang khu chăm sóc tích cực nhi khoa.
- Những bệnh nhân này thường cải thiện qua thông khí nhân tạo không xâm nhập như áp lực đường thở dương tính liên tục qua mũi nhưng cũng có thể cần đặt nội khí quản và thở máy xâm nhập. Các biện pháp này đã được sử dụng kể từ những năm 1960 và đã làm giảm đáng kể tỷ lệ tử vong liên quan đến RSV.[89]
- Nên điều trị thiếu oxy máu bằng oxy ấm, ẩm thông qua canuyl đặt vào mũi hoặc mặt nạ.
- Có thể bù dịch và cung cấp chất dinh dưỡng qua đường tiêu hóa hoặc ngoài đường tiêu hóa, tùy thuộc vào mức độ nặng của bệnh và các cân nhắc lâm sàng khác.
- Người cao tuổi, suy giảm miễn dịch, hoặc có bệnh đồng mắc có thể tiến triển thành bệnh ở mức độ nặng, cần đưa sang khu chăm sóc tích cực với hỗ trợ hô hấp và hỗ trợ dinh dưỡng và qua tĩnh mạch.
Điều trị bổ trợ
Thuốc giãn phế quản
- Không nên thường xuyên sử dụng thuốc giãn phế quản trong điều trị viêm tiểu phế quản.[61]
- Thuốc giãn phế quản có thể có ích cho những bệnh nhân bị hen suyễn, bệnh phổi tắc nghẽn mạn tính (COPD), hay bệnh ở mức độ nặng.
- Thuốc giãn phế quản có thể cải thiện tạm thời bão hoà oxy và việc thở gắng sức,[90] [91] [92] 2[C]Evidence nhưng không có bằng chứng làm giảm số ca nhập viện, thời gian nằm viện, hay thời gian áp dụng liệu pháp oxy.[83] [93] [94] [95] [96] [97] [98]
Khí dung nước muối ưu trương
- Nebulised hypertonic saline is of potential benefit in reducing symptoms of mild or moderate bronchiolitis in the hospital setting. Để đạt được hiệu quả, cần thời gian khí dung tương đối lâu, do vậy khí dung nước muối ưu trương không được khuyến cáo sử dụng tại khoa tai nạn và cấp cứu.[61] [99] [100]
- Ribavirin không được khuyến cáo sử dụng thường quy ở các bệnh nhân nhiễm RSV.[83]
- Ribavirin là một chất tương tự nucleoside tổng hợp với hoạt tính trong ống nghiệm tốt chống lại RSV. Tuy nhiên trên thực tế, không chắc chắn về lợi ích của thuốc.[20] 3[C]Evidence Một số yếu tố khiến việc sử dụng thuốc này trở nên phức tạp: chi phí tốn kém, phải được dùng sớm khi mới bị nhiễm trùng để có hiệu quả tốt nhất, và có thể gây nguy cơ cho người cho dùng thuốc, vì đó là một loại thuốc có tiềm năng gây quái thai.
- Hướng dẫn Sách Đỏ của Học viện Nhi khoa Hoa Kỳ khuyến nghị rằng, bất chấp những tranh cãi về lợi ích của thuốc, ribavirin có thể được cân nhắc sử dụng trong những bệnh cảnh nhất định liên quan đến viêm tiểu phế quản do RSV ở mức độ nặng, hoặc ở những người có nguy cơ bị bệnh nặng (ví dụ suy giảm miễn dịch và/hoặc bệnh lý tim phổi có rối loạn huyết động).[20]
- Ribavirin có thể được cân nhắc ở bệnh nhân bị suy giảm miễn dịch mắc bệnh đường hô hấp trên để ngăn ngừa bệnh lan xuống đường hô hấp dưới; tuy nhiên, dữ liệu về điều này còn hạn chế. Đối với bệnh nhân có nguy cơ cao, việc cho dùng sớm trong giai đoạn đầu của quá trình nhiễm trùng đường hô hấp trên đã chứng tỏ được lợi ích ngăn ngừa tiến triển thành nhiễm trùng ở đường hô hấp dưới.[101] [102]
- Ribavirin đã được sử dụng ở người lớn bị suy giảm miễn dịch (chủ yếu là những người được ghép tạng và bệnh nhân ung thư bị bệnh RSV mức độ nặng), mặc dù trên nhãn thuốc không ghi mục đích sử dụng này.[103] [101] Việc sử dụng thuốc sớm ở bệnh nhân được ghép tủy đã giảm tỷ lệ mắc bệnh và tỷ lệ tử vong trong nhóm bệnh nhân này.[102]
- Người lớn cao tuổi hoặc có bệnh đồng mắc bị nhiễm RSV cũng có thể hưởng lợi từ thuốc này.
Kháng sinh
- The routine administration of empirical antibiotic therapy to infants with RSV bronchiolitis is not recommended, given that the risk of concomitant bacterial infection is very low (0.2%).
- Cần cho bệnh nhân đã được xác định hoặc nghi ngờ cao nhiễm vi khuẩn dùng thuốc kháng sinh.[61]
- Đối với trẻ nhũ nhi bị viêm tiểu phế quản do RSV mức độ nặng cần đặt nội khí quản, nguy cơ bị viêm phổi do vi khuẩn cao hơn đáng kể (26%). Những trẻ nhũ nhi này có thể hưởng lợi từ việc bắt đầu cho dùng thuốc kháng sinh trong khi chờ kết quả nuôi cấy.[61] [83] [104] [105]
Corticosteroid
- Corticosteroid không có hiệu quả trong điều trị thường quy nhiễm RSV.[61] [106] [107] Hướng dẫn của Học viện Nhi khoa Hoa Kỳ và hướng dẫn của Scottish Intercollegiate Guidelines Network (Mạng lưới Hướng dẫn
- Liên Trường Đại học Scotland – SIGN) về điều trị viêm tiểu phế quản khuyến cáo không nên sử dụng thường quy corticosteroid cho bệnh lý này.[61]
- Corticosteroid có thể có lợi đối với các bệnh nhân dị ứng, hen suyễn, hay bệnh phổi mạn tính.
Immunoglobulin đường tĩnh mạch (IVIG)
- Có thể cân nhắc dùng IVIG cho bệnh nhân suy giảm miễn dịch bị nhiễm virus lan tỏa. Việc chỉ sử dụng đơn độc liệu pháp điều trị IVIG hay RSV-IG không rút ngắn đáng kể thời gian nằm viện đối với trẻ nhũ nhi bị viêm tiểu phế quản do RSV và/hoặc viêm phổi.[108] [109] Tuy nhiên IVIG đã được sử dụng như biện pháp cuối cùng ở những bệnh nhân bị nặng, tình trạng xấu dần, mắc lan tỏa nhiều loại virus (ví dụ varicella, cytomegalovirus).
- Việc sử dụng IVIG kết hợp với ribavirin hít để điều trị bệnh nhân mắc bệnh RSV đã được nghiên cứu.[110] [111] Một phân tích tổng hợp cho biết những người được điều trị kết hợp (ribavirin dạng sol khí kết hợp với IVIG hoặc palivizumab) chậm tiến triển thành nhiễm đường hô hấp dưới hơn so với những người chỉ được điều trị ribavirin dạng sol khí.[101]
Các liệu pháp kém hiệu quả hơn hoặc không hiệu quả
- Liệu pháp vật lý trị liệu lồng ngực không cho thấy cải thiện các kết quả, và cần hạn chế việc sử dụng liệu pháp này.[61] [86]
- Liệu pháp dùng thuốc long đờm với DNase người tái tổ hợp dạng khí dung chưa cho thấy hiệu quả.[112] [113] [114] [115]
- Liệu pháp surfactant dành cho bệnh nhân đặt nội khí quản chưa cho thấy hiệu quả.
- Các hỗn hợp Heli-oxy (heliox) cũng chưa cho thấy lợi ích liên quan đến tỷ lệ đặt nội khí quản, tỷ lệ xuất viện từ khoa tai nạn và cấp cứu, hay thời gian điều trị suy hô hấp trong điều trị viêm tiểu phế quản ở trẻ nhũ nhi.[116]
- Montelukast vẫn chưa được chứng tỏ là có hiệu quả trong điều trị nhiễm RSV, hay trong việc giảm thở khò khè sau viêm tiểu phế quản.[117]
Biện pháp dự phòng miễn dịch
Biện pháp dự phòng miễn dịch với palivizumab sẵn có dành cho trẻ nhũ nhi có nguy cơ cao, vì việc sử dụng trong các nhóm nguy cơ cao có thể giảm số ca nhập viện khoảng 45% đến 55%.[50] [51] [52] [53] [54] [55] [56] [118] [119] 1[B]Evidence Biện pháp dự phòng với Palivizumab ở các nhóm bệnh nhân này cũng có liên quan đến việc giảm tỷ lệ tử vong do mọi nguyên nhân trong mùa RSV.[54] Một bài tổng quan hệ thống của Cochrane không tìm ra bất kỳ khác biệt có ý nghĩa lâm sàng nào về các kết quả ở trẻ em mắc xơ nang 6 tháng sau điều trị với palivizumab hay giả dược.[120]
Dự phòng bệnh thường sử dụng palivizumab hàng tháng trong mùa RSV với tổng số 5 liều. Thuốc này không được chỉ định dùng để điều trị nhiễm RSV hoạt động[121] Trong năm 2014, Viện Hàn lâm Nhi khoa Hoa Kỳ đã cập nhật những khuyến cáo của mình đối với việc sử dụng palivizumab trong các nhóm sau đây như sau:[48]
- Trẻ nhũ nhi sinh trước 29 tuần thai dưới 12 tháng tuổi vào đầu mùa RSV.
- Trẻ nhũ nhi bị bệnh tim có thay đổi huyết động đáng kể trong năm đầu tiên của cuộc đời.
- Trẻ nhũ nhi bị bệnh phổi mạn tính do sinh non dưới 12 tháng tuổi vào đầu mùa RSV. Những trẻ nhũ nhi này được xác định sinh trước 32 tuần thai với nhu cầu liệu pháp oxy >21% trong ít nhất 28 ngày sau sinh.
- Trẻ nhũ nhi bị bệnh phổi mạn tính do sinh non có độ tuổi từ 12 đến 24 tháng và tiếp tục cần oxy bổ sung, corticosteroid, hay thuốc lợi tiểu trong vòng 6 tháng kể từ đầu mùa RSV.
- Trẻ nhũ nhi bị bệnh phổi hay thần kinh cơ đáng kể làm ảnh hưởng đến việc thanh thải chất bài tiết đường hô hấp trên và có độ tuổi dưới 12 tháng khi bắt đầu mùa RSV.
- Trẻ nhũ nhi dưới 24 tháng tuổi là người sẽ bị suy giảm miễn dịch nặng trong mùa RSV. Palivizumab được chỉ định tiêm bắp hàng tháng trong mùa RSV.[20] [48] [49]
Không có vắc-xin RSV nào được cấp phép để sử dụng cho người lớn.
Tổng quan về các chi tiết điều trị
Tham khảo cơ sở dữ liệu dược địa phương của quý vị để biết thông tin toàn diện về thuốc, bao gồm các chống chỉ định, tương tác giữa các loại thuốc, và liều dùng thay thế.
| Cấp tính (tóm tắt) | ||
| Nhóm bệnh nhân | Tx line | Điều trị |
| Bệnh nhẹ hoặc tự khỏi | 1 | Chăm sóc hỗ trợ ngoại trú hoặc nội trú |
| Bổ sung | Nước muối ưu trương khí dung | |
|
Thêm | Điều trị bệnh nền ± corticosteroid |
|
Bổ sung | Thuốc giãn phế quản |
|
Bổ sung | Ribavirin dạng hít ± immunoglobulin đường tĩnh mạch (IViG) |
| Bệnh ở mức độ trung bình | 1 | Chăm sóc hỗ trợ bệnh nhân nội trú |
| Bổ sung | Nước muối ưu trương khí dung | |
|
Thêm | Điều trị bệnh nền ± corticosteroid |
|
Bổ sung | Thuốc giãn phế quản |
|
Bổ sung | Ribavirin dạng hít ± immunoglobulin đường tĩnh mạch (IViG) |
| Bệnh ở mức độ nặng | 1 | Chăm sóc hỗ trợ trong đơn vị chăm sóc tích cực (icu) |
| Bổ sung | Immunoglobulin qua đường tĩnh mạch (IVIG) | |
| Bổ sung | Ribavirin dạng hít | |
|
Thêm | Điều trị bệnh nền ± corticosteroid |
|
Bổ sung | Thuốc giãn phế quản |
|
Bổ sung | Thuốc kháng sinh |
| Tiếp diễn (tóm tắt) | ||
|
1 | Liều dùng palivizumab hàng tháng |
|
1 | Liều dùng palivizumab hàng tháng |
|
1 | Liều dùng palivizumab hàng tháng |
|
1 | Lều dùng palivizumab hàng tháng |
|
1 | Liều dùng palivizumab hàng tháng |
Các lựa chọn điều trị
| Cấp tính | ||
| Nhóm bệnh nhân | Tx line | Điều trị |
| Bệnh nhẹ hoặc tự khỏi | 1 | Chăm sóc hỗ trợ ngoại trú hoặc nội trú |
| » Đối với hầu hết trẻ nhũ nhi mắc RSV thường nhẹ và tự khỏi và có thể được điều trị ngoại trú. Chăm sóc ngoại trú cần theo dõi thường xuyên để đảm bảo rằng tình trạng bệnh nhân không bị xấu đi. » Điều trị chủ yếu là hỗ trợ bất kể môi trường điều trị, tập trung vào cải thiện oxy, thở máy và cung cấp đủ dinh dưỡng. Trẻ nhũ nhi chỉ có thể thở bằng mũi, và tắc nghẽn mũi là một vấn đề thường gặp. Làm sạch mũi đơn giản bằng nước muối nhỏ giọt và bầu hút có thể cải thiện đáng kể việc thở gắng sức. » Trẻ nhũ nhi có nguy cơ cao bao gồm các cháu bé có tiền sử sinh non, dưới 6 tháng tuổi khi bắt đầu mùa RSV, bệnh phổi mạn tính, bệnh tim bẩm sinh phức tạp, hoặc suy giảm miễn dịch. Những bệnh nhân này cần được theo dõi sát và thường phải nhập viện. » Liệu pháp điều trị triệu chứng thường là đủ đối với người lớn khỏe mạnh, do bệnh thường giới hạn ở đường hô hấp trên và tự khỏi. » Đối với người lớn bị bệnh RSV mức độ nhẹ, liệu pháp điều trị chủ yếu là hỗ trợ và với mục tiêu cải thiện triệu chứng. |
||
| Bổ sung | Nước muối ưu trương khí dung | |
| » Nước muối ưu trương khí dung có tiềm năng đem lại lợi ích trong việc giảm triệu chứng viêm tiểu phế quản mức độ nhẹ hoặc trung bình trong bệnh viện. Với quãng thời gian sử dụng tương đối dài cần thiết để đạt được hiệu quả cải thiện, nước muối ưu trương khí dung không được khuyến cáo sử dụng tại khoa tai nạn và cấp cứu.[61] [99] [100] | ||
|
Thêm | Điều trị bệnh nền ± corticosteroid |
| » Cần tiếp tục điều trị thường xuyên bệnh hen suyễn hay bệnh phổi tắc nghẽn mạn tính (COPD) đồng mắc theo cách tiếp cận trị liệu theo từng bước. » Corticosteroid không có hiệu quả trong điều trị thường quy nhiễm RSV.4[C]Evidence Hướng dẫn của Học viện Nhi khoa Hoa Kỳ và hướng dẫn của Scottish Intercollegiate Guidelines Network (Mạng lưới Hướng dẫn Liên Trường Đại học Scotland – SIGN) về điều trị viêm tiểu phế quản khuyến cáo không nên sử dụng thường quy corticosteroid cho bệnh lý này.[61]» Corticosteroid có thể có lợi đối với các bệnh nhân dị ứng, hen suyễn, hay bệnh phổi mạn tính. » Đối với người lớn bị bệnh RSV mức độ nhẹ, đặc biệt là đối với bệnh nhân bị bệnh phổi tắc nghẽn mạn tính hoặc hen suyễn, corticosteroid đã được thử nghiệm, nhưng chưa có nghiên cứu nào cho thấy lợi ích của thuốc này. Các lựa chọn sơ cấp » Prednisolone: trẻ em: 1-2 mg/kg/ngày (tối đa 60 mg/ngày) uống chia 2 lần trong 3-10 ngày; người lớn: 40-80 mg/ngày uống chia 1-2 lần trong 3-10 ngày |
||
|
Bổ sung | Thuốc giãn phế quản |
| » Không nên thường xuyên sử dụng thuốc giãn phế quản trong điều trị viêm tiểu phế quản.[61]
» Thuốc giãn phế quản có thể có ích cho những bệnh nhân bị hen suyễn, COPD, hoặc bệnh ở mức độ nặng. » Thuốc giãn phế quản có thể cải thiện tạm thời bão hoà oxy và việc thở gắng sức,[90] [91] [92] 2[C]Evidence nhưng không có bằng chứng làm giảm số ca nhập viện, thời gian nằm viện, hay thời gian áp dụng liệu pháp oxy.[83] [93] [94] [95] [96] [97] [98] |
||
|
Bổ sung | Ribavirin dạng hít ± immunoglobulin đường tĩnh mạch (IViG) |
| » Ribavirin không được khuyến cáo sử dụng thường quy ở các bệnh nhân nhiễm RSV.[83]
» Thuốc này là một chất tương tự nucleoside tổng hợp với hoạt tính trong ống nghiệm tốt chống lại RSV. Tuy nhiên trên thực tế, lợi ích của thuốc là không chắc chắn.[20] 3[C]Evidence Một số yếu tố khiến việc sử dụng thuốc này trở nên phức tạp: chi phí tốn kém, phải được dùng sớm khi mới bị nhiễm trùng để có hiệu quả tốt nhất, và có thể gây nguy cơ cho người cho dùng thuốc, vì đó là một loại thuốc có tiềm năng gây quái thai. » Hướng dẫn Sách Đỏ của Học viện Nhi khoa Hoa Kỳ khuyến nghị rằng, bất chấp những tranh cãi về lợi ích của thuốc, ribavirin có thể được cân nhắc sử dụng trong những tình huống nhất định liên quan đến viêm tiểu phế quản do RSV ở mức độ nặng hoặc ở những người có nguy cơ bị bệnh mức độ nặng (ví dụ suy giảm miễn dịch và/hoặc bệnh lý tim phổi thay đổi huyết động đáng kể).[20] » Ribavirin có thể được cân nhắc ở bệnh nhân bị suy giảm miễn dịch mắc bệnh đường hô hấp trên để ngăn ngừa bệnh lan xuống đường hô hấp dưới; tuy nhiên, dữ liệu về điều này còn hạn chế. Đối với bệnh nhân có nguy cơ cao, việc cho dùng sớm trong giai đoạn đầu của quá trình nhiễm trùng đường hô hấp trên đã chứng tỏ được lợi ích ngăn ngừa tiến triển thành nhiễm trùng ở đường hô hấp dưới.[101] » Ribavirin đã được sử dụng ở người lớn bị suy giảm miễn dịch (chủ yếu là những người được ghép tạng và bệnh nhân ung thư bị bệnh RSV mức độ nặng), mặc dù trên nhãn thuốc không ghi mục đích sử dụng này.[103] [101] Việc sử dụng thuốc sớm ở bệnh nhân được ghép tủy đã giảm tỷ lệ mắc bệnh và tỷ lệ tử vong trong nhóm bệnh nhân này.[102] » Người cao tuổi nhiễm RSV, suy giảm miễn dịch, hoặc cũng bị mắc đồng thời các bệnh khác cũng có thể hưởng lợi từ thuốc này. » Có thể bổ sung IVIG kết hợp với ribavirin dạng hít đối với bệnh nhân bị suy giảm miễn dịch có nguy cơ cao tiến triển thành bệnh đường hô hấp dưới mức độ nặng.[101] [102] Các lựa chọn sơ cấp » ribavirin: tham khảo ý kiến chuyên gia để có hướng dẫn về liều dùng HOẶC Các lựa chọn thứ cấp » ribavirin: tham khảo ý kiến chuyên gia để có hướng dẫn về liều dùng -và- » globulin miễn dịch thông thường ở người: tham khảo ý kiến chuyên gia để có hướng dẫn về liều dùng |
||
| Bệnh ở mức độ trung bình | 1 | Chăm sóc hỗ trợ bệnh nhân nội trú |
| » Các triệu chứng thực thể của bệnh ở mức độ trung bình ở trẻ nhũ nhi bao gồm thiếu oxy máu (bão hoà oxy <90%), thở nhanh, thở gắng sức (cánh mũi phập phồng, co rút cơ liên sườn, đầu gật gù), kém ăn, và mất nước. Bệnh nhân cần được nhập viện để chăm sóc và theo dõi thêm.[61] Nên điều trị thiếu oxy máu bằng oxy ấm, ẩm thông qua gọng mũi hoặc qua mask. Cần chú ý đặc biệt với việc hỗ trợ dinh dưỡng và dịch truyền qua tĩnh mạch. Trẻ nhũ nhi ăn kém hoặc thở gắng sức hay nhịp thở tăng cần được cho nuôi ăn qua ống thông mũi dạ dày hoặc ống thông mũi ruột non. Những người không thể dung nạp thức ăn qua ruột cần được nuôi bằng dịch truyền tĩnh mạch.[61]
» Trẻ nhũ nhi có nguy cơ cao bao gồm các cháu bé có tiền sử sinh non, dưới 6 tháng tuổi khi bắt đầu mùa RSV, bệnh phổi mạn tính, bệnh tim bẩm sinh phức tạp, hoặc suy giảm miễn dịch. Những bệnh nhân này cần được theo dõi sát và thường phải nhập viện. |
||
| Bổ sung | Nước muối ưu trương khí dung | |
| » Nước muối ưu trương khí dung có tiềm năng đem lại lợi ích trong việc giảm triệu chứng viêm tiểu phế quản mức độ nhẹ hoặc trung bình trong bệnh viện. Với quãng thời gian sử dụng tương đối dài cần thiết để đạt được hiệu quả cải thiện, nước muối ưu trương khí dung không được khuyến cáo sử dụng tại khoa tai nạn và cấp cứu.[61] [99] [100] | ||
|
Thêm | Điều trị bệnh nền ± corticosteroid |
| » Cần tiếp tục điều trị thường quy bệnh hen suyễn hay bệnh phổi tắc nghẽn mạn tính đồng mắc theo cách tiếp cận trị liệu theo từng bước. » Corticosteroid không có hiệu quả trong điều trị thường quy nhiễm RSV.4[C]Evidence » Hướng dẫn của Học viện Nhi khoa Hoa Kỳ và hướng dẫn của Scottish Intercollegiate Guidelines Network (Mạng lưới Hướng dẫn Liên Trường Đại học Scotland – SIGN) về điều trị viêm tiểu phế quản khuyến cáo không nên sử dụng thường quy corticosteroid cho bệnh lý này.[61] » Corticosteroid có thể có lợi đối với các bệnh nhân dị ứng, hen suyễn, hay bệnh phổi mạn tính. » Ở người cao tuổi, suy giảm miễn dịch, hoặc có bệnh đồng mắc, corticosteroid có thể có ích lợi. Các lựa chọn sơ cấp » Prednisolone: trẻ em: 1-2 mg/kg/ngày (tối đa 60 mg/ngày) uống chia 2 lần trong 3-10 ngày; người lớn: 40-80 mg/ngày uống chia 1-2 lần trong 3-10 ngày |
||
|
Bổ sung | Thuốc giãn phế quản |
| » Không nên thường xuyên sử dụng thuốc giãn phế quản trong điều trị viêm tiểu phế quản.[61] » Thuốc giãn phế quản có thể có ích cho những bệnh nhân bị hen suyễn, COPD, hoặc bệnh ở mức độ nặng» Thuốc giãn phế quản có thể cải thiện tạm thời bão hoà oxy và việc thở gắng sức,[90] [91] [92] 2[C]Evidence nhưng không có bằng chứng làm giảm số ca nhập viện, thời gian nằm viện, hay thời gian áp dụng liệu pháp oxy.[83] [93] [94] [95] [96] [97] [98] | ||
|
Bổ sung | Ribavirin dạng hít ± immunoglobulin đường tĩnh mạch (IViG) |
| » Ribavirin không được khuyến cáo sử dụng thường quy ở các bệnh nhân nhiễm RSV.[83]
» Thuốc này là một chất tương tự nucleoside tổng hợp với hoạt tính trong ống nghiệm tốt chống lại RSV. Tuy nhiên trên thực tế, lợi ích của thuốc là không chắc chắn.[20] 3[C]Evidence Một số yếu tố khiến việc sử dụng thuốc này trở nên phức tạp: chi phí tốn kém, phải được dùng sớm khi mới bị nhiễm trùng để có hiệu quả tốt nhất, và có thể gây nguy cơ cho người cho dùng thuốc, vì đó là một loại thuốc có tiềm năng gây quái thai. » Hướng dẫn Sách Đỏ của Học viện Nhi khoa Hoa Kỳ khuyến nghị rằng, bất chấp những tranh cãi về lợi ích của thuốc, ribavirin có thể được cân nhắc sử dụng trong những tình huống nhất định liên quan đến viêm tiểu phế quản do RSV ở mức độ nặng hoặc ở những người có nguy cơ bị bệnh mức độ nặng (ví dụ suy giảm miễn dịch và/hoặc bệnh lý tim phổi thay đổi huyết động đáng kể).[20] » Ribavirin có thể được cân nhắc ở bệnh nhân bị suy giảm miễn dịch mắc bệnh đường hô hấp trên để ngăn ngừa bệnh lan xuống đường hô hấp dưới; tuy nhiên, dữ liệu về điều này còn hạn chế. Đối với bệnh nhân có nguy cơ cao, việc cho dùng sớm trong giai đoạn đầu của quá trình nhiễm trùng đường hô hấp trên đã chứng tỏ được lợi ích ngăn ngừa tiến triển thành nhiễm trùng ở đường hô hấp dưới.[101] » Ribavirin đã được sử dụng ở người lớn bị suy giảm miễn dịch (chủ yếu là những người được ghép tạng và bệnh nhân ung thư bị bệnh RSV mức độ nặng), mặc dù trên nhãn thuốc không ghi mục đích sử dụng này.[103] [101] Việc sử dụng thuốc sớm ở bệnh nhân được ghép tủy đã giảm tỷ lệ mắc bệnh và tỷ lệ tử vong trong nhóm bệnh nhân này.[102] » Người cao tuổi nhiễm RSV, suy giảm miễn dịch, hoặc cũng bị mắc đồng thời các bệnh khác cũng có thể hưởng lợi từ thuốc này. » Có thể bổ sung IVIG kết hợp với ribavirin dạng hít đối với bệnh nhân bị suy giảm miễn dịch có nguy cơ cao tiến triển thành bệnh đường hô hấp dưới mức độ nặng.[101] [102]Các lựa chọn sơ cấp » ribavirin: tham khảo ý kiến chuyên gia để có hướng dẫn về liều dùng HOẶC Các lựa chọn thứ cấp » ribavirin: tham khảo ý kiến chuyên gia để có hướng dẫn về liều dùng -và- » globulin miễn dịch thông thường ở người: tham khảo ý kiến chuyên gia để có hướng dẫn về liều dùng |
||
| Bệnh ở mức độ nặng | 1 | Chăm sóc hỗ trợ trong đơn vị chăm sóc tích cực (icu) |
| » Trẻ nhũ nhi bị thiếu oxy máu dai dẳng, suy hô hấp tiến triển, hoặc suy hô hấp mức độ nặng cần được chuyển sang đơn vị chăm sóc tích cực nhi khoa. Bệnh nhân thường cải thiện với biện pháp thở máy không xâm nhập ví dụ như máy áp lực đường thở dương tính liên tục qua mũi (CPAP) nhưng cũng có thể cần phải đặt nội khí quản thở máy xâm nhập. Các biện pháp này đã được sử dụng kể từ những năm 1960 và đã làm giảm đáng kể tỷ lệ tử vong liên quan đến RSV.[89]
» Nên điều trị thiếu oxy máu bằng oxy ấm, ẩm thông qua canuyl đặt vào mũi hoặc mặt nạ. » Có thể bù dịch và cung cấp chất dinh dưỡng qua đường tiêu hóa hoặc ngoài đường tiêu hóa, tùy thuộc vào mức độ nặng của bệnh và các cân nhắc lâm sàng khác. » Trẻ nhũ nhi có nguy cơ cao bao gồm các cháu bé có tiền sử sinh non, dưới 6 tháng tuổi khi bắt đầu mùa RSV, bệnh phổi mạn tính, bệnh tim bẩm sinh phức tạp, hoặc suy giảm miễn dịch. » Người cao tuổi, suy giảm miễn dịch, hoặc có bệnh đồng mắc có thể tiến triển thành bệnh ở mức độ nặng cần nhập ICU với hỗ trợ hô hấp, hỗ trợ dinh dưỡng và qua đường tĩnh mạch. |
||
| Bổ sung | Immunoglobulin qua đường tĩnh mạch (IVIG) | |
| » Có thể cân nhắc dùng IVIG cho bệnh nhân suy giảm miễn dịch nhiễm virus lan tỏa. » Việc chỉ sử dụng đơn độc liệu pháp điều trị IVIG hay RSV-IG không rút ngắn đáng kể thời gian nằm viện đối với trẻ nhũ nhi bị viêm tiểu phế quản do RSV và/hoặc viêm phổi.[108] [109] Tuy nhiên IVIG đã được sử dụng như biện pháp cuối cùng ở những bệnh nhân bị nặng, tình trạng xấu dần, mắc lan tỏa nhiều loại virus (ví dụ varicella, cytomegalovirus). » Việc sử dụng IVIG kết hợp với ribavirin hít để điều trị bệnh nhân mắc bệnh RSV đã được nghiên cứu.[110] [111] Một phân tích tổng hợp cho biết những người được điều trị kết hợp (ribavirin dạng sol khí kết hợp với IVIG hoặc palivizumab) chậm tiến triển thành nhiễm đường hô hấp dưới hơn so với những người chỉ được điều trị ribavirin dạng sol khí.[101] Các lựa chọn sơ cấp » globulin miễn dịch thông thường ở người: tham khảo ý kiến chuyên gia để có hướng dẫn về liều dùng |
||
| Bổ sung | Ribavirin dạng hít | |
| » Ribavirin không được khuyến cáo sử dụng thường quy ở các bệnh nhân nhiễm RSV.[83]
» Thuốc này là một chất tương tự nucleoside tổng hợp với hoạt tính trong ống nghiệm tốt chống lại RSV. Tuy nhiên trên thực tế, lợi ích của thuốc là không chắc chắn.[20] 3[C]Evidence Một số yếu tố khiến việc sử dụng thuốc này trở nên phức tạp: chi phí tốn kém, phải được dùng sớm khi mới bị nhiễm trùng để có hiệu quả tốt nhất, và có thể gây nguy cơ cho người cho dùng thuốc, vì đó là một loại thuốc có tiềm năng gây quái thai. » Hướng dẫn Sách Đỏ của Học viện Nhi khoa Hoa Kỳ khuyến nghị rằng, bất chấp những tranh cãi về lợi ích của thuốc, ribavirin có thể được cân nhắc sử dụng trong những tình huống nhất định liên quan đến viêm tiểu phế quản do RSV ở mức độ nặng hoặc ở những người có nguy cơ bị bệnh mức độ nặng (ví dụ suy giảm miễn dịch và/hoặc bệnh lý tim phổi thay đổi huyết động đáng kể).[20] » Ribavirin có thể được cân nhắc ở bệnh nhân bị suy giảm miễn dịch mắc bệnh đường hô hấp trên để ngăn ngừa bệnh lan xuống đường hô hấp dưới; tuy nhiên, dữ liệu về điều này còn hạn chế. Đối với bệnh nhân có nguy cơ cao, việc cho dùng sớm trong giai đoạn đầu của quá trình nhiễm trùng đường hô hấp trên đã chứng tỏ được lợi ích ngăn ngừa tiến triển thành nhiễm trùng ở đường hô hấp dưới.[101] » Ribavirin đã được sử dụng ở người lớn bị suy giảm miễn dịch (chủ yếu là những người được ghép tạng và bệnh nhân ung thư bị bệnh RSV mức độ nặng), mặc dù trên nhãn thuốc không ghi mục đích sử dụng này.[103] [101] Việc sử dụng thuốc sớm ở bệnh nhân được ghép tủy đã giảm tỷ lệ mắc bệnh và tỷ lệ tử vong trong nhóm bệnh nhân này.[102] » Người cao tuổi nhiễm RSV, suy giảm miễn dịch, hoặc cũng bị mắc đồng thời các bệnh khác cũng có thể hưởng lợi từ thuốc này. » Việc sử dụng ribavirin dạng hít kết hợp với IVIG để điều trị bệnh nhân nhiễm RSV đã được nghiên cứu.[110] [111] Một phân tích tổng hợp cho biết những người được điều trị kết hợp (ribavirin dạng sol khí kết hợp với IVIG hoặc palivizumab) chậm tiến triển thành nhiễm đường hô hấp dưới hơn so với những người chỉ được điều trị ribavirin dạng sol khí.[101] Các lựa chọn sơ cấp » ribavirin: tham khảo ý kiến chuyên gia để có hướng dẫn về liều dùng |
||
|
Thêm | Điều trị bệnh nền ± corticosteroid |
| » Cần tiếp tục điều trị thường quy bệnh hen suyễn hay bệnh phổi tắc nghẽn mạn tính đồng mắc theo cách tiếp cận trị liệu theo từng bước. » Corticosteroid không có hiệu quả trong điều trị thường quy nhiễm RSV.4[C]Evidence » Hướng dẫn của Học viện Nhi khoa Hoa Kỳ và hướng dẫn của Scottish Intercollegiate Guidelines Network (Mạng lưới Hướng dẫn Liên Trường Đại học Scotland – SIGN) về điều trị viêm tiểu phế quản khuyến cáo không nên sử dụng thường quy corticosteroid cho bệnh lý này.[61] » Corticosteroid có thể có lợi đối với các bệnh nhân dị ứng, hen suyễn, hay bệnh phổi mạn tính. » Ở người cao tuổi, suy giảm miễn dịch, hoặc có bệnh đồng mắc, corticosteroid có thể có ích lợi. Các lựa chọn sơ cấp » Prednisolone: trẻ em: 1-2 mg/kg/ngày (tối đa 60 mg/ngày) uống chia 2 lần trong 3-10 ngày; người lớn: 40-80 mg/ngày uống chia 1-2 lần trong 3-10 ngày |
||
|
Bổ sung | Thuốc giãn phế quản |
| » Không nên thường xuyên sử dụng thuốc giãn phế quản trong điều trị viêm tiểu phế quản.[61]
» Thuốc giãn phế quản có thể có ích cho những bệnh nhân bị hen suyễn, COPD, hoặc bệnh ở mức độ nặng.» Thuốc giãn phế quản có thể cải thiện tạm thời bão hoà oxy và việc thở gắng sức,[90] [91] [92] 2[C]Evidence nhưng không có bằng chứng làm giảm số ca nhập viện, thời gian nằm viện, hay thời gian áp dụng liệu pháp oxy.[83] [93] [94] [95] [96] [97] [98] |
||
|
Bổ sung | Thuốc kháng sinh |
| » Không khuyến cáo sử dụng thường quy điều trị kháng sinh theo kinh nghiệm đối với trẻ nhũ nhi bị viêm tiểu phế quản do RSV, do nguy cơ nhiễm vi khuẩn ở mức độ rất thấp (0,2%). Tuy nhiên, đối với trẻ nhũ nhi bị viêm tiểu phế quản do RSV mức độ nặng cần đặt nội khí quản, nguy cơ bị viêm phổi do vi khuẩn cao hơn đáng kể (26%). Những trẻ nhũ nhi này có thể hưởng lợi từ việc bắt đầu cho dùng thuốc kháng sinh trong khi chờ kết quả nuôi cấy.[61] [83] [104] [105] | ||
| Tiếp diễn | ||
|
1 | Liều dùng palivizumab hàng tháng |
| » Cập nhật năm 2014 của Học viện Nhi khoa Hoa Kỳ về những chỉ định sử dụng palivizumab đã chỉ rõ các nhóm trẻ nhũ nhi cụ thể được coi là có nguy cơ cao.[20] [48] Việc sử dụng biện pháp này trong các nhóm nguy cơ cao có thể giảm mức nhập viện 45% đến 55%.[50] [51] [52] [53] [54] [55] [56] [118] 1[B]Evidence » Biện pháp dự phòng với Palivizumab ở các nhóm bệnh nhân này cũng có liên quan đến việc giảm tỷ lệ tử vong do mọi nguyên nhân trong mùa RSV.[54] Nhóm bệnh nhân này có thể hưởng lợi từ liều dùng hàng tháng bắt đầu vào tháng đầu tiên của mùa RSV với tổng cộng 5 liều.[20] [48] [49] Các lựa chọn sơ cấp » palivizumab: 15 mg/kg tiêm bắp mỗi tháng một lần trong mùa dịch RSV |
||
|
1 | Liều dùng palivizumab hàng tháng |
| » Trẻ nhũ nhi bị bệnh phổi mạn tính do sinh non <12 tháng tuổi vào đầu mùa RSV cần được điều trị dự phòng với palivizumab. Những trẻ nhũ nhi này được xác định là sinh ra < 32 tuần thai với yêu cầu >21% liệu pháp oxy trong ít nhất 28 ngày sau sinh. Trẻ nhũ nhi bị bệnh phổi mạn tính do sinh non có độ tuổi từ 12 đến 24 tháng và tiếp tục cần oxy bổ sung, corticosteroid, hay thuốc lợi tiểu trong vòng 6 tháng kể từ đầu mùa SVHBHH cũng cần được nhận palivizumab trong mùa SVHBHH.[20] [48] [49]
» Cập nhật năm 2014 của Học viện Nhi khoa Hoa Kỳ về những chỉ định sử dụng palivizumab đã chỉ rõ các nhóm trẻ nhũ nhi cụ thể được coi là có nguy cơ cao.[20] [48] Việc sử dụng biện pháp này trong các nhóm nguy cơ cao có thể giảm mức nhập viện 45% đến 55%.[50] [51] [52] [53] [54] [55] [56] [118] 1[B]Evidence » Biện pháp dự phòng với Palivizumab ở các nhóm bệnh nhân này cũng có liên quan đến việc giảm tỷ lệ tử vong do mọi nguyên nhân trong mùa RSV.[54] Nhóm bệnh nhân này có thể hưởng lợi từ liều dùng hàng tháng bắt đầu vào tháng đầu tiên của mùa RSV với tổng cộng 5 liều.[20] [48] [49] Các lựa chọn sơ cấp » palivizumab: 15 mg/kg tiêm bắp mỗi tháng một lần trong mùa dịch RSV |
||
|
1 | Liều dùng palivizumab hàng tháng |
| » Cập nhật năm 2014 của Học viện Nhi khoa Hoa Kỳ về những chỉ định sử dụng palivizumab đã chỉ rõ các nhóm trẻ nhũ nhi cụ thể được coi là có nguy cơ cao.[20] [48] Việc sử dụng biện pháp này trong các nhóm nguy cơ cao có thể giảm mức nhập viện 45% đến 55%.[50] [51] [52] [53] [54] [55] [56] [118] 1[B]EvidenceMột bài tỏng quan hệ thống của Cochrane không tìm ra bất kỳ khác biệt có ý nghĩa lâm sàng nào về các kết quả ở trẻ em mắc xơ nang 6 tháng sau điều trị với palivizumab hay giả dược.[120]
» Biện pháp dự phòng với Palivizumab ở các nhóm bệnh nhân này cũng có liên quan đến việc giảm tỷ lệ tử vong do mọi nguyên nhân trong mùa RSV.[54] Nhóm bệnh nhân này có thể hưởng lợi từ liều dùng hàng tháng bắt đầu vào tháng đầu tiên của mùa RSV với tổng cộng 5 liều.[20] [48] [49]
Các lựa chọn sơ cấp |
||
|
1 | Lều dùng palivizumab hàng tháng |
| » Cập nhật năm 2014 của Học viện Nhi khoa Hoa Kỳ về những chỉ định sử dụng palivizumab đã chỉ rõ các nhóm trẻ nhũ nhi cụ thể được coi là có nguy cơ cao.[20] [48] Việc sử dụng biện pháp này trong các nhóm nguy cơ cao có thể giảm mức nhập viện 45% đến 55%.[50] [51] [52] [53] [54] [55] [56] [118] 1[B]Evidence » Biện pháp dự phòng với Palivizumab ở các nhóm bệnh nhân này cũng có liên quan đến việc giảm tỷ lệ tử vong do mọi nguyên nhân trong mùa RSV.[54] Nhóm bệnh nhân này có thể hưởng lợi từ liều dùng hàng tháng bắt đầu vào tháng đầu tiên của mùa RSV với tổng cộng 5 liều.[20] [48] [49] Các lựa chọn sơ cấp » palivizumab: 15 mg/kg tiêm bắp mỗi tháng một lần trong mùa dịch RSV |
||
|
1 | Liều dùng palivizumab hàng tháng |
| » Cập nhật năm 2014 của Học viện Nhi khoa Hoa Kỳ về những chỉ định sử dụng palivizumab đã chỉ rõ các nhóm trẻ nhũ nhi cụ thể được coi là có nguy cơ cao.[20] [48] Việc sử dụng biện pháp này trong các nhóm nguy cơ cao có thể giảm mức nhập viện 45% đến 55%.[50] [51] [52] [53] [54] [55] [56] [118] 1[B]Evidence » Biện pháp dự phòng với Palivizumab ở các nhóm bệnh nhân này cũng có liên quan đến việc giảm tỷ lệ tử vong do mọi nguyên nhân trong mùa RSV.[54] Nhóm bệnh nhân này có thể hưởng lợi từ liều dùng hàng tháng bắt đầu vào tháng đầu tiên của mùa RSV với tổng cộng 5 liều.[20] [48] [49] Các lựa chọn sơ cấp » palivizumab: 15 mg/kg tiêm bắp mỗi tháng một lần trong mùa dịch RSV |
||
Giai đoạn đầu
Palivizumab trong điều trị nhiễm RSV
Việc sử dụng palivizumab kết hợp với ribavirin dạng hít để điều trị bệnh nhân mắc bệnh RSV đã được nghiên cứu. Mặc dù có một vài ca bệnh không đối chứng ghi nhận thấy tình trạng dung nạp tốt và cải thiện kết quả với palivizumab, các ca bệnh còn lại không cho thấy sự cải thiện nào. Một phân tích tổng hợp cho thấy những người nhận liệu pháp điều trị kết hợp (ribavirin với immunoglobulin [IVIG] tĩnh mạch hoặc ribavirin với palivizumab) hạn chế tiến triển thành nhiễm đường hô hấp dưới hơn so với những người chỉ điều trị ribavirin dạng hít.[101] Lợi ích của palivizumab so với IVIG không nhất quán và palivizumab vẫn chỉ được cấp phép để điều trị dự phòng chống RSV ở một số trẻ em có nguy cơ cao. IVIG thường được sử dụng hơn trong trường hợp bệnh do virus ở mức độ nặng. Cần thêm các nghiên cứu khác để xác định phác đồ điều trị có lợi nhất.
Vắc-xin
Một loại kháng thể đơn dòng tái tổ hợp mới có tác dụng kéo dài nhắm vào protein RSV F đang được phát triển trên lâm sàng để phòng ngừa nhiễm trùng đường hô hấp dưới liên quan đến RSV ở trẻ nhũ nhi. Medi8897 có dược lực nâng cao hơn so với palivizumab trong ống nghiệm. Thuốc này đã được điều chế với chất thay thế [YTE] (M252Y/S254T/T256E) trong vùng Fc để ngăn thoái hóa và tăng tái tuần hoàn.[124] [125] Điều này sẽ cho phép việc dùng một liều duy nhất, có tác dụng bảo vệ trong cả mùa RSV. Các nghiên cứu giai đoạn 1/2 chứng tỏ thời gian bán thải của Medi8897 lên đến 117 ngày với tính an toàn tương tự như của giả dược.[126]
Liên lạc theo dõi
Khuyến nghị
Giám sát
Bệnh do RSV thường ở mức độ nhẹ và tự khỏi. Cần tái khám đều đặn đối với trẻ nhũ nhi được điều trị ngoại trú để đảm bảo không bỏ sót tình trạng suy hô hấp hoặc suy dinh dưỡng. Bệnh nhân bị nhiễm bệnh có thể hình thành biểu hiện thở khò khè tái diễn và thường tự khỏi vào lúc 13 tuổi.
Hướng dẫn dành cho bệnh nhân
Những người chăm sóc cần nhận thức được các triệu chứng thực thể của suy hô hấp (triệu chứng thực thể bao gồm khò khè, cánh mũi phập phồng, và co rút cơ liên sườn và/hoặc dưới sườn), ăn uống kém, và li bì.[61] Cần hướng dẫn họ đến tái khám nếu tình trạng lâm sàng của bệnh nhân xấu đi hoặc không cải thiện. Cũng cần giúp họ nhận thức được rằng thở khò khè tái diễn là hay gặp.
Các biến chứng
| Các biến chứng | Khung thời gian | Khả năng |
| Thở khò khè tái diễn | Dài hạn | Cao |
| Có mối liên quan chặt chẽ giữa nhiễm RSV và biểu hiện thở khò khè sau đó. Trẻ nhũ nhi cần nhập viện vì viêm tiểu phế quản do RSV có nguy cơ cao bị bất thường về kết quả xét nghiệm chức năng phổi và thở khò khè tái diễn trong khoảng thời gian lên tới 10 năm.[94] [95] [96] [97] [98] [129] | ||
| Hen suyễn | Dài hạn | Thấp |
| Vẫn còn những tranh cãi về việc liệu nhiễm RSV mức độ nặng là yếu tố nguy cơ đối với hen suyễn hay chỉ là đơn thuần là một dấu hiệu của bệnh đang tiến triển. Một số nghiên cứu cho rằng có mối quan hệ nhân quả.[93] [130] Tuy nhiên, một thử nghiệm ngẫu nhiên có đối chứng so sánh trẻ nhũ nhi được điều trị palivizumab chống RSV so với nhóm chứng là trẻ nhũ nhi không được điều trị dự phòng cho thấy không có khác biệt đáng kể về số bệnh nhân được chẩn đoán mắc hen suyễn, hoặc thay đổi chức năng hô hấp, ở thời điểm 6 tuổi.[131] | ||
| Viêm tiểu phế quản | Biến thiên | Cao |
| Bệnh viêm tiểu phế quản do RSV có thể gây suy hô hấp nặng. Trẻ nhũ nhi nguy cơ cao, như trẻ sinh non, bệnh phổi mạn tính, bệnh tim bẩm sinh phức tạp, hoặc suy giảm miễn dịch, có khả năng cao hơn bị bệnh ở mức độ nặng. Ngạt thở là một biến chứng thường gặp, đặc biệt là ở trẻ nhũ nhi nhỏ tuổi, và có thể là dấu hiệu của bệnh. | ||
| Viêm phổi | Biến thiên | Cao |
| RSV có thể gây viêm phổi ở trẻ em và, trong trường hợp hiếm gặp, ở cả người lớn có sức đề kháng bình thường. Viêm phổi do RSV thường có biểu hiện sốt nhẹ, ho dai dẳng, và khó chịu. | ||
Tiên lượng
Nhiễm RSV thường tự khỏi và khỏi hoàn toàn sau 10 đến 14 ngày.
Tại Hoa Kỳ, 5% trẻ nhũ nhi phải nhập viện hàng năm do viêm tiểu phế quản cần phải thở máy.[1] [127] Hàng năm, trên toàn thế giới, 1 trên 200 trẻ nhũ nhi phải nhập viện vì RSV, với tỷ lệ tử vong khoảng 5%.[128]
Tỷ lệ tấn công giảm từ 98% đối với lần nhiễm đầu tiên xuống còn 75% đối với các lần nhiễm tiếp theo.[30]
Hướng dẫn
Hướng dẫn chẩn đoán
Châu Âu
Consensus conference on acute bronchiolitis (I): methodology and recommendations [in Spanish]
Nhà xuất bản: Expert panel, Consensus conference on diagnostic and therapeutic management of acute bronchiolitis
Xuất bản lần cuối: 2010
Bắc Mỹ
The diagnosis, management, and prevention of bronchiolitis Nhà xuất bản: American Academy of Pediatrics
Xuất bản lần cuối: 2014
Hướng dẫn điều trị
Châu Âu
Consensus conference on acute bronchiolitis (I): methodology and recommendations [in Spanish]
Nhà xuất bản: Expert panel, Consensus conference on diagnostic and therapeutic management of acute bronchiolitis
Xuất bản lần cuối: 2010
Bắc Mỹ
Preventing hospitalizations for respiratory syncytial virus infection
Nhà xuất bản: Canadian Paediatric Society
Xuất bản lần cuối: 2015
The diagnosis, management, and prevention of bronchiolitis Nhà xuất bản: American Academy of Pediatrics
Xuất bản lần cuối: 2014
Updated guidance for palivizumab prophylaxis among infants and young children at increased risk of hospitalization for respiratory syncytial virus infection
Nhà xuất bản: American Academy of Pediatrics
Xuất bản lần cuối: 2014
Điểm số bằng chứng
- Giảm số ca nhập viện với palivizumab: Có bằng chứng tương đối đáng tin cậy cho thấy palivizumab có hiệu quả trong việc giảm số ca nhập viện vì bệnh viêm tiểu phế quản ở trẻ bị loạn sản phế quản phổi, ở trẻ nhũ nhi sinh non, và ở trẻ nhũ nhi bị bệnh tim bẩm sinh.[50] [51] Thuốc này được Học viện Nhi khoa Hoa Kỳ khuyến cáo sử dụng cho một số bệnh nhân nhất định.[48] Bằng chứng cấp độ B: Các thử nghiệm ngẫu nhiên đối chứng (RCT) với <200 người tham gia, các RCT có lỗi về phương pháp với >200 người tham gia, các đánh giá hệ thống (SR) có lỗi về phương pháp hoặc các nghiên cứu quan sát (thuần tập) có chất lượng cao.
- Sự cải thiện về bão hoà oxy: có bằng chứng chất lượng kém cho thấy thuốc giãn phế quản dạng hít (không phải adrenaline hay nước muối ưu trương) có thể có hiệu quả hơn giả dược trong việc cải thiện bão hoà oxy (mức ý nghĩa lâm sàng của việc này là không rõ ràng) trong điều kiện ngoại trú. Không rõ liệu thuốc giãn phế quản dạng hít có hiệu quả hơn giả dược hay không trong việc cải thiện chỉ số lâm sàng, giảm tỷ lệ trẻ em phải nhập viện, hay giảm thời gian nằm viện. Bằng chứng cấp độ C: Các nghiên cứu quan sát (thuần tập) có chất lượng thấp hoặc các thử nghiệm ngẫu nhiên đối chứng (RCT) có lỗi về phương pháp với <200 người tham gia.
- Cải thiện triệu chứng với ribavirin: có bằng chứng chất lượng kém cho thấy ribavirin có thể có hiệu quả cao hơn giả dược trong việc giảm thời gian thở máy ở trẻ em và trẻ nhũ nhi được nhập viện vì viêm tiểu phế quản do RSV, nhưng không có hiệu quả trong việc giảm tỷ lệ trẻ em bị suy hô hấp hay thời gian nằm viện. Các thử nghiệm ngẫu nhiên có đối chứng về ribavirin chỉ tuyển chọn số ít bệnh nhân và do đó có thể không đủ bằng chứng thuyết phục để phát hiện tác dụng của ribavirin lên các kết quả trên lâm sàng. Bằng chứng cấp độ C: Các nghiên cứu quan sát (thuần tập) có chất lượng thấp hoặc các thử nghiệm ngẫu nhiên đối chứng (RCT) có lỗi về phương pháp với <200 người tham gia.
- Cải thiện triệu chứng với liệu pháp corticosteroid: có bằng chứng chất lượng kém rằng liệu pháp corticosteroid không cải thiện kết quả. Tuy nhiên, khó có thể so sánh các kết quả nghiên cứu do sự khác biệt về các tiêu chuẩn lựa chọn và cách đo lường kết quả. Nhìn chung, thử nghiệm ngẫu nhiên có đối chứng về liệu pháp corticosteroid điều trị viêm tiểu phế quản nguyên phát ở trẻ nhỏ lần đầu thở khò khè không chứng minh rằng liệu pháp này có ảnh hưởng đáng kể đến kết quả lâm sàng.[122] [123] Bằng chứng cấp độ C: Các nghiên cứu quan sát (thuần tập) có chất lượng thấp hoặc các thử nghiệm ngẫu nhiên đối chứng (RCT) có lỗi về phương pháp với <200 người tham gia.
- Giảm lây nhiễm ở bệnh viện bằng việc sử dụng các biện pháp can thiệp xuất phát từ công việc chăm sóc bệnh nhân: có bằng chứng chất lượng kém cho thấy rằng việc áp dụng biện pháp tránh tụ tập, rửa tay, mặc áo choàng, đeo khẩu trang, găng tay, và kính bảo hộ có thể giảm sự lây lan của viêm tiểu phế quản. Ngoài ra, việc sử dụng các biện pháp này (và đặc biệt là rửa tay) được khuyến cáo trong các hướng dẫn sẵn có.[61] Bằng chứng cấp độ C: Các nghiên cứu quan sát (thuần tập) có chất lượng thấp hoặc các thử nghiệm ngẫu nhiên đối chứng (RCT) có lỗi về phương pháp với <200 người tham gia.
Các bài báo chủ yếu
- Bont L, Checchia PA, Fauroux B, et al. Defining the epidemiology and burden of severe respiratory syncytial virus infection among infants and children in western countries. Infect Dis Ther. 2016 Sep;5(3):271-98. Toàn văn Tóm lược
- Modjarrad K, Giersing B, Kaslow DC, et al; WHO RSV Vaccine Consultation Expert Group. WHO consultation on respiratory syncytial virus vaccine development report from a World Health Organization meeting held on 23-24 March 2015. Vaccine. 2016 Jan 4;34(2):190-7. Toàn văn Tóm lược
- American Academy of Pediatrics Committee on Infectious Diseases; American Academy of Pediatrics Bronchiolitis Guidelines Committee. Updated guidance for palivizumab prophylaxis among infants and young children at increased risk of hospitalization for respiratory syncytial virus infection. Pediatrics. 2014 Aug;134(2):415-20. Toàn văn Tóm lược
- Ralston SL, Lieberthal AS, Meissner HC, et al; American Academy of Pediatrics. Clinical practice guideline: the diagnosis, management, and prevention of bronchiolitis. Pediatrics. 2014 Nov;134(5):e1474-502. Toàn văn Tóm lược
Tài liệu tham khảo
- Shay DK, Holman RC, Newman RD, et al. Bronchiolitis-associated hospitalizations among US children, 1980-1996. JAMA. 1999 Oct 20;282(15):1440-6. Toàn văn Tóm lược
- National Center for Biotechnology Information. Taxonomy database: Pneumoviridae. [internet publication]. Toàn văn
- International Committee on Taxonomy of Viruses. Taxonomy: Order; Mononegavirales. 2017 [internet publication]. Toàn văn
- Bont L, Checchia PA, Fauroux B, et al. Defining the epidemiology and burden of severe respiratory syncytial virus infection among infants and children in western countries. Infect Dis Ther. 2016 Sep;5(3):271-98. Toàn văn Tóm lược
- Venkatesh MP, Weisman LE. Prevention and treatment of respiratory syncytial virus infection in infants: an update. Expert Rev Vaccines. 2006 Apr;5(2):261-8. Tóm lược
- ISD Scotland. Number of hospital discharges with bronchiolitis in children 0-24 months in Scotland for the years ending December 2001-2003 [statistical data]. Edinburgh: ISD Scotland; 2006.
- Hall CB, Weinberg GA, Iwane MK, et al. The burden of respiratory syncytial virus infection in young children. N Engl J Med. 2009 Feb 5;360(6):588-98. Toàn văn Tóm lược
- Zhang Y, Yuan L, Zhang Y, et al. Burden of respiratory syncytial virus infections in China: systematic review and meta-analysis. J Glob Health. 2015 Dec;5(2):020417. Toàn văn Tóm lược
- Shi T, McAllister DA, O’Brien KL, et al; RSV Global Epidemiology Network. Global, regional, and national disease burden estimates of acute lower respiratory infections due to respiratory syncytial virus in young children in 2015: a systematic review and modelling study. Lancet. 2017 Sep 2;390(10098):946-58. Toàn văn Tóm lược
- Gilchrist S, Torok TJ, Gary HE Jr, et al. National surveillance for respiratory syncytial virus, United States, 1985-1990. J Infect Dis. 1994 Oct;170(4):986-90. Tóm lược
- Centers for Disease Control and Prevention. Respiratory syncytial virus infection (RSV): trends and surveillance. March 2017 [internet publication]. Toàn văn
- Falsey AR, Hennessey PA, Formica MA, et al. Respiratory syncytial virus infection in elderly and high-risk adults. N Engl J Med. 2005 Apr 28;352(17):1749-59. Toàn văn Tóm lược
- Sundaram ME, Meece JK, Sifakis F, et al. Medically attended respiratory syncytial virus infections in adults aged >50 years: clinical characteristics and outcomes. Clin Infect Dis. 2014 Feb;58(3):342-9. Toàn văn Tóm lược
- Shiley KT, Lautenbach E, Lee I. The use of antimicrobial agents after diagnosis of viral respiratory tract infections in hospitalized adults: antibiotics or anxiolytics? Infect Control Hosp Epidemiol. 2010 Nov;31(11):1177-83. Toàn văn Tóm lược
- Peters TR, Crowe JE Jr. Respiratory syncytial virus. In: Long SS, Pickering LK, Prober CG, eds. Principles and practice of pediatric infectious diseases. 3rd ed. Philadelphia, PA: Churchill Livingstone; 2008.
- Hall CB, Douglas RG Jr, Geiman JM. Quantitative shedding patterns of respiratory syncytial virus in infants. J Infect Dis. 1975 Aug;132(2):151-6. Tóm lược
- Hall CB, Douglas RG Jr. Modes of transmission of respiratory syncytial virus. J Pediatr. 1981 Jul;99(1):100-3. Tóm lược
- Hall CB, Douglas RG Jr, Geiman JM. Possible transmission by fomites of respiratory syncytial virus. J Infect Dis. 1980 Jan;141(1):98-102. Tóm lược
- Hall CB, Douglas RG Jr, Geiman JM. Respiratory syncytial virus infections in infants: quantitation and duration of shedding. J Pediatr. 1976 Jul;89(1):11-5. Tóm lược
- Committee on Infectious Diseases; American Academy of Pediatrics. Red book. 30th ed. Elk Grove Village, IL: AAP; 2015:667-76. Toàn văn
- Hoffman SJ, Laham FR, Polack FP. Mechanisms of illness during respiratory syncytial virus infection: the lungs, the virus and the immune response. Microbes Infect. 2004 Jul;6(8):767-72. Tóm lược
- Johnson JE, Gonzales RA, Olson SJ, et al. The histopathology of fatal untreated human respiratory syncytial virus infection. Mod Pathol. 2007 Jan;20(1):108-19. Toàn văn Tóm lược
- Eisenhut M. Extrapulmonary manifestations of severe respiratory syncytial virus infection–a systematic review. Crit Care. 2006;10(4):R107. Toàn văn Tóm lược
- Aherne W, Bird T, Court SD, et al. Pathological changes in virus infections of the lower respiratory tract in children. J Clin Pathol. 1970 Feb;23(1):7-18. Toàn văn Tóm lược
- Patarcic I, Gelemanovic A, Kirin M, et al. The role of host genetic factors in respiratory tract infectious diseases: systematic review, meta-analyses and field synopsis. Sci Rep. 2015 Nov 3;5:16119. Toàn văn Tóm lược
- Zhou J, Zhang X, Liu S, et al. Genetic association of TLR4 Asp299Gly, TLR4 Thr399Ile, and CD14 C-159T polymorphisms with the risk of severe RSV infection: a meta-analysis. Influenza Other Respir Viruses. 2016 May;10(3):224-33. Toàn văn Tóm lược
- Lim FJ, de Klerk N, Blyth CC, et al. Systematic review and meta-analysis of respiratory viral coinfections in children. Respirology. 2016 May;21(4):648-55. Toàn văn Tóm lược
- Skjerven HO, Megremis S, Papadopoulos NG, et al; ORAACLE Study Group. Virus type and genomic load in acute bronchiolitis: severity and treatment response with inhaled adrenaline. J Infect Dis. 2016 Mar 15;213(6):915-21. Toàn văn Tóm lược
- Wu SH, Chen XQ, Kong X, et al. Characteristics of respiratory syncytial virus-induced bronchiolitis co-infection with Mycoplasma pneumoniae and add-on therapy with montelukast. World J Pediatr. 2016 Feb;12(1):88-95. Tóm lược
- Henderson FW, Collier AM, Clyde WA Jr., et al. Respiratory-syncytial-virus infections, reinfections and immunity: a prospective, longitudinal study in young children. N Engl J Med. 1979 Mar 8;300(10):530-4. Tóm lược
- Bradley JP, Bacharier LB, Bonfiglio J, et al. Severity of respiratory syncytial virus bronchiolitis is affected by cigarette smoke exposure and atopy. Pediatrics. 2005 Jan;115(1):e7-14. Toàn văn Tóm lược
- MacDonald NE, Hall CB, Suffin SC, et al. Respiratory syncytial viral infection in infants with congenital heart disease. N Engl J Med. 1982 Aug 12;307(7):397-400. Tóm lược
- Navas L, Wang E, de Carvalho V, et al. Improved outcome of respiratory syncytial virus infection in a high-risk hospitalized population of Canadian children. Pediatric Investigators Collaborative Network on Infections in Canada. J Pediatr. 1992 Sep;121(3):348-54. Tóm lược
- Moler FW, Khan AS, Meliones JN, et al. Respiratory syncytial virus morbidity and mortality estimates in congenital heart disease patients: a recent experience. Crit Care Med. 1992 Oct;20(10):1406-13. Tóm lược
- Wang EE, Law BJ, Boucher FD, et al. Pediatric Investigators Collaborative Network on Infections in Canada (PICNIC) study of admission and management variation in patients hospitalized with respiratory syncytial viral lower respiratory tract infection. J Pediatr. 1996 Sep;129(3):390-5. Tóm lược
- Boyce TG, Mellen BG, Mitchel EF Jr, et al. Rates of hospitalization for respiratory syncytial virus infection among children in Medicaid. J Pediatr. 2000 Dec;137(6):865-70. Tóm lược
- Hall CB, Powell KR, MacDonald NE, et al. Respiratory syncytial viral infection in children with compromised immune function. N Engl J Med. 1986 Jul 10;315(2):77-81. Tóm lược
- Simoes EA. Environmental and demographic risk factors for respiratory syncytial virus lower respiratory tract disease. J Pediatr. 2003 Nov;143(5 Suppl):S118-26. Tóm lược
- Walsh EE, Peterson DR, Falsey AR. Risk factors for severe respiratory syncytial virus infection in elderly persons. J Infect Dis. 2004 Jan 15;189(2):233-8. Toàn văn Tóm lược
- Wennergren G, Kristjánsson S. Relationship between respiratory syncytial virus bronchiolitis and future obstructive airway diseases. Eur Respir J. 2001 Dec;18(6):1044-58. Toàn văn Tóm lược
- Glenn GM, Smith G, Fries L, et al. Safety and immunogenicity of a Sf9 insect cell-derived respiratory syncytial virus fusion protein nanoparticle vaccine. Vaccine. 2013 Jan 7;31(3):524-32. Tóm lược
- Glenn GM, Fries LF, Thomas DN, et al. A randomized, blinded, controlled, dose-ranging study of a respiratory syncytial virus recombinant fusion (F) nanoparticle vaccine in healthy women of childbearing age. J Infect Dis. 2016 Feb 1;213(3):411-22. Tóm lược
- US National Institutes of Health; ClinicalTrials.gov. A study to evaluate the efficacy of an RSV F vaccine in older adults: ClinicalTrials.gov identifier:NCT02608502. November 2015 [internet publication]. Toàn văn
- US National Institutes of Health; ClinicalTrials.gov. A study to determine the safety and efficacy of the RSV F vaccine to protect infants via maternal immunization: ClinicalTrials.gov identifier:NCT02624947. December 2015 [internet publication]. Toàn văn
- Modjarrad K, Giersing B, Kaslow DC, et al; WHO RSV Vaccine Consultation Expert Group. WHO consultation on respiratory syncytial virus vaccine development report from a World Health Organization meeting held on 23-24 March 2015. Vaccine. 2016 Jan 4;34(2):190-7. Toàn văn Tóm lược
- Langley JM, Aggarwal N, Toma A, et al. A randomized, controlled, observer-blinded phase 1 study of the safety and immunogenicity of a respiratory syncytial virus vaccine with or without alum adjuvant. J Infect Dis. 2017 Jan 1;215(1):24-33. Toàn văn Tóm lược
- Morris SK, Dzolganovski B, Beyene J, et al. A meta-analysis of the effect of antibody therapy for the prevention of severe respiratory syncytial virus infection. BMC Infect Dis. 2009 Jul 5;9:106. Toàn văn Tóm lược
- American Academy of Pediatrics Committee on Infectious Diseases; American Academy of Pediatrics Bronchiolitis Guidelines Committee. Updated guidance for palivizumab prophylaxis among infants and young children at increased risk of hospitalization for respiratory syncytial virus infection. Pediatrics. 2014 Aug;134(2):415-20. Toàn văn Tóm lược
- Frogel MP, Stewart DL, Hoopes M, et al. A systematic review of compliance with palivizumab administration for RSV immunoprophylaxis. J Manag Care Pharm. 2010 Jan-Feb;16(1):46-58. Toàn văn Tóm lược
- The IMpact-RSV Study Group. Palivizumab, a humanized respiratory syncytial virus monoclonal antibody, reduces hospitalization from respiratory syncytial virus infection in high-risk infants. Pediatrics. 1998 Sep;102(3 Pt 1):531-7. Tóm lược
- Feltes TF, Cabalka AK, Meissner HC, et al. Palivizumab prophylaxis reduces hospitalization due to respiratory syncytial virus in young children with hemodynamically significant congenital heart disease. J Pediatr. 2003 Oct;143(4):532-40. Tóm lược
- Prescott WA Jr, Doloresco F, Brown J, et al. Cost effectiveness of respiratory syncytial virus prophylaxis: a critical and systematic review. Pharmacoeconomics. 2010;28(4):279-93. Tóm lược
- Wang D, Cummins C, Bayliss S, et al. Immunoprophylaxis against respiratory syncytial virus (RSV) with palivizumab in children: a systematic review and economic evaluation. Health Technol Assess. 2008 Dec;12(36):iii, ix-x, 1-86. Toàn văn Tóm lược
- Checchia PA, Nalysnyk L, Fernandes AW, et al. Mortality and morbidity among infants at high risk for severe respiratory syncytial virus infection receiving prophylaxis with palivizumab: a systematic literature review and meta¬analysis. Pediatr Crit Care Med. 2011 Sep;12(5):580-8. Tóm lược
- Pons JM, Tebé C, Paladio N, et al. Meta-analysis of passive immunoprophylaxis in paediatric patients at risk of severe RSV infection. Acta Paediatr. 2011 Mar;100(3):324-9. Tóm lược
- Wang D, Bayliss S, Meads C. Palivizumab for immunoprophylaxis of respiratory syncytial virus (RSV) bronchiolitis in high-risk infants and young children: a systematic review and additional economic modelling of subgroup analyses. Health Technol Assess. 2011 Jan;15(5):iii-iv, 1-124. Toàn văn Tóm lược
- Anderson EJ, Carbonell-Estrany X, Blanken M, et al. Burden of severe respiratory syncytial virus disease among 33-35 weeks’ gestational age infants born during multiple respiratory syncytial virus seasons. Pediatr Infect Dis J. 2017 Feb;36(2):160-7. Toàn văn Tóm lược
- Carbonell-Estrany X, Fullarton JR, Gooch KL, et al. The influence of birth weight amongst 33-35 weeks gestational age (wGA) infants on the risk of respiratory syncytial virus (RSV) hospitalisation: a pooled analysis. J Matern Fetal Neonatal Med. 2017 Jan;30(2):134-40. Tóm lược
- Mauskopf J, Margulis AV, Samuel M, et al. Respiratory syncytial virus hospitalizations in healthy preterm infants: systematic review. Pediatr Infect Dis J. 2016 Jul;35(7):e229-38. Toàn văn Tóm lược
- Mansbach JM, Camargo CA Jr. Respiratory viruses in bronchiolitis and their link to recurrent wheezing and asthma. Clin Lab Med. 2009 Dec;29(4):741-55. Toàn văn Tóm lược
- Ralston SL, Lieberthal AS, Meissner HC, et al; American Academy of Pediatrics. Clinical practice guideline: the diagnosis, management, and prevention of bronchiolitis. Pediatrics. 2014 Nov;134(5):e1474-502. Toàn văn Tóm lược
- Hall WJ, Hall CB, Speers DM. Respiratory syncytial virus infection in adults: clinical, virologic, and serial pulmonary function studies. Ann Intern Med. 1978 Feb;88(2):203-5. Tóm lược
- Welliver RC. Review of epidemiology and clinical risk factors for severe respiratory syncytial virus (RSV) infection. J Pediatr. 2003 Nov;143(5 Suppl):S112-7. Tóm lược
- Parrott RH, Kim HW, Arrobio JO, et al. Epidemiology of respiratory syncytial virus infection in Washington, D.C. II: infection and disease with respect to age, immunologic status, race and sex. Am J Epidemiol. 1973 Oct;98(4):289-300. Tóm lược
- Kim HW, Arrobio JO, Brandt CD, et al. Epidemiology of respiratory syncytial virus infection in Washington, D.C. I: importance of the virus in different respiratory tract disease syndromes and temporal distribution of infection. Am J Epidemiol. 1973 Sep;98(3):216-25. Tóm lược
- Church NR, Anas NG, Hall CB, et al. Respiratory syncytial virus-related apnea in infants: demographics and outcome. Am J Dis Child. 1984 Mar;138(3):247-50. Tóm lược
- Hall CB, Long CE, Schnabel KC. Respiratory syncytial virus infections in previously healthy working adults. Clin Infect Dis. 2001 Sep 15;33(6):792-6. Toàn văn Tóm lược
- Walsh EE, Falsey AR, Hennessey PA. Respiratory syncytial and other virus infections in persons with chronic cardiopulmonary disease. Am J Respir Crit Care Med. 1999 Sep;160(3):791-5. Toàn văn Tóm lược
- Nicholson KG, Abrams KR, Batham S, et al. Randomised controlled trial and health economic evaluation of the impact of diagnostic testing for influenza, respiratory syncytial virus and Streptococcus pneumoniae infection on the management of acute admissions in the elderly and high-risk 18- to 64-year-olds. Health Technol Assess. 2014 May;18(36):1-274, vii-viii. Tóm lược
- Krasinski K, LaCourture R, Holzman RS, et al. Screening for respiratory syncytial virus and assignment to a cohort at admission to reduce nosocomial transmission. J Pediatr. 1990 Jun;116(6):894-8. Tóm lược
- Doan Q, Enarson P, Kissoon N, et al. Rapid viral diagnosis for acute febrile respiratory illness in children in the Emergency Department. Cochrane Database Syst Rev. 2014;(9):CD006452. Toàn văn Tóm lược
- Moore C, Valappil M, Corden S, et al. Enhanced clinical utility of the NucliSens EasyQ RSV A+B Assay for rapid detection of respiratory syncytial virus in clinical samples. Eur J Clin Microbiol Infect Dis. 2006 Mar;25(3):167-74. Tóm lược
- Chartrand C, Tremblay N, Renaud C, et al. Diagnostic accuracy of rapid antigen detection tests for respiratory syncytial virus infection: systematic review and meta-analysis. J Clin Microbiol. 2015 Dec;53(12):3738-49. Toàn văn Tóm lược
- Simpson W, Hacking PM, Court SD, et al. The radiological findings in respiratory syncytial virus infection in children. II: the correlation of radiological categories with clinical and virological findings. Pediatr Radiol. 1974;2(3):155-60. Tóm lược
- Simpson W, Hacking PM, Court SD, et al. The radiological findings in respiratory syncytial virus infection in children. Part I: definitions and interobserver variation in the assessment of abnormalities on the chest x-ray. Pediatr Radiol. 1974;2(2):97-100. Tóm lược
- Friis B, Eiken M, Hornsleth A, et al. Chest x-ray appearances in pneumonia and bronchiolitis: correlation to virological diagnosis and secretory bacterial findings. Acta Paediatr Scand. 1990 Feb;79(2):219-25. Tóm lược
- Hall CB. Respiratory syncytial virus: a continuing culprit and conundrum. J Pediatr. 1999 Aug;135(2 Pt 2):2-7. Tóm lược
- Bruhn FW, Mokrohisky ST, McIntosh K. Apnea associated with respiratory syncytial virus infection in young infants. J Pediatr. 1977 Mar;90(3):382-6. Tóm lược
- Hall CB. Respiratory syncytial virus and sudden infant death. N Engl J Med. 1979 Jun 21;300(25):1440-1. Tóm lược
- Anas N, Boettrich C, Hall CB, et al. The association of apnea and respiratory syncytial virus infection in infants. J Pediatr. 1982 Jul;101(1):65-8. Tóm lược
- Kneyber MC, Brandenburg AH, de Groot R, et al. Risk factors for respiratory syncytial virus associated apnoea. Eur J Pediatr. 1998 Apr;157(4):331-5. Tóm lược
- Willwerth BM, Harper MB, Greenes DS. Identifying hospitalized infants who have bronchiolitis and are at high risk for apnea. Ann Emerg Med. 2006 Oct;48(4):441-7. Tóm lược
- Turner T, Wilkinson F, Harris C, et al. Evidence based guideline for the management of bronchiolitis. Aust Fam Physician. 2008 Jun;37(6 Spec No):6-13. Tóm lược
- Stempel HE, Martin ET, Kuypers J, et al. Multiple viral respiratory pathogens in children with bronchiolitis. Acta Paediatr. 2009 Jan;98(1):123-6. Tóm lược
- Weinberg GA, Erdman DD, Edwards KM, et al. Superiority of reverse-transcription polymerase chain reaction to conventional viral culture in the diagnosis of acute respiratory tract infections in children. J Infect Dis. 2004 Feb 15;189(4):706-10. Toàn văn Tóm lược
- Koetz A, Nilsson P, Linden M, et al. Detection of human coronavirus NL63, human metapneumovirus and respiratory syncytial virus in children with respiratory tract infections in south-west Sweden. Clin Microbiol Infect. 2006 Nov;12(11):1089-96. Toàn văn Tóm lược
- Mansbach JM, McAdam AJ, Clark S, et al. Prospective multicenter study of the viral etiology of bronchiolitis in the emergency department. Acad Emerg Med. 2008 Feb;15(2):111-8. Toàn văn Tóm lược
- Yuksel H, Yilmaz O, Akcali S, et al. Common viral etiologies of community acquired lower respiratory tract infections in young children and their relationship with long term complications [in Turkish]. Mikrobiyol Bul. 2008 Jul;42(3):429-35. Tóm lược
- Downes JJ, Wood DW, Striker TW, et al. Acute respiratory failure in infants with bronchiolitis. Anesthesiology. 1968 May-Jun;29(3):426-34. Tóm lược
- Lodrup Carlsen KC, Carlsen KH. Inhaled nebulized adrenaline improves lung function in infants with acute bronchiolitis. Respir Med. 2000 Jul;94(7):709-14. Tóm lược
- Modl M, Eber E, Weinhandl E, et al. Assessment of bronchodilator responsiveness in infants with bronchiolitis. A comparison of the tidal and the raised volume rapid thoracoabdominal compression technique. Am J Respir Crit Care Med. 2000 Mar;161(3 Pt 1):763-8. Tóm lược
- Sanchez I, De Koster J, Powell RE, et al. Effect of racemic epinephrine and salbutamol on clinical score and pulmonary mechanics in infants with bronchiolitis. J Pediatr. 1993 Jan;122(1):145-51. Tóm lược
- Sigurs N, Bjarnason R, Sigurbergsson F, et al. Respiratory syncytial virus bronchiolitis in infancy is an important risk factor for asthma and allergy at age 7. Am J Respir Crit Care Med. 2000 May;161(5):1501-7. Toàn văn Tóm lược
- Mok JY, Simpson H. Outcome for acute bronchitis, bronchiolitis, and pneumonia in infancy. Arch Dis Child. 1984 Apr;59(4):306-9. Toàn văn Tóm lược
- Murray M, Webb MS, O’Callaghan C, et al. Respiratory status and allergy after bronchiolitis. Arch Dis Child. 1992 Apr;67(4):482-7. Tóm lược
- Noble V, Murray M, Webb MS, et al. Respiratory status and allergy nine to 10 years after acute bronchiolitis. Arch Dis Child. 1997 Apr;76(4):315-9. Toàn văn Tóm lược
- Osundwa VM, Dawod ST, Ehlayel M. Recurrent wheezing in children with respiratory syncytial virus (RSV) bronchiolitis in Qatar. Eur J Pediatr. 1993 Dec;152(12):1001-3. Tóm lược
- Sims DG, Downham MA, Gardner PS, et al. Study of 8-year-old children with a history of respiratory syncytial virus bronchiolitis in infancy. Br Med J. 1978 Jan 7;1(6104):11-14. Toàn văn Tóm lược
- Everard ML, Hind D, Ugonna K, et al; SABRE Study Team. SABRE: a multicentre randomised control trial of nebulised hypertonic saline in infants hospitalised with acute bronchiolitis. Thorax. 2014 Dec;69(12):1105-12. Toàn văn Tóm lược
- Zhang L, Mendoza-Sassi RA, Klassen TP, et al. Nebulized hypertonic saline for acute bronchiolitis: a systematic review. Pediatrics. 2015 Oct;136(4):687-701. Tóm lược
- von Lilienfeld-Toal M, Berger A, Christopeit M, et al. Community acquired respiratory virus infections in cancer patients: guideline on diagnosis and management by the Infectious Diseases Working Party of the German Society for Haematology and Medical Oncology. Eur J Cancer. 2016 Nov;67:200-12. Toàn văn Tóm lược
- Dignan FL, Clark A, Aitken C, et al; Haemato-oncology Task Force of the British Committee for Standards in Haematology; British Society for Blood and Marrow Transplantation; UK Clinical Virology Network. BCSH/ BSBMT/UK Clinical Virology Network guideline: diagnosis and management of common respiratory viral infections in patients undergoing treatment for haematological malignancies or stem cell transplantation. Br J Haematol. 2016 May;173(3):380-93. Tóm lược
- Hynicka LM, Ensor CR. Prophylaxis and treatment of respiratory syncytial virus in adult immunocompromised patients. Ann Pharmacother. 2012 Apr;46(4):558-66. Tóm lược
- Levin D, Tribuzio M, Green-Wrzesinki T, et al. Empiric antibiotics are justified for infants with respiratory syncytial virus lower respiratory tract infection presenting with respiratory failure: a prospective study and evidence review. Pediatr Crit Care Med. 2010 May;11(3):390-5. Tóm lược
- Farley R, Spurling GK, Eriksson L, et al. Antibiotics for bronchiolitis in children under two years of age. Cochrane Database Syst Rev. 2014;(10):CD005189. Toàn văn Tóm lược
- Ermers MJ, Rovers MM, van Woensel JB, et al. The effect of high dose inhaled corticosteroids on wheeze in infants after respiratory syncytial virus infection: randomised double blind placebo controlled trial. BMJ. 2009 Mar 31;338:b897. Toàn văn Tóm lược
- Fernandes RM, Bialy LM, Vandermeer B, et al. Glucocorticoids for acute viral bronchiolitis in infants and young children. Cochrane Database Syst Rev. 2013;(6):CD004878. Toàn văn Tóm lược
- Rodriguez WJ, Gruber WC, Groothuis JR, et al. Respiratory syncytial virus immune globulin treatment of RSV lower respiratory tract infection in previously healthy children. Pediatrics. 1997 Dec;100(6):937-42. Tóm lược
- Hemming VG, Rodriguez W, Kim HW, et al. Intravenous immunoglobulin treatment of respiratory syncytial virus infections in infants and young children. Antimicrob Agents Chemother. 1987 Dec;31(12):1882-6. Toàn văn Tóm lược
- Marcelin JR, Wilson JW, Razonable RR; Mayo Clinic Hematology/Oncology and Transplant Infectious Diseases Services. Oral ribavirin therapy for respiratory syncytial virus infections in moderately to severely immunocompromised patients. Transpl Infect Dis. 2014 Apr;16(2):242-50. Tóm lược
- Shah JN, Chemaly RF. Management of RSV infections in adult recipients of hematopoietic stem cell transplantation. Blood. 2011 Mar 10;117(10):2755-63. Toàn văn Tóm lược
- Nasr SZ, Strouse PJ, Soskolne E, et al. Efficacy of recombinant human deoxyribonuclease I in the hospital management of respiratory syncytial virus bronchiolitis. Chest. 2001 Jul;120(1):203-8. Toàn văn Tóm lược
- Boogaard R, Hulsmann AR, van Veen L, et al. Recombinant human deoxyribonuclease in infants with respiratory syncytial virus bronchiolitis. Chest. 2007 Mar;131(3):788-95. Toàn văn Tóm lược
- Enriquez A, Chu IW, Mellis C, et al. Nebulised deoxyribonuclease for viral bronchiolitis in children younger than 24 months. Cochrane Database Syst Rev. 2012;(11):CD008395. Toàn văn Tóm lược
- Chalumeau M, Duijvestijn YC. Acetylcysteine and carbocysteine for acute upper and lower respiratory tract infections in paediatric patients without chronic broncho-pulmonary disease. Cochrane Database Syst Rev. 2013; (5):CD003124. Toàn văn Tóm lược
- Liet JM, Ducruet T, Gupta V, et al. Heliox inhalation therapy for bronchiolitis in infants. Cochrane Database Syst Rev. 2015;(9):CD006915. Toàn văn Tóm lược
- Bisgaard H, Flores-Nunez A, Goh A, et al. Study of montelukast for the treatment of respiratory symptoms of post- respiratory syncytial virus bronchiolitis in children. Am J Respir Crit Care Med. 2008 Oct 15;178(8):854-60. Toàn văn Tóm lược
- Andabaka T, Nickerson JW, Rojas-Reyes MX, et al. Monoclonal antibody for reducing the risk of respiratory syncytial virus infection in children. Cochrane Database Syst Rev. 2013;(4):CD006602. Toàn văn Tóm lược
- Chiu SN, Shao PL, Chen HC, et al. Risk of respiratory syncytial virus infection in cyanotic congenital heart disease in a subtropical area. J Pediatr. 2016 Apr;171:25-30.e1. Tóm lược
- Robinson KA, Odelola OA, Saldanha IJ. Palivizumab for prophylaxis against respiratory syncytial virus infection in children with cystic fibrosis. Cochrane Database Syst Rev. 2016;(7):CD007743. Toàn văn Tóm lược
- Hu JR, Robinson JL. Treatment of respiratory syncytial virus with palivizumab: a systematic review. World J Pediatr. 2010 Nov;6(4):296-300. Toàn văn Tóm lược
- King VJ, Viswanathan M, Bordley WC, et al. Pharmacologic treatment of bronchiolitis in infants and children: a systematic review. Arch Pediatr Adolesc Med. 2004;158:127-137. Toàn văn Tóm lược
- Corneli HM, Zorc JJ, Majahan P, et al. A multicenter, randomized, controlled trial of dexamethasone for bronchiolitis. N Engl J Med. 2007;357:331-339. Toàn văn Tóm lược
- Robbie GJ, Criste R, Dall’acqua WF, et al. A novel investigational Fc-modified humanized monoclonal antibody, motavizumab-YTE, has an extended half-life in healthy adults. Antimicrob Agents Chemother. 2013 Dec;57(12):6147-53. Toàn văn Tóm lược
- Kwakkenbos MJ, Diehl SA, Yasuda E, et al. Generation of stable monoclonal antibody-producing B cell receptor-positive human memory B cells by genetic programming. Nat Med. 2010 Jan;16(1):123-8. Toàn văn Tóm lược
- Griffin MP, Khan AA, Esser MT, et al. Safety, tolerability, and pharmacokinetics of MEDI8897, the respiratory syncytial virus prefusion F-targeting monoclonal antibody with an extended half-life, in healthy adults. Antimicrob Agents Chemother. 2017 Feb 23;61(3):e01714-16. Toàn văn Tóm lược
- Leader S, Kohlhase K. Respiratory syncytial virus-coded pediatric hospitalizations, 1997 to 1999. Pediatr Infect Dis J. 2002;21:629-632. Tóm lược
- Sung RY, Murray HG, Chan RC, et al. Seasonal patterns of respiratory syncytial virus infection in Hong Kong: a preliminary report. J Infect Dis. 1987;156:527-528. Tóm lược
- McConnochie KM, Roghmann KJ. Bronchiolitis as a possible cause of wheezing in childhood: new evidence. Pediatrics. 1984 Jul;74(1):1-10. Tóm lược
- Stein RT, Sherrill D, Morgan WJ, et al. Respiratory syncytial virus in early life and risk of wheeze and allergy by age 13 years. Lancet. 1999 Aug 14;354(9178):541-5. Tóm lược
- Scheltema NM, Nibbelke EE, Pouw J, et al. Respiratory syncytial virus prevention and asthma in healthy preterm infants: a randomised controlled trial. Lancet Respir Med. 2018 Apr;6(4):257-64. Tóm lược
- Hall CB, Douglas RG Jr. Nosocomial respiratory syncytial viral infections: should gowns and masks be used? Am J Dis Child. 1981 Jun;135(6):512-5. Tóm lược
- Gala CL, Hall CB, Schnabel KC, et al. The use of eye-nose goggles to control nosocomial respiratory syncytial virus infection. JAMA. 1986 Nov 21;256(19):2706-8. Tóm lược
- Agah R, Cherry JD, Garakian AJ, et al. Respiratory syncytial virus (RSV) infection rate in personnel caring for children with RSV infections: routine isolation procedure vs routine procedure supplemented by use of masks and goggles. Am J Dis Child. 1987 Jun;141(6):695-7. Tóm lược
- Leclair JM, Freeman J, Sullivan BF, et al. Prevention of nosocomial respiratory syncytial virus infections through compliance with glove and gown isolation precautions. N Engl J Med. 1987 Aug 6;317(6):329-34. Tóm lược
- Smith JD, MacDougall CC, Johnstone J, et al. Effectiveness of N95 respirators versus surgical masks in protecting health care workers from acute respiratory infection: a systematic review and meta-analysis. CMAJ. 2016 May 17;188(8):567-74. Toàn văn Tóm lược
Hình ảnh
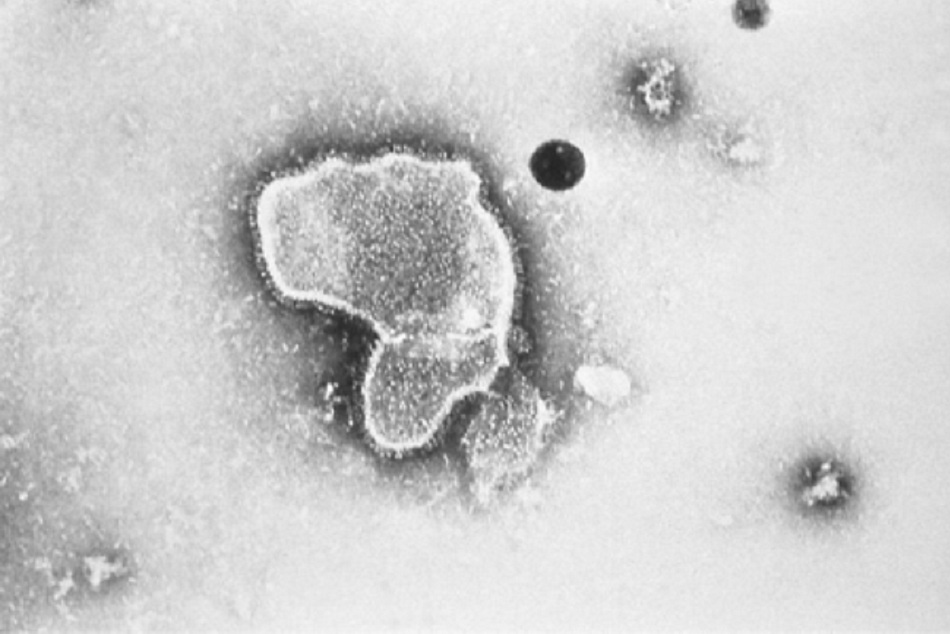
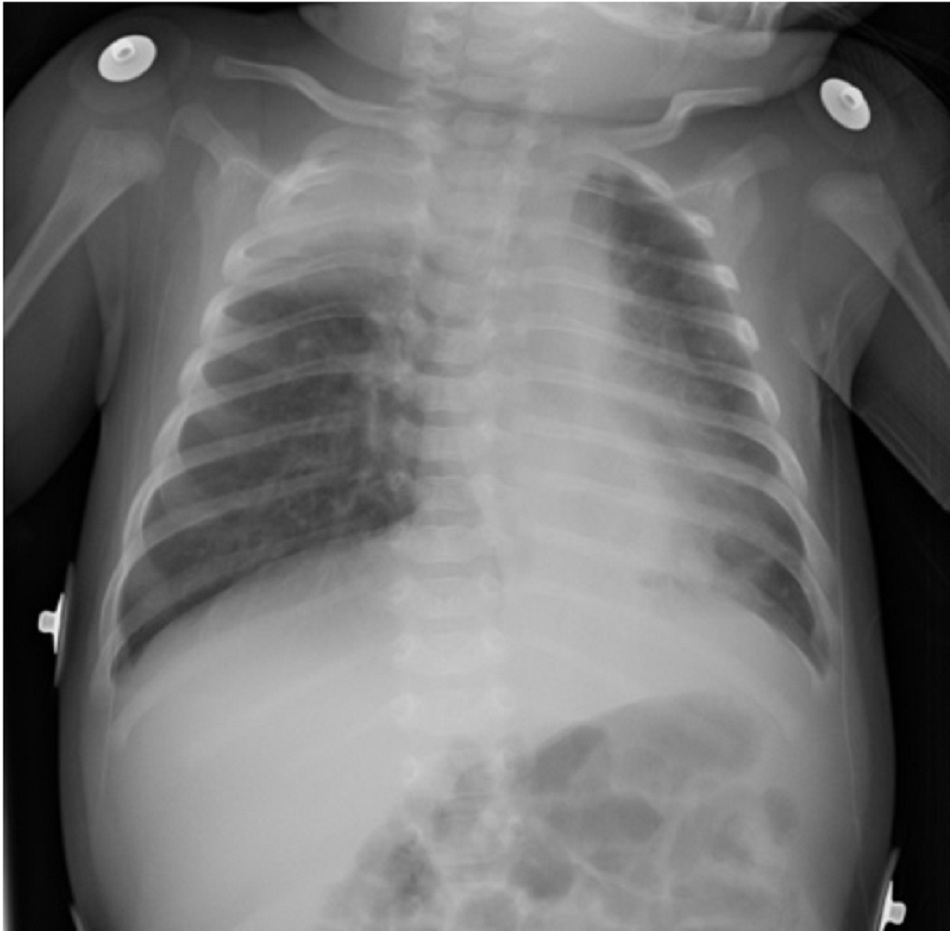
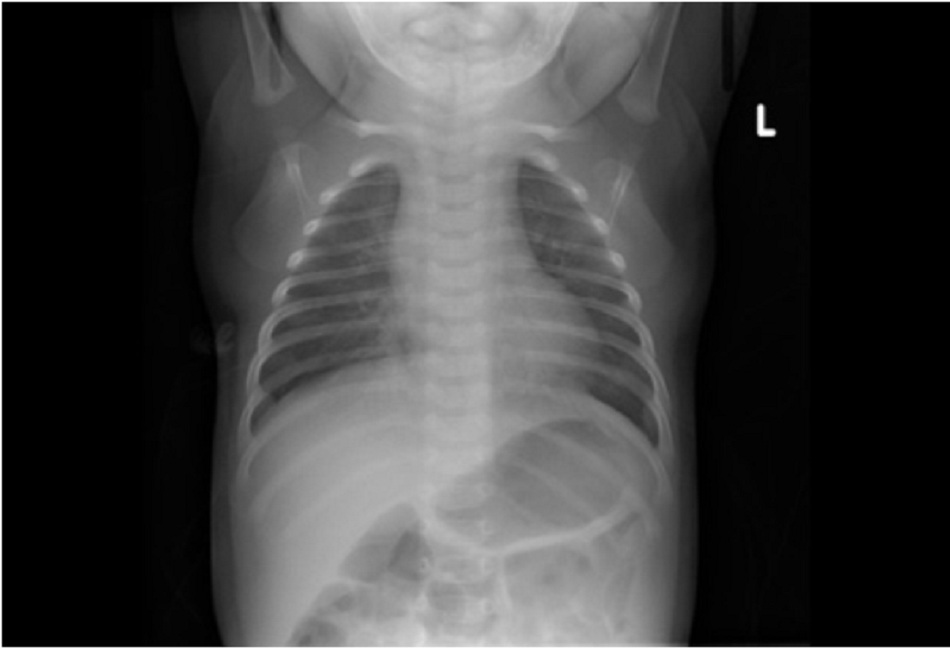
Những người có đóng góp
// Các tác giả:
Frank Esper, MD
Center for Pediatric Infectious Diseases
Cleveland Clinic Children’s Hospital, Cleveland, OH
CÔNG KHAI THÔNG TIN: FE declares that he has no competing interests.
Giovanni Piedimonte, MD, FAAP, FCCP
The Steven and Nancy Calabrese Endowed Chair for Excellence in Pediatric Care, Research, and Education
Professor & Chair of Pediatrics, Cleveland Clinic Lerner College of Medicine, Case Western Reserve University, Chief, Global Pediatric Research Operations, Cleveland Clinic Foundation, Director, Center for Pediatric Research, Lerner Research Institute, Cleveland, OH
CÔNG KHAI THÔNG TIN: GP declares that he has no competing interests.
// Lời cảm ơn:
Dr Frank Esper and Dr Giovanni Piedimonte would like to gratefully acknowledge Dr Melvin L. Wright, a previous contributor to this topic.
CÔNG KHAI THÔNG TIN: MLW declares that he has no competing interests.
// Những Người Bình duyệt:
Leonard R. Krilov, MD Chief
Pediatric Infectious Disease, Vice Chairman, Department of Pediatrics, Children’s Medical Center, Winthrop University Medical Center, Mineola, Professor of Pediatrics, School of Medicine, Stony Brook University Medical Center, Stony Brook, NY
CÔNG KHAI THÔNG TIN: LRK has participated as an investigator in multiple clinical research trials supported by grants from MedImmune. LRK has also served as a consultant to MedImmune on medical advisory boards and is a member of their speakers’ bureau.
Robert Welliver, MD
Professor of Pediatrics
Women and Children’s Hospital, Buffalo, NY
CÔNG KHAI THÔNG TIN: RW declares that he has no competing interests.
Jennifer Handforth, MB ChB, MRCPCH, DTM&H
Consultant Paediatrician
Croydon University Hospital, Croydon, UK
CÔNG KHAI THÔNG TIN: JH declares that she has no competing interests.
Xem thêm:
Nhiễm virus đậu mùa: Nguyên nhân, chẩn đoán và hướng dẫn điều trị theo BMJ