Ranitidin
Biên soạn và Hiệu đính
Dược sĩ Phan Hữu Xuân Hạo – Khoa Dược, Trường Y Dược – Đại học Duy Tân.
Danh pháp
Tên chung quốc tế
Ranitidin
Tên danh pháp theo IUPAC
(E)-1-N’-[2-[[5-[(dimethylamino)methyl]furan-2-yl]methylsulfanyl]ethyl]-1-N-methyl-2-nitroethene-1,1-diamine
Nhóm thuốc
Thuốc đối kháng với thụ thể H2 của histamin
Mã ATC
A: Thuốc cho đường tiêu hóa và chuyển hóa trong cơ thể
A02: Thuốc ức chế acid, điều trị các chứng loét dạ dày – tá tràng và đầy hơi.
A02B: Thuốc điều trị các chứng loét dạ dày – tá tràng.
A02BA: Thuốc đối kháng với thụ thể H2 của Histamin.
A02BA021: Ranitidin.
Mã UNII
884KT10YB7
Mã CAS
66357-35-5
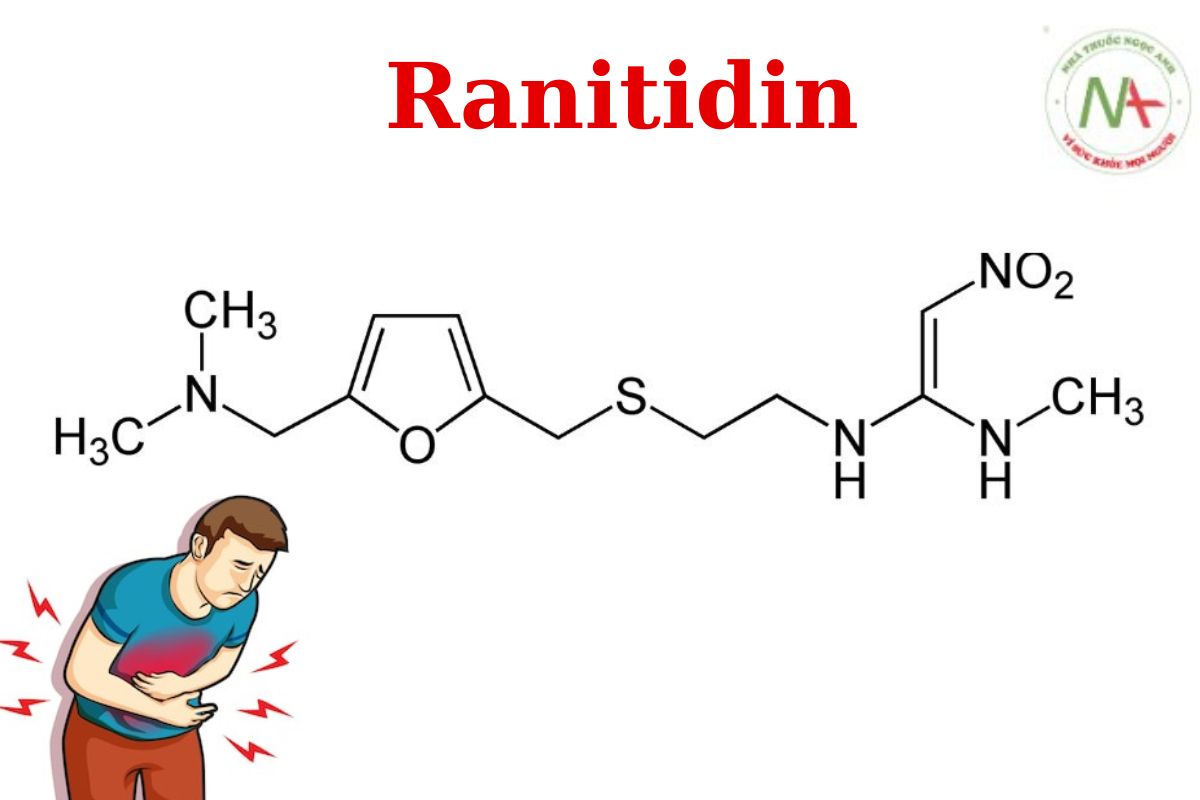
Cấu trúc phân tử
Công thức phân tử
C 13 H 22 N 4 O 3 S
Phân tử lượng
314.41 g/mol
Cấu trúc phân tử
Ranitidine là một thành viên của nhóm furan được sử dụng để điều trị bệnh loét dạ dày tá tràng (PUD) và bệnh trào ngược dạ dày thực quản. Nó có vai trò như một loại thuốc chống loét, chất đối kháng thụ thể H2, xenobiotic và chất gây dị ứng thuốc. Nó là một thành viên của furan, một hợp chất amin bậc ba , một hợp chất C-nitro và một sunfua hữu cơ.
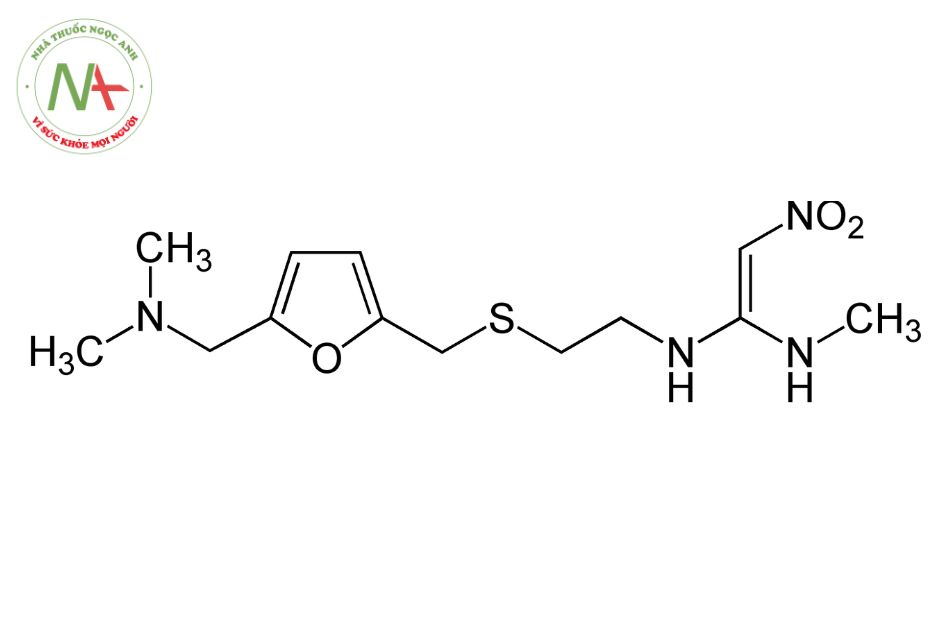
Các tính chất phân tử
Số liên kết hydro cho: 2
Số liên kết hydro nhận: 7
Số liên kết có thể xoay: 9
Diện tích bề mặt tôpô: 112 Ų
Số lượng nguyên tử nặng: 21
Phần trăm các nguyên tử: C 49.66%, H 7.05%, N 17.82%, O 15.27%, S 10.20%
Các tính chất đặc trưng
Điểm nóng chảy (° C): 69,5 ° C
LogP: 0,27
Chu kì bán hủy: 2 – 3 giờ
Khả năng liên kết với Protein huyết tương: 15%
Cảm quan
Trên thực tế thường bắt gặp Ranitidin dạng muối Hydrochloride.
Ranitidin có dạng bột kết tinh, dạng rắn có màu trắng đến vàng nhạt.
Ranitidin tan hoàn toàn trong nước, tan nhẹ trong ethanol khan, cực kì khó tan trong methylen clorid.
Ranitidin còn có tính đa hình.

Dạng bào chế
Chế phẩm Ranitidin viên nang có hàm lượng: 150 mg, 300 mg.
Ranitidin dạng dung dịch uống 75 mg/5 ml; gói bột pha 150 mg.
Ranitidin dạng viên nén có hàm lượng: 25 mg, 75 mg, 150 mg, 300 mg.
Ranitidin viên sủi bọt có hàm lượng: 150 mg, 300 mg.
Ranitidin thuốc tiêm 25 mg/ml (2 ml, 6 ml, 40 ml)
Độ ổn định và điều kiện bảo quản của Ranitidin
Ranitidin cần được bảo quản ở nơi khô ráo, tránh ẩm ướt vì tan rất tốt trong nước.
Bảo quản Ranitidin dạng viên nén ở nhiệt độ 15-30oC, tránh ánh sáng chiếu vào.
Bảo quản Ranitidin thuốc tiêm ở nhiệt độ 4-30oC, tránh ánh sáng chiếu vào.
Nếu dung dịch thuốc trong suốt hoặc hơi sẫm màu vàng thì vẫn không ảnh hưởng hiệu lực của thuốc.
Để Ranitidin xa tầm tay trẻ em.
Nguồn gốc
Ranitidin là một thuốc kháng histamin H2, được sử dụng để điều trị các triệu chứng tăng sản xuất acid dạ dày và hỗ trợ điều trị loét dạ dày tá tràng.
Năm 1976, Ranitidin được lần đầu tìm thấy ở Anh.
Năm 1981, Ranitidin phát triển và được đưa vào sử dụng thương mại.
Khi đó, Ranitidin là một trong các thuốc nằm trong Danh sách các loại thuốc thiết yếu của Tổ chức Y tế Thế giới (WHO) .
Năm 2019, Ranitidin là loại thuốc được kê đơn phổ biến đứng thứ 53 ở Hoa Kỳ, với hơn 13 triệu đơn thuốc.
Tuy nhiên, đến tháng 9 năm 2019, chất có thể gây ung thư N-nitrosodimethylamine (NDMA) đã được phát hiện trong các chế phẩm Ranitidin từ một số nhà sản xuất, dẫn đến việc thu hồi.
Vào tháng 4 năm 2020, Ranitidin đã bị rút khỏi thị trường Hoa Kỳ và bị đình chỉ tại Liên minh Châu Âu và Úc do những lo ngại này.
Dược lý và cơ chế hoạt động
Ranitidin có tác dụng làm giảm quá trình tiết acid dịch vị do cơ thể nạp thêm thức ăn và do các thuốc gây kích thích.
Ranitidin cũng làm giảm tiết acid dịch vị trong các tình trạng tăng tiết như hội chứng Zollinger-Ellison.
Khi điều trị bằng Ranitidin, thông qua các hình ảnh nội soi có thể thấy được những cải thiện rõ rệt của các mô thực quản.
Sau bữa ăn, các hormone gastrin được sản xuất bởi các tế bào niêm mạc dạ dày, kích thích giải phóng histamin. Sau đó chúng tiến hành liên kết với thụ thể histamin H2, dẫn đến việc tiết ra acid dịch vị.
Ranitidin làm giảm bài tiết acid dịch vị theo cơ chế tương tự như thế hệ tiền nhiệm của nó Cimetidin bằng cách liên kết thuận nghịch (đối kháng) với thụ thể histamin (H2), được tìm thấy trên tế bào thành dạ dày. Quá trình này dẫn đến ức chế liên kết của histamin với thụ thể này, gây giảm tiết acid ở dạ dày cả ngày, đêm và cả khi bị kích thích bởi thức ăn hay do các tác nhân khác như acid amin, insulin, pentagastrin,… .
So với Cimetidin, Ranitidin có thể ức chế tiết acid mạnh hơn gấp 3 – 13 lần.
Khả năng làm giảm các triệu chứng liên quan đến tăng acid dạ dày có thể xảy ra ngay sau 60 phút sau khi dùng một liều duy nhất và tác dụng có thể kéo dài từ 4-10 giờ, giúp giảm triệu chứng nhanh chóng và hiệu quả.
Ngoài ra, Ranitidin còn có thể giúp bảo vệ niêm mạc dạ dày, chống xuất huyết dạ dày và các tác dụng kích thích do sử dụng các thuốc như Nsaids hay Aspirin.
Ứng dụng trong y học của Ranitidin
Ranitidin được sử dụng trong điều trị các chứng viêm loét dạ dày và tá tràng lành tính. Nguyễn nhân của vết loét có thể bao gồm cả do thuốc Nsaids, loét hậu phẫu thuật, hội chứng trào ngược thực quản, hội chứng Zollinger Ellison.
Ranitidin được sử dụng trong điều trị viêm loét tá tràng mà nguyên nhân là do vi khuẩn Helicobacter pylori ( HP).
Ranitidin còn có tác dụng hiệu quả trong điều trị các chứng khó tiêu mãn tính, được đặc trưng bởi các cơn đau (đau rát chủ yếu vùng thượng vị và vùng xương ức).
Ranitidin còn được sử dụng trong điều trị các tổn thương niêm mạc dạ dày (xuất huyết, ăn mòn, phù,.. trong một số bệnh lý: viêm dạ dày cấp tính, giai đoạn tiến triển cấp tính của bệnh lý viêm dạ dày mạn tính).
Ranitidin còn được sử dụng trong dự phòng tiền mê toàn thân ở những người có nguy cơ hít phải acid ( sặc acid) do hội chứng Mendelson, đặc biệt ở phụ nữ mang thai đang chuyển dạ.
Dược động học
Hấp thu
Ranitidin được hấp thu nhanh chóng với nồng độ đỉnh đạt được trong vòng 1-3 giờ sau khi dùng thuốc.
Sinh khả dụng khoảng 50% -60% do chuyển hóa ở gan.
Trong một nghiên cứu dược động học ở nam giới khỏe mạnh, AUC 0-vô cùng là khoảng 2.488,6 ng xh / mL và Tmax trung bình là 2,83 giờ.
Thức ăn hoặc thuốc kháng acid có tác dụng hạn chế sự hấp thu.
Phân bố
Thể tích phân phối cao hơn thể tích cơ thể, và đo ở mức xấp xỉ 1,4 L / kg.
Ranitidin nó có thể phân bố vào sữa mẹ, nhưng không dễ dàng phân phối vào dịch não tủy.
Khả năng liên kết với protein huyết tương của Ranitidin là khoảng 15%.
Chuyển hóa
Chất chuyển hóa chính trong nước tiểu là N-oxit, chiếm dưới 4% liều dùng. Các chất chuyển hóa khác của ranitidine bao gồm S-oxide (1%) và desmethyl ranitidine (1%).
Phân chứa phần còn lại của liều ranitidin được bài tiết.
Thải trừ
Ranitidin được thải trừ chủ yếu qua nước tiểu nhưng cũng thải trừ qua phân. Khoảng 30% liều uống duy nhất được đo trong nước tiểu dưới dạng thuốc không thay đổi trong vòng 24 giờ sau khi uống.
Thời gian bán thải của Ranitidin khoảng 2,5-3 giờ. Có thể lâu hơn sau khi uống so với đường tiêm.
Thời gian bán thải trong huyết tương dài hơn đối với nhóm bệnh nhân cao tuổi do chức năng thận giảm và được đo ở 3 – 4 giờ.
Độc tính của Ranitidin
Độc tính của Ranitidin được tìm thấy trên động vật
Liều uống 1.000 mg / kg ở chuột nhắt và chuột cống không gây chết người. Giá trị LD50 qua đường tĩnh mạch ở chuột nhắt và chuột cống lần lượt là 77 và 83 mg/kg.
Độc tính của Ranitidin tìm thấy ở người
Đã có báo cáo về độc tính khi dùng quá liều Ranitidin. Các tác dụng phụ cấp tính được báo cáo lên đến 18 gam bằng đường uống bao gồm nhịp tim nhanh, nhịp tim chậm, chóng mặt, tiêu chảy, buồn nôn, nôn mửa và một số các tác dụng khác.
Các bất thường về dáng đi và hạ huyết áp cũng đã được quan sát thấy. Khi nghi ngờ quá liều với Ranitidin, hãy ngưng dùng thuốc và loại bỏ thuốc ra khỏi đường tiêu hóa nếu có thể, đồng thời theo dõi bệnh nhân và đưa ra liệu pháp hỗ trợ theo yêu cầu.
Tương tác của Ranitidin với thuốc khác
Một số tương tác thuốc đã được tìm thấy khi dùng Ranitidin như sau:
Dùng chung Ranitidin với các thuốc như ketoconazol, itraconazol có thể làm giảm mức độ hấp thu và tác dụng của chống nấm azol này do làm tăng pH trong dạ dày.
Dùng chung Ranitidin với các thuốc atazanavir, cefuroxim, cefpodoxim, indinavir, fosamprenavir, mesalamin, nelfinavir, các muối sắt có thể làm giảm hấp thu và tác dụng của các thuốc này.
Dùng Ranitidin với saquinavir có thể làm tăng mức hấp thu và tác dụng của saquinavir.
| infigratinib | Dùng chung với các thuốc làm giảm axit dạ dày bao gồm các chất đối kháng thụ thể H2 có thể làm giảm nồng độ trong huyết tương của infigratinib | Major |
| atazanavir | Dùng đồng thời các thuốc đối kháng thụ thể H2 có thể làm giảm sinh khả dụng đường uống của atazanavir và làm giảm đáng kể nồng độ của nó trong huyết tương | Major |
| cefuroxim | Bằng cách làm giảm axit trong dạ dày, Ranitidin có thể làm giảm sự hấp thu và nồng độ cefuroxime trong máu và làm cho thuốc giảm hiệu quả chống lại nhiễm trùng. | Moderate |
| ketoconazol | Thuốc đối kháng H2 có thể làm giảm sinh khả dụng của ketoconazol dẫn đến giảm nồng độ ketoconazol trong huyết tương. Cơ chế này liên quan đến việc tăng pH dạ dày và giảm hấp thu chất chống nấm. | Moderate |
| itraconazol | Thuốc đối kháng H2 có thể làm giảm sinh khả dụng của itraconazol dẫn đến giảm nồng độ itraconazol trong huyết tương. Cơ chế này liên quan đến việc tăng pH dạ dày và giảm hấp thu chất chống nấm. | moderate |
| Diclofenac | Thuốc kháng H2 có thể thay đổi vị trí của thuốc chống viêm không steroid (NSAID), dẫn đến tăng hoặc giảm nồng độ thuốc trong huyết tương | minor |
Tương tác với thực phẩm
Thức ăn không ảnh hưởng đến khả năng hấp thu của Ranitidin.
Tuy nhiên, cần tránh sử dụng rượu. Vì uống rượu có thể gây kích ứng niêm mạc dạ dày do đó có thể làm giảm tác dụng của Ranitidin.
Lưu ý khi dùng Ranitidin
Lưu ý và thận trọng chung khi dùng Ranitidin
Ranitidin được đào thải chủ yếu qua thận nên khi sử dụng cho bệnh nhân bị suy thận thì có thể làm nồng độ thuốc trong huyết tương tăng cao. Do đó cần cân nhắc giảm liều ở người suy thận.
Cần tránh dùng Ranitidin cho bệnh nhân có tiền sử bị người suy gan nặng hoặc rối loạn chuyển hóa porphyrin cấp. Vì khi dùng Ranitidin cho những bệnh nhân này có nguy cơ tăng tác dụng không mong muốn.
Dùng Ranitidin cho người bị bệnh tim có thể dẫn đến nguy cơ làm chậm nhịp tim.
Điều trị bằng Ranitidin có thể làm che lấp đi các triệu chứng của ung thư dạ dày và có thể dẫn đến chẩn đoán sai bệnh này. Do đó, khi mắc loét dạ dày, cần phải lưu ý loại trừ khả năng mắc ung thư trước khi dùng Ranitidin.
Lưu ý khi dùng Ranitidin với phụ nữ có thai
Ranitidin có thể vượt qua được hàng rào nhau thai. Tuy nhiên, khi dùng với liều điều trị thì không thấy có tác động bất lợi nào đến người mẹ mang thai và thai nhi.
Lưu ý khi dùng Ranitidin với phụ nữ đang cho con bú
Ranitidin có thể vượt qua hàng rào sinh lý và bài tiết vào sữa mẹ. Vì thế cần cân nhắc khi dùng Ranitidin trong giai đoạn đang cho con bú.
Lưu ý khi dùng Ranitidin cho người lái xe và vận hành máy móc
Tác dụng không mong muốn là chóng mặt và buồn ngủ của Ranitidin đã được báo cáo. Vì vậy cần thận trọng khi dung Ranitidin cho người đang lái tàu xe hay vận hành máy móc.
Một vài nghiên cứu của Ranitidin trong Y học
Ảnh hưởng của Ranitidine uống lên bài tiết N-Nitrosodimethylamine trong nước tiểu (NDMA): Một thử nghiệm lâm sàng ngẫu nhiên.
Tầm quan trọng
Vào năm 2019, Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) đã nhận được đơn kiến nghị của công dân chỉ ra rằng ranitidine chứa chất N-nitrosodimethylamine có thể gây ung thư ở người (NDMA). Ngoài ra, người khởi kiện đề xuất rằng ranitidine có thể chuyển đổi thành NDMA ở người; tuy nhiên, điều này chủ yếu dựa trên một nghiên cứu lâm sàng nhỏ phát hiện sự gia tăng bài tiết NDMA qua nước tiểu sau khi uống ranitidine đường uống.
Mục tiêu
Đánh giá sự bài tiết NDMA qua nước tiểu trong 24 giờ sau khi uống ranitidine so với giả dược.

Thiết kế
Thử nghiệm lâm sàng chéo ngẫu nhiên, mù đôi, có đối chứng với giả dược, tại một đơn vị dược học lâm sàng (West Bend, Wisconsin) được thực hiện trên 18 người tham gia khỏe mạnh. Nghiên cứu bắt đầu vào tháng 6 năm 2020 và thời gian kết thúc theo dõi người tham gia là ngày 1 tháng 7 năm 2020.
Can thiệp
Những người tham gia được chọn ngẫu nhiên vào 1 trong 4 trình tự điều trị và qua 4 giai đoạn nhận ranitidine (300 mg) và giả dược (thứ tự ngẫu nhiên) với chế độ ăn không thịt và sau đó là chế độ ăn thịt đã được chữa khỏi. Chế độ ăn kiêng thịt đã qua xử lý được thiết kế để có nhiều nitrit hơn, nitrat (vi khuẩn khử nitrat có thể chuyển nitrat thành nitrit) và NDMA.
Kết quả
Trong số 18 người tham gia được chọn ngẫu nhiên (tuổi trung bình, 33,0 [khoảng tứ phân vị {IQR}, 28,3 đến 42,8] tuổi; 9 phụ nữ [50%]; 7 người da trắng [39%], 11 người Mỹ gốc Phi [61%]; và 3 dân tộc Tây Ban Nha hoặc Latinh [17%]), 17 (94%) hoàn thành thử nghiệm. Giá trị bài tiết qua nước tiểu NDMA trung bình trong 24 giờ đối với ranitidine và giả dược lần lượt là 0,6 ng (IQR, 0 đến 29,7) và 10,5 ng (IQR, 0 đến 17,8) với chế độ ăn không có thịt và 11,9 ng (IQR, 5,6 đến 48,6) và 23,4 ng (IQR, 8,6 đến 36,7), tương ứng với chế độ ăn kiêng thịt. Không có sự khác biệt có ý nghĩa thống kê giữa ranitidine và giả dược trong việc bài tiết NDMA qua nước tiểu trong 24 giờ với chế độ ăn không có thịt (trung bình của sự khác biệt được ghép nối, 0 [IQR, -6,9 đến 0] ng; P = 0,54) hoặc được chữa khỏi -chế độ ăn kiêng (trung bình của sự khác biệt được ghép nối, -1,1 [IQR, -9,1 đến 11,5] ng; P = 0,71).
Kết luận và mức độ liên quan
Trong thử nghiệm này bao gồm 18 người tham gia khỏe mạnh, ranitidine uống (300 mg), so với giả dược, không làm tăng đáng kể lượng NDMA bài tiết qua nước tiểu trong 24 giờ khi những người tham gia tiêu thụ chế độ ăn không ướp thịt hoặc thịt đã qua xử lý. Các phát hiện không ủng hộ rằng ranitidine được chuyển đổi thành NDMA trong dân số nói chung, khỏe mạnh.
Tài liệu tham khảo
1. Drugbank, Ranitidin, truy cập ngày 12 tháng 6 năm 2022.
2. Pubchem, Ranitidin, truy cập ngày 12 tháng 6 năm 2022.
3. Bộ Y Tế (2012), Dược thư quốc gia Việt Nam, Nhà xuất bản Y học, Hà Nội
4. Florian, J., Matta, M. K., DePalma, R., Gershuny, V., Patel, V., Hsiao, C. H., … & Strauss, D. G. (2021). Effect of oral ranitidine on urinary excretion of N-nitrosodimethylamine (NDMA): a randomized clinical trial. Jama, 326(3), 240-249.
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Hàn Quốc
Xuất xứ: Italy
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Cộng Hòa Síp