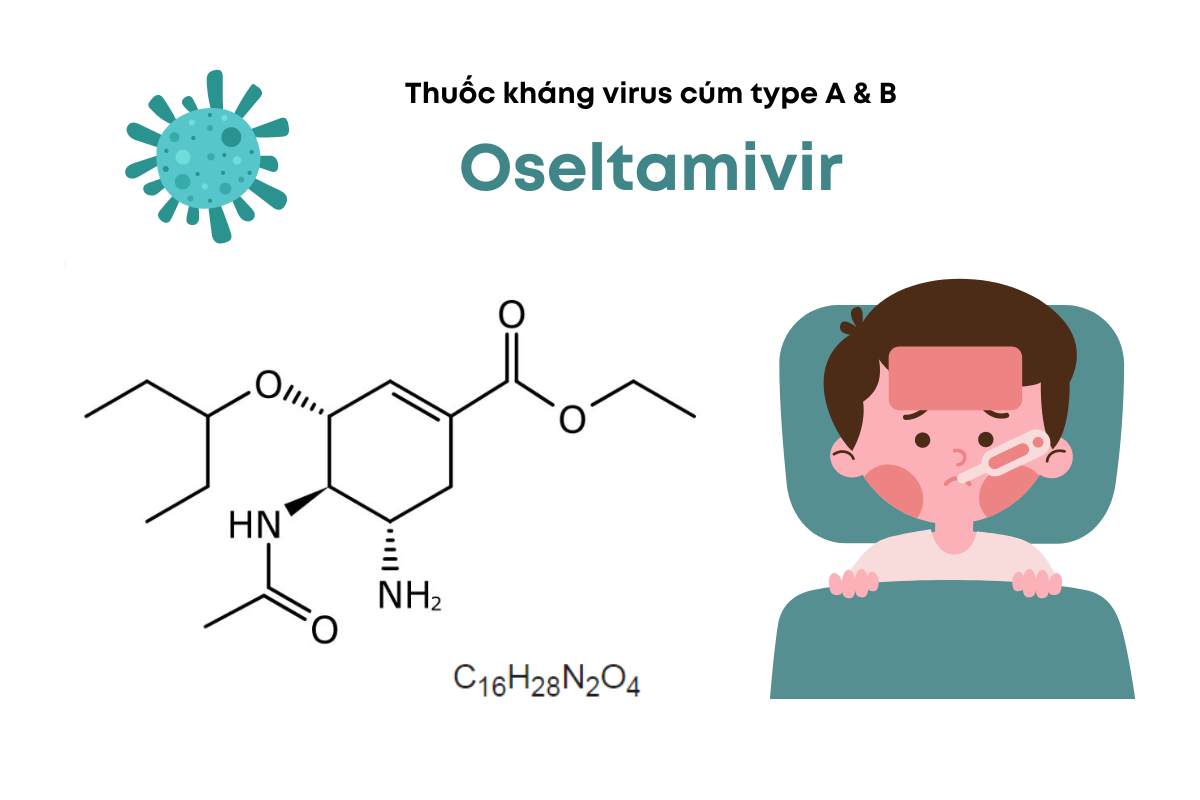
Oseltamivir
Biên soạn và Hiệu đính
Dược sĩ Phan Hữu Xuân Hạo – Khoa Dược, Trường Y Dược – Đại học Duy Tân.
Danh pháp
Tên chung quốc tế
Oseltamivir
Tên danh pháp theo IUPAC
ethyl (3R,4R,5S)-4-acetamido-5-amino-3-pentan-3-yloxycyclohexene-1-carboxylate
Nhóm thuốc
Thuốc kháng virus cúm type A và B
Mã ATC
J – Thuốc kháng khuẩn tác dụng toàn thân
J05 – Thuốc kháng virus sử dụng toàn thân
J05A – Thuốc kháng virus tác động trực tiếp
J05AH – Thuốc ức chế Neuraminidase
J05AH02 – Oseltamivir
Phân loại nguy cơ cho phụ nữ có thai
Nhóm C
Mã UNII
20O93L6F9H
Mã CAS
196618-13-0
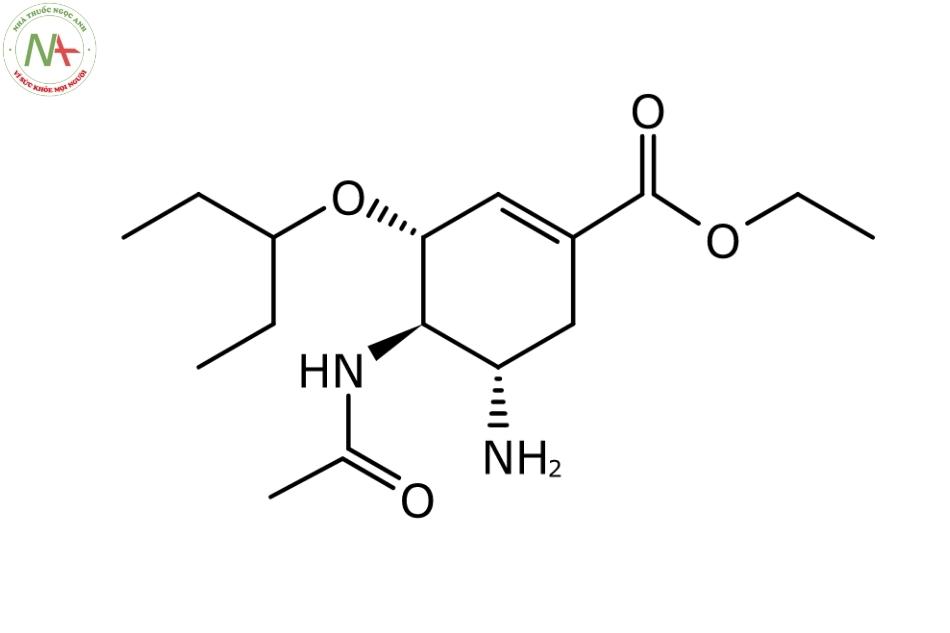
Cấu trúc phân tử
Công thức phân tử
C16H28N2O4
Phân tử lượng
312.40 g/mol
Cấu trúc phân tử
Oseltamivir là một este cyclohexanecarboxylate và là este etylic của axit oseltamivir.
Các tính chất phân tử
Số liên kết hydro cho: 2
Số liên kết hydro nhận: 5
Số liên kết có thể xoay: 8
Diện tích bề mặt tôpô: 90.6 Ų
Số lượng nguyên tử nặng: 22
Các tính chất đặc trưng
Điểm sôi: 473.3°C
Tỷ trọng riêng: 1.1 ± 0.1 g/cm3
Độ tan trong nước: 0.686 mg/mL
Hằng số phân ly pKa: 9.31
Chu kì bán hủy: 1 – 3 giờ
Khả năng liên kết với Protein huyết tương: 42%
Cảm quan
Oseltamivir có dạng bột kết tinh màu trắng, tan được trong nước.
Dạng bào chế
Viên nang: 30 mg; 45 mg; 75 mg.
Bột: 6 mg/ml.
Độ ổn định và điều kiện bảo quản
Dạng thuốc viên của oseltamivir nên được bảo quản ở nhiệt độ từ 15 đến 30 °C, tránh ẩm mốc.
Dạng thuốc nước sau khi pha nên được bảo quản trong tủ lạnh 2 – 8 °C, không được để đóng băng và phải dùng trong vòng 10 ngày, nếu thừa phải bỏ đi.
Nguồn gốc
Oseltamivir được các nhà khoa học tại Gilead Sciences phát hiện ra bằng cách sử dụng axit shikimic làm điểm khởi đầu cho quá trình tổng hợp. Theo đó, axit shikimic ban đầu chỉ có sẵn dưới dạng chiết xuất từ đại hồi (bát giác hồi hương) – một loại dược liệu phổ biến ở Trung Quốc nhưng đến năm 2006, 30% nguồn cung cấp axit shikimic được sản xuất tái tổ hợp từ E. coli.
Năm 1999, oseltamivir được FDA phê duyệt cho điều trị cúm ở người lớn và đến tháng 6/2002, EMA cũng phê duyệt oseltamivir cho dự phòng và điều trị cúm. Sau đó, một phân tích tổng hợp từ 10 thử nghiệm lâm sàng ngẫu nhiên vào năm 2003 đã kết luận rằng oseltamivir làm giảm nguy cơ nhiễm trùng đường hô hấp dưới ở người trưởng thành.
Oseltamivir dưới tên thương mại là “Tamiflu” đã được sử dụng rộng rãi trong các dịch cúm gia cầm H5N1 ở Đông Nam Á vào năm 2005. Chính phủ của Vương quốc Anh, Canada, Hoa Kỳ và Úc cũng đã dự trữ một lượng lớn oseltamivir để đề phòng dịch bệnh lớn có thể xảy ra.
Theo đó, vào tháng 11/2005, Tổng thống Hoa Kỳ lúc này là George W. Bush đã yêu cầu Quốc hội tài trợ 1 tỷ USD cho việc sản xuất và dự trữ oseltamivir, sau khi Quốc hội phê duyệt 1.8 tỷ USD cho việc sử dụng thuốc trong quân đội. Tuy nhiên, một nhận xét của Cochrane vào năm 2006 đã gây tranh cãi khi đưa ra kết luận không nên sử dụng oseltamivir trong bệnh cúm theo mùa thông thường vì hiệu quả điều trị thấp.
Vào tháng 12/2008, một công ty dược ở Ấn Độ tên là Cipla đã thắng một vụ kiện mà từ đó cho phép công ty này sản xuất một phiên bản rẻ hơn của Tamiflu, gọi là Antiflu. Đến tháng 5/2009, Cipla đã nhận được sự chấp thuận của WHO khi xác nhận rằng thuốc Antiflu có hiệu quả tương đương với Tamiflu và được đưa vào danh sách các loại thuốc được sơ tuyển của WHO.
Năm 2009, một loại virus cúm mới là A/H1N1 được phát hiện và đang lan rộng ở Bắc Mỹ. Đến tháng 6/2009, WHO tuyên bố cúm A/H1N1 là đại dịch. Do đó, Viện Y tế và Chất lượng Điều trị Quốc gia Anh (NICE), Trung tâm Kiểm soát và Phòng ngừa Dịch bệnh Hoa Kỳ (CDC), WHO và Trung tâm Kiểm soát và Phòng ngừa Dịch bệnh châu Âu (ECDC) đã duy trì khuyến nghị cho sử dụng oseltamivir.
Vào giai đoạn 2010 – 2012, Cochrane đã yêu cầu các báo cáo nghiên cứu lâm sàng đầy đủ của Roche về các thử nghiệm mà họ không cung cấp. Đến năm 2011, Cơ quan Dược phẩm Châu Âu đã cung cấp cho Cochrane các báo cáo từ 16 thử nghiệm của Roche về oseltamivir. Sau đó, nhóm nghiên cứu của Cochrane đã công bố đánh giá tạm thời dựa trên các báo cáo này vào năm 2012.
Một năm sau, Roche cũng đã công bố 77 báo cáo nghiên cứu lâm sàng đầy đủ về các thử nghiệm lâm sàng với oseltamivir sau khi GSK công bố dữ liệu của các nghiên cứu về zanamivir.
Roche đã được hưởng lợi hơn 18 tỷ USD từ oseltamivir kể từ khi ra mắt vào năm 1999. Theo đó, doanh số của oseltamivir tăng 84% trong đợt cúm ở Hoa Kỳ vào năm 2013. Vương quốc Anh đã dự trữ 40 triệu liều oseltamivir với trị giá 710 triệu USD và Hoa Kỳ cũng đã chi 1,3 tỷ USD để dự trữ 65 triệu liều oseltamivir. Tương tự, Ấn Độ cũng tăng lượng thuốc dự trữ trong kho của mình lên 10 lần.
Đến năm 2016, bằng sáng chế về oseltamivir của Roche hết hạn.
Dược lý và cơ chế hoạt động
Oseltamivir là tiền chất của oseltamivir carboxylate (chất chuyển hóa có hoạt tính của thuốc), có tác dụng ngăn cản virus cúm mới hình thành thoát ra khỏi tế bào vật chủ và xâm nhập vào tế bào lành. Theo đó, oseltamivir carboxylate có khả năng ức chế chọn lọc enzyme neuraminidase của virus, một enzym có vai trò thiết yếu trong việc cắt liên kết giữa carbohydrate và acid sialic, làm cho virus không tách được ra khỏi tế bào vật chủ và đi lây nhiễm cho các tế bào khác.
Enzyme này có bản chất là glycoprotein, là một kháng nguyên của virus có tên hệ thống là EC 3.2.1.18. Ngoài ra, neuraminidase của virus cúm A có 9 phân nhóm nhỏ hơn đã được phát hiện.
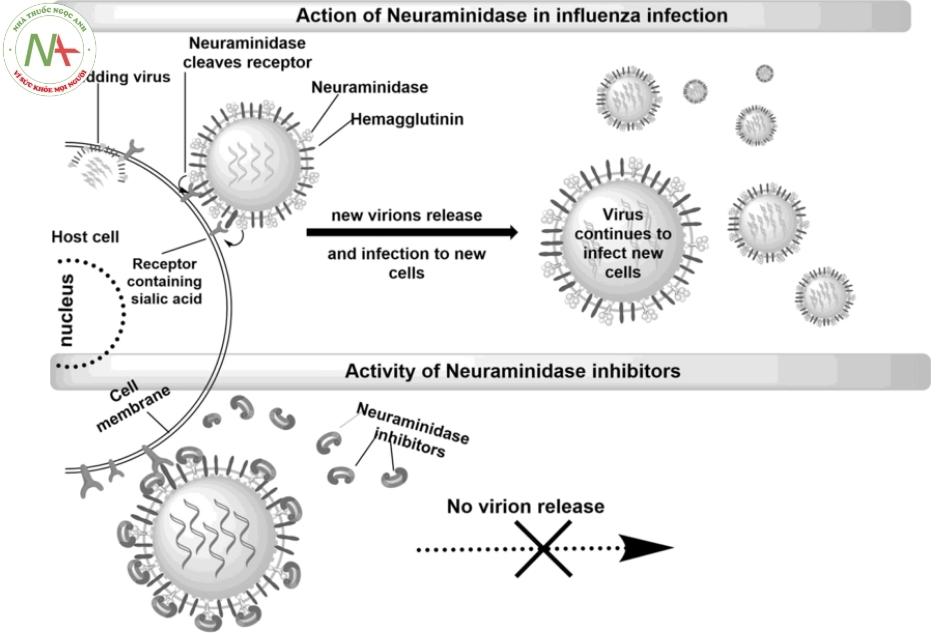
(b) Sự nhân lên của virus cúm A khi có mặt các chất ức chế neurominidase
Vì chu kỳ nhân lên của virus ở đường hô hấp là 24 – 72 giờ sau khi xuất hiện triệu chứng nên các thuốc ức chế neuraminidase nói chung phải được sử dụng càng sớm càng tốt. Tuy nhiên, có một tỷ lệ thấp virus cúm type A giảm nhạy cảm với oseltamivir carboxylate nhưng hiện tượng này chưa được ghi nhận ở virus cúm type B.
Ứng dụng trong y học
Oseltamivir được sử dụng để phòng ngừa và điều trị bệnh cúm do virus cúm A và B. Theo đó, oseltamivir nằm trong Danh sách Thuốc thiết yếu của Tổ chức Y tế Thế giới và được WHO ủng hộ sử dụng đối với bệnh nặng do nhiễm virus cúm đã được xác nhận hoặc nghi ngờ ở những người bị bệnh nặng cần phải nhập viện. Tuy nhiên, tỷ lệ giữa lợi ích và nguy cơ của oseltamivir đang gây tranh cãi. Do đó, oseltamivir đã được chuyển từ danh sách cốt lõi sang danh sách bổ sung dựa trên hiệu quả chi phí thấp hơn vào năm 2017.
Những người có nguy cơ nhiễm cúm cao
Trung tâm Kiểm soát và Phòng ngừa Dịch bệnh Hoa Kỳ (CDC) và châu Âu (ECDC), Y tế Công cộng Anh (PHE) và Học viện Nhi khoa Hoa Kỳ (AAP) đã khuyến cáo sử dụng oseltamivir cho những người bị biến chứng hoặc có nguy cơ cao bị các biến chứng. Khuyến cáo này bao gồm cả những người đang nằm viện, trẻ nhỏ, người trên 65 tuổi, người có các vấn đề sức khỏe nghiêm trọng khác, người đang mang thai, người bản địa châu Mỹ và cùng những người khác.
Tuy nhiên, một đánh giá tổng quan có hệ thống trong PLoS One đã không tìm thấy bằng chứng về lợi ích ở những người có nguy cơ và lưu ý rằng “Các thử nghiệm không được thiết kế hoặc cung cấp để đưa ra kết quả liên quan đến các biến chứng nghiêm trọng, nhập viện và tử vong”, tương tự như Tổng quan Cochrane năm 2014.
Tổng quan Cochrane cũng khuyến cáo thêm rằng: “Trên cơ sở các phát hiện của tổng quan này, các bác sĩ lâm sàng và các nhà hoạch định chính sách chăm sóc sức khỏe nên khẩn trương thay đổi các khuyến nghị hiện tại về việc sử dụng các chất ức chế neuraminidase (NIs) cho những người bị cúm”.
Sau đó, CDC, ECDC, PHE, Hiệp hội Bệnh truyền nhiễm Hoa Kỳ (IDSA), AAP, và Roche (người khởi xướng) đã bác bỏ kết luận này, một phần lập luận rằng phân tích đưa ra kết luận không thích hợp về kết quả ở những người bị bệnh nặng dựa trên kết quả thu được chủ yếu ở những người khỏe mạnh, và phân tích bao gồm kết quả từ những người không bị nhiễm cúm một cách thích hợp. Do đó, EMA đã không thay đổi nhãn thuốc theo nghiên cứu của Cochrane.
Mặt khác, một đánh giá năm 2014 trên Tạp chí Y học New England đã khuyến cáo rằng tất cả bệnh nhân được nhận vào phòng chăm sóc đặc biệt trong thời gian bùng phát dịch cúm với chẩn đoán viêm phổi mắc phải tại cộng đồng nên được dùng oseltamivir cho đến khi không có nhiễm cúm được xác định bằng xét nghiệm PCR.
Hơn nữa, một đánh giá có hệ thống và phân tích tổng hợp năm 2015 cho thấy oseltamivir có hiệu quả trong việc điều trị các triệu chứng của bệnh cúm, làm giảm thời gian nằm viện và giảm nguy cơ bị viêm tai giữa. Đánh giá tương tự cũng cho thấy oseltamivir không làm tăng đáng kể nguy cơ xảy ra các tác dụng phụ.
Trong khi đó, một đánh giá có hệ thống năm 2016 cho thấy oseltamivir có khả năng làm giảm nhẹ thời gian để giảm bớt các triệu chứng của bệnh cúm nhưng làm tăng nguy cơ “buồn nôn, nôn và các biến cố tâm thần ở người lớn và nôn mửa ở trẻ em”. Theo đó, thời gian bị ốm giảm khoảng 18 giờ.
Những người khỏe mạnh
Ở những người khỏe mạnh, CDC tuyên bố rằng thuốc kháng virus có thể được cân nhắc trong vòng 48 giờ đầu tiên. Tuy nhiên, một hướng dẫn thực hành lâm sàng của Đức đã khuyến cáo không nên sử dụng nó.
Hai phân tích tổng hợp vào năm 2013 đã kết luận rằng, lợi ích ở những người khỏe mạnh không lớn hơn so với nguy cơ. Hơn nữa, khi phân tích chỉ giới hạn ở những người đã được xác nhận nhiễm trùng, Tổng quan Cochrane vào năm 2014 (xem ở trên) đã tìm thấy bằng chứng không rõ ràng về sự thay đổi nguy cơ của biến chứng như viêm phổi, trong khi ba tổng quan khác cho thấy nguy cơ giảm.
Kết hợp lại với nhau, các nghiên cứu đã được công bố cho thấy rằng oseltamivir có thể làm giảm thời gian của các triệu chứng 0,5 – 1,0 ngày. Tuy nhiên, bất kỳ lợi ích nào của việc điều trị cũng phải được cân bằng với các tác dụng phụ, bao gồm cả các triệu chứng tâm thần và tỷ lệ nôn mửa tăng lên.
Mặt khác, đánh giá của Cochrane Collaboration vào năm 2014 kết luận rằng oseltamivir không ảnh hưởng đến nhu cầu nhập viện và cũng không có bằng chứng về việc giảm các biến chứng của cúm như viêm phổi vì thiếu các định nghĩa chẩn đoán hoặc giảm sự lây lan của virus.
Hơn nữa, cũng có bằng chứng cho thấy rằng oseltamivir ngăn sản xuất đủ số lượng kháng thể ở một số người để chống lại nhiễm trùng. Do đó, các tác giả khuyến nghị rằng hướng dẫn nên được sửa đổi để tính đến bằng chứng về lợi ích nhỏ và nguy cơ tác hại tăng lên. Tuy nhiên, CDC, ECDC, PHE, IDSA, AAP và Roche đã bác bỏ các khuyến nghị này.
Dự phòng
Kể từ năm 2017, CDC đã không còn khuyến nghị sử dụng oseltamivir nói chung để phòng ngừa do lo ngại rằng việc sử dụng rộng rãi sẽ gây ra tình trạng kháng thuốc. Họ khuyến cáo rằng, oseltamivir nên được cân nhắc ở những người có nguy cơ cao, những người đã tiếp xúc với virus cúm trong vòng 48 giờ và chưa được tiêm chủng hoặc chỉ mới được tiêm chủng gần đây. Đồng thời, CDC cũng khuyến cáo oseltamivir trong các đợt bùng phát ở các cơ sở chăm sóc dài hạn và ở những người bị ức chế miễn dịch đáng kể.
Tính đến năm 2011, các đánh giá kết luận rằng khi oseltamivir được sử dụng như một biện pháp phòng ngừa, thuốc có khả năng làm giảm nguy cơ ở những người tiếp xúc khởi phát bệnh có triệu chứng. Một đánh giá tổng quan có hệ thống với chất lượng bằng chứng từ thấp đến trung bình cho thấy oseltamivir làm giảm nguy cơ mắc bệnh cúm có triệu chứng từ 1 – 12% (giảm tương đối từ 64 đến 92%).
Tuy nhiên, oseltamivir được khuyến cáo không nên sử dụng cho những người khỏe mạnh, ít có rủi ro do chi phí, nguy cơ gây kháng thuốc và các tác dụng phụ. Kết luận được đưa ra rằng thuốc có thể hữu ích để phòng ngừa ở những người có nguy cơ cao chưa được tiêm chủng.
Dược động học
Hấp thu
Oseltamivir được hấp thu tốt ở ống tiêu hóa và được chuyển hóa lần đầu tại gan thành chất chuyển hóa có hoạt tính là oseltamivir carboxylate. Cả oseltamivir và oseltamivir carboxylate đều không có tác động nào lên hệ thống enzyme của cytochrom P450.
Thức ăn không ảnh hưởng đến nồng độ của oseltamivir trong máu. Sinh khả dụng của thuốc sau khi uống liều 75mg là trên 75% và nồng độ đỉnh trong huyết thanh đạt được là 348 ± 63 microgam/lít trong vòng 2 – 3 giờ.
Phân bố
Thể tích phân bố của oseltamivir carboxylate là khoảng 23 – 26 lít với tỷ lệ liên kết với protein huyết tương là 3%. Ngoài ra, khoảng 42% liều thuốc ở dạng nguyên vẹn cũng có khả năng gắn vào protein huyết tương.
Chuyển hóa
Oseltamivir carboxylate không bị chuyển hóa.
Thải trừ
Thời gian bán thải của oseltamivir là 1 – 3 giờ và của oseltamivir carboxylate là 6 – 10 giờ. Hơn 99% lượng oseltamivir carboxylate được đào thải qua nước tiểu.
Độc tính ở người
Các phản ứng có hại của thuốc (ADR) thường gặp liên quan đến liệu pháp oseltamivir bao gồm buồn nôn và nôn. Ở người lớn, oseltamivir có thể làm tăng nguy cơ buồn nôn với số lượng cần thiết để gây hại là 28 và đối với nôn là 22. Nghĩa là cứ 22 người trưởng thành dùng oseltamivir thì có một người bị nôn. Khi điều trị cho trẻ em, oseltamivir cũng có khả năng gây nôn và con số cần thiết để gây hại là 19.
Khi sử dụng phòng ngừa, oseltamivir cũng gây ra nhiều biến cố như đau đầu, thận và tâm thần. Mặc dù tác dụng của oseltamivir trên tim không rõ ràng nhưng thuốc có thể làm giảm các triệu chứng tim hoặc cũng có thể gây loạn nhịp tim nghiêm trọng.
Các báo cáo được ghi nhận sau khi đưa thuốc ra thị trường bao gồm: Viêm gan và tăng men gan, phát ban, sốc phản vệ, hoại tử biểu bì nhiễm độc, nhịp tim bất thường, co giật, lú lẫn, làm nặng thêm bệnh đái tháo đường, viêm đại tràng xuất huyết và hội chứng Stevens – Johnson.
Ngoài ra, các hướng dẫn của Hoa Kỳ và EU cho oseltamivir cũng có cảnh báo về các tác động tâm thần nhưng tần suất của những trường hợp này dường như thấp và vai trò gây bệnh của oseltamivir chưa được xác định. Tuy nhiên, Tổng quan Cochrane năm 2014 cho thấy các biến cố này thường đáp ứng với liều. Theo đó, trong các thử nghiệm phòng ngừa ở người lớn, cứ 94 người được điều trị thì có một người có triệu chứng.
Tính an toàn
Oseltamivir được chống chỉ định đối với người bệnh dị ứng với bất kỳ thành phần nào của thuốc, người bệnh suy thận nặng có độ thanh thải creatinin dưới 10 ml/phút cũng như người bệnh đang chạy thận nhân tạo.
Tính an toàn của oseltamivir đối với phụ nữ có thai chưa được xác định, do đó chỉ sử dụng thuốc sau khi cân nhắc giữa các yếu tố lợi ích – nguy cơ. Hơn nữa, mặc dù khả năng phân bố của thuốc vào sữa mẹ ở người vẫn chưa rõ nhưng các thử nghiệm trên động vật cho thấy oseltamivir có thể bài tiết vào sữa. Vì vậy, phụ nữ đang cho con bú không nên sử dụng thuốc hoặc ngừng cho con bú khi bắt buộc phải sử dụng oseltamivir.
Tương tác với thuốc khác
Oseltamivir rất ít gắn vào protein huyết tương và được chuyển hóa không phụ thuộc vào cytochrom P450, do đó hầu như không tương tác với các thuốc khác kích thích hoặc ức chế P450 như paracetamol, aspirin, acid acetylsalicylic, các thuốc kháng acid (có magnesi, nhôm hydroxyd, calci carbonat) và các thuốc chống đông máu.
Oseltamivir sử dụng đồng thời với các thuốc được thải trừ qua thận như amoxicillin, clorpropamid, methotrexate và phenylbutazon có thể xảy ra tương tác dược động học. Vì vậy vẫn cần chú ý khi dùng đồng thời các thuốc này mặc dù chưa thấy tương tác nào có ý nghĩa lâm sàng quan trọng.
Oseltamivir sử dụng đồng thời với probenecid có thể làm tăng nồng độ của oseltamivir carboxylate do sự bài tiết ở ống thận giảm. Tuy nhiên, với liều oseltamivir thường dùng thì tương tác này không có ý nghĩa lâm sàng quan trọng.
Oseltamivir có thể được sử dụng đồng thời với vắc xin bất hoạt để phòng cúm.
Lưu ý khi sử dụng Oseltamivir
Oseltamivir nên được sử dụng thận trọng ở người bệnh suy gan.
Ở người bệnh suy thận vừa hoặc nặng, cần giảm liều và theo dõi cẩn thận. Nếu độ thanh thải creatinin là 10 – 30 ml/phút, phải giảm liều điều trị còn 75 mg/ngày và uống trong vòng 5 ngày.
Ở người mắc bệnh bẩm sinh không dung nạp fructose, cần thận trọng khi sử dụng oseltamivir vì lượng sorbitol có trong thành phần của chế phẩm dạng nước cao hơn so với liều giới hạn.
Cần theo dõi người bệnh về các biểu hiện thần kinh – tâm thần vì đã có báo cáo cho thấy có người bệnh bị rối loạn thần kinh – tâm thần ở Nhật Bản như tự gây thương tích, có hành vi bất thường, hoang tưởng, lú lẫn và động kinh.
Thận trọng khi sử dụng thuốc đối với phụ nữ mang thai vì mặc dù dữ liệu dịch tễ học cho thấy oseltamivir không làm tăng nguy cơ dị tật bẩm sinh ở thai nhi trong bất kỳ giai đoạn nào của thai kỳ, tuy nhiên các nghiên cứu này bị giới hạn ở cỡ mẫu nhỏ, sử dụng các nhóm so sánh khác nhau và thiếu một số thông tin về liều dùng. Hơn nữa, các nghiên cứu này cũng loại trừ đánh giá chính xác về rủi ro.
Thận trọng khi sử dụng thuốc đối với phụ nữ đang cho con bú vì dữ liệu được công bố hạn chế đã cho thấy oseltamivir hiện diện trong sữa mẹ ở nồng độ thấp. Mặc dù điều này được coi là không có khả năng gây độc tính cho trẻ bú mẹ và cũng không có báo cáo nào cho thấy tác dụng phụ nghiêm trọng đối với việc phơi nhiễm thuốc qua sữa mẹ ở trẻ sơ sinh.
Một vài nghiên cứu của Oseltamivir trong Y học
Điều trị cúm bằng Oseltamivir ngoài các khuyến cáo được dán nhãn
Mục đích: Các bằng chứng đã công bố liên quan đến việc sử dụng thuốc chống cúm oseltamivir ngoài các khuyến nghị về liều lượng tiêu chuẩn được xem xét.
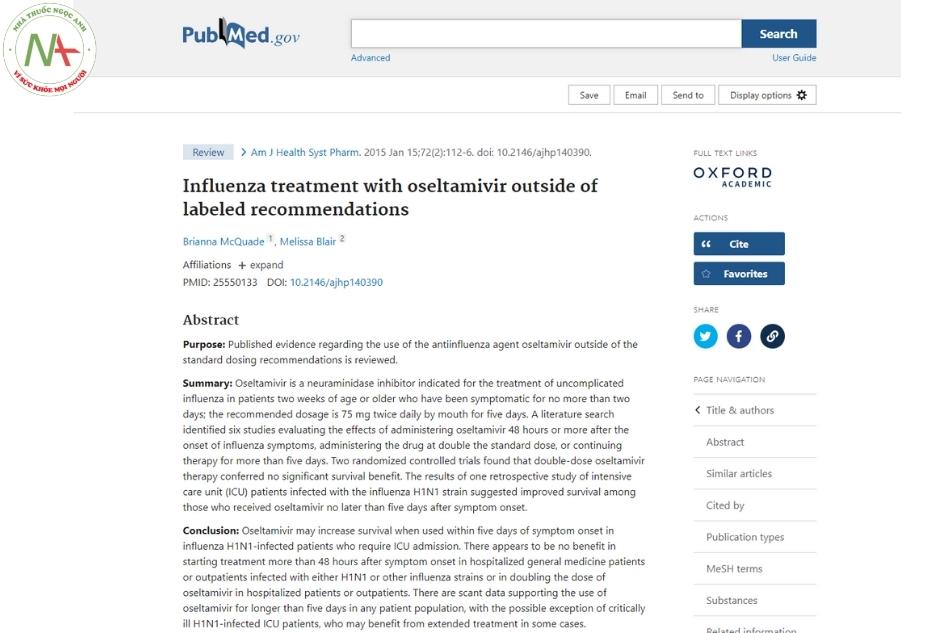
Tóm tắt: Oseltamivir là một chất ức chế neuraminidase được chỉ định để điều trị bệnh cúm không biến chứng ở bệnh nhân từ hai tuần tuổi trở lên đã có triệu chứng không quá hai ngày; liều khuyến cáo là 75 mg x 2 lần / ngày, uống trong 5 ngày.
Một tìm kiếm tài liệu đã xác định sáu nghiên cứu đánh giá tác dụng của việc sử dụng oseltamivir 48 giờ hoặc hơn sau khi bắt đầu các triệu chứng cúm, sử dụng thuốc với liều gấp đôi liều tiêu chuẩn hoặc tiếp tục điều trị trong hơn năm ngày. Hai thử nghiệm ngẫu nhiên có đối chứng cho thấy liệu pháp oseltamivir liều gấp đôi không mang lại lợi ích sống còn đáng kể.
Kết quả của một nghiên cứu hồi cứu bệnh nhân tại đơn vị chăm sóc đặc biệt (ICU) bị nhiễm chủng cúm H1N1 cho thấy khả năng sống sót được cải thiện ở những người được dùng oseltamivir không muộn hơn năm ngày sau khi bắt đầu có triệu chứng.
Kết luận: Oseltamivir có thể tăng khả năng sống sót khi được sử dụng trong vòng năm ngày kể từ khi khởi phát triệu chứng ở những bệnh nhân nhiễm cúm H1N1 yêu cầu nhập viện ICU.
Dường như không có lợi ích khi bắt đầu điều trị hơn 48 giờ sau khi bắt đầu có triệu chứng ở bệnh nhân điều trị nội khoa nhập viện hoặc bệnh nhân ngoại trú bị nhiễm H1N1 hoặc các chủng cúm khác hoặc khi tăng gấp đôi liều oseltamivir ở bệnh nhân nhập viện hoặc bệnh nhân ngoại trú.
Có rất ít dữ liệu ủng hộ việc sử dụng oseltamivir trong thời gian dài hơn năm ngày ở bất kỳ đối tượng bệnh nhân nào, ngoại trừ những bệnh nhân ICU nhiễm H1N1 bị bệnh nặng, những người này có thể được hưởng lợi từ việc điều trị kéo dài trong một số trường hợp.
Tài liệu tham khảo
- 1. Drugbank, Oseltamivir, truy cập ngày 15 tháng 7 năm 2022.
- 2. McKimm‐Breschkin, J. L. (2013). Influenza neuraminidase inhibitors: antiviral action and mechanisms of resistance. Influenza and other respiratory viruses, 7, 25-36.
- 3. McQuade, B., & Blair, M. (2015). Influenza treatment with oseltamivir outside of labeled recommendations. American journal of health-system pharmacy : AJHP : official journal of the American Society of Health-System Pharmacists, 72(2), 112–116. https://doi.org/10.2146/ajhp140390
- 4. Pubchem, Oseltamivir, truy cập ngày 15 tháng 7 năm 2022.
- 5. Bộ Y Tế (2012), Dược thư quốc gia Việt Nam, Nhà xuất bản Y học, Hà Nội
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Ý