Exemestane
Danh pháp
Tên chung quốc tế
Tên danh pháp theo IUPAC
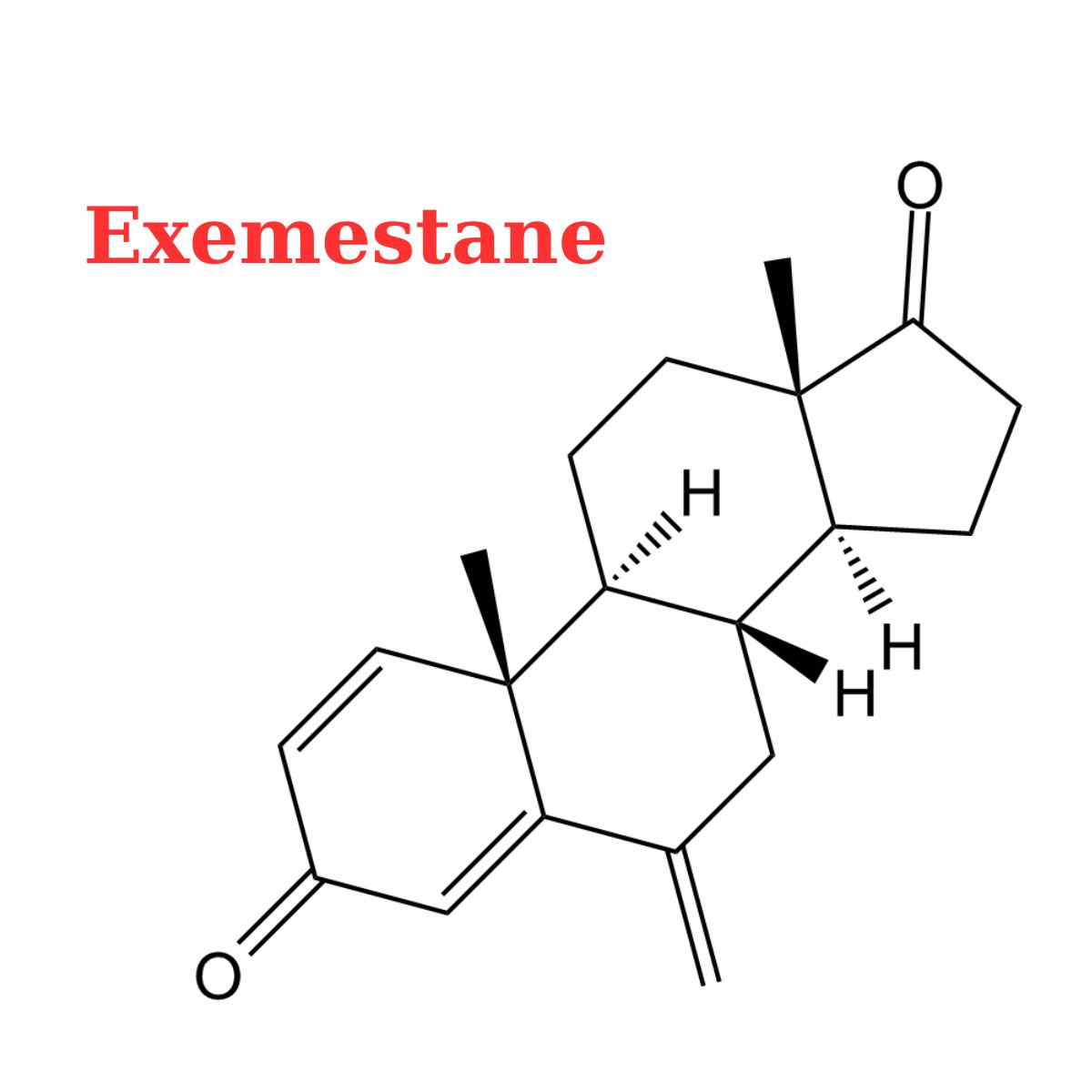
(8R,9S,10R,13S,14S)-10,13-dimethyl-6-methylidene-7,8,9,11,12,14,15,16-octahydrocyclopenta[a]phenanthrene-3,17-dione
Nhóm thuốc
Thuốc chống ung thư, ức chế aromatase
Mã ATC
L – Chất chống ung thư và điều hòa miễn dịch
L02 – Liệu pháp nội tiết
L02B – Thuốc đối kháng nội tiết tố và các chất liên quan
L02BG – Chất ức chế Aromatase
L02BG06 – Exemestane
Phân loại nguy cơ cho phụ nữ có thai
X
Mã UNII
NY22HMQ4BX
Mã CAS
107868-30-4
Cấu trúc phân tử
Công thức phân tử
C20H24O2
Phân tử lượng
296.4 g/mol
Cấu trúc phân tử
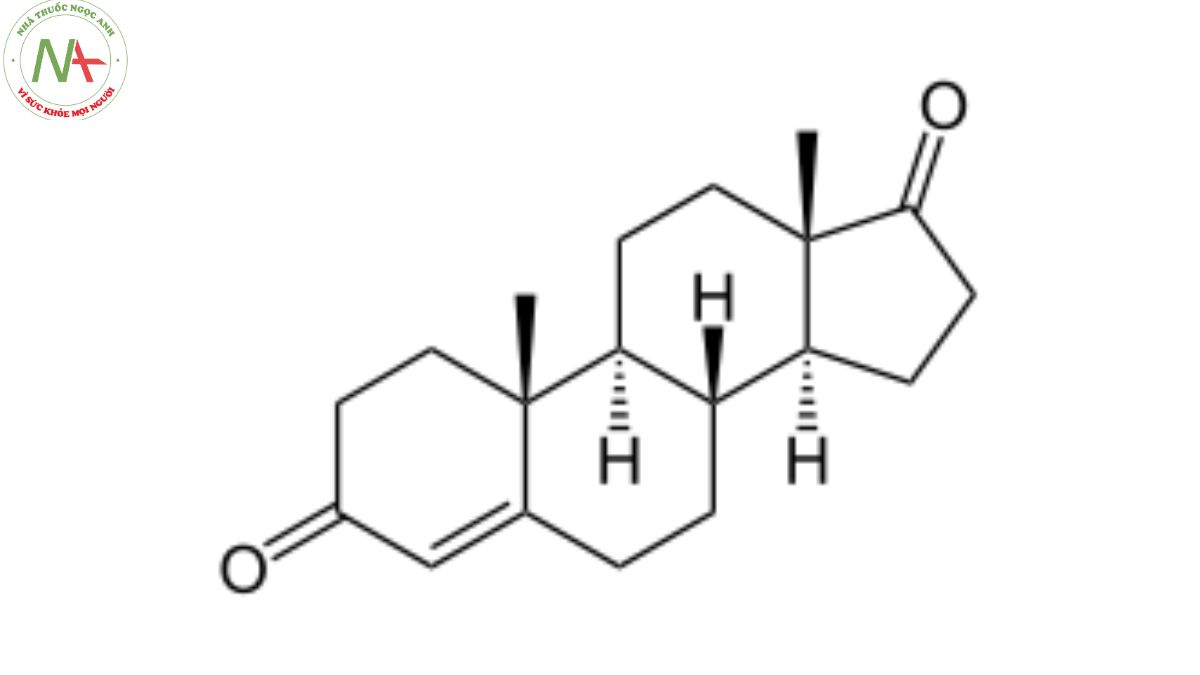
Exemestane là một steroid 17-oxo có cấu trúc là androsta-1,4-diene-3,17-dione trong đó hydrogens ở vị trí 6 được thay thế bằng liên kết đôi với nhóm methylene.
Các tính chất phân tử
Số liên kết hydro cho: 0
Số liên kết hydro nhận: 2
Số liên kết có thể xoay: 0
Diện tích bề mặt tôpô: 34.1Ų
Số lượng nguyên tử nặng: 22
Các tính chất đặc trưng
Điểm nóng chảy: 155.13°C
Điểm sôi: 453.7±45.0 °C ở 760 mmHg
Tỷ trọng riêng: 1.1±0.1 g/cm3
Độ tan trong nước: 0.00683 mg/mL
Hằng số phân ly pKa: -5
Chu kì bán hủy: 24 giờ
Khả năng liên kết với Protein huyết tương: 90%
Dạng bào chế
Viên nén 25 mg (Aromasin 25mg)
Độ ổn định và điều kiện bảo quản
Bảo quản thuốc ở nơi khô ráo, thoáng mát, tránh ánh nắng trực tiếp và nhiệt độ cao.
Đóng kín hộp thuốc sau khi sử dụng, không để thuốc tiếp xúc với không khí hoặc độ ẩm.
Không sử dụng thuốc quá hạn sử dụng hoặc có dấu hiệu biến đổi màu sắc, hình dạng hoặc mùi.
Không bỏ thuốc vào trong tủ lạnh hoặc đông lạnh, trừ khi có chỉ dẫn của bác sĩ hoặc nhà sản xuất.
Nguồn gốc
Exemestane là một loại thuốc chống ung thư vú dựa trên cơ chế ức chế enzyme aromatase, giúp giảm lượng estrogen trong cơ thể. Exemestane được phát hiện bởi các nhà nghiên cứu của công ty dược phẩm Pharmacia & Upjohn vào những năm 1980. Sau đó, công ty đã phát triển và đăng ký bằng sáng chế cho Exemestane vào năm 1991. Exemestane được bán ra thị trường với tên thương mại Aromasin vào năm 1999. Exemestane được sử dụng để điều trị ung thư vú ở phụ nữ mãn kinh, đặc biệt là những người đã điều trị bằng tamoxifen trước đó. Exemestane cũng được nghiên cứu để phòng ngừa ung thư vú ở phụ nữ có nguy cơ cao.
Dược lý và cơ chế hoạt động
Exemestane là một hợp chất chọn lọc ức chế aromatase thuộc loại steroid và không tái hồi phục. Nó hiệu quả trong việc ngăn chặn quá trình biến đổi androgen thành estrogen ở các mô ngoại biên, từ đó giảm thiểu lượng estrogen lưu thông trong tuần hoàn. Điều này quan trọng bởi estrogen là yếu tố kích thích sự phát triển của các khối u vú phụ thuộc vào estrogen. Đáng chú ý, Exemestane có cấu trúc steroid, khác biệt so với anastrozole và letrozole, những chất ức chế aromatase không chứa steroid.
Ứng dụng trong y học
Exemestane thuốc là một lựa chọn điều trị quan trọng cho phụ nữ sau mãn kinh mắc phải ung thư vú giai đoạn đầu và có đặc tính dương tính với thụ thể estrogen. Sau khi đã dùng tamoxifen trong khoảng 2-3 năm, họ có thể chuyển sang exemestane để hoàn thành 5 năm điều trị nội tiết tố bổ trợ. FDA Hoa Kỳ đã đồng ý chấp thuận sử dụng thuốc vào tháng 10 năm 1999.
Bên cạnh đó, Exemestane cũng là lựa chọn cho việc điều trị ung thư vú tiến triển ở những bệnh nhân sau mãn kinh, đặc biệt khi bệnh tiến triển sau chu kỳ điều trị bằng tamoxifen.
Đối với những phụ nữ tiền mãn kinh mắc bệnh ung thư vú và dương tính với thụ thể hormone, kết hợp giữa thuốc ức chế aromatase exemestane và phương pháp ức chế buồng trứng, so với việc dùng tamoxifen và ức chế buồng trứng, đã mở ra một hướng điều trị mới, giúp giảm nguy cơ tái phát. Các nghiên cứu TEXT và SOFT đã xác nhận sự cải thiện về khả năng sống sót mà không mắc bệnh cho nhóm bệnh nhân được điều trị bằng exemestane và ức chế buồng trứng so với nhóm dùng tamoxifen. Nhờ vậy, phụ nữ tiền mãn kinh, khi được ức chế buồng trứng, giờ đây cũng có thể được hưởng lợi từ thuốc ức chế aromatase, một loại thuốc trước đây thường chỉ được khuyến nghị cho phụ nữ sau mãn kinh.
Dược động học
Hấp thu
Exemestane nhanh chóng được hấp thụ từ đường tiêu hóa. Dù khả năng sinh học của nó có phần bị giới hạn do quá trình chuyển hóa ở gan, việc dùng thuốc sau bữa ăn giàu mỡ có thể tăng cường khả dụng sinh học lên khoảng 40%. Trong phụ nữ mắc ung thư vú, thuốc đạt nồng độ đỉnh trong huyết tương sau khoảng 1,2 giờ.
Phân bố
Exemestane được phân phối rộng rãi trong cơ thể và có khả năng kết hợp mạnh với protein trong huyết tương, lên đến 90%. Nó chủ yếu gắn với albumin và acid α1-glycoprotein.
Chuyển hóa
Thuốc chịu sự oxy hóa từ isoenzym CYP3A4 của cytochrom P450 và quá trình khử bởi aldoketoreductase, tạo ra nhiều chất chuyển không có hoạt tính.
Thải trừ
Chất chuyển hóa của Exemestane chủ yếu được loại bỏ qua đường nước tiểu (chiếm 39-45%) và qua phân (từ 36-48%). Chỉ có dưới 1% liều thuốc được thải ra qua nước tiểu ở dạng nguyên bản. Thuốc có thời gian bán rã khoảng 24 giờ.
Độc tính ở người
Exemestane có thể gây ra một loạt tác dụng phụ tương tự như các loại thuốc ức chế aromatase khác, ví dụ như anastrozole:
- Rất thường gặp: Tăng huyết áp (5-15%), mệt mỏi (8-22%), mất ngủ (11-14%), đau nhức (13%), đau đầu (7-13%), trầm cảm (6-13%), đổ mồ hôi (4-18%), rụng tóc (15%), cơn bốc hỏa (13-21%), buồn nôn (9-18%), đau bụng (6-11%), tăng phosphatase kiềm (14-15%), đau khớp (15-29%).
- Thường gặp: Phù (6-7%), thiếu máu cơ tim (2%), đau thắt ngực, chóng mặt (8-10%), lo âu (4-10%), sốt (5%), rối loạn tư duy, giảm cảm giác, viêm da (8%), ngứa, nổi mẩn, tăng cân (8%), ỉa chảy (4-10%), nôn mửa (7%), tăng cảm giác thèm ăn (3%), táo bón (5%), nhiễm khuẩn đường niệu, bilirubin tăng (5-7%), đau lưng (9%), đau chi dưới (9%), viêm khớp (6%), rối loạn thị giác (5%), creatinin tăng (6%), khó thở (10%), ho (6%).
- Ít gặp: Suy tim, tăng GGT, bệnh thần kinh, suy giảm tiểu cầu, hư xương sụn, và một số tác dụng phụ khác.
Hiện chưa có thông tin về tình trạng ngộ độc từ việc sử dụng quá liều Exemestane. Cũng không có bất kỳ phương pháp giải độc cụ thể nào cho thuốc này. Trường hợp nghi ngờ đã uống quá liều, quan trọng là phải theo dõi sát sao các triệu chứng, áp dụng biện pháp điều trị dựa trên các biểu hiện lâm sàng và hỗ trợ bệnh nhân khi cần thiết, như bổ sung nước và điện giải nếu xuất hiện nôn mửa hoặc tiêu chảy mạnh.
Tính an toàn
Exemestane có thể gây hại cho thai nên không được khuyến cáo cho phụ nữ mang thai. Bệnh nhân cần được tư vấn rõ ràng về nguy cơ của thuốc nếu họ có thai trong quá trình điều trị. Đồng thời, phụ nữ đang cho con bú cần tránh sử dụng thuốc hoặc nên ngừng cho con bú khi quyết định sử dụng Exemestane.
Tương tác với thuốc khác
Khi kết hợp với các thuốc tăng cường hoạt động của isoenzyme CYP3A4 như Rifampicin, phenytoin hay deferasirox, hàm lượng exemestane trong cơ thể giảm đi. Trong trường hợp này, liều dùng exemestane cần được điều chỉnh lên 50 mg/ngày.
Hypericum perforatum (cỏ St.John) cũng làm giảm lượng exemestane trong cơ thể. Đối với bệnh nhân mắc bệnh ung thư vú phụ thuộc vào estrogen, việc sử dụng Cimicifuga racemosa (thăng ma) hoặc Angelica sinensis (đương quy) không được khuyến cáo.
Sự kết hợp giữa exemestane và các thuốc chứa estrogen có thể ảnh hưởng đến hiệu quả của exemestane.
Ngoài ra, exemestane cũng giảm hiệu quả của maraviroc – một thuốc dùng trong việc chống lại sự xâm nhập của HIV vào tế bào lympho T CD4 bằng cách chặn receptor CCR5.
Lưu ý khi sử dụng Exemestane
Hãy đảm bảo không nhầm lẫn Exemestane với estramustine.
Thuốc có khả năng gây ra các triệu chứng như mệt mỏi, yếu đuối và chóng mặt. Nên cân nhắc khi tham gia giao thông hoặc sử dụng các thiết bị máy móc.
Nhiều tác dụng phụ (ADR) có thể xuất phát từ việc giảm estrogen. Cần theo dõi và điều trị nhanh chóng khi phát hiện.
Để phòng ngừa tình trạng loãng xương, nên kiểm tra định kỳ mật độ xương và bổ sung vitamin D cùng calci vào chế độ ăn hàng ngày.
Khuyến cáo uống Exemestane sau khi ăn. Liều khuyến nghị: 25 mg mỗi ngày, chỉ một lần. Tiếp tục dùng thuốc cho đến khi có chứng cứ về sự giảm kích thước của khối u.
Bệnh nhân mắc ung thư vú giai đoạn đầu nên dùng Exemestane lên tới 5 năm, theo hướng dẫn trị liệu hỗ trợ tiếp nối sau tamoxifen. Nếu phát hiện khối u tái xuất, hãy dừng thuốc. Đối với bệnh nhân mắc ung thư vú giai đoạn sau, tiếp tục dùng Exemestane cho đến khi có những dấu hiệu tích cực về sự tiến triển của bệnh.
Khuyến cáo bệnh nhân bổ sung thêm vitamin D và calci vào chế độ dinh dưỡng.
Một vài nghiên cứu của Exemestane trong Y học
Điều trị nội tiết so với hóa trị ở phụ nữ sau mãn kinh bị ung thư vú di căn có thụ thể hormone dương tính, HER2 âm tính: tổng quan hệ thống và phân tích tổng hợp mạng lưới
Bối cảnh: Mặc dù các hướng dẫn quốc tế hỗ trợ việc sử dụng liệu pháp hormone có hoặc không có liệu pháp nhắm mục tiêu ở phụ nữ sau mãn kinh bị ung thư vú di căn có thụ thể hormone dương tính, HER2 âm tính, việc sử dụng hóa trị ngay từ đầu vẫn phổ biến ngay cả khi không có cơn khủng hoảng nội tạng. Bởi vì phương pháp điều trị bậc một hoặc bậc hai, hoặc cả hai, dựa trên hóa trị và liệu pháp hormone hiếm khi được nghiên cứu trong các thử nghiệm ngẫu nhiên có đối chứng trực tiếp, chúng tôi nhằm mục đích so sánh hai phương pháp khác nhau này.
Phương pháp: Chúng tôi đã thực hiện đánh giá có hệ thống và phân tích tổng hợp trên mạng bằng cách tìm kiếm tài liệu có hệ thống trên PubMed, Embase, Đăng ký thử nghiệm lâm sàng trung tâm Cochrane, Web of Science và kho lưu trữ trực tuyến của các hội nghị ung thư quốc tế có liên quan nhất. Chúng tôi bao gồm tất cả các thử nghiệm ngẫu nhiên có đối chứng giai đoạn 2 và 3 điều tra hóa trị liệu có hoặc không có liệu pháp nhắm mục tiêu và liệu pháp hormone có hoặc không có liệu pháp nhắm mục tiêu như phương pháp điều trị bậc một hoặc bậc hai, hoặc cả hai, ở phụ nữ sau mãn kinh có thụ thể hormone dương tính, HER2- ung thư vú di căn âm tính, được xuất bản từ ngày 1 tháng 1 năm 2000 đến ngày 31 tháng 12 năm 2017.
Các thử nghiệm ngẫu nhiên có đối chứng được công bố gần đây liên quan đến chủ đề này sau đó cũng được thêm vào. Không có giới hạn ngôn ngữ nào được áp dụng cho tìm kiếm của chúng tôi. Một phân tích tổng hợp mạng lưới Bayes đã được thực hiện để so sánh tỷ lệ nguy cơ (HR) về tỷ lệ sống sót không tiến triển (kết quả chính) và để so sánh tỷ lệ chênh lệch (OR) đối với tỷ lệ bệnh nhân đạt được phản ứng tổng thể (kết quả phụ). Tất cả các phương pháp điều trị đều được so sánh với anastrozole và palbociclib cộng với letrozole. Nghiên cứu này được đăng ký trong cơ sở dữ liệu công cộng trực tuyến Open Science Framework, đăng ký DOI 10.17605/OSF.IO/496VR.
Kết quả: Chúng tôi đã xác định được 2689 kết quả được công bố và 140 nghiên cứu (bao gồm 50.029 bệnh nhân) được đưa vào phân tích. Palbociclib cộng với letrozole (HR 0·42; khoảng tin cậy 95% [CrI] 0·25-0·70), ribociclib cộng với letrozole (0·43; 0·24-0·77), abemaciclib cộng với anastrozole hoặc letrozole (0· 42; 0·23-0·76), palbociclib cộng với fulvestrant (0·37; 0·23-0·59), ribociclib cộng với fulvestrant (0·48; 0·31-0·74), abemaciclib cộng với fulvestrant (0 ·44; 0·28-0·70), everolimus cộng với exemestane (0·42; 0·28-0·67), và ở những bệnh nhân có đột biến PIK3CA, alpelisib cộng với fulvestrant (0·39; 0·22- 0·66), và một số phác đồ dựa trên hóa trị liệu, bao gồm phác đồ có chứa anthracycline và taxane, có liên quan đến khả năng sống sót không tiến triển tốt hơn so với chỉ dùng anastrozole.
Không có chế độ hóa trị hoặc liệu pháp hormone nào tốt hơn đáng kể so với palbociclib cộng với letrozole đối với tỉ lệ sống sót mà bệnh không tiến triển. Paclitaxel cộng với bevacizumab là phác đồ duy nhất phù hợp về mặt lâm sàng tốt hơn đáng kể so với palbociclib cộng với letrozole về tỷ lệ bệnh nhân đạt được đáp ứng tổng thể (OR 8·95; 95% CrI 1·03-76·92).
Giải thích: Trong bối cảnh bậc một hoặc bậc hai, thuốc ức chế CDK4/6 cộng với liệu pháp hormone tốt hơn liệu pháp hormone tiêu chuẩn về khả năng sống sót không tiến triển. Hơn nữa, không có chế độ hóa trị nào có hoặc không có liệu pháp nhắm mục tiêu tốt hơn đáng kể so với thuốc ức chế CDK4/6 cộng với liệu pháp hormone về khả năng sống sót không tiến triển. Dữ liệu của chúng tôi hỗ trợ các khuyến nghị trong hướng dẫn điều trị liên quan đến sự kết hợp mới của các liệu pháp hormone cộng với các liệu pháp nhắm mục tiêu như phương pháp điều trị bậc một hoặc bậc hai, hoặc ở cả hai cơ sở, ở những phụ nữ bị ung thư vú di căn âm tính với HER2 dương tính với thụ thể hormone.
Tài liệu tham khảo
- Drugbank, Exemestane, truy cập ngày 28 tháng 10 năm 2023.
- Giuliano, M., Schettini, F., Rognoni, C., Milani, M., Jerusalem, G., Bachelot, T., De Laurentiis, M., Thomas, G., De Placido, P., Arpino, G., De Placido, S., Cristofanilli, M., Giordano, A., Puglisi, F., Pistilli, B., Prat, A., Del Mastro, L., Venturini, S., & Generali, D. (2019). Endocrine treatment versus chemotherapy in postmenopausal women with hormone receptor-positive, HER2-negative, metastatic breast cancer: a systematic review and network meta-analysis. The Lancet. Oncology, 20(10), 1360–1369. https://doi.org/10.1016/S1470-2045(19)30420-6
- Pubchem, Exemestane, truy cập ngày 28 tháng 10 năm 2023.
- Bộ Y Tế (2012), Dược thư quốc gia Việt Nam, Nhà xuất bản Y học, Hà Nội
