Enzalutamide

Danh pháp
Tên chung quốc tế
Tên danh pháp theo IUPAC
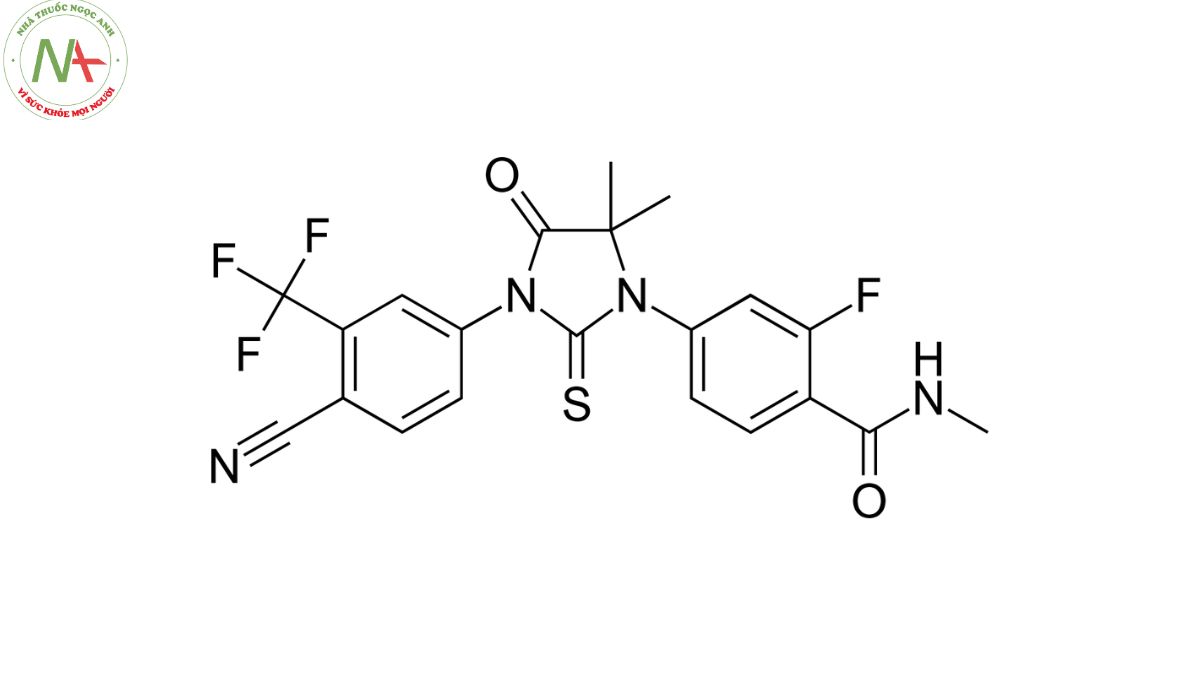
4-[3-[4-cyano-3-(trifluoromethyl)phenyl]-5,5-dimethyl-4-oxo-2-sulfanylideneimidazolidin-1-yl]-2-fluoro-N-methylbenzamide
Nhóm thuốc
Enzalutamide thuộc nhóm nào? Thuốc kháng androgen
Mã ATC
L – Chất chống ung thư và điều hòa miễn dịch
L02 – Liệu pháp nội tiết
L02B – Thuốc đối kháng nội tiết tố và các chất liên quan
L02BB – Thuốc kháng androgen
L02BB04 – Enzalutamide
Mã UNII
93T0T9GKNU
Mã CAS
915087-33-1
Cấu trúc phân tử
Công thức phân tử
C21H16F4N4O2S
Phân tử lượng
464.4 g/mol
Cấu trúc phân tử
Enzalutamide là một benzamide thu được bằng cách ngưng tụ chính thức nhóm carboxy của 4-{3-[4-cyano-3-(trifluoromethyl)phenyl]-5,5-dimethyl-4-oxo-2-thioxoimidazolidin-1-yl}-2-fluorobenzoic acid với metylamine. Nó là dẫn xuất của benzamid, imidazolidinone, hợp chất thiocarbonyl, nitrile, dẫn xuất của benzen (trifluoromethyl) và dẫn xuất của monofluorobenzen.
Các tính chất phân tử
Số liên kết hydro cho: 1
Số liên kết hydro nhận: 8
Số liên kết có thể xoay: 3
Diện tích bề mặt tôpô: 109Ų
Số lượng nguyên tử nặng: 32
Các tính chất đặc trưng
Điểm nóng chảy: 201ºC
Tỷ trọng riêng: 1.5±0.1 g/cm3
Độ tan trong nước: 0.00136 mg/mL
Hằng số phân ly pKa: -1.6
Chu kì bán hủy: 5,8 ngày
Khả năng liên kết với Protein huyết tương: 97 – 98%
Dạng bào chế
Viên nén: 40 mg, 80 mg, 160 mg
Viên nang: 40 mg

Độ ổn định và điều kiện bảo quản
Enzalutamide nên được bảo quản ở nơi khô ráo, thoáng mát, tránh ánh nắng trực tiếp và nhiệt độ cao. Ngoài ra, thuốc cũng không nên để gần các nguồn nhiệt, lửa hoặc các chất dễ cháy. Thuốc cũng không nên để trong phòng tắm hoặc nhà bếp, vì độ ẩm và hơi nước có thể làm giảm độ ổn định của thuốc.
Nguồn gốc
Enzalutamide là thuốc gì? Enzalutamide, một thành tựu quan trọng trong lĩnh vực y học, được khám phá bởi Charles Sawyers, hiện làm việc tại Trung tâm Ung thư Memorial Sloan–Kettering, và Michael Jung tại Đại học California, Los Angeles. Cùng với đồng đội, họ đã thực hiện tổng cộng hóa và đánh giá gần 200 dẫn xuất thiohydantoin của RU-59063, chất tương tự nilutamide, có khả năng đối kháng với receptor androgen (AR) trong tế bào ung thư tuyến tiền liệt ở người. Kết quả của nghiên cứu này là việc xác định enzalutamide và RD-162 là hai hợp chất tiềm năng. Sự nghiên cứu này đã được cấp bằng sáng chế vào năm 2006 và được công bố vào năm 2007.
Enzalutamide, sản phẩm được phát triển và tiếp thị bởi Medivation, đã nhận được sự chấp thuận từ Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) vào tháng 8 năm 2012 để điều trị ung thư tuyến tiền liệt giai đoạn mCRPC, và sau đó, vào tháng 7 năm 2018, để điều trị ung thư tuyến tiền liệt kháng thiến không di căn.
Đáng chú ý, enzalutamide là loại thuốc đối kháng AR mới đầu tiên được FDA phê duyệt để điều trị ung thư tuyến tiền liệt trong hơn 15 năm, là một bước tiến lớn sau khi bicalutamide, loại NSAA thế hệ đầu tiên, được giới thiệu vào năm 1995. Enzalutamide đại diện cho NSAA thế hệ thứ hai đầu tiên được giới thiệu, mở ra một kỷ nguyên mới trong điều trị bệnh lý này.
Dược lý và cơ chế hoạt động
Enzalutamide có tác dụng gì? Enzalutamide, là một thuốc kháng androgen thế hệ thứ hai, đặc biệt thiết kế để ngăn chặn hoạt động của androgen và thụ thể androgen (AR) trong ung thư tuyến tiền liệt.
Mối liên kết mật thiết giữa hoạt động AR và sự tiến triển của ung thư tuyến tiền liệt là một khía cạnh quan trọng, được gắn kết chặt chẽ với sinh lý bình thường của tế bào tuyến tiền liệt, mở ra cơ hội cho liệu pháp thiếu hụt androgen (ADT). Tuy nhiên, xuất hiện tình trạng kháng thuốc sau 2-3 năm sử dụng ADT là không tránh khỏi, có liên quan với sự tích tụ các đột biến, bao gồm đột biến cấu trúc, quá mức biểu hiện của AR và biến đổi trong các biến thể ghép nối AR. Do đó, Enzalutamide được chế tạo để đối phó với những thách thức này.
Kết quả thí nghiệm in vitro trên dòng tế bào ung thư tuyến tiền liệt VCaP ở người chỉ ra rằng enzalutamide không chỉ có thể ngăn chặn sự phát triển của tế bào mà còn gây ra apoptosis, trong khi các loại thuốc kháng androgen khác như bicalutamide không thể đạt được hiệu quả tương tự.
Trong các thử nghiệm lâm sàng trên bệnh nhân ung thư tuyến tiền liệt, enzalutamide đã được chứng minh là gây giảm PSA huyết thanh ít nhất trong 12 tuần, tuy phản ứng này có thể chỉ tồn tại ngắn hạn, dẫn đến tình trạng kháng enzalutamide. Điều quan trọng là bệnh nhân sử dụng enzalutamide cũng đã ghi nhận giảm 37% nguy cơ tử vong so với nhóm dùng giả dược.
Enzalutamide cơ chế: Enzalutamide không chỉ là một chất ức chế thụ thể androgen (AR) cạnh tranh, mà còn có tác dụng ức chế gấp ba lần trên con đường truyền tín hiệu androgen mà không gây ra hoạt tính chủ vận AR đáng kể. Nó ức chế sự liên kết androgen với thụ thể, sự chuyển vị hạt nhân của thụ thể androgen và tương tác với DNA, từ đó điều hòa lại các gen liên quan đến sự phát triển của ung thư.
Enzalutamide liên kết với AR với ái lực lớn gấp 5 đến 8 lần so với thuốc kháng androgen thế hệ thứ nhất như bicalutamide, và chỉ giảm ái lực gấp 2-3 lần so với dihydrotestosterone, phối tử tự nhiên. Phân tích lắp ghép phân tử chỉ ra rằng enzalutamide liên kết với miền liên kết phối tử của AR một cách độc đáo so với bicalutamide.
Ứng dụng trong y học
Thuốc Enzalutamide là một bước tiến quan trọng trong lĩnh vực y học, đặc biệt là trong điều trị các trường hợp ung thư tuyến tiền liệt. Được phát hiện và phát triển bởi Charles Sawyers và Michael Jung, Enzalutamide đã mở ra một hướng đi mới trong nghiên cứu và điều trị ung thư tuyến tiền liệt, mang lại hy vọng cho hàng triệu người đang phải đối mặt với bệnh lý này.
Ứng dụng chính của Enzalutamide nằm trong điều trị ung thư tuyến tiền liệt, đặc biệt là ở những trường hợp kháng lại các liệu pháp truyền thống như thiến và thuốc kháng androgen thế hệ đầu tiên. Chất này hoạt động bằng cách ức chế AR, thụ thể mà androgen (hormone nam giới) thường kết hợp, giúp kiểm soát sự phát triển của tế bào ung thư. Điều này làm giảm khả năng tế bào ung thư phát triển và lan ra xa khỏi tuyến tiền liệt.
Một điểm mạnh của Enzalutamide là khả năng ngăn chặn sự phát triển của tế bào ung thư mà không gây tác động lớn đến hoạt động của AR bình thường, điều này là quan trọng để giảm thiểu các tác dụng phụ không mong muốn. Cơ chế hoạt động tiên tiến này đã làm cho Enzalutamide trở thành lựa chọn quan trọng trong việc quản lý các trường hợp ung thư tuyến tiền liệt khó chữa trị.
Ngoài ra, Enzalutamide cũng đang được nghiên cứu để xem xét khả năng ứng dụng trong các loại ung thư khác và các bệnh lý liên quan đến AR, như ung thư vú có thụ thể estrogen dương tính. Các nghiên cứu này đang mở ra những triển vọng mới và tiềm năng lớn cho Enzalutamide có thể đóng góp vào việc mở rộng phạm vi ứng dụng của nó trong lĩnh vực y học.
Dược động học
Hấp thu
Thời điểm đạt đỉnh hấp thụ trung bình của enzalutamide là 1 giờ (khoảng từ 0,5 đến 3 giờ) sau khi dùng một viên nang 160 mg và là 2 giờ (khoảng từ 0,5 đến 6 giờ) sau khi sử dụng một viên nén 160 mg. Enzalutamide đạt được trạng thái ổn định vào ngày thứ 28, với diện tích dưới đường cong (AUC) tích lũy lên đến khoảng 8,3 lần so với liều duy nhất. Trong trạng thái ổn định, nồng độ tối đa trung bình (%CV) (Cmax) của enzalutamide là 16,6 µg/mL (23%), và của N-desmethyl enzalutamide là 12,7 µg/mL (30%), trong khi nồng độ tối thiểu trung bình (%CV) (Cmin) là 11,4 µg/mL (26%) và 13,0 µg/mL (30%) tương ứng.
Phân bố
Thể tích phân bố trung bình (%CV) sau khi dùng một liều duy nhất là 110 L (29%). Enzalutamide kết hợp với protein huyết tương từ 97% đến 98%, chủ yếu là albumin. N-desmethyl enzalutamide kết hợp với protein huyết tương ở mức 95%.
Chuyển hóa
Enzalutamide trải qua quá trình chuyển hóa chủ yếu bởi CYP2C8 và CYP3A4. CYP2C8 đóng vai trò quan trọng trong việc tạo ra chất chuyển hóa có hoạt tính, N-desmethyl enzalutamide. Carboxylesterase 1 thực hiện chuyển hóa N-desmethyl enzalutamide và enzalutamide thành chất chuyển hóa axit cacboxylic không hoạt động.
Thải trừ
Quá trình đào thải chủ yếu của enzalutamide xảy ra tại gan qua quá trình chuyển hóa. Khoảng 71% liều dùng được phát hiện trong nước tiểu (bao gồm một lượng nhỏ enzalutamide và N-desmethyl enzalutamide), và 14% được tìm thấy trong phân (0,4% liều dùng dưới dạng enzalutamide không biến đổi và 1% dưới dạng N-desmethyl enzalutamide). Độ thanh thải biểu kiến trung bình (CL/F) của enzalutamide sau một liều duy nhất là 0,56 L/giờ (khoảng từ 0,33 đến 1,02 L/giờ). Thời gian bán hủy trung bình (t1/2) của enzalutamide ở bệnh nhân sau một liều uống duy nhất là 5,8 ngày (trong khoảng từ 2,8 đến 10,2 ngày). Sau khi sử dụng một liều enzalutamide 160 mg duy nhất ở những người tình nguyện khỏe mạnh, t1/2 cuối cùng trung bình của N-desmethyl enzalutamide là khoảng từ 7,8 đến 8,6 ngày.
Độc tính ở người
Enzalutamide tác dụng phụ: Các phản ứng bất lợi thường gặp nhất (tần suất > 5%) khi sử dụng enzalutamide bao gồm suy nhược/mệt mỏi, đau lưng, tiêu chảy, đau khớp, cảm giác nóng bừng, phù ngoại biên, đau cơ xương khớp, đau đầu, nhiễm trùng đường hô hấp trên, yếu cơ, chóng mặt, mất ngủ, nhiễm trùng đường hô hấp dưới, chèn ép tủy sống và hội chứng đuôi ngựa, tiểu máu, dị cảm, lo lắng và tăng huyết áp.
Tính an toàn
Trong các thử nghiệm kiểm soát trước khi đăng ký, mức tăng aminotransferase trong huyết thanh đã được ghi nhận ở khoảng 10% bệnh nhân được điều trị bằng enzalutamide. Tuy nhiên, tỷ lệ này không cao hơn so với nhóm dùng giả dược, với khoảng 9% bệnh nhân gặp phải hiện tượng tương tự. Các bất thường về xét nghiệm gan thường nhẹ, thoáng qua và không liên quan đến các triệu chứng hoặc hiện tượng vàng da. Mức tăng ALT trên 5 lần giá trị trên mức bình thường (ULN) là rất hiếm (0,2%), và không có sự tăng này thường xuyên hơn so với nhóm điều trị bằng giả dược. Đáng chú ý, không có báo cáo về tổn thương gan rõ ràng hoặc viêm gan trong các thử nghiệm đăng ký trước đây của enzalutamide, và thông tin này cũng không xuất hiện trong nhãn sản phẩm. Kể từ khi enzalutamide được phê duyệt và sử dụng rộng rãi hơn, không có bất kỳ thông tin hay mô tả nào về đặc điểm lâm sàng của nhiễm độc gan kèm theo hiện tượng vàng da do việc sử dụng nó. Do đó, nếu có tổn thương gan xuất hiện, đó là một hiện tượng hiếm.
Trong một nghiên cứu về độc tính phát triển của phôi thai ở chuột, enzalutamide đã gây ra độc tính phát triển khi được sử dụng ở liều 10 hoặc 30 mg/kg/ngày trong suốt giai đoạn hình thành cơ quan (từ ngày thai 6-15). Các hiện tượng bao gồm tỷ lệ chết phôi thai tăng lên, mất và tái hấp thụ sau khi làm tổ, và giảm khoảng cách sinh dục ở liều ≥ 10 mg/kg/ngày, với sứt môi và thiếu xương vòm miệng ở liều 30 mg/kg/ngày. Liều 30 mg/kg/ngày cũng gây độc hại cho mẹ. Các liều được thử nghiệm ở chuột (1, 10 và 30 mg/kg/ngày) dẫn đến nồng độ toàn thân (AUC) lần lượt tương đương với khoảng 0,04, 0,4 và 1,1 lần mức phơi nhiễm ở bệnh nhân. Enzalutamide không gây độc tính phát triển ở thỏ khi sử dụng trong giai đoạn hình thành cơ quan (từ ngày thai 6-18) ở liều lượng lên tới 10 mg/kg/ngày (tương đương khoảng 0,4 lần mức phơi nhiễm ở bệnh nhân dựa trên AUC).
Trong một nghiên cứu dược động học ở chuột mang thai, việc sử dụng enzalutamide ở liều duy nhất là 30 mg/kg qua đường uống vào ngày thai thứ 14 đã dẫn đến việc enzalutamide và/hoặc các chất chuyển hóa của nó xuất hiện trong bào thai, với Cmax xấp xỉ 0,3 lần so với nồng độ tìm thấy trong huyết thanh mẹ và xuất hiện sau 4 giờ sau khi sử dụng thuốc.
Dựa trên các nghiên cứu động vật, enzalutamide có thể ảnh hưởng đến khả năng sinh sản ở nam giới có khả năng sinh sản. Do đó, nếu nam giới có đối tác nữ có khả năng sinh sản, nên sử dụng biện pháp tránh thai hiệu quả trong suốt quá trình điều trị và trong vòng 3 tháng sau khi dùng liều enzalutamide cuối cùng.
Tương tác với thuốc khác
Enzalutamide là một chất gây cảm ứng enzyme cytochrome P450 từ trung bình đến mạnh, đặc biệt là CYP3A4, CYP2C9 và CYP2C19, điều này có thể dẫn đến khả năng cao của các tương tác thuốc có ý nghĩa lâm sàng. Nồng độ tuần hoàn của enzalutamide có thể bị ảnh hưởng bởi các chất ức chế và cảm ứng của CYP2C8 và CYP3A4, do đó, việc tránh kết hợp nếu có thể là quan trọng.
Trong một nghiên cứu lâm sàng với enzalutamide đối với bệnh ung thư vú dương tính với thụ thể estrogen ER ở phụ nữ, enzalutamide đã được xác định làm giảm nồng độ trong huyết thanh của các loại thuốc ức chế aromatase như anastrozole và exemestane lần lượt là 90% và 50%. Hiện tượng này có thể gây giảm hiệu quả của các thuốc này trong điều trị.
Lưu ý khi sử dụng Enzalutamide
Đối với những người đang lái xe hoặc vận hành máy móc nặng, cần lưu ý rằng Enzalutamide, trong một số trường hợp, có thể gây chóng mặt, mất cân bằng và tình trạng không ổn định. Do đó, quá trình lái xe và vận hành máy móc nên được thực hiện một cách thận trọng. Nếu có bất kỳ vấn đề nào liên quan đến an toàn khi tham gia giao thông hoặc thực hiện các hoạt động liên quan, người sử dụng nên tham khảo ý kiến của bác sĩ.
Đối với người già, việc sử dụng Enzalutamide cần được thảo luận với bác sĩ để xác định liều lượng phù hợp, đặc biệt là đối với những người có độ tuổi trên 65. Quan trọng nhất, không nên tự ý điều chỉnh liều lượng, tăng hoặc giảm, và không nên sử dụng thuốc đột ngột mà không có chỉ định của bác sĩ.
Trước khi sử dụng, việc đọc kỹ tờ hướng dẫn sử dụng Enzalutamide là quan trọng để đảm bảo hiểu rõ về cách sử dụng và các biện pháp an toàn cần thiết.
Một vài nghiên cứu của Enzalutamide trong Y học
Các phương pháp điều trị ung thư tuyến tiền liệt nhạy cảm với nội tiết tố di căn: Đánh giá có hệ thống, Phân tích tổng hợp mạng và đánh giá lợi ích-tác hại
Bối cảnh: Hiện có nhiều phương pháp điều trị ung thư tuyến tiền liệt nhạy cảm với hormone (mHSPC) di căn, nhưng tác dụng của chúng đối với chất lượng cuộc sống liên quan đến sức khỏe (HRQoL) và sự cân bằng giữa lợi ích và tác hại vẫn chưa rõ ràng.
Mục tiêu: Để đánh giá hiệu quả lâm sàng về khả năng sống sót và HRQoL, độ an toàn và sự cân bằng giữa lợi ích và tác hại của các phương pháp điều trị mHSPC.
Thu thập bằng chứng: Chúng tôi đã tìm kiếm MEDLINE, EMBASE, CENTRAL và ClinicTrials.gov cho đến ngày 1 tháng 3 năm 2022. Các thử nghiệm ngẫu nhiên có đối chứng (RCT) so sánh docetaxel, abiraterone, enzalutamide, apalutamide, darolutamide và xạ trị kết hợp với liệu pháp thiếu hụt androgen (ADT) lẫn nhau hoặc chỉ với ADT đều đủ điều kiện. Ba nhà đánh giá độc lập thực hiện sàng lọc, trích xuất dữ liệu và nguy cơ đánh giá sai lệch một cách trùng lặp.
Tổng hợp bằng chứng: Qua mười RCT, chúng tôi nhận thấy các lợi ích sinh tồn có liên quan của ADT + docetaxel (độ chắc chắn cao theo Phân loại Khuyến nghị, Đánh giá, Phát triển và Đánh giá [GRADE]), ADT + abiraterone (độ tin cậy vừa phải), ADT + enzalutamide (độ tin cậy thấp), ADT + apalutamide (độ tin cậy cao) và ADT + docetaxel + darolutamide (độ tin cậy cao) so với ADT đơn thuần.
Liệu pháp xạ trị ADT + chỉ xuất hiện hiệu quả ở mHSPC khối lượng thấp. Chúng tôi nhận thấy mức giảm HRQoL ngắn hạn kéo dài 3-6 tháng đối với ADT + docetaxel (độ chắc chắn vừa phải) và lợi ích HRQoL tiềm năng đối với ADT + abiraterone trong tối đa 24 tháng theo dõi (độ chắc chắn vừa phải) so với chỉ riêng ADT.
Không có sự khác biệt về HRQoL đối với liệu pháp xạ trị ADT + enzalutamide, ADT + apalutamide hoặc ADT + so với chỉ dùng ADT (độ chắc chắn thấp-cao). Tỷ lệ tác dụng phụ cấp độ 3-5 tăng lên với tất cả các phương pháp điều trị kết hợp toàn thân. Đánh giá lợi ích-tác hại cho thấy xác suất cao (>60%) về lợi ích lâm sàng thực với ADT + abiraterone, ADT + enzalutamide và ADT + apalutamide, trong khi ADT + docetaxel và ADT + docetaxel + darolutamide dường như không có lợi ích (<40%).
Kết luận: Mặc dù có lợi ích đáng kể về khả năng sống sót, nhưng không có phương pháp điều trị kết hợp toàn thân nào cho thấy sự cải thiện HRQoL rõ ràng so với chỉ dùng ADT. Chúng tôi đã tìm thấy bằng chứng cho thấy sự suy giảm HRQoL ngắn hạn với ADT + docetaxel và lợi ích lâm sàng ròng cao hơn với ADT + abiraterone, ADT + apalutamide và ADT + enzalutamide. Mặc dù việc ra quyết định mang tính cá nhân vẫn quan trọng và các yếu tố kinh tế cần được xem xét, bằng chứng có thể ủng hộ ưu tiên chung cho việc kết hợp ADT với các liệu pháp nhắm mục tiêu trục thụ thể androgen so với các chiến lược chứa docetaxel.
Tóm tắt bệnh nhân: Chúng tôi đã đánh giá các phương pháp điều trị kết hợp khác nhau đối với bệnh ung thư tuyến tiền liệt nhạy cảm với hormone di căn. Mặc dù khả năng sống sót tốt hơn với tất cả các phương pháp điều trị kết hợp toàn thân, nhưng không có sự cải thiện rõ ràng nào về chất lượng cuộc sống liên quan đến sức khỏe so với liệu pháp điều trị thiếu hụt androgen đơn thuần. Các phương pháp điều trị kết hợp nội tiết tố mới có sự cân bằng giữa lợi ích và tác hại thuận lợi hơn so với các phương pháp điều trị kết hợp bao gồm hóa trị.
Tài liệu tham khảo
- Drugbank, Enzalutamide, truy cập ngày 18 tháng 11 năm 2023.
- Menges D, Yebyo HG, Sivec-Muniz S, Haile SR, Barbier MC, Tomonaga Y, Schwenkglenks M, Puhan MA. Treatments for Metastatic Hormone-sensitive Prostate Cancer: Systematic Review, Network Meta-analysis, and Benefit-harm assessment. Eur Urol Oncol. 2022 Dec;5(6):605-616. doi: 10.1016/j.euo.2022.04.007. Epub 2022 May 20. PMID: 35599144.
- Pubchem, Enzalutamide, truy cập ngày 18 tháng 11 năm 2023.
- Bộ Y Tế (2012), Dược thư quốc gia Việt Nam, Nhà xuất bản Y học, Hà Nội.
