Deferiprone
Danh pháp
Tên chung quốc tế
Tên danh pháp theo IUPAC
3-hydroxy-1,2-dimethylpyridin-4-one
Nhóm thuốc
Chất chelat hóa sắt
Mã ATC
V – Khác nhau
V03 – Tất cả các sản phẩm trị liệu khác
V03A – Tất cả các sản phẩm trị liệu khác
V03AC – Chất chelat hóa sắt
V03AC02 – Deferipron
Mã UNII
2BTY8KH53L
Mã CAS
30652-11-0
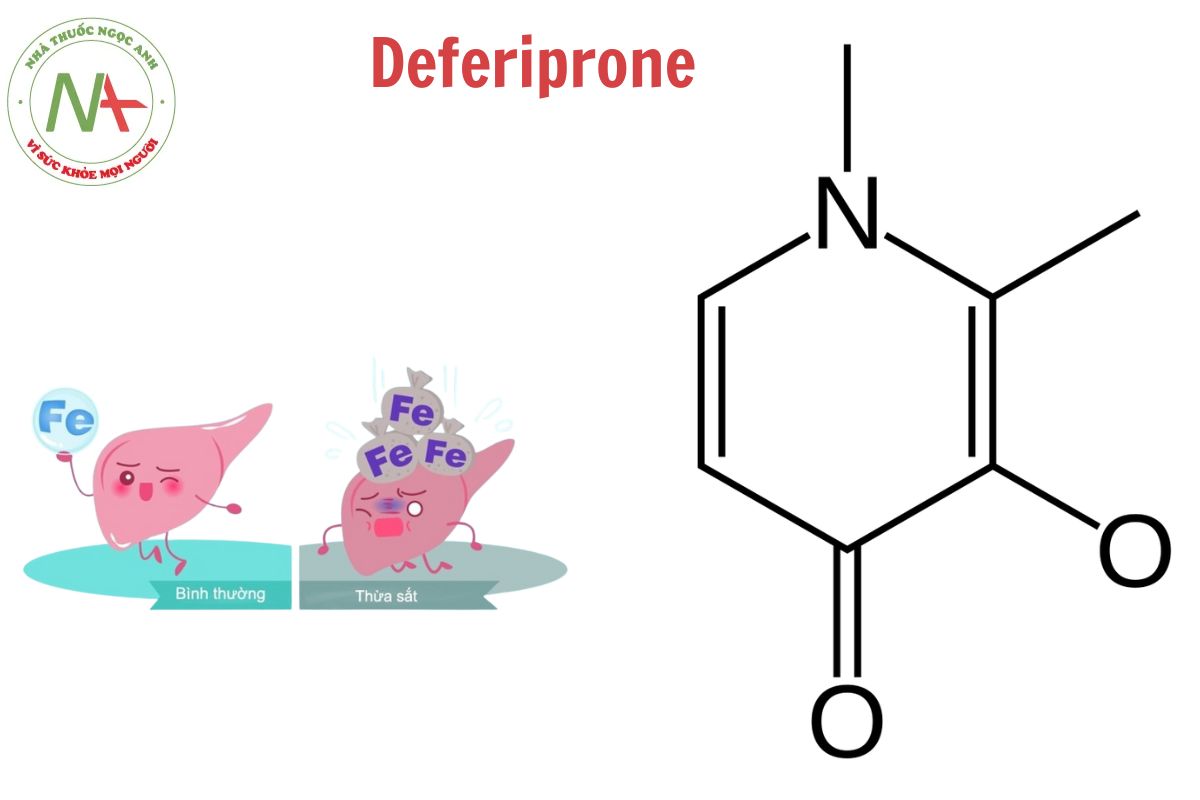
Cấu trúc phân tử
Công thức phân tử
C7H9NO2
Phân tử lượng
139.15 g/mol
Đặc điểm cấu tạo
Deferiprone có nhóm 4-pyridone được thay thế ở vị trí 1 và 2 bằng nhóm methyl và ở vị trí 3 bằng nhóm hydroxy.
Các tính chất phân tử
Số liên kết hydro cho: 1
Số liên kết hydro nhận: 3
Số liên kết có thể xoay: 0
Diện tích bề mặt cực tôpô: 40,5
Số lượng nguyên tử nặng: 10
Số lượng nguyên tử trung tâm xác định được: 0
Liên kết cộng hóa trị: 1
Tính chất
- Deferiprone có hình kim, vị đắng.
- Điểm nóng chảy 266-268°C
- Độ hòa tan trong nước tối đa 16–18 g/L ở 24°
Dạng bào chế
Viên nang cứng: Thuốc deferiprone 250mg,…
Viên nén bao phim: thuốc Deferiprone 500mg,..
Dung dịch uống

Nguồn gốc
- Tại Liên minh Châu Âu Deferipron đã được chấp thuận sử dụng trong y tế lần đầu vào tháng 8 năm 1999.
- Vào tháng 10 năm 2011, Deferiprone được phê duyệt để sử dụng trong y tế tại Hoa Kỳ.
- Dựa trên 12 nghiên cứu lâm sàng trên 236 người tham gia, tính an toàn và hiệu quả của deferipron đã được chứng minh. Trước đó những người tình nguyện này đã được cho dùng liệu pháp thải sắt trước đó nhưng không đáp ứng với thuốc này. Deferipron giảm ít nhất 20% nồng độ ferritin huyết thanh ở những người tình nguyện tham gia. Một nửa số người tình nguyện tham gia nghiên cứu đã giảm ít nhất 20% nồng độ ferritin.
Dược lý và cơ chế hoạt động
- Deferiprone cơ chế tác dụng như sau: Deferiprone là một chất thải sắt thông qua cơ chế tạo thành phức hợp ổn định 3:1 (deferibbed: sắt ) và liên kết với các ion sắt ( sắt III) sau đó được thải trừ qua nước tiểu. Deferipron có tính chọn lọc đối với sắt cao hơn so với các kim loại khác như đồng và nhôm, kẽm.
Dược động học
Hấp thu
Thuốc thải sắt deferiprone được hấp thu nhanh chóng tại đường tiêu hóa trên với nồng độ tối đa trong huyết tương đạt được sau 1 giờ và sau 2 giờ khi uống lúc đói và khi uống lúc no. Deferiprone xuất hiện trong máu trong vòng 5 đến 10 phút sau khi uống. Khi dùng cùng thức ăn, Cmax của deferipron giảm và AUC lần lượt giảm 38% và 10%.
Chuyển hóa
Deferipron được chuyển hóa thành chất chuyển hóa 3-O-glucuronide chủ yếu bởi UGT1A6 . Chất chuyển hóa này không có hoạt tính sinh học.
Phân bố
Deferiprone có thể tích phân bố là 1L/kg.
Thải trừ
Deferiprone dược thư được thải trừ khỏi huyết tương hơn 90% sau 5-6 giờ sau khi dùng. 75 đến 90% deferipron dưới dạng chất chuyển hóa được bài tiết qua nước tiểu. Thời gian bán hủy của Deferiprone là 1,9 giờ.
Ứng dụng trong y học
- Deferiprone được dùng ở những người mắc bệnh thalassemia thể nặng giúp chỉ định điều trị tình trạng quá tải sắt khi liệu pháp thải sắt hiện tại không đạt hiệu quả điều trị.
- Deferipron kết hợp với một thuốc thải sắt khác để phòng ngừa hoặc điều trị các triệu chứng, hậu quả đe dọa tính mạng do quá tải sắt cần phải điều chỉnh chuyên sâu, nhanh chóng.
Tác dụng phụ
- Tiêu hóa: buồn nôn, rối loạn tiêu hóa, nôn , đau dạ dày
- Nhiễm trùng
- đau khớp ; hoặc
- Bất thường xét nghiệm chức năng gan
Độc tính ở người
- Việc dùng quá liều Deferiprone có thể gây mất bạch cầu hạt và giảm bạch cầu trung tính, có thể dẫn đến nhiễm trùng gây tử vong. Nhiễm độc gan cũng có thể xảy ra.
- Không có trường hợp quá liều Deferiprone nào được báo cáo. Tuy nhiên, các rối loạn thần kinh như triệu chứng hạ huyết áp, rung giật nhãn cầu một bên, nhìn đôi, chậm tâm thần vận động, tiểu não đã được quan sát ở trẻ em được điều trị với liều gấp 2,5 đến 3 lần liều khuyến cáo trong hơn một năm.Các rối loạn thần kinh giảm dần sau khi ngừng sử dụng deferipron.
- Dựa trên bằng chứng về độc tính trong các nghiên cứu trên động vật, deferipron có thể gây hại cho thai nhi khi dùng cho động vật mang thai. Khi cho chuột nhắt và chuột cống uống duy nhất deferipron 100 mg/kg gây ra tình trạng tăng tiết nước bọt thoáng qua, trong khi đó, liều cao hơn 300-600 mg/kg có thể gây ảnh hưởng đến hành vi, nhiệt độ cơ thể, giảm hiệu suất đồng thời ảnh hưởng đến khả năng tránh né và vận động thụ động của động vật.
- Khi dùng ở liều thấp hơn trên chuột cho thấy Deferiprone có khả năng đi qua hàng rào máu não và gây trở ngại cho hoạt động của chuột. Trong một nghiên cứu về độc tính của deferipron ở liều 150 hoặc 200 mg/kg/ngày chia làm 2 lần (75 hoặc 100 mg/kg ngày 2 lần) ở loài gặm nhấm kéo dài 12 tháng, không cho chuột bổ sung sắt thì phát hiện các động vật thí nghiệm đã chết hoặc trong tình trạng hấp hối với tình trạng thiếu máu trầm trọng và thoái hóa và hoại tử trung tâm tiểu thùy ở mức độ nhẹ đến trung bình.
Tương tác với thuốc khác
- Deferipron khi dùng chung với tocilizumab, everolimus, blinatumomab có thể làm giảm số lượng bạch cầu và ảnh hưởng đến tế bào bạch cầu hoặc chức năng tủy xương có thể làm tăng nguy cơ.
- Deferipron và các sản phẩm có chứa nhôm, canxi, sắt, magie và/hoặc các khoáng chất khác có thể cản trở sự hấp thu của deferipron và làm giảm hiệu quả của Deferiprone.
Lưu ý khi sử dụng
- Trong quá trình dùng Deferiprone, bệnh nhân có thể bị nhiễm trùng nghiêm trọng và đôi khi gây tử vong
- Ngừng sử dụng deferipron nếu bệnh nhân có các dấu hiệu nhiễm trùng như: sốt , triệu chứng cúm, vết loét trong miệng và cổ họng, ớn lạnh, đau nhức cơ thể, vết loét da
- Deferipron có thể khiến nước tiểu chuyển sang màu nâu đỏ. Tác dụng phụ này thường không có hại.
- Bệnh nhân cần báo cho bác sĩ nếu gặp tình trạng đau bụng trên, phân màu vàng da/ đất sét.
- Cả nam giới , nữ giới trong quá trình dùng Deferiprone đều cần sử dụng biện pháp tránh thai hiệu quả để tránh mang thai.
- Phụ nữ sau liều Deferiprone cuối cùng nên tiếp tục sử dụng biện pháp tránh thai ít nhất 6 tháng.
- Trước khi dùng Deferiprone bệnh nhân nên báo cho bác sĩ nếu bị bệnh gan, hệ thống miễn dịch yếu.
- Đảm bảo trước khi dùng Deferiprone bệnh nhân không mang thai.
- Phụ nữ không nên cho con bú sau khi dùng Deferiprone trong ít nhất 2 tuần sau liều cuối.
Một vài nghiên cứu của Deferiprone trong Y học
Nghiên cứu về tác dụng của Deferipron trong bệnh Parkinson

Nghiên cứu được tiến hành với mục tiêu tác dụng của Deferiprone đối với sự tiến triển của bệnh Parkinson. Phương pháp tiến hành theo thử nghiệm ngẫu nhiên, mù đôi, giai đoạn 2, trên những đối tượng mắc bệnh Parkinson mới được chẩn đoán và chưa bao giờ dùng levodopa. Những người tham gia được chia thành 2 nhóm có cỡ mẫu bằng nhau, 1 nhóm cho dùng Deferiprone liều 15 mg/kg trọng lượng cơ thể 2 lần /ngày và 1 nhóm còn lại cho dùng dùng giả dược trong 36 tuần. Kết quả dựa trên Thang đánh giá bệnh Parkinson thống nhất do Hiệp hội Rối loạn Vận động tài trợ được đo ở tuần thứ 36. Kết quả cho thấy trong 372 người tham gia có 186 người được chỉ định dùng deferipron và 186 người dùng giả dược.Có 22,0% số người tham gia nhóm deferipron và 2,7% số người tham gia nhóm giả dược có sự tiến triển của các triệu chứng dẫn đến việc bắt đầu điều trị bằng dopaminergic. Các tác dụng phụ nghiêm trọng chính của deferipron là mất bạch cầu hạt ở 2 người tham gia và giảm bạch cầu trung tính ở 3 người tham gia. Từ đó cho thấy kết luận rằng deferipron có tác dụng kém hơn so với giả dược ở những người tham gia mắc bệnh Parkinson giai đoạn đầu chưa bao giờ dùng levodopa trong khoảng thời gian 36 tuần.
Tài liệu tham khảo
- Thư viện y học quốc gia, Deferiprone , pubchem. Truy cập ngày 20/09/2023.
- David Devos , Julien Labreuche , Olivier Rascol (2022),Trial of Deferiprone in Parkinson’s Disease ,pubmed.com. Truy cập ngày 20/09/2023.
Xuất xứ: Ấn Độ
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam
Xuất xứ: Việt Nam