Bệnh tim mạch
Bệnh Còn ống động mạch: Định nghĩa, chẩn đoán, điều trị
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
Nguồn: Sách Lâm sàng tim bẩm sinh
Chủ biên
PGS.TS.BS. Nguyễn Lân Hiếu
Tham gia biên soạn
Nguyễn Minh Hùng
Đỗ Quốc Hiển
Nguyễn Văn Hiếu
Nguyễn Duy Thắng
Dương Công Nguyên
Trong bài viết dưới đây Nhà thuốc Ngọc Anh xin gửi đến quý bạn đọc bệnh lý thường gặp trong lâm sàng tim bẩm sinh: Còn ống động mạch
Đại cương
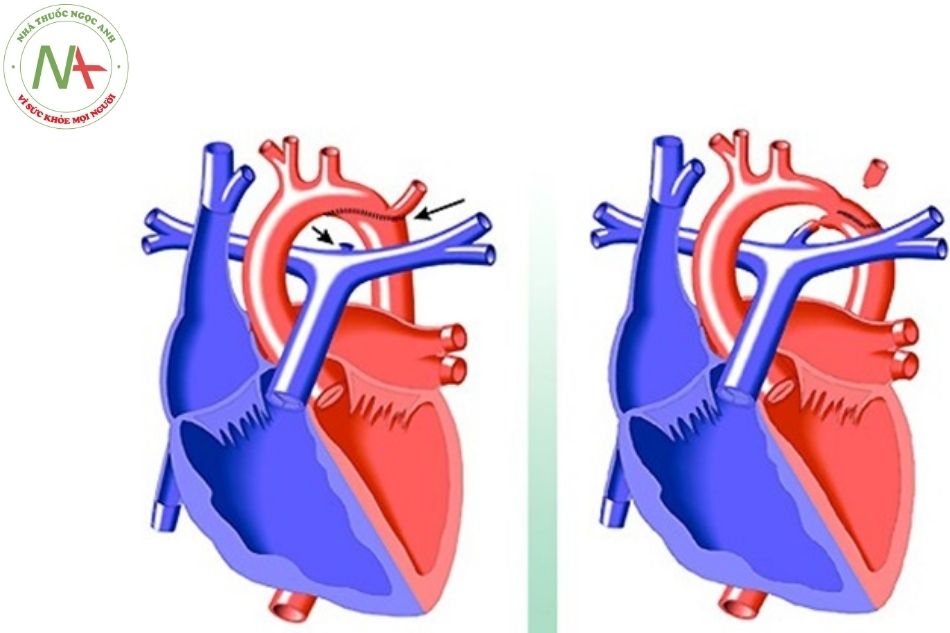
Ống động mạch (ductus arteriosus) là cấu trúc mạch máu nối giữa đoạn gần của động mạch chủ xuống với thân chung động mạch phổi gần chỗ xuất phát của động mạch phổi (thường là ĐMP trái, hiếm khi là ĐMP phải).
Bình thường, ống động mạch đóng dần từ 24 đến 48 giờ ngay sau sinh do sự co lại của lớp cơ trơn của thành ống. Sự đóng ống về mặt giải phẫu hoàn toàn tạo nên dây chằng động mạch xảy ra đến tuần thứ hai hoặc thứ ba sau sinh. Nếu quá trình đóng ống này ở trẻ không xảy ra, gọi là bệnh còn ống động mạch (patent ductus arteriosus).
Còn ống động mạch tạo sự thông thương giữa động mạch chủ và động mạch phổi và cần được đóng ống trước khi có biến chứng tăng áp động mạch phổi (pulmonary arterial hypertension – PAH) gây đảo chiều luồng thông qua ống (hội chứng Eisenmenger) và các biến chứng nặng khác của COĐM như suy tim trái, viêm nội tâm mạc nhiễm khuẩn (VNTMNK), vôi hoá thành ống động mạch.
Sự tồn tại và vai trò của ống động mạch đã được biết đến nhờ những nghiên cứu của Claudius Galen, một thầy thuốc người Hy Lạp từ thế kỉ hai sau Công nguyên. Một số nghiên cứu cho thấy đến thời cận đại vào năm 1564, nhà giải phẫu học người Ý Leonardo Botallo đã mô tả đầy đủ tổn thương bệnh và vì vậy ống động mạch còn được gọi là “ống Botallo”.
Bác sĩ Robert Gross báo cáo bệnh nhân được phẫu thuật thắt ống động mạch đầu tiên thành công vào năm 1938 tại bệnh viện trẻ em Boston.
Phương pháp đóng ống động mạch bằng đường ống thông được báo cáo lần đầu tiên bởi tác giả Portsman vào năm 1967. Cho đến nay, cùng với rất nhiều sự cải tiến về dụng cụ và thiết bị, can thiệp bít ống động mạch qua đường ống thông là phương pháp điều trị chính cho bệnh lý này.
Tỷ lệ còn ống động mạch có triệu chứng là 1/2000 trẻ sơ sinh đủ tháng hoặc chiếm 5-10% tất cả các bệnh tim bẩm sinh, hay gặp ở nữ giới (tỷ lệ nữ/nam là 2:1). Tuy nhiên, COĐM chiếm 50% ở trẻ sinh non, thiếu tháng và chiếm tới 80% trẻ sinh non thiếu tháng rất nhẹ cân (dưới 1000 gram).
Tiến triển tự nhiên của còn ống động mạch
- Trẻ sinh thiếu tháng thời gian đóng ống chậm hơn và tỉ lệ nghịch với tuổi Tỷ lệ đóng COĐM tự phát ở trẻ sinh non từ 35% tới 75% trong năm đầu đời. Một điểm đặc biệt ở trẻ sinh non là khả năng mở lại ống động mạch sau khi đã đóng ống có thể xảy ra tự phát hoặc sau điều trị với indomethacin (có nghiên cứu cho tỉ lệ tái mở lại ống khoảng 23%). Tỉ lệ tái mở ống động mạch tăng tỉ lệ nghịch tuổi thai, xảy ra thường ở trẻ có tuổi thai dưới 27 tuần khi so sánh với nhóm có tuổi thai từ 27 đến 33 tuổi thai (với tỉ lệ tương ứng là 37% và 11%).
- Ở trẻ sinh đủ tháng, sự kiện đóng ống động mạch chức năng xảy ra ở 50% trẻ sau sinh trong 24 giờ đầu, trong 90% trẻ sau 48 giờ và đạt 100% sau 72 tiếng. Quá trình đóng hoàn toàn về giải phẫu kéo dài từ hai đến ba tuần và thậm chí kéo dài tới vài tháng. COĐM lớn thường không thể tự đóng được.
- Tần suất tự đóng COĐM sau giai đoạn thơ ấu là 0,6% mỗi năm và thường xảy ra với ống ĐM kích thước nhỏ. Với COĐM lớn, 79% trẻ có thể tiến triển thành hội chứng Eisenmenger nếu không được điều trị.
Các yếu tố về gen và di truyền
- Đột biến gen trong Hội chứng Holt-Oram, hội chứng Cantu, CHARGE, DiGeorge, Down, Noonan.
- Bố mẹ COĐM làm tăng nguy cơ mắc tim bẩm sinh ở con cái lên 8%. Và bệnh nhân COĐM sẽ làm tăng 3% xuất hiện bệnh lý này ở anh chị em ruột.
Hình thái học và sinh lý bệnh
Phôi thai học
Trong sự phát triển phôi thai bình thường của cơ thể, phần bụng của cung động mạch chủ (ĐMC) số VI (sixth aortic arch) bên phải và trái hình thành nên động mạch phổi (ĐMP) phải và trái. Trong khi phần lưng của cung ĐMC số VI bên phải cuộn lại, phần lưng của cung ĐM chủ số VI bên trái hình thành OĐM và nối với ĐMC ngực xuống (descending aorta) ở vị trí ngay phía xa của động mạch (ĐM) dưới đòn trái. Về phía đầu ĐMP, OĐM thường đổ vào ở chỗ nối thân chung và nhánh ĐMP trái. OĐM là một mạch nối quan trọng giữa thân chung ĐMP và ĐMC với chức năng dẫn máu chảy từ ĐMP sang ĐMC, chuyển hướng dòng máu trong tuần hoàn bào thai.
Còn ống động mạch là dị tật rất hay gặp ở trẻ em. Bình thường sau khi trẻ ra đời, ống động mạch sẽ bị đóng về mặt chức năng (do có sự co thành mạch). OĐM bình thường sẽ đóng trong vòng 12 tiếng đến 2-3 ngày sau sinh, phụ thuộc vào nồng độ prostaglandin (PG) trong máu và nồng độ oxy trong máu động mạch. Nồng độ PGE2 cao trong tuần hoàn thai nhi là nhờ rau thai tổng hợp và do giảm độ thanh thải ở phổi. PGE2 hoạt động như một chất có tác dụng giãn cơ trơn của OĐM và duy trì hoạt động của nó trong suốt thời kỳ bào thai. Ngay sau khi trẻ sinh ra đời, nồng độ oxy trong phổi tăng cao dẫn tới làm tăng áp suất riêng phần oxy máu động mạch hậu quả gây co mạch. Đồng thời sau sinh, do không còn rau thai và tăng lưu lượng máu lên phổi dẫn tới làm giảm nhanh chóng nồng độ PGE2, làm mất tác dụng gây giãn mạch lên OĐM, kết quả gây đóng OĐM.
Sau đó OĐM có đóng về giải phẫu do có sự tăng sinh áo trong của thành mạch, xảy ra trong tuần thứ hai và thứ ba sau sinh. OĐM còn tồn tại sau khi trẻ ra đời là bất thường, dị tật này có thể xảy ra đơn thuần hoặc xảy ra phối hợp với các dị tật khác (Hình 1). Có các yếu tố lâm sàng có thể làm cho OĐM vẫn còn sau sinh. Có một tỷ lệ cao ở những trẻ sinh non và những trẻ sống vùng núi cao còn tồn tại OĐM do nguyên nhân là giảm áp suất riêng phần của oxy. COĐM cũng hay gặp ở những bệnh nhân có nhiễm trùng trong thời kỳ bào thai như hội chứng Rubella bẩm sinh và bào thai phơi nhiễm với các thuốc như acid valproic hay còn gọi là hội chứng Valproate bào thai.
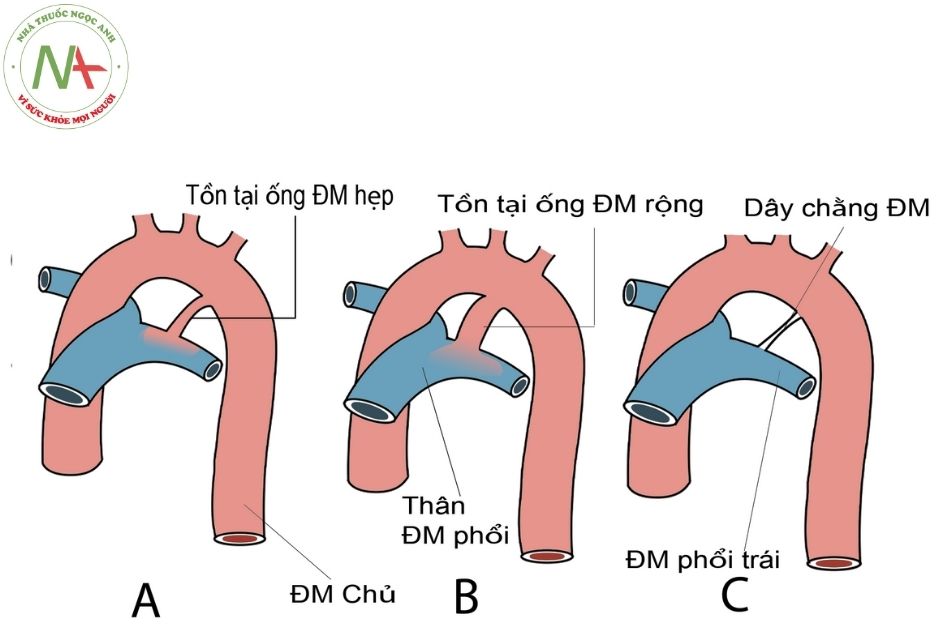
- Tồn tại ống động mạch nhỏ.
- Tồn tại ống động mạch lớn.
- Ống động mạch thoái triển bình thường tạo dây chằng động mạch. Chú thích: ĐM: Động mạch.
(Nguồn: Keith L. Moore, T.V.N. Persaud, Mark G. Torchia. Before we are born, 9th Ed 2016, 14, 222)
Phân loại hình thái học
Phân loại giải phẫu của ống động mạch sử dụng phân loại của Krichenko, đối với trẻ sinh non hình thái ống động mạch được xếp vào nhóm riêng, nhóm F:
- Type A: dạng hình nón hay “hình phễu”, chỗ hẹp nhất về phía ĐMP.
- Type B: ống ngắn có dạng “cửa sổ”, hẹp nhẹ về phía ĐMC.
- Type C: dạng hình “hình ống”, không có vị trí thắt hẹp.
- Type D: ống có dạng “hình túi”, với ống phình rộng ở giữa và thắt hẹp về phía đầu cả ĐMC và ĐMP.
- Type E: ống động mạch có dạng “hình nón thon dài” và thắt hẹp về phía ĐMP.
Riêng type F theo đề xuất của Ranjit Philip và cs, là dạng ống động mạch “type bào thai”, chỉ gặp ở trẻ đẻ non, với hình dạng dài, rộng và xoắn vặn.
Các tổn thương khác kèm theo: COĐM có thể gặp cùng với nhiều bất thường khác ở tim, đặc biệt có nhiều các dị tật phụ thuộc vào ống, có thể được chia làm 3 nhóm:
- Các bất thường chỉ có một nguồn cấp máu cho phổi như: teo tịt động mạch phổi kèm lành vách liên thất (pulmonary atresia with intact interventricular septum), tứ chứng Fallot với teo tịt động mạch phổi (tetralogy of Fallot with pulmonary atresia) mà không có tuần hoàn bàng hệ chủ – phổi và hẹp van ĐMP (pulmonary stenosis) nặng ở trẻ sơ sinh.
- Các bất thường tuần hoàn hệ thống phụ thuộc ống: hẹp khít động mạch chủ (aortic stenosis), hội chứng thiểu sản tim trái (hypoplastic left heart syndrome), Gián đoạn quai động mạch chủ (interrupted aortic arch), hẹp eo ĐMC (coarctation of the aorta) nặng.
- Chuyển gốc đại động mạch hoàn toàn (transposition of the great arteries) mà OĐM giúp cho trộn máu hai hệ thống tuần hoàn song song.
Có thể gặp COĐM đồng thời với bệnh tim bẩm sinh khác như: thông liên thất (TLT) (ventricular septal defect), thông liên nhĩ (TLN) (atrial septal defect)…
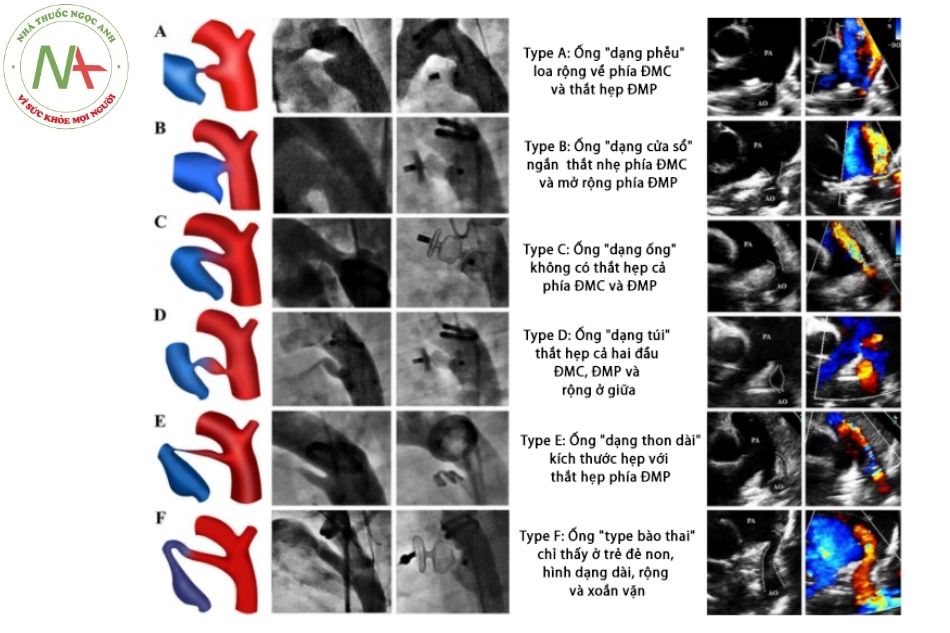
Chú thích:
Type A, C, B, C, D: Theo phân loại của Krichenko.
ĐMC: Động mạch chủ; ĐMP: Động mạch phổi.
(Nguồn: Ranjit Philip. (2016) Mor- phologic Characterization of the Patent Ductus Arteriosus in the Premature Infant and the Choice of Transcatheter Occlusion Device).
Sinh lý bệnh
Biểu hiện lâm sàng của bệnh phụ thuộc vào mức độ luồng thông trái → phải (left-to-right shunt) (phụ thuộc vào chiều dài và kích thước ống) cũng như tương quan giữa sức cản mạch phổi (pulmonary vascular resistance) và sức cản mạch hệ thống (systemic vascular resistance).
- Nếu OĐM nhỏ (Qp/Qs < 1,5) hay ống hạn chế lưu lượng sẽ có vận tốc cao, lưu lượng nhỏ và thường không gây quá tải thất trái.
- Với OĐM trung bình (Qp/Qs: 1,5 – 2,2), nhĩ trái và thất trái sẽ giãn dần do tăng máu về tim trái và có thể gây phì đại thất trái (giảm sức căng lên thành thất). Với các ống có lưu lượng lớn hơn, mức độ ảnh hưởng sẽ nhanh hơn. Việc tăng lưu lượng máu lên phổi nhiều sẽ làm thay đổi cấu trúc thành mạch và làm tăng sức cản mạch phổi.
- Với OĐM lớn (Qp/Qs > 2,2) có thể gây suy tim ở trẻ em. Theo thời gian, OĐM lớn không được can thiệp sẽ gây quá tải áp lực thất phải và ĐMP, gây tăng áp động mạch phổi (pulmonary arterial hypertension) nặng dẫn tới đảo chiều luồng thông qua OĐM (luồng thông phải → trái), và hậu là gây ra hội chứng
Chẩn đoán
Các đặc điểm lâm sàng phụ thuộc vào đường kính và chiều dài của OĐM và mối tương quan giữa sức cản mạch phổi và sức cản mạch hệ thống. Tần suất COĐM tăng ở nhóm trẻ sinh non, nhẹ cân. Chẩn đoán dựa vào các triệu chứng lâm sàng và cận lâm sàng.
Lâm sàng
COĐM im lặng (silent PDA)
- Trên lâm sàng tiếng tim bình thường, không có tiếng thổi.
- Thường phát hiện tình cờ qua siêu âm tim, không gây ảnh hưởng lên huyết động, không gây tăng áp mạch máu phổi (pulmonary hypertension) và có nguy cơ rất thấp gây viêm nội tâm mạc nhiễm khuẩn.
COĐM nhỏ
- Hay gặp, bệnh nhân ít triệu chứng hoặc không có triệu chứng, thường phát hiện muộn khi khám tim có tiếng thổi liên tục hoặc thổi tâm
- Có khi tình cờ được phát hiện qua các phương tiện chẩn đoán hình ảnh (siêu âm ..).
- Có thể có quá tải lên tim trái nhẹ, không có tăng áp mạch máu phổi, không có suy tim. Thăm khám lâm sàng thường không có gì đặc biệt ngoài tiếng thổi ở tim. Mỏm tim thường không lệch và tiếng T1,T2 không có biến đổi. Không có dấu hiệu mạch nảy mạnh chìm sâu. Cần lưu ý là tiếng thổi thường ở thì tâm thu đối với trẻ sơ sinh do áp lực động mạch chủ chỉ cao hơn động mạch phổi trong thì tâm thu. Sau giai đoạn này áp lực động mạch phổi dần dần hạ xuống và tiếng thối trở thành tiếng thổi liên tục. Cường độ tiếng thổi liên tục từ 3/6 trở xuống, đạt cực đại ngay trước và sau tiếng T2, không thay đổi theo vị trí, nghe rõ nhất ở dưới xương đòn trái.
- Viêm nội tâm mạc không phổ biến trong nhóm này nhưng được coi là một biến chứng của bệnh.
COĐM trung bình
- Bệnh nhân có thể có triệu chứng, nghe tim có tiếng thổi liên tục. Xuất hiện các dấu hiệu quá tải tim trái (giãn nhĩ trái, thất trái), tăng áp mạch máu phổi từ nhẹ đến trung bình, có thể có biểu hiện suy tim.
- Trên thăm khám lâm sàng có thể thấy tình trạng mỏm tim lệch trái do quá tải gánh thất trái và dấu hiệu mạch nảy mạnh chìm sâu. Tiếng thổi thường lớn hơn so với trường hợp OĐM nhỏ.
COĐM lớn
- Ống động mạch lớn ban đầu có thể có các biểu hiện suy tim trái do quá tải thể tích thất trái. Tuy vậy qua thời gian, tình trạng tăng áp động mạch phổi có thể tiến triển lâu dần dẫn đến tình trạng tăng sức cản mạch phổi cố định, đảo chiều luồng thông và bệnh nhân sẽ có biểu hiện tím (hội chứng Eisenmenger). Tiếng thổi liên tục đặc trưng của ống động mạch giảm và dần dần không còn.
- Ở trẻ sơ sinh, biểu hiện với các triệu chứng như chậm lớn, ăn kém và suy hô hấp. Trẻ lớn có thể biểu hiện khó thở và giảm khả năng gắng sức. Bệnh nhân người lớn có thể có biểu hiện suy tim trái (khó thở khi gắng sức, phù phổi cấp) hoặc ở giai đoạn muộn hơn là hội chứng Eisenmenger với biểu hiện tím và ngón tay dùi trống. Biểu hiện tím và ngón tay dùi trống đôi khi rõ rệt hơn ở chi dưới.
- Thăm khám lâm sàng các triệu chứng tương tự nhưng rõ rệt hơn so với trường hợp còn ống động mạch trung bình, tuy nhiên tiếng T2 thường tách đôi rõ, ngoài ra có thể nghe thấy rung tâm trương ở mỏm do tăng lưu lượng qua van hai lá. Đôi khi nghe tim không còn tiếng thổi liên tục mà chỉ còn tiếng thổi tâm thu ngắn do tăng áp phổi nhiều làm giảm dòng chảy trong kì tâm trương. Các trường hợp bệnh nhân hội chứng Eisenmenger sẽ không nghe thấy tiếng thổi nữa.
Chẩn đoán phân biệt
Tiếng thổi của COĐM có thể nhầm với tiếng thổi của các bệnh lý khác.
Tiếng thổi của COĐM là tiếng thổi liên tục, cường độ lớn, nghe ở vị trí dưới xương đòn trái lan tới bờ trái xương ức và sau lưng vùng cao bên trái. Khi luồng thông trái → phải, tiếng thổi sẽ tăng cường độ khi làm các nghiệm pháp làm tăng sức cản hệ thống, khi đó làm tăng luồng thông qua OĐM.
Tiếng thổi liên tục này cần phân biệt với một số bệnh sau:
- Rò động mạch vành (coronary artery fistula): tiếng thổi nghe được ở vùng trước tim, không phải ở phía trên đường cạnh ức trái.
- Cửa sổ chủ phế (aortopulmonary window): mạch ngoại vi nảy mạnh, tiếng thổi giống trong TLT, có các dấu hiệu của suy tim sung huyết.
- Thông động mạch tĩnh mạch phổi (pulmonary arteriovenous fistulas): tiếng thổi liên tục trên lưng, tím, ngón tay dùi trống, tim không
- Hẹp nhánh động mạch phổi ngoại biên (peripheral pulmonary stenosis): tiếng thổi liên tục có thể nghe được ở toàn vùng ngực, một bên hoặc hai bên.
- Hẹp đồng thời hở van động mạch chủ.
- Thông liên thất.
Cận lâm sàng
Điện tâm đồ
- COĐM nhỏ, hạn chế: điện tâm đồ bình thường.
- COĐM trung bình: giãn nhĩ trái (sóng P rộng, có 2 đỉnh ở DI và DII; 2 pha ở V1 với pha 2 rộng và sâu), PR kéo dài, phì đại thất trái, có thể có rung nhĩ.
- COĐM lớn, không được sửa chữa: có thêm hình ảnh phì đại hai thất, giãn nhĩ phải. Nếu áp lực ĐMP tăng cao, luồng thông đảo chiều thì có thể thấy hình ảnh phì đại thất phải chiếm ưu thế.
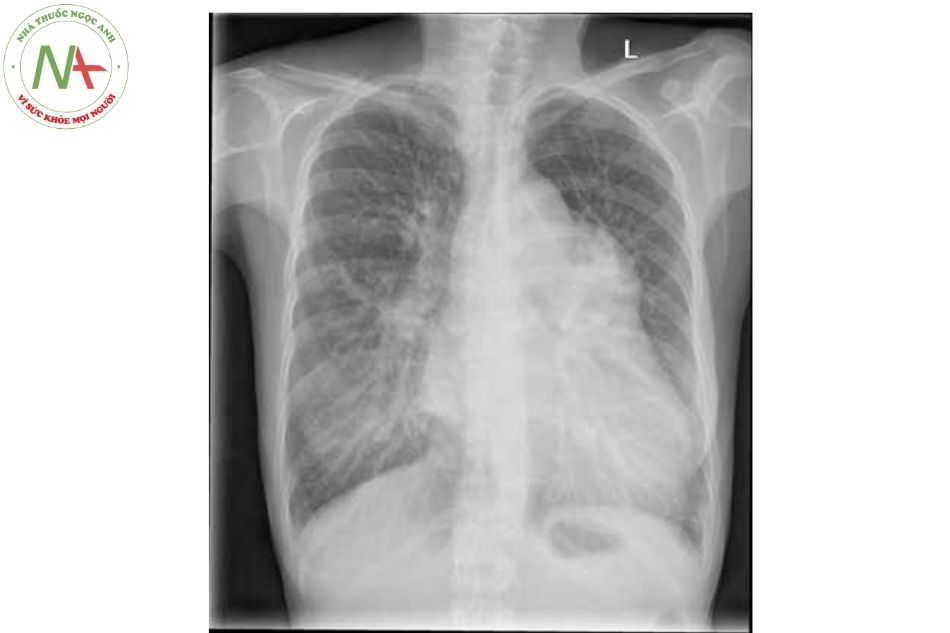
Phim Xquang lồng ngực
- Ở các bệnh nhân có ống động mạch nhỏ Xquang ngực bình thường.
- Hình ảnh quá tải thể tích tim trái: giãn nhĩ trái, giãn thất trái, giãn ĐMC lên.
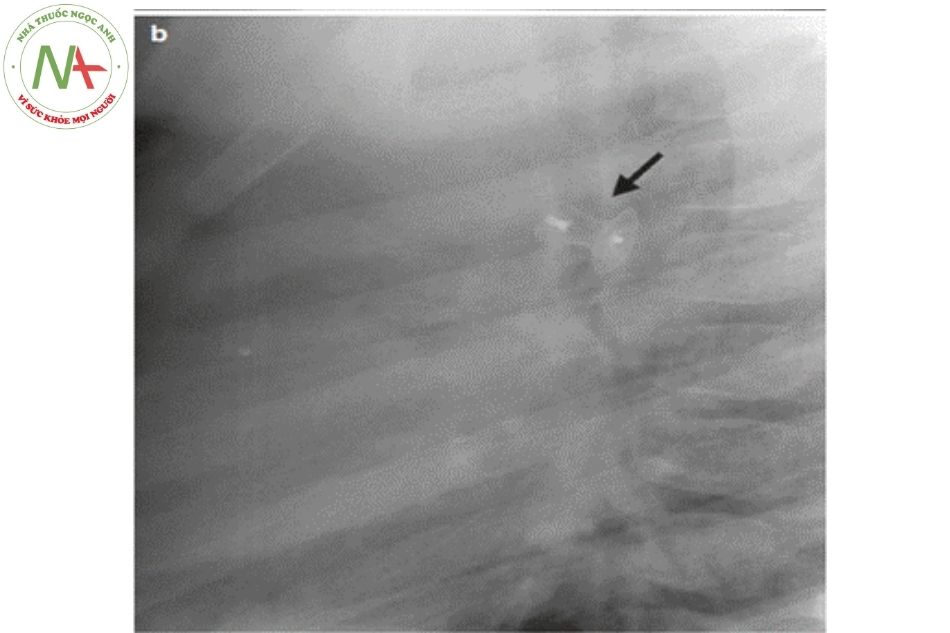
- Tăng áp mạch máu phổi: cung ĐMP nổi, tăng tưới máu mạch phổi. Ở giai đoạn muộn khi có hiện tượng tăng sức cản mạch phổi nhiều sẽ có hình ảnh co mạch phổi đoạn xa (bóng tim không to và giảm tưới máu phổi ở 1/3 ngoài trường phổi và vùng ĐMP đoạn gần giãn to).
- Có thể thấy hình ảnh calci hóa ở OĐM.
Siêu âm tim
Siêu âm 2D
Thường đánh giá hai mặt cắt chính:
- Mặt cắt cạnh ức: Ở mặt cắt trục ngắn ở phần cạnh ức cao với đầu dò chếch trái về phía chỗ chia động mạch phổi, OĐM có thể được nhìn thấy nối giữa động mạch phổi và động mạch chủ xuống. OĐM thường nối với động mạch phổi gần vị trí gốc động mạch phổi trái.
- Mặt cắt trên hõm ức: Thường thấy ống động mạch xuất phát từ động mạch chủ xuống tại ngang mức động mạch dưới đòn trái, đi ra phía trước về phía động mạch phổi. Di chuyển đầu dò sang bên và xuống dưới về xương đòn trái và xoay đầu dò theo chiều kim đồng hồ giúp cho quan sát rõ hơn OĐM và mối tương quan giải phẫu với các nhánh ĐMP và ĐMC xuống.
OĐM cũng có thể làm bỏ sót một hẹp eo ĐMC ở vị trí gần ống động mạch. Các dấu hiệu như van ĐMC hai lá, thiểu sản phần quai ĐMC, khoảng dãn rộng hơn giữa động mạch cảnh trong trái và động mạch dưới đòn trái… cần được lưu ý để tìm kiếm hẹp eo đồng chủ phối hợp.
Doppler màu
Thường nhìn thấy hình ảnh dòng màu phụt vào trong động mạch phổi. Dòng màu này thường đi theo bờ trái của động mạch phổi nhưng cũng có thể nằm ở trung tâm hoặc lệch phải. Ở bệnh nhân có áp lực động mạch phổi bình thường, dòng màu tăng tốc có thể thấy một cách dễ dàng ở cả thì tâm thu và tâm trương. Ở bệnh nhân có áp lực mạch phổi cao, có thể chỉ thấy dòng màu ở thì tâm trương.
Doppler màu cũng có giá trị trong trường hợp các ống động mạch nhỏ, các bệnh nhân người lớn do cửa sổ hình ảnh 2D có thể bị hạn chế hơn.
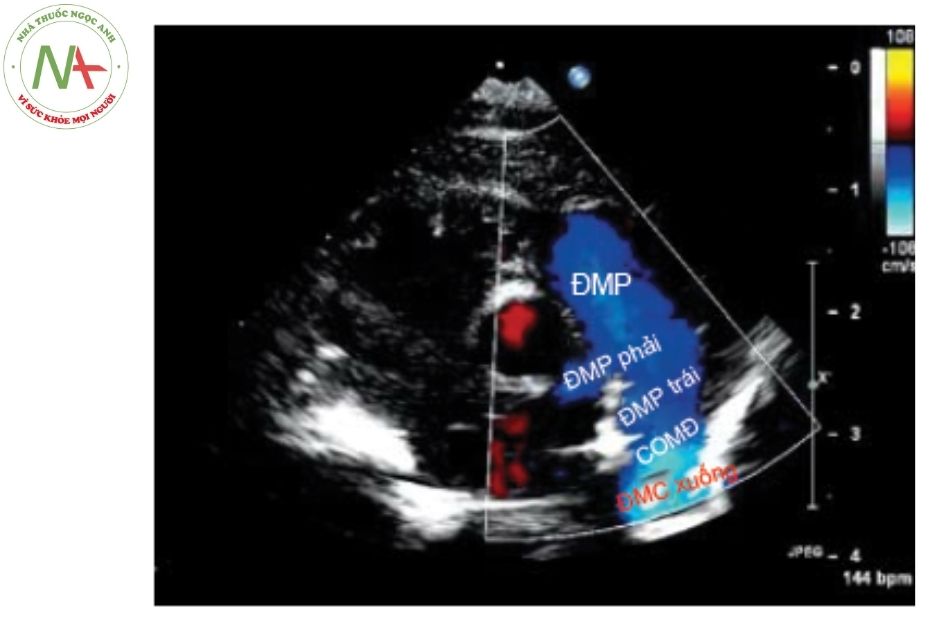
Chú thích: ĐMP: Động mạch phổi; ĐMC: Động mạch chủ.
Siêu âm Doppler
Giúp đánh giá mức độ luồng thông trái → phải và đánh giá áp lực mạch phổi.
Khi áp lực mạch phổi còn thấp hơn áp lực động mạch chủ sẽ thấy luồng thông liên tục trái → phải. Có thể dựa vào vận tốc đỉnh của luồng thông qua ống để xác định chênh áp giữa động mạch chủ và động mạch phổi, sau đó tính toán áp lực động mạch phổi bằng cách lấy huyết áp đo tay trừ đi chênh áp đo được. Vì vậy tốc độ đỉnh của luồng thông thấp có thể gợi ý tình trạng tăng áp mạch máu phổi.
Trong trường hợp áp lực mạch phổi tương đương với áp lực tuần hoàn hệ thống, trên Doppler xung có thể quan sát thấy luồng thông phải → trái thời kỳ tâm thu và luồng thông trái → phải trong thì tâm trương. Hoặc sử dụng siêu âm cản âm để xác định bọt cản âm vào ĐMC xuống mà không vào ĐMC lên.
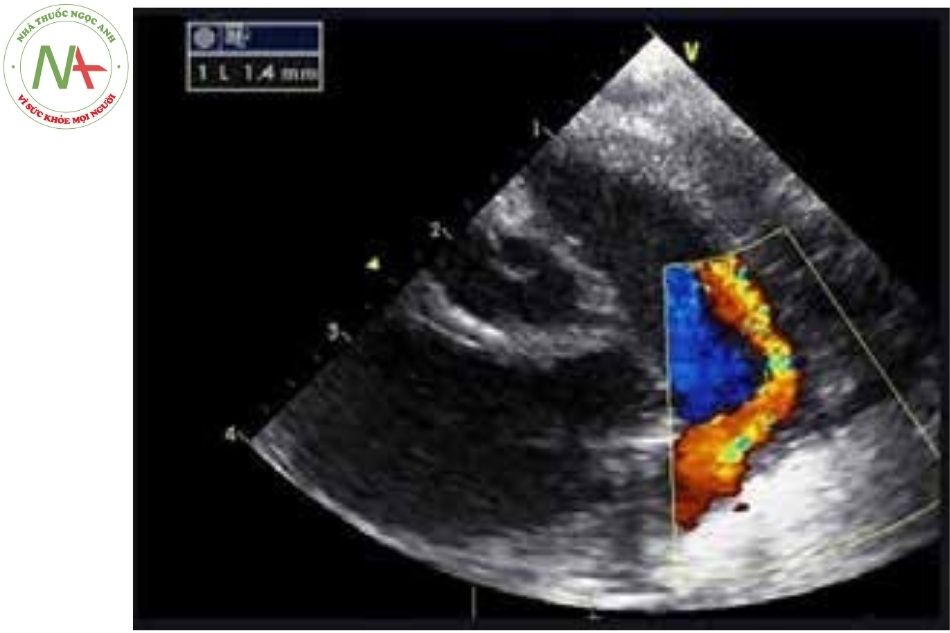
M-mode
Có thể quan sát thấy các dấu hiệu gợi ý luồng thông trái → phải, không thể chẩn đoán chính xác ống động mạch. Tỷ lệ đường kính nhĩ trái so với động mạch chủ lớn hơn 1,5 gợi ý luồng thông trái phải đáng kể.
Bảng 1. Các thông số siêu âm cho đánh giá COĐM
|
Chú thích: OĐM: ống động mạch; ĐMP: động mạch phổi; ĐMC: động mạch chủ.
Thông tim thăm dò huyết động
Việc sử dụng kỹ thuật thông tim hiếm khi cần cho chẩn đoán COĐM. Trong trường hợp bệnh nhân nghi ngờ COĐM, có tăng áp mạch máu phổi nhiều, lúc này kỹ thuật thông tim sẽ giúp cho chẩn đoán xác định COĐM, đánh giá chính xác áp lực ĐMP và sức cản mạch phổi, từ đó định hướng điều trị cho bệnh nhân.
Đối với bệnh nhân còn ống động mạch lớn, tăng áp động mạch phổi nặng, có luồng thông 2 chiều cần thông tim đánh giá sức cản mạch máu phổi, mức độ đáp ứng với nghiệm pháp giãn mạch phổi. Để đánh giá khả năng phục hồi của áp lực ĐMP, người ta tiến hành thông tim và làm nghiệm pháp giãn mạch phổi với việc hít khí oxit nitric (NO) hoặc thở Oxy hoặc các thuốc làm giãn mạch phổi (như iloprost) để quyết định khả năng đóng OĐM. Một cách đơn giản hơn, có thể đánh giá huyết động bằng nghiệm pháp đóng OĐM tạm thời với bóng, nếu tỉ số giữa áp lực tâm thu ĐMP/áp lực hệ thống < 0,5 khi đóng ống tạm thời thì có thể cân nhắc đóng được OĐM bằng dụng cụ hoặc phẫu thuật.
Chụp động mạch vành (ĐMV) được tiến hành cho nhóm bệnh nhân có nguy cơ, cần đánh giá nguy cơ mạch vành trước phẫu thuật đóng ODM.
Các kỹ thuật chẩn đoán hình ảnh khác
Chụp cắt lớp vi tính (CT) tim hoặc chụp cộng hưởng từ tim giúp ích cho chẩn đoán COĐM nếu nghi ngờ khi làm siêu âm tim hoặc do hình ảnh siêu âm tim không rõ ràng do giảm lưu lượng qua OĐM trong trường hợp có tăng áp mạch máu phổi nhiều hoặc cũng hữu ích để đánh giá hình thái giải phẫu của OĐM trước can thiệp.
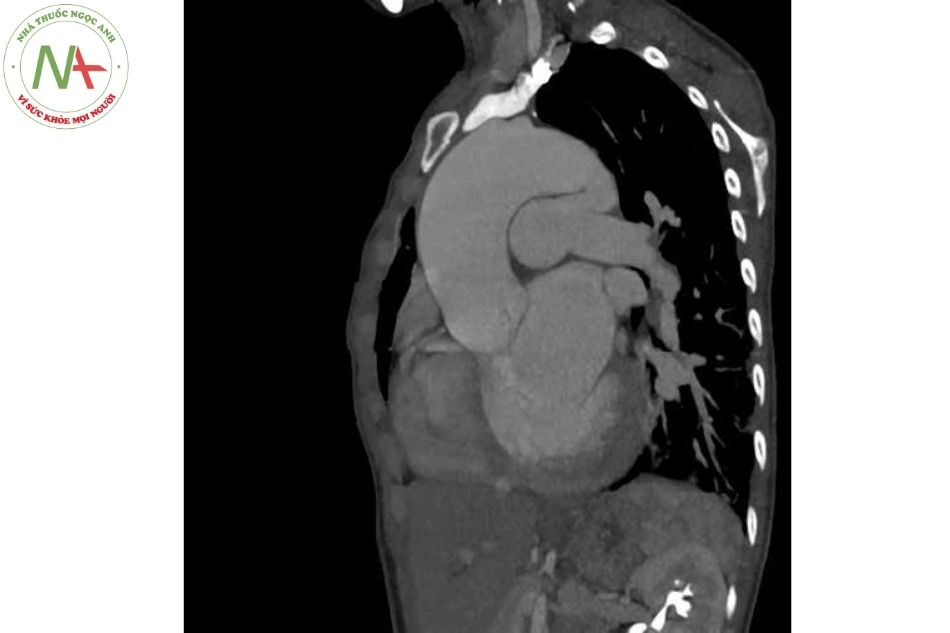
Chẩn đoán xác định
Chẩn đoán bệnh còn ống động mạch ta cần dựa vào một số dấu hiệu sau:
- Lâm sàng:
- Suy tim sung huyết: khó thở, gan to, tiểu ít, phù, nhịp tim nhanh, tim
- Mạch nảy mạnh chìm sâu.
- Thổi tâm thu hoặc thổi liên tục mạnh hơn ở thì tâm thu: khoang liên sườn II đường giữa đòn trái.
- T2 mạnh đáy tim trong trường hợp có tăng áp động mạch phổi.
- Cận lâm sàng:
- Xquang ngực thẳng: bóng tim to, tăng tưới máu phổi, cung động mạch phổi phồng.
- Siêu âm tim: giúp chẩn đoán xác định, quan sát ống động mạch trên 2 mặt cắt: cạnh ức trục ngắn và trên hõm ức. Đồng thời đóng vai trò quan trọng trong đánh giá kích thước lỗ thông, chiều luồng thông, chênh áp qua ống động mạch.
Điều trị
Khuyến cáo xử trí còn ống động mạch ở trẻ em
(theo Uỷ ban quản lý bệnh tim bẩm sinh Ấn Độ 2019 và hội Tim mạch Nhi khoa Đức 2017)
Chỉ định đóng ống động mạch:
- COĐM nhỏ: Có thể đóng một cách tự nhiên. Do đó thời gian có thể can thiệp đóng ống từ 12 tháng đến 18 tháng tuổi (Chỉ định I).
- COĐM trung bình/lớn, có triệu chứng suy tim sung huyết, tăng áp mạch máu phổi nhiều: đóng sớm (trước 3 tháng tuổi) (Chỉ định I).
- COĐM trung bình, không có suy tim: đóng từ 6 tháng đến 1 năm tuổi (Chỉ định I). Nếu có biểu hiện chậm lớn, có thể đóng OĐM sớm hơn (Chỉ định IIa).
- Giãn nhĩ trái và/hoặc giãn thất trái, hoặc có tăng áp mạch máu phổi ở bệnh nhân COĐM luồng thông trái → phải (Chỉ định I) .
- Tiền sử viêm nội tâm mạc nhiễm khuẩn (Chỉ định I).
Khuyến cáo xử trí còn ống động mạch ở người trưởng thành
(Theo hội Tim mạch châu Âu)
Chống chỉ định đóng ống động mạch:
- Bệnh nhân có tăng áp mạch máu phổi nhiều với bệnh lý tắc nghẽn mạch phổi không phục hồi không đáp ứng với test giãn mạch phổi khi làm thông tim (hội chứng Eisenmenger).
- COĐM im lặng: Không cần điều trị do ống rất nhỏ, thường phát hiện tình cờ, không ảnh hưởng huyết động, không gây tăng áp mạch máu phổi và nguy cơ gây viêm nội tâm mạc nhiễm khuẩn rất thấp.
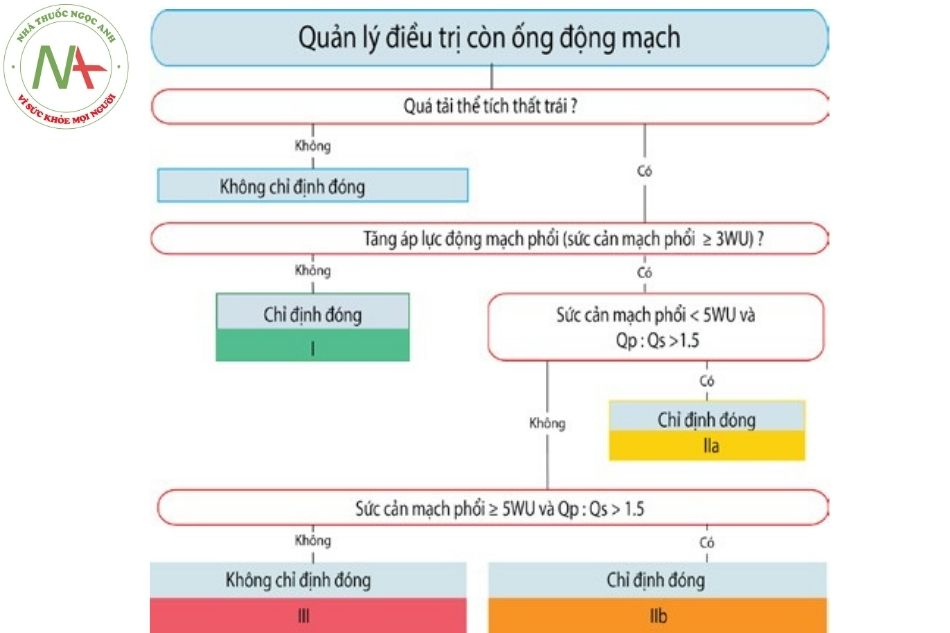
Bảng 2. Khuyến cáo ESC 2020 về đóng ống động mạch ở người trưởng thành
| Khuyến cáo | Mức khuyến cáo | Bằng chứng |
| Ở bệnh nhân có bằng chứng của việc quá tải thể tích thất trái và không tăng áp động mạch phổi (không có dấu hiệu tăng áp động mạch phổi trên thăm dò không xâm lấn hoặc thăm dò xâm lấn cho thấy sức cản mạch phổi < 3 WU), đóng ống động mạch được khuyến cáo bất kể có triệu chứng hay không. | I | C |
| Đóng ống động mạch bằng dụng cụ được khuyến cáo như biện pháp điều trị chính khi phù hợp với điều kiện kỹ thuật. | I | C |
| Ở bệnh nhân có tăng áp động mạch phổi với sức cản mạch phổi từ 3-5 WU, việc đóng ống động mạch có thể được cân nhắc khi luồng thông từ trái → phải có ý nghĩa (Qp:Qs > 1.5). | IIa | C |
| Ở bệnh nhân có tăng áp động mạch phổi với sức cản mạch phổi ≥ 5 WU, việc đóng ống động mạch có thể được cân nhắc khi luồng thông từ trái sang phải có ý nghĩa (Qp:Qs > 1.5) nhưng cần được đánh giá cẩn thận tại các trung tâm có kinh nghiệm. | IIb | C |
| Việc đóng ống động mạch không được khuyến cáo ở bệnh nhân có hội chứng Eisenmenger và ở bệnh nhân có tăng áp động mạch phổi nặng (sức cản mạch phổi≥ 5 WU) có giảm độ bão hòa oxy máu chi dưới khi gắng sức. | III | C |
Chú thích: Qp: Lưu lượng tuần hoàn phổi; Qs: Lưu lượng tuần hoàn hệ thống.
Các phương pháp đóng ống động mạch
Dùng thuốc
Các thuốc ức chế tổng hợp prostaglandin như indomethacin và ibuprofen, paracetamol được sử dụng với mục đích đóng ống động mạch ở trẻ đẻ non, nếu không có chống chỉ định.
Indomethacin không có tác dụng ở trẻ đủ tháng và trẻ lớn còn ống động mạch. Đường dùng thuốc có thể uống hoặc truyền. Ít nhất dùng 2 liều trước khi cân nhắc can thiệp đóng OĐM.
Không khuyến cáo điều trị dự phòng với indomethacin hoặc ibuprofen (Chỉ định III).
Đóng OĐM bằng dụng cụ qua đường ống thông
Ngày nay với tiến bộ cải tiến dụng cụ bít ống động mạch, có thể can thiệp bít ống động mạch cho trẻ có cân nặng thấp (kể cả trẻ đẻ non cân nặng thấp).
Kỹ thuật này được chọn cho bệnh nhân COĐM và có giải phẫu phù hợp. Hầu hết các trường hợp sử dụng dụng cụ (dù) bít OĐM, nhưng có thể sử dụng coils cho bít COĐM nhỏ (đường kính ống động mạch < 2-3 mm) hoặc còn luồng thông tồn lưu sau bít.
Phẫu thuật
Phẫu thuật được dành riêng cho những bệnh nhân không thể áp dụng được các phương pháp can thiệp đóng ống động mạch. Với đường vào qua đường mở ngực sau – bên bên trái không cần tim phổi nhân tạo, phẫu thuật viên có thể tiến hành thắt ống động mạch ở cả những trẻ sơ sinh < 1 kg.
Kỹ thuật thắt ống được lựa chọn dựa vào tuổi và kích thước của bệnh nhân:
- Phẫu thuật thắt ống ở trẻ đẻ non hoặc trẻ đủ tháng nhẹ cân (< 6 kg) có ưu thế hơn thủ thuật bít OĐM bằng dụng cụ qua da.
- Ở trẻ đủ tháng và trẻ lớn, vẫn sử dụng đường mổ qua khoang liên sườn 3 ở trẻ nhỏ và khoang liên sườn 4 ở trẻ lớn. Nhiều phẫu thuật viên lựa chọn phương pháp thắt nhiều mũi chỉ hoặc thắt và cắt để giảm thiểu tỷ lệ phải phẫu thuật lại.
- Phẫu thuật nội soi thắt ống động mạch: là một phương pháp ít xâm lấn và vẫn có hiệu quả Kỹ thuật mổ gồm quá trình phẫu tích tìm ống động mạch qua nội soi và sau đó đặt cặp clip. Chống chỉ định cho phương pháp nội soi bao gồm ống > 9 mm, đã phẫu thuật mở ngực trước đó, ống vôi hóa nhiều, đang có nhiễm trùng vị trí phẫu thuật hoặc phình ống.
- Ở hầu hết các bệnh nhân người lớn, đóng bằng dụng cụ qua da là lựa chọn hàng đầu. Phẫu thuật cũng được chỉ định khi OĐM quá lớn cho đóng bằng dụng cụ, khi OĐM có dạng phình lớn hay khi có viêm nội tâm mạc nhiễm khuẩn tiến triển. Ở người lớn, thắt ống đôi khi rất khó do OĐM thường lớn, vôi hoá và mô dễ tổn thương làm tăng nguy cơ vỡ ống khi kẹp thắt hoặc tách thành động mạch. Vì vậy, phẫu thuật chỉ đặt ra khi không thể bít OĐM qua đường ống thông được. Có thể sử dụng miếng vá vào ĐMC hoặc ĐMP sau khi cắt ống. Phẫu thuật thắt OĐM thường đi đường ngực bên, không cần chạy tuần hoàn ngoài cơ thể.
Tăng áp mạch máu phổi nhiều với bệnh lý tắc nghẽn mạch phổi không phục hồi không đáp ứng với test giãn mạch phổi khi làm thông tim là một chống chỉ định phẫu thuật.
Phẫu thuật thắt ống có nguy cơ gây các biến chứng khác như: tổn thương dây thanh quản và có thể gây liệt dây thanh âm một bên, túi phình giả OĐM, liệt cơ hoành, tràn dịch màng phổi dưỡng chấp.
Theo dõi
Sau đóng ống: theo dõi lâm sàng, điện tâm đồ và siêu âm tim trong năm đầu tiên. Tuỳ từng trường hợp cần theo dõi thêm nếu còn luồng thông tồn dư hoặc các tổn thương kết hợp khác và có tăng áp mạch máu phổi hoặc có các dấu hiệu tim mạch bất thường.
Nguy cơ viêm nội tâm mạc nhiễm khuẩn (VNTMNK) tăng tương ứng với kích thước OĐM: với các OĐM có kích thước nhỏ sẽ có nguy cơ VNTMNK thấp, cũng có những bằng chứng cho chỉ định bít COĐM nhỏ để giúp ngăn ngừa nguy cơ này.
Dự phòng kháng sinh không được khuyến cáo cho trường hợp COĐM chưa đóng, tuy nhiên khuyến cáo trong dự phòng VNTMNK trong 6 tháng từ sau khi đóng OĐM qua da hay phẫu thuật hoặc khi còn luồng thông tồn dư. Đồng thời, bệnh nhân vẫn được khuyến cáo cần tiếp tục chăm sóc răng miệng định kỳ.
Điều trị ở phụ nữ có thai
Có thai là chống chỉ định tuyệt đối ở bệnh nhân có hội chứng Eisenmenger do nguy cơ tử vong cao trong quá trình thai sản.
Có thai được dung nạp tốt nếu bệnh nhân không có tăng áp động mạch phổi.
Quá tải thể tích thất trái có thể tiến triển trong quá trình có thai ở bệnh nhân COĐM chưa can thiệp (biểu hiện các triệu chứng như khó thở hay rối loạn nhịp). Cần theo dõi diễn biến các triệu chứng suy tim trái ở 3 tháng cuối của thai kỳ và khi sinh.
Tài liệu tham khảo
1.Phạm Nguyễn Vinh, Nguyễn Lân Hiếu và cs. (2012). Khuyến cáo 2010 của Hội tim mạch học Việt Nam về xử trí bệnh tim bẩm sinh ở người lớn. Khuyến cáo 2010 về các bệnh lý tim mạch và chuyển hoá. Nhà xuất bản Y học chi nhánh Hồ Chí Minh, Tp.Hồ Chí Minh, Việt Nam, tr.23-25.
2. Helmut Baumgartner, Julie De Backer, Sonya V Babu-Narayan et al, ESC Scientific Document Group, 2020 ESC Guidelines for the management of adult congenital heart disease: The Task Force for the management of adult congenital heart disease of the European Society of Cardiology (ESC), European Heart Journal, https:// doi.org/10.1093/eurheartj/ehaa554.
3. Nikolaus A. Haas, Karl R. Schirmer et al. 2017 Guidelines for the Management of Congenital Heart Diseases in Childhood and Adolescence. Guideline committee of the German Society of Paediatric Cardiology (DGPK), Düsseldorf, Germany. Cardiology in the Young (2017), 27(Suppl. 3), S1–S105.
4. Ranjit Philip, B. Rush Waller III, Vijaykumar Agrawal et al. (2016) Morphologic Characterization of the Patent Ductus Arteriosus in the Premature Infant and the Choice of Transcatheter Occlusion Device. Catheterization and Cardiovascular Interventions 87:310–317.
5. Schneider D.J., Moore W., Patent ductus arteriosus.(2006) Circulation. ;114:1873–1882.
6. Krichenko A., Benson L.N., Burrows , Moes C.A., McLaughlin P., Freedom R.M.(1989) Angiographic clas- sification of the isolated, persistently patent ductus arteriosus and implications for percutaneous catheter occlusion. Am J Cardiol.;63:877–880.
7. DeFaria Yeh , King M.E. (2015) Congenital heart disease in the adult: what should the adult cardiologist know? Curr Cardiol Rep.;17(4):25.
8. Stout K. et al. 2018 AHA/ACC Guideline for the Management of Adults With Congenital Heart Disease. JACC 73(12): e81-192.
9. Saxena A., et al. (2019) Indian guidelines for indications and timing of intervention for common congenital heart diseases: Revised and updated consensus statement of the Working group on management of congen- ital heart diseases. Ann Pediatr Card;12:254‐286.