Bệnh hô hấp
Bệnh phổi mô kẽ: Phân loại, chẩn đoán và hướng dẫn điều trị
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
Bài viết “Bệnh phổi mô kẽ: Phân loại, chẩn đoán và hướng dẫn điều trị” – Tải file PDF Tại đây.
Tác giả TS.BS. NGUYỄN VĂN THÀNH
ĐẶT VẤN ĐỀ
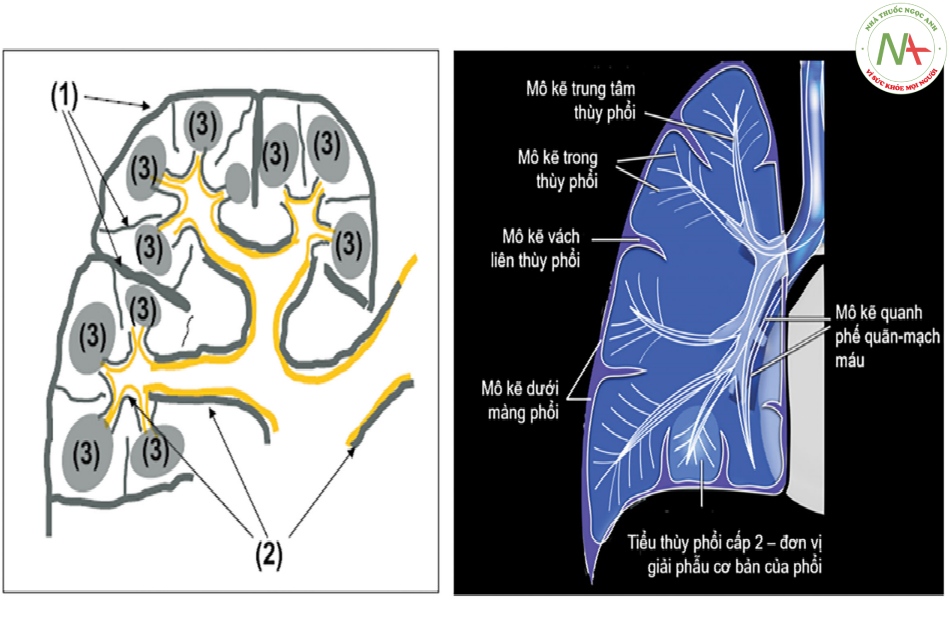
Mô kẽ phổi là thuật ngữ để chỉ cấu trúc mô liên kết (connective tissue) phân bố quanh phế quản – mạch máu, quanh phế nang và dưới màng phổi tạng.
Bệnh phổi mô kẽ (Interstitial lung disease – ILD) hay còn gọi là bệnh nhu mô phổi lan tỏa (Diffuse parenchymal lung disease – DPLD) là một thuật ngữ gộp, bao gồm nhiều bệnh, không đồng nhất, liên quan tới mô kẽ phổi với nhiều cơ chế và nhiều nguyên nhân khác nhau, gây hậu quả viêm và xơ hóa. Mặc dù một số bệnh có tác động tới mô kẽ ở tất cả các khu vực nhưng cũng có một số bệnh chỉ tập trung ở mô kẽ một khu vực nhất định. Đặc điểm chính của bệnh phổi mô kẽ là viêm, xơ hóa phổi hay kết hợp viêm và xơ hóa phổi ở các mức độ khác nhau. Một tác nhân gây bệnh có thể gây ra nhiều dạng tổn thương ở mô kẽ và, ngược lại, một dạng tổn thương ở mô kẽ cũng có thể là hậu quả của nhiều tác nhân gây bệnh khác nhau. Thuật ngữ và phân loại bệnh phổi mô kẽ đã có nhiều thay đổi theo thời gian trên cơ sở hiểu biết của y học. Có thể gộp trong khái niệm bệnh phổi mô kẽ 3 nhóm bệnh: i) Viêm phổi mô kẽ tự phát (Idiopathic interstitial pneumonias) hay còn gọi là viêm phổi không nhiễm trùng, ii) Viêm phổi quá mẫn cảm (Hypersensitivity pneumonitis) hay còn gọi là bệnh viêm phế nang dị ứng ngoại sinh (Extrinsic allergic alveolitis) và iii) Viêm phổi tổ chức hóa (Organizing pneumonia) trước đây còn gọi là viêm phổi tổ chức hóa tắc nghẽn tiểu phế quản (Bronchiolitis obliterans organizing pneumonia). Xơ hóa phổi đi kèm khí phế thũng không nằm trong khái niệm bệnh phổi mô kẽ, thông thường những bệnh nhân này có sinh bệnh học liên quan tới thuốc lá.
Viêm phổi mô kẽ tự phát
Bệnh được Von Buhl ghi nhận lần đầu vào năm 1872 và đến 1933, 1935 Louis Hamman, Arnol Rich thông báo những ca bệnh đầu tiên và đặt tên cho hiện tượng xơ hóa mô kẽ phổi lan tỏa là hội chứng Hamman-Rich. Năm 2002, trong biên bản đồng thuận phân loại bệnh viêm phổi mô kẽ tự phát ATS/ERS tách riêng viêm phổi mô kẽ tự phát khỏi nhóm các bệnh viêm nhu mô lan tỏa có xác định nguyên nhân và bệnh phổi mô kẽ tự phát tạo u hạt. Năm 2011, tuyên bố của liên Hội ATS/ERS/JRS/ALA (ATS: American Thoracic Society, ERS: European Respiratory Society, JRS: Japanese Respiratory Society, ALAT: Latin American Thoracic Association) cho phép chẩn đoán viêm phổi mô kẽ tự phát bằng hình ảnh X-quang có biểu hiện viêm mô kẽ thông thường mà không cần sinh thiết ngoại khoa. Năm 2018, tài liệu hướng dẫn lâm sàng của liên Hội trên đã đưa ra các tiêu chí nhận dạng X-quang của bệnh viêm phổi mô kẽ thông thường và chẩn đoán phân biệt. Cũng vào thời gian này, Hội Fleischner (một tổ chức quốc tế chuyên về X-quang lồng ngực) cũng đề xuất các tiêu chuẩn chẩn đoán bệnh viêm phổi mô kẽ tự phát và nhấn mạnh vai trò của CT trong chẩn đoán.
Viêm phổi quá mẫn cảm
Ramazzini là người mô tả đầu tiên bệnh phổi có liên quan tới quá mẫn từ năm 1713 trên những người lao động có tiếp xúc với hạt ngũ cốc với các biểu hiện khó thở, suy mòn và phù được cho là suy tim phải. Tới 1930 thuật ngữ “bệnh phổi của người làm nông trại” xuất hiện với mô tả của Campbell ghi nhận trên những người làm nông trại tiếp xúc với cỏ khô mốc có triệu chứng khó thở cấp tính tồn tại trong nhiều tuần lễ và phát triển xơ phổi trên một số trường hợp. Cũng trong khoảng thời gian này, Towey cũng mô tả một số trường hợp bệnh khó thở nặng, ho, ra mồ hôi ban đêm, sụt cân trên các công nhân làm đường sắt. Công nhân làm đường sắt phải tiếp xúc với bụi từ vỏ cây phong có chứa bào tử nấm Cryptostroma corticale. Towey và cộng sự đã kết luận công nhân mắc bệnh miễn dịch có liên quan tới việc hít bào tử nấm. Ngày nay bệnh viêm phổi quá mẫn cảm được xem là bệnh viêm đưa tới xơ hóa phổi do phản ứng miễn dịch trên những người có nhạy cảm với các kháng nguyên hít. Các kháng nguyên có khả năng gây bệnh thông thường có nguồn gốc từ vi sinh, chim, chất hữu cơ. Tuy nhiên cũng có đến 50% các trường hợp bệnh phổi mô kẽ không xác định được kháng nguyên. Theo thông lệ, viêm phổi quá mẫn cảm được chia thành 3 dạng cấp tính, bán cấp và mạn tính tùy thuộc vào thời gian, tần suất và mức độ phơi nhiễm. Tuy nhiên, về lâm sàng cũng có thể phân loại thành dạng hoạt động hay di chứng. Gần đây (năm 2020) tài liệu hướng dẫn lâm sàng của ATS/JRS/ALAT đề nghị phân loại có tính khách quan hơn theo cách có liên quan lâm sàng, đó là viêm phổi quá mẫn cảm có hay không xơ hóa.
Viêm phổi tổ chức hóa
Những mô tả khám nghiệm tử thi những trường hợp viêm phổi điều trị không đáp ứng tử vong được thông báo đầu tiên vào đầu thế kỷ XX. Các ghi nhận cho thấy có hiện tượng tiết dịch trong lòng phế nang cùng với sự gia tăng phân chia các nguyên bào sợi và tạo ra cấu trúc dạng mô liên kết như mô tả kinh điển của Laennec ở giai đoạn sung huyết và gan hóa nhưng sau đó không được hấp thu. Ý niệm cho rằng viêm phổi tổ chức hóa luôn luôn là di chứng từ viêm phổi nhiễm khuẩn đã thay đổi do những hiểu biết hiện nay cho thấy viêm phổi tổ chức hóa có thể xuất hiện do có tác động của hiện tượng gây độc, tự miễn hoặc không biết lý do. Năm 1986, Basset thông báo nhiều trường hợp có các biến đổi dạng xơ hóa và tổ chức hóa trong lòng phế nang trên nhiều loại bệnh mô kẽ phổi, trong đó có bệnh bụi phổi (pneumoconiosis), sarcoidosis, viêm phổi quá mẫn cảm. ATS/ERS năm 2013 sử dụng thuật ngữ viêm phổi tổ chức hóa không rõ căn nguyên (Cryptogenic organizing pneumonia) và xếp bệnh này vào nhóm các bệnh viêm phổi xơ hóa mô kẽ tự phát (Idiopathic interstitial pneumonia).
Tóm lại, bệnh phổi mô kẽ là một thuật ngữ chung để chỉ một nhóm lớn các bệnh gây ra xơ hóa phổi. Xơ hóa là tổn thương phổi không thể hồi phục và tiến triển nặng dần theo thời gian. Nhiều nguyên nhân mà chúng ta còn biết rất ít về chúng có thể gây ra hoặc làm tăng nguy cơ mắc bệnh bệnh phổi mô kẽ, bao gồm di truyền, một số loại thuốc hoặc phương pháp điều trị y tế (như xạ trị, hóa trị), phơi nhiễm hóa chất hoặc dị nguyên, nhiễm trùng. Bệnh nhân mắc các bệnh tự miễn dịch như sarcoidosis hoặc viêm khớp dạng thấp cũng có nguy cơ phát triển bệnh phổi mô kẽ. Hút thuốc lá không chỉ có thể gây ra bệnh phổi mô kẽ mà còn làm cho tình trạng bệnh trở nên tồi tệ hơn.
CHẨN ĐOÁN
Khám lâm sàng bệnh nhân bệnh phổi mô kẽ là quan trọng nhưng lại thiếu các dấu hiệu, triệu chứng giúp xác định một bệnh cụ thể. Năm 1816, Laennec đã phát minh ra ống nghe và tìm mối tương quan giữa âm thanh nghe với kết quả khám nghiệm tử thi. Ông mô tả phân biệt tiếng ran nổ và tiếng ran velcro (tiếng giống âm thanh phát ra khi mở khóa dán, velcro), là những manh mối có giá trị cho chẩn đoán lâm sàng bệnh phổi mô kẽ. Năm 1945, Eder mô tả biến dạng ngón tay và ngón chân như một dấu hiệu lâm sàng của bệnh phổi mô kẽ.
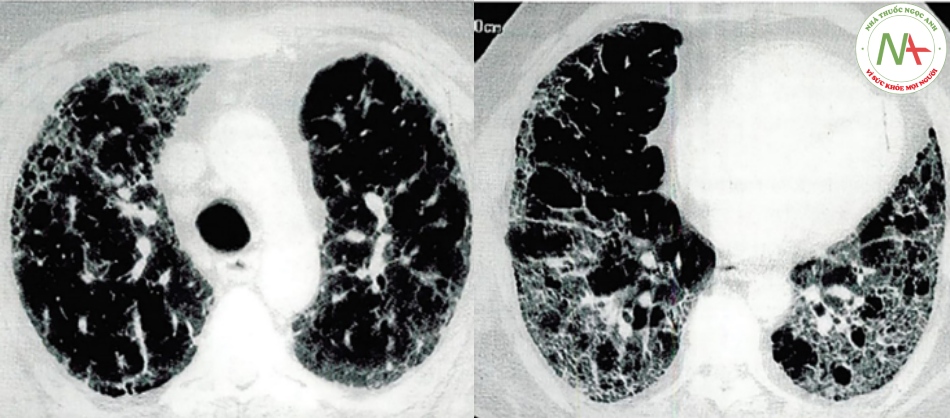
Phát minh kỹ thuật chụp X-quang vào năm 1895 là một bước tiến quan trọng của y học trong việc nhận diện hình ảnh các tổn thương phổi. Năm 1933, Kerley mô tả sự dày lên của các cấu trúc kẽ dưới màng phổi mà đôi khi gặp trong bệnh phổi mô kẽ. Scadding (năm 1961) đề xuất việc phân giai đoạn sarcoidosis bằng hình ảnh X-quang. Mặc dù MRI cũng đã được sử dụng trong chẩn đoán bệnh phổi mô kẽ nhưng CT mới thực sự mở đường cho việc tiếp cận chẩn đoán và phân loại bệnh phổi mô kẽ hiện đại. Hiệp hội Fleischner (năm 2008) xếp hình ảnh tổ ong là tiêu chuẩn chính trong chẩn đoán xơ hóa mô kẽ phổi thông thường (Usual interstitial pneumonia – UIP, hình ảnh hay gặp nhất trong bệnh phổi mô kẽ).
Nội soi phế quản mềm được đưa vào thực hành lâm sàng từ năm 1968 và dịch rửa phế quản phế nang (BAL) đã được sử dụng như một công cụ nghiên cứu và thực hành lâm sàng cho các bệnh phổi mô kẽ khác nhau. Nội soi cũng là nền tảng để phát triển các kỹ thuật sinh thiết phổi có giá trị chẩn đoán cao và hầu như có thể thay thế được sinh thiết bằng phẫu thuật mở lồng ngực. Lưu ý chỉ định nội soi và thực hiện các kỹ thuật chẩn đoán có thể làm xuất hiện đợt cấp.
Chẩn đoán bệnh phổi mô kẽ cần dựa trên tất cả các thông tin lâm sàng, X-quang và xét nghiệm nhiều nhất có thể. Tốt nhất gồm tiền sử bệnh nhân (bao gồm phơi nhiễm và nghề nghiệp), các triệu chứng, dấu hiệu lâm sàng và kết quả các xét nghiệm chức năng phổi, siêu âm tim, xét nghiệm huyết thanh cho chẩn đoán bệnh mô liên kết. Chụp CT ngực chất lượng cao, nội soi phế quản với xét nghiệm dịch rửa phế quản – phế nang, và sinh thiết phổi cần được phân tích. Cũng cần lưu ý khoảng 10% các trường hợp không thấy được bất thường trên X-quang và CT ngực.
Bảng: Tổn thương mô học và dạng bất thường trên CT ngực (Nguồn: Kevin R. Flaherty,
Fernando J. Martinez. Diagnosing interstitial lung disease: A practical approach to a difficult
problem. Clevelan D Clinic Journal of Medicine Volume 68. Number 1 January 2001).
| Tồn thương mô học tiếng Việt | Tổn thương mô học tiếng Anh | Dạng bất thường trên CT ngực |
| Viêm phổi kẽ thông thường (UIP) | Usual interstitial pneumonia | Mờ dạng tồ ong thùy dưới |
| Viêm phổi kẽ không đặc hiệu (NSIP) | Nonspecific interstitial pneumonia | Mờ dạng kính mờ thùy dưới |
| Viêm phổi tồ chức hóa (OP) | Organizing pneumonia mạch máu hoặc ngoại vi | Mờ quanh phế quản |
| Tồn thương phế nang lan tỏa (DAD) | Diffuse alveolar damage dưới hoặc lan tỏa | Mờ dạng kinh mờ thùy |
| Viêm tiểu phế quản hô hấp (RB) | Respiratory bronchiolitis trung tâm tiểu thùy | Nốt mờ dạng kính mờ |
| Viêm phổi kẽ bong vảy | Desquamative interstitial pneumonia dưới | Mở dạng kính mờ thùy |
| Viêm phổi kẽ bạch huyết | Lymphoid interstitial pneumonia hoặc nốt quanh mạch bạch huyết | Mờ dạng kính mờ |
ĐIỀU TRỊ
Nguyên tắc là loại bỏ các tác nhân được xem là căn nguyên gây viêm phổi kẽ như thuốc, hóa chất. Điều trị các bệnh lý căn nguyên của viêm phổi kẽ như lupus ban đỏ hệ thống, xơ cứng bì, viêm khớp dạng thấp, viêm đa cơ. Thở oxy kéo dài khi bệnh nhân có biểu hiện suy hô hấp.
Điều trị không sử dụng thuốc
Gây xẹp phổi trong điều trị lao là biện pháp điều trị không sử dụng thuốc sớm nhất được áp dụng trong y học vào những năm 1930 cho những trường hợp xơ hóa phổi sau lao. Đến 1963, ca ghép phổi đầu tiên được thực hiện thành công mở ra một khả năng trị liệu cho người bị xơ phổi nặng. Tuy nhiên, thành công của ghép phổi chỉ thực sự có ý nghĩa khi đi cùng với trị liệu ức chế miễn dịch kéo dài. Kỹ thuật tuần hoàn ngoài cơ thể và cung cấp oxy bằng màng ngoài cơ thể (extracorporeal membrane oxygenation, ECMO) giúp tăng cường khả năng chỉ định phẫu thuật ghép. Hiện nay, xơ hóa mô kẽ phổi tự phát là chỉ định chính trong ghép phổi. Vận động thể lực và thực hiện các nội dung của phục hồi chức năng phổi (pulmonary rehabilitation) là trị liệu được khuyến cáo trong điều trị bệnh phổi mô kẽ. Oxy trị liệu kéo dài là trị liệu được áp dụng cho những trường hợp suy hô hấp mạn tính, giảm oxy máu. Trị liệu oxy tại nhà làm tăng chất lượng sống của người bệnh.
Điều trị sử dụng thuốc
Từ những năm 1940, corticosteroid đã được sử dụng với mục tiêu ngăn chặn sự tiến triển của tình trạng viêm dẫn đến xơ hóa không hồi phục. Từ những năm 1960, một số nghiên cứu cho thấy các trường hợp điều trị corticosteroid xấu đi sau khi ngừng thuốc. Những bệnh nhân này có thể là các trường hợp xơ phổi mô kẽ tự phát có liên quan đến viêm phổi kẽ không đặc hiệu, bệnh mô liên kết, viêm phổi quá mẫn cảm. Tuy nhiên, do thiếu bằng chứng năm 2011 tài liệu hướng dẫn của liên Hội ATS/ERS/JRS/ALAT không khuyến cáo bất kỳ trị liệu đặc hiệu nào trong bệnh xơ hóa phổi mô kẽ tự phát. Sau các thử nghiệm lâm sàng có hiệu quả, các thuốc ức chế tăng sinh xơ (nintedanib, pirfenidone) hiện nay đã được chấp thuận để điều trị bệnh phổi mô kẽ tự phát. Gần đây nintedanib đã được phê duyệt cho điều trị bệnh phổi mô kẽ tiến triển, bệnh phổi mô kẽ kết hợp xơ cứng bì toàn thân.
==>> Xem thêm: Điều trị suy hô hấp và hội chứng suy hô hấp cấp tính dựa theo hướng dẫn
Tài liệu tham khảo
- Sabina A. Guler, Tamera J. Corte. Interstitial Lung Disease in 2020: A History of Progress. Clin Chest Med. 42 (2021) 229-239.
- Raghu G, Remy-Jardin M, Myers JL et al. Diagnosis of idiopathic pulmonary fibrosis. An official ATS/ERS/ JRS/ALAT clinical practice guideline. Am J Respir Crit Care Med 2018;198(5):e44-68.
- Lynch DA, Sverzellati N, Travis WD et al. Diagnostic criteria for idiopathic pulmonary fibrosis: a Fleischner society white paper. Lancet Respir Med 2018; 6(2):138-53.
- Raghu G, Remy-Jardin M, Ryerson CJ et al. Diagnosis of hypersensitivity pneumonitis in adults. An official ATS/JRS/ALAT clinical practice guideline. Am JRespir Crit Care Med 2020;202(3):e36-69.
- Travis WD, Costabel U, Hansell DM et al. An Official American Thoracic Society/ European Respiratory Society statement: update of the international multidisciplinary classification of the idiopathic interstitial pneumonias. Am J Respir Crit Care Med 2013; 188(6):733-48.
- Kevin R. Flaherty, Fernando J. Martinez. Diagnosing interstitial lung disease: A practical approach to a difficult problem. Clevelan D Clinic Journal of Medicine Volume 68. Number 1 January 2001.
