Bệnh hô hấp
Vai trò của các liệu pháp cứu hộ trong điều trị ARDS nặng
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
Bài viết “Vai trò của các liệu pháp cứu hộ trong điều trị ARDS nặng” tải về tại đây.
Tác giả: Francesco Alessandri MD, Francesco Pugliese MD và V Marco Ranieri MD.
Bản dịch của BS. Đặng Thanh Tuấn – BV Nhi Đồng 1
Tóm tắt
ARDS được đặc trưng bởi phù phổi không do tim với các hình mờ trên X quang ngực hai bên và tình trạng giảm oxy máu khó điều trị bằng liệu pháp oxy. Đây là nguyên nhân phổ biến khiến bệnh nhân phải nhập viện ICU do suy hô hấp do thiếu oxy cần thở máy. Corticosteroid không được khuyến cáo ở bệnh nhân ARDS. Các liệu pháp cứu hộ làm giảm tình trạng thiếu oxy ở những bệnh nhân không thể duy trì mức oxy hợp lý: các thao tác huy động, tư thế nằm sấp, hít oxit nitric, thông khí dao động tần số cao và oxygen hóa qua màng ngoài cơ thể giúp cải thiện quá trình oxygen hóa, nhưng tác động của chúng đối với tỷ lệ tử vong vẫn chưa được chứng minh. Quản lý dịch truyền hạn chế dường như là một chiến lược thuận lợi mà không làm giảm đáng kể tỷ lệ tử vong trong 60 ngày. Các nghiên cứu trong tương lai là cần thiết để làm rõ hiệu quả của các liệu pháp này đối với kết quả ở những bệnh nhân mắc ARDS nặng.
Giới thiệu
ARDS là một tình trạng đe dọa tính mạng, là biến chứng của nhiều loại bệnh hiểm nghèo, bao gồm nhiễm trùng huyết, viêm phổi, viêm tụy và chấn thương.1 Nó được đặc trưng bởi tình trạng viêm phổi dữ dội, vi xẹp phổi tiến triển, tổn thương phế nang lan tỏa, tăng tính thấm mạch máu phổi, tăng trọng lượng phổi và mất mô thông khí.2 ARDS có liên quan về mặt lâm sàng với tình trạng thiếu oxy nghiêm trọng, không đồng bộ giữa bệnh nhân và máy thở, và khả năng cao bị chấn thương khí áp (barotrauma) và tổn thương phổi do máy thở (VILI, ventilator-induced lung injury).3
ARDS lần đầu tiên được mô tả cách đây 50 năm bởi Ashbaugh và Petty4 trong một loạt trường hợp gồm 12 bệnh nhân có chung đặc điểm là thở nhanh và thiếu oxy kéo dài bất thường, hình mờ trên phim X quang ngực và độ giãn nở phổi kém, mặc dù có các nguyên nhân cơ bản khác nhau. Năm 1994, Hội nghị Đồng thuận Hoa Kỳ và Châu Âu đã đề xuất một định nghĩa mới về ARDS được chấp nhận trên toàn cầu.5 Vào năm 2012, định nghĩa này đã được sửa đổi bởi một hội đồng chuyên gia quốc tế và hiện được gọi là định nghĩa Berlin về ARDS (Bảng 1).6 Một nghiên cứu quan sát lớn gần đây 7đã báo cáo tỷ lệ mắc ARDS là 10,4% trong tất cả các trường hợp nhập viện ICU và 23,4% trong số tất cả các đối tượng được thở máy. ARDS dường như không được công nhận, điều trị đúng mức và có liên quan đến tỷ lệ tử vong đặc biệt cao là 46,1% đối với bệnh nhân mắc ARDS nặng.
Mục tiêu chính của điều trị ARDS là đảm bảo trao đổi khí đầy đủ đồng thời giảm thiểu nguy cơ VILI. Cho đến nay, điều trị chủ yếu là hỗ trợ và thở máy vẫn là nền tảng. Một số bệnh nhân không thể duy trì oxy đầy đủ mặc dù được hỗ trợ bằng thở máy thông thường và tình trạng thiếu oxy kháng trị đe dọa tính mạng có thể xảy ra.
Bảng 1. Định nghĩa Berlin về ARDS
|
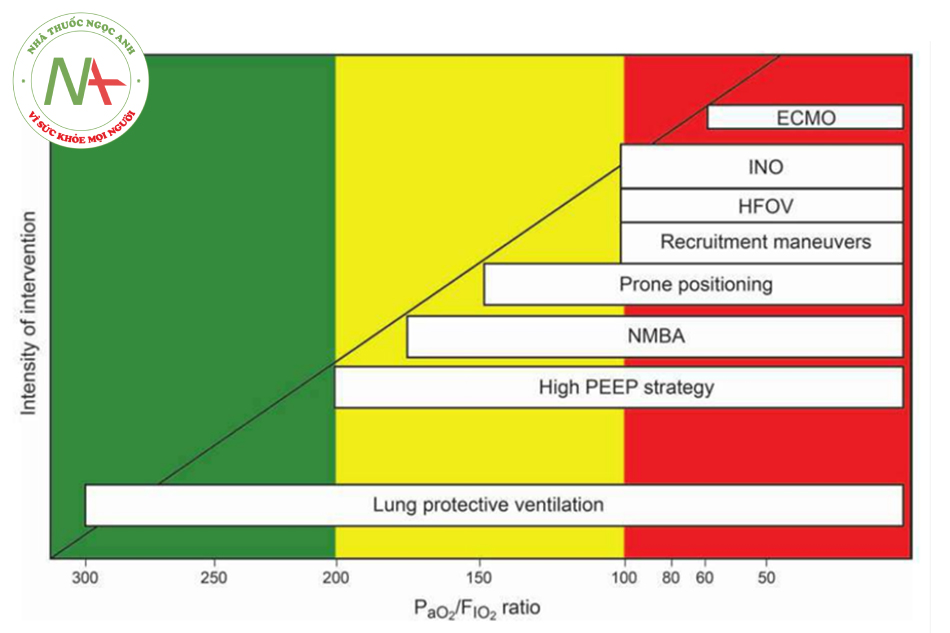
Mặc dù định nghĩa tiêu chuẩn cho tình trạng thiếu oxy kháng trị là một vấn đề đang được tranh luận, nhưng trong hầu hết các báo cáo, nó được định nghĩa là có PaO2 < 60 mm Hg, với FIO2 là 0,8– 1,0 và PEEP > 10–20 cm H2O trong > 12–24 giờ. Trong những trường hợp này, các bác sĩ có thể xem xét một số liệu pháp hỗ trợ, đây là nỗ lực cứu hộ cuối cùng để ngăn ngừa các biến chứng nghiêm trọng hoặc tử vong do thiếu oxy (Hình 1). Các liệu pháp cứu hộ chỉ là phương pháp tạm thời có thể hỗ trợ hoặc thay thế chức năng hô hấp ở những bệnh nhân suy hô hấp nặng kháng trị được hỗ trợ bằng máy thở thông thường. Mặc dù các chiến lược này cải thiện quá trình oxygen hóa, nhưng tác động của chúng đối với tỷ lệ tử vong vẫn chưa được chứng minh và chúng đòi hỏi chi phí cao hơn do nguy cơ gia tăng so với chăm sóc tiêu chuẩn. Việc tổ chức các liệu pháp này có thể được xem xét trên cơ sở cá nhân hóa và sự lựa chọn thường sẽ được quyết định bởi sự sẵn có và chuyên môn của địa phương.8,9
Thông khí và PEEP
Trong một nghiên cứu lớn do Mạng ARDS thực hiện,10 trường hợp tử vong đã giảm và số ngày không thở máy nhiều hơn ở nhóm được điều trị với thể tích khí lưu thông thấp hơn (VT 6 mL/kg trọng lượng cơ thể dự đoán) so với nhóm được điều trị bằng VT truyền thống. Giảm nồng độ interleukin-6 (IL-6) trong huyết tương, gợi ý rằng nhóm được điều trị bằng VT thấp hơn ít bị viêm phổi hơn. Giảm phản ứng viêm toàn thân đối với tổn thương phổi có thể góp phần làm tăng số ngày không bị suy cơ quan hoặc hệ thống và tỷ lệ tử vong thấp hơn ở nhóm được điều trị bằng thông khí bảo vệ phổi.10
So với thở máy thông thường, chiến lược bảo vệ có liên quan đến tỷ lệ cai thở máy cao hơn và tỷ lệ chấn thương khí áp thấp hơn ở bệnh nhân mắc ARDS, mặc dù sử dụng mức PEEP cao hơn và áp lực đường thở trung bình cao hơn.11 Nồng độ IL-8, IL6, TNF-α, IL-1β cao trong dịch rửa phế quản phế nang của bệnh nhân mắc ARDS xác nhận sự liên quan của các cytokine trong quá trình khuếch đại dòng phản ứng viêm dẫn đến suy đa cơ quan và tăng tỷ lệ tử vong. Ranieri và cộng sự12 so sánh thông khí bảo vệ phổi với chiến lược máy thở thông thường để đánh giá ảnh hưởng của thở máy đối với nồng độ cytokine trong phổi và toàn thân. Nồng độ của các chất trung gian gây viêm thấp hơn 36 giờ sau khi phân ngẫu nhiên ở nhóm thở máy bảo vệ phổi so với nhóm chiến lược thông thường. Chiến lược thông khí bảo vệ phổi này nhằm mục đích giảm thiểu VILI, có thể là kết quả của việc căng quá mức phế nang hoặc việc đóng mở lặp đi lặp lại các đơn vị phổi riêng lẻ.
Mặc dù trước đây, việc lựa chọn chế độ thở máy cụ thể (kiểm soát áp lực so với kiểm soát thể tích), được coi là phù hợp với kết quả của bệnh nhân, 2 phân tích tổng hợp gần đây không thể chỉ ra bất kỳ sự khác biệt đáng kể nào về tỷ lệ tử vong, nguy cơ chấn thương khí áp, hoặc các phản ứng sinh lý khác.13,14 Mặc dù đã sử dụng các chiến lược thông khí giới hạn áp lực và thể tích, tổn thương phổi vẫn có thể tồn tại hoặc tiến triển ở một số bệnh nhân, dẫn đến tình trạng thiếu oxy trầm trọng hơn.15 Mô phổi được sục khí hạn chế có sẵn để nhận thông khí theo chu kỳ, do đó dẫn đến siêu căng phồng khu vực và stress quá mức; không đủ PEEP dẫn đến chấn thương do cắt quá mức.
Các vùng phổi phụ thuộc của bệnh nhân mắc ARDS góp phần đáng kể vào sự phát triển của tình trạng thiếu oxy do các shunt trong các phế nang được tưới máu, không được thông khí. Các chiến lược mở mô phổi bị xẹp này có thể cải thiện quá trình oxygen hóa và giảm tỷ lệ tử vong. Điều này đặc biệt có thể là một vấn đề ở những bệnh nhân được thông khí với VT thấp, trong đó một phần đáng kể của phổi có thể vẫn bị xẹp do hạn chế về áp lực và thể tích. Terragni và cộng sự đã chụp cắt lớp vi tính phổi ở cuối kỳ thở ra và cuối thì hít vào cho 30 đối tượng được điều trị bằng thông khí bảo vệ phổi. Một phần ba số đối tượng trải qua siêu bơm phồng theo chu kỳ đáng kể với VT 6 mL/kg trọng lượng cơ thể dự đoán và áp lực bình nguyên (Pplat) < 30 cm H2O. Ở những đối tượng này, nồng độ của các chất trung gian gây viêm cao hơn và số ngày không thở máy thấp hơn so với 2/3 đối tượng ít bị siêu bơm phồng theo chu kỳ thở. Pplat < 28 cm H2O có liên quan đến siêu bơm phồng theo chu kỳ thở ít hơn so với giá trị Pplat 28–30 cm H2O. Pplat < 28 cm H2O dường như được liên kết với các cài đặt thông khí bảo vệ hơn. Cài đặt Mạng ARDS có thể không đủ để giảm thiểu VILI ở những bệnh nhân mắc ARDS có quá trình bệnh được đặc trưng bởi sự phân bố các tổn thương phổi với một ngăn nhỏ, không phụ thuộc, được thông khí bình thường và một ngăn lớn, phụ thuộc, không được sục khí. Tỷ lệ phổi không được thông khí có thể được huy động bằng cách áp dụng mức PEEP cao hơn so với mức sử dụng truyền thống (5–12 cm H2O) trong quản lý bệnh nhân mắc ARDS.17,18 Amato và cộng sự19 cho rằng strain theo chu kỳ dự đoán tổn thương phổi tốt hơn VT. Kích thước phổi chức năng trong thời gian mắc bệnh được định lượng tốt hơn bằng độ giãn nở của hệ hô hấp so với trọng lượng cơ thể dự đoán. Trong những điều kiện như vậy, đặc biệt là khi độ giãn nở của hệ hô hấp thay đổi đáng kể giữa các bệnh nhân, strain theo chu kỳ, VILI và tỷ lệ sống sót đều phải tương quan với áp lực đẩy hơn là với VT.
Mặc dù một số nghiên cứu thực nghiệm và quan sát đã tìm thấy tác dụng có lợi của việc sử dụng PEEP cao hơn trong ARDS, 3 thử nghiệm ngẫu nhiên, được công bố từ năm 2004 đến 2008, không cho thấy bất kỳ sự khác biệt nào về kết quả giữa chiến lược máy thở PEEP thấp và cao.20–22 Tuy nhiên, khi kết hợp những dữ liệu này và chỉ xem xét phân nhóm đối tượng nghiêm trọng nhất (PaO2/FIO2 < 200 mm Hg), việc sử dụng mức PEEP cao hơn đã làm giảm đáng kể tỷ lệ tử vong.23 Điều này cho thấy rằng mức độ nghiêm trọng càng lớn (và mức độ phù phổi càng lớn) thì tác dụng tích cực của PEEP trong việc giảm VILI càng lớn. Điều này cũng đã được xác nhận trong một nghiên cứu quan sát, trong đó mức PEEP cao hơn làm giảm đáng kể hiệu ứng mở và đóng chỉ ở những đối tượng có khả năng huy động cao hơn.24 Tuy nhiên, mối quan hệ giữa phù phổi và khả năng huy động đã được đặt câu hỏi bởi Cressoni và cộng sự,25 người đã phát hiện ra rằng mức PEEP cần thiết để giữ cho phổi mở độc lập với khả năng huy động toàn bộ phổi. Những kết quả này cho thấy khả năng huy động cũng phụ thuộc vào bản chất của phù nề, thời gian khởi phát và sự phân bố của bệnh trong nhu mô phổi.
Mặc dù một số phương pháp đã được đề xuất để điều chỉnh PEEP cho từng bệnh nhân, nhưng phổ biến nhất là chuẩn độ PEEP theo mục tiêu oxygen hóa/độ bão hòa dựa trên bảng PEEP/FIO2.21 Năm 1975, Suter và cộng sự16 đặt ra thuật ngữ PEEP tốt nhất là điểm mà tại đó mức độ huy động phổi được cân bằng với nguy cơ căng quá mức đồng thời. Cơ sở để xác định PEEP tốt nhất là định lượng huy động: tăng PEEP bằng cách duy trì VT không đổi, không vượt quá giới hạn an toàn của Pplat 26–28 cm H2O, hoặc sau khi thực hiện thao tác huy động, giảm PEEP cho đến khi giảm độ giãn nở xuất hiện.27 Trong một mẫu tổng hợp gồm 3.562 đối tượng mắc ARDS được thông khí với các kết hợp VT và PEEP khác nhau, tác dụng bảo vệ của PEEP cao hơn chỉ được thấy khi điều này có liên quan đến việc giảm áp lực đẩy, với ngưỡng giảm tỷ lệ tử vong tăng ở áp lực đẩy 15 cm H2O.19 Quan trọng nhất đối với cuộc thảo luận này là thực tế là mối quan hệ giữa tỷ lệ tử vong và mức P cao chỉ được quan sát thấy khi áp lực đẩy cũng trên 15 cm H2O. Áp lực đẩy đường thở là yếu tố liên quan nhiều nhất đến kết quả: tỷ lệ tử vong cao hơn chỉ được tìm thấy khi giá trị P cao hơn được quan sát thấy ở những đối tượng có áp lực đẩy cao hơn.
Nhiều kỹ thuật đã được đề xuất để theo dõi huy động phổi, chẳng hạn như siêu âm, chụp cắt lớp trở kháng điện, đo cơ học hô hấp, kỹ thuật rửa trôi nitơ và chụp cắt lớp vi tính định lượng, nhưng chưa có kỹ thuật nào đạt được sự đồng thuận chung hoặc được sử dụng thường xuyên trong môi trường lâm sàng.28–32
Bất chấp những điều không chắc chắn có thể xảy ra liên quan đến áp lực thực quản tuyệt đối cuối thì thở ra như một ước tính đáng tin cậy về áp lực màng phổi, khả năng cung cấp oxy và độ giãn nở tốt hơn đã đạt được khi PEEP được đặt theo áp lực xuyên phổi cuối thì thở ra là 0–10 cm H2O.33 Thay thế cho việc sử dụng giá trị tuyệt đối của áp lực thực quản là theo dõi xem nó thay đổi như thế nào do điều chỉnh PEEP và VT. Điều này đã được sử dụng để tính toán tổng áp lực xuyên phổi cuối thì hít vào và nó là một dấu hiệu tốt hơn cho stress phổi so với Pplat khi có sự thay đổi về độ đàn hồi của thành ngực. Đặt mức PEEP cao (>15–18 cm H2O) phải đi kèm với đánh giá huyết động kỹ lưỡng và có thể được chứng minh thêm bằng cách đo áp lực xuyên phổi và đánh giá khoảng chết sinh lý bằng capnography thể tích.34,35
=> Tham khảo thêm: Dị vật đường thở: Biểu hiện lâm sàng, Chẩn đoán và Điều trị.
Thủ thuật huy động
Các thủ thuật huy động được sử dụng như một chiến lược để cải thiện quá trình oxygen hóa và giảm nguy cơ chấn thương do xẹp phổi ở bệnh nhân mắc ARDS bằng cách mở lại và ổn định các vùng phổi bị xẹp.18 Một số thao tác huy động đã được đề xuất, bao gồm bơm phồng duy trì (sustained inflations) với giá trị CPAP là 35–50 cm H2O trong 20–40 giây, áp lực hít vào tăng dần, VT thấp hơn (kèm theo nhịp thở sâu), thở ra ngắt quãng, tăng dần PEEP và tăng chậm áp lực hít vào lên 40 cm H2O.36 Các thủ thuật huy động cố gắng tăng lượng mô phổi được sục khí để cải thiện quá trình trao đổi khí. Tuy nhiên, những điều này có thể khiến các vùng mô phổi khỏe mạnh bị tăng áp lực và nguy cơ căng quá mức.
Một số nghiên cứu đã cho thấy sự trao đổi khí được cải thiện với các thao tác huy động, nhưng điều này không chuyển thành tỷ lệ tử vong được cải thiện. Lợi ích từ các thao tác huy động có xu hướng tồn tại trong thời gian ngắn và tăng áp lực đường thở dẫn đến các tác dụng phụ thoáng qua (ví dụ: hạ huyết áp, thiếu oxy) ở một số ít bệnh nhân. Ví dụ, trong một tổng quan hệ thống gần đây, hạ huyết áp và giảm bão hòa xảy ra ở 12% và 8% đối tượng, tương ứng, trong hoặc sau các thao tác như vậy.18,36 Tuy nhiên, các tác dụng phụ dai dẳng và nghiêm trọng liên quan đến thủ thuật huy động, chẳng hạn như sự phát triển của tràn khí màng phổi, vẫn còn hiếm.37 Hơn nữa, các nghiên cứu cho đến nay vẫn chưa làm sáng tỏ kỹ thuật, thời gian và tần suất tối ưu của các thao tác huy động. Trên cơ sở dữ liệu hiện có, mặc dù các thủ thuật huy động thông thường không được khuyến nghị để điều trị ARDS, nhưng các thủ thuật như vậy có thể cải thiện đáng kể quá trình oxygen hóa ở một số bệnh nhân và nên được coi là liệu pháp cứu hộ ở những bệnh nhân bị thiếu oxy kháng trị đe dọa tính mạng.38
Steroid
Steroid có tác dụng điều hòa miễn dịch tích cực đối với sự mất cân bằng viêm, giảm phù nề, hình thành màng hyaline, suy giảm chất hoạt động bề mặt và tổn thương màng mao mạch phế nang.39 Liệu pháp liều cao và thời gian ngắn (methylprednisolone 30 mg/kg/ngày) đã chứng minh không cải thiện tỷ lệ tử vong và tăng nguy cơ nhiễm trùng.40 Một phân tích tổng hợp gần đây điều tra liều thấp hơn, được thực hiện sớm hơn và trong thời gian dài hơn, dường như đã chứng minh sự cải thiện chức năng phổi và giảm tỷ lệ tử vong.41 Tuy nhiên, còn thiếu bằng chứng thuyết phục về việc sử dụng steroid. Corticosteroid không được khuyến cáo là liệu pháp cứu hộ ở bệnh nhân ARDS, vì những cải thiện đã được quan sát thấy là bị trì hoãn và không nhất quán.42
Quản lý dịch
ARDS là phù phổi viêm giàu protein vào khoảng kẽ, thường kết hợp với thành phần thủy tĩnh. Sự gia tăng trọng lượng phổi tạo ra hiện tượng xẹp phổi do nén và làm suy yếu cơ chế phổi và trao đổi khí. Tăng áp phổi có thể dễ dàng kết hợp với tăng áp lực mao mạch phổi và suy tim. Trong khi các cơ chế phổ biến gây ra phù nề là phẫu thuật và tràn dịch màng phổi, dòng bạch huyết và sự tái hấp thu mao mạch vào phía tĩnh mạch của mạng lưới mao mạch phổi bị suy yếu do áp lực dương trong lồng ngực liên quan đến thở máy.43 Truyền dịch quá mức dẫn đến tăng lượng nước trong phổi ngoài mạch máu, đây là một dấu hiệu tiên lượng xấu trong ARDS. Quản lý dịch tối ưu cung cấp phổi khô trong khi duy trì tưới máu cơ quan.
Thử nghiệm Mạng ARDS44 được thiết kế để điều tra các nguy cơ và lợi ích của giao thức quản lý dịch. Các đối tượng mắc ARDS được chọn ngẫu nhiên vào các nhóm bảo thủ hoặc tự do. Nhóm bảo thủ cho thấy chức năng phổi được cải thiện so với nhóm tự do, với số ngày thở máy và số ngày ICU ít hơn mà không làm gia tăng suy cơ quan ngoài phổi. Tỷ lệ tử vong trong 60 ngày không giảm đáng kể. Trong 7 ngày đầu tiên, nhóm tự do có cân bằng dịch tăng khoảng 1 L/ngày, trong khi những người ở nhóm bảo thủ cân bằng dịch vẫn ở mức trung tính.
Trong phân nhóm bệnh nhân giảm protein máu, có thể có vai trò làm giảm phù nề nhanh khi tính thấm mao mạch phổi và ổn định huyết động được phục hồi, vì bệnh nhân giảm protein máu có thể được điều trị an toàn bằng phối hợp albumin và furosemide. Có thể đạt được lợi tiểu, giảm cân và bình thường hóa nồng độ protein huyết thanh, và trong 24–48 giờ đầu điều trị, PaO2/FIO2 tăng > 60 mm Hg.45 Một nghiên cứu tiếp theo của cùng một nhóm cũng báo cáo rằng PaO2/FIO2 tăng > 40 mm Hg trong 24–72 giờ so với mức giảm 13–24 mm Hg ở nhóm dùng giả dược.46 Chúng đại diện cho những cải tiến đáng kể trong quá trình oxygen hóa.
Thuốc chẹn thần kinh cơ
Thở tự nhiên dường như nguy hiểm ở những bệnh nhân mắc ARDS nặng, trong khi nó có vẻ có lợi ở những bệnh nhân mắc ARDS nhẹ đến trung bình. Các chất ức chế thần kinh cơ (NMBA) nên được dành riêng cho những trường hợp nghiêm trọng nhất để đảm bảo đồng bộ bệnh nhân-máy thở và ngăn ngừa việc tạo ra áp lực xuyên phổi và VILI cao nguy hiểm.47
Điều trị bằng truyền cisatracurium liên tục trong 48 giờ sớm trong quá trình ARDS nặng làm giảm tỷ lệ tử vong 90 ngày và chấn thương áp lực. Nó cũng làm tăng số ngày không dùng máy thở và số ngày nằm ngoài ICU. Trong bối cảnh này, nguy cơ suy nhược cơ do ICU mắc phải không tăng lên.48 Sử dụng sớm NMBAs làm giảm phản ứng tiền viêm liên quan đến ARDS và thở máy. Cơ chế chính xác dẫn đến kết quả được cải thiện là không rõ ràng. Sự đồng bộ tốt hơn có thể dẫn đến việc huy động phổi đồng đều hơn và cải thiện độ giãn nở, trao đổi khí và oxygen hóa hệ thống. Đối với tình trạng viêm phổi, điều hợp lý là việc cải thiện kiểm soát thể tích và áp lực hít vào sẽ làm giảm chấn thương thể tích, trong khi kiểm soát tốt hơn thể tích và áp lực thở ra sẽ làm giảm chấn thương do xẹp phổi; kết quả là ít viêm phổi và hệ thống hơn.49 Những lợi ích tiềm năng này phải được cân nhắc với những lo ngại phổ biến về liệu pháp NMBA, bao gồm xẹp phổi tiến triển do mất trương lực cơ hoành (dẫn đến thiếu oxy máu) và quan trọng nhất là suy nhược do ICU mắc phải.50
Thông khí dao động tần số cao
Thông khí dao động tần số cao (HFOV, Highfrequency oscillatory ventilation) là một chế độ không thông thường đã được đề xuất để đạt được các mục tiêu thông khí bảo vệ với VT rất thấp (bằng hoặc nhỏ hơn khoảng chết giải phẫu) ở tốc độ rất cao (3–6 Hz); dao động lưu lượng hình sin được áp dụng xung quanh áp lực đường thở trung bình tương đối ổn định (P̄aw). Chiến lược này tránh sự căng phồng quá mức của phế nang bằng cách cung cấp VT thấp (1–3 mL/kg), ngăn ngừa chấn thương thể tích, ngăn ngừa xẹp phế nang cuối thì thở ra và duy trì huy động phế nang bằng cách áp dụng P̄aw không đổi để tạo điều kiện huy động phổi.51
HFOV về mặt lý thuyết đạt được tất cả các mục tiêu mà các chiến lược thông khí bảo vệ phổi theo đuổi; tuy nhiên, 2 thử nghiệm lâm sàng ngẫu nhiên lớn đã không chứng minh được bất kỳ lợi ích lâm sàng nào khi HFOV được áp dụng ở người lớn mắc ARDS từ trung bình đến nặng so với chiến lược có VT thấp, PEEP cao và Pplat hạn chế. Young và cộng sự52 không cho thấy bất kỳ sự khác biệt nào về tỷ lệ tử vong với HFOV so với thở máy thông thường, trong khi Ferguson và cộng sự53 báo cáo sự gia tăng tỷ lệ tử vong với HFOV. Paw̄ cao gợi ý rằng đã xảy ra tình trạng căng quá mức của một số vùng phổi mà không tăng thông khí cho các phế nang bị xẹp hoặc ngập nước, đặc biệt là ở những đối tượng có phổi không đồng nhất và không thể huy động được. Tỷ lệ tử vong gia tăng cũng có thể là do ảnh hưởng đến huyết động do tăng nhu cầu sử dụng thuốc vận mạch và do suy thất phải thứ phát do hậu gánh tăng đáng kể. HFOV không nên được sử dụng thường xuyên thay cho thông khí bảo vệ phổi thông thường và nó nên được dành riêng như một liệu pháp cứu hộ cho những bệnh nhân bị thiếu oxy kháng trị và trong một số trường hợp ARDS nặng được chọn.54
Việc đánh giá áp lực xuyên phổi bằng cách đo áp lực thực quản có thể là một chiến lược hợp lệ để áp dụng Paw̄ sinh lý hơn, giảm nguy cơ tổn thương phổi thêm và dẫn đến huy động phổi tối đa và giảm thiểu căng thẳng quá mức.55 Nghiên cứu EPOCH (ClinicalTrials.gov NCT02342756) đang sử dụng phương pháp này để điều chỉnh PEEP trong quá trình thở máy thông thường và Paw̄ trong HFOV.56
=>Xem thêm: Liệu pháp oxy lưu lượng cao qua mũi (HFNC) trong cai thở máy.
Thuốc giãn mạch phổi chọn lọc
Thuốc giãn mạch phổi chọn lọc thường được sử dụng cho vai trò điều trị của chúng trong việc cải thiện quá trình oxygen hóa ở những bệnh nhân bị thiếu oxy kháng trị trong ARDS.57 Các thuốc này khu trú thuốc đến nhu mô phổi có khả năng thông khí, cải thiện tình trạng mất tương xứng thông khítưới máu. Thuốc giãn mạch phổi chọn lọc thường được sử dụng bao gồm oxit nitric dạng hít (INO) và epoprostenol dạng hít, một loại prostacyclin.
INO là thuốc giãn mạch cục bộ của các mao mạch trong phế nang được thông khí tốt, và nó cải thiện sự phù hợp thông khí-tưới máu ở bệnh nhân mắc ARDS và giảm sức cản mạch máu phổi, giúp cải thiện cung lượng thất phải.58 Việc sử dụng INO thường quy trong ARDS không được khuyến nghị dựa trên bằng chứng hiện tại, nhưng nó thường được sử dụng ở nhiều cơ sở. Việc sử dụng INO ở những đối tượng mắc ARDS cho thấy tỷ lệ tử vong không giảm đáng kể.59 Việc sử dụng INO có thể được cân nhắc khi bệnh nhân có nguy cơ tử vong cao do thiếu oxy máu mặc dù đã áp dụng tất cả các phương pháp điều trị khác. INO không cho thấy tác dụng có lợi đáng kể đối với thời gian thở máy và thời gian nằm trong ICU so với nhóm đối chứng.59 Mặc dù INO cải thiện quá trình oxygen hóa trong 24 giờ đầu tiên bằng cách giảm sự không phù hợp giữa thông khí và tưới máu, nhưng theo thời gian, nó sẽ gây giãn mạch ở những vùng được thông khí kém, làm tăng sự mất tương xứng giữa thông khí và tưới máu.60
Cải thiện oxygen hóa không liên quan đến việc tăng tỷ lệ sống sót vì sự cải thiện tạm thời oxygen hóa không cho thấy chức năng phổi được cải thiện, giảm tổn thương phổi hoặc giải quyết nguyên nhân cơ bản của ARDS, bao gồm cả tổn thương đa cơ quan cùng tồn tại.61 Với việc sử dụng INO, sự chênh lệch áp lực động mạch phổi ban đầu đáng kể vào ngày đầu tiên nhưng không còn xuất hiện vào ngày thứ 2–4.61 Oxit nitric là chất điều hòa quan trọng trương lực mạch máu thận và là chất điều hòa chức năng cầu thận. Khi INO lần đầu tiên được giới thiệu, sự hình thành metaemogloblin, sản xuất các loại nitơ phản ứng, hạ huyết áp và ức chế tiểu cầu là những tác động phụ chính, trong khi độc tính trên thận không phải là mối quan tâm chính.62,63 Các nghiên cứu khác nhau đã chứng minh rằng INO làm tăng nguy cơ tổn thương thận ở những người trưởng thành mắc ARDS và có khả năng tăng gấp đôi nguy cơ điều trị thay thế thận.64 Do đó, những thay đổi trong sản xuất oxit nitric có thể gây tổn thương thận cấp tính bằng cách thay đổi chức năng của ty thể, các enzym khác nhau và axit deoxyribonucleic. Mặc dù không đủ các thử nghiệm ngẫu nhiên có kiểm soát hoặc phân tích tổng hợp, các liệu pháp kết hợp với tư thế nằm sấp hoặc HFOV có thể giúp ích cho các nhóm bệnh nhân được chọn hoặc như một liệu pháp cứu hộ vì chúng có thể tăng cường hiệu quả của INO tốt hơn so với đơn trị liệu.65
Epoprostenol dạng hít đã được đề xuất như một giải pháp thay thế cho INO do hiệu quả tương tự, khả năng tác dụng phụ toàn thân thấp hơn, dễ sử dụng và chi phí thấp hơn đáng kể. Epoprostenol dạng hít đã được chứng minh là làm giảm đáng kể áp lực động mạch phổi và tăng oxygen hóa. Tuy nhiên, việc sử dụng prostacyclin là một thách thức về mặt kỹ thuật do thời gian bán hủy ngắn và tính nhạy cảm với sự thoái hóa của nó.66 Kể từ lần đầu tiên nó được công bố để điều trị ARDS vào năm 1993, còn thiếu dữ liệu về hiệu quả.57,67 Tài liệu đánh giá việc sử dụng nó còn thiếu và không có nghiên cứu nào đánh giá tỷ lệ tử vong là tiêu chí chính. Mặc dù thường được sử dụng như một liệu pháp cuối cùng, nhưng khoảng trống trong tài liệu đã dẫn đến tranh cãi xung quanh epoprostenol dạng hít liên quan đến liều lượng và độ an toàn tối ưu, cũng như nhóm bệnh nhân mục tiêu.68,69 Iloprost, một thuốc giãn mạch phổi chọn lọc khác thường được sử dụng để điều trị tăng áp phổi, có lợi ích về mặt lý thuyết ở những bệnh nhân mắc ARDS, nhưng có rất ít bằng chứng ủng hộ việc sử dụng nó cho chỉ định này.70
Nằm sấp
Tư thế nằm sấp lần đầu tiên được mô tả cách đây 40 năm như một chiến lược thay thế để cải thiện quá trình oxygen hóa ở bệnh nhân mắc ARDS.71 Một số cơ chế đã được đề xuất để giải thích hiệu ứng này, bao gồm sự phân bố lại mật độ phổi với việc huy động các vùng lưng, tăng độ đàn hồi của thành ngực, giảm shunt phế nang và tỷ lệ thông khí/tưới máu tốt hơn. Sự phân bố thuận lợi hơn của căng thẳng và sức căng trên một lãnh thổ rộng hơn và đồng nhất hơn (do thành ngực/hình dạng phổi phù hợp với thông khí) làm giảm VILI và đảo ngược suy tim phải. Do huy động phổi, sự đảo ngược tình trạng thiếu oxy và giảm áp lực đẩy là những lời giải thích hợp lý nhất cho việc giảm sức cản mạch máu phổi và kích thước tim phải trong tư thế nằm sấp.72 Sự thay đổi lực hấp dẫn làm giảm xẹp phổi và giảm thiểu chèn ép nhu mô phổi bởi tim và các cấu trúc trung thất, dẫn đến cải thiện kết hợp thông khí-tưới máu.73
Các thử nghiệm ngẫu nhiên trước đó cho thấy lợi ích tử vong không nhất quán của tư thế nằm sấp; tuy nhiên, những nghiên cứu này bao gồm tất cả các đối tượng mắc ARDS (từ nhẹ đến nặng), duy trì tư thế nằm sấp trong 6 giờ/ngày và không áp dụng thở máy bảo vệ.74,75 Bất chấp những hạn chế này, tỷ lệ sống sót tăng lên ở những đối tượng mắc ARDS nặng nhất được điều trị ở tư thế nằm sấp.74 Sau đó, 2 thử nghiệm thu nhận nhiều đối tượng thiếu oxy trầm trọng hơn với thời gian nằm sấp dài hơn (20 giờ/ngày), không cho thấy bất kỳ tác dụng có lợi nào.76,77 Tuy nhiên, phân tích tổng hợp các nghiên cứu trước đây cho thấy lợi ích sống sót đáng kể đối với các đối tượng mắc bệnh PaO2/FIO2 < 140 mm Hg lúc nhập viện.78 Thử nghiệm PROSEVA79 là một thử nghiệm ngẫu nhiên có đối chứng đa trung tâm về áp dụng sớm tư thế nằm sấp kéo dài (≥ 16 giờ/ngày) ở những đối tượng mắc ARDS nặng. Trong thử nghiệm này, mức độ nghiêm trọng của ARDS được xác định là PaO2/FIO2 ≤ 150 với PEEP ≥ 5 cm H2O, FIO2 ≥ 0,6, với VT trung bình là 6,1 mL/kg trọng lượng cơ thể dự đoán. Thử nghiệm PROSEVA cho thấy tỷ lệ tử vong giảm đáng kể ở 28 ngày và 90 ngày ở những đối tượng được điều trị bằng tư thế nằm sấp. Bắt đầu điều trị nằm sấp sớm dường như là một yếu tố quan trọng để thành công. Quá trình di chuyển bệnh nhân sang tư thế nằm sấp có thể tốn nhiều công sức và làm tăng nguy cơ vô tình rút ống nội khí quản, ống dẫn lưu hoặc ống thông, cũng như sự phát triển của các vết loét do tỳ đè.72 Mặc dù tư thế nằm sấp có một số thách thức về kỹ thuật, nhưng khi được thực hiện bởi một đội ngũ lành nghề, các tác động bất lợi tương đối thấp và chúng được khắc phục đáng kể bằng các tác động có lợi.
Các chống chỉ định của tư thế nằm sấp phải được xem xét, chẳng hạn như tăng áp lực nội sọ hoặc giảm tưới máu não, cần phẫu thuật hoặc thủ thuật can thiệp ngay lập tức, phẫu thuật lồng ngực gần đây, chấn thương hoặc phẫu thuật vùng mặt gần đây, huyết động không ổn định, mang thai hoặc hội chứng khoang bụng và gãy xương không vững của xương. cột sống, xương chậu hoặc xương đùi.80
Oxygen hóa màng ngoài cơ thể
Trong tình trạng thiếu oxy nghiêm trọng kháng với điều trị thông thường, bao gồm thông khí thể tích thấp, áp lực thấp, tư thế nằm sấp, INO và HFOV, oxygen hóa qua màng ngoài cơ thể (ECMO) có thể được sử dụng như một liệu pháp cứu hộ bằng cách đảm bảo oxygen hóa cũng như loại bỏ carbon dioxide trong khi phổi đang nghỉ ngơi với áp lực máy thở thấp và nồng độ oxy thấp.9
Hỗ trợ ECMO thường được thực hiện thông qua tiếp cận tĩnh mạch, trong đó máu được dẫn lưu qua tĩnh mạch chủ trên hoặc tĩnh mạch chủ dưới và được đưa lại vào tâm nhĩ phải. ECMO được chỉ định khi PaO2/FIO2 < 80, khi FIO2 > 90% và khi điểm tổn thương phổi là 3–4; trong trường hợp này, nguy cơ tử vong vượt quá 80%.81 Theo định nghĩa ARDS của Berlin, ECMO được đề xuất như một liệu pháp cứu hộ cho tình trạng thiếu oxy máu nghiêm trọng khi PaO2/FIO2 < 50. ECMO được xem xét khi Pplat vượt quá 32 cm H2O, FIO2 = 100%, SpO2 < 90% hoặc pH < 7,2.82
Thật vậy, một khi bệnh nhân sử dụng ECMO, máu có thể được cung cấp oxy tốt với PaCO2 bình thường và pH trung tính; đạt được mục tiêu thông khí bảo vệ phổi và giảm thiểu VILI.83 Ở những bệnh nhân ARDS đặc biệt nặng trải qua ECMO, VT giảm đáng kể gần một nửa, dẫn đến giảm đáng kể Pplat và mất huy động vì PEEP vẫn ổn định.84 Có thể mất nhiều thời gian để một số bệnh nhân mở lại phổi và có thể khó cân bằng giữa nguy cơ tổn thương do phổi quá căng và nguy cơ phổi huy động dưới mức.84
Trong vài thập kỷ qua, hầu hết các thử nghiệm đánh giá ECMO đều không có lợi ích do một số yếu tố, bao gồm khoảng thời gian kéo dài giữa thời gian khởi phát ARDS và bắt đầu hỗ trợ, khả năng loại bỏ oxy và CO2 kém của các thiết bị được sử dụng và tỷ lệ biến chứng kỹ thuật cao như chảy máu đáng kể do chống đông máu mạnh cần thiết để khắc phục khả năng tương thích sinh học kém của các bộ dây.85 Tuy nhiên, gần đây, đã có những tiến bộ đáng kể trong việc sản xuất các bộ dây ECMO tương thích sinh học hơn, hoạt động ở mức cao hơn và bền hơn.
Thử nghiệm về Thông khí thông thường hoặc ECMO cho Suy hô hấp nặng ở người trưởng thành (CESAR)86 có trụ sở tại Vương quốc Anh và kết quả tốt của các đối tượng sử dụng ECMO thế hệ mới nhất như một liệu pháp cứu hộ trong đại dịch cúm A (H1N1) đã khơi dậy sự quan tâm đến ECMO cho bệnh nhân ARDS nặng. Thử nghiệm CESAR ở các đối tượng người lớn mắc ARDS đã chứng minh tỷ lệ sống sót sau 6 tháng tăng từ 50% lên 63% ở nhóm ECMO, nhưng sự khác biệt so với nhóm đối chứng là không đáng kể. Khi kết hợp tỷ lệ tử vong và điểm kết thúc thương tật trong 6 tháng, sự khác biệt trở nên có ý nghĩa có lợi cho nhóm ECMO.86 Tuy nhiên, không thể kết luận ECMO ưu việt hơn thở máy, vì tất cả các đối tượng cần ECMO chỉ được phân bổ tại một trung tâm lành nghề và nhóm đối chứng không được thở máy theo chiến lược bảo vệ phổi.87,88
Tuy nhiên, điều trị bằng ECMO có một vị trí trong thực hành lâm sàng, như được chỉ ra trong Báo cáo Đăng ký Quốc tế của Tổ chức Hỗ trợ Sự sống Ngoài cơ thể, trong đó số lượng các phương pháp điều trị bằng ECMO dành cho người lớn đang tăng lên.89 Thử nghiệm ECMO để Cứu hộ tổn thương phổi trong ARDS nặng hiện đang diễn ra là một thử nghiệm quốc tế, đa trung tâm, ngẫu nhiên có kiểm soát so sánh thở máy thông thường với tư thế nằm sấp với ECMO ở những đối tượng mắc ARDS rất nặng (nghĩa là PaO2/FIO2 < 80 mmHg).90 Bắt đầu sớm chiến lược ECMO có thể làm giảm tỷ lệ tử vong từ 45–50% xuống <20%, với khả năng suy giảm nhận thức và tâm thần ít hơn và cải thiện chất lượng cuộc sống liên quan đến sức khỏe ở những người sống sót lâu dài.91 Những lợi ích có thể có của hỗ trợ ngoài cơ thể phải được cân bằng với các biến chứng nguy hiểm như chảy máu, huyết khối, nhiễm trùng và thiếu máu cục bộ ở chi xa.83 Không có chống chỉ định tuyệt đối cho ECMO; tất cả các trường hợp phải được thảo luận, và các chỉ định và giới hạn có thể sẽ thay đổi khi các nghiên cứu trong tương lai được thực hiện.
Tóm tắt
ARDS là một hội chứng gây ra bởi các bệnh khác nhau và dẫn đến tình trạng thiếu oxy kháng trị đe dọa tính mạng. Sự leo thang liên tục của các liệu pháp có thể được xem xét trên cơ sở cá nhân hóa. Mặc dù đã có nhiều thập kỷ điều tra về các chiến lược điều trị tiềm năng, nhưng việc sử dụng thông khí bảo vệ phổi với VT là 6 mL/kg trọng lượng cơ thể dự đoán và Pplat < 30 cm H2O vẫn là liệu pháp duy nhất được chứng minh để giảm tỷ lệ tử vong trong ARDS. Mục tiêu oxygen hóa/độ bão hòa dựa trên bảng PEEP/FIO2 là cách tiếp cận phổ biến để thiết lập PEEP, nhưng mối quan hệ giữa tỷ lệ tử vong và mức P cao chỉ được quan sát thấy khi áp lực đẩy cũng trên 15 cm H2O. Ở những bệnh nhân mắc ARDS, các thủ thuật huy động giúp cải thiện quá trình oxygen hóa, nhưng đây là phương pháp tạm thời không cải thiện tỷ lệ tử vong. Bằng chứng ủng hộ việc sử dụng steroid còn thiếu và cân bằng dịch thận trọng không vượt trội so với cân bằng tự do. NMBAs đảm bảo huy động phổi đồng đều, ngăn chặn việc tạo ra áp lực xuyên phổi cao nguy hiểm và giảm phản ứng tiền viêm liên quan đến ARDS, nhưng phương pháp này phải được cung cấp trong vòng 48 giờ đầu tiên để ngăn ngừa teo cơ hoành và suy nhược do ICU mắc phải. HFOV về mặt lý thuyết đạt được tất cả các mục tiêu của chiến lược thông khí bảo vệ phổi, tuy nhiên, các thử nghiệm lâm sàng ngẫu nhiên không chứng minh được bất kỳ lợi ích lâm sàng nào. INO tạm thời cải thiện quá trình oxygen hóa, nhưng nó không liên quan đến việc tăng tỷ lệ sống sót và không cho thấy bất kỳ lợi ích nào đối với chức năng phổi. Tư thế nằm sấp ở những bệnh nhân mắc ARDS nặng thúc đẩy sự thay đổi lực hấp dẫn, giảm thiểu chèn ép nhu mô phổi bởi tim và các cấu trúc trung thất, đồng thời cải thiện sự phù hợp giữa thông khí và tưới máu. ECMO đang được sử dụng ngày càng nhiều để hỗ trợ những người lớn bị bệnh nặng đã thất bại trong việc quản lý thông thường và nó có thể là một phương pháp điều trị cứu hộ hiệu quả cho những bệnh nhân mắc ARDS có biểu hiện suy hô hấp kháng trị nhanh chóng; tuy nhiên, các thử nghiệm có kiểm soát là cần thiết để xác định rõ hơn các chỉ định và thực hành tốt nhất cho liệu pháp này. và nó có thể là một phương pháp điều trị cứu hộ hiệu quả cho những bệnh nhân mắc ARDS bị suy hô hấp kháng trị nhanh chóng; tuy nhiên, các thử nghiệm có kiểm soát là cần thiết để xác định rõ hơn các chỉ định và thực hành tốt nhất cho liệu pháp này. và nó có thể là một phương pháp điều trị cứu hộ hiệu quả cho những bệnh nhân mắc ARDS bị suy hô hấp kháng trị nhanh chóng; tuy nhiên, các thử nghiệm có kiểm soát là cần thiết để xác định rõ hơn các chỉ định và thực hành tốt nhất cho liệu pháp này.