Bệnh tiêu hóa
Truyền dịch bằng máy hạ thân nhiệt trong cấy ghép gan
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
Tóm tắt
ĐẶT VẤN ĐỀ
Việc cấy ghép gan lấy được từ người hiến tặng sau khi chết tuần hoàn có liên quan đến việc tăng nguy cơ tắc mật không nối. Việc tưới máu bằng máy oxy già hạ thân nhiệt có thể làm giảm tỷ lệ các biến chứng về mật, nhưng dữ liệu từ các nghiên cứu có kiểm soát, tiền cứu còn hạn chế.
PHƯƠNG PHÁP
Trong thử nghiệm đa trung tâm, có đối chứng này, chúng tôi chỉ định ngẫu nhiên những bệnh nhân đang được cấy ghép gan lấy từ người hiến tặng sau khi chết tuần hoàn để nhận gan đó sau khi truyền dịch bằng máy oxy giảm nhiệt (nhóm truyền dịch bằng máy) hoặc sau khi bảo quản lạnh tĩnh thông thường một mình (đối chứng tập đoàn). Điểm kết thúc chính là tỷ lệ tắc nghẽn đường mật không nối trong vòng 6 tháng sau khi cấy ghép. Các điểm cuối phụ bao gồm các biến chứng chung và liên quan đến mảnh ghép khác.
KẾT QUẢ
Tổng cộng 160 bệnh nhân đã được ghi danh, trong đó 78 bệnh nhân nhận gan tưới máu bằng máy và 78 bệnh nhân chỉ nhận gan sau khi bảo quản lạnh tĩnh (4 bệnh nhân không nhận gan trong thử nghiệm này). Chặt chặt đường mật không nối mật xảy ra ở 6% bệnh nhân trong nhóm truyền dịch bằng máy và 18% ở nhóm chứng (tỷ lệ rủi ro, 0,36; khoảng tin cậy 95% [CI], 0,14 đến 0,94; P = 0,03). Hội chứng sau tưới máu xảy ra ở 12% số người nhận gan tưới máu bằng máy và 27% ở nhóm đối chứng (tỷ lệ rủi ro, 0,43; KTC 95%, 0,20 đến 0,91). Rối loạn chức năng allograft sớm xảy ra ở 26% số gan tưới máu bằng máy, so với 40% số gan kiểm soát (tỷ lệ rủi ro, 0,61; KTC 95%, 0,39 đến 0,96). Số lần điều trị tích lũy cho các trường hợp chít hẹp đường mật không nối mi thấp hơn gần 4 lần sau khi truyền dịch bằng máy, so với kiểm soát. Tỷ lệ các tác dụng ngoại ý là tương tự nhau ở hai nhóm.
KẾT LUẬN
Truyền dịch bằng máy oxy giảm nhiệt làm giảm nguy cơ tắc đường mật không nối sau khi cấy ghép gan lấy được từ người hiến sau khi chết tuần hoàn so với bảo quản lạnh tĩnh thông thường.
Chặt chặt đường mật không nối là một biến chứng lớn sau khi ghép gan, dẫn đến ứ mật và viêm đường mật, thường là khi sử dụng các biện pháp can thiệp đường mật hoặc thậm chí là cấy ghép lại (tức là ghép gan mới và cắt bỏ mảnh ghép đầu tiên). Tỷ lệ hẹp đường mật không nối ống cao gấp khoảng 3 lần sau khi ghép gan lấy từ người hiến tặng sau khi chết tuần hoàn so với sau khi ghép gan từ người cho chết não. Tuy nhiên, ghép gan từ những người hiến tặng sau khi chết tuần hoàn ngày càng được sử dụng nhiều hơn để cấy ghép do tình trạng thiếu tạng hiến liên tục.
Tổn thương do thiếu máu cục bộ – tái tưới máu là một cơ chế chính trong bệnh sinh của tổn thương ống mật và sự phát triển tiếp theo của tắc mật sau khi cấy ghép. Mặc dù phương pháp bảo quản lạnh tĩnh thông thường cung cấp một số biện pháp bảo vệ chống lại chấn thương do thiếu máu cục bộ – tái tưới máu, nhưng cần có các phương pháp bảo quản tiên tiến hơn để cải thiện kết quả sau khi cấy ghép gan thu được từ người hiến sau khi chết tuần hoàn và tăng tần suất sử dụng chúng.
Truyền dịch bằng máy oxygenated ex situ là một phương pháp bảo tồn năng động đã được phát triển để giảm tỷ lệ và mức độ nghiêm trọng của chấn thương do thiếu máu cục bộ – tái tưới máu và cải thiện kết quả sau khi cấy ghép nội tạng. Các nghiên cứu tiền lâm sàng đã chỉ ra rằng một thời gian ngắn (1 đến 2 giờ) tưới máu bằng máy oxy giảm nhiệt sẽ phục hồi chức năng của ty thể và làm giảm sản xuất oxy gốc và các mô hình phân tử liên quan đến tổn thương sau khi cấy ghép. Kỹ thuật tương đối đơn giản này có thể được thực hiện sau khi bảo quản lạnh tĩnh. Các kinh nghiệm lâm sàng đầu tiên cho thấy rằng phương pháp bảo quản này an toàn, giảm tỷ lệ tổn thương bảo tồn gan mật, và có liên quan đến việc cải thiện chức năng mảnh ghép sớm, so với chỉ bảo quản lạnh tĩnh. Mặc dù những phát hiện này đầy hứa hẹn và đã làm tăng sự quan tâm đến các kỹ thuật bảo quản dựa trên máy, chúng dựa trên các nhóm thuần tập trung tâm nhỏ mà không có nhóm đối chứng ngẫu nhiên. Chúng tôi đã tiến hành một thử nghiệm đa trung tâm, ngẫu nhiên, có đối chứng để so sánh việc tưới máu bằng máy oxy hóa hạ nhiệt với bảo quản lạnh tĩnh trong cấy ghép gan từ những người hiến tặng sau khi chết tuần hoàn, với tỷ lệ hẹp đường mật không nối là điểm cuối chính.
Phương pháp
THIẾT KẾ THỬ NGHIỆM VÀ GIÁM SÁT
Thử nghiệm DHOPE-DCD (Truyền oxy kép giảm nhiệt độ của Ghép gan DCD trong việc ngăn ngừa hẹp đường mật sau khi cấy ghép) do điều tra viên khởi xướng và được thiết kế như một thử nghiệm lâm sàng đa trung tâm, tiềm năng, hai nhóm, ngẫu nhiên, có đối chứng,. Thử nghiệm được thực hiện tại sáu trung tâm ghép gan ở châu Âu. Sự ngẫu nhiên hóa khối cân bằng tập trung (trong các khối sáu) được tạo bằng máy tính, với sự phân tầng theo trung tâm thử nghiệm và viêm đường mật xơ cứng nguyên phát như một dấu hiệu cho việc cấy ghép (có hoặc không). Các bệnh nhân được phân chia ngẫu nhiên theo tỷ lệ 1: 1 để nhận gan được bảo quản bằng máy truyền oxy giảm nhiệt sau khi bảo quản lạnh tĩnh trong quá trình vận chuyển (nhóm truyền dịch bằng máy) hoặc chỉ bảo quản lạnh tĩnh (nhóm chứng). Việc lấy ngẫu nhiên diễn ra ngay sau khi một lá gan của người hiến được cho là phù hợp và được bác sĩ phẫu thuật cấy ghép chấp nhận cho người nhận. Thử nghiệm không can thiệp vào quá trình phân bổ hoặc nhận nội tạng thông thường.
Giao thức thử nghiệm , có sẵn với toàn văn của bài viết này tại NEJM.org, đã được xuất bản trước đây. Đề cương đã được phê duyệt bởi các ủy ban đạo đức nghiên cứu tại mỗi địa điểm thử nghiệm và các cơ quan quản lý thiết bị y tế ở mỗi quốc gia. Bệnh nhân và nhóm thu mua nội tạng không biết về các nhiệm vụ của nhóm thử nghiệm. Các tác giả đã thiết kế và thực hiện thử nghiệm cũng như thu thập và phân tích dữ liệu. Các tác giả đầu tiên và cuối cùng đã viết bản thảo đầu tiên của bản thảo, và tất cả các tác giả đã đóng góp cho các phiên bản tiếp theo. Tất cả các tác giả đều đảm bảo về tính chính xác và đầy đủ của dữ liệu cũng như tính trung thực của thử nghiệm đối với giao thức. Quyền truy cập vào dữ liệu không bị hạn chế bởi các thỏa thuận bảo mật.
Fonds NutsOhra đã hỗ trợ thử nghiệm này. Bridge to Life đã cung cấp miễn phí dịch truyền dịch bằng máy (Belzer MPS UW machine-perfusion solution). Mỗi trung tâm tham gia đều đài thọ chi phí mua một thiết bị truyền dịch bằng máy và việc đào tạo kỹ thuật viên tưới máu do nhà sản xuất cung cấp (Organ Assist) như một phần trong trách nhiệm hậu mãi thường xuyên của họ. Tổ chức tài trợ và các công ty không có vai trò gì trong việc thiết kế thử nghiệm; thu thập, quản lý, phân tích hoặc giải thích dữ liệu; hoặc việc viết bản thảo và quyết định gửi nó để xuất bản.
BỆNH NHÂN THỬ NGHIỆM
Bệnh nhân từ 18 tuổi trở lên được ghép gan bằng chỉ ghép từ người hiến tặng sau khi chết tuần hoàn (trong các trường hợp được kiểm soát) đủ điều kiện để đưa vào thử nghiệm. Bệnh nhân bị loại trừ nếu trọng lượng cơ thể của người hiến tặng dưới 40 kg hoặc nếu người hiến tặng dương tính với vi rút suy giảm miễn dịch ở người hoặc vi rút viêm gan B hoặc C. Bệnh nhân cũng bị loại trừ nếu họ đang được cấy ghép vì suy gan tối cấp hoặc suy gan nguyên phát sau lần cấy ghép trước, không có khả năng đưa ra sự đồng ý rõ ràng, dương tính với vi rút suy giảm miễn dịch ở người, hoặc có chống chỉ định chụp đường mật cộng hưởng từ. Tất cả các bệnh nhân đã cung cấp sự đồng ý bằng văn bản.
Gan của người hiến tặng được thu nhận, bảo quản và vận chuyển đến trung tâm cấy ghép theo thực hành tiêu chuẩn, với việc sử dụng phương pháp bảo quản lạnh tĩnh thông thường. Phẫu thuật cấy ghép và chăm sóc hậu phẫu được thực hiện theo tiêu chuẩn thực hành tại địa phương.
TRUYỀN DỊCH BẰNG MÁY OXY HẠ NHIỆT
Thiết bị Hỗ trợ Gan (Organ Assist) được sử dụng để tưới máu tại chỗ cho gan. Thiết bị này cho phép kiểm soát áp suất, tưới máu kép qua tĩnh mạch cửa và động mạch gan với việc sử dụng hai máy bơm ly tâm, cung cấp dòng chảy cửa liên tục và dòng chảy động mạch nhanh với tốc độ 60 nhịp mỗi phút. Thiết bị truyền dịch được bổ sung 4 lít dung dịch truyền dịch bằng máy Belzer lạnh (Cầu nối sự sống), bổ sung 3 mmol glutathione cho mỗi lít dung dịch (Biomedica). Áp lực tưới máu là 25 mm Hg đối với động mạch gan và 5 mm Hg đối với tĩnh mạch cửa. Nhiệt độ của dịch truyền là 10 ° C. Oxy được cung cấp bởi 500 ml mỗi phút với dòng oxy 100% cho mỗi máy tạo oxy. Thời gian truyền dịch bằng máy tối thiểu theo quy định của phác đồ là 2 giờ, khoảng thời gian được coi là đủ để khôi phục lại ti thể và ATP trong gan và để bảo vệ các cơ quan chống lại tổn thương do thiếu máu cục bộ – tái tưới máu.
CÁC BIỆN PHÁP ĐIỂM CUỐI
Điểm kết thúc chính là tỷ lệ tắc nghẽn đường mật không nối thông có triệu chứng vào thời điểm 6 tháng sau khi cấy ghép. Sự xuất hiện của tắc nghẽn đường mật không nối được đánh giá chủ yếu bởi các nhóm y tế của các trung tâm tham gia trên cơ sở sự hiện diện của các tiêu chí chỉ định trước sau: được chẩn đoán bằng cách sử dụng chụp đường mật (tốt nhất là chụp đường mật cộng hưởng từ), kết hợp với các triệu chứng lâm sàng (ví dụ: vàng da hoặc viêm đường mật) hoặc tăng các biến số trong phòng thí nghiệm ứ mật, với sự hiện diện của động mạch gan. Tất cả dữ liệu lâm sàng, bao gồm cả dữ liệu từ chụp đường mật, đã được gửi đến trung tâm dữ liệu trung tâm để xem xét. Để tránh sai lệch báo cáo, chụp đường mật cộng hưởng từ được thực hiện sau 6 tháng, phù hợp với phác đồ nghiên cứu, để phát hiện bằng chứng X quang của bệnh lý đường mật (không nối mi) ở những bệnh nhân chưa được chẩn đoán trong khoảng thời gian trước đó. Chặt chặt đường mật không nối thường được phát hiện từ 3 đến 4 tháng sau khi cấy ghép, và thời gian quan sát 6 tháng do đó được coi là thích hợp để phát hiện các biến cố có ý nghĩa lâm sàng. Tất cả các phim chụp đường mật, cả ở những bệnh nhân có triệu chứng và ở những bệnh nhân không có triệu chứng, đã được xem xét bởi hai bác sĩ X quang độc lập, những người không biết về phương pháp bảo quản và các triệu chứng lâm sàng. Trong trường hợp các kết quả không thống nhất, bác sĩ X quang thứ ba đã được tư vấn cho các trường hợp không thể giải quyết bằng sự đồng thuận.
Điểm kết thúc thứ cấp bao gồm hội chứng tưới máu sau phẫu thuật, được định nghĩa là giảm hơn 30% huyết áp động mạch hệ thống trung bình trong vòng 10 phút sau khi tái tưới máu, có hoặc không tăng gấp đôi liều norepinephrine; không hoạt động chính, được định nghĩa là suy gan, không có nguyên nhân xác định, cần phải cấy ghép lại hoặc dẫn đến tử vong trong vòng 7 ngày sau khi cấy ghép; rối loạn chức năng sinh dục sớm, được đánh giá theo tiêu chí Olthoff; và thời gian lưu trú trong phòng chăm sóc đặc biệt và bệnh viện. Các điểm cuối phụ khác bao gồm huyết khối động mạch gan hoặc tĩnh mạch cửa, tắc nghẽn hoặc rò rỉ đường mật nối và sử dụng liệu pháp thay thế thận trong vòng 6 tháng sau khi cấy ghép. Các dấu hiệu huyết thanh của tổn thương và chức năng gan mật được ghi lại hàng ngày trong tuần đầu tiên và sau khi cấy ghép 1 tháng, 3 tháng và 6 tháng. Tỷ lệ sống sót của bệnh nhân và mảnh ghép được ghi nhận lên đến 1 năm sau khi ghép.
PHÂN TÍCH THỐNG KÊ
Thử nghiệm đã được cung cấp để phát hiện sự khác biệt có liên quan về mặt lâm sàng về tỷ lệ tắc nghẽn đường mật không thông mạch có triệu chứng giữa hai nhóm thử nghiệm. Trên cơ sở các báo cáo trước đây về việc cấy ghép gan thu được từ những người hiến tặng sau khi chết tuần hoàn, chúng tôi dự đoán tỷ lệ gan được bảo quản trong kho lạnh tĩnh là 29% và chúng tôi dự kiến tỷ lệ truyền máu bằng máy sẽ là 11% ( tỉ lệ giảm .60%). Trên cơ sở lũy thừa 80% và mức ý nghĩa 5% (kiểm định hai mặt) trong hai nhóm độc lập, chúng tôi tính toán rằng sẽ cần 77 lá gan trong mỗi nhóm thử nghiệm. Chúng tôi dự định đưa thêm 1 bệnh nhân vào mỗi nhóm thử nghiệm, kết quả là mỗi nhóm có 78 bệnh nhân.
Tất cả các phân tích điểm cuối đã được xác định trước trong giao thức và kế hoạch phân tích thống kê, được hoàn thiện trước khi cơ sở dữ liệu bị khóa. Điểm cuối chính được phân tích bằng cách sử dụng kiểm định chi bình phương, cũng như trong mô hình hồi quy log-nhị thức với tính toán tỷ lệ rủi ro. Các biến số xác định trước trong mô hình này dựa trên các tài liệu liên quan và bao gồm các yếu tố phân tầng (vị trí thử nghiệm và viêm đường mật xơ cứng nguyên phát) và các yếu tố nguy cơ cụ thể của người hiến tặng (chỉ số nguy cơ của người hiến tặng và thời gian thiếu máu cục bộ nóng của người hiến, được xác định là khoảng thời gian từ khi ngừng tuần hoàn đến khi tại chỗ xả lạnh ở người cho). Để nhất quán với giao thức ban đầu, chúng tôi cũng phân tích kết quả bằng cách sử dụng mô hình hồi quy logistic. Kết quả theo thời gian-sự kiện được phân tích bằng cách sử dụng các đường cong Kaplan-Meier với kiểm định thứ hạng log và mô hình hồi quy mối nguy theo tỷ lệ Cox với việc tính toán tỷ lệ nguy cơ. Các điểm cuối nhị phân thứ cấp được đánh giá bằng phép thử chi bình phương hoặc hồi quy log-nhị thức để điều chỉnh các yếu tố phân tầng. Các kết quả liên tục (được biến đổi theo log) được so sánh với việc sử dụng bài kiểm tra t của Học sinh độc lập. Dữ liệu bị thiếu được giả định là bị thiếu ngẫu nhiên và nhiều lần nhập được thực hiện khi hơn 10% tổng số bệnh nhân bị thiếu dữ liệu cho một biến cụ thể. Không có sự điều chỉnh về tính đa dạng trong phân tích các điểm cuối phụ và những phân tích này nên được coi là khám phá. Các thử nghiệm là hai mặt và kết quả được báo cáo với khoảng tin cậy 95%. Giá trị AP nhỏ hơn 0. 05 được coi là biểu thị ý nghĩa thống kê. Phân tích được thực hiện với việc sử dụng phần mềm SPSS, phiên bản 23.0 (SPSS).
Kết quả
NGƯỜI BỆNH
Từ tháng 1 năm 2016 đến tháng 7 năm 2019, chúng tôi đã đánh giá tổng số 245 bệnh nhân đủ điều kiện, trong đó 160 bệnh nhân được phân loại ngẫu nhiên. Sau khi phân loại ngẫu nhiên, bốn ca cấy ghép đã bị hủy bỏ trước khi bất kỳ quy trình thử nghiệm nào được bắt đầu. Trong một trường hợp, gan được dự định để truyền dịch bằng máy, và trong ba trường hợp, gan đã được chỉ định cho nhóm chứng. Lý do hủy bỏ là tình trạng nhiễm mỡ nặng ở hai lá gan và một động mạch bị hư hỏng không thể tái tạo ở một lá gan khác. Ba lá gan này ban đầu được coi là có thể cấy ghép và đã được chấp nhận; họ đã bị từ chối lần thứ hai trên cơ sở thông tin mới này. Ở một bệnh nhân, phúc mạc pseudomyxoma được phát hiện sau khi phẫu thuật mở ổ bụng; Việc cấy ghép đã bị hủy bỏ và gan đã được phân bổ cho một bệnh nhân khác bên ngoài cuộc thử nghiệm.
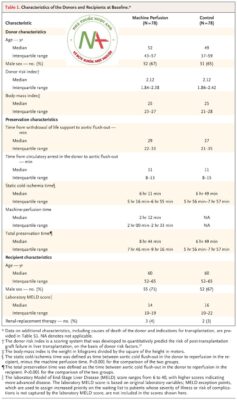
Các đặc điểm cơ bản của người cho và người nhận rất phù hợp trong hai nhóm thử nghiệm (Bảng 1). Do can thiệp, thời gian thiếu máu cục bộ lạnh tĩnh ở nhóm truyền dịch bằng máy ngắn hơn một chút so với nhóm chứng (6 giờ 11 phút so với 6 giờ 49 phút) và tổng thời gian duy trì lâu hơn (8 giờ 44 phút so với . 6 giờ 49 phút).
ĐIỂM CUỐI CHÍNH
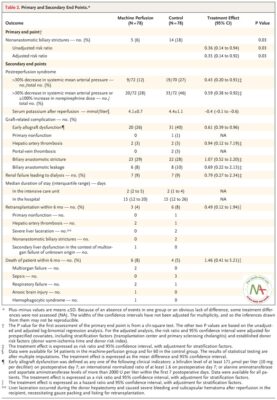
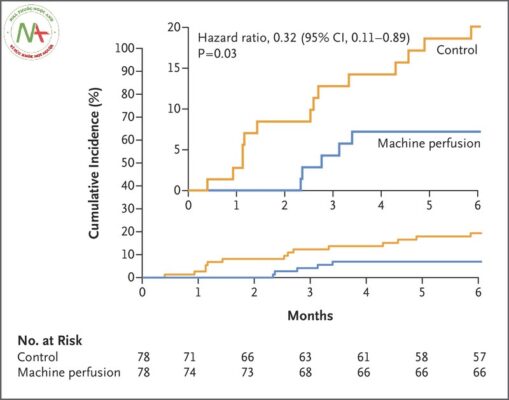
Chặt mật không nối có triệu chứng xảy ra ở 5 trong số 78 bệnh nhân (6%) trong nhóm truyền dịch bằng máy và 14 trên 78 (18%) ở nhóm chứng (tỷ lệ rủi ro, 0,36; khoảng tin cậy 95% [CI], 0,14 đến 0,94 ; P = 0,03). Khi phân tích được điều chỉnh cho các yếu tố phân tầng và các yếu tố rủi ro nhà tài trợ xác định trước trong mô hình hồi quy log-nhị thức, kết quả về cơ bản vẫn giữ nguyên (Bảng 2). Những phát hiện này đã được xác nhận trong các phân tích thời gian đến sự kiện sử dụng phương pháp Kaplan – Meier và phân tích hồi quy Cox (tỷ lệ nguy cơ, 0,32; KTC 95%, 0,11 đến 0,89; P = 0,03; P = 0,03 cũng theo thứ hạng log thử nghiệm) (Hình 1).
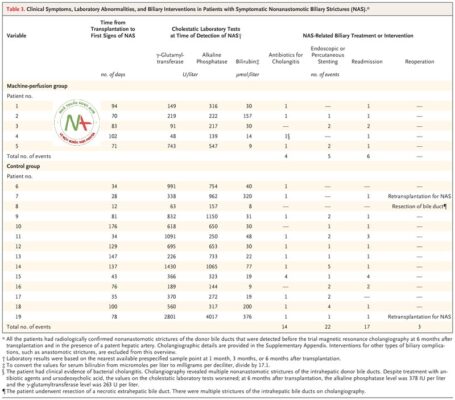
Tất cả 19 bệnh nhân bị hẹp bao quy đầu có triệu chứng đều nhận được chẩn đoán trước khi chụp đường mật cộng hưởng từ thử nghiệm được thực hiện 6 tháng sau khi cấy ghép, và tất cả đều có các triệu chứng lâm sàng hoặc các xét nghiệm phòng thí nghiệm ứ mật (hoặc cả hai) hỗ trợ chẩn đoán này. Xem xét lại hình ảnh chụp đường mật ở những bệnh nhân có triệu chứng đã xác nhận bằng chứng chụp X quang về sự chặt chẽ không nối mi.
Một phân tích độ nhạy bao gồm tất cả các bệnh nhân đã hoàn thành 6 tháng theo dõi, bao gồm cả chụp đường mật cộng hưởng từ thử nghiệm, không thay đổi kết luận (Bảng 2). Với sự khác biệt nhỏ giữa các nhóm về thời gian thiếu máu cục bộ lạnh tĩnh, chúng tôi đã tiến hành phân tích độ nhạy sau học với biến này làm hiệp biến trong mô hình hồi quy log-binomial; kết luận không thay đổi.
CÁC BIỆN PHÁP ĐIỂM CUỐI PHỤ
Trong mổ, hội chứng sau tưới máu, được định nghĩa là giảm hơn 30% huyết áp động mạch trung bình, ít xảy ra hơn ở những người nhận gan tưới máu bằng máy so với những người trong nhóm chứng (12% so với 27%; tỷ lệ rủi ro đã điều chỉnh, 0,43; KTC 95%, 0,20 đến 0,91). Sự khác biệt này vẫn còn khi chúng tôi bao gồm tăng cường hỗ trợ co thắt trong định nghĩa. Phù hợp với điều này, nồng độ kali huyết thanh trung bình (± SD) ngay sau khi cấy ghép ở nhóm truyền dịch bằng máy thấp hơn so với nhóm chứng (4,1 ± 0,7 mmol mỗi lít so với 4,4 ± 1,1 mmol mỗi lít; sự khác biệt trung bình, – 0,4 mmol mỗi lít; KTC 95%, −0,1 đến −0,6).
Rối loạn chức năng allograft sớm xảy ra ở 20 gan tưới máu bằng máy (26% bệnh nhân), so với 31 gan kiểm soát (40% bệnh nhân) (tỷ lệ rủi ro đã điều chỉnh, 0,61; KTC 95%, 0,39 đến 0,96). Không có trường hợp không hoạt động chính trong nhóm truyền dịch bằng máy, nhưng một trường hợp đã được quan sát thấy ở nhóm chứng.
Số lần điều trị tích lũy cho các trường hợp tắc mật không nối và các biến chứng liên quan trong vòng 6 tháng sau khi cấy ghép thấp hơn gần 4 ở nhóm truyền dịch bằng máy so với nhóm chứng. Hai bệnh nhân, cả hai đều ở nhóm chứng, đã trải qua cấy ghép lại vì chứng hẹp bao quy đầu nghiêm trọng.Không có sự khác biệt giữa các nhóm về tỷ lệ rò rỉ hoặc hẹp đường mật qua nối. Kết quả đánh giá mù tất cả các biểu đồ đường mật được trình bày trong Bảng S3 đến Bảng S7.
Các phân tích trong phòng thí nghiệm về các xét nghiệm chức năng gan huyết thanh được trình bày trong Hình S2. Tương ứng với tỷ lệ bệnh nhân có triệu chứng tắc mật không thông trong nhóm chứng cao hơn so với nhóm truyền dịch bằng máy, các dấu hiệu ứ mật huyết thanh ở nhóm chứng cao hơn so với nhóm truyền dịch bằng máy ở 3 tháng (phosphatase kiềm và bilirubin ) và 6 tháng (phosphatase kiềm).Không có sự khác biệt liên quan giữa hai nhóm trong việc sử dụng liệu pháp thay thế thận, trong thời gian nằm trong phòng chăm sóc đặc biệt hoặc bệnh viện, hoặc trong việc ghép và thời gian sống thêm của bệnh nhân sau 1 năm.
SỰ KIỆN AN TOÀN VÀ BẤT LỢI
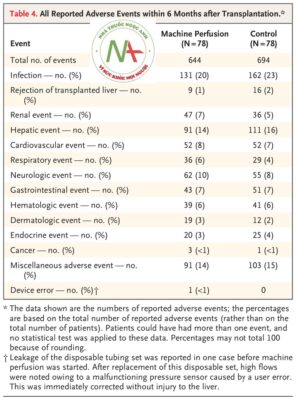
Sự phân bố của các bệnh nhân được báo cáo về các tác dụng ngoại ý là tương tự nhau trong hai nhóm. Không có sự khác biệt lâm sàng liên quan giữa hai nhóm về mức độ nghiêm trọng của các tác dụng phụ (Bảng S8).
Thảo luận
Trong thử nghiệm này liên quan đến những bệnh nhân được ghép gan từ một người hiến tặng sau khi chết tuần hoàn, những người được chỉ định ngẫu nhiên để được ghép gan sau khi truyền dịch bằng máy oxy giảm thân nhiệt có nguy cơ bị tắc mật không thông mạch có triệu chứng trong vòng 6 tháng sau khi cấy ghép, tức là khoảng 2/3. thấp hơn so với những người được chỉ định ngẫu nhiên để được ghép gan sau khi chỉ bảo quản lạnh tĩnh thông thường. Tỷ lệ thấp hơn của loại bệnh đường mật này có ý nghĩa cả về mặt thống kê và lâm sàng.
Chặt chặt đường mật không nối là kết quả của việc phục hồi không hoàn toàn sau chấn thương do thiếu máu cục bộ đường mật – tái tưới máu, dẫn đến hẹp xơ của lòng ống mật và cản trở dòng chảy của mật. Mặc dù một số bệnh nhân có thể được điều trị bằng nội soi hoặc can thiệp qua da, nhưng các biện pháp thắt chặt thường chống lại sự giãn và đặt stent, và cấy ghép lại có thể vẫn là liệu pháp điều trị dứt điểm duy nhất. Trong thử nghiệm hiện tại, số lượng tích lũy các can thiệp để thắt đường mật không nối và điều trị kháng sinh đối với bệnh viêm đường mật liên quan thấp hơn gần 4 ở các gan tưới máu bằng máy so với các gan đối chứng. Hai bệnh nhân trong nhóm đối chứng được cấy ghép lại trong vòng 6 tháng vì bệnh lý đường mật nặng.
Tác dụng bảo vệ của tưới máu bằng máy cũng được thể hiện qua việc giảm nguy cơ mắc hội chứng sau tưới máu và rối loạn chức năng cơ năng sớm. Tái tưới máu mảnh ghép thường đi kèm với gan giải phóng kali và không ổn định tuần hoàn. Trong một nghiên cứu thử nghiệm lâm sàng, sự giảm nồng độ kali huyết thanh đã được quan sát thấy sau khi cấy ghép gan truyền dịch bằng máy hạ thân nhiệt, và lợi ích này đã được xác nhận trong thử nghiệm tiền cứu hiện tại.
Ưu điểm quan trọng của truyền dịch bằng máy hạ thân nhiệt so với các phương pháp bảo quản động khác, chẳng hạn như truyền dịch bằng máy Na Uy, là tính đơn giản và an toàn nội tại tương đối của nó. Sự cố kỹ thuật dẫn đến không đủ tưới máu gan sẽ không gây bất lợi ngay lập tức vì cơ quan này được duy trì ở nhiệt độ thấp. Tình trạng này khác với truyền dịch bằng máy nahma, trong đó lỗi của thiết bị hoặc người vận hành dẫn đến thiếu máu cục bộ do ấm và có thể dẫn đến mất nội tạng. Một ưu điểm khác của truyền dịch bằng máy hạ nhiệt là nó có hiệu quả sau khi bảo quản lạnh tĩnh. Mặc dù một thiết bị truyền dịch hạ thân nhiệt có thể vận chuyển hiện đang được nghiên cứu lâm sàng, vẫn chưa xác định được liệu điều này có mang lại lợi ích bổ sung hay không.
Bất chấp sự phục hồi của ATP, quá trình trao đổi chất ở gan vẫn bị ức chế và gan không sản xuất mật trong quá trình tưới máu bằng máy này. Mặc dù việc giải phóng flavin mononucleotide của ty thể vào dịch vị có tương quan với chức năng gan sau khi cấy ghép, vẫn chưa rõ liệu điều này có dự báo nguy cơ mắc bệnh đường mật hay không. Trái ngược với truyền dịch bằng máy Na Uy, truyền dịch bằng máy hạ thân nhiệt, do đó, hiện không được coi là một công cụ để kiểm tra khả năng sống trước khi cấy ghép; đúng hơn, nó là một phương pháp để giảm tỷ lệ tổn thương do thiếu máu cục bộ – tái tưới máu. Điều này làm cho nó phù hợp với những người hiến tặng gan có nguy cơ gia tăng phát triển các biến chứng liên quan đến thiếu máu cục bộ, chẳng hạn như gan lấy từ người hiến sau khi chết tuần hoàn. Để đạt được mục tiêu này, việc truyền dịch bằng máy hạ thân nhiệt và máy tăng huyết áp phục vụ các mục tiêu khác nhau và không phải là các kỹ thuật cạnh tranh. Hai kỹ thuật này có thể được áp dụng tuần tự với những lợi ích bổ sung cho nhau. Liệu việc truyền dịch bằng máy hạ thân nhiệt cũng có lợi trong việc cấy ghép gan lấy từ người cho chết não hay không là chủ đề của các thử nghiệm lâm sàng đang diễn ra.
Trong thử nghiệm hiện tại, tưới máu bằng máy không ảnh hưởng đến sự sống sót của bệnh nhân hoặc mảnh ghép. Với tỷ lệ bệnh nhân sống sót sau khi ghép gan cao và nguy cơ mất mảnh ghép tương đối thấp, sẽ cần có những thử nghiệm lớn hơn nhiều để phát hiện ảnh hưởng đến các biện pháp kết quả này.
Việc hoàn trả công nghệ mới này bởi các nhà tài trợ chăm sóc sức khỏe sẽ liên quan đến việc đánh giá kinh tế-sức khỏe. Chi phí ghép gan từ người cho sau khi chết tuần hoàn cao hơn 25 đến 30% so với ghép gan từ người cho chết não, chủ yếu là do tỷ lệ biến chứng mật cao hơn. Việc ngăn ngừa bệnh lý đường mật sau ghép có thể không chỉ làm tăng sự chấp nhận ghép gan từ người cho sau khi chết tuần hoàn mà còn có thể làm cho việc sử dụng máy truyền dịch tiết kiệm chi phí.
Trong thử nghiệm ngẫu nhiên này liên quan đến những bệnh nhân được ghép gan lấy từ người hiến tặng sau khi chết tuần hoàn, chúng tôi nhận thấy rằng việc truyền dịch bằng máy oxy giảm thân nhiệt dẫn đến tỷ lệ tắc mật không nối thông có triệu chứng thấp hơn so với bảo quản lạnh tĩnh thông thường.