Sản xuất Dược phẩm
Tiêu chuẩn Japan-GMP? Quy trình để được cấp chứng nhận Japan-GMP
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
Trong đời sống ngày nay, thuốc là sản phẩm gắn liền với sinh mạng con người. Vì vậy để chọn lựa được thuốc chất lượng, hiệu quả và an toàn thì thuốc cần phải đạt được các tiêu chuẩn quốc tế như GMP-WHO, PIC/S-GMP, EU-GMP, Japan-GMP,…Trong đó Japan-GMP là một trong những tiêu chuẩn khắt khe về chất lượng khi kê đơn thuốc. Vậy, Tiêu chuẩn Japan-GMP là gì? Để đạt tiêu chuẩn Japan-GMP cần phải trải qua những bài thử nghiệm như thế nào? Hãy cùng Nhà Thuốc Ngọc Anh tìm hiểu những thông tin về Tiêu chuẩn Japan- GMP ngay trong bài viết sau đây nhé
Khái niệm về Tiêu chuẩn Japan-GMP
Hệ thống các tiêu chuẩn Thực hành tốt sản xuất thuốc (GMP) tại Nhật Bản được gọi là Japan-GMP.
Năm 1974, Japan-GMP đã được thiết lập tại Nhật Bản và chính thức có hiệu lực vào năm 1975.
Japan-GMP được ra đời trước cả EU-GMP (Tiêu chuẩn thực hành tốt sản xuất thuốc tại Châu Âu, ra đời năm 1989), và không ngừng được cập nhật, cải thiện và nâng cao.
Japan-GMP được xem như là một biểu trưng cho chất lượng thuốc tại Nhật Bản và được Cơ quan Dược phẩm và Thiết bị Y tế Nhật Bản ( viết tắt là PMDA) quản lý và trực tiếp cấp giấy chứng nhận cho những doanh nghiệp hay cơ sở sản xuất thuốc đảm bảo yêu cầu.
PMDA được trực thuộc bởi Bộ Y tế Lao động và An sinh Xã hội của Nhật Bản (viết tắt là MHLW).
Trên lý thuyết,Tiêu chuẩn của Nhật Bản được đánh giá là tương đương với các tiêu chuẩn quốc tế khác như PIC/S-GMP, EU-GMP, CGMP-USA…
Tuy nhiên, theo Pacific Bridge Medical (PBM), Tiêu chuẩn Japan-GMP, trên thực tế, thường đặt ra những yêu cầu về kiểm soát và đảm bảo chất lượng nghiêm ngặt hơn so với các tiêu chuẩn của các nước phương Tây.
Quy trình để được cấp Japan-GMP
Một doanh nghiệp hay cơ sở sản xuất thuốc được công nhận hay được cấp giấy phép đạt chuẩn Japan-GMP, thì các dây chuyền sản xuất thuốc của doanh nghiệp đó cần phải vượt qua nhiều bước đánh giá thường kéo dài từ 16-27 tháng và trải qua 2 giai đoạn.
Giai đoạn 1
Doanh nghiệp hoặc cơ sở sản xuất thuốc đăng ký phải được cấp giấy phép hoạt động tại Nhật Bản trong lĩnh vực dược phẩm.
Giai đoạn 2
Cơ quan có thẩm quyền tại Nhật Bản sẽ đánh giá và công nhận đạt tiêu chuẩn Japan-GMP cho sản phẩm được doanh nghiệp đăng ký.
Trong giai đoạn 2, cơ quan PMDA sẽ tiến hành đánh giá các sản phẩm được các doanh nghiệp đăng ký. Sản phẩm, sẽ được kiểm tra và đánh giá về chất lượng, tính hiệu quả và độ an toàn một cách khắt khe và cực kì kỹ lưỡng.
Ngoài ra, về hạ tầng cơ sở sản xuất, điều kiện sản xuất, máy móc thiết bị, trình độ nhân viên,.. cũng được PMDA đánh giá có đạt theo tiêu chuẩn Japan-GMP hay không.
Phương thức nộp các tài liệu cần thiết cho PMDA để áp dụng kiểm tra
Người đại diện doanh nghiệp đi đăng ký cần điền đầy đủ thông tin vào Danh sách kiểm tra 1 hoặc Danh sách kiểm tra 2 và tất cả đều phải được đính kèm với biểu mẫu đăng ký kiểm tra cùng với các tài liệu trình.
Danh sách kiểm tra 1

Danh sách kiểm tra 2
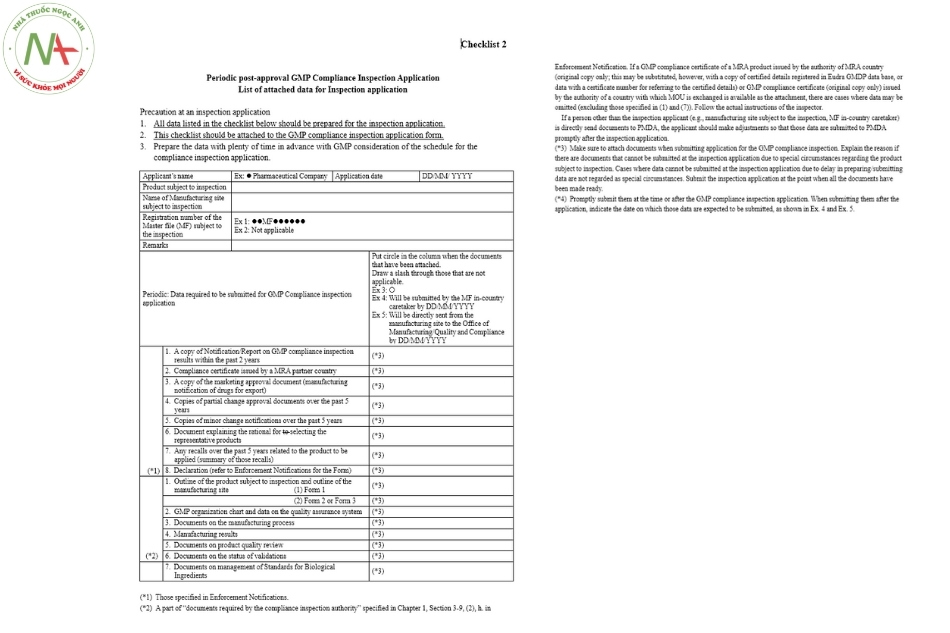
Về nguyên tắc, đơn đăng ký sẽ không được chấp nhận nếu đơn đăng ký kiểm tra không có các tài liệu cần thiết kèm theo. Doanh nghiệp cần chuẩn bị tốt các Tài liệu trước khi nộp đơn xin được kiểm tra, phê duyệt .
Sau khi nộp đơn đăng ký kiểm tra, khi người quản lý hồ sơ của doanh nghiệp hoặc địa điểm sản xuất cần kiểm tra trực tiếp gửi một phần tài liệu để trình đến Văn phòng Sản xuất / Chất lượng và Tuân thủ của PMDA, người nộp hồ sơ cần chỉ rõ các tài liệu nộp dự kiến trong Danh sách kiểm tra, cần được đính kèm với mẫu đơn đăng ký kiểm tra.
Người nộp đơn phải thực hiện rà soát và bổ sung các tài liệu có liên quan ngay sau khi nộp đơn kiểm tra. Đơn kiểm tra có thể bị rút lại nếu các tài liệu liên quan không được nộp trong thời gian dài bất kể đã nộp đơn kiểm tra.
Bạn đọc có thể tải về file Đính kèm, biểu mẫu và danh sách kiểm tra đầy đủ tại đây
Thời hạn được xét duyệt Tiêu chuẩn Japan-GMP
Từ khi nộp hồ sơ đăng ký cho đến khi được công nhận đạt tiêu chuẩn Japan-GMP của một doanh nghiệp, thường trải qua trong vòng một năm.
Để nộp hồ sơ đăng ký, thì doanh nghiệp cần đảm bảo được trải qua các vòng kiểm định về tính an toàn của sản phẩm, độ hiệu quả, chất lượng… Doanh nghiệp khi nộp hồ sơ đăng kỳ cần phải chuẩn bị đầy đủ và kỹ lưỡng các giấy chứng nhận của các khâu kiểm định kể trên và một số tài liệu có liên quan.
Thời hạn có hiệu lực của giấy chứng nhận Japan-GMP
Thời hạn hiệu lực của giấy chứng nhận Japan-GMP mà doanh nghiệp đã đạt được có giá trị là 5 năm kể từ ngày doanh nghiệp được kiểm tra gần nhất. Sau thời gian trên, các doanh nghiệp hay cơ sở sản xuất cần phải được tiến hành đánh giá lại qua các vòng của PMDA để được gia hạn giấy chứng nhận Japan-GMP khi giấy chứng nhận này hết hiệu lực.
Nếu hệ thống các tiêu chuẩn Japan-GMP có được bổ sung tiêu chuẩn mới thì các doanh nghiệp cũng phải đáp ứng theo.
Trong suốt thời gian doanh nghiệp đang được đánh giá lại các tiêu chuẩn đó, doanh nghiệp cần phải duy trì hệ thống quản lý đáp ứng với Japan – GMP và cần phải báo cáo lại các thay đổi nếu có một cách kịp thời.

Lựa chọn sản phẩm đại diện để kiểm tra định kỳ
Nếu gửi đơn đăng ký cho nhiều sản phẩm, các sản phẩm đại diện của họ phải được lựa chọn dựa trên cơ sở hợp lý rõ ràng phù hợp. Nếu có thể, các sản phẩm đại diện được chọn từ mỗi danh mục phải là những sản phẩm chưa được chọn để kiểm tra định kỳ trước đây. Đồng thời chỉ ra các sản phẩm đại diện đã được lựa chọn trong các đợt kiểm tra định kỳ trước đây.
Lưu ý rằng các sản phẩm đại diện được đề xuất có thể được yêu cầu thay đổi nếu được xác định là không phù hợp.
Quy trình kiểm tra tiêu chuẩn Japan-GMP đối với doanh nghiệp nước ngoài.
Đơn xin Kiểm tra Tuân thủ GMP của các nhà sản xuất nước ngoài sẽ được áp dụng bởi người có giấy phép lưu hành, người nộp đơn xin cấp phép lưu hành, những người đã được chấp thuận đặc biệt đối với các nhà sản xuất nước ngoài, hoặc những người có ý định nhận được sự chấp thuận đặc biệt đối với các nhà sản xuất nước ngoài. Các nhà sản xuất xin phê duyệt đặc biệt cho các nhà sản xuất nước ngoài phải chỉ định người có giấy phép tiếp thị.
Về nguyên tắc, Kiểm tra Tuân thủ GMP sẽ được PMDA tiến hành kiểm tra tại chỗ. Tuy nhiên, PMDA có thể đưa ra quyết định chỉ tiến hành kiểm tra trên các tài liệu (sau đây gọi là kiểm tra trực tiếp), xem xét rủi ro của sản phẩm, tiêu chuẩn GMP của quốc gia tương ứng và hoạt động của nó, và tình trạng tuân thủ GMP dựa trên các tài liệu được nộp trước.
PMDA sẽ báo cáo kết quả kiểm tra cho Bộ Y tế, Lao động và Phúc lợi, sử dụng biểu mẫu “Thông báo kết quả kiểm tra việc tuân thủ GMP”. PMDA sẽ cấp một bản sao của Thông báo Kết quả Kiểm tra Tuân thủ GMP cho người được cấp phép lưu hành đã đăng ký kiểm tra và một bản sao của “Báo cáo Kết quả Kiểm tra Tuân thủ GMP cho nhà sản xuất nước ngoài mà việc kiểm tra tại chỗ đã được thực hiện. Trong trường hợp kiểm tra tại bàn, bản sao của Báo cáo Kết quả Kiểm tra Tuân thủ GMP sẽ không được cấp.
Bạn đọc có thể tải về file đầy đủ tại đây.
Lợi ích mang lại khi đạt chuẩn Japan-GMP
Japan-GMP, là bộ tiêu chuẩn được xem là biểu trưng cho chất lượng ở Nhật Bản.
Và nó cũng được áp dụng như là một chuẩn chuẩn mực chất lượng cao tại một số quốc gia trên thế giới.
Hiện nay, tại Việt Nam, các doanh nghiệp, cơ sở sản xuất dược phẩm đều đang theo đuổi và mong muốn được sở hữu được dây chuyền sản xuất đạt chuẩn Japan-GMP. Điều này đã hứa hẹn sẽ mang đến rất nhiều lợi ích cho quốc gia, ngành Y tế, doanh nghiệp sản xuất nước nhà nói chung và lợi ích của người tiêu dùng nói riêng.
Đối với doanh nghiệp
- Việc doanh nghiệp sở hữu được dây chuyền sản xuất chuẩn Japan-GMP sẽ giúp doanh nghiệp có được lợi thế xuất khẩu dược phẩm của nước nhà đến với các thị trường dược phẩm khó tính, nhất là thị trường Nhật Bản và một số nước trong ASEAN.
- Tạo được sự uy tín và niềm tin của doanh nghiệp đối với các đối tác, khách hàng, nhờ đó mở ra rất nhiều cơ hội phát triển cho doanh nghiệp.
- Với các sản phẩm tân dược được sản xuất đột phá kết hợp với dây chuyền đạt chuẩn Japan-GMP, góp phần giúp các doanh nghiệp có thể đưa ngành dược phẩm của nước nhà được định danh trên bản đồ ngành dược trên toàn cầu.
- Tăng khả năng cạnh tranh sản phẩm của doanh nghiệp quốc gia mình đối với các sản phẩm nước ngoài.
- Thể hiện sự cam kết uy tín về mặt chất lượng trong sản xuất và trong kinh doanh của doanh nghiệp.
Đối với người tiêu dùng
- Một doanh nghiệp trong nước đạt chuẩn Japan-GMP, điều đó có nghĩa, người tiêu dùng trong nước đã có thể tiếp cận được với các sản phẩm đạt tiêu chuẩn hàng đầu quốc tế ngay tại nước nhà với mức chi phí phù hợp.
- Nhờ đó nâng cao chất lượng sản phẩm dược phẩm trên thị trường dược phẩm trong nước.
- Tạo được uy tín với chính người tiêu dùng trong nước. Người tiêu dùng khi sử dụng một sản phẩm mà chất lượng đã được xét duyệt qua những vòng kiểm sát khắt khe, nghiêm ngặt sẽ an tâm hơn và tin tưởng hơn vào doanh nghiệp.
Thách thức đối với doanh nghiệp để đạt tiêu chuẩn Japan-GMP.
Tiêu chuẩn Japan-GMP là bộ tiêu chuẩn mà không chỉ được rất nhiều hãng dược trong nước và cả nước ngoài mong muốn và không ngừng theo đuổi. Tuy nhiên, để đầu tư cho một dây chuyền sản xuất thuốc đạt chuẩn tiêu chuẩn này cũng đặt ra rất nhiều thách thức cho doanh nghiệp
- Chi phí để xây dựng một dây chuyền đạt chuẩn tốn kém cao gấp nhiều lần so với các dây chuyền đạt các tiêu chuẩn thông thường.
- Doanh nghiệp còn phải tuân thủ rất nhiều yêu cầu khắt khe, và nghiêm ngặt hơn một số tiêu chuẩn thông thường.
- Tốn kém nhiều thời gian và nhiều vòng kiểm tra xét duyệt để được đánh giá có đạt chuẩn.
- Bộ tiêu chuẩn Japan – GMP ngày càng hoàn thiện và nâng cấp với những tiêu chuẩn nghiêm ngặt hơn. Do đó, đòi hỏi doanh nghiệp phải không ngừng nâng cấp dây chuyền sản xuất đã đạt chuẩn để có thể vượt qua các vòng khảo sát khi gia hạn.
Danh sách các doanh nghiệp đạt chuẩn Japan-GMP ở Việt Nam
Tính đến năm 2022, Việt Nam hiện đang có 3 doanh nghiệp đạt chuẩn chất lượng Japan-GMP.
Doanh nghiệp Dược Hậu Giang
Đứng đầu trong hành trình chinh phục Japan-GMP là doanh nghiệp dược phẩm Dược Hậu Giang ( DHG- Pharma) được cấp vào ngày 05/02/2019.

Hiện tại, doanh nghiệp Dược Hậu Giang sở hữu đến 2 dây chuyền sản xuất viên nén và viên nén bao phim đạt chuẩn chất lượng Japan-GMP tại nhà máy Tân Phú Thạnh.
Hai dây chuyền đạt chuẩn chất lượng Japan-GMP này đang sản xuất các nhóm sản phẩm chủ lực của công nghiệp và chiếm khoảng 30% doanh thu công ty.
Lãnh đạo Dược Hậu Giang con cho biết, doanh nghiệp đang lên kế hoạch để tiếp tục nỗ lực chinh phục được chứng nhận Japan-GMP cho một dây chuyền khác của doanh nghiệp như dây chuyền sủi bọt và một số dây chuyền trọng yếu khác.
Công ty Rohto Mentholatum Việt Nam
Công ty TNHH Rohto-Mentholatum (Việt Nam) là Công ty con của Rohto Pharmaceutical Co., Ltd, một trong những Tập đoàn Dược phẩm hàng đầu của Nhật Bản chuyên về các sản phẩm chăm sóc sức khoẻ và sắc đẹp.
Được cấp ngày 03/10/2019
Mã số: 5123108015361
Cơ quan cấp giấy chứng nhận: cơ quan có thẩm quyền tại Nhật Bản
Một số sản phẩm của Rohto Mentholatum đã đạt tiêu chuẩn chất lượng Japan – GMP
|
Mentholatum Rohto Alguard Rohto Alguard mild Rohto Alguard s Rohto Alguard Soft Rohto C Cube Aqua Rohto C Cube Cool Rohto C Cube Cool Charge a Rohto C Cube m Rohto Eye Stretch Rohto V11
|
Rohto cool 40 α
Rohto Free One. Rohto Lacia Rohto Lycee a; New V.Rohto Rohto Soft One Eye drops Rohto Tear Free Rohto Vita 40 α Rohto Vita Cool 40 Rohto Zi b Rohto Zi Pro a
|
Công ty cổ phần Hóa – Dược Mekophar
Mekophar là một trong những doanh nghiệp dược đầu tiên của Việt Nam đạt tiêu chuẩn GMP-WHO, và là công ty dược duy nhất của Việt Nam sản xuất nguyên liệu kháng sinh Bêtalactam cung cấp cho các công ty dược trong và ngoài nước.
Nhà máy Mekophar BP tại khu công nghệ cao Quận 9, TP. HCM được công cấp giấy chứng nhận đạt chuẩn Japan – GMP vào ngày 15/10/2019.
Mã số: 5123108015995
Cơ quan cấp giấy chứng nhận: cơ quan có thẩm quyền tại Nhật Bản. Và được Cục quản lý dược Việt Nam xác nhận.
Bạn đọc có thêm tìm hiểu thêm các doanh nghiệp trong nước đạt chuẩn GMP tại đây.
Tài liệu tham khảo
- PMDA.go.jp, GMP / QMS / GCTP Inspections, truy cập ngày 11 tháng 6 năm 2022.

