Bệnh tim mạch
Sinh lý hệ tuần hoàn và huyết động học lâm sàng – Lâm sàng tim bẩm sinh
Xuất bản: UTC +7
Cập nhật lần cuối: UTC +7
Nguồn: Sách Lâm sàng tim bẩm sinh
Chủ biên
PGS.TS.BS. Nguyễn Lân Hiếu
Tham gia biên soạn
Lê Hồng Quang
Nguyễn Thị Minh Lý
Nguyễn Văn Hiếu
Cùng với sự phát triển của y học nói chung, sinh lý học tuần hoàn cũng có những tiến bộ vượt bậc với những khái niệm sâu sắc hơn và giải thích các vấn đề sinh lý rõ ràng hơn. Mô hình phù hợp để nghiên cứu sinh lý tuần hoàn đó là tâm thất được “mồi” bởi một lượng tiền gánh để tạo ra một công áp lực (pressure work). Công áp lực từ tâm thất sẽ trở thành công lưu lượng trong động mạch chủ và thân động mạch phổi. Lưu lượng tuần hoàn trong các đại động mạch sẽ được phân bố trong giường mạch máu để tối ưu hóa quá trình chuyển hóa trong tuần hoàn hệ thống và quá trình oxy hóa ở tuần hoàn phổi.
Trong bài viết dưới đây Nhà thuốc Ngọc Anh xin gửi đến quý bạn đọc tóm tắt những khái niệm cập nhật liên quan một số quá trình sinh lý tuần hoàn và huyết động học lâm sàng chính yếu và tập trung phân tích cách thức mà công áp lực trong tâm thất chuyển thành công lưu lượng trong các đại động mạch; khái niệm về sự cặp đôi giữa tâm thất và mạch máu. Các vấn đề liên quan đến sự phân bố của lưu lượng trong nội tại mỗi hệ đại tuần hoàn và hệ tiểu tuần hoàn, phân bố giữa hai hệ tuần hoàn, các yếu tố góp phần quyết định lưu lượng tuần hoàn phổi. Chương sách cũng đề cập đến hoạt động của hệ tim mạch liên quan đến hoạt động chuyển hóa hệ thống, tuần hoàn thai nhi, tuần hoàn sơ sinh và các tuần hoàn chuyển tiếp.
CHỨC NĂNG TÂM THẤT
Việc mô tả chính xác chức năng tim, nhu cầu chuyển hóa của tim cũng như sự hoạt động của tim với hệ mạch máu là nền tảng cho hiểu biết về sinh lý và sinh lý bệnh của hệ tim mạch. Trong thực hành lâm sàng hàng ngày, chúng ta mới chỉ giới hạn đến việc ước lượng áp lực tâm thu, áp lực cuối tâm trương thất trái hoặc các phép đo đánh giá sự biến đổi về thể tích (phân suất tống máu). Trên thực tế, các thăm dò hình ảnh không xâm lấn như siêu âm tim hay cộng hưởng từ đã đánh giá được chức năng tim sâu hơn trên những khía cạnh khác nhau.
Chu chuyển tim
Công trình kinh điển của Wiggers đánh giá những thay đổi tạm thời về áp lực và thể tích tâm thất trong các giai đoạn của chu chuyển tim vẫn đóng vai trò nền tảng để hiểu về chức năng tâm thất. Để đơn giản hóa, chu chuyển tim được chia thành các giai đoạn theo mô hình của Wiggers. Tuy vậy, trong thực tế giữa các giai đoạn luôn có sự giao thoa và các hiện tượng sinh lý xảy ra trong thời điểm giao thoa này. Trong các trạng thái bệnh lý có thể xảy ra sự mất phối hợp về chức năng trong tim.
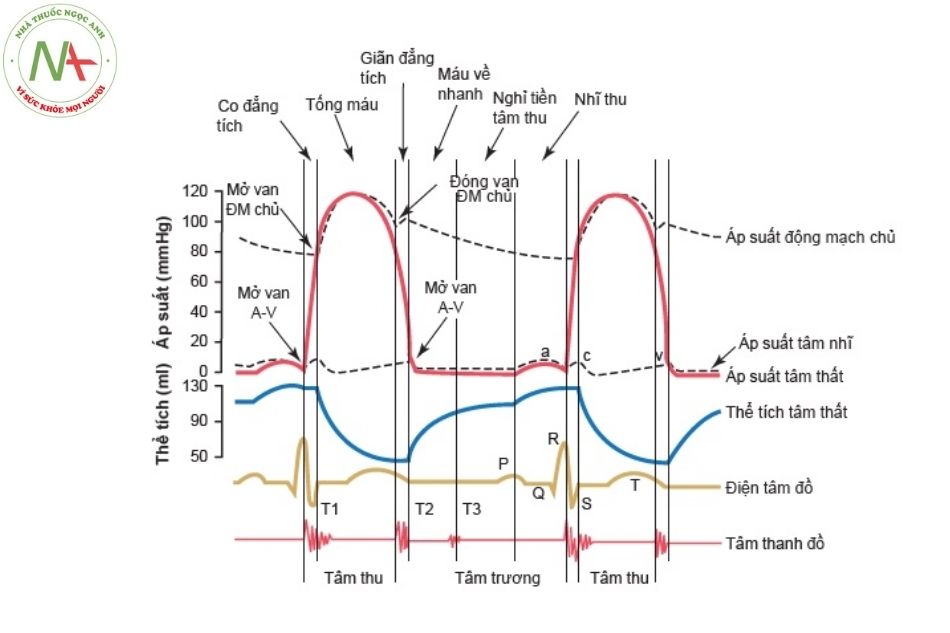
(Nguồn: Guyton and Hall-Textbook of Medical Physiology, 13th edition) Chú thích: ĐM: Động mạch; A-V: nhĩ-thất; T1, T2: Tiếng tim T1, T2.
Sóng áp lực tâm nhĩ a, c, v: Sóng a được tạo ra do tâm nhĩ co. Sóng c xuất hiện khi tâm thất bắt đầu co. Sóng v xuất hiện khi co tâm thất kết thúc.
Các giai đoạn của tâm thất trong một chu chuyển tim
- Bắt đầu bằng sự khởi phát của quá trình khử cực thất trái (và thất phải): thất trái co làm áp lực trong buồng thất tăng nhanh dần lớn hơn áp lực trong buồng nhĩ trái, tiếp tục tăng tới khi đạt đến áp lực tâm trương trong động mạch chủ. Giai đoạn này, cả van hai lá và van động mạch chủ đều đóng vì vậy gọi là giai đoạn co đẳng tích. Thay đổi chính của tâm thất trong giai đoạn này đó là sự gia tăng áp lực trong buồng thất. Vì vậy đánh giá chức năng tâm thất trong giai đoạn này đồng nghĩa với đánh giá tốc độ gia tăng áp lực trong buồng tâm thất. Một trong những chỉ số có thể đánh giá là tốc độ gia tăng áp lực tối đa trong buồng tâm thất (dP/dtMAX) hoặc một số chỉ số gián tiếp sử dụng đánh giá, nhằm làm giảm độ nhạy cảm của tâm thất trái, đặc biệt với tiền gánh.
- Áp lực trong buồng tâm thất tiếp tục tăng vượt quá áp lực trong động mạch chủ (thất trái) hoặc động mạch phổi (thất phải) đánh dấu sự bắt đầu của giai đoạn tâm thất tống máu. Chức năng tâm thất trong giai đoạn này được đánh giá bởi hiệu quả tống máu thông qua phân suất co ngắn sợi cơ hoặc phân suất tống máu. Một vài chỉ số gián tiếp được xây dựng, có tính đến yếu tố thay đổi về gánh của tâm thất, ví dụ: mối liên quan giữa thể tích tống máu và áp lực cuối tâm thu (hậu gánh) hoặc giữa vận tốc co ngắn theo chiều chu vi và áp lực cuối tâm thu thất trái (hậu gánh).
- Giai đoạn tâm trương được bắt đầu ở thời điểm áp lực tâm thất giảm thấp hơn áp lực trong động mạch chủ hoặc động mạch phổi, làm đóng van tổ chim. Tuy nhiên, quá trình thư giãn tâm thất đã xảy ra từ trước giai đoạn này. Đồng thời, có sự khác biệt về khả năng chịu gánh của tâm thất trái và thất phải, vì vậy thường có một khoảng trễ, van động mạch phổi vẫn mở mặc dù áp lực trong buồng thất phải đã giảm so với áp lực trong động mạch phổi. Sự suy giảm áp lực trong buồng thất là hiện tượng sinh lý chủ yếu trong thời kỳ tâm trương, dựa trên cơ sở này mà xây dựng các thông số đánh giá chức năng tâm trương. Các thông số bao gồm: tốc độ suy giảm áp lực tối đa (dP/dtMIN) hoặc các chỉ số liên quan nhằm mục đích làm giảm mức độ ảnh hưởng của yếu tố tiền gánh, hậu gánh và tần số tim.
- Khi áp lực trong buồng thất tiếp tục giảm dưới mức áp lực trong buồng nhĩ, van nhĩ thất được mở ra, bắt đầu quá trình đổ đầy thất. Giai đoạn đầu của quá trình đầy thất chủ yếu do áp lực trong buồng thất tiếp tục giảm; giai đoạn sau của thời kì tâm trương, yếu tố quan trọng nhất quyết định sự đổ đầy thất chính là tính chun giãn và đàn hồi của tâm thất; do đó các thông số bổ sung đánh giá chức năng tâm trương, chủ yếu dựa trên đặc điểm của giai đoạn đổ đầy.
Đường cong áp lực – thể tích tâm thất theo thời gian
Nghiên cứu các giai đoạn chu chuyển tim, không dừng lại ở sự quan sát sự biến đổi về thể tích và áp lực trong buồng thất để đánh giá chức năng tâm thất; sâu hơn nữa là nghiên cứu về đường cong áp lực – thể tích tâm thất theo thời gian của chu chuyển tim, để đánh giá hiệu quả của tương tác tâm thất và hệ mạch. Việc làm này được thực hiện dễ dàng hơn nhờ việc phát minh và sử dụng ống thông dẫn điện (conductance catheter).
Nghiên cứu về đường cong áp lực – thể tích mang lại rất nhiều thông tin hữu ích về chức năng tâm thu và tâm trương của tâm thất cũng như sự tương tác giữa tâm thất và hệ mạch.
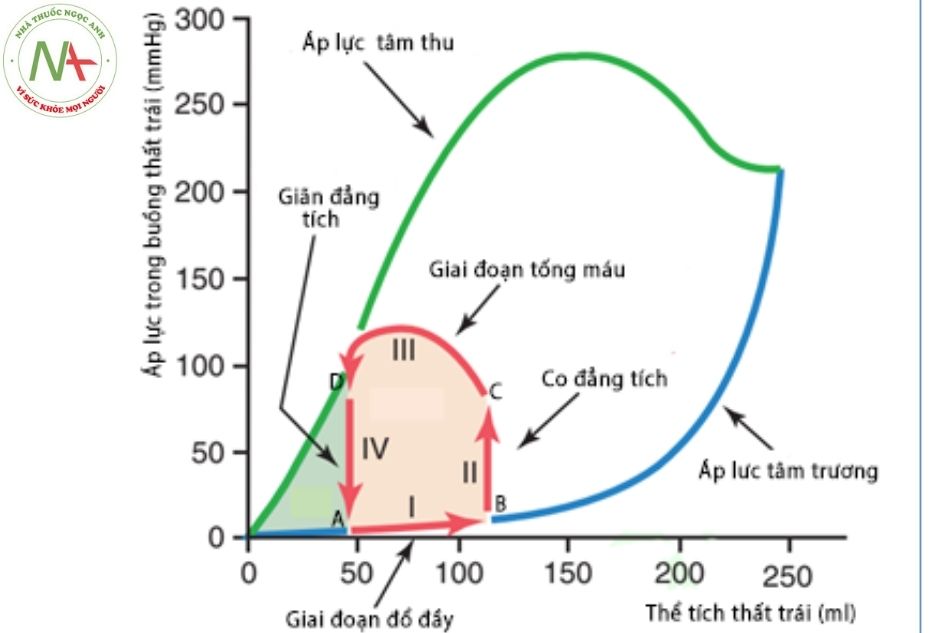
Quan sát đường cong áp lực – thể tích thất trái rút ra một số nhận xét quan trọng sau:
- Các điểm áp lực cuối tâm thu (điểm D – phía trên bên trái) sẽ có xu hướng tương quan tuyến tính với thể tích tâm thất trong điều kiện ổn định về khả năng co bóp cơ tim. Thực tế thì mối tương quan tuyến tính này tồn tại trong mọi thời điểm của chu chuyển tim, vì vậy co bóp cơ tim được đánh giá là tính đàn hồi thay đổi theo thời gian, trong đó tính đàn hồi đạt mức tối đa ở cuối giai đoạn tâm thu (EMAX – maximal elastane).
- Mối liên quan giữa thể tích và áp lực tâm thất trong thì tâm trương thể hiện khả năng thư giãn của tâm thất (compliance) (mối liên quan thể tích áp lực cuối tâm trương – EDPVR). Khi thể tích cuối tâm trương nhỏ hơn 150ml (điểm B – phía dưới bên phải), áp lực cuối tâm trương tâm thất không tăng đáng kể, cho phép dòng máu chảy dễ dàng từ nhĩ xuống thất. Khi thể tích cuối tâm trương tăng hơn 150ml, áp lực cuối tâm trương gia tăng nhanh chóng một phần do tổ chức xơ trong thành cơ tim không có khả năng giãn thêm nữa, đồng thời màng ngoài tim cũng đạt đến độ giãn gần tối đa.
- Tỷ lệ giữa áp lực cuối tâm thu và thể tích tống máu là một hằng số trong trạng thái ổn định của hậu gánh mạch máu; vì vậy đặc tính của hệ mạch máu có thể phản ánh trong một chỉ số gọi là độ đàn hồi hiệu quả của động mạch (Ea – effective arterial elastane).
Một số liên hệ chu chuyển tim trên lâm sàng
Liên hệ giữa điện tâm đồ với chu chuyển tim
Điện tâm đồ ở Hình 1 thể hiện các sóng P, Q, R, S và T là các điện thế phát sinh từ tim và được ghi lại bởi máy điện tim, đặt các điện cực trên bề mặt cơ thể.
Sóng P được tạo ra bởi sự lan truyền khử cực tâm nhĩ, tiếp theo là sự co bóp của tâm nhĩ, tương ứng đường cong áp lực tâm nhĩ sẽ đi lên nhẹ (áp lực tăng) tương ứng thời điểm ngay sau sóng P.
Khoảng 0,16 giây sau khởi phát sóng P, phức hợp sóng QRS xuất hiện do sự khử cực tâm thất gây co tâm thất và làm cho áp lực buồng thất bắt đầu tăng lên. Do vậy, phức hợp QRS bắt đầu ngay gần trước khi tâm thất bắt đầu thu.
Cuối cùng, sóng T của tâm thất mô tả giai đoạn tái cực của tâm thất, khi các sợi cơ tâm thất bắt đầu giãn. Do vậy, sóng T xuất hiện ngay trước khi kết thúc giai đoạn tâm thất co.
Liên hệ giữa tiếng tim và sự bơm máu của tim
Khi nghe tim bằng ống nghe, sẽ không nghe được tiếng mở các van do quá trình mở van diễn ra khá chậm, bình thường không tạo ra âm thanh nghe được. Tuy nhiên, khi van đóng, các lá van và máu xung quanh rung động do áp lực thay đổi đột ngột, tạo ra âm thanh truyền đi mọi hướng, lan tới lồng ngực, có thể nghe bằng ống nghe.
Khi tâm thất trái và tâm thất phải co, âm thanh đầu tiên nghe được là do đóng hai van nhĩ thất: tiếng tim trầm và tương đối dài được gọi là tiếng tim thứ nhất (T1).
Khi van động mạch chủ và van động mạch phổi đóng lại cuối thì tâm thu sẽ nghe thấy một tiếng thanh, ngắn do van đóng nhanh và sự rung động của các cấu trúc xung quanh trong một thời gian ngắn, gọi là tiếng tim thứ hai (T2).
Sự chuyển dịch công áp lực trong buồng thất thành công lưu lượng trong các đại động mạch
Công cung lượng của tim
Công thể tích nhát bóp (stroke work output) của tim là lượng năng lượng mà tim tạo ra trong mỗi nhát bóp để đẩy máu vào động mạch. Công cung lượng tim (minute work output) là năng lượng tổng cộng do hoạt động của tim tạo ra trong 1 phút, được tính bằng công thể tích nhát bóp nhân với tần số tim.
Công cung lượng tim được thể hiện dưới hai hình thức. Dạng thứ nhất chiếm phần lớn dùng để chuyển máu từ hệ tĩnh mạch áp lực thấp sang hệ động mạch áp lực cao. Dạng công này chính là công thể tích – áp lực (volume – pressure work) hay công ngoại sinh (EW – external work). Dạng thứ hai chiếm một phần nhỏ năng lượng dùng để gia tốc dòng máu đạt tới vận tốc tống máu qua van động mạch chủ và van động mạch phổi, gọi là thành phần năng lượng động học của dòng máu (kinetic energy of blood flow) trong công cung lượng tim.
Công ngoại sinh cung lượng tim thất phải thường bằng 1/6 so với công của thất trái, do áp lực tâm thu thất trái gấp khoảng 6 lần áp lực tâm thu thất phải. Phần công thêm vào của mỗi tâm thất để tạo năng lượng động học của dòng máu tỷ lệ với thể tích máu được tống đi trong mỗi nhát bóp nhân với bình phương vận tốc tống máu.
Thông thường, công cung lượng thất trái chỉ sử dụng 1% để tạo ra năng lượng động học của dòng máu, vì vậy có thể không đề cập đến trong phép tính toán công cung lượng tống máu. Tuy nhiên trong một số bệnh cảnh như trong trường hợp hẹp động mạch chủ (aortic stenosis), dòng máu qua chỗ hẹp có vận tốc rất lớn, có thể cần tới hơn 50% công cung lượng tim để tạo ra công động học của dòng máu.
Công cung lượng của tim
Để đánh giá đặc tính co cơ, cần xác định được áp lực trên cơ khi nó bắt đầu co gọi là tiền gánh và mức độ trở kháng mà cơ cần tạo ra lực co để vượt qua gọi là hậu gánh. Đối với cơ tim, tiền gánh (preload) chính là áp lực cuối tâm trương khi tâm thất được đổ đầy.
Hậu gánh (afterload) tâm thất chính là áp lực trong động mạch chủ được tâm thất đẩy vào.
Trong Hình 2, hậu gánh chính là áp lực cuối tâm thu thể hiện ở cuối đường cong pha III trong đường cong thể tích – áp lực (đôi khi hậu gánh được hiểu là sức cản trong hệ tuần hoàn động mạch hơn là áp lực).
Tầm quan trọng của việc hiểu khái niệm tiền gánh và hậu gánh chính là trong nhiều trạng thái bất thường về chức năng của tim và hệ tuần hoàn, một trong hai yếu tố: áp lực cuối tâm trương thất trái (tiền gánh), áp lực động mạch mà tâm thất phải vượt qua (hậu gánh) hoặc cả hai yếu tố tiền gánh và hậu gánh đều biến đổi rất nhiều so với trạng thái bình thường.
Sự dịch chuyển công từ áp lực trong tâm thất ra công dòng chảy trong mạch máu
Tâm thất co sinh công dưới dạng áp lực trong buồng thất làm mở van tổ chim, lúc này công ở dạng áp lực trong buồng thất sẽ chuyển thành công của lưu lượng dòng chảy trong động mạch chủ và động mạch phổi. Hiệu quả của việc chuyển đổi công này được quyết định phần lớn bởi đặc tính của hệ mạch máu.
Phương pháp truyền thống để đánh giá chức năng của hệ mạch chính là đo sức cản mạch phổi (pulmonary vascular resistance) và sức cản mạch máu hệ thống (systemic vascular resistance), hiện vẫn đang được áp dụng rộng rãi trong thực hành hàng ngày. Mặc dù chỉ số này có giá trị trong tiên lượng và định hướng điều trị, các phương pháp tính toán này dựa trên mô hình hệ tuần hoàn với sự hằng định của áp lực buồng thất, đồng thời hệ mạch máu được coi như những “ống cứng”. Trong thực tế, những đặc tính sinh lý của tim và mạch máu phức tạp hơn: tính đàn hồi của tâm thất thay đổi theo thời gian trong chu chuyển tim; hệ mạch máu với các đặc tính: trở kháng, sức cản và nguồn phản hồi năng lượng. Các yếu tố thành mạch này đều ảnh hưởng đến tâm thất trong thời kì tống máu.
Gần đây, người ta quan tâm nghiên cứu nhiều hơn về tương tác cặp đôi giữa tâm thất và hệ mạch máu vì bản chất mối liên quan này được coi là nền tảng quyết định hoạt động của hệ tuần hoàn trong các tình trạng bệnh lý. Tuy nhiên có nhiều thách thức trong quá trình tìm hiểu về tương tác giữa tâm thất và hệ mạch máu, trong đó có việc phải thiết kế được mô hình cặp đôi có đầy đủ các đặc tính của tâm thất và hệ mạch máu, đồng thời còn cần tính đến những thay đổi chức năng thống nhất trong các trạng thái sinh lý và sinh lý bệnh.
Trở kháng của hệ mạch (vascular resistance) đo tại một điểm phản ánh đặc tính của toàn bộ hệ mạch ở phía sau vị trí đo. Như vậy trở kháng đo ở động mạch chủ lên và thân động mạch phổi chính là hậu gánh của tâm thất trái và tâm thất phải. Trên cơ sở đặc điểm phức tạp của giường mạch máu và tính chất mạch đập của dòng chảy động mạch nên phổ của trở kháng thành mạch được biểu hiện dưới dạng tần số, trong khi hầu hết các thông số đánh giá chức năng tâm thất được đánh giá theo thời gian.
Một cách tiếp cận có thể áp dụng dựa trên mối liên quan về thể tích và áp lực. Trong cách tính toán này, các đặc tính mạch máu được thể hiện dưới dạng độ đàn hồi hiệu quả của động mạch (Ea) trong đó tỷ lệ giữa áp lực cuối tâm thu trong buồng thất và thể tích tống máu là một hằng số trong trạng thái ổn định của hậu gánh mạch máu. Khi đó chúng ta có thể sử dụng mô hình này để khảo sát mối liên quan giữa độ đàn hồi động mạch và độ đàn hồi tối đa của tâm thất cuối thì tâm thu (EMAX), nghiên cứu sự hòa hợp giữa tâm thất và các đặc tính thành động mạch, cũng như sự thay đổi về mức độ hòa hợp của mối quan hệ này trong trạng thái sinh lý và bệnh lý một cách đơn giản.
Ví dụ về mối liên quan về thể tích và áp lực: khi quan sát ở người bình thường có phân suất tống máu (ejection fraction) ≥ 60%, độ đàn hồi tối đa của tâm thất gấp 2 lần độ đàn hồi hiệu quả của thành động mạch. Mức tương quan này cho phép sự cân bằng tối ưu giữa công của tâm thất và tiêu thụ oxy cơ tim. Ở bệnh nhân suy tim mức trung bình, phân suất tống máu khoảng 40-50%, độ đàn hồi của tâm thất và động mạch trở nên cân bằng, tạo ra một thể tích tống máu tối ưu tại một thể tích cuối tâm trương nhất định (tuy nhiên sử dụng oxy kém hiệu quả hơn). Khi chức năng tâm thu thất trái suy giảm hơn nữa, phân suất tống máu giảm thêm, độ đàn hồi của tâm thất kém hơn so với độ đàn hồi của động mạch, nên không tạo được sự cân bằng tối ưu giữa công của tâm thất với cả lượng oxy tiêu thụ và thể tích tống máu.
Như vậy, ở trạng thái bình thường, sự hài hòa giữa tâm thất và mạch máu thể hiện ở chuyển hóa đạt hiệu quả tối đa (công sinh ra và oxy tiêu thụ). Khi chức năng tim giảm, mối liên quan cặp đôi không đạt mức tối ưu với mục tiêu duy trì thể tích tống máu trong điều kiện chức năng tim giảm. Khi chức năng tim giảm hơn nữa, cơ chế bù trừ không còn đảm bảo, có sự mất tương quan cặp đôi giữa tâm thất và mạch máu gây sụt giảm cả thể tích tống máu và hiệu quả chuyển hóa.
Một mô hình khác đánh giá tương tác cặp đôi giữa tâm thất và hệ mạch máu dựa theo thời gian, được xây dựng bởi Parker và cộng sự, còn được gọi là phương pháp đặc thù (method of characteristics). Trong công thức, tim truyền năng lượng vào hệ tuần hoàn dưới dạng các sóng di chuyển thuận chiều (đè ép và giãn nở) cho phép điều chỉnh dòng chảy và áp lực trong hệ mạch. Hệ mạch là nơi nhận sóng (chỗ chia đôi và hệ vi mạch) di chuyển ngược về phía tim. Sự tương tác giữa các sóng di chuyển xuôi chiều và ngược chiều tạo nên một đồ thị phức hợp về sự khuếch đại áp lực và dòng chảy tại các thời điểm khác nhau trong chu chuyển tim và tại các điểm khác nhau trong hệ tuần hoàn. Mô hình này được áp dụng để nghiên cứu về dòng chảy trong tuần hoàn phổi thời kì bào thai và đánh giá tương quan cặp đôi thất – mạch máu ở những trường hợp sửa tái tạo quai động mạch chủ.
==>>Xem thêm: Giải phẫu tim và mạch máu lớn – Lâm sàng tim bẩm sinh
Điều hòa dòng chảy trong hệ tuần hoàn hệ thống
Điều hòa theo cơ chế thần kinh trung ương
Điều hòa theo cơ chế thần kinh đóng vai trò quan trọng trong việc điều hòa ngay lập tức huyết áp động mạch và những thay đổi nhanh chóng về lưu lượng cục bộ trong các trạng thái căng thẳng cấp tính. Điều hòa nhanh theo cơ chế thần kinh được thực hiện thông qua các cung phản xạ (reflex arc) bao gồm: sợi hướng tâm dẫn truyền thông tin từ các vị trí tiếp nhận về trung khu xử lý thông tin ở hành tủy, các hoạt động điều hòa sẽ theo sợi ly tâm của hệ thần kinh thực vật tạo nên sự thay đổi về trương lực thành mạch.
Các sợi hướng tâm điều hòa theo cơ chế thần kinh mạnh nhất nằm ở các thụ cảm thể nhận cảm (receptor) cơ học ở xoang cảnh và quai động mạch chủ, đáp ứng với những thay đổi về áp lực động mạch – gọi là thụ cảm thể áp lực (pressure receptor). Ít nhất có 2 loại thụ cảm thể được đề cập là thụ cảm thể kiểm soát những thay đổi động của huyết áp và thụ cảm thể đáp ứng với kiểm soát huyết áp trạng thái nghỉ. Thay đổi về áp lực tại các thụ thể tiếp nhận sẽ theo các xung động hướng tâm trở về trung khu điều hòa tim và thành mạch ở hành não, tạo ra các tín hiệu điều hòa đi theo các xung động ly tâm. Cung phản xạ điều hòa trong trường hợp huyết áp tăng sẽ kích thích xoang cảnh, làm giảm nhịp tim, giãn mạch, đưa huyết áp về giá trị ban đầu. Các thụ cảm thể nhận cảm áp lực được chi phối bởi các sợi ly tâm của hệ thần kinh giao cảm, vì vậy hoạt động thần kinh giao cảm có thể điều khiển mức độ đáp ứng của thụ thể áp lực. Thụ cảm thể áp lực tại xoang cảnh có ảnh hưởng đáng kể trên huyết áp, nên đã có những hướng nghiên cứu về khả năng kích thích liên tục xoang cảnh để điều trị các trường hợp tăng huyết áp kháng trị.
Thụ cảm thể áp lực còn được tìm thấy ở thành tâm nhĩ và tâm thất. Các thụ thể này nằm trên thành hai buồng nhĩ ở vị trí nối giữa tĩnh mạch và tâm nhĩ; nằm rải rác ở tâm thất, vách liên thất. Có hai thụ thể nhĩ: thụ thể loại A phát xung động trong thì tâm nhĩ co lại, đáp ứng với những thay đổi áp lực của tâm nhĩ, thụ thể loại B phát xung trong thì tâm thất co, đáp ứng với những thay đổi về thể tích tâm nhĩ. Một cách cụ thể, các thụ thể tâm nhĩ điều hòa thể tích lòng mạch thông qua đồng thời hoạt động thần kinh giao cảm tới hệ mạch thận và theo cơ chế thể dịch. Hai loại thụ thể áp lực trong cơ tâm thất bao gồm: loại thứ nhất phát xung từng lúc theo chu chuyển tim với số lượng ít; loại thứ hai đáp ứng với các kích thích cơ học và hóa học khác nhau thông qua sợi trục thần kinh không myelin gọi là sợi C. Kích thích sợi C thông qua vai trò kích thích hệ phó giao cảm và ức chế hệ giao cảm gây huyết áp tụt và nhịp chậm.
Các thụ cảm thể hóa học (chemoreceptors) tập trung ở hành cảnh, quai ĐMC, não, mạch vành, mô cơ và phổi cũng gây các kích thích hướng tâm điều hòa hoạt động hệ tuần hoàn thông qua cơ cơ chế thần kinh. Các thụ thể này phát huy vai trò điều hòa tuần hoàn hô hấp rõ rệt trong trạng thái thiếu oxy và tăng khí CO2 máu.
Trung tâm điều hòa hoạt động của hệ tuần hoàn theo cơ chế thần kinh quan trọng nhất là hành não. Hoạt động của hành não lại được điều hòa bởi vùng dưới đồi.
Cơ chế trung tâm ở hành tủy điều hòa hoạt động của hệ thần kinh giao cảm và phó giao cảm, các sợi thần kinh ly tâm kiểm soát hệ tuần hoàn. Bộ phận nhận xung động ly tâm đầu tiên là các sợi thần kinh giao cảm co mạch, khi bị kích thích sẽ giải phóng ra norepinephrine từ các tận cùng thần kinh. Các chất khác cũng được giải phóng ra bao gồm: các monoamin, polypeptide, purine và các amino acid; một số chất có tác dụng hoạt mạch trực tiếp, một số khác lại thông qua việc điều hòa sự giải phóng norepinephrine. Các xung động trong sợi co mạch góp phần duy trì trương lực mạch máu bình thường hoặc trạng thái co mạch cơ bản, được coi là cơ chế chính điều hòa huyết áp trong trạng thái không bị căng thẳng. Các sợi co mạch khá thường gặp trong hệ cơ vân là nơi trương lực nội tại khá cao ở trạng thái nghỉ ngơi. Các sợi co mạch ít hơn ở hệ mạch não và mạch vành. Co thắt hệ tĩnh mạch qua trung gian giao cảm điều hòa trương lực tĩnh mạch và thể tích tuần hoàn.
Kích thích thần kinh giao cảm cũng có thể gây giãn mạch. Chất dẫn truyền trong sợi giãn mạch là acetylcholine (ở loài linh trưởng nó có thể là epinephrine). Các sợi giãn mạch có thể gây tăng trước lưu lượng dòng máu tới cơ xương. Tuy nhiên khi bắt đầu có hoạt động co cơ, điều hòa giãn mạch tại chỗ sẽ đóng vai trò quan trọng hơn.
Hệ thần kinh phó giao cảm chủ yếu kiểm soát chức năng tim và tần số tim, có tác dụng rất khiêm tốn kiểm soát tuần hoàn ngoại vi thông qua việc giải phóng acetylcholine. Các sợi phó giao cảm gây giãn mạch tìm thấy ở tuần hoàn não và tuần hoàn mạch vành, cũng như ở bàng quang, trực tràng và cơ quan sinh dục ngoài.
Điều hòa theo cơ chế thể dịch trung ương
Là một cơ chế điều hòa bổ trợ mạnh mẽ đối với chức năng hệ mạch máu thông qua nồng độ các hormon hoạt mạch lưu hành trong hệ tuần hoàn bao gồm: catecholamin, angiotensin II, vasopressin, eicosanoid, nitric oxide và peptides.
Các tế bào cơ trơn thành mạch có rất nhiều thụ thể với catecholamin. Các thụ thể này đồng thời đáp ứng với: catecholamin sản xuất tại chỗ, nguồn gốc từ hoạt hóa thần kinh giao cảm tại chỗ; catecholamin nội sinh lưu hành do tuyến thượng thận sản xuất ra và các thuốc giống giao cảm ngoại sinh đưa vào. Kích thích các thụ thể α adrenergic gây co mạch, kích thích thụ thể β adrenergic gây giãn mạch.
Hoạt chất angiotensin II được sinh ra từ hệ thống renin – angiotensin – aldosteron, gây đáp ứng co mạch mạnh. Tại thận, hệ thống ống lượn xa bài tiết renin đáp ứng với tình trạng giảm tưới máu động mạch thận hoặc giảm thể tích dịch ngoại bào. Renin sẽ chuyển angiotensinogen thành angiotensin I, tiếp tục được chuyển thành angiotensin II nhờ vai trò của enzym chuyển – được tạo ra chủ yếu ở phổi và nội mạc thành mạch. Chất angiotensin II vừa là chất gây co mạch trực tiếp, đồng thời còn kích thích vùng dưới đồi tổng hợp hormon chống bài niệu là vasopressin.
Các peptide lợi niệu thải natri cũng là nhóm hormon tham gia điều hòa sinh lý hệ tuần hoàn hệ thống. Có ít nhất 3 loại peptide bài niệu liên quan với natri: ANP (atrial natriuretic peptide), BNP (B type Natriuretic peptide) và CNP. ANP được giải phóng chủ yếu từ tế bào cơ tâm nhĩ, đáp ứng với kích thích gây căng giãn tâm nhĩ; ANP cũng được tế bào cơ tâm thất giải phóng với một tỷ lệ nhỏ. ANP gây giãn mạch và ức chế cơ tim, tại thận gây giảm hấp thu natri ở ống thận. ANP lưu hành trong máu tăng trong một số bệnh lý nhất định như bệnh tim bẩm sinh có tăng áp lực tâm nhĩ, suy tim sung huyết, bệnh van tim, tăng huyết áp, bệnh động mạch vành và rối loạn nhịp nhĩ.
BNP được bài tiết bởi tâm thất và tâm nhĩ đáp ứng với tình trạng quá tải về thể tích và áp lực với cùng cơ chế như chất ANP. BNP được sử dụng như một dấu ấn trong hệ tuần hoàn để đánh giá trong nhiều bệnh lý tim mạch. CNP có tác dụng tại chỗ hơn, được tạo ra trong tế bào nội mạc mạch vành và mạch tạng gây tác dụng giãn mạch tạng.
Điều hòa hệ tuần hoàn theo cơ chế tại chỗ
Nội mạc mạch máu đóng vai trò quan trọng điều hòa trương lực thành mạch nhờ việc các tế bào cơ trơn bài tiết ra các chất trung gian gây co mạch và gây giãn mạch. Các chất trung gian gây giãn mạch có nguồn gốc nội mạc bao gồm: nitric oxide (NO), prostacyclin (PGI2), adenosin và yếu tố gây tăng tái cực nguồn gốc nội mạc (EDHF – endothelial derived hyperpolarizing factor). Cấu trúc của EDHF chưa được xác định tuy nhiên nó có liên quan với CNP, kích thích giãn mạch bằng tăng tái cực cơ trơn thành mạch thông qua kênh K+. Một số chất gây co mạch có nguồn gốc nội mạc như: endothelin -1, gây tác dụng hoạt mạch phức hợp phụ thuộc vào vị trí và loại thụ thể tác động vào; angiotensin II. Gần đây một chất mới được quan tâm nghiên cứu là urotensin vừa có tác dụng gây co mạch, vừa có tác dụng gây giãn mạch.
Điều hòa theo cơ chế chuyển hóa: dòng chảy tới các mô cơ thể được điều hòa bởi những thay đổi về nhu cầu chuyển hóa tại chỗ. Ví dụ: Giảm phân áp oxy, tăng phân áp CO2 hoặc tăng nồng độ ion H+ hoặc ion K+ gây giãn tiểu động mạch không phụ thuộc vào chức năng nội mạc. Các tế bào khác ngoài tế bào nội mạc cũng có khả năng giải phóng ra chất gây giãn mạch hiệu lực cao như adenosin đáp ứng với tình trạng tăng chuyển hóa hoặc giảm áp lực oxy.
Điều hòa tại chỗ bởi tế bào hồng cầu: ngày càng nhận được nhiều quan tâm hơn. Cơ chế tương tự điều hòa theo cơ chế chuyển hóa. Sự xuất hiện của hemoglobin khử dẫn tới giải phóng các chất gây giãn mạch không hoặc có phụ thuộc vào nội mạc như: ATP (adenosine triphosphate) và NO (nitric oxide).
Điều hòa tại chỗ bằng cơ chế tự điều hòa: Khả năng tự điều hòa dòng chảy ổn định trong điều kiện dao động lớn về huyết áp của một số tạng là vô cùng quan trọng, khi bản thân tạng đó không có khả năng thay đổi đáng kể về chuyển hóa đáp ứng với tình trạng tụt huyết áp. Hiện tượng này gọi là cơ chế tự điều hòa. Cơ chế của hiện tượng tự điều hòa khác nhau giữa các giường mạch máu. Hiện tượng tự điều hòa là các đáp ứng nội tại của các tế bào cơ trơn thành mạch gây co tiểu động mạch độc lập với cơ chế nội mạch, đáp ứng với những thay đổi về áp lực xuyên thành mạch máu. Hiện tượng này xảy ra do sự tương tác giữa các integrin trên bề mặt tế bào và các protein lưới ngoại bào và sự thay đổi về dòng canxi. Các yếu tố góp phần bao gồm: sự thay đổi sản xuất các yếu tố chuyển hóa, trương lực giao cảm, và tín hiệu phản hồi từ hệ thống ống thận – cầu thận.
Điều hòa lưu lượng tuần hoàn phổi
Thể tích máu lưu hành trong hệ tuần hoàn phổi tương tự tuần hoàn hệ thống. Tuy nhiên có một số điểm khác biệt mấu chốt về sinh lý tuần hoàn phổi so với tuần hoàn hệ thống:
- Sự khác biệt căn bản về hậu gánh: hệ tuần hoàn phổi là hệ tuần hoàn áp lực thấp, sức cản thấp; với áp lực động mạch phổi trung bình ở người trưởng thành bình thường là 15 mmHg, so với áp lực động mạch trung bình của tuần hoàn hệ thống là 90
- Sự khác biệt về đặc điểm cấu trúc và chức năng của 2 hệ tuần hoàn: Trong tuần hoàn hệ thống, tính đàn hồi của hệ tuần hoàn do động mạch chủ và các nhánh mạch máu lớn đảm nhiệm, sức cản hệ tuần hoàn chủ yếu là vai trò của các động mạch và tiểu động mạch ngoại vi; đối với tuần hoàn phổi tính đàn hồi và sức cản phân bố trên toàn bộ hệ mạch. Điều này dẫn đến sự khác biệt căn bản giữa huyết áp tâm thu và tâm trương trong tuần hoàn hệ thống so với tăng áp lực động mạch phổi, đồng thời giải thích cho mối liên quan chặt chẽ giữa tính đàn hồi và sức cản hệ tuần hoàn phổi. Một hiện tượng đặc thù nữa của tuần hoàn phổi là khả năng điều hòa thụ động và tái phân bố mạch máu phổi để điều hòa áp lực động mạch phổi.‐ Ảnh hưởng của sự thay đổi phân áp oxy máu cũng khác biệt giữa tuần hoàn phổi và tuần hoàn hệ thống.
Khả năng chịu tải, độ đàn hồi và sức cản động mạch phổi
Hai thành phần quan trọng của hậu gánh tuần hoàn là độ đàn hồi (stiffness) và sức cản (resistance) của giường mạch máu. Hệ tuần hoàn phổi với đặc điểm: thân và hai nhánh động mạch phổi chỉ đóng góp 15%-20% tổng độ đàn hồi hệ mạch phổi, còn lại là vai trò của các mạch máu nhỏ ngoại vi. Như vậy đối với hệ tuần hoàn phổi, có mối liên quan chặt chẽ giữa sức cản và độ đàn hồi. Điều này làm nên sự khác biệt của tuần hoàn phổi:
(1) Mối tương quan tuyến tính giữa áp lực ĐMP tâm thu, tâm trương với áp lực ĐMP trung bình;
(2) Huyết áp hiệu số của hệ tuần hoàn phổi thường xấp xỉ bằng áp lực động mạch phổi trung bình trong khi ở hệ tuần hoàn hệ thống huyết áp hiệu số chỉ bằng khoảng 40% huyết áp trung bình;
(3) Giới hạn của tăng áp động mạch phổi (pulmonary arterial hypertension) tương đối rộng khi so sánh với tăng huyết áp hệ thống (hypertension).
Điều hòa thụ động trương lực thành mạch phổi và sự huy động mạch máu
Hệ tuần hoàn phổi có khả năng huy động nhanh các mạch máu nhỏ “không hoạt động” trong trạng thái bình thường để duy trì được hệ tuần hoàn áp lực thấp trong trạng thái có tăng lưu lượng tuần hoàn. Khi lưu lượng tuần hoàn tăng, các mạch máu nhỏ được mở thêm làm giảm sức cản chung của hệ mạch máu phổi, duy trì áp lực động mạch phổi ổn định ở mức thấp, ngay cả khi có tăng đáng kể cung lượng tim.
Vai trò của áp lực trong lồng ngực
Đặc điểm huyết động của tuần hoàn phổi được điều hòa bởi hoạt động hô hấp và áp lực âm trong lồng ngực thông qua một số cơ chế. Hoạt động hô hấp làm thay đổi pH máu, áp lực oxy trong phế nang và thể tích phổi dẫn tới thay đổi sức cản mạch phổi. Tình trạng kiềm hô hấp và kiềm chuyển hóa gây giãn mạch phổi, ngược lại tình trạng toan hóa gây co mạch phổi. Tình trạng thiếu oxy phế nang gây co tiểu động mạch phổi, giúp tái phân bố lưu lượng máu tới các vùng phế nang giàu oxy hơn giúp tăng cường sự hòa hợp thông khí, tưới máu đảm bảo máu được oxy hóa tốt hơn.
Thay đổi áp lực trong lồng ngực và thể tích phổi ảnh hưởng trực tiếp đến sức cản mạch phổi. Với cách tiếp cận này thì vai trò của chênh áp xuyên phổi (chênh lệch áp lực giữa phế nang và khoang màng phổi) và những thay đổi của thể tích phế nang quan trọng hơn áp lực trong lồng ngực. Dung tích cặn chức năng (FRC – functional residual capacity) là thể tích phổi tại đó sẽ tạo ra một thể tích khí lưu thông trong trạng thái bình thường. Ở thể tích phổi mức dung tích cặn chức năng, sức cản mạch phổi là thấp nhất.
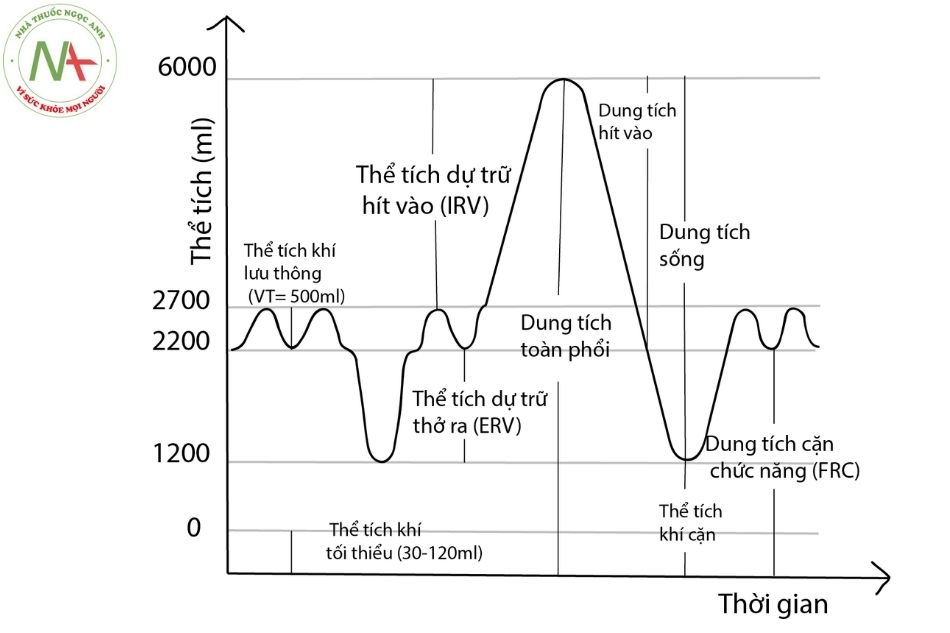
(Nguồn: Guyton and Hall Textbook of Medical Physiology, 2016)
Giường mạch máu phổi bao gồm các mạch máu phế nang và mạch máu ngoài phế nang. Mạch máu phế nang nằm ở các vách liên phế nang, áp lực phế nang là áp lực bao quanh các tiểu động mạch, mao mạch và tĩnh mạch. Trái lại các mạch máu ngoài phế nang tập trung ở khoảng kẽ và tiếp xúc với áp lực khoang màng phổi.
Khi thể tích phổi giảm dưới mức dung tích cặn chức năng, khoảng kẽ giảm thể tích làm giảm diện tích cắt ngang của mạch máu ngoài phế nang. Thể tích phổi giảm, xẹp phế nang cũng gây co mạch phổi đáp ứng với thiếu oxy lại làm tăng thêm sức cản mạch ngoài phế nang. Mặc dù sức cản mạch máu phế nang có thể giảm do giảm áp lực phế nang nhưng sức cản chung của mạch máu phổi vẫn tăng lên khi giảm thể tích phổi. Ngược lại khi thể tích phổi tăng vượt quá dung tích cặn chức năng cũng gây tăng sức cản mạch phổi do các phế nang giãn gây đè ép vào các mạch máu phế nang.
Một ảnh hưởng khác của áp lực trong lồng ngực lên hệ mạch máu phổi là khả năng xẹp lại khi áp lực lòng mạch thấp. Dòng chảy trong các mạch máu phổi bị ảnh hưởng bởi 4 yếu tố: áp lực động mạch phổi (Ppa); áp lực tĩnh mạch phổi (Ppv), áp lực phế nang bao quanh mạch máu (PA: pressure alveolar) và tính đàn hồi thành mạch.
Tác giả West đã chia phổi thành ba vùng lý thuyết đi từ đỉnh phổi xuống đáy phổi (Hình 5.5) khi ở tư thế đứng: vùng đỉnh phổi (vùng 1), vùng giữa phổi (vùng 2) và vùng đáy phổi (vùng 3). Các dòng chảy mạch phổi ở từng vùng như sau:
- Tại vùng đáy phổi (vùng 3), áp lực phế nang thấp hơn áp lực tĩnh mạch phổi nên lưu lượng máu chảy trong tuần hoàn phổi tỷ lệ với chênh lệch áp lực giữa động mạch phổi và tĩnh mạch phổi (Q ~ (Ppa – Ppv)).
- Tại vùng giữa phổi (vùng 2), áp lực phế nang cao hơn áp lực tĩnh mạch phổi làm gia tăng sức cản với dòng máu phổi, khi đó lưu lượng máu phổi tỷ lệ với chênh lệch áp lực giữa động mạch phổi và áp lực phế nang (Q ~ (Ppa – PA)).
- Tại vùng đỉnh phổi (vùng 1) là nơi áp lực phế nang cao hơn cả áp lực động mạch phổi làm đóng các mạch máu phổi và sức cản với dòng máu phổi rất lớn.
- Sau này, người ta cũng đã mô tả thêm một vùng nữa, vùng 4, trong đó lưu lượng máu phổi giảm ở phần tận đáy của phổi. Sự giảm này xảy ra là do tác động trọng lượng phổi lên mạch máu ngoài phế nang và mạch máu góc. Trọng lượng phổi sẽ chèn ép làm tăng sức cản và giảm thông khí ở vùng đáy làm gây nên các vùng thiếu oxy tương đối và do vậy đưa đến tình trạng co mạch phổi do hạ oxy.
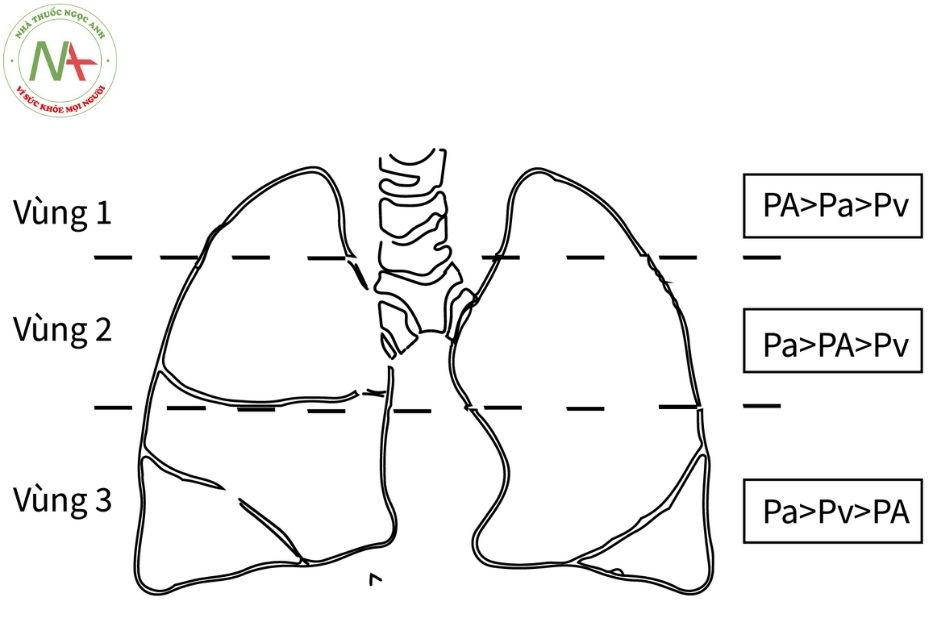
Trong trạng thái bình thường, vùng đỉnh phổi thường “không tồn tại”, lưu lượng máu phổi chủ yếu được quyết định bởi vùng 3. Khi áp lực phế nang phổi tăng cao đi kèm với giảm cung lượng tim và giảm áp lực động mạch phổi, vùng 1 có thể được mở rộng thêm như trong trường hợp giảm thể tích tuần hoàn. Trái lại trong trường hợp suy tim sung huyết, tăng áp lực tĩnh mạch phổi (Ppv) thì tăng áp lực phế nang cũng có thể không tạo khoảng chết phế nang.
Đặc biệt quan trọng đối với hồi sức bệnh nhân tim bẩm sinh (đặc biệt ở trẻ em) là ảnh hưởng của thông khí áp lực dương với mức áp lực đỉnh thở vào cao.
Tăng áp lực phế nang có thể làm giãn vùng 2 và cho phép vùng 1 thực sự hiện diện làm bất xứng thông khí/tưới máu tạo luồng thông (shunt) trong phổi gây hạ oxy máu và tăng carbonic. Tương tự, viêm phổi và phù phổi cấp có thể làm tăng vùng 4. Cuối cùng, hạ huyết áp do các nguyên nhân khác nhau có thể tăng vùng 1 và vùng 2.
Điều hòa tại chỗ cung lượng tuần hoàn phổi bởi yếu tố nội mạc
Việc phát hiện ra vai trò của yếu tố nội mạc có thể được coi là một phát minh vĩ đại trong sinh lý học tuần hoàn 25 năm qua. Nội mạc có khả năng sản sinh ra rất nhiều chất trung gian điều hòa chức năng cơ trơn thành mạch bao gồm cả tuần hoàn phổi. Các chất trung gian này cũng có vai trò chủ đạo điều hòa sự tạo ra các biến đổi về cấu trúc góp phần vào tiến triển bệnh mạn tính như trong trường hợp tăng áp động mạch phổi.
Những hiểu biết này là cơ sở của những phát kiến trong điều trị bệnh nhân với các tình trạng bệnh lý tăng áp động mạch phổi với các dược chất: đối kháng endothelin dạng uống, ức chế phosphodi- esterase và các prostanoid dạng khí dung và dạng truyền tĩnh mạch.
Điều hòa tuần hoàn phổi thông qua yếu tố thần kinh và thể dịch trung ương
Giường mạch máu phổi có sự phân bố dày đặc các tận cùng thần kinh giao cảm. Hoạt động của hệ thần kinh giao cảm thông qua các xung động hướng tâm truyền về từ các thụ cảm thể hóa học nhận cảm với tình trạng giảm oxy, cũng như tín hiệu từ các hormon lưu hành trong máu như angiotensin II, gây tăng sức cản thành mạch.
Điều hòa thông qua phân áp oxy
Đáp ứng của hệ mạch máu phổi với thay đổi phân áp oxy diễn ra theo chiều hướng ngược với đáp ứng của hệ tuần hoàn hệ thống: giảm phân áp oxy gây co mạch phổi, giúp dòng tuần hoàn phổi được phân bố tới nơi giàu trao đổi oxy hơn đảm bảo sự cân bằng giữa thông khí và tưới máu. Hiện tượng co mạch phổi đáp ứng với tình trạng thiếu oxy được nghiên cứu chi tiết trên động vật thực nghiệm, ở tế bào nội mạc động mạch phổi cô lập và tế bào cơ trơn mạch phổi. Kết quả nghiên cứu chỉ ra chính áp lực oxy trong lòng phế nang hơn là trong lòng mạch gây ra ảnh hưởng đáng kể đến co mạch phổi. Tuy nhiên cơ chế chính xác mức độ tế bào của đáp ứng này vẫn chưa được hiểu rõ và hiện tại cũng chưa có đầy đủ nghiên cứu trên người để trả lời câu hỏi này.
Cặp đôi giữa tuần hoàn và chuyển hóa mô
Theo nhận xét của Claude Bernard – nhà sinh lý vĩ đại người Pháp: “Tất cả các cơ chế của sự sống, tuy có khác nhau về cách thể hiện nhưng chỉ để phục vụ một mục đích duy nhất: đảm bảo sự hằng định của nội môi trong cơ thể sống”.
Vai trò sống còn của hệ tuần hoàn là đảm bảo lưu lượng tuần hoàn cung cấp đủ oxy cho nhu cầu chuyển hóa bình thường của cơ thể. Cơ thể sống khỏe mạnh luôn đạt được sự cân bằng giữa tiêu thụ oxy hệ thống và khả năng vận chuyển oxy, ngoại trừ trường hợp hoạt động thể lực khỏe mạnh. Trong những tình trạng bệnh lý nặng, việc cung cấp không đủ oxy có sự ảnh hưởng đáng kể đối với chuyển hóa: trong trạng thái suy tim nặng, hệ tuần hoàn không duy trì được nồng độ oxy vận chuyển tương xứng với mức độ tăng tiêu thụ oxy như trong nhiễm khuẩn nặng. Tuy nhiên đối với các tình trạng giảm nhu cầu oxy như trạng thái ngủ đông, mô cơ thể có thể thích nghi với tình trạng giảm cung lượng tuần hoàn và giảm vận chuyển oxy trong nhiều tháng.
Khả năng vận chuyển oxy được tính toán thông qua nồng độ oxy trong máu động mạch và cung lượng tim. Mức độ tiêu thụ oxy tính toán dựa trên sự chênh lệch nồng độ oxy động tĩnh mạch và cung lượng tim. Sinh lý hệ tuần hoàn đóng vai trò trung tâm duy trì mối quan hệ cân bằng giữa cung cấp và tiêu thụ oxy.
Mối liên quan giữa vận chuyển và tiêu thụ oxy hệ thống
Trên thực tế, khi cung lượng tim giảm đáng kể dẫn tới việc giảm cung cấp oxy cũng không làm ảnh hưởng quá nhiều tới mức oxy tiêu thụ và vẫn đảm bảo được chuyển hóa ở mô. Có hai cơ chế duy trì mức tiêu thụ oxy ổn định trong hoàn cảnh cung cấp oxy bị giảm là: (1) Tăng khả năng sử dụng oxy tại mô và (2) chức năng tự điều chỉnh của cơ quan duy trì lưu lượng ổn định tại chỗ ngay cả khi có giảm lưu lượng tuần hoàn tổng thể. Các cơ chế tự điều chỉnh sẽ đáp ứng được một mức độ nhất định. Khi vận chuyển oxy giảm quá thấp dưới ngưỡng cho phép, các cơ chế bù trừ không đáp ứng đủ gây mất cân bằng nội môi.
Mối liên quan giữa vận chuyển và tiêu thụ oxy hệ thống sau phẫu thuật tim
Sự thay đổi trong sử dụng và vận chuyển oxy ở người trưởng thành ngay sau mổ tim đã được nghiên cứu và mô tả chi tiết. Trường hợp điển hình: vận chuyển oxy giảm phản ánh tình trạng giảm cung lượng tim sau mổ, hiện tượng tăng tiêu thụ oxy có thể do tăng nhiệt độ hoặc tăng đáp ứng viêm hệ thống.
Trong một nghiên cứu ở trẻ em, trong những giờ đầu sau mổ tim, người ta quan sát thấy mức độ tiêu thụ oxy ngay sau mổ không liên quan tới thời gian chạy tim phổi nhân tạo hay kẹp động mạch chủ. Trong các giờ tiếp sau, lượng oxy tiêu thụ thay đổi liên quan chặt chẽ với thay đổi nhiệt độ trung tâm cơ thể. Mức độ tiêu thụ oxy tăng dần trong quá trình này tương quan song song chặt chẽ với sự thay đổi của lượng oxy vận chuyển.
Trên nền tảng chuyển hóa với vai trò đảm bảo chức năng mô, người ta dự đoán những thay đổi trong cân bằng giữa tiêu thụ oxy và vận chuyển oxy có thể dự báo tiên lượng của trẻ sau phẫu thuật tim. Một nghiên cứu phẫu thuật tim sơ sinh rút ra kết luận: tỷ lệ sử dụng oxy hệ thống nhiều hơn 50% trong 6h đầu sau mổ có tiên lượng nguy cơ cao hơn. Một số nghiên cứu khác mặc dù không mô tả được mối liên hệ giữa oxy vận chuyển hay oxy tiêu thụ và nguy cơ xảy ra biến cố, nhưng đã chỉ ra tăng nồng độ lactate huyết thanh là một yếu tố gợi ý biến cố xảy ra sau đó.
Vận chuyển và tiêu thụ oxy hệ thống ở bệnh nhân tim một tâm thất chức năng
Bệnh nhân một tâm thất chức năng có nguy cơ cao mắc hội chứng cung lượng tim thấp, tương quan giữa tiêu thụ và vận chuyển oxy bị ảnh hưởng. Đồng thời tình trạng này lại trở nên phức tạp hơn khi đo đạc các thông số lâm sàng tương quan ở hai hệ tuần hoàn.
Ở nhóm bệnh nhân sau phẫu thuật Norwood, mối quan hệ giữa vận chuyển và tiêu thụ oxy càng bị cản trở hơn do nồng độ oxy máu tĩnh mạch, khi độ bão hòa oxy dưới 30% sẽ xảy ra tình trạng chuyển hóa yếm khí và bão hòa oxy mức 40% sẽ có khiếm khuyết về phát triển thần kinh ở trẻ sống.
Thay đổi vận chuyển oxy hệ thống trong quá trình truyền catecholamin
Ở những bệnh nhân nặng cần hồi sức đã có sự mất cân bằng về vận chuyển và tiêu thụ oxy, mục tiêu quan trọng của điều trị là tăng khả năng vận chuyển oxy của tuần hoàn hệ thống thông qua cách làm tăng cung lượng tim dưới tác dụng của truyền catecholamin. Truyền catecholamin làm tăng cung lượng tim đã được chứng minh ở bệnh nhân người trưởng thành. Tuy nhiên catecholamin cũng làm tăng chuyển hóa, do đó làm tăng tiêu thụ oxy.
Với nhóm bệnh nhân khác nhau, vai trò catechol- amine với vận chuyển và tăng tiêu thụ oxy là khác nhau. Ở người trưởng thành, truyền catecholamine làm tăng tiêu thụ oxy nhiều hơn tăng khả năng vận chuyển oxy. Tuy nhiên ở trẻ sơ sinh lại không giống như vậy: ở trẻ sơ sinh, truyền catecholamin còn có tác dụng tạo nhiệt thông qua tác dụng của thuốc trên mô mỡ nâu của trẻ em. Vì vậy nghiên cứu trên cừu sơ sinh khỏe mạnh, truyền dobutamine liều cao làm tăng đáng kể sự tiêu thụ oxy vượt hơn nhiều so với tăng khả năng vận chuyển oxy. Ngoài ra ở bệnh nhân sau phẫu thuật Norwood, dopamine làm tăng tiêu thụ oxy hệ thống nên ngừng truyền sẽ giúp cải thiện cân bằng giữa tiêu thụ và vận chuyển oxy. Những bằng chứng này nhấn mạnh tầm quan trọng của việc cần phải đánh giá rộng hơn ảnh hưởng lâm sàng của bất kì dược chất nào trên hệ tim mạch hơn là chỉ tập trung vào cung lượng tim, trước khi quyết định có lựa chọn sử dụng thuốc hay không.
Sinh lý tuần hoàn thai nhi
Những hiểu biết hiện tại của y học về sinh lý hệ tuần hoàn trong giai đoạn phôi thai bao gồm: sự hình thành các buồng tim, đặc điểm huyết động, độ bão hòa oxy, hoạt động của tâm thất và sự phân bố cung lượng tim trong thời kỳ thai nhi, phần lớn dựa vào nghiên cứu thực hiện trên bào thai cừu do đặc tính tương tự của tuần hoàn bào thai cừu so với tuần hoàn bào thai người.
Vòng tuần hoàn thai nhi được cấu thành từ bốn dòng nối thông lần lượt là:
- Trong bánh rau.
- Qua ống tĩnh mạch rốn (nối với tĩnh mạch chủ dưới).
- Lỗ bầu dục (yếu tố thiết yếu góp phần đổ đầy thất trái trong giai đoạn bào thai).
- Ống động mạch (phần lớn dòng máu đi từ thất phải đến động mạch chủ qua eo động mạch chủ vào động mạch chủ xuống).
Bánh rau
Bánh rau đóng một vai trò quan trọng trong vòng tuần hoàn thai nhi, đảm bảo chức năng của phổi để trao đổi khí và chức năng của hệ tiêu hóa trong việc vận chuyển chất dinh dưỡng và bài tiết các chất chuyển hóa.
Từ phía thai nhi, rau thai được hình thành và phát triển từ màng đệm, nhận máu từ hai động mạch rốn, xuất phát ban đầu từ động mạch chậu trong của thai nhi. Động mạch rốn nằm trong dây rốn và xoắn quanh tĩnh mạch rốn rồi chia thành các nhánh nhỏ tại nơi giao giữa dây rốn và rau thai. Những nhánh này được sắp xếp “tỏa tia”. Nhánh tận động mạch rốn đâm xuyên qua màng đệm tử cung rau thai tạo thành các đám rối nối nhau nằm trong thân chính của mỗi nhung mao màng đệm. Mỗi thân chính chứa một nhánh của động mạch rốn, rồi đâm xuyên phần dày của bánh rau, từ đó phân chia thành một hệ thống mao mạch khổng lồ. Hệ thống này đi vào khoang gian gai rau chứa máu từ mẹ.
Theo nghiên cứu, có một diện tích bề mặt lớn trong mỗi nhung mao màng đệm, qua đó trao đổi khí thụ động khi có chênh lệch về phân áp đối với cả khí oxy và carbon dioxide. Trong đó, không có sự trộn lẫn giữa máu mẹ với máu của thai nhi. Theo sau quá trình oxy hóa bên trong nhung mao màng đệm, dòng máu đi vào các tĩnh mạch bên trong mỗi thân chính. Các tĩnh mạch này tạo thành hợp lưu tại nơi giao nhau giữa dây rốn và nhau thai để tạo thành tĩnh mạch rốn.
Ống tĩnh mạch
Tĩnh mạch rốn mang máu được oxy hóa với nồng độ oxy 80-90% đi từ rau thai đến dây rốn (Hình 5.6). Tĩnh mạch rốn đi vào bụng của thai nhi, chia thành xoang tĩnh mạch cửa và ống tĩnh mạch. Xoang tĩnh mạch cửa hợp với tĩnh mạch cửa của thai nhi; ống tĩnh mạch đưa máu giàu oxy đổ vào tĩnh mạch chủ dưới. Ngay vị trí phân chia bắt đầu của ống tĩnh mạch đóng là cấu trúc cơ tròn, có vai trò như cơ thắt sinh lý, sẽ co lại khi xảy ra tình trạng giảm oxy hóa máu hoặc chảy máu, giúp tăng dòng máu giàu oxy đi qua ống tĩnh mạch về tĩnh mạch chủ dưới, giảm dòng máu đi qua xoang tĩnh mạch cửa và gan. Dòng máu tĩnh mạch chủ dưới tiếp tục hướng lên trên về nhĩ phải. Tại buồng nhĩ phải, một tỷ lệ dòng máu giàu oxy chảy ngược ở bờ dưới men theo trần nhĩ phải, hay gọi là mào phân chia. Cấu trúc này, đóng vai trò giống như vách ngăn giúp chuyển hướng dòng máu đổ thẳng qua lỗ bầu dục. Quá trình này có thể được quan sát qua siêu âm tim thai.
Một tỷ lệ máu đã oxy hóa được chuyển hướng đến tim, tỷ lệ này có sự khác nhau ở các loài động vật có vú. Phần còn lại của dòng máu bị khử oxy chủ yếu trộn lẫn với dòng máu bị khử oxy đến từ mạc treo, thận, chậu và tĩnh mạch gan phải đổ về xoang vành và tĩnh mạch cánh tay đầu.
Lỗ bầu dục
Sự tồn tại của lỗ bầu dục thời kỳ bào thai là cần thiết, đảm bảo đổ đầy tim trái, do lưu lượng máu trở về từ tĩnh mạch phổi thấp. Dòng máu giàu oxy trở về tim thông qua tĩnh mạch chủ dưới, đi qua lỗ bầu dục sang tim trái. Dòng máu giàu oxy này trộn lẫn với dòng máu ít oxy từ tĩnh mạch phổi đổ về nhĩ trái. Sau sự pha trộn xảy ra ở nhĩ trái, nồng độ oxy máu đạt được tại thất trái khoảng 60%, giá trị này tại buồng thất phải là 50-55%.
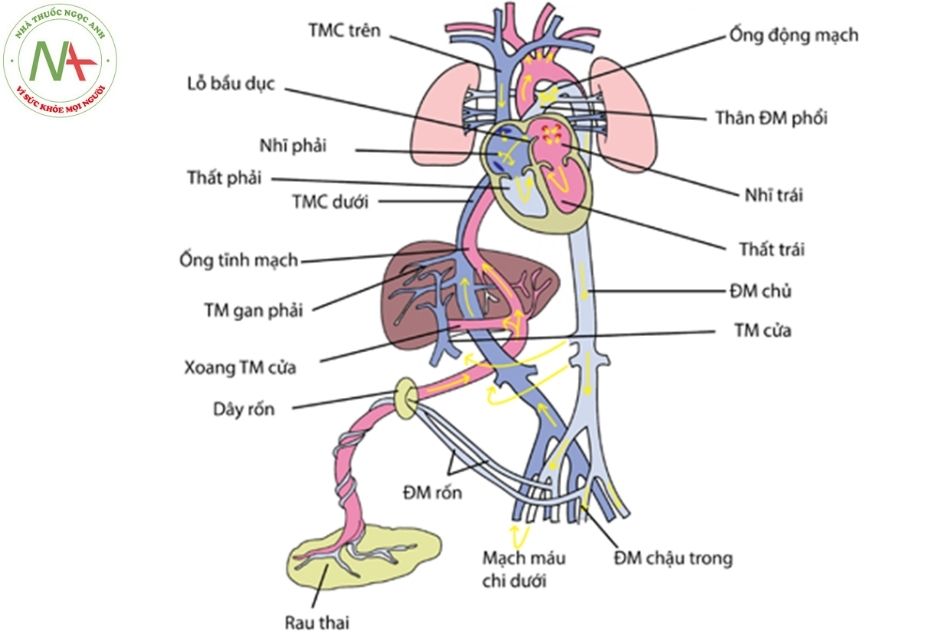
Chú thích: ĐM: Động mạch; ĐMC: Động mạch chủ, TM: Tĩnh mạch, TMC: Tĩnh mạch chủ.
Máu từ thất trái bơm vào động mạch chủ đi đến vòng tuần hoàn cánh tay đầu, cung cấp phần lớn (2/3) máu giàu oxy cho não và chi trên. Vì vậy trong bào thai, não là cơ quan phát triển nhất so với các phần còn lại của cơ thể thai nhi. Chỉ 1/3 thể tích máu từ thất trái đi qua eo động mạch chủ vào động mạch chủ ngực và phần thấp hơn của cơ thể. Mặc dù nồng độ oxy máu động mạch là tương đối thấp, sự khai thác oxy của mô vẫn đạt được tối đa do sự dịch chuyển sang trái của đường cong phân ly oxy của haemoglobin thai nhi khi so sánh với đường cong phân ly oxy của người lớn.
Ống động mạch (ductus arteriosus)
Các tĩnh mạch hỗn hợp trở về nhĩ phải có nồng độ oxy khoảng 40%. Tại nhĩ phải có sự pha trộn với dòng máu giàu oxy từ tĩnh mạch chủ dưới, tạo một dòng máu có nồng độ oxy 50-55% đi từ thất phải vào động mạch phổi. Phần lớn dòng máu tại thân động mạch phổi qua ống động mạch vào động mạch chủ xuống; chỉ một tỷ lệ nhỏ máu từ thân động mạch phổi đi đến phổi qua hai nhánh động mạch phổi phải và trái.
Ống động mạch là cấu trúc nối thân ĐMP và ĐMC xuống ở vị trí ngay sau nơi xuất phát động mạch dưới đòn trái. Cấu trúc thành ống động mạch gồm các tế bào cơ trơn màng ngoài tim, nơi sản xuất ra prostaglandin. Ở thai nhi, dòng chảy qua ống động mạch có thể thay đổi bởi sự hấp thu vào cơ thể các chất ức chế prostaglandin, giống như các chất chống viêm không steroid. Máu đi từ ống động mạch trộn với dòng máu qua eo động mạch chủ tạo ra một dòng máu có nồng độ oxy 50-55% ở động mạch chủ xuống. Từ đây, một tỷ lệ lớn dòng máu quay trở lại rau thai qua động mạch rốn để được tham gia quá trình oxy hóa.
Tuần hoàn ngay sau sinh
Những thay đổi của hệ tuần hoàn trẻ sơ sinh là do tác động của nhịp thở đầu tiên làm giảm nhanh của sức cản mạch phổi (hay còn gọi là sức cản phổi) và sự cắt đứt liên kết tuần hoàn rốn với rau thai. Sức cản mạch phổi (pulmonary vascular resistance – PVR) giảm làm tăng lưu lượng máu trong hệ tuần hoàn phổi từ 8-10 lần. Sau sinh 24h, áp lực động mạch phổi giảm còn 1/2 so với áp lực động mạch hệ thống. Sau pha giảm nhanh ban đầu, áp lực và sức cản mạch phổi sẽ giảm dần từ từ về giá trị bình thường như ở người trưởng thành trong vòng 2-6 tuần, do sự tái cấu trúc thành mạch, thoái triển cơ trơn thành mạch.
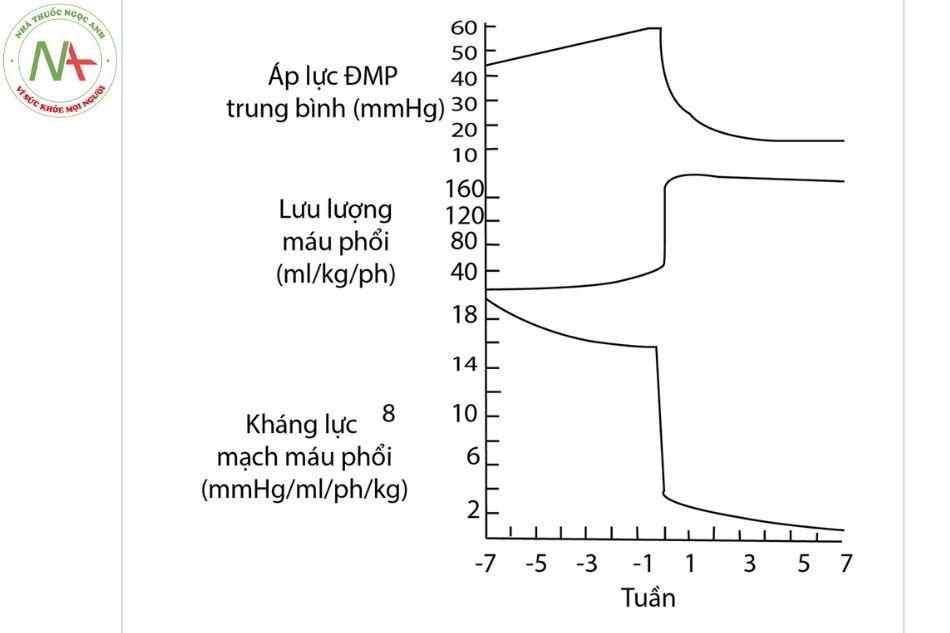
Dòng máu chảy qua ống động mạch sẽ đảo ngược chiều so với giai đoạn bào thai, trở thành chiều từ trái sang phải, cho tới khi ống động mạch đóng dần về mặt huyết động trong vài giờ đến vài ngày (thường 2-3 ngày) sau sinh. Ống động mạch có thể tồn tại kéo dài hơn ở trẻ đẻ non gây hiện tượng ăn cắp máu ở các vùng giường mạch máu có sức cản cao nhất. Hiện tượng ăn cắp máu này có thể là căn nguyên gây viêm ruột hoại tử hoặc chảy máu não thất ở trẻ đẻ non.
Trạng thái tăng lưu lượng máu lên phổi sau khi trẻ ra đời làm tăng dòng máu tĩnh mạch trở về nhĩ trái, gây ra sự đảo ngược chênh lệch áp lực giữa nhĩ trái và nhĩ phải, áp lực cao hơn trong buồng nhĩ trái sẽ làm đóng lỗ bầu dục, chấm dứt luồng thông đáng kể chiều phải trái ở tầng nhĩ như trong giai đoạn bào thai. Quá trình đóng lỗ bầu dục là một quá trình đóng thụ động.
Ống tĩnh mạch mang máu tĩnh mạch rốn chủ yếu đổ về thất trái. Vào lúc sinh, tuần hoàn rốn với rau thai bị cắt đứt làm giảm lưu lượng máu qua ống tĩnh mạch, gây đóng ống tĩnh mạch về chức năng một cách thụ động. Tuy nhiên trên thực nghiệm, người ta đã chứng minh ống tĩnh mạch biệt lập có thể đáp ứng với kích thích giao cảm và prostanoid. Thí nghiệm trên cừu sơ sinh, có thể làm mở lại ống tĩnh mạch khi sử dụng prostaglandin E1. Như vậy, quá trình đóng ống tĩnh mạch còn có một phần tác động của yếu tố thay đổi thể dịch khi trẻ sinh ra, tương tự như trường hợp đóng ống động mạch.
Hình dạng sóng áp lực của các buồng tim và mạch máu lớn
Hình dạng sóng áp lực tâm nhĩ
Thay đổi áp suất trong tâm nhĩ – sóng a, c, và v
Trên đường cong thể hiện áp lực tâm nhĩ, có ba sóng áp lực tâm nhĩ là: a, c và v.
- Sóng a được tạo ra do tâm nhĩ Thông thường, áp lực nhĩ phải tăng từ 4-6 mmHg khi nhĩ co và áp lực nhĩ trái tăng khoảng 7-8 mmHg.
- Sóng c xuất hiện khi tâm thất bắt đầu co, nguyên nhân chủ yếu là do sự phồng lên về phía tâm nhĩ của van nhĩ thất do tăng áp lực trong buồng tâm thất.
- Sóng v xuất hiện khi sự co tâm thất kết thúc; là kết quả của dòng máu chảy chậm từ tĩnh mạch vào tâm nhĩ phải khi van nhĩ thất đóng trong lúc tâm thất co. Sau đó khi sự co tâm thất kết thúc, van nhĩ thất mở ra cho phép máu tích lũy ở tâm nhĩ nhanh chóng đổ vào tâm thất và làm xuất hiện sóng v.
Đường cong sóng áp lực tâm nhĩ phải
Áp lực tâm nhĩ phải bình thường là 2 – 6 mmHg và được biểu thị bằng sóng a và v và đường cong đi xuống x và y (Hình 8). Sóng a biểu thị cho áp lực nhĩ phải khi nhĩ co xuất hiện sau sóng P trên điện tâm đồ khoảng 80 ms.
‐ Sóng v xuất hiện khi sự co tâm thất kết thúc; là kết quả của dòng máu chảy chậm từ tĩnh mạch vào tâm nhĩ phải khi van nhĩ thất đóng trong lúc tâm thất co. Sau đó khi sự co tâm thất kết thúc, van nhĩ thất mở ra cho phép máu tích lũy ở tâm nhĩ nhanh chóng đổ vào tâm thất và làm xuất hiện sóng v.
Đường cong sóng áp lực tâm nhĩ phải
Áp lực tâm nhĩ phải bình thường là 2 – 6 mmHg và được biểu thị bằng sóng a và v và đường cong đi xuống x và y (Hình 8). Sóng a biểu thị cho áp lực nhĩ phải khi nhĩ co xuất hiện sau sóng P trên điện tâm đồ khoảng 80 ms.
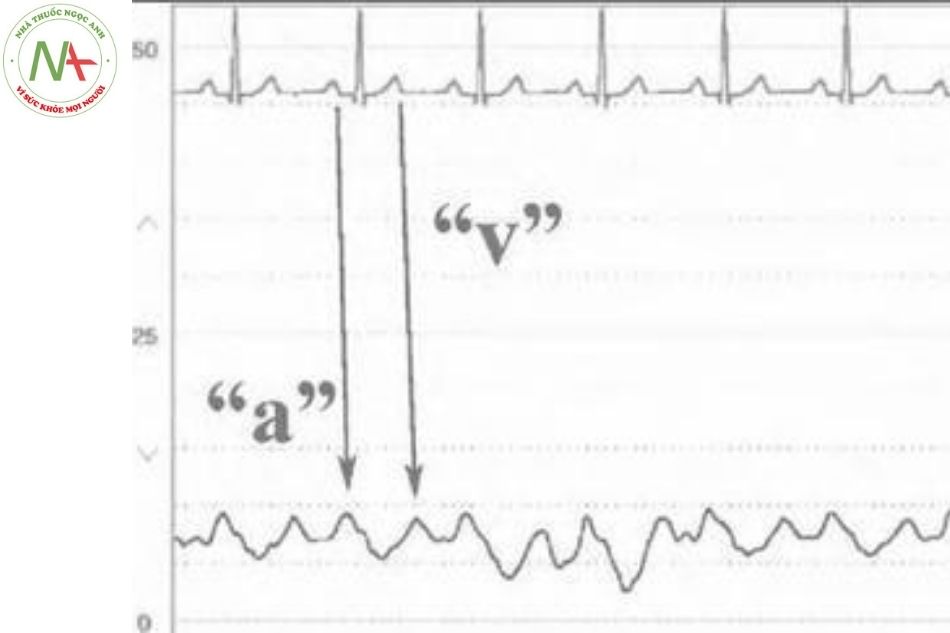
Đường đi xuống x biểu thị cho sự giảm áp lực của sóng a và phản ánh cả quá trình tâm nhĩ giãn. Trong rung nhĩ, sóng a thường mất đi nhưng có thể vẫn có đường đi xuống x do có hiện tượng chậm giãn của tâm nhĩ (Hình 9).
Đôi khi có thể thấy sóng c sau sóng a do chuyển động đột ngột của vòng van ba lá về phía tâm nhĩ phải khi bắt đầu thì tâm thất thu. Sóng c sau sóng a và cùng thời gian với khoảng PR trên điện tâm đồ; block nhĩ thất cấp 1 làm sóng c rõ ràng hơn (Hình 10). Khi có sự hiện diện của một sóng c, áp lực giảm theo sau tạo thành đường đi xuống x.
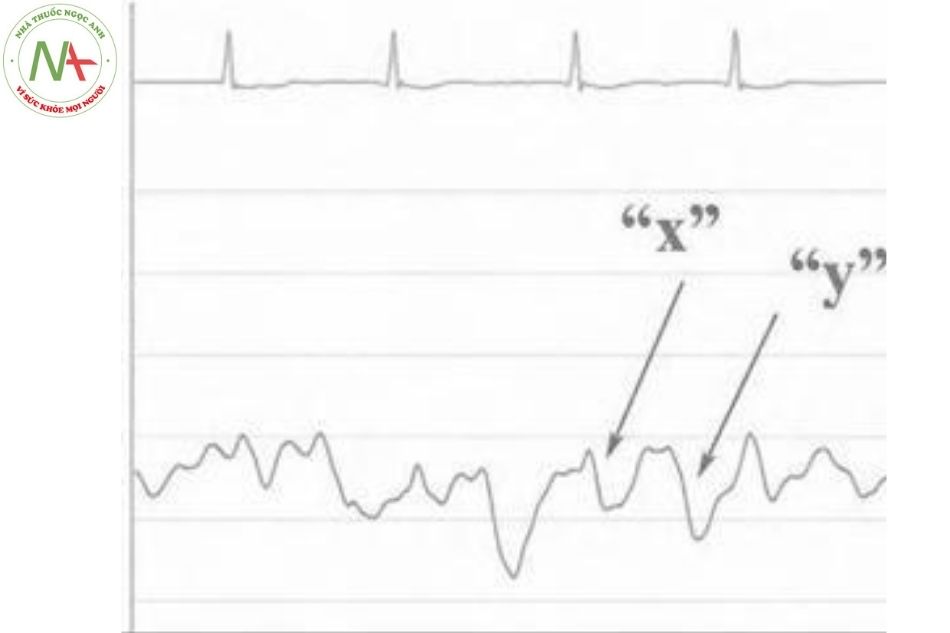
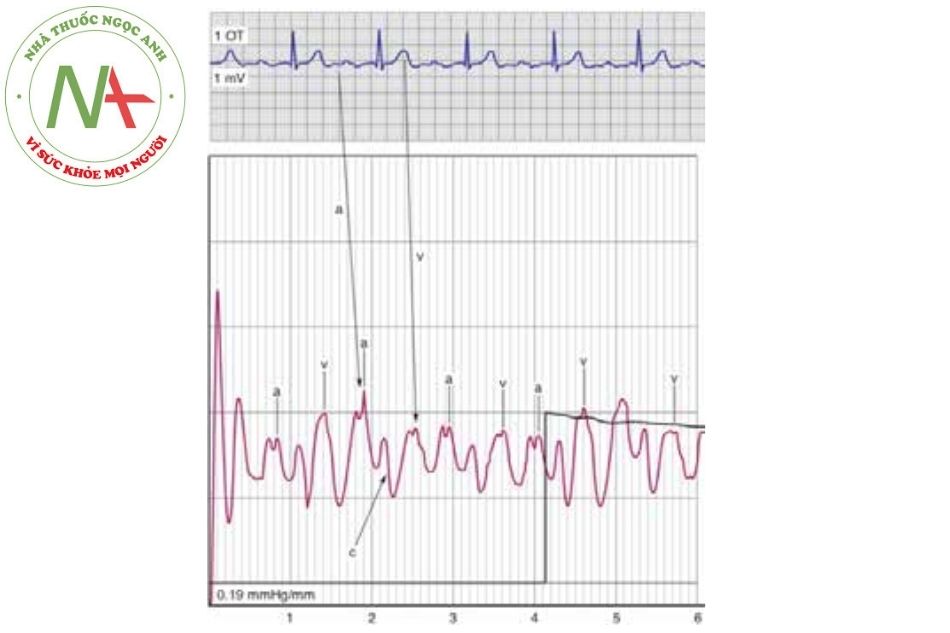
Sóng áp lực tiếp theo là sóng v. Sóng này xảy ra cùng lúc với thì tâm thất thu, khi van ba lá đóng lại, biểu hiện của sóng v là do sự gia tăng áp lực do đổ đầy tâm nhĩ trong thì tâm trương. Tăng sự đổ đầy tâm nhĩ phải làm sóng v lớn hơn. Đỉnh của sóng v nhĩ phải xảy ra ở cuối thì tâm thất thu, khi tâm nhĩ đã được đổ đầy tối đa tương ứng với sự kết thúc của sóng T trên điện tâm đồ. Sự giảm áp lực xảy ra sau sóng v gọi là đường đi xuống y và do sự làm rỗng nhanh của tâm nhĩ phải khi mở van ba lá. Sau đó cơ tâm nhĩ co và bắt đầu một chu kỳ tim tiếp theo.
Khi hình dạng sóng tâm nhĩ phải bình thường, sóng a thường vượt quá sóng v. Khi hít vào, áp lực trung bình nhĩ phải giảm do tác động của sự giảm áp lực trong khoang lồng ngực và quá trình đổ đầy thất phải thụ động tăng lên, đường đi xuống y trở nên nổi bật hơn (Hình 11).
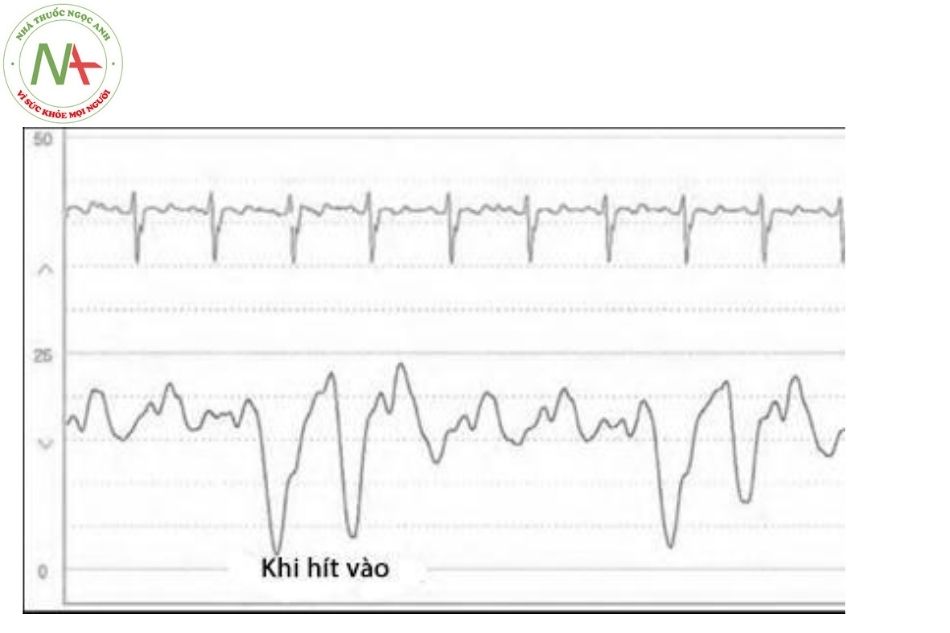
Hình dạng sóng áp lực thất phải
Áp lực tâm thu thất phải bình thường là 20-30 mmHg và áp lực cuối tâm trương thất phải là 0-8 mmHg. Hình dạng sóng thất phải có điểm đặc trưng là sóng tăng áp nhanh khi thất co và giảm áp nhanh khi thất giãn với một pha tâm trương được mô tả có áp lực khởi đầu thấp sau đó tăng dần (Hình 12).
Áp lực nhĩ phải tác động một vài mmHg đến áp lực cuối tâm trương thất phải trừ khi có hẹp van ba lá. Khi nhĩ co, sóng a có thể xuất hiện trên hình dạng sóng thất ở cuối tâm trương (Hình 5.13) và đó là biểu hiện bất thường vì thất phải bình thường sẽ thích ứng với áp lực nhĩ phải và không làm tăng đáng kể áp lực. Do đó, sự hiện diện của sóng a trên hình dạng sóng thất phải thường cho thấy sự giảm thích ứng và có thể là biểu hiện của tăng áp động mạch phổi, phì đại thất phải hay quá tải thể tích.
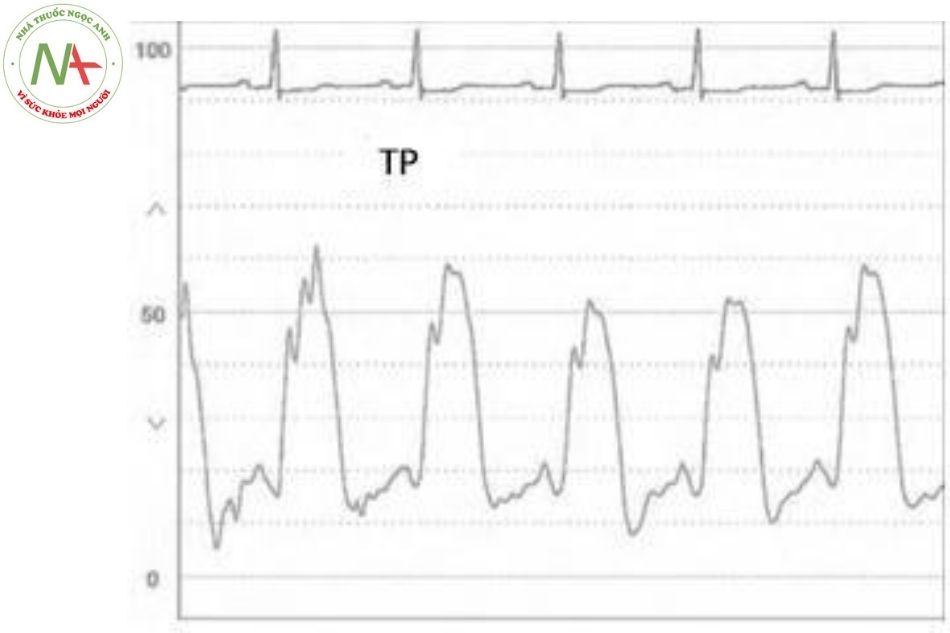
Hình ảnh sóng áp lực động mạch phổi
Áp lực tâm thu động mạch phổi bình thường là 20-30 mmHg và áp lực tâm trương bình thường là 4-12 mmHg (Hình 5.14). Áp lực tâm thu ở động mạch phổi và ở thất phải không có sự khác biệt trừ khi có hẹp van hay hẹp động mạch phổi.
Hình dạng sóng áp lực động mạch phổi tương tự như của các động mạch khác, pha tăng áp lực nhanh, đỉnh ở tâm thu và pha giảm áp liên quan với đóng van động mạch phổi ở thì tâm trương.
- Đỉnh áp lực tâm thu xảy ra cùng với sóng T trên điện tâm đồ.
- Hình dạng sóng áp lực động mạch phổi giống như hình dạng sóng áp lực trong các buồng tim phải và phụ thuộc vào sự thay đổi của hô hấp (Hình 5.15). Hít vào làm giảm áp lực trong lồng ngực và thở ra làm tăng áp lực trong lồng ngực.
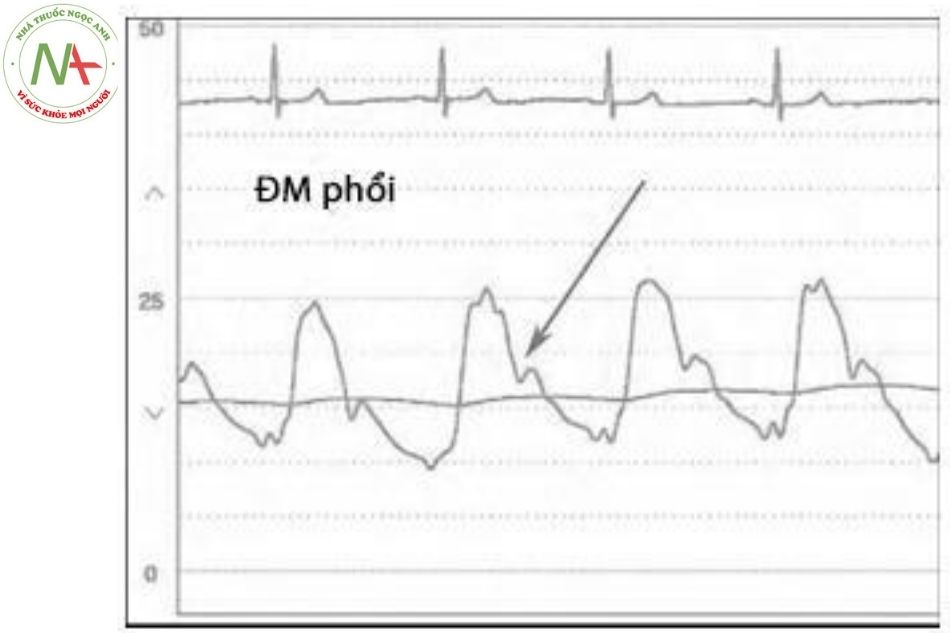
Áp lực thay đổi liên quan đến hô hấp tác động đến các buồng tim thường nhỏ và ít quan trọng. Tuy nhiên, với những bệnh nhân đang thở máy do bệnh phổi, béo phì hay suy hô hấp có thể tạo ra những thay đổi đáng kể áp lực lồng ngực, dẫn đến những khác biệt rõ rệt áp lực động mạch phổi trong khi hô hấp (Hình 17).
Hầu hết các chuyên gia cho rằng cuối thì thở ra (end-expiration) là thời điểm thích hợp để đánh giá áp lực động mạch phổi (và các buồng tim khác) vì áp lực trong lồng ngực gần bằng 0 nhất. Áp lực động mạch phổi cuối tâm trương thường được sử dụng để ước tính áp lực nhĩ trái, tuy nhiên khá không chính xác đặc biệt là khi sức cản mạch máu phổi bất thường.
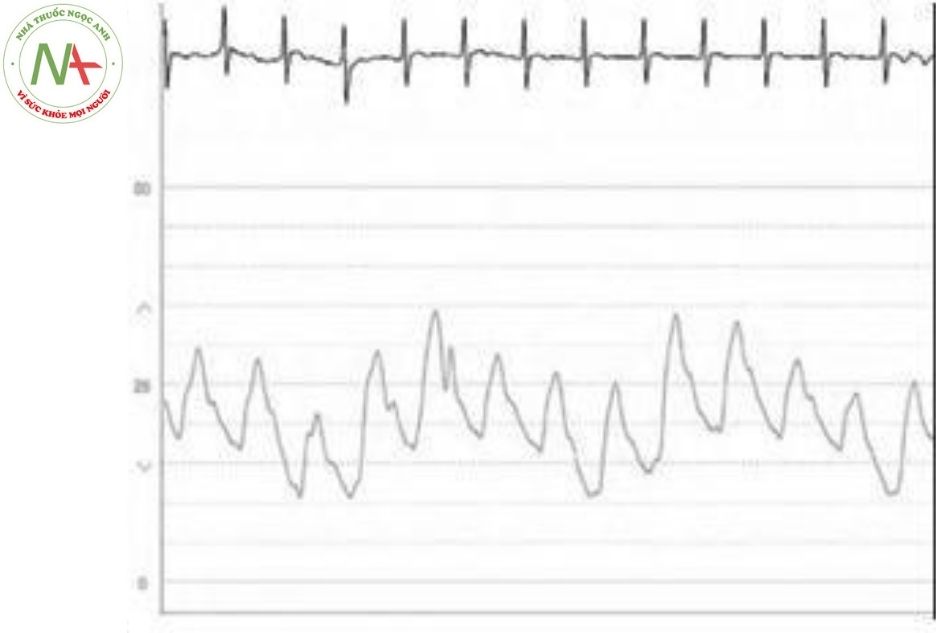
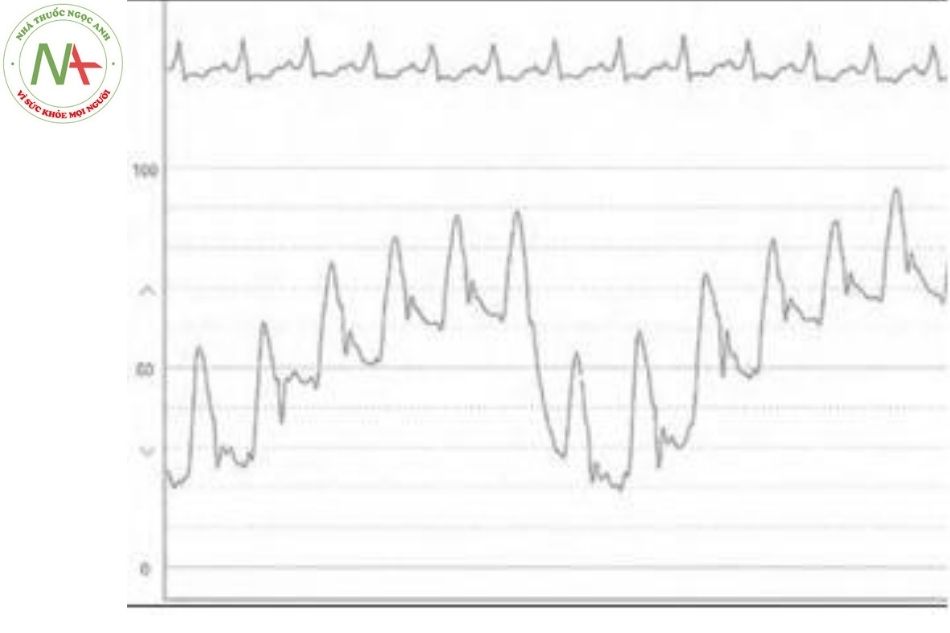
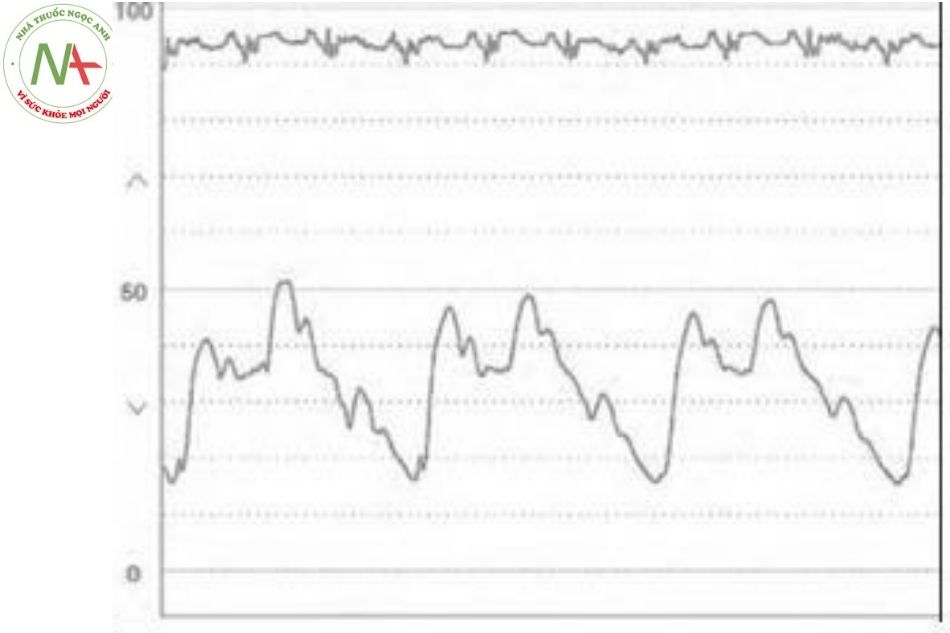
Hình dạng sóng áp lực mao mạch phổi bít
Giá trị trung bình bình thường của áp lực mao mạch phổi bít (pulmonary capillary wedge pressure – PCWP) là 2-14 mmHg (Hình 5.18). Một PCWP có giá trị đúng chỉ khi được đo trong trường hợp không có dòng chảy động mạch phổi xuôi dòng (bít) đo ở lỗ tận cùng ống thông (catheter) và như vậy áp lực được truyền qua một cột chất lỏng liên tục từ tâm nhĩ trái qua các tĩnh mạch phổi và giường mao mạch phổi đến đầu ống thông ở động mạch phổi.
Trong những điều kiện này, PCWP là biểu hiện của áp lực nhĩ trái với sóng a và v và đường đi xuống x và y.
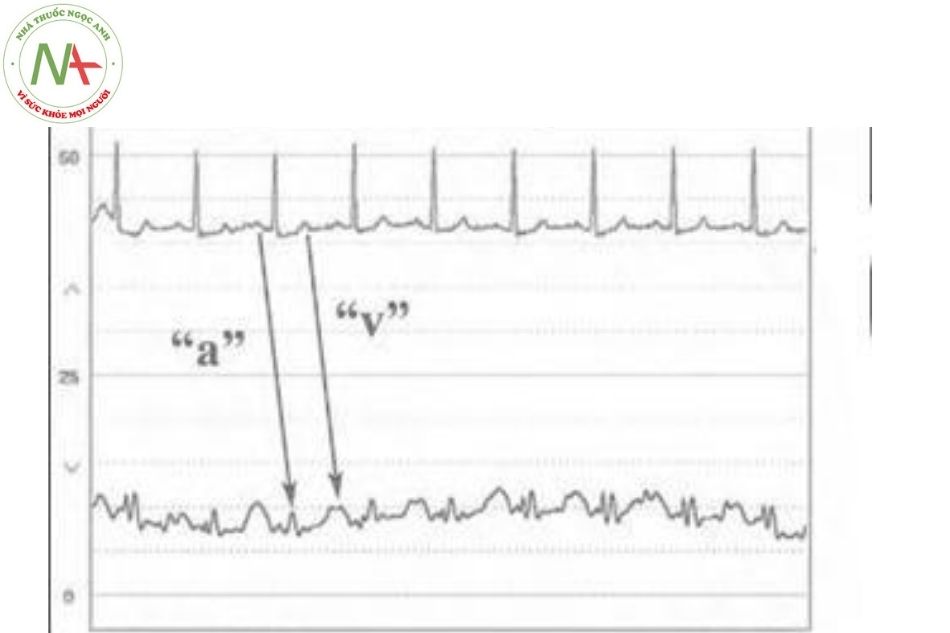
Theo dõi PCWP cho thấy một vài điểm khác biệt quan trọng so với hình dạng sóng áp lực tâm nhĩ trái khi đo trực tiếp.
- Sóng c đôi khi được xác định ở dạng sóng tâm nhĩ, nhưng không có trên PCWP do tính giảm dần của áp lực.
- Sóng v điển hình thường vượt quá sóng a trên theo dõi
Vì sóng áp lực được truyền thông qua giường mao mạch phổi nên có một độ trễ có ý nghĩa xảy ra giữa một sóng trên điện tâm đồ và khởi phát của sóng áp lực tương ứng. Độ trễ này có thể thay đổi đáng kể tùy thuộc vào khoảng cách sóng áp lực truyền đi.
Khi PCWP được đo bằng catheter ở vị trí xa hơn, độ trễ quan sát được sẽ ngắn hơn. Điển hình là đỉnh sóng a sau sóng P trên điện tâm đồ khoảng 240 ms chứ không phải 80 ms như đã thấy khi theo dõi áp lực nhĩ phải. Tương tự như vậy, đỉnh sóng v xảy ra sau khi sóng T đã được ghi nhận trên điện tâm đồ.
Mối liên hệ giữa áp lực thực sự của nhĩ trái và PCWP được thể hiện trong Hình 5.19. Lưu ý rằng thời gian trễ giữa sự kiện sinh lý tương tự và tính giảm dần của PCWP liên quan đến dạng sóng áp lực nhĩ trái có ý nghĩa phản ánh giá trị áp lực thấp hơn một chút so với áp lực nhĩ trái. Nhìn chung PCWP trung bình dao động trong vài mmHg so với áp lực trung bình nhĩ trái đặc biệt là khi áp lực mao mạch phổi bít và áp lực tâm thu động mạch phổi thấp.
Áp lực động mạch phổi cao gây khó khăn để nhận định đúng giá trị của áp lực bít và làm sai lệch giá trị của áp lực mao mạch phổi bít so với áp lực nhĩ trái.
Đánh giá chuẩn xác áp lực PCWP không phải lúc nào cũng dễ dàng và khả thi. Tuy nhiên, phổi gồm ba vùng sinh lý có áp lực riêng biệt là áp lực phế nang, áp lực động mạch phổi và áp lực tĩnh mạch phổi. Để đặc tính hoá mối tương quan này, West đã chia phổi thành ba vùng lý thuyết đi từ đỉnh phổi xuống đáy phổi và dựa vào tương quan giữa áp lực động mạch phổi (Pa) hay áp lực dòng máu vào, áp lực phế nang (PA) và áp lực tĩnh mạch phổi (Pv) hay áp lực dòng máu đi ra (các vùng phổi của West – Hình 5.5 phần trên, mục 4. Điều hòa lưu lượng tuần hoàn phổi).
- Vùng 1 điển hình ở đỉnh phổi, nơi có áp lực phế nang (PA) cao hơn áp lực trung bình của động mạch và tĩnh mạch phổi.
- Vùng 2 nằm ở trung tâm phổi, ở đây áp lực động mạch phổi (Pa) cao hơn áp lực phế nang và cao hơn áp lực tĩnh mạch phổi. Các vùng này không được dùng để đo PCWP vì mao mạch ở đây xẹp.
- Vùng 3 là đáy phổi, ở đây áp lực phế nang thấp hơn cả áp lực động mạch và tĩnh mạch phổi, cho phép truyền trực tiếp áp lực nhĩ trái tới đầu Vùng 3 phổi là nơi PCWP phản ánh chính xác áp lực nhĩ trái. May mắn là khi thông tim, hầu hết bệnh nhân ở tư thế nằm ngửa và phần lớn phổi là vùng 3. Ngoài ra, vì hầu hết dòng máu sẽ chảy tới vùng đó, đầu catheter của bóng chèn thường kết thúc ở vùng 3.
Các tình huống liên quan đến vị trí của đầu catheter ở các vùng khác không phải vùng 3 bao gồm sử dụng mode thở áp lực dương cuối thì thở ra (PEEP), thở máy (áp suất phế nang tăng và ít tăng nhất ở vùng 3 phổi) và giảm thể tích tuần hoàn. Tuy nhiên, việc chứng minh đầu catheter nằm dưới mức nhĩ trái sẽ đảm bảo vị trí tại vùng 3 và có độ chính xác cao hơn.
Đặc điểm của quá trình đo PCWP chuẩn bao gồm:
- Hiện diện rõ ràng sóng a và v (lưu ý là sóng a thường không có trong rung nhĩ và các pha sóng ở từng giai đoạn có thể không khác biệt khi áp lực hạ thấp).
- Xác định đầu catheter ở đầu xa động mạch phổi đã được cố định và bóng chèn đã được bơm dưới màn hình Xquang.
Độ bão hòa oxy thu được từ vị trí đo PCWP lớn hơn 90%.
Áp lực trung bình có thể tăng lên đột ngột khi bóng chèn bị thủng hoặc khi rút catheter từ vị trí đo PCWP ra khỏi động mạch phổi.
Trong tất cả các dấu hiệu này, khi đo PCWP độ bão hòa oxy từ đầu catheter lớn hơn 90% là đặc điểm nhận định chính xác nhất. Áp lực “quá bít” xảy ra khi đầu catheter nằm ở động mạch phổi ngoại biên và bóng chèn bị bơm quá mức; vị trí catheter này có thể dẫn đến rách động mạch phổi – một biến chứng có thể gây tử vong của đặt catheter động mạch phổi. Áp lực quá bít gây ra sai lệch khi đo PCWP, không có sóng a và v và sự theo dõi này không phản ánh áp lực nhĩ trái.
Giá trị PCWP trung bình xấp xỉ 0-5 mmHg và thấp hơn áp lực tâm thu động mạch phổi trừ khi có tình trạng tăng sức cản mạch máu phổi. Đo chính xác PCWP có thể khó khăn và không khả thi ở những bệnh nhân tăng áp động mạch phổi. Vì vậy, việc đo áp lực nhĩ trái bằng cách chọc qua vách liên nhĩ để đo trực tiếp áp lực nhĩ trái là quan trọng khi đánh giá hẹp van hai lá và khi phẫu thuật viên không thể xác định được áp lực bít.
Nhìn chung có một mối tương quan giữa áp lực mao mạch phổi bít, áp lực nhĩ trái và áp lực cuối tâm trương thất trái. Áp lực mao mạch phổi bít không liên quan với áp lực cuối tâm trương thất trái khi có hẹp van hai lá, hở van hai lá hoặc hở van động mạch chủ nặng, tắc nghẽn tĩnh mạch phổi, tăng rõ rệt áp lực dương cuối thì thở ra, u nhầy nhĩ trái hoặc vị trí đặt catheter không phải ở vùng 3 của phổi.
Hình dạng sóng áp lực thất trái
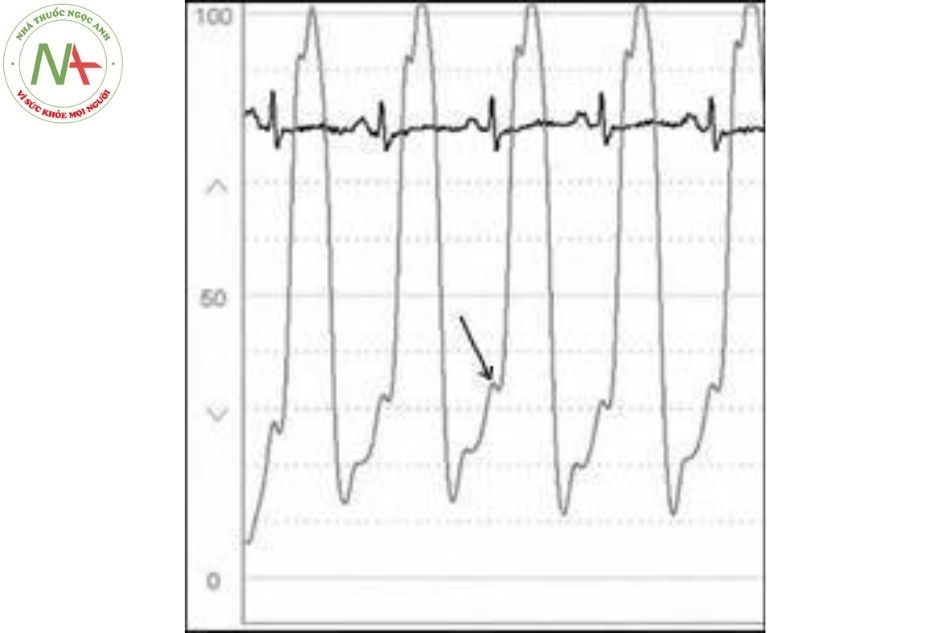
Áp lực tâm thu thất trái bình thường là 90-140 mmHg và áp lực cuối tâm trương bình thường là 10-16 mmHg. Hình dạng sóng áp lực thất trái được đặc trưng bởi đường áp lực đi lên nhanh thẳng đứng khi tâm thất co, đạt đỉnh áp lực tâm thu và sau đó giảm nhanh.
Áp lực đầu tâm trương thường rất thấp và tăng chậm trong cả tâm trương. Tương tự như dạng sóng thất phải, sóng a có thể được tìm thấy khi theo dõi thất trái ở cuối thì tâm trương, tuy nhiên điều này là bất thường và gợi ý gián tiếp thất trái noncompliant (không giãn nở).
Áp lực cuối tâm trương thất trái (left ventricular end-diastolic pressure – LVEDP) được định nghĩa là áp lực ngay sau sóng a và trước khi tăng đột ngột áp lực tâm thu khi thất co. Tuy nhiên, xác định áp lực cuối tâm trương thất trái đôi khi có thể khác đi. Áp lực cuối tâm trương tăng có thể lẫn vào đường đi lên của áp lực thất trái và làm mờ nhạt LVEDP (Hình 21).
Như vậy, với sự xuất hiện của sóng a lớn, áp lực ngay sau sóng a đại diện cho LVEDP (Hình 22). Thay đổi áp lực lồng ngực theo các giai đoạn hô hấp có thể ảnh hưởng đến LVEDP và áp lực cuối thì thở ra.
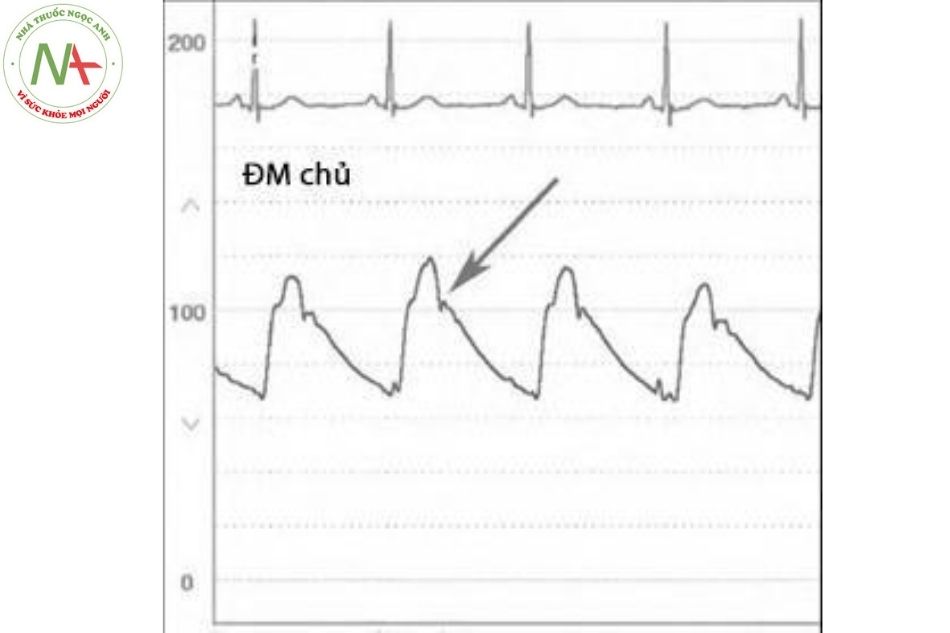
Hình dạng sóng áp lực động mạch
Áp lực tâm thu động mạch chủ bình thường là 90-140 mmHg và áp lực tâm trương bình thường là 60-90 mmHg. Hình dạng sóng áp lực trung tâm động mạch chủ có đường sóng lên nhanh, đỉnh tâm thu và sóng dội ngược dạng nóc do van động mạch chủ đóng khi giảm áp lực (Hình 5.23). Đỉnh áp lực tâm thu động mạch chủ bằng với đỉnh áp lực tâm thu thất trái trừ khi có tắc nghẽn thất trái tại van động mạch chủ hoặc tại đoạn gần của động mạch chủ.
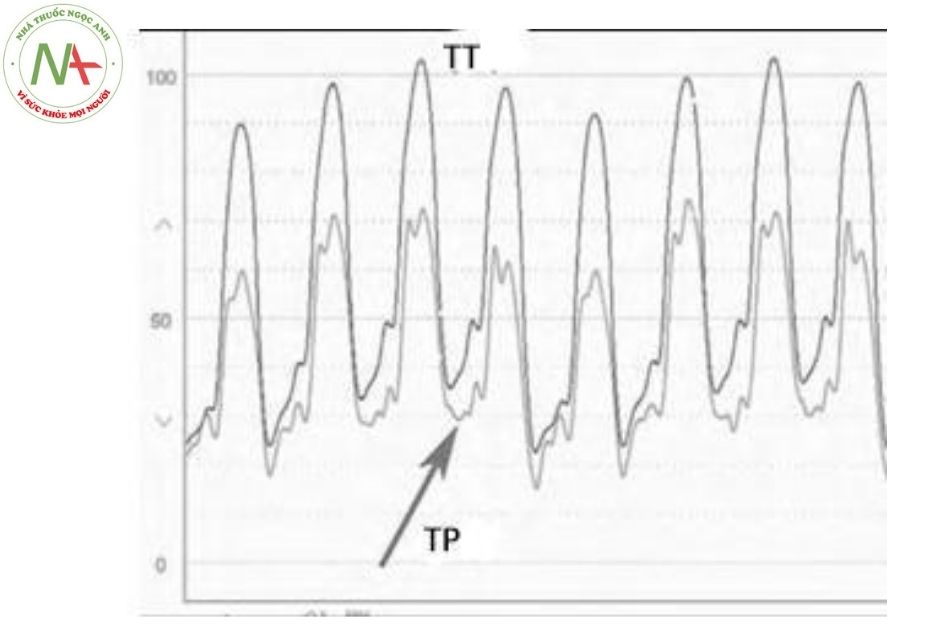
Đo áp lực trung tâm động mạch chủ gồm hai phần: đo sóng áp lực do tống máu thất trái và tổng hợp sóng áp lực được tạo ra do sóng phản hồi. Sóng phản hồi là kết quả khi máu được tống đi và gặp một vùng có sức cản như điểm mạch phân nhánh hay đoạn mạch ngoằn ngoèo. Khi làn sóng áp lực truyền đến và đập vào những vùng này, chúng sẽ được dội ngược lại về tim. Những sóng áp lực đập vào van động mạch chủ sẽ tạo ra các sóng áp lực bổ sung chuyển tiếp và nhỏ hơn sóng đến. Vì thế, hình dạng sóng áp lực đại diện là tổng hợp của tất cả các xung lực hướng về phía trước.
Hiện tượng này ít rõ ràng hơn khi áp lực đại điện được lấy gần van động mạch chủ. Ảnh hưởng gia tăng thêm sóng từ van động mạch chủ thường không đáng kể. Tuy nhiên, trong một số trường hợp, sóng phản hồi có thể có giá trị đáng kể.
- Các yếu tố làm gia tăng ảnh hưởng của sóng phản hồi gồm suy tim, hở van động mạch chủ, tăng huyết áp hệ thống, động mạch chủ xơ cứng do tuổi cao hay bệnh động mạch ngoại biên, tắc nghẽn động mạch chủ hay động mạch chậu – đùi, hoặc động mạch gấp khúc và co nhỏ.
- Các yếu tố làm giảm sóng phản hồi bao gồm giãn mạch, giảm thể tích tuần hoàn và hạ huyết áp.
Sóng phản hồi thường xuất hiện muộn ở dạng sóng áp lực động mạch chủ do sự chậm trễ thời gian từ khi hình thành đến khi tổng hợp với sóng ở trước.
Ảnh hưởng của sóng phản hồi đặc biệt đáng chú ý trong các dạng sóng động mạch ngoại biên (động mạch cánh tay, động mạch đùi và động mạch quay). Đỉnh áp lực tâm thu lớn hơn áp lực trung tâm động mạch chủ từ 10-20 mmHg do sự khuếch đại ngoại biên của các sóng phản hồi. Đường viền của dạng sóng thay đổi hơn khi tới van động mạch chủ vì có đường đi lên dốc hơn, đỉnh tâm thu hẹp hơn (đỉnh nhọn) và sóng dội ngược dạng nóc giảm đáng kể hoặc biến mất.
Đo áp lực đồng thời của hai hay nhiều buồng tim
Quy trình thủ thuật thông tim thu thập giá trị các áp lực đồng thời ở hai hay nhiều buồng tim với mục đích sàng lọc một vài trường hợp đặc biệt. Ghi áp lực đồng thời thất trái – thất phải và áp lực đồng thời thất trái – PCWP cần được thực hiện ở tất cả bệnh nhân cần đánh giá huyết động khi thông tim trái và phải.
Mục đích của hai quá trình này là đánh giá sinh lý và hẹp van hai lá. Đo áp lực đồng thời bao gồm áp lực thất trái và áp lực trung tâm động mạch chủ hoặc áp lực động mạch đùi khi chẩn đoán hẹp động mạch chủ, tắc nghẽn đường ra thất trái hoặc chèn ép động mạch chủ; và đồng thời áp lực thất phải và áp lực động mạch phổi khi có hẹp van hay hẹp động mạch phổi. Áp lực đồng thời nhĩ trái và thất trái được đo trong trường hợp hẹp van hai lá khi đo áp lực mao mạch phổi bít PCWP không đầy đủ hoặc không khả thi.
Kết hợp áp lực thất phải và áp lực thất trái
Quá trình này được thực hiện trong tất cả các đánh giá huyết động. Tương tác khá phức tạp xảy ra giữa các buồng tim, màng ngoài tim và khoang lồng ngực trong chu kỳ hô hấp. Nhìn chung, ở những bệnh nhân không có sự hạn chế chức năng sinh lý, ảnh hưởng của các tương tác này làm áp lực tâm trương thất trái và phải chênh lệch nhau ít nhất 5 mmHg, thay đổi trong chu kỳ hô hấp.
Thay đổi đỉnh áp lực tâm thu khi hít vào và thở ra ở thất phải và trái xảy ra đồng thời với nhau (Hình 24). Bất thường này có trong bệnh viêm màng ngoài tim co thắt và bệnh cơ tim hạn chế.
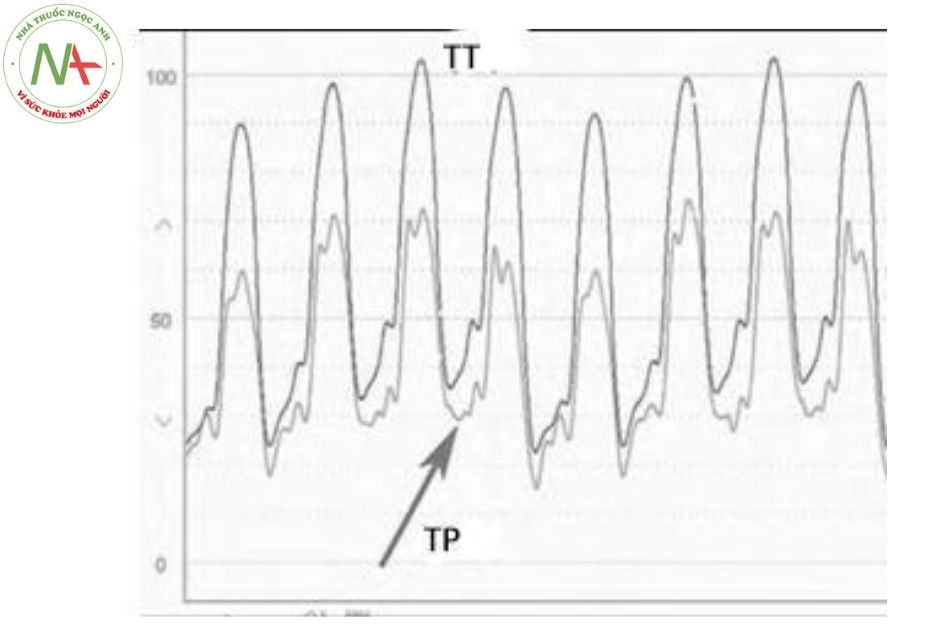
Chú thích: TT: Thất trái; TP: Thất phải
Ảnh hưởng huyết động do các bất thường dẫn truyền được phản ánh đồng thời trong cả áp lực thất trái và thất phải. Bình thường, dạng sóng thất phải nằm trong giới hạn của sóng thất trái (Hình 25).
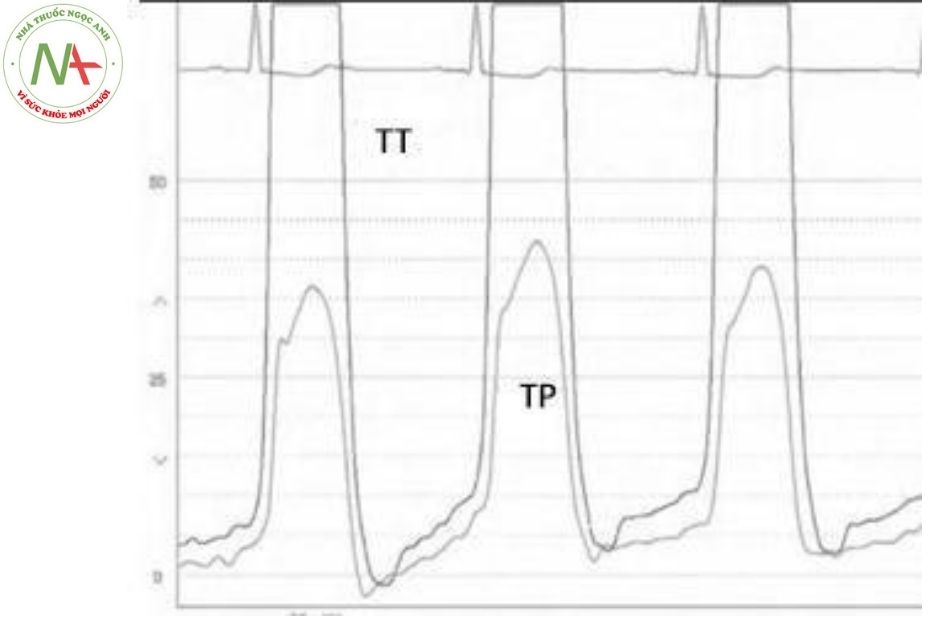
Chú thích: TT: Thất trái; TP: Thất phải
Khi có block nhánh phải sẽ làm chậm quá trình co thất phải so với thất trái, dẫn đến độ trễ của sóng áp lực thất phải so với thất trái và sự chuyển dịch sóng sẽ về bên phải (Hình 26). Điều ngược lại xảy ra khi có block nhánh trái (Hình 27).
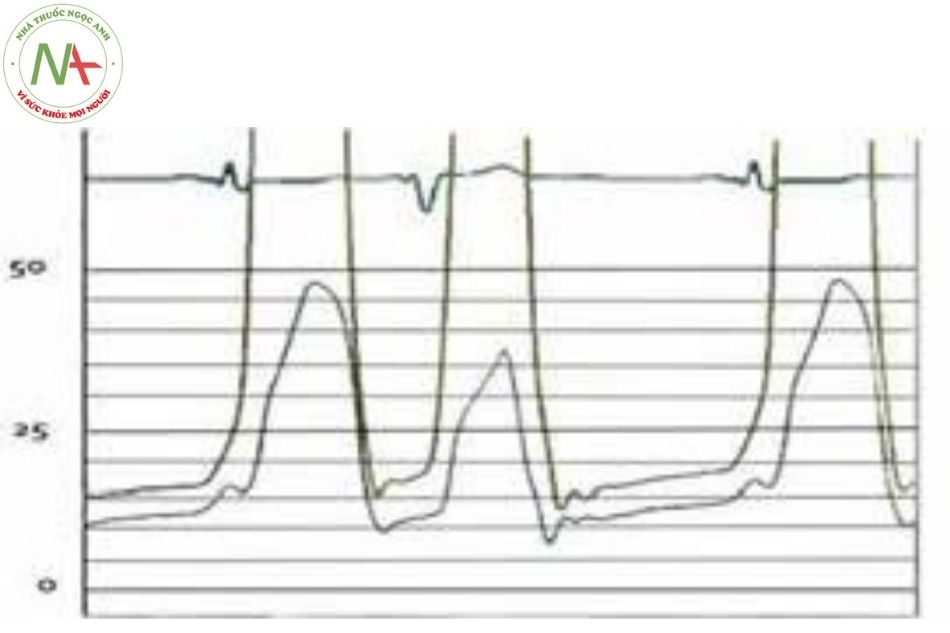
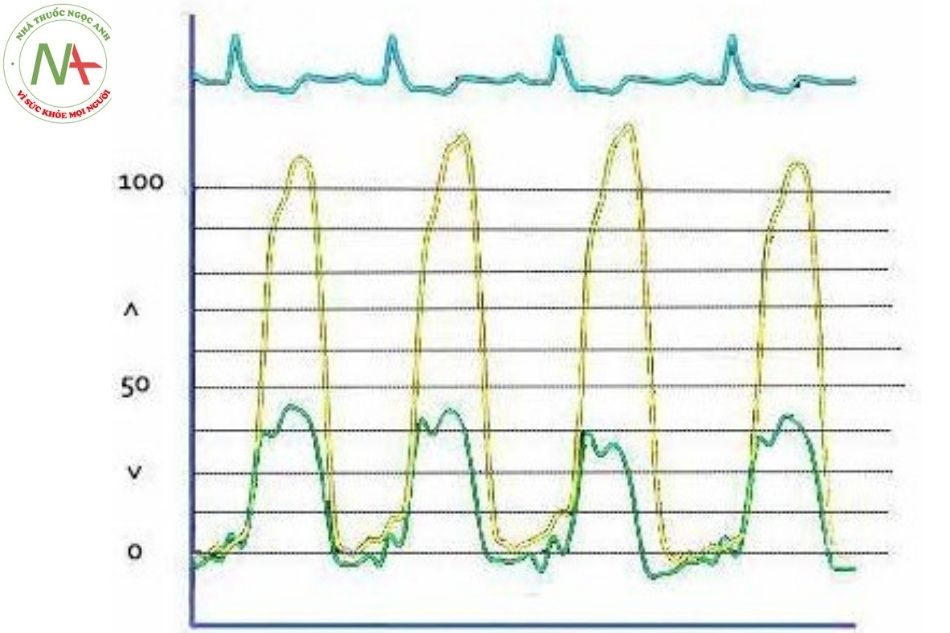
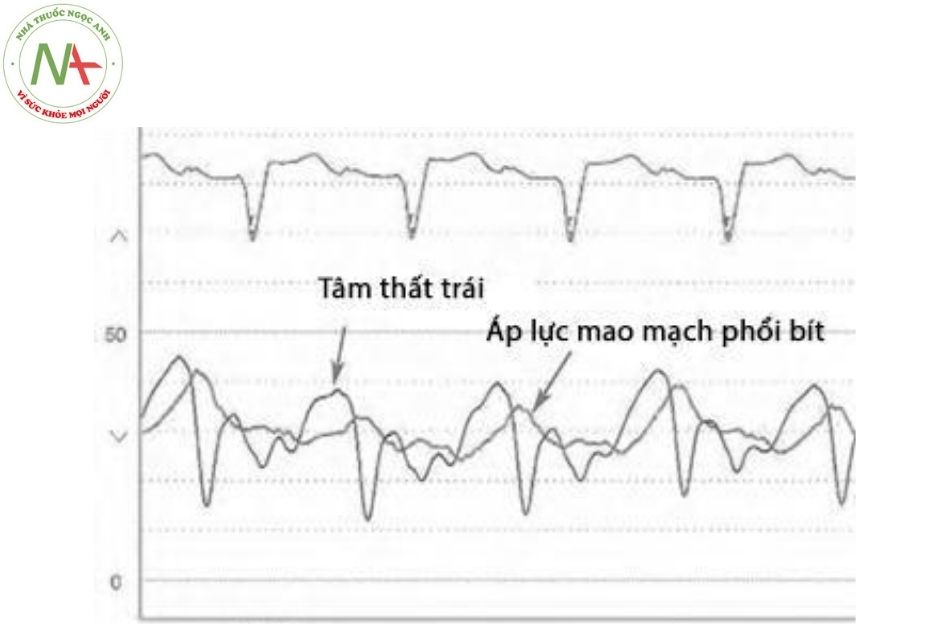
Kết hợp áp lực mao mạch phổi bít (hoặc nhĩ trái) và áp lực thất trái
Mục đích của sự kết hợp này là để chẩn đoán hẹp van hai lá. Ngoài ra, đo đồng thời áp lực thất trái và áp lực mao mạch phổi bít (LV-PCWP) cần thực hiện để xác định kích thước lỗ van hai lá ở những bệnh nhân đã được chẩn đoán hẹp van hai lá. Bình thường, không có chênh áp giữa áp lực mao mạch phổi bít (PCWP) và áp lực cuối tâm trương thất trái (LVEDP).
Kết hợp áp lực trung tâm động mạch chủ (động mạch đùi) và áp lực thất trái
Đo đồng thời áp lực thất trái và áp lực trung tâm động mạch chủ được thực hiện trong các trường hợp hẹp động mạch chủ đã biết hoặc nghi ngờ hẹp động mạch chủ, đây là phương pháp xác định chênh áp qua van cần thiết để ước tính diện tích van.
Thông thường, sẽ đo áp lực đồng thời thất trái và động mạch đùi. Tuy nhiên, có khác biệt giữa áp lực trung tâm động mạch chủ và áp lực động mạch đùi. Sự khác nhau này bao gồm khuếch đại ngoại biên làm cho áp lực ở động mạch đùi cao hơn áp lực trung tâm động mạch chủ và trường hợp bệnh động mạch ngoại biên, huyết khối catheter hoặc xoắn động mạch đùi làm cho áp lực trung tâm động mạch chủ cao hơn áp lực động mạch đùi.
Tài liệu tham khảo
1.Guyton and Hall Textbook of Medical Physiology, 13th edition, Elsevier,
2. Moss and Adams’ Heart disease in Infants, Children and Adolescents, 9th edition, Wolters
3. Ragosta M. Normal Waveforms, Artifacts, and Pitfalls. Textbook of Clinical Hemodynamics. Saunders Elsevier, 2008:16-37.
4. Oishi P, Teitel DF, Hoffman JI, Fineman JR. Cardiovascular Physiology. Roger’s Textbook of Pediatric Intensive Care, 4th Edition. Mosby,
5. Courtois M, Fattal PG, Kovacs SJ, et al. Anatomically and physiologically based reference level for measurement of intracardiac pressures. Circulation 1995; 92:1994-2000.
6. Brown LK, Kahl FR, Link KM, et al. Anatomic landmarks for use when measuring intracardiac pressure with fluid filled catheters. Am J Cardiol 2000; 86:121-124.
7. Swan HJ. The Swan-Ganz catheter. Dis Mon 1991; 37:509-543.
8. Jenkins BS, Bradley RD, Branthwaite MA. Evaluation of pulmonary arterial end-diastolic pressure as an indirect estimate of left atrial mean pressure. Circulation 1970; 42: 75-78.
9. Sharkey Beyond the wedge: Clinical physiology and the Swan-Ganz catheter. Am J Med 1987; 83:111-122.
10. Walston A, Kendall ME. Comparison of pulmonary wedge and left atrial pressure in man. Am Heart J 1973; 86:159-164.
11. Summerhill EM, Baram M. Principles of pulmonary artery catheterization in the critically ill. Lung 2005; 183: 209-219.
12. Haskell RJ, French Accuracy of left atrial and pulmonary artery wedge pressure in pure mitral regurgitation in predicting left ventricular end- diastolic pressure. Am J Cardiol 1988; 61:136-141.
13. Kern MJ, Christopher Hemodynamic rounds series II: The LVEDP. Cathet Cardiovasc Diagn 1998; 44: 70-74.